Hematopoese CAPÍTULO 1. Tópicos-chave
|
|
|
- Cláudio Azeredo Miranda
- 9 Há anos
- Visualizações:
Transcrição
1 CAPÍTULO 1 Hematopoese Tópicos-chave Locais de hematopoese 2 Células-tronco hematopoéticas e células progenitoras 2 Estroma da medula óssea 3 Células-tronco tecido-específicas 5 Regulação da hematopoese 6 Fatores de crescimento hematopoéticos 6 Receptores de fatores de crescimento e transdução de sinais 8 O ciclo celular 10 Apoptose 11 Fatores de transcrição 12 Moléculas de adesão 13
2 2 A. V. Hoffbrand e P. A. H. Moss Este primeiro capítulo trata de aspectos gerais da formação de células sanguíneas (hematopoese). São também discutidos os processos que regulam a hematopoese e os estágios iniciais da formação de eritrócitos (eritropoese), de granulócitos e monócitos (mielopoese) e de plaquetas (trombocitopoese). Locais de hematopoese Nas primeiras semanas da gestação, o saco vitelino é o principal local de hematopoese. A hematopoese definitiva, entretanto, deriva de uma população de células-tronco observada, pela primeira vez, na aorta dorsal, designada região AGM (aorta-gônadas-mesonefros). Acredita-se que esses precursores comuns às células endoteliais e hematopoéticas (hemangioblastos) aninhem-se no fígado, no baço e na medula óssea; de 6 semanas até 6 a 7 meses de vida fetal, o fígado e o baço são os principais órgãos hematopoéticos e continuam a produzir células sanguíneas até cerca de duas semanas após o nascimento (Tabela 1.1; ver Figura 7.1b). A medula óssea é o sítio hematopoético mais importante a partir de 6 a 7 meses de vida fetal e, durante a infância e a vida adulta, é a única fonte de novas células sanguíneas. As células em desenvolvimento situam-se fora dos seios da medula óssea; as maduras são liberadas nos espaços sinusais e na microcirculação medular e, a partir daí, na circulação geral. Nos dois primeiros anos, toda a medula óssea é hematopoética, mas, durante o resto da infância, há substituição progressiva da medula dos ossos longos por gordura, de modo que a medula hemopoética no adulto é confinada ao esqueleto central e às extremidades proximais do fêmur e do úmero (Tabela 1.1). Mesmo nessas regiões hematopoéticas, cerca de 50% da medula é composta de gordura (Figura 1.1). A medula óssea gordurosa remanescente é capaz de reverter para hematopoética e, em muitas doenças, também pode haver expansão da hematopoese aos ossos longos. Além disso, o fígado e o baço podem retomar seu papel hematopoético fetal ( hematopoese extramedular ). Células-tronco hematopoéticas e células progenitoras A hematopoese inicia-se com uma célula-tronco pluripotente, que tanto pode autorrenovar-se como também dar origem às distintas linhagens celulares. Essas células são capazes de repovoar uma medula cujas células-tronco tenham sido eliminadas por irradiação ou quimioterapia letais. As células-tronco hematopoéticas são escassas, talvez uma em 20 milhões de células nucleadas da medula óssea. Embora tenham fenótipo exato desconhecido, ao exame imunológico são CD34 +, CD38 e têm a aparência de um linfócito de tamanho pequeno ou médio (ver Figura 23.3). Residem em nichos especializados. A diferenciação celular a partir da célula- -tronco passa por uma etapa de progenitores hematopoéticos comprometidos, isto é, com potencial de desenvolvimento restrito (Figura 1.2). Tabela 1.1 Locais de hematopoese Feto De 0 a 2 anos Adultos 0-2 meses (saco vitelino) 2-7 meses (fígado, baço) 5-9 meses (medula óssea) Medula óssea (praticamente todos os ossos) Vértebras, costelas, crânio, esterno, sacro e pelve, extremidades proximais dos fêmures Figura 1.1 Biópsia de medula óssea normal (crista ilíaca posterior). Coloração por hematoxilina-eosina; aproximadamente 50% do tecido intertrabecular é hematopoético, e 50%, gordura.
3 Fundamentos em Hematologia 3 Célula-tronco pluripotente CFU GEMM Célula progenitora mieloide mista Célula-tronco linfoide BFU E CFU GMEo CFU baso Progenitor de eritroides CFU E CFU Meg Progenitor de megacariócito CFU GM Progenitor de granulócito e monócito CFU Eo Progenitor de eosinófilo Timo CFU-M CFU-G B T NK Eritrócitos Plaquetas Monócitos Neutrófilos Eosinófilos Basófilos Linfócitos Células NK Figura 1.2 Diagrama mostrando a célula-tronco multipotente da medula óssea e as linhagens celulares que dela se originam. Várias células progenitoras podem ser identificadas por cultura em meio semissólido pelo tipo de colônia que formam. É possível que um progenitor eritroide/megacariocítico seja formado antes de o progenitor linfoide comum divergir do progenitor mieloide misto granulocítico/monocítico/eosinofílico. Baso, basófilo; BFU, unidade formadora explosiva; CFU, unidade formadora de colônia; E, eritroide; Eo, eosinófila; GEMM, granulocítica, eritroide, monocítica e megacariocítica; GM, granulócito, monócito; Meg, megacariócito; NK, natural killer. A existência de células progenitoras separadas para cada linhagem pode ser demonstrada por técnicas de cultura in vitro. Células progenitoras muito precoces devem ser cultivadas a longo prazo em estroma de medula óssea, ao passo que células progenitoras tardias costumam ser cultivadas em meios semissólidos. Um exemplo é o primeiro precursor mieloide misto detectável, que origina granulócitos, eritrócitos, monócitos e megacariócitos, chamado de CFU (unidade formadora de colônias)-gemm (Figura 1.2). A medula óssea também é o local primário de origem de linfócitos (Capítulo 9), que se diferenciam de um precursor linfocítico comum. A célula-tronco tem capacidade de autorrenovação (Figura 1.3), de modo que a celularidade geral da medula, em condições estáveis de saúde, permanece constante. Há considerável ampliação na proliferação do sistema: uma célula-tronco, depois de 20 divisões celulares, é capaz de produzir cerca de 10 6 células sanguíneas maduras (Figura 1.3). As células precursoras, contudo, são capazes de responder a fatores de crescimento hematopoético com aumento de produção seletiva de uma ou outra linhagem celular de acordo com as necessidades. O desenvolvimento de células maduras (eritrócitos, granulócitos, monócitos, megacariócitos e linfócitos) será abordado em outras seções deste livro. Estroma da medula óssea A medula óssea constitui-se em ambiente adequado para sobrevida, autorrenovação e formação de células progenitoras diferenciadas. Esse meio é composto por células do estroma e uma
4 4 A. V. Hoffbrand e P. A. H. Moss Multiplicação Autorrenovação Diferenciação (a) Células maduras Células-tronco (b) Células progenitoras multipotentes Precursores comprometidos Figura 1.3 (a) Com a diferenciação crescente, as células da medula óssea perdem a capacidade de autorrenovação à medida que amadurecem. (b) Uma única célula-tronco produz, depois de múltiplas divisões (mostradas pelas linhas verticais), > 10 6 células maduras. rede microvascular (Figura 1.4). As células do estroma incluem adipócitos, fibroblastos, células endoteliais e macrófagos, e secretam moléculas extracelulares, como colágeno, glicoproteínas (fibronectina e trombospondina) e glicosaminoglicanos (ácido hialurônico e derivados condroitínicos) para formar uma matriz extracelular, além de secretarem vários fatores de crescimento necessários à sobrevivência da célula-tronco. Células-tronco mesenquimais, também chamadas células estromais mesenquimais multipotentes ou células mesenquimais aderentes, são críticas na formação do estroma. Junto com os osteoblastos, formam nichos e fornecem os fatores de crescimento, moléculas de adesão e citoquinas que dão suporte às células-tronco, por exemplo, a proteína que permeia as células estromais liga-se a um receptor NOTCH1 nas Célula-tronco Matriz extracelular Macrófago Célula adiposa Célula endotelial Fibroblasto Molécula de adesão Fator de crescimento Ligante Receptor de fator de crescimento Figura 1.4 A hematopoese ocorre em microambiente adequado ( nicho ) fornecido pela matriz do estroma na qual as células-tronco crescem e se dividem. Há locais de reconhecimento específico e de adesão (ver p. 13); glicoproteínas extracelulares e outros componentes estão envolvidos na ligação.
5 Fundamentos em Hematologia 5 células-tronco, tornando-se um fator de transcrição envolvido no ciclo celular. As células-tronco são capazes de circular no organismo e são encontradas em pequeno número no sangue periférico. Para deixar a medula óssea, as células devem atravessar o endotélio vascular e esse processo de mobilização é aumentado pela administração de fatores de crescimento, como o fator estimulante de colônias granulocíticas (G-CSF) (ver p. 6). O processo reverso, de volta ao lar (homing), parece depender de um gradiente quimiocinético, no qual tem papel crítico o fator derivado do estroma (SDF-1). Várias interações críticas suportam a viabilidade das células-tronco e a produção no estroma, incluindo o fator de células-tronco (SCF) e proteínas permeantes estromais e seus respectivos receptores KIT e NOTCH, expressos em células-tronco. Células-tronco tecido-específicas Células-tronco estão presentes em diferentes órgãos. São pluripotentes e podem gerar vários tipos de tecidos, como células epiteliais, células nervosas (Figura 1.5). Estudos em pacientes e em animais que receberam transplante de células-tronco hematopoéticas (ver Capítulo 23) sugerem que as células hematopoéticas doadas podem contribuir para os tecidos, como o neural, o hepático e o muscular. A contribuição de células hematopoéticas de doadores adultos a tecidos não hematopoéticos, entretanto, se houver, é mínima. A persistência de células pluripotentes na vida pós-natal, a presença de células-tronco mesenquimais na medula óssea e a fusão de células transplantadas com células do hospedeiro foram propostas como explicação Célula totipotente (a) Células-tronco embrionárias Células mieloides e linfoides Fígado, etc. Célula-tronco epitelial Célula-tronco hematopoética Músculo, tendão, cartilagem, gordura, etc. Célula-tronco mesenquimal Célula-tronco nervosa Tecido nervoso (b) Células-tronco adultas Figura 1.5 (a) Células da camada interna do blastocisto no embrião recém-formado são capazes de gerar todos os tecidos do organismo e são designadas totipotentes. (b) Células-tronco especializadas adultas, da medula óssea, dos tecidos nervoso, epitelial e outros, originam células diferenciadas do mesmo tecido.
6 6 A. V. Hoffbrand e P. A. H. Moss alternativa de muitos resultados sugestivos de plasticidade das células-tronco. Regulação da hematopoese A hematopoese começa com mitoses das células-tronco; em cada divisão, uma célula-filha repõe a célula-tronco (autorrenovação) e a outra se compromete em diferenciação. Essas células progenitoras precocemente comprometidas expressam baixos níveis dos fatores de transcrição que as comprometem com linhagens específicas; a seleção da linhagem de diferenciação, portanto, pode variar tanto por alocação aleatória como por sinais externos recebidos pelas células progenitoras. Vários fatores de transcrição regulam a sobrevivência das células-tronco (p. ex., SCL, GATA-2, NO- TCH-1), enquanto outros estão envolvidos na diferenciação ao longo das principais linhagens celulares. Por exemplo, PU.1 e a família CEBP comprometem células para a linhagem mieloide leucocitária, enquanto GATA-1 e FOG-1 têm um papel essencial na diferenciação eritropoética e megacariocítica. Fatores de crescimento hematopoéticos Os fatores de crescimento hematopoéticos são hormônios glicoproteicos que regulam a proliferação e a diferenciação das células progenitoras hematopoéticas e a função das células sanguíneas maduras. Podem agir no local em que são produzidos por contato célula a célula ou podem circular no plasma. Também podem ligar-se à matriz extracelular, formando nichos aos quais aderem as células-tronco e as células progenitoras. Os fatores de crescimento podem causar não só proliferação celular, mas também podem estimular a diferenciação, a maturação, prevenir a apoptose e afetar as funções de células maduras (Figura 1.6). Os fatores de crescimento compartilham certo número de propriedades (Tabela 1.2) e agem em diferentes etapas da hematopoese (Tabela 1.3, Figura 1.7). Tabela 1.2 Características gerais dos fatores de crescimento mieloides e linfoides Glicoproteínas que agem em concentrações muito baixas Atuam hierarquicamente Em geral, são produzidos por muitos tipos de células Em geral, afetam mais de uma linhagem Em geral, ativos nas células-tronco/progenitoras e nas células funcionais finais Em geral, têm interações sinérgicas ou aditivas com outros fatores de crescimento Muitas vezes, agem no equivalente neoplásico da célula normal Ações múltiplas: proliferação, diferenciação, maturação, ativação funcional, prevenção de apoptose de células progenitoras Tabela 1.3 Fatores de crescimento hematopoético Agem nas células do estroma IL-1 TNF Agem nas células-tronco pluripotentes SCF FLT3-L VEGF Agem nas células progenitoras multipotentes IL-3 GM-CSF IL-6 G-CSF Trombopoetina Agem em células progenitoras comprometidas G-CSF* M-CSF IL-5 (CSF-eosinófilo) Eritropoetina Trombopoetina* CSF, fator estimulante de colônias; FLT3-L, FLT3 ligante; G-CSF, fator estimulante de colônias granulocíticas; GM-CSF, fator estimulante de colônias granulocíticas e macrofágicas; IL, interleuquina; M-CSF, fator estimulante de colônias macrofágicas; SCF, fator de célula-tronco; TNF, fator de necrose tumoral; VEGF, fator de crescimento do endotélio vascular. * Estes também agem sinergicamente com fatores anteriormente ativos em progenitores pluripotentes.
7 Fundamentos em Hematologia 7 Célula inicial Proliferação G-CSF Monócito Diferenciação G-CSF Neutrófilo Maturação G-CSF Supressão da apoptose G-CSF Ativação funcional Célula final G-CSF Ativação de fagocitose, destruição, secreção Figura 1.6 Fatores de crescimento podem estimular a proliferação de células primitivas da medula óssea, dirigir a diferenciação para um ou outro tipo de célula, estimular a maturação celular, suprimir a apoptose ou afetar a função de células maduras pós-mitóticas, como ilustrado nesta figura para o fator estimulante de colônias granulocíticas (G-CSF) em relação a um progenitor primitivo mieloide e a um neutrófilo. Células do estroma são as principais fontes de fatores de crescimento, com exceção da eritropoetina 90% são sintetizados no rim, e da trombopoetina, sintetizada principalmente no fígado. Um aspecto importante da ação dos fatores de crescimento é que eles podem agir sinergicamente no estímulo a proliferação ou diferenciação de uma célula em particular; além disso, a ação de um fator de crescimento em uma célula pode estimular a produção de outro fator de crescimento ou de um receptor de fator. O SCF e o ligante de FLT (FLT-L) agem localmente nas células-tronco pluripotentes e nos progenitores primitivos mieloides e linfoides (Figura 1.7). A interleuquina-3 (IL-3) e o GM-CSF são fatores de crescimento multipotenciais com atividades parcialmente superpostas. O G-CSF e a trombopoetina aumentam os efeitos de SCF, FLT-L, IL-3 e GM-CSF na sobrevida e na diferenciação das células hematopoéticas primitivas. Esses fatores mantêm um pool de células- -tronco e células progenitoras hematopoéticas sobre o qual agem os fatores de ação tardia, a eritropoetina, o G-CSF, o M-CSF, a IL-5 e a trombopoetina, para aumentar a produção de uma ou outra linhagem em resposta às necessi-
8 8 A. V. Hoffbrand e P. A. H. Moss SCF IL-3 PSC IL-3 GM-CSF TPO CFU- GEMM GM-CSF BFU EMeg CFU- GMEo BFU E EPO CFU Meg M-CSF CFU GM G-CSF CFU Eo IL-5 CFU E CFU M CFU G Eritrócitos Plaquetas Monócitos Neutrófilos Eosinófilos Figura 1.7 Diagrama do papel dos fatores de crescimento na hematopoese normal. Múltiplos fatores de crescimento agem nas células-tronco primitivas e progenitoras da medula óssea. EPO, eritropoetina; PSC, célula-tronco pluripotente; SCF, fator de célula-tronco; TPO, trombopoetina. Para outras abreviaturas, ver a Figura 1.2. dades do organismo. A formação de granulócitos e monócitos, por exemplo, pode ser estimulada por infecção ou inflamação por meio da liberação de IL-1 e fator de necrose tumoral (TNF), os quais, por sua vez, estimulam células do estroma a produzir fatores de crescimento em uma rede interativa (ver Figura 8.4). Contrariamente, citoquinas, como o fator de crescimento transformador- (TGF- ) e o interferon- (IFN- ) podem exercer um efeito negativo na hematopoese e podem desempenhar algum papel no desenvolvimento de anemia aplástica (ver p. 289). Receptores de fatores de crescimento e transdução de sinais Os efeitos biológicos dos fatores de crescimento são mediados por receptores específicos nas células-alvo. Muitos receptores (p. ex., receptor de eritropoetina [EPO-R], GMCSF-R) pertencem à superfamília dos receptores hematopoéticos, que dimerizam após haver conexão com os respectivos ligantes. A dimerização do receptor leva à ativação de uma complexa série de vias de transdução de sinais intracelulares; as três principais são a via JAK/STAT, a via proteinoquinase ativada por mitogênio (MAP) e a via fosfatidil-inositol 3 (PI3) quinase (Figura 1.8; ver também Figura 15.2). As proteinoquinases Janus-associadas (JAK) são uma família de quatro proteinoquinases tirosina-específicas que se associam aos domínios intracelulares dos receptores de fatores de crescimento (Figura 1.8). Uma molécula de fator de crescimento liga-se simultaneamente ao domínio extracelular de duas ou três moléculas receptoras, causando sua agregação. A agregação dos receptores induz à ativação dos JAKs, que, então, fosforilam membros do transdutor de sinal e do ativador de transcrição (STAT) da família dos fatores de transcrição. A consequência é a dimerização e a translocação destes, do cito-
9 Fundamentos em Hematologia 9 Fator de crescimento Membrana plasmática Quinase PI3 JAK JAK AKT STATs RAS RAF Apoptose bloqueada Dímeros ativos de STAT MAP-quinase Núcleo MYC, FOS Ativação da expressão gênica M Expressão gênica G2 G1 S E2F Rb p53 Dano do DNA Figura 1.8 Controle da hematopoese por fatores de crescimento. Os fatores agem em células que expressam o receptor correspondente. A ligação de um fator de crescimento a seu receptor ativa as vias JAK/STAT, MAPK e fosfatidil-inositol 3-quinase (PI3K) (ver Figura 15.2), o que provoca ativação transcricional de genes específicos. E2F é um fator de transcrição necessário para a transição celular da fase G1 para a fase S. E2F é inibido pelo gene tumor-supressor Rb (retinoblastoma), o qual pode ser ativado indiretamente por p53. A síntese e a degradação de diversas ciclinas (Figura 1.10) estimulam a célula a passar pelas diferentes fases do ciclo celular. Os fatores de crescimento também podem suprimir a apoptose pela ativação de AKT (proteinoquinase B). plasma para o núcleo, através da membrana nuclear. Dentro do núcleo, dímeros STAT ativam a transcrição de genes específicos. Um modelo para o controle da expressão gênica por um fator de transcrição é mostrado na Figura 1.9. A importância clínica dessa via foi comprovada pelo achado de uma mutação que ativa o gene JAK2 como causa da policitemia vera (ver p. 203). JAK também pode ativar a via MAPK, que é regulada por Ras e controla a proliferação. Quinases PI3 fosforilam lipídios do inositol, os quais têm um amplo espectro de efeitos em
10 10 A. V. Hoffbrand e P. A. H. Moss Domínio de ligação com DNA Domínio de transativação RNA-polimerase + Fatores acessórios Transcrição Amplificador de sequência de DNA Caixa de sequência TATA (promotor) Gene estrutural Figura 1.9 Modelo para controle de expressão gênica por um fator de transcrição. O domínio de ligação com DNA de um fator de transcrição liga uma sequência amplificadora específica adjacente a um gene estrutural. O domínio de transativação então liga uma molécula de RNA-polimerase, aumentando sua ligação com a caixa TATA. A RNA- -polimerase inicia a transcrição do gene estrutural para formar mrna. A translação do mrna pelo ribossomo gera a proteína codificada pelo gene. sequência, incluindo ativação de AKT, que causa bloqueio da apoptose e outras ações (Figura 1.8; ver Figura 15.2). Domínios diferentes da proteína receptora intracelular podem sinalizar para diferentes processos, como proliferação ou supressão da apoptose, mediados por fatores de crescimento. Um segundo grupo, menor, de fatores de crescimento, incluindo SCF, FLT-3L e M-CSF (Tabela 1.3), liga-se a receptores que têm um domínio extracelular semelhante ao das imunoglobulinas, ligado por uma ponte transmembrana a um domínio tirosinoquinase citoplásmico. A ligação de fatores de crescimento resulta na dimerização desses receptores e na consequente ativação do domínio da tirosinoquinase. A fosforilação de resíduos de tirosina no próprio receptor gera sítios de ligação para proteínas sinalizadoras que iniciam complexas cascatas de eventos bioquímicos, resultando em alterações na expressão gênica, na proliferação celular e na prevenção da apoptose. O ciclo celular O ciclo de divisão celular, em geral designado simplesmente como ciclo celular, é um processo complexo que se situa no núcleo da hematopoese. A desregulação da proliferação celular também é a chave do desenvolvimento de neoplasias malignas. A duração do ciclo celular varia de tecido para tecido, mas os princípios básicos são comuns a todos. O ciclo é dividido em uma fase mitótica (fase M), durante a qual a célula divide-se fisicamente, e uma interfase, durante a qual os cromossomos duplicam-se e a célula cresce antes da divisão (Figura 1.10). A fase M é subdividida em mitose, na qual se divide o núcleo, e citoquinese, em que ocorre a fissão celular. A interfase é dividida em três estágios principais: fase G 1, na qual a célula começa a orientar-se no sentido da replicação; fase S, durante a qual é duplicado o conteúdo de DNA (Figura 1.10b) e os cromossomos replicam-se; e fase G 2, na qual as organelas são copiadas, aumentando o volume citoplasmático. Se as células repousarem antes da divisão, elas entram em um estágio G 0, em que podem permanecer por longos períodos. O número de células em cada estágio do ciclo pode ser avaliado pela exposição da célula a um agente químico ou a um marcador radioativo que se incorpore ao DNA recém-formado ou por citometria em fluxo. O ciclo celular é controlado em dois checkpoints, que agem como freios para coordenar o processo de divisão no fim das fases G 1 e G 2. Duas classes principais de moléculas controlam esses checkpoints, proteinoquinases ciclina-dependentes (Cdk), que fosforilam alvos proteicos em sequência, e ciclinas, que se ligam às Cdks e regulam sua atividade. Um exemplo da importância desses sistemas é de-
11 Fundamentos em Hematologia 11 Conteúdo de DNA Cdk2 (a) (b) 4c 2c Ciclina B monstrado pelo linfoma de células do manto que resulta da ativação constitucional da ciclina D1 como resultado de uma translocação cromossômica (ver p. 266). Apoptose Fase M M G 2 G 1 Cdk2 S Interfase Ciclina A G 0 Cdk2 Fase do ciclo celular Ciclina E G 1 S G 2 M Figura 1.10 (a) Estágios do ciclo celular. A progressão por meio do ciclo celular é regulada por combinações específicas de proteinoquinases ciclina-dependentes (Cdk) e proteinociclinas. A síntese e a degradação de diferentes ciclinas estimulam a célula a passar por meio das diferentes fases do ciclo, embora o papel exato de cada heterodímer ainda não esteja estabelecido. (b) Relação entre o conteúdo de DNA da célula, expresso em unidades arbitrárias como 2c aumentando para 4c, e sua posição no ciclo celular. (Adaptada de Wickramasinghe S.N. [1975] Human Bone Marrow, Blackwell Scientific, Oxford, p. 13.) Apoptose (morte celular programada) é um processo regulado de morte celular fisiológica pelo qual células individuais são estimuladas a ativar proteínas intracelulares que levam à própria morte. Morfologicamente, é caracterizada por encolhimento celular, condensação da cromatina nuclear, fragmentação do núcleo e quebra do DNA em sítios internucleossômicos. É um processo importante de manutenção da homeostasia tecidual na hematopoese e no desenvolvimento de linfócitos. A apoptose resulta da ação de cisteína-proteases intracelulares, chamadas de caspases, que são ativadas depois da clivagem e levam à digestão de DNA por endonuclease e desintegração do esqueleto celular (Figura 1.11). Há duas vias principais pelas quais as caspases são ativadas. A primeira é a sinalização por meio de proteínas da membrana como Fas ou receptor de TNF via seu domínio de morte intracelular. Um exemplo desse mecanismo é mostrado por células T citotóxicas ativadas, expressando ligante FAS que induz apoptose em células-alvo. A segunda via faz-se pela liberação de citocromo c das mitocôndrias. O citocromo c liga-se à APAF-1 que, então, ativa as caspases. O dano ao DNA induzido por irradiação ou por quimioterapia pode agir por essa via. A proteína p53 tem um papel importante em sentir quando há dano ao DNA. Ela ativa a apoptose, aumentando o nível celular de BAX, que estimula a liberação de citocromo c (Figura 1.11) e bloqueia o ciclo celular, impedindo que a célula lesada se divida (Figura 1.8). O nível celular de p53 é rigidamente controlado por uma segunda proteína, MDM2. Depois da morte, as células apoptóticas expõem moléculas que levam à ingestão pelos macrófagos. Tal como as moléculas que favorecem apoptose, há várias proteínas intracelulares que protegem as células contra a apoptose. O exemplo mais bem-caracterizado é a BLC-2, protótipo de uma família de proteínas relacionadas, algumas das quais são antiapoptóticas, e outras, como a BAX, que são pró-apoptóticas. A relação intracelular de BAX e BCL-2 determina a suscetibilidade relativa das células à apoptose (p. ex., determina a sobrevida de plaquetas) e pode agir pela regulação da liberação de citocromo c pelas mitocôndrias. Muitas das alterações genéticas associadas a doenças malignas diminuem o índice de apoptose e prolongam a sobrevida celular. O
12 12 A. V. Hoffbrand e P. A. H. Moss APOPTOSE Fator de morte (p. ex., ligante FAS) Liberação de citocromo c Caspases Procaspases Domínio de morte Inibe Proteína BAX aumentada p53 BCL-2 BCL-2 aumentada Expressão do gene BAX Dano ao DNA Fator de sobrevivência (p. ex., fator de crescimento) Fármacos citotóxicos Radiação Figura 1.11 Representação da apoptose. A apoptose é iniciada via dois estímulos principais: (i) sinal por meio de receptores da membrana celular como receptor de FAS ou fator de necrose tumoral (TNF) ou (ii) liberação de citocromo c da mitocôndria. Os receptores de membrana sinalizam apoptose por um domínio intracelular de morte levando à ativação de caspases que digerem DNA. O citocromo c liga-se à proteína citoplasmática Apaf-1, levando à ativação de caspases. A relação intracelular de pró-apoptóticos (p. ex., BAX) e antiapoptóticos (p. ex., BCL-2) da família BCL-2 pode influenciar a liberação de citocromo c. Fatores de crescimento aumentam o nível de BCL-2, inibindo a liberação de citocromo c, enquanto o dano de DNA, ativando a p53, aumenta o nível de BAX que, por sua vez, aumenta a liberação de citocromo c. exemplo mais claro é a translocação do gene da BCL-2 para o lócus da cadeia pesada de imunoglobulina na translocação t(14; 18) no linfoma folicular. A superexpressão da proteína BCL-2 torna as células B malignas menos suscetíveis à apoptose. A apoptose é o destino normal da maioria das células B que são selecionadas nos centros germinativos linfoides. Várias translocações que levam à fusão de proteínas, como t(9; 22), t(1; 14) e t(15; 17), também resultam em inibição da apoptose (ver Capítulo 11). Além disso, genes que codificam proteínas envolvidas na mediação de apoptose quando há dano ao DNA, como a p53 e a ATM, também sofrem mutações frequentes e podem ficar inativos em doenças hematopoéticas malignas. Necrose é a morte celular com células adjacentes devido a isquemia, trauma químico ou hipertermia. As células incham e há perda da integridade da membrana plasmática. Em geral, há um infiltrado inflamatório em resposta à liberação dos conteúdos celulares. A autofagia é a digestão de organelas celulares por lisossomos. Pode estar envolvida em morte celular, mas, em algumas situações, também na manutenção da sobrevida celular por nutrientes reciclados. Fatores de transcrição Fatores de transcrição regulam a expressão gênica pelo controle da transcrição de genes específicos ou de famílias de genes. Contêm ao menos dois domínios: um domínio de ligação ao DNA, como um zíper de leucina ou hélice- -alça-hélice, que se liga a uma sequência específica do DNA, e um domínio de ativação, que contribui para a montagem do complexo de transcrição em um gene promotor (Figura 1.9). Mutação, deleção ou translocação de fatores de
13 Fundamentos em Hematologia 13 transcrição são a causa subjacente de muitos casos de neoplasias hematológicas. Moléculas de adesão Uma grande família de moléculas de glicoproteínas, chamadas moléculas de adesão, medeia a ligação de células precursoras da medula, leucócitos e plaquetas a vários componentes da matriz extracelular, ao endotélio, a outras superfícies e umas às outras. As moléculas de adesão na superfície de leucócitos são denominadas receptores e interagem com moléculas (chamadas ligantes) na superfície de células-alvo potenciais. Há três famílias principais: 1 Superfamília de imunoglobulinas Inclui receptores que reagem com antígenos (receptores de células T e imunoglobulinas) e moléculas superficiais de adesão independentes de antígenos. 2 Selectinas São principalmente envolvidas na adesão de leucócitos e plaquetas ao endotélio na inflamação e na coagulação. 3 Integrinas São envolvidas na adesão celular à matriz extracelular, por exemplo, ao colágeno na cicatrização de feridas e na adesão de leucócitos e de plaquetas. As moléculas de adesão são importantes no desenvolvimento e na manutenção das respostas inflamatória e imunológica e nas interações de plaquetas e leucócitos com a parede dos vasos. A expressão de moléculas de adesão pode ser modificada por fatores extra e intracelulares e essa alteração pode ser quantitativa ou funcional. A expressão dessas moléculas pode ser aumentada por IL-1, TNF, interferon-, ativação de células T, adesão a proteínas extracelulares e infecção viral. O padrão de expressão das moléculas de adesão em células tumorais pode determinar seu modo de disseminação e sua localização tecidual, por exemplo, o padrão de metástases de células carcinomatosas e de células de linfomas em padrão folicular ou difuso. As moléculas de adesão também podem determinar que as células circulem na corrente sanguínea ou permaneçam fixas no tecido. Há, também, a possibilidade de determinarem parcialmente a suscetibilidade de células tumorais às defesas imunológicas do organismo. RESUMO A hematopoese (formação das células sanguíneas) origina-se de células-tronco pluripotentes na medula óssea. Células-tronco dão origem a células progenitoras que, após divisão e diferenciação, formam eritrócitos, granulócitos (neutrófilos, eosinófilos e basófilos), monócitos, plaquetas e linfócitos B e T. O tecido hematopoético ocupa cerca de 50% do espaço medular na medula óssea normal do adulto. A hematopoese no adulto é confinada ao esqueleto central; em lactentes e crianças jovens, o tecido hematopoético extende-se pelos ossos longos dos membros superiores e inferiores. Células-tronco residem na medula óssea em nichos formados por células do estroma e, em pequeno número, circulam no sangue. Fatores de crescimento ligam-se a receptores celulares específicos e produzem uma cascata de eventos de fosforilação no núcleo celular. Fatores de transcrição conduzem a mensagem aos genes que devem ser ativados para estimular divisão celular, diferenciação, atividade funcional ou suprimir apoptose.
14 14 A. V. Hoffbrand e P. A. H. Moss Fatores de transcrição são moléculas que se ligam ao DNA e controlam a transcrição de genes específicos ou de famílias de genes. Apoptose é um processo fisiológico de morte celular decorrente da ativação de caspases. A relação intracelular entre proteínas pró-apoptóticas (p. ex., BAX) e proteínas antiapoptóticas (p. ex., BCL-2) determina a suscetibilidade da célula à apoptose. Moléculas de adesão são uma ampla família de glicoproteínas que medeiam o acoplamento de precursores mieloides, leucócitos maduros e plaquetas à matriz extracelular, ao endotélio e uns aos outros. Acesse (em inglês) para testar seus conhecimentos sobre este capítulo.
φ Fleury Stem cell Mastócitos Mieloblastos Linfócito pequeno Natural Killer (Grande linfócito granular) Hemácias Linfócito T Linfócito B Megacariócito
 Hemopoese Marcos Fleury [email protected] Hematopoese É o processo de formação, maturação e liberação das células sanguíneas Eritropoese Leucopoese Trombopoese - Hemácias - Leucócitos - Plaquetas Tem como
Hemopoese Marcos Fleury [email protected] Hematopoese É o processo de formação, maturação e liberação das células sanguíneas Eritropoese Leucopoese Trombopoese - Hemácias - Leucócitos - Plaquetas Tem como
Proliferação. Diferenciação. Apoptose. Maturação. Ativação funcional. SCF PSC TPO CFU GEMM. BFU EMeg CFU GMEo BFU E IL-3. CFU EMeg CFU GM EPO.
 Hematopoese Requisitos básicos. 1. Stem cells (células tronco hematopoéticas). 2. Meio ambiente medular (fibroblastos, macrófagos e células endoteliais). 3. Fatores de crescimento (GM-CSF, Eritropoietina...)
Hematopoese Requisitos básicos. 1. Stem cells (células tronco hematopoéticas). 2. Meio ambiente medular (fibroblastos, macrófagos e células endoteliais). 3. Fatores de crescimento (GM-CSF, Eritropoietina...)
CAPÍTULO 1 Hematopoese
 CAPÍTULO 1 Hematopoese Tópicos-chave Locais de hematopoese 2 Células-tronco e células progenitoras hematopoéticas 2 Estroma da medula óssea 4 Regulação da hematopoese 4 Fatores de crescimento hematopoéticos
CAPÍTULO 1 Hematopoese Tópicos-chave Locais de hematopoese 2 Células-tronco e células progenitoras hematopoéticas 2 Estroma da medula óssea 4 Regulação da hematopoese 4 Fatores de crescimento hematopoéticos
Requisitos básicos. Nas regiões hematopoéticas, 50% do tecido medular é representado por gordura. O tecido hematopoético pode ocupar áreas de gordura.
 Hematopoese Requisitos básicos. 1. Stem cells (células tronco hematopoéticas). 2. Meio ambiente medular (fibroblastos, macrófagos e células endoteliais). 3. Fatores de crescimento (GM-CSF, Eritropoietina...)
Hematopoese Requisitos básicos. 1. Stem cells (células tronco hematopoéticas). 2. Meio ambiente medular (fibroblastos, macrófagos e células endoteliais). 3. Fatores de crescimento (GM-CSF, Eritropoietina...)
Aula teórica: Hematopoese
 Aula teórica: Hematopoese MED, 2017 Elementos figurados do sangue periférico Glóbulos vermelhos, eritrócitos ou hemácias 4-5 milhões/ml Glóbulos brancos ou leucócitos 6-9 mil/ml Polimorfonucleares (granulócitos)
Aula teórica: Hematopoese MED, 2017 Elementos figurados do sangue periférico Glóbulos vermelhos, eritrócitos ou hemácias 4-5 milhões/ml Glóbulos brancos ou leucócitos 6-9 mil/ml Polimorfonucleares (granulócitos)
Hematopoese. Prof a. Marta G. Amaral, Dra. Histofisiologia
 Hematopoese Prof a. Marta G. Amaral, Dra. Histofisiologia 1º fase: 18 dia Origem Mesoderma extra-embrionário recobre o saco vitelino ilhotas de Wolff e Pander Células da periferia endotélio Células do
Hematopoese Prof a. Marta G. Amaral, Dra. Histofisiologia 1º fase: 18 dia Origem Mesoderma extra-embrionário recobre o saco vitelino ilhotas de Wolff e Pander Células da periferia endotélio Células do
Hematopoese. Prof. Archangelo P. Fernandes Profa. Alessandra Barone
 Hematopoese Prof. Archangelo P. Fernandes Profa. Alessandra Barone www.profbio.com.br Sangue Tecido fluido circulante, formado por uma fase sólida de células diferenciadas e por uma fase líquida denominada
Hematopoese Prof. Archangelo P. Fernandes Profa. Alessandra Barone www.profbio.com.br Sangue Tecido fluido circulante, formado por uma fase sólida de células diferenciadas e por uma fase líquida denominada
Medula Óssea. Doutoranda: Luciene Terezina de Lima
 Medula Óssea Doutoranda: Luciene Terezina de Lima Hemopoese É a produção de células sanguineas. Processo dinamico que requer o reabastecimento de mais de 7x10 9 células (leucócitos, eritrócitos e plaquetas)/
Medula Óssea Doutoranda: Luciene Terezina de Lima Hemopoese É a produção de células sanguineas. Processo dinamico que requer o reabastecimento de mais de 7x10 9 células (leucócitos, eritrócitos e plaquetas)/
Universidade Federal do Amazonas ICB Dep. Morfologia Disciplina: Biologia Celular Aulas Teóricas
 Universidade Federal do Amazonas ICB Dep. Morfologia Disciplina: Biologia Celular Aulas Teóricas Noções básicas da Mitose e Meiose Ciclo Celular Noções básicas da Mitose e Meiose Ciclo Celular Fase S e
Universidade Federal do Amazonas ICB Dep. Morfologia Disciplina: Biologia Celular Aulas Teóricas Noções básicas da Mitose e Meiose Ciclo Celular Noções básicas da Mitose e Meiose Ciclo Celular Fase S e
Hematopoese Aspectos gerais
 Hematopoese Aspectos gerais Hematopoese As células do sangue têm um tempo de vida limitado! Renovação celular proliferação mitótica Células precursoras. Órgãos hemocitopoéticos: Vida pré-natal: Mesoderma
Hematopoese Aspectos gerais Hematopoese As células do sangue têm um tempo de vida limitado! Renovação celular proliferação mitótica Células precursoras. Órgãos hemocitopoéticos: Vida pré-natal: Mesoderma
UNIVERSIDADE DE CUIABÁ NÚCLEO DE DISCIPLINAS INTEGRADAS DISCIPLINA DE CIÊNCIAS MORFOFUNCIONAIS IV A ORIGEM DAS CÉLULAS SANGUÍNEAS - HEMATOPOIESE
 UNIVERSIDADE DE CUIABÁ NÚCLEO DE DISCIPLINAS INTEGRADAS DISCIPLINA DE CIÊNCIAS MORFOFUNCIONAIS IV A ORIGEM DAS CÉLULAS SANGUÍNEAS - HEMATOPOIESE 1 HEMATOPOIESE 2 Processo de formação do componente celular
UNIVERSIDADE DE CUIABÁ NÚCLEO DE DISCIPLINAS INTEGRADAS DISCIPLINA DE CIÊNCIAS MORFOFUNCIONAIS IV A ORIGEM DAS CÉLULAS SANGUÍNEAS - HEMATOPOIESE 1 HEMATOPOIESE 2 Processo de formação do componente celular
Célula tronco. Célula tronco
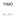 TIMO CB, 2017 Célula tronco Progenitor mielóide Progenitor linfóide Célula tronco Linfócito B Linfócito T Célula NK CFU-E CFU-Meg CFU-Bas CFU-Eos CFU-GM eritrócitos plaquetas basófilo eosinófilo neutrófilo
TIMO CB, 2017 Célula tronco Progenitor mielóide Progenitor linfóide Célula tronco Linfócito B Linfócito T Célula NK CFU-E CFU-Meg CFU-Bas CFU-Eos CFU-GM eritrócitos plaquetas basófilo eosinófilo neutrófilo
Hematopoiese. 11ª Aula Teórica. Medula óssea Baço Timo Gânglios linfáticos. 7 de Novembro de 2007 Cláudia Cavadas
 11ª Aula Teórica 7 de Novembro de 2007 Cláudia Cavadas Hematopoiese As células sanguíneas têm uma vida relativamente curta Constante renovação em orgãos HEMATOPOIÉTICOS Medula óssea Baço Timo Gânglios
11ª Aula Teórica 7 de Novembro de 2007 Cláudia Cavadas Hematopoiese As células sanguíneas têm uma vida relativamente curta Constante renovação em orgãos HEMATOPOIÉTICOS Medula óssea Baço Timo Gânglios
Granulopoese. Profa Elvira Shinohara
 Granulopoese Profa Elvira Shinohara Granulopoese = formação de neutrófilos, eosinófilos e basófilos Neutrófilos Eosinófilos Meia vida de 7 horas no sangue Basófilos NÚMERO TOTAL DE CÉLULAS NUCLEADAS NA
Granulopoese Profa Elvira Shinohara Granulopoese = formação de neutrófilos, eosinófilos e basófilos Neutrófilos Eosinófilos Meia vida de 7 horas no sangue Basófilos NÚMERO TOTAL DE CÉLULAS NUCLEADAS NA
Célula tronco. Célula tronco
 TIMO MED 2017 Célula tronco Progenitor mielóide Progenitor linfóide Célula tronco Linfócito B Linfócito T Célula NK CFU-E CFU-Meg CFU-Bas CFU-Eos CFU-GM eritrócitos plaquetas basófilo eosinófilo neutrófilo
TIMO MED 2017 Célula tronco Progenitor mielóide Progenitor linfóide Célula tronco Linfócito B Linfócito T Célula NK CFU-E CFU-Meg CFU-Bas CFU-Eos CFU-GM eritrócitos plaquetas basófilo eosinófilo neutrófilo
TECIDO HEMATOPOIÉTICO E SANGUÍNEO
 TECIDO HEMATOPOIÉTICO E SANGUÍNEO CARACTERÍSTICAS Denomina-se hematopoiese o processo de formação dos elementos figurados do sangue; A hematopoiese antes do nascimento ocorre no saco vitelínico do embrião
TECIDO HEMATOPOIÉTICO E SANGUÍNEO CARACTERÍSTICAS Denomina-se hematopoiese o processo de formação dos elementos figurados do sangue; A hematopoiese antes do nascimento ocorre no saco vitelínico do embrião
Anexo 2. Chave de classificação. Célula-tronco hematopoética (CT-H)
 Anexo 2 Chave de classificação Célula-tronco hematopoética (CT-H) Principal característica: é uma célula-tronco multipotente, pois tem o potencial de gerar linhagens de células que darão origem aos diversos
Anexo 2 Chave de classificação Célula-tronco hematopoética (CT-H) Principal característica: é uma célula-tronco multipotente, pois tem o potencial de gerar linhagens de células que darão origem aos diversos
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Hemocitopoese Disciplina: Histologia Prof. Me. Cássio Resende de Morais Introdução Elementos figurados; Hemácias: Transporte
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Hemocitopoese Disciplina: Histologia Prof. Me. Cássio Resende de Morais Introdução Elementos figurados; Hemácias: Transporte
Aspectos gerais da estrutura celular
 Ciclo celular Aspectos gerais da estrutura celular A célula é a unidade básica da vida Altamente organizada, dividida em compartimentos As células surgem de outras células préexistentes As células são
Ciclo celular Aspectos gerais da estrutura celular A célula é a unidade básica da vida Altamente organizada, dividida em compartimentos As células surgem de outras células préexistentes As células são
CÉLULAS SANGUÍNEAS. Professora Janaina Serra Azul Monteiro Evangelista
 CÉLULAS SANGUÍNEAS Professora Janaina Serra Azul Monteiro Evangelista No nosso sangue circulam vários tipos de células Glóbulos vermelhos Que também podem ser chamados hemácias ou eritrócitos. Glóbulos
CÉLULAS SANGUÍNEAS Professora Janaina Serra Azul Monteiro Evangelista No nosso sangue circulam vários tipos de células Glóbulos vermelhos Que também podem ser chamados hemácias ou eritrócitos. Glóbulos
TROMBOPOESE ou TROMBOCITOPOESE ou PLAQUETOPOESE
 TROMBOPOESE ou TROMBOCITOPOESE ou PLAQUETOPOESE Estrutura das plaquetas Fonte: Fundamentos de Hematologia, 2004. Pools plaquetários Medula óssea Circulante 2/3 sangue periférico 1/3 baço Pools plaquetários
TROMBOPOESE ou TROMBOCITOPOESE ou PLAQUETOPOESE Estrutura das plaquetas Fonte: Fundamentos de Hematologia, 2004. Pools plaquetários Medula óssea Circulante 2/3 sangue periférico 1/3 baço Pools plaquetários
Hematopoese. Prof. Prof. Dr. Valcinir Aloisio Scalla Vulcani Medicina Veterinária Universidade Federal de Goiás Regional Jataí
 Hematopoese Prof. Prof. Dr. Valcinir Aloisio Scalla Vulcani Medicina Veterinária Universidade Federal de Goiás Regional Jataí Hematopoese, hematopoiese, hemopoese Os três termos são encontrados na literatura
Hematopoese Prof. Prof. Dr. Valcinir Aloisio Scalla Vulcani Medicina Veterinária Universidade Federal de Goiás Regional Jataí Hematopoese, hematopoiese, hemopoese Os três termos são encontrados na literatura
TECIDO HEMATOPOIETICO E SANGUÍNEO
 TECIDO HEMATOPOIETICO E SANGUÍNEO CARACTERÍSTICAS O sangue é o único tecido conjuntivo líquido do copo; Funções: + Transporte (O 2, CO 2, nutrientes, resíduos, hormônios); + Regulação (ph, temperatura,
TECIDO HEMATOPOIETICO E SANGUÍNEO CARACTERÍSTICAS O sangue é o único tecido conjuntivo líquido do copo; Funções: + Transporte (O 2, CO 2, nutrientes, resíduos, hormônios); + Regulação (ph, temperatura,
Resposta Imunológica humoral. Alessandra Barone
 Resposta Imunológica humoral Alessandra Barone Estimulada por antígenos extracelulares Mediada por anticorpos produzidos por plasmócitos. Linfócito B Resposta T independente: Estimulada diretamente por
Resposta Imunológica humoral Alessandra Barone Estimulada por antígenos extracelulares Mediada por anticorpos produzidos por plasmócitos. Linfócito B Resposta T independente: Estimulada diretamente por
APOPTOSE, OU MORTE CELULAR PROGRAMADA
 APOPTOSE, OU MORTE CELULAR PROGRAMADA é um processo essencial para a manutenção do desenvolvimento dos seres vivos, sendo importante para eliminar células supérfluas ou defeituosas. As células têm um conjunto
APOPTOSE, OU MORTE CELULAR PROGRAMADA é um processo essencial para a manutenção do desenvolvimento dos seres vivos, sendo importante para eliminar células supérfluas ou defeituosas. As células têm um conjunto
Citologia e Histologia I Tecido Sanguíneo. Docente: Sheila C. Ribeiro Maio/2016
 Citologia e Histologia I Tecido Sanguíneo Docente: Sheila C. Ribeiro Maio/2016 Introdução Hematopoese Hemocitopoese Hemopoese Produção células sanguíneas Diferenciação e Maturação Renovação, Proliferação
Citologia e Histologia I Tecido Sanguíneo Docente: Sheila C. Ribeiro Maio/2016 Introdução Hematopoese Hemocitopoese Hemopoese Produção células sanguíneas Diferenciação e Maturação Renovação, Proliferação
TECIDOS LINFÓIDES PRIMÁRIOS ONTOGENIA DE LINFÓCITOS
 TECIDOS LINFÓIDES PRIMÁRIOS ONTOGENIA DE LINFÓCITOS Organização anatômica do sistema imune De onde vêm e para onde vão as células do sistema imune Como é a organização dos tecidos/órgãos linfóides Tecidos
TECIDOS LINFÓIDES PRIMÁRIOS ONTOGENIA DE LINFÓCITOS Organização anatômica do sistema imune De onde vêm e para onde vão as células do sistema imune Como é a organização dos tecidos/órgãos linfóides Tecidos
MSc. Romeu Moreira dos Santos
 MSc. Romeu Moreira dos Santos 2018 2015 INTRODUÇÃO As células do sistema imune (SI) inato e adaptativo estão presentes como: células circulantes no sangue e na linfa; aglomerados anatomicamente definidos
MSc. Romeu Moreira dos Santos 2018 2015 INTRODUÇÃO As células do sistema imune (SI) inato e adaptativo estão presentes como: células circulantes no sangue e na linfa; aglomerados anatomicamente definidos
Microambiente tumoral. Cristiane C. Bandeira A. Nimir
 Microambiente tumoral Cristiane C. Bandeira A. Nimir [email protected] PROGRESSÃO E AGRESSÃO TUMORAL CÉLULA NEOPLÁSICA: - Acúmulo de mutações CONTROLE DO CICLO CELULAR!! PROGRESSÃO E AGRESSÃO TUMORAL
Microambiente tumoral Cristiane C. Bandeira A. Nimir [email protected] PROGRESSÃO E AGRESSÃO TUMORAL CÉLULA NEOPLÁSICA: - Acúmulo de mutações CONTROLE DO CICLO CELULAR!! PROGRESSÃO E AGRESSÃO TUMORAL
Regulação gênica em Eucariotos. Prof. Dr. Marcelo Ricardo Vicari
 Regulação gênica em Eucariotos REGULAÇÃO GÊNICA Neurônio e célula de fígado: células de um mesmo indivíduo e que contêm a mesmo genoma REGULAÇÃO GÊNICA Diferenciação celular 1973 REGULAÇÃO GÊNICA Dolly:
Regulação gênica em Eucariotos REGULAÇÃO GÊNICA Neurônio e célula de fígado: células de um mesmo indivíduo e que contêm a mesmo genoma REGULAÇÃO GÊNICA Diferenciação celular 1973 REGULAÇÃO GÊNICA Dolly:
Hematopoese, células-tronco e diferenciação Imunofenotipagem. Silvia I.A.C.de Pires Ferreira HEMOSC Lab Medico Santa Luzia Florianópolis, SC
 Hematopoese, células-tronco e diferenciação Imunofenotipagem Silvia I.A.C.de Pires Ferreira HEMOSC Lab Medico Santa Luzia Florianópolis, SC Hematopoese - Conceito Processo biológico coordenado com a expressão
Hematopoese, células-tronco e diferenciação Imunofenotipagem Silvia I.A.C.de Pires Ferreira HEMOSC Lab Medico Santa Luzia Florianópolis, SC Hematopoese - Conceito Processo biológico coordenado com a expressão
Resposta imune adquirida do tipo celular
 Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune adquirida do tipo celular Profa. Dra. Silvana Boeira Imunidade adquirida Imunidade adaptativa = específica = adquirida
Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune adquirida do tipo celular Profa. Dra. Silvana Boeira Imunidade adquirida Imunidade adaptativa = específica = adquirida
UNIVERSIDADE ESTADUAL DA BAHIA - UNEB DEPARTAMENTO DE CIÊNCIAS DA VIDA DCV CCS006 - BIOLOGIA CELULAR. Sinalização Celular SALVADOR - BA 2016
 UNIVERSIDADE ESTADUAL DA BAHIA - UNEB DEPARTAMENTO DE CIÊNCIAS DA VIDA DCV CCS006 - BIOLOGIA CELULAR Sinalização Celular PROFª POLYANNA CARÔZO DE OLIVEIRA SALVADOR - BA 2016 Introdução Evolução da multicelularidade
UNIVERSIDADE ESTADUAL DA BAHIA - UNEB DEPARTAMENTO DE CIÊNCIAS DA VIDA DCV CCS006 - BIOLOGIA CELULAR Sinalização Celular PROFª POLYANNA CARÔZO DE OLIVEIRA SALVADOR - BA 2016 Introdução Evolução da multicelularidade
MSc. Romeu Moreira dos Santos
 MSc. Romeu Moreira dos Santos 2017 2015 INTRODUÇÃO As células do sistema imune (SI) inato e adaptativo estão presentes como: células circulantes no sangue e na linfa; aglomerados anatomicamente definidos
MSc. Romeu Moreira dos Santos 2017 2015 INTRODUÇÃO As células do sistema imune (SI) inato e adaptativo estão presentes como: células circulantes no sangue e na linfa; aglomerados anatomicamente definidos
Hematologia Clínica : bases fisiopatológicas
 Para entender Hematologia: compartimento 1 = medula óssea ( MO), onde são produzidas as células sanguíneas compartimento 2 = sangue periférico (SP), onde circulam as células compartimento 3 = órgãos linfóides
Para entender Hematologia: compartimento 1 = medula óssea ( MO), onde são produzidas as células sanguíneas compartimento 2 = sangue periférico (SP), onde circulam as células compartimento 3 = órgãos linfóides
Inflamação aguda e crônica. Profa Alessandra Barone
 e crônica Profa Alessandra Barone Inflamação Inflamação Resposta do sistema imune frente a infecções e lesões teciduais através do recrutamento de leucócitos e proteínas plasmáticas com o objetivo de neutralização,
e crônica Profa Alessandra Barone Inflamação Inflamação Resposta do sistema imune frente a infecções e lesões teciduais através do recrutamento de leucócitos e proteínas plasmáticas com o objetivo de neutralização,
Órgãos e Células do Sistema Imune
 Curso: farmácia Componente curricular: Imunologia Órgãos e Células do Sistema Imune DEYSIANE OLIVEIRA BRANDÃO ORIGEM DO SISTEMA IMUNE Origina-se a partir de células jovens denominadas STEM CELLS ou hemocitoblastos.
Curso: farmácia Componente curricular: Imunologia Órgãos e Células do Sistema Imune DEYSIANE OLIVEIRA BRANDÃO ORIGEM DO SISTEMA IMUNE Origina-se a partir de células jovens denominadas STEM CELLS ou hemocitoblastos.
BIOLOGIA. Moléculas, células e tecidos. Estudo dos tecidos Parte 2. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos Parte 2 Professor: Alex Santos Tópicos em abordagem Parte 2 Tecido conjuntivo I Visão geral do tecido conjuntivo II O tecido conjuntivo propriamente dito(tcpd) 2.1
BIOLOGIA Moléculas, células e tecidos Parte 2 Professor: Alex Santos Tópicos em abordagem Parte 2 Tecido conjuntivo I Visão geral do tecido conjuntivo II O tecido conjuntivo propriamente dito(tcpd) 2.1
Fases do ciclo celular O ciclo celular dos eucariotos está dividido em quatro fases separadas: M, G 1
 CICLO CELULAR A vida das células é formada por dois períodos: INTÉRFASE: inicia no fim da mitose e estende até iniciar a próxima mitose. MITOSE: Reprodução celular, com as seguintes finalidades: Nos unicelulares:
CICLO CELULAR A vida das células é formada por dois períodos: INTÉRFASE: inicia no fim da mitose e estende até iniciar a próxima mitose. MITOSE: Reprodução celular, com as seguintes finalidades: Nos unicelulares:
BIOLOGIA. Moléculas, células e tecidos. Ciclo celular. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos Professor: Alex Santos Tópicos em abordagem I Conceitos fundamentais II Estágios do ciclo celular III Visão geral da regulação do ciclo celular IV Importância do ciclo
BIOLOGIA Moléculas, células e tecidos Professor: Alex Santos Tópicos em abordagem I Conceitos fundamentais II Estágios do ciclo celular III Visão geral da regulação do ciclo celular IV Importância do ciclo
Bases celulares, histológicas e anatômicas da resposta imune. Pós-doutoranda Viviane Mariguela
 Bases celulares, histológicas e anatômicas da resposta imune Pós-doutoranda Viviane Mariguela As células do sistema imune (SI) inato e adaptativo estão presentes como: - células circulantes no sangue e
Bases celulares, histológicas e anatômicas da resposta imune Pós-doutoranda Viviane Mariguela As células do sistema imune (SI) inato e adaptativo estão presentes como: - células circulantes no sangue e
SANGUE Funções (transporte):
 Funções (transporte): Nutrientes Produtos do metabolismo Metábolitos Hormônios e outras moléculas sinalizadoras Eletrólitos Funções (transporte): Células diapedese tecidos diapedese microorganismo diapedese
Funções (transporte): Nutrientes Produtos do metabolismo Metábolitos Hormônios e outras moléculas sinalizadoras Eletrólitos Funções (transporte): Células diapedese tecidos diapedese microorganismo diapedese
Apoptose, ou morte celular programada
 Apoptose, ou morte celular programada é um processo essencial para a manutenção do desenvolvimento dos seres vivos, sendo importante para eliminar células supérfluas ou defeituosas. As células têm um conjunto
Apoptose, ou morte celular programada é um processo essencial para a manutenção do desenvolvimento dos seres vivos, sendo importante para eliminar células supérfluas ou defeituosas. As células têm um conjunto
Resposta Imunológica celular. Alessandra Barone
 Resposta Imunológica celular Alessandra Barone Resposta mediada pelos linfócitos T: TCD4 e TCD8 Resposta contra microrganismos que estão localizados no interior de fagócitos e de células não fagocíticas
Resposta Imunológica celular Alessandra Barone Resposta mediada pelos linfócitos T: TCD4 e TCD8 Resposta contra microrganismos que estão localizados no interior de fagócitos e de células não fagocíticas
03/03/2015. Acúmulo de Leucócitos. Funções dos Leucócitos. Funções dos Leucócitos. Funções dos Leucócitos. Inflamação Aguda.
 Acúmulo de Leucócitos Os leucócitos se acumulam no foco inflamatório seguindo uma sequência de tempo específica Neutrófilos (6-12 h) Monócitos: Macrófagos e céls. dendríticas (24-48 h) Linfócitos e plasmócitos
Acúmulo de Leucócitos Os leucócitos se acumulam no foco inflamatório seguindo uma sequência de tempo específica Neutrófilos (6-12 h) Monócitos: Macrófagos e céls. dendríticas (24-48 h) Linfócitos e plasmócitos
Prof. Gilson C. Macedo. Fases da resposta de células T. Principais características da ativação de células T. Sinais necessários
 Ativação de Linfócitos T Para que ocorra ação efetora das células T há necessidade de ativação deste tipo celular. Prof. Gilson C. Macedo Fases da resposta de células T Fases da resposta de células T Ativação
Ativação de Linfócitos T Para que ocorra ação efetora das células T há necessidade de ativação deste tipo celular. Prof. Gilson C. Macedo Fases da resposta de células T Fases da resposta de células T Ativação
Imunologia. Diferenciar as células e os mecanismos efetores do Sistema imune adquirido do sistema imune inato. AULA 02: Sistema imune adquirido
 Imunologia AULA 02: Sistema imune adquirido Professor Luiz Felipe Leomil Coelho Departamento de Ciências Biológicas E-mail: [email protected] OBJETIVO Diferenciar as células e os mecanismos efetores
Imunologia AULA 02: Sistema imune adquirido Professor Luiz Felipe Leomil Coelho Departamento de Ciências Biológicas E-mail: [email protected] OBJETIVO Diferenciar as células e os mecanismos efetores
Imunologia. Introdução ao Sistema Imune. Lairton Souza Borja. Módulo Imunopatológico I (MED B21)
 Imunologia Introdução ao Sistema Imune Módulo Imunopatológico I (MED B21) Lairton Souza Borja Objetivos 1. O que é o sistema imune (SI) 2. Revisão dos componentes do SI 3. Resposta imune inata 4. Inflamação
Imunologia Introdução ao Sistema Imune Módulo Imunopatológico I (MED B21) Lairton Souza Borja Objetivos 1. O que é o sistema imune (SI) 2. Revisão dos componentes do SI 3. Resposta imune inata 4. Inflamação
Importância dos processos de sinalização. Moléculas sinalizadoras (proteínas, peptídeos, aminoácidos, hormônios, gases)
 Sinalização celular Importância dos processos de sinalização Seres unicelulares Seres multicelulares Moléculas sinalizadoras (proteínas, peptídeos, aminoácidos, hormônios, gases) Receptores Proteínas -
Sinalização celular Importância dos processos de sinalização Seres unicelulares Seres multicelulares Moléculas sinalizadoras (proteínas, peptídeos, aminoácidos, hormônios, gases) Receptores Proteínas -
Células do Sistema Imune
 Tecnologias de Informação e Comunicação na Educação Professora Ana Paula Peconick Tutor Karlos Henrique Martins Kalks Lavras/MG 2011 1 P ágina Ficha catalográfica preparada pela Divisão de Processos Técnicos
Tecnologias de Informação e Comunicação na Educação Professora Ana Paula Peconick Tutor Karlos Henrique Martins Kalks Lavras/MG 2011 1 P ágina Ficha catalográfica preparada pela Divisão de Processos Técnicos
Bases celulares, histológicas e anatômicas da resposta imune. Pós-doutoranda Viviane Mariguela
 Bases celulares, histológicas e anatômicas da resposta imune Pós-doutoranda Viviane Mariguela As células do SI inato e adaptativo estão presentes como: - células circulantes no sangue e na linfa; - aglomerados
Bases celulares, histológicas e anatômicas da resposta imune Pós-doutoranda Viviane Mariguela As células do SI inato e adaptativo estão presentes como: - células circulantes no sangue e na linfa; - aglomerados
TECIDO CONJUNTIVO São responsáveis pelo estabelecimento e
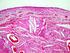 Prof. Bruno Pires TECIDO CONJUNTIVO São responsáveis pelo estabelecimento e do corpo. Isso ocorre pela presença de um conjunto de moléculas que conectam esse tecido aos outros, por meio da sua. Estruturalmente
Prof. Bruno Pires TECIDO CONJUNTIVO São responsáveis pelo estabelecimento e do corpo. Isso ocorre pela presença de um conjunto de moléculas que conectam esse tecido aos outros, por meio da sua. Estruturalmente
Ontogenia de Linfócito T. Alessandra Barone
 Ontogenia de Linfócito T Alessandra Barone Ontogenia de Linfócitos Desenvolvimento dos linfócitos Necessidade de desenvolvimento e maturação de linfócitos para produção de receptores de antígenos Estímulos
Ontogenia de Linfócito T Alessandra Barone Ontogenia de Linfócitos Desenvolvimento dos linfócitos Necessidade de desenvolvimento e maturação de linfócitos para produção de receptores de antígenos Estímulos
Bases celulares, histológicas e anatômicas da resposta imune. Pós-doutoranda Viviane Mariguela
 Bases celulares, histológicas e anatômicas da resposta imune Pós-doutoranda Viviane Mariguela As células do sistema imune (SI) inato e adaptativo estão presentes como: - células circulantes no sangue e
Bases celulares, histológicas e anatômicas da resposta imune Pós-doutoranda Viviane Mariguela As células do sistema imune (SI) inato e adaptativo estão presentes como: - células circulantes no sangue e
Tecido conjuntivo e tecido osseo
 Tecido conjuntivo e tecido osseo Tipos de tecido conjuntivo Tecidos responsáveis por unir, ligar, nutrir, proteger e sustentar os outros tecidos Tecidos Conjuntivos Propriamente Ditos Frouxo Denso Modelado
Tecido conjuntivo e tecido osseo Tipos de tecido conjuntivo Tecidos responsáveis por unir, ligar, nutrir, proteger e sustentar os outros tecidos Tecidos Conjuntivos Propriamente Ditos Frouxo Denso Modelado
Biologia Molecular e Celular II. Controle do crescimento celular
 Biologia Molecular e Celular II Controle do crescimento celular 2016 Controle extracelular do crescimento e divisão Tamanho de um órgão ou organismo é definido por 3 processos celulares: Crescimento; Divisão;
Biologia Molecular e Celular II Controle do crescimento celular 2016 Controle extracelular do crescimento e divisão Tamanho de um órgão ou organismo é definido por 3 processos celulares: Crescimento; Divisão;
Hematopoiese. Aarestrup, F.M.
 Hematopoiese Stem cells - pluripotencial Baixa frequência -1/10 4 cels da M.O Proliferação e diferenciação - linhagens linfóide e mielóide (3.7 X 10 11 cels/dia) Cels do estroma M.O - hematopoietic-inducing
Hematopoiese Stem cells - pluripotencial Baixa frequência -1/10 4 cels da M.O Proliferação e diferenciação - linhagens linfóide e mielóide (3.7 X 10 11 cels/dia) Cels do estroma M.O - hematopoietic-inducing
Aspectos Moleculares da Inflamação:
 Patologia Molecular Lucas Brandão Aspectos Moleculares da Inflamação: os mediadores químicos inflamatórios Inflamação São uma série de eventos programados que permitem com que Leucócitos e outras proteínas
Patologia Molecular Lucas Brandão Aspectos Moleculares da Inflamação: os mediadores químicos inflamatórios Inflamação São uma série de eventos programados que permitem com que Leucócitos e outras proteínas
Sangue e Sistema Linfoide
 Sangue e Sistema Linfoide Objetivos da aula os estudantes deverão ser capazes de... Listar os componentes celulares (fração celular) e não celulares (fração fluida) do sangue e relatar sua morfologia e
Sangue e Sistema Linfoide Objetivos da aula os estudantes deverão ser capazes de... Listar os componentes celulares (fração celular) e não celulares (fração fluida) do sangue e relatar sua morfologia e
Imunologia. Células do Sistema Imune. Professora Melissa Kayser
 Imunologia Células do Sistema Imune Professora Melissa Kayser Composição do sangue Origem Origem Células sanguíneas Hematoxilina: Corante básico. Eosina: Corante ácido. Células do sistema imune Leucograma
Imunologia Células do Sistema Imune Professora Melissa Kayser Composição do sangue Origem Origem Células sanguíneas Hematoxilina: Corante básico. Eosina: Corante ácido. Células do sistema imune Leucograma
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS. Tecido Conjuntivo
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Tecido Conjuntivo Disciplina: Histologia Prof. Me. Cássio Resende de Morais Características gerais Apresenta diferentes
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Tecido Conjuntivo Disciplina: Histologia Prof. Me. Cássio Resende de Morais Características gerais Apresenta diferentes
BIOLOGIA. Moléculas, células e tecidos. Estudo dos tecidos Parte. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos Parte Professor: Alex Santos Tópicos em abordagem Parte 6 Tecido sanguíneo I Características II Funções III Composição IV Visão geral da hematopoese: V Considerações
BIOLOGIA Moléculas, células e tecidos Parte Professor: Alex Santos Tópicos em abordagem Parte 6 Tecido sanguíneo I Características II Funções III Composição IV Visão geral da hematopoese: V Considerações
HEMATOLOGIA ºAno. 8ª Aula. Hematologia- 2010/2011
 HEMATOLOGIA 2010-11 3ºAno Prof. Leonor Correia 8ª Aula Hematologia- 2010/2011 Monocitopoiese Monócitos (morfologia, funções, cinética, composição química) Linfocitopoiese - Diferenciação linfocitária (morfológica,
HEMATOLOGIA 2010-11 3ºAno Prof. Leonor Correia 8ª Aula Hematologia- 2010/2011 Monocitopoiese Monócitos (morfologia, funções, cinética, composição química) Linfocitopoiese - Diferenciação linfocitária (morfológica,
Ciclo Celular e Controle do Ciclo Celular
 Ciclo Celular e Controle do Ciclo Celular Profa. Dra. Maria Tercília Vilela de Azeredo Oliveira Profa. Dra. Ester Tartarotti MSc. Rita Luiza Peruquetti Divisão Celular Deve ser regulada e Coordenada Ciclo
Ciclo Celular e Controle do Ciclo Celular Profa. Dra. Maria Tercília Vilela de Azeredo Oliveira Profa. Dra. Ester Tartarotti MSc. Rita Luiza Peruquetti Divisão Celular Deve ser regulada e Coordenada Ciclo
CITOCINAS. Aarestrup, F.M.
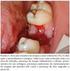 CITOCINAS Propriedades gerais Proteínas de baixo peso molecular Comunicação Cel-Cel Mensageiros do sistema imune Receptores de membrana Signal transduction Célula Alvo Expressão de genes Gene Citocina
CITOCINAS Propriedades gerais Proteínas de baixo peso molecular Comunicação Cel-Cel Mensageiros do sistema imune Receptores de membrana Signal transduction Célula Alvo Expressão de genes Gene Citocina
Fisiologia das Plaquetas
 Fisiologia das Plaquetas Definição Funções Origem/Formação = Trombocitopoese Estrutura: 4 regiões Não Activadas e Activadas Participação na Hemostase Caso: Plasma Rico em Plaquetas Componentes do Sangue
Fisiologia das Plaquetas Definição Funções Origem/Formação = Trombocitopoese Estrutura: 4 regiões Não Activadas e Activadas Participação na Hemostase Caso: Plasma Rico em Plaquetas Componentes do Sangue
Tecido Conjuntivo. Prof Cristiano Ricardo Jesse
 Tecido Conjuntivo Prof Cristiano Ricardo Jesse Tecido conjuntivo Estabelecimento e manutenção da forma do corpo Conjunto de moléculas Conecta e liga as células e órgãos Suporte ao corpo Tecido conjuntivo
Tecido Conjuntivo Prof Cristiano Ricardo Jesse Tecido conjuntivo Estabelecimento e manutenção da forma do corpo Conjunto de moléculas Conecta e liga as células e órgãos Suporte ao corpo Tecido conjuntivo
PROJET O SANGUE PROFº ME. FERNANDO BELAN DAT A CLIENT E BIOLOGIA MAIS
 PROJET O SANGUE PROFº ME. FERNANDO BELAN DAT A 2016 CLIENT E BIOLOGIA MAIS Função Leva O2 e nutrientes para todas as células; Retra CO2 e excretas. Transporta hormônios; Proteção contra invasores (leucócitos)
PROJET O SANGUE PROFº ME. FERNANDO BELAN DAT A 2016 CLIENT E BIOLOGIA MAIS Função Leva O2 e nutrientes para todas as células; Retra CO2 e excretas. Transporta hormônios; Proteção contra invasores (leucócitos)
Reparação. Regeneração Tecidual 30/06/2010. Controlada por fatores bioquímicos Liberada em resposta a lesão celular, necrose ou trauma mecânico
 UNIVERSIDADE FEDERAL DO PARANÁ COORDENAÇÃO DO CURSO DE MEDICINA VETERINÁRIA DISCIPLINA DE PATOLOGIA VETERINÁRIA Reparação Prof. Raimundo Tostes Reparação Regeneração: reposição de um grupo de células destruídas
UNIVERSIDADE FEDERAL DO PARANÁ COORDENAÇÃO DO CURSO DE MEDICINA VETERINÁRIA DISCIPLINA DE PATOLOGIA VETERINÁRIA Reparação Prof. Raimundo Tostes Reparação Regeneração: reposição de um grupo de células destruídas
Profº André Montillo
 Profº André Montillo www.montillo.com.br Sistema Imunológico Simples: Não Antecipatório / Inespecífico Sistema Imune Antígeno Específico: Antecipatório Sistema Imunológico Simples: Não Antecipatório /
Profº André Montillo www.montillo.com.br Sistema Imunológico Simples: Não Antecipatório / Inespecífico Sistema Imune Antígeno Específico: Antecipatório Sistema Imunológico Simples: Não Antecipatório /
Disciplina: Imunologia Tema: Imunologia Iniciando o Conteúdo
 Disciplina: Imunologia Tema: Imunologia Iniciando o Conteúdo Os microrganismos patogênicos são capazes de provocar doenças? A principal função do sistema imunológico é, prevenir ou limitar infecções causadas
Disciplina: Imunologia Tema: Imunologia Iniciando o Conteúdo Os microrganismos patogênicos são capazes de provocar doenças? A principal função do sistema imunológico é, prevenir ou limitar infecções causadas
Tecido Conjuntivo. Professora: Me. Gilcele
 Tecido Conjuntivo Professora: Me. Gilcele Tecido Conjuntivo - Características Histológicas: Células separadas por muito material extracelular Menor densidade celular Vários tipos de células Vasos sangüíneos
Tecido Conjuntivo Professora: Me. Gilcele Tecido Conjuntivo - Características Histológicas: Células separadas por muito material extracelular Menor densidade celular Vários tipos de células Vasos sangüíneos
06/11/2009 TIMO. Seleção e educação de linfócitos ÓRGÃOS LINFÓIDES E CÉLULAS DO SISTEMA IMUNE ÓRGÃOS LINFÓIDES. Primários: Medula óssea e timo
 ÓRGÃOS LINFÓIDES Primários: Medula óssea e timo ÓRGÃOS LINFÓIDES E CÉLULAS DO SISTEMA IMUNE Secundários: Linfonodos Baço Tecidos linfóides associado a mucosa Prof. Renato Nisihara Ossos chatos Esterno,,
ÓRGÃOS LINFÓIDES Primários: Medula óssea e timo ÓRGÃOS LINFÓIDES E CÉLULAS DO SISTEMA IMUNE Secundários: Linfonodos Baço Tecidos linfóides associado a mucosa Prof. Renato Nisihara Ossos chatos Esterno,,
Tecidos do Corpo Humano
 Tecidos do Corpo Humano Epitelial Conjuntivo Muscular Nervoso Nutrição, Fono_ 2018 Tecido Conjuntivo Constituído por um grupo de células com características diversificadas, imersas em matriz extracelular
Tecidos do Corpo Humano Epitelial Conjuntivo Muscular Nervoso Nutrição, Fono_ 2018 Tecido Conjuntivo Constituído por um grupo de células com características diversificadas, imersas em matriz extracelular
ONCOLOGIA. Aula I Profª.Enfª: Darlene Carvalho (www.darlenecarvalho.webnode.com.br)
 ONCOLOGIA Aula I Profª.Enfª: Darlene Carvalho (www.darlenecarvalho.webnode.com.br) CLASSIFICAÇÃO DAS CÉLULAS Lábeis Estáveis Perenes CLASSIFICAÇÃO DAS CÉLULAS Células lábeis: São aquelas em constante renovação
ONCOLOGIA Aula I Profª.Enfª: Darlene Carvalho (www.darlenecarvalho.webnode.com.br) CLASSIFICAÇÃO DAS CÉLULAS Lábeis Estáveis Perenes CLASSIFICAÇÃO DAS CÉLULAS Células lábeis: São aquelas em constante renovação
Resposta imune inata (natural ou nativa)
 Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune inata (natural ou nativa) Profa. Dra. Silvana Boeira Acreditou-se por muitos anos que a imunidade inata fosse inespecífica
Universidade Federal do Pampa Campus Itaqui Curso de Nutrição Imunologia Resposta imune inata (natural ou nativa) Profa. Dra. Silvana Boeira Acreditou-se por muitos anos que a imunidade inata fosse inespecífica
03/08/2016. Patologia Clínica e Análises Laboratoriais Prof. Me. Diogo Gaubeur de Camargo
 2 3 4 5 6 Patologia Clínica e Análises Laboratoriais Prof. Me. Diogo Gaubeur de Camargo Especialidade médica Exames complementares Análise: Sangue; Urina; Líquor; Liquído peritoneal; Etc... Hematologia
2 3 4 5 6 Patologia Clínica e Análises Laboratoriais Prof. Me. Diogo Gaubeur de Camargo Especialidade médica Exames complementares Análise: Sangue; Urina; Líquor; Liquído peritoneal; Etc... Hematologia
Apresenta abundante material intersticial (matriz intersticial) e células afastadas.
 TECIDO CONJUNTIVO Apresenta abundante material intersticial (matriz intersticial) e células afastadas. A matriz intersticial apresenta: substância fundamental amorfa. fibras proteicas. Os principais tipos
TECIDO CONJUNTIVO Apresenta abundante material intersticial (matriz intersticial) e células afastadas. A matriz intersticial apresenta: substância fundamental amorfa. fibras proteicas. Os principais tipos
Bases Moleculares do Desenvolvimento II
 Faculdade de Medicina de Ribeirão Preto - USP Módulo de Embriologia Geral Bases Moleculares do Desenvolvimento II Prof. Carolina Gonçalves Santos Questões da Biologia do Desenvolvimento 1 - Morfogênese
Faculdade de Medicina de Ribeirão Preto - USP Módulo de Embriologia Geral Bases Moleculares do Desenvolvimento II Prof. Carolina Gonçalves Santos Questões da Biologia do Desenvolvimento 1 - Morfogênese
Sangue: funções gerais
 Sangue Sangue: funções gerais Transporte de nutrientes para órgãos e tecidos; Regulação térmica e hídrica; Transporte de gases para órgãos e tecidos; Defesa do organismo; Coagulação. Componentes do Sangue
Sangue Sangue: funções gerais Transporte de nutrientes para órgãos e tecidos; Regulação térmica e hídrica; Transporte de gases para órgãos e tecidos; Defesa do organismo; Coagulação. Componentes do Sangue
CICLO CELULAR Eduardo Montagner Dias
 CICLO CELULAR Eduardo Montagner Dias O ciclo celular é um processo através do qual uma célula somática duplica seu material genético e o reparte igualmente às suas células-filhas. É didaticamente dividido
CICLO CELULAR Eduardo Montagner Dias O ciclo celular é um processo através do qual uma célula somática duplica seu material genético e o reparte igualmente às suas células-filhas. É didaticamente dividido
ESPECIALIZAÇÃO OU DIFERENCIAÇÃO CELULAR. Moisés Araújo
 ESPECIALIZAÇÃO OU DIFERENCIAÇÃO CELULAR O QUE É ESPECIALIZAÇÃO CELULAR? CONJUNTO DAS MODIFICAÇÕES QUIMICAS, FÍSICAS OU ESTRUTURAIS E FUNCIONAIS DAS CÉLULAS EMBRIONÁRIAS, INICIALMENTE SIMPLES E INDIFERENCIADAS,
ESPECIALIZAÇÃO OU DIFERENCIAÇÃO CELULAR O QUE É ESPECIALIZAÇÃO CELULAR? CONJUNTO DAS MODIFICAÇÕES QUIMICAS, FÍSICAS OU ESTRUTURAIS E FUNCIONAIS DAS CÉLULAS EMBRIONÁRIAS, INICIALMENTE SIMPLES E INDIFERENCIADAS,
Histologia. Leonardo Rodrigues EEEFM GRAÇA ARANHA
 Histologia. Leonardo Rodrigues EEEFM GRAÇA ARANHA Histologia Ramo da Biologia que estuda os tecidos; Tecido - é um conjunto de células, separadas ou não por substâncias intercelulares e que realizam determinada
Histologia. Leonardo Rodrigues EEEFM GRAÇA ARANHA Histologia Ramo da Biologia que estuda os tecidos; Tecido - é um conjunto de células, separadas ou não por substâncias intercelulares e que realizam determinada
Apoptose. Prof. Tiago Collares, Dr. (MSN) ( )
 Apoptose Prof. Tiago Collares, Dr. [email protected] (MSN) [email protected] (e-mail ) $99.50 $82.74 $31.86 Necessidades de Morte Celular em Organismos Multicelulares - Característica latente;
Apoptose Prof. Tiago Collares, Dr. [email protected] (MSN) [email protected] (e-mail ) $99.50 $82.74 $31.86 Necessidades de Morte Celular em Organismos Multicelulares - Característica latente;
Aulas e discussão dos casos.
 Aulas e discussão dos casos http://hematofmusp.weebly.com Hematologia Clínica Objetivos do curso Sintomas e Sinais Clínicos História e Exame Físico O que não está funcionando no Sistema Raciocínio Clínico
Aulas e discussão dos casos http://hematofmusp.weebly.com Hematologia Clínica Objetivos do curso Sintomas e Sinais Clínicos História e Exame Físico O que não está funcionando no Sistema Raciocínio Clínico
Expansão clonal de Linfócitos T Helper
 Expansão clonal de Linfócitos T Helper Ativação dos linfócitos T Entrada do antígeno no organismo Captura do antígeno pelas células dendríticas Migração da célula dendrítica para gânglio linfático ou baço
Expansão clonal de Linfócitos T Helper Ativação dos linfócitos T Entrada do antígeno no organismo Captura do antígeno pelas células dendríticas Migração da célula dendrítica para gânglio linfático ou baço
Tecido conjuntivo. Capítulos 5, 6, 7, 8 e 12 Histologia Básica Junqueira e Carneiro
 Tecido conjuntivo Capítulos 5, 6, 7, 8 e 12 Histologia Básica Junqueira e Carneiro Tecido conjuntivo Tecido conjuntivo propriamente dito é composto de uma porção celular e de uma matriz extracelular que
Tecido conjuntivo Capítulos 5, 6, 7, 8 e 12 Histologia Básica Junqueira e Carneiro Tecido conjuntivo Tecido conjuntivo propriamente dito é composto de uma porção celular e de uma matriz extracelular que
O SANGUE HUMANO. Professora Catarina
 O SANGUE HUMANO Professora Catarina SANGUE Principais funções: Transportar O 2 e nutrientes a todas as células do corpo; Recolher CO 2 e excreções; Transportar hormônios; Proteger o corpo contra a invasão
O SANGUE HUMANO Professora Catarina SANGUE Principais funções: Transportar O 2 e nutrientes a todas as células do corpo; Recolher CO 2 e excreções; Transportar hormônios; Proteger o corpo contra a invasão
Complexo Principal de Histocompatibilidade. Alessandra Barone
 Complexo Principal de Histocompatibilidade Alessandra Barone MHC Complexo principal de histocompatibilidade (MHC) ou antígeno leucocitário humano (HLA) Conjunto de proteínas associadas a membrana celular
Complexo Principal de Histocompatibilidade Alessandra Barone MHC Complexo principal de histocompatibilidade (MHC) ou antígeno leucocitário humano (HLA) Conjunto de proteínas associadas a membrana celular
UNISALESIANO. Profª Tatiani
 UNISALESIANO Profª Tatiani CARACTERÍSTICAS FÍSICO- QUÍMICAS DO SANGUE O sangue constitui o líquido corporal que se encontra dentro dos vasos sanguíneos e que através do sistema circulatório participa da
UNISALESIANO Profª Tatiani CARACTERÍSTICAS FÍSICO- QUÍMICAS DO SANGUE O sangue constitui o líquido corporal que se encontra dentro dos vasos sanguíneos e que através do sistema circulatório participa da
Tecido Conjuntivo. Prof a. Marta G. Amaral, Dra. Histofisiologia
 Tecido Conjuntivo Prof a. Marta G. Amaral, Dra. Histofisiologia Origem: mesênquima Características: Células + material intercelular (SFA e fibras) Funções 1. Sustentação e preenchimento: osso, estroma
Tecido Conjuntivo Prof a. Marta G. Amaral, Dra. Histofisiologia Origem: mesênquima Características: Células + material intercelular (SFA e fibras) Funções 1. Sustentação e preenchimento: osso, estroma
MORTE CELULAR NECROSE APOPTOSE AUTOFAGIA ACIDENTAL PROGRAMADA TRAUMATISMO DOENÇA PROCESSO FISIOLÓGICO NORMAL PROGRAMA GENETICAMENTE REGULADO
 Morte Celular MORTE CELULAR ACIDENTAL PROGRAMADA TRAUMATISMO DOENÇA PROCESSO FISIOLÓGICO NORMAL PROCESSO PATOLÓGICO PROGRAMA GENETICAMENTE REGULADO NECROSE APOPTOSE AUTOFAGIA MORTE CELULAR ACIDENTAL PROGRAMADA
Morte Celular MORTE CELULAR ACIDENTAL PROGRAMADA TRAUMATISMO DOENÇA PROCESSO FISIOLÓGICO NORMAL PROCESSO PATOLÓGICO PROGRAMA GENETICAMENTE REGULADO NECROSE APOPTOSE AUTOFAGIA MORTE CELULAR ACIDENTAL PROGRAMADA
Células do Sistema Imune
 Células Células do Sistema Imune Linfócitos NK Células Dendríticas Macrófagos e Monócitos Neutrófilos Eosinófilos Mastócitos Basófilos 1 2 Linfócitos São as únicas células com receptores específicos para
Células Células do Sistema Imune Linfócitos NK Células Dendríticas Macrófagos e Monócitos Neutrófilos Eosinófilos Mastócitos Basófilos 1 2 Linfócitos São as únicas células com receptores específicos para
Lisossomas - são vesículas limitadas por membrana distintas dos grânulos alfa e contêm enzimas lisossómicas;
 Plaquetas Células pequenas e sem núcleo, formadas na medula óssea a partir do citoplasma de grandes células chamadas megacariócitos; Formam tampões que ocluem os locais de lesão vascular, aderindo ao tecido
Plaquetas Células pequenas e sem núcleo, formadas na medula óssea a partir do citoplasma de grandes células chamadas megacariócitos; Formam tampões que ocluem os locais de lesão vascular, aderindo ao tecido
