Cinética química: como estudar os fatores que interferem na velocidade das reações?
|
|
|
- Washington de Mendonça
- 5 Há anos
- Visualizações:
Transcrição
1 CINÉTICA QUÍMICA: COMO ESTUDAR OS FATORES QUE INTERFEREM NA VELOCIDADE DAS REAÇÕES? ORIENTADOR METODOLÓGICO Cinética química: como estudar os fatores que interferem na velocidade das reações? Objetivos de aprendizagem: Conceituar velocidade média e relacionar cinética química com cálculo estequiométrico; Compreender os fatores que interferem na velocidade de uma reação química; Expressar a lei de velocidade de uma reação química; 1) A ) C 3) E 4) A Determinar a energia de ativação. Praticando: 5) a) A limalha de ferro tem superfície de contato maior que a barra de ferro, reagindo mais rapidamente. b) O níquel atua como catalisador, diminuindo a energia de ativação da reação e, consequentemente, aumentando a sua velocidade. 6) a) A lanterna II apresentará chama mais inten- mente granulado) possui maior superfície de contato do que o da lanterna I, resultando em uma maior velocidade da reação de formação de acetileno. Assim, a queima de uma maior quantidade de acetileno por unidade de tempo faz com que a chama da lanterna II seja mais intensa. b) A lanterna II se apagará primeiro, pois o carbure- sendo totalmente consumido em menos tempo. 7) B 8) C 9) a) V = k x [H O ] x [I - ] x [H + ] b) Porque a reação não é elementar. 10) a) V = k x [HBr] x [O ] b) 0, mol 11) Aumenta 9 vezes 1) a) 3 a ordem. b) K = 0,384 L x mol - x s -1 13) a) Aumenta 4 vezes. b) Aumenta vezes. c) Aumenta 7 vezes. 14) F V F F V F 15) B 16) B Aprofundando: 17) 5g/min 0g/min 15g/min 1,5g/min 18) = 3,0 x 10-4 mol x L -1 x s -1 19) D 0) A 1) C ) D 3) B 4) A 5) A 6) D 7) A 1 EMQUI04
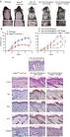
2 CINÉTICA QUÍMICA: COMO ESTUDAR OS FATORES QUE INTERFEREM NA VELOCIDADE DAS REAÇÕES? 8) Taxa de formação de ácido lático: 1,5 x 10 - mmol/l x s. 9) V = 0,05 mol/min de O. 30) V = 48 mol/h. 31) a) V = 0,005 mol/min b) V = 0,005 mol/min c) V = 0,006 mol/min (HBr) e V = 0,003 mol/min (Br ) 3) I, pois a inclinação da reta é maior. 33) a) V = k x [NO ] x [O 3 ] b) A velocidade duplica. 34) Como as ordens de reação são iguais ao res- [B] 1 Substituindo dados do teste 3, temos: = k k = L. mol -. s -1 Substituindo os dados dos testes e 3, temos: (1) V =. 10. X 1 () V =. X. 0 1 V =. X. 0 Igualando as equações 1 e :. 10. X =. X x = x = 0x x = 10 mol/l b) A curva I corresponde à reação com o alumínio em pó. A curva II corresponde à reação com o alumínio em placas. Esta associação ocorre porque o alumínio pulverizado, devido a sua maior superfície de contato, reagirá mais rapidamente. 40) v = k [H ] x [IC ] 41) Expressão da velocidade: v = k [HBr] [NO ]; logo, a ordem global é igual a. Mecanismo I. Na etapa lenta, as ordens de reação do HBr e do NO são iguais às obtidas experimentalmente. 4) D 43) a) Como a velocidade média permanece constante no intervalo de tempo entre 0 e 14 min, a velocidade inicial é dada por: V 1 = -([H ] [H ] inicial ) / (t t inicial ) = (3 10) / (14-0) = 0,5mol/L.min. b) Após 10 min de reação, [H ] = 5 mol/l Como H + I HI, [HI] após 10 min = 10 mol/l 35) a) X: a ordem; Y: 1 a ordem. b) Aumenta 18 vezes. 36) C 37) A 38) A 39) a) Tomando 1 L como referência de volume: Curva I: 0,6 mol x L -1 produzido em 1 min v 1 = 0,6 mol x L -1 x min -1 Curva II: 0, mol produzido em 1 min v = 0, mol x L -1 x min -1 Razão: 0,6 0, = 3 EMQUI04
3 EQUILÍBRIO QUÍMICO: DESLOCAMENTO DE EQUILÍBRIO E CÁLCULO DE PH ORIENTADOR METODOLÓGICO Equilíbrio químico: deslocamento de equilíbrio e cálculo de ph Objetivos de aprendizagem: Compreender quando uma reação reversível está em equilíbrio químico; Expressar a constante de equilíbrio em função das concentrações molares e em função das pressões parciais Estudar os fatores que provocam o deslocamento de um equilíbrio químico; Calcular o grau e a constante de ionização e de dissociação; 1) C ) D 3) E 4) D 5) C 6) A Determinar os valores de ph e poh. Praticando: 7) K c = 5,0 x 10 - mol/l; K p = 3,17 atm 8) (UERJ) A 9) H (g) + I (g) HI(g) 0,50 M 0,50 M 0,0M -x -x + x (0,50 - x) M (0,50 - x) M xm K = c [HI] [H ] [I ] x 0,39 M = (x) x 0,50 - x (0,50 - x) 10) a) t = 400 milissegundos e no equilíbrio as concentrações das espécies presentes não mais se alteram. b) Kc = [FeSCN + ]/[Fe +3 ].[SCN] = (5x10 3 )/(8x10 3 ). (x10 3 ) = 31,5. 11) D 1) B 13) A reação direta é exotérmica porque o aumento da temperatura diminuiu a constante de equilíbrio neste sentido, favorecendo a reação inversa e indicando que a reação inversa é endotérmica. 14) C 15) A 16) A 17) (UNICAMP) A concentração máxima de nico- por volta de 10 minutos e é de 0 ng/ml. Isso corresponde a 0 x 10 9 /16 mol/ml, ou x 10-7 mol/l. A concentração de H + no sangue quando o ph é 7,4 é, aproximadamente, 10-7,4 mol/l, ou seja, 4 x 10-8 mol/ L, um valor menor que x 10-7 mol/l, que é a concentração total de nicotina no sangue. b) A constante de equilíbrio da reação é dada por K= [nicotina][h + ]/[nicotina-h + ], ou seja, 1,0 x 10-8 /4 x 10-8 = [nicotina]/[nicotina-h + ] 0,5 = [nicotina]/[nicotina-h + ] 0,5 x [nicotina-h + ] = [nicotina] 18) D 19) A 0) B 1) E [H ] = [I ] = 0,50-0,39 = 0,11M [HI] = x 0,39 = 0,78 M ) C 3 EMQUI05
4 EQUILÍBRIO QUÍMICO: DESLOCAMENTO DE EQUILÍBRIO E CÁLCULO DE PH 3) D 4) B 5) B 6) E 7) A Aprofundando: 8) a) A expressão da constante de equilíbrio para a reação acima é: K = [NH 3(g) ] / [N (g) ] [H (g) ] 3 Substituindo-se pelas concentrações de equilíbrio, encontra-se o valor da constante: K = (0,15) /(0,15)(1) 3 = 0,15 b) 1 mol de N (g) mols NH 3(g) Logo: 8g de N produzirão x17g de NH 3 = 34g 9) (UNICAMP) B 30) (ENEM) D 31) (ENEM) B 3) B 33) D 34) A 35) B 36) E 37) D 38) D 39) (UERJ) A 40) (ENEM) D 41) B 4) a) O ácido mais fraco é o HClO, pois apresenta menor constante de ionização. b) É o equilíbrio III, pois se o valor do equilíbrio é ambos os reagentes são maiores que as concentrações dos produtos. 43) a) K b = [NH 4+ ]x[oh -] /[NH 4 OH] b) O equilíbrio será deslocado para a esquerda, diminuindo o ph da solução. c) K b ; M = 0,0 mol/l d) 00 x 0,0 = M x 800 M = 0,005 mol/l 44) a) Adição de C (s) não altera o equilíbrio, pois sua concentração é constante. b) Equilíbrio desloca-se para a direita, pois o aumento de temperatura desloca o equilíbrio no sentido da reação endotérmica. c) Adição de catalisador não desloca equilíbrio. 45) E 46) Ácido carbônico, ácido acético e ácido cítrico. 47) I) a) K a = 1,69 x 10-5 b) ph =,89 II) a) Não se altera. b) ph = 3,89 48) [ H + ] X / [ H + ] Y = ) (UERJ) [OH-] = 10- poh = - log 10- = ph = 14 - ph = 1 A concentração diminuirá. Os íons H+ do ácido irão reagir com os íons OH- do meio, formando água. O equilíbrio irá se deslocar para a direita e a amônia será consumida. 50) E 51) A 5) C 53) E 54) D EMQUI05 4
5 EQUILÍBRIO QUÍMICO: DESLOCAMENTO DE EQUILÍBRIO E CÁLCULO DE PH 55) E 56) C 57) a) K a = [H + ]x[c H 3 O ] / [HC H 3 O ] b) [OH - ] 10-1 mol.l -1 poh = 1 ph = 13 58) B 59) B 60) a) N. b) Nenhuma. c) Ambas as concentrações aumentam; d) [H ] aumenta e [NH 3 ] diminui. 61) a) K c =, b) A reação é exotérmica porque, quando ocorre uma elevação da temperatura ( entre t 4 e t 5 ), observa-se a diminuição da concentração de produto (N O 4 ), mostrando que o equilíbrio é deslocado no sentido da formação do reagente (NO ). 6) a) AA + H O AA + H 3 O + b) Ki = [AA ].[H 3 O + ]/[AA] c) Ácido acetilsalicílico: C 9 H 8 O 4. Massa molar: 180 g/mol. n = massa/massa molar = 0,540/180 = 0,003 mol [AA]i = n/v = 0,003/1,5 = 0,00 mol/l Ki = [AA ].[H 3 O + ]/[AA] = x.x/[aa] :. 3,.10 4 = x²/.10 3 :. x = mol/l. d) ph = log[h+] = log(8.10-4) = 8 salicílico, neste ph, estará na sua forma não ionizada principalmente. 63) a) Teste número 1. Porque o sentido direto da reação é favorecido por temperaturas menores e pressões maiores. b) Q = [SO 3 ]²/[SO ]².[O ] = 0²/1².1,6 = 50 Como Q = K c a 1000 C, o sistema está em equilíbrio químico. 5 EMQUI05
6 EQUILÍBRIO QUÍMICO: DESLOCAMENTO DE EQUILÍBRIO E CÁLCULO DE PH EMQUI05 6
7 ELETROQUÍMICA: PILHAS E ELETRÓLISE ORIENTADOR METODOLÓGICO Eletroquímica: pilhas e eletrólise Objetivos de aprendizagem: Conceituar oxidação, redução e número de oxidação; Reconhecer reações de oxirredução associadas ao número de oxidação e aprender a balanceá-las; Reconhecer as características para a formação de uma pilha; Interpretar e calcular a ddp e a medida da força oxidante e redutora; Conceituar eletrólise ígnea e em solução aquosa e analisar as semirreações e reação global da eletrólise. Praticando: 1) E ) B 3) A 4) E 5) C 6) C 7) E 8) C 9) A 10) C 11) D 1) A 13) E 14) B 15) B 16) A 17) B 18) a) Arranjo 1, pois o arranjo está montado três. Quanto maior a corrente elétrica fornecida, maior será a massa depositada. b) s. 19) B Aprofundando: 0) B 1) C ) D 3) V - F - F - V - F 4) A 5) Cu + + Fe 0 Cu 0 + Fe ddp = +0,34 + 0,44 = + 0,78 V 6) ddp = 0,76 + 0,34 = 0 V Massa de Ag depositada: 108 g.mol-1 0,01 mol.l-1 0,5 L = 0,54 g No anodo da pilha: Zn0 (s) Zn+ (aq) + eno catodo da eletrólise: Ag+ (aq) + e- Ag0 (s) 1 mol de Zn (s) fornece elétrons para a deposição de mols de Ag (s). 65,5 g Zn 16 g Ag x 0,54 g x = 0,164 g 7) A 8) E 9) D 30) E 31) C 7 EMQUI06
8 ELETROQUÍMICA: PILHAS E ELETRÓLISE 3) B 33) B 34) A 35) C 36) a) Cr e Cr(s) (aq) b) Manganês. 37) E 1 : +1,5 V E : 0,1 V E 3 : 0,094 V EMQUI06 8
9 Lantanídeos Actinídeos Metais Semimetais Ametais Halogênios Gases Nobres Estrôncio Magnésio Lítio Be 9 1 Mg 4 0 Ca Sr Cálcio 7 87 Fr (3) Frâncio 56 Ba Ra (6) Rádio Rutherfódio 55 Cs 133 Césio Bário 37 Rb 85,5 Rubídio Potássio 11 Na 3 19 K 39 Escândio 1 Sc Y 89 7 Hf 178,5 104 Rf (61) Háfnio Ítrio Zircônio Ti Zr 91 Titânio Vanádio 3 V Nb Ta Db 6 Dúbnio Seabórgio 106 Sg (63) Tântalo Tungstênio 74 W 184 Nióbio Molibdênio 4 Cr 5 4 Mo 96 Tecnécio Cromo Manganês 5 Mn Tc (98) 75 Re Bh (6) Bóhrio 108 Hs (65) Hássio Meitenério Rênio 76 Os 190 Ósmio Rutênio 6 Fe Ru 101 Ferro 7 Co Rh Ir Mt (68) Darmstádio Irídio Ródio Cobalto 8 Ni 58,5 46 Pd 106,5 78 Pt Ds (81) Platina Paládio Níquel 9 Cu 63,5 47 Ag Au Uuh (80) Ouro Mercúrio Prata Cádmio Cobre 30 Zn 65,5 48 Cd 11,5 80 Hg 00,5 11 Ununtrio (85) Uus Zinco Sódio Alumínio Berílio 5 B Al 7 31 Ga In Ti Uut (84) Ununquádio 114 Uuq (89) 115 Uup 71 Tálio Chumbo 8 Pb 07 Bismuto Índio Estanho 50 Sn 119 Antimônio Gálio Germânio 14 Si 8 3 Ge 7,5 Arsênio Silício Boro Carbono 6 C 1 Nitrogênio N P As Sb 1 83 Bi Po (09) Polônio 5 Te 17,5 Telúrio 34 Se 79 Selênio Fósforo Enxofre 8 O S 3 Oxigênio 9 F Cl 35,5 35 Br I At (10) Astato Radônio 86 Rn () Íodo Xenônio 54 Xe 7 Bromo Criptônio 36 Kr 84 Cloro Argônio 18 Ar 40 Flúor 10 Ne 7 Neônio He 4 57 La Ac 7 Actínio Latânio 58 Ce Th 3 Tório Protactínio Cério Praseodímio 59 Pr Pa 31 Neodímio 60 Nd U 38 Urânio Netúnio Promécio 61 Pm (145) 93 Np 37 Plutônio Samário Európio 6 Sm Pu (44) Amerício 63 Eu Am (43) Gadolínio 64 Gd Cm (47) Cúrio Berquélio 65 Tb Bk (47) Califórnio Térbio Disprósio 66 Dy 16,5 98 Cf (51) Einstênio 67 Ho Es (5) Hólmio 68 Er Fm (57) Férmio Mendelévio Érbio 69 Tm Md (58) Nobélio Túlio 70 Yb No (59) Laurêncio SÍMBOLO massa atômica aproximada Intérbio 71 Lu Lr (6) NOME Lutécio 1,0 1,5 0,9 0,8 0,8 0,7 1, 1,0 1,0 0,9 0,7 0,9 1, 1,4 1,4 1,6 1,6 1,6 1,8 1,5 1,7 1,5 1,8 1,8 1,8 1,6 1,6 1,7 1,5 1,7 1,8 1,8 1,8 1, 1, 1, 1, 1, 1, 1, 1, 1, Roentgênio Hélio I A II A III B IV B V B VI B VII B VIII B I B II B Rg Coperníco Cn Ununpentio o Ununhéxio III A IV A V A VI A VII A Ununséptio Ununóctio 1,1 H Li 57 a a 103,,,,,,,4 7 77,0,5 1,8 1,8 3,0 3,5,1,0,5,4,1 4,0 3,0,8,5,0, VIII A 118 Uuo 93 1,5 1,5 Hidrogênio grupo período ,5 Atômico Número gatividade eletronegatividade
LISTA DE EXERCÍCIOS 3º ANO
 º AN Questão Questão Questão Questão Química I a) L ------- 0,0 mol (Na) L ------- 0,0 x, g (Na) 0 L ------- m m =, g b) 0,0 mol.l x 00 ml = 0 mol.l x Vf Vf = 000 ml c) c = 0, mol.l x, g.mol =, g.l Questão
º AN Questão Questão Questão Questão Química I a) L ------- 0,0 mol (Na) L ------- 0,0 x, g (Na) 0 L ------- m m =, g b) 0,0 mol.l x 00 ml = 0 mol.l x Vf Vf = 000 ml c) c = 0, mol.l x, g.mol =, g.l Questão
LISTA DE EXERCÍCIOS 3º ANO
 Química II Questão Questão Questão Letra E Questão Questão Questão Questão Questão 8 Letra E Questão As(s) + (g) As(s) Cada mol de arsênio (mol = g) libera 0kJ, assim mols de arsênio irá formar mols de
Química II Questão Questão Questão Letra E Questão Questão Questão Questão Questão 8 Letra E Questão As(s) + (g) As(s) Cada mol de arsênio (mol = g) libera 0kJ, assim mols de arsênio irá formar mols de
Xenubi é um jogo de cartas com as mesmas regras do Super Trunfo, porém sobre propriedades periódicas.
 nubi é um jogo de cartas com as mesmas regras do Super Trunfo, porém sobre propriedades periódicas. ISTRÇÕES * Jogue em duplas * Cada dupla deve ter o mesmo número de cartas. * A dupla pode compartilhar
nubi é um jogo de cartas com as mesmas regras do Super Trunfo, porém sobre propriedades periódicas. ISTRÇÕES * Jogue em duplas * Cada dupla deve ter o mesmo número de cartas. * A dupla pode compartilhar
Os elementos químicos sempre foram agrupados de modo a termos elementos semelhantes juntos, tendo desta maneira o desenvolvimento de várias tabelas
 Os elementos químicos sempre foram agrupados de modo a termos elementos semelhantes juntos, tendo desta maneira o desenvolvimento de várias tabelas até os nossos dias atuais P E R Í O D O S A TABELA PERIÓDICA
Os elementos químicos sempre foram agrupados de modo a termos elementos semelhantes juntos, tendo desta maneira o desenvolvimento de várias tabelas até os nossos dias atuais P E R Í O D O S A TABELA PERIÓDICA
Verifique se cada caderno das disciplinas específicas contém 8 questões que você deve resolver, sem rasuras ou falhas.
 Você está recebendo do fiscal três cadernos de prova (2 de disciplinas específicas correspondentes ao curso escolhido por você no ato da inscrição e 1 de redação). Verifique se cada caderno das disciplinas
Você está recebendo do fiscal três cadernos de prova (2 de disciplinas específicas correspondentes ao curso escolhido por você no ato da inscrição e 1 de redação). Verifique se cada caderno das disciplinas
MODALIDADE EM2. 3 a Olimpíada de Química do Rio de Janeiro 2008 EM2 1 a Fase
 MODALIDADE EM2 Leia atentamente as instruções abaixo: Esta prova destina-se exclusivamente aos alunos das 2 a séries do ensino médio. A prova contém dez questões objetivas, cada uma com cinco alternativas,
MODALIDADE EM2 Leia atentamente as instruções abaixo: Esta prova destina-se exclusivamente aos alunos das 2 a séries do ensino médio. A prova contém dez questões objetivas, cada uma com cinco alternativas,
PUC - RIO Rio VESTIBULAR 2013 PROVAS DISCURSIVAS DE QUÍMICA LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO.
 PUC - RIO - 03 Rio VESTIBULAR 03 o DIA TARDE GRUPO Outubro / 0 PROVAS DISCURSIVAS DE QUÍMICA LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO. 0 - Você recebeu do fiscal o seguinte material: a) este Caderno, com
PUC - RIO - 03 Rio VESTIBULAR 03 o DIA TARDE GRUPO Outubro / 0 PROVAS DISCURSIVAS DE QUÍMICA LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO. 0 - Você recebeu do fiscal o seguinte material: a) este Caderno, com
Segundo dia QUÍMICA Vestibular CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS (com massas atômicas referidas ao isótopo 12 do carbono)
 Segundo dia QUÍMIA Vestibular 004 LASSIFIAÇÃ PERIÓDIA DS ELEMENTS (com massas atômicas referidas ao isótopo 1 do carbono) 1 4 5 6 7 idrogênio Lítio Sódio Potássio Rubídio ésio Frâncio 1 18 1 1,0 Li 7,0
Segundo dia QUÍMIA Vestibular 004 LASSIFIAÇÃ PERIÓDIA DS ELEMENTS (com massas atômicas referidas ao isótopo 1 do carbono) 1 4 5 6 7 idrogênio Lítio Sódio Potássio Rubídio ésio Frâncio 1 18 1 1,0 Li 7,0
Os Pesos Atômicos Deixam de Ser Constantes: Dez Elementos Passam a Ter Intervalos de Pesos Atômicos
 Atualidades em Química Os Pesos Atômicos Deixam de Ser Constantes: Dez Elementos Passam a Ter Intervalos de Pesos Atômicos Romeu C. Rocha-Filho e Aécio Pereira Chagas Em 2011, a União Internacional de
Atualidades em Química Os Pesos Atômicos Deixam de Ser Constantes: Dez Elementos Passam a Ter Intervalos de Pesos Atômicos Romeu C. Rocha-Filho e Aécio Pereira Chagas Em 2011, a União Internacional de
E P E ANALISTA DE PESQUISA ENERGÉTICA GÁS E BIOENERGIA LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO.
 08 E P E LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO. EDITAL N o 001/2012 - EPE 01 - Você recebeu do fiscal o seguinte material: a) este caderno, com os enunciados das 50 (cinquenta) questões das Provas Objetivas
08 E P E LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO. EDITAL N o 001/2012 - EPE 01 - Você recebeu do fiscal o seguinte material: a) este caderno, com os enunciados das 50 (cinquenta) questões das Provas Objetivas
QUÍMICA - 1 o ANO MÓDULO 06 CLASSIFICAÇÃO PERIÓDICA
 QUÍMICA - 1 o ANO MÓDULO 06 CLASSIFICAÇÃO PERIÓDICA Hidrogênio Azufre L Plomo Nitrógeno Magnesio Plata Carbono I Hierro G Oro Oxígeno Z Cinc Mercurio Fósforo C Cobre Calcio 1 o grupo 1 2 3 4 5 6 7 8 9
QUÍMICA - 1 o ANO MÓDULO 06 CLASSIFICAÇÃO PERIÓDICA Hidrogênio Azufre L Plomo Nitrógeno Magnesio Plata Carbono I Hierro G Oro Oxígeno Z Cinc Mercurio Fósforo C Cobre Calcio 1 o grupo 1 2 3 4 5 6 7 8 9
121,8 127,6 126,9 131,3. Sb Te I Xe 27,0 28,1 31,0 32,1 35,5 39,9 69,7 72,6 74,9 79,0 79,9 83, Ga Ge As Se Br Kr. In Sn 114,8 118,7.
 PRVA DE QUÍMICA º 2º 3º 4º 5º 6º 7º TABELA PERIÓDICA DS ELEMENTS (IA),0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr Mn Fe
PRVA DE QUÍMICA º 2º 3º 4º 5º 6º 7º TABELA PERIÓDICA DS ELEMENTS (IA),0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr Mn Fe
Somente identifique sua prova com o código de inscrição (não coloque seu nome);
 Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas as páginas; Não é permitida
Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas as páginas; Não é permitida
Química. A) Considerando-se que o pk a1 é aproximadamente 2, quais os valores de pk a2 e pk a3?
 Química 01. O gráfico a seguir representa a variação do ph de 50 ml de uma solução aquosa de um ácido H 3 X em função do volume de NaOH 0,30 moll -1 adicionado. A) Considerando-se que o pk a1 é aproximadamente
Química 01. O gráfico a seguir representa a variação do ph de 50 ml de uma solução aquosa de um ácido H 3 X em função do volume de NaOH 0,30 moll -1 adicionado. A) Considerando-se que o pk a1 é aproximadamente
Universidade Federal do Ceará 2ª ETAPA PROVA ESPECÍFICA DE QUÍMICA PROVA ESPECÍFICA DE QUÍMICA. Data: Duração: 04 horas CORRETOR 1
 1ª AVALIAÇÃO AVALIAÇÃO FINAL CORRETOR 1 01 02 03 04 05 06 07 08 Reservado à CCV Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Reservado à CCV 2ª ETAPA PROVA ESPECÍFICA
1ª AVALIAÇÃO AVALIAÇÃO FINAL CORRETOR 1 01 02 03 04 05 06 07 08 Reservado à CCV Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Reservado à CCV 2ª ETAPA PROVA ESPECÍFICA
Somente identifique sua prova com o código de inscrição (não coloque seu nome);
 Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas as páginas; Não é permitida
Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas as páginas; Não é permitida
Exame de Seleção Mestrado em Química Turma 2014 I. Candidato: RG:
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2014
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2014
COMISSÃO PERMANENTE DE SELEÇÃO COPESE PRÓ-REITORIA DE GRADUAÇÃO PROGRAD CONCURSO VESTIBULAR 2010 PROVA DE QUÍMICA
 Questão 1: A pirita (FeS 2 ), mineral conhecido como ouro de tolo, é utilizada na fabricação de ácido sulfúrico. Uma das formas de produção desse ácido, a partir da pirita, é o aquecimento em etapas sequenciais
Questão 1: A pirita (FeS 2 ), mineral conhecido como ouro de tolo, é utilizada na fabricação de ácido sulfúrico. Uma das formas de produção desse ácido, a partir da pirita, é o aquecimento em etapas sequenciais
MÓDULO 6 MATRIZ DA PROVA
 ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (11º ANO) Programa iniciado 2016/2017 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (11º ANO) Programa iniciado 2016/2017 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
Anexo 1. Tabela de constantes. g = 10 m s -2. Velocidade de propagação da luz no vácuo c = 3, m s -1
 Anexo 1 Tabela de constantes Velocidade de propagação da luz no vácuo c = 3,00 10 8 m s -1 Módulo da aceleração gravítica de um corpo junto à superfície da Terra g = 10 m s - Constante de gravitação universal
Anexo 1 Tabela de constantes Velocidade de propagação da luz no vácuo c = 3,00 10 8 m s -1 Módulo da aceleração gravítica de um corpo junto à superfície da Terra g = 10 m s - Constante de gravitação universal
Química. CURSOS Química Industrial, Química - Modalidade Licenciatura e Tecnologia em Mineração
 PROCESSO SELETIVO 2006/1 Química CURSOS Química Industrial, Química - Modalidade Licenciatura e Tecnologia em Mineração Só abra este caderno quando o fiscal autorizar. Leia atentamente as instruções abaixo.
PROCESSO SELETIVO 2006/1 Química CURSOS Química Industrial, Química - Modalidade Licenciatura e Tecnologia em Mineração Só abra este caderno quando o fiscal autorizar. Leia atentamente as instruções abaixo.
Identificação do candidato UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2018.
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2018.
Exame de Seleção Mestrado em Química Turma 2013 II CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS 11 1B. 26 Fe 55,8 44 Ru 101,1 76 Os 190,2
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2013
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2013
001. PROVA I. Vestibular Medicina 2018
 Vestibular Medicina 2018 001. PROVA I Confira seus dados impressos neste caderno. Assine com caneta de tinta azul ou preta apenas no local indicado. Qualquer identificação fora do local indicado acarretará
Vestibular Medicina 2018 001. PROVA I Confira seus dados impressos neste caderno. Assine com caneta de tinta azul ou preta apenas no local indicado. Qualquer identificação fora do local indicado acarretará
121,8 127,6 126,9 131,3. Sb Te I Xe. Pb Bi Po At Rn 69,7 72,6 74,9 79,0 79,9 83, Ga Ge As Se Br Kr. In Sn 114,8 118,7.
 PROVA DE QUÍMICA TABELA PERIÓDICA DOS ELEMENTOS º 2º 3º 4º 5º 6º 7º (IA) H,0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr
PROVA DE QUÍMICA TABELA PERIÓDICA DOS ELEMENTOS º 2º 3º 4º 5º 6º 7º (IA) H,0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr
QUÍMICA CURSOS AGRONOMIA EDUCAÇÃO FÍSICA FISIOTERAPIA CIÊNCIAS BIOLÓGICAS FARMÁCIA ZOOTECNIA QUÍMICA INDUSTRIAL. Identificação do candidato
 QUÍMICA PROCESSO SELETIVO 2008/2 22 de junho de 2008 CADERNO DE PROVA DISCURSIVA RESPOSTAS ESPERADAS PELAS BANCAS ELABORADORAS QUÍMICA CURSOS AGRONOMIA EDUCAÇÃO FÍSICA FISIOTERAPIA CIÊNCIAS BIOLÓGICAS
QUÍMICA PROCESSO SELETIVO 2008/2 22 de junho de 2008 CADERNO DE PROVA DISCURSIVA RESPOSTAS ESPERADAS PELAS BANCAS ELABORADORAS QUÍMICA CURSOS AGRONOMIA EDUCAÇÃO FÍSICA FISIOTERAPIA CIÊNCIAS BIOLÓGICAS
Classificação Periódica dos Elementos
 Classificação Periódica dos Elementos 1 2 3 1 Massa atômica relativa. A incerteza no último dígito é 1, exceto quando indicado entre parênteses. Os valores com * referemse Número Atômico 18 ao isótopo
Classificação Periódica dos Elementos 1 2 3 1 Massa atômica relativa. A incerteza no último dígito é 1, exceto quando indicado entre parênteses. Os valores com * referemse Número Atômico 18 ao isótopo
Ministério da Educação Universidade Federal do Paraná Setor Palotina
 Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 5 Íons e Introdução a Tabela Periódica Prof. Isac G. Rosset Prof. Isac G. Rosset - UFPR - Palotina - Ciências Exatas 2 1 d p s
Ministério da Educação Universidade Federal do Paraná Setor Palotina Aula 5 Íons e Introdução a Tabela Periódica Prof. Isac G. Rosset Prof. Isac G. Rosset - UFPR - Palotina - Ciências Exatas 2 1 d p s
EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2009/01
 Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2009/01 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES: - identifique
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2009/01 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES: - identifique
Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular
 Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Data: 24.10.2010 Duração das 13 às 18 horas. Conhecimentos Específicos: Matemática: 01 a 05 Redação Química: 06 a 10
Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Data: 24.10.2010 Duração das 13 às 18 horas. Conhecimentos Específicos: Matemática: 01 a 05 Redação Química: 06 a 10
MÓDULO 1 MATRIZ DA PROVA
 ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA QUÍMICA (12º ANO) MÓDULO 3 MATRIZ DA PROVA
 Cursos Científico - Humanísticos de Ciências e Tecnologias ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA Ensino Recorrente de Nível Secundário QUÍMICA (12º ANO) MÓDULO 3 TIPO DE PROVA: ESCRITA DURAÇÃO:
Cursos Científico - Humanísticos de Ciências e Tecnologias ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA Ensino Recorrente de Nível Secundário QUÍMICA (12º ANO) MÓDULO 3 TIPO DE PROVA: ESCRITA DURAÇÃO:
121,8 127,6 126,9 131,3. Sb Te I Xe. In Sn 69,7 72,6 74,9 79,0 79,9 83,8 112,4 107,9 85,5 87,6 88,9 91,2 92,9 95,9 (98) 101,1 102,9 106,4 140,1
 PROVA DE QUÍMICA º 2º 3º 4º 5º 6º 7º TABELA PERIÓDICA DOS ELEMENTOS (IA) H,0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr
PROVA DE QUÍMICA º 2º 3º 4º 5º 6º 7º TABELA PERIÓDICA DOS ELEMENTOS (IA) H,0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DOS VALES DO JEQUITINHONHA E MUCURI DIAMANTINA MINAS GERAIS PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO
 MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DOS VALES DO JEQUITINHONHA E MUCURI DIAMANTINA MINAS GERAIS PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO EDITAL Nº 009/2017, DE 21 DE DEZEMBRO DE 2016 SELEÇÃO DO
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DOS VALES DO JEQUITINHONHA E MUCURI DIAMANTINA MINAS GERAIS PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO EDITAL Nº 009/2017, DE 21 DE DEZEMBRO DE 2016 SELEÇÃO DO
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA QUÍMICA (12º ANO) MÓDULO 2 MATRIZ DA PROVA
 Cursos Científico - Humanísticos de Ciências e Tecnologias ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA Ensino Recorrente de Nível Secundário QUÍMICA (12º ANO) MÓDULO 2 TIPO DE PROVA: ESCRITA DURAÇÃO:
Cursos Científico - Humanísticos de Ciências e Tecnologias ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA Ensino Recorrente de Nível Secundário QUÍMICA (12º ANO) MÓDULO 2 TIPO DE PROVA: ESCRITA DURAÇÃO:
Universidade Federal de Goiás. Instituto de Química. Coordenadoria de Pós-Graduação em Química
 Nº. de Inscrição Universidade Federal de Goiás Instituto de Química Coordenadoria de Pós-Graduação em Química EXAME DE SELEÇÃO DO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA 2018/2 IDENTIFICAÇÃO DO CANDIDATO
Nº. de Inscrição Universidade Federal de Goiás Instituto de Química Coordenadoria de Pós-Graduação em Química EXAME DE SELEÇÃO DO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA 2018/2 IDENTIFICAÇÃO DO CANDIDATO
Tabela Periódica* 1 H 1,0. Massa atômica. 20,2 18 Ar 39,9 2º VESTIBULAR UFOP Fe. 29 Cu. 28 Ni. 27 Co. 58,9 45 Rh 102,9 77 Ir 192,2 109 Mt
 Tabela Periódica* 1 1 18 1 1,0 2 Número atômico 1 1,0 13 14 15 16 17 2 e 4,0 2 3 3 Li 6,9 11 Na 23,0 4 Be 9,0 Massa atômica 12 Mg 24,3 3 4 5 6 7 8 9 10 11 12 5 B 10,8 13 Al 27,0 6 C 12,0 14 Si 28,1 7 N
Tabela Periódica* 1 1 18 1 1,0 2 Número atômico 1 1,0 13 14 15 16 17 2 e 4,0 2 3 3 Li 6,9 11 Na 23,0 4 Be 9,0 Massa atômica 12 Mg 24,3 3 4 5 6 7 8 9 10 11 12 5 B 10,8 13 Al 27,0 6 C 12,0 14 Si 28,1 7 N
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação
 Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2012/1 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES IMPROTANTES: -
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2012/1 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES IMPROTANTES: -
LEIA ATENTAMENTE AS INSTRUÇÕES
 CADERNO DE QUESTÕES UNIVERSIDADE FEDERAL DE GOIÁS PRÓ-REITORIA DE GRADUAÇÃO CENTRO DE SELEÇÃO PROCESSO SELETIVO/2010-2 GRUPO 1 Química 1º DIA 06/06/2010 SÓ ABRA ESTE CADERNO QUANDO AUTORIZADO LEIA ATENTAMENTE
CADERNO DE QUESTÕES UNIVERSIDADE FEDERAL DE GOIÁS PRÓ-REITORIA DE GRADUAÇÃO CENTRO DE SELEÇÃO PROCESSO SELETIVO/2010-2 GRUPO 1 Química 1º DIA 06/06/2010 SÓ ABRA ESTE CADERNO QUANDO AUTORIZADO LEIA ATENTAMENTE
Exame de Seleção Mestrado em Química Turma Candidato: CPF:
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2014.2
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2014.2
QUÍMICA. Questões de 09 a 12
 GRUP 1 TIP A QUÍ. 11 QUÍMICA Questões de 09 a 12 09. ácido sulfúrico, um dos insumos mais importantes da indústria química, é produzido pelo chamado Processo de Contato. Esse processo envolve as seguintes
GRUP 1 TIP A QUÍ. 11 QUÍMICA Questões de 09 a 12 09. ácido sulfúrico, um dos insumos mais importantes da indústria química, é produzido pelo chamado Processo de Contato. Esse processo envolve as seguintes
MÓDULO 2 MATRIZ DA PROVA
 ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
Somente identifique sua prova com o código de inscrição (não coloque seu nome);
 Minas Gerais PPGMQMG 1/019 Orientações gerais Somente identifique sua prova com o código de inscrição (não coloque seu nome); Assim que assinar a lista de presença verifique seu código de inscrição e preencha
Minas Gerais PPGMQMG 1/019 Orientações gerais Somente identifique sua prova com o código de inscrição (não coloque seu nome); Assim que assinar a lista de presença verifique seu código de inscrição e preencha
Identificação do candidato UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2018.
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2018.
Somente identifique sua prova com o código de inscrição (não coloque seu nome);
 Minas Gerais PPGMQMG 2/2018 Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas
Minas Gerais PPGMQMG 2/2018 Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas
Universidade Federal do Ceará Coordenadoria de Concursos - CCV 2ª ETAPA PROVA ESPECÍFICA DE QUÍMICA PROVA ESPECÍFICA DE QUÍMICA
 1ª AVALIAÇÃO CORRETOR 1 01 02 03 04 05 06 07 08 Reservado à CCV AVALIAÇÃO FINAL Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Reservado à CCV 2ª ETAPA PROVA ESPECÍFICA
1ª AVALIAÇÃO CORRETOR 1 01 02 03 04 05 06 07 08 Reservado à CCV AVALIAÇÃO FINAL Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Reservado à CCV 2ª ETAPA PROVA ESPECÍFICA
COMISSÃO PERMANENTE DE SELEÇÃO COPESE PRÓ-REITORIA DE GRADUAÇÃO PROGRAD CONCURSO PISM III - TRIÊNIO PROVA DE QUÍMICA
 Questão 1: Uma forma de se alterar a velocidade de reações químicas é adicionar uma substância, denominada de catalisador, que praticamente não sofre alteração ao final do processo reacional. A velocidade
Questão 1: Uma forma de se alterar a velocidade de reações químicas é adicionar uma substância, denominada de catalisador, que praticamente não sofre alteração ao final do processo reacional. A velocidade
QUÍMICA. Questões de 01 a 04
 GRUPO 1 QUÍ. 1 QUÍMICA Questões de 01 a 04 01. Os íons cálcio dissolvidos em água são responsáveis pela dureza desta. Em determinadas regiões do Estado de Minas Gerais, nas estações de tratamento de água,
GRUPO 1 QUÍ. 1 QUÍMICA Questões de 01 a 04 01. Os íons cálcio dissolvidos em água são responsáveis pela dureza desta. Em determinadas regiões do Estado de Minas Gerais, nas estações de tratamento de água,
Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular
 Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Data: 08..2009 Duração: 05 horas Conhecimentos Específicos: Matemática: 01 a 05 Redação Química: 06 a Coloque, de imediato,
Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Data: 08..2009 Duração: 05 horas Conhecimentos Específicos: Matemática: 01 a 05 Redação Química: 06 a Coloque, de imediato,
FÍSICO-QUÍMICA 8ºANO. Tema: Símbolos Químicos e Fórmulas Químicas
 FÍSICO-QUÍMICA 8ºANO Tema: Símbolos Químicos e Fórmulas Químicas Símbolos e fórmulas químicas Desde sempre o homem tenta comunicar com símbolos. As letras das palavras escritas constituem uma linguagem
FÍSICO-QUÍMICA 8ºANO Tema: Símbolos Químicos e Fórmulas Químicas Símbolos e fórmulas químicas Desde sempre o homem tenta comunicar com símbolos. As letras das palavras escritas constituem uma linguagem
Química *R * LEIA COM ATENÇÃO AS INSTRUÇÕES ABAIXO. BACHARELADO. Peso das questões no componente. Peso dos componentes no cálculo da nota
 Novembro/2014 Química BACHARELAD LEIA CM ATENÇÃ AS INSTRUÇÕES ABAIX. 37 Partes Número das questões Peso das questões no componente Peso dos componentes no cálculo da nota 40% 60% 25% 15% 75% - - 10. Atenção!
Novembro/2014 Química BACHARELAD LEIA CM ATENÇÃ AS INSTRUÇÕES ABAIX. 37 Partes Número das questões Peso das questões no componente Peso dos componentes no cálculo da nota 40% 60% 25% 15% 75% - - 10. Atenção!
UNIVERSIDADE FEDERAL DE ALAGOAS POLÍCIA MILITAR DE ALAGOAS CORPO DE BOMBEIROS MILITAR DE ALAGOAS. Coordenadoria Permanente do Vestibular (COPEVE)
 UNIVERSIDADE FEDERAL DE ALAGOAS POLÍCIA MILITAR DE ALAGOAS CORPO DE BOMBEIROS MILITAR DE ALAGOAS Coordenadoria Permanente do Vestibular (COPEVE) PSS - 2002 QUÍMICA INSTRUÇÕES - Ao receber este caderno
UNIVERSIDADE FEDERAL DE ALAGOAS POLÍCIA MILITAR DE ALAGOAS CORPO DE BOMBEIROS MILITAR DE ALAGOAS Coordenadoria Permanente do Vestibular (COPEVE) PSS - 2002 QUÍMICA INSTRUÇÕES - Ao receber este caderno
VERSÃO 1. Prova Escrita de Física e Química A. 10.º e 11.º Anos de Escolaridade. Prova 715/2.ª Fase
 EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 74/2004, de 26 de Março Prova Escrita de Física e Química A 10.º e 11.º Anos de Escolaridade Prova 715/2.ª Fase 15 Páginas Duração da Prova: 120 minutos.
EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 74/2004, de 26 de Março Prova Escrita de Física e Química A 10.º e 11.º Anos de Escolaridade Prova 715/2.ª Fase 15 Páginas Duração da Prova: 120 minutos.
QUESTÕES OBJETIVAS. 9) Qual reação química pode ser relacionada com a seguinte expressão de constante de equilíbrio?
 QUESTÕES OBJETIVAS 9) Qual reação química pode ser relacionada com a seguinte expressão de constante de equilíbrio? Kc = [FeCl 2 ] 3 [Al 2 (SO 4 ) 3 ] [FeSO 4 ] 3 [AlCl 3 ] 2 a) reação em que o ferro sofre
QUESTÕES OBJETIVAS 9) Qual reação química pode ser relacionada com a seguinte expressão de constante de equilíbrio? Kc = [FeCl 2 ] 3 [Al 2 (SO 4 ) 3 ] [FeSO 4 ] 3 [AlCl 3 ] 2 a) reação em que o ferro sofre
QUESTÕES OBJETIVAS. As afirmativas seguintes, referentes aos elementos a, b, c, d, e, são corretas, EXCETO:
 QUESTÕES OBJETIVAS 9) O esquema abaixo representa uma tabela periódica simplificada. Li a b Ca Sc c O e d As afirmativas seguintes, referentes aos elementos a, b, c, d, e, são corretas, EXCETO: a) c é
QUESTÕES OBJETIVAS 9) O esquema abaixo representa uma tabela periódica simplificada. Li a b Ca Sc c O e d As afirmativas seguintes, referentes aos elementos a, b, c, d, e, são corretas, EXCETO: a) c é
QUÍMICA EXAME DISCURSIVO 03/12/2017 2ª FASE CADERNO DE PROVA INSTRUÇÕES INFORMAÇÕES GERAIS BOA PROVA!
 2ª FASE EXAME DISCURSIVO 03/12/2017 QUÍMICA CADERNO DE PROVA Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
2ª FASE EXAME DISCURSIVO 03/12/2017 QUÍMICA CADERNO DE PROVA Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
 02/12/2012 Química Caderno de prova Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está na página 13. Não abra o
02/12/2012 Química Caderno de prova Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está na página 13. Não abra o
Química. 2ª Fase Exame Discursivo 29/11/2015. Caderno de prova. Instruções. Informações gerais. Boa prova!
 2ª Fase Exame Discursivo 29/11/2015 Química Caderno de prova Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
2ª Fase Exame Discursivo 29/11/2015 Química Caderno de prova Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
Qui. Allan Rodrigues Xandão (Gabriel Pereira)
 Semana 10 Allan Rodrigues Xandão (Gabriel Pereira) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
Semana 10 Allan Rodrigues Xandão (Gabriel Pereira) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. CRONOGRAMA
MÓDULO 5 MATRIZ DA PROVA
 ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (11º ANO) Programa iniciado 2016/2017 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (11º ANO) Programa iniciado 2016/2017 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
AVALIAÇÃO 05 QUÍMICA III UNIDADE Valor = 10,0 (Dez)
 Aluno(a) Turma N o Série 2 a Ensino Médio Data 16 / 08 / 11 INSTRUÇÕES: AVALIAÇÃO 05 QUÍMICA III UNIDADE Valor = 10,0 (Dez) I. Leia cuidadosamente o enunciado de cada questão, formule suas respostas com
Aluno(a) Turma N o Série 2 a Ensino Médio Data 16 / 08 / 11 INSTRUÇÕES: AVALIAÇÃO 05 QUÍMICA III UNIDADE Valor = 10,0 (Dez) I. Leia cuidadosamente o enunciado de cada questão, formule suas respostas com
Universidade Federal de Goiás. Instituto de Química. Coordenação de Pós-Graduação em Química EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2015/1
 Nº. de Inscrição Universidade Federal de Goiás Instituto de Química Coordenação de Pós-Graduação em Química EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2015/1 IDENTIFICAÇÃO DO CANDIDATO - Número de Inscrição:
Nº. de Inscrição Universidade Federal de Goiás Instituto de Química Coordenação de Pós-Graduação em Química EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2015/1 IDENTIFICAÇÃO DO CANDIDATO - Número de Inscrição:
CURSOS Ciências Habilitação em Química e Química Industrial. Só abra este caderno quando o fiscal autorizar. Leia atentamente as instruções abaixo.
 PROCESSO SELETIVO 2003/2 QUÍMICA CURSOS Ciências Habilitação em Química e Química Industrial Só abra este caderno quando o fiscal autorizar. Leia atentamente as instruções abaixo. 1. 2. 3. 4. Esta prova
PROCESSO SELETIVO 2003/2 QUÍMICA CURSOS Ciências Habilitação em Química e Química Industrial Só abra este caderno quando o fiscal autorizar. Leia atentamente as instruções abaixo. 1. 2. 3. 4. Esta prova
Física e Química A Tabela de Constantes Formulário Tabela Periódica
 Física e Quíica A Tabela de Constantes Forulário Tabela Periódica http://fisicanalixa.blogspot.pt/ CONSTANTES Velocidade de propagação da luz no vácuo c = 3,00 10 8 s 1 Módulo da aceleração gravítica de
Física e Quíica A Tabela de Constantes Forulário Tabela Periódica http://fisicanalixa.blogspot.pt/ CONSTANTES Velocidade de propagação da luz no vácuo c = 3,00 10 8 s 1 Módulo da aceleração gravítica de
TABELA PERIÓDICA DOS ELEMENTOS. N atômico 1 H Massa atômica 1, Ru 101,1 76 Os 190,2 108 Hs (265) 45 Rh 102,9 77
 Ministério da Educação Secretaria de Educação Profissional e Tecnológica Instituto Federal de Educação, Ciência e Tecnologia de Minas Gerais Campus São João Evangelista Disciplina: Química II Professor:
Ministério da Educação Secretaria de Educação Profissional e Tecnológica Instituto Federal de Educação, Ciência e Tecnologia de Minas Gerais Campus São João Evangelista Disciplina: Química II Professor:
Simulado de Conhecimentos Específicos
 1A 1 1 H 1,0 3 Li 7,0 11 Na 3,0 19 K 39,0 37 Rb 85,5 55 Cs 133,0 87 Fr (3) A 4 Be 9,0 1 Mg 4,0 0 Ca 40,0 38 Sr 88,0 56 Ba 137,0 88 Ra (6) Elementos de Transição 3B 4B 5B 6B 7B 8B 1B B 13 14 15 16 17 3A
1A 1 1 H 1,0 3 Li 7,0 11 Na 3,0 19 K 39,0 37 Rb 85,5 55 Cs 133,0 87 Fr (3) A 4 Be 9,0 1 Mg 4,0 0 Ca 40,0 38 Sr 88,0 56 Ba 137,0 88 Ra (6) Elementos de Transição 3B 4B 5B 6B 7B 8B 1B B 13 14 15 16 17 3A
Identificação do candidato. Exame de Seleção Mestrado em Química Turma I CANDIDATO: RG:
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2017.
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2017.
MÓDULO 1,2,3 MATRIZ DA PROVA
 ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 135 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 135 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS 195, , , , 97
 PRVA de QUÍMICA MÓDUL III do PISM (00-005) 4 5 6 7, 00 4 Li 6, 94 9, 0 Na, 99 4, 9 0 K 9, 0 40, 08 7 8 Rb 85, 47 87, 6 55 56 Cs, 9 7, 87 88 Fr, 0 Be Mg Ca Sr Ba Ra 6, 0 CLASSIFICAÇÃ PERIÓDICA DS ELEMENTS
PRVA de QUÍMICA MÓDUL III do PISM (00-005) 4 5 6 7, 00 4 Li 6, 94 9, 0 Na, 99 4, 9 0 K 9, 0 40, 08 7 8 Rb 85, 47 87, 6 55 56 Cs, 9 7, 87 88 Fr, 0 Be Mg Ca Sr Ba Ra 6, 0 CLASSIFICAÇÃ PERIÓDICA DS ELEMENTS
Não arredonde nenhum valor de massa consultado na tabela periódica.
 Ministério da Educação Secretaria de Educação Profissional e Tecnológica Instituto Federal de Educação, Ciência e Tecnologia de Minas Gerais Campus São João Evangelista Disciplina: Química II Professor:
Ministério da Educação Secretaria de Educação Profissional e Tecnológica Instituto Federal de Educação, Ciência e Tecnologia de Minas Gerais Campus São João Evangelista Disciplina: Química II Professor:
Química A Semiextensivo V. 2
 Química A Semiextensivo V. Exercícios 0) B 0) A 0) A Símbolo N: elemento Nitrogênio Símbolo P: elemento Fósforo (do latim Phosphorus) Símbolo K: elemento Potássio (do latim Kalium) Trata-se de uma questão
Química A Semiextensivo V. Exercícios 0) B 0) A 0) A Símbolo N: elemento Nitrogênio Símbolo P: elemento Fósforo (do latim Phosphorus) Símbolo K: elemento Potássio (do latim Kalium) Trata-se de uma questão
AULA 03 Tabela Periódica
 Faculdade de Tecnologia e Ciências FTC Colegiado de Engenharia Civil Química Geral AULA 03 Tabela Periódica PROFESSORA: Shaiala Aquino shaiaquino@hotmail.com Henry Moseley A.B.Chancourtois ( 1820-1886)
Faculdade de Tecnologia e Ciências FTC Colegiado de Engenharia Civil Química Geral AULA 03 Tabela Periódica PROFESSORA: Shaiala Aquino shaiaquino@hotmail.com Henry Moseley A.B.Chancourtois ( 1820-1886)
QUÍMICA 1 0 PERÍODO ENSINO MÉDIO TABELA PERIÓDICA A LEI PERIÓDICA
 QUÍMICA 1 0 PERÍD 1 0 PERÍD ENSIN MÉDI QUÍMICA TABELA PERIÓDICA A LEI PERIÓDICA A medida que se conhece um grande número de elementos químicos e várias de suas propriedades, sentiu-se a necessidade de
QUÍMICA 1 0 PERÍD 1 0 PERÍD ENSIN MÉDI QUÍMICA TABELA PERIÓDICA A LEI PERIÓDICA A medida que se conhece um grande número de elementos químicos e várias de suas propriedades, sentiu-se a necessidade de
QUESTÕES OBJETIVAS. 10) Com relação aos produtos formados, todas as reações químicas a seguir estão corretas, EXCETO:
 QUESTÕES BJETIVAS 9) ar atmosférico, na ausência de poluição, é composto fundamentalmente de N 2, 2, Ar, C 2 e vapor d água. Nos locais poluídos, sobretudo em centros urbanos e industriais, muitas outras
QUESTÕES BJETIVAS 9) ar atmosférico, na ausência de poluição, é composto fundamentalmente de N 2, 2, Ar, C 2 e vapor d água. Nos locais poluídos, sobretudo em centros urbanos e industriais, muitas outras
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação
 Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2011/1 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES IMPROTANTES: -
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2011/1 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES IMPROTANTES: -
Duração da Prova: 120 minutos. Tolerância: 30 minutos. Na folha de respostas, indique de forma legível a versão da prova (Versão 1 ou Versão 2).
 EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 139/2012, de 5 de julho Prova Escrita de Física e Química A 10.º e 11.º Anos de Escolaridade Prova 715/1.ª Fase 16 Páginas Duração da Prova: 120 minutos.
EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 139/2012, de 5 de julho Prova Escrita de Física e Química A 10.º e 11.º Anos de Escolaridade Prova 715/1.ª Fase 16 Páginas Duração da Prova: 120 minutos.
química EXAME DISCURSIVO 2ª fase 30/11/2014
 EXAME DISCURSIVO 2ª fase 30/11/2014 química Caderno de prova Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
EXAME DISCURSIVO 2ª fase 30/11/2014 química Caderno de prova Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
Universidade Federal de Goiás. Instituto de Química. Coordenação de Pós-Graduação em Química
 Universidade Federal de Goiás Instituto de Química Coordenação de Pós-Graduação em Química Nº. de Inscrição EXAME DE SELEÇÃO DO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA 2017/2 IDENTIFICAÇÃO DO CANDIDATO -
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-Graduação em Química Nº. de Inscrição EXAME DE SELEÇÃO DO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA 2017/2 IDENTIFICAÇÃO DO CANDIDATO -
PROVA DE QUÍMICA MÓDULO I DO PISM (triênio )
 PRVA DE QUÍMICA MÓDUL I D PISM (triênio 006-008) CLASSIFICAÇÃ PERIÓDICA DS ELEMENTS 1 18 1 3 4 6 7 1 1,0 3 Li 6,9 11 Na 3,0 19 K 39,1 37 Rb 8, Cs 13,9 67 Fr 3,0 4 Be 9,0 1 Mg 4,3 0 Ca 40,1 38 Sr 87,6 6
PRVA DE QUÍMICA MÓDUL I D PISM (triênio 006-008) CLASSIFICAÇÃ PERIÓDICA DS ELEMENTS 1 18 1 3 4 6 7 1 1,0 3 Li 6,9 11 Na 3,0 19 K 39,1 37 Rb 8, Cs 13,9 67 Fr 3,0 4 Be 9,0 1 Mg 4,3 0 Ca 40,1 38 Sr 87,6 6
Gabarito - Química - Grupo A
 1 a QUESTÃO: (1,5 ponto) Avaliador Revisor A estrutura dos compostos orgânicos começou a ser desvendada nos meados do séc. XIX, com os estudos de ouper e Kekulé, referentes ao comportamento químico do
1 a QUESTÃO: (1,5 ponto) Avaliador Revisor A estrutura dos compostos orgânicos começou a ser desvendada nos meados do séc. XIX, com os estudos de ouper e Kekulé, referentes ao comportamento químico do
Nome: Escola: 1 Esta prova contém 20 questões de múltipla escolha e três questões discursivas.
 Nome: Escola: Instruções: 1 Esta prova contém 20 questões de múltipla escolha e três questões discursivas. 2 Antes de iniciar a prova, confira se todas as folhas estão presentes. Caso haja algum problema,
Nome: Escola: Instruções: 1 Esta prova contém 20 questões de múltipla escolha e três questões discursivas. 2 Antes de iniciar a prova, confira se todas as folhas estão presentes. Caso haja algum problema,
Colégio Santa Dorotéia
 Colégio Santa Dorotéia Área de Ciências da Natureza Disciplina: Química Ano: 2º Ensino Médio Professora: Luana P. Nunes P. Dayrell Química Atividades para Estudos Autônomos Data: 3 / 4 / 2018 Aluno(a):
Colégio Santa Dorotéia Área de Ciências da Natureza Disciplina: Química Ano: 2º Ensino Médio Professora: Luana P. Nunes P. Dayrell Química Atividades para Estudos Autônomos Data: 3 / 4 / 2018 Aluno(a):
EXAME Discursivo. 2 A fase 01/12/2013. Boa prova!
 2 A fase EXAME Discursivo 01/12/2013 Química Caderno de prova Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
2 A fase EXAME Discursivo 01/12/2013 Química Caderno de prova Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
GERÊNCIA DE REJEITOS RADIOATIVOS DE BAIXO E MÉDIO NÍVEIS DE RADIAÇÃO
 Resolução CNEN nº 167/14 Abril / 2014 GERÊNCIA DE REJEITOS RADIOATIVOS DE BAIXO E MÉDIO NÍVEIS DE RADIAÇÃO Histórico da norma: Norma CNEN-NE-6.05 - Revogada Publicação: DOU 17.12.1985 Resolução CNEN 167/14
Resolução CNEN nº 167/14 Abril / 2014 GERÊNCIA DE REJEITOS RADIOATIVOS DE BAIXO E MÉDIO NÍVEIS DE RADIAÇÃO Histórico da norma: Norma CNEN-NE-6.05 - Revogada Publicação: DOU 17.12.1985 Resolução CNEN 167/14
Exame de Seleção Mestrado em Química Turma 2015 I
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2015
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2015
QUÍMICA LISTA DE RECUPERAÇÃO 3º BIMESTRE - 1º ANO. Professor: GIL KENNEDY DATA: 25 / 09 / 2017
 LISTA DE RECUPERAÇÃO 3º BIMESTRE - 1º ANO Professor: GIL KENNEDY DATA: 25 / 09 / 2017 QUÍMICA QUESTÃO 01 Localize na tabela periódica o elemento químico de número atômico 16. Sobre esse elemento, responda
LISTA DE RECUPERAÇÃO 3º BIMESTRE - 1º ANO Professor: GIL KENNEDY DATA: 25 / 09 / 2017 QUÍMICA QUESTÃO 01 Localize na tabela periódica o elemento químico de número atômico 16. Sobre esse elemento, responda
SÓ ABRA QUANDO AUTORIZADO.
 UNIVERSIDADE FEDERAL DE MINAS GERAIS QUÍMICA Prova de 2 a Etapa SÓ ABRA QUANDO AUTORIZADO. Leia atentamente as instruções que se seguem. 1 - Este Caderno de Prova contém cinco questões, constituídas de
UNIVERSIDADE FEDERAL DE MINAS GERAIS QUÍMICA Prova de 2 a Etapa SÓ ABRA QUANDO AUTORIZADO. Leia atentamente as instruções que se seguem. 1 - Este Caderno de Prova contém cinco questões, constituídas de
Universidade Federal de Uberlândia PROGRAD Pró-Reitoria de Graduação. - Comissão Permanente de Vestibular PROCESSO SELETIVO
 Universidade Federal de Uberlândia PROGRAD Pró-Reitoria de Graduação - Comissão Permanente de Vestibular PROCESSO SELETIVO 2009/2 2 SEGUNDO DIA 13 de julho de 2009 Início às 14h, com duração de 4h e 30
Universidade Federal de Uberlândia PROGRAD Pró-Reitoria de Graduação - Comissão Permanente de Vestibular PROCESSO SELETIVO 2009/2 2 SEGUNDO DIA 13 de julho de 2009 Início às 14h, com duração de 4h e 30
Fluorescência de Raios-X: Fusão de Amostra com Borato
 Fluorescência de Raios-X: Fusão de Amostra com Borato 1.Parâmetro(s) medido (s): Al 2 O 3, CaO, Cr 2 O 3, Fe 2 O 3, K 2 O, MgO, MnO, Na 2 O, Nb, NiO, P 2 O 5, SiO 2, Sn, Sr, Ta, TiO 2, V, W, Y, Zr. 2.Tamanho
Fluorescência de Raios-X: Fusão de Amostra com Borato 1.Parâmetro(s) medido (s): Al 2 O 3, CaO, Cr 2 O 3, Fe 2 O 3, K 2 O, MgO, MnO, Na 2 O, Nb, NiO, P 2 O 5, SiO 2, Sn, Sr, Ta, TiO 2, V, W, Y, Zr. 2.Tamanho
ESCOPO DA ACREDITAÇÃO ABNT NBR ISO/IEC ENSAIO. Determinação da Demanda Química de Oxigênio pelo método colorimétrico com refluxo fechado
 ESCOPO DA ACREDITAÇÃO ABNT NBR ISO/IEC 17025 ENSAIO Norma de Origem: NIT-DICLA-016 Folha: 1 Total de Folhas: 9 RAZÃO SOCIAL/DESIGNAÇÃO DO LABORATÓRIO BASF S.A. Laboratorio Central de Controle de Qualidade
ESCOPO DA ACREDITAÇÃO ABNT NBR ISO/IEC 17025 ENSAIO Norma de Origem: NIT-DICLA-016 Folha: 1 Total de Folhas: 9 RAZÃO SOCIAL/DESIGNAÇÃO DO LABORATÓRIO BASF S.A. Laboratorio Central de Controle de Qualidade
Si, Ge, SiO 2, ZnS, etc. PF s e dureza elevados Insolúveis Isolantes (ou semicondutores)
 Sólidos covalentes C, diamante C, grafite Si, Ge, SiO 2, ZnS, etc. PF s e dureza elevados Insolúveis Isolantes (ou semicondutores) Sólidos covalentes TEV: rede 3D de ligações covalentes C, diamante (sp
Sólidos covalentes C, diamante C, grafite Si, Ge, SiO 2, ZnS, etc. PF s e dureza elevados Insolúveis Isolantes (ou semicondutores) Sólidos covalentes TEV: rede 3D de ligações covalentes C, diamante (sp
FÍSICA. Questões de 01 a 04
 GRUPO 1 TIPO A FÍS. 1 FÍSICA Questões de 01 a 04 01. Considere o movimento de queda de uma partícula de massa, m, em um meio fluido cuja força de viscosidade pode ser modelada como sendo proporcional à
GRUPO 1 TIPO A FÍS. 1 FÍSICA Questões de 01 a 04 01. Considere o movimento de queda de uma partícula de massa, m, em um meio fluido cuja força de viscosidade pode ser modelada como sendo proporcional à
SÓ ABRA QUANDO AUTORIZADO.
 UNIVERSIDADE FEDERAL DE MINAS GERAIS QUÍMICA Prova de 2 a Etapa SÓ ABRA QUANDO AUTORIZADO. Leia atentamente as instruções que se seguem. 1 - Este Caderno de Prova contém cinco questões, constituídas de
UNIVERSIDADE FEDERAL DE MINAS GERAIS QUÍMICA Prova de 2 a Etapa SÓ ABRA QUANDO AUTORIZADO. Leia atentamente as instruções que se seguem. 1 - Este Caderno de Prova contém cinco questões, constituídas de
13 (III A) 12 (II B) 11 (I B) (VIII B) 28 Ni 58,7. 27 Co 58,9. 29 Cu 63,5. 30 Zn 65,4. 45 Rh 102,9. 46 Pd 106,4. 47 Ag 107,9. 48 Cd 112,4.
 2 ESTIBULAR UFMG v TABELA PERIÓDICA DOS ELEMENTOS 1 (I A) 18 (0) 1º 1 H 1,0 2 (II A) 1 H 1,0 13 (III A) 14 (IV A) 15 (V A) 16 (VI A) 17 (VII A) 2 He 4,0 2º 3 Li 6,9 4 Be 9,0 5 B 10,8 6 C 12,0 7 N 14,0
2 ESTIBULAR UFMG v TABELA PERIÓDICA DOS ELEMENTOS 1 (I A) 18 (0) 1º 1 H 1,0 2 (II A) 1 H 1,0 13 (III A) 14 (IV A) 15 (V A) 16 (VI A) 17 (VII A) 2 He 4,0 2º 3 Li 6,9 4 Be 9,0 5 B 10,8 6 C 12,0 7 N 14,0
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
 1 1 1 H 1, 00 2 3 4 2 Li 6, 94 Be 9, 01 11 12 3 Na Mg 22, 99 24, 31 19 20 4 K 39, 10 Ca 40, 08 37 38 5 Rb Sr 85, 47 87, 62 55 56 6 Cs 132, 91 Ba 137, 33 87 88 7 Fr Ra 223, 02 226, 03 CLASSIFICAÇÃ PERIÓDICA
1 1 1 H 1, 00 2 3 4 2 Li 6, 94 Be 9, 01 11 12 3 Na Mg 22, 99 24, 31 19 20 4 K 39, 10 Ca 40, 08 37 38 5 Rb Sr 85, 47 87, 62 55 56 6 Cs 132, 91 Ba 137, 33 87 88 7 Fr Ra 223, 02 226, 03 CLASSIFICAÇÃ PERIÓDICA
003. Ciências da Natureza e Matemática (Questões 13 24)
 VNSP1709 03003001 VESTIBULAR MEIO DE ANO 2017 Prova de Conhecimentos Específicos e Redação 10.06.2017 003. Ciências da Natureza e Matemática (Questões 13 24) Confira seus dados impressos neste caderno.
VNSP1709 03003001 VESTIBULAR MEIO DE ANO 2017 Prova de Conhecimentos Específicos e Redação 10.06.2017 003. Ciências da Natureza e Matemática (Questões 13 24) Confira seus dados impressos neste caderno.
OMQ 2018: Questões. Instruções:
 Instruções: 1 Esta prova contém 20 questões de múltipla escolha e três questões discursivas. 2 Antes de iniciar a prova, confira se todas as folhas estão presentes. Caso haja algum problema, solicite a
Instruções: 1 Esta prova contém 20 questões de múltipla escolha e três questões discursivas. 2 Antes de iniciar a prova, confira se todas as folhas estão presentes. Caso haja algum problema, solicite a
Versão 1. Na folha de respostas, indique de forma legível a versão do teste.
 Teste Intermédio de Física e Química A Versão Teste Intermédio Física e Química A Versão Duração do Teste: 90 minutos 03.03.0 0.º Ano de Escolaridade Decreto-Lei n.º 74/004, de 6 de Março Na folha de respostas,
Teste Intermédio de Física e Química A Versão Teste Intermédio Física e Química A Versão Duração do Teste: 90 minutos 03.03.0 0.º Ano de Escolaridade Decreto-Lei n.º 74/004, de 6 de Março Na folha de respostas,
CURSOS Ciências Habilitação em Química e Química Industrial. Só abra este caderno quando o fiscal autorizar. Leia atentamente as instruções abaixo.
 PROCESSO SELETIVO 2004/1 QUÍMICA CURSOS Ciências Habilitação em Química e Química Industrial Só abra este caderno quando o fiscal autorizar. Leia atentamente as instruções abaixo. 1. 2. 3. 4. Este caderno
PROCESSO SELETIVO 2004/1 QUÍMICA CURSOS Ciências Habilitação em Química e Química Industrial Só abra este caderno quando o fiscal autorizar. Leia atentamente as instruções abaixo. 1. 2. 3. 4. Este caderno
QUÍMICA 2ª FASE EXAME DISCURSIVO 11/12/2016 CADERNO DE PROVA INSTRUÇÕES INFORMAÇÕES GERAIS BOA PROVA!
 2ª FASE EXAME DISCURSIVO 11/12/2016 QUÍMICA CADERNO DE PROVA Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
2ª FASE EXAME DISCURSIVO 11/12/2016 QUÍMICA CADERNO DE PROVA Este caderno, com dezesseis páginas numeradas sequencialmente, contém dez questões de Química. A Classificação Periódica dos Elementos está
