HIV 1&2 CombFirm. Figura 1. Princípio do Teste
|
|
|
- Gonçalo da Fonseca Carvalho
- 10 Há anos
- Visualizações:
Transcrição
1 HIV 1&2 CombFirm B Os resultados dos testes do kit ImmunoComb II HIV1& 2 CombFirm são comparáveis àqueles obtidos por Western Blot. Ao invés da necessidade de realizar dois blots demorados, a reatividade para anticorpos para o HIV-1 ou 2 pode ser rapidamente confirmada em um único teste simples. Princípio do Teste O teste ImmunoComb II HIV1&2 CombFirm é um ensaio imunoenzimático (EIA) indireto em fase sólida. A fase sólida é um pente com doze projeções ( dentes ). Cada pente tem seis pares de dentes, com seis pontos de antígenos por par (3 pontos em cada dente). O dente da esquerda de cada par traz um ponto superior sensibilizado com imunoglobulina humana (Controle Interno) e os dois marcadores proteicos p24 (gag) e p31 (pol). O dente da direita tem os pontos das três proteínas derivadas de env gp41, gp120 e gp36. A Placa Reveladora tem 6 fileiras (A-F), cada fileira contendo uma solução de reagente pronta para uso em diferentes etapas do ensaio. O teste é realizado por etapas, movendo-se o pente de fileira a fileira com incubação em cada etapa. Antes de iniciar o teste, as amostras de soro ou plasma são adicionadas ao diluente, nas cavidades da fileira A da Placa Reveladora. O Pente é então inserido nas cavidades da fileira A. Os anticorpos anti-hiv, se presentes na amostra, irão ligar-se especificamente aos antígenos de HIV, no dente do Pente (Figura 1). Os componentes não ligados são lavados na fileira B. Na fileira C, o IgG anti-hiv capturado no dente e a imunoglobulina humana do ponto superior (Controle Interno), reagirão com anticorpos anti-igg humana marcados com fosfatase alcalina (FA). Nas próximas duas fileiras, os componentes não ligados são removidos por lavagem. Na fileira F, a fosfatase alcalina ligada irá reagir com os componentes cromogênicos. Os resultados são visualizados como pontos cinza azulados na superfície do dente do Pente. Formação do complexo antígeno HIV-anticorpo; 30 min Código: Formato: 3 x 6 tests Utilização In Vitro O kit ImmunoComb II HIV 1&2 CombFirm é um teste confirmatório. O teste permite confirmar uma amostra de soro ou plasma humano inicialmente reativo para HIV. Podem ser realizados dezoito testes com um kit. Introdução O vírus da imunodeficiência humana (HIV) é um retrovírus, identificado em 1983 como o agente etiológico da Síndrome da Imunodeficiência Adquirida (AIDS). Foram diferenciados dois tipos, HIV-1 e HIV-2, com prognóstico e porcentagem de transmissão diferente. As principais vias de transmissão do vírus HIV são: contato sexual, contaminação pelo sangue ou produtos do sangue e transmissão da mãe para o recém-nascido. O HIV infecta predominantemente os linfócitos CD4, que desempenham um papel chave no sistema imune humano. A diminuição progressiva do nível de CD4 durante o desenvolvimento da doença leva a uma condição de imunocomprometimento, facilitando as infecções oportunistas, com conseqüências fatais. O vírus HIV é formado por uma molécula RNA genômica associada com a transcriptase reversa (RT), protegida por um capsídeo e um envelope. O envelope do vírus é o alvo principal para a resposta humoral de anticorpos. Conseqüentemente, os testes de triagem de HIV, altamente sensíveis, estão baseados primeiramente na detecção de anticorpos para antígenos derivados de componentes de envelope (env). Para diferenciar reações verdadeiras de falsas, um resultado positivo em um ensaio de triagem de HIV deve ser retestado e confirmado por um teste de maior especificidade. A confirmação sorológica de uma infecção por HIV, comumente realizada usando um ensaio de Western Blot, está baseada na detecção diferencial de anticorpos direcionados contra os antígenos do HIV. O teste ImmunoComb II HIV1&2 CombFirm emprega cinco diferentes antígenos, recombinantes e sintéticos de HIV para a determinação sorológica rápida do perfil de anticorpos HIV. Dois antígenos são proteínas derivadas de pol e de gag, reativas com os dois tipos de HIV, enquanto que três antígenos são proteínas ou peptídeos derivados do env, específicos tanto para HIV-1 como para HIV-2. Os antígenos estão posicionados separadamente, em concentrações fixas, e livres de antígenos tissulares, que podem contaminar as preparações de antígenos dos lisados virais, comumente usados nos Western Blots. Anticorpo Anti-HIV Conjugado anti-igg Humano Substrato cromogenico Figura 1. Princípio do Teste Ligação do conjugado anti-igg Humano, 20 min Reação enzimatica colorida,10 min O kit inclui um Controle (anticorpos para HIV-1 e HIV-2) e um Controle Negativo, para serem incluídos em cada ensaio. Ao término do teste, o par de dentes usado com o Controle deve mostrar todos os 6 pontos cinza azulados, e aqueles usados com o Controle Negativo devem mostrar apenas o ponto do Controle Interno. O ponto do Controle Interno deve também aparecer em todos os outros dentes, para confirmar se o kit está funcionando adequadamente e se o teste foi realizado corretamente. Conteúdo do kit Pentes O kit contém 3 Pentes de plástico. Cada Pente tem 6 pares de dentes, um par para cada teste (Figura 2). Os dois dentes do par tem números idênticos. Cada par de dentes está sensibilizado com seis áreas reativas: Posição No dente esquerdo No dente direito Superior Anticorpos anti- IgG humana Glicoproteína recombinante (Controle Interno) gp120 derivada de Central Inferior Proteína recombinante p24 derivada de gag (específica para anti-hiv-1 & anti-hiv-2) Proteína recombinante p31 derivada de pol (específica para anti-hiv-1 & anti-hiv-2) env HIV-1. Peptídeo sintético derivado de glicoproteína transmembrana gp41 de env HIV-1. Peptídeo sintético derivado de glicoproteína transmembrana gp36 de env HIV /B4 1
2 ImmunoComb II Controle Interno p24 Figure 2. Pente p31 gp120 gp41 gp36 Os pentes são fornecidos em embalagens de alumínio, contendo dessecante. Placas Reveladoras O kit contém 3 Placas Reveladoras cobertas por folhas de alumínio. Cada Placa Reveladora (Figura 3) contém todos os reagentes necessários para o teste. A Placa Reveladora consiste de 6 fileiras (A- F). A fileira A está dividida em 6 cavidades, enquanto as outras fileiras estão divididas em 12 cavidades cada. O conteúdo de cada fileira é: Fileira A Fileira B Fileira C Fileira D Fileira E Fileira F Diluente de amostra Anticorpos de cabra anti-igg humana, marcados com fosfatase alcalina Solução substrato cromogênico contendo 5-bromo- 4-cloro-3-indolil fosfato (BCIP) e azul de nitrotetrazolium (NBT) Figura 3. Placa Reveladora Controle 1 frasco (tampa vermelha) de 0,4 ml de plasma humano diluído, positivo para anticorpos anti-hiv-1 e anti-hiv-2, inativado pela adição de b-propilactona e pelo calor. Controle Negativo 1 frasco (tampa verde) de 0,4 ml de plasma humano diluído, inativado pelo calor, negativo para anticorpos para HIV. Perfurador para a perfuração da folha de alumínio que cobre as cavidades da Placa Reveladora. Segurança e Precauções Embora tenha sido inativado, trabalhar o controle positivo como potencialmente infeccioso. Todos os materiais de origem humana usados na preparação do kit foram testados e considerados não reativos para antígeno de superfície da hepatite B, anticorpos para hepatite C e anticorpos para HIV. Como nenhum teste pode garantir completamente a ausência de contaminação viral, todas as soluções de referência e amostras humanas devem ser manipuladas como potencialmente infectantes. Usar luvas cirúrgicas e avental. Seguir os procedimentos aceitos para laboratório para trabalhar com soro ou plasma. Não pipetar com a boca. Descartar todas as amostras, Pentes, Placas Reveladoras e outros materiais utilizados com o kit como resíduo bioinfectante. Não misturar reagentes de lotes diferentes. Não usar o kit após o vencimento. Armazenamento e Estabilidade do Kit Kit é fornecidoa 2-8º C. Durante o transporte o kit pode suportar temperaturas de <30º C por curtos períodos de tempo não excedendo no total as 48 horas.os controles internos indicam que o kit não foi afectado durante o transporte. Armazenar o kit na embalagem original de 2 a 8º C. Não congelar o kit. Após a primeira utilização do kit os componentes devem ser armazenados de 2 a 8º C. A performance do kit após a primeira utilização é estável até à data de validade do mesmo, quando armazenados de 2 a 8º C. Após a primeira utilização, o pente e a placa não podem ser usados mais do que três vezes. Manipulação de Amostras Você pode testar tanto soro como plasma. As amostras podem ser armazenadas por 7 dias de 2-8 ºC antes do teste. Para armazenar por mais de 7 dias, congelar as amostras a - 20 ºC ou inferior. Centrifugar as amostras de soro após descongelamento. Testar o sobrenadante. Evitar ciclos repetidos de congelamento e descongelamento. Foram encontrados anticoagulantes tais como Heparin, EDTA e Citrato de Sódio não tendo qualquer efeito nos Procedimento do Teste Material Necessário Pipeta de precisão e ponteiras descartáveis para dispensar 50 µl. Tesoura. Cronômetro ou relógio de laboratório. Preparando o Teste Trazer todos os componentes, Placa Reveladora, pentes, reagentes e amostras à temperatura ambiente e realizar o teste à temperatura de 22 26ºC. Preparando a Placa Reveladora 1. Incubar a Placa Reveladora em uma incubadora a 37ºC por 30 minutos; ou deixar a temperatura ambiente (22 26ºC) por 3 horas. 2. Cobrir a bancada de trabalho com papel absorvente para ser descartado como resíduo bioinfectante no final do teste. 3. Misturar os reagentes agitando a Placa Reveladora. Nota: Não remover a folha de alumínio da Placa Reveladora. Furar a cobertura de alumínio usando a ponteira descartável da pipeta ou o perfurador, somente quando indicado, nas instruções do Teste. Preparando o Pente Precaução: Para assegurar o funcionamento correto do teste, não tocar nos dentes do pente. 1. Rasgar a embalagem de alumínio do Pente na extremidade marcada. Remover o Pente. 2. O Pente e a Placa Reveladora podem ser utilizados total ou parcialmente. Para usar parte de um pente: a. Determinar quantos pares de dentes são necessários para testar as amostras e controles. Será necessário um par para cada teste. Cada par de dentes mostra o número 34 do código do kit, para permitir a identificação dos dentes destacados. b. Dobrar e quebrar o Pente verticalmente ou cortar com a tesoura (veja Figura 4) para destacar o número necessário de pares de dentes (nº de testes incluindo 2 controles). Não separar os dentes pareados. c. Retornar a parte do Pente não utilizada para o saco de alumínio (com o dessecante). Fechar bem a embalagem, por exemplo, com um clips, para manter seco. Armazenar o Pente na caixa original do kit de 2 8ºC para uso posterior. ImmunoComb II Figura 4. Quebrando o Pente Instruções do Teste Reação Antígeno-Anticorpo (Fileira A da Placa Reveladora) 1. Pipetar 50 µl de amostra. Perfurar a cobertura de alumínio de uma cavidade da fileira A da Placa Reveladora com a ponteira da pipeta ou com o perfurador e dispensar a amostra no fundo da cavidade. Misturar enchendo e esvaziando repetidamente a ponteira com a solução. Descartar a ponteira. 2. Repetir o passo 1 para as outras amostras, incluindo um Controle e um Negativo fornecidos com o kit. Usar uma nova cavidade da fileira A e trocar a ponteira para cada amostra ou controle. 434/B4 2
3 3. a) Inserir o Pente (o lado impresso de frente para você) nas cavidades da fileira A contendo as amostras e controles. Misturar: Retirar e inserir o Pente nas cavidades várias vezes. b) Deixar o Pente na fileira A por 30 minutos exatos. Ajustar o cronômetro. Próximo do final dos 30 minutos, perfurar a cobertura da fileira B usando o perfurador. Não abrir mais cavidades que o necessário. c) No final dos 30 minutos, retirar o Pente da fileira A. Absorver o líquido residual nas pontas dos dentes em papel absorvente limpo. Não tocar na superfície frontal dos dentes. Primeira Lavagem (Fileira B) 4. Inserir o Pente nas cavidades da fileira B. Agitar: Retirar e inserir vigorosamente o Pente nas cavidades e deixar pelo menos 10 segundos para obter uma lavagem apropriada. Repetir a agitação várias vezes no período de 2 minutos; neste intervalo perfurar a cobertura da fileira C. Após 2 minutos, retirar o Pente e absorver o líquido residual como no passo 3c. Ligação do Conjugado (Fileira C) 5. Inserir o Pente nas cavidades da fileira C. Misturar como no passo 3a. Ajustar o cronômetro para 20 minutos. Perfurar a cobertura da fileira D. Após 20 minutos, tirar o Pente e absorver o líquido residual. Segunda Lavagem (Fileira D) 6. Inserir o Pente nas cavidades da fileira D. Agitar repetidamente durante 2 minutos, como no passo 4. Neste intervalo, perfurar a cobertura da fileira E. Depois de 2 minutos, retirar o Pente e absorver o líquido residual. Terceira Lavagem (Fileira E) 7. Inserir o Pente nas cavidades da fileira E. Agitar repetidamente durante 2 minutos. Neste intervalo, perfurar a cobertura da fileira F. Após de 2 minutos, retirar o Pente e absorver o líquido residual. Reação de Cor (Fileira F) 8. Inserir o Pente nas cavidades da fileira F. Misturar. Ajustar o cronômetro para 10 minutos. Após 10 minutos, retirar o Pente. Reação de Parada (Fileira E) 9. Inserir o Pente novamente na fileira E. Após 1 minuto, retirar o Pente e deixar secar ao ar livre. Descarte do Resíduo Descartar as Placas Reveladoras utilizadas, ponteiras das pipetas, papel absorvente e luvas como lixo bioinfectante. Armazenamento da parte não utilizada do kit Placa Reveladora Se todas as cavidades da Placa Reveladora não foram utilizadas, podem ser guardadas para uso futuro: Selar as cavidades utilizadas com fita adesiva, de forma a evitar respingos, mesmo que a Placa Reveladora tenha sido esvaziada. Outros materiais do kit: Retornar o restante das Placas Reveladoras, Pentes, perfurador, controles e instruções de uso ao kit. Armazenar de 2 a 8ºC. Resultados dos Testes Validação Para confirmar o funcionamento correto do teste e demonstrar que os resultados são válidos, as três condições abaixo devem ser cumpridas (veja figura 5): 1. O Controle deve produzir seis pontos cinza azulados no par correspondente do dente do Pente. 2. O Controle Negativo deve produzir um ponto superior (Controle interno) no dente esquerdo do par e nenhum outro ponto. 3. Cada amostra testada deve produzir um ponto superior (Controle interno) no dente esquerdo do par. Se alguma destas três condições não for cumprida, os resultados são inválidos e as amostras e controles devem ser retestados. Controle Controle Negtivo Figura 5. Validação dos testes. Resultados Inválidos Interpretação dos Resultados O desenvolvimento do ponto do Controle Interno indica que a amostra correspondente é negativa para a sorologia HIV. Uma amostra é considerada indeterminada quando apresenta somente um ponto circular isolado colorido de antígeno de HIV ou ambos os pontos p24 e p31 sem pontos no dente direito. Uma amostra apresentando no mínimo dois pontos circulares coloridos de antígeno de HIV, incluindo um representando o gp41 ou gp36 (veja a Figura 2), é definido como HIV positivo. Nestes casos a diferenciação entre HIV-1 e HIV-2 pode ser obtida como segue: A ausência de um ponto para o gp36 e presença do gp41 e/ou gp120 indica que a amostra é positiva para anticorpos HIV-1. A presença de um ponto para o gp36 indica que a amostra é positiva para anticorpos HIV-2. Os padrões mais prevalentes de pontos e suas interpretações estão resumidos na Tabela 1. Tabela 1. Interpretação dos resultados Padrões dos pontos de HIV presentes em: Interpretação Dente esquerdo Dente direito para p24 e/ou p31 gp41 HIV-1 Ausência de ponto gp41 e gp120 p24 e/ou p31 gp36 isolada ou com HIV-2 gp41 p24 e/ou p31 gp36, gp41 e gp120 HIV-2 isolado ou co-infecção com HIV-1 p24 e/ou p31 Ausência de ponto ou gp120 Indeterminado Ausência de ponto gp41 ou gp120 e/ou gp36 Ausência de ponto Ausência de ponto Negativo Importante: Qualquer ponto fracamente colorido no dente deve ser interpretado como reativo. No caso de um resultado indeterminado, coletar uma nova amostra de sangue e repetir o teste. Documentação dos Resultados Como a cor desenvolvida no Pente é estável, os pentes podem ser guardados para documentação. Limitações O ImmunoComb II HIV 1&2 CombFirm é um ensaio suplementar destinado para confirmar a presença de anticorpos para antígenos HIV, em amostras inicialmente reativas. Na ausência de critérios uniformes aceitáveis para a interpretação de perfis de anticorpos para HIV, a interpretação acima descrita deve ser considerada como uma diretriz recomendada. Todavia, a reatividade para anticorpos para HIV-1/HIV-2 não deve ser considerada como único critério para o diagnóstico da Síndrome da Imunodeficiência Adquirida (AIDS) ou da infecção pelo HIV. Visto que a produção de anticorpos pode ser prolongada, seguindo a exposição inicial ao HIV, ou ser suprimida devido a condições de imunocomprometimento de um paciente, um resultado negativo com este teste não deve ser considerado como evidência conclusiva que o paciente não tenha sido exposto ao ou infectado pelo HIV. Características de Desempenho* A. Estudo Multicêntrico Um estudo multicêntrico foi realizado em 559 amostras incluindo 154 indivíduos HIV negativos, 318 pacientes HIV-1 positivos, 35 pacientes que foram positivos por ELISA e indeterminados (Ind.) para HIV-1 por Western Blot (WB), assim como 52 indivíduos que foram positivos por ELISA e negativos por WB. A população negativa incluiu mulheres grávidas, pessoas com doenças autoimunes e com infecção por hepatite. Os resultados estão demonstrados na Tabela 2. Tabela 2. Estudo Multicêntrico a Status de HIV-1 ImmunoComb II HIV 1 & 2 CombFirm ELISA WB Negativo HIV-1 Ind. Negativo Negativo Ind b Negativo a Resultados preliminares b Incluindo seis WB apresentando apenas p17 ou p55 434/B4 3
4 As seguintes características de desempenho foram calculadas incluindo apenas resultados positivos ou negativos inequívocos: Sensibilidade 99,7% Especificidade 100% B. Amostras de Pacientes originários da África Um estudo foi realizado em amostras de indivíduos com origem africana. A população compreendida de 48 indivíduos HIV negativos, 51 pacientes infectados com HIV-1, 84 infetados com HIV-2 e 9 coinfectados com HIV-1 e HIV-2. Os resultados estão demonstrados na Tabela 3. Tabela 3. Amostras de Origem Africana Status de HIV a ImmunoComb II HIV 1 & 2 CombFirm Neg. HIV 1 HIV 2 HIV Ind. Negativo HIV HIV b HIV a Por ELISA e WB b Reativo apenas com gp36 Os dados, excluindo os resultados indeterminados, apresentaram 100% de sensibilidade e especificidade para HIV. Todas as amostras positivas para HIV-1, incluindo 5 amostras com subtipo O, foram corretamente identificadas. Entre as amostras positivas para HIV-2, 10 apresentaram reação cruzada contra a gp120, resultando em uma especificidade diferencial total de 93,8%. * Informação detalhada disponível mediante solicitação. Bibliografia Center for Disease Control Interpretation and use of the Western Blot assay for serodiagnosis of Human Immunodeficiency Virus type 1 infection. MMWR 38 (S-7): 1-4. Dax EM HIV testing and stating, disease progression, and markers. Curr Opinion Infect Dis 6: Groopman JE, Chen FW, Hope JA, Andrews JM, Swift RL, Benton CV, Sullivan JL, Volberding PA, Sites DP, Landesman S, Gold J,Baker L, Craven D, Boohes FE Serological characterization of HTLV-III infection in AIDS and related disorders. J Infect Dis 153: Higgins JR, Pederson NC, Carison JR Detection and differentiation by sandwich enzyme-linked immunosorbent test for human T-cell lymphotropic virus III, lymphadenopathy-associated virus (LAV) and acquired immunodeficiency syndrome-associated retroviruslike clinical isolates. J Clin Microbiol 24: Jackson JB, Balfour HH Practical diagnostic testing for human immunodeficiency virus. Clin Microbiol Rev, 1: Lacroix M, Penney CL, Dwyer RJ, Stern MD, Bellini F, Dionne G, Tsoukas C A peptide-based microtiter ELISA kit for the detection of antibodies to HIV-1 and HIV-2, Fifth International Conference on AIDS. Montréal. W.B.P Gnann Jr JW, McGormick JB, Mitchell S, Nelson JA, Oldstone Synthetic peptide immunoassay distinguishes HIV type 1 and type 2 infections. Science 237: Myers RA, Patel JD, Joseph JM Identifying HIV-2-seropositive individuals by reevaluating HIV 1 indeterminate sera. J Acquir Immunedef Syndr 5: Samgadharan MG, Veronese F, Lee S, Gallo RC Immunological properties of HTLV-III antigens recognized by sera of patients with AIDS and AIDS-related complex and of asymptomatic carriers of HTLV-III infection. Cancer Res 45: 4574s-4577s. Produzido por: ORGENICS LTD. P.O.Box 360, Yavne ISRAEL Registro e Distribuição: ORGENICS DO BRASIL LTDA. Alameda dos Ubiatans, Planalto Paulista São Paulo - SP CNPJ : / Atendimento ao consumidor SAC: (11) FAX: (11) [email protected] Uso exclusivo para diagnóstico "in vitro" Registro ANVISA nº Resp. Técnico : Marcelo Ferreira Carlos Cuhna CRF-SP CONSERVAR ENTRE 2-8ºC Versão: 434/B4 (12/2004) Legenda dos símbolos CARD PLATE CONTROL + CONTROL - PERFORATOR IVD Σ 18 REF LOT ImmunoComb cartão Placas reveladora Controlo Controlo Negativo Perfurador Consulte instruções para o uso Atenção, veja as instruções de uso No Dispositivo Médico Diagnóstico In Vitro Limitação da temperatura Contem suficiente material para 18 testes Fabricante Número de catálogo código do lote Uso até número de série Fabricante: P.O.Box 360 Yavne 70650, Israel Tel: Fax: /B4 4
5 Resumo dos Principais Procedimentos do Teste Pré-incubação da Placa Reveladora: 3 hrs, a temperature ambiente ou 30 minutos a 37 C Aspirar as amostras e controles Adicionar as amostras e controles no orifício A. Misturar. Remover o pente da embalagem. Colocar o Pente no orificio A e misturar. Incubar Abrir os orificios B Absorver o líquido acumulado nos dentes Inserir o Pente e agitar na coluna B. Incubar Após misturar/agitar & incubar nas colunas C, D E. Reação de cor na fileira F 9 10 Resultados Resumo do Procedimento de Teste As instruções resumidas abaixo são para usuários experientes do kit ImmunoComb II HIV 1 & 2 CombFirm. (Para instruções detalhadas, por favor, veja o texto completo). 1. Deixe que todos os reagentes e amostras atinjam a temperatura ambiente e realize o teste em temperatura ambiente. 2. Dispense 50 µl de cada amostra e controle em cavidades da fileira A da Placa Reveladora e misture. 3. Coloque o Pente na fileira A e continue como descrito na Tabela 1: 1 Tabela 1. Resumo do Procedimento de Teste. Etapa Fileira Proceda como a seguir Reação antígeno-anticorpo A Misture; incube por 30 minutos; absorva. Lavagem B Agite; incube por 2 minutos; absorva. Ligação do conjugado C Misture; incube por 20 minutos; absorva. Lavagem D Agite; incube por 2 minutos; absorva. Lavagem E Agite; incube por 2 minutos; absorva. Reação de cor F Misture; incube por 10 minutos. Reação de parada E Incube por 1 minuto; seque ao ar livre. Dobrando e quebrando o Pente /B4 5
Aos bioquímicos, técnicos de laboratório e estagiários do setor de imunologia.
 POP-I 67 Página 1 de 5 1. Sinonímia Teste rápido Anti-½ - OraQuick ADVANCE 2. Aplicabilidade Aos bioquímicos, técnicos de laboratório e estagiários do setor de imunologia. 3. Aplicação clínica O ensaio
POP-I 67 Página 1 de 5 1. Sinonímia Teste rápido Anti-½ - OraQuick ADVANCE 2. Aplicabilidade Aos bioquímicos, técnicos de laboratório e estagiários do setor de imunologia. 3. Aplicação clínica O ensaio
Aos bioquímicos, técnicos de laboratório e estagiários do setor de imunologia e hematologia.
 POP n.º: I70 Página 1 de 5 1. Sinonímia Teste rápido Anti-, VIKIA Biomeriéux. 2. Aplicabilidade Aos bioquímicos, técnicos de laboratório e estagiários do setor de imunologia e hematologia. 3. Aplicação
POP n.º: I70 Página 1 de 5 1. Sinonímia Teste rápido Anti-, VIKIA Biomeriéux. 2. Aplicabilidade Aos bioquímicos, técnicos de laboratório e estagiários do setor de imunologia e hematologia. 3. Aplicação
Elaborado por: Karina Salvador Revisado por: Hilda Helena Wolff Aprovado por: Andréa Cauduro
 ANTI- 1 Manual CAMBRIDGE BIOTECH -1 POP: BM 05 Página 1 de 7 1. Sinonímia ANTI, TESTE CONFIRMATÓRIO. 2. Aplicabilidade Aos bioquímicos e técnicos do setor de imunologia. 3. Aplicação clínica Os testes
ANTI- 1 Manual CAMBRIDGE BIOTECH -1 POP: BM 05 Página 1 de 7 1. Sinonímia ANTI, TESTE CONFIRMATÓRIO. 2. Aplicabilidade Aos bioquímicos e técnicos do setor de imunologia. 3. Aplicação clínica Os testes
HAV Ab. do ensaio. O teste é realizado por etapas, movendo-se o Pente de fileira a fileira com incubação em cada etapa.
 HAV Ab P do ensaio. O teste é realizado por etapas, movendo-se o Pente de fileira a fileira com incubação em cada etapa. Antes de iniciar o teste, as amostras de soro ou plasma são prédiluídas a 1:50 e
HAV Ab P do ensaio. O teste é realizado por etapas, movendo-se o Pente de fileira a fileira com incubação em cada etapa. Antes de iniciar o teste, as amostras de soro ou plasma são prédiluídas a 1:50 e
HIV 1&2 CombFirm. Figura 1. Princípio do Teste
 HIV 1&2 CombFirm P Princípio do Teste O teste ImmunoComb II HIV1&2 CombFirm é um ensaio imunoenzimático (EIA) indireto em fase sólida. A fase sólida é um pente com doze projeções ( dentes ). Cada pente
HIV 1&2 CombFirm P Princípio do Teste O teste ImmunoComb II HIV1&2 CombFirm é um ensaio imunoenzimático (EIA) indireto em fase sólida. A fase sólida é um pente com doze projeções ( dentes ). Cada pente
Anti HBc Ref. 414. Controle Negativo
 Anti HBc Ref. 414 Sistema para a determinação qualitativa de anticorpos totais contra o antígeno core do vírus da hepatite B (anti-hbc) em soro ou plasma. ELISA - Competição PREPARO DA SOLUÇÃO DE LAVAGEM
Anti HBc Ref. 414 Sistema para a determinação qualitativa de anticorpos totais contra o antígeno core do vírus da hepatite B (anti-hbc) em soro ou plasma. ELISA - Competição PREPARO DA SOLUÇÃO DE LAVAGEM
ALBUMINA BOVINA 22% PROTHEMO. Produtos Hemoterápicos Ltda. PARA TESTES EM LÂMINA OU TUBO SOMENTE PARA USO DIAGNÓSTICO IN VITRO
 ALBUMINA BOVINA 22% PROTHEMO Produtos Hemoterápicos Ltda. PARA TESTES EM LÂMINA OU TUBO SOMENTE PARA USO DIAGNÓSTICO IN VITRO Conservar entre: 2º e 8ºC Não congelar Conservante: Azida de Sódio 0,1 % Responsável
ALBUMINA BOVINA 22% PROTHEMO Produtos Hemoterápicos Ltda. PARA TESTES EM LÂMINA OU TUBO SOMENTE PARA USO DIAGNÓSTICO IN VITRO Conservar entre: 2º e 8ºC Não congelar Conservante: Azida de Sódio 0,1 % Responsável
Etapa complementar para o diagnóstico da infecção pelo HIV princípios metodológicos
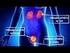 Aula 11 Etapa complementar para o diagnóstico da infecção pelo HIV princípios metodológicos As amostras com resultados reagentes, na etapa de triagem, devem ser submetidas à etapa complementar. Nessa etapa,
Aula 11 Etapa complementar para o diagnóstico da infecção pelo HIV princípios metodológicos As amostras com resultados reagentes, na etapa de triagem, devem ser submetidas à etapa complementar. Nessa etapa,
ANTI D IgM +IgG Monoclonal (Humano)
 ANTI D IgM +IgG Monoclonal (Humano) PROTHEMO Produtos Hemoterápicos Ltda. Reagente para classificação do fator Rh PARA TESTES EM LÂMINA OU TUBO Somente para Uso Diagnóstico IN VITRO Conservar entre: 2-8
ANTI D IgM +IgG Monoclonal (Humano) PROTHEMO Produtos Hemoterápicos Ltda. Reagente para classificação do fator Rh PARA TESTES EM LÂMINA OU TUBO Somente para Uso Diagnóstico IN VITRO Conservar entre: 2-8
ANTI-A ANTI-B ANTI-AB
 ANTI-A ANTI-B ANTI-AB Monoclonal Murino IgM PROTHEMO Produtos Hemoterápicos Ltda. Reagentes para classificação do sistema sangüíneo ABO PARA TESTES EM LÂMINA OU TUBO Somente para Uso Diagnóstico IN VITRO
ANTI-A ANTI-B ANTI-AB Monoclonal Murino IgM PROTHEMO Produtos Hemoterápicos Ltda. Reagentes para classificação do sistema sangüíneo ABO PARA TESTES EM LÂMINA OU TUBO Somente para Uso Diagnóstico IN VITRO
ANTI IgG (Soro de Coombs)
 ANTI IgG (Soro de Coombs) Soro Anti Gamaglobulinas Humanas PROTHEMO Produtos Hemoterápicos Ltda. PARA TESTES EM LÂMINA OU TUBO SOMENTE PARA USO DIAGNÓSTICO IN VITRO Conservar entre: 2º e 8ºC Não congelar
ANTI IgG (Soro de Coombs) Soro Anti Gamaglobulinas Humanas PROTHEMO Produtos Hemoterápicos Ltda. PARA TESTES EM LÂMINA OU TUBO SOMENTE PARA USO DIAGNÓSTICO IN VITRO Conservar entre: 2º e 8ºC Não congelar
Helicobacter pylori IgG
 P Helicobacter pylori IgG Princípio do Teste O teste ImmunoComb Helicobacter pylori IgG é um ensaio imunoenzimático (EIA) indireto em fase sólida. A fase sólida é um pente com 12 projeções ( dentes ).
P Helicobacter pylori IgG Princípio do Teste O teste ImmunoComb Helicobacter pylori IgG é um ensaio imunoenzimático (EIA) indireto em fase sólida. A fase sólida é um pente com 12 projeções ( dentes ).
GRUPO HOSPITALAR CONCEIÇÃO HOSPITAL NOSSA SENHORA DA CONCEIÇÃO LABORATÓRIO DE ANÁLISES CLÍNICAS
 1. Sinonímia VIDAS DUO 2. Aplicabilidade Aos bioquímicos do setor de imunologia. 3. Aplicação clínica POP n.º: I 56 Página 1 de 7 O vírus da imunodeficiência humana () é um retrovírus RNA, transmitido
1. Sinonímia VIDAS DUO 2. Aplicabilidade Aos bioquímicos do setor de imunologia. 3. Aplicação clínica POP n.º: I 56 Página 1 de 7 O vírus da imunodeficiência humana () é um retrovírus RNA, transmitido
GRUPO HOSPITALAR CONCEIÇÃO HOSPITAL NOSSA SENHORA DA CONCEIÇÃO LABORATÓRIO DE ANÁLISES CLÍNICAS
 POP n.º: I 29 Página 1 de 5 1. Sinonímia Pesquisa de anticorpos frios. 2. Aplicabilidade Bioquímicos e auxiliares de laboratório do setor de Imunologia. 3. Aplicação clínica As Crioaglutininas são anticorpos
POP n.º: I 29 Página 1 de 5 1. Sinonímia Pesquisa de anticorpos frios. 2. Aplicabilidade Bioquímicos e auxiliares de laboratório do setor de Imunologia. 3. Aplicação clínica As Crioaglutininas são anticorpos
ANTI HUMANO. Anti IgG Anti C 3 d Poliespecífico
 ANTI HUMANO Anti IgG Anti C 3 d Poliespecífico PROTHEMO Produtos Hemoterápicos Ltda. PARA TESTES EM LÂMINA OU TUBO SOMENTE PARA USO DIAGNÓSTICO IN VITRO Conservar entre: 2º e 8ºC Não congelar Conservante:
ANTI HUMANO Anti IgG Anti C 3 d Poliespecífico PROTHEMO Produtos Hemoterápicos Ltda. PARA TESTES EM LÂMINA OU TUBO SOMENTE PARA USO DIAGNÓSTICO IN VITRO Conservar entre: 2º e 8ºC Não congelar Conservante:
Helicobacter pylori IgG
 Helicobacter pylori IgG B Princípio do Teste O teste ImmunoComb II Helicobacter pylori IgG é um ensaio imunoenzimático (EIA) indireto em fase sólida. A fase sólida é um pente com 12 projeções ( dentes
Helicobacter pylori IgG B Princípio do Teste O teste ImmunoComb II Helicobacter pylori IgG é um ensaio imunoenzimático (EIA) indireto em fase sólida. A fase sólida é um pente com 12 projeções ( dentes
ANEXO II. 1 HEPATITE B VÍRUS DA HEPATITE B (Hepatitis B Vírus HBV)
 ANEXO II ANEXO DA RESOLUÇÃO SESA Nº.../2009 MANUAL DE ORIENTAÇÃO PARA ALTERAÇÃO DA CAUSA DE REJEIÇÃO DO CÓDIGO 57 (INCONCLUSIVO), PELOS SERVIÇOS DE HEMOTERAPIA NO SHTWEB. 1. Segundo a RDC nº 153 de 14
ANEXO II ANEXO DA RESOLUÇÃO SESA Nº.../2009 MANUAL DE ORIENTAÇÃO PARA ALTERAÇÃO DA CAUSA DE REJEIÇÃO DO CÓDIGO 57 (INCONCLUSIVO), PELOS SERVIÇOS DE HEMOTERAPIA NO SHTWEB. 1. Segundo a RDC nº 153 de 14
INSTRUÇÕES DE USO CARTUCHO-BULA. CLEARLENS SOLUÇÃO MULTIUSO Solução Multiuso para Lentes de Contato
 INSTRUÇÕES DE USO CARTUCHO-BULA CLEARLENS SOLUÇÃO MULTIUSO DESCRIÇÃO: CLEARLENS Solução Multiuso tem ação de limpar, desinfetar, enxaguar, lubrificar e conservar as lentes de contato sem irritar os olhos.
INSTRUÇÕES DE USO CARTUCHO-BULA CLEARLENS SOLUÇÃO MULTIUSO DESCRIÇÃO: CLEARLENS Solução Multiuso tem ação de limpar, desinfetar, enxaguar, lubrificar e conservar as lentes de contato sem irritar os olhos.
INSTRUÇÕES DE USO CARTUCHO-BULA. CLEARLENS SOLUÇÃO CONSERVADORA Solução Conservadora para Lentes de Contato
 INSTRUÇÕES DE USO CARTUCHO-BULA CLEARLENS SOLUÇÃO CONSERVADORA DESCRIÇÃO: CLEARLENS Solução Conservadora tem ação de desinfetar e conservar as lentes de contato sem irritar os olhos. Elimina microorganismos
INSTRUÇÕES DE USO CARTUCHO-BULA CLEARLENS SOLUÇÃO CONSERVADORA DESCRIÇÃO: CLEARLENS Solução Conservadora tem ação de desinfetar e conservar as lentes de contato sem irritar os olhos. Elimina microorganismos
A Secretária de Vigilância Sanitária do Ministério da Saúde, no uso de suas atribuições, e considerando:
 Detecção de anticorpos anti-hiv - Portaria 488 de 17/6/1998 Ementa: As unidades hemoterápicas, públicas e privadas, que realizam atividades de Hematologia, ficam obrigadas a cumprir as etapas do conjunto
Detecção de anticorpos anti-hiv - Portaria 488 de 17/6/1998 Ementa: As unidades hemoterápicas, públicas e privadas, que realizam atividades de Hematologia, ficam obrigadas a cumprir as etapas do conjunto
Teste Rápido DPP HIV
 Orientações para utilização de Teste Rápido DPP HIV com amostra de fluido oral Ministério da Saúde Secretaria de Vigilância em Saúde 2014 Ministério da Saúde Todos os direitos reservados. É permitida a
Orientações para utilização de Teste Rápido DPP HIV com amostra de fluido oral Ministério da Saúde Secretaria de Vigilância em Saúde 2014 Ministério da Saúde Todos os direitos reservados. É permitida a
IMUNO ENSAIOS USANDO CONJUGADOS
 IMUNO ENSAIOS USANDO CONJUGADOS REAÇÕES USANDO REAGENTES MARCADOS Conjugado: molécula constituída por duas substâncias ligadas covalentemente e que mantêm as propriedades funcionais de ambas Ex: globulina
IMUNO ENSAIOS USANDO CONJUGADOS REAÇÕES USANDO REAGENTES MARCADOS Conjugado: molécula constituída por duas substâncias ligadas covalentemente e que mantêm as propriedades funcionais de ambas Ex: globulina
Hepatites B e C. são doenças silenciosas. VEJA COMO DEIXAR AS HEPATITES LONGE DO SEU SALÃO DE BELEZA.
 Hepatites B e C são doenças silenciosas. VEJA COMO DEIXAR AS HEPATITES LONGE DO SEU SALÃO DE BELEZA. heto hepatite manucure.indd 1 Faça sua parte. Não deixe as hepatites virais frequentarem seu salão.
Hepatites B e C são doenças silenciosas. VEJA COMO DEIXAR AS HEPATITES LONGE DO SEU SALÃO DE BELEZA. heto hepatite manucure.indd 1 Faça sua parte. Não deixe as hepatites virais frequentarem seu salão.
GRUPO HOSPITALAR CONCEIÇÃO HOSPITAL FÊMINA LABORATÓRIO DE ANÁLISES CLÍNICAS SETOR DE BIOQUÍMICA TIPAGEM ABO/Rh EM GEL CENTRIFUGAÇÃO
 1. Sinonímia: POP n.º: B21 Página 1 de 12 GRUPO SANGÜÍNEO e FATOR RH, RH e GRUPO. Mnemônico: AB 2. Aplicabilidade: Bioquímicos do setor de bioquímica do LAC-HF. 3. Aplicação clínica: Determinação do grupo
1. Sinonímia: POP n.º: B21 Página 1 de 12 GRUPO SANGÜÍNEO e FATOR RH, RH e GRUPO. Mnemônico: AB 2. Aplicabilidade: Bioquímicos do setor de bioquímica do LAC-HF. 3. Aplicação clínica: Determinação do grupo
HIV 1&2 BiSpot. Uso exclusivo para diagnóstico "in vitro" Procedimento. Figura 1. Princípio do teste 432/B4 1
 B ligarão especificamente aos peptídios sintéticos nos pontos inferior e/ou intermediário nos dentes do pente (Figura 1). Simultaneamente, as imunoglobulinas presentes nas amostras serão capturadas pelos
B ligarão especificamente aos peptídios sintéticos nos pontos inferior e/ou intermediário nos dentes do pente (Figura 1). Simultaneamente, as imunoglobulinas presentes nas amostras serão capturadas pelos
Biologia Celular e Molecular
 DEPARTAMENTO DE ZOOLOGIA FACULDADE DE CIÊNCIAS E TECNOLOGIA UNIVERSIDADE DE COIMBRA Biologia Celular e Molecular Detecção de proteínas por western-blotting 2007-2008 Na electroforese em gel de poliacrilamida
DEPARTAMENTO DE ZOOLOGIA FACULDADE DE CIÊNCIAS E TECNOLOGIA UNIVERSIDADE DE COIMBRA Biologia Celular e Molecular Detecção de proteínas por western-blotting 2007-2008 Na electroforese em gel de poliacrilamida
GRUPO SANGUÍNEO e FATOR RH, RH e GRUPO. Mnemônico: GSF
 POP n.º: B93 Página 1 de 7 1. Sinonímia: GRUPO SANGUÍNEO e FATOR RH, RH e GRUPO. Mnemônico: GSF 2. Aplicabilidade: Bioquímicos do setor de bioquímica do LAC-HNSC. 3. Aplicação clínica: Determinação do
POP n.º: B93 Página 1 de 7 1. Sinonímia: GRUPO SANGUÍNEO e FATOR RH, RH e GRUPO. Mnemônico: GSF 2. Aplicabilidade: Bioquímicos do setor de bioquímica do LAC-HNSC. 3. Aplicação clínica: Determinação do
INSTRUÇÕES DE USO / CARTUCHO-BULA. CLEARLENS SOLUÇÃO LIMPADORA Solução Limpadora para Lentes de Contato
 INSTRUÇÕES DE USO / CARTUCHO-BULA CLEARLENS SOLUÇÃO LIMPADORA Solução Limpadora para Lentes de Contato DESCRIÇÃO: CLEARLENS Solução Limpadora tem ação de limpar, desinfetar, remover acúmulos de proteínas
INSTRUÇÕES DE USO / CARTUCHO-BULA CLEARLENS SOLUÇÃO LIMPADORA Solução Limpadora para Lentes de Contato DESCRIÇÃO: CLEARLENS Solução Limpadora tem ação de limpar, desinfetar, remover acúmulos de proteínas
OraQuick ADVANCE HIV-1/2 Teste Rápido para a Detecção de Anticorpos HIV-1/2. Plasma. Amostras HIV-1. Amostras HIV-1. Amostras
 Dispositivo Médico para Diagnóstico In vitro Nome Mandatário Fabricante Distribuidor Tipo de Teste Teste rápido. OraQuick ADVANCE /2 Teste Rápido para a Detecção de Anticorpos /2 Aplicação Diagnóstica
Dispositivo Médico para Diagnóstico In vitro Nome Mandatário Fabricante Distribuidor Tipo de Teste Teste rápido. OraQuick ADVANCE /2 Teste Rápido para a Detecção de Anticorpos /2 Aplicação Diagnóstica
Incubação. Incubação. Fase sólida (Poço de uma placa de 96 poços) IgG Anti-HIV Presente na amostra do indivíduo
 Aula 5 Diagnóstico laboratorial da infecção pelo HIV Em 1985, surgiu a primeira geração de ensaios para o diagnóstico da infecção pelo HIV. Esses ensaios empregavam antígenos virais, obtidos a partir da
Aula 5 Diagnóstico laboratorial da infecção pelo HIV Em 1985, surgiu a primeira geração de ensaios para o diagnóstico da infecção pelo HIV. Esses ensaios empregavam antígenos virais, obtidos a partir da
ScanGel ScanBrom 86445 12 ml
 ScanGel ScanBrom 86445 12 ml BROMELINA PARA TESTE DE COMPATIBILIDADE IVD Todos os produtos fabricados e comercializados pela empresa Bio-Rad são submetidos a um sistema de garantia de qualidade, desde
ScanGel ScanBrom 86445 12 ml BROMELINA PARA TESTE DE COMPATIBILIDADE IVD Todos os produtos fabricados e comercializados pela empresa Bio-Rad são submetidos a um sistema de garantia de qualidade, desde
Econômico no uso Supersol LG é composto com alto teor de tensoativos, que permite sua utilização em altas diluições para uma limpeza perfeita.
 JohnsonDiversey Suma Supersol LG Detergente em pó para limpeza geral. Versátil A formulação balanceada permite que o detergente Supersol LG seja utilizado tanto para limpeza geral, quanto para lavagem
JohnsonDiversey Suma Supersol LG Detergente em pó para limpeza geral. Versátil A formulação balanceada permite que o detergente Supersol LG seja utilizado tanto para limpeza geral, quanto para lavagem
MÓDULO PRÁTICO. Curso de Actualização sobre Diagnóstico da Infecção HIV-SIDA 11 Nov 2010
 MÓDULO PRÁTICO 11 Nov 2010 MÓDULO PRÁTICO Quirina dos Santos-Costa Pharm D, PhD Student Assistant Lecturer Unidade dos Retrovírus e Infecções Associadas - Centro de Patogénese Molecular Faculdade de Farmácia,
MÓDULO PRÁTICO 11 Nov 2010 MÓDULO PRÁTICO Quirina dos Santos-Costa Pharm D, PhD Student Assistant Lecturer Unidade dos Retrovírus e Infecções Associadas - Centro de Patogénese Molecular Faculdade de Farmácia,
TR DPP HIV-1/2 Bio-Manguinhos / TR DPP Sífilis
 Pedro Paulo Ferreira Ribeiro Diagnóstico HIV ELISA Teste Rápido Diagnóstico Sífilis ELISA VDRL Testes antigênicos não treponêmicos ou testes lipoídicos: - VDRL (Venereal Disease Research Laboratory) -
Pedro Paulo Ferreira Ribeiro Diagnóstico HIV ELISA Teste Rápido Diagnóstico Sífilis ELISA VDRL Testes antigênicos não treponêmicos ou testes lipoídicos: - VDRL (Venereal Disease Research Laboratory) -
3M TM Petrifilm TM Placa para Contagem de Leveduras e Bolores. Guia de. Interpretação
 3M TM TM Placa para Contagem de Leveduras e Bolores Guia de Interpretação 3M TM TM Placa para Contagem de Leveduras e Bolores Este guia apresenta resultados das placas 3M para Contagem de Leveduras e Bolores.
3M TM TM Placa para Contagem de Leveduras e Bolores Guia de Interpretação 3M TM TM Placa para Contagem de Leveduras e Bolores Este guia apresenta resultados das placas 3M para Contagem de Leveduras e Bolores.
PROGENSA PCA3 Urine Specimen Transport Kit
 PROGENSA PCA3 Urine Specimen Transport Kit Instruções para o médico Para uso em diagnóstico in vitro. Exclusivamente para exportação dos EUA. Instruções 1. Pode ser útil pedir ao paciente que beba uma
PROGENSA PCA3 Urine Specimen Transport Kit Instruções para o médico Para uso em diagnóstico in vitro. Exclusivamente para exportação dos EUA. Instruções 1. Pode ser útil pedir ao paciente que beba uma
FICHA DE DADOS DE SEGURANÇA DO PRODUTO Data: 01.12.98
 FICHA DE DADOS DE SEGURANÇA DO PRODUTO Data: 01.12.98 1. Identificação do Produto / Reagente e da empresa Nome Comercial do Produto: Microalbumin Standard Series Número do Catálogo: MAL/STS-5X1 Fabricante:
FICHA DE DADOS DE SEGURANÇA DO PRODUTO Data: 01.12.98 1. Identificação do Produto / Reagente e da empresa Nome Comercial do Produto: Microalbumin Standard Series Número do Catálogo: MAL/STS-5X1 Fabricante:
MONITORAMENTO DA QUALIDADE: CONTROLE DE QUALIDADE INTERNO E EXTERNO
 MONITORAMENTO DA QUALIDADE: CONTROLE DE QUALIDADE INTERNO E EXTERNO Dra. Patrícia Regina Araújo Laboratório de Sorologia Associação beneficente de Coleta de Sangue-COLSAN Controle da Qualidade Toda ação
MONITORAMENTO DA QUALIDADE: CONTROLE DE QUALIDADE INTERNO E EXTERNO Dra. Patrícia Regina Araújo Laboratório de Sorologia Associação beneficente de Coleta de Sangue-COLSAN Controle da Qualidade Toda ação
HIV em gestantes: garantindo a acurácia diagnóstica. Dra Ester Sabino Fundação Pró-Sangue/ Hemocentro de São Paulo Diagnósticos da América
 HIV em gestantes: garantindo a acurácia diagnóstica Dra Ester Sabino Fundação Pró-Sangue/ Hemocentro de São Paulo Diagnósticos da América Distribuição de freqüência de títulos sorológicos de duas populações
HIV em gestantes: garantindo a acurácia diagnóstica Dra Ester Sabino Fundação Pró-Sangue/ Hemocentro de São Paulo Diagnósticos da América Distribuição de freqüência de títulos sorológicos de duas populações
CONTROLE DE COPIA: PT-LB-IM-021 ANTI HIV 22/10/2015
 PT-LB-IM-1 1/6 1. INTRODUÇÃO / FINALIDADE DO MÉTODO O vírus da imunodeficiência humana é o agente causador da síndrome da imunodeficiência adquirida (AIDS). A AIDS foi pela primeira vez descrita nos Estados
PT-LB-IM-1 1/6 1. INTRODUÇÃO / FINALIDADE DO MÉTODO O vírus da imunodeficiência humana é o agente causador da síndrome da imunodeficiência adquirida (AIDS). A AIDS foi pela primeira vez descrita nos Estados
Construction. Aparelho pneumático para aplicação de SikaBond -T52 FC. Descrição do produto. Dados do produto
 Ficha de Produto Edição de Abril de 2011 Nº de identificação: 99.102 Versão nº 1 SikaBond Dispenser-5400 Aparelho pneumático para aplicação de SikaBond -T52 FC Descrição do produto SikaBond Dispenser-5400
Ficha de Produto Edição de Abril de 2011 Nº de identificação: 99.102 Versão nº 1 SikaBond Dispenser-5400 Aparelho pneumático para aplicação de SikaBond -T52 FC Descrição do produto SikaBond Dispenser-5400
Para utilizar na preparação e isolamento de linfócitos purificados directamente a partir de sangue total FOLHETO INFORMATIVO
 Para utilizar na preparação e isolamento de linfócitos purificados directamente a partir de sangue total FOLHETO INFORMATIVO Para Utilizar no Diagnóstico In Vitro PI-TT.610-PT-V5 Informação sobre o produto
Para utilizar na preparação e isolamento de linfócitos purificados directamente a partir de sangue total FOLHETO INFORMATIVO Para Utilizar no Diagnóstico In Vitro PI-TT.610-PT-V5 Informação sobre o produto
HIV-1/2 3.0 STRIP TEST BIOEASY
 To remove this message please register.instruções de Uso 3.0 STRIP TEST BIOEASY pág. 1 HIV-1/2 3.0 STRIP TEST BIOEASY ód.: 03FK12 MÉTODO: Teste imunocromatográfico FINALIDADE: A síndrome da imunodeficiência
To remove this message please register.instruções de Uso 3.0 STRIP TEST BIOEASY pág. 1 HIV-1/2 3.0 STRIP TEST BIOEASY ód.: 03FK12 MÉTODO: Teste imunocromatográfico FINALIDADE: A síndrome da imunodeficiência
Ficha de Informação de Segurança de Produtos Químicos VEDAPREN FAST - TERRACOTA
 1. Identificação do produto e da empresa Nome do produto: Códigos internos de identificação do produto: 111690, 111691, 121714 e 111689 Nome da empresa: Otto Baumgart Ind. e Com. S/A Endereço: Rua Coronel
1. Identificação do produto e da empresa Nome do produto: Códigos internos de identificação do produto: 111690, 111691, 121714 e 111689 Nome da empresa: Otto Baumgart Ind. e Com. S/A Endereço: Rua Coronel
HIV no período neonatal prevenção e conduta
 HIV no período neonatal prevenção e conduta O HIV, agente causador da AIDS, ataca as células do sistema imune, especialmente as marcadas com receptor de superfície CD4 resultando na redução do número e
HIV no período neonatal prevenção e conduta O HIV, agente causador da AIDS, ataca as células do sistema imune, especialmente as marcadas com receptor de superfície CD4 resultando na redução do número e
Sandra Heidtmann 2010
 Sandra Heidtmann 2010 Definições: Amostra: Pequena parte ou porção de alguma coisa que se dá para ver, provar ou analisar, a fim de que a qualidade do todo possa ser avaliada ou julgada; Coleta: Ato de
Sandra Heidtmann 2010 Definições: Amostra: Pequena parte ou porção de alguma coisa que se dá para ver, provar ou analisar, a fim de que a qualidade do todo possa ser avaliada ou julgada; Coleta: Ato de
MODELO DE FORMATO DE BULA
 APRESENTAÇÕES Frasco conta-gotas (75 mg/ml) com 15 ml. USO ORAL USO ADULTO E PEDIÁTRICO COMPOSIÇÃO Cada 25 gotas de LUFTAL (equivalente a 1 ml) contém 75 mg de simeticona. Ingredientes inativos: propilenoglicol,
APRESENTAÇÕES Frasco conta-gotas (75 mg/ml) com 15 ml. USO ORAL USO ADULTO E PEDIÁTRICO COMPOSIÇÃO Cada 25 gotas de LUFTAL (equivalente a 1 ml) contém 75 mg de simeticona. Ingredientes inativos: propilenoglicol,
RéguaFox. alumínio e policarbonato. manual de instruções
 RéguaFox alumínio e policarbonato manual de instruções ÍNDICE 1-Introdução...1 2-Especificações técnicas...1 3-Conteúdo da embalagem...2 4-Instruções de uso...2 5-Precauções de segurança...2 6-Manutenção
RéguaFox alumínio e policarbonato manual de instruções ÍNDICE 1-Introdução...1 2-Especificações técnicas...1 3-Conteúdo da embalagem...2 4-Instruções de uso...2 5-Precauções de segurança...2 6-Manutenção
Mantém cores originais A aplicação de TASKI Tapi 101 não altera as cores originais das superfícies.
 TASKI Tapi 101 Detergente para limpeza de tapetes e carpetes. Alto nível de espuma. F71a Detergente neutro TASKI Tapi 101 é um detergente neutro específico para a limpeza de tapetes, carpetes e revestimentos
TASKI Tapi 101 Detergente para limpeza de tapetes e carpetes. Alto nível de espuma. F71a Detergente neutro TASKI Tapi 101 é um detergente neutro específico para a limpeza de tapetes, carpetes e revestimentos
Regulamenta o uso de testes rápidos para diagnóstico da infecção pelo HIV em situações especiais.
 ATUALIZAÇÃO E NORMATIZAÇÃO DO DIAGNÓSTICO LABORATORIAL DO HIV PORT 151/OUT 2009 Lúcia Sena Farmacêutica-Bioquímica do Programa de DST/AIDS do município de Duque de Caxias HISTÓRICO Diagnóstico Laboratorial
ATUALIZAÇÃO E NORMATIZAÇÃO DO DIAGNÓSTICO LABORATORIAL DO HIV PORT 151/OUT 2009 Lúcia Sena Farmacêutica-Bioquímica do Programa de DST/AIDS do município de Duque de Caxias HISTÓRICO Diagnóstico Laboratorial
Pesquisa de Fosfatase Alcalina em Leite Fluido por Colorimetria
 1 Escopo MAPA/SDA/CGAL Página 1 de 5 Este método tem como objetivo descrever os procedimentos para o ensaio Pesquisa de Fosfatase Alcalina em Leite Fluido por Colorimetria. 2 Fundamentos O principal objetivo
1 Escopo MAPA/SDA/CGAL Página 1 de 5 Este método tem como objetivo descrever os procedimentos para o ensaio Pesquisa de Fosfatase Alcalina em Leite Fluido por Colorimetria. 2 Fundamentos O principal objetivo
Diogo Penha Soares [email protected]
 TESTE DE AMPLIFICAÇÃO DO ÁCIDO NUCLÉICO (NAT) PARA DETECÇÃO DOS VÍRUS HIV-1 NO SANGUE DOADO: uma análise de custo-efetividade sob a perspectiva do Sistema Único de Saúde do Brasil Diogo Penha Soares [email protected]
TESTE DE AMPLIFICAÇÃO DO ÁCIDO NUCLÉICO (NAT) PARA DETECÇÃO DOS VÍRUS HIV-1 NO SANGUE DOADO: uma análise de custo-efetividade sob a perspectiva do Sistema Único de Saúde do Brasil Diogo Penha Soares [email protected]
PASSO 1: ANTES DE MANUSEAR A AMOSTRA, PREPARAR TODOS OS EQUIPAMENTOS DE TRANSPORTE
 Transporte no País: Como enviar com segurança amostras de sangue humano de casos suspeitos de Ebola dentro do país por meio de transporte rodoviário, ferroviário e marítimo PASSO 1: ANTES DE MANUSEAR A
Transporte no País: Como enviar com segurança amostras de sangue humano de casos suspeitos de Ebola dentro do país por meio de transporte rodoviário, ferroviário e marítimo PASSO 1: ANTES DE MANUSEAR A
DENGUE IgG/IgM. Imuno-Rápido. WAMA Diagnóstica. CÓD. 626025-R: 25 determinações. 40 determinações
 MS 10310030096 Imuno-Rápido DENGUE IgG/IgM CÓD. 626010-R: 10 determinações CÓD. 626020-R: 20 determinações CÓD. 626025-R: 25 determinações CÓD. 626040-R: 40 determinações WAMA Diagnóstica Rua Aldo Germano
MS 10310030096 Imuno-Rápido DENGUE IgG/IgM CÓD. 626010-R: 10 determinações CÓD. 626020-R: 20 determinações CÓD. 626025-R: 25 determinações CÓD. 626040-R: 40 determinações WAMA Diagnóstica Rua Aldo Germano
1. INTRODUÇÃO / FINALIDADE DO MÉTODO
 1/6 1. INTRODUÇÃO / FINALIDADE DO MÉTODO A sífilis é uma doença venérea causada pelo Treponema pallidum, que possui a capacidade de invadir as mucosas inatas ou a pele em áreas de abrasão. O contato sexual
1/6 1. INTRODUÇÃO / FINALIDADE DO MÉTODO A sífilis é uma doença venérea causada pelo Treponema pallidum, que possui a capacidade de invadir as mucosas inatas ou a pele em áreas de abrasão. O contato sexual
Instruções de Uso. ImmunoComb CANINE EHRLICHIA. N Cat. do Produto: 50CEH201/50CEH210 USO VETERINÁRIO - PRODUTO IMPORTADO
 Instruções de Uso ImmunoComb CANINE EHRLICHIA Kit para a detecção de anticorpos IgG de Ehrlichia canis N Cat. do Produto: 50CEH201/50CEH210 USO VETERINÁRIO - PRODUTO IMPORTADO Instruction Cat. No: 63CEH511
Instruções de Uso ImmunoComb CANINE EHRLICHIA Kit para a detecção de anticorpos IgG de Ehrlichia canis N Cat. do Produto: 50CEH201/50CEH210 USO VETERINÁRIO - PRODUTO IMPORTADO Instruction Cat. No: 63CEH511
HEPATITES. Prof. Fernando Ananias HEPATITE = DISTÚRBIO INFLAMATÓRIO DO FÍGADO
 HEPATITES Prof. Fernando Ananias HEPATITE = DISTÚRBIO INFLAMATÓRIO DO FÍGADO Hepatites virais: agentes etiológicos A B C D E Vírus hepatotrópicos G TT Herpes vírus EBV CMV Enterovírus Adenovírus Febre
HEPATITES Prof. Fernando Ananias HEPATITE = DISTÚRBIO INFLAMATÓRIO DO FÍGADO Hepatites virais: agentes etiológicos A B C D E Vírus hepatotrópicos G TT Herpes vírus EBV CMV Enterovírus Adenovírus Febre
Questionário - Proficiência Clínica
 Tema Elaboradora TESTE DE ANTIGLOBULINA E SUA APLICAÇÃO EM LABORATÓRIOS Margarida de Oliveira Pinho, Bióloga, Responsável pelo Setor de Imunohematologia e Coordenação da equipe técnica do Serviço de Hemoterapia
Tema Elaboradora TESTE DE ANTIGLOBULINA E SUA APLICAÇÃO EM LABORATÓRIOS Margarida de Oliveira Pinho, Bióloga, Responsável pelo Setor de Imunohematologia e Coordenação da equipe técnica do Serviço de Hemoterapia
O manipulador de alimentos tem que conferir todas as informações do rótulo?
 Os consumidores têm o direito de conhecer as características e a composição nutricional dos alimentos que adquirem. A legislação nacional estabelece algumas normas para registro dessas informações na rotulagem
Os consumidores têm o direito de conhecer as características e a composição nutricional dos alimentos que adquirem. A legislação nacional estabelece algumas normas para registro dessas informações na rotulagem
Dupla ação Além de limpador é um excelente renovador de brilho, em especial de ceras lustráveis.
 Optimum Floral Detergente Limpa Pisos Eficiente e prático Possui em sua formulação detergentes e ceras que possibilitam realizar em uma só operação a limpeza e conservação de pisos / acabamentos. Versatilidade
Optimum Floral Detergente Limpa Pisos Eficiente e prático Possui em sua formulação detergentes e ceras que possibilitam realizar em uma só operação a limpeza e conservação de pisos / acabamentos. Versatilidade
BROCAS CIRÚRGICAS INTRA LOCK SYSTEM
 S CIRÚRGICAS INTRA LOCK SYSTEM (Brocas Cirúrgicas Odontológicas) INFORMAÇÕES DE IDENTIFICAÇÃO DO PRODUTO As Brocas Cirúrgicas fazem parte do sistema INTRA-LOCK SYSTEM. Deste grupo de instrumentais fazem
S CIRÚRGICAS INTRA LOCK SYSTEM (Brocas Cirúrgicas Odontológicas) INFORMAÇÕES DE IDENTIFICAÇÃO DO PRODUTO As Brocas Cirúrgicas fazem parte do sistema INTRA-LOCK SYSTEM. Deste grupo de instrumentais fazem
Termômetro Digital de Testa e Ouvido
 Termômetro Digital de Testa e Ouvido Ouvido Testa Ambientes Modelo T1000 MANUAL DE INSTRUÇÕES PRECAUÇÕES, ADVERTÊNCIAS E CUIDADOS ESPECIAIS Não exponha o dispositivo a temperaturas extremas, umidade,
Termômetro Digital de Testa e Ouvido Ouvido Testa Ambientes Modelo T1000 MANUAL DE INSTRUÇÕES PRECAUÇÕES, ADVERTÊNCIAS E CUIDADOS ESPECIAIS Não exponha o dispositivo a temperaturas extremas, umidade,
Manual de Instruções
 Manual de Instruções Kit de Instrumental para Cirurgia do Túnel do Carpo VOLMED Nome Técnico: KIT CIRÚRGICO Fabricante: VOLMED BRASIL EQUIPAMENTOS LTDA -ME AV. SÃO GABRIEL, 291 JD. PAULISTA CEP: 13574-540
Manual de Instruções Kit de Instrumental para Cirurgia do Túnel do Carpo VOLMED Nome Técnico: KIT CIRÚRGICO Fabricante: VOLMED BRASIL EQUIPAMENTOS LTDA -ME AV. SÃO GABRIEL, 291 JD. PAULISTA CEP: 13574-540
ScanGel ABO Complete/RH/K Duo 86719 2 x 24 cards 86709 2 x 144 cards Cards ScanGel ABO Complete/RH1 Duo e ScanGel Monoclonal RH/K Phenotypes Duo
 ScanGel ABO Complete/RH/K Duo 86719 2 x 24 cards 86709 2 x 144 cards Cards ScanGel ABO Complete/RH1 Duo e ScanGel Monoclonal RH/K Phenotypes Duo GEL FORMULADO COM REAGENTES MONOCLONAIS DE ORIGEM MURINA
ScanGel ABO Complete/RH/K Duo 86719 2 x 24 cards 86709 2 x 144 cards Cards ScanGel ABO Complete/RH1 Duo e ScanGel Monoclonal RH/K Phenotypes Duo GEL FORMULADO COM REAGENTES MONOCLONAIS DE ORIGEM MURINA
ANEXO I REGRAS PARA COLETA, ACONDICIONAMENTO, PRESERVAÇÃO E ENCAMINHAMENTO DE MATERIAIS BIOLÓGICOS PARA ANÁLISE BIOLÓGICA.
 Estado de Santa Catarina Secretaria de Estado da Segurança Pública e Defesa do Cidadão Instituto Geral de Perícias Instituto de Análises Laboratoriais Laboratório de Genética Forense ANEXO I REGRAS PARA
Estado de Santa Catarina Secretaria de Estado da Segurança Pública e Defesa do Cidadão Instituto Geral de Perícias Instituto de Análises Laboratoriais Laboratório de Genética Forense ANEXO I REGRAS PARA
Instruções de Uso do Aplicador
 CM09FEV11 AXERON (testosterona) solução tópica Instruções de Uso do Aplicador Antes de usar seu novo aplicador de AXERON leia as Instruções de Uso. Siga cuidadosamente as instruções ao utilizar o aplicador
CM09FEV11 AXERON (testosterona) solução tópica Instruções de Uso do Aplicador Antes de usar seu novo aplicador de AXERON leia as Instruções de Uso. Siga cuidadosamente as instruções ao utilizar o aplicador
ORIENTAÇÃO SOBRE INFORMAÇÕES OBRIGATÓRIAS EM VESTIMENTAS DE PROTEÇÃO INDIVIDUAL PARA RISCO QUÍMICO COM AGROTÓXICOS
 ORIENTAÇÃO SOBRE INFORMAÇÕES OBRIGATÓRIAS EM VESTIMENTAS DE PROTEÇÃO INDIVIDUAL PARA RISCO QUÍMICO COM AGROTÓXICOS MÉTODO UTILIZADO As orientações constantes deste documento são uma compilação das exigências
ORIENTAÇÃO SOBRE INFORMAÇÕES OBRIGATÓRIAS EM VESTIMENTAS DE PROTEÇÃO INDIVIDUAL PARA RISCO QUÍMICO COM AGROTÓXICOS MÉTODO UTILIZADO As orientações constantes deste documento são uma compilação das exigências
O consumidor deve estar atento às informações do rótulo?
 Os consumidores têm o direito de conhecer as características e a composição nutricional dos alimentos que adquirem. A legislação nacional estabelece algumas normas para registro dessas informações na rotulagem
Os consumidores têm o direito de conhecer as características e a composição nutricional dos alimentos que adquirem. A legislação nacional estabelece algumas normas para registro dessas informações na rotulagem
TETMOSOL Sabonete sulfiram. Sabonete com 4 g de sulfiram em embalagem contendo 1 sabonete de 80 g.
 TETMOSOL Sabonete sulfiram I) IDENTIFICAÇÃO DO MEDICAMENTO TETMOSOL Sabonete sulfiram APRESENTAÇÕES Sabonete com 4 g de sulfiram em embalagem contendo 1 sabonete de 80 g. USO TÓPICO USO ADULTO E PEDIÁTRICO
TETMOSOL Sabonete sulfiram I) IDENTIFICAÇÃO DO MEDICAMENTO TETMOSOL Sabonete sulfiram APRESENTAÇÕES Sabonete com 4 g de sulfiram em embalagem contendo 1 sabonete de 80 g. USO TÓPICO USO ADULTO E PEDIÁTRICO
FICHA DE INFORMAÇÕES DE SEGURANÇA DE PRODUTOS QUÍMICOS
 Página: 1/5 1- Identificação do produto e da empresa - Nome do produto: FOSFATO DE CÁLCIO MONOBÁSICO H 2O - Código interno de identificação do produto: F1027 - Nome da empresa: Labsynth Produtos para Laboratórios
Página: 1/5 1- Identificação do produto e da empresa - Nome do produto: FOSFATO DE CÁLCIO MONOBÁSICO H 2O - Código interno de identificação do produto: F1027 - Nome da empresa: Labsynth Produtos para Laboratórios
GOVERNO DO ESTADO DE MINAS GERAIS SECRETARIA DE ESTADO DE SAÚDE SUPERINTENDÊNCIA DE ASSISTÊNCIA FARMACÊUTICA DIRETORIA DE MEDICAMENTOS ESTRATÉGICOS
 INFORME ESTENDIDO GLICOSÍMETROS Senhor Farmacêutico Municipal, Considerando a distribuição dos novos glicosímetros da marca CEPA GC modelo TD 4230, bem como a necessidade da correta instrução aos pacientes/responsáveis
INFORME ESTENDIDO GLICOSÍMETROS Senhor Farmacêutico Municipal, Considerando a distribuição dos novos glicosímetros da marca CEPA GC modelo TD 4230, bem como a necessidade da correta instrução aos pacientes/responsáveis
HIV 1 & 2 TriSpot Ag - Ab
 . HIV 1 & 2 TriSpot Ag - Ab B Para iniciar o teste, as amostras de soro ou plasma são adicionadas ao diluente nas cavidades da fileira A da placa reveladora. O Pente é então inserido nas cavidades da fileira
. HIV 1 & 2 TriSpot Ag - Ab B Para iniciar o teste, as amostras de soro ou plasma são adicionadas ao diluente nas cavidades da fileira A da placa reveladora. O Pente é então inserido nas cavidades da fileira
IDENTIFICAÇÃO E CONFIRMAÇÃO DE GRUPOS FUNCIONAIS: Parte 1: ALDEÍDOS E CETONAS
 PRÁTICA N o. 02 IDENTIFICAÇÃO E CONFIRMAÇÃO DE GRUPOS FUNCIONAIS: Parte 1: ALDEÍDOS E CETONAS OBJETIVOS: Esta prática tem como objetivo a identificação e confirmação de grupos funcionais de aldeídos e
PRÁTICA N o. 02 IDENTIFICAÇÃO E CONFIRMAÇÃO DE GRUPOS FUNCIONAIS: Parte 1: ALDEÍDOS E CETONAS OBJETIVOS: Esta prática tem como objetivo a identificação e confirmação de grupos funcionais de aldeídos e
HIV-1 BLOT 1.3 TESTE WESTERN BLOT
 0123 HIV-1 BLOT 1.3 TESTE WESTERN BLOT DATA DE REVISÃO: 05/05 MAJ 0011-BRA-0 (kit com 18 testes) : 11010-018 (kit com 36 testes) : 11010-036 (kit com 108 testes) : 11010-108 NOME E APLICAÇÃO O MP Diagnostics
0123 HIV-1 BLOT 1.3 TESTE WESTERN BLOT DATA DE REVISÃO: 05/05 MAJ 0011-BRA-0 (kit com 18 testes) : 11010-018 (kit com 36 testes) : 11010-036 (kit com 108 testes) : 11010-108 NOME E APLICAÇÃO O MP Diagnostics
TOTVS Gestão Hospitalar Manual Ilustrado Central de Material Esterilizado. 11.8x. março de 2015 Versão: 3.0
 TOTVS Gestão Hospitalar Manual Ilustrado Central de Material Esterilizado 11.8x março de 2015 Versão: 3.0 1 Sumário 1 Objetivos... 4 2 Introdução... 4 3 Cadastros... 5 3.1 Cadastros de Unidades de CME...
TOTVS Gestão Hospitalar Manual Ilustrado Central de Material Esterilizado 11.8x março de 2015 Versão: 3.0 1 Sumário 1 Objetivos... 4 2 Introdução... 4 3 Cadastros... 5 3.1 Cadastros de Unidades de CME...
FISPQ (Ficha de Informações de Segurança de Produtos Químicos) SAPÓLIO RADIUM PÓ (Limão, Pinho, Clássico, Lavanda, Bouquet e Laranja)
 Página 1 de 6 1 - IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA Nome: Sapólio Radium Pó Códigos Internos: Limão: 14001 / 14017 Pinho: 14005 / 14018 Clássico: 14033 Lavanda: 14031 Bouquet: 14030 Laranja: 14032
Página 1 de 6 1 - IDENTIFICAÇÃO DO PRODUTO E DA EMPRESA Nome: Sapólio Radium Pó Códigos Internos: Limão: 14001 / 14017 Pinho: 14005 / 14018 Clássico: 14033 Lavanda: 14031 Bouquet: 14030 Laranja: 14032
Ficha de Informações de Segurança de Produto Químico Conforme NBR14725, de julho/2001 e 91/155 EC
 Pág.:1/4 1 Identificação do produto e da empresa Produto: Fabricante: JohnsonDiversey Brasil Ltda. Rua Nossa Senhora do Socorro, 125 Socorro São Paulo SP CEP 04764-020 Tel.: 0XX11 5681-1300 / Fax: 0XX11
Pág.:1/4 1 Identificação do produto e da empresa Produto: Fabricante: JohnsonDiversey Brasil Ltda. Rua Nossa Senhora do Socorro, 125 Socorro São Paulo SP CEP 04764-020 Tel.: 0XX11 5681-1300 / Fax: 0XX11
 Exame de Laboratórios de Bioquímica e Biofísica Licenciatura em Bioquímica 1ª Época 27 de Junho de 2006 Por favor responda às questões da 1ª parte e 2ª partes em folhas separadas 1ª Parte 1. Suponha que
Exame de Laboratórios de Bioquímica e Biofísica Licenciatura em Bioquímica 1ª Época 27 de Junho de 2006 Por favor responda às questões da 1ª parte e 2ª partes em folhas separadas 1ª Parte 1. Suponha que
FICHA TÉCNICA - MASSA LEVE -
 FICHA TÉCNICA - MASSA LEVE - Massa Leve é um aditivo capaz de produzir concreto poroso de baixa massa especifica aparente, com ótima estabilidade, isto é, com reduzida queda de volume na aplicação. Características
FICHA TÉCNICA - MASSA LEVE - Massa Leve é um aditivo capaz de produzir concreto poroso de baixa massa especifica aparente, com ótima estabilidade, isto é, com reduzida queda de volume na aplicação. Características
GRUPO HOSPITALAR CONCEIÇÃO HOSPITAL NOSSA SENHORA DA CONCEIÇÃO LABORATÓRIO DE ANÁLISES CLÍNICAS
 POP n.º: I 22 Página 1 de 5 1. Sinonímia Beta 2 Microglobulina, b2m 2. Aplicabilidade Aos técnicos e bioquímicos do setor de imunologia 3. Aplicação clínica A beta-2-microglobulina é uma proteína presente
POP n.º: I 22 Página 1 de 5 1. Sinonímia Beta 2 Microglobulina, b2m 2. Aplicabilidade Aos técnicos e bioquímicos do setor de imunologia 3. Aplicação clínica A beta-2-microglobulina é uma proteína presente
Ata Parcial. Item 0001
 Ata Parcial Às 09:00 horas do dia 12 de abril de 2012, reuniu-se o Pregoeiro Oficial da Prefeitura Municipal de Santana do Livramento e respectivos membros da Equipe de apoio, designados pela portaria
Ata Parcial Às 09:00 horas do dia 12 de abril de 2012, reuniu-se o Pregoeiro Oficial da Prefeitura Municipal de Santana do Livramento e respectivos membros da Equipe de apoio, designados pela portaria
ALLERGAN PRODUTOS FARMACÊUTICOS LTDA
 REFRESH ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril sem conservante álcool polivinílico 1,4% povidona 0,6% BULA PARA O PACIENTE APRESENTAÇÃO Solução Oftálmica Estéril Lubrificante, sem
REFRESH ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril sem conservante álcool polivinílico 1,4% povidona 0,6% BULA PARA O PACIENTE APRESENTAÇÃO Solução Oftálmica Estéril Lubrificante, sem
COLETA DE AMOSTRA 01 de 06
 01 de 06 1. PRINCÍPIO Para que os resultados dos métodos de análise expressem valores representativos da quantidade total de substância disponível, é imprescindível recorrer a técnica de coleta definida
01 de 06 1. PRINCÍPIO Para que os resultados dos métodos de análise expressem valores representativos da quantidade total de substância disponível, é imprescindível recorrer a técnica de coleta definida
TÉCNICA EM LABORATÓRIO/HEMOTERAPIA
 UFF UNIVERSIDADE FEDERAL FLUMINENSE CCM CENTRO DE CIÊNCIAS MÉDICAS HUAP HOSPITAL UNIVERSITÁRIO ANTONIO PEDRO TÉCNICA EM LABORATÓRIO/HEMOTERAPIA Parte I: Múltipla Escolha 01 Quanto à classificação do grupo
UFF UNIVERSIDADE FEDERAL FLUMINENSE CCM CENTRO DE CIÊNCIAS MÉDICAS HUAP HOSPITAL UNIVERSITÁRIO ANTONIO PEDRO TÉCNICA EM LABORATÓRIO/HEMOTERAPIA Parte I: Múltipla Escolha 01 Quanto à classificação do grupo
MANUAL DE COLETA DE AMOSTRAS
 MANUAL DE COLETA DE AMOSTRAS Rua: Victor Sopelsa, nº 3000 Bairro Salete E-mail: [email protected] Fone: (49) 3441-1086 Fax: (49) 3441-1084 Cep: 89.700-000 Concórdia Santa Catarina Responsável /Gerente
MANUAL DE COLETA DE AMOSTRAS Rua: Victor Sopelsa, nº 3000 Bairro Salete E-mail: [email protected] Fone: (49) 3441-1086 Fax: (49) 3441-1084 Cep: 89.700-000 Concórdia Santa Catarina Responsável /Gerente
[HIV-1/2 NEW] REF [34020]
![[HIV-1/2 NEW] REF [34020] [HIV-1/2 NEW] REF [34020]](/thumbs/27/10157951.jpg) [HIV-1/2 NEW] REF [34020] Finalidade do teste O teste Access HIV-1/2 New utiliza uma técnica imunoenzimática quimioluminescente de partículas paramagnéticas para detecção de anticorpos dirigidos anti-hiv-1
[HIV-1/2 NEW] REF [34020] Finalidade do teste O teste Access HIV-1/2 New utiliza uma técnica imunoenzimática quimioluminescente de partículas paramagnéticas para detecção de anticorpos dirigidos anti-hiv-1
Manutenção. Manutenção
 Manutenção Esta seção inclui: "Adicionando tinta" na página 7-32 "Esvaziando a bandeja de cera" na página 7-36 "Substituindo o kit de manutenção" na página 7-39 "Limpando a lâmina de liberação de papel"
Manutenção Esta seção inclui: "Adicionando tinta" na página 7-32 "Esvaziando a bandeja de cera" na página 7-36 "Substituindo o kit de manutenção" na página 7-39 "Limpando a lâmina de liberação de papel"
Imunocromatografia e Dot-ELISA. Andréa Calado
 Imunocromatografia e Dot-ELISA Andréa Calado IMUNOCROMATOGRAFIA A imunocromatografia é uma técnica que começou a ser desenvolvida nos anos 60, sendo primeiro criada para o estudo das proteínas séricas;
Imunocromatografia e Dot-ELISA Andréa Calado IMUNOCROMATOGRAFIA A imunocromatografia é uma técnica que começou a ser desenvolvida nos anos 60, sendo primeiro criada para o estudo das proteínas séricas;
109 FOOD IGG MEDITERRANEAN
 Pagina 1 of 14 1. Identificação do Produto / Reagente e da empresa Nome Comercial do Produto: - MICROPLACA Fabricante: Genesis Diagnostics Ltd. Henry Crabb Road, Littleport, Cambridgeshire, CB6 1SE UK.
Pagina 1 of 14 1. Identificação do Produto / Reagente e da empresa Nome Comercial do Produto: - MICROPLACA Fabricante: Genesis Diagnostics Ltd. Henry Crabb Road, Littleport, Cambridgeshire, CB6 1SE UK.
ACIDENTES DE TRABALHO COM MATERIAL BIOLÓGICO E/OU PERFUROCORTANTES ENTRE OS PROFISSIONAIS DE SAÚDE
 ACIDENTES DE TRABALHO COM MATERIAL BIOLÓGICO E/OU PERFUROCORTANTES ENTRE OS PROFISSIONAIS DE SAÚDE Os acidentes de trabalho com material biológico e/ou perfurocortante apresentam alta incidência entre
ACIDENTES DE TRABALHO COM MATERIAL BIOLÓGICO E/OU PERFUROCORTANTES ENTRE OS PROFISSIONAIS DE SAÚDE Os acidentes de trabalho com material biológico e/ou perfurocortante apresentam alta incidência entre
