Explorando a Nave Terra
|
|
|
- Vítor Sanches Beppler
- 9 Há anos
- Visualizações:
Transcrição
1 Explorando a Nave Terra Kit 1: Elementos, Minerais e Cristais Caderno de Respostas Kit Mirim de Geociências Christopher e Brenda Brooks
2
3 Explorando a Nave Terra Kit 1: Elementos, Minerais e Cristais Caderno de Respostas Kit Mirim de Geociências por Christopher Brooks Université de Montréal e Brenda Brooks Ontario College of Teachers Kit prático de Geociências para estudantes do ensino fundamental no Brasil com idade entre 9 a 12 anos; atende as expectativas internacionais para no ensino de geociências no ensino fundamental.
4 Dedicatória: a Phyllis Brooks, o eterno professor ( ). Copyright 2012 AESI Todos os direitos reservados Nenhuma parte desta publicação pode ser reproduzida ou utilizada em nenhuma forma ou por quaisquer meios sem prévia autorização escrita dos proprietários dos direitos da obra. Composição e ilustrações por Martin Brooks Solutions Montreal, QC, CANADÁ mb-pc.com Tradução por: Giuliano e Juliana Reis Editado por: Ligia Gurgel Publicado originalmente no Canadá Impresso no Brasil ISBN
5 Conteúdo 3 Oficina 1 Sólidos simples na Nave Terra 11 Oficina 2 Você é feito da mesma matéria das estrelas! 19 Oficina 3 Lápis, uma mistura misteriosa 27 Oficina 4 Dois minerais metálicos magníficos 37 Oficina 5 É quartzo, claro! 47 Oficina 6 Por favor, mineral, me dê um tempo! 55 Oficina 7 Material duro na queda
6
7 3 Nome do aluno: Oficina 1: Sólidos simples na Nave Terra Revisão da oficina Glossário dos termos da Oficina 1 brilho: quão bem a luz reflete em uma superfície. Um objeto sólido pode ser brilhante (reflete bem) ou sem brilho (reflete pouco). O brilho do quartzo é chamado de vítreo. cor: a forma como um sólido reflete a luz em sua superfície. concoidal: quando a fratura lisa do vidro possui linhas curvilíneas que lembram uma concha. densidade: o peso de um sólido quando comparado com outro de mesmas dimensões. dureza: a resistência de um sólido ao ser arranhado por outro. fratura: como um sólido se quebra. Pode ser de forma lisa ou áspera. opacidade: o quanto a luz passa através de um sólido. Um objeto sólido pode ser transparente, translúcido ou opaco. opaco: quando a luz não passa através de um sólido ele produz uma sombra quando iluminado. transparente: quando a luz passa facilmente através de um sólido. translúcido: quando a luz passa parcialmente através de um sólido e a imagem parece embaçada.
8 4 Atividade 1 Qual a diferença entre o vidro e a cera? Linha Nome e descrição da propriedade 1 Cor: verde (vidro); branco (cera) 2 Opacidade: transparente (vidro); translúcido (cera) 3 Brilho: brilhante (vidro); fosco (cera) 4 Dureza: duro (vidro); mole (cera) 5 Fratura (ou a forma como elas quebram): áspera (cera); lisa ou liso-concoidal (vidro) 6 Densidade: mais denso (pesado, vidro); menos denso (leve, cera) Quando for corrigir a atividade do laboratório, compare as suas respostas com as que estão na tabela de propriedades. Se você acertou mais de 3, parabéns pelo desempenho. Se acertou uma ou duas, não desamine.
9 5 Atividades 2 a 6 Tabela de propriedades físicas Propriedade (alternativas) Vidro Cera Cerâmica Cor (branco ou verde) Opacidade (transparente, translúcido ou opaco) Brilho (brilhante ou sem brilho) Dureza: pode ser arranhado por um prego (sim ou não) Fratura (lisa, liso-concoidal ou áspera) verde branco branco transparente translúcido opaco brilhante sem brilho sem brilho não sim não liso-concoidal áspera lisa Densidade (pesado ou leve) mais pesado que a cera mais leve que o vidro e a cerâmica mais pesada que a cera Atividade 4: Como eles se quebram? Vidro Cera 1 cm 1 cm
10 6 Questões de múltipla escolha e respostas Utilize um lápis para marcar um X na resposta que você julga ser a correta. Questão #1 De que maneira o vidro e a cera refletem luz? a. ( X ) O vidro é brilhante, mas a cera não tem brilho. b. ( X ) O vidro é sem brilho, a cera é brilhante. Algumas pessoas dizem que o vidro tem um brilho vítreo e a cera não tem brilho (Surpresa, surpresa, hein?) Questão #2 Qual a cor e a opacidade do vidro e da cera? a. ( X ) O vidro é verde e transparente, enquanto a cera é branca e translúcida. b. ( X ) O vidro é verde e transparente, enquanto a cera é branca e opaca. Mesmo o vidro sendo verde-escuro, você ainda pode ver através dele, o que quer dizer que ele é transparente. A cera, entretanto, permite que alguma luz a atravesse, mas você não pode ver completamente através dela. Assim, ela é chamada de translúcida. Questão #3 Qual é a dureza do vidro e da cera? a. ( X ) O vidro é menos duro que o prego, a cera é mais dura. b. ( X ) O vidro é mais duro que o prego, a cera é menos dura. Agora tente arranhá-los com a sua unha e escreva o que você observou na página 10 do seu Caderno de Atividades. Questão #4 De que maneira o vidro e a cera se quebram? a. ( X ) Os dois se quebram da mesma maneira e de forma suave (produzindo fratura lisa). b. ( X ) O vidro apresenta fratura lisa, e a cera, uma fratura mais áspera. Questão #5 Qual a melhor maneira de descrever a aparência da superfície do vidro? a. ( X ) De ostra. b. ( X ) De concha. Algumas das superfícies do vidro são totalmente lisas; outras são lisas, mas com linhas curvilíneas que lembram uma concha. Se a amostra na caixa de amostras não permitir ver com muita clareza, dê uma boa olhada na imagem que se encontra na página 7 do seu Manual da Oficina.
11 7 Questão #6 Qual é mais denso: o vidro ou a cera? a. ( X ) O vidro. b. ( X ) A cera. É mais fácil observar isso quando ambas as amostras são do mesmo tamanho. Questão #7 De que maneira o vidro e a cerâmica refletem luz? a. ( X ) O vidro é mais brilhante, a cerâmica é menos brilhante. b. ( X ) O vidro é menos brilhante, a cerâmica é mais brilhante. Questão #8 De que maneira o vidro e a cerâmica diferem em cor e opacidade? a. ( X ) O vidro é verde-escuro e transparente, enquanto a cerâmica é branca e translúcida. b. ( X ) O vidro é verde-escuro e transparente, enquanto a cerâmica é branca e opaca. A cerâmica é o único sólido opaco entre as três substâncias estudadas. Questão #9 Qual é a dureza do vidro e da cera? a. ( X ) O vidro é mais duro que o prego; a cerâmica é menos dura. b. ( X ) O vidro e a cerâmica são ambos mais duros que o prego. Questão #10 Como o vidro e a cerâmica se quebram (dica: observe apenas a porção rachada da cerâmica)? a. ( X ) O vidro é mais liso, enquanto a cerâmica é mais áspera. b. ( X ) Ambos possuem superfície lisa. Questão #11 Qual é mais denso: o vidro ou a cerâmica? a. ( X ) O vidro é mais denso que a cerâmica. b. ( X ) Ambos possuem a mesma densidade. É difícil descobrir se os exemplos não possuírem as mesmas dimensões; o maior pode ser mais pesado, mas menos denso.
12 8 Atividade 7 Mapa conceitual Conheça o diagrama da árvore conceitual. Ela vai ajudar você a construir o seu primeiro mapa conceitual. O que é um conceito? É uma ideia que permite organizar o que você aprendeu. Na Oficina 1, você aprendeu sobre as propriedades físicas dos sólidos. Isso será o nosso conceito. No rodapé da folha, há uma lista das palavras mais importantes que pertencem a esse conceito. Escreva cada uma das palavras nos balões vazios. É tudo que você tem para iniciar o seu primeiro mapa conceitual. Agora retorne à Atividade 8. brilho fratura opacidade densidade dureza As propriedades são: cor Propriedades físicas dos sólidos Palavras conceituais: cor opacidade dureza fratura brilho densidade
13 9 Desafio: Palavras cruzadas Instruções: O tema dessas palavras cruzadas é As propriedades dos sólidos. Desvende cada pista e escreva sua resposta nos espaços correspondentes. Se precisar de ajuda, olhe no Glossário do seu Caderno de Atividades. V T F I R R 8D T R A N S P A R E N T E R N T N E S U S O L R I 1D U R E Z A D C A I 9B D D R E 2C O N C O I D A L L H 3O P A C O As propriedades dos sólidos Horizontal 1. Mede quão resistente é um sólido 2. Quando um vidro se quebra de maneira curvilínea 3. O que o sólido é quando projeta uma sombra 4. O nome que recebem os sólidos que permitem a passagem da luz Vertical 5. Como um sólido se quebra 6. O brilho do vidro 7. Quando um sólido parece 8. Indica o peso do sólido 9. Nome da maneira como os sólidos refletem a luz
14 10 Espaço para anotações:
15 11 Nome do aluno: Oficina 2: Você é feito da mesma matéria das estrelas! Revisão da oficina Glossário dos termos da Oficina 2 alumínio: é um elemento metálico que não ocorre naturalmente nós temos de fabricá-lo. átomo: a menor parte de um elemento a qual ainda possui todas as características dele. Consiste de um núcleo atômico central em volta do qual existe uma nuvem de elétrons. átomo de carbono: átomo com seis elétrons em sua nuvem de elétrons que existe em volta do núcleo. átomo de hidrogênio: o átomo mais simples do universo, formado por um núcleo em volta do qual orbita apenas um elétron. bilhão: mil milhões. brilho metálico: a maneira brilhante como a maioria dos metais reflete a luz. brilho vítreo: a maneira como o vidro reflete a luz. elemento: uma das 92 substâncias puras que constituem o universo que podemos enxergar (grande parte do universo é escura e não podemos vê-la de forma alguma); cada elemento é formado por átomos específicos e que o tornam diferente dos outros elementos. elétrons: partículas bem pequenas que quase não têm massa; orbitam ao redor do núcleo. página seguinte
16 12 gazilhões: uma palavra que inventamos para representar uma quantidade realmente enorme. grafite: nome popular da grafita, um tipo de carbono e um dos elementos sólidos mais moles. maleável: um sólido que pode ser dobrado sem quebrar; é uma propriedade de alguns elementos, como o alumínio. núcleo atômico: a parte central de um átomo onde toda a sua massa está concentrada. silício: é um elemento parecido com metal que não ocorre naturalmente nós temos de fabricá-lo. Atividades 1 a 4 Tabela de propriedades da grafite, do alumínio e do silício Propriedades (Opções) Grafite Alumínio Silício Cor (preto, prata, ou cinza) preto prata cinza Opacidade (transparente, translúcido ou opaco) opaco opaco opaco Brilho (vítreo, metálico ou fosco) metálico ou fosco metálico metálico Dureza: vai arranhar a placa de vidro? (sim ou não) não não sim Fratura (lisa ou áspera) pode ser ou lisa ou áspera lisa áspera Maleável (sim ou não) não sim não
17 13 Atividades 5 Desenhe o modelo atômico do hidrogênio núcleo nuvens de elétrons Quadro 1: Modelo atômico do hidrogênio Atividade 6 Desenhe o modelo atômico do carbono núcleo nuvens de elétrons Quadro 2: Modelo atômico do carbono
18 14 Questões de múltipla escolha e respostas Utilize um lápis para marcar um X na resposta que você julga ser a correta. Questão #1 Qual das substâncias tem cor preta? a. ( X ) A grafite. b. ( X ) O alumínio. Questão #2 Qual é a diferença entre a cor do alumínio e a do sílicio? a. ( X ) O alumínio e o sílicio são prateados. b. ( X ) O alumínio é prateado, o sílicio é cinza. Questão #3 Qual das amostras é translúcida? a. ( X ) O alumínio e o silício. b. ( X ) Nenhuma delas, ambas são opacas. Questão #4 Como é o brilho do silício? a. ( X ) Vítreo. b. ( X ) Metálico. O brilho metálico tem sempre um aspecto brilhante como o de um metal polido e a superfície reluzente. O brilho vítreo é menos intenso. Questão #5 Como é o brilho da grafite? a. ( X ) Metálico. b. ( X ) Vítreo. Cuidado - ele também pode ser fosco Questão #6 Somente uma dessas substâncias é dura o suficiente para arranhar a placa de vidro. Qual delas? a. ( X ) O silício. b. ( X ) A grafite. Questão #7 Qual a diferença entre o silício e a grafite quando se quebram (dica: se você não tem certeza, confira a amostra da grafite de outro grupo)? a. ( X ) O silício é mais liso, a grafite é mais áspera. b. ( X ) O silício é mais áspero, mas a grafite pode ser tanto lisa como áspera.
19 Questão #8 Qual dessas substâncias é maleável? a. ( X ) A grafite. b. ( X ) O alumínio. É por isso que é muito utilizado na cozinha. Tente embrulhar as sobras do jantar com grafite! 15 Questão #9 Com base no barulho que produz ao bater na mesa, o que você pode dizer sobre o núcleo do seu modelo do átomo de hidrogênio? a. ( X ) É muito pesado. b. ( X ) É muito leve. Questão #10 Com base no barulho que produz ao bater na mesa, o que você pode dizer sobre a nuvem de elétrons do seu modelo do átomo de hidrogênio? a. ( X ) É muito pesada. b. ( X ) É muito leve. Questão #11 Com base em suas observações, quando você separa o núcleo da nuvem de elétrons, você ainda tem um átomo? a. ( X ) Sim. b. ( X ) Não. Na vida real, somente os físicos que estudam átomos podem fazer isso: eles provocam a colisão dos átomos com a utilização de máquinas incríveis chamadas de aceleradores de partículas. Questão #12 Como o núcleo do átomo de carbono difere do núcleo do átomo de hidrogênio? a. ( X ) É mais leve. b. ( X ) É mais pesado. Questão #13 Se o núcleo de um átomo de silício é maior que o núcleo de um átomo de carbono, qual deles é mais pesado (dica: pense no experimento de queda com as duas bolas metálicas)? a. ( X ) O silício. b. ( X ) O carbono. Questão #14 Em um universo formado por 92 elementos, quantos tipos diferentes de átomos existem? a. ( X ) 9 b. ( X ) 92
20 16 Atividade 7 Mapa conceitual O diagrama da árvore conceitual está de volta para que você complete o seu mapa conceitual construído na Oficina 1. Na parte inferior da página, estão listadas seis palavras-chave que você aprendeu na Oficina 2. Três delas são tipos de brilho, três são tipos de opacidade. Note que os balões vazios estão conectados com alguns dos espaços que você preencheu na Oficina 1. Ao escrever as novas palavras nos balões vazios, você aumentará o seu mapa conceitual. É uma ideia que permite organizar o que você aprendeu. fosco metálico vítreo transparente translúcido tipos brilho tipos opaco fratura opacidade densidade dureza As propriedades são: cor Palavras conceituais: transparente translúcido Propriedades físicas dos sólidos opaco metálico vítreo fosco
21 17 Desafio para pensar: caça-palavra Instruções: Encontre as palavras escondidas abaixo e circule-as como mostra o exemplo. B A A L U M I N I O D A P A T O M S I B C X I V U Z T T N Q L I U N E R R J K L D T H I L N E U P Q Ú W B I L H Õ E S C N A T E M O N C W H L D D C A R B O N O J M E J L S F H V E O M C B R C Z L N E C E I E O U M N N O B T A C U I D L O L L V T Ó E O M N É G R A F I T E I E Í L C O E S M L F S A T C M S C V T O R G T D B E L X J Q O H S I Á R K I D C P T W Y R K W J M J O E E N T O I N Ê G O R D I H G O Y L O S O L L J L A C L P A R F T T A G D S N E G Z Z M I L H Õ E S A M E T Á L I C O L U S T R E S G Palavras: ALUMÍNIO ÁTOMO BILHÕES BRILHO VÍTREO CARBONO DEMÓCRITO ELEMENTO ELÉTRON GRAFITE HIDROGÊNIO MALEÁVEL METÁLICO MILHÕES NÚCLEO SILÍCIO
22 18 Espaço para anotações:
23 19 Nome do aluno: Oficina 3: Lápis, uma mistura misteriosa Revisão da oficina Glossário dos termos da Oficina 3 argila: uma rocha macia feita de partículas de rochas e minerais que são pequenos demais para serem vistos. cerâmica de grafite: o material principal dos lápis, feito pelo aquecimento de uma pasta de argila e grafite em uma fornalha própria. chumbo: um elemento metálico que é muito pesado, mas que não ocorre naturalmente nós temos de fabricá-lo. chumbo negro: um nome antigo dado à grafita, quando se acreditava que ela fosse uma variedade de chumbo. grafite: nome popular da grafita, um mineral macio feito de uma só substância pura, o carbono. mistura física: uma mistura onde os ingredientes podem ser separados em seus estados originais. mistura química: uma mistura onde os ingredientes foram de tal forma alterados durante o processo de mistura que não podem ser separados em seus estados originais. pergaminho: feito de peles de animais estendidas e raspadas; era usado para escrever por civilizações antigas.
24 20 Atividade 1 Tabela de propriedades físicas da grafite e do chumbo Propriedade (alternativas) Grafite Chumbo Cor (preto, prata ou cinza-prateado) preto cinza-prateado Opacidade (transparente, translúcido ou opaco) opaco opaco Brilho (vítreo ou metálico) Dureza (mais duro ou mais mole que a moeda de cobre) Fratura (lisa, áspera ou ambas) metálico não pode ser ou lisa ou áspera metálico não sem resposta Maleável (sim ou não) não sim Atividade 2 Escrever com grafite e chumbo Maria Brasil Maria Brasil Quadro 1: Grafite Quadro 2: Chumbo
25 21 Atividade 4 Melhorar a grafite Maria Brasil Maria Brasil Quadro 3: Lápis 4H Quadro 4: Lápis 4B Questões de múltipla escolha e respostas Utilize um lápis para marcar um X na resposta que você julga ser a correta. Questão #1 Qual dos seguintes materiais é mais mole que uma moeda de cobre? a. ( X ) O chumbo. b. ( X ) A grafite. c. ( X ) Os dois. Questão #2 Qual dos seguintes materiais é maleável? a. ( X ) O chumbo. b. ( X ) A grafite. Questão #3 Qual dos seguintes materiais tem um brilho metálico? a. ( X ) O chumbo (na superfície recém-cortada). b. ( X ) A grafite. c. ( X ) Os dois. O chumbo reage com o oxigênio da atmosfera, o que torna sua superfície cinza-escura e fosca; superfícies recém-expostas mostram sua cor verdadeira. Questão #4 Qual dos seguintes materiais tem cor cinza-prataeda? a. ( X ) O chumbo (na superfície recém-cortada). b. ( X ) A grafite.
26 22 Questão #5 Qual dos seguintes materiais marca facilmente o papel e deixa uma marca preta? a. ( X ) A grafite. b. ( X ) O chumbo. Questão #6 Qual das seguintes explicações é a mais correta para a resposta dada na questão anterior? a. ( X ) O chumbo é mais mole que a grafite. b. ( X ) A grafite é mais mole que o chumbo. Neste caso, você está usando papel para testar a dureza. Questão #7 Com base no que aprendeu nesta oficina, qual das seguintes afirmativas é a correta? a. ( X ) Os lápis modernos são feitos de grafite. b. ( X ) Os lápis modernos são feitos de chumbo. Os lápis não seriam muito úteis se rasgassem o papel todas as vezes que você escrevesse. Questão #8 Qual das afirmativas abaixo melhor explica a razão pela qual se acreditava que os lápis eram feitos com chumbo e não com grafite? a. ( X ) A pessoa que inventou o lápis tinha um cachorro chamado Cabeça de Chumbo. b. ( X ) Quando a grafite foi descoberta, foi confundida com chumbo e chamada de chumbo negro. O chumbo era chamado de plumbum em latim, mas você não precisa se lembrar desse nome. Questão #9 Como seriam os lápis se fossem feitos de pedaços de grafite? a. ( X ) Eles sujariam nossas mãos e cadernos. b. ( X ) Seriam tão moles que se desgastariam muito rápido. c. ( X ) Ambas as alternativas ilustram graves problemas. Questão #10 Se quiser criar lápis úteis e duráveis, o que deve fazer? a. ( X ) Achar um jeito de fazer a grafite ficar mais dura. b. ( X ) Achar um jeito de segurar o lápis sem tocar na grafite. c. ( X ) Ambas as alternativas indicam procedimentos essenciais. Os lápis antigos eram enrolados em tecido, mas depois a madeira passou a ser usada.
27 23 Questão #11 De que maneira a cerâmica preta é diferente da amostra de areia? a. ( X ) A areia é feita de diferentes grãos, enquanto a cerâmica não possui grãos visíveis. b. ( X ) A cerâmica é feita de diferentes grãos, enquanto a areia não possui grãos visíveis. Questão #12 Qual dos seguintes materiais pode ser facilmente separado em seus ingredientes originais? a. ( X ) A cerâmica. b. ( X ) A areia. Questão #13 Com base nas respostas dadas nas questões #9 e #10, em qual tipo de mistura eles se classificam? a. ( X ) A cerâmica é uma mistura química e areia é uma mistura física. b. ( X ) A cerâmica é uma mistura física e areia é uma mistura química. O processo de aquecer a mistura de argila e grafite promove uma mudança química que forma a cerâmica. Questão #14 Qual a diferença na dureza dos lápis 4H e 4B? a. ( X ) O lápis 4H é mais mole que o lápis 4B. b. ( X ) O lápis 4H é mais duro que o lápis 4B. Alguns artistas gostam de desenhar com grafite quase pura e utilizam lápis 6B até 9B. Questão #15 Qual a explicação para essa diferença de dureza? a. ( X ) A cerâmica de grafite no lápis 4H tem mais argila e menos grafite. b. ( X ) A cerâmica de grafite no lápis 4H tem menos argila e mais grafite. Em se aumentando a quantidade de argila na cerâmica, é possível fazer lápis mais duros como 2H, 4H, 6H etc. Em se aumentando a quantidade de grafite na mistura, é possível fazer lápis mais moles como 2B, 4B, 6B etc.
28 24 Atividade 7 Mapa conceitual O diagrama da árvore conceitual está de volta para que você faça um minimapa conceitual sobre o que forma um lápis. Na parte inferior da página, estão listadas algumas das ideias importantes que você aprendeu na Oficina 3. No diagrama da árvore, veja se você consegue escrever essas palavras nos espaços apropriados de forma que o conjunto delas tenha sentido. argila grafite tinta preta feita de cerâmica de grafite colorido com contendo cor externa do lápis centro do lápis lápis As propriedades são: Palavras conceituais: cor externa do lápis centro do lápis cerâmica de grafite O que forma um lápis? argila grafite tinta preta
29 25 Desafio: palavras embaralhadas Instruções: Para resolver este desafio, desembaralhe as palavras nas linhas abaixo (siga o exemplo). Depois, use a sequência das letras numeradas para formar a palavra misteriosa. Se precisar de ajuda, dê uma olhada na lista de palavras no glossário do relatório do laboratório. Palavras RGFAEIT G R 2 A F I T E RAGNEMIPHO 3 P E R G A M I N H O ASRUMTI M 4 I 5 S T U R A ERAMOLA A M A R E 1 L O Palavra misteriosa L A P I S
30 26 Espaço para anotações:
31 27 Nome do aluno: Oficina 4: Dois minerais metálicos magníficos Revisão da oficina Glossário dos termos da Oficina 4 composto: formado quando dois ou mais elementos se combinam. Se eles ocorrem naturalmente no estado sólido, são chamados de minerais. enxofre: esse elemento ocorre naturalmente como um mineral de cor amarelobrilhante perto de fontes termais e vulcões. ferro: é o elemento metálico mais utilizado. O Brasil tem enormes depósitos de ferro, e a Vale S. A. é a maior mineradora de ferro da Nave Terra. galena: um mineral feito de chumbo e enxofre. hematita: um mineral feito de ferro e oxigênio. ligações atômicas: energia elétrica que cola diferentes átomos para formar moléculas. minerais: substâncias puras que ocorrem na natureza no estado sólido. São feitos de um ou mais elementos. molécula: formada por átomos de dois ou mais elementos, é a menor parte do mineral que conserva as suas propriedades químicas originais. pirita: um mineral feito de ferro e enxofre, conhecido como ouro dos tolos por causa da sua cor. reação química: é uma reação entre dois ou mais átomos que envolve a mistura das nuvens de elétrons que circundam o núcleo de cada átomo. traço: uma marca que o mineral deixa quando arranhado na placa branca de cerâmica; mostra a verdadeira cor do mineral.
32 28 Atividade 1 Tabela de propriedades físicas da galena e seus ingredientes Propriedades (alternativas) Cor (amarelo, cinza ou cinza-prateado) Traço (amarelo, preto ou cinza-prateado) Opacidade (transparente, translúcido ou opaco) Brilho (vítreo, metálico ou fosco) Ingredientes Mineral Chumbo Enxofre Galena cinza-prateado amarelo cinza-prateada cinza-prateado amarelo preto opaco opaco opaco metálico fosco metálico Vai arranhar a placa de vidro? (sim ou não) não não não A unha vai arranhá-lo? (sim ou não) sim não não Fratura (lisa ou áspera) lisa áspera muitas superfícies planas em 90 o Maleável (sim ou não) sim não não Magnético (sim ou não) não não não
33 29 Atividade 2 Tabela de propriedades físicas de pirita e seus ingredientes Propriedades (alternativas) Cor (amarelo, amarelo-latão, cinza) Traço (amarelo, pretoesverdeado ou prata) Opacidade (transparente, translúcido ou opaco) Brilho (vítreo, metálico ou fosco) Vai arranhar a placa de vidro? (sim ou não) A unha vai arranhá-lo? (sim ou não) Ingredientes Mineral Ferro Enxofre Pirita cinza amarelo amarelo-latão prata amarelo preto-esverdeado opaco opaco opaco metálico fosco metálico não não sim não não não Fratura (lisa ou áspera) áspera áspera áspera Magnético (sim ou não) sim não não
34 30 Atividade 4 Bolas de aço, cotonetes e uma molécula de galena núcleo do átomo de chumbo núcleo do átomo de enxofre nuvens de elétrons nuvens de elétrons Quadro 1: Modelo da uma molécula de galena Atividade 5 Tabela de propriedades físicas da hematita Propriedades (alternativas) Ferro Hematita Cor (cinza, cinza-prateado) cinza cinza Traço (cinza, vermelho-escuro ou prata) prata vermelho-escuro Brilho (vítreo, metálico ou fosco) metálico metálico (pode ser fosco) Magnético (sim ou não) sim não
35 31 Questões de múltipla escolha e respostas Utilize um lápis para marcar um X na resposta que você julga ser a correta. Questão #1 O enxofre é mais duro que uma unha? a. ( X ) Sim. b. ( X ) Não. Questão #2 Qual característica física o chumbo e a galena compartilham? a. ( X ) Traço e dureza. b. ( X ) Cor e brilho. Questão #3 De que maneira o chumbo e a galena são diferentes? a. ( X ) O chumbo é maleável (dobra), a galena não. b. ( X ) A galena é maleável (dobra), o chumbo não. Questão #4 Qual dos seguintes elementos é magnético? a. ( X ) O chumbo. b. ( X ) O ferro. Questão #5 Qual é a dureza da pirita? a. ( X ) Ela é mais mole que a placa de vidro. b. ( X ) Ela é mais dura que a placa de vidro. Questão #6 Como é o brilho da pirita e da galena? a. ( X ) Metálico. b. ( X ) Vítreo. Questão #7 O que o traço da pirita revela sobre a cor verdadeira desse mineral? a. ( X ) Que ela é amarelo-latão. b. ( X ) Que ela é preto-esverdeada. Isso mostra o valor do teste do risco para minerais com brilho metálico.
36 32 Questão #8 O que você pode dizer sobre os minerais e os elementos que os formam? a. ( X ) O elemento se parece com o mineral de que é feito. b. ( X ) Algumas propriedades são similares, mas a maioria é diferente. Questão #9 Quantos tipos diferentes de átomos existem em uma molécula de galena? a. ( X ) Um. b. ( X ) Dois. O chumbo e o enxofre. Questão #10 O que mantém os diferentes átomos na molécula de galena juntos? a. ( X ) O núcleo de cada átomo. b. ( X ) Os elétrons ao redor do núcleo. Questão #11 Qual é a diferença de tamanho entre um átomo e uma molécula? a. ( X ) Um átomo é bem menor, uma molécula é bem maior. b. ( X ) Um átomo é bem maior, uma molécula é bem menor. Questão #12 Qual tipo de mistura é um mineral? a. ( X ) Uma mistura física de diferentes elementos que podem ser facilmente reconhecidos. b. ( X ) Uma mistura química de diferentes elementos que formam uma molécula que não se parece com nenhum dos elementos. Questão #13 Qual dos seguintes é magnético? a. ( X ) O ferro. b. ( X ) A hematita. Questão #14 O que o traço da hematita revela sobre a cor verdadeira desse mineral? a. ( X ) Que ela é vermelho-escura. b. ( X ) Que ela é cinza.
37 33 Atividade 5 Mapa conceitual O diagrama da árvore conceitual está de volta para que você faça um novo mapa conceitual sobre minerais. No fim da página, estão listadas as palavras mais importantes aprendidas na Oficina 4. Para ajudar você, duas dessas palavras já foram colocadas no diagrama da árvore. Sua tarefa é escrever o restante das palavras nos espaços vazios de forma que façam sentido juntas. Pela primeira vez nós vamos utilizar palavras de ligação entre os espaços para mostrar como os conceitos se conectam. átomos de carbono átomos de enxofre átomos de ferro átomos de chumbo feita de feita de feita de átomos de enxofre enxofre grafite pirita galena exemplos exemplos elementos compostos São dividos em: Palavras conceituais: elementos compostos enxofre átomos de carbono Minerais grafite pirita galena átomos de ferro átomos de enxofre átomos de chumbo
38 34 Desafio: Jogo das palavras embaralhadas Instruções: Para resolver esse desafio, desembaralhe as palavras e, depois, copie as letras dos espaços numerados nos quadrinhos com os mesmos números da palavra misteriosa. Como exemplo, a primeira palavra foi revelada. Se você precisar de ajuda, olhe as palavras no glossário do relatório do laboratório. Palavras TOMAO A T 1 O M 4 O TAFRARU F R A 7 T 2 U R A MAENILR M I N E 3 R A L 6 GIEMSNAMTO M A G N E T I S M 5 LOMLUCESA M 8 O L E C U L A 11 S ELAGAN G A 9 L E N A GAÇOÃIL L I G Ç Ã 10 O O Palavra misteriosa O U R O D O S T O O L S
39 Espaço para anotações: 35
40 36 Espaço para anotações:
41 37 Nome do aluno: Oficina 5: É quartzo, claro! Revisão da oficina Glossário dos termos da Oficina 5 aresta: a linha onde duas faces de um cristal se juntam. cristal: o formato especial que um mineral adquire a partir de superfícies planas (faces). face: uma superfície plana sobre um cristal. geodo: uma cavidade natural na rocha onde os cristais crescem. poliedro: uma forma sólida de três dimensões constituída de faces que se encontram ao longo das suas arestas e cujos ápices se encontram (ver vértice). prisma: sólido geométrico com faces opostas e paralelas umas às outras (à exceção do prisma triangular). pseudociência: ciência imaginária na qual as ideias que não podem ser testadas são consideradas verdadeiras. pirâmide: quando as faces triangulares se encontram no vértice. quartzo: um mineral muito comum feito de metal de silício e oxigênio gasoso. vértice: em um poliedro, é qualquer ponto onde três ou mais arestas se encontram. O mais alto vértice da pirâmide é chamado de ápice.
42 38 Atividades 1 e 2 Tabela de propriedades físicas Propriedade (alternativas) Silício Quartzo branco Quartzo cinza Cor (branco, cinza) cinza branco cinza Traço (branco, cinza, claro) Opacidade (transparente, translúcido, opaco) Brilho (vítreo, metálico ou fosco) preto claro claro opaco translúcido translúcido metálico vítreo vítreo Vai arranhar a placa de vidro? (sim ou não) sim sim sim Fratura (lisa ou áspera) áspera áspera áspera
43 39 Atividade 3 Formato de um cristal de quartzo perfeito Ápice Vértice Aresta Face Pirâmide Vista superior de um cristal de quartzo perfeito Prisma Base irregular Esqueleto de um cristal de quartzo perfeito Como um cristal de quartzo aumenta de tamanho (cresce) Quadro 1 Quadro 2 Tabela: A Geometria de um Cristal de Quartzo Característica Parte da pirâmide Parte do prisma Cristal de quartzo como um todo Quantos ápices? Quantos vértices? Quantas arestas? Quantas faces?
44 40 Atividade 4 Aumentar cristais de quartzo no papel Escala: Quadro 3: Vista superior do seu cristal de quartzo
45 41 Questões de múltipla escolha e respostas Utilize um lápis para marcar um X na resposta que você julga ser a correta. Questão #1 Qual das seguintes propriedades é diferente entre o silício e o quartzo branco? a. ( X ) A cor. b. ( X ) A dureza. Questão #2 Qual das seguintes propriedades é a mesma para o silício e o quartzo branco? a. ( X ) A cor. b. ( X ) A dureza. Questão #3 Como é o brilho do quartzo branco quando comparado com o do silício? a. ( X ) O do quartzo é metálico e o do silício é fosco. b. ( X ) O do quartzo é vítreo e o do silício é metálico. Questão #4 A dureza, a fratura e o brilho são diferentes entre o quartzo branco e o cinza? a. ( X ) Sim. b. ( X ) Não. Questão #5 Qual é a única propriedade que distingue o quartzo cinza do branco? a. ( X ) A opacidade. b. ( X ) A cor. Questão #6 Qual dessas opções se refere às propriedades físicas dos minerais? a. ( X ) Cada mineral tem um grupo especial de propriedades. b. ( X ) A cor pode ser diferente entre amostras de um mesmo mineral. c. ( X ) As opções a. e b. estão corretas. Em outras palavras, a cor pode enganar. Questão #7 Quantos vértices, arestas e faces existem em um prisma de cristal de quartzo perfeito? a. ( X ) 6, 6, 6 b. ( X ) 6, 12, 6
46 42 Questão #8 Quantos vértices, arestas e faces existem na pirâmide de um cristal de quartzo perfeito? a. ( X ) 7, 12, 6 b. ( X ) 6, 6, 6 Questão #9 Quantas arestas, vértices e faces existem em um cristal de quartzo perfeito (não incluindo a base irregular)? a. ( X ) 7, 12, 12 b. ( X ) 7, 18, 12 Questão #10 Penta, hexa e octa são os números 5, 6 e 8 em grego. Então, vista de cima, qual é a forma apresentada pelos cristais de quartzo? a. ( X ) Pentágono. b. ( X ) Hexágono. c. ( X ) Octógono. Questão #11 Qual das seguintes opções melhor descreve suas observações sobre como os cristais de quartzo crescem? a. ( X ) À medida que os cristais crescem, eles mantêm sua forma original. b. ( X ) À medida que os cristais crescem, eles mantêm o mesmo ângulo entre as faces. c. ( X ) Ambas as opções estão corretas. Cristais de quartzo podem parecer um pouco diferentes, mas mantêm sua forma básicas (hexágono). Questão #12 Com base no que você aprendeu, qual é a condição mais importante para que os cristais com uma forma bonita se formem em uma rocha? a. ( X ) Uma rocha sólida. b. ( X ) Espaço para crescer.
47 43 Atividades 6 Mapa conceitual O diagrama da árvore conceitual esta de volta para que você acrescente outras palavras ao mapa conceitual sobre as propriedades dos sólidos, que você começou na Oficina 1 e continuou na Oficina 2. Na parte inferior da página, nós listamos as palavras-chave sobre cristais da Oficina 5. Encontre o balão para os formatos de cristais e os balões vazios que estão ligados a ele, então preencha-os corretamente com as palavras da lista abaixo. A propósito, o seu mapa conceitual é agora cahamado de As Propriedades dos Minerais. fosco metálico vítreo transparente translúcido faces tipos brilho fratura tipos opacidade opaco arestas que têm forma de cristal densidade vértices exemplo cristal de quartzo dureza As propriedades são: cor Palavras conceituais: forma de cristal cristal de quartzo faces Minerais arestas vértices
48 44 Desafio: Palavras cruzadas Instruçaões: Decifre cada dica para achar as palavras corretas, depois coloque-as nos espaços indicados pelos números das pistas. Se precisar de ajuda, dê uma olhada nas palavras do Glossário dessa oficina P H O P E N T A G O N O S E 2 G U 3 V E R T I 4 C D O R O L I E D R O I C O S I T E X A G O N O A N L C T O G O N O I A 1 E Horizontal 1. Figura com cinco lados 3. O ponto de encontro de três arestas 5. Nome dado a um objeto tridimensional 6. Figura com seis lados 7. Figura com oito lados Vertical 1. Ciência imaginária 2. Onde os cristais se formam 4. O nome dado ao formato perfeito de um mineral
49 Espaço para anotações: 45
50 46 Espaço para anotações:
51 47 Nome do aluno: Oficina 6: Por favor, mineral, me dê um tempo! Revisão da oficina Glossário dos termos da Oficina 6 calcita: um mineral muito comum feito de átomos de cálcio, carbono e oxigênio. clivagem: a superfície lisa e plana que se forma quando um mineral com ligações atômicas fracas é quebrado. cristalografia: originalmente era somente o estudo dos cristais. Agora é a ciência que estuda como os átomos estão arranjados em substâncias sólidas. fratura irregular: superfície irregular formada quando um mineral com ligações atômicas fortes é quebrado. romboedro: formato tridimensional regular que se parece com um cubo esticado com lados opostos paralelos.
52 48 Atividade 2 Galena e o saquinho com pedaços de galena Vista superior Quadro 1: O formato da galena Atividade 5 A clivagem da calcita Vista inferior Vista lateral Vista superior Vista inferior Vista lateral Quadro 2: O formato do romboide calcita
53 49 Questões de múltipla escolha e respostas Utilize um lápis para marcar um X na resposta que você julga ser a correta. Questão #1 O pedaço grande de quartzo branco tem um formato especial ou superfície plana? a. ( X ) Sim. b. ( X ) Não. Questão #2 Os pedaços de quartzo do saquinho têm um formato especial ou superfície plana? a. ( X ) Sim. b. ( X ) Não. Questão #3 Qual das alternativas seguintes melhor descreve como o quartzo se quebra? a. ( X ) Quando o quartzo se quebra, possui uma fratura irregular e sem formato especial. b. ( X ) Quando o quartzo se quebra, forma superfícies planas lisas e todas com a mesma forma. Questão #4 O que você pode dizer sobre o formato do pedaço grande de galena? a. ( X ) É parecido com um bloco. b. ( X ) Não possui formato definido. Os lados se encontram em ângulos retos. Questão #5 O que você pode dizer sobre o formato dos pedaços menores de galena? a. ( X ) Eles se parecem com o pedaço maior. b. ( X ) Eles não possuem formato definido. Questão #6 Qual das alternativas seguintes melhor descreve como a galena se quebra? a. ( X ) Forma pedaços pequenos que não possuem formato específico. b. ( X ) Forma pequenos blocos de a mesma forma mas de tamanhos diferentes.
54 50 Questão #7 Como você descreve o formato do pedaço maior da calcita? a. ( X ) Ele se parece com um cubo esticado denominado romboide. b. ( X ) Não possui formato específico. Os lados não formam ângulos retos. Questão #8 O que você pode dizer sobre o formato dos pedaços menores da calcita? a. ( X ) Eles se parecem com o pedaço maior. b. ( X ) Não possuem formato específico. Questão #9 Qual das seguintes conclusões melhor descreve como a calcita se quebra? a. ( X ) Ela forma pedaços menores sem formato particular. b. ( X ) Ela forma pequenos romboides de mesmo formato, mas com tamanhos diferentes. Questão #10 Quão fortes são as ligações atômicas ( cola ) na pirita, e como você sabe? a. ( X ) Fracas, pois a pirita não possui clivagem. b. ( X ) Fortes, pois a pirita não possui clivagem. Questão #11 Se você quebrar o cristal de quartzo, obterá uma grande quantidade de pequenos cristais? a. ( X ) Não, pois o quartzo não possui clivagem, somente fraturas. b. ( X ) Sim, pois o saquinho com pequenos pedaços de quartzo está cheio de pequenos cristais. Questão #12 Como são chamadas as superfícies do romboide da calcita? a. ( X ) Clivagem. b. ( X ) Fratura. O cristal de calcita pode também parecer um romboide de clivagem.
55 51 Questão #13 Quantos lados o romboide de calcita possui? a. ( X ) 2 b. ( X ) 3 c. ( X ) 6 Questão #14 Quantas diferentes superfícies de clivagem possui um romboide de calcita? a. ( X ) 2 b. ( X ) 3 c. ( X ) 6 Os lados opostos paralelos do romboide são as mesmas superfícies de clivagem. Questão #15 O que realmente nos diz a superfície de clivagem? a. ( X ) A maneira como os átomos do mineral estão organizados. b. ( X ) Como os átomos do mineral estão ligados ( colados ). c. ( X ) Ambas as alternativas estão corretas. As superfícies de clivagem são como uma janela: permitem que a gente veja como os átomos de um mineral estão organizados.
56 52 Atividade 6 Mapa conceitual E hora de ampliar seu diagrama das propriedades dos minerais. O diagrama da árvore conceitual lhe forneceu mais duas palavras chave, e tudo que você tem a fazer é escrevêlas nos balões. fosco metálico vítreo transparente translúcido tipos faces brilho fratura tipos opacidade opaco traço arestas que tem forma de cristal densidade vértices exemplo cristal de quartzo dureza clivagem As propriedades são: cor Palavras conceituais: traço Minerais clivagem
57 53 Desafio para pensar: Caça-palavras Instruções: Ache as seguintes palavras na grade de palavras. Observe a direção em que cada palavra está apontada e responda às questões no final do desafio. Uma palavra e sua direção foram indicadas no quebra-cabeça como exemplo. 7 J B Y R T B A V Y W R C A U A I U R A J H W L L W V I I U T O O R I H Z W F F T B Ã O C V K G M B C A B Ç W J A D J V F 6 Palavras: LIGAÇÃO BLOCOS CALCITA Desafio: B R R A P Y G R G U M O F G G P I E L F J A H R H I O V M O P K E T M T L C L V R O M B O I D E S 4 C A L C I O M H C M G L G T L K O K O J L Q T E P S O C O L B 3 M A I L C A I A I I W L N C S T Z A R A Q O T W X I Y P E 1 F C W D D I A L 2 M V I 5 CÁLCIO CLIVAGEM CRISTALOGRAFIA FRATURA ROMBOIDE FORTE Circule o número de direções em que as palavras estão apontando FRACO
58 54 Espaço para anotações:
59 55 Nome do aluno: Oficina 7: Material duro na queda Revisão da oficina Glossário dos termos da Oficina 7 abrasivos: são materiais duros, resistentes e fortes que desgastam superfícies mais macias, menos resistentes. dentículos: saliências duras na pele de um tubarão. Eles fazem a pele do tubarão áspera como uma lixa. escala de dureza: Frederich Mohs, um mineralogista alemão, selecionou os dez minerais mais conhecidos e os organizou em ordem crescente de dureza (veja a Tabela: Escala de dureza dos minerais). feldspato: o mineral mais comum na crosta da Nave Terra. Tem duas clivagens, então se quebra em blocos. granada: um mineral vermelho-escuro que não tem clivagem, ou seja, é duro!
60 56 Nome do mineral Número de dureza Dureza dos materiais de teste Grafite 1 Gipsita 2 unha - 2½ Calcita 3 moeda de cobre - 3 Fluorita 4 Apatita 5 nossos dentes - 5 placa de vidro - 5½ prego - 5½ Feldspato 6 placa de traço - 6½ Quartzo 7 Topázio 8 Coríndon 9 Diamante 10 Tabela: Escala de dureza dos minerais
61 57 Atividades 1 e 2 Número de dureza e escolha de um material abrasivo Mineral Número de dureza Como seria a pasta de dentes formada por esse mineral? Grafite 1 mole demais; deixaria os dentes pretos Enxofre 2½ mole demais; deixaria os dentes amarelos Galena 2½ arenosa (como quando se come uma salada que não foi bem lavada); deixaria os dentes cinza Calcita 3 nem dura demais, nem mole demais; e deixaria uma cor boa Hematita 6 dura demais; deixaria os dentes vermelhos Pirita 6 dura demais; deixaria uma cor cinza-metálica Feldspato 6 dura demais Quartzo 7 dura demais
62 58 Atividade 4 Tabela de propriedades de abrasivos comuns Material Fratura Clivagem Dureza Vidro irregular nenhuma 5½ Quartzo irregular nenhuma 7 Granada irregular nenhuma 7½ Questões de múltipla escolha e respostas Utilize um lápis para marcar um X na resposta que você julga ser a correta. Questão #1 Se um mineral tem dureza 2½, o que você pode concluir? a. ( X ) O mineral não pode ser arranhado por sua unha. b. ( X ) O mineral pode ser arranhado por sua unha. É claro que o mineral também não pode arranhar sua unha. Questão #2 A hematita arranha a calcita? a. ( X ) Sim. b. ( X ) Não. Sim, mas não facilmente: é importante utilizar a lupa para observar o arranhão na moeda. Questão #3 A calcita arranha uma moeda de cobre (tente e utilize a sua lupa para ter certeza)? a. ( X ) Sim. b. ( X ) Não. Questão #4 A pirita arranha o feldspato? a. ( X ) Sim. b. ( X ) Não.
63 59 Questão #5 Qual a dureza da pirita? a. ( X ) 5 b. ( X ) 6 Questão #6 Enxofre e galena têm a mesma dureza. Qual? a. ( X ) 4 b. ( X ) 2 Questão #7 Qual dos seguintes grupos de minerais não formaria, por causa da cor, bons abrasivos para pastas de dentes? a. ( X ) Grafite, enxofre e galena. b. ( X ) Quartzo e calcita. Questão #8 Quais dos seguintes minerais não seriam, por causa da dureza, bons abrasivos para pastas de dentes? a. ( X ) Grafite, enxofre e galena. b. ( X ) Quartzo, pirita e feldspato. Questão #9 Qual dos seguintes minerais seria a melhor opção como abrasivo para pasta de dentes? a. ( X ) Calcita. b. ( X ) Quartzo. Vamos dar à calcita um grande Obrigado! Questão #10 Qual é a principal diferença entre as duas amostras de lixa? a. ( X ) A composição dos grãos. b. ( X ) O tamanho dos grãos. Questão #11 Que tipo de fratura o vidro, o quartzo e a granada têm em comum? a. ( X ) Irregular. b. ( X ) Lisa.
64 60 Questão #12 O vidro, o quartzo e a granada têm superfícies frágeis devido à sua clivagem? a. ( X ) Sim. b. ( X ) Não. Questão #13 Qual mineral do vidro é o mais duro: o quartzo ou a granada? a. ( X ) O quartzo. b. ( X ) A granada. Questão #14 Quais propriedades são esperadas para o corindo uma vez que é um abrasivo resistente? a. ( X ) Sem clivagem e com fraturas irregulares. b. ( X ) Dureza extrema. c. ( X ) Ambas estão corretas.
65 61 Desafio para pensar: Palavras cruzadas Instruções: O tema desse jogo de palavras cruzadas é Abrasivos e a tabela de dureza de Mohs. Decifre cada pista para encontrar as palavras e coloque-as nos espaços indicados pelos números das pistas. Ao terminar, responda à questão para resolver a charada. 7 G G Q U A R T Z O R A A N 6 C F E L D S P A T O I D R T A I E N 5 C D 1 T U B A R Ã O L N C 4 G I P S I T A T A Horizontal: 1. Lixa viva 2. Abrasivo rosa 3. O abrasivo encontrado na areia da praia 4. O segundo abrasivo mais duro na tabela de Mohs Vertical: 5. O abrasivo na pasta de dentes 6. O mineral mais duro na tabela de Mohs 7. Abrasivo vermelho mais duro que o quartzo 8. O mineral mais mole na tabela de Mohs Questão: Quais minerais presentes na tabela de dureza de Mohs não estão nas palavras cruzadas? Resposta: fluorita, apatita, topázio e diamante
66
67
68
Explorando a Nave Terra
 Explorando a Nave Terra Kit 1: Elementos, Minerais e Cristais Caderno de Atividades Kit Mirim de Geociências Christopher e Brenda Brooks Explorando a Nave Terra Kit 1: Elementos, Minerais e Cristais Caderno
Explorando a Nave Terra Kit 1: Elementos, Minerais e Cristais Caderno de Atividades Kit Mirim de Geociências Christopher e Brenda Brooks Explorando a Nave Terra Kit 1: Elementos, Minerais e Cristais Caderno
GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS
 GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS Prof. Dr. Daniel Caetano 2011-2 Visão Geral 1 2 3 4 5 6 Motivação Matéria Sólida Minerais Grupos de Minerais Identificação dos Minerais Origens: Minerais
GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS Prof. Dr. Daniel Caetano 2011-2 Visão Geral 1 2 3 4 5 6 Motivação Matéria Sólida Minerais Grupos de Minerais Identificação dos Minerais Origens: Minerais
GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS
 GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS Prof. Dr. Daniel Caetano 2012-1 Objetivos Compreender a diferença entre minerais e rochas Apresentar os conceitos químicos que embasam a compreensão do
GEOLOGIA PARA ENGENHARIA CIVIL MINERAIS E ROCHAS Prof. Dr. Daniel Caetano 2012-1 Objetivos Compreender a diferença entre minerais e rochas Apresentar os conceitos químicos que embasam a compreensão do
As propriedades físicas dos minerais
 Os minerais Os minerais As propriedades físicas dos minerais As propriedades físicas usualmente empregues são as seguintes: Cor Traço ou risca Transparência ou diafanidade Brilho Dureza Densidade Hábito
Os minerais Os minerais As propriedades físicas dos minerais As propriedades físicas usualmente empregues são as seguintes: Cor Traço ou risca Transparência ou diafanidade Brilho Dureza Densidade Hábito
PROPRIEDADES FÍSICAS DOS MINERAIS
 PROPRIEDADES FÍSICAS DOS MINERAIS Oliveira, Francisco Sérgio Silva de. O48p Propriedades físicas dos minerais / Francisco Sérgio Silva de Oliveira. Varginha, 2015. 13 slides. Sistema requerido: Adobe Acrobat
PROPRIEDADES FÍSICAS DOS MINERAIS Oliveira, Francisco Sérgio Silva de. O48p Propriedades físicas dos minerais / Francisco Sérgio Silva de Oliveira. Varginha, 2015. 13 slides. Sistema requerido: Adobe Acrobat
Explorando a Nave Terra
 Explorando a Nave Terra Kit 2: Rochas e Minerais Caderno de Atividades Kit Mirim de Geociências Christopher e Brenda Brooks Explorando a Nave Terra Kit 2: Rochas e Minerais Caderno de Atividades Kit Mirim
Explorando a Nave Terra Kit 2: Rochas e Minerais Caderno de Atividades Kit Mirim de Geociências Christopher e Brenda Brooks Explorando a Nave Terra Kit 2: Rochas e Minerais Caderno de Atividades Kit Mirim
Geologia, problemas e materiais do quotidiano
 Biologia e Geologia 11º ano Tema 4 Geologia, problemas e materiais do quotidiano 4.2. Processos e materiais importantes em ambientes terrestres 2016 Propriedades dos Minerais As rochas são formadas, em
Biologia e Geologia 11º ano Tema 4 Geologia, problemas e materiais do quotidiano 4.2. Processos e materiais importantes em ambientes terrestres 2016 Propriedades dos Minerais As rochas são formadas, em
Conceitos importantes: a) Matéria : Tudo o que possui massa e ocupa lugar no espaço.
 SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
Vida e matéria. Aula de hoje
 Vida e matéria Aula de hoje Energia e matéria são constituintes essenciais do universo e dos seres vivos. A energia fornece força para manter as estruturas juntas ou separadas, e mover as coisas de um
Vida e matéria Aula de hoje Energia e matéria são constituintes essenciais do universo e dos seres vivos. A energia fornece força para manter as estruturas juntas ou separadas, e mover as coisas de um
Compreendendo a Terra
 Frank Press Raymond Siever John Grotzinger Thomas H. Jordan Compreendendo a Terra 4a Edição Mineral: matéria prima da Terra Lecture Slides prepared by Peter Copeland Bill Dupré Copyright 2004 by W. H.
Frank Press Raymond Siever John Grotzinger Thomas H. Jordan Compreendendo a Terra 4a Edição Mineral: matéria prima da Terra Lecture Slides prepared by Peter Copeland Bill Dupré Copyright 2004 by W. H.
Prof. Dr. Renato Pirani Ghilardi Dept. Ciências Biológicas UNESP/Bauru - SP. Tipos de Rochas
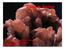 Prof. Dr. Renato Pirani Ghilardi Dept. Ciências Biológicas UNESP/Bauru - SP Tipos de Rochas MINERAIS E ROCHAS Mineral: elemento ou composto químico resultante de processos inorgânicos, de composição química
Prof. Dr. Renato Pirani Ghilardi Dept. Ciências Biológicas UNESP/Bauru - SP Tipos de Rochas MINERAIS E ROCHAS Mineral: elemento ou composto químico resultante de processos inorgânicos, de composição química
2. Observe cada amostra e desenhe no seu caderno ou em fichas feitas de cartolina.
 Ficha 1 Identificando os minerais Observe o conteúdo da caixa do Kit. Há etiquetas identificando cada item, mas para evitar confusão na hora de guardar após as atividades, vamos cadastrar cada mineral
Ficha 1 Identificando os minerais Observe o conteúdo da caixa do Kit. Há etiquetas identificando cada item, mas para evitar confusão na hora de guardar após as atividades, vamos cadastrar cada mineral
14/08/2016. Introdução à Engenharia Geotécnica. Minerais. Agosto Minerais
 Introdução à Engenharia Geotécnica Minerais Vítor Pereira Faro [email protected] Sidnei Helder Cardoso Teixeira [email protected] Agosto 2016 Minerais 1 MINERAIS A história da utilização dos minerais resulta
Introdução à Engenharia Geotécnica Minerais Vítor Pereira Faro [email protected] Sidnei Helder Cardoso Teixeira [email protected] Agosto 2016 Minerais 1 MINERAIS A história da utilização dos minerais resulta
GEOLOGIA. Professor: Adilson Soares Site:
 GEOLOGIA Professor: Adilson Soares E-mail: [email protected] Site: www.geologia.wiki.br Minerais e Rochas 1. Minerais e Rochas - conceito - propriedades dos minerais - tipos de rochas - ciclo das
GEOLOGIA Professor: Adilson Soares E-mail: [email protected] Site: www.geologia.wiki.br Minerais e Rochas 1. Minerais e Rochas - conceito - propriedades dos minerais - tipos de rochas - ciclo das
Experimento 2: Dimensão do átomo Objetivos:
 Experimento 2: Dimensão do átomo Objetivos: mostrar ao aluno que os átomos são muito menores que a dimensão de pequeno que eles têm em sua concepção e que a ciência trabalha com modelos para facilitar
Experimento 2: Dimensão do átomo Objetivos: mostrar ao aluno que os átomos são muito menores que a dimensão de pequeno que eles têm em sua concepção e que a ciência trabalha com modelos para facilitar
02- Quais das propriedades a seguir são as mais indicadas para verificar se é pura uma certa amostra sólida de uma substância conhecida?
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
O ÁTOMO pág. 66. Átomo: do grego, indivisível.
 O ÁTOMO pág. 66 Átomo: do grego, indivisível. Núcleo: Prótons + Nêutrons Eletrosfera: Elétrons Número atômico (Z): nº de prótons no núcleo Número de massa (A): nº de prótons + nêutrons Prótons: carga positiva
O ÁTOMO pág. 66 Átomo: do grego, indivisível. Núcleo: Prótons + Nêutrons Eletrosfera: Elétrons Número atômico (Z): nº de prótons no núcleo Número de massa (A): nº de prótons + nêutrons Prótons: carga positiva
Deep Sea Drilling Vessel (D/V) CHIKYU is the first riser equipped scientific drilling vessel built for science at the planning stage.
 Deep Sea Drilling Vessel (D/V) CHIKYU is the first riser equipped scientific drilling vessel built for science at the planning stage. It is capable of drilling up to 7,000m deep sea floor and aim to the
Deep Sea Drilling Vessel (D/V) CHIKYU is the first riser equipped scientific drilling vessel built for science at the planning stage. It is capable of drilling up to 7,000m deep sea floor and aim to the
Lição 20 Sumário 24/10/17
 Lição 20 Sumário 24/10/17 Tpc Questões da página 47 Rochas e Minerais As rochas são materiais terrestres formados por minerais. Na sua constituição as rochas podem ter um ou mais minerais juntos. Os minerais
Lição 20 Sumário 24/10/17 Tpc Questões da página 47 Rochas e Minerais As rochas são materiais terrestres formados por minerais. Na sua constituição as rochas podem ter um ou mais minerais juntos. Os minerais
Laboratório Didático II
 1 Laboratório Didático II Experimentos da aula prática de Geologia Setembro 2012 GEOLOGIA Prof. Vanderlei S. Bagnato 1. Introdução Geral Na Geologia, lidamos com materiais naturais, em sua maioria minerais.
1 Laboratório Didático II Experimentos da aula prática de Geologia Setembro 2012 GEOLOGIA Prof. Vanderlei S. Bagnato 1. Introdução Geral Na Geologia, lidamos com materiais naturais, em sua maioria minerais.
ELEMENTOS QUÍMICOS E SUA CLASSIFICAÇÃO PERIÓDICA
 SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR SARGENTO NADER ALVES DOS SANTOS SÉRIE/ANO: 9º TURMA(S):
SECRETARIA DE SEGURANÇA PÚBLICA/SECRETARIA DE EDUCAÇÃO POLÍCIA MILITAR DO ESTADO DE GOIÁS COMANDO DE ENSINO POLICIAL MILITAR COLÉGIO DA POLÍCIA MILITAR SARGENTO NADER ALVES DOS SANTOS SÉRIE/ANO: 9º TURMA(S):
É PROIBIDO PORTAR CELULAR.
 Química Avaliação Mensal 1 os anos Décio maio/12 Nome: Nº: Turma: INSTRUÇÕES GERAIS 1. Nenhum material deve estar embaixo das carteiras. Livros e mochilas devem ficar guardados no armário. 2. Sobre a mesa,
Química Avaliação Mensal 1 os anos Décio maio/12 Nome: Nº: Turma: INSTRUÇÕES GERAIS 1. Nenhum material deve estar embaixo das carteiras. Livros e mochilas devem ficar guardados no armário. 2. Sobre a mesa,
SÓLIDOS GEOMÉTRICOS. Materiais manipulativos para o ensino de COLEÇÃO MATHEMOTECA. ORGANIZADORAS Katia Stocco Smole Maria Ignez Diniz
 COLEÇÃO MATHEMOTECA ORGANIZADORAS Katia Stocco Smole Maria Ignez Diniz Anos iniciais do ensino fundamental Materiais manipulativos para o ensino de SÓLIDOS GEOMÉTRICOS ATIVIDADES 1. Faça as construções
COLEÇÃO MATHEMOTECA ORGANIZADORAS Katia Stocco Smole Maria Ignez Diniz Anos iniciais do ensino fundamental Materiais manipulativos para o ensino de SÓLIDOS GEOMÉTRICOS ATIVIDADES 1. Faça as construções
Escola Portuguesa do Lubango Hélder Giroto Paiva Processos e materias geológicos importantes em ambientes terrestres
 Escola Portuguesa do Lubango Hélder Giroto Paiva Processos e materias geológicos importantes em ambientes terrestres Conceito de Mineral 4 Mineral é uma substância sólida, homogénea, cristalina, de composição
Escola Portuguesa do Lubango Hélder Giroto Paiva Processos e materias geológicos importantes em ambientes terrestres Conceito de Mineral 4 Mineral é uma substância sólida, homogénea, cristalina, de composição
DEFINIÇÃO DE MINERAL. Fig. 1: ametista
 MINERALOGIA DEFINIÇÃO DE MINERAL Um mineral é uma substância sólida, natural e inorgânica, de estrutura cristalina e com composição química fixa ou variável dentro de limites bem definidos (exceto o mercúrio).
MINERALOGIA DEFINIÇÃO DE MINERAL Um mineral é uma substância sólida, natural e inorgânica, de estrutura cristalina e com composição química fixa ou variável dentro de limites bem definidos (exceto o mercúrio).
INSTRUMENTAL DE DESENHO TÉCNICO
 INSTRUMENTAL DE DESENHO TÉCNICO ADQUIRIR Lápis ou lapiseiras; Borracha; Jogo de Esquadros; Régua graduada Compasso; Gabaritos; Escalímetro; Prancheta; Régua paralela. Fita adesiva; LAPISEIRA Não necessita
INSTRUMENTAL DE DESENHO TÉCNICO ADQUIRIR Lápis ou lapiseiras; Borracha; Jogo de Esquadros; Régua graduada Compasso; Gabaritos; Escalímetro; Prancheta; Régua paralela. Fita adesiva; LAPISEIRA Não necessita
QUÍMICA GERAL. Aula 01 07/02/2013. Elementos, Substâncias e Misturas. Elementos, Substâncias e Misturas. Introdução. Elementos, Substâncias e Misturas
 QUÍMICA GERAL Aula 01 Elementos, Substâncias e 1 Introdução A matéria é formada por moléculas, que por sua vez são formadas por partículas minúsculas chamadas de átomos. Matéria Átomos Elementos Tabela
QUÍMICA GERAL Aula 01 Elementos, Substâncias e 1 Introdução A matéria é formada por moléculas, que por sua vez são formadas por partículas minúsculas chamadas de átomos. Matéria Átomos Elementos Tabela
Ciências. Química e Física. Escola Estadual de Ensino Médio Demétrio Ribeiro. Prof. Thales Fagundes Machado. 9º ano Ensino Fundamental
 Escola Estadual de Ensino Médio Demétrio Ribeiro Ciências Química e Física 9º ano Ensino Fundamental Prof. Thales Fagundes Machado [email protected] Alegrete RS 2015 03. Propriedades da matéria: Propriedades
Escola Estadual de Ensino Médio Demétrio Ribeiro Ciências Química e Física 9º ano Ensino Fundamental Prof. Thales Fagundes Machado [email protected] Alegrete RS 2015 03. Propriedades da matéria: Propriedades
Atomística: as origens do átomo
 9º ANO» UNIDADE 2» Atomística: as origens do átomo MATÉRIA PODE SER DEFINIDA COMO TUDO QUE TEM MASSA E OCUPA LUGAR NO ESPAÇO Matéria formada por átomos. Átomos formam as substâncias químicas. www.sejaetico.com.br
9º ANO» UNIDADE 2» Atomística: as origens do átomo MATÉRIA PODE SER DEFINIDA COMO TUDO QUE TEM MASSA E OCUPA LUGAR NO ESPAÇO Matéria formada por átomos. Átomos formam as substâncias químicas. www.sejaetico.com.br
Oficina: Propriedades dos materiais
 Oficina: Propriedades dos materiais Oficina de CN/EF Presencial e EAD Desde que acordamos até a hora que vamos dormir mexemos e utilizamos vários objetos para diferentes fins. Observe ao seu redor. Perceba
Oficina: Propriedades dos materiais Oficina de CN/EF Presencial e EAD Desde que acordamos até a hora que vamos dormir mexemos e utilizamos vários objetos para diferentes fins. Observe ao seu redor. Perceba
Sugestão: Use papel transparente para copiar as figuras e comparar os lados e os ângulos.
 Você se lembra dos triângulos e quadriláteros do final da Aula 28? Eles estão reproduzidos na figura abaixo. Observe que a forma de cada triângulo, por exemplo, varia conforme aumentamos ou diminuímos
Você se lembra dos triângulos e quadriláteros do final da Aula 28? Eles estão reproduzidos na figura abaixo. Observe que a forma de cada triângulo, por exemplo, varia conforme aumentamos ou diminuímos
A geologia é uma ciência que estuda a composição, estruturas e movimentos formadores da crosta terrestre. Esta subdivide-se em:
 Colégio Henrique Hennry Curso: Técnico de operações em Sistemas de petróleo Disciplina: Princípio de Geologia Introdução -1 A geologia é uma ciência que estuda a composição, estruturas e movimentos formadores
Colégio Henrique Hennry Curso: Técnico de operações em Sistemas de petróleo Disciplina: Princípio de Geologia Introdução -1 A geologia é uma ciência que estuda a composição, estruturas e movimentos formadores
Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! CIÊNCIAS - UNIDADE 3 ÁTOMOS E LIGAÇÕES QUÍMICAS
 Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! Use canetas coloridas ou escreva palavras destacadas, para facilitar na hora de estudar. E capriche! Não se esqueça
Lembrete: Antes de começar a copiar cada unidade, coloque o cabeçalho da escola e a data! Use canetas coloridas ou escreva palavras destacadas, para facilitar na hora de estudar. E capriche! Não se esqueça
Condutores e Isolantes Térmicos
 Condutores e Isolantes Térmicos O calor se transfere dos objetos mais quentes para os mais frios. Se vários objetos a temperaturas diferentes estão em contato, os que estão mais quentes acabarão esfriando
Condutores e Isolantes Térmicos O calor se transfere dos objetos mais quentes para os mais frios. Se vários objetos a temperaturas diferentes estão em contato, os que estão mais quentes acabarão esfriando
TRATAMENTO TÉRMICO PARTE 2
 TRATAMENTO TÉRMICO PARTE 2 Antes de falarmos sobre tratamento térmico, devemos conhecer estruturas cristalinas Estrutura Cristalina O que é uma Estrutura Cristalina? É a maneira segundo a qual os átomos,
TRATAMENTO TÉRMICO PARTE 2 Antes de falarmos sobre tratamento térmico, devemos conhecer estruturas cristalinas Estrutura Cristalina O que é uma Estrutura Cristalina? É a maneira segundo a qual os átomos,
B B C O A B 8 A C B. Sugestão: Use papel transparente para copiar as figuras e comparar os lados e os ângulos.
 Você se lembra dos triângulos e quadriláteros do final da Aula 28? Eles estão reproduzidos na figura abaixo. Observe que a forma de cada triângulo, por exemplo, varia conforme aumentamos ou diminuímos
Você se lembra dos triângulos e quadriláteros do final da Aula 28? Eles estão reproduzidos na figura abaixo. Observe que a forma de cada triângulo, por exemplo, varia conforme aumentamos ou diminuímos
TABELA PERIÓDICA PARTE 1
 PROJETO KAL - 2016 QUÍMCA AULA 06 TABELA PERÓDCA PARTE 1 Recordar é viver: Modelo Atômico de Rutherford-Bohr: Também conhecido como modelo atômico planetário, ele mostra como os elétrons se comportam ao
PROJETO KAL - 2016 QUÍMCA AULA 06 TABELA PERÓDCA PARTE 1 Recordar é viver: Modelo Atômico de Rutherford-Bohr: Também conhecido como modelo atômico planetário, ele mostra como os elétrons se comportam ao
Colégio Pedro II Campus São Cristóvão II Disciplina: Ciências 2º Trimestre/ 9º ano TABELA PERIÓDICA
 Colégio Pedro II Campus São Cristóvão II Disciplina: Ciências 2º Trimestre/ 9º ano TABELA PERIÓDICA Agosto/2017 OS ELEMENTOS QUÍMICOS Podemos definir um elemento químico como sendo o conjunto de átomos
Colégio Pedro II Campus São Cristóvão II Disciplina: Ciências 2º Trimestre/ 9º ano TABELA PERIÓDICA Agosto/2017 OS ELEMENTOS QUÍMICOS Podemos definir um elemento químico como sendo o conjunto de átomos
Formação e estrutura dos principais minerais
 Formação e estrutura dos principais minerais Cada tipo de mineral, constitui uma espécie mineral. Ex: quarzto (SiO 2 ). Sempre que sua cristalização se der em condições geológicas ideais, a sua organização
Formação e estrutura dos principais minerais Cada tipo de mineral, constitui uma espécie mineral. Ex: quarzto (SiO 2 ). Sempre que sua cristalização se der em condições geológicas ideais, a sua organização
Disciplina: Química Professor: Rubens Barreto. III Unidade
 Disciplina: Química Professor: Rubens Barreto III Unidade Ligações Químicas Ligações iônicas Tipos de Ligações Ligações covalentes Ligações metálicas Os gases nobres e a regra do octeto Todas as substâncias
Disciplina: Química Professor: Rubens Barreto III Unidade Ligações Químicas Ligações iônicas Tipos de Ligações Ligações covalentes Ligações metálicas Os gases nobres e a regra do octeto Todas as substâncias
26/08/15 SUBSTÂNCIAS E MISTURAS. Prof. Ms. Mayanderson (Xuxu)
 SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
Sulfureto (S2-) Catiões (alguns exemplos, raio dado em 10-8 cm) 1,81 1,84. 2) Semi-metais (Ar, arsénio, Bi, bismuto, Sb, antimónio) Grafite (C)
 Classificação Aniões (alguns exemplos) A classificação dos minerais baseia-se na sua composição química, nomeadamente no anião ou grupo aniónico dominante Óxido (O2-) o mais abundante! 1,40 Sulfureto (S2-)
Classificação Aniões (alguns exemplos) A classificação dos minerais baseia-se na sua composição química, nomeadamente no anião ou grupo aniónico dominante Óxido (O2-) o mais abundante! 1,40 Sulfureto (S2-)
COLÉGIO SHALOM 8 ANO Professora: Bethânia Rodrigues 65 Geometria. Aluno(a):. Nº.
 COLÉGIO SHALOM 8 ANO Professora: Bethânia Rodrigues 65 Geometria Aluno(a):. Nº. Trabalho De Recuperação final E a receita é uma só: fazer as pazes com você mesmo, diminuir a expectativa e entender que
COLÉGIO SHALOM 8 ANO Professora: Bethânia Rodrigues 65 Geometria Aluno(a):. Nº. Trabalho De Recuperação final E a receita é uma só: fazer as pazes com você mesmo, diminuir a expectativa e entender que
A importância dos minerais de argila: Estrutura e Características. Luiz Paulo Eng. Agrônomo
 A importância dos minerais de argila: Estrutura e Características Luiz Paulo Eng. Agrônomo Argilo-minerais O Quando se fala em minerais, normalmente vemnos à mente a imagem de substâncias sólidas, duras,
A importância dos minerais de argila: Estrutura e Características Luiz Paulo Eng. Agrônomo Argilo-minerais O Quando se fala em minerais, normalmente vemnos à mente a imagem de substâncias sólidas, duras,
Metais. informativo técnico
 Metais informativo técnico METAIS Móveis de metal são uma escolha de materiais para mobília, usados tanto em área interna quanto em área externa. A variedade de ligas metálicas existentes permite o uso
Metais informativo técnico METAIS Móveis de metal são uma escolha de materiais para mobília, usados tanto em área interna quanto em área externa. A variedade de ligas metálicas existentes permite o uso
Mat. Monitor: Roberta Teixeira
 Professor: Rafael Jesus Monitor: Roberta Teixeira Exercícios de revisão sobre geometria espacial 22 set EXERCÍCIOS DE AULA 1. Dois dados, com doze faces pentagonais cada um, têm a forma de dodecaedros
Professor: Rafael Jesus Monitor: Roberta Teixeira Exercícios de revisão sobre geometria espacial 22 set EXERCÍCIOS DE AULA 1. Dois dados, com doze faces pentagonais cada um, têm a forma de dodecaedros
Comunicações Ópticas. Profº: Cláudio Henrique Albuquerque Rodrigues, M. Sc.
 Comunicações Ópticas Profº: Cláudio Henrique Albuquerque Rodrigues, M. Sc. Corpos luminosos e Corpos iluminados O Sol, as estrelas, uma lâmpada ou uma vela, acesas, são objetos que emitem luz própria,
Comunicações Ópticas Profº: Cláudio Henrique Albuquerque Rodrigues, M. Sc. Corpos luminosos e Corpos iluminados O Sol, as estrelas, uma lâmpada ou uma vela, acesas, são objetos que emitem luz própria,
 10 11 Escola Municipal Francis Hime SÓLIDOS GEOMÉTRICOS 6º ANO Nome: 1601 Geometria: Uma ciência de muitos povos A geometria, assim como as ciências, nasceu das necessidades e das observações do homem.
10 11 Escola Municipal Francis Hime SÓLIDOS GEOMÉTRICOS 6º ANO Nome: 1601 Geometria: Uma ciência de muitos povos A geometria, assim como as ciências, nasceu das necessidades e das observações do homem.
Olimpíada Mineira de Química
 Olimpíada Mineira de Química O M Q 2 0 0 9 Nome: Escola: Instruções: 1 Esta prova contém 12 questões de múltipla escolha e duas questões abertas, abrangendo um total de 11 páginas. 2 Antes de iniciar a
Olimpíada Mineira de Química O M Q 2 0 0 9 Nome: Escola: Instruções: 1 Esta prova contém 12 questões de múltipla escolha e duas questões abertas, abrangendo um total de 11 páginas. 2 Antes de iniciar a
Se os tubos opostos forem de mesmo comprimento, teremos as várias possibilidades de paralelogramos, incluindo o retângulo.
 Ernesto Rosa Poliedros de canudinhos rígidos possuem muitas vantagens: são fáceis de se fazer com sucata como tubinhos de canetas, bambus etc. (mas no mercado há tubos plásticos à venda), são ótimos nas
Ernesto Rosa Poliedros de canudinhos rígidos possuem muitas vantagens: são fáceis de se fazer com sucata como tubinhos de canetas, bambus etc. (mas no mercado há tubos plásticos à venda), são ótimos nas
Homogêneo: algo que não pode ser fisicamente dividido em componentes químicos mais simples.
 MINERAIS HALITA Um mineral é um sólido, homogêneo, natural, com uma composição química definida e um arranjo atômico altamente ordenado. É geralmente formado por processos inorgânicos. Sólido: as substâncias
MINERAIS HALITA Um mineral é um sólido, homogêneo, natural, com uma composição química definida e um arranjo atômico altamente ordenado. É geralmente formado por processos inorgânicos. Sólido: as substâncias
COMO SÃO IDENTIFICADOS E CLASSIFICADOS OS MINERAIS?
 COMO SÃO IDENTIFICADOS E CLASSIFICADOS OS MINERAIS? Props mecânicas Props elétricas Cor, brilho, traço, luminescência, birrefringência etc... Props intrínsecas Condutividade, piezeletricidade, etc... Props
COMO SÃO IDENTIFICADOS E CLASSIFICADOS OS MINERAIS? Props mecânicas Props elétricas Cor, brilho, traço, luminescência, birrefringência etc... Props intrínsecas Condutividade, piezeletricidade, etc... Props
INSTRUÇÕES PARA TODOS OS MODELOS SÉRIE 866x / 876 x
 Produtos de Qualidade para a forma como você vive INSTRUÇÕES PARA TODOS OS MODELOS SÉRIE 866x / 876 x IMPORTANTE: GUARDAR PARA REFERÊNCIAS FUTURAS! Para obter dicas úteis e instruções, acesse nosso site:
Produtos de Qualidade para a forma como você vive INSTRUÇÕES PARA TODOS OS MODELOS SÉRIE 866x / 876 x IMPORTANTE: GUARDAR PARA REFERÊNCIAS FUTURAS! Para obter dicas úteis e instruções, acesse nosso site:
Ligações Químicas. Professor Haroldo
 Ligações Químicas Professor Haroldo 1. A regra do dueto e do octeto: Para se estabilizar um elemento precisa possuir sua camada de valência igual à camada de valência do GÁS NOBRE MAIS PRÓXIMO (8 e -,
Ligações Químicas Professor Haroldo 1. A regra do dueto e do octeto: Para se estabilizar um elemento precisa possuir sua camada de valência igual à camada de valência do GÁS NOBRE MAIS PRÓXIMO (8 e -,
2-) Descreva algumas das diferenças entre mistura de cores de luz e mistura de cores de tintas.
 Lista cores 1-) Três fontes de luz projetam luz sobre um anteparo como mostrado na figura ao lado. Cada fonte projeta uma região circular de cor diferente. A. Nomeie cada parte do anteparo com a cor apropriada.
Lista cores 1-) Três fontes de luz projetam luz sobre um anteparo como mostrado na figura ao lado. Cada fonte projeta uma região circular de cor diferente. A. Nomeie cada parte do anteparo com a cor apropriada.
Olimpíada Mineira. de Química. Tabela de Respostas das Questões 1 a a b c d
 Olimpíada Mineira Nome: Escola: Instruções: 1 Esta prova contém 12 questões de múltipla escolha e duas questões abertas, abrangendo um total de 11 páginas. 2 Antes de iniciar a prova, confira se todas
Olimpíada Mineira Nome: Escola: Instruções: 1 Esta prova contém 12 questões de múltipla escolha e duas questões abertas, abrangendo um total de 11 páginas. 2 Antes de iniciar a prova, confira se todas
ARRANJOS ATÔMICOS. Química Aplicada. Profº Vitor de Almeida Silva
 ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
GEOMETRIA ESPACIAL TETRAEDRO HEXAEDRO OCTAEDRO DODECAEDRO ICOSAEDRO REGULARES RETO POLIEDROS OBLÍQUO PRISMA REGULAR IRREGULARES RETA OBLÍQUA PIRÂMIDE
 GEOMETRIA ESPACIAL SÓLIDOS GEOMÉTRICOS POLIEDROS REGULARES SÓLIDOS DE REVOLUÇÃO IRREGULARES CONE TETRAEDRO HEXAEDRO OCTAEDRO DODECAEDRO ICOSAEDRO ESFERA CILINDRO PRISMA PIRÂMIDE RETO OBLÍQUO RETO RETO
GEOMETRIA ESPACIAL SÓLIDOS GEOMÉTRICOS POLIEDROS REGULARES SÓLIDOS DE REVOLUÇÃO IRREGULARES CONE TETRAEDRO HEXAEDRO OCTAEDRO DODECAEDRO ICOSAEDRO ESFERA CILINDRO PRISMA PIRÂMIDE RETO OBLÍQUO RETO RETO
PRINCÍPIOS DA ÓPTICA. Professor Paulo Christakis, M.Sc. 10/10/2016 1
 PRINCÍPIOS DA ÓPTICA 10/10/2016 1 O QUE É A LUZ? A luz é uma forma de energia que não necessita de um meio material para se propagar. A luz do Sol percorre a distância de 150 milhões de quilômetros com
PRINCÍPIOS DA ÓPTICA 10/10/2016 1 O QUE É A LUZ? A luz é uma forma de energia que não necessita de um meio material para se propagar. A luz do Sol percorre a distância de 150 milhões de quilômetros com
Ano / Turma: Data: / / Classificação: Observações: Espaço do aluno
 Es c o la Bá s i c a d o s 2 º e 3 º c i c lo s d e S an t o An t ó n i o Ficha de Avaliação Sumativa M a t e m á t i c a Nome: N.º Professor: Ano / Turma: Data: / / Classificação: Observações: A MINHA
Es c o la Bá s i c a d o s 2 º e 3 º c i c lo s d e S an t o An t ó n i o Ficha de Avaliação Sumativa M a t e m á t i c a Nome: N.º Professor: Ano / Turma: Data: / / Classificação: Observações: A MINHA
Minerais e Rochas. Obsidiana (fonte: c_minerals) Carvão (fonte:
 Mineral É um elemento ou composto químico, via de regra resultante de processos inorgânicos, de composição química geralmente definida e encontrado naturalmente na crosta terrestre. (Leinz & Amaral, 1978).
Mineral É um elemento ou composto químico, via de regra resultante de processos inorgânicos, de composição química geralmente definida e encontrado naturalmente na crosta terrestre. (Leinz & Amaral, 1978).
Fundamentos de mineralogia e o ciclo de geração das rochas
 UNIVERSIDADE FEDERAL DO PAMPA Fundamentos de mineralogia e o ciclo de geração das rochas Prof. Paulo Jorge de Pinho Itaqui, março de 2017 Generalidades Crosta terrestre composta por ROCHAS compostas por
UNIVERSIDADE FEDERAL DO PAMPA Fundamentos de mineralogia e o ciclo de geração das rochas Prof. Paulo Jorge de Pinho Itaqui, março de 2017 Generalidades Crosta terrestre composta por ROCHAS compostas por
Aula 31.1 Conteúdo: Fundamentos da Geometria: Ponto, Reta e Plano. FORTALECENDO SABERES CONTEÚDO E HABILIDADES DINÂMICA LOCAL INTERATIVA MATEMÁTICA
 CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA Aula 31.1 Conteúdo: Fundamentos da Geometria: Ponto, Reta e Plano. 2 CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA Habilidades: Identificar
CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA Aula 31.1 Conteúdo: Fundamentos da Geometria: Ponto, Reta e Plano. 2 CONTEÚDO E HABILIDADES FORTALECENDO SABERES DESAFIO DO DIA Habilidades: Identificar
2.1 Princípios gerais da ligação química. Ligações químicas
 2.1 Princípios gerais da ligação química Ligações químicas A associação de átomos formando moléculas, ou em agregados de maiores dimensões como, por exemplo, nos metais, é possível pelo estabelecimento
2.1 Princípios gerais da ligação química Ligações químicas A associação de átomos formando moléculas, ou em agregados de maiores dimensões como, por exemplo, nos metais, é possível pelo estabelecimento
AULA PRÁTICA DE QUÍMICA GERAL Estudando a água parte 37 Comparando os calores específicos da água e da areia
 AULA PRÁTICA DE QUÍMICA GERAL Estudando a água parte 37 Comparando os calores específicos da água e da areia 9º NO DO ENSINO FUNDAMENTAL - 1º ANO DO ENSINO MÉDIO INTRODUÇÃO Uma das propriedades mais importantes
AULA PRÁTICA DE QUÍMICA GERAL Estudando a água parte 37 Comparando os calores específicos da água e da areia 9º NO DO ENSINO FUNDAMENTAL - 1º ANO DO ENSINO MÉDIO INTRODUÇÃO Uma das propriedades mais importantes
A Natureza Elétrica dos Materiais
 A Natureza Elétrica dos Materiais As primeiras ideias sobre a constituição da matéria Demócrito Gregos ÁTOMOS - A matéria possuia espaço vazio; - Indestrutíveis; - Dotadas de movimento; - Diversos formatos.
A Natureza Elétrica dos Materiais As primeiras ideias sobre a constituição da matéria Demócrito Gregos ÁTOMOS - A matéria possuia espaço vazio; - Indestrutíveis; - Dotadas de movimento; - Diversos formatos.
Aula 5: Propriedades e Ligação Química
 Aula 5: Propriedades e Ligação Química Relacionar o tipo de ligação química com as propriedades dos materiais Um entendimento de muitas propriedades físicas dos materiais é previsto através do conhecimento
Aula 5: Propriedades e Ligação Química Relacionar o tipo de ligação química com as propriedades dos materiais Um entendimento de muitas propriedades físicas dos materiais é previsto através do conhecimento
2 CILINDRO E ESFERA 1 CUBO E ESFERA. 2.1 Cilindro inscrito. 1.1 Cubo inscrito. 2.2 Cilindro circunscrito. 1.2 Cubo circunscrito
 Matemática Pedro Paulo GEOMETRIA ESPACIAL XI A seguir, nós vamos analisar a relação entre alguns sólidos e as esferas. Os sólidos podem estar inscritos ou circunscritos a uma esfera. Lembrando: A figura
Matemática Pedro Paulo GEOMETRIA ESPACIAL XI A seguir, nós vamos analisar a relação entre alguns sólidos e as esferas. Os sólidos podem estar inscritos ou circunscritos a uma esfera. Lembrando: A figura
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final 3ª Etapa 2014 Disciplina: Matemática Série: 2ª Professor (a): Ana Cristina Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final 3ª Etapa 2014 Disciplina: Matemática Série: 2ª Professor (a): Ana Cristina Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
CAPÍTULO 2 MINERAIS 1) CONCEITO
 CAPÍTULO 2 MINERAIS 1) CONCEITO Os minerais são os elementos constituintes das rochas, logo o conhecimento dos minerais implica no conhecimento das rochas. Mineral é toda substância formada por processos
CAPÍTULO 2 MINERAIS 1) CONCEITO Os minerais são os elementos constituintes das rochas, logo o conhecimento dos minerais implica no conhecimento das rochas. Mineral é toda substância formada por processos
Prof. Márcio Nascimento. 1 de abril de 2015
 Geometria dos Sólidos Prof. Márcio Nascimento [email protected] Universidade Estadual Vale do Acaraú Centro de Ciências Exatas e Tecnologia Curso de Licenciatura em Matemática Disciplina: Geometria
Geometria dos Sólidos Prof. Márcio Nascimento [email protected] Universidade Estadual Vale do Acaraú Centro de Ciências Exatas e Tecnologia Curso de Licenciatura em Matemática Disciplina: Geometria
Nome: Nº Ano: Turma: Disciplina: Professor: Data: / / GABARITO - LISTA DE REFORÇO MATEMÁTICA 2 0 ANO EF
 Nome: Nº Ano: Turma: Disciplina: Professor: Data: / / GABARITO - LISTA DE REFORÇO MATEMÁTICA 2 0 ANO EF 01) Observando a figuras e simplesmente contando, determine o número de faces, arestas e o vértices
Nome: Nº Ano: Turma: Disciplina: Professor: Data: / / GABARITO - LISTA DE REFORÇO MATEMÁTICA 2 0 ANO EF 01) Observando a figuras e simplesmente contando, determine o número de faces, arestas e o vértices
PROCESSO DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO FÍSICA E QUÍMICA DE MATERIAIS 2 SEMESTRE DE 2016 UNIVERSIDADE FEDERAL DE SÃO JOÃO DEL REI
 PROCESSO DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO FÍSICA E QUÍMICA DE MATERIAIS 2 SEMESTRE DE 2016 UNIVERSIDADE FEDERAL DE SÃO JOÃO DEL REI ÁREA DE CONCENTRAÇÃO: FÍSICA E QUÍMICA DE MATERIAIS NÍVEL:
PROCESSO DE SELEÇÃO PARA O PROGRAMA DE PÓS-GRADUAÇÃO FÍSICA E QUÍMICA DE MATERIAIS 2 SEMESTRE DE 2016 UNIVERSIDADE FEDERAL DE SÃO JOÃO DEL REI ÁREA DE CONCENTRAÇÃO: FÍSICA E QUÍMICA DE MATERIAIS NÍVEL:
Ocorrem ligações químicas quando os átomos se unem e se ligam quimicamente, formando assim as moléculas. Observe: H 2
 Introdução Ocorrem ligações químicas quando os átomos se unem e se ligam quimicamente, formando assim as moléculas. Observe: H 2 Essas moléculas se classificam em substâncias simples e substâncias compostas.
Introdução Ocorrem ligações químicas quando os átomos se unem e se ligam quimicamente, formando assim as moléculas. Observe: H 2 Essas moléculas se classificam em substâncias simples e substâncias compostas.
Dureza Brinell. Entretanto, a dureza de um material é um conceito relativamente complexo de definir, originando diversas interpretações.
 A UU L AL A Dureza Brinell Ao escrever a lápis ou lapiseira, você sente com facilidade a diferença entre uma grafite macia, que desliza suavemente sobre o papel, e uma grafite dura, que deixa o papel marcado.
A UU L AL A Dureza Brinell Ao escrever a lápis ou lapiseira, você sente com facilidade a diferença entre uma grafite macia, que desliza suavemente sobre o papel, e uma grafite dura, que deixa o papel marcado.
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
Ciências dos materiais- 232
 1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
COLÉGIO 7 DE SETEMBRO
 6 o Ensino Fundamental COLÉGIO 7 DE SETEMBRO FUNDADOR PROF. EDILSON BRASIL SOÁREZ O Colégio que ensina o aluno a estudar TD As Rochas Central de Atendimento: 4006.7777 ALUNO(A): N o TURMA: PROFESSORES:
6 o Ensino Fundamental COLÉGIO 7 DE SETEMBRO FUNDADOR PROF. EDILSON BRASIL SOÁREZ O Colégio que ensina o aluno a estudar TD As Rochas Central de Atendimento: 4006.7777 ALUNO(A): N o TURMA: PROFESSORES:
APOSTILA DE QUÍMICA 2º BIMESTRE
 Nome: nº: Bimestre: 2º Ano/série: 9º ano Ensino: Fundamental Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA 2º BIMESTRE TEORIA 1 EVOLUÇÃO DOS MODELOS ATÔMICOS 1.
Nome: nº: Bimestre: 2º Ano/série: 9º ano Ensino: Fundamental Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA 2º BIMESTRE TEORIA 1 EVOLUÇÃO DOS MODELOS ATÔMICOS 1.
ESTADO SÓLIDO. paginapessoal.utfpr.edu.br/lorainejacobs. Profª. Loraine Jacobs
 ESTADO SÓLIDO [email protected] paginapessoal.utfpr.edu.br/lorainejacobs Profª. Loraine Jacobs Estado Sólido Tradicionalmente, um sólido é definido como uma substância que mantém um volume e uma
ESTADO SÓLIDO [email protected] paginapessoal.utfpr.edu.br/lorainejacobs Profª. Loraine Jacobs Estado Sólido Tradicionalmente, um sólido é definido como uma substância que mantém um volume e uma
Introdução à Nanotecnologia
 Introdução à Nanotecnologia Ele 1060 Aula 3 2010-01 Fundamentos Vamos começar pelo mundo macro. Como são classificados os Metais; materiais sólidos? Cerâmicos; Polímeros; Compósitos. Metais Elementos metálicos
Introdução à Nanotecnologia Ele 1060 Aula 3 2010-01 Fundamentos Vamos começar pelo mundo macro. Como são classificados os Metais; materiais sólidos? Cerâmicos; Polímeros; Compósitos. Metais Elementos metálicos
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ANO. 1- Considere as temperaturas de fusão e ebulição (pressão = 1 atm) de quatro compostos dados na tabela abaixo.
 EXERCÍCIOS DE CIÊNCIAS PARA O 9 ANO 1- Considere as temperaturas de fusão e ebulição (pressão = 1 atm) de quatro compostos dados na tabela abaixo. Com base nos dados da tabela, responda as questões a seguir.
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ANO 1- Considere as temperaturas de fusão e ebulição (pressão = 1 atm) de quatro compostos dados na tabela abaixo. Com base nos dados da tabela, responda as questões a seguir.
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
Capítulo 3 - MINERAIS
 Capítulo 3 - MINERAIS CONCEITOS MINERAL é toda substância homogênea, sólida ou líquida, de origem inorgânica que surge naturalmente na crosta terrestre. Normalmente com composição química definida e, se
Capítulo 3 - MINERAIS CONCEITOS MINERAL é toda substância homogênea, sólida ou líquida, de origem inorgânica que surge naturalmente na crosta terrestre. Normalmente com composição química definida e, se
QUÍMICA A Ciênca Central 9ª Edição
 QUÍMICA A Ciênca Central 9ª Edição Capítulo 2 átomos, moléculas e íons David P. White Teoria atômica da matéria John Dalton (1803 1807): Cada elemento é composto de átomos. Todos os átomos de um elemento
QUÍMICA A Ciênca Central 9ª Edição Capítulo 2 átomos, moléculas e íons David P. White Teoria atômica da matéria John Dalton (1803 1807): Cada elemento é composto de átomos. Todos os átomos de um elemento
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA INTENSIVA
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA INTENSIVA 01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA INTENSIVA 01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando
QUÍMICA. Transformações Químicas. Elementos Químicos, Tabela Periódica e Reações Químicas Parte 3. Prof ª. Giselle Blois
 QUÍMICA Transformações Químicas Elementos Químicos, Tabela Periódica e Reações Químicas Parte 3 Prof ª. Giselle Blois Resumindo: Os elementos químicos são representados por símbolos gráficos oriundos de
QUÍMICA Transformações Químicas Elementos Químicos, Tabela Periódica e Reações Químicas Parte 3 Prof ª. Giselle Blois Resumindo: Os elementos químicos são representados por símbolos gráficos oriundos de
OBJETIVOS MÉTODO EXPERIMENTAL
 OBJETIVOS Mostrar que há dois tipos de carga elétrica. Estudar qualitativamente as forças que atuam entre corpos carregados. Mostrar que as forças entre corpos carregados podem ser entendidas em termos
OBJETIVOS Mostrar que há dois tipos de carga elétrica. Estudar qualitativamente as forças que atuam entre corpos carregados. Mostrar que as forças entre corpos carregados podem ser entendidas em termos
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA FMJ
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA FMJ 03. Item C O equador da figura mostrada pode ser representado como abaixo. 01. Item B I Correto. A energia para quebrar a ligação H F (568 kj/mol) é
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 02 TURMA FMJ 03. Item C O equador da figura mostrada pode ser representado como abaixo. 01. Item B I Correto. A energia para quebrar a ligação H F (568 kj/mol) é
Física dos Materiais
 4300502 1º Semestre de 2014 Instituto de Física Universidade de São Paulo Professor: Luiz C C M Nagamine E-mail: [email protected] Fone: 3091.6877 homepage: http://disciplinas.stoa.usp.br/course/view.php?id=10070
4300502 1º Semestre de 2014 Instituto de Física Universidade de São Paulo Professor: Luiz C C M Nagamine E-mail: [email protected] Fone: 3091.6877 homepage: http://disciplinas.stoa.usp.br/course/view.php?id=10070
a) 1m. b) 0,5 m. c) 0,6 m. d) 0,314 m. e) 0,628 m. que S pertence à reta determinada por A e E e que AE 2cm, AD 4cm e AB 5cm. sólido seja igual a 4 3
 Lista 06 Matemática Geometria Espacial 1. (Fuvest 015) A grafite de um lápis tem quinze centímetros de comprimento e dois milímetros de espessura. Dentre os valores abaixo, o que mais se aproxima do número
Lista 06 Matemática Geometria Espacial 1. (Fuvest 015) A grafite de um lápis tem quinze centímetros de comprimento e dois milímetros de espessura. Dentre os valores abaixo, o que mais se aproxima do número
ÓPTICA GEOMÉTRICA: Parte da Física que descreve fenômenos luminosos a partir da noção de raio de luz, alguns princípios fundamentais e Geometria.
 ÓPTICA Introdução ÓPTICA GEOMÉTRICA: Parte da Física que descreve fenômenos luminosos a partir da noção de raio de luz, alguns princípios fundamentais e Geometria. LUZ: Dependendo do fenômeno estudado
ÓPTICA Introdução ÓPTICA GEOMÉTRICA: Parte da Física que descreve fenômenos luminosos a partir da noção de raio de luz, alguns princípios fundamentais e Geometria. LUZ: Dependendo do fenômeno estudado
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica
 Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
Palitos - 5 a série Actividade:
 Palitos - 5 a série Actividade: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Disponha sete palitos da seguinte forma. 1 Agora, acrescente seis palitos e obtenha o número 1 000. Utilizando 11 palitos, monte uma
Palitos - 5 a série Actividade: 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 Disponha sete palitos da seguinte forma. 1 Agora, acrescente seis palitos e obtenha o número 1 000. Utilizando 11 palitos, monte uma
Introdução à Óptica Geométrica
 Introdução à Óptica Geométrica ÓPTICA GEOMÉTRICA: Parte da Física que descreve fenômenos luminosos a partir da noção de raio de luz, alguns princípios fundamentais e Geometria. LUZ: Dependendo do fenômeno
Introdução à Óptica Geométrica ÓPTICA GEOMÉTRICA: Parte da Física que descreve fenômenos luminosos a partir da noção de raio de luz, alguns princípios fundamentais e Geometria. LUZ: Dependendo do fenômeno
PUC Goiás MAF Coordenação de Química Lista de exercícios transformações Químicas Profa Sandra R. Longhin Goiânia. 05 de abril de 2011
 1 PUC Goiás MAF Coordenação de Química Lista de exercícios transformações Químicas Profa Sandra R. Longhin Goiânia. 05 de abril de 2011 01. A temperatura de ebulição é, entre outras, uma propriedade das
1 PUC Goiás MAF Coordenação de Química Lista de exercícios transformações Químicas Profa Sandra R. Longhin Goiânia. 05 de abril de 2011 01. A temperatura de ebulição é, entre outras, uma propriedade das
LISTA B QUÍMICA TONI ATITUDE
 LISTA B QUÍMICA TONI ATITUDE Site: www.sosprofessor.xpg.com.br Lei da conservação (lei de Lavoisier)= em um sistema fechado a massa total não varia Lei da proporção constante (lei de Proust)= os elementos
LISTA B QUÍMICA TONI ATITUDE Site: www.sosprofessor.xpg.com.br Lei da conservação (lei de Lavoisier)= em um sistema fechado a massa total não varia Lei da proporção constante (lei de Proust)= os elementos
Lista de exercícios e Interpretação de texto 5o ano de 09 a 13/05/16
 Lista de exercícios e Interpretação de texto 5o ano de 09 a 13/05/16 Crê no Senhor Jesus e serás salvo tu e a tua casa. (Atos 16:31 b) RETAS PARALELAS E RETAS CONCORRENTES SEGUNDA-FEIRA 09/05 TERÇA-FEIRA
Lista de exercícios e Interpretação de texto 5o ano de 09 a 13/05/16 Crê no Senhor Jesus e serás salvo tu e a tua casa. (Atos 16:31 b) RETAS PARALELAS E RETAS CONCORRENTES SEGUNDA-FEIRA 09/05 TERÇA-FEIRA
