CLEXANE enoxaparina sódica
|
|
|
- Sandra Custódio Silva
- 8 Há anos
- Visualizações:
Transcrição
1 MODELO DE BULA Esta bula sofreu aumento de tamanho para adequação à legislação vigente da ANVISA. Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. CLEXANE enoxaparina sódica APRESENTAÇÕES - Solução injetável 20 mg/0,2 ml: embalagem com 2 e 10 seringas pré-enchidas com sistema de segurança. - Solução injetável 40 mg/0,4 ml: embalagem com 2 e 10 seringas pré-enchidas com sistema de segurança. - Solução injetável 60 mg/0,6 ml: embalagem com 2 seringas pré-enchidas graduadas com sistema de segurança. - Solução injetável 80 mg/0,8 ml: embalagem com 2 seringas pré-enchidas graduadas com sistema de segurança. - Solução injetável 100 mg/1,0 ml: embalagem com 2 seringas pré-enchidas graduadas com sistema de segurança. USO SUBCUTÂNEO OU INTRAVENOSO (a via de administração varia de acordo com a indicação do produto). USO ADULTO. COMPOSIÇÃO Cada seringa pré-enchida de CLEXANE contém: Apresentação 20 mg 40 mg 60 mg 80 mg 100 mg enoxaparina sódica 20,0 mg 40,0 mg 60,0 mg 80,0 mg 100,0 mg água para injetáveis q.s.p. 0,2 ml 0,4 ml 0,6 ml 0,8 ml 1,0 ml INFORMAÇÕES AO PACIENTE 1. PARA QUE ESTE MEDICAMENTO É INDICADO? Este medicamento é destinado para: - tratamento da trombose venosa profunda (formação ou presença de um coágulo sanguíneo dentro de um vaso) com ou sem embolia pulmonar (presença de um coágulo em uma artéria do pulmão); - tratamento da angina instável (dor no peito) e infarto do miocárdio sem onda Q, administrado concomitantemente ao ácido acetilsalicílico; - tratamento de infarto agudo do miocárdio (infarto do coração) com elevação do segmento ST, incluindo pacientes a serem tratados clinicamente ou com subsequente intervenção coronariana percutânea (cateterismo cardíaco);
2 - profilaxia do tromboembolismo venoso (prevenção da obstrução de um vaso sanguíneo por um coágulo de sangue na corrente sanguínea), em particular aqueles associados à cirurgia ortopédica ou à cirurgia geral; - profilaxia do tromboembolismo venoso em pacientes acamados devido a doenças agudas incluindo insuficiência cardíaca (alteração na função do coração), falência respiratória, infecções severas e doenças reumáticas (doenças inflamatórias e degenerativas que afetam as articulações e estruturas vizinhas); - prevenção da formação de trombo no circuito de circulação extracorpórea durante a hemodiálise (método artificial para filtrar o sangue). 2. COMO ESTE MEDICAMENTO FUNCIONA? CLEXANE diminui o risco de desenvolvimento de uma trombose venosa profunda e sua consequência mais grave, a embolia pulmonar. CLEXANE previne e trata estas duas patologias, evitando sua progressão ou recorrência, além de tratar angina instável e o infarto do miocárdio. CLEXANE também evita a coagulação do sangue no circuito de hemodiálise. A duração do tratamento com CLEXANE pode variar de um indivíduo para o outro. A atividade anti-xa (antitrombótica) média no sangue é observada 3 a 5 horas após a administração subcutânea. 3. QUANDO NÃO DEVO USAR ESTE MEDICAMENTO? CLEXANE não deve ser utilizado nos seguintes casos: - hipersensibilidade (alergia) à enoxaparina sódica, à heparina e seus derivados, inclusive outras heparinas de baixo peso molecular; - hemorragias ativas de grande porte e condições com alto risco de desenvolvimento de hemorragia incontrolável, incluindo acidente vascular cerebral hemorrágico (derrame cerebral) recente. 4. O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO? ADVERTÊNCIAS E PRECAUÇÕES CLEXANE não deve ser administrado por via intramuscular. Hemorragia (sangramento) Assim como com outros anticoagulantes, pode ocorrer sangramento em qualquer local (vide Quais os males que este medicamento pode me causar? ). Se ocorrer sangramento, a origem da hemorragia deve ser investigada e tratamento apropriado deve ser instituído. CLEXANE, assim como qualquer outra terapia anticoagulante, deve ser utilizada com cautela em condições com alto risco de hemorragia, tais como: - alterações na hemostasia (alteração nos mecanismos que controlam a formação e a dissolução de coágulos); - histórico de úlcera péptica (úlcera no estômago); - derrame cerebral recente; - hipertensão arterial (pressão alta) severa não controlada; - retinopatia diabética (lesão na retina causada pelas complicações do diabetes mellitus); - neurocirurgia ou cirurgia oftálmica (no olho) recente; - uso concomitante de medicamentos que afetem a hemostasia (vide Interações Medicamentosas ). Monitoramento da contagem de plaquetas (elemento do sangue que participa da coagulação sanguínea) 2
3 O risco de trombocitopenia (diminuição no número de plaquetas) induzida por heparina também existe com heparinas de baixo peso molecular. Pode ocorrer trombocitopenia (diminuição no número de plaquetas sanguíneas), geralmente entre o 5º e 21º dia após o início do tratamento com CLEXANE. Portanto, recomenda-se a realização de contagem plaquetária antes do início e regularmente durante o tratamento com CLEXANE. Na prática, em caso de confirmação de diminuição significativa da contagem plaquetária (30 a 50% do valor inicial), o tratamento com CLEXANE deve ser imediatamente interrompido e substituído por outra terapia. Advertências Gerais As heparinas de baixo peso molecular (HBPM) não devem ser intercambiáveis, pois existem diferenças entre elas quanto ao processo de fabricação, peso molecular, atividade anti-xa específica, unidade e dosagem. Isto ocasiona diferenças em suas atividades farmacocinéticas e biológicas associadas (por exemplo, a atividade antitrombina e a interação com as plaquetas). Portanto, é necessário obedecer às instruções de uso de cada medicamento. Anestesia espinhal/peridural Assim como com outros anticoagulantes, foram relatados casos de hematoma intraespinhal (acúmulo de sangue devido ao rompimento de vasos sanguíneos dentro da coluna espinhal) com o uso concomitante de enoxaparina sódica e anestesia espinhal/peridural, que podem resultar em paralisia prolongada ou permanente. Estes eventos são raros com a administração de doses iguais ou inferiores a 40 mg/dia de CLEXANE. O risco destes eventos pode ser aumentado com administração de doses maiores de CLEXANE, uso de cateter epidural no pós-operatório ou em caso de administração concomitante de medicamentos que alteram a hemostasia, tais como anti-inflamatórios não esteroidais (vide Interações Medicamentosas ). O risco parece também ser aumentado por traumatismo ou punções espinhais (na espinha) repetidas ou em pacientes com histórico de cirurgia ou deformidade espinhal. Para reduzir o risco potencial de sangramento associado ao uso concomitante de CLEXANE e anestesia/analgesia peridural ou espinhal, deve-se considerar o perfil farmacocinético do fármaco. A introdução e remoção do cateter devem ser realizadas quando o efeito anticoagulante de CLEXANE estiver baixo. A introdução ou remoção do cateter deve ser postergada para horas após a administração de CLEXANE na profilaxia da trombose venosa profunda, enquanto que em pacientes recebendo doses maiores de CLEXANE (1 mg/kg duas vezes ao dia ou 1,5 mg/kg uma vez ao dia), será necessário maior postergação (24 horas). A dose subsequente de CLEXANE deve ser administrada no mínimo 2 horas após a remoção do cateter. Caso o médico decida administrar anticoagulantes durante o uso de anestesia peridural/espinhal, deve-se empregar extrema cautela e monitoramento frequente para detectar qualquer sinal ou sintoma de lesão neurológica, tais como, dor na região lombar, deficiências sensoriais e motoras (dormência ou fraqueza dos membros inferiores), alterações intestinais e/ou urinárias. Você deve informar imediatamente a seu médico caso apresentem qualquer sintoma ou sinal descrito acima. Em caso de suspeita de sinais ou sintomas de hematoma intraespinhal, devem ser efetuados o diagnóstico e tratamento, incluindo descompressão da medula espinhal, com urgência. Trombocitopenia induzida pela heparina CLEXANE deve ser utilizado com extrema cautela em pacientes com histórico de trombocitopenia induzida pela heparina, com ou sem trombose. O risco de trombocitopenia induzida por heparina pode persistir por vários anos. Em caso de suspeita de histórico de trombocitopenia induzida por heparina, os testes de agregação plaquetária in vitro têm valor preditivo limitado. A decisão do uso de CLEXANE em tais casos deve ser tomada somente por um especialista. 3
4 Procedimentos de revascularização coronária percutânea Para minimizar o risco de sangramento após a instrumentação vascular durante o tratamento da angina instável e do infarto do miocárdio, deve-se respeitar precisamente os intervalos entre as doses recomendadas de CLEXANE. É importante estabelecer a hemostasia no local da punção após a intervenção coronariana percutânea. Caso tenha sido utilizado um dispositivo de fechamento, a bainha de acesso vascular pode ser removida imediatamente. Caso tenha sido utilizado um método de compressão manual, a bainha deve ser removida 6 horas após a última administração intravenosa ou subcutânea de CLEXANE. Se o tratamento com CLEXANE continuar, a próxima dose programada de CLEXANE não deve ser administrada antes de 6 a 8 horas após a remoção da bainha. Deve-se ter atenção especial ao local do procedimento para detecção de sinais de sangramento ou formação de hematoma. Gravidez e lactação Estudos em animais não demonstraram qualquer evidência de fetotoxicidade ou teratogenicidade (capacidade de produzir dano ao embrião ou feto durante a gravidez).. Em ratas prenhes, a passagem de 35 S-enoxaparina sódica através da placenta é mínima. Em humanos, não existe evidência da passagem da enoxaparina sódica através da placenta durante o segundo trimestre da gravidez. Ainda não existem informações disponíveis a este respeito durante o primeiro e terceiro trimestres da gravidez. Como não foram realizados estudos adequados e bem controlados em gestantes e uma vez que os estudos realizados em animais nem sempre são bons indicativos da resposta humana, deve-se utilizar CLEXANE durante a gravidez somente se o médico considerar como estritamente necessário. Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Em ratas lactantes, a concentração de 35 S-enoxaparina sódica ou de seus metabólitos marcados no leite é muito baixa. Não se sabe se a enoxaparina sódica inalterada é excretada no leite humano. A absorção oral da enoxaparina sódica é improvável, porém, como precaução, não se deve amamentar durante o tratamento com CLEXANE. Gestantes com próteses mecânicas valvulares cardíacas Não foram realizados estudos adequados para avaliar a utilização de CLEXANE na tromboprofilaxia (prevenção na formação de coágulos) em gestantes com próteses mecânicas valvulares cardíacas. Em um estudo clínico em gestantes com próteses mecânicas valvulares cardíacas, administrou-se enoxaparina (1 mg/kg duas vezes ao dia) para redução do risco de tromboembolismo, 2 de 8 gestantes desenvolveram coágulos resultando em bloqueio da válvula, resultando em óbitos materno e fetal. Houve relatos isolados pós-comercialização de trombose em gestantes com próteses mecânicas valvulares cardíacas enquanto eram medicadas com enoxaparina para tromboprofilaxia. Gestantes com próteses mecânicas valvulares cardíacas podem apresentar maior risco de tromboembolismo (obstrução de um vaso sanguíneo por um coágulo de sangue na corrente sanguínea) (vide Advertências e Precauções - Próteses mecânicas valvulares cardíacas ). Populações especiais Pacientes idosos: não foi observado aumento na tendência de hemorragia em idosos com doses profiláticas. Porém, pacientes idosos (especialmente pacientes com idade igual ou maior a 80 anos) podem ter um aumento no risco de complicações hemorrágicas com doses terapêuticas. Portanto, aconselha-se um monitoramento clínico cuidadoso (vide Como devo usar este medicamento ). Pacientes idosos podem apresentar retardo na eliminação de CLEXANE (vide Como devo usar este medicamento ). 4
5 Crianças: a segurança e eficácia de CLEXANE em crianças ainda não foram estabelecidas. Próteses mecânicas valvulares cardíacas: o uso de CLEXANE não foi adequadamente estudado para casos de tromboprofilaxia em pacientes com próteses mecânicas valvulares cardíacas. Foram relatados casos isolados de trombose com próteses valvulares cardíacas em pacientes com próteses mecânicas valvulares que receberam CLEXANE para tromboprofilaxia. A avaliação destes casos é limitada devido aos fatores causais serem confusos, incluindo doenças anteriores e dados clínicos insuficientes. Alguns destes casos foram em gestantes nas quais a trombose resultou em óbitos materno e fetal. Gestantes com próteses mecânicas valvulares cardíacas podem apresentar maior risco para tromboembolismo (vide Advertências e Precauções - Gestantes com próteses mecânicas valvulares cardíacas ). Insuficiência renal (nos rins): em pacientes com insuficiência renal, existe aumento da exposição ao CLEXANE, aumentando também o risco de hemorragia. Como a exposição ao CLEXANE aumenta significativamente em pacientes com insuficiência renal severa (clearance de creatinina < 30 ml/min), o ajuste posológico é recomendado para dosagens terapêuticas e profiláticas. Embora não seja recomendado ajuste posológico em pacientes com insuficiência renal moderada (clearance de creatinina ml/min) e leve (clearance de creatinina ml/min), é aconselhável realizar um monitoramento clínico cuidadoso (vide Como devo usar este medicamento ). Peso baixo: um aumento na exposição ao CLEXANE em doses profiláticas (não ajustadas ao peso) tem sido observado em mulheres e homens com baixo peso (< 45 kg e < 57 kg, respectivamente), que pode resultar em maior risco de hemorragia. Portanto, é aconselhável realizar um monitoramento clínico cuidadoso nestes pacientes. Alterações na capacidade de dirigir veículos e operar máquinas A utilização de CLEXANE não afeta a habilidade de dirigir ou operar máquinas. INTERAÇÕES MEDICAMENTOSAS - medicamento-medicamento Recomenda-se a interrupção do uso de medicamentos que afetam a hemostasia antes do início do tratamento com CLEXANE, a menos que seu uso seja estritamente indicado. Converse com seu médico caso esteja utilizando os medicamentos abaixo: salicilatos sistêmicos, ácido acetilsalicílico e outros anti-inflamatórios não-esteroidais (AINEs), incluindo o cetorolaco; dextrana 40, ticlopidina e clopidogrel; glicocorticoides sistêmicos; agentes trombolíticos e anticoagulantes; outros agentes antiplaquetários, incluindo os antagonistas de glicoproteína IIb/IIIa. Em caso de indicação do uso de qualquer uma destas associações, deve-se utilizar CLEXANE sob cuidadoso monitoramento clínico e laboratorial quando apropriado. - medicamento-exame laboratorial Nas doses utilizadas na profilaxia do tromboembolismo venoso, CLEXANE não influencia significativamente o tempo de sangramento e os testes de coagulação global, nem afeta a agregação plaquetária (união de plaquetas) ou a ligação do fibrinogênio (proteína do sangue relacionada à coagulação sanguínea) às plaquetas. Pode ocorrer aumento do tempo de tromboplastina parcial ativada (TTPa) e do tempo de coagulação ativada (TCA) (exames laboratoriais que avaliam a coagulação) com a administração de doses mais altas. Aumentos no TTPa e TCA não estão linearmente 5
6 correlacionados ao aumento da atividade antitrombótica de CLEXANE, sendo, portanto, inadequados e inseguros para monitoramento da atividade de CLEXANE. Informe ao seu médico se você está fazendo uso de algum outro medicamento. Não use medicamento sem o conhecimento do seu médico. Pode ser perigoso para a sua saúde. 5. ONDE, COMO E POR QUANTO TEMPO POSSO GUARDAR ESTE MEDICAMENTO? CLEXANE deve ser mantido em temperatura ambiente (entre 15 e 30ºC), protegido da luz. Número de lote e datas de fabricação e validade: vide embalagem. Não use medicamento com o prazo de validade vencido. Guarde-o em sua embalagem original. Após abertas, as seringas de CLEXANE devem ser utilizadas imediatamente. Se houver solução remanescente após o uso, esta deverá ser descartada. Características do medicamento Solução límpida, incolor a amarelo pálido. Antes de usar, observe o aspecto do medicamento. Caso ele esteja no prazo de validade e você observe alguma mudança no aspecto, consulte o farmacêutico para saber se poderá utilizá-lo. Todo medicamento deve ser mantido fora do alcance das crianças. 6. COMO DEVO USAR ESTE MEDICAMENTO? MODO DE USAR A via de administração de CLEXANE varia dependendo da indicação do produto. Abaixo estão descritas as técnicas de injeção subcutânea e bolus intravenoso. Técnica de injeção subcutânea de seringas pré-enchidas com sistema de segurança: Em caso de auto-injeção, o profissional da saúde irá informar como administrar suas injeções antes de você sair do hospital. É essencial que você siga exatamente estas instruções. Caso você tenha dúvidas, solicite ao profissional da saúde mais explicações. A injeção subcutânea aplicada corretamente (no tecido subcutâneo, abaixo da pele) é essencial para reduzir a dor e ferimento no local da injeção. Para evitar ferimentos acidentais com a agulha após a injeção, as seringas pré-enchidas são providas de um dispositivo de segurança automático. Preparo do local para injeção: O local recomendado para injeção é na gordura da parte inferior do abdômen, pelo menos 5 centímetros de distância do umbigo para fora e em ambos os lados. Antes da injeção, lavar as mãos. Limpar com álcool o local selecionado para injeção. Você deve selecionar um local diferente do abdômen inferior a cada aplicação. Preparo da seringa antes da injeção: Verifique se a seringa não está danificada e se o medicamento dentro está como uma solução límpida, sem partículas. Se a seringa estiver danificada ou o medicamento não for límpido, utilizar outra seringa. - Para as doses de 20 mg e 40 mg: Retire a capa protetora da agulha (figura 1). 6
7 Uma gota pode aparecer na ponta da agulha. Caso isto ocorra, remova-a antes de injetar o medicamento através de batidas suaves no corpo da seringa com a agulha apontada para baixo. - Para as doses de 60 mg, 80 mg e 100 mg: Retire a capa protetora da agulha (figura 1). Ajuste a dose a ser injetada (se necessário): A quantidade do medicamento a ser injetada deve ser ajustada dependendo do peso corpóreo do paciente; consequentemente qualquer excesso do medicamento deve ser expelido antes da injeção. Segure a seringa apontando para baixo (para manter a bolha de ar na seringa) e expelindo o excesso do medicamento em um recipiente adequado. Nota: caso o excesso de medicamento não seja expelido antes da aplicação, o dispositivo de segurança não será ativado ao final da injeção. Quando não houver a necessidade de ajuste da dose, a seringa pré-enchida está pronta para o uso. Não expelir qualquer bolha de ar da seringa antes de administrar a injeção. Uma gota pode aparecer na ponta da agulha. Se isso ocorrer, remova a gota antes da administração através de batidas no corpo da seringa com a agulha apontada para baixo. figura 1 Administração da injeção: 1. A seringa pré-enchida (20mg/0,2mL e 40mg/0,4mL) já está pronta para uso. Para evitar a perda da medicação, não pressione o êmbolo para expelir qualquer bolha de ar antes de administrar a injeção. 2. A injeção deve ser administrada com o paciente preferencialmente deitado, por injeção subcutânea profunda, no tecido subcutâneo da parede abdominal, alternando entre os lados esquerdo e direito a cada aplicação. 3. A agulha deve ser introduzida perpendicularmente na espessura de uma prega cutânea feita entre os dedos polegar e indicador. A prega deve ser mantida durante todo o período da injeção (figura 2). figura 2 4. O dispositivo de segurança é automaticamente ativado, quando o êmbolo é pressionado até o final, deste modo protegendo completamente a agulha usada e 7
8 sem causar desconforto ao paciente. A ativação do dispositivo de segurança só é possível se o êmbolo for completamente abaixado. Nota: o dispositivo de segurança somente poderá ser ativado com a seringa completamente vazia. (figura 3) figura 3 Técnica de injeção intravenosa (bolus) Apenas para a indicação de tratamento de infarto agudo do miocárdio com elevação do segmento ST: CLEXANE deve ser administrado através de uma linha intravenosa e não deve ser misturado ou coadministrado com outros medicamentos. Para evitar a possibilidade de mistura de CLEXANE com outros medicamentos, o acesso intravenoso escolhido deve ser lavado com quantidade suficiente de solução salina ou solução dextrose antes e imediatamente após a administração do bolus intravenoso de CLEXANE para limpar o dispositivo de acesso do medicamento. CLEXANE pode ser utilizado com segurança com solução salina normal 0,9% ou dextrose a 5% em água. Bolus intravenoso inicial de 30 mg: utiliza-se uma seringa pré-enchida de CLEXANE graduada e despreza-se o excesso do volume, obtendo apenas 30 mg (0,3 ml) na seringa. Aplica-se, então, a dose de 30 mg diretamente injetada na linha intravenosa. Bolus adicional para pacientes submetidos à intervenção coronariana percutânea quando a última dose subcutânea de CLEXANE foi administrada há mais de 8 horas antes de o balão ser inflado: para pacientes submetidos à intervenção coronariana percutânea, um bolus intravenoso adicional de 0,3 mg/kg deve ser administrado se a última dose subcutânea de CLEXANE foi administrada há mais de 8 horas antes de o balão ser inflado (vide Posologia - Tratamento do infarto agudo do miocárdio com elevação do segmento ST ). Para assegurar a precisão do pequeno volume a ser injetado, recomenda-se a diluição do medicamento para uma solução de 3 mg/ml. Para obter uma solução a 3 mg/ml utilizando uma seringa pré-enchida de 60 mg de CLEXANE, recomenda-se usar uma bolsa de infusão de 50 ml (contendo, por exemplo, solução salina normal 0,9% ou dextrose a 5% em água). Com o auxílio de uma seringa, retira-se 30 ml da solução contida na bolsa e despreza-se este volume. Aos 20 ml restantes na bolsa de infusão, injeta-se o conteúdo total de uma seringa pré-enchida graduada de 60 mg. Mistura-se gentilmente a solução final. Retira-se com uma seringa o volume requerido da solução para administração na linha intravenosa. Recomenda-se que esta solução seja preparada imediatamente antes de sua utilização. Após finalizada a diluição, o volume a ser injetado na linha intravenosa deve ser calculado utilizando-se a seguinte fórmula: [volume da solução diluída (ml) = peso do paciente (kg) x 0,1] ou utilizando a tabela abaixo. 8
9 Peso do paciente (kg) Volume de solução a 3 mg/ml a ser injetado na linha intravenosa Dose requerida (0,3 mg/kg) (mg) Volume a ser injetado (ml) após ser diluído para a concentração final de 3 mg/ml 45 13,5 4, ,5 5, ,5 6, ,5 7, ,5 8, ,5 9, POSOLOGIA A posologia de CLEXANE é determinada pela predisposição individual de ocorrer o tromboembolismo venoso em situações desencadeantes como cirurgia, imobilização prolongada e trauma, entre outras. Dessa maneira, são considerados com risco moderado os indivíduos que apresentem os seguintes fatores predisponentes: idade superior a 40 anos, obesidade, varizes dos membros inferiores, neoplasia, doença pulmonar ou cardíaca crônica, estrogenioterapia, puerpério, infecções sistêmicas, entre outros. São considerados com alto risco os indivíduos com histórico de tromboembolismo venoso prévio, neoplasia abdominal ou pélvica, cirurgia ortopédica de grande porte dos membros inferiores, entre outros. 1. Profilaxia da trombose venosa em pacientes cirúrgicos Em pacientes que apresentam risco moderado de tromboembolismo (por exemplo: cirurgia abdominal), a dose recomendada de CLEXANE é de 20 mg ou 40 mg uma vez ao dia por via subcutânea. Na cirurgia geral, a primeira injeção deve ser administrada 2 horas antes da intervenção cirúrgica. Em pacientes com alto risco de tromboembolismo (por exemplo: cirurgia ortopédica), a dose recomendada de CLEXANE administrada por via subcutânea é de 40 mg uma vez ao dia, iniciada 12 horas antes da cirurgia, ou de 30 mg, duas vezes ao dia, iniciada 12 a 24 horas após a cirurgia. O tratamento com CLEXANE é geralmente prescrito por um período médio de 7 a 10 dias. Um tratamento mais prolongado pode ser apropriado em alguns pacientes e deve ser continuado enquanto houver risco de tromboembolismo venoso e até que o paciente seja ambulatorial. A administração única diária de 40 mg de CLEXANE por mais 3 semanas, além da profilaxia inicial (em geral, após a alta hospitalar), comprovou ser benéfica em pacientes submetidos à cirurgia ortopédica. Para recomendações especiais sobre o intervalo entre as dosagens para anestesia espinhal/peridural e procedimentos de revascularização coronária percutânea: (vide O que devo saber antes de usar este medicamento? ). 2. Profilaxia do tromboembolismo venoso em pacientes clínicos A dose recomendada para pacientes clínicos é de 40 mg de CLEXANE, uma vez ao dia, administrada por via subcutânea. A duração do tratamento deve ser de no mínimo, 6 dias, 9
10 devendo ser continuado até que o paciente recupere a capacidade plena de se locomover, por um período máximo de 14 dias. 3. Tratamento da trombose venosa profunda com ou sem embolismo pulmonar A posologia de CLEXANE recomendada para o tratamento da trombose venosa profunda é de 1,5 mg/kg, uma vez ao dia ou 1 mg/kg, duas vezes ao dia, administrado por via subcutânea. Em pacientes com distúrbios tromboembólicos complicados, recomenda-se a administração da dose de 1 mg/kg, duas vezes ao dia. O tratamento com CLEXANE é geralmente prescrito por um período médio de 10 dias. A terapia anticoagulante oral deve ser iniciada quando apropriada e o tratamento deve ser mantido até que o efeito terapêutico do anticoagulante tenha sido atingido. 4. Prevenção da formação de trombo no circuito de circulação extracorpórea durante a hemodiálise A dose recomendada é de 1 mg/kg de CLEXANE. Em pacientes com alto risco hemorrágico, a dose deve ser reduzida para 0,5 mg/kg quando o acesso vascular for duplo ou 0,75 mg/kg quando o acesso vascular for simples. Durante a hemodiálise, CLEXANE deve ser introduzida na linha arterial do circuito, no início da sessão de hemodiálise. O efeito desta dose geralmente é suficiente para uma sessão com duração de 4 horas, entretanto, caso haja aparecimento de anéis de fibrina, por exemplo, após uma sessão mais longa que o normal, pode ser administrada dose complementar de 0,5 a 1,0 mg/kg de CLEXANE. 5. Tratamento de angina instável e infarto do miocárdio sem onda Q A dose de CLEXANE recomendada é de 1 mg/kg a cada 12 horas, por via subcutânea, administrada concomitantemente com ácido acetilsalicílico oral (100 a 325 mg, uma vez ao dia). Nestes pacientes, o tratamento com CLEXANE deve ser prescrito por no mínimo 2 dias e mantido até estabilização clínica. A duração normal do tratamento é de 2 a 8 dias. 6. Tratamento do infarto agudo do miocárdio com elevação do segmento ST A dose recomendada de CLEXANE é de um bolus intravenoso único de 30 mg acompanhado de uma dose de 1 mg/kg por via subcutânea, seguido por 1 mg/kg por via subcutânea a cada 12 horas (as duas primeiras doses subcutâneas devem ser de no máximo 100 mg cada dose e as demais doses 1 mg/kg por via subcutânea). Para pacientes com mais de 75 anos de idade, verifique instruções específicas descritas abaixo em Populações Especiais Idosos. Quando administrado em conjunto com um trombolítico (específico para fibrina ou não), CLEXANE deve ser administrado entre 15 minutos antes e 30 minutos depois do início da terapia fibrinolítica. Todos os pacientes devem receber ácido acetilsalicílico tão logo seja diagnosticado o infarto agudo do miocárdio com elevação do segmento ST. Esta medicação deve ser mantida com dosagem de 75 a 325 mg uma vez ao dia, a menos que haja contraindicação para o seu uso. A duração recomendada do tratamento com CLEXANE é de 8 dias ou até que o paciente receba alta do hospital, considerando-se o que ocorrer primeiro. Para pacientes submetidos à intervenção coronariana percutânea: se a última dose subcutânea de CLEXANE foi administrada há menos de 8 horas antes de o balão ser inflado, não é necessária dose adicional deste medicamento. Entretanto, caso a última dose subcutânea tenha sido administrada há mais de 8 horas antes de o balão ser inflado, uma dose adicional de 0,3 mg/kg de CLEXANE deve ser administrada através de bolus intravenoso. 10
11 Risco de uso por via de administração não recomendada Não há estudos dos efeitos de CLEXANE administrado por vias não recomendadas. Portanto, por segurança e para garantir a eficácia deste medicamento, a administração deve ser somente por via intravenosa ou subcutânea (dependendo da indicação terapêutica), conforme recomendado pelo médico. Populações Especiais Idosos Para o tratamento do infarto agudo do miocárdio com elevação do segmento ST em pacientes idosos (com idade igual ou maior a 75 anos), não deve ser administrado o bolus intravenoso inicial. A dose inicial é de 0,75 mg/kg por via subcutânea a cada 12 horas (as duas primeiras doses subcutâneas devem ser de no máximo 75 mg cada dose e as demais 0,75 mg/kg por via subcutânea). Para as demais indicações do produto, não é necessário realizar ajuste posológico em idosos, a menos que a função renal (dos rins) esteja prejudicada (vide Posologia - Insuficiência renal e O que devo saber antes de usar este medicamento? ). Insuficiência renal (vide O que devo saber antes de usar este medicamento ) Insuficiência renal severa: é necessário realizar ajuste posológico em pacientes com insuficiência renal severa (clearance de creatinina < 30 ml/min), de acordo com as tabelas a seguir, uma vez que a exposição ao CLEXANE é significativamente aumentada nesta população de pacientes. Para uso terapêutico, os seguintes ajustes posológicos são recomendados: Dose padrão Insuficiência renal severa 1 mg/kg por via subcutânea, duas vezes ao dia 1 mg/kg por via subcutânea, uma vez ao dia 1,5 mg/kg por via subcutânea, uma vez ao dia 1 mg/kg por via subcutânea, uma vez ao dia Tratamento do infarto agudo do miocárdio com elevação do segmento ST em pacientes com idade inferior a 75 anos 30 mg em bolus intravenoso único acompanhado de uma dose de 1 mg/kg por via subcutânea, seguido de 1 mg/kg por via subcutânea duas vezes ao dia (as duas primeiras doses subcutâneas devem ser de no máximo 100 mg cada) 30 mg em bolus intravenoso único acompanhado de uma dose de 1 mg/kg por via subcutânea, seguido de 1 mg/kg por via subcutânea uma vez ao dia (a primeira dose subcutânea deve ser de no máximo 100 mg) Tratamento do infarto agudo do miocárdio com elevação do segmento ST em pacientes com idade maior ou igual a 75 anos 0,75 mg/kg por via subcutânea duas vezes ao dia SEM bolus intravenoso inicial (as duas primeiras doses subcutâneas devem ser de no máximo 75 mg cada) 1 mg/kg por via subcutânea uma vez ao dia SEM bolus intravenoso inicial (a primeira dose subcutânea deve ser de no máximo 100 mg) Para uso profilático, os seguintes ajustes posológicos são recomendados: Dose padrão Insuficiência renal severa 40 mg por via subcutânea, uma vez ao dia 20 mg por via subcutânea, uma vez ao dia 20 mg por via subcutânea, uma vez ao dia 20 mg por via subcutânea, uma vez ao dia Estes ajustes posológicos não se aplicam à indicação em hemodiálise. 11
12 Insuficiência renal leve e moderada: embora não seja recomendado realizar ajuste posológico em pacientes com insuficiência renal moderada (clearance de creatinina ml/min) e leve (clearance de creatinina ml/min), é aconselhável que se faça um monitoramento clínico cuidadoso. Insuficiência hepática (do fígado): em decorrência da ausência de estudos clínicos, recomenda-se cautela em pacientes com insuficiência do fígado. Siga a orientação de seu médico, respeitando sempre os horários, as doses e a duração do tratamento. Não interrompa o tratamento sem o conhecimento de seu médico. 7. O QUE DEVO FAZER QUANDO EU ME ESQUECER DE USAR ESTE MEDICAMENTO? Caso esqueça de administrar uma dose, administre-a assim que possível, no entanto, se estiver próximo do horário da dose seguinte, espere por este horário, respeitando sempre o intervalo determinado pela posologia. Nunca devem ser administradas duas doses ao mesmo tempo. Em caso de dúvidas, procure orientação do farmacêutico ou de seu médico. 8. QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR? A enoxaparina foi avaliada em mais de pacientes que receberam o medicamento em estudos clínicos. Estes estudos incluíram 1776 pacientes para profilaxia de trombose venosa profunda seguida de cirurgia ortopédica ou abdominal em pacientes com risco de complicações tromboembólicas, 1169 para profilaxia de trombose venosa profunda em pacientes intensamente doentes com mobilidade severamente restrita, 559 para tratamento de trombose venosa profunda com ou sem embolismo pulmonar, 1578 para tratamento de angina instável e infarto do miocárdio sem onda Q e para tratamento de infarto agudo do miocárdio com elevação do segmento ST. O regime de enoxaparina sódica administrada durante estes estudos clínicos varia dependendo da indicação. A dose de enoxaparina sódica foi de 40 mg por via subcutânea uma vez ao dia para profilaxia de trombose venosa profunda seguida de cirurgia ou em pacientes intensamente doentes com mobilidade severamente restrita. No tratamento da trombose venosa profunda com ou sem embolismo pulmonar, pacientes recebendo enoxaparina foram tratados também com uma dose de 1 mg/kg por via subcutânea a cada 12 horas ou uma dose de 1,5 mg/kg por via subcutânea uma vez ao dia. Nos estudos clínicos para o tratamento de angina instável e infarto do miocárdio sem onda Q, as doses foram de 1 mg/kg por via subcutânea a cada 12 horas e no estudo clinico para tratamento de infarto agudo do miocárdio com elevação do segmento ST, o regime de enoxaparina sódica foi de 30 mg por via intravenosa em bolus seguida de 1 mg/kg por via subcutânea a cada 12 horas. As reações adversas observadas nestes estudos clínicos e reportadas na experiência póscomercialização estão detalhadas abaixo: Reação muito comum: ocorre em mais de 10% dos pacientes que utilizam este medicamento. Reação comum: ocorre entre 1% e 10% dos pacientes que utilizam este medicamento. Reação incomum: ocorre entre 0,1% e 1% dos pacientes que utilizam este medicamento. Reação rara: ocorre entre 0,01% e 0,1% dos pacientes que utilizam este medicamento. Reação muito rara: ocorre em menos de 0,01% dos pacientes que utilizam este medicamento. Reação com frequência desconhecida (que não pode ser estimada a partir dos dados). As reações adversas observadas pós-comercialização são classificados como de frequência desconhecida. 12
13 Hemorragias Em estudos clínicos, hemorragias foram as reações mais comumente reportadas. Estas incluem hemorragias de grande porte, relatadas no máximo em 4,2% dos pacientes (pacientes cirúrgicos**). Alguns destes casos foram fatais. Assim como com outros anticoagulantes, pode ocorrer hemorragia na presença de fatores de risco associados, tais como: lesões orgânicas suscetíveis a sangramento, procedimentos invasivos ou uso concomitante de medicamentos que afetam a hemostasia (conjunto de mecanismos que o organismo emprega para evitar hemorragia) (vide O que devo saber antes de usar este medicamento? e Interações Medicamentosas ). Distúrbios vasculares: Profilaxia (prevenção) em pacientes cirúrgicos: - Muito comum: hemorragia* (sangramento) - Rara: hemorragia retroperitoneal (espaço anatômico atrás da cavidade abdominal) Profilaxia em pacientes sob tratamento médico: - Comum: hemorragia* Tratamento em pacientes com trombose venosa profunda com ou sem embolismo pulmonar: - Muito comum: hemorragia* - Incomum: hemorragia intracraniana (dentro do crânio), hemorragia retroperitoneal Tratamento em pacientes com angina instável e infarto do miocárdio sem onda Q: - Comum: hemorragia* - Rara: hemorragia retroperitoneal Tratamento em pacientes com infarto agudo do miocárdio com elevação do segmento ST: - Comum: hemorragia* - Incomum: hemorragia intracraniana, hemorragia retroperitoneal * como hematoma (acúmulo de sangue fora dos vasos sanguíneos), outras equimoses (extravasamento de sangue na pele) além do local da injeção, ferimento com hematoma, hematúria (sangue na urina), epistaxe (sangramento no nariz) e hemorragia gastrintestinal. ** em pacientes cirúrgicos as complicações hemorrágicas foram consideradas de grande porte: (1) se a hemorragia causou um evento clínico significativo, ou (2) se acompanhado por uma diminuição da hemoglobina 2 g/dl ou transfusão de 2 ou mais unidades de produto sanguíneo. As hemorragias retroperitoneal e intracraniana foram sempre consideradas de grande porte. Trombocitopenia e trombocitose Distúrbios do sangue e sistema linfático Profilaxia em pacientes cirúrgicos - Muito comum: trombocitose (aumento de plaquetas > /mm 3 ) - Comum: trombocitopenia (diminuição no número de plaquetas sanguíneas) Profilaxia em pacientes sob tratamento médico - Incomum: trombocitopenia Tratamento em pacientes com trombose venosa profunda com ou sem embolismo pulmonar - Muito comum: trombocitose (aumento de plaquetas > /mm 3 ) - Comum: trombocitopenia Tratamento em pacientes com angina instável e infarto do miocárdio sem onda Q 13
14 - Incomum: trombocitopenia Tratamento em pacientes com infarto agudo do miocárdio com elevação do segmento ST - Comum: trombocitose (aumento de plaquetas > /mm 3 ), trombocitopenia - Muito rara: trombocitopenia imunoalérgica Outras reações adversas clinicamente relevantes Estas reações estão apresentadas abaixo, qualquer que sejam as indicações, por sistema órgão classe, frequência e ordem decrescente de gravidade. Distúrbios do sistema imune: - Comum: reação alérgica - Rara: reação anafilática/anafilactoide (reação de hipersensibilidade, conhecida popularmente como alérgica) - ver também experiência pós-comercialização. Distúrbios hepatobiliares: - Muito comum: aumento das enzimas hepáticas, principalmente transaminases (níveis de transaminases > 3 vezes o limite superior de normalidade) Distúrbios da pele e tecido subcutâneo: - Comum: urticária (erupção na pele, geralmente de origem alérgica, que causa coceira), prurido (coceira e/ou ardência), eritema (vermelhidão) - Incomum: dermatite bolhosa (tipo de reação alérgica na pele) Distúrbios gerais e condições no local da administração: - Comum: hematoma, dor e outras reações no local da injeção (como edema, hemorragia, hipersensibilidade, inflamação, tumoração (inchaço), dor ou reação não especificada) - Incomum: irritação no local, necrose na pele do local de injeção Investigação: - Rara: hiperpotassemia (aumento da dosagem do potássio no sangue) Experiência pós-comercialização As reações adversas a seguir foram identificadas durante o período após a aprovação do uso de CLEXANE. As reações adversas são derivadas de relatos espontâneos e, portanto a frequência é desconhecida (não pode ser estimada a partir dos dados). Distúrbios do sistema imune - Reação anafilática/anafilactoide, incluindo choque Distúrbios do sistema nervoso - Dor de cabeça Distúrbios vasculares - Foram relatados casos de hematoma espinhal (ou hematoma neuroaxial) com o uso concomitante de enoxaparina sódica e anestesia espinhal/peridural ou punção espinhal. Estas reações resultaram em graus variados de lesão neurológica, incluindo paralisia por tempo prolongado ou permanente (vide item 4. O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO? ). Distúrbios do sangue e linfáticos: - Anemia hemorrágica - Casos de trombocitopenia imunoalérgica com trombose, em alguns casos, a trombose foi complicada por infarto orgânico ou isquemia de extremidade (irrigação deficiente de sangue nas extremidades devido à constrição ou obstrução dos vasos sanguíneos) (videitem 4. O QUE DEVO SABER ANTES DE USAR ESTE MEDICAMENTO? ) - Eosinofilia (aumento do número de um tipo de leucócito do sangue chamado eosinófilo) 14
15 Distúrbios da pele e tecidos subcutâneos: - Vasculite cutânea (inflamação da parede de um vaso), necrose cutânea (morte das células da pele) geralmente ocorrendo no local da administração, (estes fenômenos são geralmente precedidos por púrpura (extravasamento de sangue para fora dos capilares da pele ou mucosa formando manchas) ou placas eritematosas (com vermelhidão), infiltradas e dolorosas), devendo-se interromper o tratamento com CLEXANE - Nódulos no local de injeção (nódulos inflamatórios que não são inclusões císticas de enoxaparina) que desaparecem após alguns dias e não devem ser motivo para interrupção do tratamento - Alopecia Distúrbios hepatobiliares: - Lesão hepatocelular (lesão das células do fígado) - Lesão colestática (lesão causada pelo acúmulo de bile, devido à redução/obstrução do fluxo de bile) Distúrbios musculoesqueléticos e de tecido conjuntivo - Osteoporose (doença que atinge os ossos) em terapia prolongada (acima de 3 meses) Atenção: este produto é um medicamento que possui nova indicação terapêutica no país e, embora as pesquisas tenham indicado eficácia e segurança aceitáveis, mesmo que indicado e utilizado corretamente, podem ocorrer eventos adversos imprevisíveis ou desconhecidos. Nesse caso, informe a seu médico. 9. O QUE FAZER SE ALGUÉM USAR UMA QUANTIDADE MAIOR DO QUE A INDICADA DESTE MEDICAMENTO? Sintomas e severidade: a superdose acidental após administração intravenosa, extracorporal ou subcutânea de CLEXANE pode causar complicações hemorrágicas. A absorção de CLEXANE após a administração oral, mesmo em altas doses, é pouco provável. Tratamento e antídoto: os efeitos anticoagulantes podem ser em grande parte, neutralizados pela administração intravenosa lenta de protamina. A dose de protamina depende da dose de CLEXANE administrada, ou seja, 1 mg de protamina neutraliza o efeito anticoagulante de 1 mg de CLEXANE, se CLEXANE foi administrado nas primeiras 8 horas. Uma infusão de 0,5 mg de protamina para 1 mg de CLEXANE pode ser administrada se CLEXANE foi administrado há mais de 8 horas à administração da protamina, ou se tiver sido determinado que uma segunda dose de protamina seja necessária. Após 12 horas da injeção de CLEXANE, a administração da protamina pode não ser necessária. Entretanto, mesmo com doses elevadas de protamina, a atividade anti-xa de CLEXANE nunca é completamente neutralizada (máximo de aproximadamente 60%). Em caso de uso de grande quantidade deste medicamento, procure rapidamente socorro médico e leve a embalagem ou bula do medicamento, se possível. Em caso de intoxicação ligue para , se você precisar de mais orientações. DIZERES LEGAIS VENDA SOB PRESCRIÇÃO MÉDICA MS
16 Farm. Resp.: Antonia A. Oliveira CRF-SP nº Registrado por: Sanofi-Aventis Farmacêutica Ltda. Av. Mj. Sylvio de M. Padilha, 5200 São Paulo SP CNPJ / Indústria Brasileira Marca registrada Fabricado por: Sanofi Winthrop Industrie 180 Rue Jean Jaurès Maisons-Alfort - França Importado por: Sanofi-Aventis Farmacêutica Ltda. Rua Conde Domingos Papaiz, 413 Suzano SP CNPJ / Sanofi-Aventis Farmacêutica Ltda. Rua Eduardo José Leal, 717, Parte 2A Navegantes SC CNPJ / OU Registrado por: Sanofi-Aventis Farmacêutica Ltda. Av. Mj. Sylvio de M. Padilha, 5200 São Paulo SP CNPJ / Indústria Brasileira Marca registrada Fabricado por: Sanofi Winthrop Industrie 180 Rue Jean Jaurès Maisons-Alfort - França Importado e Embalado por: Sanofi-Aventis Farmacêutica Ltda. Rua Conde Domingos Papaiz, 413 Suzano SP CNPJ / Importado por: Sanofi-Aventis Farmacêutica Ltda. Rua Eduardo José Leal, 717, Parte 2A Navegantes SC CNPJ / IB
17 Anexo B Histórico de Alteração para a Bula Número do expediente NA Nome do assunto 10463) PRODUTO BIOLÓGICO Inclusão Inicial de Texto de Bula RDC 60/12 Data da notificação/petição Data de aprovação da petição Itens alterados 29/05/ /05/2013 QUAIS OS MALES QUE ESTE MEDICAMENTO PODE ME CAUSAR? REAÇÕES ADVERSAS DIZERES LEGAIS
Versa. Bula para paciente. Solução injetável. 100 mg/ml
 Versa Bula para paciente Solução injetável 100 mg/ml VERSA enoxaparina sódica Solução injetável FORMA FARMACÊUTICA E APRESENTAÇÕES: Versa (enoxaparina sódica) solução injetável: 20 mg/0,2 ml, 40 mg/0,4
Versa Bula para paciente Solução injetável 100 mg/ml VERSA enoxaparina sódica Solução injetável FORMA FARMACÊUTICA E APRESENTAÇÕES: Versa (enoxaparina sódica) solução injetável: 20 mg/0,2 ml, 40 mg/0,4
DOBEVEN. Apsen Farmacêutica S.A. Cápsula gelatinosa dura 500 mg
 DOBEVEN Apsen Farmacêutica S.A. Cápsula gelatinosa dura 500 mg DOBEVEN dobesilato de cálcio APSEN FORMA FARMACÊUTICA Cápsula gelatinosa dura APRESENTAÇÕES Cápsula gelatinosa dura contendo 500 mg de dobesilato
DOBEVEN Apsen Farmacêutica S.A. Cápsula gelatinosa dura 500 mg DOBEVEN dobesilato de cálcio APSEN FORMA FARMACÊUTICA Cápsula gelatinosa dura APRESENTAÇÕES Cápsula gelatinosa dura contendo 500 mg de dobesilato
cloridrato de betaxolol Medicamento Genérico, Lei nº 9.787, de 1999 Solução Oftálmica Estéril Cristália Prod. Quím. Farm. Ltda.
 cloridrato de betaxolol Medicamento Genérico, Lei nº 9.787, de 1999 Solução Oftálmica Estéril Cristália Prod. Quím. Farm. Ltda. MODELO DE BULA PARA O PACIENTE 1 IDENTIFICAÇÃO DO MEDICAMENTO cloridrato
cloridrato de betaxolol Medicamento Genérico, Lei nº 9.787, de 1999 Solução Oftálmica Estéril Cristália Prod. Quím. Farm. Ltda. MODELO DE BULA PARA O PACIENTE 1 IDENTIFICAÇÃO DO MEDICAMENTO cloridrato
Kavit fitomenadiona. Solução Injetável 10 mg/ml. Cristália Produtos Químicos Farmacêuticos Ltda. MODELO DE BULA PARA O PACIENTE
 Kavit fitomenadiona Solução Injetável 10 mg/ml Cristália Produtos Químicos Farmacêuticos Ltda. MODELO DE BULA PARA O PACIENTE IDENTIFICAÇÃO DO MEDICAMENTO KAVIT fitomenadiona APRESENTAÇÃO Caixa contendo
Kavit fitomenadiona Solução Injetável 10 mg/ml Cristália Produtos Químicos Farmacêuticos Ltda. MODELO DE BULA PARA O PACIENTE IDENTIFICAÇÃO DO MEDICAMENTO KAVIT fitomenadiona APRESENTAÇÃO Caixa contendo
DOBEVEN. dobesilato de cálcio. APRESENTAÇÕES Cápsula gelatinosa dura contendo 500 mg de dobesilato de cálcio: Caixas com 5 e 30 cápsulas.
 DOBEVEN dobesilato de cálcio APRESENTAÇÕES Cápsula gelatinosa dura contendo 500 mg de dobesilato de cálcio: Caixas com 5 e 30 cápsulas. USO ORAL USO ADULTO COMPOSIÇÃO Cada cápsula gelatinosa dura contém:
DOBEVEN dobesilato de cálcio APRESENTAÇÕES Cápsula gelatinosa dura contendo 500 mg de dobesilato de cálcio: Caixas com 5 e 30 cápsulas. USO ORAL USO ADULTO COMPOSIÇÃO Cada cápsula gelatinosa dura contém:
ENOXALOW enoxaparina sódica. Forma farmacêutica e apresentações Solução injetável. Via de administração: IV/SC
 ENOXALOW enoxaparina sódica Forma farmacêutica e apresentações Solução injetável. Via de administração: IV/SC 20 mg/0,2 ml cartucho com 1 ou 10 seringas. 40 mg/0,4 ml cartucho com 1 ou 10 seringas. 60
ENOXALOW enoxaparina sódica Forma farmacêutica e apresentações Solução injetável. Via de administração: IV/SC 20 mg/0,2 ml cartucho com 1 ou 10 seringas. 40 mg/0,4 ml cartucho com 1 ou 10 seringas. 60
DOBEVEN. dobesilato de cálcio. APRESENTAÇÕES Cápsula gelatinosa dura contendo 500 mg de dobesilato de cálcio: Caixas com 5 e 30 cápsulas.
 DOBEVEN dobesilato de cálcio APSEN FORMA FARMACÊUTICA Cápsula gelatinosa dura APRESENTAÇÕES Cápsula gelatinosa dura contendo 500 mg de dobesilato de cálcio: Caixas com 5 e 30 cápsulas. USO ORAL USO ADULTO
DOBEVEN dobesilato de cálcio APSEN FORMA FARMACÊUTICA Cápsula gelatinosa dura APRESENTAÇÕES Cápsula gelatinosa dura contendo 500 mg de dobesilato de cálcio: Caixas com 5 e 30 cápsulas. USO ORAL USO ADULTO
OFTPRED. Suspensão Oftálmica Estéril. acetato de prednisolona 10 mg/ml BULA PARA O PACIENTE LATINOFARMA INDÚSTRIAS FARMACÊUTICAS LTDA
 OFTPRED LATINOFARMA INDÚSTRIAS FARMACÊUTICAS LTDA Suspensão Oftálmica Estéril acetato de prednisolona 10 mg/ml BULA PARA O PACIENTE COLÍRIO OFTPRED acetato de prednisolona 1,0% APRESENTAÇÕES Suspensão
OFTPRED LATINOFARMA INDÚSTRIAS FARMACÊUTICAS LTDA Suspensão Oftálmica Estéril acetato de prednisolona 10 mg/ml BULA PARA O PACIENTE COLÍRIO OFTPRED acetato de prednisolona 1,0% APRESENTAÇÕES Suspensão
Trimeb. (maleato de trimebutina)
 Trimeb (maleato de trimebutina) Bula para paciente Cápsula mole 200 mg Página 1 Trimeb (maleato de trimebutina) Cápsula mole FORMA FARMACÊUTICA E APRESENTAÇÕES Embalagens com 20, 30 ou 60 cápsulas contendo
Trimeb (maleato de trimebutina) Bula para paciente Cápsula mole 200 mg Página 1 Trimeb (maleato de trimebutina) Cápsula mole FORMA FARMACÊUTICA E APRESENTAÇÕES Embalagens com 20, 30 ou 60 cápsulas contendo
ALLERGAN PRODUTOS FARMACÊUTICOS LTDA
 RELESTAT ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril cloridrato de epinastina 0,05% BULA PARA O PACIENTE APRESENTAÇÕES Solução Oftálmica Estéril Frasco plástico conta-gotas contendo
RELESTAT ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril cloridrato de epinastina 0,05% BULA PARA O PACIENTE APRESENTAÇÕES Solução Oftálmica Estéril Frasco plástico conta-gotas contendo
Keflaxina Sandoz do Brasil Ind. Farm. Ltda. Pó para Suspensão Oral 50 mg/ml
 Keflaxina Sandoz do Brasil Ind. Farm. Ltda. Pó para Suspensão Oral 50 mg/ml I. IDENTIFICAÇÃO DO MEDICAMENTO Keflaxina cefalexina APRESENTAÇÃO Suspensão oral 250 mg/5ml. Embalagem contendo frasco com pó
Keflaxina Sandoz do Brasil Ind. Farm. Ltda. Pó para Suspensão Oral 50 mg/ml I. IDENTIFICAÇÃO DO MEDICAMENTO Keflaxina cefalexina APRESENTAÇÃO Suspensão oral 250 mg/5ml. Embalagem contendo frasco com pó
DIGEDRAT. (maleato de trimebutina)
 DIGEDRAT (maleato de trimebutina) Cosmed Indústria de Cosméticos e Medicamentos S.A. Cápsula mole 200mg I - IDENTIFICAÇÃO DO DIGEDRAT maleato de trimebutina APRESENTAÇÕES Cápsula mole Embalagens contendo
DIGEDRAT (maleato de trimebutina) Cosmed Indústria de Cosméticos e Medicamentos S.A. Cápsula mole 200mg I - IDENTIFICAÇÃO DO DIGEDRAT maleato de trimebutina APRESENTAÇÕES Cápsula mole Embalagens contendo
Calcium Sandoz F. Calcium Sandoz FF NOVARTIS BIOCIÊNCIAS S.A. Comprimido Efervescente. 500mg de cálcio. 1.000mg de cálcio
 Calcium Sandoz F Calcium Sandoz FF NOVARTIS BIOCIÊNCIAS S.A. Comprimido Efervescente 500mg de cálcio 1.000mg de cálcio Calcium Sandoz F Calcium Sandoz FF carbonato de cálcio + lactogliconato de cálcio
Calcium Sandoz F Calcium Sandoz FF NOVARTIS BIOCIÊNCIAS S.A. Comprimido Efervescente 500mg de cálcio 1.000mg de cálcio Calcium Sandoz F Calcium Sandoz FF carbonato de cálcio + lactogliconato de cálcio
PRESMIN LATINOFARMA INDÚSTRIAS FARMACÊUTICAS LTDA. Solução Oftálmica Estéril. betaxolol (cloridrato) 5,6 mg/ml
 PRESMIN LATINOFARMA INDÚSTRIAS FARMACÊUTICAS LTDA. Solução Oftálmica Estéril betaxolol (cloridrato) 5,6 mg/ml COLÍRIO PRESMIN betaxolol 0,5% MEDICAMENTO SIMILAR EQUIVALENTE AO MEDICAMENTO DE REFERÊNCIA
PRESMIN LATINOFARMA INDÚSTRIAS FARMACÊUTICAS LTDA. Solução Oftálmica Estéril betaxolol (cloridrato) 5,6 mg/ml COLÍRIO PRESMIN betaxolol 0,5% MEDICAMENTO SIMILAR EQUIVALENTE AO MEDICAMENTO DE REFERÊNCIA
Benestare policabofila cálcica. Medley Indústria Farmacêutica Ltda. Comprimido revestido 625 mg
 Benestare policabofila cálcica Medley Indústria Farmacêutica Ltda. Comprimido revestido 625 mg Benestare policarbofila cálcica APRESENTAÇÕES Comprimidos revestidos de 625 mg: embalagens com 14 e 30 comprimidos.
Benestare policabofila cálcica Medley Indústria Farmacêutica Ltda. Comprimido revestido 625 mg Benestare policarbofila cálcica APRESENTAÇÕES Comprimidos revestidos de 625 mg: embalagens com 14 e 30 comprimidos.
RAPILAX. Kley Hertz S/A Indústria e Comércio Solução Oral Gotas 7,5 mg/ml picossulfato de sódio
 RAPILAX Kley Hertz S/A Indústria e Comércio Solução Oral Gotas 7,5 mg/ml picossulfato de sódio RAPILAX picossulfato de sódio APRESENTAÇÃO Solução oral contendo: 7,5 mg/ml de picossulfato de sódio em frasco
RAPILAX Kley Hertz S/A Indústria e Comércio Solução Oral Gotas 7,5 mg/ml picossulfato de sódio RAPILAX picossulfato de sódio APRESENTAÇÃO Solução oral contendo: 7,5 mg/ml de picossulfato de sódio em frasco
loratadina Laboratório Globo Ltda. Xarope 1 mg/ml
 loratadina Laboratório Globo Ltda. Xarope 1 mg/ml loratadina Medicamento genérico Lei nº 9.787, de 1999 FORMA FARMACÊUTICA E APRESENTAÇÃO: loratadina xarope 1 mg/ml. Embalagem contendo 1 frasco de 100
loratadina Laboratório Globo Ltda. Xarope 1 mg/ml loratadina Medicamento genérico Lei nº 9.787, de 1999 FORMA FARMACÊUTICA E APRESENTAÇÃO: loratadina xarope 1 mg/ml. Embalagem contendo 1 frasco de 100
DIGESAN Sanofi-Aventis Farmacêutica Ltda. Cápsulas 10mg
 DIGESAN Sanofi-Aventis Farmacêutica Ltda. Cápsulas 10mg Esta bula sofreu aumento de tamanho para adequação a legislação vigente da ANVISA. Esta bula é continuamente atualizada. Favor proceder a sua leitura
DIGESAN Sanofi-Aventis Farmacêutica Ltda. Cápsulas 10mg Esta bula sofreu aumento de tamanho para adequação a legislação vigente da ANVISA. Esta bula é continuamente atualizada. Favor proceder a sua leitura
dicloridrato de cetirizina Solução oral 1mg/mL
 dicloridrato de cetirizina Solução oral 1mg/mL MODELO DE BULA COM INFORMAÇÕES AO PACIENTE dicloridrato de cetirizina Medicamento genérico Lei nº 9.787, de 1999. APRESENTAÇÃO Solução oral 1mg/mL Embalagem
dicloridrato de cetirizina Solução oral 1mg/mL MODELO DE BULA COM INFORMAÇÕES AO PACIENTE dicloridrato de cetirizina Medicamento genérico Lei nº 9.787, de 1999. APRESENTAÇÃO Solução oral 1mg/mL Embalagem
BULA DE NALDECON DOR COMPRIMIDOS
 BULA DE NALDECON DOR COMPRIMIDOS BRISTOL-MYERS SQUIBB NALDECON DOR paracetamol Dores em geral Febre Uma dose = 2 comprimidos FORMA FARMACÊUTICA E APRESENTAÇÃO NALDECON DOR é apresentado em displays com
BULA DE NALDECON DOR COMPRIMIDOS BRISTOL-MYERS SQUIBB NALDECON DOR paracetamol Dores em geral Febre Uma dose = 2 comprimidos FORMA FARMACÊUTICA E APRESENTAÇÃO NALDECON DOR é apresentado em displays com
BELPELE. Farmoquímica S/A GEL 3 mg/g. Belpele_AR011113_Bula Paciente
 BELPELE Farmoquímica S/A GEL 3 mg/g BULA PACIENTE BELPELE adapaleno APRESENTAÇÕES: Gel adapaleno 3 mg/g (0,3%) embalagem contendo bisnaga com 30g. VIA TÓPICA USO ADULTO E PEDIÁTRICO ACIMA DE 12 ANOS COMPOSIÇÃO:
BELPELE Farmoquímica S/A GEL 3 mg/g BULA PACIENTE BELPELE adapaleno APRESENTAÇÕES: Gel adapaleno 3 mg/g (0,3%) embalagem contendo bisnaga com 30g. VIA TÓPICA USO ADULTO E PEDIÁTRICO ACIMA DE 12 ANOS COMPOSIÇÃO:
IDENTIFICAÇÃO DO MEDICAMENTO DAFLON. 500mg: diosmina 450mg + hesperidina 50mg micronizada. 1000mg: diosmina 900mg + hesperidina 100mg micronizada
 1 IDENTIFICAÇÃO DO MEDICAMENTO DAFLON 500mg: diosmina 450mg + hesperidina 50mg micronizada 1000mg: diosmina 900mg + hesperidina 100mg micronizada APRESENTAÇÕES: DAFLON 500mg: embalagem contendo 15, 30
1 IDENTIFICAÇÃO DO MEDICAMENTO DAFLON 500mg: diosmina 450mg + hesperidina 50mg micronizada 1000mg: diosmina 900mg + hesperidina 100mg micronizada APRESENTAÇÕES: DAFLON 500mg: embalagem contendo 15, 30
loratadina Xarope 1mg/mL
 loratadina Xarope 1mg/mL MODELO DE BULA COM INFORMAÇÕES AO PACIENTE loratadina Medicamento genérico Lei nº 9.787, de 1999. APRESENTAÇÃO Xarope 1mg/mL Embalagem contendo 1 frasco com 100mL + copo-medida.
loratadina Xarope 1mg/mL MODELO DE BULA COM INFORMAÇÕES AO PACIENTE loratadina Medicamento genérico Lei nº 9.787, de 1999. APRESENTAÇÃO Xarope 1mg/mL Embalagem contendo 1 frasco com 100mL + copo-medida.
CREMEFENERGAN prometazina. APRESENTAÇÃO Creme 20mg/g: bisnaga de 30 g. USO TÓPICO. USO ADULTO E PEDIÁTRICO ACIMA DE 2 ANOS.
 Esta bula sofreu aumento do tamanho para adequação a legislação vigente da ANVISA. Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. CREMEFENERGAN prometazina
Esta bula sofreu aumento do tamanho para adequação a legislação vigente da ANVISA. Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. CREMEFENERGAN prometazina
Ethamolin. oleato de monoetanolamina FORMA FARMACÊUTICA E APRESENTAÇÃO:
 Ethamolin oleato de monoetanolamina FORMA FARMACÊUTICA E APRESENTAÇÃO: ETHAMOLIN consiste em uma solução aquosa de oleato de monoetanolamina a 5% para uso injetável apresentado em caixas contendo 6 ampolas
Ethamolin oleato de monoetanolamina FORMA FARMACÊUTICA E APRESENTAÇÃO: ETHAMOLIN consiste em uma solução aquosa de oleato de monoetanolamina a 5% para uso injetável apresentado em caixas contendo 6 ampolas
BRONQTRAT BRONQTRAT INFANTIL. cloridrato de ambroxol
 BRONQTRAT BRONQTRAT INFANTIL cloridrato de ambroxol Natulab Laboratório SA. Xarope adulto de 30mg/5mL Xarope pediátrico de 15mg/5mL BRONQTRAT XAROPE PACIENTE BRONQTRAT cloridrato de ambroxol APRESENTAÇÕES
BRONQTRAT BRONQTRAT INFANTIL cloridrato de ambroxol Natulab Laboratório SA. Xarope adulto de 30mg/5mL Xarope pediátrico de 15mg/5mL BRONQTRAT XAROPE PACIENTE BRONQTRAT cloridrato de ambroxol APRESENTAÇÕES
Sinavel EMS SIGMA PHARMA LTDA. Comprimido revestido. 100mg
 Sinavel EMS SIGMA PHARMA LTDA Comprimido revestido 100mg IDENTIFICAÇÃO DO MEDICAMENTO Sinavel brometo de pinavério APRESENTAÇÕES: Comprimidos revestidos de 100 mg: embalagem contendo 10, 20, 30, 40 ou
Sinavel EMS SIGMA PHARMA LTDA Comprimido revestido 100mg IDENTIFICAÇÃO DO MEDICAMENTO Sinavel brometo de pinavério APRESENTAÇÕES: Comprimidos revestidos de 100 mg: embalagem contendo 10, 20, 30, 40 ou
CLORIDRATO DE AMBROXOL. Geolab Indústria Farmacêutica S/A Xarope Adulto 6mg/mL Infantil 3mg/mL
 CLORIDRATO DE AMBROXOL Geolab Indústria Farmacêutica S/A Xarope Adulto 6mg/mL Infantil 3mg/mL MODELO DE BULA PARA O PACIENTE Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de
CLORIDRATO DE AMBROXOL Geolab Indústria Farmacêutica S/A Xarope Adulto 6mg/mL Infantil 3mg/mL MODELO DE BULA PARA O PACIENTE Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de
Silimalon (slimarina + metionina)
 Silimalon (slimarina + metionina) Zydus Nikkho Farmacêutica Ltda Drágeas 70 mg / 100 mg Bula do Paciente Silimalon drágea- Versão 01 11/2010- paciente Página 1 I - IDENTIFICAÇÃO DO MEDICAMENTO SILIMALON
Silimalon (slimarina + metionina) Zydus Nikkho Farmacêutica Ltda Drágeas 70 mg / 100 mg Bula do Paciente Silimalon drágea- Versão 01 11/2010- paciente Página 1 I - IDENTIFICAÇÃO DO MEDICAMENTO SILIMALON
UROVIT (cloridrato de fenazopiridina)
 UROVIT (cloridrato de fenazopiridina) União Química Farmacêutica Nacional S.A 100 mg e 200 mg UROVIT cloridrato de fenazopiridina IDENTIFICAÇÃO DO PRODUTO FORMA FARMACÊUTICA E APRESENTAÇÕES 100 mg: embalagem
UROVIT (cloridrato de fenazopiridina) União Química Farmacêutica Nacional S.A 100 mg e 200 mg UROVIT cloridrato de fenazopiridina IDENTIFICAÇÃO DO PRODUTO FORMA FARMACÊUTICA E APRESENTAÇÕES 100 mg: embalagem
IDENTIFICAÇÃO DO MEDICAMENTO. BenicarAnlo olmesartana medoxomila anlodipino
 IDENTIFICAÇÃO DO MEDICAMENTO BenicarAnlo olmesartana medoxomila anlodipino APRESENTAÇÕES BenicarAnlo é apresentado em embalagens com 7 comprimidos revestidos de olmesartana medoxomila e anlodipino (como
IDENTIFICAÇÃO DO MEDICAMENTO BenicarAnlo olmesartana medoxomila anlodipino APRESENTAÇÕES BenicarAnlo é apresentado em embalagens com 7 comprimidos revestidos de olmesartana medoxomila e anlodipino (como
TASULIL. Geolab Indústria Farmacêutica S/A Cápsula 0,4mg
 TASULIL Geolab Indústria Farmacêutica S/A Cápsula 0,4mg MODELO DE BULA PARA O PACIENTE Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. Tasulil cloridrato
TASULIL Geolab Indústria Farmacêutica S/A Cápsula 0,4mg MODELO DE BULA PARA O PACIENTE Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. Tasulil cloridrato
MARIOL INDUSTRIAL LTDA.
 PARACETAMOL GOTAS Medicamento genérico Lei n 9.787 de 1999 MARIOL INDUSTRIAL LTDA. Solução Oral (Gotas) 200 mg/ml PARACETAMOL paracetamol DCB: 06827 FORMA FARMACÊUTICA Solução Oral VIA DE ADMINISTRAÇÃO
PARACETAMOL GOTAS Medicamento genérico Lei n 9.787 de 1999 MARIOL INDUSTRIAL LTDA. Solução Oral (Gotas) 200 mg/ml PARACETAMOL paracetamol DCB: 06827 FORMA FARMACÊUTICA Solução Oral VIA DE ADMINISTRAÇÃO
BULA STUB CÁPSULAS DE LIBERAÇÃO PROLONGADA 0,4 MG
 BULA STUB CÁPSULAS DE LIBERAÇÃO PROLONGADA 0,4 MG FABRICANTE: S.C. GEDEON RICHTER EMBALADO EM: ACTAVIS FARMACÊUTICA Ltda. I) IDENTIFICAÇÃO DO MEDICAMENTO STUB cloridrato de tansulosina APRESENTAÇÕES Cápsulas
BULA STUB CÁPSULAS DE LIBERAÇÃO PROLONGADA 0,4 MG FABRICANTE: S.C. GEDEON RICHTER EMBALADO EM: ACTAVIS FARMACÊUTICA Ltda. I) IDENTIFICAÇÃO DO MEDICAMENTO STUB cloridrato de tansulosina APRESENTAÇÕES Cápsulas
Bula com informações ao Paciente soro antibotrópico (pentavalente) e antilaquético. solução injetável IDENTIFICAÇÃO DO MEDICAMENTO
 soro antibotrópico (pentavalente) e antilaquético solução injetável IDENTIFICAÇÃO DO MEDICAMENTO soro antibotrópico (pentavalente) e antilaquético APRESENTAÇÃO O soro antibotrópico (pentavalente) e antilaquético,
soro antibotrópico (pentavalente) e antilaquético solução injetável IDENTIFICAÇÃO DO MEDICAMENTO soro antibotrópico (pentavalente) e antilaquético APRESENTAÇÃO O soro antibotrópico (pentavalente) e antilaquético,
FLUISOLVAN. Geolab Indústria Farmacêutica S/A Xarope Adulto 6mg/mL Infantil 3mg/mL
 FLUISOLVAN Geolab Indústria Farmacêutica S/A Xarope Adulto 6mg/mL Infantil 3mg/mL MODELO DE BULA PARA O PACIENTE Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento.
FLUISOLVAN Geolab Indústria Farmacêutica S/A Xarope Adulto 6mg/mL Infantil 3mg/mL MODELO DE BULA PARA O PACIENTE Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento.
Solução Glicofisiológica
 Solução Glicofisiológica Solução injetável cloreto de sódio + glicose 9 mg/ml + 50 mg/ml 1 Forma farmacêutica e apresentações: Solução injetável MODELO DE BULA Solução Glicofisiológica cloreto de sódio
Solução Glicofisiológica Solução injetável cloreto de sódio + glicose 9 mg/ml + 50 mg/ml 1 Forma farmacêutica e apresentações: Solução injetável MODELO DE BULA Solução Glicofisiológica cloreto de sódio
Anexo A. Micotiazol CAZI QUIMICA FARMACÊUTICA IND. E COM. LTDA. Solução Tópica
 Anexo A Micotiazol CAZI QUIMICA FARMACÊUTICA IND. E COM. LTDA Solução Tópica Ácido benzóico... 20 mg Ácido salicílico... 20 mg Iodo metálico... 2,5 mg Licor de Hoffman q.s.p.... 1,0 ml 1 MODELO DE BULA
Anexo A Micotiazol CAZI QUIMICA FARMACÊUTICA IND. E COM. LTDA Solução Tópica Ácido benzóico... 20 mg Ácido salicílico... 20 mg Iodo metálico... 2,5 mg Licor de Hoffman q.s.p.... 1,0 ml 1 MODELO DE BULA
PYR-PAM pamoato de pirvínio
 PYR-PAM pamoato de pirvínio DRÁGEA 100 MG Bula do Paciente Pyr-Pam UCI-FARMA Conforme RDC 47/09 Página 1 PYR-PAM pamoato de pirvínio FORMA FARMACÊUTICA E APRESENTAÇÃO PYR-PAM DRÁGEA 100 MG: cartucho contendo
PYR-PAM pamoato de pirvínio DRÁGEA 100 MG Bula do Paciente Pyr-Pam UCI-FARMA Conforme RDC 47/09 Página 1 PYR-PAM pamoato de pirvínio FORMA FARMACÊUTICA E APRESENTAÇÃO PYR-PAM DRÁGEA 100 MG: cartucho contendo
Ebastel. Bula para paciente. Comprimido revestido. 10 mg
 Ebastel Bula para paciente Comprimido revestido 10 mg EBASTEL ebastina Comprimido revestido FORMAS FARMACÊUTICAS E APRESENTAÇÕES Embalagens com 10 comprimidos revestidos contendo 10 mg de ebastina USO
Ebastel Bula para paciente Comprimido revestido 10 mg EBASTEL ebastina Comprimido revestido FORMAS FARMACÊUTICAS E APRESENTAÇÕES Embalagens com 10 comprimidos revestidos contendo 10 mg de ebastina USO
GUTTALAX picossulfato de sódio Solução oral 7,5 mg
 GUTTALAX picossulfato de sódio Solução oral 7,5 mg GUTTALAX SOLUÇÃO PACIENTE Guttalax picossulfato de sódio abcd APRESENTAÇÃO Solução oral 7,5 mg/ml: frasco com 20 ml. USO ORAL USO ADULTO E PEDIÁTRICO
GUTTALAX picossulfato de sódio Solução oral 7,5 mg GUTTALAX SOLUÇÃO PACIENTE Guttalax picossulfato de sódio abcd APRESENTAÇÃO Solução oral 7,5 mg/ml: frasco com 20 ml. USO ORAL USO ADULTO E PEDIÁTRICO
NEOSSOLVAN. (cloridrato de ambroxol)
 NEOSSOLVAN (cloridrato de ambroxol) Brainfarma Indústria Química e Farmacêutica S.A. Xarope Pediátrico 15mg/5mL Xarope Adulto 30mg/5mL I - IDENTIFICAÇÃO DO MEDICAMENTO: NEOSSOLVAN cloridrato de ambroxol
NEOSSOLVAN (cloridrato de ambroxol) Brainfarma Indústria Química e Farmacêutica S.A. Xarope Pediátrico 15mg/5mL Xarope Adulto 30mg/5mL I - IDENTIFICAÇÃO DO MEDICAMENTO: NEOSSOLVAN cloridrato de ambroxol
brometo de pinavério Comprimido revestido 50mg
 brometo de pinavério Comprimido revestido 50mg MODELO DE BULA COM INFORMAÇÕES AO PACIENTE brometo de pinavério Medicamento genérico Lei nº 9.787, de 1999. APRESENTAÇÃO Comprimido revestido 50mg Embalagens
brometo de pinavério Comprimido revestido 50mg MODELO DE BULA COM INFORMAÇÕES AO PACIENTE brometo de pinavério Medicamento genérico Lei nº 9.787, de 1999. APRESENTAÇÃO Comprimido revestido 50mg Embalagens
Neo Fresh. (carmelose sódica)
 Neo Fresh (carmelose sódica) Brainfarma Indústria Química e Farmacêutica S.A. Solução oftálmica estéril 5mg/mL (0,5%) I - IDENTIFICAÇÃO DO MEDICAMENTO: NEO FRESH carmelose sódica 0,5% APRESENTAÇÃO Solução
Neo Fresh (carmelose sódica) Brainfarma Indústria Química e Farmacêutica S.A. Solução oftálmica estéril 5mg/mL (0,5%) I - IDENTIFICAÇÃO DO MEDICAMENTO: NEO FRESH carmelose sódica 0,5% APRESENTAÇÃO Solução
Antrofi promestrieno. Eurofarma Laboratórios S.A. Creme vaginal 10 mg/g
 Antrofi promestrieno Eurofarma Laboratórios S.A. Creme vaginal 10 mg/g Antrofi promestrieno CREME VAGINAL FORMAS FARMACÊUTICAS E APRESENTAÇÕES APRESENTAÇÕES Bisnaga com 30 g de creme vaginal acompanhada
Antrofi promestrieno Eurofarma Laboratórios S.A. Creme vaginal 10 mg/g Antrofi promestrieno CREME VAGINAL FORMAS FARMACÊUTICAS E APRESENTAÇÕES APRESENTAÇÕES Bisnaga com 30 g de creme vaginal acompanhada
RILAN UCI-FARMA INDÚSTRIA FARMACÊUTICA LTDA. SOLUÇÃO NASAL. 20 mg/ml
 RILAN UCI-FARMA INDÚSTRIA FARMACÊUTICA LTDA. SOLUÇÃO NASAL 20 mg/ml I) IDENTIFICAÇÃO DO RILAN NASAL 2% SPRAY cromoglicato dissódico FORMA FARMACÊUTICA E APRESENTAÇÃO RILAN NASAL 2% SPRAY: cartucho com
RILAN UCI-FARMA INDÚSTRIA FARMACÊUTICA LTDA. SOLUÇÃO NASAL 20 mg/ml I) IDENTIFICAÇÃO DO RILAN NASAL 2% SPRAY cromoglicato dissódico FORMA FARMACÊUTICA E APRESENTAÇÃO RILAN NASAL 2% SPRAY: cartucho com
Aglucose acarbose EMS S/A. Comprimidos. 50 e 100 mg
 Aglucose acarbose EMS S/A. Comprimidos 50 e 100 mg I - IDENTIFICAÇÃO DO MEDICAMENTO Aglucose acarbose USO ORAL USO ADULTO APRESENTAÇÕES Comprimidos 50 mg: Caixa contendo 4, 30 e 60 comprimidos. Comprimidos
Aglucose acarbose EMS S/A. Comprimidos 50 e 100 mg I - IDENTIFICAÇÃO DO MEDICAMENTO Aglucose acarbose USO ORAL USO ADULTO APRESENTAÇÕES Comprimidos 50 mg: Caixa contendo 4, 30 e 60 comprimidos. Comprimidos
Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. CLEXANE enoxaparina sódica
 MODELO DE TEXTO DE BULA SANOFI-AVENTIS Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. CLEXANE enoxaparina sódica FORMA FARMACÊUTICA E APRESENTAÇÕES
MODELO DE TEXTO DE BULA SANOFI-AVENTIS Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. CLEXANE enoxaparina sódica FORMA FARMACÊUTICA E APRESENTAÇÕES
Excipientes: albumina humana, cloreto de sódio, cloridrato de arginina, citrato de sódio.
 Haemocomplettan P fibrinogênio APRESENTAÇÃO Haemocomplettan P 1g: embalagem contendo 1 frasco-ampola com 1 g de pó liofilizado para solução injetável e infusão. VIA INTRAVENOSA USO ADULTO E PEDIÁTRICO
Haemocomplettan P fibrinogênio APRESENTAÇÃO Haemocomplettan P 1g: embalagem contendo 1 frasco-ampola com 1 g de pó liofilizado para solução injetável e infusão. VIA INTRAVENOSA USO ADULTO E PEDIÁTRICO
Nome do medicamento: OSTEOPREVIX D Forma farmacêutica: Comprimido revestido Concentração: cálcio 500 mg/com rev + colecalciferol 200 UI/com rev.
 Nome do medicamento: OSTEOPREVIX D Forma farmacêutica: Comprimido revestido Concentração: cálcio 500 mg/com rev + colecalciferol 200 UI/com rev. OSTEOPREVIX D carbonato de cálcio colecalciferol APRESENTAÇÕES
Nome do medicamento: OSTEOPREVIX D Forma farmacêutica: Comprimido revestido Concentração: cálcio 500 mg/com rev + colecalciferol 200 UI/com rev. OSTEOPREVIX D carbonato de cálcio colecalciferol APRESENTAÇÕES
Abbott Laboratórios do Brasil Ltda Rua Michigan 735, Brooklin São Paulo - SP CEP: 04566-905
 MODELO DE BULA PARA O PACIENTE SYNAGIS palivizumabe I - IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Pó liófilo injetável de: - 100 mg em embalagem com 01 frasco-ampola para dose única contendo palivizumabe
MODELO DE BULA PARA O PACIENTE SYNAGIS palivizumabe I - IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Pó liófilo injetável de: - 100 mg em embalagem com 01 frasco-ampola para dose única contendo palivizumabe
Magnésia Bisurada carbonato de magnésio carbonato básico de bismuto carbonato de cálcio bicarbonato de sódio
 Magnésia Bisurada carbonato de magnésio carbonato básico de bismuto carbonato de cálcio bicarbonato de sódio IDENTIFICAÇÃO DO MEDICAMENTO Nome comercial: Magnésia Bisurada Nome genérico: carbonato de magnésio,
Magnésia Bisurada carbonato de magnésio carbonato básico de bismuto carbonato de cálcio bicarbonato de sódio IDENTIFICAÇÃO DO MEDICAMENTO Nome comercial: Magnésia Bisurada Nome genérico: carbonato de magnésio,
APRESENTAÇÕES Comprimidos revestidos com 500 mg de policarabofila base. Embalagens com 30 comprimidos revestidos.
 MUVINOR policarbofila cálcica APRESENTAÇÕES Comprimidos revestidos com 500 mg de policarabofila base. Embalagens com 30 comprimidos revestidos. USO ORAL USO ADULTO (ACIMA DE 12 ANOS DE IDADE) COMPOSIÇÃO
MUVINOR policarbofila cálcica APRESENTAÇÕES Comprimidos revestidos com 500 mg de policarabofila base. Embalagens com 30 comprimidos revestidos. USO ORAL USO ADULTO (ACIMA DE 12 ANOS DE IDADE) COMPOSIÇÃO
Tylemax Gotas. Natulab Laboratório SA. Solução Oral. 200 mg/ml
 Tylemax Gotas Natulab Laboratório SA. Solução Oral 200 mg/ml TYLEMAX paracetamol APRESENTAÇÕES Solução oral em frasco plástico opaco gotejador com 10, 15 e 20ml, contendo 200mg/mL de paracetamol. USO ADULTO
Tylemax Gotas Natulab Laboratório SA. Solução Oral 200 mg/ml TYLEMAX paracetamol APRESENTAÇÕES Solução oral em frasco plástico opaco gotejador com 10, 15 e 20ml, contendo 200mg/mL de paracetamol. USO ADULTO
Naramig GlaxoSmithKline Brasil Ltda. Comprimidos 2,5mg
 Naramig GlaxoSmithKline Brasil Ltda. Comprimidos 2,5mg LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO I - IDENTIFICAÇÃO DO MEDICAMENTO Naramig cloridrato de naratriptana APRESENTAÇÃO Naramig
Naramig GlaxoSmithKline Brasil Ltda. Comprimidos 2,5mg LEIA ESTA BULA ATENTAMENTE ANTES DE INICIAR O TRATAMENTO I - IDENTIFICAÇÃO DO MEDICAMENTO Naramig cloridrato de naratriptana APRESENTAÇÃO Naramig
Micotiazol CAZI QUIMICA FARMACÊUTICA IND. E COM. LTDA. Solução Tópica
 Anexo A Micotiazol CAZI QUIMICA FARMACÊUTICA IND. E COM. LTDA Solução Tópica Ácido benzóico... 20 mg Ácido salicílico... 20 mg Iodo metálico... 2,5 mg Licor de Hoffman q.s.p.... 1,0 ml 1 MODELO DE BULA
Anexo A Micotiazol CAZI QUIMICA FARMACÊUTICA IND. E COM. LTDA Solução Tópica Ácido benzóico... 20 mg Ácido salicílico... 20 mg Iodo metálico... 2,5 mg Licor de Hoffman q.s.p.... 1,0 ml 1 MODELO DE BULA
cloxazolam Eurofarma Laboratórios S.A. Comprimido 1 mg e 2 mg
 cloxazolam Eurofarma Laboratórios S.A. Comprimido 1 mg e 2 mg cloxazolam Medicamento genérico Lei nº 9.787, de 1999 Comprimido FORMAS FARMACÊUTICAS E APRESENTAÇÕES: Embalagens com 20 e 30 comprimidos contendo
cloxazolam Eurofarma Laboratórios S.A. Comprimido 1 mg e 2 mg cloxazolam Medicamento genérico Lei nº 9.787, de 1999 Comprimido FORMAS FARMACÊUTICAS E APRESENTAÇÕES: Embalagens com 20 e 30 comprimidos contendo
ACULAR LS SOLUÇÃO OFTÁLMICA CETOROLACO TROMETAMOL 0.4%
 ACULAR LS SOLUÇÃO OFTÁLMICA CETOROLACO TROMETAMOL 0.4% Bula para o Paciente CCDS V 3.0 Jul 2012 0 APRESENTAÇÃO Solução Oftálmica Estéril Frasco plástico conta-gotas contendo 5 ml ou 10 ml de solução oftálmica
ACULAR LS SOLUÇÃO OFTÁLMICA CETOROLACO TROMETAMOL 0.4% Bula para o Paciente CCDS V 3.0 Jul 2012 0 APRESENTAÇÃO Solução Oftálmica Estéril Frasco plástico conta-gotas contendo 5 ml ou 10 ml de solução oftálmica
TROMBOFOB Pomada heparina sódica nicotinato de benzila
 MODELO DE BULA PARA O PACIENTE I) IDENTIFICAÇÃO DO MEDICAMENTO: TROMBOFOB Pomada heparina sódica nicotinato de benzila APRESENTAÇÃO Pomada dermatológica de: - 50U + 2mg: Embalagem com 1 bisnaga de 40 g.
MODELO DE BULA PARA O PACIENTE I) IDENTIFICAÇÃO DO MEDICAMENTO: TROMBOFOB Pomada heparina sódica nicotinato de benzila APRESENTAÇÃO Pomada dermatológica de: - 50U + 2mg: Embalagem com 1 bisnaga de 40 g.
TROMBOSE VENOSA PROFUNDA (TVP) E TROMBOEMBOLISMO PULMONAR (TEP)
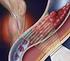 TROMBOSE VENOSA PROFUNDA (TVP) E TROMBOEMBOLISMO PULMONAR (TEP) - Fatores de risco: Idade superior a 40 anos Acidente vascular cerebral (isquêmico ou hemorrágico) Paralisia de membros inferiores Infarto
TROMBOSE VENOSA PROFUNDA (TVP) E TROMBOEMBOLISMO PULMONAR (TEP) - Fatores de risco: Idade superior a 40 anos Acidente vascular cerebral (isquêmico ou hemorrágico) Paralisia de membros inferiores Infarto
Betadine. Aché Laboratórios Farmacêuticos comprimido 16 mg e 24 mg
 Betadine Aché Laboratórios Farmacêuticos comprimido 16 mg e 24 mg MODELO DE BULA PARA O PACIENTE I) IDENTIFICAÇÃO DO MEDICAMENTO BETADINE dicloridrato de betaistina FORMA FARMACÊUTICA E APRESENTAÇÕES BETADINE
Betadine Aché Laboratórios Farmacêuticos comprimido 16 mg e 24 mg MODELO DE BULA PARA O PACIENTE I) IDENTIFICAÇÃO DO MEDICAMENTO BETADINE dicloridrato de betaistina FORMA FARMACÊUTICA E APRESENTAÇÕES BETADINE
VITAFER (sulfato ferroso) EMS S/A. comprimido revestido. 109 mg
 VITAFER (sulfato ferroso) EMS S/A comprimido revestido 109 mg I) IDENTIFICAÇÃO DO MEDICAMENTO Vitafer sulfato ferroso APRESENTAÇÃO Comprimido revestido de 109 mg. Embalagem contendo frasco com 50 comprimidos
VITAFER (sulfato ferroso) EMS S/A comprimido revestido 109 mg I) IDENTIFICAÇÃO DO MEDICAMENTO Vitafer sulfato ferroso APRESENTAÇÃO Comprimido revestido de 109 mg. Embalagem contendo frasco com 50 comprimidos
ACICLOVIR. Geolab Indústria Farmacêutica S/A Creme 50mg/g
 ACICLOVIR Geolab Indústria Farmacêutica S/A Creme 50mg/g MODELO DE BULA PARA O PACIENTE Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. aciclovir Medicamento
ACICLOVIR Geolab Indústria Farmacêutica S/A Creme 50mg/g MODELO DE BULA PARA O PACIENTE Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. aciclovir Medicamento
BULA PACIENTE AMINOLEX HALEX ISTAR
 BULA PACIENTE AMINOLEX HALEX ISTAR SOLUÇÃO INJETÁVEL 24 mg/ml Aminolex IDENTIFICAÇÃO DO MEDICAMENTO Aminolex FORMA FARMACÊUTICA E APRESENTAÇÕES Solução injetável 24mg/ml. Ampola de vidro de 10 ml Solução
BULA PACIENTE AMINOLEX HALEX ISTAR SOLUÇÃO INJETÁVEL 24 mg/ml Aminolex IDENTIFICAÇÃO DO MEDICAMENTO Aminolex FORMA FARMACÊUTICA E APRESENTAÇÕES Solução injetável 24mg/ml. Ampola de vidro de 10 ml Solução
ácido acetilsalicílico
 ácido acetilsalicílico EMS S/A Comprimido 100mg I IDENTIFICAÇÃO DO MEDICAMENTO ácido acetilsalicílico Medicamento genérico Lei n 9.787, de 1999 APRESENTAÇÕES Comprimidos Comprimidos contendo 100 mg de
ácido acetilsalicílico EMS S/A Comprimido 100mg I IDENTIFICAÇÃO DO MEDICAMENTO ácido acetilsalicílico Medicamento genérico Lei n 9.787, de 1999 APRESENTAÇÕES Comprimidos Comprimidos contendo 100 mg de
cloridrato de pioglitazona EMS S/A comprimido 15 mg/ 30 mg / 45 mg
 cloridrato de pioglitazona EMS S/A comprimido 15 mg/ 30 mg / 45 mg I) IDENTIFICAÇÃO DO MEDICAMENTO cloridrato de pioglitazona medicamento genérico Lei n 9.787, de 1999 APRESENTAÇÕES: cloridrato de pioglitazona
cloridrato de pioglitazona EMS S/A comprimido 15 mg/ 30 mg / 45 mg I) IDENTIFICAÇÃO DO MEDICAMENTO cloridrato de pioglitazona medicamento genérico Lei n 9.787, de 1999 APRESENTAÇÕES: cloridrato de pioglitazona
omeprazol Biosintética Farmacêutica Ltda. cápsulas 20 mg
 omeprazol Biosintética Farmacêutica Ltda. cápsulas 20 mg BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO omeprazol Medicamento genérico Lei nº 9.787, de
omeprazol Biosintética Farmacêutica Ltda. cápsulas 20 mg BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO omeprazol Medicamento genérico Lei nº 9.787, de
AVAXIM 80U vacina hepatite A (inativada) - 80U. A vacina hepatite A (inativada) - 80U - AVAXIM 80U deve ser administrada por VIA INTRAMUSCULAR.
 Modelo de Bula Página 1 de 6 AVAXIM 80U vacina hepatite A (inativada) - 80U FORMA FARMACÊUTICA E APRESENTAÇÕES Suspensão injetável. - Cartucho contendo uma seringa de 1 dose de 0,5mL; - Cartucho contendo
Modelo de Bula Página 1 de 6 AVAXIM 80U vacina hepatite A (inativada) - 80U FORMA FARMACÊUTICA E APRESENTAÇÕES Suspensão injetável. - Cartucho contendo uma seringa de 1 dose de 0,5mL; - Cartucho contendo
TYNEO. (paracetamol)
 TYNEO (paracetamol) Brainfarma Indústria Química e Farmacêutica S.A. Solução Oral 200mg/mL I - IDENTIFICAÇÃO DO MEDICAMENTO: TYNEO paracetamol APRESENTAÇÃO Solução oral gotas 200mg/mL: Embalagem com 1
TYNEO (paracetamol) Brainfarma Indústria Química e Farmacêutica S.A. Solução Oral 200mg/mL I - IDENTIFICAÇÃO DO MEDICAMENTO: TYNEO paracetamol APRESENTAÇÃO Solução oral gotas 200mg/mL: Embalagem com 1
ALLERGAN PRODUTOS FARMACÊUTICOS LTDA
 LACRIL ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril álcool polivinílico 1,4% BULA PARA O PACIENTE Lubrificante Ocular APRESENTAÇÃO Solução Oftálmica Estéril Frasco plástico conta-gotas
LACRIL ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril álcool polivinílico 1,4% BULA PARA O PACIENTE Lubrificante Ocular APRESENTAÇÃO Solução Oftálmica Estéril Frasco plástico conta-gotas
DDAVP Hemo Laboratórios Ferring acetato de desmopressina. IDENTIFICAÇÃO DO MEDICAMENTO DDAVP Hemo acetato de desmopressina
 DDAVP Hemo Laboratórios Ferring acetato de desmopressina IDENTIFICAÇÃO DO MEDICAMENTO DDAVP Hemo acetato de desmopressina APRESENTAÇÕES Solução Injetável de 15 mcg/ml de acetato de desmopressina disponível
DDAVP Hemo Laboratórios Ferring acetato de desmopressina IDENTIFICAÇÃO DO MEDICAMENTO DDAVP Hemo acetato de desmopressina APRESENTAÇÕES Solução Injetável de 15 mcg/ml de acetato de desmopressina disponível
BUDECORT Aqua budesonida
 BUDECORT Aqua budesonida I) IDENTIFICAÇÃO DO MEDICAMENTO BUDECORT Aqua budesonida APRESENTAÇÕES Suspensão em spray nasal de 32 mcg/dose em embalagens com um frasco contendo 120 doses. Suspensão em spray
BUDECORT Aqua budesonida I) IDENTIFICAÇÃO DO MEDICAMENTO BUDECORT Aqua budesonida APRESENTAÇÕES Suspensão em spray nasal de 32 mcg/dose em embalagens com um frasco contendo 120 doses. Suspensão em spray
cloridrato de loperamida Laboratório Globo Ltda. comprimidos 2 mg
 cloridrato de loperamida Laboratório Globo Ltda. comprimidos 2 mg cloridrato de loperamida Medicamento genérico Lei nº 9.787, de 1999 APRESENTAÇÕES Comprimidos de 2 mg em embalagem com 12 e 200 comprimidos.
cloridrato de loperamida Laboratório Globo Ltda. comprimidos 2 mg cloridrato de loperamida Medicamento genérico Lei nº 9.787, de 1999 APRESENTAÇÕES Comprimidos de 2 mg em embalagem com 12 e 200 comprimidos.
FINASTIL (finasterida)
 FINASTIL (finasterida) EMS SIGMA PHARMA LTDA Comprimido Revestido 5 mg IDENTIFICAÇÃO DO MEDICAMENTO FINASTIL finasterida APRESENTAÇÕES Comprimidos revestidos de 5 mg de finasterida acondicionados em embalagem
FINASTIL (finasterida) EMS SIGMA PHARMA LTDA Comprimido Revestido 5 mg IDENTIFICAÇÃO DO MEDICAMENTO FINASTIL finasterida APRESENTAÇÕES Comprimidos revestidos de 5 mg de finasterida acondicionados em embalagem
ENEMAPLEX fosfato de sódio monobásico monoidratado + fosfato de sódio dibásico heptaidratado. Forma farmacêutica: Solução de enema
 ENEMAPLEX fosfato de sódio monobásico monoidratado + fosfato de sódio dibásico heptaidratado Forma farmacêutica: Solução de enema 1 MODELO DE BULA ENEMAPLEX fosfato de sódio monobásico monoidratado + fosfato
ENEMAPLEX fosfato de sódio monobásico monoidratado + fosfato de sódio dibásico heptaidratado Forma farmacêutica: Solução de enema 1 MODELO DE BULA ENEMAPLEX fosfato de sódio monobásico monoidratado + fosfato
ANADOR PRT paracetamol 750 mg. Forma farmacêutica e apresentação Comprimidos 750 mg: embalagem com 20 e 256 comprimidos.
 ANADOR PRT paracetamol 750 mg Antitérmico e analgésico Forma farmacêutica e apresentação Comprimidos 750 mg: embalagem com 20 e 256 comprimidos. Outra forma farmacêutica e apresentação Solução oral: frasco
ANADOR PRT paracetamol 750 mg Antitérmico e analgésico Forma farmacêutica e apresentação Comprimidos 750 mg: embalagem com 20 e 256 comprimidos. Outra forma farmacêutica e apresentação Solução oral: frasco
CONCENTRAÇÃO 160 mg/ml de fosfato de sódio monobásico e 60 mg/ml de fosfato de sódio dibásico.
 L-ENEMA Fosfato de Sódio Monobásico, Fosfato de Sódio Dibásico. FORMA FARMACÊUTICA Solução retal APRESENTAÇÕES Linha Farma: Frasco graduado de polietileno de baixa densidade incolor, com cânula retal previamente
L-ENEMA Fosfato de Sódio Monobásico, Fosfato de Sódio Dibásico. FORMA FARMACÊUTICA Solução retal APRESENTAÇÕES Linha Farma: Frasco graduado de polietileno de baixa densidade incolor, com cânula retal previamente
mononitrato de isossorbida Biosintética Farmacêutica Ltda. comprimidos 20 mg 40 mg
 mononitrato de isossorbida Biosintética Farmacêutica Ltda. comprimidos 20 mg 40 mg BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO mononitrato de isossorbida
mononitrato de isossorbida Biosintética Farmacêutica Ltda. comprimidos 20 mg 40 mg BULA PARA PACIENTE Bula de acordo com a Resolução-RDC nº 47/2009 I- IDENTIFICAÇÃO DO MEDICAMENTO mononitrato de isossorbida
Propil* propiltiouracila
 Propil* propiltiouracila PARTE I IDENTIFICAÇÃO DO PRODUTO Nome: Propil* Nome genérico: propiltiouracila Forma farmacêutica e apresentação: Propil* 100 mg em embalagem contendo 30 comprimidos. USO ADULTO
Propil* propiltiouracila PARTE I IDENTIFICAÇÃO DO PRODUTO Nome: Propil* Nome genérico: propiltiouracila Forma farmacêutica e apresentação: Propil* 100 mg em embalagem contendo 30 comprimidos. USO ADULTO
Solugel e Solugel Plus peróxido de benzoíla 40 mg/g e 80 mg/g
 Solugel e Solugel Plus peróxido de benzoíla 40 mg/g e 80 mg/g Solugel e Solugel Plus peróxido de benzoíla APRESENTAÇÕES Solugel : Gel de peróxido de benzoíla 40mg/g (4%) em bisnaga contendo 45 g. Solugel
Solugel e Solugel Plus peróxido de benzoíla 40 mg/g e 80 mg/g Solugel e Solugel Plus peróxido de benzoíla APRESENTAÇÕES Solugel : Gel de peróxido de benzoíla 40mg/g (4%) em bisnaga contendo 45 g. Solugel
FRESHCLEAR ALLERGAN PRODUTOS FARMACÊUTICOS LTDA. Solução Oftálmica Estéril. cloridrato de fenilefrina 0,12% álcool polivinílico 1,4%
 FRESHCLEAR ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril cloridrato de fenilefrina 0,12% álcool polivinílico 1,4% BULA PARA O PACIENTE APRESENTAÇÕES Solução Oftálmica Estéril Frasco plástico
FRESHCLEAR ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril cloridrato de fenilefrina 0,12% álcool polivinílico 1,4% BULA PARA O PACIENTE APRESENTAÇÕES Solução Oftálmica Estéril Frasco plástico
LUMIGAN ALLERGAN PRODUTOS FARMACÊUTICOS LTDA
 LUMIGAN ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril bimatoprosta (0,03%) BULA PARA O PACIENTE Bula para o Paciente Pág. 1 de 7 APRESENTAÇÕES Solução Oftálmica Estéril Frasco plástico
LUMIGAN ALLERGAN PRODUTOS FARMACÊUTICOS LTDA Solução Oftálmica Estéril bimatoprosta (0,03%) BULA PARA O PACIENTE Bula para o Paciente Pág. 1 de 7 APRESENTAÇÕES Solução Oftálmica Estéril Frasco plástico
Nasoclean GlaxoSmithKline Brasil Ltda. Solução Nasal 9mg/mL
 Nasoclean GlaxoSmithKline Brasil Ltda. Solução Nasal 9mg/mL LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO I. IDENTIFICAÇÃO DO MEDICAMENTO Nasoclean Solução salina de água do mar APRESENTAÇÃO
Nasoclean GlaxoSmithKline Brasil Ltda. Solução Nasal 9mg/mL LEIA ATENTAMENTE ESTA BULA ANTES DE INICIAR O TRATAMENTO I. IDENTIFICAÇÃO DO MEDICAMENTO Nasoclean Solução salina de água do mar APRESENTAÇÃO
Sedalgina. Drágea 30mg+300mg+30mg
 Sedalgina Drágea 30mg+300mg+30mg MODELO DE BULA COM INFORMAÇÕES AO PACIENTE Sedalgina mucato de isometepteno dipirona cafeína APRESENTAÇÕES Drágea 30mg+300mg+30mg Embalagens contendo 20, 30, 60, e 200
Sedalgina Drágea 30mg+300mg+30mg MODELO DE BULA COM INFORMAÇÕES AO PACIENTE Sedalgina mucato de isometepteno dipirona cafeína APRESENTAÇÕES Drágea 30mg+300mg+30mg Embalagens contendo 20, 30, 60, e 200
Proctyl. Takeda Pharma Ltda. Supositório. 100 mg (policresuleno) + 27 mg (cloridrato de cinchocaína)
 Proctyl Takeda Pharma Ltda. Supositório 100 mg (policresuleno) + 27 mg (cloridrato de cinchocaína) BULA PARA PACIENTE RDC 47/2009 APRESENTAÇÕES Supositório retal de 100 mg (policresuleno) + 27 mg (cloridrato
Proctyl Takeda Pharma Ltda. Supositório 100 mg (policresuleno) + 27 mg (cloridrato de cinchocaína) BULA PARA PACIENTE RDC 47/2009 APRESENTAÇÕES Supositório retal de 100 mg (policresuleno) + 27 mg (cloridrato
APRESENTAÇÃO Creme vaginal de 10 mg/g: embalagem com 35 g + 6 aplicadores descartáveis.
 clotrimazol Medicamento Genérico, Lei nº 9.787, de 1999 APRESENTAÇÃO Creme vaginal de 10 mg/g: embalagem com 35 g + 6 aplicadores descartáveis. USO VAGINAL USO ADULTO COMPOSIÇÃO Cada grama de creme vaginal
clotrimazol Medicamento Genérico, Lei nº 9.787, de 1999 APRESENTAÇÃO Creme vaginal de 10 mg/g: embalagem com 35 g + 6 aplicadores descartáveis. USO VAGINAL USO ADULTO COMPOSIÇÃO Cada grama de creme vaginal
Icacort. Bayer S.A. Creme dermatológico. 10 mg/g de nitrato de isoconazol 1 mg/g de valerato de diflucortolona.
 Icacort Bayer S.A. Creme dermatológico 10 mg/g de nitrato de isoconazol 1 mg/g de valerato de diflucortolona. 1 Icacort nitrato de isoconazol valerato de diflucortolona APRESENTAÇÕES Cartucho contendo
Icacort Bayer S.A. Creme dermatológico 10 mg/g de nitrato de isoconazol 1 mg/g de valerato de diflucortolona. 1 Icacort nitrato de isoconazol valerato de diflucortolona APRESENTAÇÕES Cartucho contendo
Sulfato de Terbutalina. Hipolabor Farmacêutica Ltda. Solução Injetável. 0,5mg/mL
 Sulfato de Terbutalina Hipolabor Farmacêutica Ltda. Solução Injetável 0,5mg/mL 1 sulfato de terbutalina Medicamento genérico Lei 9.787, de 1999 NOME GENÉRICO: Sulfato de terbutalina FORMA FARMACÊUTICA:
Sulfato de Terbutalina Hipolabor Farmacêutica Ltda. Solução Injetável 0,5mg/mL 1 sulfato de terbutalina Medicamento genérico Lei 9.787, de 1999 NOME GENÉRICO: Sulfato de terbutalina FORMA FARMACÊUTICA:
TEXTO DE BULA LORAX. Lorax 1 ou 2 mg em embalagens contendo 20 ou 30 comprimidos. Cada comprimido contém 1 ou 2 mg de lorazepam respectivamente.
 TEXTO DE BULA LORAX I) IDENTIFICAÇÃO DO MEDICAMENTO Lorax lorazepam APRESENTAÇÕES Lorax 1 ou 2 mg em embalagens contendo 20 ou 30 comprimidos. Cada comprimido contém 1 ou 2 mg de lorazepam respectivamente.
TEXTO DE BULA LORAX I) IDENTIFICAÇÃO DO MEDICAMENTO Lorax lorazepam APRESENTAÇÕES Lorax 1 ou 2 mg em embalagens contendo 20 ou 30 comprimidos. Cada comprimido contém 1 ou 2 mg de lorazepam respectivamente.
Embalagem com frasco contendo 100 ml de xarope + 1 copo medida. Cada ml de xarope contém 0,3 mg de sulfato de terbutalina.
 BRICANYL Broncodilatador sulfato de terbutalina I) IDENTIFICAÇÃO DO MEDICAMENTO BRICANYL Broncodilatador sulfato de terbutalina APRESENTAÇÃO Embalagem com frasco contendo 100 ml de xarope + 1 copo medida.
BRICANYL Broncodilatador sulfato de terbutalina I) IDENTIFICAÇÃO DO MEDICAMENTO BRICANYL Broncodilatador sulfato de terbutalina APRESENTAÇÃO Embalagem com frasco contendo 100 ml de xarope + 1 copo medida.
desloratadina EMS S/A Comprimido Revestido 5 mg
 desloratadina EMS S/A Comprimido Revestido 5 mg IDENTIFICAÇÃO DO MEDICAMENTO desloratadina FORMA FARMACÊUTICA E APRESENTAÇÃO Comprimidos revestidos de 5 mg. Embalagem contendo 10 ou 30 comprimidos revestidos.
desloratadina EMS S/A Comprimido Revestido 5 mg IDENTIFICAÇÃO DO MEDICAMENTO desloratadina FORMA FARMACÊUTICA E APRESENTAÇÃO Comprimidos revestidos de 5 mg. Embalagem contendo 10 ou 30 comprimidos revestidos.
Anexo A ACFOL CAZI QUIMICA FARMACÊUTICA IND. E COM. LTDA. Comprimidos e Solução Oral (gotas) 5 mg
 Anexo A ACFOL CAZI QUIMICA FARMACÊUTICA IND. E COM. LTDA Comprimidos e Solução Oral (gotas) 5 mg MODELO DE BULA (adequação à RDC n.º 47/09 Republicada em DOU 19/01/2010) INFORMAÇÕES AO PACIENTE ACFOL I
Anexo A ACFOL CAZI QUIMICA FARMACÊUTICA IND. E COM. LTDA Comprimidos e Solução Oral (gotas) 5 mg MODELO DE BULA (adequação à RDC n.º 47/09 Republicada em DOU 19/01/2010) INFORMAÇÕES AO PACIENTE ACFOL I
ALIVIUM ibuprofeno Gotas. ALIVIUM gotas é indicado para uso oral. ALIVIUM gotas 100 mg/ml apresenta-se em frascos com 20 ml.
 ALIVIUM ibuprofeno Gotas FORMAS FARMACÊUTICAS/APRESENTAÇÕES: ALIVIUM gotas é indicado para uso oral. ALIVIUM gotas 100 mg/ml apresenta-se em frascos com 20 ml. USO ADULTO E PEDIÁTRICO (acima de 6 meses
ALIVIUM ibuprofeno Gotas FORMAS FARMACÊUTICAS/APRESENTAÇÕES: ALIVIUM gotas é indicado para uso oral. ALIVIUM gotas 100 mg/ml apresenta-se em frascos com 20 ml. USO ADULTO E PEDIÁTRICO (acima de 6 meses
Micoral Laboratório Farmacêutico Elofar Ltda. Creme dermatológico 20 mg/g
 Micoral Laboratório Farmacêutico Elofar Ltda. Creme dermatológico 20 mg/g MICORAL cetoconazol APRESENTAÇÃO Creme em bisnaga de 30 g, contendo 20 mg/g de cetoconazol. USO TÓPICO USO ADULTO E PEDIÁTRICO
Micoral Laboratório Farmacêutico Elofar Ltda. Creme dermatológico 20 mg/g MICORAL cetoconazol APRESENTAÇÃO Creme em bisnaga de 30 g, contendo 20 mg/g de cetoconazol. USO TÓPICO USO ADULTO E PEDIÁTRICO
FLATICONA (dimeticona) BELFAR LTDA. Gotas 75 mg/ml
 FLATICONA (dimeticona) BELFAR LTDA. Gotas 75 mg/ml FLATICONA Dimeticona APRESENTAÇÕES Frasco contendo 10 ml e 20 ml com 75 mg/ml. USO ORAL USO ADULTO E PEDIÁTRICO COMPOSIÇÃO Cada ml de FLATICONA contém:
FLATICONA (dimeticona) BELFAR LTDA. Gotas 75 mg/ml FLATICONA Dimeticona APRESENTAÇÕES Frasco contendo 10 ml e 20 ml com 75 mg/ml. USO ORAL USO ADULTO E PEDIÁTRICO COMPOSIÇÃO Cada ml de FLATICONA contém:
LORAX lorazepam I - IDENTIFICAÇÃO DO MEDICAMENTO. Nome comercial: Lorax Nome genérico: lorazepam
 LORAX lorazepam I - IDENTIFICAÇÃO DO MEDICAMENTO Nome comercial: Lorax Nome genérico: lorazepam APRESENTAÇÕES Lorax 1 mg ou 2 mg em embalagens contendo 30 comprimidos. VIA DE ADMINISTRAÇÃO: USO ORAL USO
LORAX lorazepam I - IDENTIFICAÇÃO DO MEDICAMENTO Nome comercial: Lorax Nome genérico: lorazepam APRESENTAÇÕES Lorax 1 mg ou 2 mg em embalagens contendo 30 comprimidos. VIA DE ADMINISTRAÇÃO: USO ORAL USO
Fragmin dalteparina sódica. Fragmin solução injetável 12500 UI/mL (anti-xa) em embalagem contendo 10 seringas pré-enchidas com 0,2 ml (2500 UI).
 Fragmin dalteparina sódica I IDENTIFICAÇÃO DO PRODUTO Nome comercial: Fragmin Nome genérico: dalteparina sódica APRESENTAÇÕES Fragmin solução injetável 12500 UI/mL (anti-xa) em embalagem contendo 10 seringas
Fragmin dalteparina sódica I IDENTIFICAÇÃO DO PRODUTO Nome comercial: Fragmin Nome genérico: dalteparina sódica APRESENTAÇÕES Fragmin solução injetável 12500 UI/mL (anti-xa) em embalagem contendo 10 seringas
BRICANYL BRONCODILATADOR sulfato de terbutalina. AstraZeneca do Brasil Ltda. Xarope. 0,3 mg/ml
 BRICANYL BRONCODILATADOR sulfato de terbutalina AstraZeneca do Brasil Ltda. Xarope 0,3 mg/ml BRICANYL Broncodilatador sulfato de terbutalina I) IDENTIFICAÇÃO DO BRICANYL Broncodilatador sulfato de terbutalina
BRICANYL BRONCODILATADOR sulfato de terbutalina AstraZeneca do Brasil Ltda. Xarope 0,3 mg/ml BRICANYL Broncodilatador sulfato de terbutalina I) IDENTIFICAÇÃO DO BRICANYL Broncodilatador sulfato de terbutalina
acetilcisteína União Química Farmacêutica Nacional S.A xarope 20 mg/ml
 acetilcisteína União Química Farmacêutica Nacional S.A xarope 20 mg/ml acetilcisteína Medicamento Genérico, Lei nº 9.787, de 1999. Xarope IDENTIFICAÇÃO DO PRODUTO FORMA FARMACÊUTICA E APRESENTAÇÃO Xarope
acetilcisteína União Química Farmacêutica Nacional S.A xarope 20 mg/ml acetilcisteína Medicamento Genérico, Lei nº 9.787, de 1999. Xarope IDENTIFICAÇÃO DO PRODUTO FORMA FARMACÊUTICA E APRESENTAÇÃO Xarope
