QUÍMICA Conceitos Fundamentais de Química
|
|
|
- Ana Vitória Zagalo Marreiro
- 5 Há anos
- Visualizações:
Transcrição
1 Conceitos Fundamentais de Química São Paulo do Potengi/RN
2 O que devemos aprender nesta aula: Entender e compreender alguns conceitos fundamentais da química; Conhecer a matéria e sua classificação; Identificar os tipos de misturas e como elas se separam; Saber mais sobre as propriedades físicas e químicas da matéria; Diferenciar calor de temperatura;
3 Sumário 1. Conceitos Fundamentais de Química 1.1 A matéria e sua classificação; 1.2 Misturas e processos de separação; 1.3 Propriedades físicas e químicas; 1.4 Energia, calor, temperatura; 2. Exercícios; 3. Síntese da aula; 4. Referências bibliográficas.
4 1. Conceitos Fundamentais de Química De quê o UNIVERSO é formado? Matéria + Energia Tudo que tem massa e ocupa um lugar no espaço Capacidade de realizar trabalho/ação VOCÊ 4
5 1. Conceitos Fundamentais de Química O que é Química e o que ela estuda? É uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. 5
6 1. Conceitos Fundamentais de Química MATÉRIA, CORPO E OBJETO 6
7 1. Conceitos Fundamentais de Química ESTRUTURA DA MATÉRIA A matéria é formada por moléculas, que por sua vez são formadas por elementos que são constituídos de partículas minúsculas chamadas de átomos. átomo elemento molécula matéria 7
8 1. Conceitos Fundamentais de Química 8
9 Vídeo sobre Átomo 9
10 1.1 A matéria e sua classificação Matéria Substância São aquelas formadas por apenas uma variedade de molécula. Ou seja, todas as moléculas são iguais. Mistura É uma junção de duas ou mais substâncias puras diferentes. Simples Composta Homogênea AR Heterogênea ÁGUA + AREIA 10 solução
11 1.1 A matéria e sua classificação Substância 11
12 1.1 A matéria e sua classificação Substância SUBSTÂNCIA PURA FÓRMULA MOLECULAR CLASSIFICAÇÃO cloro Cl 2 simples gás carbônico CO 2 composta ácido nítrico HNO 3 composta enxofre S 8 simples sacarose C 12 H 22 O 11 composta cobre Cu simples ácido sulfúrico H 2 SO 4 composta glicose C 6 H 12 O 6 composta nitrogênio N 2 simples hélio He simples 12
13 1.1 A matéria e sua classificação Mistura Se a matéria não é totalmente uniforme, então ela é uma mistura heterogênea. Se a matéria é totalmente uniforme, ela é homogênea. Se a matéria homogênea pode ser separada por meios físicos, então ela é uma mistura. Se a matéria homogênea não pode ser separada por meios físicos, então ela é uma substância pura. 13
14 Vídeo sobre Substâncias 14
15 Vamos Exercitar?! 1) As substâncias químicas podem ser classificadas em simples ou compostas. Indique a alternativa que apresenta três substâncias simples e duas compostas, respectivamente. a) H 2 O, Hg, HI, Fe, H 2 S b) Au, O 2, CO 2, HCl, NaCl, c) S, O 2, O 3, CH 4, CO 2 d) H 2 SO 4, Cu, Fe, H 2, O 2 e) Au, Ag, Cl 2, H 2 CO 3, H 2 15
16 Vamos Exercitar?! 2) (Unicastelo) Considere os seguintes produtos: 1 pedra de granito 1 copo de água mineral 1 barra de ouro 1 balão cheio de ar 1 colher de cloreto de sódio São misturas homogêneas: a) a pedra de granito e o ar contido no balão b) a água mineral e o ar contido no balão c) a barra de ouro e a água mineral d) a pedra de granito e o cloreto de sódio e) a barra de ouro e o cloreto de sódio Pedra de granito: mistura, por ser composta por quartzo, feldspato e mica, e heterogênea, pois cada um desses componentes apresenta uma coloração diferente. Barra de ouro: substância simples. Colher de cloreto de sódio: substância composta (sódio e cloro). 16
17 Vamos Exercitar?! 3) Considere os sistemas a seguir, em que os átomos são representados por esferas: I II III IV Determine onde encontramos: a) Substância pura; (I e IV) b) Mistura; (II e III) c) Somente substância simples; (I) d) Somente substância composta. (IV) 17
18 Vamos Exercitar?! 4) Considere apenas o sistema III e determine: I II III IV a) O número de átomos presentes; (10) b) O número de elementos químicos; (3) c) O número de moléculas; (4) d) O número de tipos de substâncias; (3) e) O número de tipos de substâncias binárias; f) O número de substâncias diatômicas. (2) (1) 18
19 19
20 1.2 Misturas e processos de separação O que é isso? É um conjunto de processos FÍSICOS que visam separar os componentes de uma mistura SEM alterá-los. 20
21 1.2 Misturas e processos de separação Fases e Componentes Fases é o aspecto visual uniforme. Componentes - Espécies químicas presentes na mistura. 21
22 1.2 Misturas e processos de separação Esquema geral simplificado: Filtração Misturas Heterogênea Decantação Funil de separação Centrifugação Catação Flotação Separação Magnética Homogênea 22 Destilação Cristalização/Evaporação
23 MISTURAS HETEROGÊNEAS 23
24 1.2 Misturas e processos de separação Filtração Filtração simples: se faz através de uma superfície porosa chamada filtro, o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa. Filtração à vácuo: Ocorre a aceleração pela rarefação do ar, abaixo do filtro. Nas filtrações sob pressão reduzida, usa-se funil com fundo de porcelana porosa (funil de Büchner) 24
25 1.2 Misturas e processos de separação Decantação Decantação: Deixa-se a mistura em repouso até que o componente sólido tenha-se depositado completamente (sedimentação). Remove-se em seguida, o líquido, entornando-se cuidadosamente o frasco, ou com auxílio de um sifão (sifonação). 25
26 1.2 Misturas e processos de separação Funil de separação Funil de separação: é muito utilizado para separar líquidos imiscíveis (não se misturam). Coloca-se a mistura em um funil de separação, quando a superfície de separação das camadas líquidas estiver bem nítida, abre-se a torneira e deixa-se escoar o líquido da camada inferior (maior densidade). 26
27 1.2 Misturas e processos de separação Centrifugação Centrifugação: é usada para acelerar a sedimentação do sólido, como ocorre de rotina na realização de exames de sangue, e separação dos componentes do leite. 27
28 1.2 Misturas e processos de separação Catação Catação: método artesanal de separação de sólidos. Exemplo: através da catação, se separa os feijões bons dos ruins, antes de cozinhá-los. 28
29 1.2 Misturas e processos de separação Flotação Flotação: Trata-se a mistura com um líquido de densidade intermediária em relação às dos componentes. O componente menos denso que o líquido flutuará, separando-se assim do componente mais denso, que se depositará. O líquido empregado não deve, contudo, dissolver os componentes. 29
30 1.2 Misturas e processos de separação Separação Magnética Separação magnética: Só pode ser usada quando um dos componentes é atraído por um imã. 30
31 MISTURAS HOMOGÊNEAS 31
32 1.2 Misturas e processos de separação Destilação Destilação simples: O princípio do processo consiste em aquecer a mistura (Sólido- Líquido) até a ebulição; com isso o componente líquido separa-se do sistema sob a forma de vapor, que a seguir é resfriado, condensando-se, e o líquido é recolhido em outro recipiente. 32
33 1.2 Misturas e processos de separação Destilação Destilação fracionada: Aquecendo-se a mistura (líquido-líquido) em um balão de destilação, os líquidos destilam-se na ordem crescente de seus pontos de ebulição e podem ser separados. O petróleo é separado em suas frações por destilação fracionada. 33
34 1.2 Misturas e processos de separação Cristalização/Evaporação Evaporação ou Cristalização: consiste na evaporação do solvente e consequente cristalização dos sais outrora diluídos. Exemplos: salinas. 34
35 1.2 Misturas e processos de separação Qual a diferença entre evaporação e destilação simples? 35
36 1.2 Misturas e processos de separação Na EVAPORAÇÃO ocorre a perda de um dos componentes, já na DESTILAÇÃO SIMPLES todos os componentes utilizados na mistura são recuperados. 36
37 Vamos Exercitar?! 5) 37
38 Vamos Exercitar?! 6) 7) 8) 38
39 Vamos Exercitar?! 9) 39
40 Vamos Exercitar?! 10) 40
41 Vamos Exercitar?! 11) 41
42 1.3 Propriedades físicas e químicas As substâncias têm propriedades características; são estas propriedades que permitem distingui-las umas das outras. As propriedades características de uma substância podem ser: 42
43 1.3 Propriedades físicas e químicas Propriedades Físicas Gerais Massa Extensão Impenetrabilidade Divisibilidade Elasticidade Maleabilidade Ductilidade Específicas Densidade P.F e P.S P.E e P.C Organoléptica Cor Cheiro Sabor Brilho Dureza 43
44 1.3 Propriedades físicas e químicas Propriedades Físicas Gerais Massa Extensão (Volume) Divisibilidade Quantidade de matéria contida num corpo Propriedade que a matéria tem de ocupar um lugar no espaço A matéria de ser dividida em partes menores de modo contínuo 44
45 1.3 Propriedades físicas e químicas Propriedades Físicas Gerais Impenetrabilidade Dois corpos não podem ocupar o mesmo lugar no espaço 45
46 1.3 Propriedades físicas e químicas Propriedades Físicas Gerais Elasticidade Maleabilidade Ductilidade Um corpo sofre deformação, quando submetido à tração, e retornar parcial ou totalmente à forma original Propriedade de ser redutível a lâminas finas 46 É a capacidade de ser deformado, esticado e dobrado, sem rachar e sem perder sua resistência. Ex.: ouro, prata, cobre etc.
47 1.3 Propriedades físicas e químicas Propriedades Físicas Específicas Ponto de Fusão e Solidificação Ponto de Ebulição e Condensação Densidade ou Massa Específica As propriedades específicas caracterizam cada tipo de substância. 47
48 1.3 Propriedades físicas e químicas LÍQUIDO SUBLIMAÇÃO SÓLIDO 48 GASOSO
49 Mudanças de estados físicos
50 Ponto de Fusão e Solidificação Ponto de Fusão é a temperatura em que uma substância muda do estado sólido para o estado líquido. SÓLIDO LÍQUIDO Ponto de Solidificação corresponde ao processo inverso, embora as temperaturas sejam equivalentes. LÍQUIDO 50 SÓLIDO
51 Ponto de Ebulição e Condensação Ponto de Ebulição é a temperatura em que uma substância muda do estado líquido para o estado gasoso. LÍQUIDO GASOSO Ponto de condensação corresponde ao processo inverso, embora as temperaturas sejam equivalentes. GASOSO 51 LÍQUIDO
52 tes-of-matter/latest/states-ofmatter_pt_br.html
53 1.3 Propriedades físicas e químicas Propriedades Físicas Específicas Densidade ou Massa Específica É uma propriedade específica de cada material que serve para identificar uma substância. Essa grandeza pode ser enunciada da seguinte forma: é a relação entre a massa (m) e o volume (v) de determinado material (sólido, líquido ou gasoso). 53
54 1.3 Propriedades físicas e químicas Propriedades Físicas Organoléptica 54
55 1.3 Propriedades físicas e químicas Propriedades Químicas Combustibilidade Oxirredução Explosão Efervescência 55
56 Vamos Exercitar?! 12) (UFMG) Uma amostra de uma substância pura X teve algumas de suas propriedades determinadas. Todas as alternativas apresentam propriedades que são úteis para identificar essa substância, exceto: a) Densidade. b) massa da amostra. c) solubilidade em água. d) temperatura de ebulição. e) temperatura de fusão. 13) (Fuvest-SP) Quais propriedades a seguir são as mais indicadas para verificar se é pura uma certa amostra sólida de uma substância conhecida? a) Cor e densidade. b) Cor e massa. c) Ponto de fusão e densidade. d) Cor e ponto de fusão. e) Densidade e volume. 56
57 Vamos Exercitar?! 14) Qual das propriedades físicas abaixo é específica da matéria? a) Cor b) Massa c) Volume d) Ponto de Fusão e) Temperatura 15) Em condições normais, o ponto de ebulição da água é 100 C. Podemos afirmar que esta é uma propriedade: a) específica b) genérica c) funcional d) geral e) organoléptica. 57
58 Vamos Exercitar?! 16) A seguir são apresentadas algumas propriedades do cloreto de sódio (NaCl sal de cozinha): I. Sólido; II. Cristalizado no sistema cúbico com faces centradas; III. Branco; IV. Com ponto de fusão a 800,4 C; V. Com ponto de ebulição a 1413 C; VI. Com solubilidade de 357 g/l a 25 C; VII. Com sabor salgado; VIII. Inodoro; IX. Em água, origina solução neutra; X. No estado sólido, reage com ácido sulfúrico concentrado, produzindo gás clorídrico. São propriedades especificas: a) somente I, III e VIII. b) somente IV, V e VI. c) somente III, V e VII d) somente I e X. e) nenhuma das citadas. 58
59 Vamos Exercitar?! 17) (PUC-MG) Em um laboratório de química, foram encontrados cinco recipientes sem rótulo, cada um contendo uma substância pura líquida e incolor. Para cada uma dessas substâncias, um estudante determinou as seguintes propriedades: 1. Ponto de ebulição 2. Massa 3. Volume 4. Densidade Assinale as propriedades que podem permitir ao estudante a identificação desses líquidos. a) 1 e 2 b) 1 e 3 c) 2 e 4 d) 1 e 4 59
60 1.4 Energia, calor, temperatura Energia é a capacidade de algo de realizar trabalho, ou seja, gerar força num determinado corpo, substância ou sistema físico. Formas de energia Energia Cinética: relacionada com o movimento dos corpos; Energia Térmica: relacionada com o calor e as altas temperaturas; Energia Nuclear: energia libertada quando ocorre uma reação nuclear. Energia Química: energia que está armazenada em todas as matérias com ligações químicas, e que é libertada quando ocorre a quebra dessas ligações; 60 Energia Solar: alternativa renovável de fornecimento de energia para diversas utilidades através da captação dos raios solares; Energia Elétrica: pode ser produzida a partir de usinas hidroelétricas ou através de fontes renováveis, como a energia solar e eólica. Energia Eólica: forma de energia alternativa e que provém dos ventos;
61 1.4 Energia, calor, temperatura Energia Térmica Calor Flui de um corpo (com maior temperatura) ao outro (de menor temperatura) quando há diferença de temperatura entre ambos. Cinética Temperatura Movimento ou agitação das moléculas e o estado térmico de um corpo (quente ou frio). Caracteriza a agitação das moléculas de um corpo Designa a troca de energia entre corpos 61
62 1.4 Energia, calor, temperatura Convecção térmica ocorre entre líquidos e gases; é o que acontece com o aquecimento das mãos molhada, aonde criam-se "correntes de convecção" e a água que está próxima do fogo sobe, enquanto a que está fria desce. Propagação do Calor Condução térmica é dada pela agitação das moléculas, por exemplo, ao segurar uma barra de ferro e aquecer a outra extremidade Irradiação térmica é por meio de ondas eletromagnéticas, sem que seja necessário o contato entre os corpos, por exemplo, se aquecer perto de uma lareira. 62
63 1.4 Energia, calor, temperatura Temperatura Para medir a temperatura é necessário um aparelho chamado termômetro (feito de mercúrio), cujo valor da pode ser apresentado nas escalas: Celsius ( C), kelvin (K) ou Fahrenheit ( F). 63
64 Síntese da aula Matéria Mistura Substância Heterogênea ÁGUA + AREIA Simples Composta Homogênea AR Átomos e moléculas Separação Destilação Filtração Decantação Cristalização/Evaporação Centrifugação Separação Funil de separação Catação Separação Magnética Sublimação
65 Síntese da aula Propriedades Físicas Químicas Gerais Massa Extensão Impenetrabilidade Divisibilidade Elasticidade Maleabilidade Ductilidade Específicas Densidade P.F e P.S P.E e P.C Organoléptica Cor Cheiro Sabor Brilho Dureza Combustibilidade Explosão Oxirredução Efervescência
66 Síntese da aula Energia é a capacidade de algo de realizar trabalho Térmica Calor Designa a troca de energia entre corpos Cinética Temperatura Caracteriza a agitação das moléculas de um corpo
67 Lista de Exercícios 67
68 Referências bibliográficas CANTO, E. L.; PERUZZO, F. M. Química na abordagem do cotidiano. v. 1, Editora Moderna FELTRE, R. Química Geral. v. 1. 7ª ed. São Paulo: Moderna, MACHADO, A. H.; MORTIMER, E. F.; Química: Ensino Médio. v. 1. 2ª ed. São Paulo: Editora Scipione, REIS, M. Química. v. 1. 2ª ed. São Paulo: Ática, USBERCO, J. Química. 5º ed. São Paulo: Saraiva, Volume Único. 68
Separação de misturas
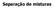 Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
Separação de misturas Filtração: A separação se faz através de uma superfície porosa chamada filtro; o componente sólido ficará retido sobre a sua superfície, separando-se assim do líquido que atravessa.
MÉTODOS DE SEPARAÇÃO DE MISTURAS. 9º ano
 MÉTODOS DE SEPARAÇÃO DE MISTURAS 9º ano Separações de Misturas são utilizadas para decompor misturas de substâncias em um sistema qualquer nos dois ou mais componentes originais. Podem ser para separar
MÉTODOS DE SEPARAÇÃO DE MISTURAS 9º ano Separações de Misturas são utilizadas para decompor misturas de substâncias em um sistema qualquer nos dois ou mais componentes originais. Podem ser para separar
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
PROCESSOS DE SEPARAÇÃO. Professor Cassio Pacheco
 PROCESSOS DE SEPARAÇÃO Professor Cassio Pacheco SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido
PROCESSOS DE SEPARAÇÃO Professor Cassio Pacheco SEPARAÇÃO DE MISTURAS HETEROGÊNEAS (Processos mecânicos de separação) Sistema sólido - sólido Separação magnética: Separa misturas do tipo sólido-sólido
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK
 PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
Apostila de Química 12 A Matéria
 Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES. Prof a. Giselle Blois. Estudo da matéria: substâncias, misturas, processos de separação Parte 2
 QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria.
 O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
O Que é Química? Pra que serve a Química?²
 O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
PROCESSOS DE SEPARAÇÃO. Prof. Ms. George Verçoza
 PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
Separação de Misturas
 Separação de Misturas Letícia Silva 1 Linguagem Científica Na ciência se faz necessário o uso de uma linguagem onde o significado das palavras não deixa margem de dúvidas ou interpretações diferentes.
Separação de Misturas Letícia Silva 1 Linguagem Científica Na ciência se faz necessário o uso de uma linguagem onde o significado das palavras não deixa margem de dúvidas ou interpretações diferentes.
PROCESSOS DE SEPARAÇÃO. Jeosafá Lima
 PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
PROCESSOS DE SEPARAÇÃO Jeosafá Lima Misturas homogêneas e heterogêneas Uma mistura é constituída por duas ou mais substâncias, sejam elas simples ou compostas. https://www.youtube.com/watch?v=6jcxdhovkcm
Processos físicos de separação de misturas
 Processos físicos de separação de misturas Misturas heterogêneas sólido-sólido Catação Peneiração Flutuação Separação Magnética Dissolução Fracionada Sublimação CATAÇÃO Baseia-se na identificação visual
Processos físicos de separação de misturas Misturas heterogêneas sólido-sólido Catação Peneiração Flutuação Separação Magnética Dissolução Fracionada Sublimação CATAÇÃO Baseia-se na identificação visual
LOUCOS POR QUÍMICA. PROF. Neif Nagib
 LOUCOS POR QUÍMICA PROF. Neif Nagib SEPARAÇÃO DE MISTURAS Prof. Neif Nagib CATAÇÃO É um método rudimentar baseado na diferença de tamanho e aspecto das partículas de uma mistura de sólidos granulados.
LOUCOS POR QUÍMICA PROF. Neif Nagib SEPARAÇÃO DE MISTURAS Prof. Neif Nagib CATAÇÃO É um método rudimentar baseado na diferença de tamanho e aspecto das partículas de uma mistura de sólidos granulados.
Tratamento de água. Adaptado de Luciana de Araújo
 Tratamento de água Adaptado de Luciana de Araújo A Química está presente no tratamento da água que chega nas nossas casas? Se sim, como? Estados físicos da água Mudança de estado físico No vídeo... Ouvimos
Tratamento de água Adaptado de Luciana de Araújo A Química está presente no tratamento da água que chega nas nossas casas? Se sim, como? Estados físicos da água Mudança de estado físico No vídeo... Ouvimos
SEPARAÇÃO DE MISTURAS
 SEPARAÇÃO DE MISTURAS Métodos de separação de misturas HETEROGÊNEAS SÓLIDO SÓLIDO: Catação Ventilação Levigação Separação magnética Dissolução fracionada Peneiração Flotação SÓLIDO LÍQUIDO: Decantação
SEPARAÇÃO DE MISTURAS Métodos de separação de misturas HETEROGÊNEAS SÓLIDO SÓLIDO: Catação Ventilação Levigação Separação magnética Dissolução fracionada Peneiração Flotação SÓLIDO LÍQUIDO: Decantação
d) Separação Magnética: Esse processo é empregado quando um dos componentes da mistura é atraído por um imã.
 8. PROCESSOS DE SEPARAÇÃO DE MISTURAS A natureza comporta uma imensa mistura de substancias. A maioria dos materiais que utilizamos no cotidiano é composta de misturas. Na maioria das vezes o que interessa,
8. PROCESSOS DE SEPARAÇÃO DE MISTURAS A natureza comporta uma imensa mistura de substancias. A maioria dos materiais que utilizamos no cotidiano é composta de misturas. Na maioria das vezes o que interessa,
CIÊNCIAS 9º Ano Ensino Fundamental
 CIÊNCIAS 9º Ano Ensino Fundamental QUÍMICA Densidade É uma propriedade específica da matéria que mede a relação entre a massa e o volume de um material, a uma dada pressão e temperatura. No SI (Sistema
CIÊNCIAS 9º Ano Ensino Fundamental QUÍMICA Densidade É uma propriedade específica da matéria que mede a relação entre a massa e o volume de um material, a uma dada pressão e temperatura. No SI (Sistema
SIMPLES SUBSTÂNCIA PURA COMPOSTA HOMOGÊNEO MISTURA HOMOGÊNEA SISTEMA SUBSTÂNCIA PURA HETEROGÊNEO MISTURA HETEROGÊNEA
 Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
SEPARAÇÃO DE MISTURAS
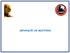 SEPARAÇÃO DE MISTURAS Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias. Água do mar Não apresenta muita utilidade H 2 O NaCl Apresentam inúmeras aplicações
SEPARAÇÃO DE MISTURAS Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias. Água do mar Não apresenta muita utilidade H 2 O NaCl Apresentam inúmeras aplicações
Prof. José Valter SEPARAÇÃO DE MISTURAS
 1 Separação de misturas heterogêneas: LEVIGAÇÃO É usada para componentes de misturas de sólidos, quando um dos componentes é facilmente arrastado pelo líquido. Separação do ouro das areias auríferas Separação
1 Separação de misturas heterogêneas: LEVIGAÇÃO É usada para componentes de misturas de sólidos, quando um dos componentes é facilmente arrastado pelo líquido. Separação do ouro das areias auríferas Separação
Exercícios Métodos de Separação. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017
 Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
La Salle Águas Claras 9º ano. Propriedades da Matéria
 La Salle Águas Claras 9º ano Propriedades da Matéria Matéria Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Uma porção delimitada de matéria recebe
La Salle Águas Claras 9º ano Propriedades da Matéria Matéria Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Uma porção delimitada de matéria recebe
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas:
 Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
Gabarito: Lista Classificação de Sistemas Químicos e Separação de Misturas: Resposta da questão 1: a) Cromo (Cr), manganês (Mn), alumínio ( (A l ) ) e Ferro (Fe). b) A distribuição: 2 2 6 2 6 2 5 1s 2s
COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROFESSOR: JOÃO MEDEIROS
 COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: JOÃO MEDEIROS 2012 Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias.
COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: JOÃO MEDEIROS 2012 Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias.
Equipamentos e Técnicas laboratoriais: Amostragem e separação de misturas
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA CÂMPUS LAGES Equipamentos e Técnicas laboratoriais: Amostragem e separação de
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA CÂMPUS LAGES Equipamentos e Técnicas laboratoriais: Amostragem e separação de
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
Química B Intensivo V. 1
 1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
1 Química B Intensivo V. 1 Exercícios 01) B 02) B a) Falsa. O leite in natura é uma mistura heterogênea e não apresenta as mesmas propriedades em toda a extensão da amostra. b) Verdadeira. A gelatina é
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS.
 SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente:
 2 1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente: a) decantação e liquefação. b) sedimentação e destilação. c) filtração e sublimação.
2 1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente: a) decantação e liquefação. b) sedimentação e destilação. c) filtração e sublimação.
26/08/15 SUBSTÂNCIAS E MISTURAS. Prof. Ms. Mayanderson (Xuxu)
 SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
Composição Densidade (g/mol) Carvão 0,3 0,6 Ossos 1,7 2,0 Areia 2,0 2,4 Solo 2,6 2,8 Pedras 2,6 5,0
 QUÍMICA Arqueologistas usam diferenças de densidade para separar as misturas que eles obtêm por escavação. Indique a opção correta para uma mostra que contém a seguinte composição: Composição Densidade
QUÍMICA Arqueologistas usam diferenças de densidade para separar as misturas que eles obtêm por escavação. Indique a opção correta para uma mostra que contém a seguinte composição: Composição Densidade
Tarefa 22 Professor Gustavo
 6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
Colégio XIX de Março Educação do jeito que deve ser
 Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO
 6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
Módulo inicial Materiais: Diversidade e Constituição. Química 10.º ano Ano lectivo 2007/2008
 Química 10.º ano Ano lectivo 2007/2008 Escola Secundária José Saramago Marta Paulino e Ângela Patrício O que é um Material? É algo que tem massa e ocupa espaço. Classificação Materiais: Componentes Origem
Química 10.º ano Ano lectivo 2007/2008 Escola Secundária José Saramago Marta Paulino e Ângela Patrício O que é um Material? É algo que tem massa e ocupa espaço. Classificação Materiais: Componentes Origem
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017
 ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 1º ano Nome Nº Turma Data 15/12 Nota 08 Disciplina QUÍMICA TRABALHO Prof. ORLANDO Valor 30 ESTUDOS INDEPENDENTES DE RECUPERAÇÃO 01) Na química temos
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 1º ano Nome Nº Turma Data 15/12 Nota 08 Disciplina QUÍMICA TRABALHO Prof. ORLANDO Valor 30 ESTUDOS INDEPENDENTES DE RECUPERAÇÃO 01) Na química temos
QUÍMICA INORGÂNICA ESTRUTURA ATÔMICA PROF. NEIF NAGIB
 QUÍMICA INORGÂNICA ESTRUTURA ATÔMICA PROF. NEIF NAGIB JONH DALTON: Postulados de Dalton: 1- Toda matéria é formada por entidades extremamente pequenas, os átomos. 2- Os átomos são indivisíveis. 3- O número
QUÍMICA INORGÂNICA ESTRUTURA ATÔMICA PROF. NEIF NAGIB JONH DALTON: Postulados de Dalton: 1- Toda matéria é formada por entidades extremamente pequenas, os átomos. 2- Os átomos são indivisíveis. 3- O número
PROMILITARES 09/08/2018 QUÍMICA. Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS
 QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
09) Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
01) Indique a alternativa que completa corretamente as lacunas do seguinte período: Um elemento químico é representado pelo seu..., é identificado pelo número de... e pode apresentar diferentes números
Classificação da matéria
 Classificação da matéria Prof. : Drielle Caroline Substâncias Como vimos na aula anterior, um conjunto de átomos com as mesmas propriedades químicas constitui um elemento químico, e cada substância é caracterizada
Classificação da matéria Prof. : Drielle Caroline Substâncias Como vimos na aula anterior, um conjunto de átomos com as mesmas propriedades químicas constitui um elemento químico, e cada substância é caracterizada
Colégio XIX de Março Educação do jeito que deve ser
 Colégio XIX de Março Educação do jeito que deve ser 2017 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 16/05/2017 Nota: Professor(a): Paulo Fernando Valor da Prova: 40 pontos Orientações
Colégio XIX de Março Educação do jeito que deve ser 2017 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 16/05/2017 Nota: Professor(a): Paulo Fernando Valor da Prova: 40 pontos Orientações
QUÍMICA PROF. AMANDA THOMÉ
 QUÍMICA PROF. AMANDA THOMÉ // QUESTÃO 01 A natureza apresenta grande diversidade de materiais. É preciso analisar a composição e as propriedades desses materiais para que eles possam ser utilizados ou
QUÍMICA PROF. AMANDA THOMÉ // QUESTÃO 01 A natureza apresenta grande diversidade de materiais. É preciso analisar a composição e as propriedades desses materiais para que eles possam ser utilizados ou
Os estados físicos da matéria sólido, líquido e gasoso são chamados também de estados de agregação da matéria. No esquema abaixo,
 QUÍMICA (QUESTÕES 1 10) QUESTÃO 1 Os estados físicos da matéria sólido, líquido e gasoso são chamados também de estados de agregação da matéria. No esquema abaixo, marque a alternativa que representa CORRETAMENTE
QUÍMICA (QUESTÕES 1 10) QUESTÃO 1 Os estados físicos da matéria sólido, líquido e gasoso são chamados também de estados de agregação da matéria. No esquema abaixo, marque a alternativa que representa CORRETAMENTE
FQ A - 10ºF FÍSICO-QUÍMICA 1. PO TOS DE MUDA ÇA DE ESTADO FÍSICO DA MATÉRIA
 FÍSICO-QUÍMICA 1. PO TOS DE MUDA ÇA DE ESTADO FÍSICO DA MATÉRIA O ponto de fusão designa a temperatura à qual uma substância passa do estado sólido ao estado líquido nas condições normais de pressão, coexistindo
FÍSICO-QUÍMICA 1. PO TOS DE MUDA ÇA DE ESTADO FÍSICO DA MATÉRIA O ponto de fusão designa a temperatura à qual uma substância passa do estado sólido ao estado líquido nas condições normais de pressão, coexistindo
Resoluções das Atividades
 Resoluções das Atividades Sumário Módulo 1 Substâncias puras, misturas e sistemas Análise imediata... 1 Módulo 2 Cálculos químicos... 3 Módulo 3 úmero de oidação (o) idação e redução (redo)... 6 Módulo
Resoluções das Atividades Sumário Módulo 1 Substâncias puras, misturas e sistemas Análise imediata... 1 Módulo 2 Cálculos químicos... 3 Módulo 3 úmero de oidação (o) idação e redução (redo)... 6 Módulo
Colégio XIX de Março Educação do jeito que deve ser
 Colégio XIX de Março Educação do jeito que deve ser 2017 1ª PROVA PARCIAL DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 25/03/2017 Nota: Professor(a): Paulo Fernando Valor da Prova: 40 pontos Orientações
Colégio XIX de Março Educação do jeito que deve ser 2017 1ª PROVA PARCIAL DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 25/03/2017 Nota: Professor(a): Paulo Fernando Valor da Prova: 40 pontos Orientações
A matéria e suas propriedades
 A matéria e suas propriedades Letícia Silva 1 A Química Como vimos na aula anterior, desde épocas muito remotas a Química estava presente no cotidiano de nossos antepassados. Agora olhe ao seu redor e
A matéria e suas propriedades Letícia Silva 1 A Química Como vimos na aula anterior, desde épocas muito remotas a Química estava presente no cotidiano de nossos antepassados. Agora olhe ao seu redor e
Substâncias e Transformações
 Substâncias e Transformações PAESPE 2018 Aula: Mariany Fernandes O QUE É UM SISTEMA? É uma porção limitada do universo, considerada como um todo para efeito de estudo. Homogêneo Heterogêneo Homogêneo:
Substâncias e Transformações PAESPE 2018 Aula: Mariany Fernandes O QUE É UM SISTEMA? É uma porção limitada do universo, considerada como um todo para efeito de estudo. Homogêneo Heterogêneo Homogêneo:
AULA 1 FRENTE 1. Por causa do lançamento, na atmosfera, de grande quantidade de gás carbônico, causador do efeito estufa.
 Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
Sumário. Química. Frente 1. Frente 2. Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88. Capítulo 4: A Tabela Periódica 96
 Sumário Química Frente 1 Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88 Frente 2 Capítulo 4: A Tabela Periódica 96 QUÍMICA frente 1 ARTHUR HSIEH DREAMSTIME.COM Separação de misturas,
Sumário Química Frente 1 Capítulo 2: Separação de misturas, fenômenos físicos e químicos 88 Frente 2 Capítulo 4: A Tabela Periódica 96 QUÍMICA frente 1 ARTHUR HSIEH DREAMSTIME.COM Separação de misturas,
Atividade extra. Questão 1 Cecierj Questão 2 Cecierj Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
BIMESTRAL QUÍMICA - 1ºBIMESTRE
 BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
Ciências Físico-Químicas 7º ano Ficha de trabalho nº14 Separação dos componentes de uma mistura
 Para separar os constituintes de uma mistura pode-se recorrer a diferentes processos de separação. Os processos de separação permitem separar diferentes substâncias que inicialmente foram juntas, mantendo
Para separar os constituintes de uma mistura pode-se recorrer a diferentes processos de separação. Os processos de separação permitem separar diferentes substâncias que inicialmente foram juntas, mantendo
AULA 1 FRENTE 1. Por causa do lançamento, na atmosfera, de grande quantidade de gás carbônico, causador do efeito estufa.
 Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
Exercícios propostos AULA 1 FRENTE 1 1 Assinale na coluna da esquerda para causa e na coluna da direita para consequência do efeito estufa: I I Queimadas nas florestas II II Degelo das calotas polares
QUÍMICA TAISSA LUKJANENKO
 QUÍMICA TAISSA LUKJANENKO SUBSTÂNCIA PURA MISTURA ESTUDO DAS SUBSTÂNCIAS E MISTURAS SUBSTÂNCIA: material formado por moléculas quimicamente iguais. Substância simples: é constituída de uma molécula formada
QUÍMICA TAISSA LUKJANENKO SUBSTÂNCIA PURA MISTURA ESTUDO DAS SUBSTÂNCIAS E MISTURAS SUBSTÂNCIA: material formado por moléculas quimicamente iguais. Substância simples: é constituída de uma molécula formada
Estado Físico Características Macroscópicas Características Microscópicas
 Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
Sistemas materiais Estados de agregação Estado Físico Características Macroscópicas Características Microscópicas Sólido forma e volume constantes. partículas com arranjo característico; formam estruturas
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
Lista de exercícios 1 Química 1 Professor Sávio
 Lista de exercícios 1 Química 1 Professor Sávio 01 - (UEL PR/Janeiro) Quando Fahrenheit definiu a escala termométrica que hoje leva o seu nome, o primeiro ponto fixo definido por ele, o 0F, corresponde
Lista de exercícios 1 Química 1 Professor Sávio 01 - (UEL PR/Janeiro) Quando Fahrenheit definiu a escala termométrica que hoje leva o seu nome, o primeiro ponto fixo definido por ele, o 0F, corresponde
A diferença entre misturas homogêneas e heterogêneas é o número de fases.
 Separação de misturas e saneamento RESUMO Vamos descrever os diversos processos de separação das misturas heterogêneas e homogêneas. Esses processos são de grande importância e largamente empregados nas
Separação de misturas e saneamento RESUMO Vamos descrever os diversos processos de separação das misturas heterogêneas e homogêneas. Esses processos são de grande importância e largamente empregados nas
QUÍMICA 1ª Série Ensino Médio
 LISTA 02 CENTRO EDUCACIONAL SIGMA QUÍMICA 1ª Série Ensino Médio Materiais Puros e Impuros Método de separação de Misturas Estados de agregação da matéria Números do átomo e distribuição eletrônica Leis
LISTA 02 CENTRO EDUCACIONAL SIGMA QUÍMICA 1ª Série Ensino Médio Materiais Puros e Impuros Método de separação de Misturas Estados de agregação da matéria Números do átomo e distribuição eletrônica Leis
Conceitos importantes: a) Matéria : Tudo o que possui massa e ocupa lugar no espaço.
 SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
Curso Pré-ENEM. Química. Profª M.ª Juliana Silva Leite
 Curso Pré-ENEM Química Profª M.ª Juliana Silva Leite O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES
Curso Pré-ENEM Química Profª M.ª Juliana Silva Leite O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES
Substâncias e Misturas
 ESTADO DE SANTA CATARINA EEB DR JORGE LACERDA Substâncias e Misturas Profª Luiza P. R. Martins Química 1º ano Estados físicos (de agregação) da matéria Vapor Características microscópicas 2 Ebulição, Vaporização
ESTADO DE SANTA CATARINA EEB DR JORGE LACERDA Substâncias e Misturas Profª Luiza P. R. Martins Química 1º ano Estados físicos (de agregação) da matéria Vapor Características microscópicas 2 Ebulição, Vaporização
QUÍMICA Profº JAISON
 QUÍMICA Profº JAISON Determine o número atômico e o número de massa dos átomos A e B, que são isóbaros e apresentam a seguinte representação: 10+x 5x A 11+x 4x+8 B Afinal, o que é matéria? Chamamos de
QUÍMICA Profº JAISON Determine o número atômico e o número de massa dos átomos A e B, que são isóbaros e apresentam a seguinte representação: 10+x 5x A 11+x 4x+8 B Afinal, o que é matéria? Chamamos de
4.1. Separação dos componentes de misturas heterogéneas
 4.1. Separação dos componentes de misturas heterogéneas Separação dos componentes de misturas heterogéneas Para separar os componentes de misturas utilizam-se processos físicos de separação. Durante o
4.1. Separação dos componentes de misturas heterogéneas Separação dos componentes de misturas heterogéneas Para separar os componentes de misturas utilizam-se processos físicos de separação. Durante o
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. DISCIPLINA:Química SÉRIE: 3º. ALUNO(a): Lista de Exercícios P1 I Bimestre
 GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 3º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 3º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
TAREFA DA SEMANA DE 28 DE ABRIL A 02 DE MAIO
 TAREFA DA SEMANA DE 28 DE ABRIL A 02 DE MAIO QUÍMICA 1ª SÉRIE TEXTO PARA A PRÓXIMA QUESTÃO: DADOS: Constante universal dos gases perfeitos: 0,082 atm.l/mol.k Elemento Número Massa atômico atômica H 1 1,0
TAREFA DA SEMANA DE 28 DE ABRIL A 02 DE MAIO QUÍMICA 1ª SÉRIE TEXTO PARA A PRÓXIMA QUESTÃO: DADOS: Constante universal dos gases perfeitos: 0,082 atm.l/mol.k Elemento Número Massa atômico atômica H 1 1,0
Experimentos de Química Orgânica
 Experimentos de Química Orgânica Conhecimento dos procedimentos experimentais Montagem dos equipamentos e execução da reação REAGENTES PRODUTO PRINCIPAL + PRODUTOS SECUNDÁRIOS SOLVENTES + CATALISADORES
Experimentos de Química Orgânica Conhecimento dos procedimentos experimentais Montagem dos equipamentos e execução da reação REAGENTES PRODUTO PRINCIPAL + PRODUTOS SECUNDÁRIOS SOLVENTES + CATALISADORES
Lista de Exercício para a Prova Mensal de Química 1º Ano
 Lista de Exercício para a Prova Mensal de Química 1º Ano Professor (a): Cassio Pacheco 1- Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente:
Lista de Exercício para a Prova Mensal de Química 1º Ano Professor (a): Cassio Pacheco 1- Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente:
Propriedades da matéria e mudanças de estado físico
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Propriedades da matéria e mudanças de estado físico Professor: José Tiago Pereira Barbosa 1 Propriedades da Matéria A matéria é
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Propriedades da matéria e mudanças de estado físico Professor: José Tiago Pereira Barbosa 1 Propriedades da Matéria A matéria é
PROMILITARES 16/08/2018 QUÍMICA. Professora Caroline Azevedo SEPARAÇÃO DE MISTURAS
 QUÍMICA Professora Caroline Azevedo SEPARAÇÃO DE MISTURAS Misturas Mistura Homogênea: duas ou mais substâncias com 1 fase. Mistura Heterogênea: duas ou mais substâncias com mais de 1 fase. Processos de
QUÍMICA Professora Caroline Azevedo SEPARAÇÃO DE MISTURAS Misturas Mistura Homogênea: duas ou mais substâncias com 1 fase. Mistura Heterogênea: duas ou mais substâncias com mais de 1 fase. Processos de
1º trimestre Sala de estudos Ciências Data: março/2017 Ensino Fundamental 9º ano Classe: Profª. Elisete Nome: nº
 . 1º trimestre Sala de estudos Ciências Data: março/2017 Ensino Fundamental 9º ano Classe: Profª. Elisete Nome: nº Conteúdo: Propriedades da matéria; mudanças de estado físico; transformações de unidades..
. 1º trimestre Sala de estudos Ciências Data: março/2017 Ensino Fundamental 9º ano Classe: Profª. Elisete Nome: nº Conteúdo: Propriedades da matéria; mudanças de estado físico; transformações de unidades..
MÉTODOS DE SEPARAÇÃO DE MISTURAS Professora Mariana Geração 2016
 MÉTODOS DE SEPARAÇÃO DE MISTURAS Professora Mariana Geração 2016 SEPARAÇÃO DE MISTURAS A maioria dos materiais encontrados na natureza não é substância pura, ou seja, não é constituída de um único tipo
MÉTODOS DE SEPARAÇÃO DE MISTURAS Professora Mariana Geração 2016 SEPARAÇÃO DE MISTURAS A maioria dos materiais encontrados na natureza não é substância pura, ou seja, não é constituída de um único tipo
Métodos de Separação de Misturas
 Métodos de Separação de Misturas O que é uma mistura? Mistura: associação de duas ou mais substâncias em porções arbitrárias, separáveis por meios mecânicos ou físicos e em que cada um dos componentes
Métodos de Separação de Misturas O que é uma mistura? Mistura: associação de duas ou mais substâncias em porções arbitrárias, separáveis por meios mecânicos ou físicos e em que cada um dos componentes
Atividade complementar de Química. Como escolher a melhor técnica de separação de misturas?
 Atividade complementar de Química Como escolher a melhor técnica de separação de misturas? Educação de Jovens e Adultos Existem inúmeras técnicas de separação de misturas, algumas muito simples que não
Atividade complementar de Química Como escolher a melhor técnica de separação de misturas? Educação de Jovens e Adultos Existem inúmeras técnicas de separação de misturas, algumas muito simples que não
Ligações Químicas. Professor Haroldo
 Ligações Químicas Professor Haroldo 1. A regra do dueto e do octeto: Para se estabilizar um elemento precisa possuir sua camada de valência igual à camada de valência do GÁS NOBRE MAIS PRÓXIMO (8 e -,
Ligações Químicas Professor Haroldo 1. A regra do dueto e do octeto: Para se estabilizar um elemento precisa possuir sua camada de valência igual à camada de valência do GÁS NOBRE MAIS PRÓXIMO (8 e -,
Estados de agregação da matéria. Mudanças de estado. Fenômenos
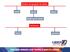 Estados de agregação da matéria sólido líquido gasoso Mudanças de estado Fenômenos físicos químicos Sistemas Interação Aspecto Composição aberto isolado substância mistura fechado homogêneo heterogêneo
Estados de agregação da matéria sólido líquido gasoso Mudanças de estado Fenômenos físicos químicos Sistemas Interação Aspecto Composição aberto isolado substância mistura fechado homogêneo heterogêneo
esféricas maciças e indivisíveis.
 a) A-I, B-II, C-III b) A-II, B-III, C-I c) A-III, B-I, C-II d) A-III, B-II, C-I e) A-II, B-I, C-III LISTA DE EXERCÍCIOS DE QUÍMICA 1º Ano do Ensino Médio Professor: Anderson Paschôa É preciso estudar todos
a) A-I, B-II, C-III b) A-II, B-III, C-I c) A-III, B-I, C-II d) A-III, B-II, C-I e) A-II, B-I, C-III LISTA DE EXERCÍCIOS DE QUÍMICA 1º Ano do Ensino Médio Professor: Anderson Paschôa É preciso estudar todos
Início. Substância pura simples. É formado por apenas um tipo de elemento químico. Exemplo: gás oxigênio (O 2), gás nitrogênio (N 2), ferro (Fe)
 Professores: Alinne Borges Tiago Albuquerque Sandro Sobreira Exercícios Substâncias puras e misturas Material que apresenta TF e TE constantes a uma dada pressão e densidade característica em determinada
Professores: Alinne Borges Tiago Albuquerque Sandro Sobreira Exercícios Substâncias puras e misturas Material que apresenta TF e TE constantes a uma dada pressão e densidade característica em determinada
Note que, no Sistema Internacional de Unidades (SI) o calor é medido em calorias (cal) ou joules (J).
 Calor e temperatura Prof. lucasmarqui Calor e Temperatura são dois conceitos fundamentais na termologia (Termofísica) os quais, são considerados sinônimos. No entanto, o calor designa a troca de energia
Calor e temperatura Prof. lucasmarqui Calor e Temperatura são dois conceitos fundamentais na termologia (Termofísica) os quais, são considerados sinônimos. No entanto, o calor designa a troca de energia
EXERCÍCIOS DE QUÍMICA
 INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
INTRODUÇÃO AO ESTUDO DA QUÍMICA FENÔMENOS FÍSICOS E QUÍMICOS SUBSTÂNCIAS PURAS E MISTURAS ATOMICIDADE - ALOTROPIA 1. (UFPE) Em quais das passagens a seguir está ocorrendo transformação química? (1) O reflexo
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma:
 TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas:
 01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
01) (USF-SP) Considerando-se as aparelhagens esquematizadas: Dessas afirmações, apenas: a) I é correta. d) I e II são corretas. b) II é correta. e) II e III são corretas. c) III é correta. 05) (UFPE-PE)
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL CAMPUS RIO GRANDE INSTRUMENTAÇÃO INDUSTRIAL
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL CAMPUS RIO GRANDE INSTRUMENTAÇÃO INDUSTRIAL Aula 16 2 MEDIDORES DE TEMPERATURA 3 INTRODUÇÃO Todas as substâncias são constituídas
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO RIO GRANDE DO SUL CAMPUS RIO GRANDE INSTRUMENTAÇÃO INDUSTRIAL Aula 16 2 MEDIDORES DE TEMPERATURA 3 INTRODUÇÃO Todas as substâncias são constituídas
Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g)
 Aula 04 1/abr Marcelo Conteúdo EXTRA-classe: Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g) Fenômeno físico: não altera a natureza
Aula 04 1/abr Marcelo Conteúdo EXTRA-classe: Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g) Fenômeno físico: não altera a natureza
9 o EF. Jeosafá de P. Lima
 9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
Aulas Multimídias Santa Cecília Professor Tiago Quick Disciplina: Química Série: 9º ano EF
 Aulas Multimídias Santa Cecília Professor Tiago Quick Disciplina: Química Série: 9º ano EF Professor: Tiago Albuquerque Slides: Alinne Borges alinne.borges@gmail.com Exercícios Substâncias puras e misturas
Aulas Multimídias Santa Cecília Professor Tiago Quick Disciplina: Química Série: 9º ano EF Professor: Tiago Albuquerque Slides: Alinne Borges alinne.borges@gmail.com Exercícios Substâncias puras e misturas
Química B Extensivo V. 2
 Extensivo V. 2 Resolva Aula 5 5.01) A 5.02) C 5.03) Colocar água para separar o salitre e decantar ou filtrar. Depois pôr sulfeto de carbono no sólido restante para retirar o enxofre. que sobra é o carvão.
Extensivo V. 2 Resolva Aula 5 5.01) A 5.02) C 5.03) Colocar água para separar o salitre e decantar ou filtrar. Depois pôr sulfeto de carbono no sólido restante para retirar o enxofre. que sobra é o carvão.
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano
 EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017
 III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
2. Ao afirmarmos que o gelo seco sublima, estamos nos referindo à:
 1. Observe as figuras a seguir, onde os átomos são representados por esferas e cada tamanho representa um átomo diferente. Depois, assinale a alternativa VERDADEIRA: ( A ) Nas figuras 1 e 2 encontramos
1. Observe as figuras a seguir, onde os átomos são representados por esferas e cada tamanho representa um átomo diferente. Depois, assinale a alternativa VERDADEIRA: ( A ) Nas figuras 1 e 2 encontramos
Prof.: HÚDSON SILVA. Soluções. Frente 2 Módulo 5. Coeficiente de Solubilidade.
 Prof.: HÚDSON SILVA Frente 2 Módulo 5 Soluções. Coeficiente de Solubilidade. # SOLUÇÕES É uma mistura homogênea de duas ou mais substâncias. Exemplos: Água + Açúcar, Gasolina + Álcool, CLASSIFICAÇÃO DOS
Prof.: HÚDSON SILVA Frente 2 Módulo 5 Soluções. Coeficiente de Solubilidade. # SOLUÇÕES É uma mistura homogênea de duas ou mais substâncias. Exemplos: Água + Açúcar, Gasolina + Álcool, CLASSIFICAÇÃO DOS
