Química A Intensivo V. 1
|
|
|
- Rachel Klettenberg de Almada
- 8 Há anos
- Visualizações:
Transcrição
1 1 Química A Intensivo V. 1 Exercícios 01) Incorreta. O modelo atômico de Dalton não prevê a existência de elétrons. 02. Correta. Segundo Dalton, os átomos eram indestrutíveis e, durante uma reação química, mantinham-se inalterados, preservando as massas inicial e final constantes. 04. Incorreta. Thomson, ao determinar a razão entre a massa e a carga do elétron, confirmou a divisibilidade do átomo. 08. Correta. A emissão de luz por parte dos átomos devese à transição dos elétrons dentro dos níveis de energia, o que só aparece no modelo de Bohr. 16. Incorreta. Não há, no modelo de Dalton, o conhecimento de ligação iônica e tampouco, no átomo, a presença de elétrons como responsáveis pelas ligações químicas. 02) A Os raios catódicos, descobertos por Thomson em 1897, são partículas carregadas negativamente e denominadas de elétrons. 03) Correta. A base científica de Dalton foi a lei de Proust. 02. Correta. Segundo Dalton, a matéria era formada por átomos indivisíveis e indestrutíveis. 04. Correta. Quando Thomson afirmou que o átomo era constituído de prótons e elétrons, concluiu que havia a possibilidade de separá-los e, portanto, dividir o átomo. 08. Incorreta. O modelo atômico de Thomson é o pudim com passas. 16. Correta. Dalton criou o seu modelo atômico baseado na lei das proporções definidas, enunciada por Proust e que é uma das leis das reações químicas. 04) D I. Falsa. O correto é elétron no lugar de próton. II. Verdadeira. Quando o elétron absorve energia, afasta-se do núcleo e vai para um mais energético dentro da eletrosfera. III.Falsa. O correto é absorve energia. IV.Verdadeira. O estado x do elétron é a sua órbita estacionária e, após a sua promoção, quando ele retornar para essa órbita, deverá manter a sua energia constante; assim, se antes havia absorvido energia, na volta irá liberar a mesma quantidade de energia absorvida, ou seja, z unidades de energia. 05) Correta. Átomo é a partícula mínima que caracteriza o elemento químico e é, em última análise, o formador dos corpos (porção limitada da matéria). 02. Incorreta. Os átomos são quimicamente diferentes quando têm números atômicos diferentes. 04. Incorreta. Os elétrons possuem carga elétrica negativa. 08. Incorreta. Os prótons e elétrons possuem massas e cargas diferentes. 16. Correta. Os nêutrons são partículas subatômicas que não apresentam carga elétrica. 32. Incorreta. Os átomos são partículas que possuem, na sua maior extensão, espaços vazios. 06) C I. Verdadeira. Segundo Bohr, somente certas órbitas eletrônicas são permitidas para o elétron e este não emite energia quando as percorre. II. Verdadeira. Na órbita estacionária de energia, segundo Bohr, o elétron mantém sua energia constante. III.Falsa.O elétron absorve energia. IV.Verdadeira. Na transição de uma camada mais externa para outra mais próxima do núcleo, o elétron emite um quantum de energia. V. Falsa.Os postulados de Bohr não faziam previsões sobre o núcleo atômico. 07) A Quando um átomo transforma-se em um íon, esse átomo perde ou ganha elétrons e, portanto, mantém o seu núcleo inalterado, ficando com o mesmo número de prótons, ou seja, com o mesmo número atômico (Z). 08) C Isótopos são definidos como elementos de diferentes números de massa e mesmo número atômico. 09) Incorreta. O número de carga em I é igual a 2, pois a espécie possui dez elétrons (10 ) e oito prótons (8 + ). 02. Correta. Como a carga em II é zero, o número de prótons (8) deve ser igual ao número de elétrons. 04. Incorreta. Para a carga zero, em III o número de elétrons (6) deve ser igual ao número de prótons. 08. Incorreta. Em IV, temos uma carga igual a 2 e, assim, seis prótons (6 + ) e oito elétrons (8 ). 16. Correta. O elemento químico que possui dois prótons em seu núcleo é o hélio (He). 10) B I. Correta. Substâncias simples são formadas pelo mesmo elemento químico. II. Incorreta. O par I e I 2 não constitui um exemplo de alotropia, a qual, por definição, exige duas (ou mais) substâncias simples diferentes provenientes do mesmo elemento químico, e o ânion I não é uma substância simples. III.Correta. Na ionização de um dado elemento químico, só há variação no número de elétrons, e nunca no número de prótons de seus átomos. IV.Incorreta. Substâncias simples, como O 3 e O 2, apresentam sempre Nox igual a zero.
2 2 11) A As configurações eletrônicas corretas dos íons Cd 2+ (Z = 48), Zn 2+ (Z = 30) e Ca 2+ (Z = 20) são, respectivamente, [Kr]4d 10, [Ar]3d 10 e [Ne]3s 2 3p 6, em que: [Ne] = 1s 2 2s 2 2p 6 ; [Ar] = 1s 2 2s 2 2p 6 3s 2 3p 6 ; [Kr] = 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6. Atenção: Lembre que, na configuração de cátions, retiramos em primeiro lugar os elétrons da última camada. 12) A O alumínio possui configuração eletrônica no estado fundamental 1s 2 2s 2 2p 6 3s 2 3p 1. No composto A ( SO ). 6H 2 O, o l Al encontra-se no estado de oxidação 3 +, portanto cedeu três elétrons da sua camada de valência, adquirindo a configuração eletrônica 1s 2 2s 2 2p 6, idêntica à do elemento neônio (Ne Z = 10). 13) A Z = 25 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 5 Z = 26 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 6 Z = 27 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 7 Z = 28 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 8 Preenchimento sucessivo no mesmo : 3; no mesmo sub: d. 14) B Z = p + e 38 e Ordem energética: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 2 Ordem geométrica: s 2s 2p 3s 3p 3d 4s 4p 5s s 5 2 antepenúltimo penúltimo último 15) D A configuração eletrônica do ânion A completa é: 1s 2 2s 2 2p 6 3s 2 3p 6, o que evidencia a presença de 18 elétrons. Como na forma de ânion o átomo ganha 2 elétrons, podemos afirmar que a configuração eletrônica do átomo A neutro é: 1s 2 2s 2 2p 6 3s 2 3p 4, o que nos leva a um número de elétrons igual a 16 e, como nos átomos neutros o número de prótons é igual ao de elétrons, concluímos que o número atômico (Z) de A é ) D Fazendo a configuração eletrônica do elemento, temos: II. Verdadeiro. Em cada, há tantos subníveis quanto for o valor de seu número quântico principal. III.Verdadeiro. Por exemplo: no L (n = 2), há 4 orbitais; no N (n=4), há 16 orbitais. IV.Falso. O princípio em questão é o de Wolfgang Pauli, e não de Linus Pauling. V. Falso. Em um orbital p, pode haver no máximo 2 elétrons. Nos três orbitais p, aparecem 6 elétrons. VI. Falso. O ângulo entre os três orbitais do sub p é sempre 90. VII.Falso. Orbital é uma região de máxima probabilidade em localizar o elétron. VIII.Falso. O tipo de orbital apresentado nesta afirmativa não existe, segundo Pauli, em átomo nenhum. 18) Correta. 02. Incorreta. n = 4, l = 1, m = +1 e s = Incorreta. n = 3, l = 2, m = 2 e s = Correta. 16. Correta. 32. Correta. 19) E A = 40 n = 22 A = Z + n Z = A n = = s 2s 2p 3s 3p 2 6 K 2 K 8 K 8 camada de valência 20) C n Indica a distância elétron núcleo e a energia do elétron. l Fornece a forma da trajetória do elétron e a forma do seu orbital. m l Mostra a orientação espacial do orbital. m s Relaciona-se com o spin eletrônico ou o sentido da rotação do elétron. 21) A Ca (Z = 20) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 Somando o número de elétrons, que é igual ao de prótons, encontramos um número atômico igual a ) V V V F F F F F I. Verdadeiro. A idéia de subníveis é conseqüência do modelo atômico de Sommerfeld, que propôs para a eletrosfera dos átomos órbitas circulares e órbitas elípticas.
3 3 22) C I. Correta. Gás oxigênio (O 2 ) e gás ozônio (O 3 ) são alótropos por diferença de atomicidade. II. Correta. S (Z = 16) 1s 2 2s 2 2p 6 3s 2 3p 4 O elétron diferenciador é o quarto elétron de 3p, ou seja, se considerarmos que o primeiro elétron a entrar em um orbital tenha spin = 1, teremos: 2 25) D Para reduzir ao mínimo qualquer confusão possível entre as idéias antigas (órbitas) e as novas, tornou-se hábito utilizar o termo orbital para indicar um de energia associado a uma dada distribuição de probabilidades eletrônicas. 26) 23) E III. Incorreta. O oxigênio é o segundo elemento mais eletronegativo da tabela periódica, só perdendo para o flúor. IV.Incorreta. O oxigênio, ao ganhar 2 elétrons, transforma-se num ânion de carga 2. número de nêutrons de W = 10n n W = A Z = = (3x) (2x 4) 10 = x + 4 x = 6 número atômico de T = (2x 4) Z T = = 8 configuração eletrônica de T 1s 2 2s 2 2p 4 distribuição eletrônica de T 2 1s 2 2s 2 2p 6 (devido ao ganho de 2 e ) distribuição eletrônica do He 1s 2 número de nêutrons de T n T = A Z = 16 8 = 8 24) Correto. A (Z = 17) 1s 2 2s 2 2p 6 3s 2 3p 5 CV = 7 e Forma ânions monovalentes. 02. Incorreto. B (Z = 20) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 O átomo B possui 4 camadas, enquanto o átomo A possui 3 camadas. 04. Correto. O elétron de diferenciação do átomo B está em 4s 2 e possui: n = 4, l = 0 e m = Incorreto. O átomo A é um ametal, enquanto B é um metal e, ao ligarem-se, fazem ligação iônica. 16. Incorreto. O átomo A tende a ganhar um elétron, enquanto o átomo B a perder dois elétrons, assim a proporção que satisfaz o octeto de ambos é BA 2. 27) D O átomo X possui Z = 13, porque ao perder 3 elétrons ficou com 10 elétrons e, portanto, na forma neutra apresentava 13 elétrons e 13 prótons. Estado fundamental indica átomo neutro, ou seja, átomo com número prótons igual ao número elétrons; assim, a configuração eletrônica de X é: 1s 2 2s 2 2p 6 3s 2 3p 1. Como o elétron de diferenciação é o último elétron a entrar na configuração eletrônica normal de um átomo no estado fundamental, podemos afirmar que o elétron se encontra no sub 3p. 28) B Observe que a configuração normal do átomo termina em 3p 5 e sua configuração completa tem a seguinte forma: 1s 2 2s 2 2p 6 3s 2 3p 5, com um total de 17 elétrons, e, portanto, com 17 prótons no seu estado fundamental. 29) E átomo neutro número p + = número e = 9 Assim, a configuração eletrônica do átomo é: 1s 2 2s 2 2p 5. A distribuição dos elétrons no sub 2p é: Podemos notar que todos os orbitais do sub p possuem elétrons e, portanto, há probabilidade de se encontrarem elétrons em todas as regiões numeradas, porque, mesmo no orbital p z incompleto, a densidade de probabilidades está, igualmente, distribuída nas regiões 5 e 6.
4 4 30) C n A + n B + n C = 50 Z + Z + X = 40 n A = n C 28 Z = W X Z = 28 + X W equação 1 W = 28 + X Z A massa de B (Y) é igual à soma de prótons (Z) mais equação 2 nêutrons (18) Y = Z + 18 Como a soma de todos os prótons e todos os nêutrons é igual à soma de todas as massas, temos: 28 + Y+ W = 90 Y = W Y = 62 W Z + 18 = X Z Z = equação 2 equação 1 = X + Z X = 16 Sabemos que: Z + Z + X = 40 2Z = Z = 12 c) Incorreto. A configuração IV representa o elemento nitrogênio. d) Incorreto. O silício é um semimetal. e) Incorreto. A configuração III representa um metal. 34) D a) Correto. O elétron mais energético do N (IV) está em 2p 3 e tem n = 2. b) Correto. O elétron mais energético do C (I) está em 2p 2 e tem l = 1, ou seja, sub p. c) Correto. Os elétrons de valência do silício (II) estão em 3s 2 e 3p 2 e têm l = 0 e l = 1. d) Incorreto. O elemento III está localizado no quarto período da tabela periódica. e) Correto. O elétron mais energético de I está em 2p 2 e tem n = 2 e l = 1; o elétron mais energético de IV está em 2p 3 e também tem n = 2 e l = 1. 35) Correta. O césio possui em seu núcleo 55 prótons. 02. Incorreta. O cobalto é um elemento de transição, e o césio é um elemento representativo. 04. Incorreta. O césio, metal alcalino, forma hidróxidos do tipo M(OH). 08. Correta. Co (Z = 27) 1s 2 2s 2 2p 6 3s 2 3p 6 3d 7 4s Incorreta. Co (Z = 27 e A = 60) A = Z + n n = A Z = = = 33 nêutrons 32. Incorreta. O césio está localizado no sexto período e no grupo 1 da classificação periódica. 36) D I. Correta. metais alcalinos ns 1 = configuração de valência II. Incorreta. Em um mesmo período, os elementos apresentam o mesmo número de camadas. III.Incorreta. O sub mais energético dos elementos de transição interna é o sub f, da antepenúltima camada. 31) E 32 A A = Z + n n = A Z P 15 Z n = = 17 nêutrons 32) D a) Incorreto. O iodo é um halogênio. b) Incorreto. O sódio é um metal alcalino. c) Incorreto. Somente o ferro é elemento de transição. d) Correto. O fósforo é um não-metal ou ametal. e) Incorreto. O tecnécio é um elemento de transição. 33) A a) Correto. Carbono e silício pertencem à mesma família da tabela periódica e, assim, possuem o mesmo número de elétrons na camada de valência e propriedades químicas semelhantes. b) Incorreto. A configuração III é de um elemento de transição. 37) Incorreto. Todos os elementos constantes da tabela são representativos. 02. Correto. O metais alcalinos (K e Na) somam uma fração em massa igual a 0,47% (0,36 + 0,11), que é maior do que a do halogênio Cl = 0,40%. 04. Correto. Para cada 100 g de massa corpórea, o hidrogênio participa com 10 g e, portanto, 10 mol de átomos que equivalem a 6, átomos de H; já o oxigênio, para as mesmas 100 g, participa com 64,5 g, o que nos leva a, aproximadamente, 4 mol de átomos e um total de 2, átomos de O. 08. Correto. Alcalino-terrosos. Ca + Mg = 1,93% > K + Na = 0,47% alcalinos. 16. Incorreto. São gases nas CATP: oxigênio, hidrogênio, nitrogênio e cloro. 38) Correta. O nióbio é um elemento do grupo 05 ou VB, portanto é um elemento de transição.
5 5 02. Incorreta. O símbolo correto é Nb. 04. Correta. As ligas metálicas são exemplos de solução sólida. 08. Incorreta. O Nb 3+ (Z = 41) apresenta a seguinte configuração eletrônica: 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 6 5s 0 4d 2, que não é uma configuração de gás nobre. 16. Correta. O nióbio, como elemento de transição, pode apresentar Nox variável: +3 e ) D Elementos cujas configurações eletrônicas recebem o último elétron em sub d são classificados como elementos de transição. 40) E I. Correta. Devido a sua boa condutividade elétrica e grande ductibilidade, o cobre é usado na fabricação de fios elétricos. II. Correta. Os adubos químicos denominados de NPK (como uréia, superfosfatos e cloreto de potássio) utilizam potássio na sua produção. III.Incorreta. Os metais mais comumente utilizados na fabricação de panelas são o ferro e o alumínio. IV.Incorreta. O aço é uma liga metálica que tem o ferro e o carbono na sua composição, com porcentagens deste último variáveis entre 0,03% e 2,00%. V. Correta. Por ser um metal líquido na temperatura ambiente e de fácil dilatação, o mercúrio é utilizado na fabricação de termômetros.
Química Atomística Profª: Bruna Villas Bôas. Exercícios
 NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
Próton Nêutron Elétron
 Próton Nêutron Elétron ARNOLD SOMMERFELD MODELO ATÔMICO DE ARNOLD SOMMERFELD - 1916 Ao pesquisar o átomo, Sommerfeld concluiu que os elétrons de um mesmo nível, ocupam órbitas de trajetórias diferentes
Próton Nêutron Elétron ARNOLD SOMMERFELD MODELO ATÔMICO DE ARNOLD SOMMERFELD - 1916 Ao pesquisar o átomo, Sommerfeld concluiu que os elétrons de um mesmo nível, ocupam órbitas de trajetórias diferentes
Teoria Atômica. Constituição da matéria. Raízes históricas da composição da matéria. Modelos atômicos. Composição de um átomo.
 Teoria Atômica Constituição da matéria Raízes históricas da composição da matéria Modelos atômicos Composição de um átomo Tabela periódica Raízes Históricas 6000 a.c.: descoberta do fogo 4000 a.c.: vidros,
Teoria Atômica Constituição da matéria Raízes históricas da composição da matéria Modelos atômicos Composição de um átomo Tabela periódica Raízes Históricas 6000 a.c.: descoberta do fogo 4000 a.c.: vidros,
Resoluções das Atividades
 Resoluções das Atividades Sumário Módulo 1 Teoria atômica básica e leis ponderais Evolução dos modelos atômicos Modelo atômico atual 1 Módulo 2 Números quânticos; Distribuição eletrônica Paramagnetismo,
Resoluções das Atividades Sumário Módulo 1 Teoria atômica básica e leis ponderais Evolução dos modelos atômicos Modelo atômico atual 1 Módulo 2 Números quânticos; Distribuição eletrônica Paramagnetismo,
Próton Nêutron Elétron
 Próton Nêutron Elétron Próton Nêutron Elétron Número de prótons: 54 2 Nome do elemento: BORO BERÍLIO HÉLIO Esta Os quantidade diferentes tipos de prótons de átomos recebe (elementos o nome químicos) de
Próton Nêutron Elétron Próton Nêutron Elétron Número de prótons: 54 2 Nome do elemento: BORO BERÍLIO HÉLIO Esta Os quantidade diferentes tipos de prótons de átomos recebe (elementos o nome químicos) de
O Átomo. a + thomos = sem divisão
 O Átomo 1. O nome átomo tem origem na Grécia Antiga no sec. V a.c. Os pensadores antigos falavam da existência de partículas invisíveis e indivisíveis que formariam toda matéria. a + thomos = sem divisão
O Átomo 1. O nome átomo tem origem na Grécia Antiga no sec. V a.c. Os pensadores antigos falavam da existência de partículas invisíveis e indivisíveis que formariam toda matéria. a + thomos = sem divisão
Prova de Recuperação Bimestral de Ciências Nome Completo: Data: / /2010
 COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
Química. Resolução das atividades complementares. Q42 Ligação metálica
 Resolução das atividades complementares 3 Química Q42 Ligação metálica p. 59 1 (Cefet-PR) Analise as afirmações a seguir: I. O metal X é leve, sofre pouca corrosão e é bastante utilizado na construção
Resolução das atividades complementares 3 Química Q42 Ligação metálica p. 59 1 (Cefet-PR) Analise as afirmações a seguir: I. O metal X é leve, sofre pouca corrosão e é bastante utilizado na construção
TD nº 02 Química 2 1º ano - 2011
 Prof. Willame TD nº 02 Química 2 1º ano - 2011 TABELA PERIÓDICA 1. A organização dos elementos Com a descoberta de uma grande variedade de átomos, tornou-se necessária à criação de uma sistemática de classificação.
Prof. Willame TD nº 02 Química 2 1º ano - 2011 TABELA PERIÓDICA 1. A organização dos elementos Com a descoberta de uma grande variedade de átomos, tornou-se necessária à criação de uma sistemática de classificação.
Química A Intensivo V. 1
 Química A Intensivo V. 1 Exercícios 01)A A ideia apresentada na alternativa A, além de algo impossível, não estava incluída na teoria de Dalton que afirmava que átomos iguais pertenciam ao mesmo elemento
Química A Intensivo V. 1 Exercícios 01)A A ideia apresentada na alternativa A, além de algo impossível, não estava incluída na teoria de Dalton que afirmava que átomos iguais pertenciam ao mesmo elemento
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
Apostila de Química Geral
 Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é:
 01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos
 Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
478 a.c. Leucipo e seu discípulo Demócrito
 MODELOS ATÔMICOS 478 a.c. Leucipo e seu discípulo Demócrito - A matéria após sofrer várias subdivisões, chegaria a uma partícula indivisível a que chamaram de átomo. - ÁTOMO a = sem tomos = divisão - Esta
MODELOS ATÔMICOS 478 a.c. Leucipo e seu discípulo Demócrito - A matéria após sofrer várias subdivisões, chegaria a uma partícula indivisível a que chamaram de átomo. - ÁTOMO a = sem tomos = divisão - Esta
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves
 Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
Química. Resolução das atividades complementares. Q36 Classificação de elementos
 Resolução das atividades complementares 3 Química Q36 Classificação de elementos p. 24 1 (Fatec-SP) Imagine que a tabela periódica seja o mapa de um continente, e que os elementosquímicos constituem as
Resolução das atividades complementares 3 Química Q36 Classificação de elementos p. 24 1 (Fatec-SP) Imagine que a tabela periódica seja o mapa de um continente, e que os elementosquímicos constituem as
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS PARTE 1 01. A classificação periódica apresenta os elementos na: a) seqüência crescente de números de massa; b) ordem de reatividade química; c) seqüência crescente
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS PARTE 1 01. A classificação periódica apresenta os elementos na: a) seqüência crescente de números de massa; b) ordem de reatividade química; c) seqüência crescente
Lista exercícios N1 Química Geral Tabela Periódica, distribuição eletrônica e ligações químicas.
 1 Parte I - Considere as informações abaixo: Lista exercícios N1 Química Geral Tabela Periódica, distribuição eletrônica e ligações químicas. Núcleo: Prótons e nêutrons. Eletrosfera: elétrons Os átomos
1 Parte I - Considere as informações abaixo: Lista exercícios N1 Química Geral Tabela Periódica, distribuição eletrônica e ligações químicas. Núcleo: Prótons e nêutrons. Eletrosfera: elétrons Os átomos
DISTRIBUIÇÃO ELETRÔNICA E N OS QUâNTICOS TEORIA - PARTE II. Elétron de diferenciação e elétrons de valência. Distribuição eletrônica de íons
 DISTRIBUIÇÃO ELETRÔNICA E N OS QUâNTICOS TEORIA - PARTE II Elétron de diferenciação e elétrons de valência O elétron de diferenciação é definido como o último elétron do subnível mais energético de um
DISTRIBUIÇÃO ELETRÔNICA E N OS QUâNTICOS TEORIA - PARTE II Elétron de diferenciação e elétrons de valência O elétron de diferenciação é definido como o último elétron do subnível mais energético de um
Ligações Químicas Ligação Iônica Ligação Metálica
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
A ESTRUTURA ATÔMICA REPRESENTAÇÃO
 A ESTRUTURA ATÔMICA O modelo nuclear admite que o átomo é formado por uma região central extremamente pequena, o núcleo, em torno do qual giram diminutas partículas, constituindo uma outra região, a eletrosfera.
A ESTRUTURA ATÔMICA O modelo nuclear admite que o átomo é formado por uma região central extremamente pequena, o núcleo, em torno do qual giram diminutas partículas, constituindo uma outra região, a eletrosfera.
1º trimestre Ciências Sala de estudos Data: Abril/2015 Ensino Fundamental 9º ano classe: Profª Elisete Nome: nº
 1º trimestre Ciências Sala de estudos Data: Abril/2015 Ensino Fundamental 9º ano classe: Profª Elisete Nome: nº Valor: 10 Nota:.. Conteúdo: Atomística e MRU 1) Observe o trecho da história em quadrinhos
1º trimestre Ciências Sala de estudos Data: Abril/2015 Ensino Fundamental 9º ano classe: Profª Elisete Nome: nº Valor: 10 Nota:.. Conteúdo: Atomística e MRU 1) Observe o trecho da história em quadrinhos
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09
 Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 2ºTeste Sumativo 1ºPeríodo Duração do Teste:60 minutos Data: 05 / 12 / 08 Prof. Dulce Godinho
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 2ºTeste Sumativo 1ºPeríodo Duração do Teste:60 minutos Data: 05 / 12 / 08 Prof. Dulce Godinho
Goiânia, / / 2014. Elemento Configuração 1 1s 2 2s 2 2p 6 3s 1 2 1s 2 2s 2 2p 4 3 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 4 1s 2 2s 2 2p 6 3s 2 3p 6
 Lista de exercícios - Química Aluno (a): Nº. Professora: Núbia de Andrade Série: 1º ano (Ensino médio) Turma: Goiânia, / / 2014. Questão 01) Localize na Tabela Periódica o elemento químico de número atômico
Lista de exercícios - Química Aluno (a): Nº. Professora: Núbia de Andrade Série: 1º ano (Ensino médio) Turma: Goiânia, / / 2014. Questão 01) Localize na Tabela Periódica o elemento químico de número atômico
A) a existência do oceano líquido é uma hipótese possível, pois um sal solúvel só forma uma mistura homogênea com a água, quando ela está líquida.
 TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
MODELOS ATÔMICOS. Química Professora: Raquel Malta 3ª série Ensino Médio
 MODELOS ATÔMICOS Química Professora: Raquel Malta 3ª série Ensino Médio PRIMEIRA IDEIA DO ÁTOMO 546 a.c. Tales de Mileto: propriedade da atração e repulsão de objetos após atrito; 500 a.c. Empédocles:
MODELOS ATÔMICOS Química Professora: Raquel Malta 3ª série Ensino Médio PRIMEIRA IDEIA DO ÁTOMO 546 a.c. Tales de Mileto: propriedade da atração e repulsão de objetos após atrito; 500 a.c. Empédocles:
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS
 Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
Energias de ionização (ev) 1ª 2ª 3ª 4ª 5ª 6ª 7ª 8ª X 5,4 75,6 122,4 Y 13,6 35,2 54,9 77,4 113,9 138,1 739,1 871,1
 1. (Cefet MG 2014) Na tabela a seguir, estão representadas as energias de ionização de dois elementos X e Y pertencentes ao segundo período do quadro periódico. Elementos Energias de ionização (ev) 1ª
1. (Cefet MG 2014) Na tabela a seguir, estão representadas as energias de ionização de dois elementos X e Y pertencentes ao segundo período do quadro periódico. Elementos Energias de ionização (ev) 1ª
Lista de Exercício de Química - N o 6
 Lista de Exercício de Química - N o 6 Profa. Marcia Margarete Meier 1) Arranje em ordem crescente de energia, os seguintes tipos de fótons de radiação eletromagnética: raios X, luz visível, radiação ultravioleta,
Lista de Exercício de Química - N o 6 Profa. Marcia Margarete Meier 1) Arranje em ordem crescente de energia, os seguintes tipos de fótons de radiação eletromagnética: raios X, luz visível, radiação ultravioleta,
APSA 2 - Tabela Periódica 10º Ano Novembro de 2011
 1. Dada a distribuição eletrónica dos elementos a seguir, indique qual deles apresenta maior e menor raio atómico 3Li: 1s 2 2s 1 7N: 1s 2 2s 2 2p 3 9F: 1s 2 2s 2 2p 5 R: Maior raio Atómico = Li Menor raio
1. Dada a distribuição eletrónica dos elementos a seguir, indique qual deles apresenta maior e menor raio atómico 3Li: 1s 2 2s 1 7N: 1s 2 2s 2 2p 3 9F: 1s 2 2s 2 2p 5 R: Maior raio Atómico = Li Menor raio
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007
 Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
Evolução do modelo atómico
 Os neutrões só foram descobertos em 1932 por Chadwick. Evolução do modelo atómico Demócrito (400 a.c.) Enunciou a primeira ideia de átomo como sendo a partícula elementar que constitui toda a matéria.
Os neutrões só foram descobertos em 1932 por Chadwick. Evolução do modelo atómico Demócrito (400 a.c.) Enunciou a primeira ideia de átomo como sendo a partícula elementar que constitui toda a matéria.
Thomson denominou este segundo modelo atômico de Pudim de Passas.
 EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade do que era constituída a matéria parecia ser impossível de ser desvendada. Até que em 450 a.c. o filósofo grego Leucipo de Mileto afirmava
EVOLUÇÃO DOS MODELOS ATÔMICOS Durante algum tempo a curiosidade do que era constituída a matéria parecia ser impossível de ser desvendada. Até que em 450 a.c. o filósofo grego Leucipo de Mileto afirmava
Qualidade Ambiental Química
 Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
sábado, 28 de julho de 12 Prof: Alex
 Modelo de Sommerfeld (1916) Modelo de Sommerfeld (1916) Sommerfeld aperfeiçoou o modelo de BOHR, incluindo órbitas elípticas para o elétron, que teria energias diferentes dependendo do tipo de órbita descrita.
Modelo de Sommerfeld (1916) Modelo de Sommerfeld (1916) Sommerfeld aperfeiçoou o modelo de BOHR, incluindo órbitas elípticas para o elétron, que teria energias diferentes dependendo do tipo de órbita descrita.
ESPECTRO ELETROMAGNÉTICO
 COLÉGIO ESTADUAL RAINHA DA PAZ, ENSINO MÉDIO REPOSIÇÃO DAS AULAS DO DIA 02 e 03/07/2012 DAS 1 ª SÉRIES: A,B,C,D,E e F. Professor MSc. Elaine Sugauara Disciplina de Química ESPECTRO ELETROMAGNÉTICO As ondas
COLÉGIO ESTADUAL RAINHA DA PAZ, ENSINO MÉDIO REPOSIÇÃO DAS AULAS DO DIA 02 e 03/07/2012 DAS 1 ª SÉRIES: A,B,C,D,E e F. Professor MSc. Elaine Sugauara Disciplina de Química ESPECTRO ELETROMAGNÉTICO As ondas
Resoluções das atividades
 Resoluções das atividades Sumário Aula 1 Evolução dos modelos atômicos: da alquimia ao modelo atômico de Thomson... 1 Aula 2 Evolução dos modelos atômicos: de Rutherford ao modelo atômico de Sommerfeld...
Resoluções das atividades Sumário Aula 1 Evolução dos modelos atômicos: da alquimia ao modelo atômico de Thomson... 1 Aula 2 Evolução dos modelos atômicos: de Rutherford ao modelo atômico de Sommerfeld...
RESUMO 1 MODELOS ATÔMICOS
 RESUMO 1 MODELOS ATÔMICOS A constituição da matéria é motivo de muita curiosidade entre os povos antigos. Filósofos buscam há tempos a constituição dos materiais. Resultado dessa curiosidade implicou na
RESUMO 1 MODELOS ATÔMICOS A constituição da matéria é motivo de muita curiosidade entre os povos antigos. Filósofos buscam há tempos a constituição dos materiais. Resultado dessa curiosidade implicou na
Lista de Exercícios de Recuperação do 3 Bimestre
 Lista de Exercícios de Recuperação do 3 Bimestre Instruções gerais: Resolver os exercícios à caneta e em folha de papel almaço ou monobloco (folha de fichário). Copiar os enunciados das questões. Entregar
Lista de Exercícios de Recuperação do 3 Bimestre Instruções gerais: Resolver os exercícios à caneta e em folha de papel almaço ou monobloco (folha de fichário). Copiar os enunciados das questões. Entregar
LIGAÇÕES QUÍMICAS TEORIA CORPUSCULAR
 LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
Módulo: Tabela Periódica Atividade: Estudo da Tabela Periódica e Distribuição Eletrônica de Linus Pauling
 Guia do Professor Módulo: Tabela Periódica Atividade: Estudo da Tabela Periódica e Distribuição Eletrônica de Linus Pauling I Introdução A atividade Distribuição Eletrônica favorece o desenvolvimento de
Guia do Professor Módulo: Tabela Periódica Atividade: Estudo da Tabela Periódica e Distribuição Eletrônica de Linus Pauling I Introdução A atividade Distribuição Eletrônica favorece o desenvolvimento de
Estão corretos: a) apenas I, II e V. b) apenas I, III e IV. c) apenas II, III e V. d) I, II, III, IV e V. e) apenas I, II, III, IV.
 1. (Ufpr 2014) As teorias atômicas vêm se desenvolvendo ao longo da história. Até o início do século XIX, não se tinha um modelo claro da constituição da matéria. De lá até a atualidade, a ideia de como
1. (Ufpr 2014) As teorias atômicas vêm se desenvolvendo ao longo da história. Até o início do século XIX, não se tinha um modelo claro da constituição da matéria. De lá até a atualidade, a ideia de como
COLÉGIO NOSSA SENHORA DA PIEDADE. Programa de Recuperação Paralela. 2ª Etapa 2014. 1ª série Turma: FG
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
3.2. ORBITAIS E NÚMEROS QUÂNTICOS 3.3. CONFIGURAÇÕES ELETRÔNICAS. Aline Lamenha
 3.2. ORBITAIS E NÚMEROS QUÂNTICOS 3.3. CONFIGURAÇÕES ELETRÔNICAS Aline Lamenha OBJETIVOS Referir os contributos de vários cientistas e das suas propostas de modelo atómico, para a criação do modelo atómico
3.2. ORBITAIS E NÚMEROS QUÂNTICOS 3.3. CONFIGURAÇÕES ELETRÔNICAS Aline Lamenha OBJETIVOS Referir os contributos de vários cientistas e das suas propostas de modelo atómico, para a criação do modelo atómico
Nº máximo 2 8 18 32 32 18 2. Camadas K L M N O P Q 20 Ca (Z=20) 2 8??
 Ligações químicas Na natureza, todos os sistemas tendem a adquirir a maior estabilidade possível. Os átomos ligam-se uns aos outros para aumentar a sua estabilidade. Os gases nobres são as únicas substâncias
Ligações químicas Na natureza, todos os sistemas tendem a adquirir a maior estabilidade possível. Os átomos ligam-se uns aos outros para aumentar a sua estabilidade. Os gases nobres são as únicas substâncias
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo
 Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Química. Química 3 SUMÁRIO. e Pré-vestibular
 Química SUMÁRIO Química 1 MÓDULO 1 Estrutura da matéria - Atomística... 3 Estrutura da matéria: modelos atômicos, Z, A, isótopos e íons Estrutura da matéria: A eletrosfera MÓDULO 2 Classificação periódica
Química SUMÁRIO Química 1 MÓDULO 1 Estrutura da matéria - Atomística... 3 Estrutura da matéria: modelos atômicos, Z, A, isótopos e íons Estrutura da matéria: A eletrosfera MÓDULO 2 Classificação periódica
São Mateus ES, Novembro de 1998 SUMÁRIO. I Introdução. II Desenvolvimento. 2.1 Leis da reações químicas. III Conclusão.
 São Mateus ES, Novembro de 1998 SUMÁRIO I Introdução II Desenvolvimento 2.1 Leis da reações químicas III Conclusão IV Bibliografia I Introdução Tentar-se-à mostrar nesta obra uma pesquisa sobre a Lei das
São Mateus ES, Novembro de 1998 SUMÁRIO I Introdução II Desenvolvimento 2.1 Leis da reações químicas III Conclusão IV Bibliografia I Introdução Tentar-se-à mostrar nesta obra uma pesquisa sobre a Lei das
Eletricidade Aula 1. Profª Heloise Assis Fazzolari
 Eletricidade Aula 1 Profª Heloise Assis Fazzolari História da Eletricidade Vídeo 2 A eletricidade estática foi descoberta em 600 A.C. com Tales de Mileto através de alguns materiais que eram atraídos entre
Eletricidade Aula 1 Profª Heloise Assis Fazzolari História da Eletricidade Vídeo 2 A eletricidade estática foi descoberta em 600 A.C. com Tales de Mileto através de alguns materiais que eram atraídos entre
Exercícios de Revisão de Química 1º ano
 Questão 01) Dentre as alternativas abaixo, indicar a que contém a afirmação correta. a) Dois átomos que possuem o mesmo número de nêutrons pertencem ao mesmo elemento químico. b) Dois átomos com o mesmo
Questão 01) Dentre as alternativas abaixo, indicar a que contém a afirmação correta. a) Dois átomos que possuem o mesmo número de nêutrons pertencem ao mesmo elemento químico. b) Dois átomos com o mesmo
AULA 02: TABELA PERIÓDICA
 AULA 02: TABELA PERIÓDICA 1. INTRODUÇÃO A Tabela Periódica é, efetivamente, um instrumento organizador de conhecimentos sobre os elementos químicos, onde estes estão ordenados por ordem crescente de número
AULA 02: TABELA PERIÓDICA 1. INTRODUÇÃO A Tabela Periódica é, efetivamente, um instrumento organizador de conhecimentos sobre os elementos químicos, onde estes estão ordenados por ordem crescente de número
Propriedades Químicas
 Álvaro Montebelo Barcelos Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
Álvaro Montebelo Barcelos Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
ESTRUTURA DOS MATERIAIS CERÂMICOS
 ESTRUTURA DOS MATERIAIS CERÂMICOS Os sólidos são caracterizados por uma associação muito próxima de átomos, em geral representados por esferas rígidas, em contato uns com os outros e mantidos juntos por
ESTRUTURA DOS MATERIAIS CERÂMICOS Os sólidos são caracterizados por uma associação muito próxima de átomos, em geral representados por esferas rígidas, em contato uns com os outros e mantidos juntos por
Evolução do Modelo Atómico
 Evolução do Modelo Atómico Desde a antiguidade que os homens se preocupavam em saber de que é que as «coisas» são feitas. No entanto, existiam perspectivas diversas sobre o assunto, a mais conhecida das
Evolução do Modelo Atómico Desde a antiguidade que os homens se preocupavam em saber de que é que as «coisas» são feitas. No entanto, existiam perspectivas diversas sobre o assunto, a mais conhecida das
Lista de exercícios 12 Propriedades periódicas
 Lista de exercícios 12 Propriedades periódicas 01. (UEG) O gráfico a seguir indica a primeira variação do potencial de ionização, em função dos números atômicos. Analise o gráfico, consulte a tabela periódica
Lista de exercícios 12 Propriedades periódicas 01. (UEG) O gráfico a seguir indica a primeira variação do potencial de ionização, em função dos números atômicos. Analise o gráfico, consulte a tabela periódica
Correção da ficha de trabalho N.º3
 Correção da ficha de trabalho N.º3 1- Classifique as afirmações seguintes em verdadeiras ou falsas, corrigindo estas últimas: A. A passagem de um átomo de um estado excitado ao estado fundamental é acompanhada
Correção da ficha de trabalho N.º3 1- Classifique as afirmações seguintes em verdadeiras ou falsas, corrigindo estas últimas: A. A passagem de um átomo de um estado excitado ao estado fundamental é acompanhada
-2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE
 -2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
-2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
ESTRUTURA ATÔMICA OS PRIMEIROS MODELOS ATÔMICOS
 1 ESTRUTURA ATÔMICA OS PRIMEIROS MODELOS ATÔMICOS Alguns filosófo da Grécia Antiga já admitiam que toda e qualquer matéria seria formada por minúsculas partículas indivisíveis, que foram denominadas átomos
1 ESTRUTURA ATÔMICA OS PRIMEIROS MODELOS ATÔMICOS Alguns filosófo da Grécia Antiga já admitiam que toda e qualquer matéria seria formada por minúsculas partículas indivisíveis, que foram denominadas átomos
Lista 1 Atomística e tabela periódica
 Lista 1 Atomística e tabela periódica 1. (Ufrn 2013) A Lei Periódica e sua representação gráfica, a Tabela Periódica, são dois conhecimentos essenciais para a química e para os químicos. D. Mendeleev (1834-1907),
Lista 1 Atomística e tabela periódica 1. (Ufrn 2013) A Lei Periódica e sua representação gráfica, a Tabela Periódica, são dois conhecimentos essenciais para a química e para os químicos. D. Mendeleev (1834-1907),
UNIDADE 3 - COORDENAÇÃO ATÔMICA
 A força de repulsão entre os elétrons de dois átomos, quando estão suficientemente próximos, é responsável, em conjunto com as forças de atração, pela posição de equilíbrio dos átomos na ligação química
A força de repulsão entre os elétrons de dois átomos, quando estão suficientemente próximos, é responsável, em conjunto com as forças de atração, pela posição de equilíbrio dos átomos na ligação química
Tabela periódica e propriedades periódicas
 Tabela periódica e propriedades periódicas Mendeleev Vários cientistas procuravam agrupar os átomos de acordo com algum tipo de semelhança, mas o químico russo Dmitri Ivanovich Mendeleev foi o primeiro
Tabela periódica e propriedades periódicas Mendeleev Vários cientistas procuravam agrupar os átomos de acordo com algum tipo de semelhança, mas o químico russo Dmitri Ivanovich Mendeleev foi o primeiro
PROPRIEDADES PERIÓDICAS I
 PROPRIEDADES PERIÓDICAS I Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 EXERCÍCIOS DE APLICAÇÃO 01 Considere as primeiras, segundas, terceiras e quartas energias de ionização dos elementos
PROPRIEDADES PERIÓDICAS I Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 EXERCÍCIOS DE APLICAÇÃO 01 Considere as primeiras, segundas, terceiras e quartas energias de ionização dos elementos
Lista de exercícios 11 Classificação periódica
 Lista de exercícios 11 Classificação periódica 01. (UNESP) Associar os números das regiões da tabela periódica esquematizada a seguir com: a) os metais alcalinos, b) os não-metais, c) os gases nobres,
Lista de exercícios 11 Classificação periódica 01. (UNESP) Associar os números das regiões da tabela periódica esquematizada a seguir com: a) os metais alcalinos, b) os não-metais, c) os gases nobres,
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final Disciplina: Química Ano: 2012 Professor (a): Elisa Landim Turma: 1º FG Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final Disciplina: Química Ano: 2012 Professor (a): Elisa Landim Turma: 1º FG Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista
Configurações eletrônicas
 Configurações eletrônicas Metais de transição Depois de Ar, os orbitais d começam a ser preenchidos. Depois que os orbitais 3d estiverem preenchidos, os orbitais 4p começam a ser preenchidos. Metais de
Configurações eletrônicas Metais de transição Depois de Ar, os orbitais d começam a ser preenchidos. Depois que os orbitais 3d estiverem preenchidos, os orbitais 4p começam a ser preenchidos. Metais de
Atomística Estrutura do Átomo
 Atomística Estrutura do Átomo 1. (Udesc 2014) O enunciado Em um mesmo átomo, não podem existir dois elétrons com o mesmo conjunto de números quânticos refere-se a(ao): a) Princípio da Exclusão de Pauli.
Atomística Estrutura do Átomo 1. (Udesc 2014) O enunciado Em um mesmo átomo, não podem existir dois elétrons com o mesmo conjunto de números quânticos refere-se a(ao): a) Princípio da Exclusão de Pauli.
- LIGAÇÕES IÔNICAS: Na (1s 2 2s 2 2p 6 3s 1 ) + Cl (1s 2 2s 2 2p 6 3s 2 3p 5 ) Na + (1s 2 2s 2 2p 6 ) + Cl - (1s 2 2s 2 2p 6 3s 2 3p 6 )
 - LIGAÇÕES IÔNICAS: A ligação iônica é a ligação química formada pela atração eletrostática entre íons positivos e íons negativos. A ligação se dá entre dois átomos quando um elétron, ou mais um, se transfere
- LIGAÇÕES IÔNICAS: A ligação iônica é a ligação química formada pela atração eletrostática entre íons positivos e íons negativos. A ligação se dá entre dois átomos quando um elétron, ou mais um, se transfere
Adaptado de Professora: Miwa Yoshida. www.colegionobel.com.br/2004quimica1oano/atomo.ppt
 Adaptado de Professora: Miwa Yoshida www.colegionobel.com.br/2004quimica1oano/atomo.ppt Leucipo de Mileto ( 440 a.c.) & Demócrito (460 a.c. - 370 a.c. ) A ideia de dividirmos uma porção qualquer de matéria
Adaptado de Professora: Miwa Yoshida www.colegionobel.com.br/2004quimica1oano/atomo.ppt Leucipo de Mileto ( 440 a.c.) & Demócrito (460 a.c. - 370 a.c. ) A ideia de dividirmos uma porção qualquer de matéria
COMENTÁRIO DA PROVA DE QUÍMICA EQUIPE DE QUÍMICA DO CURSO POSITIVO
 COMENTÁRIO DA PROVA DE QUÍMICA Sem sombra de dúvida, a prova deste ano está muito melhor que a dos anos anteriores. Maior abrangência com temas mais relevantes e grau de dificuldade de médio para difícil,
COMENTÁRIO DA PROVA DE QUÍMICA Sem sombra de dúvida, a prova deste ano está muito melhor que a dos anos anteriores. Maior abrangência com temas mais relevantes e grau de dificuldade de médio para difícil,
História da Química: Empédocles (Séc. V a.c.)
 Prof.: Manzi História da Química: Empédocles (Séc. V a.c.) Teoria sobre os 4 elementos: Terra, Fogo, água e ar Aristóteles ( 350 a.c.) Quando a matéria recebe a forma ela se organiza nos quatro elementos
Prof.: Manzi História da Química: Empédocles (Séc. V a.c.) Teoria sobre os 4 elementos: Terra, Fogo, água e ar Aristóteles ( 350 a.c.) Quando a matéria recebe a forma ela se organiza nos quatro elementos
Elementos do bloco p
 Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
NÚMERO DE OXIDAÇÃO. Porém, nem todos os compostos que existem são formados por íons. Observe a seguinte estrutura: METANO H C
 NÚMER DE XIDAÇÃ INTRDUÇÃ Na química há reações chamadas reações de óxido-redução que são de extrema importância no nosso dia-a-dia. Essas reações (que serão estudadas na próxima unidade) podem apresentar
NÚMER DE XIDAÇÃ INTRDUÇÃ Na química há reações chamadas reações de óxido-redução que são de extrema importância no nosso dia-a-dia. Essas reações (que serão estudadas na próxima unidade) podem apresentar
QUÍMICA QUESTÃO 41 QUESTÃO 42
 Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Os elementos que têm 5 elétrons de valência, ou seja, pertencem à família VA, são P e As, portanto está correto o item D.
 01 Os elementos que têm 5 elétrons de valência, ou seja, pertencem à família VA, são P e As, portanto está correto o item D. 02 A energia de ionização cresce para direita da tabela periódica, portanto
01 Os elementos que têm 5 elétrons de valência, ou seja, pertencem à família VA, são P e As, portanto está correto o item D. 02 A energia de ionização cresce para direita da tabela periódica, portanto
LIGAÇÕES QUÍMICAS. Um novo jeito de se aprender química Helan Carlos e Lenine Mafra- Farmácia- 2014.2
 ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
Nível 1 2 3 4 5 6 7 Camada K L M N O P Q Número máximo de elétrons 2 8 18 32 32 18 2
 DISTRIBUIÇÃO ELETRÔNICA E TABELA PERIÓDICA dos ELEMENTOS INTRODUÇÃO O conhecimento químico é necessário para uma melhor compreensão sobre as propriedades físicas, químicas e mecânicas dos materiais utilizados,
DISTRIBUIÇÃO ELETRÔNICA E TABELA PERIÓDICA dos ELEMENTOS INTRODUÇÃO O conhecimento químico é necessário para uma melhor compreensão sobre as propriedades físicas, químicas e mecânicas dos materiais utilizados,
Átomo e Modelos Atô t m ô ic i o c s o
 Átomo e Modelos Atômicos Demócrito (Sec. V a.c.) defendeu a idéia de que a matéria era composta por pequeníssimas partículas. Átomo Demócrito (460 370 A.C.) Modelo baseado apenas na intuição e na lógica.
Átomo e Modelos Atômicos Demócrito (Sec. V a.c.) defendeu a idéia de que a matéria era composta por pequeníssimas partículas. Átomo Demócrito (460 370 A.C.) Modelo baseado apenas na intuição e na lógica.
Projeto Embuá Unidade de Aprendizagem: ENERGIA
 Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Química 1 Química Geral 1
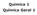 α α = 2 3 2 2 34 2 2 34 56787 977 7 767 34 2 56787 97657 23456789 9 24869 234869 + 567 7657 23456789 24869 24869 2 3 4 35 4 34 + = = Química Geral A Lei Periódica é estabelecida nestes termos: As
α α = 2 3 2 2 34 2 2 34 56787 977 7 767 34 2 56787 97657 23456789 9 24869 234869 + 567 7657 23456789 24869 24869 2 3 4 35 4 34 + = = Química Geral A Lei Periódica é estabelecida nestes termos: As
ânodo TUBO B lâmina de Au anteparo com ZnS
 UFSC 2003 Uma das principais partículas atômicas é o elétron. Sua descoberta foi efetuada por J. J. Thomson em uma sala do Laboratório Cavendish, na Inglaterra, ao provocar descargas de elevada voltagem
UFSC 2003 Uma das principais partículas atômicas é o elétron. Sua descoberta foi efetuada por J. J. Thomson em uma sala do Laboratório Cavendish, na Inglaterra, ao provocar descargas de elevada voltagem
SIMULADO DE QUÍMICA. 1) Para eliminar a poeira e outras impurezas sólidas do ar, muitos aparelhos de purificação usam método da:
 SIMULADO DE QUÍMICA 1) Para eliminar a poeira e outras impurezas sólidas do ar, muitos aparelhos de purificação usam método da: a) ( ) filtração; b) ( ) flotação; c) ( ) separação de mistura; d) ( ) ventilação.
SIMULADO DE QUÍMICA 1) Para eliminar a poeira e outras impurezas sólidas do ar, muitos aparelhos de purificação usam método da: a) ( ) filtração; b) ( ) flotação; c) ( ) separação de mistura; d) ( ) ventilação.
Exercícios Sobre Atomística - Início dos modelos atômicos I
 Exercícios Sobre Atomística - Início dos modelos atômicos I 01. (Cftmg) O filme Homem de Ferro 2 retrata a jornada de Tony Stark para substituir o metal paládio, que faz parte do reator de seu peito, por
Exercícios Sobre Atomística - Início dos modelos atômicos I 01. (Cftmg) O filme Homem de Ferro 2 retrata a jornada de Tony Stark para substituir o metal paládio, que faz parte do reator de seu peito, por
ELETRODO OU SEMIPILHA:
 ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
EXERCÍCIOS - TABELA PERIÓDICA - 2012
 EXERCÍCIOS - TABELA PERIÓDICA - 2012 1- (CEUB) Examine atentamente o gráfico que mostra a variação de determinada propriedade X com o número atômico Z. A) A propriedade X é uma propriedade periódica. B)
EXERCÍCIOS - TABELA PERIÓDICA - 2012 1- (CEUB) Examine atentamente o gráfico que mostra a variação de determinada propriedade X com o número atômico Z. A) A propriedade X é uma propriedade periódica. B)
Química Geral 3º ANO
 Química Geral 3º ANO Teoria de Arrhenius Teoria Ácido-Base Teoria de Arrhenius Teoria Ácido-Base Ácido são substâncias que, dissolvidas em água, se ionizam liberando, na forma de cátions, exclusivamente
Química Geral 3º ANO Teoria de Arrhenius Teoria Ácido-Base Teoria de Arrhenius Teoria Ácido-Base Ácido são substâncias que, dissolvidas em água, se ionizam liberando, na forma de cátions, exclusivamente
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito)
 SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
SEMI 2016 UNIDADES 04 e 05 Química A (Com gabarito) 1 - (UFPR) - Considere um elemento químico (E) com número atômico (Z) igual a 16. a) Qual sua configuração eletrônica para o estado fundamental? a) 1s
INTERAÇÃO DOS RAIOS-X COM A MATÉRIA
 INTERAÇÃO DOS RAIOS-X COM A MATÉRIA RAIOS-X + MATÉRIA CONSEQUÊNCIAS BIOLÓGICAS EFEITOS DAZS RADIAÇÕES NA H2O A molécula da água é a mais abundante em um organismo biológico, a água participa praticamente
INTERAÇÃO DOS RAIOS-X COM A MATÉRIA RAIOS-X + MATÉRIA CONSEQUÊNCIAS BIOLÓGICAS EFEITOS DAZS RADIAÇÕES NA H2O A molécula da água é a mais abundante em um organismo biológico, a água participa praticamente
Química 1ª série Ensino Médio v. 1. Gabarito comentado
 Química 1ª série Ensino Médio v. 1 Exercícios Gabarito comentado Neste material você encontrará, além das respostas das atividades propostas no material didático Energia, resoluções completas com comentários
Química 1ª série Ensino Médio v. 1 Exercícios Gabarito comentado Neste material você encontrará, além das respostas das atividades propostas no material didático Energia, resoluções completas com comentários
Hidrogênio x Hidrogênio Hidrogênio x Não metal Não metal x Não metal
 LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
Esse grupo já foi conhecido como gases raros e gases inertes.
 GASES NOBRES GRUPO 18 OU VIIIA Esse grupo já foi conhecido como gases raros e gases inertes. Gases raros não é apropriado porque o argônio (Ar) não é raro (é mais abundante que o CO 2 no ar). Gases Inertes
GASES NOBRES GRUPO 18 OU VIIIA Esse grupo já foi conhecido como gases raros e gases inertes. Gases raros não é apropriado porque o argônio (Ar) não é raro (é mais abundante que o CO 2 no ar). Gases Inertes
UFSC. Química (Amarela) 31) Resposta: 43. Comentário
 UFSC Química (Amarela) 1) Resposta: 4 01. Correta. Ao perder elétrons, o núcleo exerce maior atração sobre os elétrons restantes, diminuindo o raio. Li 1s2 2s 1 Li+ 1s 2 Raio atômico: átomo neutro > íon
UFSC Química (Amarela) 1) Resposta: 4 01. Correta. Ao perder elétrons, o núcleo exerce maior atração sobre os elétrons restantes, diminuindo o raio. Li 1s2 2s 1 Li+ 1s 2 Raio atômico: átomo neutro > íon
Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2
 11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
Tabel e a l P rió dica
 Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
CENTRO DE EDUCAÇÃO INTEGRADA Educando para o pensar Tema Integrador 2013 / Construindo o amanhã: nós agimos, o planeta sente CONTEÚDOS PROGRAMÁTICOS
 CENTRO DE EDUCAÇÃO INTEGRADA Educando para o pensar Tema Integrador 2013 / Construindo o amanhã: nós agimos, o planeta sente BIOLOGIA I TRIMESTRE A descoberta da vida Biologia e ciência Origem da vida
CENTRO DE EDUCAÇÃO INTEGRADA Educando para o pensar Tema Integrador 2013 / Construindo o amanhã: nós agimos, o planeta sente BIOLOGIA I TRIMESTRE A descoberta da vida Biologia e ciência Origem da vida
PLANEJAMENTO ANUAL / TRIMESTRAL Conteúdos Competências / Habilidades Avaliação/Atividades
 Estrutura atômica I (Unid. 02 e 3) COLÉGIO LA SALLE BRASÍLIA Associação Brasileira de Educadores Lassalistas ABEL SGAS Q. 906 Conj. E C.P. 320 Fone: (061) 3443-7878 CEP: 70390-060 - BRASÍLIA - DISTRITO
Estrutura atômica I (Unid. 02 e 3) COLÉGIO LA SALLE BRASÍLIA Associação Brasileira de Educadores Lassalistas ABEL SGAS Q. 906 Conj. E C.P. 320 Fone: (061) 3443-7878 CEP: 70390-060 - BRASÍLIA - DISTRITO
LIGAÇÕES INTERATÔMICAS
 UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
a) Qual a configuração eletrônica do cátion do alumínio isoeletrônico ao gás nobre neônio?
 Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Leis Históricas da Estequiometria
 Estequiometria A proporção correta da mistura ar-combustível para o motor de uma carro de corrida pode ser tão importante quanto a habilidade do piloto para ganhar a corrida. As substâncias químicas, como
Estequiometria A proporção correta da mistura ar-combustível para o motor de uma carro de corrida pode ser tão importante quanto a habilidade do piloto para ganhar a corrida. As substâncias químicas, como
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 07 TURMA ANUAL
 RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 07 TURMA ANUAL 01. Item D Os elementos que têm 5 elétrons de valência, ou seja, pertencem à família VA, são P e As, portanto está correto o item D. 02. Item B A energia
RESOLUÇÃO DE EXERCÍCIOS PROPOSTOS AULA 07 TURMA ANUAL 01. Item D Os elementos que têm 5 elétrons de valência, ou seja, pertencem à família VA, são P e As, portanto está correto o item D. 02. Item B A energia
