Identificação de novas variantes causativas e investigação da heterogeneidade clínica da Síndrome Aurículo-Condilar
|
|
|
- Luiz Guilherme Graça Carrilho
- 5 Há anos
- Visualizações:
Transcrição
1 Vanessa Luiza Romanelli Tavares Identificação de novas variantes causativas e investigação da heterogeneidade clínica da Síndrome Aurículo-Condilar Identification of novel causative variants and investigation of clinical heterogeneity of Auriculocondylar Syndrome São Paulo 2016
2 Vanessa Luiza Romanelli Tavares Identificação de novas variantes causativas e investigação da heterogeneidade clínica da Síndrome Aurículo-Condilar Identification of novel causative variants and investigation of clinical heterogeneity of Auriculocondylar Syndrome Tese apresentada ao Instituto de Biociências da Universidade de São Paulo, para a obtenção do Título de Doutora em Ciências, na Área de Biologia/Genética. Orientadora: Profª Drª Maria Rita dos Santos e Passos-Bueno São Paulo 2016
3 RESUMO Considerada uma doença de primeiro e segundo arcos faríngeos (FaSPAD), a Síndrome Aurículo-Condilar (ACS) apresenta como principais características micrognatia, malformação auricular típica chamada de question mark ear (QME) e hipoplasia do côndilo mandibular. Variabilidade clínica inter e intrafamiliar, bem como heterogeneidade genética são observadas na ACS. A doença segrega tanto de maneira autossômica dominante quanto recessiva. Variantes patogênicas tem sido identificadas em GNAI3, PLCB4 e EDN1 como responsáveis pela maioria dos casos investigados. Ainda, estudos não publicados do nosso grupo sugerem a ocorrência de um quarto locus causativo de ACS. No presente trabalho tivemos por objetivo identificar as variantes causativas de ACS em casos anteriormente descritos e casos ainda não reportados e nos propusemos a investigar a heterogeneidade clínica da ACS. Identificamos variantes patogênicas nos genes PLCB4 e GNAI3 em 5 de 6 casos de ACS. No caso restante (1 6), restringimos o quarto locus candidato a conter variante causativa de ACS. Estudos adicionais estão sendo realizados afim de identificá-la. Sugerimos também que todas as variantes em GNAI3, aqui e anteriormente descritas, interfiram direta ou indiretamente com a ligação GDP GTP, agindo com um mecanismo dominante negativo. Além disso, encontramos achados clínicos adicionais em pacientes com ACS e variantes em PLCB4.
4 ABSTRACT Considered as a first and second pharyngeal arch disease (FaSPAD), the Auriculocondylar Syndrome (ACS) presents with micrognathia, a typical ear malformation called question mark ear (QME), and mandibular condyle hypoplasia as main features. Intra and inter-familial clinical variability as well as genetic heterogeneity are observed in ACS. The disease segregates in both autosomal dominant and recessive manner. Pathogenic variants have been identified in GNAI3, PLCB4, and EDN1 in the majority of the investigated cases. Furthermore, non-published studies of our group indicate a fourth locus associated with ACS. In the present study, our aim was to identify the causative variants of ACS in previously and not reported cases and also to investigate the clinical heterogeneity of ACS. We identified pathogenic variants in PLCB4 and GNAI3 in 5 out of 6 ACS cases. In the remaining case (1 6), we narrow down the fourth candidate region to contain causative variant of ACS. Additional studies are being conducted to identify it. We also hypothesized that all GNAI3 variants, herein and previously described, interfere with the GDP GTP binding, acting through a dominant negative mechanism. Furthermore, we found additional clinical findings in patients with ACS and PLCB4 variants.
5 INTRODUÇÃO GERAL A Síndrome Aurículo-Condilar (ACS, MIM , , ) é uma doença rara que possue diferentes modos de herança dependendo da variante patogênica encontrada: a maioria dos casos apresenta herança autossômica dominante com penetrância incompleta; enquanto uma minoria apresenta padrão de herança autossômico recessivo (revisto em Clouthier et al., 2013). Ao longo desse capítulo apresentaremos o fenótipo de ACS, seguindo para uma breve descrição de estruturas embrionárias importantes para a compreensão da via molecular envolvida com a doença. Apresentaremos também as variantes causais e respectivos mecanismos de ação recentemente relacionados com a síndrome. CARACTERÍSTICAS CLÍNICAS DA SÍNDROME AURICULO-CONDILAR A ACS apresenta como principais características fenotípicas a micrognatia, hipoplasia do côndilo mandibular e uma malformação auricular típica, chamada de question mark ear (QME). A QME é definida por uma fenda total ou parcial entre o lóbulo e a hélice da orelha, conferindo a aparência de um ponto de interrogação a esta estrutura e pode ser observada como característica isolada nos pacientes chamada de QME isolada (IQME, MIM ) (Gerkes et al., 2008; Guion-almeida et al., 1999; Guion-Almeida et al., 2002; Jampol et al., 1998; Masotti et al., 2008; Shkalim et al., 2008; Storm et al., 2005, Cosman et al., 1970; Al-Qattan, 1998; Uuspaa, 1978; Priolo et al., 2000). Ainda, as malformações mandibulares de alguns pacientes levaram Rieder et al. (2012) à hipótese de que uma transformação homeótica estaria ocorrendo nos
6 pacientes com a ACS, onde a mandíbula assumiria um padrão fenotípico semelhante à maxila (tópico reinterado adiante). Outros achados frequentemente encontrados na ACS são microstomia, maloclusão, bochechas salientes, glossoptose, agenesia ou hipoplasia do côndilo mandibular e alterações da articulação temporomandibular (ATM) (Figura 1). Esta última característica pode remeter a uma redução na mobilidade da mandíbula à apenas alguns milímetros de abertura da boca (Gerkes et al., 2008; Guion-almeida et al., 1999; Guion-Almeida et al., 2002; Jampol et al., 1998; Masotti et al., 2008; Storm et al., 2005; Priolo et al., 2000). Figura 1. Variabilidade fenotípica vista em casos distintos de pacientes com a ACS. (A) paciente com micrognatia grave levando à necessidade de traqueostomia e bochechas proeminentes. (B) Projeção lateral de tecido mole na base da língua; (C) Paciente com micrognatia e malformação auricular. (D) Variabilidade intra-familial da ACS, com ênfase na malformação auricular; note na figura da direita a constrição auricular resultante na question mark ear (QME). (E) Paciente com microstomia, bochechas proeminentes, micrognatia; a seta indica uma proeminência na região posterior da orelha (post-auricular tag). Figuras retiradas e modificadas de (A) Storm et al., (2005); (B) Rieder et al., (2012); (C) Guion-Almeida et al., (2002); (D) Masotti et al., (2008); e (E) Gordon et al., (2013a).
7 A ACS manifesta-se com grande variabilidade clínica inter e intrafamiliar. Nos casos mais graves as alterações podem estar associadas à dificuldades respiratórias, com necessidade de traqueostomia. Outras características vistas com menos frequência incluem assimetria facial, fenda palatina, diminuição da audição, apêndice na região posterior da orelha (post-auricular tags) (Guion-Almeida et al., 2002; Masotti et al., 2008; Storm et al., 2005), apneia obstrutiva e central, projeção de tecidos moles lateralmente na base da língua, alterações gastrointestinais e macropênis. Às alterações extra-craniofaciais cabe ressaltar que foram somente vistas em casos onde a doença se apresenta de maneira recessiva e com variantes patogênicas em PLCB4 (Gordon et al., 2013a; Kido et al., 2013; Rieder et al., 2012). Observa-se que alguns sinais clínicos da ACS, tais como malformações auriculares e micrognatia, se sobrepõem ao de outras síndromes craniofaciais de primeiro e segundo arcos faríngeos, como síndrome de Treacher Collins (TCS; MIM ), espectro Óculo-Aurículo Vertebral (OAVS; MIM ) e sequência de Pierre Robin (PRS, MIM ). Contudo, as malformações de orelha presentes no OAVS e na TCS são diferentes das vistas na ACS, que parecem bem específicas em relação à constrição auricular. A TCS também apresenta hipoplasia dos arcos zigomáticos e coloboma palpebral, que a diferencia de ACS, enquanto que na OAVS podem ocorrer alterações cardíacas, renais e do sistema nervoso central (Gorlin, 2001; Gordon et al., 2013a). DESENVOLVIMENTO EMBRIONÁRIO As principais estruturas acometidas na ACS são originadas do primeiro e segundo arcos faríngeos (também chamados de arcos branquiais), que por sua vez são compostos por células da crista neural (NCC), com um centro de células de origem
8 mesodérmica. Assim, classifica-se esta malformação como uma doença de primeiro e segundo arcos faríngeos embrionários (Graham et al., 2004; Passos-Bueno et al., 2009; Sadler, 1995). As NCC tem origem na borda entre a ectoderme neural e não-neural e uma complexa via de sinalização coordena sua indução, migração e proliferação (Figura 2) (Crane & Trainor, 2006; Knecht & Bronner-Fraser, 2002; Ruffins & Bronner-Fraser, 2000). Migrando em direção aos arcos faríngeos, elas irão contribuir para um conjunto específico de elementos (Larsen, 1997; Carlson, 2005). O primeiro arco faríngeo apresenta dois domínios: a proeminência ou processo maxilar, que dará origem à maxila, osso zigomático e parte do osso temporal; e a proeminência ou processo mandibular. O primeiro arco faríngeo também dará origem a estruturas como os músculos da mastigação, parte da bigorna (ou incus) e martelo (ou malleus), parte da orelha externa e da língua. Já o segundo arco faríngeo origina, dentre outros, parte da orelha externa, o estribo, processo estilóide e o menor corno do osso hióide, enquanto o corno maior do hióide é derivado do terceiro arco faríngeo (Figura 3) (revisto em Johnson, 2010; Minoux & Rijli, 2010). O primeiro arco faríngeo e o processo frontonasal estão envolvidos na formação facial que tem início no decorrer da quarta semana do desenvolvimento embrionário humano. Na quarta semana ocorre a fusão dos dois processos mandibulares, derivados do primeiro arco branquial, na linha média. Enquanto que, na quinta e sexta semanas de gestação, os processos maxilares crescem em direção à linha média resultando em sua fusão entre a sexta e sétima semanas (revisto em Johnson et al., 2010; Garcia & Fernández, 2001).
9 Figura 2. A borda da placa neural (verde) é induzida pela sinalização entre a neuroectoderme (roxo) e a ectoderme não neural (azul) e do mesoderma paraxial abaixo (amarelo). Durante a neurulação, as bordas da placa neural (dobramento neural) se elevam, ocasionando a formação do tubo neural. Células da crista neural (verde) se delaminam das pregas neurais e migram (modificada de Gammil & Bronner-Fraser, 2003). A partir do quinto mês fetal o centro de crescimento do côndilo mandibular será responsável pelo alongamento da mandíbula durante os primeiros 10 anos de vida pósnatal (Garcia & Fernández, 2001 e revisto em Serrano et al., 2011). A importância do côndilo nesse período é reforçada pela observação de lesões no côndilo em camundongos com 3 semanas de idade, as quais resultam na redução do crescimento condilar e mandibular, levando à assimetria da mandíbula e deslocamento lateral (Nakano et al., 2009).
10 Figura 3. Na imagem do embrião, migração das células da crista neural partindo dos rombômeros para os arcos faríngeos. Ao lado (humano), principais estruturas faciais formadas a partir de populações de células da crista neural. AS, osso alisfenóide; BA1-BA3, arcos faríngeos 1-3; DE, osso dentário; di, diencéfalo; FNP, processo frontonasal; FR osso frontal; HY, osso hióide; IN, bigorna (incus); MA, martelo (ou malleus); mês, mesencéfalo; MX, osso maxilar; NA, osso nasal; PA osso parietal; R1-R7 rombômeros 1-7; SQ, osso esquamosal; ST, estribo; ZY, osso zigomático (modificado de Santagati & Rijli, 2003). Já a formação da orelha externa começa com massas auriculares advindas do mesênquima do primeiro e segundo arcos, as quais, com 41 dias de desenvolvimento embrionário, apresentam-se em número de seis (Figura 4). A fusão dessas massas auriculares formará a orelha externa e diversos autores tem tentado correlacionar qual das seis massas auriculares é responsável pela formação de cada parte da orelha externa, entretanto, sem terem chegado à um consenso. À medida que os arcos mandibulares crescem, as orelhas são puxadas para a região respectiva da face, onde tomam posição definitiva na 12ª semana (revisto em Park, 1999; e O Rahilly & Muller, 1992; Garcia & Fernández, 2001; Carlson, 2005).
11 Figura 4. Interação entre os primeiro (verde) e segundo (vermelho) arcos faríngeos para a formação da orelha externa. Abaixo, microscopia eletrônica de um embrião com cinco semanas de gestação. Massas nodulares de mesênquima se organizam e se fundem para a formação da orelha externa. ASPECTOS GENÉTICOS DA ACS A ACS é uma doença que segrega majoritariamente com padrão de herança autossômico dominante, mas que pode também apresentar-se com herança autossômica recessiva. Estima-se que a prevalência seja <1/ (Orphanet, coordenado pelo French INSERM team; O primeiro estudo genético sobre a ACS foi conduzido por nosso grupo em duas famílias com fenótipo segregando de maneira autossômica dominante, no qual definimos, por meio de análise de ligação, o primeiro locus candidato mapeado na região 1p21.1-q23.3. Observamos ligação destes marcadores e a ACS somente em uma das duas famílias estudadas, indicando a ocorrência de heterogeneidade genética (Masotti et al., 2008). A família para a qual não houve evidência de ligação na região do
12 cromossomo 1 (família que chamaremos de F1 no presente trabalho) foi investigada durante meu projeto de mestrado e identificamos um quarto locus candidato a conter a variante causativa de ACS (dados não publicados; Romanelli Tavares, 2011). Recentemente, variantes patogênicas foram descritas em três genes, confirmando a ocorrência de heterogeneidade genética para a doença: guanine nucleotide-binding protein (G protein), alpha inhibiting activity polypeptide 3 (GNAI3, MIM ), localizado dentro da região candidata 1p21.1-q23.3 e confirmando, portanto, o estudo de ligação de Masotti et al. (2008) (Gordon et al., 2013a; Rieder et al., 2012); phospholipase C, beta 4 (PLCB4, MIM ), localizado em 20p12.2 (Gordon et al., 2013a; Kido et al., 2013; Rieder et al., 2012); endothelin 1 (EDN1, MIM ), localizado em 6p24.1 (Gordon et al., 2013b). O número total de casos da ACS molecularmente investigados ainda é pequeno - apenas 21 casos, dentre os aproximadamente 50 descritos (incluindo IQME) (revisto em Gordon et al., 2013a). Dentre estes, 95,2% (20/21) dos pacientes estudados tiveram variantes identificadas em um dos três genes descritos: 80% segregam com padrão autossômico dominante, tendo mostrado alterações em qualquer um dos três genes identificados; e 20% segregam de maneira autossômica recessiva, onde somente variantes patogênicas em PLCB4 e EDN1 foram encontradas (Figura 5) (Gordon et al., 2013b; Gordon et al., 2013a; Kido et al., 2013; Rieder et al., 2012). O único caso publicado, investigado e ainda não solucionado refere-se ao paciente A001 descrito em Rieder et al. (2012), para o qual não foram encontradas variantes patogênicas em GNAI3 e PLCB4. Dados dos autores, de variantes selecionadas por sequenciamento completo de exoma, não mostram evidências de alterações no gene EDN1 (relacionado
13 à ACS posteriormente à publicação). Além da família F1 (acima referida), que possui evidência de ligação para um quarto locus causativo de ACS, temos conhecimento de um terceiro caso para o qual não foram encontradas variantes em GNAI3, PLCB4 e EDN1 (comunicação pessoal Christopher T. Gordon, Abril, 2014). Dentre os casos autossômico dominantes, observa-se penetrância incompleta (estimativa ainda desconhecida) somente em famílias com variantes patogênicas em PLCB4 ou GNAI3; enquanto que, casos de alterações de novo só foram reportados para pacientes com variantes causais em PLCB4 (Gordon et al., 2013a; Rieder et al., 2012). Figura 5. Porcentagem de casos da ACS investigados molecularmente. Ao centro: gráfico contendo a porcentagem de variantes em GNAI3, PLCB4 e EDN1 e casos não elucidados (somente os publicados). À esquerda (gráfico em verde): casos com variantes patogênicas em EDN1. À direita (gráfico em azul): casos com variantes causativas de ACS no gene PLCB4. Para GNAI3, todas as variantes encontradas estão em heterozigose.
14 GNAI3 Proteínas G são ativadas por receptores transmembrana e são compostas por 3 (três) subunidades: alfa (α), beta (β) e gama (γ). O gene GNAI3 codifica a subunidade alfa da proteína a qual, quando ativada por guanosina trifosfato (GTP), regula efetores intracelulares (Gene ID 2773; revisto em Sprang et al., 1997). Até recentemente, foram encontradas duas variantes em heterozigose presentes em GNAI3, preditas missense, em três casos distintos de ACS: p.(gly40arg) e p.(ser47asn) (Gordon et al., 2013a; Rieder et al., 2012). Todas foram herdadas e se localizam no domínio G1 box da proteína, um dos cinco motivos (G1-G5) altamente conservados e envolvidos na ligação de guanosina difosfato (GDP)/GTP à subunidade alfa da proteína G (Wennerberg et al., 2005) (Figura 6A). Através da modelagem estrutural in silico da proteína, foi sugerido que a variante p.(gly40arg) atue por mecanismo de ganho de função (Rieder et al., 2012). Contudo, Gordon et al. (2013a) sugerem que a variante que modifica o resíduo Ser47 atue com um mecanismo dominante negativo e propõe que o mesmo ocorra com a outra alteração identificada. Esta última hipótese é baseada em estudos in vitro que mostram que uma variante equivalente à p.(ser47asn), presente no domínio G1 de HRAS (p.ser17asn), tem como consequência efeito dominante negativo com propriedades inibitórias de crescimento (revisto em Barren & Artemyev, 2007; Feig 1999). Devido à tal divergência de mecanismos de ação das variantes em GNAI3, estudos adicionais precisam ser realizados para elucidar esta questão. PLCB4 Enzimas fosfolipase C (PLC) fazem a transdução de sinais intracelulares através da produção de inositoltrifosfato (IP3) e diacilglicerol (DAG), oriundos da catálise de fosfatidilinositol 4,5-bifosfato (PIP2). Atualmente 11 isoformas de PLC foram descritas
15 e classificadas entre as subfamílias beta (β), gama (γ), delta (δ) e epsilon (ε). O gene PLCB4 pertence a subfamília β que contém quatro membros (PLCB1-4). As PLCB são proteínas que contém um domínio N-terminal PH (pleckstrin homology), domínio EF (EF hand-like), domínios catalíticos X e Y e um domínio C2 de ligação ao cálcio (revisto em Rhee, 2001; Gene ID 5332). Variantes em PLCB4 correspondem à maioria das alterações identificadas em pacientes com ACS, segregando com padrão de herança autossômico dominante e também recessivo: 2/13 das variantes patogênicas em PLCB4 ocorrem em homozigose e levam à perda de função da proteína, sendo: 1 caso com deleção intragênica que ocasiona troca do quadro de leitura (frameshift), resultando em códon de parada prematuro; e 1 caso de heterozigoto composto predito por romper sítio de splice (Figura 6C). Estas variantes resultam no aparecimento de alterações extra-craniofaciais, como distúrbios gastrointestinais e macropênis mencionados anteriormente (Gordon et al., 2013a; Kido et al., 2013). 11/13 das variantes patogênicas em PLCB4 ocorrem em heterozigose, são preditas missense e se localizam dentro dos domínios catalíticos X e Y da proteína (Figura 6B) (Gordon et al., 2013a; Rieder et al., 2012), domínios estes presentes em todas as 11 isoformas de PLC (revisto em Rhee, 2001); Essas alterações são preditas por afetarem pontes de hidrogênio e iônicas essenciais para a ação de PLCB4 na catálise de PIP2 em IP3 e DAG, agindo com um mecanismo funcional dominante negativo (Gordon et al., 2013a; Kido et al., 2013; Rieder et al., 2012). Essa hipótese é baseada na presença de variantes missense nos domínios catalíticos X e Y do gene schmerle (she) de zebrafish (Danio rerio), que codifica uma proteína ortóloga de Plcβ3
16 (homóloga à PLCβ4) e ocasionam um efeito dominante negativo com redução de elementos faciais cartilaginosos (Walker, et al., 2007 e Gordon et al., 2013a). EDN1 A EDN1 é uma proteína primeiro traduzida como pre-proendotelina com 212 aminoácidos, posteriormente quebrada pela furina em 2 sítios específicos de reconhecimento (na região C-terminal da sequencia consenso Arg-Ser-Lys-Arg) para gerar a big-endothelin, então com 38 aminoácidos; e a seguir, a endothelin converting enzyme (ECE) faz a quebra da big-endothelin em EDN1 madura e ativa, com 21 aminoácidos (revisto em Clouthier et al., 2013; Gordon et al., 2013b). Variantes em EDN1 foram observadas segregando de forma autossômica dominante e também recessiva, observadas em casos distintos de ACS e com grande variabilidade fenotípica. Uma das variantes patogênicas encontradas em EDN1, a p.(lys91glu), é predita por alterar o sítio de reconhecimento da furina, enquanto que a variante p.(pro77his) se localiza dentro da bigedn1 e é predita por desestabilizar a proteína. Ambas foram vistas em homozigose e em pacientes com o fenótipo da ACS. Sugere-se que as variantes atuem de maneira hipomórfica, uma vez que camundongos Edn1 homozigotos nulos desenvolvem um fenótipo mais grave do que o encontrado nos pacientes com estas alterações. Variantes em heterozigose, p.(val64asp) (localizada na EDN1 madura) e p.(tyr83*) (localizada na bigedn1), também foram encontradas e preditas por diminuir a capacidade de ligação do peptídeo e levar a um alelo nulo via decaimento mediado por alteração nonsense, respectivamente (Figura 6D). Quando presentes, as variantes em heterozigose causam somente IQME nos pacientes. Assim, é proposto que
17 as diferenças fenotípicas encontradas em casos de variantes em homozigose e heterozigose em EDN1 estariam relacionadas com a quantidade de proteína residual funcional (Gordon et al., 2013b). Figura 6. Esquema das proteínas GNAI3, PLCB4 (gene representado abaixo) e EDN1 e as respectivas variantes patogênicas encontradas em casos da ACS (indicadas abaixo de cada esquema). Os domínios conservados de GNAI3 e PLCB4 foram reportados como vistos no Conserved Domain Database (CDD). EDN1 foi modificado de Gordon et al., 2013b. (A) GNAI3 mostrando os domínios G1-G5 box em cinza; (B) PLCB4 mostrando os domínios em cinza: PH (pleckstrin homology), EF (EF hand-like), domínios catalíticos X e Y e C2 (domínio de ligação ao cálcio); (C) região parcial do PLCB4 mostrando intron 12 ao intron 25; exons representados como barras verticais pretas ao longo da barra horizontal; regiões entre exons representam os introns; alelos que compõem o heterozigoto composto estão em regiões aceptora e doadora de splicing, respectivamente na imagem. (D) EDN1: bigedn1 mostrada em duas escalas de cinza; EDN1 madura mostrada em cor cinza escuro; cabeças de setas vazias indicam o sítio de clivagem da furina; cabeça de seta cheia (preto) indica o sítio de clivagem de ECE; SP região de sinal de peptídeo.
18 VIA EDN1-EDNRA-DLX5/6 DE SINALIZAÇÃO As proteínas PLCB4 e GNAI3 são preditas por atuarem como mediadores intracelulares na via da endotelina receptor de endotelina tipo A (EDN1-EDNRA) (Rieder et al., 2012) como discutido adiante. Por sua vez, as variantes patogênicas encontradas em EDN1, em pacientes com ACS, confirmam o envolvimento da via com a doença. A ACS é causada por alterações em domínios faciais específicos derivados das NCC que migram para os arcos faríngeos. A sinalização através do Ednra, um receptor transmembrana acoplado à proteína G, é fundamental para o estabelecimento da identidade das NCC no domínio mandibular do primeiro arco faríngeo (Kurihara et al., 1994; Clouthier et al., 1998; Clouthier et al., 2010). Camundongos com perda de Edn1, Ece1 ou Ednra apresentam graves alterações de estruturas derivadas da proeminência mandibular do primeiro arco e dos arcos 2-4, como: malformações da mandíbula, malleus, incus e estruturas da traqueia; além de uma transformação homeótica da mandíbula em estrutura semelhante à maxila (duplicação da maxila) (Clouthier et al., 1998; Yanagisawa et al., 1998; Kurihara et al., 1994). Para entender um pouco mais sobre o papel da endotelina é importante saber que os arcos faríngeos podem ser divididos em três domínios (Tavares et al., 2012 revisto em Clouthier et al., 2013): (1) domínio distal, que dá origem a cartilagem de Meckel, osso mandibular e parte do malleus em camundongo (Ruest et al., 2003); (2) domínio intermediário, que em camundongos dá origem a uma porção da mandíbula proximal, parte do incus e o tecido fibroso ao redor da junção entre o malleus e o incus (Ruest et al., 2003; Tavares et al., 2012; Tucker et al., 2004); (3) e o domínio proximal, ainda não bem definido em
19 camundongo, mas que provavelmente dá origem à estruturas mais proximais da mandíbula (Depew et al., 2005; Ruest et al., 2004). Nos domínios distal e intermediário, a ativação de Ednra leva a expressão de Dlx5/Dlx6 (Ozeki et al., 2004; Ruest et al., 2004; Charité et al., 2001). É proposto que os genes Dlx estabeleçam a segmentação dorso-ventral dentro dos arcos faríngeos com um padrão combinatório, semelhante ao que acontece com os genes Hox na segmentação antero-posterior dos arcos (Clouthier et al., 2013). Camundongos Dlx5 -/- Dlx6 -/- mostram uma transformação homeótica da mandíbula em maxila, perdendo domínios de expressão de genes que atuam no desenvolvimento mandibular no primeiro arco faríngeo (Alx4, dhand, Dlx3, Dlx5/6, Bmp7 e Pitx1) enquanto que a expressão de genes que participam do desenvolvimento na proeminência maxilar (Dlx1, Dlx2, Msx1, Msx2 e Prx1 ) se mantém (Beverdam et al., 2002; Depew et al., 2002). Também no domínio distal do arco faríngeo, Dlx5/Dlx6 induzem a expressão de basic helix-loophelix transcription factor Hand2 onde, por sua vez, Hand2 inibe Dlx5 e Dlx6. Esse mecanismo de regulação negativa é fundamental para estabelecer a identidade proximodistal do arco mandibular durante o desenvolvimento embrionário uma vez que a inativação de Hand2 nas NCC, em camundongos, resulta em alterações no desenvolvimento mandibular e, principalmente, aglossia (Barron et al., 2011) (Figura 7). Contudo, a indução de Hand2 por Dlx5/Dlx6 ocorre, provavelmente, de maneira alternada e compensatória, uma vez que embriões de camundongo Dlx5 -/- ou Dlx6 -/- não apresentam diminuição da expressão de Hand2 (Jeong et al., 2008). Já dentro do domínio intermediário, a sinalização de Ednra regula a expressão de Dlx3 e Nkx3.2 (Clouthier et al., 2000; Tavares et al., 2012; Miller et al., 2003).
20 Figura 7. Camundongos mutantes para genes ativados na via Edn1-Ednra. À direita de cada imagem marcação para osso (vermelho coloração de vermelho de alizarina) e cartilagem (azul coloração de azul de alcian). (A) Camundongo com fenótipo selvagem (wt); (B) Camundongo mutante Ednra - - ; observe nas duas imagens a mandíbula menor em comparação com a mostrada na figura A. (C) Camundongo selvagem (wt) e mutante Dlx ; cabeça de seta branca indica tecido mole atípico; vb e vbf: folículo de vibrissa. À direita da imagem: cabeça de seta verde indica perda de estruturas nasais; UI: incisivos superiores hipoplásticos; mx*: transformação do osso dentário em maxila (mx); LI: incisivos inferiores rudimentares. (D) Camundongo selvagem (wt) e mutante Hand2 cko ; note a ausência da língua [(t), em wt; (*) em Hand2 cko ]; md: mandíbula; in: incisivos; mv: vibrissas. À direita da imagem: retrognatia; md: mandíbula. Figuras retiradas e modificadas de: (A,B) Clouthier et al., 2013 (veja também Ruest et al., 2004 para mais detalhes; (C) Depew et al., 2002; e (D) Barron et al., 2011.
21 Com isso vemos a importância do papel da EDN1-DLX5/6 durante o desenvolvimento mandibular e fica evidente que as alterações na via EDN1-EDNRA em modelos animais levam à malformações muito parecidas às ocorridas em pacientes com ACS. Alterações similares também foram observadas em camundongos Gαq (-/-) Gα11 (+/-) que possuem malformações em estruturas craniofaciais como mandíbula e anel timpânico semelhantes, embora menos graves, às alterações presentes em camundongos com deficiência de Edn1 (Kurihara et al., 1994) e Ednra (Clouthier et al., 1998). Os estudos indicam que Gαq e Gα11 sejam mediadoras da sinalização de Edn1 nos arcos faríngeos, uma vez que uma única cópia de Gα11 resulta na diminuição da expressão de Dlx3 e Dlx6 e mostra que níveis mínimos de expressão e atividade de Gαq e Gα11 são necessárias para a expressão de alguns alvos da via da endotelina-1 (Ivey et al., 2003). Ainda, a literatura mostra que o gene she (schlerme) em zebrafish, que codifica um ortólogo a Plcb3 (homólogo de PLCB4) age abaixo do receptor de endotelina, uma vez que mutações nesse gene resultam na redução da expressão de dlx5a, dlx6a e dlx3b e em alterações de estruturas derivadas dos arcos faríngeos: como hipoplasia e fusão dos arcos faríngeos. As alterações craniofaciais assemelham-se às ocorridas quando a via da Edn1 é comprometida, no entanto sendo menos graves (Walker et al., 2007). Baseado nestes estudos de Gαq, Gα11 e Plcb3, bem como nos achados clínicos dos pacientes com ACS origina-se a hipótese de que PLCB4 e GNAI3 atuem na via EDN1-EDNRA (Figura 8). Além desses, o trabalho de Rieder et al. (2012) mostra a redução de genes alvos de EDN1-EDNRA, DLX5 e DLX6, em osteoblastos mandibulares de quatro pacientes com mutações em PLCB4 ou GNAI3 não aparentados e um caso molecularmente não resolvido de ACS.
22 Figura 8. Via proposta da sinalização intracelular induzida por Edn1-Ednra. Azul: camundongo e zebrafish. Verde: humanos. Rosa: camundongos. Vide texto para maiores detalhes. Retirado e modificado de Clouthier et al. (2013). Diante da introdução acerca do tema, podemos concluir que a ACS é uma doença altamente heterogênea tanto no que diz respeito às variantes causativas, quanto ao espectro de variabilidade clínica ainda pouco caracterizado. Também, o mecanismo de ação das variantes patogênicas encontradas em GNAI3 precisa ser elucidado, uma vez que os estudos recentes são controversos em propor ganho de função ou dominante negativo. Ainda, embora a identificação de loci e variantes causativas da ACS tenham ocorrido de forma crescente nos últimos três anos, nem todos os mecanismos genéticos relacionados com a síndrome são conhecidos. Além de uma quantidade significativa de casos ainda não investigados molecularmente e casos sem alterações nos três loci já relacionados com a doença, estudos anteriores do nosso grupo, realizados em pacientes da família F1, apresentam fortes evidências para a ocorrência de um quarto locus relacionado com a síndrome.
23 CONCLUSÕES GERAIS 1. Identificamos três variantes em GNAI3, assim determinando a causa da ACS na família originalmente ligada a região 1p21.1-q23.3 e as primeiras variantes de novo em dois casos de ACS esporádicos; 2. Propomos que todas as variantes em GNAI3, até o momento descritas, interfiram direta ou indiretamente na ligação GDP/GTP, levando a um efeito dominante negativo; 3. Identificamos duas variantes em PLCB4, ainda não descritas, que corroboram o efeito dominante negativo; 4. Confirmamos e restringimos o quarto locus candidato a conter variante causativa de ACS; 5. Encontramos achados clínicos, ainda não descritos, em pacientes com ACS e variantes em PLCB4; 6. Pacientes com variantes em GNAI3 podem apresentar perda auditiva sensorineural e ou condutiva.
24 REFERÊNCIAS BIBLIOGRÁFICAS Referente à introdução: Websites: Orphanet, coordenado pelo French INSERM team, OMIM Online Mendelian Inheritence in Man, CDD Conserved Domain Database, Gene, Al-Qattan, M. M. (1998). Cosman (question mark) ear: congenital auricular cleft between the fifth and sixth hillocks. Plastic and reconstructive surgery 102(2): Barren, B., & Artemyev, N. O. (2007). Review Mechanisms of Dominant Negative G-Protein a Subunits, 3514(December 2006), Barron, F., Woods, C., Kuhn, K., Bishop, J., Howard, M. J., & Clouthier, D. E. (2011). Downregulation of Dlx5 and Dlx6 expression by Hand2 is essential for initiation of tongue morphogenesis. Development, 138(11), Beverdam, A., Merlo, G. R., Paleari, L., Mantero, S., Genova, F., Barbieri, O., Levi, G. (2002). Jaw transformation with gain of symmetry after Dlx5/Dlx6 inactivation: mirror of the past? Genesis (New York, N.Y. : 2000), 34(4), Carlson, B.M.. Human Enbryology and Developmental Biology. 3rd Ed. Elsevier: Philadelphia, PA, USA Gammil & Bronner-Fraser, 2003 Charité, J., McFadden, D. G., Merlo, G., Levi, G., Clouthier, D. E., Yanagisawa, M., Olson, E. N. (2001). Role of Dlx6 in regulation of an endothelin-1-dependent, dhand branchial arch enhancer. Genes & Development, 15(22), Clouthier, D. E., Garcia, E., & Schilling, T. F. (2010). Regulation of facial morphogenesis by endothelin signaling: insights from mice and fish. American Journal of Medical Genetics. Part A, 152A(12), Clouthier, D. E., Hosoda, K., Richardson, J. a, Williams, S. C., Yanagisawa, H., Kuwaki, T., Yanagisawa, M. (1998). Cranial and cardiac neural crest defects in endothelin-a receptordeficient mice. Development (Cambridge, England), 125(5), Clouthier, D. E., Passos-Bueno, M. R., Tavares, A. L. P., Lyonnet, S., Amiel, J., & Gordon, C. T. (2013). Understanding the basis of auriculocondylar syndrome: Insights from human, mouse and zebrafish genetic studies. American Journal of Medical Genetics Part C: Seminars in Medical Genetics, 163(4), Clouthier, D. E., Williams, S. C., Yanagisawa, H., Wieduwilt, M., Richardson, J. A., & Yanagisawa, M. (2000). Signaling pathways crucial for craniofacial development revealed by endothelin-a receptor-deficient mice. Developmental Biology, 217(1), Cosman, B., H. Bellin, et al. (1970). The Question Mark ear. Plastic and reconstructive surgery 46(5):
25 Crane, J., & Trainor, P. A. (2006). Neural crest stem and progenitor cells. Annual Review of Cell and Developmental Biology, 22, Depew, M. J., Lufkin, T., & Rubenstein, J. L. R. (2002). Specification of jaw subdivisions by Dlx genes. Science (New York, N.Y.), 298(5592), Depew, M. J., Simpson, C. a, Morasso, M., & Rubenstein, J. L. R. (2005). Reassessing the Dlx code: the genetic regulation of branchial arch skeletal pattern and development. Journal of Anatomy, 207(5), Feig, L. a. (1999). Tools of the trade: use of dominant-inhibitory mutants of Ras-family GTPases. Nature Cell Biology, 1(2), E25 E27. Garcia, S.M.L., Fernández C.G.. Embriologia. 2ª Ed. Editora Artmed: Porto Alegre Gerkes, E. H., van Ravenswaaij, C. M. a, & van Essen, A. J. (2008). Question mark ears and post-auricular tags. European Journal of Medical Genetics, 51(3), Gordon, C. T., Petit, F., Kroisel, P. M., Jakobsen, L., Zechi-Ceide, R. M., Oufadem, M., Amiel, J. (2013b). Mutations in endothelin 1 cause recessive auriculocondylar syndrome and dominant isolated question-mark ears. American Journal of Human Genetics, 93(6), Gordon, C. T., Vuillot, A., Marlin, S., Gerkes, E., Henderson, A., AlKindy, A., Amiel, J. (2013a). Heterogeneity of mutational mechanisms and modes of inheritance in auriculocondylar syndrome. Journal of Medical Genetics, 50(3), Gorlin, R.J.; Cohen, M.M.; Levin, L.S. (1990) Syndromes of the head and neck. Oxford University Press 3rd Ed. Oxford, UK Graham, A., Begbie, J., & McGonnell, I. (2004). Significance of the cranial neural crest. Developmental Dynamics : An Official Publication of the American Association of Anatomists, 229(1), Guion-almeida, M. L., Kokitsu-nakata, N. M., & Zechi-ceide, R. M. (1999). Auriculo-Condylar Syndrome : Further Evidence for a New Disorder, 133(April), Guion-Almeida, M. L., Zechi-Ceide, R. M., Vendramini, S., & Kokitsu-Nakata, N. M. (2002). Auriculo-condylar syndrome: additional patients. American Journal of Medical Genetics, 112(2), Ivey, K., Tyson, B., Ukidwe, P., McFadden, D. G., Levi, G., Olson, E. N., Wilkie, T. M. (2003). Galphaq and Galpha11 proteins mediate endothelin-1 signaling in neural crestderived pharyngeal arch mesenchyme. Developmental Biology, 255(2), Jampol, M., Repetto, G., Keith, D. a, Curtin, H., Remensynder, J., & Holmes, L. B. (1998). New syndrome? Prominent, constricted ears with malformed condyle of the mandible. American Journal of Medical Genetics, 75(5), Jeong, J., Li, X., McEvilly, R. J., Rosenfeld, M. G., Lufkin, T., & Rubenstein, J. L. R. (2008). Dlx genes pattern mammalian jaw primordium by regulating both lower jaw-specific and upper jaw-specific genetic programs. Development (Cambridge, England), 135(17), Johnson, J. M., Moonis, G., Green, G. E., Carmody, R., & Burbank, H. N. (2010). Syndromes of the First and Second Branchial Arches, Part 1: Embryology and Characteristic Defects. American Journal of Neuroradiology, Kido, Y., Gordon, C. T., Sakazume, S., Ben Bdira, E., Dattani, M., Wilson, L. C., Nagai, T. (2013). Further characterization of atypical features in auriculocondylar syndrome caused by recessive PLCB4 mutations. American Journal of Medical Genetics. Part A, 161(9), Knecht, A. K., & Bronner-Fraser, M. (2002). Induction of the neural crest: a multigene process.
26 Nature Reviews. Genetics, 3(6), Kurihara Y., Kurihara H., Suzuki H., Kodama T., Maemura K., Nagai R., Oda H., Kuwaki T., Cao W.-H., Kamada N., Jishage K.,Ouchi Y., Azuma S., Toyoda Y., Ishikawa T., Kumada M., Yazaki Y. (1994). Elevated blood pressure and craniofacial abnormalities in mice deficient in endothelin-1. Nature, 368, Larsen, W.J.. Human embryology. 2nd Edition. Ed. New York: Churchill Livingstone Masotti, C., Oliveira, K. G., Poerner, F., Splendore, A., Souza, J., Freitas, R. D. S., Passos- Bueno, M. R. (2008). Auriculo-condylar syndrome: mapping of a first locus and evidence for genetic heterogeneity. European Journal of Human Genetics : EJHG, 16(2), Miller, C. T., Yelon, D., Stainier, D., & Kimmel, C. B. (2003). Two endothelin 1 effectors, hand2 and bapx1, pattern ventral pharyngeal cartilage and the jaw joint. Development (Cambridge, England), 130(7), Minoux, M., & Rijli, F. M. (2010). Molecular mechanisms of cranial neural crest cell migration and patterning in craniofacial development. Development (Cambridge, England), 137(16), Nakano, M., Fujita, T., Ohtani, J., Kawata, T., Kaku, M., Motokawa, M., Tanne, K. (2009). Effects of mandibular advancement on growth after condylectomy. Journal of Dental Research, 88(3), Ozeki, H., Kurihara, Y., Tonami, K., Watatani, S., & Kurihara, H. (2004). Endothelin-1 regulates the dorsoventral branchial arch patterning in mice. Mechanisms of Development, 121(4), O Rahilly, R., Müller, F. Human embryology and teratology. New York: Wiley-Liss Park, C. (1999). Lower auricular malformations: their representation, correction, and embryologic correlation. Plastic and Reconstructive Surgery, 104(1), Passos-Bueno, M. R., Ornelas, C. C., & Fanganiello, R. D. (2009). Syndromes of the first and second pharyngeal arches: A review. American Journal of Medical Genetics. Part A, 149A(8), Priolo, M., M. Lerone, et al. (2000). Question mark ears, temporomandibular joint malformation and hypotonia: auriculo-condylar syndrome or a distinct entity? Clinical dysmorphology 9(4): Rhee, S. G. (2001). Regulation of Phosphoinositide-specific Phospholipase C. Annual Review of Biochemistry, 70, Rieder, M. J., Green, G. E., Park, S. S., Stamper, B. D., Gordon, C. T., Johnson, J. M., Cunningham, M. L. (2012). A human homeotic transformation resulting from mutations in PLCB4 and GNAI3 causes auriculocondylar syndrome. American Journal of Human Genetics, 90(5), Romanelli Tavares, V.L. Identificação de mutações associadas à Síndrome Aurículo-Condilar. Julho de páginas. Dissertação (Mestrado) Instituto de Biociências da Universidade de São Paulo. Departamento de Genética e Biologia Evolutiva, Universidade de São Paulo, São Paulo Ruest, L. B., Dager, M., Yanagisawa, H., Charité, J., Hammer, R. E., Olson, E. N., Clouthier, D. E. (2003). dhand-cre transgenic mice reveal specific potential functions of dhand during craniofacial development. Developmental Biology, 257(2), Ruest, L.-B., Xiang, X., Lim, K.-C., Levi, G., & Clouthier, D. E. (2004). Endothelin-A receptordependent and -independent signaling pathways in establishing mandibular identity. Development (Cambridge, England), 131(18), Ruffins, S., & Bronner-Fraser, M. (2000). A critical period for conversion of ectodermal cells to
27 a neural crest fate. Developmental Biology, 218(1), Sadler, T.W.. Langman s Medical Embryology. 7th Ed. Williams & Wilkins: Baltmore, Maryland, USA Santagati, F., & Rijli, F. M. (2003). Cranial neural crest and the building of the vertebrate head. Nature Reviews. Neuroscience, 4(10), Serrano, M. J., So, S., Svoboda, K. K. H., & Hinton, R. J. (2011). Cell fate mediators Notch and Twist in mouse mandibular condylar cartilage. Archives of Oral Biology, 56(6), Shkalim, V., Eliaz, N., Linder, N., Merlob, P., & Basel-Vanagaite, L. (2008). Autosomal dominant isolated question mark ear. American Journal of Medical Genetics. Part A, 146A(17), Sprang, S. R. (1997). G protein mechanisms: insights from structural analysis. Annual Review of Biochemistry, 66, Storm, A. L., Johnson, J. M., Lammer, E., Green, G. E., & Cunniff, C. (2005). Auriculocondylar syndrome is associated with highly variable ear and mandibular defects in multiple kindreds. American Journal of Medical Genetics. Part A, 138A(2), Tavares, A. L. P., Garcia, E. L., Kuhn, K., Woods, C. M., Williams, T., & Clouthier, D. E. (2012). Ectodermal-derived Endothelin1 is required for patterning the distal and intermediate domains of the mouse mandibular arch. Developmental Biology, 371(1), Tucker, A. S., Watson, R. P., Lettice, L. a, Yamada, G., & Hill, R. E. (2004). Bapx1 regulates patterning in the middle ear: altered regulatory role in the transition from the proximal jaw during vertebrate evolution. Development (Cambridge, England), 131(6), Uuspaa, V. (1978). Combined bilateral external ear deformity and hypoplastic mandible. Case report. Scandinavian journal of plastic and reconstructive surgery 12(2): Walker, M. B., Miller, C. T., Swartz, M. E., Eberhart, J. K., & Kimmel, C. B. (2007). phospholipase C, beta 3 is required for Endothelin1 regulation of pharyngeal arch patterning in zebrafish. Developmental Biology, 304(1), Wennerberg, K., Rossman, K. L., & Der, C. J. (2005). The Ras superfamily at a glance. Journal of Cell Science, 118(Pt 5), Yanagisawa, H., Yanagisawa, M., Kapur, R. P., Richardson, J. a, Williams, S. C., Clouthier, D. E., Hammer, R. E. (1998). Dual genetic pathways of endothelin-mediated intercellular signaling revealed by targeted disruption of endothelin converting enzyme-1 gene. Development (Cambridge, England), 125(5),
26/06/2013. Sexta passada Aula de HOJE As Estruturas Faciais derivam primariamente dos Arcos Branquiais. Os Arcos Branquiais são separados por Fendas
 Sexta passada Aula de HOJE As Estruturas Faciais derivam primariamente dos Arcos Branquiais 6 Os Arcos Branquiais são separados por Fendas O ESTOMODEU (ou boca primitiva) se forma após o rompimento da
Sexta passada Aula de HOJE As Estruturas Faciais derivam primariamente dos Arcos Branquiais 6 Os Arcos Branquiais são separados por Fendas O ESTOMODEU (ou boca primitiva) se forma após o rompimento da
Embriologia da face e da cavidade oral
 Embriologia da face e da cavidade oral Dia 0 Dia 3 Dia 5 Dia 15 Dia 20 1 0 Mês 14-16 DIAS Gastrulação RELEMBRAR ectoderma epiblasto ectoderma mesoderma mesoderma endoderma endoderma 23 dias Remoção da
Embriologia da face e da cavidade oral Dia 0 Dia 3 Dia 5 Dia 15 Dia 20 1 0 Mês 14-16 DIAS Gastrulação RELEMBRAR ectoderma epiblasto ectoderma mesoderma mesoderma endoderma endoderma 23 dias Remoção da
Sinalização no desenvolvimento de membros. 17/04/2018 Nathalie Cella
 Sinalização no desenvolvimento de membros 17/04/2018 Nathalie Cella ncella@usp.br O que são genes HOX/Homeobox/Homeóticos? 1. São fatores de transcrição com um domínio ligante a DNA (domínio homeobox ou
Sinalização no desenvolvimento de membros 17/04/2018 Nathalie Cella ncella@usp.br O que são genes HOX/Homeobox/Homeóticos? 1. São fatores de transcrição com um domínio ligante a DNA (domínio homeobox ou
COMO É FORMADO O BICO? O embrião visto de frente. Prominência FRONTO- NASAL. Primeiro Arco Branquial
 COMO É FORMADO O BICO? Prominência FRONTO- NASAL Primeiro Arco Branquial Irene Yan Dept. Biologia Celular e do Desenvolvimento -ICB USP Ireneyan@icb.usp.br O embrião visto de frente A Proeminência fronto-nasal
COMO É FORMADO O BICO? Prominência FRONTO- NASAL Primeiro Arco Branquial Irene Yan Dept. Biologia Celular e do Desenvolvimento -ICB USP Ireneyan@icb.usp.br O embrião visto de frente A Proeminência fronto-nasal
O que são genes HOX/Homeobox/Homeóticos? Codificam proteínas que causam HOMEosis HOMEO: similar Sis: transformação
 Mutações homeóticas trocam segmentos corporais O que são genes HOX/Homeobox/Homeóticos? Codificam proteínas que causam HOMEosis HOMEO: similar Sis: transformação Ultrabithorax Antennapedia O que são genes
Mutações homeóticas trocam segmentos corporais O que são genes HOX/Homeobox/Homeóticos? Codificam proteínas que causam HOMEosis HOMEO: similar Sis: transformação Ultrabithorax Antennapedia O que são genes
Identificação de mutações associadas à Síndrome Aurículo-Condilar. Identification of mutated alleles associated with Auriculo-Condylar Syndrome
 Vanessa Luiza Romanelli Tavares Identificação de mutações associadas à Síndrome Aurículo-Condilar Identification of mutated alleles associated with Auriculo-Condylar Syndrome Instituto de Biociências Universidade
Vanessa Luiza Romanelli Tavares Identificação de mutações associadas à Síndrome Aurículo-Condilar Identification of mutated alleles associated with Auriculo-Condylar Syndrome Instituto de Biociências Universidade
Sinalização no desenvolvimento de membros. 25/04/2017 Nathalie Cella
 Sinalização no desenvolvimento de membros 25/04/2017 Nathalie Cella ncella@usp.br Mini-revisão de anatomia braço antebraço mão Hox especifica o mesênquima que se tornará estilopódio, zeugopódio e autopódio
Sinalização no desenvolvimento de membros 25/04/2017 Nathalie Cella ncella@usp.br Mini-revisão de anatomia braço antebraço mão Hox especifica o mesênquima que se tornará estilopódio, zeugopódio e autopódio
Ana Krepischi
 Ana Krepischi ana.krepischi@gmail.com https://youtu.be/wfy_kpfs3la DESENVOLVIMENTO DE DENTES agenesia hipodontia ALTERAÇÕES DENTÁRIAS ESTRUTURAIS amelogênese imperfeita dentinogêse imperfeita SÍNDROMES
Ana Krepischi ana.krepischi@gmail.com https://youtu.be/wfy_kpfs3la DESENVOLVIMENTO DE DENTES agenesia hipodontia ALTERAÇÕES DENTÁRIAS ESTRUTURAIS amelogênese imperfeita dentinogêse imperfeita SÍNDROMES
02/05/2019. CRISTA NEURAL é uma população que migra da região mais dorsal do Tubo Neural. Porque os tentilhões de Darwin tem bicos diferentes?
 Porque os tentilhões de Darwin tem bicos diferentes? As células da crista neural são essenciais para a septação aorticopulmonar. O que surgiu primeiro? O Cérebro ou o Crânio? ( A CRISTA NEURAL é uma população
Porque os tentilhões de Darwin tem bicos diferentes? As células da crista neural são essenciais para a septação aorticopulmonar. O que surgiu primeiro? O Cérebro ou o Crânio? ( A CRISTA NEURAL é uma população
FOLHETOS GERMINATIVOS
 Prof. Adj. Wellerson Rodrigo Scarano Departamento de Morfologia IBB/UNESP FOLHETOS GERMINATIVOS ectoderme mesoderme endoderme 1 ORGANOGÊNESE RUDIMENTAR diferenciação inicial da mesoderme - Paraxial (Somitos)
Prof. Adj. Wellerson Rodrigo Scarano Departamento de Morfologia IBB/UNESP FOLHETOS GERMINATIVOS ectoderme mesoderme endoderme 1 ORGANOGÊNESE RUDIMENTAR diferenciação inicial da mesoderme - Paraxial (Somitos)
Organogênese Rudimentar
 Organogênese Rudimentar Prof. Dr. Wellerson Rodrigo Scarano Prof. Adjunto de Embriologia Departamento de Morfologia Organogênese Rudimentar Processo de formação dos esboços primários dos órgãos a partir
Organogênese Rudimentar Prof. Dr. Wellerson Rodrigo Scarano Prof. Adjunto de Embriologia Departamento de Morfologia Organogênese Rudimentar Processo de formação dos esboços primários dos órgãos a partir
09-May-17. Como será que a crista neural se comporta na cardiogênese de anfíbios?
 As células da crista neural são essenciais para a septação aorticopulmonar. Como será que a crista neural se comporta na cardiogênese de anfíbios? Porque os tentilhões de Darwin tem bicos diferentes? (
As células da crista neural são essenciais para a septação aorticopulmonar. Como será que a crista neural se comporta na cardiogênese de anfíbios? Porque os tentilhões de Darwin tem bicos diferentes? (
Face e cavidade bucal
 Face e cavidade bucal Formação da Face e pescoço Na aula passada: -Aparelho faríngeo Arcos faríngeos Bolsas faríngeas Fendas faríngeas Membranas faríngeas -Tireóide Na aula de hoje - Língua - Face - Cavidades
Face e cavidade bucal Formação da Face e pescoço Na aula passada: -Aparelho faríngeo Arcos faríngeos Bolsas faríngeas Fendas faríngeas Membranas faríngeas -Tireóide Na aula de hoje - Língua - Face - Cavidades
Controle da Expressão Gênica em Eucariotes
 Controle da Expressão Gênica em Eucariotes 1 2 3 Transcrição: Expressão/Ativação do gene Processamento Pós-transcrição: Remoção de introns/poliadenilação, Caping, Transporte Degradação mrna: Estabilidade
Controle da Expressão Gênica em Eucariotes 1 2 3 Transcrição: Expressão/Ativação do gene Processamento Pós-transcrição: Remoção de introns/poliadenilação, Caping, Transporte Degradação mrna: Estabilidade
Organização do Genoma
 Organização do Genoma Bibliografia: The Cell A Molecular Approach (Fourth Edition) Geoffrey M. Cooper & Robert E. Hausman. ASM Press & Sinauer Associates, Inc. 2007. (Disponível para ser requisitado na
Organização do Genoma Bibliografia: The Cell A Molecular Approach (Fourth Edition) Geoffrey M. Cooper & Robert E. Hausman. ASM Press & Sinauer Associates, Inc. 2007. (Disponível para ser requisitado na
Sinalização do desenvolvimento de membros. Nathalie Cella
 Sinalização do desenvolvimento de membros Nathalie Cella ncella@usp.br Mini-revisão de anatomia Eixo dos membros braço coxa antebraço canela mão pé O que determina onde o broto do membro se formará? Genes
Sinalização do desenvolvimento de membros Nathalie Cella ncella@usp.br Mini-revisão de anatomia Eixo dos membros braço coxa antebraço canela mão pé O que determina onde o broto do membro se formará? Genes
Qual das seguintes teorias nos diz que o condocrânio domina o desmocrânio?
 Relativamente aos níveis de controlo do crescimento: a) Centro de crescimento é a zona na qual se produz o crescimento; b) Lugar de crescimento é a zona onde se produz um crescimento independente; c) Todos
Relativamente aos níveis de controlo do crescimento: a) Centro de crescimento é a zona na qual se produz o crescimento; b) Lugar de crescimento é a zona onde se produz um crescimento independente; c) Todos
20/10/2009 DOBRAMENTO DO EMBRIÃO DOBRAMENTO DO EMBRIÃO DOBRAMENTO DO EMBRIÃO. dá FORMA CILÍNDRICA ao embrião
 DOBRAMENTO DO EMBRIÃO 4 sem. PERÍODO EMBRIONÁRIO (Dobramento do Embrião) dá FORMA CILÍNDRICA ao embrião acontece nos planos mediano: ÂNTERO POSTERIOR e horizontal: LÁTERO-LATERALLATERAL decorre do rápido
DOBRAMENTO DO EMBRIÃO 4 sem. PERÍODO EMBRIONÁRIO (Dobramento do Embrião) dá FORMA CILÍNDRICA ao embrião acontece nos planos mediano: ÂNTERO POSTERIOR e horizontal: LÁTERO-LATERALLATERAL decorre do rápido
Embriologia. Prof. Dr. Tharsus Dias Takeuti. Guarantã do Norte MT 2018
 Embriologia Prof. Dr. Tharsus Dias Takeuti Guarantã do Norte MT 2018 Terceira semana Disco embrionário ganha mais uma camada Aparecimento da linha primitiva Desenvolvimento da notocorda Diferenciação das
Embriologia Prof. Dr. Tharsus Dias Takeuti Guarantã do Norte MT 2018 Terceira semana Disco embrionário ganha mais uma camada Aparecimento da linha primitiva Desenvolvimento da notocorda Diferenciação das
UNIVERSIDADE FEDERAL DO PARANÁ Setor de Ciências Biológicas Departamento de Genética BG403 - GENÉTICA ANIMAL. Lista de Exercícios
 UNIVERSIDADE FEDERAL DO PARANÁ Setor de Ciências Biológicas Departamento de Genética Profa Angelica Boldt BG403 - GENÉTICA ANIMAL Lista de Exercícios T7 GENÉTICA DE POPULAÇÕES 1) As propriedades genéticas
UNIVERSIDADE FEDERAL DO PARANÁ Setor de Ciências Biológicas Departamento de Genética Profa Angelica Boldt BG403 - GENÉTICA ANIMAL Lista de Exercícios T7 GENÉTICA DE POPULAÇÕES 1) As propriedades genéticas
2. O desenvolvimento embrionário dos vertebrados é dividido nas seguintes etapas: segmentação, gastrulação e organogênese.
 1. O estudo da embriologia fornece subsídios para a compreensão dos processos biológicos envolvidos na formação e no desenvolvimento embrionário e fetal humano. Sobre esse assunto, é CORRETO afirmar: a)
1. O estudo da embriologia fornece subsídios para a compreensão dos processos biológicos envolvidos na formação e no desenvolvimento embrionário e fetal humano. Sobre esse assunto, é CORRETO afirmar: a)
CONCURSO PÚBLICO ESPECIALISTA DE LABORATÓRIO EDITAL IB ATAD
 CONCURSO PÚBLICO ESPECIALISTA DE LABORATÓRIO EDITAL IB ATAD 24-2012 1ª Prova: Múltipla Escolha Data: 05-09-2012 INSTRUÇÕES PARA FAZER A PROVA: 1) COLOCAR NOME EM TODAS AS PÁGINAS 2) ESCREVER DE FORMA LEGÍVEL
CONCURSO PÚBLICO ESPECIALISTA DE LABORATÓRIO EDITAL IB ATAD 24-2012 1ª Prova: Múltipla Escolha Data: 05-09-2012 INSTRUÇÕES PARA FAZER A PROVA: 1) COLOCAR NOME EM TODAS AS PÁGINAS 2) ESCREVER DE FORMA LEGÍVEL
01/06/2014. Deve ser: - Escrita a mão. - Incluir bibliografia (preferencialmente LIVRO).
 Trabalho a ser entregue no dia da prova (escrita a mão): Este trabalho terá valor de 3,0 na prova prática. Deve ser: - Escrita a mão. - Incluir bibliografia (preferencialmente LIVRO). Escolha uma malformação
Trabalho a ser entregue no dia da prova (escrita a mão): Este trabalho terá valor de 3,0 na prova prática. Deve ser: - Escrita a mão. - Incluir bibliografia (preferencialmente LIVRO). Escolha uma malformação
Derivados da Crista Neural Neurulação
 Derivados da Crista Neural Neurulação GASTRULAÇÃO NEURULAÇÃO Crista Neural DOBRAMENTO DO CORPO FECHAMENTO DO TUBO ENDODÉRMICO EXPANSÃO DO ÂMNION Fim da Gastrulação Início da Neurulação Langman-Embriologia
Derivados da Crista Neural Neurulação GASTRULAÇÃO NEURULAÇÃO Crista Neural DOBRAMENTO DO CORPO FECHAMENTO DO TUBO ENDODÉRMICO EXPANSÃO DO ÂMNION Fim da Gastrulação Início da Neurulação Langman-Embriologia
Conceito: qualquer modificação súbita e hereditária no conjunto gênico de um organismo, que não é explicada pela recombinação da variabilidade
 MUTAÇÃO Conceito: qualquer modificação súbita e hereditária no conjunto gênico de um organismo, que não é explicada pela recombinação da variabilidade genética pré-existente. Organismo mutante: é aquele
MUTAÇÃO Conceito: qualquer modificação súbita e hereditária no conjunto gênico de um organismo, que não é explicada pela recombinação da variabilidade genética pré-existente. Organismo mutante: é aquele
Neurulação. Neurulação? 28/04/2016. Sistema nervoso dos echinoderma. Características Evolutivas. Principais eventos em Biologia do Desenvolvimento
 Principais eventos em Biologia do Desenvolvimento Neurulação Gametogênese e Fertilização Clivagem Gastrulação Neurulação Organogênese MSc. Carolina Purcell Laboratório de Embriologia Molecular de Vertebrados
Principais eventos em Biologia do Desenvolvimento Neurulação Gametogênese e Fertilização Clivagem Gastrulação Neurulação Organogênese MSc. Carolina Purcell Laboratório de Embriologia Molecular de Vertebrados
NOME: DATA: / / 2010
 D E P A R T A M E N T O D E G E N É T I C A E B I O L O G I A E V O L U T I V A C O N C U R S O P Ú B L I C O - E D I T A L I B - A T A D - 2 9-2 0 1 0 M É D I C O 1 NOME: DATA: / / 2010 1. Assinale a(s)
D E P A R T A M E N T O D E G E N É T I C A E B I O L O G I A E V O L U T I V A C O N C U R S O P Ú B L I C O - E D I T A L I B - A T A D - 2 9-2 0 1 0 M É D I C O 1 NOME: DATA: / / 2010 1. Assinale a(s)
DESENVOLVIMENTO DO SISTEMA RESPIRATÓRIO. Profª Me. Tatiane da Silva Poló
 DESENVOLVIMENTO DO SISTEMA RESPIRATÓRIO Profª Me. Tatiane da Silva Poló INÍCIO DO DESENVOLVIMENTO 4ª semana Local: assoalho da extremidade caudal da faringe primitiva (originada do intestino anterior)
DESENVOLVIMENTO DO SISTEMA RESPIRATÓRIO Profª Me. Tatiane da Silva Poló INÍCIO DO DESENVOLVIMENTO 4ª semana Local: assoalho da extremidade caudal da faringe primitiva (originada do intestino anterior)
De onde as células vêm? PARA ONDE vão? 2. O que estas células PODEM ser? 3. QUANDO elas decidem o que vão ser?
 LABORATÓRIO DE EMBRIOLOGIA MOLECULAR DE VERTEBRADOS Departamento de Biologia Celular e do Desenvolvimento ICB-USP Vias de sinalização em desenvolvimento Vias de sinalização em desenvolvimento Magritte,
LABORATÓRIO DE EMBRIOLOGIA MOLECULAR DE VERTEBRADOS Departamento de Biologia Celular e do Desenvolvimento ICB-USP Vias de sinalização em desenvolvimento Vias de sinalização em desenvolvimento Magritte,
Crescimento da Mandíbula. Cartilagem de Meckel e Mandíbula Óssea
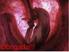 Cartilagem de Meckel e Mandíbula Óssea O primeiro par de arcos branquiais é o precursor da maxila e da mandíbula Porém, a maxila é derivada de uma pequena proeminência deste arco branquial, muito menor
Cartilagem de Meckel e Mandíbula Óssea O primeiro par de arcos branquiais é o precursor da maxila e da mandíbula Porém, a maxila é derivada de uma pequena proeminência deste arco branquial, muito menor
EXERCÍCIOS GENÉTICA MENDELIANA
 Lista de exercícios GENÉTICA MENDELIANA 1) "Cada caráter é condicionado por um par de fatores que se separam na formação dos gametas". Mendel ao enunciar essa lei já admitia, embora sem conhecer, a existência
Lista de exercícios GENÉTICA MENDELIANA 1) "Cada caráter é condicionado por um par de fatores que se separam na formação dos gametas". Mendel ao enunciar essa lei já admitia, embora sem conhecer, a existência
1. Na família abaixo há três indivíduos afetados por uma doença neurológica muito rara.
 1. Na família abaixo há três indivíduos afetados por uma doença neurológica muito rara. I Dê as razões para que essa doença tenha ou não tenha herança: a ligada ao X dominante. Não é esse o padrão de herança,
1. Na família abaixo há três indivíduos afetados por uma doença neurológica muito rara. I Dê as razões para que essa doença tenha ou não tenha herança: a ligada ao X dominante. Não é esse o padrão de herança,
Intervenção Multidisciplinar: evidências sobre Sequência de Pierre Robin, Síndrome de Crouzon e Velocardiofacial
 Intervenção Multidisciplinar: evidências sobre Sequência de Pierre Robin, Síndrome de Crouzon e Velocardiofacial Apresentadores: Caroline Pascon (graduanda em fonoaudiologia) Michele Haduo (graduanda em
Intervenção Multidisciplinar: evidências sobre Sequência de Pierre Robin, Síndrome de Crouzon e Velocardiofacial Apresentadores: Caroline Pascon (graduanda em fonoaudiologia) Michele Haduo (graduanda em
Biologia e Ciências Naturais. Prof. Paulo Henrique Mueller.
 Prof. Paulo Henrique Mueller GENÉTICA É a ciência que estuda o material hereditário e os mecanismos de transmissão ao longo das gerações. É o processo pelo qual as características são passadas dos genitores
Prof. Paulo Henrique Mueller GENÉTICA É a ciência que estuda o material hereditário e os mecanismos de transmissão ao longo das gerações. É o processo pelo qual as características são passadas dos genitores
Embriologia 05/09/2018. Embriologia e desenvolvimento da face. Estímulos Genéticos
 UNIVERSIDADE VEIGA DE ALMEIDA GRADUAÇÃO EM FONOAUDIOLOGIA Embriologia e desenvolvimento da face Prof Christiane Albuquerque e Prof Viviane Marques Embriologia CRESCIMENTO E DESENVOLVIMENTO CRANIO-FACIAL
UNIVERSIDADE VEIGA DE ALMEIDA GRADUAÇÃO EM FONOAUDIOLOGIA Embriologia e desenvolvimento da face Prof Christiane Albuquerque e Prof Viviane Marques Embriologia CRESCIMENTO E DESENVOLVIMENTO CRANIO-FACIAL
Pergunta 1: Como é determinado o n. de somitos?
 Pergunta 1: Como é determinado o n. de somitos? corn snake (Pantherophis Guttatus) : 315 somitos House snake (Lamprophis Fuliginosus): 300 somitos Whiptail Lizare (Aspidoscelis uniparens): 90 somitos zebra-fish
Pergunta 1: Como é determinado o n. de somitos? corn snake (Pantherophis Guttatus) : 315 somitos House snake (Lamprophis Fuliginosus): 300 somitos Whiptail Lizare (Aspidoscelis uniparens): 90 somitos zebra-fish
Herança não Mendeliana. Determinação da Cor dos Olhos
 Herança não Mendeliana Determinação da Cor dos Olhos Herança não Mendeliana -Fenótipos sem padrão de segregação mendeliano -Poligênica interações alélicas e -Oligogênica gênicas -Fatores ambientais -Modificações
Herança não Mendeliana Determinação da Cor dos Olhos Herança não Mendeliana -Fenótipos sem padrão de segregação mendeliano -Poligênica interações alélicas e -Oligogênica gênicas -Fatores ambientais -Modificações
Ontogênese de linfócitos T
 Ontogênese de linfócitos T Linfócitos T Linfócitos T Os linfócitos T formados durante o desenvolvimento intratímico são: Linfócitos T (TCR γδ) Linfócitos T (TCR αβ) CD4+ CD8+ T reguladores Linfócitos NKT
Ontogênese de linfócitos T Linfócitos T Linfócitos T Os linfócitos T formados durante o desenvolvimento intratímico são: Linfócitos T (TCR γδ) Linfócitos T (TCR αβ) CD4+ CD8+ T reguladores Linfócitos NKT
Gene tica. O que é genética? É o estudo dos genes e de sua transmissão para as futuras gerações. Genética Clássica -> Mendel(1856)
 Gene tica Conceitos básicos Na semente estão contidas todas as partes do corpo do homem que serão formadas. A criança que se desenvolve no útero da mãe tem as raízes da barba e do cabelo que nascerão um
Gene tica Conceitos básicos Na semente estão contidas todas as partes do corpo do homem que serão formadas. A criança que se desenvolve no útero da mãe tem as raízes da barba e do cabelo que nascerão um
Macroevolução molecular
 Evo-Devo Macroevolução molecular Evolução e Desenvolvimento (Evo-Devo) A árvore temporal da vida Professor Fabrício R Santos fsantos@icb.ufmg.br Departamento de Biologia Geral, UFMG 2012 Biologia evolutiva
Evo-Devo Macroevolução molecular Evolução e Desenvolvimento (Evo-Devo) A árvore temporal da vida Professor Fabrício R Santos fsantos@icb.ufmg.br Departamento de Biologia Geral, UFMG 2012 Biologia evolutiva
BIOLOGIA LISTA 02 2ª SÉRIE 18 / 03 / Professor(a): Olívia. d)
 BIOLOGIA LISTA 02 Professor(a): Olívia 2ª SÉRIE 18 / 03 / 2019 1. A doença renal policística autossômica recessiva, conhecida em inglês pela sigla ARPKD, é uma rara enfermidade hereditária. Para desenvolver
BIOLOGIA LISTA 02 Professor(a): Olívia 2ª SÉRIE 18 / 03 / 2019 1. A doença renal policística autossômica recessiva, conhecida em inglês pela sigla ARPKD, é uma rara enfermidade hereditária. Para desenvolver
APÊNDICE I - Versão original das tabelas 4, 5 e 6 e a lista com os conteúdos mantidos e eliminados nas tabelas finais apresentadas no corpo da tese
 APÊNDICE I - Versão original das tabelas 4, 5 e 6 e a lista com os conteúdos mantidos e eliminados nas tabelas finais apresentadas no corpo da tese Tabela 4 - Conteúdos mencionados como básicos pelos professores/docentes
APÊNDICE I - Versão original das tabelas 4, 5 e 6 e a lista com os conteúdos mantidos e eliminados nas tabelas finais apresentadas no corpo da tese Tabela 4 - Conteúdos mencionados como básicos pelos professores/docentes
LISTA REC 1º BIM BIOLOGIA
 LISTA REC 1º BIM Professora: JANDER SÉRIE: 3º ANO DATA: / / BIOLOGIA Genética: - Segunda Lei de Mendel - Análise de heredogramas - Interações Gênicas Roteiro de Recuperação Terceiro Ano Pagina 1 de 5 Lista
LISTA REC 1º BIM Professora: JANDER SÉRIE: 3º ANO DATA: / / BIOLOGIA Genética: - Segunda Lei de Mendel - Análise de heredogramas - Interações Gênicas Roteiro de Recuperação Terceiro Ano Pagina 1 de 5 Lista
BIOLOGIA. Hereditariedade e diversidade da vida. 1ª e 2ª leis de Mendel Parte 3. Professor: Alex Santos
 BIOLOGIA Hereditariedade e diversidade da vida Parte 3 Professor: Alex Santos Tópicos em abordagem: Parte 3 Extensões as Leis de Mendel: Visão geral I Ausência de dominância II Codominância III Genes letais
BIOLOGIA Hereditariedade e diversidade da vida Parte 3 Professor: Alex Santos Tópicos em abordagem: Parte 3 Extensões as Leis de Mendel: Visão geral I Ausência de dominância II Codominância III Genes letais
INTERAÇÃO GÊNICA II PARTE 2
 INTERAÇÃO GÊNICA II PARTE 2 CONCEITOS ASSOCIADOS COM INTERAÇÃO GÊNICA (3) Interação Gênica Epistasia Doenças complexas DEFINIÇÕES q Região de DNA que codifica RNAm, que por sua vez codifica uma sequência
INTERAÇÃO GÊNICA II PARTE 2 CONCEITOS ASSOCIADOS COM INTERAÇÃO GÊNICA (3) Interação Gênica Epistasia Doenças complexas DEFINIÇÕES q Região de DNA que codifica RNAm, que por sua vez codifica uma sequência
Morfogênese da região bucofaríngea
 Universidade de Brasília (UnB) Universidade Aberta do Brasil (UAB) Aula 13: Morfogênese da região bucofaríngea Síntese: Diferenciação dos tecidos básicos na formação da mandíbula, maxilar lábios, ossículos
Universidade de Brasília (UnB) Universidade Aberta do Brasil (UAB) Aula 13: Morfogênese da região bucofaríngea Síntese: Diferenciação dos tecidos básicos na formação da mandíbula, maxilar lábios, ossículos
Profa. Dra. Iêda Guedes Depto Histologia e Embriologia - CCB Universidade Federal do Pará
 Módulo: Morfológicas I Disciplina: Histologia Curso: Odontologia Profa. Dra. Iêda Guedes Depto Histologia e Embriologia - CCB Universidade Federal do Pará Vista de embrião com 22 dias Primeiro Arco
Módulo: Morfológicas I Disciplina: Histologia Curso: Odontologia Profa. Dra. Iêda Guedes Depto Histologia e Embriologia - CCB Universidade Federal do Pará Vista de embrião com 22 dias Primeiro Arco
SOMITOGÊNESE 14/05/2013. Pergunta 2: Como é determinado onde serão formados os membros? Pergunta 1: Como é determinado o n. de somitos?
 O padrão embrionário é gradualmente refinado http://www.youtube.com/watch?v=uaedzlrnbgy 1) O corpo do artrópodo é segmentado primeiro molecularmente (PARASEGMENTO), depois anatomicamente (SEGMENTO) 2)
O padrão embrionário é gradualmente refinado http://www.youtube.com/watch?v=uaedzlrnbgy 1) O corpo do artrópodo é segmentado primeiro molecularmente (PARASEGMENTO), depois anatomicamente (SEGMENTO) 2)
Controle genético do desenvolvimento animal. John Wiley & Sons, Inc.
 Controle genético do desenvolvimento animal Drosophila foi um dos primeiros organismos-modelo para análise genética do desenvolvimento. Genética e Desenvolvimento O desenvolvimento de um animal multicelular
Controle genético do desenvolvimento animal Drosophila foi um dos primeiros organismos-modelo para análise genética do desenvolvimento. Genética e Desenvolvimento O desenvolvimento de um animal multicelular
LISTA DE EXERCÍCIOS 3º ANO
 Alelos: a (chifres) e A (sem chifres) macho sem chifres: Aa cabra 1 com chifres: aa cabra 2 com chifres: aa cabra 3 sem chifres: Aa Cruzamento-teste: a fêmea com pelagem preta foi cruzada com indivíduo
Alelos: a (chifres) e A (sem chifres) macho sem chifres: Aa cabra 1 com chifres: aa cabra 2 com chifres: aa cabra 3 sem chifres: Aa Cruzamento-teste: a fêmea com pelagem preta foi cruzada com indivíduo
Terceira e quarta semana: gastrulação e neurulação. Professor: Arturo Arnáez Vaella
 Terceira e quarta semana: gastrulação e neurulação Professor: Arturo Arnáez Vaella Introdução Gastrulação: - Surgimento da linha primitiva - Formação da notocorda - Formação do disco embrionário trilaminar
Terceira e quarta semana: gastrulação e neurulação Professor: Arturo Arnáez Vaella Introdução Gastrulação: - Surgimento da linha primitiva - Formação da notocorda - Formação do disco embrionário trilaminar
Resumo de Face e Arcos Faríngeos
 Resumo de Face e Arcos Faríngeos Professor: Brito. FACE A face humana é formada entre a 4 e a 10 semana pela fusão de cinco proeminências faciais: a proeminência frontonasal, um par de proeminências maxilares
Resumo de Face e Arcos Faríngeos Professor: Brito. FACE A face humana é formada entre a 4 e a 10 semana pela fusão de cinco proeminências faciais: a proeminência frontonasal, um par de proeminências maxilares
PADRÃO DE HERANÇA LIGADA AO CROMOSSOMO X
 PADRÃO DE HERANÇA LIGADA AO CROMOSSOMO X HOMENS: apresenta um X e um Y XY sexo heterogamético o seus gametas serão metade com cromossomo X e metade com cromossomo Y MULHER: apresenta dois X XX sexo homogamético
PADRÃO DE HERANÇA LIGADA AO CROMOSSOMO X HOMENS: apresenta um X e um Y XY sexo heterogamético o seus gametas serão metade com cromossomo X e metade com cromossomo Y MULHER: apresenta dois X XX sexo homogamético
Aula 4: Genética da Transmissão III
 LGN215 - Genética Geral Aula 4: Genética da Transmissão III Prof. Dr. Antonio Augusto Franco Garcia Monitora: Maria Marta Pastina Experimentos de Mendel Inicialmente, Mendel estudou cruzamentos considerando
LGN215 - Genética Geral Aula 4: Genética da Transmissão III Prof. Dr. Antonio Augusto Franco Garcia Monitora: Maria Marta Pastina Experimentos de Mendel Inicialmente, Mendel estudou cruzamentos considerando
3ª semana do desenvolvimento 1ª parte. Prof a. Marta G. Amaral, Dra. Embriologia molecular
 3ª semana do desenvolvimento 1ª parte Prof a. Marta G. Amaral, Dra. Embriologia molecular O que é gastrulação? Gastrulação é um conjunto de movimentos celulares que levarão a formação das camadas germinativas:
3ª semana do desenvolvimento 1ª parte Prof a. Marta G. Amaral, Dra. Embriologia molecular O que é gastrulação? Gastrulação é um conjunto de movimentos celulares que levarão a formação das camadas germinativas:
é um tipo de gráfico que representa a herança genética de determinada característica dos indivíduos representados...
 é um tipo de gráfico que representa a herança genética de determinada característica dos indivíduos representados... EXEMPLO DE UM HEREDOGRAMA Herança Autossômica Dominante Critérios da Herança Autossômica
é um tipo de gráfico que representa a herança genética de determinada característica dos indivíduos representados... EXEMPLO DE UM HEREDOGRAMA Herança Autossômica Dominante Critérios da Herança Autossômica
LISTA DE EXERCÍCIOS 2º ANO
 A bainha de mielina constitui de lipídios, sendo um isolante elétrico, o impulso passa de maneira saltatória pelo axônio, sendo mais rápido do que um neurônio não mielinizado. Ao entrar em contato com
A bainha de mielina constitui de lipídios, sendo um isolante elétrico, o impulso passa de maneira saltatória pelo axônio, sendo mais rápido do que um neurônio não mielinizado. Ao entrar em contato com
Conceitos Básicos de Genética. Relação Fenótipo-Genótipo
 Conceitos Básicos de Genética Relação Fenótipo-Genótipo Genética É a disciplina dentro da Biologia que estuda os mecanismos da hereditariedade. O que é genética? É o estudo dos genes e de sua transmissão
Conceitos Básicos de Genética Relação Fenótipo-Genótipo Genética É a disciplina dentro da Biologia que estuda os mecanismos da hereditariedade. O que é genética? É o estudo dos genes e de sua transmissão
Número de genes versus número de proteínas em eucariotos
 Número de genes versus número de proteínas em eucariotos Bioquímica II SQM0416 Júlia Assirati Tomie Kuriyama Victória Montenegro de Campos Resumo Introdução Características do genoma humano Como foram
Número de genes versus número de proteínas em eucariotos Bioquímica II SQM0416 Júlia Assirati Tomie Kuriyama Victória Montenegro de Campos Resumo Introdução Características do genoma humano Como foram
Nome: Exercícios de Genética (Conceitos e 1a. Lei de Mendel) Atividade Avaliativa 0 a 2,5
 Nome: Exercícios de Genética (Conceitos e 1a. Lei de Mendel) Atividade Avaliativa 0 a 2,5 Turma 3o. Ano A/B disciplina Biologia Professora Carina Justino 1. Um casal buscou um serviço de aconselhamento
Nome: Exercícios de Genética (Conceitos e 1a. Lei de Mendel) Atividade Avaliativa 0 a 2,5 Turma 3o. Ano A/B disciplina Biologia Professora Carina Justino 1. Um casal buscou um serviço de aconselhamento
Fundamentos da Genética. Professor: Anderson Marques de Souza 2016
 Fundamentos da Genética Professor: Anderson Marques de Souza 2016 Genética: Conceitos Básicos 1º estuda a transmissão de características da célula-mãe para a célula-filha; 2º estuda as características
Fundamentos da Genética Professor: Anderson Marques de Souza 2016 Genética: Conceitos Básicos 1º estuda a transmissão de características da célula-mãe para a célula-filha; 2º estuda as características
ARTICULAÇÃO TÊMPORO- MANDIBULAR
 http://www.icb.usp.br/~ireneyan/embriologiamolecular_arquivos/aulas/odontousp ireneyan@usp.br Mandíbula: Anatomia super super básica ARTICULAÇÃO TÊMPORO- MANDIBULAR Mandíbula: Anatomia super super básica
http://www.icb.usp.br/~ireneyan/embriologiamolecular_arquivos/aulas/odontousp ireneyan@usp.br Mandíbula: Anatomia super super básica ARTICULAÇÃO TÊMPORO- MANDIBULAR Mandíbula: Anatomia super super básica
Mecanismos de comunicação celular 26/05/2015
 Mecanismos de comunicação celular 26/05/2015 Alvos terapêuticos Hopkins & Groom (2002) Nature Reviews Drug Discovery 1:727 Elementos da comunicação celular LIGANTE RECEPTOR Há dois tipos de receptores
Mecanismos de comunicação celular 26/05/2015 Alvos terapêuticos Hopkins & Groom (2002) Nature Reviews Drug Discovery 1:727 Elementos da comunicação celular LIGANTE RECEPTOR Há dois tipos de receptores
. a d iza r to u a ia p ó C II
 II Sugestões de avaliação Ciências 8 o ano Unidade 3 5 Unidade 3 Nome: Data: 1. As bactérias não têm núcleo nem DNA. Você concorda com essa afirmação? Justifique. 2. Uma mulher de 40 anos de idade está
II Sugestões de avaliação Ciências 8 o ano Unidade 3 5 Unidade 3 Nome: Data: 1. As bactérias não têm núcleo nem DNA. Você concorda com essa afirmação? Justifique. 2. Uma mulher de 40 anos de idade está
Influência das Variantes Genéticas Funcionais do Sistema Renina-Angiotensina na Doença Arterial Coronária.
 José Ramón Lanz Luces Influência das Variantes Genéticas Funcionais do Sistema Renina-Angiotensina na Doença Arterial Coronária. Tese apresentada à Faculdade de Medicina da Universidade de São Paulo para
José Ramón Lanz Luces Influência das Variantes Genéticas Funcionais do Sistema Renina-Angiotensina na Doença Arterial Coronária. Tese apresentada à Faculdade de Medicina da Universidade de São Paulo para
Leia estas instruções:
 Leia estas instruções: 1 2 Confira se os dados contidos na parte inferior desta capa estão corretos e, em seguida, assine no espaço reservado para isso. Caso se identifique em qualquer outro local deste
Leia estas instruções: 1 2 Confira se os dados contidos na parte inferior desta capa estão corretos e, em seguida, assine no espaço reservado para isso. Caso se identifique em qualquer outro local deste
Genética. Resolução de exercícios! Vai filhããão! Prof. Rafael Rosolen T Zafred
 Genética Resolução de exercícios! 1...2...3... Vai filhããão! Prof. Rafael Rosolen T Zafred Revisão Dominante x Recessivo Heterozigoto x Homozigoto Domina o outro gene; UM gene manifesta o fenótipo; DOIS
Genética Resolução de exercícios! 1...2...3... Vai filhããão! Prof. Rafael Rosolen T Zafred Revisão Dominante x Recessivo Heterozigoto x Homozigoto Domina o outro gene; UM gene manifesta o fenótipo; DOIS
QUARTA A OITAVA SEMANA DO DESENVOLVIMENTO EMBRIONÁRIO
 QUARTA A OITAVA SEMANA DO DESENVOLVIMENTO EMBRIONÁRIO ASPECTOS INTERNOS E EXTERNOS DO EMBRIÃO 1 O PERÍODO DE ORGANOGÊNESE OCORRE DA QUARTA À OITAVA SEMANA DO DESENVOLVIMENTO EMBRIONÁRIO. AO FINAL DA OITAVA
QUARTA A OITAVA SEMANA DO DESENVOLVIMENTO EMBRIONÁRIO ASPECTOS INTERNOS E EXTERNOS DO EMBRIÃO 1 O PERÍODO DE ORGANOGÊNESE OCORRE DA QUARTA À OITAVA SEMANA DO DESENVOLVIMENTO EMBRIONÁRIO. AO FINAL DA OITAVA
Fertilização. Professor: Arturo Arnáez Vaella
 Fertilização Professor: Arturo Arnáez Vaella Introdução Fonte: http://biologia-no-vestibular.blogspot.com.br/2012/06/ufpb-reproducao-humana.html Introdução Para poder fertilizar o ovócito o espermatozoide
Fertilização Professor: Arturo Arnáez Vaella Introdução Fonte: http://biologia-no-vestibular.blogspot.com.br/2012/06/ufpb-reproducao-humana.html Introdução Para poder fertilizar o ovócito o espermatozoide
disciplina Genética Humana (e Evolução)
 disciplina Genética Humana (e Evolução) INSTITUTO DE BIOCIÊNCIAS Departamento de Genética e Biologia Evolutiva UNIVERSIDADE DE SÃO PAULO 2017 Professoras responsáveis: Carla Rosenberg (carlarosenberg@ib.usp.br)
disciplina Genética Humana (e Evolução) INSTITUTO DE BIOCIÊNCIAS Departamento de Genética e Biologia Evolutiva UNIVERSIDADE DE SÃO PAULO 2017 Professoras responsáveis: Carla Rosenberg (carlarosenberg@ib.usp.br)
DO CROMOSSOMO AOS GENES
 DO CROMOSSOMO AOS GENES Prof. Paulo Cesar Naoum Academia de Ciência e Tecnologia Não é raro as pessoas perguntarem a respeito de como se descobriram as localizações dos genes nos cromossomos. Da forma
DO CROMOSSOMO AOS GENES Prof. Paulo Cesar Naoum Academia de Ciência e Tecnologia Não é raro as pessoas perguntarem a respeito de como se descobriram as localizações dos genes nos cromossomos. Da forma
GENE: ESTRUTURA E FUNÇÃO. Aparecida Maria Fontes Ribeirão Preto Julho/ 2019
 GENE: ESTRUTURA E FUNÇÃO Aparecida Maria Fontes Ribeirão Preto Julho/ 2019 Por que estudar gene: estrutura e função na medicina? Como o nosso conhecimento e nossa prática atuais da medicina dependem de
GENE: ESTRUTURA E FUNÇÃO Aparecida Maria Fontes Ribeirão Preto Julho/ 2019 Por que estudar gene: estrutura e função na medicina? Como o nosso conhecimento e nossa prática atuais da medicina dependem de
Escola Prof. Reynaldo dos Santos Vila Franca de Xira Biologia - 12º ano - Teste de Avaliação Fevereiro 2019 Unidade 2: Hereditariedade
 Escola Prof. Reynaldo dos Santos Vila Franca de Xira Biologia - 12º ano - Teste de Avaliação Fevereiro 2019 Unidade 2: Hereditariedade Leia atentamente o texto e as questões que se seguem e indique a resposta
Escola Prof. Reynaldo dos Santos Vila Franca de Xira Biologia - 12º ano - Teste de Avaliação Fevereiro 2019 Unidade 2: Hereditariedade Leia atentamente o texto e as questões que se seguem e indique a resposta
disciplina Genética Humana
 disciplina Genética Humana INSTITUTO DE BIOCIÊNCIAS Departamento de Genética e Biologia Evolutiva UNIVERSIDADE DE SÃO PAULO 2017 Professoras responsáveis: Carla Rosenberg (carlarosenberg@ib.usp.br) Ana
disciplina Genética Humana INSTITUTO DE BIOCIÊNCIAS Departamento de Genética e Biologia Evolutiva UNIVERSIDADE DE SÃO PAULO 2017 Professoras responsáveis: Carla Rosenberg (carlarosenberg@ib.usp.br) Ana
BIOLOGIA - 2 o ANO MÓDULO a LEI DE MENDEL
 BIOLOGIA - 2 o ANO MÓDULO 42 2 a LEI DE MENDEL V V R R P Amarelas lisas x v v r r Verdes rugosas F1 100% de amarelas lisas = Vv Rr P Amarelas lisas x Amarelas lisas F2 Amarelas lisas (56,25%) Amarelas
BIOLOGIA - 2 o ANO MÓDULO 42 2 a LEI DE MENDEL V V R R P Amarelas lisas x v v r r Verdes rugosas F1 100% de amarelas lisas = Vv Rr P Amarelas lisas x Amarelas lisas F2 Amarelas lisas (56,25%) Amarelas
Módulo de Embriologia Geral
 Faculdade de Medicina de Ribeirão Preto - USP Módulo de Embriologia Geral Responsável: Prof. Ricardo G. P. Ramos Diferenciação Celular 1) Gametogênese e Fertilização Embriologia Geral Humana 2) As Duas
Faculdade de Medicina de Ribeirão Preto - USP Módulo de Embriologia Geral Responsável: Prof. Ricardo G. P. Ramos Diferenciação Celular 1) Gametogênese e Fertilização Embriologia Geral Humana 2) As Duas
ORGANOGÊNESE FASE EMBRIONÁRIA
 ORGANOGÊNESE FASE EMBRIONÁRIA ORGANOGÊNESE (organo: organismo e gênese: origem) Importância: embrião. A maior parte do desenvolvimento dos órgãos: (varia com a espécie) Ao final deste período: Principais
ORGANOGÊNESE FASE EMBRIONÁRIA ORGANOGÊNESE (organo: organismo e gênese: origem) Importância: embrião. A maior parte do desenvolvimento dos órgãos: (varia com a espécie) Ao final deste período: Principais
Radiologia médica - Anatomia I. Total de 7 páginas 1
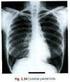 OSSOS DA FACE Ossos da face crescem até aos 16 anos; Com amadurecimento: os ossos do crânio se expandem, dentes se formam e emergem, seios paranasais aumentam. Ossos Nasais Ossos da face (14): 2 ossos
OSSOS DA FACE Ossos da face crescem até aos 16 anos; Com amadurecimento: os ossos do crânio se expandem, dentes se formam e emergem, seios paranasais aumentam. Ossos Nasais Ossos da face (14): 2 ossos
03/10/2012 NEURULAÇÃO. Estabelecimento das células neurais
 NEURULAÇÃO - Neurula Aparência colunar Placa neural NEURULAÇÃO 1 2 NEURULAÇÃO Região anterior Região posterior 3 4 Estabelecimento das células neurais Especificação Células recebem sinais para se tornarem
NEURULAÇÃO - Neurula Aparência colunar Placa neural NEURULAÇÃO 1 2 NEURULAÇÃO Região anterior Região posterior 3 4 Estabelecimento das células neurais Especificação Células recebem sinais para se tornarem
Visualização de Hélices
 Grupo: Curso: Turma: Data: Visualização de Hélices Objetivos Visualizar a estrutura tridimensional de hélices presentes na estrutura de proteínas e peptídeos, usandose recursos computacionais. Analisar
Grupo: Curso: Turma: Data: Visualização de Hélices Objetivos Visualizar a estrutura tridimensional de hélices presentes na estrutura de proteínas e peptídeos, usandose recursos computacionais. Analisar
CAPÍTULO 13. BIOLOGIA MOLECULAR DA Hb S
 CAPÍTULO 13 348 BIOLOGIA MOLECULAR DA Hb S INTRODUÇÃO A heterogeneidade das manifestações clínicas entre doentes com o genótipo SS da anemia falciforme sempre foi um enigma para os clínicos. Com o progresso
CAPÍTULO 13 348 BIOLOGIA MOLECULAR DA Hb S INTRODUÇÃO A heterogeneidade das manifestações clínicas entre doentes com o genótipo SS da anemia falciforme sempre foi um enigma para os clínicos. Com o progresso
VARIANTES GENÉTICAS DO GENE CYP21A2 ASSOCIADAS À HIPERPLASIA ADRENAL CONGÊNITA POR SIMULAÇÃO COMPUTACIONAL
 VARIANTES GENÉTICAS DO GENE CYP21A2 ASSOCIADAS À HIPERPLASIA ADRENAL CONGÊNITA POR SIMULAÇÃO COMPUTACIONAL Clebson Pantoja PIMENTEL PIMENTEL, Clebson Pantoja. Variantes genéticas do gene CYP21A2 associadas
VARIANTES GENÉTICAS DO GENE CYP21A2 ASSOCIADAS À HIPERPLASIA ADRENAL CONGÊNITA POR SIMULAÇÃO COMPUTACIONAL Clebson Pantoja PIMENTEL PIMENTEL, Clebson Pantoja. Variantes genéticas do gene CYP21A2 associadas
Mecanismos bio-moleculares responsáveis pela captação e interpretação dos sinais do meio externo e interno comunicação celular
 Mecanismos bio-moleculares responsáveis pela captação e interpretação dos sinais do meio externo e interno comunicação celular Transferência citoplasmática direta de sinais elétricos e químicos Como as
Mecanismos bio-moleculares responsáveis pela captação e interpretação dos sinais do meio externo e interno comunicação celular Transferência citoplasmática direta de sinais elétricos e químicos Como as
Disco embrionário bilaminar
 Origem do embrião 1 Disco embrionário bilaminar 2 3 GASTRULAÇÃO - 3 a semana Aparecimento da linha primitiva Desenvolvimento da notocorda Diferenciação das três camadas germinativas (disco bilaminar trilaminar)
Origem do embrião 1 Disco embrionário bilaminar 2 3 GASTRULAÇÃO - 3 a semana Aparecimento da linha primitiva Desenvolvimento da notocorda Diferenciação das três camadas germinativas (disco bilaminar trilaminar)
Extensão da herança a Mendeliana
 Extensão da herança a Mendeliana Genética Básica Licenciatura em Biologia Victor Martin Quintana Flores Diferentes padrões de herança a Mendeliana Tipo Descrição Mendeliana simples Ligado ao X Alelos letais
Extensão da herança a Mendeliana Genética Básica Licenciatura em Biologia Victor Martin Quintana Flores Diferentes padrões de herança a Mendeliana Tipo Descrição Mendeliana simples Ligado ao X Alelos letais
Bases da Hereditariedade. Profa. Vanessa Silveira
 Bases da Hereditariedade Profa. Vanessa Silveira Roteiro de Aula 1. A informação genética: conceitos básicos 2. Base da Hereditariedade Leis de Mendel 3. Padrões clássicos de herança 4. Padrões não clássicos
Bases da Hereditariedade Profa. Vanessa Silveira Roteiro de Aula 1. A informação genética: conceitos básicos 2. Base da Hereditariedade Leis de Mendel 3. Padrões clássicos de herança 4. Padrões não clássicos
Bio. Rubens Oda. Monitor: Hélio Fresta
 Professor: Alexandre Bandeira Rubens Oda Monitor: Hélio Fresta Interação gênica e pleiotropia 16/18 out RESUMO Na Primeira Lei de Mendel, um par de alelos determinava uma característica. Na interação gênica,
Professor: Alexandre Bandeira Rubens Oda Monitor: Hélio Fresta Interação gênica e pleiotropia 16/18 out RESUMO Na Primeira Lei de Mendel, um par de alelos determinava uma característica. Na interação gênica,
Guião do Módulo I.II. Biologia Molecular, Celular e do Desenvolvimento Humano e Genética
 Guião do Módulo I.II. Biologia Molecular, Celular e do Desenvolvimento Humano e Genética Ano lectivo 2014/15-2º Semestre Mestrado Integrado em Medicina Faculdade de Medicina da Universidade de Lisboa Índice
Guião do Módulo I.II. Biologia Molecular, Celular e do Desenvolvimento Humano e Genética Ano lectivo 2014/15-2º Semestre Mestrado Integrado em Medicina Faculdade de Medicina da Universidade de Lisboa Índice
Genética Molecular. Tema 1: Genética Molecular. Prof. Leandro Parussolo
 Instituto Federal de Santa Catarina Câmpus Florianópolis Unidade Curricular: Biologia I Tema 1: Genética Molecular Genética Molecular Prof. Leandro Parussolo leandro.parussolo@ifsc.edu.br Genética Estuda
Instituto Federal de Santa Catarina Câmpus Florianópolis Unidade Curricular: Biologia I Tema 1: Genética Molecular Genética Molecular Prof. Leandro Parussolo leandro.parussolo@ifsc.edu.br Genética Estuda
GENÉTICA DO OLHO. Alex Schmidt; Guilherme Cossetin; Júlia Toral Gutteres; Sandra Gelati; Juliana Rosa
 GENÉTICA DO OLHO Alex Schmidt; Guilherme Cossetin; Júlia Toral Gutteres; Sandra Gelati; Juliana Rosa Trabalho de Pesquisa; Centro de Educação Básica Francisco de Assis-EFA INTRODUÇÃO O olho é uma parte
GENÉTICA DO OLHO Alex Schmidt; Guilherme Cossetin; Júlia Toral Gutteres; Sandra Gelati; Juliana Rosa Trabalho de Pesquisa; Centro de Educação Básica Francisco de Assis-EFA INTRODUÇÃO O olho é uma parte
EMBRIOLOGIA. M.Sc. Prof.ª Viviane Marques
 EMBRIOLOGIA M.Sc. Prof.ª Viviane Marques Fonoaudióloga, Neurofisiologista e Mestre em Fonoaudiologia Coordenadora da Pós-graduação em Fonoaudiologia Hospitalar Chefe da Equipe de Fonoaudiologia do Hospital
EMBRIOLOGIA M.Sc. Prof.ª Viviane Marques Fonoaudióloga, Neurofisiologista e Mestre em Fonoaudiologia Coordenadora da Pós-graduação em Fonoaudiologia Hospitalar Chefe da Equipe de Fonoaudiologia do Hospital
Estudo de Mecanismos Regulatórios e Mapeamento de Genes Associados a Malformações Craniofaciais
 Cibele Masotti Estudo de Mecanismos Regulatórios e Mapeamento de Genes Associados a Malformações Craniofaciais Instituto de Biociências Universidade de São Paulo São Paulo 2007 Cibele Masotti Estudo de
Cibele Masotti Estudo de Mecanismos Regulatórios e Mapeamento de Genes Associados a Malformações Craniofaciais Instituto de Biociências Universidade de São Paulo São Paulo 2007 Cibele Masotti Estudo de
Bio. Bio. Monitor: Sarah Elis
 Professor: Rubens Oda Monitor: Sarah Elis Exercícios sobre a primeira lei de Mendel e probabilidades 06 set EXERCÍCIOS DE AULA 1. Em uma certa espécie de mamíferos, há um caráter mendeliano com co-dominância
Professor: Rubens Oda Monitor: Sarah Elis Exercícios sobre a primeira lei de Mendel e probabilidades 06 set EXERCÍCIOS DE AULA 1. Em uma certa espécie de mamíferos, há um caráter mendeliano com co-dominância
Sumário ANEXO I COMUNICADO HERMES PARDINI
 Sumário ANEXO I COMUNICADO HERMES PARDINI Conteúdo ANTICORPOS ANTI Mi-2 ALTERAÇÕE NO EXAME... 2 ANTICORPOS ANTI ANTÍGENO HEPÁTICO SOLÚVEL ALTERAÇÃO DE INFORMAÇÕES DO HELP E LAYOUT... 3 PARVOVÍRUS B19 NOVO
Sumário ANEXO I COMUNICADO HERMES PARDINI Conteúdo ANTICORPOS ANTI Mi-2 ALTERAÇÕE NO EXAME... 2 ANTICORPOS ANTI ANTÍGENO HEPÁTICO SOLÚVEL ALTERAÇÃO DE INFORMAÇÕES DO HELP E LAYOUT... 3 PARVOVÍRUS B19 NOVO
Interação Gênica. Hélvio M. Gervásio
 Interação Gênica Hélvio M. Gervásio INTERAÇÃO GÊNICA Interação gênica ocorre quando dois ou mais pares de alelos diferentes atuam na determinação de um único caráter INTERAÇÃO GÊNICA Exemplo: Crista em
Interação Gênica Hélvio M. Gervásio INTERAÇÃO GÊNICA Interação gênica ocorre quando dois ou mais pares de alelos diferentes atuam na determinação de um único caráter INTERAÇÃO GÊNICA Exemplo: Crista em
Origem da variação. Conceitos importantes. Variação Genética e Evolução. Deriva. Seleção. Mutação. Migração
 Origem da variação Conceitos importantes Variação genética -> variantes alélicos São originados por mutação e intensificados por mecanismos recombinatórios e sexuais Diversidade ou variabilidade genética:
Origem da variação Conceitos importantes Variação genética -> variantes alélicos São originados por mutação e intensificados por mecanismos recombinatórios e sexuais Diversidade ou variabilidade genética:
07-Apr-16 SOMITOGÊNESE. o que são somitos
 SOMITOGÊNESE o que são somitos 1 Os somitos são formados : a) De forma periódica b) Bilateral c) Com identidade anteroposterior d) Com identidade axial 2 Mesoderma Intermediário Mesoderma Paraxial Mesoderma
SOMITOGÊNESE o que são somitos 1 Os somitos são formados : a) De forma periódica b) Bilateral c) Com identidade anteroposterior d) Com identidade axial 2 Mesoderma Intermediário Mesoderma Paraxial Mesoderma
Cromossômicas Monogênicas Poligênicas ou Multifatoriais Mitocondriais
 Distúrbios Monogênicos ou MENDELIANOS DISTÚRBIOS MONOGÊNICOS E PRINCIPAIS PADRÕES DE HERANÇA Profa. Dra. Milena Flória-Santos Departamento de Enfermagem Materno-Infantil e Saúde Pública Escola de Enfermagem
Distúrbios Monogênicos ou MENDELIANOS DISTÚRBIOS MONOGÊNICOS E PRINCIPAIS PADRÕES DE HERANÇA Profa. Dra. Milena Flória-Santos Departamento de Enfermagem Materno-Infantil e Saúde Pública Escola de Enfermagem
