1.1. Elementos químicos: constituição, isótopos e massa atómica relativa
|
|
|
- Cecília da Conceição Silveira
- 8 Há anos
- Visualizações:
Transcrição
1 Escola Secundária Vitorino Nemésio Curso Profissional de Técnico de Energias Renováveis 1º ano Módulo Q 1 Estrutura atómica. Tabela Periódica. Ligação Química. Documento de apoio 1. Estrutura atómica 1.1. Elementos químicos: constituição, isótopos e massa atómica relativa Átomos, moléculas e iões Todas as substâncias têm na base da sua constituição átomos. Os átomos podem associar-se, formando moléculas. Átomos ou moléculas podem ficar carregados electricamente, chamando-se, nesse caso, iões. As unidades estruturais da matéria podem ser, portanto, átomos, moléculas ou iões (Fig. 1). Figura 1 unidades estruturais da matéria. Toda a matéria é, em última análise, constituída por átomos, pois são os átomos que estão na base da constituição das moléculas e dos iões. Composição do átomo (protões, neutrões e electrões) A noção de átomo foi evoluindo ao longo da história. A palavra átomo vem do grego a + thomos (indivisível). Contudo, hoje sabe-se que o átomo é constituído por partículas mais pequenas, sendo, portanto, uma partícula divisível. O átomo (Fig. 2) compreende um núcleo, contendo protões e neutrões, e tem à volta do núcleo electrões. Figura 2 Modelo de um átomo. Cátia Homem Página 1
2 Quanto à carga eléctrica das partículas sub-atómicas podemos afirmar o seguinte: Os protões são partículas com carga positiva. Os meutrões são partículas neutras, ou seja não têm carga. Os electrões são partículas com carga negativa. É no pequeno núcleo, no centro do átomo, que se concentra quase toda a massa do átomo, uma vez que a massa dos electrões é muito menor do que a dos protões ou dos neutrões (tabela 1) Tabela 1 quadro síntese das partículas constituintes de um átomo. *Em unidades de massa do protão. **Em unidades de carga do protão. Como se pode concluir através da análise da tabela a massa do protão é praticamente igual à massa do neutrão, sendo a massa do electrão desprezável. Os átomos não têm carga eléctrica, uma vez que o número de protões (carga positiva) é igual ao número de electrões (carga negativa). Os átomos são, pois, electricamente neutros. As moléculas também não têm carga, uma vez que são feitas de átomos. Os iões não são mais do que átomos ou moléculas em que não existe compensação de cargas positivas e negativas, uma vez que lhe foram extraídos ou adicionados electrões. Os iões negativos possuem, pelo menos, mais um electrão do que o número de protões do núcleo. Já os iões positivos têm um número de protões superior ao número de electrões. Caracterização de um elemento químico (número atómico, número de massa e símbolo químico) O número atómico caracteriza um determinado elemento químico. O número atómico apenas toma valores inteiros e representa o número de protões existentes em todos os átomos desse elemento. Esse elemento é representado simbolicamente por um símbolo químico. Exemplo: todos os átomos de número atómico 1 são do mesmo elemento químico o hidrogénio (símbolo H), todos os átomos de número atómico 8 são do mesmo elemento químico o oxigénio (símbolo O). Assim podemos afirmar que: Átomos do mesmo elemento químico têm obrigatoriamente o mesmo número atómico. Cátia Homem Página 2
3 Contudo, átomos do mesmo elemento não têm de ser obrigatoriamente iguais. Estes podem diferir no número de neutrões que possuem, apresentando por isso diferente número de massa (soma do número atómico (número de protões) com o número de neutrões). Assim a um mesmo elemento químico podem corresponder diferentes valores do número de massa, uma vez que apesar do número de protões ser sempre o mesmo o número de neutrões pode variar. Os átomos do mesmo elemento químico que apresentam diferente número de massa, ou seja diferente número de neutrões são designados por isótopos. A palavra isótopo resulta do grego iso + thoposo, o que significa o mesmo lugar (na Tabela Periódica). A maioria dos elementos químicos possui isótopos. Genericamente, representamos as espécies químicas (átomos ou iões) com a notação (Fig. 3): Figura 3 Representação esquemática das espécies químicas. Massa atómica relativa A massa atómica relativa caracteriza cada elemento químico. Para determinar a massa atómica relativa de um elemento químico contribuem as massas isotópicas relativas, de acordo com as abundâncias dos isótopos naturais. A massa atómica relativa pode ser calculada através da seguinte expressão matemática: A r( E) = X 1 A r1 + X 2 A 100 Onde: X 1 abundância relativa do isótopo 1 do elemento (em percentagem). X 2 abundância relativa do isótopo 2 do elemento (em percentagem). A r1 massa isotópica relativa do isótopo 1. A r2 massa isotópica relativa do isótopo 2. Quase todos os elementos químicos têm isótopos. Por isso, a massa atómica relativa não é representada obrigatoriamente por números inteiros. Como já vimos anteriormente os iões são partículas que têm excesso ou carência de electrões. Podemos, então, interpretar a carga de um ião monoatómico como a diferença entre o número de de electrões que possui e o número atómico do respectivo átomo. Cátia Homem Página 3 r
4 Propriedades dos elementos versus propriedades das substâncias elementares correspondentes Não confundir elemento químico com substância elementar. O critério de organização dos elementos baseia-se nas diferenças e semelhanças das respectivas propriedades. Torna-se então necessário distinguir propriedades do elemento de propriedades das substâncias elementares. São propriedades dos elementos: a distribuição electrónica; o raio atómico; o número atómico; a massa atómica relativa; a energia de ionização. São propriedades das substâncias elementares (constituídas por elementos): o ponto de fusão; o ponto de ebulição; a massa volúmica ou densidade; o estado físico (sólido, líquido ou gasoso); a cor; a classificação em metais, não-metais e semimetais Modelo atómico actual simplificado Distribuição electrónica O modelo actual para o átomo é o modelo da nuvem electrónica segundo este, o átomo é constituído por um núcleo com protões e neutrões (com excepção do Hidrogénio-1 que só tem um protão), rodeado por uma nuvem electrónica, formada por electrões. Os electrões distribuem-se à volta do núcleo por níveis de energia ou camadas. O modelo mais simples para a distribuição electrónica é o que considera as designações atribuídas aos diferentes níveis energéticos K, L, M Segundo este modelo, os electrões de um átomo de número atómico Z vão distribuir-se em diferentes níveis de energia e a diferentes distâncias do núcleo. Assim, haverá electrões, em média, mais próximos do núcleo e menos energéticos e outros mais afastados e mais energéticos. Cátia Homem Página 4
5 Cada nível n é caracterizado por uma letra: ao primeiro (com electrões de menor energia) é atribuída a letra K, ao segundo a letra L, ao terceiro a letra M, e assim sucessivamente, seguindo a ordem alfabética. A tabela 2 mostra a associação entre o nível de energia e a letra que o caracteriza. Nível de energia n Designação 1 K 2 L 3 M 4 N O número máximo de electrões que podem existir em cada nível é: dois electrões no primeiro, K ou também caracterizado por n = 1; oito electrões no segundo, L ou também caracterizado por n = 2; dezoito electrões no terceiro, M ou também caracterizado por n = 3; e que obedece à relação: número máximo de electrões no nível n =2n 2 No entanto, a última camada só pode conter um máximo de oito electrões (excepto a primeira que só pode conter dois electrões). Estas informações estão sistematizadas na tabela 3. Nível de energia n Designação Número máximo de electrões no nível n (2n 2 ) 1 K 2 (2 2 1 ) Número máximo de electrões quando for a última L 8 (2 2 ) M 18 (2 3 ) 8 4 N 2 32 (2 4 ) 8 Tabela 3 nível de energia, designação, número de electrões máximo de electrões por nível e número máximo de electrões quando for a última camada. Exemplificando (tabela 4): Átomo Número atómico Distribuição electrónica H 1 K 1 Li 3 K 2 L 1 C 6 K 2 L 4 Na 11 K 2 L 8 M 1 Ca 20 K 2 L 8 M 8 N 2 Tabela 4 exemplificação do que foi dito anteriormente. Este tipo de distribuição simplificado usa-se, fundamentalmente, na escrita das estruturas de Lewis. Cátia Homem Página 5
6 Representação de Lewis Quando os átomos interagem para formar uma ligação, apenas os electrões de valência vão interagir, pelo que só as distribuições electrónicas de valência são importantes. Os electrões mais internos, electrões do cerne, são fortemente atraídos pelos núcleos, não se envolvendo na ligação. Os electrões de valência são os electrões do nível mais externo de um átomo. Estes electrões são especialmente importantes, pois situam-se no nível mais energético do átomo, determinando as propriedades químicas do elemento e sendo responsáveis pelo modo como um átomo se liga a outros. Como saber quais os electrões de valência? 1. Fazer a configuração electrónica do elemento. 2. Identificar os electrões de valência como sendo aqueles que ficarem na última camada, ou seja, no último nível de energia. Exemplo: 3 Li configuração electrónica K 2 L 1 o lítio tem 1 electrão de valência. A representação dos electrões de valência de cada átomo pode ser feita através da representação de Lewis. Na representação de Lewis o símbolo químico do elemento representa o núcleo do átomo, no hidrogénio e no Hélio, ou o núcleo e os electrões do cerne (electrões que se encontram nos níveis menos energéticos, ou seja todos os electrões com excepção dos electrões do último nível de energia), para os restantes elementos químicos. O símbolo químico surge rodeado por pontos ou por cruzes que representam os electrões de valência. O número de prontos ou cruzes é igual ao número de electrões de valência. Os pontos ou cruzes são colocados da seguinte forma: um(a) em cada um dos quatro lados do símbolo do elemento. A seguir, são agrupados(as) aos pares, até se esgotarem os electrões de valência. Na tabela 5 estão representadas as configurações / distribuições electrónicas de valência dos átomos dos elementos dos segundo e terceiro períodos. Tabela 5 representação das distribuições electrónicas de valência dos átomos dos elementos do segundo e terceiro períodos. Cátia Homem Página 6
7 2. Tabela periódica 2.1. Tabela Periódica: evolução e organização actual Evolução da Tabela Periódica Vários cientistas sentiram a necessidade de organizar os elementos conhecidos em tabelas, de modo a salientar propriedades comuns. Assim, em 1661, Robert Boyle escreveu o seguinte: os elementos são certos corpos primitivos e simples que não são formados por outros corpos e que são os ingredientes de que se compõem todos os corpos compostos. Antoine Lavoisier, adoptou o conceito de elemento em Resolveu classificar os cerca de 30 elementos então conhecidos em metais, gases não-metais e elementos terrosos. Esta terá sido a primeira tentativa de ordenação sistemática dos elementos. Em 1829, Johann Döbereiner estabeleceu as tríadas grupos de três elementos com propriedades semelhantes e organizadas por ordem crescente de massas atómicas. Em 1862, Alexandre de Chancourtois organizou os elementos por ordem crescente de massas atómicas, colocou-os sobre uma linha helicoidal que recobria uma superfície cilíndrica formando como que um caracol o caracol de Chancourtois. Em 1864, John Newlands organizou os elementos por ordem crescente de massas atómicas, de tal modo que os elementos com propriedades semelhantes repetiam-se em intervalos de 8, isto é o oitavo elemento, a partir de um qualquer, apresentava propriedades semelhantes às do elemento considerado como ponto de partida Lei das oitavas. Em 1872, Dmitri Mendeleev publicou uma tabela periódica baseada na repetição periódica e regular das propriedades dos elementos, onde dispunha os cerca de 60 elementos até então conhecidos, por ordem crescente de massas atómicas, as suas propriedades variavam de forma regular. Os elementos foram, dispostos por Mendeleev, em linhas horizontais e verticais, por ordem crescente de massas atómicas, mas deixando espaços vazios destinados aos elementos que, na sua opinião, viriam a ser descobertos. Esta foi a primeira Tabela Periódica. Cátia Homem Página 7
8 Tabela 6 Tabela Periódica proposta por Mendeleev, em Em 1913, Henry Moseley estabeleceu o conceito de número atómico, identificando-o com a carga positiva do núcleo dos átomos de cada elemento, verificando que esse número coincidia com o número de ordem do elemento na Tabela Periódica. De acordo com a Lei Periódica de Moseley, as propriedades dos elementos repetem-se periodicamente quando estes são colocados por ordem crescente de número atómico. É nesta lei periódica que se baseia a Tabela Periódica actual. Organização da Tabela Periódica actual A Tabela Periódica actual está organizada em 18 grupos e 7 períodos. Os elementos, que se situam nos grupos 1,2,13,14,15,16,17 e 18, são denominados de elementos representativos. Os elementos, que se situam nos grupos 3,4,5,6,7,8,9,10,11 e 12, são denominados de elementos de transição. Cátia Homem Página 8
9 Tabela periódica actual Cátia Homem Página 9
10 2.2. Localização dos elementos na Tabela Periódica: o período e o grupo Disposição dos elementos químicos na Tabela Periódica Na Tabela Periódica os elementos químicos estão dispostos por ordem crescente de número atómico, segundo linhas designadas por períodos. Actualmente a Tabela Periódica está organizada em sete períodos. O conjunto dos elementos dispostos na mesma linha pertence ao mesmo período. A Tabela Periódica também está organizada segundo 18 colunas de elementos químicos. Cada uma destas colunas tem o nome de grupo. O conjunto de elementos dispostos na mesma coluna pertence ao mesmo grupo. Alguns grupos têm nomes próprios (tabela 7). Tabela 7 nomes próprios de alguns grupos. Relação entre a posição (grupo e período) dos elementos representativos na Tabela Periódica e as respectivas distribuições electrónicas Os elementos do mesmo grupo têm igual configuração electrónica de valência. É da configuração electrónica de valência que dependem as propriedades químicas. O número do período a que pertence um elemento coincide com o número do último nível de energia. Nos grupos 1 e 2 dos elementos representativos, o número do grupo é igual ao número de electrões de valência; nos grupos 13 a 18 (até Z=18) o número do grupo obtém-se adicionando 10 ao número de electrões de valência. A posição dos elementos na Tabela Periódica tem relação directa com a distribuição electrónica dos átomos dos seus elementos. Assim: A distribuição electrónica determina a estrutura da Tabela Periódica; Elementos do mesmo grupo possuem o mesmo número de electrões de valência, o que lhes confere comportamento químico semelhante. Exemplo: O Lítio, 3 Li, pertence ao 2º período e ao grupo 1. Porquê? A configuração electrónica do lítio é: K 2 L 1, pelo que o lítio tem 1 electrão de valência. O lítio pertence ao grupo 1 da Tabela Periódica porque tem 1 electrão de valência e é um elemento representativo. Cátia Homem Página 10
11 O lítio pertence ao 2º período da Tabela Periódica porque tem os electrões distribuídos por dois níveis de energia. Periodicidade de algumas propriedades físicas e químicas dos elementos Existem várias propriedades que apresentam uma variação regular ao longo dos grupos e dos períodos da Tabela Periódica. Contudo, apenas estudaremos o raio atómico e a energia de ionização Variação do raio atómico e da energia de ionização dos elementos da Tabela Periódica Raio atómico O raio atómico de um elemento consiste no raio de uma esfera representativa de um átomo isolado desse elemento. Energia de ionização A energia de ionização é a energia necessária para retirar uma mole de electrões a uma mole de átomos, no estado fundamental e gasoso. A energia de ionização exprime-se normalmente em KJmol -1. Variação do raio atómico dos elementos representativos, ao longo de um período e ao longo de um grupo, com o número atómico O tamanho dos átomos depende de dois factores: a atracção nuclear (entre o núcleo e os electrões) e a repulsão electrónica. Verifica-se que, de uma forma geral, na Tabela Periódica: O raio atómico diminui ao longo de um período. Tal facto deve-se ao aumento do número atómico. A presença de mais protões no núcleo determina uma maior atracção dos electrões pelos núcleos. Devemos notar que, ao longo de um período, também aumenta o número de electrões, o que, por si só, conduziria a uma maior repulsão electrónica e a um aumento do raio atómico. Como se verifica experimentalmente que o raio atómico diminui ao longo de um período, concluímos que o aumento do número de electrões é, em regra, menos importante do que o aumento da carga nuclear. Quando transitamos de período, por exemplo ao passar do elemento néon (Z = 10) para o sódio (Z = 11), há também um aumento da carga nuclear mas, no entanto, o raio atómico aumenta significativamente (r Ne = 71 pm; r Na = 186 pm). Tal deve-se ao preenchimento de um nível de energia maior que leva a que os electrões de valência passem a estar, em média, mais afastados do núcleo. Assim, de uma forma geral: O raio atómico aumenta ao longo de um grupo. Cátia Homem Página 11
12 A figura 4 apresenta os raios atómicos dos elementos representativos, mostrando que, de facto, o raio atómico diminui ao longo do período. Por exemplo, o raio atómico do oxigénio (Z = 8) é menor do que o do azoto (Z = 7), e este, por sua vez, é menor ainda que o do carbono (Z = 6). Figura 4 Raio atómico dos elementos representativos. Variação da energia de ionização dos elementos representativos, ao longo de um período e ao longo de um grupo, com o número atómico Ao longo de um grupo da Tabela Periódica aumenta o número de níveis de energia e, com ele, a energia do electrão. Assim, se o electrão possui mais energia é mais fácil removê-lo, concluindo-se que: Note-se que, regra geral: A energia de ionização diminui ao longo de um grupo. A primeira energia de ionização aumenta ao longo de um período Ao longo do período a carga nuclear vai aumentando, mas o electrão a remover está no mesmo nível de energia. À medida que progredimos no período, o electrão de valência vai ficando sujeito a maior atracção, sendo necessária mais energia para o «arrancar» do núcleo. Figura 5 Variação da primeira energia de ionização dos elementos representativos na tabela periódica ( J/átomo). Cátia Homem Página 12
13 2.4. Propriedades dos elementos e propriedades das substâncias elementares Informações contidas na Tabela Periódica que se referem aos elementos e às substâncias elementares A Tabela Periódica fornece-nos informações acerca de determinado elemento. Algumas delas são: a distribuição electrónica / configuração electrónica; o raio atómico; o número atómico; a massa atómica relativa; a energia de ionização. A Tabela Periódica, também, nos fornece informações acerca das substâncias elementares. Algumas delas são: o ponto de fusão; o ponto de ebulição; a massa volúmica ou densidade; o estado físico (sólido, líquido ou gasoso); a classificação em metais, não-metais e semimetais. 3. Estrutura molecular Ligação química 3.1. Ligação química: modelo de ligação covalente Ligação química covalente As moléculas formam-se por ligações entre átomos chamadas ligações covalentes. Numa ligação covalente entre dois átomos, existem, pelos menos, dois electrões que são partilhados pelos átomos. Apenas os electrões de valência podem participar na ligação covalente. Numa ligação covalente cada electrão partilhado é atraído por ambos os núcleos. São estes electrões que asseguram a ligação covalente conferindo estabilidade à ligação. Para simbolizar a estrutura de moléculas simples utiliza-se a representação de Lewis. Na fórmula de estrutura de uma molécula pode representar-se cada par de electrões por uma pequena barra. No entanto muitas vezes utiliza-se a representação por e que serve para distinguir os electrões partilhados por cada átomo. Regra do octeto Regra do octeto Os átomos ligam-se partilhando electrões de forma a ficarem com oito electrões de valência à sua volta. Cátia Homem Página 13
14 Exemplo de formas de estruturas de moléculas Molécula de hidrogénio Figura 6 representação pela notação de Lewis da molécula de hidrogénio. Na ligação covalente da molécula de hidrogénio, dois átomos de hidrogénio instáveis, por apenas possuírem um electrão na última camada, partilham um electrão, cada um, ficando cada um dos átomos com dois electrões e, desta forma, com maior estabilidade. Molécula de oxigénio A molécula de oxigénio obedece à regra do octeto. Assim, se cada átomo de oxigénio tem seis electrões de valência, para ficar estável, cada átomo, necessitava de mais dois electrões. Pelo que na molécula de oxigénio cada um dos átomos partilha dois electrões, de modo a que cada átomo fique com oito electrões à sua volta. Figura 7 representação pela notação de Lewis da molécula de oxigénio. Repare-se que no caso do oxigénio nem todos os electrões de valência participaram na ligação química covalente. Estes electrões são denominados electrões não ligantes. Molécula de dióxido de carbono A molécula de dióxido de carbono obedece à regra do octeto. Assim: cada átomo de oxigénio tem seis electrões de valência, para ficar estável, cada átomo, necessitava de mais dois electrões; o átomo de carbono tem quatro electrões de valência, para ficar estável necessitava de mais quatro electrões; conclui-se que na molécula de dióxido de carbono cada um dos átomos de oxigénio partilha dois electrões, e o átomo de carbono partilha quatro electrões de modo a que cada átomo fique com oito electrões à sua volta. Figura 8 representação pela notação de Lewis da molécula de oxigénio. Cátia Homem Página 14
15 Ligações covalentes: simples, duplas e triplas. Ordem de ligação A ordem de ligação é dada pelo número de pares de electrões envolvidos em cada uma das ligações. As ligações covalentes podem ser simples, duplas e triplas. Na ligação covalente simples existem dois electrões (um par de electrões) a serem partilhados pelos átomos ligados. A ordem de ligação é 1. Na ligação covalente dupla existem quatro electrões (dois pares de electrões) a serem partilhados pelos átomos ligados. A ordem de ligação é 2. Na ligação covalente tripla existem seis electrões (três pares de electrões) a serem partilhados pelos átomos ligados. A ordem de ligação é 3. Em geral, quanto maior é a ordem de ligação, mais forte é a ligação. Comprimento de ligação O comprimento de ligação é uma propriedade das ligações químicas e diz respeito à distância média entre os dois núcleos de dois átomos ligados numa molécula. O comprimento da ligação simples é maior do que o comprimento da ligação dupla. O comprimento da ligação dupla é maior do que o comprimento da ligação tripla. Energia de ligação Energia de ligação ou energia de uma ligação covalente é a energia que se liberta quando dois átomos isolados se ligam para estabelecer uma ligação covalente, estando os átomos no estado gasoso e fundamental. A energia da ligação simples é menor do que a energia da ligação dupla. A energia da ligação dupla é menor do que a energia da ligação tripla. Energia de dissociação Energia de dissociação é a energia mínima que é necessário fornecer a uma molécula para quebrar a ligação química entre dois átomos. A energia de ligação é geralmente simétrica da energia de dissociação. Numa molécula diatómica a energia de dissociação é simétrica da energia de ligação. Relação entre energia de ligação, ordem de ligação e comprimento de ligação para moléculas diatómicas A um maior comprimento de ligação corresponde uma menor energia de ligação e vice-versa. Cátia Homem Página 15
16 Geralmente, quanto maior é a ordem de ligação, mais forte é a ligação, consequentemente maior é a energia de ligação e menor é o comprimento de ligação e vice-versa. Maior energia de ligação Maior ordem de ligação ligação mais forte Menor comprimento de ligação Figura 10 relação entre energia de ligação, ordem de ligação e comprimento de ligação. Electronegatividade A electronegatividade é um parâmetro que mede a tendência que um átomo tem para atrair os electrões que partilha com outro átomo ao qual está ligado, ou seja é a tendência de um átomo numa ligação química para atrair a si os electrões que formam esta ligação química. Existem várias tabelas com valores de electronegatividade, no entanto a mais utilizada é a escala de Pauling. Figura 9 valores de electronegatividade segundo Pauling Moléculas polares e moléculas apolares Molécula apolar molécula em que existe uma distribuição de carga simétrica. Isto acontece quando os electrões compartilhados são igualmente atraídos pelos núcleos dos dois átomos. Um exemplo é quando se estabelece uma ligação covalente entre dois átomos do mesmo elemento. Molécula polar molécula em que existe uma distribuição de carga assimétrica. Isto acontece quando os electrões compartilhados não são igualmente atraídos pelos núcleos dos dois átomos. Um exemplo é quando se estabelece uma ligação covalente entre dois átomos de elementos diferentes. Temos de ter em conta a electronegatividade de cada uma dos átomos envolvidos na ligação para sabermos se uma molécula constituída por dois átomos é polar ou apolar. Cátia Homem Página 16
17 Geometria molecular Os átomos de uma molécula não estão dispostos de uma forma qualquer. O arranjo destes átomos é aquele que confere à molécula a menor energia, isto é, a maior estabilidade. A geometria molecular é o arranjo tridimensional dos átomos numa molécula, designando-se a respectiva fórmula por fórmula esterioquímica. A geometria de uma molécula é aquela que minimiza a repulsão entre todos os pares electrónicos de valência (teoria da repulsão dos pares electrónicos de valência). Um dos parâmetros importantes na geometria de uma molécula é o seu ângulo de ligação. O ângulo de ligação é o menor dos ângulos definidos por duas ligações covalentes de um mesmo átomo. Algumas geometrias moleculares e respectivo ângulo de ligação Geometria linear Todas as moléculas que apenas possuam dois átomos têm geometria linear. Exemplo: H 2. Figura 10 Geometrias das moléculas lineares H 2, HF e F 2: fórmulas de estrutura e nuvens electrónicas. Também existem moléculas com três átomos que também possuem geometria linear, isto acontece quando o átomo central não possui electrões não ligantes, é o caso da molécula de dióxido de carbono (CO 2 ). O ângulo de ligação numa molécula com geometria linear é de 180º. Figura 11 Geometria da molécula linear CO 2 : fórmula de estrutura. Geometria triangular plana Esta geometria é característica das moléculas que possuem: um átomo central, sem pares de electrões não ligantes, ligado a três outros átomos. Exemplo: molécula de trihidreto de boro, BH 3. O ângulo de ligação numa molécula com geometria triangular plana é de 120º. Figura 12 Geometria da molécula triangular plana BH 3 : fórmula de estrutura e ângulo de ligação. Cátia Homem Página 17
18 Geometria piramidal trigonal Esta geometria é característica das moléculas que possuem: um átomo central, com um par de electrões não ligantes, ligado a três outros átomos. Exemplo: molécula de amoníaco, NH 3. O ângulo de ligação na molécula de amoníaco é de 107º. Figura 13 Geometria da molécula piramidal trigonal NH 3 : fórmula de estrutura. Geometria tetraédrica Esta geometria é característica das moléculas que possuem: um átomo central, sem pares de electrões não ligantes, ligado a quatro outros átomos. Exemplo: molécula de metano, CH 4. O ângulo de ligação na molécula de metano é de 109,5º. Figura 14 Geometria da molécula tetraédrica CH 4 : fórmula de estrutura Ligação química: modelo de ligação iónica A ligação iónica resulta das forças eléctricas de atracção entre iões de sinais contrários, ou seja, entre iões positivos (catiões) e negativos (aniões). Nas condições padrão todos os compostos iónicos são sólidos cristalinos. A estabilidade global de um composto iónico resulta das interacções de todos os iões e não apenas da interacção entre um anião e um catião. Nos compostos iónicos a fórmula química traduz apenas a proporção entre os iões e consequentemente a electroneutralidade do composto. Neste caso, a fórmula química não corresponde a nenhuma unidade estrutural mínima. Notação de Lewis Os iões podem ser representados através da notação de Lewis. Esta representação é semelhante à utilizada para os átomos. Contudo, no caso do ião é necessário acrescentar a sua carga. Exemplo: representação do anião fluoreto, F -, segundo a notação de Lewis (figura 15). Figura 15 Representação do anião fluoreto, F -, segundo a notação de Lewis. Cátia Homem Página 18
19 Os compostos iónicos, também, podem ser representados através da notação de Lewis. Esta representação é semelhante à utilizada para as moléculas. Contudo, no caso do composto iónico é necessário acrescentar a carga de cada um dos iões envolvidos na ligação iónica. Exemplo: representação do composto iónico fluoreto de Lítio, LiF, segundo a notação de Lewis (figura 16). Figura 16 Representação do composto iónico fluoreto de lítio, LiF, segundo a notação de Lewis Ligação química: modelo de ligação metálica Ligação metálica ligação que se estabelece entre átomos, de metais, do mesmo elemento químico. Exemplo: o ferro representa-se por Fe. A estrutura de um metal corresponde a um arranjo ordenado de iões positivos imersos num mar de electrões de valência deslocalizados, ou seja, os electrões de valência não estão rigidamente atraídos a um mesmo ião positivo. Figura 17 Representação esquemática da ligação metálica. Bibliografia consultada: Dantas, M; Ramalho, M (2007). Jogo de partículas A Física e Química A Química bloco 1 10º /11º ano. Lisboa: Texto Editores. Dantas, M; Ramalho, M (2007). Jogo de partículas B Física e Química B Química 10º ano. Lisboa: Texto Editores. Magalhães, J (2007). Elementos Química A 10º ano. Carnaxide: Santillana Constância. Paiva, J; et al (2007). 10 Q Física e Química A Química bloco 1 10º / 11º ano. Lisboa: Texto Editores. Simões, T; Queirós, M; Simões, M (2004). Química em contexto Física e Química B Química 10º ano. Porto: Porto Editora. Programa componente de formação cientifica disciplina de Física e Química cursos profissionais de nível secundário. Cátia Homem Página 19
Tabela periódica e propriedades periódicas
 Tabela periódica e propriedades periódicas Mendeleev Vários cientistas procuravam agrupar os átomos de acordo com algum tipo de semelhança, mas o químico russo Dmitri Ivanovich Mendeleev foi o primeiro
Tabela periódica e propriedades periódicas Mendeleev Vários cientistas procuravam agrupar os átomos de acordo com algum tipo de semelhança, mas o químico russo Dmitri Ivanovich Mendeleev foi o primeiro
MOLÉCULAS NA TROPOSFERA. Espécies Maioritárias e Espécies Vestigiais
 MOLÉCULAS NA TROPOSFERA Espécies Maioritárias e Espécies Vestigiais 18-01-2013 Dulce Campos 2 Estudo da molécula de oxigénio A atmosfera é constituída maioritariamente por moléculas. Os átomos ligam-se,
MOLÉCULAS NA TROPOSFERA Espécies Maioritárias e Espécies Vestigiais 18-01-2013 Dulce Campos 2 Estudo da molécula de oxigénio A atmosfera é constituída maioritariamente por moléculas. Os átomos ligam-se,
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007
 Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
Apostila de Química Geral
 Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09
 Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 2ºTeste Sumativo 1ºPeríodo Duração do Teste:60 minutos Data: 05 / 12 / 08 Prof. Dulce Godinho
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 2ºTeste Sumativo 1ºPeríodo Duração do Teste:60 minutos Data: 05 / 12 / 08 Prof. Dulce Godinho
Evolução do modelo atómico
 Os neutrões só foram descobertos em 1932 por Chadwick. Evolução do modelo atómico Demócrito (400 a.c.) Enunciou a primeira ideia de átomo como sendo a partícula elementar que constitui toda a matéria.
Os neutrões só foram descobertos em 1932 por Chadwick. Evolução do modelo atómico Demócrito (400 a.c.) Enunciou a primeira ideia de átomo como sendo a partícula elementar que constitui toda a matéria.
Ligações Químicas Ligação Iônica Ligação Metálica
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
Evolução do Modelo Atómico
 Evolução do Modelo Atómico Desde a antiguidade que os homens se preocupavam em saber de que é que as «coisas» são feitas. No entanto, existiam perspectivas diversas sobre o assunto, a mais conhecida das
Evolução do Modelo Atómico Desde a antiguidade que os homens se preocupavam em saber de que é que as «coisas» são feitas. No entanto, existiam perspectivas diversas sobre o assunto, a mais conhecida das
Correção da ficha de trabalho N.º3
 Correção da ficha de trabalho N.º3 1- Classifique as afirmações seguintes em verdadeiras ou falsas, corrigindo estas últimas: A. A passagem de um átomo de um estado excitado ao estado fundamental é acompanhada
Correção da ficha de trabalho N.º3 1- Classifique as afirmações seguintes em verdadeiras ou falsas, corrigindo estas últimas: A. A passagem de um átomo de um estado excitado ao estado fundamental é acompanhada
LIGAÇÕES QUÍMICAS TEORIA CORPUSCULAR
 LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
QUIMICA ORGÂNICA BÁSICA
 QUIMICA ORGÂNICA BÁSICA Hibridização Revisão - Química Orgânica Básica 1 Tabela Periódica 2 Moléculas Diatômicas 3 Moléculas Poliatômicas 4 Eletronegatividade 5 A interação da luz e a matéria 6 Hibridização
QUIMICA ORGÂNICA BÁSICA Hibridização Revisão - Química Orgânica Básica 1 Tabela Periódica 2 Moléculas Diatômicas 3 Moléculas Poliatômicas 4 Eletronegatividade 5 A interação da luz e a matéria 6 Hibridização
Química Atomística Profª: Bruna Villas Bôas. Exercícios
 NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é:
 01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
APSA 2 - Tabela Periódica 10º Ano Novembro de 2011
 1. Dada a distribuição eletrónica dos elementos a seguir, indique qual deles apresenta maior e menor raio atómico 3Li: 1s 2 2s 1 7N: 1s 2 2s 2 2p 3 9F: 1s 2 2s 2 2p 5 R: Maior raio Atómico = Li Menor raio
1. Dada a distribuição eletrónica dos elementos a seguir, indique qual deles apresenta maior e menor raio atómico 3Li: 1s 2 2s 1 7N: 1s 2 2s 2 2p 3 9F: 1s 2 2s 2 2p 5 R: Maior raio Atómico = Li Menor raio
GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES. Professor Cristiano
 GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES Professor Cristiano GEOMETRIA MOLECULAR É o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Dependendo dos átomos que a
GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES Professor Cristiano GEOMETRIA MOLECULAR É o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Dependendo dos átomos que a
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE
 LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
Estrutura Eletrônica e Ligação Aula 2. QO-427 Prof. J. Augusto
 Estrutura Eletrônica e Ligação Aula 2 QO-427 Prof. J. Augusto Química Orgânica Orgânica até meados de 1800 referia-se a compostos de fontes com vida ( fontes minerais eram inorgânicos ) Wöhler em 1828
Estrutura Eletrônica e Ligação Aula 2 QO-427 Prof. J. Augusto Química Orgânica Orgânica até meados de 1800 referia-se a compostos de fontes com vida ( fontes minerais eram inorgânicos ) Wöhler em 1828
= 0 molécula. cada momento dipolar existente na molécula. Lembrando que u R
 Lista de Exercícios de Geometria e Ligações 1) Numere a segunda coluna (estruturas geométricas) de acordo com a primeira coluna (compostos químicos). 1. NH 3 ( ) linear 2. CO 2 ( ) angular 3. H 2 O ( )
Lista de Exercícios de Geometria e Ligações 1) Numere a segunda coluna (estruturas geométricas) de acordo com a primeira coluna (compostos químicos). 1. NH 3 ( ) linear 2. CO 2 ( ) angular 3. H 2 O ( )
Prova de Recuperação Bimestral de Ciências Nome Completo: Data: / /2010
 COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
Propriedades Físicas de alguns compostos
 Propriedades Físicas de alguns compostos Tipo de ligação e temperatura de fusão COMPOSTO Tipo de ligação T fusão / o C NaCl iónica 801 Cu metálica 1083 Si covalente 1410 H 2 O intermolecular 0 C 6 H 6
Propriedades Físicas de alguns compostos Tipo de ligação e temperatura de fusão COMPOSTO Tipo de ligação T fusão / o C NaCl iónica 801 Cu metálica 1083 Si covalente 1410 H 2 O intermolecular 0 C 6 H 6
Hidrogênio x Hidrogênio Hidrogênio x Não metal Não metal x Não metal
 LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo
 Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Agrupamento de Escolas da Senhora da Hora
 Agrupamento de Escolas da Senhora da Hora Curso Profissional de Técnico de Gestão de Equipamentos Informáticos Informação Prova da Disciplina de Física e Química - Módulo: 1 Estrutura Atómica. Tabela Periódica.
Agrupamento de Escolas da Senhora da Hora Curso Profissional de Técnico de Gestão de Equipamentos Informáticos Informação Prova da Disciplina de Física e Química - Módulo: 1 Estrutura Atómica. Tabela Periódica.
Próton Nêutron Elétron
 Próton Nêutron Elétron ARNOLD SOMMERFELD MODELO ATÔMICO DE ARNOLD SOMMERFELD - 1916 Ao pesquisar o átomo, Sommerfeld concluiu que os elétrons de um mesmo nível, ocupam órbitas de trajetórias diferentes
Próton Nêutron Elétron ARNOLD SOMMERFELD MODELO ATÔMICO DE ARNOLD SOMMERFELD - 1916 Ao pesquisar o átomo, Sommerfeld concluiu que os elétrons de um mesmo nível, ocupam órbitas de trajetórias diferentes
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA
 PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA TEMAS 1. Estrutura da matéria 1.1 Elementos, átomos e iões 1.2
PROVA ESPECIALMENTE ADEQUADA DESTINADA A AVALIAR A CAPACIDADE PARA A FREQUÊNCIA DO ENSINO SUPERIOR DOS MAIORES DE 23 ANOS PROVA DE QUÍMICA TEMAS 1. Estrutura da matéria 1.1 Elementos, átomos e iões 1.2
AULA PRÁTICA DE SALA DE AULA FQA - Espécies maioritárias e vestigiais 10º ANO 8 fev. 2013
 AULA PRÁTICA DE SALA DE AULA FQA - Espécies maioritárias e vestigiais 10º ANO 8 fev. 2013 / Nome: nº 1. Atualmente, a troposfera é constituída por espécies maioritárias, como o azoto, N 2, o oxigénio,
AULA PRÁTICA DE SALA DE AULA FQA - Espécies maioritárias e vestigiais 10º ANO 8 fev. 2013 / Nome: nº 1. Atualmente, a troposfera é constituída por espécies maioritárias, como o azoto, N 2, o oxigénio,
Teoria Atômica. Constituição da matéria. Raízes históricas da composição da matéria. Modelos atômicos. Composição de um átomo.
 Teoria Atômica Constituição da matéria Raízes históricas da composição da matéria Modelos atômicos Composição de um átomo Tabela periódica Raízes Históricas 6000 a.c.: descoberta do fogo 4000 a.c.: vidros,
Teoria Atômica Constituição da matéria Raízes históricas da composição da matéria Modelos atômicos Composição de um átomo Tabela periódica Raízes Históricas 6000 a.c.: descoberta do fogo 4000 a.c.: vidros,
CONTEÚDO E HABILIDADES DINÂMICA LOCAL INTERATIVA INTERATIVIDADE FINAL AULA QUÍMICA. Unidade III. Ligações químicas e funções inorgânicas.
 Unidade III Ligações químicas e funções inorgânicas. 2 Aula 12.1 Conteúdo: Geometria molecular Polaridade das moléculas 3 Habilidades: Relacionar informações apresentadas em diferentes formas de linguagem
Unidade III Ligações químicas e funções inorgânicas. 2 Aula 12.1 Conteúdo: Geometria molecular Polaridade das moléculas 3 Habilidades: Relacionar informações apresentadas em diferentes formas de linguagem
3.2. ORBITAIS E NÚMEROS QUÂNTICOS 3.3. CONFIGURAÇÕES ELETRÔNICAS. Aline Lamenha
 3.2. ORBITAIS E NÚMEROS QUÂNTICOS 3.3. CONFIGURAÇÕES ELETRÔNICAS Aline Lamenha OBJETIVOS Referir os contributos de vários cientistas e das suas propostas de modelo atómico, para a criação do modelo atómico
3.2. ORBITAIS E NÚMEROS QUÂNTICOS 3.3. CONFIGURAÇÕES ELETRÔNICAS Aline Lamenha OBJETIVOS Referir os contributos de vários cientistas e das suas propostas de modelo atómico, para a criação do modelo atómico
LIGAÇÕES INTERATÔMICAS
 UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
LIGAÇÃO QUÍMICA NO CARBONO GEOMETRIA MOLECULAR HIBRIDAÇÃO. 06-11-2006 Maria da Conceição Paiva 1
 LIGAÇÃO QUÍMICA NO CARBONO GEOMETRIA MOLECULAR IBRIDAÇÃO 06-11-2006 Maria da Conceição Paiva 1 Geometria molecular O arranjo tri-dimensional dos átomos numa molécula geometria molecular A teoria da repulsão
LIGAÇÃO QUÍMICA NO CARBONO GEOMETRIA MOLECULAR IBRIDAÇÃO 06-11-2006 Maria da Conceição Paiva 1 Geometria molecular O arranjo tri-dimensional dos átomos numa molécula geometria molecular A teoria da repulsão
TD nº 02 Química 2 1º ano - 2011
 Prof. Willame TD nº 02 Química 2 1º ano - 2011 TABELA PERIÓDICA 1. A organização dos elementos Com a descoberta de uma grande variedade de átomos, tornou-se necessária à criação de uma sistemática de classificação.
Prof. Willame TD nº 02 Química 2 1º ano - 2011 TABELA PERIÓDICA 1. A organização dos elementos Com a descoberta de uma grande variedade de átomos, tornou-se necessária à criação de uma sistemática de classificação.
Breve história da Tabela Periódica
 Breve história da Tabela Periódica Apesar dos parcos conhecimentos de Química que cada um possa ter, com certeza que já ouviu falar da Tabela Periódica, uma disposição sistemática dos elementos químicos
Breve história da Tabela Periódica Apesar dos parcos conhecimentos de Química que cada um possa ter, com certeza que já ouviu falar da Tabela Periódica, uma disposição sistemática dos elementos químicos
ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos
 Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
Respostas da terceira lista de exercícios de química. Prof a. Marcia M. Meier
 Respostas da terceira lista de exercícios de química Prof a. Marcia M. Meier 1) O íon brometo não aceita mais de um elétron, pois este segundo elétron ocupará numeros quânticos maiores quando comparado
Respostas da terceira lista de exercícios de química Prof a. Marcia M. Meier 1) O íon brometo não aceita mais de um elétron, pois este segundo elétron ocupará numeros quânticos maiores quando comparado
Química. Resolução das atividades complementares. Q42 Ligação metálica
 Resolução das atividades complementares 3 Química Q42 Ligação metálica p. 59 1 (Cefet-PR) Analise as afirmações a seguir: I. O metal X é leve, sofre pouca corrosão e é bastante utilizado na construção
Resolução das atividades complementares 3 Química Q42 Ligação metálica p. 59 1 (Cefet-PR) Analise as afirmações a seguir: I. O metal X é leve, sofre pouca corrosão e é bastante utilizado na construção
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS
 Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
DISTRIBUIÇÃO ELETRÔNICA E N OS QUâNTICOS TEORIA - PARTE II. Elétron de diferenciação e elétrons de valência. Distribuição eletrônica de íons
 DISTRIBUIÇÃO ELETRÔNICA E N OS QUâNTICOS TEORIA - PARTE II Elétron de diferenciação e elétrons de valência O elétron de diferenciação é definido como o último elétron do subnível mais energético de um
DISTRIBUIÇÃO ELETRÔNICA E N OS QUâNTICOS TEORIA - PARTE II Elétron de diferenciação e elétrons de valência O elétron de diferenciação é definido como o último elétron do subnível mais energético de um
Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron:
 Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
Química. Resolução das atividades complementares. Q49 Polaridade das moléculas
 Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
Escola Básica da Gafanha da Encarnação Físico-Química 8º ano Ficha de trabalho 2014/2015 Nome N.º Turma Data: Enc. Educação Professora
 Escola Básica da Gafanha da Encarnação Físico-Química 8º ano Ficha de trabalho 2014/2015 Nome N.º Turma Data: Enc. Educação Professora 1. A Maria adicionou uma colher de chocolate em pó a um copo com Leite
Escola Básica da Gafanha da Encarnação Físico-Química 8º ano Ficha de trabalho 2014/2015 Nome N.º Turma Data: Enc. Educação Professora 1. A Maria adicionou uma colher de chocolate em pó a um copo com Leite
IBM1018 Física Básica II FFCLRP USP Prof. Antônio Roque Aula 3
 Linhas de Força Mencionamos na aula passada que o físico inglês Michael Faraday (79-867) introduziu o conceito de linha de força para visualizar a interação elétrica entre duas cargas. Para Faraday, as
Linhas de Força Mencionamos na aula passada que o físico inglês Michael Faraday (79-867) introduziu o conceito de linha de força para visualizar a interação elétrica entre duas cargas. Para Faraday, as
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
Apresentar, através da configuração eletrônica, propriedades físicas e químicas dos elementos químicos.
 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS (I) META Apresentar, através da configuração eletrônica, propriedades físicas e químicas dos elementos químicos. OBJETIVOS Ao final desta aula, o aluno deverá: reconhecer
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS (I) META Apresentar, através da configuração eletrônica, propriedades físicas e químicas dos elementos químicos. OBJETIVOS Ao final desta aula, o aluno deverá: reconhecer
- LIGAÇÕES IÔNICAS: Na (1s 2 2s 2 2p 6 3s 1 ) + Cl (1s 2 2s 2 2p 6 3s 2 3p 5 ) Na + (1s 2 2s 2 2p 6 ) + Cl - (1s 2 2s 2 2p 6 3s 2 3p 6 )
 - LIGAÇÕES IÔNICAS: A ligação iônica é a ligação química formada pela atração eletrostática entre íons positivos e íons negativos. A ligação se dá entre dois átomos quando um elétron, ou mais um, se transfere
- LIGAÇÕES IÔNICAS: A ligação iônica é a ligação química formada pela atração eletrostática entre íons positivos e íons negativos. A ligação se dá entre dois átomos quando um elétron, ou mais um, se transfere
O carbono é um dos elementos químicos com capacidade de formar cadeias, ligando-se entre si e com outros elementos químicos.
 ITS Química do Petróleo 3 Módulo: Prof.ª Mônica Fonseca Química Orgânica: É a parte da Química que estuda os compostos do carbono. Compostos orgânicos naturais: as principais fontes de compostos orgânicos
ITS Química do Petróleo 3 Módulo: Prof.ª Mônica Fonseca Química Orgânica: É a parte da Química que estuda os compostos do carbono. Compostos orgânicos naturais: as principais fontes de compostos orgânicos
Configurações eletrônicas
 Configurações eletrônicas Metais de transição Depois de Ar, os orbitais d começam a ser preenchidos. Depois que os orbitais 3d estiverem preenchidos, os orbitais 4p começam a ser preenchidos. Metais de
Configurações eletrônicas Metais de transição Depois de Ar, os orbitais d começam a ser preenchidos. Depois que os orbitais 3d estiverem preenchidos, os orbitais 4p começam a ser preenchidos. Metais de
Ligações Químicas. Profª. Drª Narlize Silva Lira. Agosto /2014
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Ligações Químicas Profª. Drª Narlize Silva Lira Agosto /2014 A Química Orgânica e a Vida A química orgânica
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Ligações Químicas Profª. Drª Narlize Silva Lira Agosto /2014 A Química Orgânica e a Vida A química orgânica
MATRIZ DE EXAME DE QUÍMICA
 MATRIZ DE EXAME DE QUÍMICA Módulo Q1 Estrutura Atómica. Tabela Periódica. Ligação Química Formação: Científica Duração: 90 minutos Tipo de prova: escrita Ano Letivo 2015 16 1. ESTRUTURA DA PROVA Alguns
MATRIZ DE EXAME DE QUÍMICA Módulo Q1 Estrutura Atómica. Tabela Periódica. Ligação Química Formação: Científica Duração: 90 minutos Tipo de prova: escrita Ano Letivo 2015 16 1. ESTRUTURA DA PROVA Alguns
Capítulo LIGAÇÕES QUÍMICAS
 Capítulo LIGAÇÕES QUÍMICAS Um dos aspectos mais intrigantes da química é o estudo das forças que agem entre os átomos. Às mais fortes destas forças, denominadas ligações químicas, são forças que unem átomos
Capítulo LIGAÇÕES QUÍMICAS Um dos aspectos mais intrigantes da química é o estudo das forças que agem entre os átomos. Às mais fortes destas forças, denominadas ligações químicas, são forças que unem átomos
LIGAÇÕES QUÍMICAS. Prof a. Dr a. Carolina Fortes Rigos
 LIGAÇÕES QUÍMICAS Prof a. Dr a. Carolina Fortes Rigos INTRODUÇÃO O QUE DETERMINA O TIPO DE LIGAÇÃO EM CADA SUBSTÂNCIA E SUAS DIFERENTES PROPRIEDADES FÍSICAS E QUÍMICAS? ESTRUTURA ELETRÔNICA FORÇAS DAS
LIGAÇÕES QUÍMICAS Prof a. Dr a. Carolina Fortes Rigos INTRODUÇÃO O QUE DETERMINA O TIPO DE LIGAÇÃO EM CADA SUBSTÂNCIA E SUAS DIFERENTES PROPRIEDADES FÍSICAS E QUÍMICAS? ESTRUTURA ELETRÔNICA FORÇAS DAS
LIGAÇÕES QUÍMICAS. Um novo jeito de se aprender química Helan Carlos e Lenine Mafra- Farmácia- 2014.2
 ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
Eletricidade Aula 1. Profª Heloise Assis Fazzolari
 Eletricidade Aula 1 Profª Heloise Assis Fazzolari História da Eletricidade Vídeo 2 A eletricidade estática foi descoberta em 600 A.C. com Tales de Mileto através de alguns materiais que eram atraídos entre
Eletricidade Aula 1 Profª Heloise Assis Fazzolari História da Eletricidade Vídeo 2 A eletricidade estática foi descoberta em 600 A.C. com Tales de Mileto através de alguns materiais que eram atraídos entre
AULA 02: TABELA PERIÓDICA
 AULA 02: TABELA PERIÓDICA 1. INTRODUÇÃO A Tabela Periódica é, efetivamente, um instrumento organizador de conhecimentos sobre os elementos químicos, onde estes estão ordenados por ordem crescente de número
AULA 02: TABELA PERIÓDICA 1. INTRODUÇÃO A Tabela Periódica é, efetivamente, um instrumento organizador de conhecimentos sobre os elementos químicos, onde estes estão ordenados por ordem crescente de número
ESCOLA SECUNDÁRIA FERREIRA DIAS, AGUALVA - SINTRA
 ESCOLA SECUNDÁRIA FERREIRA DIAS, AGUALVA - SINTRA CURSOS PROFISSIONAIS Disciplina: FÍSICA E QUÍMICA Módulo (*) : Q1 Estrutura Atómica. Tabela Periódica. Ligação Química (*) e extensão do módulo, se aplicável.
ESCOLA SECUNDÁRIA FERREIRA DIAS, AGUALVA - SINTRA CURSOS PROFISSIONAIS Disciplina: FÍSICA E QUÍMICA Módulo (*) : Q1 Estrutura Atómica. Tabela Periódica. Ligação Química (*) e extensão do módulo, se aplicável.
Prova de Química Resolvida Segunda Etapa Vestibular UFMG 2011 Professor Rondinelle Gomes Pereira
 QUESTÃO 01 Neste quadro, apresentam-se as concentrações aproximadas dos íons mais abundantes em uma amostra de água típica dos oceanos e em uma amostra de água do Mar Morto: 1. Assinalando com um X a quadrícula
QUESTÃO 01 Neste quadro, apresentam-se as concentrações aproximadas dos íons mais abundantes em uma amostra de água típica dos oceanos e em uma amostra de água do Mar Morto: 1. Assinalando com um X a quadrícula
Elementos do bloco p
 Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Química Inorgânica II Professor: Eduardo Cassús
 Química Inorgânica II Professor: Eduardo Cassús Teoria do Orbital Molecular A Teoria do Orbital Molecular usa os métodos da teoria de grupos para descrever a ligação química em moléculas. A simetria e
Química Inorgânica II Professor: Eduardo Cassús Teoria do Orbital Molecular A Teoria do Orbital Molecular usa os métodos da teoria de grupos para descrever a ligação química em moléculas. A simetria e
ESTRUTURAS CRISTALINAS - TEORIA
 ESTRUTURAS CRISTALINAS - TEORIA Introdução Sólidos são compostos que apresentam uma alta regularidade estrutural. Com exceção dos sólidos amorfos, nos quais essa regularidade só existe em um curto espaço,
ESTRUTURAS CRISTALINAS - TEORIA Introdução Sólidos são compostos que apresentam uma alta regularidade estrutural. Com exceção dos sólidos amorfos, nos quais essa regularidade só existe em um curto espaço,
Problemas de Termodinâmica e Estrutura da Matéria
 Problemas de Termodinâmica e Estrutura da Matéria 5 a série 5.1) O filamento de tungsténio de uma lâmpada incandescente está à temperatura de 800 C. Determine o comprimento de onda da radiação emitida
Problemas de Termodinâmica e Estrutura da Matéria 5 a série 5.1) O filamento de tungsténio de uma lâmpada incandescente está à temperatura de 800 C. Determine o comprimento de onda da radiação emitida
Ensino Médio Unidade Parque Atheneu. Professor (a): Me. DIOGO LOPES Aluno (a): Série: 3ª Data: / / 2015. LISTA DE QUÍMICA I
 Ensino Médio Unidade Parque Atheneu Professor (a): Me. DIOGO LOPES Aluno (a): Série: 3ª Data: / / 2015. LISTA DE QUÍMICA I OBS: Sua lista semanal deverá ser respondida em folha de papel almaço, copiando
Ensino Médio Unidade Parque Atheneu Professor (a): Me. DIOGO LOPES Aluno (a): Série: 3ª Data: / / 2015. LISTA DE QUÍMICA I OBS: Sua lista semanal deverá ser respondida em folha de papel almaço, copiando
Departamento de Química ICEx UFMG Exercícios de Fixação LIGAÇÃO COVALENTE
 Departamento de Química ICEx UFMG Exercícios de Fixação LIGAÇÃO COVALENTE Questão 1 Considerando os íons NO 2+ e NO 2-, faça o que se pede: a. Represente cada um dos íons através de um número adequado
Departamento de Química ICEx UFMG Exercícios de Fixação LIGAÇÃO COVALENTE Questão 1 Considerando os íons NO 2+ e NO 2-, faça o que se pede: a. Represente cada um dos íons através de um número adequado
Teoria Ácido-Base e Reações Químicas
 Aula ao Vivo Teoria Ácido-Base e Reações Químicas Química Allan Rodrigues 27.04.2015 Existem várias teorias sobre ácidos e bases. Dentre elas, temos a teoria do químico sueco Svante August Arrhenius, que
Aula ao Vivo Teoria Ácido-Base e Reações Químicas Química Allan Rodrigues 27.04.2015 Existem várias teorias sobre ácidos e bases. Dentre elas, temos a teoria do químico sueco Svante August Arrhenius, que
Introdução à Eletricidade e Lei de Coulomb
 Introdução à Eletricidade e Lei de Coulomb Introdução à Eletricidade Eletricidade é uma palavra derivada do grego élektron, que significa âmbar. Resina vegetal fossilizada Ao ser atritado com um pedaço
Introdução à Eletricidade e Lei de Coulomb Introdução à Eletricidade Eletricidade é uma palavra derivada do grego élektron, que significa âmbar. Resina vegetal fossilizada Ao ser atritado com um pedaço
ANO LETIVO 2013/2014 PROVAS DE ACESSO AO ENSINO SUPERIOR PARA CANDIDATOS MAIORES DE 23 ANOS EXAME DE QUÍMICA CONTEÚDOS PROGRAMÁTICOS
 ANO LETIVO 2013/2014 PROVAS DE ACESSO AO ENSINO SUPERIOR PARA CANDIDATOS MAIORES DE 23 ANOS EXAME DE QUÍMICA CONTEÚDOS PROGRAMÁTICOS 1. MATERIAIS: DIVERSIDADE E CONSTITUIÇÃO 1.1 Materiais 1.1.1 Materiais
ANO LETIVO 2013/2014 PROVAS DE ACESSO AO ENSINO SUPERIOR PARA CANDIDATOS MAIORES DE 23 ANOS EXAME DE QUÍMICA CONTEÚDOS PROGRAMÁTICOS 1. MATERIAIS: DIVERSIDADE E CONSTITUIÇÃO 1.1 Materiais 1.1.1 Materiais
C mp m o p o Eléctr t ico o Un U i n fo f r o me
 Campo Eléctrico Uniforme Tal como o campo gravítico pode ser considerado uniforme numa estreita região perto da superfície da Terra, também o campo eléctrico pode ser uniforme numa determinada região do
Campo Eléctrico Uniforme Tal como o campo gravítico pode ser considerado uniforme numa estreita região perto da superfície da Terra, também o campo eléctrico pode ser uniforme numa determinada região do
IBM1018 Física Básica II FFCLRP USP Prof. Antônio Roque Aula 6. O trabalho feito pela força para deslocar o corpo de a para b é dado por: = =
 Energia Potencial Elétrica Física I revisitada 1 Seja um corpo de massa m que se move em linha reta sob ação de uma força F que atua ao longo da linha. O trabalho feito pela força para deslocar o corpo
Energia Potencial Elétrica Física I revisitada 1 Seja um corpo de massa m que se move em linha reta sob ação de uma força F que atua ao longo da linha. O trabalho feito pela força para deslocar o corpo
Um capacitor é um sistema elétrico formado por dois condutores separados por um material isolante, ou pelo vácuo.
 Capacitores e Dielétricos Um capacitor é um sistema elétrico formado por dois condutores separados por um material isolante, ou pelo vácuo. Imaginemos uma configuração como a de um capacitor em que os
Capacitores e Dielétricos Um capacitor é um sistema elétrico formado por dois condutores separados por um material isolante, ou pelo vácuo. Imaginemos uma configuração como a de um capacitor em que os
TEORIA DO ORBITAL MOLECULAR
 Teoria do Orbital Molecular - Prof. J. D. Ayala - 1 - TEORIA DO ORBITAL MOLECULAR ORBITAIS NAS MOLÉCULAS A teoria dos orbitais moleculares (MO) constitui uma alternativa para se ter uma visão da ligação.
Teoria do Orbital Molecular - Prof. J. D. Ayala - 1 - TEORIA DO ORBITAL MOLECULAR ORBITAIS NAS MOLÉCULAS A teoria dos orbitais moleculares (MO) constitui uma alternativa para se ter uma visão da ligação.
Módulo: Tabela Periódica Atividade: Estudo da Tabela Periódica e Distribuição Eletrônica de Linus Pauling
 Guia do Professor Módulo: Tabela Periódica Atividade: Estudo da Tabela Periódica e Distribuição Eletrônica de Linus Pauling I Introdução A atividade Distribuição Eletrônica favorece o desenvolvimento de
Guia do Professor Módulo: Tabela Periódica Atividade: Estudo da Tabela Periódica e Distribuição Eletrônica de Linus Pauling I Introdução A atividade Distribuição Eletrônica favorece o desenvolvimento de
Olimpíada Brasileira de Química
 Programa Nacional Olimpíadas de Química SOLUÇÕES ESCOLHIDAS Olimpíada asileira de Química Questão 11 - Resolução apresentada pelo estudante Guilherme Eiichi da Silva - Colégio Objetivo Luís Góes - SP.
Programa Nacional Olimpíadas de Química SOLUÇÕES ESCOLHIDAS Olimpíada asileira de Química Questão 11 - Resolução apresentada pelo estudante Guilherme Eiichi da Silva - Colégio Objetivo Luís Góes - SP.
A) a existência do oceano líquido é uma hipótese possível, pois um sal solúvel só forma uma mistura homogênea com a água, quando ela está líquida.
 TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
UNIDADE 3 - COORDENAÇÃO ATÔMICA
 A força de repulsão entre os elétrons de dois átomos, quando estão suficientemente próximos, é responsável, em conjunto com as forças de atração, pela posição de equilíbrio dos átomos na ligação química
A força de repulsão entre os elétrons de dois átomos, quando estão suficientemente próximos, é responsável, em conjunto com as forças de atração, pela posição de equilíbrio dos átomos na ligação química
Tabel e a l P rió dica
 Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
PROFESSOR LOURIVAL NETO
 QUÍMICA EM 1 DIA PROFESSOR LOURIVAL NETO UBERLÂNDIA LIGAÇÕES QUÍMICAS Iônica: Ocorre devido a transferência de elétrons! Ìons mantêmse em um cristal Retículo cristalino. A força eletrostática mantém os
QUÍMICA EM 1 DIA PROFESSOR LOURIVAL NETO UBERLÂNDIA LIGAÇÕES QUÍMICAS Iônica: Ocorre devido a transferência de elétrons! Ìons mantêmse em um cristal Retículo cristalino. A força eletrostática mantém os
Forças intermoleculares, Disciplina de Química Geral Profa. Marcia Margarete Meier
 , líquidos e sólidos 1 Uma comparação entre líquidos e sólidos As propriedades físicas das substâncias entendidas em termos de teoria cinética molecular : Os gases são altamente compressíveis, assumem
, líquidos e sólidos 1 Uma comparação entre líquidos e sólidos As propriedades físicas das substâncias entendidas em termos de teoria cinética molecular : Os gases são altamente compressíveis, assumem
Adaptado de Professora: Miwa Yoshida. www.colegionobel.com.br/2004quimica1oano/atomo.ppt
 Adaptado de Professora: Miwa Yoshida www.colegionobel.com.br/2004quimica1oano/atomo.ppt Leucipo de Mileto ( 440 a.c.) & Demócrito (460 a.c. - 370 a.c. ) A ideia de dividirmos uma porção qualquer de matéria
Adaptado de Professora: Miwa Yoshida www.colegionobel.com.br/2004quimica1oano/atomo.ppt Leucipo de Mileto ( 440 a.c.) & Demócrito (460 a.c. - 370 a.c. ) A ideia de dividirmos uma porção qualquer de matéria
PRINCÍPIOS DA ESTRUTURA EM SÓLIDOS. QFL-4010 Prof. Gianluca C. Azzellini
 PRINCÍPIOS DA ESTRUTURA EM SÓLIDOS Estrutura dos Sólidos Tipo Exemplo Unidades Natureza Estruturais da ligação Iônico NaCl, CaCl 2 Íons positivos Iônica - Atração e negativos Eletrostática forte Metálico
PRINCÍPIOS DA ESTRUTURA EM SÓLIDOS Estrutura dos Sólidos Tipo Exemplo Unidades Natureza Estruturais da ligação Iônico NaCl, CaCl 2 Íons positivos Iônica - Atração e negativos Eletrostática forte Metálico
Química 1 Química Geral 1
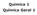 α α = 2 3 2 2 34 2 2 34 56787 977 7 767 34 2 56787 97657 23456789 9 24869 234869 + 567 7657 23456789 24869 24869 2 3 4 35 4 34 + = = Química Geral A Lei Periódica é estabelecida nestes termos: As
α α = 2 3 2 2 34 2 2 34 56787 977 7 767 34 2 56787 97657 23456789 9 24869 234869 + 567 7657 23456789 24869 24869 2 3 4 35 4 34 + = = Química Geral A Lei Periódica é estabelecida nestes termos: As
REFLEXÃO DA LUZ: ESPELHOS 412EE TEORIA
 1 TEORIA 1 DEFININDO ESPELHOS PLANOS Podemos definir espelhos planos como toda superfície plana e polida, portanto, regular, capaz de refletir a luz nela incidente (Figura 1). Figura 1: Reflexão regular
1 TEORIA 1 DEFININDO ESPELHOS PLANOS Podemos definir espelhos planos como toda superfície plana e polida, portanto, regular, capaz de refletir a luz nela incidente (Figura 1). Figura 1: Reflexão regular
Química. Resolução das atividades complementares. Q50 Forças intermoleculares
 Resolução das atividades complementares 4 Química Q50 Forças intermoleculares p. 15 1 (Unifor-CE) Considerando a natureza das ligações químicas intermoleculares existentes nas substâncias: Etanol C 2 H
Resolução das atividades complementares 4 Química Q50 Forças intermoleculares p. 15 1 (Unifor-CE) Considerando a natureza das ligações químicas intermoleculares existentes nas substâncias: Etanol C 2 H
Próton Nêutron Elétron
 Próton Nêutron Elétron Próton Nêutron Elétron Número de prótons: 54 2 Nome do elemento: BORO BERÍLIO HÉLIO Esta Os quantidade diferentes tipos de prótons de átomos recebe (elementos o nome químicos) de
Próton Nêutron Elétron Próton Nêutron Elétron Número de prótons: 54 2 Nome do elemento: BORO BERÍLIO HÉLIO Esta Os quantidade diferentes tipos de prótons de átomos recebe (elementos o nome químicos) de
-2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE
 -2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
-2014- CONTEÚDO SEPARADO POR TRIMESTRE E POR AVALIAÇÃO CIÊNCIAS 9º ANO 1º TRIMESTRE DISCURSIVA OBJETIVA QUÍMICA FÍSICA QUÍMICA FÍSICA Matéria e energia Propriedades da matéria Mudanças de estado físico
As forças atrativas entre duas moléculas são significativas até uma distância de separação d, que chamamos de alcance molecular.
 Tensão Superficial Nos líquidos, as forças intermoleculares atrativas são responsáveis pelos fenômenos de capilaridade. Por exemplo, a subida de água em tubos capilares e a completa umidificação de uma
Tensão Superficial Nos líquidos, as forças intermoleculares atrativas são responsáveis pelos fenômenos de capilaridade. Por exemplo, a subida de água em tubos capilares e a completa umidificação de uma
MANUTENÇÃO ELÉTRICA INDUSTRIAL * ENROLAMENTOS P/ MOTORES CA *
 MANUTENÇÃO ELÉTRICA INDUSTRIAL * ENROLAMENTOS P/ MOTORES CA * Vitória ES 2006 7. ENROLAMENTOS PARA MOTORES DE CORRENTE ALTERNADA A maneira mais conveniente de associar vários condutores de um enrolamento
MANUTENÇÃO ELÉTRICA INDUSTRIAL * ENROLAMENTOS P/ MOTORES CA * Vitória ES 2006 7. ENROLAMENTOS PARA MOTORES DE CORRENTE ALTERNADA A maneira mais conveniente de associar vários condutores de um enrolamento
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL
 RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
3ª Aula Átomos polielectrónicos e Propriedades Periódicas
 QUÍMICA (Eng. Civil+Minas) 2011/12 3ª Aula Átomos polielectrónicos e Propriedades Periódicas Docente: Ana Maria Rego F 2,1 r 1,2 F 1,2 F 2 r 1 F 1 r 2 Para se determinar F 1,2, temos de conhecer a distribuição
QUÍMICA (Eng. Civil+Minas) 2011/12 3ª Aula Átomos polielectrónicos e Propriedades Periódicas Docente: Ana Maria Rego F 2,1 r 1,2 F 1,2 F 2 r 1 F 1 r 2 Para se determinar F 1,2, temos de conhecer a distribuição
Átomos Poli-electrónicos
 Átomos Poli-electrónicos A resolução analítica da equação de Schrödinger para átomos poli-electrónicos é um problema bastante complexo que, só pode ser concretizado mediante algumas aproximações. Em particular,
Átomos Poli-electrónicos A resolução analítica da equação de Schrödinger para átomos poli-electrónicos é um problema bastante complexo que, só pode ser concretizado mediante algumas aproximações. Em particular,
COLÉGIO NOSSA SENHORA DA PIEDADE. Programa de Recuperação Final. 1ª Etapa 2013. Ano: 1
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final 1ª Etapa 2013 Disciplina: Química Professora: Maria Luiza Ano: 1 Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista de
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final 1ª Etapa 2013 Disciplina: Química Professora: Maria Luiza Ano: 1 Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista de
EXAME ENSINO PROFISSIONAL
 AGRUPAMENTO DE ESCOLAS DE OLIVEIRA DE FRADES EXAME ENSINO PROFISSIONAL Disciplina: Física e Química Módulo: Q1 Tipo de Prova: Escrita Duração: 90 minutos Ano letivo: 2012/2013 Conteúdos Objectivos Estrutura
AGRUPAMENTO DE ESCOLAS DE OLIVEIRA DE FRADES EXAME ENSINO PROFISSIONAL Disciplina: Física e Química Módulo: Q1 Tipo de Prova: Escrita Duração: 90 minutos Ano letivo: 2012/2013 Conteúdos Objectivos Estrutura
Módulo III: A visão quantomecânica da ligação covalente
 Módulo III: A visão quantomecânica da ligação covalente Aula 6: Teoria clássica de ligação de valência (TLV clássica) 4. Hibridação de orbitais atômicos Como o átomo de carbono é capaz de formar quatro
Módulo III: A visão quantomecânica da ligação covalente Aula 6: Teoria clássica de ligação de valência (TLV clássica) 4. Hibridação de orbitais atômicos Como o átomo de carbono é capaz de formar quatro
L I G A Ç Õ E S Q U Í M I C A S
 L I G A Ç Õ E S Q U Í M I C A S PR. AGAMENN RBERT < 2010 Prof. Agamenon Roberto LIGAÇÕES QUÍMICAS www.agamenonquimica.com 2 LIGAÇÕES QUÍMICAS 1. INTRDUÇÃ Existe uma grande quantidade de substâncias na
L I G A Ç Õ E S Q U Í M I C A S PR. AGAMENN RBERT < 2010 Prof. Agamenon Roberto LIGAÇÕES QUÍMICAS www.agamenonquimica.com 2 LIGAÇÕES QUÍMICAS 1. INTRDUÇÃ Existe uma grande quantidade de substâncias na
Associe corretamente a coluna da direita à da esquerda.
 1. (G1 - ifba 2014) A respeito da geometria, polaridade e ligações químicas das moléculas dos compostos, previstas por suas estruturas de Lewis, pode-se afirmar corretamente que a) a molécula do PC 3 é
1. (G1 - ifba 2014) A respeito da geometria, polaridade e ligações químicas das moléculas dos compostos, previstas por suas estruturas de Lewis, pode-se afirmar corretamente que a) a molécula do PC 3 é
UNIDADE 4 - ESTRUTURA CRISTALINA
 UNIDADE 4 - ESTRUTURA CRISTALINA 4.1. INTRODUÇÃO Em geral, todos os metais, grande parte dos cerâmicos e certos polímeros cristalizam-se quando se solidificam. Os átomos se arranjam em uma estrutura tridimensional
UNIDADE 4 - ESTRUTURA CRISTALINA 4.1. INTRODUÇÃO Em geral, todos os metais, grande parte dos cerâmicos e certos polímeros cristalizam-se quando se solidificam. Os átomos se arranjam em uma estrutura tridimensional
Química. Resolução das atividades complementares. Q36 Classificação de elementos
 Resolução das atividades complementares 3 Química Q36 Classificação de elementos p. 24 1 (Fatec-SP) Imagine que a tabela periódica seja o mapa de um continente, e que os elementosquímicos constituem as
Resolução das atividades complementares 3 Química Q36 Classificação de elementos p. 24 1 (Fatec-SP) Imagine que a tabela periódica seja o mapa de um continente, e que os elementosquímicos constituem as
IX Olimpíada Catarinense de Química 2013. Etapa I - Colégios
 I Olimpíada Catarinense de Química - 2013 I Olimpíada Catarinense de Química 2013 Etapa I - Colégios Imagem: Oxidação Fonte:Gilson Rocha Reynaldo, 2013 Primeiro Ano Conselho Regional de Química CRQ III
I Olimpíada Catarinense de Química - 2013 I Olimpíada Catarinense de Química 2013 Etapa I - Colégios Imagem: Oxidação Fonte:Gilson Rocha Reynaldo, 2013 Primeiro Ano Conselho Regional de Química CRQ III
Qualidade Ambiental Química
 Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
QUÍMICA. LIGAÇÕES QUÍMICAS -GEOMETRIA e POLARIDADE MOLECULAR - HIBRIDIZAÇÃO - FORÇAS INTERMOLECULARES - PIRES
 QUÍMICA Prof. Daniel Pires LIGAÇÕES QUÍMICAS -GEOMETRIA e POLARIDADE MOLECULAR - HIBRIDIZAÇÃO - FORÇAS INTERMOLECULARES - PIRES 1. Considere as seguintes moléculas: H O; PC؃; BHƒ; SF e CO. a) Indique
QUÍMICA Prof. Daniel Pires LIGAÇÕES QUÍMICAS -GEOMETRIA e POLARIDADE MOLECULAR - HIBRIDIZAÇÃO - FORÇAS INTERMOLECULARES - PIRES 1. Considere as seguintes moléculas: H O; PC؃; BHƒ; SF e CO. a) Indique
CAPACITORES. Vestibular1 A melhor ajuda ao vestibulando na Internet Acesse Agora! www.vestibular1.com.br
 CAPACITORES DEFINIÇÕES Quando as placas do capacitor estão carregadas com cargas iguais e de sinais diferentes, estabelece-se entre as placas uma diferença de potencial V que é proporcional à carga. Q
CAPACITORES DEFINIÇÕES Quando as placas do capacitor estão carregadas com cargas iguais e de sinais diferentes, estabelece-se entre as placas uma diferença de potencial V que é proporcional à carga. Q
