Em maior ou menor extensão, a maioria dos materiais
|
|
|
- Moisés Covalski Prado
- 8 Há anos
- Visualizações:
Transcrição
1 Experimentação no Ensino de Química Experimento sobre a Influência do ph na Corrosão do Ferro Daltamir Justino Maia, Nádia Segre, Andreza Costa Scatigno e Mercia Breda Stella A corrosão é um processo que, na maioria das vezes, degrada os materiais, em especial estruturas metálicas, gerando grande prejuízo. Em ambientes ácidos, que ocorre em grande parte nos ambientes terrestres, esse processo pode tornar-se ainda mais pronunciado. Esse experimento ilustra o quanto o processo de corrosão torna-se mais rápido à medida que o valor de ph diminui, isto é, à medida que o meio torna-se mais ácido. eletroquímica, corrosão, ataque ácido 71 Recebido em 04/09/2013, aceito em 18/05/2014 Em maior ou menor extensão, a maioria dos materiais experimenta algum tipo de interação com um grande número de ambientes diversos (Callister, 2008). Com frequência, tais interações comprometem a utilidade de um material como resultado da deterioração das suas propriedades mecânicas. Esses efeitos devem ser levados em consideração na hora da escolha do material mais adequado para um tipo de projeto a fim de garantir que os componentes não falhem prematuramente (Askeland; Phulé 2008). Em seus projetos, um grande desafio para todos os profissionais que empregam metais além de outros tipos de materiais tais como concretos e plásticos é impedir que estes sofram ataques corrosivos/destrutivos (Shackelford, 2008). Como a prevenção completa é muito difícil, as perdas devem ser minimizadas. Os mecanismos de deterioração são muito diversos para os diferentes tipos de materiais, mas, para os metais, existe uma efetiva perda de material, seja por dissolução (corrosão) ou pela formação de uma incrustação ou película de material não metálico (oxidação). A corrosão pode ser definida como o ataque destrutivo e não intencional sofrido por um metal, que normalmente A seção Experimentação no ensino de Química descreve experimentos cuja implementação e interpretação contribuem para a construção de conceitos científicos por parte dos alunos. Os materiais e reagentes usados são facilmente encontráveis, permitindo a realização dos experimentos em qualquer escola. começa na superfície do material. O problema da corrosão metálica apresenta proporções significativas. Em termos econômicos, foi estimado que aproximadamente 5% da receita de um país industrializado são gastos na prevenção da corrosão e na manutenção ou na substituição de produtos perdidos ou contaminados como resultado das reações de corrosão. Isso sem falar dos acidentes ou perdas de vidas humanas provocadas por contaminações, poluição e falta de segurança dos equipamentos (Merçon et al., 2004). Uma vez que a corrosão é provocada por uma reação química, a velocidade com a qual esta se processa dependerá, até certo ponto, da temperatura e da concentração das espécies envolvidas. Outros fatores, tais como os esforços mecânicos e a erosão, também podem contribuir para a corrosão (Smith, 1998). A maioria dos metais é corroída de algum modo por efeito da água e da atmosfera, portanto, as espécies presentes na água (principalmente espécies iônicas) acabam tendo uma importância muito grande nos processos de deterioração dos metais. Por exemplo, a acidez devido à presença de espécies na água, que pode ser medida por meio dos valores de phs, tem um papel fundamental na corrosão dos metais. Atmosfera oxidativa O ambiente terrestre atual é naturalmente oxidativo
2 72 devido à presença de oxigênio e água (O 2 e O), portanto, espontaneamente, os metais tendem a sofrer oxidação quando em contato com essas substâncias. Além disso, à medida que substâncias ácidas estão presentes na água, a velocidade de oxidação dos metais tende a aumentar. A chuva é normalmente ácida (valores de ph menor que 7) devido à presença de ácido carbônico (formado pela reação entre o gás carbônico e a água: CO 2 + O CO 3 ). Quando a água está saturada de gás carbônico, o valor de ph fica em torno de 5,6. Portanto, até valor de,6, não usamos o termo chuva ácida para esse tipo de precipitação (Maia et al., 2005). No entanto, a presença de poluentes tais como óxidos de enxofre (SO 2 e SO 3 ) e de nitrogênio (N 2 O, NO e NO 2 ), presentes na atmosfera, principalmente em atmosferas poluídas, forma ácidos, aumentando a acidez da chuva. Existem registros de chuvas com valor de ph em torno de 2,0, lembrando que a escala de ph é logarítmica, isto é, para cada unidade de ph, temos uma variação de 10 unidades na concentração de H +. Isso significa que, de 5,6 para 2, temos um aumento de quase vezes na concentração de H + (Maia et al., 2005). Considerações eletroquímicas Para os materiais metálicos, o processo de corrosão é normalmente um processo eletroquímico, isto é, uma reação química em que existe uma transferência de elétrons de uma espécie química para outra (processo denominado de oxidorredução). Caracteristicamente, os átomos metálicos têm seus elétrons retirados, no que é chamada uma reação de oxidação. A quantidade de elétrons retirada de um determinado metal é uma característica dele e pode variar de um metal para outro. Por exemplo, para a prata, o ferro e o alumínio, podemos ter os seguintes processos de oxidação: Ag Ag + + 1e - Fe Fe e - Al Al e - As espécies que retiram os elétrons do metal sofrem um processo denominado de redução. Essas espécies, ao retirarem elétrons e provocarem a oxidação de outras, são denominadas de agentes oxidantes. O ar atmosférico, devido à presença de gás oxigênio (compõe 20% do ar seco) e água (presente na forma de vapor), é um ambiente propício à oxidação. Por exemplo, ligas de aço, cujo principal metal constituinte é o ferro, quando expostas ao oxigênio e à água (O 2 e O), sofrem corrosão com o passar do tempo e formam a ferrugem, que é uma mistura de óxidos e hidróxidos de ferro hidratados. Dependendo do valor de ph e das concentrações de gás oxigênio e água, essa mistura tem proporções diferentes, principalmente, das seguintes espécies: Fe 3 /Fe 2 O 3. O/Fe(OH) 2 /Fe(OH) 3. Quanto maior o teor de Fe 3 (preto), mais percebemos que o objeto em questão está sofrendo corrosão. Quanto mais Fe 2 O 3. O, maior a intensidade da coloração alaranjada ou castanho avermelhada. O Fe(OH) 2 puro é branco, mas em contato com oxigênio, torna-se verde. O Fe(OH) 3 puro é marrom. Portanto, dependendo da predominância de cada uma dessas espécies, temos uma tonalidade mais pronunciada do produto da corrosão. O ambiente ácido acelera o processo de oxidação Quanto mais ácido o ambiente (maior concentração de íons H + ), maior a velocidade de oxidação das estruturas metálicas. Em um ambiente ácido, o processo predominante de oxidação pode ser representado da seguinte maneira: Redução do O 2 por ação dos íons hidrogênio: O H + + 4e - 2 O Oxidação dos íons metálicos: Fe Fe e - Quanto mais ácido um meio, maior a diferença entre a concentração de íons H + em relação aos íons OH - (meio ácido: [H + ] > [OH - ]). Nesse caso, o produto formado será preferencialmente óxido de ferro (Fe 3 coloração preta). Efeito do ph O efeito da acidez na velocidade de corrosão do ferro, em água aerada e em temperatura ambiente, pode ser verificado na Figura 1 (Gentil 2011). Figura 1: Correlação entre o ph e a taxa de corrosão do ferro (Gentil, 2011). Verifica-se uma interferência cada vez mais positiva (aumento da corrosão) quando temos valores de phs abaixo de 4. Para valores de phs entre 4 e 10, a taxa de corrosão independe do ph e depende somente da rapidez com que o oxigênio difunde para a superfície metálica. Quando os valores de phs são maiores que 10, esse aumento mais pronunciado da alcalinidade do meio faz com que a taxa de corrosão diminua, pois o ferro se torna passivo em presença de álcalis e oxigênio dissolvido.
3 Experimento Reagentes e materiais 100 ml de ácido clorídrico (HCl) 0,1 mol L -1 (pode ser encontrado na forma concentrada em lojas de construção como ácido muriático); 100 ml de ácido nítrico (HNO 3 ) 0,1 mol L -1 ; 1 pacote de esponja de aço; água destilada; 14 balões volumétricos de 100 ml; béqueres; balança; pipeta graduada (10 ml); pisseta; proveta (100 ml); pera de borracha; bomba de aspergir. Preparo das soluções de HCl e HNO 3 A partir da solução 0,1 mol L -1 () de ácido clorídrico, por meio de diluições sucessivas, foram preparadas soluções com valores de, 3, 4, 5, 6 e 7. O mesmo procedimento foi feito na preparação das soluções de ácido nítrico. A partir da solução estoque desse ácido (0,1 mol L -1 ), prepararam-se as outras soluções com valores de, 3, 4, 5, 6 e 7. Procedimento Pesar 14 amostras de esponjas de aço. Se possível, ajustar para que elas tenham aproximadamente a mesma massa para melhor comparação cada esponja pode ser cortada em dois pedaços. Colocar cada esponja sobre um anteparo (placa de petri ou similar). Colocar a solução de ácido clorídrico () na bomba de aspergir, regular a saída e borrifar 10 vezes sobre a esponja. Lavar a bomba de aspergir e repetir o procedimento para cada uma das outras soluções (, 3, 4, 5, 6 e 7). Repetir o mesmo procedimento utilizando as soluções de ácido nítrico. Deixe as 14 amostras em repouso durante 24 horas. Esse período assegura que a esponja fique completamente seca, garantindo que o aumento de massa é devido basicamente ao processo de oxidação. Depois, verifique visualmente o que ocorreu com cada uma das amostras e pese cada uma comparando com a massa inicial. O ácido pode ser descartado na pia, desde que esteja diluído ou neutralizado. Resultados Após um dia de oxidação (24 horas), podemos verificar visualmente que o processo oxidativo é mais eficaz quando os valores de ph estão abaixo de 4 (meios mais ácidos): maior taxa de corrosão tanto para as amostras em contato com soluções de ácido clorídrico quanto nas amostras em contato com soluções de ácido nítrico. As Figuras 2 e 3 ilustram as amostras de esponjas de aço oxidadas. Nos dois casos, as corrosões em soluções com valores de ph 3 foram mais intensas, enquanto em valores de, 5, 6 e 7, a diferença não foi tão evidente (praticamente constante). Visualmente já é possível observar que o processo oxidativo é bem mais intenso nas amostras com valores de ph =1, de maior acidez, tanto para o ácido clorídrico quanto para o ácido nítrico. Isso indica que o maior efeito oxidativo ocorre pela presença dos Figura 2: Amostras de esponja de aço após um dia de oxidação frente às soluções de ácido clorídrico. I) solução 1,0 x 10-1 mol L -1 (); II) solução 1,0 x 10-2 mol L -1 (); III) solução 1,0 x 10-3 mol L -1 (); IV) solução 1,0 x 10-4 mol L -1 (); V) solução 1,0 x 10-5 mol L -1 (); solução 1,0 x 10-6 mol L -1 (); solução 1,0 x 10-7 mol L -1 (). Figura 3: Amostras de esponja de aço após um dia de oxidação frente às soluções de ácido nítrico. I) solução 1,0 x 10-1 mol L -1 (); II) solução 1,0 x 10-2 mol L -1 (); III) solução 1,0 x 10-3 mol L -1 (); IV) solução 1,0 x 10-4 mol L -1 (); V) solução 1,0 x 10-5 mol L -1 (); solução 1,0 x 10-6 mol L -1 (); solução 1,0 x 10-7 mol L -1 (). 73
4 Tabela 1: Massas das esponjas de aço antes e após um dia de oxidação frente às soluções de ácido clorídrico. I I Massa inicial (g) 3,858 3,915 3,608 3,438 3,391 3,313 3,458 Massa final (g) 4,076 4,102 3,675 3,450 3,397 3,317 3,464 Aumento de massa (g) 0,218 0,187 0,067 0,012 0,006 0,004 0,006 % do aumento de massa 5,35% 4,56% 1,82% 0,35% 0,18% 0,12% 0,17% Tabela 2: Massas das esponjas de aço antes e após um dia de oxidação frente às soluções de ácido nítrico. I I Massa inicial (g) 3,921 3,714 3,740 3,140 3,679 3,695 3,543 Massa final (g) 4,102 3,852 3,783 3,147 3,684 3,697 3,549 Aumento de massa (g) 0,181 0,138 0,043 0,007 0,005 0,002 0,006 % do aumento de massa 4,41% 3,58% 1,14% 0,22% 0,14% 0,05% 0,17% 74 íons H + independente do ácido utilizado. Em soluções com elevada concentração de íons H + (valores de ph abaixo de 4), ocorre redução destes (2H + + 2e - ) e consequente oxidação do ferro (Callister, 2008). No entanto, quando as soluções são menos concentradas e com a presença de oxigênio, ocorre preferencialmente o seguinte processo redutivo: O 2 + 4H + + 4e - 2 O. A velocidade de corrosão diminui entre valores de phs 4 e 7, pois esta depende somente da rapidez com que o oxigênio difunde para a superfície metálica. As Tabelas 1 e 2 apresentam as massas das esponjas antes e depois de um dia de oxidação, a variação de massa ocorrida e a porcentagem de aumento de massa. O aumento de massa é devido à ferrugem que se forma, principalmente na forma de hidróxido de ferro III Fe(OH) 3, pois a cor predominante, conforme pode ser visto pelas Figuras 2 e 3, é amarronzada. O maior aumento de massa, à medida que o valor de ph diminui, é reflexo da maior taxa de corrosão da esponja de aço. Esse aumento é mais pronunciado à medida que o meio torna-se mais ácido. Utilizando os valores de porcentagem do aumento de massa em função do valor de ph, podemos construir um gráfico similar ao da Figura 1, tanto para o HCl quanto para o HNO 3, e comprovar a dependência da corrosão com a concentração de H +. Esses resultados estão presentes no Gráfico 1. O aumento na massa das amostras não fere a Lei de Conservação das Massas (Lavoisier), pois esse aumento é em decorrência da incorporação de hidrogênio e oxigênio na amostra por meio do processo de oxidação. Podemos calcular Gráfico 1: Correlação entre o ph e a corrosão (porcentagem no aumento de massa) do ferro em soluções aquosas de HCl e de HNO 3. a quantidade de ferro que sofreu oxidação, considerando que todo aumento de massa foi em decorrência da reação: Nesse caso, as esponjas ficaram preferencialmente na cor marrom. Para cada aumento de massa de 51 g, ocorre a oxidação de 56 g de ferro (1 mol). Desse modo, podemos determinar a quantidade de matéria que oxidou em cada amostra. As Tabelas 3 e 4 apresentam os valores de massa para cada amostra analisada. Tabela 3: Massa e quantidade de matéria de ferro que sofreu oxidação após um dia de contato com soluções de ácido clorídrico. I I Aumento de massa (g) 0,218 0,187 0,067 0,012 0,006 0,004 0,006 Massa de ferro que oxidou (g) 0,239 0,205 0,074 0,013 0,007 0,004 0,007 Quantidade de matéria (mol) 4,27 x ,66 x ,32 x ,32 x ,25 x ,14 x ,25 x 10-4
5 Tabela 4: Massa e quantidade de matéria de ferro que sofreu oxidação após um dia de contato com soluções de ácido nítrico. I I Aumento de massa (g) 0,181 0,138 0,043 0,007 0,005 0,002 0,006 Massa de ferro que oxidou (g) 0,199 0,152 0,047 0,008 0,005 0,002 0,007 Quantidade de matéria (mol) 3,55 x ,71 x ,39 x ,4 x ,93 x ,57 x ,25 x 10-4 Conclusões O experimento comprova o aumento da taxa de corrosão em materiais ferrosos em soluções cada vez mais ácidas, principalmente quando os valores de phs tornam-se menores que 4. Isso explica porque os problemas de corrosão de estruturas metálicas em aço tendem a ser mais intensos em algumas regiões mais industrializadas e poluídas (devido à formação da chuva ácida). A porcentagem e o comportamento do metal frente à corrosão é praticamente a mesma, independente do tipo de ácido, comprovando que o mais importante no aumento da corrosão é a concentração de íons H + no meio. Esse experimento, simples de ser realizado com materiais de fácil acesso e descarte, demonstra a influência da acidez na corrosão de um material metálico, podendo auxiliar no aprendizado dos conceitos de oxidorredução. Os alunos podem também correlacionar a problemática da corrosão e a influência do meio ambiente (poluição) nesse processo, principalmente no que diz respeito à chuva ácida. Também é possível trabalhar os conceitos da Lei de Conservação das Massas de Lavoisier com essas amostras e chamar a atenção para o aumento de massa nas esponjas, que foi em decorrência da incorporação de hidrogênio e oxigênio na formação da ferrugem. Daltamir Justino Maia (daltamir.maia@gmail.com), graduado em química pela UNICAMP, mestre e doutor pela UNICAMP, é professor titular no grupo Anhanguera Educacional. Campinas, SP BR. Nádia Segre (nsegre@yahoo. com), bacharel em Química pela UNICAMP, mestre em Físico-Química e Doutorado em Ciências pelo Instituto de Química da UNICAMP, é professora titular na Faculdade Anhanguera. Sorocaba, SP BR. Andreza Costa Scatigno (decost@ig.com.br), graduada em Química e em Química Tecnológica pela UNESP-Araraquara, mestre em Biotecnologia pela UNESP-Araraquara, doutora em Ciências pela USP, é pesquisadora e professora do grupo Anhanguera Educacional, da FACENS e do Pitágoras. Sorocaba, SP BR. Mercia Breda Stella (merciabreda@uol.com.br), graduada em biomedicina pela UMC e nutrição pela FESB, mestre em Ciências Bioquímica pelo Instituto de Química USP e Doutora em Bioquímica pelo Instituto de Biologia UNICAMP, é professora titular de Bioquímica e Biofísica da Faculdade Anhanguera de Campinas FAC III e titular e regente de Bioquímica e Biofísica da Faculdade de Medicina de Jundiaí. Campinas, SP BR. 75 Referências ASKELAND, D.R.; PHULÉ, P.P. Ciência e engenharia dos materiais. São Paulo: Cengage Learning, CALLISTER JR., W.D. Fundamentos da ciência e engenharia de materiais. 2. ed. Rio de Janeiro: LTC, GENTIL, V. Corrosão. 6. ed. Rio de Janeiro: LTC, MAIA, D.J.; GAZOTTI, W.A.; CANELA, M.C.; SIQUEIRA, A.E. Chuva ácida: um experimento para introduzir conceitos de equilíbrio químico e acidez no ensino médio. Química Nova na Escola, n. 21, p , MERCON, F.; GUIMARÃES, P.I.C.; MAINER, F.B. Corrosão: um exemplo usual de fenômeno químico. Química Nova na Escola, n. 19, p , SHACKELFORD, J.F. Ciência dos materiais. 6. ed. São Paulo: Pearson, SMITH, W.F. Princípios de ciência e engenharia dos materiais. São Paulo: McGraw-Hill, Para saber mais DUTRA, A.C.; NUNES, L.P. Proteção catódica técnica de combate à corrosão. Rio de Janeiro: Técnica, MAIA, D.J.; BIANCHI, J.C.A. Fundamentos de química. São Paulo: Pearson, Abstract: Experiment about the influence of ph on iron corrosion. Corrosion is a process often responsible for materials degradation, in particular for steel structures, causing significant damages. In acidic environments, which is very common in terrestrial environments, this degradation process can become even more pronounced. The experiment proposed in this work illustrates that the lower the ph the higher the etching process. Keywords: electrochemical, corrosion, acid attack
DATA: 17/11/2015. 2. (ENEM) Discutindo sobre a intensificação do efeito estufa, Francisco Mendonça afirmava:
 EXERCÍCIOS REVISÃO QUÍMICA AMBIENTAL (EFEITO ESTUFA, DESTRUIÇÃO DA CAMADA DE OZÔNIO E CHUVA ÁCIDA) e EQUILÍBRIO QUÍMICO DATA: 17/11/2015 PROF. ANA 1. Na década de 70, alguns cientistas descobriram quais
EXERCÍCIOS REVISÃO QUÍMICA AMBIENTAL (EFEITO ESTUFA, DESTRUIÇÃO DA CAMADA DE OZÔNIO E CHUVA ÁCIDA) e EQUILÍBRIO QUÍMICO DATA: 17/11/2015 PROF. ANA 1. Na década de 70, alguns cientistas descobriram quais
Introdução. Princípios da corrosão: reações de oxiredução potencial de eletrodo - sistema redox em equilíbrio - Diagrama de Pourbaix
 Introdução Princípios da corrosão: reações de oxiredução potencial de eletrodo - sistema redox em equilíbrio - Diagrama de Pourbaix Introdução Conceitos de oxidação e redução 1 - Ganho ou perda de oxigênio
Introdução Princípios da corrosão: reações de oxiredução potencial de eletrodo - sistema redox em equilíbrio - Diagrama de Pourbaix Introdução Conceitos de oxidação e redução 1 - Ganho ou perda de oxigênio
PROVA DE QUÍMICA - 1998 Segunda Etapa
 PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
Química Analítica Avançada: Volumetria de Neutralização. Prof a Lilian Silva 2011
 Química Analítica Avançada: Volumetria de Neutralização Prof a Lilian Silva 2011 INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução
Química Analítica Avançada: Volumetria de Neutralização Prof a Lilian Silva 2011 INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução
Leis Históricas da Estequiometria
 Estequiometria A proporção correta da mistura ar-combustível para o motor de uma carro de corrida pode ser tão importante quanto a habilidade do piloto para ganhar a corrida. As substâncias químicas, como
Estequiometria A proporção correta da mistura ar-combustível para o motor de uma carro de corrida pode ser tão importante quanto a habilidade do piloto para ganhar a corrida. As substâncias químicas, como
Química Geral I. Experimento 3 Tendências Periódicas
 Universidade Estadual do Norte Fluminense Centro de Ciência e Tecnologia Laboratório de Ciências Químicas Química Geral I Experimento 3 Tendências Periódicas 1 - OBJETIVOS Relacionar a reatividade química
Universidade Estadual do Norte Fluminense Centro de Ciência e Tecnologia Laboratório de Ciências Químicas Química Geral I Experimento 3 Tendências Periódicas 1 - OBJETIVOS Relacionar a reatividade química
Materiais / Materiais I
 Materiais / Materiais I Guia para o Trabalho Laboratorial n.º 4 CORROSÃO GALVÂNICA E PROTECÇÃO 1. Introdução A corrosão de um material corresponde à sua destruição ou deterioração por ataque químico em
Materiais / Materiais I Guia para o Trabalho Laboratorial n.º 4 CORROSÃO GALVÂNICA E PROTECÇÃO 1. Introdução A corrosão de um material corresponde à sua destruição ou deterioração por ataque químico em
a) Qual a configuração eletrônica do cátion do alumínio isoeletrônico ao gás nobre neônio?
 Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Leis Ponderais e Cálculo Estequiométrico
 Leis Ponderais e Cálculo Estequiométrico 1. (UFF 2009) Desde a Antiguidade, diversos povos obtiveram metais, vidro, tecidos, bebidas alcoólicas, sabões, perfumes, ligas metálicas, descobriram elementos
Leis Ponderais e Cálculo Estequiométrico 1. (UFF 2009) Desde a Antiguidade, diversos povos obtiveram metais, vidro, tecidos, bebidas alcoólicas, sabões, perfumes, ligas metálicas, descobriram elementos
O Conceito de Corrosão Engenharia SACOR, setembro/1999
 O Conceito de Corrosão Engenharia SACOR, setembro/1999 A corrosão é a deterioração de metais e ligas por ação química do meio ambiente. Sendo este meio a água do mar ou o solo, metais e ligas que nele
O Conceito de Corrosão Engenharia SACOR, setembro/1999 A corrosão é a deterioração de metais e ligas por ação química do meio ambiente. Sendo este meio a água do mar ou o solo, metais e ligas que nele
Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal FCAV - UNESP. CURSO: Agronomia. DISCIPLINA: Química Geral
 Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal FCAV - UNESP CURSO: Agronomia DISCIPLINA: Química Geral ASSUNTO: Soluções e Unidades de Concentração 1 1. TIPOS MAIS COMUNS DE SOLUÇÃO Solução
Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal FCAV - UNESP CURSO: Agronomia DISCIPLINA: Química Geral ASSUNTO: Soluções e Unidades de Concentração 1 1. TIPOS MAIS COMUNS DE SOLUÇÃO Solução
TRATAMENTO DA ÁGUA. Professora: Raquel Malta Química 3ª série - Ensino Médio
 TRATAMENTO DA ÁGUA Professora: Raquel Malta Química 3ª série - Ensino Médio Água poluída: água inadequada para beber ou para fazer nossa higiene. Diversas substâncias naturalmente presentes na água são
TRATAMENTO DA ÁGUA Professora: Raquel Malta Química 3ª série - Ensino Médio Água poluída: água inadequada para beber ou para fazer nossa higiene. Diversas substâncias naturalmente presentes na água são
P2 - PROVA DE QUÍMICA GERAL - 11/10/08
 P2 - PROVA DE QUÍMICA GERAL - 11/10/08 Nome: Gabarito Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Constantes: R 8,314 J mol -1 K -1 0,0821
P2 - PROVA DE QUÍMICA GERAL - 11/10/08 Nome: Gabarito Nº de Matrícula: Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 Constantes: R 8,314 J mol -1 K -1 0,0821
PROCESSO SELETIVO 2006 QUESTÕES OBJETIVAS
 3 PROCESSO SELETIVO 2006 QUESTÕES OBJETIVAS QUÍMICA 01 - O dispositivo de segurança que conhecemos como air-bag utiliza como principal reagente para fornecer o gás N 2 (massa molar igual a 28 g mol -1
3 PROCESSO SELETIVO 2006 QUESTÕES OBJETIVAS QUÍMICA 01 - O dispositivo de segurança que conhecemos como air-bag utiliza como principal reagente para fornecer o gás N 2 (massa molar igual a 28 g mol -1
QUESTÕES DE CARACTERIZAÇÃO E ANÁLISE AMBIENTAL. O 2(g) O 2(aq)
 QUESTÕES DE CARACTERIZAÇÃO E ANÁLISE AMBIENTAL Questão 01 O agente oxidante mais importante em águas naturais é, sem a menor dúvida, o oxigênio molecular dissolvido, O 2. O equilíbrio entre o oxigênio
QUESTÕES DE CARACTERIZAÇÃO E ANÁLISE AMBIENTAL Questão 01 O agente oxidante mais importante em águas naturais é, sem a menor dúvida, o oxigênio molecular dissolvido, O 2. O equilíbrio entre o oxigênio
MANUSEIO DE ÓLEO DIESEL B ORIENTAÇÕES E PROCEDIMENTOS
 MANUSEIO E ARMAZENAMENTO DE ÓLEO DIESEL B ORIENTAÇÕES E PROCEDIMENTOS Com a criação do Programa Nacional de Produção e Uso de Biodiesel, em 2004, e a aprovação da Lei 11.097, de 13 de janeiro de 2005,
MANUSEIO E ARMAZENAMENTO DE ÓLEO DIESEL B ORIENTAÇÕES E PROCEDIMENTOS Com a criação do Programa Nacional de Produção e Uso de Biodiesel, em 2004, e a aprovação da Lei 11.097, de 13 de janeiro de 2005,
Prof a. Dr a. Luciana M. Saran
 HCl 0,1N FCAV/UNESP CURSO: Agronomia DISCIPLINA: Química Analítica Fundamentos da Análise Titrimétrica (Volumétrica) NaOH 0,1N Prof a. Dr a. Luciana M. Saran Fenolftaleína 1 O QUE É? ANÁLISE TITRIMÉTRICA
HCl 0,1N FCAV/UNESP CURSO: Agronomia DISCIPLINA: Química Analítica Fundamentos da Análise Titrimétrica (Volumétrica) NaOH 0,1N Prof a. Dr a. Luciana M. Saran Fenolftaleína 1 O QUE É? ANÁLISE TITRIMÉTRICA
Preparação e padronização de uma solução 0,10 mol/l de ácido clorídrico
 Universidade Estadual de Goiás UnUCET - Anápolis Química Industrial Química Experimental II Preparação e padronização de uma solução 0,10 mol/l de ácido clorídrico Alunos: Bruno Ramos; Wendel Thiago; Thales
Universidade Estadual de Goiás UnUCET - Anápolis Química Industrial Química Experimental II Preparação e padronização de uma solução 0,10 mol/l de ácido clorídrico Alunos: Bruno Ramos; Wendel Thiago; Thales
MANUSEIO E ARMAZENAMENTO DE ÓLEO DIESEL B ORIENTAÇÕES E PROCEDIMENTOS
 MANUSEIO E ARMAZENAMENTO DE ÓLEO DIESEL B ORIENTAÇÕES E PROCEDIMENTOS Com a criação do Programa Nacional de Produção e Uso de Biodiesel, em 2004, e a aprovação da Lei nº 11.097, de 13 de janeiro de 2005,
MANUSEIO E ARMAZENAMENTO DE ÓLEO DIESEL B ORIENTAÇÕES E PROCEDIMENTOS Com a criação do Programa Nacional de Produção e Uso de Biodiesel, em 2004, e a aprovação da Lei nº 11.097, de 13 de janeiro de 2005,
ANÁLISE DE ALCALINIDADE DAS ÁGUAS SUBTERRÂNEAS DO INSTITUTO FEDERAL CATARINENSE - CAMPUS CAMBORIÚ.
 ANÁLISE DE ALCALINIDADE DAS ÁGUAS SUBTERRÂNEAS DO INSTITUTO FEDERAL CATARINENSE - CAMPUS CAMBORIÚ. Naiane Ramilio 1, Ana Cristina Franzoi TEIXEIRA 2, Adriano MARTENDAL 3 1 Estudante do Curso Técnico em
ANÁLISE DE ALCALINIDADE DAS ÁGUAS SUBTERRÂNEAS DO INSTITUTO FEDERAL CATARINENSE - CAMPUS CAMBORIÚ. Naiane Ramilio 1, Ana Cristina Franzoi TEIXEIRA 2, Adriano MARTENDAL 3 1 Estudante do Curso Técnico em
LIMPEZA E PREPARAÇÃO DE VIDRARIAS PARA ANÁLISE DE COMPOSTOS ORGÂNICOS
 LIMPEZA E PREPARAÇÃO DE VIDRARIAS PARA ANÁLISE DE COMPOSTOS ORGÂNICOS Jéssica Alessandra da Silva Moura, Gilvan Takeshi Yogui Para fins de referência, este documento pode ser citado como: Moura, J.A.S.;
LIMPEZA E PREPARAÇÃO DE VIDRARIAS PARA ANÁLISE DE COMPOSTOS ORGÂNICOS Jéssica Alessandra da Silva Moura, Gilvan Takeshi Yogui Para fins de referência, este documento pode ser citado como: Moura, J.A.S.;
Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B
 Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B Curvas de titulação ² A curva de titulação é a representação gráfica de como
Volumetria ácido-base (continuação) Prof a Alessandra Smaniotto QMC 5325 - Química Analítica - Farmácia Turmas 02102A e 02102B Curvas de titulação ² A curva de titulação é a representação gráfica de como
ELETRODO OU SEMIPILHA:
 ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
ELETROQUÍMICA A eletroquímica estuda a corrente elétrica fornecida por reações espontâneas de oxirredução (pilhas) e as reações não espontâneas que ocorrem quando submetidas a uma corrente elétrica (eletrólise).
MECANISMOS BÁSICOS DE CORROSÃO
 Centro Universitário de Brasília Disciplina: Química Tecnológica Geral Professor: Edil Reis MECANISMOS BÁSICOS DE CORROSÃO No estudo dos processos corrosivos devem ser sempre consideradas as variáveis
Centro Universitário de Brasília Disciplina: Química Tecnológica Geral Professor: Edil Reis MECANISMOS BÁSICOS DE CORROSÃO No estudo dos processos corrosivos devem ser sempre consideradas as variáveis
Pilha de moedas. Introdução. Materiais Necessários
 Intro 01 Introdução A pilha eletroquímica é um sistema constituído por anodo (eletrodo de oxidação), catodo (eletrodo de redução), eletrólito (condutor iônico) e condutor metálico (condutor de corrente
Intro 01 Introdução A pilha eletroquímica é um sistema constituído por anodo (eletrodo de oxidação), catodo (eletrodo de redução), eletrólito (condutor iônico) e condutor metálico (condutor de corrente
Práticas de Físico Química QB75B. Experimento 7
 1 PR UNIVERSIDADE TECNOLÓGICA EDERAL DO PARANÁ MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE TECNOLÓGICA EDERAL DO PARANÁ - UTPR DEPARTAMENTO ACADÊMICO DE QUÍMICA E BIOLOGIA BACHARELADO EM QUÍMICA Práticas de ísico
1 PR UNIVERSIDADE TECNOLÓGICA EDERAL DO PARANÁ MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE TECNOLÓGICA EDERAL DO PARANÁ - UTPR DEPARTAMENTO ACADÊMICO DE QUÍMICA E BIOLOGIA BACHARELADO EM QUÍMICA Práticas de ísico
Orientações e Procedimentos para o Manuseio e Armazenagem de Óleo Diesel B
 Setembro, 2010. Orientações e Procedimentos para o Manuseio e Armazenagem de Óleo Diesel B Com a criação do Programa Nacional de Produção e Uso de Biodiesel, em 2004, e a aprovação da Lei 11.097, de 13
Setembro, 2010. Orientações e Procedimentos para o Manuseio e Armazenagem de Óleo Diesel B Com a criação do Programa Nacional de Produção e Uso de Biodiesel, em 2004, e a aprovação da Lei 11.097, de 13
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA
 SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
MECANISMOS DA CORROSÃO. Professor Ruy Alexandre Generoso
 MECANISMOS DA CORROSÃO Professor Ruy Alexandre Generoso MECANISMOS DA CORROSÃO De acordo com o meio corrosivo e o material, podem ser apresentados diferentes mecanismos. Os principais são: MECANISMO QUÍMICO
MECANISMOS DA CORROSÃO Professor Ruy Alexandre Generoso MECANISMOS DA CORROSÃO De acordo com o meio corrosivo e o material, podem ser apresentados diferentes mecanismos. Os principais são: MECANISMO QUÍMICO
3.1 Determinação do Teor de Ácido Ascórbico e de Ácido Cítrico no
 Capítulo 3 Procedimento Experimental. CAPÍTULO 3 PROCEDIMENTO EXPERIMENTAL Resíduo 3.1 Determinação do Teor de Ácido Ascórbico e de Ácido Cítrico no O primeiro passo foi à preparação das soluções necessárias
Capítulo 3 Procedimento Experimental. CAPÍTULO 3 PROCEDIMENTO EXPERIMENTAL Resíduo 3.1 Determinação do Teor de Ácido Ascórbico e de Ácido Cítrico no O primeiro passo foi à preparação das soluções necessárias
Introdução à Química Inorgânica
 Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
QUÍMICA QUESTÃO 41 QUESTÃO 42
 Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
DURAÇÃO DA PROVA: 03 HORAS
 INSTRUÇÕES: PRCESS SELETIV 2013/2 - CPS PRVA DISCURSIVA DE QUÍMICA CURS DE GRADUAÇÃ EM MEDICINA 1. Só abra a prova quando autorizado. 2. Veja se este caderno contém 5 (cinco) questões discursivas. Caso
INSTRUÇÕES: PRCESS SELETIV 2013/2 - CPS PRVA DISCURSIVA DE QUÍMICA CURS DE GRADUAÇÃ EM MEDICINA 1. Só abra a prova quando autorizado. 2. Veja se este caderno contém 5 (cinco) questões discursivas. Caso
B) (até três pontos) Para os pares de espécies apresentados em i, ii e iii, tem-se, respectivamente, Al +, F - e Li.
 Química 1. O raio atômico (ou iônico) é uma propriedade periódica que exerce grande influência na reatividade dos átomos (ou dos íons). A) Explique, em termos de carga nuclear efetiva, a variação apresentada
Química 1. O raio atômico (ou iônico) é uma propriedade periódica que exerce grande influência na reatividade dos átomos (ou dos íons). A) Explique, em termos de carga nuclear efetiva, a variação apresentada
ipea políticas sociais acompanhamento e análise 7 ago. 2003 117 GASTOS SOCIAIS: FOCALIZAR VERSUS UNIVERSALIZAR José Márcio Camargo*
 GASTOS SOCIAIS: FOCALIZAR VERSUS UNIVERSALIZAR José Márcio Camargo* Como deve ser estruturada a política social de um país? A resposta a essa pergunta independe do grau de desenvolvimento do país, da porcentagem
GASTOS SOCIAIS: FOCALIZAR VERSUS UNIVERSALIZAR José Márcio Camargo* Como deve ser estruturada a política social de um país? A resposta a essa pergunta independe do grau de desenvolvimento do país, da porcentagem
Lista de Exercícios Fundamentos de Análise Volumétrica ALGUNS EXERCÍCIOS SÃO DE AUTORIA PRÓPRIA. OS DEMAIS SÃO ADAPTADOS DE LIVROS CITADOS ABAIXO.
 ALGUNS EXERCÍCIOS SÃO DE AUTORIA PRÓPRIA. OS DEMAIS SÃO ADAPTADOS DE LIVROS CITADOS ABAIXO. 1 Quantos mililitros de ácido nítrico 0,125 M são necessários para titular 1,30 g de hidróxido de bário? MASSAS
ALGUNS EXERCÍCIOS SÃO DE AUTORIA PRÓPRIA. OS DEMAIS SÃO ADAPTADOS DE LIVROS CITADOS ABAIXO. 1 Quantos mililitros de ácido nítrico 0,125 M são necessários para titular 1,30 g de hidróxido de bário? MASSAS
TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS
 TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS 1) Numa célula eletroquímica a solução tem que ser um eletrólito, mas os eletrodos
TESTES REFERENTES A PARTE 1 DA APOSTILA FUNDAMENTOS DA CORROSÃO INDIQUE SE AS AFIRMAÇÕES A SEGUIR ESTÃO CERTAS OU ERRADAS 1) Numa célula eletroquímica a solução tem que ser um eletrólito, mas os eletrodos
MODELO DE RELATÓRIO TÉCNICO 1 INTRODUÇÃO
 MODELO DE RELATÓRIO TÉCNICO 1 INTRODUÇÃO (Parte teórica, relacionada ao estudo em questão) 2 OBJETIVO (Objetivo do trabalho ou do relatório) 3 PROCEDIMENTOS EXPERIMENTAIS 3.1 MATERIAIS (Todos os materiais
MODELO DE RELATÓRIO TÉCNICO 1 INTRODUÇÃO (Parte teórica, relacionada ao estudo em questão) 2 OBJETIVO (Objetivo do trabalho ou do relatório) 3 PROCEDIMENTOS EXPERIMENTAIS 3.1 MATERIAIS (Todos os materiais
UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR
 UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Carbono é um elemento cujos átomos podem se organizar sob a forma de diferentes alótropos. Alótropos H de combustão a 25
UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Carbono é um elemento cujos átomos podem se organizar sob a forma de diferentes alótropos. Alótropos H de combustão a 25
O interesse da Química é analisar as...
 O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014
 RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
UNIVERSIDADE ABERTA DO BRASIL UNIVERSIDADE FEDERAL DA PARAIBA - UFPB VIRTUAL LICENCIATURA EM CIÊNCIAS BIOLÓGICAS A DISTÂNCIA
 UNIVERSIDADE ABERTA DO BRASIL UNIVERSIDADE FEDERAL DA PARAIBA - UFPB VIRTUAL LICENCIATURA EM CIÊNCIAS BIOLÓGICAS A DISTÂNCIA DISCIPLINA BIOQUÍMICA ESTRUTURAL Ministrante: Prof. Dr. Carlos Alberto de Almeida
UNIVERSIDADE ABERTA DO BRASIL UNIVERSIDADE FEDERAL DA PARAIBA - UFPB VIRTUAL LICENCIATURA EM CIÊNCIAS BIOLÓGICAS A DISTÂNCIA DISCIPLINA BIOQUÍMICA ESTRUTURAL Ministrante: Prof. Dr. Carlos Alberto de Almeida
Figura 1: Disponível em: http://3.bp.blogspot.com/-a3v8ofbk0k0/tyxbs6h5l8i/ AAAAAAAAAGo/eEZ-PJDZJlg/s1600/Charge.jpg acesso em 20/10/2014 ás 19:00 h
 TÍTULO: Recarregando a energia MOTIVAÇÃO 1: Figura 1: Disponível em: http://3.bp.blogspot.com/-a3v8ofbk0k0/tyxbs6h5l8i/ AAAAAAAAAGo/eEZ-PJDZJlg/s1600/Charge.jpg acesso em 20/10/2014 ás 19:00 h MOTIVAÇÃO
TÍTULO: Recarregando a energia MOTIVAÇÃO 1: Figura 1: Disponível em: http://3.bp.blogspot.com/-a3v8ofbk0k0/tyxbs6h5l8i/ AAAAAAAAAGo/eEZ-PJDZJlg/s1600/Charge.jpg acesso em 20/10/2014 ás 19:00 h MOTIVAÇÃO
TESTES DE CORROSÃO Domingos J C Spinelli SurTec do Brasil Ltda Abril/2000
 TESTES DE CORROSÃO Domingos J C Spinelli SurTec do Brasil Ltda Abril/2000 1 O Teste de corrosão é a interpretação dos resultados que pode ser um dos mais controvertidos assuntos na indústria de galvanoplastia.
TESTES DE CORROSÃO Domingos J C Spinelli SurTec do Brasil Ltda Abril/2000 1 O Teste de corrosão é a interpretação dos resultados que pode ser um dos mais controvertidos assuntos na indústria de galvanoplastia.
COLÉGIO SANTA TERESINHA R. Madre Beatriz 135 centro Tel. (33) 3341-1244 www.colegiosantateresinha.com.br
 PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
ELETRO FLOCULAÇÃO Um caminho até a purificação 1. Laiza Delfino 2. Larissa Marinho das Neves 2. Sheila Caroline 2. Victor Rodrigues Coelho 2
 ELETRO FLOCULAÇÃO Um caminho até a purificação 1 Laiza Delfino 2 Larissa Marinho das Neves 2 Sheila Caroline 2 Victor Rodrigues Coelho 2 Lucas Antonio Xavier 3 RESUMO A necessidade por água limpa é cada
ELETRO FLOCULAÇÃO Um caminho até a purificação 1 Laiza Delfino 2 Larissa Marinho das Neves 2 Sheila Caroline 2 Victor Rodrigues Coelho 2 Lucas Antonio Xavier 3 RESUMO A necessidade por água limpa é cada
Escola Básica da Gafanha da Encarnação Físico-Química 8º ano Ficha de trabalho 2014/2015 Nome N.º Turma Data: Enc. Educação Professora
 Escola Básica da Gafanha da Encarnação Físico-Química 8º ano Ficha de trabalho 2014/2015 Nome N.º Turma Data: Enc. Educação Professora 1. A Maria adicionou uma colher de chocolate em pó a um copo com Leite
Escola Básica da Gafanha da Encarnação Físico-Química 8º ano Ficha de trabalho 2014/2015 Nome N.º Turma Data: Enc. Educação Professora 1. A Maria adicionou uma colher de chocolate em pó a um copo com Leite
PROCEDIMENTO EXPERIMENTAL A MACROESCALA
 PROCEDIMENTO EXPERIMENTAL A MACROESCALA Parte I Produção do óxido de cobre Ponto de Partida 1- Preparar uma amostra de 300 mg de cobre a partir de um fio de cobre ou de uma folha de cobre. 2- Colocar a
PROCEDIMENTO EXPERIMENTAL A MACROESCALA Parte I Produção do óxido de cobre Ponto de Partida 1- Preparar uma amostra de 300 mg de cobre a partir de um fio de cobre ou de uma folha de cobre. 2- Colocar a
MÉTODO DE ANÁLISE. Emissão inicial: 23.04.2007 Última revisão: 25.07.2012
 Pág.: 1/5 1.0. OBJETIVO Determinar o teor Zinco em Óxido de Zinco, Pó de Zinco, ligas metálicas de Zinco e resíduos de Zinco. 2.0. ABRANGÊNCIA Laboratório de Controle de Qualidade. 3.0 DEFINIÇÕES Não se
Pág.: 1/5 1.0. OBJETIVO Determinar o teor Zinco em Óxido de Zinco, Pó de Zinco, ligas metálicas de Zinco e resíduos de Zinco. 2.0. ABRANGÊNCIA Laboratório de Controle de Qualidade. 3.0 DEFINIÇÕES Não se
1 Introdução. 2 Material
 TUTORIAL Criação de Engrenagens em Acrílico Autor: Luís Fernando Patsko Nível: Intermediário Criação: 18/01/2006 Última versão: 18/12/2006 PdP Pesquisa e Desenvolvimento de Produtos http://www.maxwellbohr.com.br
TUTORIAL Criação de Engrenagens em Acrílico Autor: Luís Fernando Patsko Nível: Intermediário Criação: 18/01/2006 Última versão: 18/12/2006 PdP Pesquisa e Desenvolvimento de Produtos http://www.maxwellbohr.com.br
CONTEÚDOS OBJETIVOS PERÍODO
 ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 8.º ANO DE ESCOLARIDADE
ESCOLA BÁSICA2,3 EUGÉNIO DOS SANTOS 2013 2014 página 1 ESCOLA BÁSICA DO 2.º E 3.º CICLOS EUGÉNIO DOS SANTOS PLANIFICAÇÃO E METAS DE APRENDIZAGEM DA DISCIPLINA DE CIÊNCIAS FÍSICO-QUÍMICAS 8.º ANO DE ESCOLARIDADE
ANO LETIVO 2013/2014 PROVAS DE ACESSO AO ENSINO SUPERIOR PARA CANDIDATOS MAIORES DE 23 ANOS EXAME DE QUÍMICA CONTEÚDOS PROGRAMÁTICOS
 ANO LETIVO 2013/2014 PROVAS DE ACESSO AO ENSINO SUPERIOR PARA CANDIDATOS MAIORES DE 23 ANOS EXAME DE QUÍMICA CONTEÚDOS PROGRAMÁTICOS 1. MATERIAIS: DIVERSIDADE E CONSTITUIÇÃO 1.1 Materiais 1.1.1 Materiais
ANO LETIVO 2013/2014 PROVAS DE ACESSO AO ENSINO SUPERIOR PARA CANDIDATOS MAIORES DE 23 ANOS EXAME DE QUÍMICA CONTEÚDOS PROGRAMÁTICOS 1. MATERIAIS: DIVERSIDADE E CONSTITUIÇÃO 1.1 Materiais 1.1.1 Materiais
Estequiometria. Prof a. Dr a. Flaviana Tavares Vieira
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Estequiometria Prof a. Dr a. Flaviana Tavares Vieira -A palavra estequiometria deriva das palavras
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Estequiometria Prof a. Dr a. Flaviana Tavares Vieira -A palavra estequiometria deriva das palavras
Introduzir o estudo das fórmulas químicas e seus diversos tipos, além de mostrar as fórmulas de determinados compostos.
 INTRODUÇÃO AO ESTUDO DAS FÓRMULAS QUÍMICAS Aula 8 META Introduzir o estudo das fórmulas químicas e seus diversos tipos, além de mostrar as fórmulas de determinados compostos. OBJETIVOS Ao final desta aula,
INTRODUÇÃO AO ESTUDO DAS FÓRMULAS QUÍMICAS Aula 8 META Introduzir o estudo das fórmulas químicas e seus diversos tipos, além de mostrar as fórmulas de determinados compostos. OBJETIVOS Ao final desta aula,
IDENTIFICAÇÃO E CONFIRMAÇÃO DE GRUPOS FUNCIONAIS: Parte 1: ALDEÍDOS E CETONAS
 PRÁTICA N o. 02 IDENTIFICAÇÃO E CONFIRMAÇÃO DE GRUPOS FUNCIONAIS: Parte 1: ALDEÍDOS E CETONAS OBJETIVOS: Esta prática tem como objetivo a identificação e confirmação de grupos funcionais de aldeídos e
PRÁTICA N o. 02 IDENTIFICAÇÃO E CONFIRMAÇÃO DE GRUPOS FUNCIONAIS: Parte 1: ALDEÍDOS E CETONAS OBJETIVOS: Esta prática tem como objetivo a identificação e confirmação de grupos funcionais de aldeídos e
1. DETERMINAÇÃO DE UMIDADE PELO MÉTODO DO AQUECIMENTO DIRETO- TÉCNICA GRAVIMÉTRICA COM EMPREGO DO CALOR
 UNIVERSIDADE DE CUIABÁ - UNIC FACULDADE DE NUTRIÇÃO DISCIPLINA: BROMATOLOGIA 2º/ 4 O PROFA. IVETE ARAKAKI FUJII. DETERMINAÇÃO DE UMIDADE PELO MÉTODO DO AQUECIMENTO DIRETO- TÉCNICA GRAVIMÉTRICA COM EMPREGO
UNIVERSIDADE DE CUIABÁ - UNIC FACULDADE DE NUTRIÇÃO DISCIPLINA: BROMATOLOGIA 2º/ 4 O PROFA. IVETE ARAKAKI FUJII. DETERMINAÇÃO DE UMIDADE PELO MÉTODO DO AQUECIMENTO DIRETO- TÉCNICA GRAVIMÉTRICA COM EMPREGO
3M Proteção Respiratória
 3M Proteção Respiratória Mais segurança. Mais conforto. Mais produtividade. 3Inovação 3M Respiradores de Pressão Positiva Tecnologia traduzida em proteção e conforto que você só conhece depois de experimentar
3M Proteção Respiratória Mais segurança. Mais conforto. Mais produtividade. 3Inovação 3M Respiradores de Pressão Positiva Tecnologia traduzida em proteção e conforto que você só conhece depois de experimentar
Qualidade Ambiental Química
 Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
Experimento. Técnicas de medição de volumes em Laboratório. Prof. Honda Experimento Técnicas de medição de volumes em Laboratório Página 1
 Experimento Técnicas de medição de volumes em Laboratório Objetivo: Conhecer os materiais volumétricos e as técnicas de utilização desses materiais. I. Introdução teórica: Medir volumes de líquidos faz
Experimento Técnicas de medição de volumes em Laboratório Objetivo: Conhecer os materiais volumétricos e as técnicas de utilização desses materiais. I. Introdução teórica: Medir volumes de líquidos faz
Projeto Embuá Unidade de Aprendizagem: ENERGIA
 Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
10/02/2014. O Processo de Dissolução. Solução: é uma mistura homogênea de soluto e solvente. Solvente: Componente cujo estado físico é preservado.
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Solução: é uma mistura homogênea de soluto e solvente. Solvente: Componente cujo estado físico
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Solução: é uma mistura homogênea de soluto e solvente. Solvente: Componente cujo estado físico
http://www.quimica.net/emiliano 1
 Resolução da Prova de Química Vestibular Verão UPF 2004 Professor Emiliano hemello www.quimica.net/emiliano emiliano@quimica.net Questões Resolução: B Resoluções Em 1875, rookes colocou gases muito rarefeitos
Resolução da Prova de Química Vestibular Verão UPF 2004 Professor Emiliano hemello www.quimica.net/emiliano emiliano@quimica.net Questões Resolução: B Resoluções Em 1875, rookes colocou gases muito rarefeitos
CORROSÃO EM ESTRUTURAS DE CONCRETO. Prof. Ruy Alexandre Generoso
 CORROSÃO EM ESTRUTURAS DE CONCRETO Prof. Ruy Alexandre Generoso É um dos materiais mais importantes de engenharia usado em construções. É usado nos mais variados tipos de construções tais como: barragens,
CORROSÃO EM ESTRUTURAS DE CONCRETO Prof. Ruy Alexandre Generoso É um dos materiais mais importantes de engenharia usado em construções. É usado nos mais variados tipos de construções tais como: barragens,
QUÍMICA COMENTÁRIO DA PROVA DE QUÍMICA
 COMENTÁRIO DA PROVA DE QUÍMICA Prova boa, com questões claras e nível superior ao do ano passado. Nota-se, no entanto, a falta de uma revisão criteriosa, feita por algum professor da área, que não tenha
COMENTÁRIO DA PROVA DE QUÍMICA Prova boa, com questões claras e nível superior ao do ano passado. Nota-se, no entanto, a falta de uma revisão criteriosa, feita por algum professor da área, que não tenha
Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza
 Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza 1) a-) Calcular a solubilidade do BaSO 4 em uma solução 0,01 M de Na 2 SO 4 Dissolução do Na 2 SO 4 : Dado: BaSO
Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza 1) a-) Calcular a solubilidade do BaSO 4 em uma solução 0,01 M de Na 2 SO 4 Dissolução do Na 2 SO 4 : Dado: BaSO
química FUVEST ETAPA Resposta QUESTÃO 1 QUESTÃO 2 c) Determine o volume adicionado da solução
 Química QUESTÃO 1 Um recipiente contém 100 ml de uma solução aquosa de H SO 4 de concentração 0,1 mol/l. Duas placas de platina são inseridas na solução e conectadas a um LED (diodo emissor de luz) e a
Química QUESTÃO 1 Um recipiente contém 100 ml de uma solução aquosa de H SO 4 de concentração 0,1 mol/l. Duas placas de platina são inseridas na solução e conectadas a um LED (diodo emissor de luz) e a
Química experimental - Unidade mestra para química geral e eletroquímica - Volume 2 - Físico-química - EQ102A.
 Autores: Luiz Antonio Macedo Ramos e Rosane Bittencourt Wirth. - Revisor: Leandro dos Santos Silveira - Direitos autorais reservados Índice Remissivo... 4 9999.994... 6 Instruções para o professor....6
Autores: Luiz Antonio Macedo Ramos e Rosane Bittencourt Wirth. - Revisor: Leandro dos Santos Silveira - Direitos autorais reservados Índice Remissivo... 4 9999.994... 6 Instruções para o professor....6
MF-613.R-3 - MÉTODO DE DETERMINAÇÃO DE METAIS EM PARTÍCULAS EM SUSPENSÃO NO AR POR ESPECTROMETRIA DE ABSORÇÃO ATÔMICA COM CHAMA.
 MF-613.R-3 - MÉTODO DE DETERMINAÇÃO DE METAIS EM PARTÍCULAS EM SUSPENSÃO NO AR POR ESPECTROMETRIA DE ABSORÇÃO ATÔMICA COM CHAMA. Notas: Aprovado pela Deliberação CECA nº 3.967, de 16 de janeiro de 2001
MF-613.R-3 - MÉTODO DE DETERMINAÇÃO DE METAIS EM PARTÍCULAS EM SUSPENSÃO NO AR POR ESPECTROMETRIA DE ABSORÇÃO ATÔMICA COM CHAMA. Notas: Aprovado pela Deliberação CECA nº 3.967, de 16 de janeiro de 2001
14 COMBUSTÍVEIS E TEMPERATURA DE CHAMA
 14 COMBUSTÍVEIS E TEMPERATURA DE CHAMA O calor gerado pela reação de combustão é muito usado industrialmente. Entre inúmeros empregos podemos citar três aplicações mais importantes e frequentes: = Geração
14 COMBUSTÍVEIS E TEMPERATURA DE CHAMA O calor gerado pela reação de combustão é muito usado industrialmente. Entre inúmeros empregos podemos citar três aplicações mais importantes e frequentes: = Geração
Equilíbrio Químico do íon bicarbonato: Efeito da concentração. Introdução. Materiais Necessários
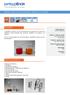 Intro 01 Introdução O equilíbrio químico do íon bicarbonato faz parte de uma série de sistemas como formação das cavernas, equilíbrio no sangue e no oceano. Como a concentração de CO 2 pode afetar o equilíbrio
Intro 01 Introdução O equilíbrio químico do íon bicarbonato faz parte de uma série de sistemas como formação das cavernas, equilíbrio no sangue e no oceano. Como a concentração de CO 2 pode afetar o equilíbrio
Resolução: 0,86ºC. x = 0,5 mol etanol/kg acetona. 0,5 mol 1000 g de acetona. 200 g de acetona. y = 0,1 mol de etanol. 1 mol de etanol (C 2 H 6 O) 46 g
 (ACAFE) Foi dissolvida uma determinada massa de etanol puro em 200 g de acetona acarretando em um aumento de 0,86 C na temperatura de ebulição da acetona. Dados: H: 1 g/mol, C: 12 g/mol, O: 16 g/mol. Constante
(ACAFE) Foi dissolvida uma determinada massa de etanol puro em 200 g de acetona acarretando em um aumento de 0,86 C na temperatura de ebulição da acetona. Dados: H: 1 g/mol, C: 12 g/mol, O: 16 g/mol. Constante
IDENTIFICAÇÃO, ACOMPANHAMENTO E GERENCIAMENTO DE INDICADORES DE RUÍDO AMBIENTAL EM PROCESSOS INDUSTRIAIS. Lucinda Oliveira Amaro a
 IDENTIFICAÇÃO, ACOMPANHAMENTO E GERENCIAMENTO DE INDICADORES DE RUÍDO AMBIENTAL EM PROCESSOS INDUSTRIAIS Lucinda Oliveira Amaro a a Engenharia Química (Graduação-UFC), Engenharia e Ciência de Materiais
IDENTIFICAÇÃO, ACOMPANHAMENTO E GERENCIAMENTO DE INDICADORES DE RUÍDO AMBIENTAL EM PROCESSOS INDUSTRIAIS Lucinda Oliveira Amaro a a Engenharia Química (Graduação-UFC), Engenharia e Ciência de Materiais
Experimento 4 Cromatografia de papel
 Experimento 4 Cromatografia de papel Objetivo Estudo da cromatografia de papel como método de separação e caracterização. Temas abordados Misturas homogêneas, técnicas de separação, forças intermoleculares,
Experimento 4 Cromatografia de papel Objetivo Estudo da cromatografia de papel como método de separação e caracterização. Temas abordados Misturas homogêneas, técnicas de separação, forças intermoleculares,
EQUILÍBRIO QUÍMICO 1
 EQUILÍBRIO QUÍMICO 1 1- Introdução Uma reação química é composta de duas partes separadas por uma flecha, a qual indica o sentido da reação. As espécies químicas denominadas como reagentes ficam à esquerda
EQUILÍBRIO QUÍMICO 1 1- Introdução Uma reação química é composta de duas partes separadas por uma flecha, a qual indica o sentido da reação. As espécies químicas denominadas como reagentes ficam à esquerda
3 METODOLOGIA EXPERIMENTAL
 43 3 METODOLOGIA EXPERIMENTAL 3. 1 METODOLOGIAS DE ANÁLISES 3.1.1 Método de Quantificação de Surfactantes (MBAS) em Águas 3.1.2 Princípio e aplicabilidade Os surfactantes aniônicos SLS (Lauril Sulfato
43 3 METODOLOGIA EXPERIMENTAL 3. 1 METODOLOGIAS DE ANÁLISES 3.1.1 Método de Quantificação de Surfactantes (MBAS) em Águas 3.1.2 Princípio e aplicabilidade Os surfactantes aniônicos SLS (Lauril Sulfato
QIE0001 Química Inorgânica Experimental Prof. Fernando R. Xavier. Prática 09 Síntese do cloreto de pentaaminoclorocobalto(iii)
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC QIE0001 Química Inorgânica Experimental Prof. Fernando R. Xavier Prática 09 Síntese do cloreto
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS CCT DEPARTAMENTO DE QUÍMICA DQMC QIE0001 Química Inorgânica Experimental Prof. Fernando R. Xavier Prática 09 Síntese do cloreto
Degradação de Polímeros
 Degradação de Polímeros Degradação de Polímeros e Corrosão Prof. Hamilton Viana Prof. Renato Altobelli Antunes 1. Introdução Degradação é qualquer reação química destrutiva dos polímeros. Pode ser causada
Degradação de Polímeros Degradação de Polímeros e Corrosão Prof. Hamilton Viana Prof. Renato Altobelli Antunes 1. Introdução Degradação é qualquer reação química destrutiva dos polímeros. Pode ser causada
MANUAL BÁSICO DE TRATAMENTO FÍSICO
 MANUAL BÁSICO DE TRATAMENTO FÍSICO Ao abordar o tratamento físico, discutiremos assuntos relacionados à limpeza com acessórios (aspiração, remoção de sujeiras com peneiras, limpeza das bordas, entre outros),
MANUAL BÁSICO DE TRATAMENTO FÍSICO Ao abordar o tratamento físico, discutiremos assuntos relacionados à limpeza com acessórios (aspiração, remoção de sujeiras com peneiras, limpeza das bordas, entre outros),
Aluno (a): Nº. Disciplina: Química Goiânia, / / 2014
 Lista de Exercícios Aluno (a): Nº. Professora: Núbia de Andrade Série: 1º ano (Ensino médio) Turma: Disciplina: Química Goiânia, / / 2014 01) A mudança de fase denominada sublimação ocorre quando a) o
Lista de Exercícios Aluno (a): Nº. Professora: Núbia de Andrade Série: 1º ano (Ensino médio) Turma: Disciplina: Química Goiânia, / / 2014 01) A mudança de fase denominada sublimação ocorre quando a) o
Como funciona uma autoclave. Introdução. Materiais Necessários. A autoclave
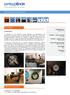 Intro 01 Introdução A autoclave A autoclave é um aparelho muito utilizado em laboratórios de pesquisas e hospitais para a esterilização de materiais. O processo de autoclavagem consiste em manter o material
Intro 01 Introdução A autoclave A autoclave é um aparelho muito utilizado em laboratórios de pesquisas e hospitais para a esterilização de materiais. O processo de autoclavagem consiste em manter o material
Gestão do Conhecimento A Chave para o Sucesso Empresarial. José Renato Sátiro Santiago Jr.
 A Chave para o Sucesso Empresarial José Renato Sátiro Santiago Jr. Capítulo 1 O Novo Cenário Corporativo O cenário organizacional, sem dúvida alguma, sofreu muitas alterações nos últimos anos. Estas mudanças
A Chave para o Sucesso Empresarial José Renato Sátiro Santiago Jr. Capítulo 1 O Novo Cenário Corporativo O cenário organizacional, sem dúvida alguma, sofreu muitas alterações nos últimos anos. Estas mudanças
Aula 2: O estudo da matéria
 KROTON S.A. UNIC EDUCACIONAL LTDA. ENGENHARIA DE PRODUÇÃO 2015/1 Aula 2: O estudo da matéria A Matéria Conceitos; Tudo que tem massa e ocupa lugar no espaço. - O que é massa? - Como se afere a massa de
KROTON S.A. UNIC EDUCACIONAL LTDA. ENGENHARIA DE PRODUÇÃO 2015/1 Aula 2: O estudo da matéria A Matéria Conceitos; Tudo que tem massa e ocupa lugar no espaço. - O que é massa? - Como se afere a massa de
Cortec VpCI - 377 / VpCI - 377 Winterized
 Cortec VpCI - 377 / VpCI - 377 Winterized Descrição do Produto VpCI - 377 é um concentrado à base de água, criado para ser um substituto completo de preventivos à base de óleo para proteção de componentes
Cortec VpCI - 377 / VpCI - 377 Winterized Descrição do Produto VpCI - 377 é um concentrado à base de água, criado para ser um substituto completo de preventivos à base de óleo para proteção de componentes
UNIVERSIDADE ESTADUAL DE PONTA GROSSA PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO PROGRAMA DE PÓS-GRADUAÇÃO QUÍMICA APLICADA - MESTRADO
 strado em Química Aplicada Seleção 2007 1/6 1 a etapa do Processo de Seleção 2007 - Parte 1 Questão 01: (A) Arranje, em ordem crescente de comprimento de onda, os seguintes tipos de fótons de radiação
strado em Química Aplicada Seleção 2007 1/6 1 a etapa do Processo de Seleção 2007 - Parte 1 Questão 01: (A) Arranje, em ordem crescente de comprimento de onda, os seguintes tipos de fótons de radiação
Noções básicas de Segurança em Laboratório. Professora Mirian Maya Sakuno
 Noções básicas de Segurança em Laboratório Professora Mirian Maya Sakuno Laboratório labor = trabalho + oratorium = lugar de concentração Uso inadequado do laboratório PERIGO!!! Regras básicas Não... não
Noções básicas de Segurança em Laboratório Professora Mirian Maya Sakuno Laboratório labor = trabalho + oratorium = lugar de concentração Uso inadequado do laboratório PERIGO!!! Regras básicas Não... não
COLÉGIO NOSSA SENHORA DE LOURDES 2ª SÉRIE Ensino Médio -2015. Roteiro de estudos para recuperação trimestral
 COLÉGIO NOSSA SENHORA DE LOURDES 2ª SÉRIE Ensino Médio -2015 Disciplina: Professor (a): QUÍMICA LUÍS FERNANDO Roteiro de estudos para recuperação trimestral Conteúdo: Referência para estudo: Sites recomendados:
COLÉGIO NOSSA SENHORA DE LOURDES 2ª SÉRIE Ensino Médio -2015 Disciplina: Professor (a): QUÍMICA LUÍS FERNANDO Roteiro de estudos para recuperação trimestral Conteúdo: Referência para estudo: Sites recomendados:
Coagulação ST 502 ST 503. Discentes: : Alyson Ribeiro Daniel Morales Denise Manfio Jenifer Silva Paula Dell Ducas Wander Zapata
 Coagulação e Floculação ST 502 ST 503 Docente: : Profº Peterson Bueno de Moraes Discentes: : Alyson Ribeiro Daniel Morales Denise Manfio Jenifer Silva Paula Dell Ducas Wander Zapata 1. Introdução A água
Coagulação e Floculação ST 502 ST 503 Docente: : Profº Peterson Bueno de Moraes Discentes: : Alyson Ribeiro Daniel Morales Denise Manfio Jenifer Silva Paula Dell Ducas Wander Zapata 1. Introdução A água
 Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
6 Conclusões e Trabalhos futuros 6.1. Conclusões
 6 Conclusões e Trabalhos futuros 6.1. Conclusões Neste trabalho estudou-se o comportamento do sistema que foi denominado pendulo planar com a adição de uma roda de reação na haste do pendulo composta de
6 Conclusões e Trabalhos futuros 6.1. Conclusões Neste trabalho estudou-se o comportamento do sistema que foi denominado pendulo planar com a adição de uma roda de reação na haste do pendulo composta de
Determinação de bases voláteis totais em pescados por acidimetria
 Página 1 de 8 1 Escopo Este método tem por objetivo determinar o teor de bases voláteis totais em pescados, indicando o seu grau de conservação. 2 Fundamentos As bases voláteis totais (N-BVT) compreendem
Página 1 de 8 1 Escopo Este método tem por objetivo determinar o teor de bases voláteis totais em pescados, indicando o seu grau de conservação. 2 Fundamentos As bases voláteis totais (N-BVT) compreendem
CURSO DE AQUITETURA E URBANISMO
 1- Generalidades PROPRIEDADES DO CONCRETO FRESCO Todas as misturas de concreto devem ser adequadamente dosadas para atender aos requisitos de: Economia; Trabalhabilidade; Resistência; Durabilidade. Esses
1- Generalidades PROPRIEDADES DO CONCRETO FRESCO Todas as misturas de concreto devem ser adequadamente dosadas para atender aos requisitos de: Economia; Trabalhabilidade; Resistência; Durabilidade. Esses
http://www.rumoaoita.com / - Material escrito por: Marlos Cunha (ITA T-12) Métodos de Balanceamento
 Métodos de Balanceamento Conteúdo Introdução... 1 Método das tentativas... 1 Método algébrico... 1 Método do íon-elétron... 2 Método da oxi-redução... 3 Auto oxi-redução... 3 Balanceamento dependendo do
Métodos de Balanceamento Conteúdo Introdução... 1 Método das tentativas... 1 Método algébrico... 1 Método do íon-elétron... 2 Método da oxi-redução... 3 Auto oxi-redução... 3 Balanceamento dependendo do
AVALIAÇÃO DA EFICIÊNCIA DO REAGENTE DE FENTON NO TRATAMENTO DO EFLUENTE DE LAVAGEM DE UMA RECICLADORA DE PLÁSTICOS PARA FINS DE REUSO
 AVALIAÇÃO DA EFICIÊNCIA DO REAGENTE DE FENTON NO TRATAMENTO DO EFLUENTE DE LAVAGEM DE UMA RECICLADORA DE PLÁSTICOS PARA FINS DE REUSO Elisângela Garcia Santos RODRIGUES 1, Hebert Henrique de Souza LIMA
AVALIAÇÃO DA EFICIÊNCIA DO REAGENTE DE FENTON NO TRATAMENTO DO EFLUENTE DE LAVAGEM DE UMA RECICLADORA DE PLÁSTICOS PARA FINS DE REUSO Elisângela Garcia Santos RODRIGUES 1, Hebert Henrique de Souza LIMA
Peça com o cilindro antes de ser cromado
 ELIPSE E3 REDUZ OS GASTOS COM REAGENTES QUÍMICOS E MÃO-DE-OBRA UTILIZADOS NA CROMAGEM DOS CILINDROS DA STIHL Solução da Elipse Software permite que apenas nove operadores, por turno, controlem todas as
ELIPSE E3 REDUZ OS GASTOS COM REAGENTES QUÍMICOS E MÃO-DE-OBRA UTILIZADOS NA CROMAGEM DOS CILINDROS DA STIHL Solução da Elipse Software permite que apenas nove operadores, por turno, controlem todas as
Você sabia. As garrafas de PET são 100% recicláveis. Associação Brasileira da Indústria do PET
 Você sabia? As garrafas de PET são 100% recicláveis Associação Brasileira da Indústria do PET O Brasil é um dos maiores recicladores de PET do mundo A reciclagem é uma atividade industrial que gera muitos
Você sabia? As garrafas de PET são 100% recicláveis Associação Brasileira da Indústria do PET O Brasil é um dos maiores recicladores de PET do mundo A reciclagem é uma atividade industrial que gera muitos
Água e Solução Tampão
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
CORROSÃO. Química Geral Prof a. Dr a. Carla Dalmolin
 CORROSÃO Química Geral Prof a. Dr a. Carla Dalmolin CORROSÃO - DEFINIÇÃO Ferrugem Deterioração Oxidação Perda de material ASTM G15: Reação química ou eletroquímica entre um material (geralmente metálico)
CORROSÃO Química Geral Prof a. Dr a. Carla Dalmolin CORROSÃO - DEFINIÇÃO Ferrugem Deterioração Oxidação Perda de material ASTM G15: Reação química ou eletroquímica entre um material (geralmente metálico)
EXPERIÊNCIA 06: DETERMINAÇÃO DA MASSA MOLAR DE UM GÁS
 1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química EXPERIÊNCIA 06: DETERMINAÇÃO DA MASSA MOLAR DE UM GÁS 1. Comportamento dos gases Ao se examinar o comportamento experimental
1 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química EXPERIÊNCIA 06: DETERMINAÇÃO DA MASSA MOLAR DE UM GÁS 1. Comportamento dos gases Ao se examinar o comportamento experimental
CONCURSO DE ADMISSÃO AO CURSO DE FORMAÇÃO E GRADUAÇÃO QUÍMICA CADERNO DE QUESTÕES 2014/2015
 Informações de Tabela Periódica CONCURSO DE ADMISSÃO AO CURSO DE FORMAÇÃO E GRADUAÇÃO QUÍMICA CADERNO DE QUESTÕES 2014/2015 Folha de Dados Elemento H C N O F Al Cl Zn Sn I Massa atômica (u) 1,00 12,0 14,0
Informações de Tabela Periódica CONCURSO DE ADMISSÃO AO CURSO DE FORMAÇÃO E GRADUAÇÃO QUÍMICA CADERNO DE QUESTÕES 2014/2015 Folha de Dados Elemento H C N O F Al Cl Zn Sn I Massa atômica (u) 1,00 12,0 14,0
Abril Educação Água Aluno(a): Número: Ano: Professor(a): Data: Nota:
 Abril Educação Água Aluno(a): Número: Ano: Professor(a): Data: Nota: Questão 1 A água e o ar são indispensáveis para a sobrevivência dos seres vivos, mas o homem vem poluindo esses meios de forma muitas
Abril Educação Água Aluno(a): Número: Ano: Professor(a): Data: Nota: Questão 1 A água e o ar são indispensáveis para a sobrevivência dos seres vivos, mas o homem vem poluindo esses meios de forma muitas
