BIOLOGIA. Distribuição gratuita. Venda proibida.
|
|
|
- Edison Monteiro Anjos
- 8 Há anos
- Visualizações:
Transcrição
1 Distribuição gratuita. Venda proibida. BIOLOGIA 1) Após publicar os resultados de seus experimentos que levaram à construção da primeira célula bacteriana controlada por um genoma sintético., Craig Venter declarou: -Esta é a primeira criatura do planeta capaz de se replicar cujo pai é um computador. Em relação a esse experimento inovador, é correto afirmar que (A) o genoma sintético construído equivalia ao de uma bactéria com um dos maiores genomas conhecidos. (B) um erro na inserção de uma única base nitrogenada no genoma sintético pode prejudicar o funcionamento do genoma. (C) o genoma sintético desenvolveu seu próprio citoplasma. (D) o DNA da bactéria hospedeira foi retirado de seu núcleo celular. (E) as bactérias são organismos especiais para esse tipo de experimento por não apresentarem recombinação genética. QUESTÃO 1 LETRA B Cientistas do Instituto J. Craig Venter anunciaram no dia 20 de maio de 2010 o desenvolvimento da primeira célula portadora de um genoma sintético. Este genoma artificial é uma cópia do genoma da bactéria Mycoplasma mycoides a qual foram adicionadas sequências de DNA montadas em laboratório. Apesar de ser um genoma produzido em laboratório, o código genético do organismo funciona da mesma forma que qualquer outro ser vivo. Portanto, o processo de tradução é igual. Nesse processo, um conjunto de três bases em sequência em um RNA mensageiro (portador da mensagem transcrita a partir do DNA) é responsável pela identificação de cada aminoácido que compõe uma proteína. Assim, a inserção de uma única base no genoma poderia alterar a leitura de nucleotídeos, podendo impedir a produção de proteínas essenciais à sobrevivência do organismo. O aluno deveria lembrar que a conjugação (processo de transferência de DNA de uma bactéria a outra) é um mecanismo de recombinação. 2) A farinha popularizada com o nome de "ração humana" é o resultado de uma mistura de produtos à base de fibras. Uma receita amplamente difundida dessa farinha contém os seguintes componentes: fibra de trigo, leite de soja em pó, linhaça marrom, açúcar mascavo, aveia em flocos, gergelim com casca, gérmen de trigo, gelatina sem sabor, guaraná em pó, levedura de cerveja e cacau em pó. Com base na receita e em seus constituintes, assinale com V (verdadeiro) ou F (falso) as afirmações que seguem. ( ) A receita é rica nas fontes alimentares de vitaminas do complexo B. ( ) A levedura de cerveja é utilizada em pesquisa como modelo experimental. ) A receita é rica nas fontes alimentares das vitaminas A e C. ( ) O açúcar mascavo não apresenta restrição de uso pelos diabéticos dependentes de insulina. (A) V - V - F - F. (D) F - V - F - V. (B) V - F - V - V. (E) V - F - V - F. (C) F - V - V - F. QUESTÃO 2 LETRA A As vitaminas citadas na terceira afirmativa não possuem como fontes os componentes citados no enunciado. Acerca destas é importante salientar: Vitamina A (Antixeroftálmica) Quando a carência de vitamina A persiste durante certo tempo, a córnea (membrana translúcida do olho) se torna espessa e ulcerada, as glândulas lacrimais reduzem sua atividade e surge a xeroftalmia, que pode levar à cegueira total. Fontes: leite e seus derivados, ovos, fígado, cenoura, couve, mamão, laranja, etc. Vitamina C (Ácido ascórbico) Na carência de vitamina C as paredes dos capilares sanguíneos tornam-se frágeis, favorecendo a ocorrência de hemorragias generalizadas, como nas gengivas e até mesmo no cérebro. Fontes: frutas cítricas (laranja e limão), cereja, caqui, goiaba, mamão, banana, maçã, morango, batata, rabanete, alface, repolho, pimentão, espinafre, etc. O açúcar mascavo é o mais simples de ser obtido e não passa pelo processo de branqueamento e refino utilizados na produção do açúcar comumente usado. Ele também consiste em sacarose (glicose + frutose) no estado sólido e cristalino. É produzido comercialmente a partir de cana de açúcar ou de beterraba. Exatamente por isso deve ter uso restrito por diabéticos, pois estes não possuem a produção de insulina, que aumenta a permeabilidade das células para a gllicose. 3) A figura abaixo mostra dois peixes identificados pelos números 1 e 2 que apresentam adaptações fisiológicas para sobreviver em diferentes ambientes. As setas indicam o fluxo de sais e de água em cada peixe. Peixe teleósteo Peixe teleósteo de água doce marinho Considere as seguintes afirmações, sobre características desses peixes. I -O peixe 1 é hipertônico em relação ao ambiente. II -O peixe 1 capta sais por transporte ativo. III-O peixe 2 perde água para o meio por osmose. (B) Apenas li. (E) I, II e IlI. QUESTÃ LETRA E Peixes que vivem em água doce (Figura 1), possuem concentração osmótica maior do que o meio externo (hipertônicos). Sendo assim, a água do ambiente tende a entrar no animal através de osmose. Esta grande quantidade de água que entra no organismo permite a produção de urina diluída e em grande volume, o que acaba por influenciar na perda de uma grande quantidade de sais que serão eliminados através da urina. Desta forma, estes peixes possuem células especiais localizadas nas brânquias, as quais, através de transporte ativo, transferem sais do meio externo para o corpo do animal, o que auxilia na regulação osmótica interna. Já os peixes marinhos (Figura 2) são hipotônicos em relação à água do mar (concentração osmótica interna menor que a externa). Sendo assim, o peixe tende a perder água para o meio através de osmose (transporte passivo). Para evitar a desidratação, estes animais precisam beber água marinha e, através das células das brânquias, eliminam o excesso de sais do corpo por transporte ativo. 4) Assinale a alternativa que preenche corretamente as lacunas do enunciado abaixo, na ordem em que aparecem. Os encontram-se nos centros organizadores de... '." da maioria dos eucariontes e estão envolvidos na formação do fuso mitótico. (A) ribossomos -microfilamentos (B) lisossomos -filamentos intermediários (C) centríolos -microtúbulos (D) ribossomos -filamentos intermediários (E) centríolos -microfilamentos QUESTÃO 4 LETRA C Os centríolos são estruturas citoplasmáticas existentes nas células dos protistas, dos animais e dos vegetais, sendo ausente nas células dos vegetais superiores (gimnosper-
2 mas e angiospermas). Em geral, uma célula animal apresenta um par de centríolos dispostos perpendicularmente entre si, formando um diplossomo. Na célula que não está em divisão, os centríolos situam-se próximos do núcleo em uma região denominada centro celular ou centrossomo. O centro celular corresponde a uma região organizadora dos microtúbulos que se irradiam a partir do centro celular. A função dos centríolos está ligada ao processo de divisão celular, na formação do fuso acromático; e de dois tipos de estrutura celular: cílios e flagelos. 5) A coluna da esquerda, abaixo, apresenta diferentes fases da meiose; a da direita, as fontes de variabilidade genética de duas dessas fases. Associe adequadamente a coluna da direita à 1 - prófase I 2 - anáfase I ( ) permutação 3 - prófase II 4 - matáfase II ( ) segregação independente de 5 - anáfase II homólogos (A) 1 e 2. (D) 4 e 5. (B) 2 e 3. (E) 5 e 1. (C) 3 e 4. QUESTÃO 5 LETRA A O tipo de divisão celular fundamental para organismos de reprodução sexuada é a meiose, uma vez que ela forma quatro células com a metade do número de cromossomos da espécie. Nos animais, os gametas femininos e masculinos são formados a partir da divisão meiótica, em virtude de que esse processo assume fundamental importância na evolução dos seres vivos. Na meiose existe, durante a prófase I, a possibilidade de que pedaços de DNA sejam trocados entre cromossomos homólogos. É a permutação ou crossing-over, termo inglês bastante popularizado. Como consequência disso, as células-filhas são geneticamente diferentes das parentais. Esse fenômeno é chamado de recombinação gênica e é muito importante, porque aumenta a variabilidade genética da espécie. Outro fator que aumenta a variabilidade é o posicionamento dos pares homólogos durante a metáfase I e a sua consequente separação na anáfase I. Cada gameta será portador de diferentes combinações dos cromossomos parentais. 6) A fotossíntese consiste em um processo metabólico pelo qual a energia da luz solar é utilizada na conversão de dióxido de carbono e de água em carboidratos e oxigênio. Com relação a esse processo, considere as seguintes afirmações. l - A produção de carboidratos ocorre na etapa fotoquímica. II - A água é a fonte do oxigênio produzido pela fotossíntese. III - A etapa química ocorre no estroma dos cloroplastos. (E) l, II e III. QUESTÃO 6 LETRA D Na fotossíntese existem duas fases subsequentes, uma conhecida como fase clara ou etapa fotoquímica e outra chamada fase escura ou etapa química. Na etapa fotoquímica, que ocorre nos tilacóides do cloroplasto, a energia luminosa oxida a molécula de clorofila que libera elétrons utilizados na fotólise, quebra da molécula de água em oxigênio, que vai para a atmosfera; e hidrogênio, encaminhado para a fase escura para a produção de glicose. Portanto, a produção de carboidratos não ocorre nesta fase como diz a afirmativa I. Elétrons da clorofila são utilizados, também, na produção de ATP via mecanismo de transporte de elétrons. Na etapa química, que ocorre no estroma do cloroplasto, o CO 2 captado da atmosfera é incorporado a um ciclo de reações que culmina, com a participação do H e de ATP oriundos da etapa fotoquímica, com a produção de vários carboidratos, dentre eles a glicose. 7) Assinale a alternativa que preenche corretamente as lacunas do enunciado abaixo, na ordem em que aparecem. A... é o processo no qual os folhetos germinativos embrionários são formados. Nos vertebrados, o folheto denominado... originará o coração, os vasos e as células sanguíneas. (A) clivagem ectoderma (D) clivagem endoderma (B) gastrulação mesoderma (E) gastrulação ectoderma (C) neurulação endoderma QUESTÃO 7 LETRA B Os folhetos germinativos embrionários são a endoderme, a mesoderme e a ectoderme. Logo após a fecundação, inicia-se a clivagem (ou segmentação), processo através do qual o zigoto se duplica originando novas células. Nesse processo forma-se a mórula, quando se atinge de 16 a 32 células, sendo esta uma massa compacta. Posteriormente, temos a blástula, que se caracteriza por possuir uma cavidade denominada blastocele. A partir daí, inicia-se a formação da gástrula, caracterizada pela embolia dos macrômeros, resultando em duas camadas de células: a mais externa, denominada ectoderme; e a mais interna, denominada mesentoderme, que se dividirá em endoderme e mesoderme. A mesoderme forma os somitos, que originarão, entre outras estruturas, o coração, os vasos e as células sanguíneas. 8) O esquema abaixo mostra alguns dos componentes do tecido conjuntivo frouxo. Assinale a alternativa correta em relação ao tecido conjuntivo frouxo. (A) Nele não ocorre vascularização. (B) Ele apresenta distribuição corporal restrita. (C) A célula marcada com a seta 1 é um fibroblasto. (D) A célula marcada com a seta 2 é uma hemácia. (E) As fibras assinaladas com as setas 3 são de actina e miosina. QUESTÃO 8 LETRA C Tecido conjuntivo frouxo, que apoia e nutri os epitélios, é formado por substância fundamental mole e gelatinosa, com uma grande quantidade de fibras. Tem entre outros tipos de células os fibroblastos que formam fibras que dão resistência aos tecidos. 9) O Programa Nacional de Imunização do Ministério da Saúde disponibiliza, na rede pública, vacinas imprescindíveis para a saúde de crianças de diferentes idades. Assinale a alternativa que apresenta apenas doenças virais que podem ser prevenidas pelo uso de vacinas previstas pelo programa citado. (A) tuberculose - hepatite B - difteria - meningite (B) poliomielite - tétano - pneumonia - febre amarela (C) sarampo - febre tifóide - coqueluche - hepatite B (D) poliomielite - rubéola - caxumba - sarampo (E) difteria - tétano - coqueluche - varicela QUESTÃO 9 LETRA D São causadas por bactérias: tuberculose, difteria, tétano, febre tifóide e coqueluche. Todas as outras são causadas por vírus. É bom lembrar que a meningite e a pneumonia possuem agentes infectantes, tanto virais quanto bacterianos. 10) Diversos órgãos vegetais fazem parte de nossa alimentação. Em termos biológicos, a abóbora, o tomate e o pimentão constituem (A) frutos verdadeiros. (D) infrutescências. (B) pseudofrutos. (E) frutos partenocárpicos. (C) legumes. QUESTÃO 10 LETRA A O fruto é uma característica exclusiva das plantas classificadas como angiospermas. Um fruto verdadeiro é formado a partir do desenvolvimento do ovário da flor, após a ocorrência da fecundação entre os gametas feminino e masculino da planta. Dessa forma, o fruto protegerá o embrião presente internamente na semente (Ex: abóbora, tomate, pimentão). Frutos partenocárpicos são aqueles nos quais não ocorreu fecundação e, consequentemente, não apresentam sementes (ex: banana, abacaxi). Os pseudofrutos são aqueles em que a parte que armazena reservas, tornando-se comestível, não é derivada do desenvolvimento do ovário, mas sim de outras partes da flor, como o receptáculo floral e o pedúnculo (Ex: maçã, caju, morango). Legumes são os frutos produzidos pelas plantas leguminosas, apresentando, portanto, a forma de vagem (Ex: vagem de feijão, de soja, de amendoim). Infrutescência é o conjunto de frutos originados a partir de um conjunto de flores (inflorescências). Estes conjuntos podem apresentar-se de formas variadas, como cachos ou espigas (Ex: uva, milho). 11) Alguns elementos químicos denominados macronutrientes são essenciais e necessários, em quantidades relativamente grandes, ao crescimento vegetal. São macrdnutrientes os elementos químicos (A) C, H, O. (D) Ca, 6, K. (B) N, P, Cu. (E) Na, P, K. (C) N, Fe, Ca. QUESTÃO 11 LETRA A A decomposição da matéria orgânica libera nutrientes minerais no solo que são essenciais para o desenvolvimento das plantas. Estes nutrientes são absorvidos principalmente pelas raízes e usados em diferentes proporções pelo vegetal. Os macronutrientes são aqueles utilizados em maior quantidade, sendo que a falta destes no solo causa anomalias diversas no desenvolvimento da planta. Na categoria dos macronutrientes encontramos carbono (C), hidrogênio (H), oxigênio (O), nitrogênio (N), fósforo (P), potássio (K), enxofre (S), magnésio (Mg) e cálcio (Ca). 12) A planta denominada erva-de-passarinho é uma hemiparasita. Nesse caso, o tecido vegetal da árvore hospedeira, onde os elementos nutritivos são absorvidos, é o (A) colênquima. (D) parênquima. (B) floema. (E) xilema. (C) esclerênquima. QUESTÃO 12 LETRA E A erva de passarinho é uma planta parasita que se desenvolve em galhos e troncos de árvores, principalmente em ambiente urbano. Devido ao fato de suas folhas apresentarem cloroplastos, são capazes de realizar fotossíntese, sendo, portanto, consideradas hemiparasitas (parcialmente parasitas), já que suas raízes modificadas (haustórios) retiram da planta hospedeira apenas os elementos minerais (seiva bruta) que circulam no interior dos vasos condutores do xilema. 13) Leia a tira abaixo. Adaptado de: VERISSIMO, 'Luis Fernando. Terramagazine. São Paulo, 26 dez Invertebrados como os citados na tira têm em comum (A) exoesqueleto de quitina. (6) circulação fechada. (C) respiração traqueal. (D) excreção por meio de nefrídeos. (E) corpo metamerizado. QUESTÃO 13 LETRA E Esta questão demonstra uma relação de parentesco evolutivo entre os anelídeos (mais antigos) e os artrópodes (mais recentes). Dentre as alternativas apresentadas, o corpo metamerizado ou segmentado é a característica comum aos dois filos, inclusive demonstrando sua relação de parentesco. O exoesqueleto de quitina ocorre nos artrópodes e em outros ecdisozoários, como as lombrigas (nematelmintos). A circulação fechada está presente nos anelídeos, nos cefalópodes e nos vertebrados; sendo aberta nos artrópodes. A respiração traqueal (e também branquial) ocorre em vários artrópodes, mas não nas minhocas, que respiram através da pele. A excreção por nefrídios (um par por segmento) está presente nas minhocas, enquanto nos artrópodes a excreção se dá através dos túbulos de Malpighi (insetos), glândulas coxais(aracnídeos) ou glândulas verdes (crustáceos). 14) Com relação às aves, considere as seguintes afirmações. I - Elas apresentam taxa metabólica elevada. II - Suas penas atuam como isolante térmico. III - Sua excreta nitrogenada é a ureia. (D) Apenas I e II. QUESTÃO 14 LETRA D As aves, assim como os mamíferos, possuem taxa metabólica elevada por possuírem circulação dupla e fechada, bem como pulmões muito eficientes, o que lhes garante um excelente aporte de oxigênio possibilitando-lhes a endotermia ou homeotermia. As penas das aves são estruturas leves e resistentes que protegem contra ferimentos na pele, lhes dão a forma aerodinâmica e são excelentes isolantes térmicos. A excreta nitrogenada das aves (e também dos répteis) é o ácido úrico, que é praticamente insolúvel em água, o que garante economia de água tanto na fase adulta, mas principalmente na fase embrionária. A uréia é mais tóxica que o ácido úrico e necessita de água para ser eliminada. 15) Um reduzido suprimento de sangue no músculo cardíaco de mamíferos acarreta (A) a diminuição do suprimento de oxigênio. (B) o aumento do número de hemácias. (C) o aumento do número de mitocôndrias. (D) o aumento do metabolismo oxidativo. (E) a diminuição da concentração de ácido, Iáctico. QUESTÃO 15 LETRA A O oxigênio é transportado aos tecidos através do sangue. Quando o suprimento de sangue é reduzido, o músculo cardíaco recebe menos oxigênio. O aumento no número de hemácias ocorre quando há maior dificuldade em conseguir oxigênio, como em altitudes elevadas. A elevação do número de mitocôndrias e do metabolismo oxidativo se dá quando ocorre o aumento da quantidade de oxigênio. Quando temos menos oxigênio, ocorre maior concentração de ácido lático, devido à fermentação, e não o contrário. 16) Recentemente, ocorreu um campeonato de permanência em sauna úmida na Finlândia que ocasionou a morte de um dos competidores. Em relação à capacidade termorreguladora corporal na situação descrita, considere as seguintes afirmações. I - O calor produziu vasodilatação dos capilares periféricos da pele. II - A pressão arterial diminuiu. III - O suor produzido reduziu a temperatura da pele. QUESTÃO 16 LETRA E Os mamíferos são organismos endotérmicos ou homeotérmicos porque possuem mecanismos para manterem sua temperatura constante. Numa situação como a descrita na questão, isto é, calor excessivo, ocorrem alguns fenômenos como a vasodilatação periférica, onde mais sangue circula próximo à superfície do corpo dissipando calor para o meio. A pressão arterial diminui como uma forma de reduzir o metabolismo e gerar menos calor. O suor, ao evaporar, ajuda na diminuição da temperatura corporal. 17) Uma das técnicas atualmente utilizadas para analisar casos de paternidade civil é o emprego de marcadores de microssatélites. Os microssatélites são repetições de trechos de DNA que ocorrem em número variável na população. O número de repetições é transmitido geneticamente. A análise de microssatélites foi utilizada em um teste de paternidade. A tabela abaixo apresenta os resultados relativos ao número de repetições encontradas para a mãe, para o suposto pai e para o filho, em diferentes locos. Com base nos dados apresentados na tabela, é correto afirmar que (A),apenas um indivíduo, pela análise, é homozigoto para o loco 6. 2
3 (B) os locas 2, 4 e 7 excluem a possibilidade de paternidade do suposto pai. (C) o filho é heterozigoto para a maioria dos locos analisados. (D) a mãe referida não é mãe biológica deste filho. (E) os locos 1 e 3 excluem a possibilidade de paternidade do suposto pai. QUESTÃO 17 LETRA B Questão interessantíssima que utiliza uma das técnicas de biologia molecular para detectar a paternidade. A tabela mostra os alelos da mãe, do suposto pai e do filho presentes em sete locos diferentes. A análise dos alelos mostra que o filho, que deve receber, obrigatoriamente, um alelo da mãe e um do pai, não possui o alelo oriundo do suposto pai nos locos 2, 4 e 7, o que exclui este indivíduo da paternidade. 18) As flores de uma determinada planta podem ser brancas, vermelhas ou creme. A cor branca (ausência de deposição de pigmento) é condicionada por alelo recessivo (aa). O alelo A determina a deposição de pigmento. O alelo dominante B produz pigmento vermelho, enquanto seu recessivo, a cor creme. Cruzando-se plantas heterozigotas para os dois genes entre si, a probabilidade de obtermos uma planta branca é de (A) 3/16. (D) 9/16. (B) 4/16. (E) 12/16. (C) 7/16. QUESTÃO 18 LETRA B Um caso de epistasia recessiva onde plantas portadoras de genótipo A_ tem pigmentos e plantas com genótipo aa não os possuem. Um outro par de alelos é responsável pelas cores: B_ forma vermelho e bb forma cor creme nas folhas. Portanto, indivíduos A_B_ tem flores vermelhas, A_bb tem flores creme e aa tem flores brancas. Ao cruzar dois duplo- heterozigotos, a probabilidade gerada na descendência seria 9/16 indivíduos de flores vermelhas, 3/16 indivíduos de flores creme e 4/16 indivíduos de flores brancas. Os padrões de herança epistáticos possuem como característica a soma de classes fenotípicas. 19) Em geral, os cromossomos sexuais de mamíferos fêmeas consistem de um par de cromossomos X. Machos possuem um cromossomo X e um cromossomo sexual quenão é encontrado em fêmeas: o cromossomo Y. Assinale com V (verdadeiro) ou F (falso) as afirmações abaixo, referentes ao sistema XY de determinação sexual de mamíferos. ( ) Os genes ligados ao cromossomo X são os que apresentam como função a diferenciação sexual. ( ) Os cromossomos X e Y pareiam durante a meiose. ( ) A inativação de um dos cromossomos X em fêmeas permite o mecanismo de compensação de dose. ( ) Fenótipos recessivos ligados ao X são mais frequentes em fêmeas que em machos. (A) F - F - F - V. (D) V - F - F - V. (B) F - V - F - V. (E) V - V - V - F. (C) F - V - V - F. QUESTÃO 19 LETRA C A diferenciação sexual é proporcionada por genes presentes na região do cromossomo Y não homóloga ao cromossomo X. Estes genes são chamados de holândricos, pois sua expressão ocorre apenas no homem. Um destes genes é conhecido como SRY (sigla em inglês para região do Y relacionada à determinação do sexo) que inicia a formação da genitália masculina por volta da 10ª semana gestacional. A não expressão deste gene ocasiona o pseudo-hermafroditismo masculino onde o indivíduo, cromossomicamente XY, possui genitália externa semelhante à feminina. A mulher é portadora de dois locos, um em cada cromossomo X. Já o homem, por ser portador de apenas um X, tem a desvantagem de ter maior frequência de fenótipos recessivos ligados ao cromossomo X, pois com apenas um alelo recessivo ele é afetado pela característica. Já a mulher necessita de dois alelos, um da mãe e um do pai, para apresentar o fenótipo de afetada, o que é muito mais raro de ocorrer nas populações. 20) Entre as adaptações da presa contra a predação, está o mimetismo. No mimetismo batesiano, uma espécie comestível mimetiza uma espécie não comestível, ou nociva. Considere as seguintes afirmações, referentes à estabilidade desse tipo de mimetismo. I - O predador que captura um indivíduo de uma espéde não comestível ou nociva evita qualquer presa de aparênda semelhante. II - O mímico evolui em direção à aparência de uma espécie não comestível mais depressa do que a espécie não comestível acumula diferenças em relação ao mímico. III - O mímico deve ser de uma espécie menos comum que a espécie não comestível. QUESTÃO 20 LETRA E Mimetismo é uma adaptação ambiental em que a seleção natural favorece, dentro de uma população, organismos cujos tipos têm maior capacidade de sobrevivência devido à sua aparência externa. No mimetismo, um organismo imita a forma, a cor ou o comportamento de outro organismo, tirando disto algum proveito, ou seja, se livram de predadores. 21) Três espécies diploides diferentes de plantas da família do girassol, convivendo em uma mesma área geográfica, geraram híbridos férteis incapazes de cruzar com as espécies ancestrais. Essas espécies novas se espalharam por uma área geográfica maior que a ocupada pelas espécies parentais. Nesse caso, o processo e o mecanismo de especiação que melhor se adaptam à situação descrita são, respectivamente, (A) a alopatria e o efeito do fundador. (B) a simpatria e a poliploidia. (C) a pârapatria e o fluxo gênico. (D) a alopatria e a seleção sexual. (E) a simpatria e o efeito do fundador. QUESTÃO 21 LETRA B A questão trata de três espécies diferentes de girassol vivendo na mesma área, logo, temos um caso de simpatria, isto é, o processo de especiação ocorre num mesmo local. Caso tivéssemos isolamento geográfico o processo ocorreria em lugares diferentes, portanto, alopatria. Para termos parapatria seria necessário que uma espécie se espalhasse numa faixa contínua, onde pudesse haver dispersão de indivíduos e, posteriormente, isolamento reprodutivo. Como se tratam de três espécies de plantas que geram híbridos, podemos ter a poliploidia (indivíduos 3n, 4n, etc). Para que tivéssemos o efeito do fundador seria necessária a invasão de alguns indivíduos de uma espécie num novo ambiente. 22) Observe a teia alimentar representada no diagrama abaixo. Com base neste diagrama, assinale a afirmação correta. (A) O mosquito e o gavião ocupam níveis tróficos diferentes. (B) O nível trófico dos produtores não está representado no diagrama. (C) O homem e o gambá ocupam o mesmo nível trófico. (D) O pássaro e o gato ocupam o mesmo nicho ecológico. (E) O gavião e o gambá são equivalentes ecológicos. QUESTÃO 22 LETRA C A teia alimentar em questão traz o milho como representante do nível trófico dos produtores, onde temos como herbívoros (consumidores primários) o rato, o inseto, a galinha e o ovo (elemento produzido pela galinha através de seus próprios recursos energéticos, o que o coloca no mesmo nível trófico da galinha, já que possui energia disponível para o próximo nível trófico). Como consumidores secundários estão o gambá, o homem, o pássaro, a cobra e o gato, já que todos se alimentam de pelo menos algum consumidor primário. E como consumidores terciários aparecem o gavião e o mosquito alimentando-se de consumidores secundários (lembre-se que o sangue do homem é um elemento produzido pelo próprio homem, garantindo energia para o próximo nível trófico). Em relação ao recurso alimento, os representantes dos mesmos níveis tróficos ocupam o mesmo nicho ecológico. 23) A reação química abaixo está relacionada à origem de vários produtos. Considere os produtos citados a seguir. 1 - álcool combustível (etanol) 4 - óleo de soja 2 - petróleo 5 - pão 3 - papel higiênico Quais desses produtos têm sua origem relacionada à equação apresentada acima? (A) Apenas 1 e 2. (D) Apenas 2, 3 e 5. (6) Apenas 3 e 4. (E) 1, 2, 3, 4 e 5. (C) Apenas 1, 4 e 5. QUESTÃO 23 LETRA E Para resolver esta questão é essencial considerar a origem dos produtos listados. Já que a reação química em questão trata da fotossíntese, os produtos com origem vegetal estarão relacionados à equação apresentada. O álcool combustível é obtido a partir da fermentação de açúcares, os quais são produtos da fotossíntese, sendo este o motivo pelo qual é muito empregada a cana de açúcar para a produção de etanol. O petróleo é resultado da deposição e posterior transformação química de restos orgânicos (animais e VEGETAIS) no fundo de lagos e mares. O papel higiênico é derivado da celulose, molécula de reserva das plantas, sendo um polímero de glicose (produto final da fotossíntese). O óleo de soja é extraído das sementes da soja, sendo, portanto, um produto vegetal. Os pães têm como base em sua produção os farináceos, produtos derivados de vegetais como, por exemplo, o trigo (farinha de trigo), mandioca (farinha de mandioca) e o milho (farinha de milho). Sendo assim, todos os produtos listados têm origem vegetal, estando diretamente relacionados à reação de fotossíntese. 24) Os ecossistemas terrestres transferem através dos rios um grande fluxo de elementos para os mares. Com relação ao fluxo de materiais e nutrientes em sentido inverso, ou seja, dos mares para os sistemas terrestres, considere as seguintes afirmações. I - A extração de petróleo em grandes profundidades do subsolo oceamco transfere para os ecossistemas terrestres o fósforo utilizado na adubação agrícola. II - Os ecossistemas terrestres recebem alguns elementos do meio oceânico através da brisa marinha ("maresia''). III - O consumo de peixe marinho pela população humana transfere elementos do meio oceânico para o terrestre. QUESTÃO 24 LETRA D A formação do petróleo vem da deposição, no fundo de lagos e mares, de restos de animais e vegetais mortos ao longo de milhares de anos, ou seja, muito antes do surgimento da agricultura. Estes restos iam sendo cobertos por sedimentos, e mais tarde esses sedimentos se transformaram em rochas sedimentares. A ação do calor e da alta pressão provocados pelo empilhamento dessas camadas possibilitou reações complexas, formando o petróleo. O fósforo utilizado na adubação agrícola vem de outras fontes como rochas. 25) Ver questão no site QUESTÃO 25 LETRA C Vegatação ciliar é a designação dada à vegetação que ocorre nas margens de rios e mananciais. O termo refere-se ao fato de que ela pode ser tomada como uma espécie de "cílio", que protege os cursos de água do assoreamento (diminuição da profundidade dos rios por areias e argilas trazidas pela erosão). É também importante no processo de barragem de detritos e para estabilização de barrancos. Outro aspecto diz respeito ao fato de ser via de trânsito da fauna, propiciando o fluxo gênico entre as populações presentes nas diversas comunidades. QUÍMICA 26) Considere os seguintes processos realizados por um estudante em um laboratório. 1 - filtração de uma solução aquosa de KMnO 4 de cor violeta 2 - destilação de uma solução aquosa de K 2 Cr 2 O 7 de coloração alaranjada 3 - decantação de uma solução aquosa de CuSO4 de coloração azul Após a realização de cada um desses processos, o estudante constatou que a fase líquida obtida é incolor em (A) apenas 1. (D) apenas 1 e 2. (B) apenas 2. (E) 1,2 e 3. (C) apenas 3. QUESTÃO 26 LETRA B A solução 1 não pode ser fracionada por um filtro porque é homogênea e, portanto, não terá sua coloração alterada. A solução 2, quando destilada, possibilita a recuperação do solvente (água), que é incolor. A solução 3 não pode ser fracionada por decantação, pois se trata de um sistema homogêneo, e decantação separa líquidos imiscíveis com densidades diferentes, o que não é o caso e, portanto, não há como ter sua coloração alterada. 27) Desde o século XIX, uma das questões mais preocupantes para os químicos era a definição do peso dos átomos. Atualmente, as massas atômicas dos elementos químicos são representadas, em sua maior parte, por números fracionários. O, elemento magneslo, por exemplo, apresenta massa atômica aproximada de 24,3 unidades de massa atômica. Uma justificativa adequada para este valor fracionário é que (A) os átomos de magnésio podem apresentar um número de elétrons diferente do número de prótons. (B) o número de nêutrons é sempre maior que o número de prótons nos átomos de magnésio. (C) o elemento magnésio pode originar diferentes variedades alotrópicas. (D) a massa de um átomo de magnésio é relativamente 24,3 vezes maior que a de um átomo do isótopo 12 do carbono. (E) o elemento magnésio é formado por uma mistura de isótopos naturais que apresentam massas atômicas diferentes. QUESTÃO 27 LETRA E Como a questão solicita a justificativa para a massa atômica aproximada do elemento magnésio, que corresponde a 24,3 unidades de massa atômica, o aluno deveria lembrar que a maioria dos elementos químicos tem isótopos naturais e, como tal, o valor da massa atômica corresponde á média aritmética ponderada das massas dos isótopos. 28) Na fabricação de vidros, utilizam-se, principalmente, areia (dióxido de silído), cal (óxido de cálcio) e barrilha (carbonato de sódio). Outras substâncias que passam por reações químicas específicas também podem ser incluídas nesse processo. Abaixo, são apresentadas fórmulas de cinco substâncias que participam de reações realizadas na fabricação do vidro. 1 - SiO SO CO 4 - Na 2 C 5-CaO Assinale a afirmação correta, sobre essas substâncias. (A) As substâncias 1, 4 e 5 são sólidas na temperatura ambiente. (B) Somente a substância 4 pode ser considerada iônica. (C) Todas as substâncias podem ser consideradas óxidos. (D) A substância 2 é insolúvel em água. (E) As substâncias 1 e 3 são apolares com baixos pontos de fusão. QUESTÃO 28 LETRA A Analisando as substâncias apresentadas teremos: 1 SiO 2 sílica composto covalente (somente ligação covalente entre seus átomos sem formar moléculas), portanto, com alto ponto de fusão e ebulição. 2 SO 2 gás sulfuroso composto molecular (forma moléculas) polar com baixo ponto de ebulição, é gás a temperatura ambiente. 3 CO monóxido de carbono composto molecular polar com baixo ponto de ebulição, é gás à temperatura ambiente. 4 Na 2 C carbonato de sódio composto iônico, portanto, com alto ponto de fusão e ebulição, é sólido à temperatura ambiente. 5 CaO óxido de cálcio composto iônico com alto ponto de fusão e ebulição. 29) Usando-se a técnica de espectrometria de massas, é possível determinar a razão 13 C/ 12 C no vinho espumante e em suas bolhas de gás carbônico. Dependendo do valor 3
4 dessa razão, é possível afirmar se o açúcar e o gás carbônico foram formados somente pelo processo natural de fermentacão ou se houve adição desses compostos durante o processo de produção do vinho espumante. Considere as seguintes afirmações, em relação às espécies 12 C e 13 C. I - As espécies 12 C e 13 C ocupam a mesma posição na tabela periódica. II - A espécie 13 C é mais densa que a espécie 12 C, porque ela apresenta um próton a mais. III - A espécie 13 C é mais eletronegativa que a espécie 12 C, porque ela apresenta um elétron a mais. (D) Apenas I e II. (E) Apenas II e III. QUESTÃO 29 LETRA A I) As espécies 12 C e 13 C, sendo isótopos (ISO = igual; TOPOS = lugar), ocupam a mesma posição na tabela periódica. II) Por serem isótopos, 12 C e 13 C possuem o mesmo número de prótons. III) Para o isótopo 12 C, o número de massa 12 é a soma de 6 prótons e 6 nêutrons. Para o isótopo 13C, o número de massa 13 é a soma de 6 prótons e 7 nêutrons. Os isótopos têm o mesmo número de elétrons e, portanto, as mesmas propriedades químicas. 30) Em 2010, o Prêmio Nobel de Química foi atribuído aos pesquisadores Richard F. Heck, Ei-ichi Negishi e Akira Suzuki. Eles dividiram o prêmio por terem desenvolvido novos métodos que revolucionaram a maneira de se obterem moléculas complexas levando à produção de novos medicamentos e de outros materiais úteis no nosso cotidiano. Esses métodos consistem em acoplar, na presença de um catalisador, um haleto orgânico com uma olefina (Reação de Heck), um organozinco (Reação de Negishi) ou um organoboro (Reação de Suzuki), propiciando a formação de uma nova ligação carbono-carbono. Abaixo, são mostrados exemplos de reagentes utilizados nessas reações. Considere as seguintes afirmações, sobre esses exemplos de reagentes. I - Todos os carbonos do composto 1 apresentam geometria trigonal-plana. II - No composto 2, o boro apresenta geometria tetraédrica. III - No composto 3, dois carbonos apresentam geometria linear, e um carbono apresenta geometria tetraédrica. (A) Apenas II. (D) Apenas I e III. (B) Apenas III. (C) Apenas I e li. QUESTÃ0 LETRA D A questão apresenta algumas moléculas com carbono e boro, solicitando suas formas geométricas. As formas que o carbono pode apresentar são mostradas abaixo. O boro, que faz três ligações covalentes, também tem sua estrutura indicada. No composto 1 todos os carbonos apresentam uma ligação dupla, logo todos têm geometria trigonal plana; no composto 2, o boro também tem estrutura trigonal-plana e no composto 3 há dois carbonos unidos por uma liga tripla, presente apenas em carbonos de geometria linear. 31) A grande importância da água para a vida está diretamente relacionada à especificidade de suas propriedades. Considere as seguintes afirmações, sobre as propriedades da substância água. I - A forma esférica das gotas de água é consequência de sua tensão superficial particularmente elevada. II - A água, nas condições ambiente, apresenta-se no estado líquido devido às fortes ligações de hidrogênio entre suas moléculas. III - A presença de dois átomos de hidrogênio para cada átomo de oxigênio confere à molécula uma geometria trigonal que determina sua elevada polaridade. (C) Apenas I e II. QUESTÃ1 LETRA C Afirmativa I A tensão superficial é formada por moléculas de água ligadas em uma geometria específica, na qual as ligações de hidrogênio são mais fortes em igual intensidade, formando uma superfície esférica. Correta. Afirmativa II A água é fortemente polar, tendo entre suas moléculas as ligações de hidrogênio, que são relativamente fortes, fazendo com que seu ponto de ebulição seja mais elevado do que o esperado; por isso a água é líquida em temperatura ambiente. Correta. Afirmativa III A geometria molecular da água é angular, e não trigonal como mencionado. Errada. 32) O tiossulfato de sódio é utilizado na formulação de banhos fixadores para materiais fotográficos. A obtenção do tiossulfato de sódio ocorre a partir de uma solução que contém sulfeto de sódio e carbonato de sódio, através da qual se passa uma corrente de dióxido de enxofre, conforme a equação abaixo. Na 2 C + x Na 2 S + y SO 2 z Na 2 S 2 + r CO 2 Para que essa equação química seja corretamente ajustada a partir de um mol de carbonato de sódio, os coeficientes x, y, z e r devem ser, respectivamente, (A) 1, 2, 2 e 1. (D) 2, 4, 3 e 1. (B) 1, 3, 2 e 3. (E) 3, 2, 4 e 2. (C) 2, 1, 3 e 2. QUESTÃ2 LETRA D Acertando os coeficientes pelo método das tentativas, chegamos ao resultado: fixando 1 mol de Na 2 C, conforme solicita o enunciado, obtemos: 1 Na 2 C + 2Na 2 S + 4SO 2 3 Na 2 S 2 + 1CO 2. 33) Para retirar manchas de roupas coloridas, existe, no mercado, um produto alvejante sem cloro, cuja eficácia está associada ao seu "poder O 2 ". O principal componente desse produto é o percarbonato de sódio, cuja fórmula é 2Na 2 C.3H 2 O 2. A adição de carbonato de sódio permite a obtenção de um peróxido de hidrogênio mais estável, de fácil transporte, e que se dissolve com facilidade em água, liberando H 2 O e O 2 gasoso, o qual tem o poder de branquear e desinfetar. Na decomposição do peróxido de hidrogênio em H 2 O e O 2 gasoso, o peróxido de hidrogênio (A) é somente um agente oxidante. (B) é somente um agente redutor. (C) atua como detergente tensoativo. (D) atua como catalisador. (E) atua simultaneamente como oxidante e como redutor. QUESTÃ3 LETRA E A reação de decomposição do peróxido de hidrogênio pode ser representada pela equação abaixo, onde também estão indicados os estados de oxidação do oxigênio: Podemos observar que o oxigênio varia o nox duplamente: oxida para formar O 2 e reduz para formar O 2, podendo ser classificado como oxidante e redutor. 34) A coluna da esquerda, abaixo, relaciona cinco misturas realizadas experimentalmente; a coluna da direita, os tipos de classificação de quatro daquelas misturas. Associe corretamente a coluna da direita à da esquerda. 1 - NaN + H 2 O ( ) solução básica 2 - NH 4 CI + H 2 O ( ) solução não eletrolítica 3 -CaO + H 2 O ( ) solução ácida 4 -C 6 H 14 + H 2 O ( ) mistura com duas fases 5 -C 6 H 12 O 6 + H 2 O líquidas (A) (D) (B) (E) (C) QUESTÃ4 LETRA E Analisadas as soluções apresentadas, teremos CaO + H 2 O Ca(OH) 2 - base pouco solúvel, solução básica; C 6 H 12 O 6 (glicose) + H 2 O solução molecular, portanto, não condutora de corrente elétrica; NH 4 Cl + H 2 O NH 4 Cl é uma sal derivado de ácido forte (HCl) e base fraca (NH 4 OH), produzindo solução ácida; C 6 H 14 + H 2 O mistura de um hidrocarboneto (apolar) com a água (polar), resultando em um sistema heterogêneo. 35) A substituição de aço por alumínio permite a fabricação de veículos mais leves, com consequente redução do consumo de combustíveis e aumento da resistência à corrosão. Modelos mais recentes já empregam em torno de 90 kg de alumínio por unidade produzida. O alumínio é geralmente extraído da bauxita, minério que contém Al 2. Quantos automóveis podem ser produzidos com o alumínio obtido a partir de kg de bauxita, com 50% de Al 2? (A) 5. (B) 6. (C) 9. (D) 12. (E) 54. QUESTÃ5 LETRA B Como a amostra de bauxita contém 50 % de Al 2, parte-se de kg deste óxido. Portanto: 1 mol Al 2 (102 g) mols Al (54 g) kg m m = 540 kg de alumínio O enunciado da questão informa que cada automóvel possui 90 kg de alumínio. Logo, 90 kg automóvel 540 kg x x = 6 automóveis 36) A estrutura correta para um hidrocarboneto alifático saturado que tem fórmula molecular C 11 H 22 e que apresenta grupamentos etila e isopropila em sua estrutura é QUESTÃ6 LETRA C Um novo conceito estabelecido pela IU- PAC (União Internacional de Química Pura e Aplicada - html) define cadeia alifática como qualquer cadeia carbônica que não seja aromática. Entretanto, a maioria dos autores de livros didáticos utilizados no Ensino Médio apresenta cadeia alifática como sinônimo de cadeia aberta, sendo esse o senso comum. Portanto, todas as cadeias indicadas na questão são alifáticas, mas apenas a alternativa C é a que apresenta os substituintes etil e isopropil. A fórmula molecular C 11 H 22 representa a fórmula geral C n H 2n, que corresponde a alcenos ou cicloalcanos. 37) Pasteur foi o primeiro cientista a realizar a separação de uma mistura racêmica nos respectivos enantiômeros. Ele separou dois tipos de cristais do tartarato duplo de amônio e sódio que haviam sido obtidos por cristalização em tanques de fermentação de uvas. Estes cristais eram de duas formas quirais opostas, um dos quais correspondia à imagem especular não superponível do outro. Sobre esses cristais, são feitas as seguintes afirmações. I - Os dois tipos de cristais apresentam o mesmo ponto de fusão. II - Se um dos tipos de cristal for dissolvido em água e originar uma solução dextrógira, ao prepararmos outra solução, de mesma concentração, com o outro tipo de cristal, teremos uma solução levógira. III - Uma solução aquosa que contenha a mesma quantidade de matéria dos dois tipos de cristais não deverá apresentar atividade ótica. QUESTÃ7 LETRA E Uma molécula assimétrica é dita opticamente ativa. Nesta condição, apresenta pelo menos duas formas espaciais diferentes: uma chamada dextrógira (que exerce um desvio da luz planopolarizada para a direita) e outra levógira (que exerce desvio para a esquerda). Os isômeros dextrógiro e levógiro são enantiômeros um do outro. As propriedades físicas (pontos de fusão e ebulição, por exemplo) são iguais para os enantiômeros. A mistura equimolar destes isômeros é inativa e chamada racêmica. Logo as três afirmações estão corretas. 38) Observe os seguintes compostos. Em relação a estes compostos, é correto afirmar que o mais volátil e o mais solúvel em água são, respectivamente, (A) hexan-3-ona e hexan-1,3,6-triol. (B) hexan-3-ona e hexano. (C) hexano e hexan-3-ona. (D) hexano e hexan-1,3,6-triol. (E) hexan-1,3,6-triol e hexan-3-ona. QUESTÃ8 LETRA D Nos compostos orgânicos podemos prever a solubilidade e a temperatura de ebulição através da análise da polaridade molecular. Em ordem decrescente de ponto de ebulição e solubilidade em água, temos a seguinte ordem genérica: ácidos carboxílicos > alcoóis > aminas > cetonas e aldeídos >>> hidrocarbonetos Logo, o álcool hexan-1,3,6-triol é o mais solúvel e o hexano o de menor ponto de ebulição, isto é, o mais volátil. 39) A capsaicina e a zingerona são moléculas responsáveis pela sensação de ardor que sentimos ao ingerir pimenta malagueta e gengibre, respectivamente. Ver ilustração no site Os grupos funcionais comuns às duas moléculas são (A) amida, éter e hidroxila alcoólica. (B) cetona e hidroxila fenólica. (C) éster e hidroxila alcoólica. (D) cetona e éster. (E) éter e hidroxila fenólica. QUESTÃ9 LETRA E As funções orgânicas apresentadas são: 4
5 40) Assinale a alternativa que preenche corretamente a lacuna do enunciado abaixo. O polietileno é obtido através da reação de polimerização do etileno, que, por sua vez, é proveniente do petróleo. Recentemente, foi inaugurada, no Polo Petroquímico do RS, uma planta para a produção de plástico verde. Nesse caso, o etileno usado na reação de polimerização é obtido a partir do etanol, uma fonte natural renovável, e não do petróleo. A reação de transformação do etanol (CH 3 CH 2 OH) em etileno (CH 2 =CH 2 ) é uma reação de.... (A) substituição (D) eliminação (B) adição (E) oxidação (C) hidrólise QUESTÃO 40 LETRA D O fenômeno representa uma reação de eliminação, na qual uma molécula de álcool é desidratada a 170 C, obtendo-se um alceno. 41) A lisina é oxidada no organismo, formando a hidroxilisina, que é um componente do colágeno. Por outro lado, a degradação da lisina por bactérias durante a putrefação de tecidos animais leva à formação da cadaverina, cujo nome dá uma ideia de seu odor. Ver figura no site Assinale a afirmação correta em relação a estes compostos. (A) A hidroxilisina é um glicídio. (B) A cadaverina é um lipídio. (C) A lisina é uma proteína. (D) A lisina e a hidroxilisina são aminoácidos. (E) A hidroxilisina apresenta ligação peptídica. QUESTÃO 41 LETRA D Um aminoácido é uma substância que apresenta dois grupos funcionais: ácido carboxílico e amina. 42) O ácido fórmico é um ácido fraco, de fórmula HCOOH, encontrado nas formigas e na urtiga, e é o responsável pela sensação de queimadura. Considere as seguintes afirmações, a respeito de soluções aquosas deste ácido. I - Quanto mais diluída for uma solução de ácido fórmico, maior a concentração de íons H + presentes. II - O ph da solução de ácido fórmico aumenta com o aumento da diluição do ácido. III - O ph de uma solução com 0,1 mol L 1 de ácido fórmico é igual ao ph de uma solução de mesma concentração de ácido fórmico contendo 0,1 mol L 1 de formiato de sódio (HCOONa). (C) Apenas I e II. QUESTÃO 42 LETRA B I - Quanto mais diluída for a solução de ácido fórmico, menor será a concentração de íons H +. II Quanto mais diluída uma solução de ácido, menor a concentração de H +, e maior o ph da solução. III A adição do sal proporciona um aumento na concentração do ânion forniato, o que faz com que diminua a ionização do ácido. Com isso há um aumento no ph da solução. 43) A Lei de Hess, elaborada pelo químico suíço Germain Henry Hess em 1840, afirma, em terminologia moderna, que a variação de entalpia de uma reação química depende apenas dos reagentes de partida e dos produtos finais, e não depende do número de etapas ou intermediários necessários para a conversão dos primeiros nos últimos. A respeito da Lei de Hess, considere as seguintes afirmações. I - O metabolismo de um mol de glicose no organismo, formando gás carbônico e água, e a combustão de um mol de glicose num calorímetro liberam a mesma quantidade de calor. II - Se numa reação de isomerização o conteúdo de entalpia do produto for inferior ao do reagente, a reação será exotérmica. III - Há sempre a mesma variação de entalpia para uma dada reação de combustão de hidrocarbonetos, não importando se a água formada for líquida ou gasosa. (C) Apenas I e II. QUESTÃO 43 LETRA C I - Está correta, pois tanto o metabolismo da glicose no organismo quanto sua combustão em um calorímetro correspondem à mesma reação química. C 6 H 12 O O 2 6 CO H 2 O II - Está correta, pois toda reação cujo conteúdo de entalpia dos produtos é inferior ao dos reagentes é exotérmica, ou seja, libera calor. III - Está incorreta, pois a variação de entalpia da reação depende, também, do estado físico de reagentes e produtos. 44) Quando se adiciona água à cal viva, forma-se a cal extinta, de acordo com a reação abaixo. CaO (s) + H 2 O (I) Ca(OH) 2 (s) DH = 236 kcal mol 1 Se 5,6 g de cal viva forem adicionados a 1 kg de água, inicialmente a 20ºC, a temperatura final da água com cal, sabendo-se que o calor específico da água é de 1 cal g 1 (ºC) 1, será de aproximadamente (A) 23,6 ºC. (D) 53,6 ºC. (B) 33,6 ºC. (E) 63,6 ºC. (C) 43,6 ºC QUESTÃO 44 LETRA C Questão que exige a utilização da fórmula do calor sensível, em que há fornecimento de calor causando variação da temperatura do sistema: Q = m.c.δt A reação dada mostra que a reação de CaO com água libera 236 kcal por mol, ou seja, 56g de óxido de cálcio. Para 5,6g do óxido, que é 10 vezes menor, libera uma energia igual a 23,6 kcal (ou cal). Usando esta quantidade de calor Q e aplicando na fórmula, temos: = ΔT, onde 1000 é a massa da água (1 kg). Portanto, ΔT = 23,6 ºC. Se a variação de temperatura é 23,6 ºC e a temperatura inicial é 20 ºC, concluímos que a temperatura final é 43,6 ºC. 45) A reação relógio, equacionada abaixo, é uma curiosa reação bastante usada em demonstrações, na qual duas soluções quase incolores são misturadas e, após um determinado tempo, a mistura adquire subitamente uma coloração azul intensa, devido à formação de um complexo do iodo molecular com amido adicionado como indicador. 2 I (aq) + S 2 O 2 8 (aq) I 2 (aq) + 2 SO 2 4 (aq) (lenta) I 2 (aq) +2 S 2 O 2 3 (aq) 2 I (aq) + S 4 O 2 6 (aq) (rápida) A respeito dessa reação, considere as seguintes afirmações. I - A coloração azul aparece quando o iodo molecular formado na primeira etapa acumula, pois não é mais consumido na segunda etapa da reação. II - O tempo necessário para o aparecimento da cor azul não depende da concentração de tiossulfato. III - Para que haja formação da coloração azul, é necessário que o tiossulfato esteja estequiometricamente em excesso. (A) Apenas I (D) Apenas II e III. (B) Apenas li. (C) Apenas I e li. QUESTÃO 45 LETRA A Afirmativa I A falta de tiossulfato na segunda etapa da reação faz com que se acumule o complexo formado por I 2 e amido, o que dá coloração ao sistema. Correta. Afirmativa II O tempo de aparecimento da cor azul depende da concentração de tiossulfato, pois enquanto este estiver presente no sistema não se acumulará I 2. Errada. Afirmativa III Para que apareça a coloração azul no sistema, o tiossulfato deve estar em falta, e não em excesso. Errada. 46) Considere o enunciado abaixo e as três propostas para completá-lo. A produção de ácido sulfúrico de uma nação é considerada como bom indicador de sua força industrial. O ácido sulfúrico é produzido a partir de enxofre, de oxigênio e de água, por via do processo de contato. Uma das etapas desse processo consiste na oxidação do dióxido de enxofre a trióxido de enxofre, com o uso de oxigênio na presença de pentóxido de vanádio, que atua como catalisador, conforme a equação química abaixo. V 2 O 5 2 SO 2 + O 2(g) 2 S A ação do pentóxido de vanádio nessa reação é de 1 - diminuir o valor da constante de equilíbrio da reação. 2 - aumentar a concentração de S no equilíbrio. 3 - possibilitar outro mecanismo para a reação com energia de ativação menor. Quais propostas estão corretas? (A) Apenas 1. (D) Apenas 2 e 3. (B) Apenas 2. (E) 1,2 e 3. (C) Apenas 3. QUESTÃO 46 LETRA C Catalisadores são espécies químicas que diminuem a energia de ativação, através de caminhos alternativos, aumentando a velocidade de reação, sem interferir nos produtos formados. 47) A constante de equilíbrio da reação de conversão abaixo tem o valor de 0,5. Glicose 6-Fosfato Frutose 6-Fosfato Se essa reação parte de Glicose 6-Fosfato pura, o grau de conversão deste reagente em produto, quando a reação atinge o equilíbrio, é de aproximadamente (A) 10%. (B) 25%. (C) 33%. (D) 50%. (E) 66%. QUESTÃO 47 LETRA C A reação química apresentada tem constante de equilíbrio que será dada por O grau de conversão (grau de equilíbrio) será a razão entre a quantidade de glicose consumida e a quantidade inicial de glicose. Pode-se supor que, no equilíbrio, haja 1 mol de glicose e 0,5 mol de frutose (de acordo com o valor de Kc apresentado). Como a quantidade de frutose formada deve ser igual a de glicose consumida, conclui-se que a quantidade inicial de glicose era 1,5 mol (1,0 + 0,5). Assim sendo, Grau de conversão = 0,5/1,5 0,33 ou 33 % 48) A sacarose é extraordinariamente solúvel em água, como mostram os dados da tabela abaixo. Prepara-se uma solução saturada dissolvendo 65 g de sacarose em 25 g de água a 50 C. A quantidade de água a ser adicionada a esta solução inicial, de modo que, quando a solução resultante for resfriada até 30 C, tenhamos uma solução saturada de sacarose em água, sem presença de precipitados, é de aproximadamente (A) 2,5 g. (B) 4,5 g. (C) 10,0 g. (D) 15,8 g. (E) 40,0 g. QUESTÃO 48 LETRA B Para que a solução seja saturada e sem presença de precipitado, a relação entre a quantidade de soluto e a de solvente deve estar na exata proporção do coeficiente de solubilidade, que, a 30ºC, é de 220 g de sacarose para 100 g de H 2 O. Como a solução possui 65 g de soluto, teremos: 220 g sacarose g água 65g sacarose x x 29,5 g de água A solução já possuía 25 g de água, logo resta completá-la com aproximadamente 4,5 g de solvente. 49) A obtenção de metais puros por eletrodeposição é uma das aplicações práticas da eletroquímica. A eletrodeposição pode ser entendida como uma reação entre elétrons e íons. Sabendo-se que um mol de elétrons tem a carga de C (constante de Faraday), a massa de alumínio que será depositada a partir de uma solução de AI 2 (SO 4 ) 3 por uma corrente de 1,0 A fluindo durante 3 horas é de aproximadamente (A) 1,0 g. (B) 2,0 g. (C) 3,0 g. (D) 9,0 g. (E) 27,0 g. QUESTÃO 49 LETRA A O cálculo da massa pode ser feito pelo uso da fórmula abaixo. Inicialmente, calcula-se o equivalente-grama (E) do alumínio, dividindo sua massa molar (27 g/mol) pelo seu nox (+3). Logo, 9 g/equivalente. A corrente elétrica (i) é expressa em Ampère e o tempo em segundos. 50) Em viagens espaciais, é crucial que os mantimentos sejam leves e ocupem pouco espaço. Nestas situações, os alimentos são preparados por liofilização e precisam, antes do consumo, ser reidratados e reaquecidos. No processo de liofilização, a temperatura da amostra é reduzida até abaixo de 0 ºC, de modo que toda a água presente congele. Na sequência, a pressão é reduzida até abaixo da pressão do ponto triplo e, finalmente, o alimento é lentamente aquecido até uma temperatura acima do ponto de congelamento, de modo que a água sublime lentamente. Como resultado das três etapas do processo, há perda de até 97% do conteúdo de água. Considere o diagrama de fases da água esquematizado abaixo. O processo de liofilização acima descrito pode ser representado neste diagrama pela sequência de etapas (A) 1, 2 e 3. (D) 4, 5 e 1. (B) 2, 3 e 4. (E) 4, 5 e 2. (C) 3, 4 e 5. QUESTÃO 50 LETRA B O primeiro procedimento, de diminuição da temperatura da água de modo que congele, é indicado pela seta nº 2, que representa a passagem do estado sólido ao líquido. Somente a seta nº 3 representa um abaixamento de pressão, e só a nº 4 representa sublimação, que é a passagem do estado sólido para vapor. GEOGRAFIA 51) Leia o enunciado abaixo. Bolívar Cambará viajará, na próxima semana, de ônibus de Porto Alegre a São Paulo pela BR 101. Ao comprar sua passagem, conseguiu com a vendedora um assento junto à janela do ônibus para receber diretamente os raios solares no turno da manhã. Com base nesses dados, considere as seguintes afirmações. I - A viagem de Bolívar Cambará representará um deslocamento no pais no sentido sul-norte. II - Bolivar Cambará ocupará um assento no lado direito do ônibus. III - O assento de Bolivar Cambará ficará junto, a uma janela voltada para o leste. (D) Apenas II e III. QUESTÃO 51 LETRA E Ao sair de Porto Alegre e rumar para São Paulo, o ônibus de Bolívar Cambará descreve uma trajetória do sul para o norte. Neste sentido, o leste, lugar onde o sol surge pela manhã, estará à direita do ônibus. 52) Observe o quadro abaixo, que apresenta as coordenadas geográficas de cinco cidades do mundo. 5
6 Com base nos dados do quadro, é correto afirmar que (A) a cidade 1 se localiza no hemisfério ocidental. (B) a cidade 2 se situa na zona tropical do hemisfério norte. (C) o ponto antípoda da cidade 3 é 36 o N e 174 o W. (D) a cidade 4 se encontra na China. (E) a cidade 5 tem temperatura média anual de aproximadamente 23 o C. QUESTÃO 52 LETRA E A cidade 1 localiza-se no hemisfério oriental, pois está a 1º E; a cidade 2 localiza-se ao sul do Trópico de Câncer (23ºN) e, portanto, na zona temperada; o ponto antípoda (o ponto oposto) da cidade 3 é de 36ºN e 6ºW; a China localiza- se no hemisfério oriental e não no ocidental como propõe a alternativa 4. A cidade 5 localiza- se a 10ºN, o que a coloca na zona intertropical do planeta. 53) Um professor solicita aos alunos uma cópia reduzida de um mapa através de fotocopiadora. No mapa original, a distância entre A e B, que é de um centímetro, representa 500 metros na realidade. A respeito desta situação, assinale a alternativa correta. (A) A distância entre A e B, na cópia reduzida, continua a representar 500 metros. (B) A escala do mapa original é 1:50.000, e a da cópia reduzida é 1: (C) A distânda entre A e B, na cópia reduzida, passa a representar metros. (D) A escala do mapa original é 1:5.000, e a da cópia reduzida é 1: (E) A distância entre A e B, na cópia reduzida, representa 50 metros. QUESTÃO 53 LETRA A A questão solicita o raciocínio do aluno sobre escalas, que é a relação em um mapa entre a realidade e a sua representação gráfica. Pode-se mudar o tamanho do traçado no mapa, aumentando-o ou diminuindo-o em função da escala utilizada, mas a distância real continua sendo a mesma em qualquer situação. 54) A coluna da esquerda, abaixo, apresenta o nome de duas das principais projeções cartográficas; a da direita, características relacionadas a uma ou a outra dessas projeções. Associe adequadamente a coluna da direita à da esquerda. 1 -projeção de ( ) mantém as formas dos Mercator continentes 2 -projeção de ( ) as regiões polares aparecem Peters muito exageradas ( ) dá destaque ao mundo subdesenvolvido ( ) é excelente para a navegação (A) (D) (B) (E) (C) QUESTÃO 54 LETRA B Deve-se considerar que a projeção de Peters nasceu com cunho de crítica a de Mercator, valorizando as áreas subdesenvolvidas da Terra. Na projeção de Peters, as áreas dos continentes são precisamente representadas, e as formas, distorcidas. Mercator, por sua vez, primou pela forma dos continentes em detrimento da área. Por se tratar de uma projeção cilíndrica os paralelos e os meridianos são traçados ortogonalmente. Historicamente essa projeção vinculou-se às navegações por facilitar o traçado de rotas marítimas. 55) Observe a figura abaixo, que representa a disposição das placas Iitosféricas. Assinale a altemativa correta a respeito desta figura. Ver figura no site (A) A letra C indica o limite entre placas Iitosféricas convergentes. (B) O número 3 indica a placa Iitosférica denominada Nazca. (C) O número 1 indica a placa Iitosférica denominada Pacífica. (D) O número 2 indica a placa Iitosférica denominada Americana. (E) A letra D indica o limite entre placas Iitosféricas divergentes. QUESTÃO 55 LETRA A A resposta correta, a letra C, indica o limite convergente entre as placas de Nasca e a Placa Sul-Americana. Nas demais alternativas, o número 3 indica a placa Africana; o número 1 a placa Norte-Americana; o número 2 a placa Euroasiática; e a letra D indica o limite convergente entre as placas do Pacífico e Norte- Americana. 56) A figura abaixo representa uma bacia hidrográfica e sua rede de drenagem. Os elementos destacados com as letras A, B e C indicam, respectivamente, (A) afluente, foz e efluente. (B) nascente, exutório e divisor de águas. (C) nascente, afluente e divisor de águas. (D) divisor de águas, exutório e afluente. (E) efluente, divisor de águas e foz. QUESTÃO 56 LETRA B O desenho apresentado na questão representa uma bacia hidrográfica e seus afluentes. As nascentes do rio estão representadas pela letra A. Já a foz, exutório ou seu nível de base pela letra B. A letra C representa o relevo, que interfere na divisão das águas em uma região, pois as águas sempre correm das partes mais altas para as mais baixas. 57) As figuras abaixo representam uma comparação entre um riacho natural e outro canalizado. Considere as seguintes afirmações, sobre os efeitos da canalização na dinâmica de um curso d água. I - A retirada da cobertura vegetal ocasiona o desaparecimento da sombra, causando danos à flora e aos organismos aquáticos sensíveis ao calor. II - A eliminação dos meandros fluviais e da cobertura vegetal aumenta a velocidade das águas do riacho. III - A canalização consiste em retilinizar, aprofundar e revestir leitos fluviais, com o objetivo de aumentar a capacidade de infiltração dos solos e, assim, diminuir o extravasamento do leito fluvial. (D) Apenas I e II. QUESTÃO 57 LETRA D Ao se canalizar o curso de um rio, impermeabilizando o seu leito, é mister que haja uma considerável diminuição na infiltração das águas no solo. O que significará, também, um aumento nas vazões máximas no curso da água. Já a eliminação dos meandros fluviais, que são as curvas que um rio descreve em sua trajetória, favorece o aumento da velocidade das águas, uma vez que essas curvas significam desvios na correnteza. Ao ser retirada a mata ciliar, aumenta-se a erosão das encostas, levando ao assoreamento do rios e ao desaparecimento da sombra, trazendo malefícios à flora e à fauna. 58) Assinale com V (verdadeiro) ou F (falso) as afirmações abaixo, referentes à constituição e à formação dos solos. ( ) O horizonte A de um perfil de solo é a camada mineral mais próxima à superfície e caracteriza-se pela concentração de matéria orgânica. ( ) Os solos das regiões áridas e semiáridas, quando comparados aos solos das regiões úmidas, comumente apresentam grandes quantidades de argila e de matéria orgânica. ( ) Nas áreas de declividade acentuada, os solos são mais rasos porque a alta velocidade de escoamento das águas diminui a infiltração e, consequentemente, o intemperismo. ( ) A acidificação dos solos é um processo que ocorre naturalmente na biosfera, porém os solos das regiões tropicais são submetidos o ano inteiro a altas temperaturas e à ação intensa das chuvas, favorecendo a formação de solos mais ácidos. (A) F - V - F - V. (D) F - V - V - F. (B) V - F - V - V. (E) V - F - F - F. (C) F - F - V - V. QUESTÃO 58 LETRA B Em um perfil de solo, o horizonte A representa a camada mais próxima da superfície e concentra a matéria orgânica para o desenvolvimento das plantas. O horizonte B apresenta material intemperizado e constitui-se num estágio intermediário entre os horizontes B e C. O horizonte C corresponde ao material mais próximo da rocha matriz. Nas regiões áridas e semi-áridas, onde predomina o intemperismo químico, os solos são rasos e pedregosos pela falta de água, que dissolve os materiais retirados das rochas. Nas áreas com grande declividade a velocidade do escoamento superficial diminui a infiltração da água, impedindo a formação de solos espessos. De maneira geral, a formação dos solos ácidos é o resultado da combinação de muitos fatores, com grande importância para as condições climáticas, em termos de alta temperatura e intensidade de chuvas. Estas condições favorecem a rápida decomposição da rocha com a lixiviação de bases trocáveis e a consequente intemperização do solo e formação da acidez. Em função disso, a maioria dos solos tropicais apresenta níveis de acidez elevados. 59) Considere o enunciado abaixo e as três propostas para completá-lo. O fenômeno oceânico-atmosférico La Nina caracteriza-se por um resfriamento anormal nas águas superficiais do oceano Pacífico Equatorial nos setores central e oriental. Entre os efeitos desse fenômeno, pode-se citar corretamente 1 - a tendência de chuvas abundantes no norte e no leste da Amazônia. 2 - o aumento da precipitação e da vazão dos rios no Uruguai. 3 - a existência de chuvas abaixo da normal climatológica no Rio Grande do Sul. Quais propostas estão corretas? (A) Apenas 1. (D) Apenas 1 e 3. (B) Apenas 2. (E) Apenas 2 e 3. (C) Apenas 3. QUESTÃO 59 LETRA D O vento leste, responsável pelo deslocamento de água superficial aquecida em direção à Austrália desencadeia o processo de ressurgência de água fria. Estando as águas mais frias, ocorre menor evaporação, logo há menos umidade disponível na atmosfera da região centro-sul da América do Sul. O fenômeno La Niña traz secas ao verão gaúcho e uruguaio, dificultando a produção de verão de culturas irrigadas, como o arroz. No entanto, outras regiões brasileiras, como a Norte e Nordeste recebem maiores índices pluviométricos, favorecendo as culturas sazonais na caatinga. 60) Considere as afirmações abaixo, sobre grandes paisagens naturais do globo. I - Os desertos, como o Saara, o Gobi e o Kalahari, caracterizam-se pelos contrastes térmicos entre o dia, extremamente quente, e a noite, bastante fria. II - Os Alpes, na Europa, os Andes, no continente americano, o Atlas, na África, são cadeias montanhosas formadas por dobramentos antigos de idade pré-cambriana. III - As amplitudes térmicas dos climas tropical e equatorial, tanto diárias quanto anuais, são baixas; consequentemente, a variação da temperatura é geralmente pequena. QUESTÃO 60 LETRA C Um dos principais fatores do clima diz respeito à quantidade de umidade presente no ar. A água, por possuir um grande calor específico, contribui para uma menor variação de temperatura. Por conta disso, paisagens naturais mais úmidas tendem a apresentar uma baixa variação térmica, ao passo que ambientes desérticos, possuem uma grande amplitude térmica, podendo apresentar uma variação diária de mais de 40 C. No que diz respeito às paisagens montanhosas dos Andes, dos Alpes e dos Atlas, tratamse de cordilheiras ativas, formando áreas conhecidas como dobramentos modernos. Essas regiões são bastante suscetíveis a terremotos e vulcanismos. 61) Assinale a alternativa que preenche corretamente as lacunas do texto abaixo, na ordem em que aparecem. O chaparral, ou vegetação mediterrânea, é um bioma marcado por verões secos e quentes. A paisagem é formada basicamente por maquis e garrigues, espécies arbustivas de folhas duras e grossas, sempre verdes, adaptadas à longa estiagem. Tipicamente europeia, essa paisagem vegetal aparece também nas extremidades setentrional e meridional da África e em áreas costeiras da Austrália meridional, do... e... (A) sul da Argentina - de Madagascar (B) sul da Argentina - da Nova Zelândia (C) sul da Argentina - do sudeste dos Estados Unidos (D) Chile - do sudoeste dos Estados Unidos (E) Chile - do Peru QUESTÃO 61 LETRA D A vegetação descrita no enunciado é típica das regiões onde os invernos apresentam-se chuvosos, e os verões secos. Esta variação climática recebe o nome de Mediterrâneo, pois é característica da porção sul da Europa, às margens do mar Mediterrâneo. Outras regiões onde encontramos esta variação climática além das mencionadas na questão são o sul do Chile, e o sudoeste dos Estados Unidos, próximo à fronteira com o México. Detalhe: a própria denominação Chaparral, usada no enunciado, é típica dessa fronteira estadunidense-mexicana, o que poderia auxiliar na resposta. 62) Observe a figura abaixo. Ver figura no site A anamorfose geográfica é um recurso cartográfico que representa as superfícies dos países em áreas proporcionais a uma determinada quantidade. A anamorfose acima representa (A) o Produto Nacional Bruto (PNB). (B) a população mundial. (C) as reservas de petróleo. (D) a produção de energia hidroelétrica. (E) o Índice de Desenvolvimento Humano (IOH). QUESTÃO 62 LETRA A Na anamorfose apresentada na questão os países que possuem as maiores superfícies são Estados Unidos e Japão, seguidos por Alemanha, China, Reino Unido e Itália, entre outros. Essa informação significa que o fenômeno representado ali é o Produto Nacional Bruto dos países. (Note que o continente africano aparece com dimensões insignificantes). Caso essa anamorfose se referisse à população (alternativa B), China e Índia deveriam ser os países com maiores dimensões; a reservas de petróleo (C), os países da Península Arábica e o Canadá; energia hidrelétrica (D), o Brasil; e o IDH (E), Noruega, Austrália e Islândia. 63) Observe a figura abaixo, que apresenta informações sobre o petróleo mundial. Ver figura no site Em relação à figura, considere as afirmações que seguem. I - Entre as áreas favoráveis, destacam-se as explorações petrolíferas localizadas em território russo e no Oriente Médio. II - O local do vazamento de petróleo ocorrido nos Estados Unidos em abril de 2010 não corresponde a uma região de alta produtividade de petróleo. III - As regiões de alta produtividade correspondem às áreas de maior número de campos petrolíferos. 6
7 (D) Apenas II e III. QUESTÃO 63 LETRA A As grandes jazidas de petróleo localizam-se em estruturas conhecidas como bacias sedimentares, terrenos normalmente mais planos e baixos, típicos de mares costeiros e planícies continentais. O mapa mostra que as regiões de alta produtividade de petróleo não necessariamente são aquelas que apresentam a maior quantidade de poços. Assim, podemos destacar a grande presença de campos petrolíferos no continente europeu, porém sem nenhuma área de superprodução. 64) Observe o mapa do continente africano abaixo. Em relação à área sombreada do mapa, são feitas as seguintes afirmações. I - Nela, encontra-se a Nigéria, país com grandes reservas de ouro e diamante, cobiçadas por grupos rebeldes que reivindicam melhor distribuição das receitas advindas da exploração das minas. II - Em parte do litoral, localiza-se a Somália, que enfrenta um caos político e institucional, devido aos ataques de piratas e embarcações que navegam nas águas próximas à costa. III - Na área, atuam forças militares da Organização das Nações Unidas (ONU) e da União Africana (UA), que tentam prevenir os ataques e as ameaças contra civis na região do Darfur, no oeste do Sudão, palco de conflito entre árabes e não-árabes. (D) Apenas II e III. QUESTÃO 64 LETRA D A área em destaque no mapa africano abrange os países Sudão, Eritréia, Djibuti, Quênia e a Somália, na região do Chifre da África. A Nigéria, país rico em petróleo, localiza-se na região africana do Golfo da Guiné, junto à porção equatorial do oceano Atlântico. Por sua vez, a Somália, país fragmentado em diferentes territórios disputados por grupos islâmicos, expande tais conflitos para o mar que o circunda, agindo em especial, sobre os grandes navios petroleiros que navegam nas águas do golfo de Áden. Já o Sudão, o maior país africano, está inserido na área em destaque e apresenta graves conflitos de origem religiosa e econômica, sobretudo na área conhecida como Darfur, na fronteira com Chade. 65) O relatório da Organização para Cooperação e Desenvolvimento Econômico (OCDE), publicado em 2009, denominado Perspectivas Econômicas da América Latina 2010, informa que mais de 20 milhões de latino-americanos e caribenhos residem fora de seu país de nascimento, encontrando-se cerca de 75% deles nos Estados Unidos. Em relação a essa temática, considere os enunciados abaixo. 1 - A imigração de haitianos é historicamente significativa no país. Os trabalhadores haitianos foram inicialmente atraídos pela escassez de mão de obra e pelos salários relativamente elevados nas plantações de cana-de-açúcar. 2 - O país registrou fluxos de emigração em grande escala nas últimas décadas e, atualmente, cerca de 4,7% dos nacionais desse país vivem no exterior. Venezuela e Estados Unidos são os prindpais países de destino, seguidos por Espanha, Equador e Panamá. Os países a que se referem os enunciados 1 e 2 são, respectivamente, (A) México e Peru. (D) Cuba e Costa Rica. (B) Jamaica e Bolívia. (E) Belize e Suriname. (C) República Dominicana e Colômbia. QUESTÃO 65 LETRA C Na afirmativa 1, temos o Haiti, país vizinho da República Dominicana. Ambos países estão situados nas porções oeste e leste, respectivamente, da ilha de Hispaniola, no mar do Caribe. A República Dominicana é um tradicional destino de migração dos haitianos que buscam escapar do caos e pobreza existentes em seu país. Já a afirmativa 2 nos traz a Colômbia, país que em razão dos conflitos envolvendo as Forças Armadas Revolucionárias da Colômbia (FARC), grupos paramilitares e o exército colombiano, tem apresentado um dos maiores contingentes de emigrantes nos anos recentes. 66) A final da Copa do Mundo FIFA de 2010 deu-se entre dois países europeus: Espanha e Países Baixos (também conhecido como Holanda). Com relação a cada um desses países, considere as afirmações abaixo. 1 - É integrante da União Europeia. 2 - Adota como moeda única o euro. 3 - O regime político adotado é o de República Parlamentarista. 4 - A maior parte de seu PIB é de origem agropecuária e industrial. São válidas para ambos os países somente as afirmações (A) 1 e 2. (D) 2 e 4. (B) 1 e 3. (E) 3 e 4. (C) 2 e 3. QUESTÃO 66 LETRA A Espanha e Holanda são, ambos, países integrantes da União Européia (UE) e da Zona do Euro grupo de países no interior da UE que adotam o Euro como moeda oficial. Porém, ambos são monarquias constitucionais, regimes onde a chefia de Estado é exercida por um Rei (Espanha) ou Rainha (Holanda), e a chefia de governo é exercida pelo Primeiro-Ministro. Já na questão econômica, ambos encontram-se naquilo que podemos denominar economias pós-industriais, com mais de 70% de seu PIB composto pelo setor terciário (serviços). 67) Ver questão no site QUESTÃO 67 LETRA C Planaltos são formas de relevo com altitudes superiores a 300m. Podem ser encontrados em qualquer estrutura geológica. Os planaltos podem apresentar-se sob a forma de escarpas, serras e chapadas, que são superfícies de topos planos. No Brasil predominam os planaltos e as depressões. As depressões podem ser absolutas (abaixo do nível do mar) e relativas (deprimidas em relação às áreas ao seu redor). Elas têm altitudes entre 100 e 500m e possuem estrutura geológica variada. Resultam de intenso processo erosivo. Entre as depressões do Brasil destacam-se a Depressão Periférica da Borda Leste da Bacia do Paraná e a Depressão Central do Rio Grande do Sul. Os tabuleiros no Nordeste do Brasil são, em geral, sedimentares e encontrados ao longo da costa. Possuem altitudes entre 20 e 50m e, trabalhados pelo mar, formam falésias. 68) Assinale com V (verdadeiro) ou F (falso) as afirmações abaixo, referentes ao litoral brasileiro. ( ) Os manguezais brasileiros têm ampla distribuição longitudinal, e cerca de 85% deles concentram-se no litoral dos estados de São Paulo, Paraná e Santa Catarina. ( ) A Ilha da Trindade e o Arquipélago de Martin Vaz são pontos emersos de uma cadeia de vulcões submarinos extintos, situados defronte à costa do estado do Espírito Santo. ( ) Na porção oeste do oceano Atlântico, na costa nordeste do Brasil, a Corrente Equatorial Sul é interceptada pelo continente sul-americano, desviando-se para sul e para norte, formando as correntes do Brasil e das Guianas, respectivamente. ( ) O único fenômeno da ressurgência costeira bem conhecido no Brasil é o da região de Salvador, na Bahia, o que contribui para tornar a região uma das mais produtivas de pescado no país. (A) V - V - F - F. (D) F - V - F - V. (B) F - V - V - F. (E) F - F - V - V. (C) V - F - F - V. QUESTÃO 68 LETRA B O litoral brasileiro se subdivide conforme as características físico-naturais a que está submetido. Assim, de modo geral, a costa brasileira é banhada por águas quentes da corrente Equatorial Sul que, ao alcançar o litoral nordestino, se subdivide na corrente das Guianas, rumando para do Caribe; e na corrente do Brasil, que ruma para o litoral sul do país. As águas aquecidas que banham o Brasil possibilitam o surgimento dos manguezais junto a ambientes mixoalinos (mistura de águas doce e salgada) com pouca energia e oxigenação, áreas costeiras protegidas das fortes ondulações. O mangues estendem- se desde o litoral sul de SC, no município de Laguna até o litoral norte do Brasil, no estado do Amapá. Dentre as características litorâneas tem-se ainda a existência de inúmeras ilhas originadas de vulcões extintos, surgidos durante o processo de fragmentação da América do Sul e da África. O Brasil possui o fenômeno de ressurgência junto ao litoral do Rio de Janeiro, mais especificamente no município de Cabo Frio, possibilitando uma pesca abundante na região. 69) Em 2010, o Instituto de Pesquisa Econômica Aplicada (IPEA) publicou comunicado sobre estudo que analisa a situação da pobreza brasileira entre 1995 e As linhas de pobreza absoluta e de pobreza extrema, utilizadas no estudo, foram estabelecidas pelo critério de rendimento médio domiciliar per capital respectivamente, de até meio salário mínimo mensal e de até um quarto de salário mínimo mensal. Em relação a essa temática, é correto afirmar que (A) a diminuição das taxas de pobreza absoluta e extrema entre os estados brasileiros ocorreu de maneira simétrica e uniforme. (B) os estados que apresentaram maior diminuição das taxas de pobreza absoluta, no período de 1995 a 2008, foram Santa Catarina e Paraná. (C) as taxas de pobreza tanto absoluta quanto extrema caíram em todas as grandes regiões brasileiras, exceto no Nordeste, onde ocorreu aumento da pobreza absoluta e extrema. (D) o forte crescimento econômico verificado no período de 1995 a 2008 no país foi suficiente para elevar o padrão de vida de todos os brasileiros. (E) Pernambuco, Ceará e Bahia foram os estados que, em 2008, apresentaram a maior desigualdade de renda no país. QUESTÃO 69 LETRA B Mesmo parecendo uma questão na qual o aluno teria que ter conhecimento prévio da pesquisa em si, a pergunta faz menção à temática, que é a evolução da pobreza no Brasil. É de ciência da maior parte da população que o país vivencia uma onda de prosperidade e distribuição de renda, ainda que parca, que tem surtido efeitos positivos na sociedade. Mas, para um país continental, com todas as disparidades regionais, não seria possível que isso ocorresse de maneira simétrica, portanto excluímos a A. Na alternativa C, a inverdade está na afirmação sobre o Nordeste que através do programa de transferência de renda, também teve seus índices diminuídos. Na D devemos tomar cuidado com a afirmação de que todos os brasileiros elevaram seus padrões de vida a partir do crescimento econômico, lembrando que não adianta crescimento econômico se não há distribuição dos recursos. Na E poderíamos questionar se a maior desigualdade não estaria na região Sudeste, ou ainda que a pesquisa apresentada não estaria avaliando um único ano, e sim um período maior. Nos resta a alternativa B, que faz menção a dois dos seis melhores estados no ranking do IDH, Índice de Desenvolvimento Humano, o que, portanto, é um forte indicador da diminuição da pobreza. 70) Recente pesquisa, divulgada em 2010 pelo IBGE, retratou a situação atual do saneamento básico brasileiro, a partir de dados de Em relação a esse tema, é correto afirmar que (A) aumentou o percentual de municípios brasileiros que destinam seus resíduos sólidos a vazadouros a céu aberto (lixões). (B) apenas um terço dos domicílios brasileiros são abastecidos de água por rede geral. (C) Pará e Amazonas estão entre os estados brasileiros com o maior percentual de municípios que distribuem água sem nenhum tipo de tratamento. (D) a quase totalidade dos municípios da Região Sul tem rede coletora de esgoto. (E) dois terços dos municípios brasileiros com rede de esgotamento geral fazem o tratamento de seus esgotos. QUESTÃO 70 LETRA C Segundo a Pesquisa Nacional de Saneamento Básico (PNSB) 2008, cujos resultados apresentam as variações entre os dados coletados em 2000 e 2008, em 6,6% dos municípios brasileiros a água é distribuída sem nenhum tipo de tratamento um índice pequeno quando comparado aos 18,1% do ano A região com o maior percentual desses municípios é a Norte 20,8% do total com Pará e Amazonas apresentando, respectivamente, os maiores percentuais. A região Nordeste vem na sequência neste item, com Piauí e Maranhão como os estados com maiores índices. Quanto às demais alternativas, na A o número de municípios que destinam seus resíduos sólidos aos vazadouros (lixões) a céu aberto diminuiu de 72,3% para 50,8% no período; na B, 99,4% dos municípios brasileiros têm abastecimento de água por rede geral; na D, apenas a região Sudeste apresenta um índice elevado de municípios com rede coletora de esgoto (95,1%), sendo que todas as demais apresentam índices menores que 50%; e na E, são apenas 28,5% os municípios brasileiros que fazem tratamento de esgoto. 71) Com relação ao recente processo de urbanização brasileiro, é correto afirmar que (A) o fenômeno urbano, no Brasil, caracteriza-se pelo crescimento homogêneo das aglomerações urbanas, sobretudo pelo aumento da produção industrial. (B) o maior controle por parte do Estado brasileiro contribui para a diminuição do crescimento das grandes cidades brasileiras. (C) o aumento da participação das cidades médias, na economia nacional, favorece a desconcentração da riqueza dos grandes centros urbanos do Brasil. (D) a aceleração do movimento migratório para as grandes metrópoles nacionais é impulsionada pelo crescimento industrial e pelas melhorias na qualidade de vida. (E) o aumento de organizações criminosas com poder paralelo ao Estado dificulta o crescimento das médias cidades e a implementação de políticas habitacionais. QUESTÃO 71 LETRA C O processo de rápida urbanização, vivenciado no Brasil nos idos dos anos 70, contribuiu para que hoje existam grandes aglomerados populacionais sem a devida estrutura, seja ela econômica, social, urbana ou cidadã. Tal condição gera ilhas de acumulação e também enclaves de pobreza e a grande diferença entre elas aumenta a chance de confrontos urbanos. Para fugir desse problema, uma parcela mais abastada da população acaba migrando para cidades que são menores, mas que sejam capazes de promover certos benefícios da urbanidade as cidades médias o que, por sua vez, acaba por distribuir a riqueza no país. 72) O mapa abaixo apresenta algumas das bacias hidrográficas do estado do Rio Grande do Sul. Em relação a essas bacias hidrográficas, são feitas as seguintes afirmações. I - O rio Santa Maria é o principal curso fluvial da bacia identificada pelo número 1, que se caracteriza pela expansão da atividade mineradora, graças à abundância de carvão naquela área. II - A bacia identificada pelo número 2 corresponde à dos rios Vacacaí-Vacacaí-Mirim, cujo rio principal desemboca no rio Jacuí e, portanto, faz parte da Região Hidrográfica do Guaíba. III - A bacia identificada pelo número 3 integra a Região Hidrográfica Litorânea, abrangendo área de municípios como Bagé, Caçapava do Sul e Tapes. 7
8 (D) Apenas I e II. (E) Apenas II e III. QUESTÃO 72 LETRA E Na região hidrográfica do Rio Uruguai, está a Bacia do Ibicuí, identificada com o número 1, que tem entre os seus tributários o rio Santa Maria, o que já seria suficiente pra invalidar a afirmativa I, que indica que o Santa Maria é o rio principal. Mas ainda temos a referência à mineração de carvão, que não ocorre ali e sim na bacia do Baixo- Jacuí, pertencente à Região Hidrográfica do Guaíba. A bacia identificada pelo número 2 é sim a do Vacacaí-Vacacaí Mirim que, ao desembocar no Jacuí, carrega consigo muito da poluição gerada pela grande presença da rizicultura (arroz) na bacia. A bacia 3, bacia do rio Camaquã, drena boa parte do Planalto Sul-Rio-Grandense, e desemboca na Laguna dos Patos, que por sua vez atinge o oceano Atlântico através do canal de Rio Grande. 73) Considere as seguintes afirmações, sobre os problemas ambientais no Rio Grande do Sul. I - Entre os assentamentos humanos mais atingidos por inundações, nesta última década, estão os que se localizam às margens dos rios dos Sinos, Gravataí e caí, que fazem parte da bacia hidrográfica do Guaíba. II - A partir de 1950, difundiram-se, no estado, monoculturas agrícolas em grandes extensões com o uso de mecanização, resultando no surgimento de processos erosivos e perdas de solos, principalmente nas regiões do alto Uruguai e do alto Jacuí. III - Nos meses de verão, frequentemente, constata-se a elevação dos índices de coliformes fecais nas praias, rios e lagoas de alguns municípios da planície costeira, devido à ocupação mais intensa e à falta de infraestrutura em saneamento básico. (D) Apenas II e III. QUESTÃO 73 LETRA E Somente o uso coerente da água garantirá que as próximas gerações também disponham dela. Sinos, Gravataí e Caí são rios que em seus cursos inferiores apresentam alta taxa de assoreamento, uma vez que em suas margens erguem-se grandes cidades da RMPA (Região Metropolitana de Porto Alegre) ou seja: o solo é bastante exposto, e grande quantidade de materiais são carreados para o leito, fazendo com que os referidos rios transbordem em enchentes nas épocas de mais chuvas. No Planalto Médio do RS, região também conhecida como Zona da Produção, os fortes usos do solo perante a mecanização, principalmente da soja e trigo, contribuíram sim para a perda de solo. O saneamento básico, principalmente coleta e tratamento do esgoto cloacal, tem sido a política do governo gaúcho, uma vez que a planície costeira, principalmente no Litoral Norte, está com grandes taxas de crescimento urbano e, sazonalmente recebe fluxo acentuado de migrantes, que, devido às condições atuais de saneamento, contribuem para a elevação dos índices de coliformes fecais. 74) Observe as pirâmides populacionais abaixo, referentes à população do Rio Grande do Sul. Com base na leitura destas pirâmides populacionais, considere as seguintes afirmações, referentes ao intervalo de 2000 a I - A população maior de 60 anos diminui. II - A população total aumenta. III - A expectativa de vida aumenta. (D) Apenas I e II. (E) Apenas II e III. QUESTÃO 74 LETRA E A análise de população seria uma questão que o aluno enfrentaria nesse exame uma vez que em 2010 tivemos a realização do 12º censo brasileiro (1872, 1890, 1900, 1920, 1940, 1950, 1960, 1970, 1980, 1991, 2000 e 2010). Fica claro na comparação entre pirâmides que teremos, em função de uma série de melhorias nos âmbitos sociais, políticos e econômicos, o gradual envelhecimento da população; levando ao aumento da população total, mesmo com a contínua diminuição da natalidade/fecundidade. 75) A tabela abaixo fornece dados de alguns dos municípios gaúchos que, em 2008, tinham mais de 100 mil habitantes. Assinale a alternativa que apresenta os nomes dos municípios gaúchos correspondentes aos números 1, 2, 3 e 4, respectivamente. (A) Uruguaiana - Alvorada - Pelotas - Caxias do Sul (B) Caxias do Sul - Uruguaiana - Alvorada - Pelotas (C) Caxias do Sul - Uruguaiana - Pelotas - Alvorada (D) Pelotas - Alvorada - Uruguaiana - Caxias do Sul (E) Pelotas - Uruguaiana - Alvorada - Caxias do Sul QUESTÃO 75 LETRA B O aluno atento estaria preparado para a resolução dessa questão, uma vez que poderia optar por pelo menos duas análises distintas: área e população. Sobre a área, é bastante tranquilo relembrar que a metade sul do RS é formada por grandes propriedades e historicamente seus municípios apresentam grandes territórios, como, por exemplo, Uruguaiana e Pelotas. Já Alvorada, município da Região Metropolitana de Porto Alegre, tenderia a apresentar área mais modesta em função da grande densidade da região. Tratando da população, temos Porto Alegre como a cidade de maior contingente populacional, seguida de Caxias do Sul, Pelotas, Canoas, Gravataí, Santa Maria, Viamão, Novo Hamburgo, Alvorada e São Leopoldo, cidades com mais de 200 mil habitantes. EXPEDIENTE Biologia: André Fozzy, César Matos, Cesar Milheiro e Cláudia Senandes Química: Alberto Becker, Carlos Valério, Flávio Schifino, Jorge Ruffini, Kadu Barbosa e Marcus Ribeiro Geografia: Alexandre Rosa, Felipe Costa, Marcelito Câmara, Teresinha Marques e Tomás Reck Gastronomia: Marcelo Cóser Coordenador: André Fozzy 8
RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011
 RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011 Questão 26 Como a questão pede a separação do sólido solúvel do líquido, o único processo recomendado é a destilação simples. Lembrando que filtração e decantação
RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011 Questão 26 Como a questão pede a separação do sólido solúvel do líquido, o único processo recomendado é a destilação simples. Lembrando que filtração e decantação
BIOLOGIA. Em relação a esse experimento inovador, é correto afirmar que
 BIOLOGIA 01. Após publicar os resultados de seus experimentos que levaram à construção da primeira célula bacteriana controlada por um genoma sintético, Craig Venter declarou: Esta é a primeira criatura
BIOLOGIA 01. Após publicar os resultados de seus experimentos que levaram à construção da primeira célula bacteriana controlada por um genoma sintético, Craig Venter declarou: Esta é a primeira criatura
BIOLOGIA. A sequência correta de preenchimento dos parênteses, de cima para baixo, é
 BIOLOGIA 01 Após publicar os resultados de seus experimentos que levaram à construção da primeira célula bacteriana controlada por um genoma sintético, Craig Venter declarou: Esta é a primeira criatura
BIOLOGIA 01 Após publicar os resultados de seus experimentos que levaram à construção da primeira célula bacteriana controlada por um genoma sintético, Craig Venter declarou: Esta é a primeira criatura
CICLOS BIOGEOQUÍMICOS
 CICLOS BIOGEOQUÍMICOS O fluxo de energia em um ecossistema é unidirecional e necessita de uma constante renovação de energia, que é garantida pelo Sol. Com a matéria inorgânica que participa dos ecossistemas
CICLOS BIOGEOQUÍMICOS O fluxo de energia em um ecossistema é unidirecional e necessita de uma constante renovação de energia, que é garantida pelo Sol. Com a matéria inorgânica que participa dos ecossistemas
Água e Solução Tampão
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
QUÍMICA QUESTÃO 41 QUESTÃO 42
 Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
PROVA DE QUÍMICA - 1998 Segunda Etapa
 PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PlanetaBio Resolução de Vestibulares UFRJ 2007 www.planetabio.com
 1-O gráfico a seguir mostra como variou o percentual de cepas produtoras de penicilinase da bactéria Neisseria gonorrhoeae obtidas de indivíduos com gonorréia no período de 1980 a 1990. A penicilinase
1-O gráfico a seguir mostra como variou o percentual de cepas produtoras de penicilinase da bactéria Neisseria gonorrhoeae obtidas de indivíduos com gonorréia no período de 1980 a 1990. A penicilinase
QUÍMICA CELULAR NUTRIÇÃO TIPOS DE NUTRIENTES NUTRIENTES ENERGÉTICOS 4/3/2011 FUNDAMENTOS QUÍMICOS DA VIDA
 NUTRIÇÃO QUÍMICA CELULAR PROFESSOR CLERSON CLERSONC@HOTMAIL.COM CIESC MADRE CLÉLIA CONCEITO CONJUNTO DE PROCESSOS INGESTÃO, DIGESTÃO E ABSORÇÃO SUBSTÂNCIAS ÚTEIS AO ORGANISMO ESPÉCIE HUMANA: DIGESTÃO ONÍVORA
NUTRIÇÃO QUÍMICA CELULAR PROFESSOR CLERSON CLERSONC@HOTMAIL.COM CIESC MADRE CLÉLIA CONCEITO CONJUNTO DE PROCESSOS INGESTÃO, DIGESTÃO E ABSORÇÃO SUBSTÂNCIAS ÚTEIS AO ORGANISMO ESPÉCIE HUMANA: DIGESTÃO ONÍVORA
5ª SÉRIE/6º ANO - ENSINO FUNDAMENTAL UM MUNDO MELHOR PARA TODOS
 5ª SÉRIE/6º ANO - ENSINO FUNDAMENTAL UM MUNDO MELHOR PARA TODOS Auno(a) N 0 6º Ano Turma: Data: / / 2013 Disciplina: Ciências UNIDADE I Professora Martha Pitanga ATIVIDADE 01 CIÊNCIAS REVISÃO GERAL De
5ª SÉRIE/6º ANO - ENSINO FUNDAMENTAL UM MUNDO MELHOR PARA TODOS Auno(a) N 0 6º Ano Turma: Data: / / 2013 Disciplina: Ciências UNIDADE I Professora Martha Pitanga ATIVIDADE 01 CIÊNCIAS REVISÃO GERAL De
Prova de Química e Biologia
 Provas Especialmente Adequadas Destinadas a Avaliar a Capacidade para a Frequência dos Cursos Superiores do IPVC dos Maiores de 23 Anos Prova de Química e Biologia Prova modelo Prova Específica de Química
Provas Especialmente Adequadas Destinadas a Avaliar a Capacidade para a Frequência dos Cursos Superiores do IPVC dos Maiores de 23 Anos Prova de Química e Biologia Prova modelo Prova Específica de Química
A) a existência do oceano líquido é uma hipótese possível, pois um sal solúvel só forma uma mistura homogênea com a água, quando ela está líquida.
 TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2
 11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
COMENTÁRIO DA PROVA DE BIOLOGIA
 COMENTÁRIO DA PROVA DE BIOLOGIA A prova de Biologia da UFPR apresentou uma boa distribuição de conteúdos ao longo das nove questões. O grau de dificuldade variou entre questões médias e fáceis, o que está
COMENTÁRIO DA PROVA DE BIOLOGIA A prova de Biologia da UFPR apresentou uma boa distribuição de conteúdos ao longo das nove questões. O grau de dificuldade variou entre questões médias e fáceis, o que está
 Curso superior em Agronomia GESA- Grupo de estudo em solos agrícolas Absorção de nutrientes e Fotossíntese Bambuí-MG 2009 Alunas: Erica Marques Júlia Maluf É o processo pelo qual a planta sintetiza compostos
Curso superior em Agronomia GESA- Grupo de estudo em solos agrícolas Absorção de nutrientes e Fotossíntese Bambuí-MG 2009 Alunas: Erica Marques Júlia Maluf É o processo pelo qual a planta sintetiza compostos
ECOLOGIA GERAL FLUXO DE ENERGIA E MATÉRIA ATRAVÉS DE ECOSSISTEMAS
 ECOLOGIA GERAL Aula 05 Aula de hoje: FLUXO DE ENERGIA E MATÉRIA ATRAVÉS DE ECOSSISTEMAS Sabemos que todos os organismos necessitam de energia para se manterem vivos, crescerem, se reproduzirem e, no caso
ECOLOGIA GERAL Aula 05 Aula de hoje: FLUXO DE ENERGIA E MATÉRIA ATRAVÉS DE ECOSSISTEMAS Sabemos que todos os organismos necessitam de energia para se manterem vivos, crescerem, se reproduzirem e, no caso
Aluno (a): Professor:
 3º BIM P1 LISTA DE EXERCÍCIOS CIÊNCIAS 6º ANO Aluno (a): Professor: Turma: Turno: Data: / / Unidade: ( ) Asa Norte ( ) Águas Lindas ( )Ceilândia ( ) Gama ( )Guará ( ) Pistão Norte ( ) Recanto das Emas
3º BIM P1 LISTA DE EXERCÍCIOS CIÊNCIAS 6º ANO Aluno (a): Professor: Turma: Turno: Data: / / Unidade: ( ) Asa Norte ( ) Águas Lindas ( )Ceilândia ( ) Gama ( )Guará ( ) Pistão Norte ( ) Recanto das Emas
A A A A A A A A A A A A A A A BIOLOGIA
 BIOLOGI 1 Nos últimos 10.000 anos, o nível de evaporação da água do Mar Morto tem sido maior que o de reposição. Dessa forma, a concentração de sais tem aumentado, já que o sal não evapora. principal fonte
BIOLOGI 1 Nos últimos 10.000 anos, o nível de evaporação da água do Mar Morto tem sido maior que o de reposição. Dessa forma, a concentração de sais tem aumentado, já que o sal não evapora. principal fonte
TERMOQUÍMICA. O que é o CALOR? Energia térmica em transito
 TERMOQUÍMICA Termoquímica PROF. Prof. DAVID David TERMOQUÍMICA O que é o CALOR? Energia térmica em transito TERMOQUÍMICA Estuda as quantidades de calor liberadas ou absorvidas durante as reações químicas
TERMOQUÍMICA Termoquímica PROF. Prof. DAVID David TERMOQUÍMICA O que é o CALOR? Energia térmica em transito TERMOQUÍMICA Estuda as quantidades de calor liberadas ou absorvidas durante as reações químicas
Química D Extensivo V. 3
 Química D Extensivo V. 3 Exercícios 01) Alternativa correta: A 5 4 3 2 1 CH 3 CH 2 CH CH CH 2 OH CH 3 CH 3 metil metil 02) Alternativa correta: D 8 7 6 5 4 3 2 1 CH 3 C = CH CH 2 CH 2 CH CH 2 CH 2 OH CH
Química D Extensivo V. 3 Exercícios 01) Alternativa correta: A 5 4 3 2 1 CH 3 CH 2 CH CH CH 2 OH CH 3 CH 3 metil metil 02) Alternativa correta: D 8 7 6 5 4 3 2 1 CH 3 C = CH CH 2 CH 2 CH CH 2 CH 2 OH CH
TEXTO PARA A PRÓXIMA QUESTÃO (Ufc) Na(s) questão(ões) a seguir escreva no espaço apropriado a soma dos itens corretos.
 Respiração e Fermentação 1. (Fuvest) O fungo 'Saccharomyces cerevisiae' (fermento de padaria) é um anaeróbico facultativo. Quando cresce na ausência de oxigênio, consome muito mais glicose do que quando
Respiração e Fermentação 1. (Fuvest) O fungo 'Saccharomyces cerevisiae' (fermento de padaria) é um anaeróbico facultativo. Quando cresce na ausência de oxigênio, consome muito mais glicose do que quando
3ªsérie B I O L O G I A
 3.1 QUESTÃO 1 Três consumidores, A, B e C, compraram, cada um deles, uma bebida em embalagem longa vida, adequada às suas respectivas dietas. As tabelas abaixo trazem informações nutricionais sobre cada
3.1 QUESTÃO 1 Três consumidores, A, B e C, compraram, cada um deles, uma bebida em embalagem longa vida, adequada às suas respectivas dietas. As tabelas abaixo trazem informações nutricionais sobre cada
EXAME DE BIOLOGIA Prova de Acesso - Maiores 23 Anos (21 de Abril de 2009)
 INSTITUTO POLITÉCNICO DE BEJA EXAME DE BIOLOGIA Prova de Acesso - Maiores 23 Anos (21 de Abril de 2009) Nome do Candidato Classificação Leia as seguintes informações com atenção. 1. O exame é constituído
INSTITUTO POLITÉCNICO DE BEJA EXAME DE BIOLOGIA Prova de Acesso - Maiores 23 Anos (21 de Abril de 2009) Nome do Candidato Classificação Leia as seguintes informações com atenção. 1. O exame é constituído
Questão 89. Questão 91. Questão 90. alternativa A. alternativa E
 Questão 89 O esquema representa o sistema digestório humano e os números indicam alguns dos seus componentes. Nível de açúcar no sangue mg/100ml 200 150 100 50 B A 0 1 2 3 4 5 Número de horas após a alimentação
Questão 89 O esquema representa o sistema digestório humano e os números indicam alguns dos seus componentes. Nível de açúcar no sangue mg/100ml 200 150 100 50 B A 0 1 2 3 4 5 Número de horas após a alimentação
Ecologia. 1) Níveis de organização da vida
 Introdução A ciência que estuda como os seres vivos se relacionam entre si e com o ambiente em que vivem e quais as conseqüências dessas relações é a Ecologia (oikos = casa e, por extensão, ambiente; logos
Introdução A ciência que estuda como os seres vivos se relacionam entre si e com o ambiente em que vivem e quais as conseqüências dessas relações é a Ecologia (oikos = casa e, por extensão, ambiente; logos
Sobre as substâncias representadas pelas estruturas I e II, é INCORRETO afirmar:
 8 GABARITO 1 1 O DIA 2 o PROCESSO SELETIVO/2005 QUÍMICA QUESTÕES DE 16 A 30 16. Devido à sua importância como catalisadores, haletos de boro (especialmente B 3 ) são produzidos na escala de toneladas por
8 GABARITO 1 1 O DIA 2 o PROCESSO SELETIVO/2005 QUÍMICA QUESTÕES DE 16 A 30 16. Devido à sua importância como catalisadores, haletos de boro (especialmente B 3 ) são produzidos na escala de toneladas por
REVISÃO QUÍMICA. Profº JURANDIR QUÍMICA
 REVISÃO QUÍMICA Profº JURANDIR QUÍMICA DADOS 01. (ENEM 2004) Em setembro de 1998, cerca de 10.000 toneladas de ácido sulfúrico (H 2 SO 4 ) foram derramadas pelo navio Bahamas no litoral do Rio Grande
REVISÃO QUÍMICA Profº JURANDIR QUÍMICA DADOS 01. (ENEM 2004) Em setembro de 1998, cerca de 10.000 toneladas de ácido sulfúrico (H 2 SO 4 ) foram derramadas pelo navio Bahamas no litoral do Rio Grande
COLÉGIO SANTA TERESINHA R. Madre Beatriz 135 centro Tel. (33) 3341-1244 www.colegiosantateresinha.com.br
 PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
 Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
CADERNO DE ATIVIDADES CIÊNCIAS
 COLÉGIO ARNALDO 2015 CADERNO DE ATIVIDADES CIÊNCIAS Aluno (a): 4º ano: Turma: Professor (a): Valor: 20 pontos Este trabalho deverá ser entregue IMPRETERIVELMENTE no dia da prova. Conteúdo de Recuperação
COLÉGIO ARNALDO 2015 CADERNO DE ATIVIDADES CIÊNCIAS Aluno (a): 4º ano: Turma: Professor (a): Valor: 20 pontos Este trabalho deverá ser entregue IMPRETERIVELMENTE no dia da prova. Conteúdo de Recuperação
Resolução: 0,86ºC. x = 0,5 mol etanol/kg acetona. 0,5 mol 1000 g de acetona. 200 g de acetona. y = 0,1 mol de etanol. 1 mol de etanol (C 2 H 6 O) 46 g
 (ACAFE) Foi dissolvida uma determinada massa de etanol puro em 200 g de acetona acarretando em um aumento de 0,86 C na temperatura de ebulição da acetona. Dados: H: 1 g/mol, C: 12 g/mol, O: 16 g/mol. Constante
(ACAFE) Foi dissolvida uma determinada massa de etanol puro em 200 g de acetona acarretando em um aumento de 0,86 C na temperatura de ebulição da acetona. Dados: H: 1 g/mol, C: 12 g/mol, O: 16 g/mol. Constante
Função orgânica nossa de cada dia. Profa. Kátia Aquino
 Função orgânica nossa de cada dia Profa. Kátia Aquino Vamos analisar! Funções Carboidratros (ou Glicídios) Energética: eles são os maiores fornecedores de energia para os seres vivos, principalmente a
Função orgânica nossa de cada dia Profa. Kátia Aquino Vamos analisar! Funções Carboidratros (ou Glicídios) Energética: eles são os maiores fornecedores de energia para os seres vivos, principalmente a
química 2 Questão 37 Questão 38 Questão 39 alternativa C na alternativa B. Sabendo-se que a amônia (NH 3)
 química 2 Questão 37 Questão 38 abendo-se que a amônia (N 3) é constituída por moléculas polares e apresenta boa solubilidade em água. o diclorometano (2 2) não possui isômeros. ua molécula apresenta polaridade,
química 2 Questão 37 Questão 38 abendo-se que a amônia (N 3) é constituída por moléculas polares e apresenta boa solubilidade em água. o diclorometano (2 2) não possui isômeros. ua molécula apresenta polaridade,
PlanetaBio Resolução de Vestibulares FUVEST 2010 1ª fase www.planetabio.com
 1- O Índice de Massa Corporal (IMC) é o número obtido pela divisão da massa de um indivíduo adulto, em quilogramas, pelo quadrado da altura, medida em metros. É uma referência adotada pela Organização
1- O Índice de Massa Corporal (IMC) é o número obtido pela divisão da massa de um indivíduo adulto, em quilogramas, pelo quadrado da altura, medida em metros. É uma referência adotada pela Organização
Introdução. Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo.
 Introdução Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo. Existem também sistemas, em que as reações direta e inversa
Introdução Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo. Existem também sistemas, em que as reações direta e inversa
Química. Resolução das atividades complementares. Q49 Polaridade das moléculas
 Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
Resolução das atividades complementares 4 Química Q49 Polaridade das moléculas p 7 1 Em relação à polaridade das moléculas, responda: a) Quais as condições para que uma molécula seja polar? b) Uma molécula
Matéria: Química Assunto: Materiais Prof. Gilberto Ramos
 Matéria: Química Assunto: Materiais Prof. Gilberto Ramos Química Materiais, suas propriedades e usos Estados Físicos Estado vem do latim status (posição,situação, condição,modo de estar). O estado físico
Matéria: Química Assunto: Materiais Prof. Gilberto Ramos Química Materiais, suas propriedades e usos Estados Físicos Estado vem do latim status (posição,situação, condição,modo de estar). O estado físico
O interesse da Química é analisar as...
 O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
O interesse da Química é analisar as... PROPRIEDADES CONSTITUINTES SUBSTÂNCIAS E MATERIAIS TRANSFORMAÇÕES ESTADOS FÍSICOS DOS MATERIAIS Os materiais podem se apresentar na natureza em 3 estados físicos
Padrão de respostas às questões discursivas
 Padrão de respostas às questões discursivas A seguir encontram-se as questões das provas discursivas da 2ª ETAPA do Vestibular UFF 2011, acompanhadas das respostas esperadas pelas bancas. GABARITO BIOLOGIA
Padrão de respostas às questões discursivas A seguir encontram-se as questões das provas discursivas da 2ª ETAPA do Vestibular UFF 2011, acompanhadas das respostas esperadas pelas bancas. GABARITO BIOLOGIA
FLUXO DE ENERGIA E CICLOS DE MATÉRIA
 FLUXO DE ENERGIA E CICLOS DE MATÉRIA Todos os organismos necessitam de energia para realizar as suas funções vitais. A energia necessária para a vida na Terra provém praticamente toda do sol. Contudo,
FLUXO DE ENERGIA E CICLOS DE MATÉRIA Todos os organismos necessitam de energia para realizar as suas funções vitais. A energia necessária para a vida na Terra provém praticamente toda do sol. Contudo,
QUÍMICA. Questão 31. Questão 32
 QUÍMICA Questão 3 Em 9,9 g de um sal de cálcio encontra-se 0,5 mol desse elemento. Qual a massa molar do ânion trivalente que forma esse sal? Dado: Ca 40 g/mol. (A) 39 g/mol. (B) 278 g/mol. (C) 63,3 g/mol.
QUÍMICA Questão 3 Em 9,9 g de um sal de cálcio encontra-se 0,5 mol desse elemento. Qual a massa molar do ânion trivalente que forma esse sal? Dado: Ca 40 g/mol. (A) 39 g/mol. (B) 278 g/mol. (C) 63,3 g/mol.
PROCESSO SELETIVO 2006 QUESTÕES OBJETIVAS
 3 PROCESSO SELETIVO 2006 QUESTÕES OBJETIVAS QUÍMICA 01 - O dispositivo de segurança que conhecemos como air-bag utiliza como principal reagente para fornecer o gás N 2 (massa molar igual a 28 g mol -1
3 PROCESSO SELETIVO 2006 QUESTÕES OBJETIVAS QUÍMICA 01 - O dispositivo de segurança que conhecemos como air-bag utiliza como principal reagente para fornecer o gás N 2 (massa molar igual a 28 g mol -1
B) (até três pontos) Para os pares de espécies apresentados em i, ii e iii, tem-se, respectivamente, Al +, F - e Li.
 Química 1. O raio atômico (ou iônico) é uma propriedade periódica que exerce grande influência na reatividade dos átomos (ou dos íons). A) Explique, em termos de carga nuclear efetiva, a variação apresentada
Química 1. O raio atômico (ou iônico) é uma propriedade periódica que exerce grande influência na reatividade dos átomos (ou dos íons). A) Explique, em termos de carga nuclear efetiva, a variação apresentada
Resolução Comentada - Química
 Resolução Comentada - Química UFTM 2013 1 Fase Vestibular UFTM 2013 1 Resolução Prova de Química Tipo 1 Questão 76 A soja é considerada um dos alimentos mais completos em termos de propriedades nutricionais,
Resolução Comentada - Química UFTM 2013 1 Fase Vestibular UFTM 2013 1 Resolução Prova de Química Tipo 1 Questão 76 A soja é considerada um dos alimentos mais completos em termos de propriedades nutricionais,
COLÉGIO NOSSA SENHORA DA PIEDADE. Programa de Recuperação Paralela. 2ª Etapa 2014. 1ª série Turma: FG
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
muito gás carbônico, gás de enxofre e monóxido de carbono. extremamente perigoso, pois ocupa o lugar do oxigênio no corpo. Conforme a concentração
 A UU L AL A Respiração A poluição do ar é um dos problemas ambientais que mais preocupam os governos de vários países e a população em geral. A queima intensiva de combustíveis gasolina, óleo e carvão,
A UU L AL A Respiração A poluição do ar é um dos problemas ambientais que mais preocupam os governos de vários países e a população em geral. A queima intensiva de combustíveis gasolina, óleo e carvão,
a) Qual a configuração eletrônica do cátion do alumínio isoeletrônico ao gás nobre neônio?
 Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
FISIOLOGIA RENAL EXERCÍCIOS DE APRENDIZAGEM
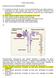 EXERCÍCIOS DE APRENDIZAGEM FISIOLOGIA RENAL 01. A sudorese (produção de suor) é um processo fisiológico que ajuda a baixar a temperatura do corpo quando está muito calor ou quando realizamos uma atividade
EXERCÍCIOS DE APRENDIZAGEM FISIOLOGIA RENAL 01. A sudorese (produção de suor) é um processo fisiológico que ajuda a baixar a temperatura do corpo quando está muito calor ou quando realizamos uma atividade
EXERCÍCIOS DE REVISÃO CITOPLASMA E METABOLISMO
 Componente Curricular: Biologia Professor: Leonardo Francisco Stahnke Aluno(a): Turma: Data: / /2015 EXERCÍCIOS DE REVISÃO CITOPLASMA E METABOLISMO 1. A respeito da equação ao lado, que representa uma
Componente Curricular: Biologia Professor: Leonardo Francisco Stahnke Aluno(a): Turma: Data: / /2015 EXERCÍCIOS DE REVISÃO CITOPLASMA E METABOLISMO 1. A respeito da equação ao lado, que representa uma
A biodiversidade em diferentes ambientes. http://www.prof2000.pt/users/ccaf/exercicios/ecossistemas/biomas.htm
 A biodiversidade em diferentes ambientes http://www.prof2000.pt/users/ccaf/exercicios/ecossistemas/biomas.htm Unidade básica da vida a célula Quem foi Robert Hooke? Por volta de 1667, o cientista inglês
A biodiversidade em diferentes ambientes http://www.prof2000.pt/users/ccaf/exercicios/ecossistemas/biomas.htm Unidade básica da vida a célula Quem foi Robert Hooke? Por volta de 1667, o cientista inglês
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é:
 01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
CALORIMETRIA, MUDANÇA DE FASE E TROCA DE CALOR Lista de Exercícios com Gabarito e Soluções Comentadas
 COLÉGIO PEDRO II PRÓ-REITORIA DE PÓS-GRADUAÇÃO, PESQUISA, EXTENSÃO E CULTURA PROGRAMA DE RESIDÊNCIA DOCENTE RESIDENTE DOCENTE: Marcia Cristina de Souza Meneguite Lopes MATRÍCULA: P4112515 INSCRIÇÃO: PRD.FIS.0006/15
COLÉGIO PEDRO II PRÓ-REITORIA DE PÓS-GRADUAÇÃO, PESQUISA, EXTENSÃO E CULTURA PROGRAMA DE RESIDÊNCIA DOCENTE RESIDENTE DOCENTE: Marcia Cristina de Souza Meneguite Lopes MATRÍCULA: P4112515 INSCRIÇÃO: PRD.FIS.0006/15
PROPRIEDADES DA MATÉRIA
 Profª Msc.Anna Carolina A. Ribeiro PROPRIEDADES DA MATÉRIA RELEMBRANDO Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Corpo- Trata-se de uma porção
Profª Msc.Anna Carolina A. Ribeiro PROPRIEDADES DA MATÉRIA RELEMBRANDO Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Corpo- Trata-se de uma porção
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves
 Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS. Aluno(a): Turma:
 IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS Aluno(a): Turma: Querido (a) aluno (a), Este estudo dirigido foi realizado para que você revise
IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS Aluno(a): Turma: Querido (a) aluno (a), Este estudo dirigido foi realizado para que você revise
Nesse sistema de aquecimento,
 Enem 2007 1- Ao beber uma solução de glicose (C 6 H 12 O 6 ), um corta-cana ingere uma substância: (A) que, ao ser degradada pelo organismo, produz energia que pode ser usada para movimentar o corpo. (B)
Enem 2007 1- Ao beber uma solução de glicose (C 6 H 12 O 6 ), um corta-cana ingere uma substância: (A) que, ao ser degradada pelo organismo, produz energia que pode ser usada para movimentar o corpo. (B)
MEIOS DE CULTURA DESENVOLVIMENTO OU PRODUÇÃO DE MEIOS DE CULTURA. Necessidade Bactérias Leveduras
 MEIOS DE CULTURA Associação equilibrada de agentes químicos (nutrientes, ph, etc.) e físicos (temperatura, viscosidade, atmosfera, etc) que permitem o cultivo de microorganismos fora de seu habitat natural.
MEIOS DE CULTURA Associação equilibrada de agentes químicos (nutrientes, ph, etc.) e físicos (temperatura, viscosidade, atmosfera, etc) que permitem o cultivo de microorganismos fora de seu habitat natural.
- Nosso corpo é formado por inúmeras estruturas macro e microscópicas;
 CAPÍTULO 01 A CÉLULA - Nosso corpo é formado por inúmeras estruturas macro e microscópicas; - O funcionamento interligado e harmonioso dessas estruturas mantém o corpo vivo, em funcionamento; A ORGANIZAÇÃO
CAPÍTULO 01 A CÉLULA - Nosso corpo é formado por inúmeras estruturas macro e microscópicas; - O funcionamento interligado e harmonioso dessas estruturas mantém o corpo vivo, em funcionamento; A ORGANIZAÇÃO
Questão 1. Questão 3. Questão 2 1ª PARTE: QUESTÕES OBJETIVAS. alternativa E. alternativa B. A, B e C pertenceriam, respectivamente, a organismos
 1ª PARTE: QUESTÕES OBJETIVAS Questão 1 O exame de um epitélio e do tecido nervoso de um mesmo animal revelou que suas células apresentam diferentes características. Isso ocorre porque a) as moléculas de
1ª PARTE: QUESTÕES OBJETIVAS Questão 1 O exame de um epitélio e do tecido nervoso de um mesmo animal revelou que suas células apresentam diferentes características. Isso ocorre porque a) as moléculas de
As bactérias operárias
 A U A UL LA As bactérias operárias Na Aula 47 você viu a importância da insulina no nosso corpo e, na Aula 48, aprendeu como as células de nosso organismo produzem insulina e outras proteínas. As pessoas
A U A UL LA As bactérias operárias Na Aula 47 você viu a importância da insulina no nosso corpo e, na Aula 48, aprendeu como as células de nosso organismo produzem insulina e outras proteínas. As pessoas
Introdução à Química Inorgânica
 Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
Prova de Recuperação Bimestral de Ciências Nome Completo: Data: / /2010
 COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
O DNA é formado por pedaços capazes de serem convertidos em algumas características. Esses pedaços são
 Atividade extra Fascículo 2 Biologia Unidade 4 Questão 1 O DNA é formado por pedaços capazes de serem convertidos em algumas características. Esses pedaços são chamados de genes. Assinale abaixo quais
Atividade extra Fascículo 2 Biologia Unidade 4 Questão 1 O DNA é formado por pedaços capazes de serem convertidos em algumas características. Esses pedaços são chamados de genes. Assinale abaixo quais
LINKAGE E OS MAPAS GENÉTICOS
 Disciplina: Biologia Série: 2ª série EM - 1º TRIM Professora: Ivone Azevedo da Fonseca Assunto: Linkage e os Mapas Genéticos Humanos LINKAGE E OS MAPAS GENÉTICOS Os trabalhos de Gregor Mendel não foram
Disciplina: Biologia Série: 2ª série EM - 1º TRIM Professora: Ivone Azevedo da Fonseca Assunto: Linkage e os Mapas Genéticos Humanos LINKAGE E OS MAPAS GENÉTICOS Os trabalhos de Gregor Mendel não foram
COMENTÁRIO GERAL (EQUIPE DE BIOLOGIA)
 COMENTÁRIO GERAL (EQUIPE DE BIOLOGIA) A prova de Biologia ENEM 2010 apresentou como eixo central questões envolvendo meio ambiente e ecologia geral. Desta forma houve um desequilíbrio na distribuição de
COMENTÁRIO GERAL (EQUIPE DE BIOLOGIA) A prova de Biologia ENEM 2010 apresentou como eixo central questões envolvendo meio ambiente e ecologia geral. Desta forma houve um desequilíbrio na distribuição de
A) Escreva a equação que representa a semi-reação de redução e seu respectivo potencial padrão.
 QUÍMICA QUESTÃ 01 Aparelhos eletrônicos sem fio, tais como máquinas fotográficas digitais e telefones celulares, utilizam, como fonte de energia, baterias recarregáveis. Um tipo comum de bateria recarregável
QUÍMICA QUESTÃ 01 Aparelhos eletrônicos sem fio, tais como máquinas fotográficas digitais e telefones celulares, utilizam, como fonte de energia, baterias recarregáveis. Um tipo comum de bateria recarregável
BIOLOGIA COMENTÁRIO DA PROVA DE BIOLOGIA
 COMENTÁRIO DA PROVA DE BIOLOGIA Nota-se claramente que a prova de biologia da segunda fase da UFPR refletiu um esforço no sentido de privilegiar questões que envolvam raciocínio lógico aplicado ao domínio
COMENTÁRIO DA PROVA DE BIOLOGIA Nota-se claramente que a prova de biologia da segunda fase da UFPR refletiu um esforço no sentido de privilegiar questões que envolvam raciocínio lógico aplicado ao domínio
Matéria e energia nos ecossistemas
 Aula de hoje Matéria e energia nos ecossistemas Matéria e energia nos ecossistemas A forma e funcionamento dos organismos vivos evoluiu parcialmente il em respostas às condições prevalecentes no mundo
Aula de hoje Matéria e energia nos ecossistemas Matéria e energia nos ecossistemas A forma e funcionamento dos organismos vivos evoluiu parcialmente il em respostas às condições prevalecentes no mundo
Solução Comentada Prova de Biologia
 11. Em relação à importância dos organismos autotróficos na modificação da atmosfera na Terra primitiva, analise as proposições abaixo e marque com V as verdadeiras e com F as falsas. 1 ( ) Com a liberação
11. Em relação à importância dos organismos autotróficos na modificação da atmosfera na Terra primitiva, analise as proposições abaixo e marque com V as verdadeiras e com F as falsas. 1 ( ) Com a liberação
Questão 1 Questão 2. Questão 3. Resposta. Resposta
 Questão 1 Questão 2 O esquema abaixo representa as principais relações alimentares entre espécies que vivem num lago de uma região equatorial. a) O câncer é uma doença genética, mas na grande maioria dos
Questão 1 Questão 2 O esquema abaixo representa as principais relações alimentares entre espécies que vivem num lago de uma região equatorial. a) O câncer é uma doença genética, mas na grande maioria dos
Organização do Material Genético nos Procariontes e Eucariontes
 Organização do Material Genético nos Procariontes e Eucariontes Organização do Material Genético nos Procariontes e Eucariontes Procariontes Eucariontes Localização Organização Forma Disperso no citoplasma
Organização do Material Genético nos Procariontes e Eucariontes Organização do Material Genético nos Procariontes e Eucariontes Procariontes Eucariontes Localização Organização Forma Disperso no citoplasma
FUVEST 2002. 08/01/2002 Biologia
 FUVEST 2002 08/01/2002 Biologia Q.01 O quadro abaixo destaca dois conceitos biológicos: câncer e sistema respiratório de insetos. a) Faça uma breve descrição de como o nefasto hábito de fumar está associado
FUVEST 2002 08/01/2002 Biologia Q.01 O quadro abaixo destaca dois conceitos biológicos: câncer e sistema respiratório de insetos. a) Faça uma breve descrição de como o nefasto hábito de fumar está associado
A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas.
 A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas. Não há reação química que ocorra sem variação de energia! A energia é conservativa. Não pode ser criada
A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas. Não há reação química que ocorra sem variação de energia! A energia é conservativa. Não pode ser criada
Resolução Resolução OBJETIVO 2004
 1 Nas bactérias, a cadeia respiratória encontra-se associada à membrana plasmática e os ácidos nucléicos estão associados ao citoplasma. a) É assim também em um protista, em um animal e em um vegetal?
1 Nas bactérias, a cadeia respiratória encontra-se associada à membrana plasmática e os ácidos nucléicos estão associados ao citoplasma. a) É assim também em um protista, em um animal e em um vegetal?
CADERNO DE EXERCÍCIOS 2D
 CADERNO DE EXERCÍCIOS 2D Ensino Fundamental Ciências da Natureza II Habilidade da Questão Conteúdo Matriz da EJA/FB 01 Fisiologia Vegetal (Transporte e absorção de H34, H40, H41, H63 substâncias); Fotossíntese
CADERNO DE EXERCÍCIOS 2D Ensino Fundamental Ciências da Natureza II Habilidade da Questão Conteúdo Matriz da EJA/FB 01 Fisiologia Vegetal (Transporte e absorção de H34, H40, H41, H63 substâncias); Fotossíntese
CIÊNCIAS PROVA 4º BIMESTRE 7º ANO PROJETO CIENTISTAS DO AMANHÃ
 PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 4º BIMESTRE 7º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. As fotografias
PREFEITURA DA CIDADE DO RIO DE JANEIRO SECRETARIA MUNICIPAL DE EDUCAÇÃO SUBSECRETARIA DE ENSINO COORDENADORIA DE EDUCAÇÃO CIÊNCIAS PROVA 4º BIMESTRE 7º ANO PROJETO CIENTISTAS DO AMANHÃ 2010 01. As fotografias
Maxillaria silvana Campacci
 Ecologia Aula 1 Habitat É o lugar que reúne as melhores condições de vida para uma espécie. Temperatura, quantidade de água, intensidade da luz solar e tipo de solo determinam se o habitat é adequado ao
Ecologia Aula 1 Habitat É o lugar que reúne as melhores condições de vida para uma espécie. Temperatura, quantidade de água, intensidade da luz solar e tipo de solo determinam se o habitat é adequado ao
De onde vêm as lágrimas?
 De onde vêm as lágrimas? É toda substância que, em solução aquosa, sofre dissociação, liberado pelo menos um cátion diferente de H + e um ânion diferente de OH -. a) Presença de oxigênio b) Sal não oxigenado
De onde vêm as lágrimas? É toda substância que, em solução aquosa, sofre dissociação, liberado pelo menos um cátion diferente de H + e um ânion diferente de OH -. a) Presença de oxigênio b) Sal não oxigenado
CAPÍTULO 02 A TEIA ALIMENTAR
 CAPÍTULO 02 A TEIA ALIMENTAR Cadeia alimentar: é uma seqüência de seres vivos relacionando-se dentro de um ecossistema, onde um ser serve de alimento para outro ser. Exemplo: Capim capivara onça bactéria
CAPÍTULO 02 A TEIA ALIMENTAR Cadeia alimentar: é uma seqüência de seres vivos relacionando-se dentro de um ecossistema, onde um ser serve de alimento para outro ser. Exemplo: Capim capivara onça bactéria
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA
 SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
Projeto Embuá Unidade de Aprendizagem: ENERGIA
 Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
3º trimestre- LISTA DE EXERCICIOS - Biologia - CESINHA Ensino Médio 1º ano classe: Prof. Cesinha Nome: nº
 . 3º trimestre- LISTA DE EXERCICIOS - Biologia - CESINHA Ensino Médio 1º ano classe: Prof. Cesinha Nome: nº Valor: 10 Nota:. 1. (Uel 2015) Leia o texto a seguir. Quando se fala em divisão celular, não
. 3º trimestre- LISTA DE EXERCICIOS - Biologia - CESINHA Ensino Médio 1º ano classe: Prof. Cesinha Nome: nº Valor: 10 Nota:. 1. (Uel 2015) Leia o texto a seguir. Quando se fala em divisão celular, não
Fração. Página 2 de 6
 1. (Fgv 2014) De acordo com dados da Agência Internacional de Energia (AIE), aproximadamente 87% de todo o combustível consumido no mundo são de origem fóssil. Essas substâncias são encontradas em diversas
1. (Fgv 2014) De acordo com dados da Agência Internacional de Energia (AIE), aproximadamente 87% de todo o combustível consumido no mundo são de origem fóssil. Essas substâncias são encontradas em diversas
Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza
 Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza 1) a-) Calcular a solubilidade do BaSO 4 em uma solução 0,01 M de Na 2 SO 4 Dissolução do Na 2 SO 4 : Dado: BaSO
Lista de Exercícios 4 Indústrias Químicas Resolução pelo Monitor: Rodrigo Papai de Souza 1) a-) Calcular a solubilidade do BaSO 4 em uma solução 0,01 M de Na 2 SO 4 Dissolução do Na 2 SO 4 : Dado: BaSO
TRATAMENTO DA ÁGUA. Professora: Raquel Malta Química 3ª série - Ensino Médio
 TRATAMENTO DA ÁGUA Professora: Raquel Malta Química 3ª série - Ensino Médio Água poluída: água inadequada para beber ou para fazer nossa higiene. Diversas substâncias naturalmente presentes na água são
TRATAMENTO DA ÁGUA Professora: Raquel Malta Química 3ª série - Ensino Médio Água poluída: água inadequada para beber ou para fazer nossa higiene. Diversas substâncias naturalmente presentes na água são
NECESSIDADE BÁSICAS DOS SERES VIVOS. Estágio docência: Camila Macêdo Medeiros
 NECESSIDADE BÁSICAS DOS SERES VIVOS Estágio docência: Camila Macêdo Medeiros Necessidades básicas O planeta oferece meios que satisfaçam as necessidades básicas dos seres vivos. Necessidades básicas dos
NECESSIDADE BÁSICAS DOS SERES VIVOS Estágio docência: Camila Macêdo Medeiros Necessidades básicas O planeta oferece meios que satisfaçam as necessidades básicas dos seres vivos. Necessidades básicas dos
Recuperação. Células tecidos órgãos sistemas. - As células são as menores unidades vivas e são formadas por três regiões:
 Recuperação Capítulo 01 - Níveis de organização Células tecidos órgãos sistemas - As células são as menores unidades vivas e são formadas por três regiões: A- Membrana Plasmática - Revestimento da célula;
Recuperação Capítulo 01 - Níveis de organização Células tecidos órgãos sistemas - As células são as menores unidades vivas e são formadas por três regiões: A- Membrana Plasmática - Revestimento da célula;
1º SIMULADO ESPECIFICO / PRÉ-MEDICINA PROF. ZÉ ROBERTO
 PROF. ZÉ ROBERTO COMENTÁRIO: O físico inglês Isaac Newton (1642-1726) 1726) realizou a experiência de decomposição da luz em 1666, na residência de sua família, no campo, quando se refugiava da epidemia
PROF. ZÉ ROBERTO COMENTÁRIO: O físico inglês Isaac Newton (1642-1726) 1726) realizou a experiência de decomposição da luz em 1666, na residência de sua família, no campo, quando se refugiava da epidemia
PlanetaBio Resolução de Vestibulares UFRJ 2006 www.planetabio.com
 1-No processo evolutivo, centenas de espécies podem ser criadas em um tempo relativamente curto. Esse fenômeno é conhecido como radiação adaptativa. No grupo dos répteis, ocorreu uma grande radiação adaptativa
1-No processo evolutivo, centenas de espécies podem ser criadas em um tempo relativamente curto. Esse fenômeno é conhecido como radiação adaptativa. No grupo dos répteis, ocorreu uma grande radiação adaptativa
Universidade Federal de Pelotas FAEM - DZ Curso de Zootecnia Genética Aplicada à Produção Animal
 Universidade Federal de Pelotas FAEM - DZ Curso de Zootecnia Genética Aplicada à Produção Animal Genética clássica: mono, di e polihibridismo, alelismo múltiplo. A PRIMEIRA LEI DE MENDEL OU PRINCÍPIO DA
Universidade Federal de Pelotas FAEM - DZ Curso de Zootecnia Genética Aplicada à Produção Animal Genética clássica: mono, di e polihibridismo, alelismo múltiplo. A PRIMEIRA LEI DE MENDEL OU PRINCÍPIO DA
PROVA COMENTADA PELOS PROFESSORES DO CURSO POSITIVO
 PROFESSORES DO POSITIVO COMENTÁRIO DA PROVA DE BIOLOGIA A prova da segunda fase da UFPR foi muito bem distribuída em termos de conteúdo. As questões, de forma geral, foram bem elaboradas e se caracterizaram
PROFESSORES DO POSITIVO COMENTÁRIO DA PROVA DE BIOLOGIA A prova da segunda fase da UFPR foi muito bem distribuída em termos de conteúdo. As questões, de forma geral, foram bem elaboradas e se caracterizaram
BIOLOGIA. Consumidores Primários. Consumidores Secundários. Consumidores Terciários III
 46 c Em vários córregos existentes na periferia de uma cidade, foram encontradas larvas denominadas miracídios. Essas larvas dariam segmento ao ciclo de vida do verme 1 se pudessem se instalar no corpo
46 c Em vários córregos existentes na periferia de uma cidade, foram encontradas larvas denominadas miracídios. Essas larvas dariam segmento ao ciclo de vida do verme 1 se pudessem se instalar no corpo
A descoberta da célula
 A descoberta da célula O que são células? As células são a unidade fundamental da vida CITOLOGIA A área da Biologia que estuda a célula, no que diz respeito à sua estrutura e funcionamento. Kytos (célula)
A descoberta da célula O que são células? As células são a unidade fundamental da vida CITOLOGIA A área da Biologia que estuda a célula, no que diz respeito à sua estrutura e funcionamento. Kytos (célula)
APROFUNDAMENTO DE QUIMICA ORGÂNICA LISTA 04 09/10/2014. Assunto: Estudo das Funções Orgânicas
 APROFUNDAMENTO DE QUIMICA ORGÂNICA LISTA 04 09/10/2014 Assunto: Estudo das Funções Orgânicas 01-( Medicina Jundiaí 2014 ) Considere as fórmulas estruturais de substâncias utilizadas como antibióticos:
APROFUNDAMENTO DE QUIMICA ORGÂNICA LISTA 04 09/10/2014 Assunto: Estudo das Funções Orgânicas 01-( Medicina Jundiaí 2014 ) Considere as fórmulas estruturais de substâncias utilizadas como antibióticos:
Um estudante de 23 anos, doador de sangue tipo universal, é moreno, tem estatura mediana e pesa 85 kg. Todas as alternativas apresentam
 Um estudante de 23 anos, doador de sangue tipo universal, é moreno, tem estatura mediana e pesa 85 kg. Todas as alternativas apresentam características hereditárias desse estudante que são influenciadas
Um estudante de 23 anos, doador de sangue tipo universal, é moreno, tem estatura mediana e pesa 85 kg. Todas as alternativas apresentam características hereditárias desse estudante que são influenciadas
EXERCÍCIOS PARA O 8 ANO (2015)
 EXERCÍCIOS PARA O 8 ANO (2015) 1- A Fábrica Celular Células de bactérias (procarióticas) e células animais (eucarióticas), apresentam semelhanças e diferenças. a) Qual a estrutura presente em ambas que
EXERCÍCIOS PARA O 8 ANO (2015) 1- A Fábrica Celular Células de bactérias (procarióticas) e células animais (eucarióticas), apresentam semelhanças e diferenças. a) Qual a estrutura presente em ambas que
BANCO DE QUESTÕES - BIOLOGIA - 1ª SÉRIE - ENSINO MÉDIO ==============================================================================================
 PROFESSOR: Leonardo Mariscal BANCO DE QUESTÕES - BIOLOGIA - 1ª SÉRIE - ENSINO MÉDIO ============================================================================================== Assunto: Organelas citoplasmáticas
PROFESSOR: Leonardo Mariscal BANCO DE QUESTÕES - BIOLOGIA - 1ª SÉRIE - ENSINO MÉDIO ============================================================================================== Assunto: Organelas citoplasmáticas
QUESTÕES DE CARACTERIZAÇÃO E ANÁLISE AMBIENTAL. O 2(g) O 2(aq)
 QUESTÕES DE CARACTERIZAÇÃO E ANÁLISE AMBIENTAL Questão 01 O agente oxidante mais importante em águas naturais é, sem a menor dúvida, o oxigênio molecular dissolvido, O 2. O equilíbrio entre o oxigênio
QUESTÕES DE CARACTERIZAÇÃO E ANÁLISE AMBIENTAL Questão 01 O agente oxidante mais importante em águas naturais é, sem a menor dúvida, o oxigênio molecular dissolvido, O 2. O equilíbrio entre o oxigênio
Ciclos Biogeoquímicos
 Os organismos retiram constantemente da natureza os elementos químicos de que necessitam, mas esses elementos sempre retornam ao ambiente. O processo contínuo de retirada e de devolução de elementos químicos
Os organismos retiram constantemente da natureza os elementos químicos de que necessitam, mas esses elementos sempre retornam ao ambiente. O processo contínuo de retirada e de devolução de elementos químicos
