Vacina contra o câncer de colo de útero
|
|
|
- Marco Bugalho Álvares
- 8 Há anos
- Visualizações:
Transcrição
1 Vacina contra o câncer de colo de útero Antes de prescrever, recomendamos a leitura da Circular aos Médicos (bula) para informações detalhadas sobre o produto.
2 A vantagem da proteção com a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) Proteção contra o câncer de colo de útero Eficaz contra os tipos de papilomavírus humano que causam aproximadamente 70% de todos os cânceres de colo do útero em estudos clínicos Fase II e Fase III DURADOURA Proteção demonstrada com o decorrer do tempo A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) demonstrou memória imunológica em estudos clínicos indicação de proteção de longo prazo 1 Não houve casos de infecção para a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) durante estudos clínicos de 5 anos,1 MAIS Ajuda a proteger pacientes contra outras doenças: verrugas genitais câncer de vulva e de vagina displasia cervical Assim como para qualquer vacina, a administração da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) pode não resultar em proteção a todos os indivíduos. Esta vacina não se destina ao tratamento de verrugas genitais ativas; câncer de colo de útero, de vulva nem de vagina, nem neoplasias de colo de útero, de vulva ou vagina (NIC, NIV ou NIVa). Antes de prescrever, recomendamos a leitura da Circular aos Médicos (bula) para informações detalhadas sobre o produto. Veja Desenho de Estudo A Veja Desenho de Estudo B A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é indicada para a prevenção dos cânceres de colo de útero, de vulva e de vagina; lesões pré-cancerosas ou displásicas; verrugas genitais e infecção causadas pelo papilomavírus humano tipos 6, 11, 16 e 18. Informações Selecionadas de Segurança A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é contra-indicada para indivíduos que sejam hipersensíveis às substâncias ativas ou a qualquer dos excipientes da vacina.
3 Proteção e prevenção Eficácia contra o câncer de colo de útero CÂNCER DO COLO DO ÚTERO, Um caso no grupo que recebeu a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) (n=8.492) versus 85 casos no grupo que recebeu placebo (n=8.462) [IC95% 93,3-100,0] 99% EFICAZ contra a NIC 2/3 ou AIS relacionados ao papilomavírus humano tipos 16 e 18 Os tipos 16 e 18 causam aproximadamente 70% de todos os casos de câncer do colo do útero A eficácia da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) foi avaliada em quatro estudos clínicos fase II e III controlados com placebo, duplo-cegos e randômicos. Juntos, esses estudos avaliaram mulheres que tinham 16 a 26 anos de idade na data da inclusão. Veja o Desenho de Estudo A. O câncer invasivo do colo do útero não pode ser usado como desfecho para estudos de eficácia com vacinas de papilomavírus humano devido à importância do emprego de medidas secundárias de prevenção. Portanto, os precursores imediatos, NIC 2 (displasia cervical moderada), NIC 3 (displasia cervical de alto grau, incluindo carcinoma in situ) e AIS são os desfechos mais adequados para a demonstração da prevenção do câncer do colo do útero por vacinas de papilomavírus humano. Adenocarcinoma in situ. Um caso de NIC 3 ocorreu no grupo que recebeu a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18), no qual os tipos de papilomavírus humano 16 e 52 foram detectados. Esse indivíduo havia sido cronicamente infectado pelo tipo 52 (infecção no dia 1, mês 32,5 e mês 33,6) em 8 de 11 espécimes, inclusive no tecido excisado durante o procedimento de excisão eletrocirúrgica de alça. O tipo 16 foi encontrado em 1 de 11 espécimes no mês 32,5, mas não foi detectado no tecido excisado durante o procedimento.
4 Proteção duradoura Não houve casos de infecção com a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) demonstrou memória imunológica Resposta de anticorpos a papilomavírus humano 16 no mês 61 Evidências de proteção de longo prazo podem ser estabelecidas por: resposta demonstrada da memória imunológica 1 eficácia clínica alta e contínua 1 avaliação contínua com base em estudos de extensão Fase III 2 Estudo Nórdico compromisso de longo-prazo com a prevenção do câncer do colo do útero 2 Média Geométrica dos Títulos (GMT) (mmu/ml) com IC 95% Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) n= Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) n= EVIDÊNCIA DE MEMÓRIA IMUNOLÓGICA: Os níveis de anticorpos eram ~2 vezes maiores do que 1 mês após a série de vacinação Os resultados serão analisados continuamente por pelo menos 10 anos Análises de eficácia 3 anos 5 anos 7 anos 2003 Início do estudo anos 2013 Conclusão do estudo Tempo, meses Tempo Série de administração da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) Vacinação no dia 0, mês 2 e mês 6 Aplicação de antígeno Aplicação de antígeno no mês 60 Respostas semelhantes antipapilomavírus humano foram observadas também para os tipos 6, 11 e Estudo de extensão Fase III Estudos de acompanhamento dos registros das voluntárias de pesquisa indivíduos de estudo de NIC 2/3 incluídos na região nórdica Tais registros serão utilizados para definir a duração da eficácia de longo prazo A memória imunológica é evidência de que suas pacientes vacinadas poderão produzir uma resposta de anticorpos forte o bastante para protegê-las contra infecção futura 1 Houve infecções contínuas com o placebo. 1 Em um estudo randômico, controlado com placebo, com 551 mulheres de 16 a 23 anos de idade, um subconjunto de 241 indivíduos foram avaliados por mais dois anos de acompanhamento (meses 37-60, por um total de 5 anos) 1. Veja Desenho de Estudo B. Os níveis de anticorpos foram 1,3; 4,2 e 1,7 vezes mais altos do que as GMTs após a dose três para os tipos 6, 11 e 18, respectivamente.
5 Mais proteção para mais meninas e jovens mulheres A vacina contra o câncer de colo de útero que ajuda a proteger contra as verrugas genitais A vacina contra o câncer do colo do útero ajuda a proteger contra o câncer de vulva/vagina e contra a displasia cervical VERRUGAS GENITAIS CÂNCER DE VULVA/VAGINA DISPLASIA CERVICAL 99 % EFICAZ Os tipos 6 e 11 causam ~90% de todos os casos de verrugas genitais. 100 % EFICAZ contra a NIV 2/3 ou NIVa 2/3 relacionadas ao papilomavírus humano 16 e 18 Os tipos 16 e 18 causam ~70% dos casos de câncer de vulva/vagina, NIV 2/3 e NIVa 2/3 96 % EFICAZ contra a NIC 2/3 relacionada aos papilomavírus humanos 6, 11, 16 e 18 (NIC 1, NIC 2/3) Os tipos 6, 11, 16 e 18 causam ~35% a 50% de todos os casos de NIC 1 contra as verrugas genitais relacionadas ao papilomavírus humano tipos 6 e 11 Nenhum caso no grupo que recebeu a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) (n=7.771) versus 15 casos no grupo que recebeu placebo (n=7.742) (IC 95%: 30,9-100,0) Seis casos no grupo que recebeu a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) (n=7.863) versus 148 casos no grupo que recebeu placebo (n=7.863) (IC 95%: 91,0-98,5) Dois casos no grupo que recebeu vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) (n= 6.931) versus 156 casos no grupo que recebeu placebo (n=6.854) (IC 95%: 95,34-99,8) A eficácia da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) foi avaliada em quatro estudos clínicos controlados com placebo, duplo-cegos e randômicos fases II e III. Em conjunto, esses estudos avaliaram mulheres com idade entre 16 e 26 anos à época da inclusão. Veja Desenho de Estudo A. [Quadrivalent Human Papillomavirus (Types 6, 11, 16, 18) Recombinant Vaccine] Today, you can do more
6 Conseqüências físicas e emocionais do papilomavírus humano As conseqüências de curto prazo podem ser graves As verrugas genitais podem ser desgastantes e embaraçosas 3 >30 milhões de novos casos diagnosticados em todo o mundo a cada ano 4 Podem se desenvolver já aos três meses 5 Os tratamentos podem ser traumáticos e embaraçosos 6 As conseqüências de longo prazo podem ser fatais O câncer do colo do útero é precedido por NIC de grau alto em 1 cada 2 casos de câncer do colo do útero no mundo é fatal10 >12% dos casos de NIC 3 podem evoluir para câncer invasivo 11 Verrugas genitais não tratadas Os tratamentos freqüentemente associados a verrugas genitais 6,7 Crioterapia congelamento usando nitrogênio líquido Terapia a laser vaporização usando energia de luz infravermelha focada Eletrocirurgia destruição usando coagulação térmica Podofilotoxina indução de necrose histológica usando um agente antimicótico Imiquimod indução da produção de citocinas pró-inflamatórias Reproduzidas com permissão de A. Ferenczy. ~25% dos casos retornam após vários meses, independentemente do tratamento 7 O câncer de vagina e o de vulva são precedidos por NIVa e NIV de grau alto em 1 cada 3 em 1 cada 4 casos de câncer vagina é fatal12 casos de câncer de vulva é fatal12 ~6% de todos os tipos de câncer ginecológico são de vagina e de vulva 13 Tanto os tipos oncogênicos quanto não-oncogênicos de papilomavírus humano podem causar resultados anormais no exame de Papanicolaou 8 A falta de programas de prevenção torna o câncer de vulva e o de vagina difíceis de detectar. 13 ~3,5 milhões de exames de Papanicolaou anormais exigem acompanhamento médico a cada ano nos Estados Unidos.,9 Os números representam mais de 30 tipos de papilomavírus humano, não apenas os tipos 6, 11, 16 e 18.
7 Mais razões para tomar a vacina hoje Segundo a Organização Mundial da Saúde O momento mais eficaz para a vacinação de meninas e mulheres jovens é antes de se tornarem sexualmente ativas 14 O papilomavírus humano é disseminado principalmente por meio do contato sexual; a transmissão via contato manual-genital e oral-genital também foi documentada. 15 Apenas um encontro pode ser suficiente a infecção pode ocorrer em até um mês após o primeiro contato sexual. 15 A vacinação de meninas e mulheres jovens é recomendada em diversos calendários de imunização ACIP/CDC,16 Idade em anos Meninas de 11 a 12 anos de idade para a vacinação de rotina Adolescentes e mulheres de 13 a 26 anos de idade não vacinadas anteriormente Meninas de 9 e 10 anos podem também ser vacinadas ACIP/CDC= Comitê Consultivo de Práticas de Imunização do Centro de Controle de Doenças dos EUA. Pacientes com infecção anterior por papilomavírus humano, exames anormais de Papanicolaou ou verrugas genitais podem ser protegidas contra os tipos de papilomavírus humano da vacina com os quais ainda não tenham sido infectadas. Não é tarde demais para proteger as pacientes anteriormente expostas Em estudos clínicos com a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18),17 As mulheres infectadas com 1 ou mais tipos de papilomavírus humano da vacina ainda foram protegidas contra a doença causada pelos demais tipos Somente 0,1% das mulheres tiveram exame positivo para todos os 4 tipos de papilomavírus humano da vacina. 17 Suas pacientes sexualmente ativas ainda podem se beneficiar Análises clínicas mundiais de mais de 20 mil mulheres jovens de 16 a 26 anos de idade com histórico de 5 parceiros sexuais. 2 Com base nas recomendações do ACIP 16 O exame de Papanicolaou para DNA ou anticorpos a papilomavírus humano não é necessário antes da vacinação em qualquer idade. Mulheres com exames anormais de Papanicolaou ou com verrugas genitais podem ser vacinadas. Cada consulta é sua chance de administrar a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18)
8 Tolerabilidade e posologia Perfil favorável de tolerabilidade Reações adversas sistêmicas e no local da injeção relacionadas à vacina Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) Placebo com adjuvante (n= 3,470) Placebo de solução salina (n= 594) Sistêmicas Febre % 10 8 Dor % Inchaço % Local da Injeção Eritema % Ferimento % Prurido % Observadas dentre as recipientes da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) em uma freqüência de pelo menos 1,0 % e maior que a do placebo. Veja Desenho de Estudo C. 1 a 15 dias após a vacinação. 1 a 5 dias após a vacinação Dos indivíduos com reações no local da injeção, 94% consideraram sua reação adversa de intensidade leve ou moderada. As desistências do estudo devido a reações adversas relacionadas à vacina foram de 0,2%. Exames de Papanicolaou ou programas de prevenção do câncer do colo do útero deverão continuar mesmo após a aplicação da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18). Esta vacina não protege contra os tipos de papilomavírus humano não incluídos na vacina. Esta vacina não se destina a uso para o tratamento de doenças causadas pelo papilomavírus humano. Deve-se evitar gravidez durante o regime de vacinação com a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18). Assim como para todas as vacinas injetáveis, tratamento médico adequado deverá estar sempre prontamente disponível em caso de reações anafiláticas raras após a administração da vacina Posologia recomendada 1 1ª dose: hoje 2ª dose: dois meses 2 após a 1º dose 3 3ª dose: seis meses após a 1º dose A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) deverá ser administrada por via intramuscular na região deltóide superior do braço ou na área ântero-lateral superior da coxa em três doses separadas de 0,5 ml. Nenhuma diluição ou reconstituição será necessária. Flexibilidade posológica no período de um ano Se um esquema alternativo de vacinação for necessário, a segunda dose deverá ser administrada pelo menos um mês após a primeira dose e a terceira dose deverá ser administrada pelo menos três meses após a segunda dose. Uso com outros medicamentos Em estudos clínicos, a eficácia, o perfil de segurança e a imunogenicidade da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) não sofreram impacto de : analgésicos (11,9%) antibióticos (6,9%) medicamentos antiinflamatórios (9,5%) vitaminas (4,3%) Em estudos clínicos, o uso dos seguintes medicamentos não pareceu afetar as respostas imunológicas à vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) : contraceptivos hormonais (57,5%) corticosteróides (3,3%) Uso concomitante com a vacina contra a hepatite B (recombinante): resultados de estudos clínicos indicam que a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) pode ser administrada concomitantemente (em diferente local de injeção) com a vacina contra a hepatite B (recombinante). II Porcentagem de indivíduos nos estudos clínicos que estavam usando concomitantemente os medicamentos específicos. II Veja Desenho de Estudo D.
9 Administração da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) As informações a seguir foram retiradas da bula do produto. Antes de administrar a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18), recomendamos a leitura da Circular aos Médicos (bula) completa para informações detalhadas sobre o produto. Classe terapêutica A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é uma vacina quadrivalente recombinante que protege contra os tipos 6, 11, 16 e 18 do papilomavírus humano. Indicações A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é indicada para a prevenção do câncer do colo do útero, de vulva e de vagina, bem como de lesões pré-cancerosas ou displásicas, verrugas genitais e infecção causadas pelos tipos 6, 11, 16 e 18 do papilomavírus humano. Posologia e administração A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é recomendada para crianças e adolescentes de 9 a 17 anos de idade e mulheres de 18 a 26 anos de idade. A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) deverá ser administrada por via intramuscular em três doses separadas de 0,5 ml, segundo o seguinte esquema : Primeira dose: na data escolhida Segunda dose: dois meses após a primeira dose Terceira dose: seis meses após a primeira dose Deve-se estimular a adesão dos pacientes ao esquema de vacinação aos 0, 2 e 6 meses. Entretanto, em estudos clínicos, a eficácia foi demonstrada em indivíduos que haviam recebido todas as três doses em um período de um ano. Se um esquema de vacinação alternativo for necessário, a segunda dose deve ser administrada pelo menos um mês após a primeira dose e a terceira dose deve ser administrada pelo menos três meses após a segunda dose. Contra-Indicações A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é contra-indicada a indivíduos hipersensíveis aos princípios ativos ou a qualquer dos excipientes da vacina. Precauções Gerais Assim como para qualquer vacina, a vacinação com a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) pode não resultar em proteção a todos os recipientes da vacina. Esta vacina não se destina ao tratamento de verrugas genitais ativas; câncer de colo de útero, de vulva ou de vagina, nem NIC, NIV ou NIVa. A exemplo de todas as vacinas injetáveis, deve haver sempre tratamento médico disponível em caso de reações anafiláticas raras após a administração da vacina. Esta vacina não protege contra as doenças que não sejam causadas pelo papilomavírus humano. A decisão de administrar ou retardar a vacinação devido a alguma doença febril atual ou recente dependerá da intensidade dos sintomas e de sua etiologia. A febre baixa em si e a infecção respiratória superior em geral não são contra-indicações à vacinação. Indivíduos com resposta imune comprometida, seja devido a uso de terapia imunossupressora, defeito genético, infecção pelo Vírus da Imunodeficiência Humana (HIV), ou outras causas podem mostrar resposta de anticorpos reduzida à imunização ativa (veja a seção INTERAÇÕES MEDICAMENTOSAS da Bula). Esta vacina deverá ser administrada com cautela a indivíduos com trombocitopenia ou qualquer distúrbio de coagulação, porque poderá ocorrer sangramento após a administração intramuscular em tais indivíduos. Gravidez A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) não é recomendada durante a gravidez. Indivíduos que desenvolvam sintomas que indiquem hipersensibilidade após receber uma dose da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) não deverão receber as doses adicionais da vacina.
10 Desenho dos estudos Desenho do Estudo A A eficácia da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) foi avaliada em quatro estudos clínicos controlados com placebo, duplo-cegos, randômicos Fase II e III. O primeiro estudo fase II avaliou o componente papilomavírus humano 16 de a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) (Protocolo 005; N=2.391) e o segundo avaliou todos os 4 componentes da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) (Protocolo 007; N=551). Os estudos Fase III avaliaram a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) em (FUTURE* I) e (FUTURE II) indivíduos. Em conjunto, esses estudos avaliaram mulheres de 16 a 26 anos de idade na inclusão. A duração mediana do acompanhamento foi de 3,9; 2,9; 2,9 e 2,9 anos para o Protocolo 005, Protocolo 007, FUTURE I e FUTURE II, respectivamente. As mulheres que haviam sido expostas ao papilomavírus humano tipos 6, 11, 16 ou 18 antes do recrutamento foram incluídas. Os indivíduos receberam vacina ou placebo no dia da inclusão, dois e seis meses depois disso. As análises primárias de eficácia foram conduzidas em mulheres que receberam todas as três doses no período de um ano da inclusão, sem ter incorrido em importantes desvios do protocolo de estudo e nunca expostas aos tipos correspondentes de papilomavírus humano antes da dose 1 até um mês após a dose 3 (mês 7) (população de eficácia-por-protocolo). Desenho do Estudo B Em um estudo randômico, controlado com placebo com 551 mulheres de 16 a 23 anos de idade, um subconjunto de 241 indivíduos foi avaliado por mais 2 anos de acompanhamento (meses 37-60, por um total de cinco anos). Os indivíduos que originalmente haviam recebido vacinação na inclusão, mês 2 e mês 6, receberam uma aplicação de antígeno (uma outra dose de vacina) no mês 60. Os que haviam recebido placebo, receberam a primeira dose de um regime de três doses da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) no mês 60. As resposta antipapilomavírus humano foram determinadas uma semana e quatro semanas após a aplicação do antígeno (nos indivíduos que originalmente haviam recebido a vacina) ou após a dose 1 (para indivíduos que originalmente haviam recebido placebo). 1 Desenho do Estudo C Em cinco estudos clínicos (quatro deles controlados com placebo), os indivíduos receberam a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) ou placebo no dia da inclusão e aproximadamente dois e seis meses mais tarde. Em todos exceto um dos estudos clínicos, a segurança foi avaliada usando cartão de vacinação (CV) vigilância auxiliar por 14 dias depois de cada injeção de a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) (n=6.160) ou placebo (n=4.064). Desenho do Estudo D A segurança e a imunogenicidade da co-administração da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) e vacina contra a hepatite B (recombinante) (mesma consulta, injeções em locais diferentes) foram avaliadas em um estudo randômico com mulheres que tinham de 16 a 24 anos de idade na data da inclusão. A resposta imune e o perfil de segurança da vacina contra a hepatite B (recombinante) e da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) foram semelhantes seja com os indivíduos vacinados na mesma consulta, seja em consultas diferentes. * FUTURE (Females United To Uniterally Reduce Endo/Ectocervical Disease): Mulheres Unidas para Reduzir Unilateralmente a Doença Endo-Ectocervical.
11 Referências bibliográficas 1. Olsson S-E, Villa LL, Costa RLR, et al. Induction of immune memory following administration of a prophylactic quadrivalent human papillomavirus (HPV) types 6/11/16/18 L1 virus-like particle (VLP) vaccine. Vaccine. 2007;25: Circular aos médicos da Vacina Quadrivalente Recombinante (tipos 6, 11, 16 e 18). Laboratório Merck Sharp & Dohme, São Paulo, Barr E, Tamms G. Quadrivalent human papillomavirus vaccine. Clin Infect Dis. 2007;45: World Health Organization. Executive summary: the state of world health Disponível no site: Acessado em 7 de dezembro de Dupin N. Genital warts. Clin Dermatol. 2004;22: Palefsky J. What Your Doctor May Not Tell You About HPV and Abnormal Pap Smears. New York, NY: Warner Books; Lacey CJN. Therapy for genital human papillomavirus-related disease. J Clin Virol. 2005;32(suppl):S82 S Centers for Disease Control and Prevention. Division of STD Prevention. Sexually transmitted diseases: genital HPV infection [fact sheet]. Disponível no site: Acessado em 7 de dezembro de National Cancer Institute. The Pap test: questions and answers [fact sheet]. Disponível no site: Acessado em 7 de dezembro de World Health Organization. Initiative for Vaccine Research. Viral cancers. Disponível no site: Acessado em 7 de dezembro de Östör AG. Natural history of cervical intraepithelial neoplasia: a critical review. Int J Gynecol Pathol 1993;12: American Cancer Society. Cancer Facts & Figures Atlanta, Ga: American Cancer Society; Joura EA, Leodolter S, Hernandez-Avila M, et al. Efficacy of a quadrivalent prophylactic human papillomavirus (types 6, 11, 16, and 18) L1 virus-like-particle vaccine against high-grade vulval and vaginal lesions: a combined analysis of three randomised clinical trials. Lancet. 2007;369: World Health Organization. Bulletin: vaccinating against cervical cancer. Disponível no site: Acessado em 7 de dezembro de Winer RL, Lee S-K, Hughes JP, Adam DE, Kiviat NB, Koutsky LA. Genital human papillomavirus infection: incidence and risk factors in a cohort of female university students. Am J Epidemiol. 2003;157: Centers for Disease Control and Prevention. Quadrivalent human papillomavirus vaccine: recommendations of the Advisory Committee on Immunization Practices (ACIP). MMWR. 2007;56(RR-2): Ferris DG, for the FUTURE II Study Group. Prophylactic Efficacy of a Quadrivalent Human Papillomavirus (HPV) Vaccine in Women with Virological Evidence of HPV Infection. JID. 2007; 196:
12 Resumo da Circular aos Médicos VACINA QUADRIVALENTE RECOMBINANTE CONTRA PAPILOMAVÍRUS HUMANOS (TIPOS 6, 11, 16 E 18). INDICAÇÕES: a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é indicada para a prevenção de câncer, lesões pré-cancerosas ou displásicas, verrugas genitais e infecção causada pelos tipos de HPV presentes na vacina. A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é indicada para a prevenção das seguintes condições causadas pelos HPV 16 e 18: câncer cervical, da vulva e da vagina; adenocarcinoma do colo do útero in situ (AIS); neoplasia intra-epitelial cervical (NIC) de grau 2 e grau 3; neoplasia intra-epitelial vulvar (NIV) de grau 2 e grau 3; neoplasia intra-epitelial vaginal (NIVa) de grau 2 e grau 3. A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é indicada para a prevenção das seguintes condições causadas pelos HPV 6, 11, 16 e 18: neoplasia intra-epitelial cervical (NIC) de grau 1; verrugas genitais (condiloma acuminado); NIV de grau 1 e NIVa de grau 1; infecção por HPV. CONTRA-INDICAÇÕES: hipersensibilidade aos princípios ativos ou a qualquer dos excipientes da vacina. As pessoas que desenvolvem sintomas indicativos de hipersensibilidade após receber uma dose da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) não devem receber outras doses. ADVERTÊNCIAS: como ocorre com todas as vacinas, a vacinação com a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) pode não resultar em proteção para todos os que recebem a vacina. A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) não é indicada para tratamento de verrugas genitais ativas, câncer cervical, vulvar ou vaginal, NIC, NIV ou NIVa. Esta vacina não proporcionará proteção contra doenças que não sejam causadas pelo HPV. A exemplo de todas as vacinas injetáveis, deve haver sempre tratamento médico disponível em caso de reações anafiláticas raras após a administração da vacina. Pessoas com resposta imunológica comprometida seja por uso de terapia imunossupressora, defeito genético, infecção por vírus da imunodeficiência humana (HIV), ou por outras causas podem apresentar resposta de anticorpos reduzida à imunização ativa (veja INTERAÇÕES MEDICAMENTOSAS). Esta vacina deve ser administrada com cuidado a pessoas com trombocitopenia ou qualquer distúrbio de coagulação porque pode ocorrer sangramento após administração intramuscular nessas pessoas. O profissional de saúde deve informar o paciente, parente ou o responsável que a vacinação não substitui a rotina de triagem de câncer cervical. Mulheres que receberam a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) devem continuar a triagem de câncer cervical, conforme estabelecido pelo médico. Gravidez: categoria de risco B. INTERAÇÕES MEDICAMENTOSAS: Uso com Outras Vacinas: os resultados dos estudos clínicos indicam que a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) pode ser administrada concomitantemente (em locais de administração diferentes) com a vacina contra hepatite B (recombinante). O uso concomitante da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) com vacinas diferentes da vacina contra hepatite B ainda não foi estudado. Assim, não é indicado o uso concomitante da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) com vacinas diferentes da vacina contra hepatite B (por exemplo vacina dt [difteria e tétano], sarampo e rubéola). Uso com Medicamentos Comuns: nos estudos clínicos, 11,9%, 9,5%, 6,9% e 4,3% das participantes utilizavam analgésicos, antiinflamatórios, antibióticos e preparações vitamínicas, respectivamente. A eficácia, a imunogenicidade e o perfil de segurança da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) não sofreram impacto com o uso desses medicamentos. Uso com Contraceptivos Hormonais: nos estudos clínicos, 57,5% das mulheres (com 16 a 26 anos de idade) que receberam a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) usavam contraceptivos hormonais; essa associação não pareceu afetar as respostas imunológicas à vacina. Uso com Esteróides: nos estudos clínicos, 1,7% (n=158), 0,6% (n=56) e 1,0% (n=89) das participantes utilizavam imunossupressores inalatórios, tópicos e parenterais, respectivamente, próximo do horário da administração de uma dose da vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18). Esses medicamentos não pareceram afetar as respostas imunológicas à vacina. Muito poucas participantes nos estudos clínicos estavam tomando esteróides, e a extensão da imunossupressão foi supostamente baixa. Uso com Medicamentos Imunossupressores Sistêmicos: não existem dados sobre o uso concomitante de imunossupressores potentes com a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18). As pessoas que recebem agentes imunossupressores (doses sistêmicas de corticosteróides, antimetabólitos, agentes alquilantes, agentes citotóxicos) podem não responder de maneira ideal à imunização ativa. REAÇÕES ADVERSAS: as reações adversas mais freqüentemente relatadas por indivíduos que receberam a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) e a freqüência observada foram: locais dor (81,3%), inchaço (24, 2%), eritema (23,2%), hemorragia (3,2%) e prurido (2,7%); sistêmicas febre (10,1%). POSOLOGIA E ADMINISTRAÇÂO: a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) é recomendada para meninas e mulheres com 9 a 26 anos de idade. A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) deve ser administrada por via intramuscular em três doses separadas de 0,5 ml, de acordo com o seguinte esquema: primeira dose - em data a escolher; segunda dose 2 meses após a primeira dose; terceira dose 6 meses após a primeira dose. Deve-se estimular a adesão dos pacientes ao esquema de vacinação aos 0, 2 e 6 meses. No entanto, nos estudos clínicos, demonstrou-se eficácia nas pessoas que receberam todas as três doses em um período de um ano. Se for necessário um esquema de vacinação alternativo, a segunda dose deve ser administrada no mínimo um mês após a primeira dose e a terceira dose, no mínimo três meses após a segunda dose. Recomenda-se a leitura da Circular aos Médicos (bula) completa para mais informações sobre reconstituição, conservação e armazenamento. REGISTRO MS: VENDA SOB PRESCRIÇÃO MÉDICA. Nota: antes de prescrever a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18), recomendamos a leitura da Circular aos Médicos (bula) completa, para informações detalhadas sobre os produtos. A PERSISTIREM OS SINTOMAS, O MÉDICO DEVERÁ SER CONSULTADO.
13 A vantagem da proteção com a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) Proteção contra o câncer de colo de útero Eficácia demonstrada contra os tipos de papilomavírus humano que causam aproximadamente 70% de todos os casos de câncer de colo do útero em estudos clínicos Fase II e Fase III DURADOURA Proteção demonstrada com o decorrer do tempo A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) demonstrou memória imunológica em estudos clínicos indicação de proteção de longo prazo 1 Não houve casos de infecção para a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) durante estudos clínicos de 5 anos,1 MAIS A vantagem de ajudar a proteger pacientes contra outras doenças: verrugas genitais câncer de vulva e de vagina displasia cervical Veja Desenho de Estudo A. Veja Desenho de Estudo B. Faça tudo o que puder por suas pacientes vacine hoje Antes de prescrever a vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18), recomendamos a leitura da Circular aos Médicos (bula) completa para informações detalhadas sobre o produto. Copyright 2007 Merck & Co., Inc., Whitehouse Station, NJ, USA. Todos os direitos reservados. MC 553/ GRD-2007-MVD DA GRD-08-BR-(MVD )-553-DA
A vacina contra o câncer de colo de útero elaborada para fazer mais*
 A vacina contra o câncer de colo de útero elaborada para fazer mais* *Proteção adicional contra as verrugas genitais, cânceres de vulva e vagina e displasia cervical. Antes de prescrever, recomendamos
A vacina contra o câncer de colo de útero elaborada para fazer mais* *Proteção adicional contra as verrugas genitais, cânceres de vulva e vagina e displasia cervical. Antes de prescrever, recomendamos
RESPOSTA RÁPIDA 43/2014. VACINA HPV em paciente com diagnóstico de HPV+ (neoplasia + intraepitelial grau I)
 RESPOSTA RÁPIDA 43/2014 VACINA HPV em paciente com diagnóstico de HPV+ (neoplasia + intraepitelial grau I) SOLICITANTE NÚMERO DO PROCESSO Dra. Herilene de Oliveira Andrade Juíza de Direito da Comarca de
RESPOSTA RÁPIDA 43/2014 VACINA HPV em paciente com diagnóstico de HPV+ (neoplasia + intraepitelial grau I) SOLICITANTE NÚMERO DO PROCESSO Dra. Herilene de Oliveira Andrade Juíza de Direito da Comarca de
Identificação do Medicamento. Vacina quadrivalente recombinante contra papilomavírus humano. (tipos 6, 11, 16 e 18)
 Identificação do Medicamento Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) FORMA FARMACÊUTICA E APRESENTAÇÕES A vacina quadrivalente recombinante contra papilomavírus
Identificação do Medicamento Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) FORMA FARMACÊUTICA E APRESENTAÇÕES A vacina quadrivalente recombinante contra papilomavírus
Você sabia? 8 em cada 10 homens e mulheres já pegaram ou pegarão algum tipo de HPV. 1,2
 Você sabia? O HPV é um vírus silencioso que atinge homens e mulheres e que pode causar câncer de colo do útero e verrugas genitais. 1 8 em cada 10 já pegaram ou pegarão algum tipo de HPV. 1,2 20% das pessoas
Você sabia? O HPV é um vírus silencioso que atinge homens e mulheres e que pode causar câncer de colo do útero e verrugas genitais. 1 8 em cada 10 já pegaram ou pegarão algum tipo de HPV. 1,2 20% das pessoas
vacina papilomavírus humano 6, 11, 16 e 18 (recombinante)
 IDENTIFICAÇÃO DO MEDICAMENTO vacina papilomavírus humano 6, 11, 16 e 18 (recombinante) APRESENTAÇÕES A vacina papilomavírus humano 6, 11, 16 e 18 (recombinante) é uma suspensão injetável estéril para administração
IDENTIFICAÇÃO DO MEDICAMENTO vacina papilomavírus humano 6, 11, 16 e 18 (recombinante) APRESENTAÇÕES A vacina papilomavírus humano 6, 11, 16 e 18 (recombinante) é uma suspensão injetável estéril para administração
HPV. Câncer do Colo do Útero Verrugas Genitais. G u i a d e P ediatria
 HPV Câncer do Colo do Útero Verrugas Genitais G u i a d e P ediatria Você tenta fazer tudo que é possível para proteger sua filha, para garantir que tudo dê certo hoje e amanhã. Ela confia em você. Essa
HPV Câncer do Colo do Útero Verrugas Genitais G u i a d e P ediatria Você tenta fazer tudo que é possível para proteger sua filha, para garantir que tudo dê certo hoje e amanhã. Ela confia em você. Essa
Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18)
 IDENTIFICAÇÃO DO MEDICAMENTO: Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) APRESENTAÇÕES A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6,
IDENTIFICAÇÃO DO MEDICAMENTO: Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) APRESENTAÇÕES A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6,
VACINA CONTRA PAPILOMAVÍRUS HUMANO HPV
 1º Trimestre 2007 VACINA CONTRA PAPILOMAVÍRUS HUMANO HPV Em junho de 2006, foi aprovada pela FDA (Food And Drug Administration) dos Estados Unidos (EUA) uma vacina recombinante quadrivalente contra papilomavírus
1º Trimestre 2007 VACINA CONTRA PAPILOMAVÍRUS HUMANO HPV Em junho de 2006, foi aprovada pela FDA (Food And Drug Administration) dos Estados Unidos (EUA) uma vacina recombinante quadrivalente contra papilomavírus
Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18)
 IDENTIFICAÇÃO DO MEDICAMENTO Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) APRESENTAÇÕES A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6,
IDENTIFICAÇÃO DO MEDICAMENTO Vacina quadrivalente recombinante contra papilomavírus humano (tipos 6, 11, 16 e 18) APRESENTAÇÕES A vacina quadrivalente recombinante contra papilomavírus humano (tipos 6,
Vacina anti HPV. Dra. Maristela Vargas Peixoto
 Vacina anti HPV Dra. Maristela Vargas Peixoto Segundo o CDC, ocorrem cerca de 300 milhões de casos de infecção cervical pelo HPV por ano, e cerca de 400.000 casos de carcinomas invasivos 0,13% das pacientes
Vacina anti HPV Dra. Maristela Vargas Peixoto Segundo o CDC, ocorrem cerca de 300 milhões de casos de infecção cervical pelo HPV por ano, e cerca de 400.000 casos de carcinomas invasivos 0,13% das pacientes
INFORME TÉCNICO DA VACINA HPV (PAPILOMAVÍRUS HUMANO 6, 11, 16, 18 (RECOMBINANTE)) - 2015
 INFORME TÉCNICO DA VACINA HPV (PAPILOMAVÍRUS HUMANO 6, 11, 16, 18 (RECOMBINANTE)) - 2015 Apresentação O Ministério da Saúde com o objetivo de reforçar as atuais ações de prevenção do câncer do colo do
INFORME TÉCNICO DA VACINA HPV (PAPILOMAVÍRUS HUMANO 6, 11, 16, 18 (RECOMBINANTE)) - 2015 Apresentação O Ministério da Saúde com o objetivo de reforçar as atuais ações de prevenção do câncer do colo do
Natural History of HPV Infections NIC 1 NIC 2 NIC 3
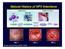 Natural History of HPV Infections NIC 1 NIC 2 NIC 3 Vacina Quadrivalente (GARDASIL ) Eficácia cia na Prevenção de NIC 2/3+ (20 meses) Vacina HPV (n=8.489) Placebo (n=8.460) Eficácia cia da Vacina I. C.
Natural History of HPV Infections NIC 1 NIC 2 NIC 3 Vacina Quadrivalente (GARDASIL ) Eficácia cia na Prevenção de NIC 2/3+ (20 meses) Vacina HPV (n=8.489) Placebo (n=8.460) Eficácia cia da Vacina I. C.
-Os Papiloma Vírus Humanos (HPV) são vírus da família Papovaviridae.
 -Os Papiloma Vírus Humanos (HPV) são vírus da família Papovaviridae. -Chamado de HPV, aparece na forma de doenças como condiloma acuminado, verruga genital ou crista de galo. -Há mais de 200 subtipos do
-Os Papiloma Vírus Humanos (HPV) são vírus da família Papovaviridae. -Chamado de HPV, aparece na forma de doenças como condiloma acuminado, verruga genital ou crista de galo. -Há mais de 200 subtipos do
O primeiro passo para evitar o câncer do colo do útero é se informar. Que tal começar agora?
 O primeiro passo para evitar o câncer do colo do útero é se informar. Que tal começar agora? Folheto Consumidora 9x15cm.indd 1 7/21/08 6:07:48 PM A cada ano, 500.000 mulheres no mundo têm câncer do colo
O primeiro passo para evitar o câncer do colo do útero é se informar. Que tal começar agora? Folheto Consumidora 9x15cm.indd 1 7/21/08 6:07:48 PM A cada ano, 500.000 mulheres no mundo têm câncer do colo
HPV = human papillomavirus ou papillomavirus humano; É um tipo de vírus que ataca o tecido epitelial humano (Cutts et Al, 2007; Soper, 2006);
 HPV HPV HPV = human papillomavirus ou papillomavirus humano; É um tipo de vírus que ataca o tecido epitelial humano (Cutts et Al, 2007; Soper, 2006); São conhecidos mais de 100 tipos de HPV (Linhares e
HPV HPV HPV = human papillomavirus ou papillomavirus humano; É um tipo de vírus que ataca o tecido epitelial humano (Cutts et Al, 2007; Soper, 2006); São conhecidos mais de 100 tipos de HPV (Linhares e
Últimas evidências da efetividade das vacinas contra o HPV. Perspectivas clínicas
 Últimas evidências da efetividade das vacinas contra o HPV Perspectivas clínicas Fábio Russomano 30 de agosto de 2008 É permitida a reprodução total ou parcial, desde que citada a fonte: Russomano F, 2008
Últimas evidências da efetividade das vacinas contra o HPV Perspectivas clínicas Fábio Russomano 30 de agosto de 2008 É permitida a reprodução total ou parcial, desde que citada a fonte: Russomano F, 2008
Vacinação contra o HPV
 Vacinação contra o HPV Meleiro, março de 2014 Enfermeira Cristiane Sec Mun Saúde de Meleiro. ESF Papiloma Vírus Humano - HPV O HPV é um vírus (papilomavírus humano) transmitido pelo contato direto com
Vacinação contra o HPV Meleiro, março de 2014 Enfermeira Cristiane Sec Mun Saúde de Meleiro. ESF Papiloma Vírus Humano - HPV O HPV é um vírus (papilomavírus humano) transmitido pelo contato direto com
REQUERIMENTO DE INFORMAÇÃO N.º,DE 2011
 REQUERIMENTO DE INFORMAÇÃO N.º,DE 2011 (Do Sr. Antonio Carlos Mendes Thame) Requer informações ao Senhor Ministro de Estado da Saúde a respeito das estimativas das despesas orçamentárias para o qüinqüênio
REQUERIMENTO DE INFORMAÇÃO N.º,DE 2011 (Do Sr. Antonio Carlos Mendes Thame) Requer informações ao Senhor Ministro de Estado da Saúde a respeito das estimativas das despesas orçamentárias para o qüinqüênio
- Vacina monovalente contra a poliomielite (VIP)
 VACINAÇÃO PERTENCENTE AO PNV - A Vacina contra a Tuberculose (BCG) Tipo de vacina: Vacina de bacilos vivos atenuados Mycobacterium bovis : Gravidez Imunodeficiência celular, congénita ou adquirida Tratamentos
VACINAÇÃO PERTENCENTE AO PNV - A Vacina contra a Tuberculose (BCG) Tipo de vacina: Vacina de bacilos vivos atenuados Mycobacterium bovis : Gravidez Imunodeficiência celular, congénita ou adquirida Tratamentos
Guia Prático. Vacinação da Mulher
 Guia Prático Vacinação da Mulher 2014 GUIA DA VACINAÇÃO DA MULHER Federação Brasileira das Associações de Ginecologia e Obstetrícia DIRETORIA Presidente: Etelvino de Souza Trindade Secretária Executiva:
Guia Prático Vacinação da Mulher 2014 GUIA DA VACINAÇÃO DA MULHER Federação Brasileira das Associações de Ginecologia e Obstetrícia DIRETORIA Presidente: Etelvino de Souza Trindade Secretária Executiva:
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Gardasil, suspensão injectável. Vacina contra o Papilomavírus Humano [Tipos 6, 11, 16, 18] (Recombinante, adsorvida). 2. COMPOSIÇÃO
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Gardasil, suspensão injectável. Vacina contra o Papilomavírus Humano [Tipos 6, 11, 16, 18] (Recombinante, adsorvida). 2. COMPOSIÇÃO
SUPERINTENDÊNCIA DE POLÍTICAS DE ATENÇÃO INTEGFRAL À SAÚDE Gerência de Saúde da Mulher, Criança e Adolescente
 SUPERINTENDÊNCIA DE POLÍTICAS DE ATENÇÃO INTEGFRAL À SAÚDE Gerência de Saúde da Mulher, Criança e Adolescente Clique para editar o estilo do subtítulo mestre Dr. Claudio Gonzaga Amorim Área Técnica do
SUPERINTENDÊNCIA DE POLÍTICAS DE ATENÇÃO INTEGFRAL À SAÚDE Gerência de Saúde da Mulher, Criança e Adolescente Clique para editar o estilo do subtítulo mestre Dr. Claudio Gonzaga Amorim Área Técnica do
Papiloma Vírus Humano - HPV
 VACINAÇÃO HPV 2015 Papiloma Vírus Humano - HPV O vírus HPV é altamente contagioso, sendo possível contaminar-se com uma única exposição. A sua transmissão se dá por contato direto com a pele ou mucosa
VACINAÇÃO HPV 2015 Papiloma Vírus Humano - HPV O vírus HPV é altamente contagioso, sendo possível contaminar-se com uma única exposição. A sua transmissão se dá por contato direto com a pele ou mucosa
Susana Aidé Profª Adjunta de Ginecologia da Uff
 Susana Aidé Profª Adjunta de Ginecologia da Uff Câncer % Associada com Alguns Tipos de HPV 90 80 70 60 50 40 30 20 10 0 + Colo do Útero+,1,2 Larínge e Trato OroVaginal/ Peniano 2,4 Anal 2,4 Aerodigestivo
Susana Aidé Profª Adjunta de Ginecologia da Uff Câncer % Associada com Alguns Tipos de HPV 90 80 70 60 50 40 30 20 10 0 + Colo do Útero+,1,2 Larínge e Trato OroVaginal/ Peniano 2,4 Anal 2,4 Aerodigestivo
Vacinas contra HPV. Fábio Russomano
 Vacinas contra HPV Curso de Atualização em Patologia do Trato Genital Inferior e Colposcopia ABG RJ Instituto de Ginecologia da UFRJ 20 de junho de 2009 Fábio Russomano Sumário Cenário do Câncer de Colo
Vacinas contra HPV Curso de Atualização em Patologia do Trato Genital Inferior e Colposcopia ABG RJ Instituto de Ginecologia da UFRJ 20 de junho de 2009 Fábio Russomano Sumário Cenário do Câncer de Colo
vacina tétano Forma farmacêutica e apresentação: Suspensão injetável. - Cartucho contendo uma seringa de dose única.
 1 vacina tétano Forma farmacêutica e apresentação: Suspensão injetável. - Cartucho contendo uma seringa de dose única. A vacina tétano deve ser administrada por via intramuscular. Não utilize a vacina
1 vacina tétano Forma farmacêutica e apresentação: Suspensão injetável. - Cartucho contendo uma seringa de dose única. A vacina tétano deve ser administrada por via intramuscular. Não utilize a vacina
Fernanda Valdameri Scapinello Médica Infectologista
 VACINA PARA HPV F d V ld i S i ll Fernanda Valdameri Scapinello Médica Infectologista HPV Doença Sexualmente Transmissível mais comum no mundo Período de 12 meses: homem sexualmente ativo adquirir um
VACINA PARA HPV F d V ld i S i ll Fernanda Valdameri Scapinello Médica Infectologista HPV Doença Sexualmente Transmissível mais comum no mundo Período de 12 meses: homem sexualmente ativo adquirir um
CANCER DE COLO DE UTERO FERNANDO CAMILO MAGIONI ENFERMEIRO DO TRABALHO
 CANCER DE COLO DE UTERO FERNANDO CAMILO MAGIONI ENFERMEIRO DO TRABALHO CANCER DE COLO DE UTERO O câncer de colo uterino é o câncer mais comum entre as mulheres no Brasil, correspondendo a, aproximadamente,
CANCER DE COLO DE UTERO FERNANDO CAMILO MAGIONI ENFERMEIRO DO TRABALHO CANCER DE COLO DE UTERO O câncer de colo uterino é o câncer mais comum entre as mulheres no Brasil, correspondendo a, aproximadamente,
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO VETERINÁRIO Equilis Prequenza Te, suspensão injetável para equinos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose de 1 ml:
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO VETERINÁRIO Equilis Prequenza Te, suspensão injetável para equinos 2. COMPOSIÇÃO QUALITATIVA E QUANTITATIVA Por dose de 1 ml:
A VACINA QUADRIVALENTE CONTRA HPV 17. 1. O que é a VACINA QUADRIVALENTE CONTRA HPV?
 O que é o HPV 5-8? O HPV é um vírus silencioso na maioria das vezes. Muitos destes são eliminados sem sequer a pessoa se dar conta que teve contato. Existem mais de 100 tipos de HPV e destes, aproximadamente,
O que é o HPV 5-8? O HPV é um vírus silencioso na maioria das vezes. Muitos destes são eliminados sem sequer a pessoa se dar conta que teve contato. Existem mais de 100 tipos de HPV e destes, aproximadamente,
CÓLERA/ DIARRÉIA DO VIAJANTE
 ANTITETÂNICA Indicada para prevenção do tétano. Utilizada para imunização de adultos e idosos, inclusive gestantes (após a 12ª semana). Contraindicação: Não há, exceto àquelas comuns a todas as vacinas:
ANTITETÂNICA Indicada para prevenção do tétano. Utilizada para imunização de adultos e idosos, inclusive gestantes (após a 12ª semana). Contraindicação: Não há, exceto àquelas comuns a todas as vacinas:
Direcção-Geral da Saúde
 Assunto: Programa Nacional de Vacinação (PNV) Introdução da vacina contra infecções por Vírus do Papiloma Humano Nº: 22/DSCS/DPCD DATA: 17/10/08 Para: Contacto na DGS: Médicos e enfermeiros dos Centros
Assunto: Programa Nacional de Vacinação (PNV) Introdução da vacina contra infecções por Vírus do Papiloma Humano Nº: 22/DSCS/DPCD DATA: 17/10/08 Para: Contacto na DGS: Médicos e enfermeiros dos Centros
Vacinas Bivalente e Quadrivalente: Prós e contras
 IX S impós io de Atualização em G inecolog ia Oncológ ica III S impós io de G enitos copia do DF AB PTG IC C apítulo DF 12-14 de Maio de 2011 Vacinas Bivalente e Quadrivalente: Prós e contras Fábio Russomano
IX S impós io de Atualização em G inecolog ia Oncológ ica III S impós io de G enitos copia do DF AB PTG IC C apítulo DF 12-14 de Maio de 2011 Vacinas Bivalente e Quadrivalente: Prós e contras Fábio Russomano
vacina hepatite A (inativada)
 vacina hepatite A (inativada) Forma farmacêutica e apresentações: Suspensão injetável. Cartucho contendo uma seringa de uma dose de 0,5 ml. Cartucho contendo 5 seringas de uma dose de 0,5 ml. Cartucho
vacina hepatite A (inativada) Forma farmacêutica e apresentações: Suspensão injetável. Cartucho contendo uma seringa de uma dose de 0,5 ml. Cartucho contendo 5 seringas de uma dose de 0,5 ml. Cartucho
Derrotar o cancro do útero
 Portuguese translation of Beating cervical cancer The HPV vaccine questions and answers for parents of girls in Year 9 Derrotar o cancro do útero A vacina HPV perguntas e respostas para os pais de jovens
Portuguese translation of Beating cervical cancer The HPV vaccine questions and answers for parents of girls in Year 9 Derrotar o cancro do útero A vacina HPV perguntas e respostas para os pais de jovens
Nilma Antas Neves Profa Ginecologia da Universidade Federal da Bahia Presidente da Comissão de Vacinas da FEBRASGO Vice-Presidente da ABPTGIC
 Nilma Antas Neves Profa Ginecologia da Universidade Federal da Bahia Presidente da Comissão de Vacinas da FEBRASGO Vice-Presidente da ABPTGIC 1. Indicações e proteção global contra doenças 2. Imunidade
Nilma Antas Neves Profa Ginecologia da Universidade Federal da Bahia Presidente da Comissão de Vacinas da FEBRASGO Vice-Presidente da ABPTGIC 1. Indicações e proteção global contra doenças 2. Imunidade
Edison Natal Fedrizzi. Declaração de conflito de interesse
 Edison Natal Fedrizzi Declaração de conflito de interesse Não recebi qualquer forma de pagamento ou auxílio financeiro de entidade pública ou privada para pesquisa ou desenvolvimento de método diagnóstico
Edison Natal Fedrizzi Declaração de conflito de interesse Não recebi qualquer forma de pagamento ou auxílio financeiro de entidade pública ou privada para pesquisa ou desenvolvimento de método diagnóstico
RASTREIO EM SITUAÇÕES ESPECIAIS
 RASTREIO EM SITUAÇÕES ESPECIAIS Maria José de Camargo IFF / FIOCRUZ CERVIX www.cervixcolposcopia.com.br Gestantes Pós-menopausa Histerectomizadas Imunossuprimidas Adolescentes Mulheres sem história de
RASTREIO EM SITUAÇÕES ESPECIAIS Maria José de Camargo IFF / FIOCRUZ CERVIX www.cervixcolposcopia.com.br Gestantes Pós-menopausa Histerectomizadas Imunossuprimidas Adolescentes Mulheres sem história de
Cancer de Colo do Útero
 Cancer de Colo do Útero Câncer de colo do útero são alterações celulares que tem uma progressão gradativa e é por isto que esta é uma doença curável quando descoberta no início. Esta é a razão do exame
Cancer de Colo do Útero Câncer de colo do útero são alterações celulares que tem uma progressão gradativa e é por isto que esta é uma doença curável quando descoberta no início. Esta é a razão do exame
RECOMENDAÇÕES TÉCNICAS DA VACINA CONTRA FEBRE AMARELA
 RECOMENDAÇÕES TÉCNICAS DA VACINA CONTRA FEBRE AMARELA SECRETARIA ESTADUAL DE SAÚDE SUPERITENDÊNCIA DE VIGILÂNCIA EM SAÚDE GERÊNCIA DE IMUNIZAÇÃO E REDE FRIO ESQUEMA VACINAL NOTA INFORMATIVA Nº143/CGPNI/DEVIT/SVS/MS/18/122014
RECOMENDAÇÕES TÉCNICAS DA VACINA CONTRA FEBRE AMARELA SECRETARIA ESTADUAL DE SAÚDE SUPERITENDÊNCIA DE VIGILÂNCIA EM SAÚDE GERÊNCIA DE IMUNIZAÇÃO E REDE FRIO ESQUEMA VACINAL NOTA INFORMATIVA Nº143/CGPNI/DEVIT/SVS/MS/18/122014
Vacina Pentavalente. Nomenclatura. Proteção. Forma Farmacêutica Apresentação
 Vacina Pentavalente Nomenclatura Proteção Forma Farmacêutica Apresentação Lab. Produtor Composição Indicação Precauções Contra Indicações - Vacina adsorvida difteria, tétano, pertussis, hepatite B (recombinante)
Vacina Pentavalente Nomenclatura Proteção Forma Farmacêutica Apresentação Lab. Produtor Composição Indicação Precauções Contra Indicações - Vacina adsorvida difteria, tétano, pertussis, hepatite B (recombinante)
Perguntas e respostas sobre a vacinação contra o HPV
 Perguntas e respostas sobre a vacinação contra o HPV 1) A vacina é mesmo necessária? Atualmente, cerca de 5% de todos os cânceres do homem e 10% dos da mulher são causados pelo HPV, que atinge mais de
Perguntas e respostas sobre a vacinação contra o HPV 1) A vacina é mesmo necessária? Atualmente, cerca de 5% de todos os cânceres do homem e 10% dos da mulher são causados pelo HPV, que atinge mais de
vacina tétano Potência estimada com o limite inferior de confiança em P = 0.95.
 1 vacina tétano Forma farmacêutica e apresentação: Suspensão injetável. - Cartucho contendo uma seringa de dose única. A vacina tétano deve ser administrada por via intramuscular. Não utilize a vacina
1 vacina tétano Forma farmacêutica e apresentação: Suspensão injetável. - Cartucho contendo uma seringa de dose única. A vacina tétano deve ser administrada por via intramuscular. Não utilize a vacina
Informação pode ser o melhor remédio. Hepatite
 Informação pode ser o melhor remédio. Hepatite HEPATITE A hepatite é uma inflamação do fígado provocada na maioria das vezes por um vírus. Diferentes tipos de vírus podem provocar hepatite aguda, que se
Informação pode ser o melhor remédio. Hepatite HEPATITE A hepatite é uma inflamação do fígado provocada na maioria das vezes por um vírus. Diferentes tipos de vírus podem provocar hepatite aguda, que se
2) Qual a importância da vacina conter as duas linhagens de vírus B?
 VACINAS INFLUENZA NO BRASIL EM 2015 Renato Kfouri Vice-presidente da SBIm Juarez Cunha Diretor da SBIm 1) Como são as novas vacinas quadrivalentes? As vacinas influenza utilizadas em nosso país até o ano
VACINAS INFLUENZA NO BRASIL EM 2015 Renato Kfouri Vice-presidente da SBIm Juarez Cunha Diretor da SBIm 1) Como são as novas vacinas quadrivalentes? As vacinas influenza utilizadas em nosso país até o ano
HPV. Papiloma Virus. Trata-se de uma infecção adquirida através de contato sexual.
 HPV Papiloma Virus Todo ano, cerca de 230 mil mulheres morrem no mundo vítimas do câncer no colo do útero. E, para o surgimento desse tipo de câncer, é necessário que a vítima tenha sido infectada pelo
HPV Papiloma Virus Todo ano, cerca de 230 mil mulheres morrem no mundo vítimas do câncer no colo do útero. E, para o surgimento desse tipo de câncer, é necessário que a vítima tenha sido infectada pelo
Gino-Loprox ciclopirox olamina
 Modelo de Bula SANOFI-AVENTIS FARMACÊUTICA LTDA Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. Gino-Loprox ciclopirox olamina Forma farmacêutica e apresentação
Modelo de Bula SANOFI-AVENTIS FARMACÊUTICA LTDA Esta bula é continuamente atualizada. Favor proceder a sua leitura antes de utilizar o medicamento. Gino-Loprox ciclopirox olamina Forma farmacêutica e apresentação
HPV. Câncer do Colo do Útero Verrugas Genitais. G u i a d e G i n e c o l o g i a
 HPV Câncer do Colo do Útero Verrugas Genitais G u i a d e G i n e c o l o g i a Para você que é corajosa e tem confiança no futuro. Você tem muitos planos para obter sucesso profissional sem perder a alegria
HPV Câncer do Colo do Útero Verrugas Genitais G u i a d e G i n e c o l o g i a Para você que é corajosa e tem confiança no futuro. Você tem muitos planos para obter sucesso profissional sem perder a alegria
Vacinas contra o pneumococo
 .... Simpósio Nacional de Doença Pneumocócica e Influenza São Paulo, 20 e 21 de Setembro de Vacinas contra o pneumococo Lúcia Helena de Oliveira Assessora Regional para Novas Vacinas Unidade de Imunizações
.... Simpósio Nacional de Doença Pneumocócica e Influenza São Paulo, 20 e 21 de Setembro de Vacinas contra o pneumococo Lúcia Helena de Oliveira Assessora Regional para Novas Vacinas Unidade de Imunizações
RASTREIO DO CANCRO DO COLO DO ÚTERO E VACINAÇÃO CONTRA O HPV. Pedro Vieira Baptista
 2012 Norte 24 de Outubro Quinta-feira RASTREIO DO CANCRO DO COLO DO ÚTERO E VACINAÇÃO CONTRA O HPV Pedro Vieira Baptista Para começar... Referência a condilomatose anogenital por autores gregos e romanos.
2012 Norte 24 de Outubro Quinta-feira RASTREIO DO CANCRO DO COLO DO ÚTERO E VACINAÇÃO CONTRA O HPV Pedro Vieira Baptista Para começar... Referência a condilomatose anogenital por autores gregos e romanos.
IMUNOBIOLÓGICOS UTILIZADOS NA UNIDADE NEONATAL
 USO DE IMUNOBIOLÓGICOS NA ENFERMAGEM UNIDADE NEONATAL Rotinas Assistenciais da Maternidade-Escola da Universidade Federal do Rio de Janeiro A garantia da imunização por meio das vacinas básicas disponibilizadas
USO DE IMUNOBIOLÓGICOS NA ENFERMAGEM UNIDADE NEONATAL Rotinas Assistenciais da Maternidade-Escola da Universidade Federal do Rio de Janeiro A garantia da imunização por meio das vacinas básicas disponibilizadas
BULA PARA O PACIENTE
 BULA PARA O PACIENTE Modelo de texto de bula Aldara imiquimode Forma farmacêutica: Creme Apresentação: Cartucho contendo 6 (12) sachês com 250 mg Aldara (imiquimode) deve ser administrado da seguinte forma:
BULA PARA O PACIENTE Modelo de texto de bula Aldara imiquimode Forma farmacêutica: Creme Apresentação: Cartucho contendo 6 (12) sachês com 250 mg Aldara (imiquimode) deve ser administrado da seguinte forma:
VACINAS ANTIPNEUMOCÓCICAS CONJUGADAS
 VACINAS ANTIPNEUMOCÓCICAS CONJUGADAS As vacinas conjugadas são aquelas nas quais os antígenos bacterianos são ligados a carreadores protéicos, facilitando o processamento pelos linfócitos T, gerando então,
VACINAS ANTIPNEUMOCÓCICAS CONJUGADAS As vacinas conjugadas são aquelas nas quais os antígenos bacterianos são ligados a carreadores protéicos, facilitando o processamento pelos linfócitos T, gerando então,
Papilomavírus Humano HPV
 Papilomavírus Humano HPV -BIOLOGIA- Alunos: André Aroeira, Antonio Lopes, Carlos Eduardo Rozário, João Marcos Fagundes, João Paulo Sobral e Hélio Gastão Prof.: Fragoso 1º Ano E.M. T. 13 Agente Causador
Papilomavírus Humano HPV -BIOLOGIA- Alunos: André Aroeira, Antonio Lopes, Carlos Eduardo Rozário, João Marcos Fagundes, João Paulo Sobral e Hélio Gastão Prof.: Fragoso 1º Ano E.M. T. 13 Agente Causador
Vacina pneumocócica, polivalente, MSD. A Vacina pneumocócica, polivalente, MSD é apresentada em frascos de dose única (0,5 ml).
 FORMA FARMACÊUTICA E APRESENTAÇÃO Vacina pneumocócica, polivalente, MSD A Vacina pneumocócica, polivalente, MSD é apresentada em frascos de dose única (0,5 ml). USO PEDIÁTRICO E ADULTO COMPOSIÇÃO Cada
FORMA FARMACÊUTICA E APRESENTAÇÃO Vacina pneumocócica, polivalente, MSD A Vacina pneumocócica, polivalente, MSD é apresentada em frascos de dose única (0,5 ml). USO PEDIÁTRICO E ADULTO COMPOSIÇÃO Cada
QUAIS OS TIPOS DE HPV MAIS COMUNS QUE PODEM CAUSAR CÂNCER?
 O QUE É O HPV? Sigla para Papilomavírus Humano, são vírus capazes de infectar a pele ou a mucosa. Existem mais de 150 tipos diferentes de HPV, dos quais 40 podem infectar o trato genital e, destes, 12
O QUE É O HPV? Sigla para Papilomavírus Humano, são vírus capazes de infectar a pele ou a mucosa. Existem mais de 150 tipos diferentes de HPV, dos quais 40 podem infectar o trato genital e, destes, 12
CONSELHO REGIONAL DE ENFERMAGEM DO RIO GRANDE DO SUL Autarquia Federal Lei nº 5.905/73
 PARECER CTSAB Nº 02/2013 Porto Alegre, 08 de julho de 2013. Aplicação de nitrogênio líquido em lesões genitais a partir de prescrição médica por profissional enfermeiro. I - Relatório Trata-se de um Parecer
PARECER CTSAB Nº 02/2013 Porto Alegre, 08 de julho de 2013. Aplicação de nitrogênio líquido em lesões genitais a partir de prescrição médica por profissional enfermeiro. I - Relatório Trata-se de um Parecer
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Gardasil, suspensão injectável. Vacina contra o Papilomavírus Humano [Tipos 6, 11, 16, 18] (Recombinante, adsorvida). 2. COMPOSIÇÃO
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Gardasil, suspensão injectável. Vacina contra o Papilomavírus Humano [Tipos 6, 11, 16, 18] (Recombinante, adsorvida). 2. COMPOSIÇÃO
A vacina contra o HPV - perguntas e respostas para pais de raparigas no 9º ano a partir de setembro de 2014
 Portuguese translation of Beating cervical cancer The HPV vaccine questions and answers for parents of girls in Year 9 from September 2014 Combater o cancro do colo do útero A vacina contra o HPV - perguntas
Portuguese translation of Beating cervical cancer The HPV vaccine questions and answers for parents of girls in Year 9 from September 2014 Combater o cancro do colo do útero A vacina contra o HPV - perguntas
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 Este medicamento está sujeito a monitorização adicional. Isto irá permitir a rápida identificação de nova informação de segurança. Pede-se aos profissionais
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 Este medicamento está sujeito a monitorização adicional. Isto irá permitir a rápida identificação de nova informação de segurança. Pede-se aos profissionais
Vacina contra Papilomavírus. humano (HPV): Promessas e Desafios. Edson D. Moreira Jr., MD, PhD. Centro de Pesquisas Gonçalo. Moniz FIOCRUZ - Bahia
 Vacina contra Papilomavírus humano (HPV): Promessas e Desafios Edson D. Moreira Jr., MD, PhD Centro de Pesquisas Gonçalo Moniz FIOCRUZ - Bahia Sumário Biologia do HPV Epidemiologia e Impacto das Doenças
Vacina contra Papilomavírus humano (HPV): Promessas e Desafios Edson D. Moreira Jr., MD, PhD Centro de Pesquisas Gonçalo Moniz FIOCRUZ - Bahia Sumário Biologia do HPV Epidemiologia e Impacto das Doenças
Associação Brasileira de Patologia do Trato Genital Inferior e Colposcopia Boletim Eletrônico Dezembro 2012 60ª edição
 Associação Brasileira de Patologia do Trato Genital Inferior e Colposcopia Boletim Eletrônico Dezembro 2012 60ª edição QUAIS AS EVIDÊNCIAS CIENTÍFICAS DE ALÍVIO DA DOR EM MULHERES COM NEOPLASIA INTRAEPITELIAL
Associação Brasileira de Patologia do Trato Genital Inferior e Colposcopia Boletim Eletrônico Dezembro 2012 60ª edição QUAIS AS EVIDÊNCIAS CIENTÍFICAS DE ALÍVIO DA DOR EM MULHERES COM NEOPLASIA INTRAEPITELIAL
IMPORTANTE. Os imunobiológicos devem ser mantidos no REFRIGERADOR com temperatura entre -2 e +8 C.
 Administração de Imunobiológicos IMPORTANTE Os imunobiológicos devem ser mantidos no REFRIGERADOR com temperatura entre -2 e +8 C. Contra indicações gerais: Imunodeficiência congênita ou adquirida Neoplasias
Administração de Imunobiológicos IMPORTANTE Os imunobiológicos devem ser mantidos no REFRIGERADOR com temperatura entre -2 e +8 C. Contra indicações gerais: Imunodeficiência congênita ou adquirida Neoplasias
Citologia ou teste de HPV no rastreio primário?
 UNICAMP Citologia ou teste de HPV no rastreio primário? Luiz Carlos Zeferino Professor Titular em Ginecologia Departamento de Tocoginecologia Faculdade de Ciências Médicas CAISM - UNICAMP Clique para editar
UNICAMP Citologia ou teste de HPV no rastreio primário? Luiz Carlos Zeferino Professor Titular em Ginecologia Departamento de Tocoginecologia Faculdade de Ciências Médicas CAISM - UNICAMP Clique para editar
Perguntas e respostas sobre imunodeficiências primárias
 Perguntas e respostas sobre imunodeficiências primárias Texto elaborado pelos Drs Pérsio Roxo Júnior e Tatiana Lawrence 1. O que é imunodeficiência? 2. Estas alterações do sistema imunológico são hereditárias?
Perguntas e respostas sobre imunodeficiências primárias Texto elaborado pelos Drs Pérsio Roxo Júnior e Tatiana Lawrence 1. O que é imunodeficiência? 2. Estas alterações do sistema imunológico são hereditárias?
HPV em mulheres infectadas pelo HIV Goldman ARNP, MPH
 Welcome to I-TECH HIV/AIDS Clinical Seminar Series 30 de Agosto de 2012 HPV em mulheres infectadas pelo HIV Goldman ARNP, MPH Objectivos 1. Discutir a epidemiologia do HPV entre mulheres infectadas pelo
Welcome to I-TECH HIV/AIDS Clinical Seminar Series 30 de Agosto de 2012 HPV em mulheres infectadas pelo HIV Goldman ARNP, MPH Objectivos 1. Discutir a epidemiologia do HPV entre mulheres infectadas pelo
NOVAS TECNOLOGIAS DE PREVENÇÃO CIRCUNCISÃO MÉDICA MASCULINA
 NOVAS TECNOLOGIAS DE PREVENÇÃO CIRCUNCISÃO MÉDICA MASCULINA Dr. Robinson Fernandes de Camargo Interlocução de DST/Aids da Coordenadoria Regional de Saúde - Sudeste CIRCUNCISÃO MÉDICA MASCULINA No início
NOVAS TECNOLOGIAS DE PREVENÇÃO CIRCUNCISÃO MÉDICA MASCULINA Dr. Robinson Fernandes de Camargo Interlocução de DST/Aids da Coordenadoria Regional de Saúde - Sudeste CIRCUNCISÃO MÉDICA MASCULINA No início
vacina hepatite B (recombinante)
 vacina hepatite B (recombinante) FORMA FARMACÊUTICA E APRESENTAÇÕES Suspensão injetável - Cartucho contendo 1 frasco-ampola com 1 dose de 0,5mL; - Cartucho contendo 20 frascos-ampola com 1 dose de 0,5mL;
vacina hepatite B (recombinante) FORMA FARMACÊUTICA E APRESENTAÇÕES Suspensão injetável - Cartucho contendo 1 frasco-ampola com 1 dose de 0,5mL; - Cartucho contendo 20 frascos-ampola com 1 dose de 0,5mL;
vacina febre amarela (atenuada)
 Modelo de Bula Página 1 de 6 vacina febre amarela (atenuada) FORMA FARMACÊUTICA E APRESENTAÇÕES Pó liofilizado para suspensão injetável + diluente para reconstituição. Cartucho contendo 1 frasco-ampola
Modelo de Bula Página 1 de 6 vacina febre amarela (atenuada) FORMA FARMACÊUTICA E APRESENTAÇÕES Pó liofilizado para suspensão injetável + diluente para reconstituição. Cartucho contendo 1 frasco-ampola
HPV: DIAGNÓSTICO E PREVENÇÃO
 HPV: DIAGNÓSTICO E PREVENÇÃO Bruna Rezende, Rassan Dyego Romão Silva e Antonio Jose Dias Martins Faculdade Alfredo Nasser Aparecida de Goiânia GO Brasil rassandyego@hotmail.com Orientadora: Daniella Cavalcante
HPV: DIAGNÓSTICO E PREVENÇÃO Bruna Rezende, Rassan Dyego Romão Silva e Antonio Jose Dias Martins Faculdade Alfredo Nasser Aparecida de Goiânia GO Brasil rassandyego@hotmail.com Orientadora: Daniella Cavalcante
PROJETO DE LEI No, DE 2009
 PROJETO DE LEI No, DE 2009 (DO SR. CAPITÃO ASSUMÇÃO) Dispõe sobre a imunização de mulheres com a vacina contra o papilomavírus humano (HPV), na rede pública do Sistema Único de Saúde de todos os estados
PROJETO DE LEI No, DE 2009 (DO SR. CAPITÃO ASSUMÇÃO) Dispõe sobre a imunização de mulheres com a vacina contra o papilomavírus humano (HPV), na rede pública do Sistema Único de Saúde de todos os estados
QUESTIONÁRIO DE FOLLOW-UP - HOMEM VIH NEGATIVO
 INSTRUÇÕES PARA A EQUIPA DO ESTUDO: Os participantes no estudo devem preencher o questionário de follow-up com intervalos regulares de -6 meses. Certifique-se de que é distribuído o questionário adequado.
INSTRUÇÕES PARA A EQUIPA DO ESTUDO: Os participantes no estudo devem preencher o questionário de follow-up com intervalos regulares de -6 meses. Certifique-se de que é distribuído o questionário adequado.
VaIN II II e III há indicação para tratamentos não- excisionais?
 Trocando Idéias XIV - 2009 VaIN II II e III há indicação para tratamentos não- excisionais? Walquíria Quida Salles Pereira Primo Doutorado e Mestrado UnB Professora da Pós-graduação UnB Unidade de Ginecologia
Trocando Idéias XIV - 2009 VaIN II II e III há indicação para tratamentos não- excisionais? Walquíria Quida Salles Pereira Primo Doutorado e Mestrado UnB Professora da Pós-graduação UnB Unidade de Ginecologia
QUESTIONÁRIO DE AVALIAÇÃO INICIAL - HOMEM VIH POSITIVO
 INSTRUÇÕES PARA A EQUIPA DO ESTUDO: Após inscrição no estudo, os participantes devem preencher este questionário de avaliação inicial. Certifique-se de que é distribuído o questionário adequado. Após o
INSTRUÇÕES PARA A EQUIPA DO ESTUDO: Após inscrição no estudo, os participantes devem preencher este questionário de avaliação inicial. Certifique-se de que é distribuído o questionário adequado. Após o
ANEXO CONDIÇÕES OU RESTRIÇÕES RESPEITANTES À UTILIZAÇÃO SEGURA E EFICAZ DO MEDICAMENTO A SEREM IMPLEMENTADAS PELOS ESTADOS-MEMBROS
 ANEXO CONDIÇÕES OU RESTRIÇÕES RESPEITANTES À UTILIZAÇÃO SEGURA E EFICAZ DO MEDICAMENTO A SEREM IMPLEMENTADAS PELOS ESTADOS-MEMBROS 1 Os Estados-Membros devem garantir que todas as condições ou restrições
ANEXO CONDIÇÕES OU RESTRIÇÕES RESPEITANTES À UTILIZAÇÃO SEGURA E EFICAZ DO MEDICAMENTO A SEREM IMPLEMENTADAS PELOS ESTADOS-MEMBROS 1 Os Estados-Membros devem garantir que todas as condições ou restrições
VACINA PENTAVALENTE CADERNO DO TREINANDO
 SUPERINTENDÊNCIA DE VIGILÂNCIA EM SAÚDE GERÊNCIA DE IMUNIZAÇÕES E REDE DE FRIO Av. Anhanguera, 5195 Setor Coimbra Goiânia GO Fone: (62) 3201-4547/4543 FAX: (62) 3201-4545 E-mail: pnigoias@gmail.com VACINA
SUPERINTENDÊNCIA DE VIGILÂNCIA EM SAÚDE GERÊNCIA DE IMUNIZAÇÕES E REDE DE FRIO Av. Anhanguera, 5195 Setor Coimbra Goiânia GO Fone: (62) 3201-4547/4543 FAX: (62) 3201-4545 E-mail: pnigoias@gmail.com VACINA
EFEITOS ADVERSOS A MEDICAMENTOS
 EFEITOS ADVERSOS A MEDICAMENTOS INTRODUÇÃO As informações contidas neste folheto têm a finalidade de orientar as pessoas que passaram ou que podem passar pela experiência não-desejada dos efeitos adversos
EFEITOS ADVERSOS A MEDICAMENTOS INTRODUÇÃO As informações contidas neste folheto têm a finalidade de orientar as pessoas que passaram ou que podem passar pela experiência não-desejada dos efeitos adversos
DIAGNÓSTICO MÉDICO DADOS EPIDEMIOLÓGICOS FATORES DE RISCO FATORES DE RISCO 01/05/2015
 01/05/2015 CÂNCER UTERINO É o câncer que se forma no colo do útero. Nessa parte, há células que podem CÂNCER CERVICAL se modificar produzindo um câncer. Em geral, é um câncer de crescimento lento, e pode
01/05/2015 CÂNCER UTERINO É o câncer que se forma no colo do útero. Nessa parte, há células que podem CÂNCER CERVICAL se modificar produzindo um câncer. Em geral, é um câncer de crescimento lento, e pode
Informe Técnico - SARAMPO nº2 /2010 Atualização da Situação Epidemiológica
 1 SECRETARIA DE ESTADO DA SAÚDE COORDENADORIA DE CONTROLE DE DOENÇAS CENTRO DE VIGILÂNCIA EPIDEMIOLÓGICA PROF. ALEXANDRE VRANJAC Av. Dr. Arnaldo, 351-6º andar SP/SP CEP: 01246-000 Fone: (11)3082-0957 Fax:
1 SECRETARIA DE ESTADO DA SAÚDE COORDENADORIA DE CONTROLE DE DOENÇAS CENTRO DE VIGILÂNCIA EPIDEMIOLÓGICA PROF. ALEXANDRE VRANJAC Av. Dr. Arnaldo, 351-6º andar SP/SP CEP: 01246-000 Fone: (11)3082-0957 Fax:
INFORME TÉCNICO DA VACINA PAPILOMAVÍRUS HUMANO 6, 11, 16 E 18 (RECOMBINANTE) 2015
 MINISTÉRIO DA SAÚDE SECRETARIA DE VIGILÂNCIA EM SAÚDE DEPARTAMENTO DE VIGILÂNCIA DE DOENÇAS TRANSMISSÍVEIS COORDENAÇÃO-GERAL DO PROGRAMA NACIONAL DE IMUNIZAÇÕES INFORME TÉCNICO DA VACINA PAPILOMAVÍRUS
MINISTÉRIO DA SAÚDE SECRETARIA DE VIGILÂNCIA EM SAÚDE DEPARTAMENTO DE VIGILÂNCIA DE DOENÇAS TRANSMISSÍVEIS COORDENAÇÃO-GERAL DO PROGRAMA NACIONAL DE IMUNIZAÇÕES INFORME TÉCNICO DA VACINA PAPILOMAVÍRUS
VAMOS FALAR SOBRE. AIDS + DSTs
 VAMOS FALAR SOBRE AIDS + DSTs AIDS A AIDS (Síndrome da Imunodeficiência Adquirida) atinge indiscriminadamente homens e mulheres e tem assumido proporções assustadoras desde a notificação dos primeiros
VAMOS FALAR SOBRE AIDS + DSTs AIDS A AIDS (Síndrome da Imunodeficiência Adquirida) atinge indiscriminadamente homens e mulheres e tem assumido proporções assustadoras desde a notificação dos primeiros
NEOPLASIA INTRAEPITELIAL VULVAR RIO DE JANEIRO 2013
 NEOPLASIA INTRAEPITELIAL VULVAR diagnóstico e conduta RIO DE JANEIRO 2013 A NIV aumentou em 4 vezes nos EUA entre 1973 e 2000 A regressão da NIV existe O câncer invasor está presente em 3% das mulheres
NEOPLASIA INTRAEPITELIAL VULVAR diagnóstico e conduta RIO DE JANEIRO 2013 A NIV aumentou em 4 vezes nos EUA entre 1973 e 2000 A regressão da NIV existe O câncer invasor está presente em 3% das mulheres
do Acidente Vascular Cerebral
 Tratamento Vacina Contra da Fase a Rubéola Aguda do Acidente Vascular Cerebral Academia Sociedade Brasileira de de Neurologia Pediatria Elaboração Final: 24 19 de Julho de 2001 2002 Autoria: Gagliardi
Tratamento Vacina Contra da Fase a Rubéola Aguda do Acidente Vascular Cerebral Academia Sociedade Brasileira de de Neurologia Pediatria Elaboração Final: 24 19 de Julho de 2001 2002 Autoria: Gagliardi
Desmistificando o HPV
 Desmistificando o HPV Como já havia lido que o tratamento está relacionado ao sistema imunológico, fui em busca de informações para aumentar a imunidade: alimentação, remédios caseiros e afins. Desde
Desmistificando o HPV Como já havia lido que o tratamento está relacionado ao sistema imunológico, fui em busca de informações para aumentar a imunidade: alimentação, remédios caseiros e afins. Desde
QUESTIONÁRIO DE FOLLOW-UP - HOMEM VIH POSITIVO
 INSTRUÇÕES PARA A EQUIPA DO ESTUDO: Os participantes no estudo devem preencher o questionário de follow-up com intervalos regulares de - meses. Certifique-se de que é distribuído o questionário adequado.
INSTRUÇÕES PARA A EQUIPA DO ESTUDO: Os participantes no estudo devem preencher o questionário de follow-up com intervalos regulares de - meses. Certifique-se de que é distribuído o questionário adequado.
APRESENTAÇÃO DA EFICÁCIA DA VACINA HPV DISTRIBUÍDA PELO SUS A PARTIR DE 2014 COM BASE NOS ESTUDOS FUTURE I, FUTURE II, E VILLA et al.
 APRESENTAÇÃO DA EFICÁCIA DA VACINA HPV DISTRIBUÍDA PELO SUS A PARTIR DE 2014 COM BASE NOS ESTUDOS FUTURE I, FUTURE II, E VILLA et al. Chaline Barbosa de Laia NUNES 1, Kimberly Marques ARRUDA 1 * & Théa
APRESENTAÇÃO DA EFICÁCIA DA VACINA HPV DISTRIBUÍDA PELO SUS A PARTIR DE 2014 COM BASE NOS ESTUDOS FUTURE I, FUTURE II, E VILLA et al. Chaline Barbosa de Laia NUNES 1, Kimberly Marques ARRUDA 1 * & Théa
Trocando Idéias XVII 29 de agosto de 2012
 Trocando Idéias XVII 29 de agosto de 2012 Infecção extragenital por HPV Câncer Oral Clique para editar o estilo do subtítulo mestre Flávia de Miranda Corrêa Divisão de Epidemiologia Coordenação Geral de
Trocando Idéias XVII 29 de agosto de 2012 Infecção extragenital por HPV Câncer Oral Clique para editar o estilo do subtítulo mestre Flávia de Miranda Corrêa Divisão de Epidemiologia Coordenação Geral de
ALERGIA A INSETOS PICADORES (CHOQUE ANAFILÁTICO)
 ALERGIA A INSETOS PICADORES (CHOQUE ANAFILÁTICO) As abelhas do gênero Apis (abelha-europa ou abelha-africana), as vespas (marimbondos) e as formigas lava-pés são insetos do gênero dos himenópteros que
ALERGIA A INSETOS PICADORES (CHOQUE ANAFILÁTICO) As abelhas do gênero Apis (abelha-europa ou abelha-africana), as vespas (marimbondos) e as formigas lava-pés são insetos do gênero dos himenópteros que
Perguntas e Respostas: Protocolo HVTN 910
 Perguntas e Respostas: Protocolo HVTN 910 Versão 1- Atualizado em 18/Nov/2011 1. O que é o Protocolo HVTN 910? O Protocolo HVTN 910 é um estudo clínico que avaliará por quanto tempo vacinas experimentais
Perguntas e Respostas: Protocolo HVTN 910 Versão 1- Atualizado em 18/Nov/2011 1. O que é o Protocolo HVTN 910? O Protocolo HVTN 910 é um estudo clínico que avaliará por quanto tempo vacinas experimentais
Abbott Laboratórios do Brasil Ltda Rua Michigan 735, Brooklin São Paulo - SP CEP: 04566-905
 MODELO DE BULA PARA O PACIENTE SYNAGIS palivizumabe I - IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Pó liófilo injetável de: - 100 mg em embalagem com 01 frasco-ampola para dose única contendo palivizumabe
MODELO DE BULA PARA O PACIENTE SYNAGIS palivizumabe I - IDENTIFICAÇÃO DO MEDICAMENTO APRESENTAÇÕES Pó liófilo injetável de: - 100 mg em embalagem com 01 frasco-ampola para dose única contendo palivizumabe
cartões de bolso serié 2 SEXO SEGURO
 cartões de bolso serié 2 SEXO SEGURO 1 O que quer dizer sexo seguro? Sexo seguro quer dizer, práticas sexuais responsáveis sem riscos de engravidar, ou de contrair uma infecção transmitida sexualmente,
cartões de bolso serié 2 SEXO SEGURO 1 O que quer dizer sexo seguro? Sexo seguro quer dizer, práticas sexuais responsáveis sem riscos de engravidar, ou de contrair uma infecção transmitida sexualmente,
vacina meningocócica AC
 vacina meningocócica AC Forma farmacêutica e apresentação Pó liofilizado injetável. - Cartucho contendo 1 frasco-ampola de uma dose e uma seringa com 0,5 ml de diluente. A vacina meningocócica AC deve
vacina meningocócica AC Forma farmacêutica e apresentação Pó liofilizado injetável. - Cartucho contendo 1 frasco-ampola de uma dose e uma seringa com 0,5 ml de diluente. A vacina meningocócica AC deve
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO
 ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Gardasil, suspensão injetável. Vacina contra o Papilomavírus Humano [Tipos 6, 11, 16, 18] (Recombinante, adsorvida). 2. COMPOSIÇÃO
ANEXO I RESUMO DAS CARACTERÍSTICAS DO MEDICAMENTO 1 1. NOME DO MEDICAMENTO Gardasil, suspensão injetável. Vacina contra o Papilomavírus Humano [Tipos 6, 11, 16, 18] (Recombinante, adsorvida). 2. COMPOSIÇÃO
do Acidente Vascular Cerebral
 Tratamento Vacina Contra da Fase - Rubéola Aguda do Acidente Vascular Cerebral Autoria: Academia Sociedade Brasileira de de Neurologia Pediatria Elaboração Final: 24 22 de Julho Maio de 2001 2008 Participantes:
Tratamento Vacina Contra da Fase - Rubéola Aguda do Acidente Vascular Cerebral Autoria: Academia Sociedade Brasileira de de Neurologia Pediatria Elaboração Final: 24 22 de Julho Maio de 2001 2008 Participantes:
