O uso crónico de anticonvulsivantes leva quase sempre à macrocitose (aumento do MCV), mesmo na ausência de anemia.
|
|
|
- Eduardo Garrau Martini
- 8 Há anos
- Visualizações:
Transcrição
1 Ácido Fólico O ácido fólico tem um papel importante na manutenção da hematopoiese, no processo de síntese do DNA e em diferentes processos metabólicos. É absorvido no intestino delgado e armazenado no fígado, mantendo uma reserva suficiente por um período de 3 a 5 meses. A deficiência está associada à escassez na dieta, a situações que levam ao aumento da ingestão (medicamento), a fármacos, a patologias que interferem no metabolismo e/ou na absorção e aos síndromes de má absorção. A sua avaliação é útil na investigação de anemias, no acompanhamento da terapia de reposição, na avaliação de alcoólicos crónicos, durante a gravidez, nos diferentes síndromes de má absorção e nos distúrbios de absorção pós-cirurgia para obesidade mórbida. A anemia megaloblástica é a principal manifestação clínica da deficiência de ácido fólico. Outras manifestações como doença depressiva, alterações neurológicas e psiquiátricas e fetos com defeitos do tubo neural estão associadas também à sua deficiência. Níveis séricos diminuídos são encontrados também na gravidez (33%), em anemias hemolíticas, em hepatopatias, em neoplasias, em pacientes hemodialisados, no alcoolismo crónico, em alterações intestinais que levam a má absorção e no uso de alguns medicamentos. As drogas podem interferir tanto na sua absorção como no seu metabolismo. O uso de anticonvulsivantes (fenitoína, fenobarbital e primidona), de contraceptivos orais e, mais raramente, o uso de antiácidos e antagonistas do receptor H2 alteram a absorção. O seu metabolismo pode ser alterado por uso de antimicrobianos que levam à diminuíção das bactérias intestinais importantes no processo de metabolização. Os quimioterápios, especialmente o metotrexate e o uso de álcool, também interferem no seu metabolismo. O álcool interfere tanto no metabolismo como na absorção. O uso crónico de anticonvulsivantes leva quase sempre à macrocitose (aumento do MCV), mesmo na ausência de anemia. Ácido Lático Em condições adequadas de oxigenação, a glicose é metabolizada por via aeróbica para a produção de energia. Os produtos de seu metabolismo são convertidos em piruvato, que por sua vez é metabolizado no ciclo de Krebs. Já em condições de hipóxia tecidual grave, o metabolismo aeróbico torna-se incapaz de funcionar e, assim, o piruvato é convertido em ácido láctico, utilizando o metabolismo anaeróbico. O ácido láctico é um ácido com ph 3,9, e, por isso, praticamente todo ele é encontrado na circulação sob a forma de L-lactato. É derivado principalmente do músculo-esquelético, cérebro, rins e eritrócitos. A sua concentração sanguínea depende da taxa de produção nos tecidos e das taxas de metabolização hepática e renal. Cerca de 65% do lactato produzido é usado pelo fígado, especialmente na gliconeogénese. A remoção extra-hepática do lactato ocorre por oxidação na musculatura esquelética e no córtex renal. Com a normalização dos níveis de oxigenação, o lactato acumulado nas células é novamente convertido em piruvato, retornando ao ciclo normal.
2 Os níveis séricos do ácido láctico estão relacionados com a disponibilidade de oxigénio. Na avaliação da oxigenação, a concentração de po 2 indica a captação alveolar pulmonar do O 2. A medida da saturação de O 2 determina o teor de oxigenação arterial, enquanto o lactato é uma medida sensível e confiável de hipóxia tecidual. Eleva-se precocemente antes que outras alterações clínicas ou gasométricas possam ser detectadas, é por isso considerado um marcador precoce de hipóxia tecidual. SECUNDÁRIA À HIPÓXIA TECIDUAL Choque, hipovolemia, insuficiência ventricular esquerda, infarte agudo do miocárdio, edema pulmonar, estados per e pós- operatórios, cirurgia cardíaca, circulação extracorpórea DISTÚRBIOS METABÓLICOS (PRODUÇÃO EXCESSIVA - DIIMINUIÇÃO DA REMOÇÃO HEPÁTICA) Diabetes mellitus, insuficiência hepática, neoplasias, linfomas, leucemias, intoxicações por drogas (acetaminofeno e salicilatos), etanol, metanol, erros inatos do metabolismo, exercício excessivo e hiperventilação. A acidose láctica pode ter origem na hipóxia tecidual ou pode ocorrer em consequência de outras patologias que levem a alterações metabólicas. Em geral, as etiologias desassociadas da hipóxia apresentam valores menos elevados. Em pacientes com acidose metabólica, uma diferença aniónica elevada sugere o diagnóstico de acidose láctica. É do que se deve suspeitar quando a soma dos aniões menos a soma dos catiões ultrapassa 18 meq/l. Isso, é claro, na ausência de outras causas que possam levar a uma diferença aniónica, como insuficiência renal, cetonémia importante e intoxicação por metanol. [(Na+ + K + ) - (Cl - +HCO3 - )] > 18 meq/l Os seus níveis podem estar alterados noutros líquidos orgánicos como líquor e líquidos pleural, ascítico e peritoneal, auxiliando no diagnóstico diferencial entre infecções bacterianas e virícas. Ácido Úrico O ácido úrico é o maior produto do catabolismo das purinas. É armazenado no organismo num pool de alto turnover, sendo oriundo do catabolismo das proteínas da dieta e de fontes endógenas, concentrando-se principalmente no fígado. Cerca de 60% desse é trocado diariamente por formação e excreção concomitantes. O ácido úrico é excretado principalmente por via renal. Apenas uma pequena parcela (1/3) é eliminada por via gastrointestinal. Não existe uma relação directa entre os valores séricos e os valores urinários. Os níveis séricos do ácido úrico são determinados pela relação entre a dieta, a produção endógena e os mecanismos de reabsorção e de excreção. Os mecanismos de reabsorção e de excreção renais são complexos, e podem ocorrer alterações na filtração glomerular, na reabsorção tubular proximal, na secreção tubular e na reabsorção após secreção.
3 Diversos factores como dieta, predisposição genética, sexo, idade, peso, medicamentos, uso de álcool e associação com outras patologias como diabetes mellitus e distúrbios lipídicos podem alterar os valores séricos e levar a um desequilíbrio entre a absorção e a excreção de ácido úrico. Os seus valores sofrem uma variação diurna, com valores mais elevados pela manhã e mais baixos à noite. A hiperuricémia é a forma comum de se definir o aumento da concentração sérica de ácido úrico que ultrapasse os valores de referência. Pode ocorrer por diferentes mecanismos, associados com aumento da produção ou diminuição da excreção renal. Ocorre nas dietas ricas em carnes, especialmente vísceras (fígado e rim), vegetais leguminosos e trigo. Também é encontrada nas dislipidémias, nas anemias hemolíticas, na anemia perniciosa e noutras situações em que há aumento do turnover de ácidos nucleicos (excesso de destruição celular), como ocorre nas neoplasias e no curso de quimioterapia e de radioterapia, especialmente no tratamento de linfomas e de leucemias. A policitemia, o mieloma múltiplo e o infarte agudo do miocárdio extenso podem também aumentar o metabolismo das nucleoproteínas. Alterações da função renal, hipertensão arterial, hipotireoidismo, hiperparatireoidismo, diabetes insipidus, diabetes mellitus, doença de Addison e uso de drogas como salicilatos e alguns diuréticos podem induzir à diminuição da velocidade de excreção de ácido úrico. Portanto, os níveis séricos do ácido úrico podem apresentar-se alterados numa gama de situações clínicas, incluindo a gota. A gota é responsável por apenas 10 a 15% das hiperuricemias. A maioria dos pacientes com gota sofre tanto de superprodução como de hipoexcreção. A gota caracteriza-se clinicamente por hiperuricémia, precipitação de urato monossódico em fluidos biológicos supersaturados e depósito de urato por todo o corpo, com excepção do sistema nervoso central, mas com maior predisposição para articulações, cartilagem periarticular, ossos, bursa e tecidos moles subcutâneos. São comuns ataques recorrentes de artrite, nefropatia e, frequentemente, nefrolitíase. Os depósitos de uratos são responsáveis pelos sinais e sintomas da artrite gotosa, pois levam a uma severa reacção inflamatória no local. Nos rins são descritos três tipos distintos de lesões: a nefropatia gotosa com depósito de uratos no parenquima, o depósito intratubular agudo de cristais de urato e a nefrolitíase. Os homens respondem por cerca de 90% dos casos de gota. Normalmente, ela é classificada como primária quando decorre de um erro metabólico, directamente ligado ao aumento da produção ou à diminuição da excreção, e como secundária quando decorre do aumento do ácido úrico em consequência de outras numerosas etiologias. AUMENTO DA FORMAÇÃO DIMINUIÇÃO DA SECREÇÃO Aumento da síntese de purinas Idiopática Desordens metabólicas hereditárias Insuficiência renal crónica Excesso de ingestão de purinas Aumento da reabsorção renal Aumento do turnover de ácidos nucléicos Drogas (diuréticos e salicitatos) Hipóxia tecidual Intoxicação por chumbo Hipertensão arterial Outras doenças endócrinas A hipouricémia é rara, podendo ser secundária a diferentes situações como uma doença hepatocelular grave, que leva à diminuição da síntese de purina, deficiência
4 da reabsorção tubular de ácido úrico congénita, como no síndrome de Fanconi, ou adquirida, por supertratamento com drogas uricosúricas, na secreção inadequada da hormona antidiurética, na doença de Wilson, na xantinúria, nas intoxicações por metais pesados e nas dietas pobres em purina. A quantidade de ácido úrico presente na urina varia de acordo com o ph: é tanto menor quanto maior for o ph. A excreção urinária de ácido úrico aumentada pode ocorrer isolada ou associada a outros distúrbios metabólicos (com aumento da produção endógena), pelo aumento da ingestão de purinas e pelo uso de drogas uricosúricas, principalmente na fase inicial do tratamento. A diminuição dos níveis urinários de ácido úrico pode estar associada a gota crónica e a uma dieta pobre em purinas. Como já citado, não existe correlação directa entre os níveis séricos e urinários do ácido úrico. A sua avaliação é útil na investigação das litíases renais. Os cristais de ácido úrico são achados frequentes em crianças em fase de crescimento acelerado e noutras situações de aumento do metabolismo de nucleoproteínas. Algumas drogas, como antiinflamatórios, aspirina, vitamina C, além dos diuréticos, podem alterar a sua excreção. Ácido Valpróico O ácido valpróico (valproato de sódio) é utilizado no tratamento das convulsões tónico-clónicas, mioclónicas e atónicas e das ausências. Embora o seu mecanismo de acção não seja totalmente conhecido, acredita-se que actue aumentando a atividade do sistema inibidor, mediado pelo ácido gama-aminobutírico (GABA). A absorção é rápida e completa, com picos séricos entre 1 a 4 horas após a administração oral. As concentrações séricas terapêuticas usuais são de 50 a 100 mg/ml. A sua acção inicia-se cerca de 4 horas após a administração oral, e o estado de equilíbrio normalmente é alcançado num período entre 1 a 4 dias. Cerca de 90% da droga é metabolizada no fígado, e uma grande percentagem (93%) está ligado a proteínas plasmáticas, principalmente à albumina. Por isso, em situações com diminuição proteica, cirrose, uremia e uso de drogas que competem com essa ligação, a taxa de ácido valpróico livre (fração biologicamente activa) pode aumentar. A semi-vida sérica no adulto é de 16 horas, podendo ser prolongada por uso de bebidas alcoólicsa e diminuída pela associação com fenitoína, fenobarbital, carbamazepina e primidona. Com o uso crónico, a semi-vida é reduzida para 12 horas. Em crianças, a semi-vida é de 12 horas. Em recém-nascidos e nas doenças hepáticas em que o metabolismo é reduzido, a semi-vida é prolongada. O ácido valpróico deve ser utilizado com cautela em gestantes, devido aos seus prováveis efeitos teratogénicos. Os efeitos colaterais incluem sedação, distúrbios gástricos, reacções hematológicas (a mais comum é a plaquetopenia), ataxia, ganho de peso, sonolência e coma. Foram descritos casos raros de hepatotoxicidade e pancreatite graves ou fatais. A sua dosagem é de grande utilidade para avaliar os níveis de adesão ao tratamento e detectar as concentrações em níveis tóxicos. Níveis baixos podem ser encontrados por falta de adesão à terapia.
5 Normalmente, a colleita deve ser realizada em pacientes que estejam medicados com o medicamento há pelo menos, 2 a 4 dias, e sempre antes da próxima dose. Entretanto, nos casos de suspeita de intoxicação, a colheita pode ser realizada a qualquer altura. Para facilitar a interpretação, é importante conhecer a hora em que a última dose foi ingerida. Agregação Plaquetária Entre as propriedades das plaquetas estão a manutenção da homeostasia, a adesão à superfície endotelial danificada, a agregação em resposta a uma variedade de estímulos e a secreção de factores de coagulação, vasoconstritores e factores de crescimento após a sua activação. O processo de formação do trombo plaquetário inicia-se com a lesão endotelial. Quando ocorre uma lesão vascular, a matriz colagénea e as proteínas subendoteliais ficam expostas. É nesse local que os receptores de membrana das plaquetas se ligam, resultando na adesão plaquetária, a primeira etapa do processo de formação do trombo plaquetário. Múltiplos agonistas são gerados neste momento. Eles induzem a activação plaquetária, ocasionando alterações nos receptores da glicoproteína (GP) IIb/IIIa e levando a um estado de receptividade à ligação do fibrinogénio. Nessa fase, as plaquetas encontram-se definitivamente activadas. Em seguida, inicia-se o processo de agregação plaquetária, com a ligação múltipla e cruzada do fibrinogénio aos receptores GP IIb/IIIa. As causas de diminuição da agregação plaquetária podem ser congénitas ou adquiridas. Entre as causas congénitas estão a doença de von Willebrand, a trombastenia de Glanzmann e o síndrome de Bernard-Soulier. Todas estas patologias estão relacionadas com defeitos na fase de adesão plaquetária. As plaquetas aderem a superfícies estranhas por meio da ligação das glicoproteínas da sua membrana, tendo como participante indispensável uma proteína plasmática, na verdade um componente do complexo molecular do fator VIII da coagulação chamado fator de von Willebrand. Esse mecanismo pode ser estudado em laboratórios pelo tempo de sangria, teste de adesividade plaquetária, teste de agregação plaquetária com ristocetina, dosagem do co-factor da ristocetina e dosagem do fator VIII. A doença de von Willebrand e a ausência congénita do factor de von Willebrand ou do co-factor da ristocetina fazem com que a agregação seja anormal com todos os estimulantes utilizados usualmente. Na doença de von Willebrand dos tipos IA e IIA, a agregação com a ristocetina é geralmente anormal, mas está aumentada no tipo IIB. A trombastenia de Glanzmann, embora rara, é a principal doença autossómica recessiva que afecta a interacção entre as plaquetas. Caracteriza-se por um prolongamento do tempo de sangria, episódios recorrentes de sangramentos mucocutâneos e ausência de resposta agregante aos estimulantes normais com resultado positivo à ristocetina. Na síndrome de Bernard-Soulier, ocorre ausência de resposta das plaquetas ao factor de von Willebrand; as plaquetas respondem normalmente aos estimulantes usuais, mas sem se agregarem em resposta à ristocetina. Entre as condições adquiridas que causam diminuição da agregação plaquetária, temos o uso de medicações inibidoras, doenças auto-imunes que produzem anticorpos contra as plaquetas, desordens mieloproliferativas, uremia por
6 insuficiência renal, desordens adquiridas do armazenamento de ADP e produtos de degradação da fibrina. Algumas condições podem produzir aumento da agregação plaquetária, como sejam, quadros de hipercoagulabilidade que indicam um risco de acidente vascular cerebral, trombose venosa profunda e outras condições associadas à formação de coágulo. Na avaliação de pacientes com desordens plaquetárias qualitativas, deve ser sempre considerado o estudo da agregação plaquetária, indicado também para os pacientes com sangramento mucocutâneo de natureza prolongada e contagem plaquetária normal. O teste de agregação pode ser utilizado na monitorização de pacientes tratados com antiagregantes plaquetários, como ácido acetilsalicílico e ficlodipina. O teste com ácido araquidónico em vigência do uso dessas drogas resulta na agregação diminuída ou ausente. O quadro a seguir actualiza os resultados da agregação plaquetária nas diversas patologias e com os diferentes agentes agregantes. ADP Ácido Adrenalina Ristocetina Colagénio Araquidónico PATOLOGIA 1º 2º Fase Fase Glanzmann A A A V A A Von Willebrand N N N V N N Bernard- Soulier N N V A N N Uso de AAs ou similares N A V N V A A=Anormal N=Normal V=Variáveis O exame é realizado a partir do plasma do paciente em num instrumento fotóptico denominado agregómetro. O plasma enriquecido em plaquetas é colocado em contato com agentes agregantes. Ocorre, então, a formação crescente de grandes agregados plaquetários, acompanhados de diminuição da turbidez da amostra. A mudança na densidade óptica é transmitida pelo instrumento, em percentagem de agregação. Os agentes agregantes normalmente utilizados no teste são ADP (adenosina difosfato), colagénio, adrenalina, ácido araquidónico e ristocetina. A informação clínica do paciente quanto ao uso de medicamentos de acção plaquetária é importante para se ter certeza de que o resultado observado, caso alterado, será devido a uma desordem qualitativa subjacente. A disfunção plaquetária poderá ser observada nalgumas condições clínicas, como insuficiência renal e desordens mieloproliferativas. Albumina De todas as proteínas séricas, a albumina é a que está presente em maior concentração, correspondendo a cerca de 60% do total de proteínas. É sintetizada exclusivamente pelo fígado, aparecendo primeiro no citoplasma dos hepatócitos como um precursor chamado pré-albumina. A sua semi-vida biológica é de cerca de 3 semanas. Tem um papel muito importante em diversas funções do organismo, como sejam a manutenção da pressão osmótica do plasma e o transporte de substâncias. Por isso, está relacionada fisiopatologicamente às alterações do equilíbrio hídrico e aos mecanismos de desentoxificação do organismo, já que tem a
7 capacidade de fixar substâncias, não só do tipo fisiológico, tais como bilirrubina, magnésio, cálcio e ácido úrico, como também diversos medicamentos, como penicilina e sulfa-penicilinas, entre outros. A hiperalbuminémia é rara e na maioria dos casos indica situações clínicas de desidratação ou hiperinfusão com albumina. Já a hipoalbuminémia é frequente, e pode apresentar-se em consequência de diferentes mecanismos, como diminuição da síntese por lesões hepáticas, má nutrição e síndromes de má absorção, aumento do catabolismo, como na fase de resposta aguda, perdas excessivas, como no síndrome nefrótico, outras lesões renais com perda protéica, disfunção da tiróide, úlcera péptica, alcoolismo crónico, gravidez, hemorragias, queimaduras, perdas intestinais e perdas para espaço interestecial, como ascites e outros derrames volumosos. Nos casos de doenças crónicas como tuberculose e neoplasias, a diminuição ocorre tanto por alteração da síntese como pelo aumento do catabolismo. A queda de albumina pode também estar relacionada a uma rápida hidratação, superhidratação, necrose grave difusa do fígado, hepatite crónica activa e neoplasias. Portanto, essa avaliação é clinicamente importante na verificação das condições nutricionais, no acompanhamento da síntese, do catabolismo e das perdas protéicas. Níveis séricos entre 2,0 e 2,5 g/dl correlacionam-se com a manifestação de edema. Consultar a electroforese das proteínas Aldolase É uma enzima presente em quase todos os tecidos. É composta pelas subunidades A, B e C, que formam quatro isoenzimas, sendo que a subunidade A responde pela maior parcela da aldolase sérica. AAAA predomina nos músculos esqueléticos BBBB predomina no fígado CCCC predomina no cérebro e noutros tecidos AAAC presente nos tecidos, porém em baixa concentração A determinação sérica da aldolase é de grande importância clínica na avaliação das doenças primárias da musculatura esquelética. As maiores elevações são encontradas na distrofia muscular progressiva de Duchenne. Níveis alterados também podem ser observados nas miosites e dermatomiosites. Os seus níveis correlacionam-se com a massa muscular. A perda muscular progressiva faz diminuir os valores por perda da capacidade de síntese; portanto, só se encontram valores alterados nas fases precoces das distrofias, quando a massa muscular se encontra relativamente preservada. Valores normais são encontrados nas patologias musculares de causa neurológica como esclerose múltipla, poliomielite e miastenia gravis. A sua elevação não é específica para doenças musculares. O aumento da aldolase pode ser encontrado no infarte do miocárdio (pico em 24 a 48 horas), hepatites virícas agudas, pancreatite hemorrágica, gangrena, tumores da próstata, neoplasias hepáticas primárias e secundárias, anemia megaloblástica, leucemia granulocítica e em pacientes medicados com fenotiazida.
8 Alfa-1-Antitripsina É uma das proteínas de fase aguda e, como tal, apresenta-se aumentada nas doenças inflamatórias agudas e crónicas, neoplasias, pós-traumas ou cirurgias e durante a gravidez ou terapia com estrogénio. Níveis diminuídos estão associados a deficiência congênita. Na deficiência homozigota, cerca de 10% das crianças desenvolvem hepatopatias importantes, inclusive hepatite neonatal e cirrose. Os adultos tendem a apresentar quadro de enfisema na terceira ou quarta década de vida e quadros de cirrose assintomática, hepatite crónica activa e carcinoma hepatocelular. A doença é sugerida pela ausência da banda alfa-1 na eletroforese (a alfa-1- antitripsina representa 90% dessa banda) e confirmada pela dosagem sérica da alfa-1-antitripsina. Nos homozigotos, os níveis séricos encontram-se acentuadamente diminuídos ou, mais raramente, ausentes. Nos heterozigotos, os níveis séricos apresentam-se diminuídos em níveis moderados. A alfa-1-antitripsina deve ser investigada em todos os lactentes com complicações hepáticas. Alfa-1-Glicoproteína Ácida Proteína também conhecida como orosomucóide, é sintetizada basicamente no fígado, podendo ser sintetizada, ainda, por leucócitos e por células tumorais. É filtrada em grande quantidade pelo glomérulo, o que acarreta uma semi-vida curta, de cerca de 5 dias. Como uma proteína de fase aguda, grandes concentrações séricas podem ser observadas em processos infecciosos e inflamatórios agudos, durante a gravidez, infarte agudo do miocárdio, mielomas, doença de Hodgkin, neoplasias, traumas, queimaduras e colagenoses. Níveis séricos diminuídos podem ser encontrados em estados de desnutrição, lesões hepáticas graves e patologias com grande perda protéica. Os níveis encontrados nos derrames cavitários podem ser de ajuda no diagnóstico diferencial entre transudados e exsudados. São encontrados níveis baixos nos transudados, elevados nos exsudados e extremamente elevados nos exsudados de origem neoplásica. A sua função biológica ainda não foi bem definida. No entanto, alguns trabalhos indicam uma participação importante no transporte de hormonas e drogas. É um dos melhores marcadores de actividade inflamatória, já que retorna a níveis normais em menos tempo do que as outras proteínas de fase aguda. Alfa-Fetoproteína A alfa-fetoproteína (AFP) é a principal glicoproteína plasmática precoce do feto humano. É sintetizada pelo fígado fetal, os seus níveis elevam-se durante a 14ª semana de gestação, atingindo os índices normais do adulto em 6 a 10 meses após o nascimento. Nos adultos, está presente em níveis baixos, em homens e em mulheres não-grávidas saudáveis.
9 Em pacientes com carcinomas hepatocelulares e tumores testiculares (nãoseminomas), encontram-se níveis elevados. Valores elevados também podem ser encontrados em cerca de 20% dos carcinomas gástricos e pancreáticos e numa pequena percentagem de carcinomas do pulmão e do cólon. Nem sempre as elevações de AFP estão associadas a malignidade. Os níveis podem estar elevados em doenças inflamatórias do fígado, como hepatite viríca, hepatite crónica e cirrose hepática. Níveis altos de AFP também podem estar presentes em doenças inflamatórias intestinais, como a doença de Crohn, e na colite ulcerosa, que também produzem elevações do antígeno carcinoembrionário (CEA). A maior indicação da determinação de AFP é a monitorização do tratamento de carcinomas hepatocelulares e de tumores testiculares (não-seminomas) e das suas recidivas. Após o tratamento, os valores retornam ao normal dentro de 4 a 6 semanas. O aumento após esse período ou a permanência de valores elevados indicam, respectivamente, recidiva e persistência da doença. Os níveis de AFP estão correlacionados ao tamanho do tumor. Nos tumores testiculares, é utilizada em associação com a beta-gonadotrofina coriónica (bhcg), sendo extremamente útil no diagnóstico diferencial. Os seminomas cursam com AFP negativa e bhcg elevada; nos não-seminomas, ambas se elevam. É inútil a sua utilização como rastreamento na população, por causa de significativas elevações em diferentes patologias, benignas e malignas. Consultar Gonadotrofina Coriônica. Alfa-Fetoproteína na Gravidez A alfa-fetoproteína (AFP) produzida pelo feto é transferida para o líquido amniótico por meio da urina fetal. Os níveis no soro fetal estão em concentrações aproximadamente 150 vezes mais baixas do que no líquido amniótico. A AFP também aparece no soro materno por transferência pela placenta ou por difusão através das membranas fetais. Picos acontecem em torno da 32a semana de gestação. Em contraste com os níveis típicos do segundo trimestre, de 10 a 12 mg/ml no líquido amniótico, os níveis no soro materno durante esse mesmo período são de apenas 30 a 35 ng/ml. No segundo trimestre, os níveis de AFP no soro materno aumentam cerca de 15% por semana, enquanto os níveis no líquido amniótico declinam aproximadamente 13% por semana. Em lesões fetais abertas, como espinha bífida e anencefalia, ocorre perda da AFP para o líquido amniótico, elevando os níveis de AFP. No soro materno, a AFP é um teste de triagem para defeitos congênitos fetais como os do tubo neural, espinha bífida, anencefalia e também para a síndrome de Down. A triagem adequada para essas alterações requer um protocolo integrado que envolve exames laboratoriais, ultra-sonografias, médicos obstetras e aconselhamento genético. Uma triagem falso-positiva pode ser provocada por subestimação da idade gestacional, gestação múltipla inesperada ou hemorragia de placenta. As duas razões anteriores podem ser excluídas por meio do exame de ultra-som e pela repetição da avaliação, 1 semana depois. Se tais condições não estiverem
10 presentes, um teste positivo alto indica risco, com probabilidade, aproximadamente, de 1 em 50 de uma anomalia fetal. A combinação da idade materna na data da coleta do sangue e os níveis de AFP irá predizer o fator de risco para a síndrome de Down. O HCG e o estriol são usados freqüentemente para um aumento adicional da precisão da avaliação de risco da síndrome de Down (teste triplo). Consultar Teste Triplo. Amilase As amilases são enzimas que catalisam a hidrólise da amilopectina, da amilose e do glicogênio. A amilase presente no sangue e na urina de indivíduos normais é de origem pancreática (predominantemente forma P) e das glândulas salivares (forma S). A avaliação dos níveis séricos da amilase tem grande utilidade clínica no diagnóstico das doenças do pâncreas e na investigação da função pancreática. Na pancreatite aguda, os níveis de amilase podem alcançar valores de quatro a seis vezes o limite superior de referência, elevando-se em 2 a 12 horas e retornando a níveis normais em 3 a 4 dias. A magnitude da elevação da amilase não se correlaciona com a gravidade da lesão pancreática. Cerca de 20% dos casos de pancreatite aguda podem cursar com valores normais de amilase. Por isso, a dosagem concomitante dos níveis de lipase é importante, permitindo o diagnóstico desses casos. Nos casos que evoluem com formação de pseudocistos, os níveis de amilase continuam elevados por mais tempo. Os abcessos pancreáticos também podem aumentar os níveis séricos da amilase. As pancreatites crónicas cursam com níveis normais ou pouco elevados de amilase. O carcinoma pancreático cursa com níveis normais; a elevação aparece em menos de 5% dos pacientes. Na maior parte dos casos, os níveis de amilase só se elevam quando o tumor provoca a obstrução do ducto pancreático principal. As causas não-pancreáticas de aumento da amilase incluem lesões inflamatórias das glândulas salivares, como parotidite, apendicite aguda, gravidez tubárica rota, úlcera péptica perfurada, trauma pancreático, obstrução intestinal, aneurisma dissecante da aorta, pós-operatório de cirurgias toráxicas e abdominais, queimaduras, doenças do trato biliar, traumas e uso de um grande número de drogas como morfina e derivados. A amilase pode estar elevada também em neoplasias como as pulmonares e as ováricas, e estudos apontam que a elevação se dá à custa da amilase do tipo S. Os níveis urinários de amilase permanecem alterados por períodos mais longos que os séricos. Nos casos de complicação com pseudocisto de pâncreas, a amilase urinária pode permanecer elevada por semanas após os níveis séricos terem retornado ao normal. Nos indivíduos com função renal normal, a proporção entre a clearance de amilase e a creatinina é constante, com valores de referência usuais de 2 a 5%. Na pancreatite, a clearance da amilase está aumentado, e, portanto, a proporção entre a clearance de amilase/creatinina está elevada. Valores acima de 8% são comuns na pancreatite aguda. Valores elevados podem ser encontrados também em queimados, na insuficiência renal e no mieloma múltiplo. Na macroamilasemia, a amilase encontra-se ligada a uma imunoglobulina, e o complexo formado é muito grande para ser filtrado pelos glomérulos, o que leva a uma hiperamilasemia aparente que não indica doença; os valores séricos são muito
11 altos, e os valores urinários, normais. Nesses casos, utilizam-se os resultados da relação entre a clearance de amilase/creatinina para se fazer o diagnóstico diferencial. Isso porque, na macroamilasemia, a relação é muito baixa, ao contrário da relação encontrada na pancreatite aguda. ANCA Os anticorpos anticitoplasma de neutrófilos (ANCA) são auto-anticorpos contra uma serina protease, a proteinase 3. Os ANCA estão associados primariamente à granulomatose de Wegener. São muitas vezes os únicos anticorpos presentes nessa patologia. São encontrados também em quadros de vasculite, poliartrite nodosa microangiopática, poliangeíte microscópica, glomerulonefrite necrotizante microscópica e síndrome de Churg-Strauss. Também podem estar presentes em diversas patologias gastrointestinais e reumáticas, ou após o uso de certas drogas. Quando esses anticorpos são incubados com neutrófilos normais fixados em etanol, podem ser observados dois padrões de imunofluorescência: o citoplasmático (c- ANCA) e o perinuclear (p-anca). O padrão c-anca é encontrado em cerca de 85% dos casos de granulomatose de Wegener, e os seus títulos correlacionam-se com a atividade da doença. Em pacientes com vasculite, esses anticorpos são geralmente dirigidos contra a mieloperoxidase, o que leva à visualização do padrão perinuclear (p-anca). Esse padrão também pode ser observado na poliartrite nodosa microangiopática, na poliangeíte microscópica, na glomerulonefrite necrotizante microscópica e na síndrome de Churg-Strauss. O padrão p-anca deve ser distinguido dos anticorpos antinucleares (ANA). A sua presença pode ser encontrada em doenças intestinais e na artrite reumatóide. Técnicas de imunoblotting ou de ELISA são melhores do que a imunofluorescência por apresentarem maior precisão e por permitirem a identificação dos antígenos alvos associados a esses anticorpos. Enzima Conversora da Angiotensina (ECA) A enzima conversora da angiotensina (ECA) actua na conversão de angiotensina I em angiotensina II, representando um papel importante na homeostase da pressão arterial. É produzida principalmente no pulmão. Embora, a sua medida tenha pouca utilidade no diagnóstico e tratamento da hipertensão arterial, entre as alterações genéticas consideradas como possíveis etiologias das doenças cardiovasculares, a que tem despertado maior atenção é o polimorfismo genético do gene que codifica a ECA. Num grande número de indivíduos, observaram-se diferenças marcantes nos níveis plasmáticos da ECA. Essa variabilidade é efeito de um polimorfismo genético no gene codificante para a enzima. A análise dos níveis de ECA no plasma circulante demonstrou uma associação directa entre os genótipos relativos ao polimorfismo e os níveis da proteína. Dessa forma, indivíduos que apresentam o genótipo DD possuem aproximadamente o dobro da concentração de ECA circulante, em relação a aqueles com genótipo II, enquanto o genótipo DI apresenta níveis intermediários de ECA. O polimorfismo D/I encontra-se correlacionado com 47% da variação total
12 do nível de ECA circulante no plasma. Estudos realizados demonstraram que o genótipo DD está associado à alta incidência de EAM, consistindo num factor de risco independente, aumentando em 2,7 vezes o risco relativo de desenvolver tal patologia. O efeito deletério do genótipo DD pode resultar de uma super expressão da ECA, levando a um aumento local de angiotensina II em regiões vasculares como a circulação coronária, podendo ser considerado como um novo e potente factor de risco para o EAM. A utilização mais frequente do doseamento dos níveis de ECA é no diagnóstico e acompanhamento da evolução da sarcoidose. Os seus níveis, encontram-se elevados em 40-85% dos pacientes adultos com sarcoidose activa e diminuem em resposta à terapia com corticosteróides. Na sarcoidose pulmonar pode estar aumentada no soro e no lavado bronco-alveolar. Não é um marcador específico de sarcoidose, visto que concentrações elevadas podem também ser encontradas noutras patologias pulmonares como enfisema, asma, carcinoma de pequenas células, carcinoma de células escamosas, tuberculose, silicose, abestose e pneumonias. Está elevada, porém, em menor frequência, noutras doenças granulomatosas como a lepra e a tuberculose e noutras patologias como esclerose múltipla, doença de Addison, hepatopatias, hipertiroidismo, doença de Gaucher e ocasionalmente em linfomas não-hodgkin e no linfoma de Lennert. Níveis séricos diminuídos podem ser encontrados no hipotiroidismo, anorexia nervosa, doença hepática crónica e em diferentes patologias malignas. A determinação da ECA no LCR (líquido cefalo raquidiano) tem particular interesse no diagnóstico da neurosarcoidoise que ocorre em 5% dos pacientes com sarcoidose. Entretanto, a sua utilização é controversa, visto que, níveis elevados podem também ser encontrados na esclerose múltipla, neuro-sífilis e em encefalites virícas. Anticardiolipina A cardiolipina é um fosfolipído aniónico. A maioria dos anticorpos anticardiolipina (ACA) reage cruzadamente com outros fosfolipídos. Devido a esta característica e pela sua maior facilidade de detecção, são utilizados na investigação da presença de anticorpos antifosfolipídos. Assim como os anticorpos anticardiolipina, os anticoagulantes lúpicos (ACL) são também anticorpos antifosfolipídos. Interferem nos procedimentos de screening de coagulação, sendo uma causa comum de prolongamento do aptt (tempo de tromboplastina parcial ativado). Existem algumas características clínicas comuns aos pacientes com a síndrome de antifosfolipídio (AFL): trombose venosa, trombose arterial, abortos recorrentes e trombocitopenia. Esses anticorpos são hoje reconhecidos como uma das causas mais importantes de hipercoagulabilidade e trombose. Aproximadamente 50% dos pacientes apresentam síndrome AFL primária, isto é, não-associada a doenças sistémicas, enquanto os restantes apresentam a forma secundária.
13 A trombose é a apresentação mais comum da síndrome de AFL, e o local da trombose (arterial ou venosa) pode definir síndromes com diferentes características clínicas e laboratoriais: anticardiolipina (AFL-ACA) - positivo e anticoagulante lúpico (AFL-ACL) - positivo. A prevalência, a etiologia e a conduta desses síndromes, relacionadas porém distintas, são diferentes. A apresentação AFL-ACA é mais comum do que a AFL- ACL. A relação de prevalência é de 5 para 1. Ambas estão associadas a tromboses, abortos e trombocitopenia. A AFL-ACA está associada a trombose arterial e venosa, inclusive com quadros de trombose venosa profunda e embolia pulmonar, doenças coronárias e cerebrovasculares prematuras. Em contrapartida, o síndrome AFL-ACL é associado mais frequentemente a trombose venosa, que envolve os quadros de trombose venosa periférica, mesentérica, renal, hepática, sistema porta e veia cava. A trombose arterial raramente acontece na síndrome AFL-ACL. A atividade dos ACA em níveis elevados, na presença de ACL, é um fator de risco importante para trombose arterial. Os abortos normalmente acontecem no terceiro trimestre da gravidez e são associados a trombose da placenta. Embora as mulheres com abortos espontâneos periódicos no primeiro trimestre possam ter AFL, outras causas de perda fetal no primeiro trimestre são mais comuns. A contagem de plaquetas pode ser normal ou ligeiramente baixa. Aproximadamente 30% dos pacientes têm contagem de plaquetas abaixo de /mL durante o curso da doença. Paradoxalmente, esses pacientes ainda apresentam risco para trombose. O tratamento é iniciado quando a contagem de plaquetas se encontra abaixo de /mL (especialmente quando abaixo de /mL), por causa do risco aumentado de hemorragia. Os anticorpos anticardiolipina são medidos por testes imunoenzimáticos. A utilização combinada da pesquisa desses anticorpos com o anticoagulante lúpico (ACL) melhora a sensibilidade para a descoberta de anticorpos antifosfolipído. Aproximadamente 60% dos pacientes são positivos tanto para ACL quanto para ACA, e 40% são positivos somente para ACA ou ACL. Podem ser encontrados associados a doenças como lúpus eritematoso sistémico (LES), outras doenças do tecido conjuntivo, infecção pelo HIV e por outros microrganismos, neoplasias e um quadro induzido por drogas. São encontrados numa pequena parcela da população saudável. No LES, a presença do anticorpo anticoagulante lúpico ocorre em cerca de 70% dos casos. Na pesquisa de sífilis, pode levar a uma reação de VDRL falsamente positiva. O diagnóstico de síndrome antifosfolipídico exige a constatação da presença de uma das características clínicas citadas e um teste positivo. Os testes podem ser o do anticoagulante lúpico, os de anticorpos anticardiolipina ou ambos. Consultar Anticoagulante Lúpico. Anticorpos Anti-célula Parietal A pesquisa de anticorpos anti-célula parietal é importante para auxiliar o diagnóstico diferencial da anemia perniciosa e da atrofia gástrica. Anticorpos anti-
14 célula parietal são encontrados em cerca de 90% dos pacientes com anemia perniciosa e em 60% dos casos de atrofia gástrica. A sua presença não se correlaciona com a má absorção de vitamina B12, mas sim com o nível de destruição das células parietais. Não são anticorpos específicos, sendo encontrados em 20 a 30% dos pacientes com doenças auto-imunes e em 16% de pacientes assintomáticos com mais de 60 anos. Podem estar presentes em pacientes com úlcera ou carcinoma gástrico. É possível ocorrer reactividade cruzada entre os anticorpos anti-célula parietal e antitiroideus em pacientes que apresentem concomitância das patologias (tiroidite e anemia perniciosa). Nalguns casos, pode ocorrer um decréscimo nos níveis de anticorpos, decorrente, provavelmente, da diminuição do número de células parietais. Anticorpos anti-célula parietal (ACP) são encontrados em aproximadamente 5% da população saudável. Alguns estudos referem uma alta frequência (90-100%) de ACP na anemia perniciosa. A relação de ACP com as gastrites tipo A (caracterizadas por atrofia da mucosa do fundo gástrico, acloridria, tendência a evoluir para anemia perniciosa e associação com doença endócrina auto-imune) é bem conhecida. O papel patológico dos ACP na anemia perniciosa ainda é obscuro. Nas doenças hepáticas auto-imunes, são encontrados ACP em 100% dos pacientes com cirrose biliar primária, em 75% das hepatites auto-imunes e em 29% dos pacientes com doença hepática crónica. Anticorpos Anticoagulante Lúpico Os anticorpos anticoagulantes lúpicos (ACL) são imunoglobulinas da classe IgG ou IgM. Assim como os anticorpos anticardiolipina (ACA), os anticoagulantes lúpicos fazem parte da família dos antifosfolipídos e interferem nos procedimentos de screening de coagulação que dependem da presença de fosfolipídios. Constituem uma causa comum do prolongamento do tempo de tromboplastina parcial ativado (APTT). Os ACL são espécie-específicos e são neutralizados pela adição de fosfolipídos (plasma rico em plaquetas). São anticorpos muito heterogéneos no que diz respeito às suas características imunológicas e à variação de complexos fosfolipídicos e protéicos que actuam como seu alvo antigénico. Dados recentes sugerem que outras proteínas, como a proteína C, a proteína S e a trombomodulina, são também alvos para ACL. Apesar da sua actividade anticoagulante in vitro, na prática os anticoagulantes lúpicos estão relacionados com manifestações tromboembólicas recorrentes arteriais (menos frequentemente) e venosas, abortos repetidos, e, em certos casos, são encontrados em pacientes hígidos, assim como em diferentes situações clínicas, como doenças auto-imunes, neoplasias, quadros infecciosos virais, bacterianos e parasitários, distúrbios neurológicos e uso de alguns medicamentos. A detecção laboratorial de ACL não deve ser baseada num único teste. Deve-se realizar uma combinação de testes de screening com ensaios para excluir deficiências de factor de coagulação ou a presença de um inibidor de factor, os quais podem dar origem a resultados falso-positivos para ACL. Ou seja, a detecção deve ser realizada em etapas: screening para identificação da alteração; exclusão
15 de déficit de factor, confirmando assim a presença de um inibidor e a caracterização do tipo de inibidor. É importante também a interferência da heparina e dos anticoagulantes orais nos resultados, determinando, portanto, que o teste seja realizado apenas após 2 semanas da suspensão dos anticoagulantes orais e 48 horas após a última dose de heparina. Na avaliação do síndrome antifosfolipídico, alguns dados indicam que os ensaios de ACL predizem com mais segurança trombose, perda fetal recorrente e trombocitopenia do que os ensaios para ACA. Entretanto, aproximadamente 60% dos pacientes são positivos tanto para ACL quanto para ACA, enquanto os 40% restantes são positivos apenas para ACA ou para ACL. Consultar Anticardiolipina. Anticorpos Anti-GAD Os anticorpos antidescarboxilase do ácido glutâmico (anti-gad), anti-insulina (anti- IN) e anti-ilhota (anti-il) são evidências auto-imunes que predizem o aparecimento de diabetes mellitus insulino-dependente (DMID). Esses anticorpos estão presentes na maioria dos pacientes recentemente diagnosticados como portadores de DMID e em 80% daqueles que irão progredir para esse quadro. Diferenças marcantes são encontradas de acordo com o sexo do indivíduo. Nas mulheres portadoras de DMID, independentemente da idade, o teste apresenta-se positivo em mais de 80%, enquanto nos meninos menores de 10 anos essa taxa diminui para cerca de 50%, atingindo os valores da população diabética feminina nos homens adultos. Resumidamente, a diabetes mellitus permanece sendo diagnosticado através de critérios clínicos e da determinação sérica de glicose. Os marcadores imunológicos ainda não têm um papel diagnóstico definido. O valor preditivo positivo de um teste isoladamente é baixo na população em geral, mas a combinação de vários marcadores aumenta esse valor, alcançando níveis entre 50 e 60% nalguns estudos. Anticorpos Anti-ilhotas Pancreáticas Anticorpos anti-ilhota (anti-il), anticorpos anti-insulina (anti-in) e anticorpos antidescarboxilase do ácido glutâmico (anti-gad) são evidências auto-imunes que predizem o aparecimento de diabetes mellitus insulino-dependente (DMID). Anticorpos anti-ilhotas demonstram uma reação imunológica contra as células productoras de insulina. Esse teste tem sido utilizado para se prever o aparecimento de diabetes mellitus insulino-dependente (DMID). Chegou-se a essas conclusões após estudarem três grupos distintos de indivíduos: pacientes com DM auto-imune, os seus parentes de primeiro grau e indivíduos normais. Entre 80 a 85% dos pacientes com DMID e 3 a 4% dos parentes de primeiro grau de pacientes portadores de DMID apresentam anticorpos anti-ilhotas, mesmo antes de se mostrarem com aumento da glicemia.
16 A especificidade desse teste para DMID encontra-se entre 96 e 99%. Um resultado positivo em indivíduos normais pode representar um aumento transitório inespecífico ou uma progressão para DMID. Como principal indicação clínica, temos o parentesco em primeiro grau com indivíduos portadores de DMID, para que se possa ter um marcador preditivo do aparecimento da doença. O método usual para se detectar anti-ilhotas é a imunofluorescência indireta. A classe de anticorpos IgG antigliadina (AGA IgG) foi o primeiro marcador sorológico para essa doença. É mais sensível que a classe IgA (AGA IgA), embora seja menos específica. Apesar de o AGA IgA ser mais específico para a DC, 2% dos pacientes com essa patologia têm deficiência selectiva dessa classe de anticorpos. Resultados positivos de AGA IgG e IgA têm sensibilidade de 96% a 100% e especificidade de 96% a 97%. Esses anticorpos também são utilizados na monitorização do tratamento da DC e tendem a diminuir ou a desaparecer com uma dieta livre de glúten. Anticorpos Antiinsulina Os anticorpos anti-insulina (anti-in), anti-ilhota (anti-il) e os anticorpos antidescarboxilase do ácido glutâmico (anti-gad) são evidências auto-imunes que predizem o aparecimento de diabetes mellitus insulino-dependente (DMID). Os anticorpos anti-insulina estão presentes em 50% dos pacientes com DMID no momento do diagnóstico, antes do início da insulinoterapia. A sensibilidade do teste é de 50 a 70%, e ele é mais vezes positivo em crianças e adultos jovens. O doseamento de insulina em presença desses anticorpos é prejudicado, tornandose impreciso para o acompanhamento clínico. Anticorpos Antinucleares Os anticorpos antinucleares (ANA) são encontrados frequentemente numa variedade de doenças reumáticas auto-imunes. São úteis na investigação dessas doenças, auxiliando no diagnóstico de patologias como lúpus eritematoso sistémico (LES), esclerose sistémica progressiva (ESP), doença mista do tecido conjuntivo (DMTC), síndrome de Sjögren (SS), poliomiosite e dermatomiosite. Os ANA podem estar presentes numa pequena percentagem da população aparentemente sã; esta frequência é maior nas mulheres e aumenta com a idade. Segundo a literatura, a positividade entre 20 a 60 anos varia entre percentagens mais altas (13,3%) para títulos baixos e mais baixas (3,3%) para títulos mais elevados. A pesquisa dos anticorpos antinucleares pode ser realizada por diferentes técnicas; a imunofluorescência indireta é a mais utilizada, devido à sua maior sensibilidade, reprodutibilidade e facilidade de execução. A sensibilidade aumenta significativamente quando se utiliza como substrato láminas com células Hep 2 (células de carcinoma de laringe humana), por causa da maior expressão de antígenios na superfície dessas células comparados aos expressos nas células de fígado ou de rins de camundongos, que se utilizavam anteriormente. Em geral, é possível detectar melhor a presença de ANA por associação de três anti-soros isotipos específicos (anti-igg, anti-iga e anti-igm). A pesquisa realizada por essa
17 técnica serve de triagem inicial para a presença de ANA. É normalmente denominada pesquisa de factor antinuclear (FAN) ou ANA (antinuclear antibody). A realização de outras metodologias, tais como as imunoenzimáticas, permite uma avaliação isolada dos diferentes auto-anticorpos, sugeridos pelos padrões de fluorescência encontrados no FAN. A identificação desses ANA permite um diagnóstico mais preciso, e eles podem ser utilizados, em muitos casos, como marcador para uma das diferentes doenças reumáticas auto-imunes. Muitas dessas patologias apresentam um perfil distinto de auto-anticorpos que auxilia o diagnóstico. Fator Antinuclear - FAN Nas pesquisas realizadas por imunofluorescência indirecta, os resultados são expressos em títulos, segundo as diluições empregues. É possível trabalhar utilizando-se como limite títulos de 1/40, que permitem maior sensibilidade, ou de 1/80, que permitem maior especificidade, ou seja, um menor número de falsopositivos. Na prática clínica, são considerados significativos títulos superiores a 1/160. Os resultados com títulos positivos são acompanhados pela descrição do padrão de fluorescência encontrado, que serve como orientação da presença de um antígeno específico e, em alguns casos, como padrão diagnóstico. Em determinadas situações, em especial no LES em actividade, pode ocorrer a observação de mais de um padrão de fluorescência. PADRÕES DE PATOLOGIA ANTÍGENOS FLUORECÊNCIA RELACIONADAS PERIFÉRICO DNA de dupla hélice ou de hélice LES única, histona e RNA HOMOGÊNIO DNA de dupla hélice ou de hélice LES, AR, lúpus induzido por única, histona e RNA drogas PERIFÉRICO/ DNA de dupla hélice ou de hélice LES HOMOGÊNEO única, histona e RNA PONTILHADO GROSSO SM, RNP LES, DMTC PONTILHADO FINO NUCLEAR SS-A (RO) SS-B (La) SS, LES NUCLEOLAR Proteínas Nucleolares ESP CENTROMÉRICO Proteínas de centrómeros Síndrome de CREST O padrão pontilhado, pode também ser referido como padrão salpicado. Outros padrões de fluorescência podem ser encontrados em menor frequência. O pontilhado citoplasmático grosso ou reticular, associado à presença de anticorpos antimitocôndrias em pacientes com cirrose biliar primária; o citoplasmático homogêneo, relacionado a proteínas ribossômicas em pacientes com LES; e o padrão pontilhado fino citoplasmático, que pode estar associado à presença de anticorpos anti-jo-1, anti-pcna e proteínas da membrana celular, em pacientes com LES, outras patologias do tecido conjuntivo e hepatopatias auto-imunes.
18 Anticorpos Anti-DNA Nativo ou de Dupla Hélice A pesquisa desse anticorpo, realizada por imunofluorescência indirecta, utilizando como substrato a Crithidia luciliae, apresenta boa sensibilidade e alta especificidade. A técnica imunoenzimática, apesar de mais sensível, é menos específica, levando a riscos de resultados falso-positivos (identificação de DNA de hélice única). A sua presença é considerada um marcador para o diagnóstico de lúpus eritematoso sistémico, sendo detectado em 50 a 70% dos casos em actividade. Ao contrário de outros auto-anticorpos, os seus títulos apresentam relação directa com a actividade da doença, sendo extremamente úteis para o acompanhamento da terapia e da reactivação da doença. Quanto maior o título, maior a actividade da doença. Nalguns casos (cerca de 30%), apesar de as evidências clínicas e laboratoriais indicarem lúpus eritematoso sistémico, o anticorpo anti-dna nativo pode não ser detectado. Acredita-se que, nesses casos, os auto-anticorpos estejam sob a forma de imunocomplexos. Anti-ENA - Auto-anticorpos contra Antígenos Extraídos do Núcleo AUTO-ANTICORPOS CONTRA ANTÍGENOS EXTRAÍDOS DO NÚCLEO SM LES RNP DMTC, LES, ESP, AR e Polimiosite SS-A (Ro) SS, LES, lúpus neonatal e forma cutânea subaguda SS-B (La) SS, LES, lúpus neonatal e forma cutânea subaguda Scl 70 ESP Jo -1 Polimiosite e dermatomiosite O padrão pontilhado, pode também ser referido como padrão salpicado. Outros padrões de fluorescência podem ser encontrados em menor frequência. O pontilhado citoplasmático grosso ou reticular, associado à presença de anticorpos antimitocôndrias em pacientes com cirrose biliar primária; o citoplasmático homogêneo, relacionado a proteínas ribossómicas em pacientes com LES; e o padrão pontilhado fino citoplasmático, que pode estar associado à presença de anticorpos anti-jo-1, anti-pcna e proteínas da membrana celular, em pacientes com LES, outras patologias do tecido conjuntivo e hepatopatias auto-imunes. Sm Os auto-anticorpos anti-sm ("Smith") são dirigidos contra ribonucleoproteínas de baixo peso molecular. Estão presentes em 20 a 30% de pacientes de LES, geralmente acompanhados de positividade para outros anticorpos, entre eles o anti-rnp. Em contraste com os auto-anticorpos anti-dna de dupla hélice, que tendem a apresentar níveis flutuantes em paralelo à actividade da doença, os autoanticorpos anti-sm não variam muito com o passar do tempo. A sua presença correlaciona-se com o padrão pontilhado grosso na pesquisa de ANA por imunofluorescência indirecta. Podem ser encontrados também, embora mais raramente, noutras doenças do tecido conjuntivo, como a DMTC. É considerado um marcador diagnóstico do LES. A sua positividade noutras patologias que não as do tecido conjuntivo tem sido
19 descrita nalguns estudos que relatam a sua presença em gamapatias monoclonais e uveítes. RNP Os auto-anticorpos anti-rnp são encontrados em altos títulos na doença mista do tecido conjuntivo (DMTC). São úteis como marcadores para a DMTC, já que são detectados em altos títulos em 90% dos pacientes com essa patologia. Podem apresentar-se positivos também, porém com menos frequência, no LES, ESP, SS, artrite reumatóide e polimiosite. Nos pacientes com LES, os auto-anticorpos anti-rnp apresentam-se positivos em cerca de 26 a 40% dos casos, geralmente com outros anticorpos antinucleares também positivos. A sua presença no LES é considerada indício de bom prognóstico, pois indica menor probabilidade de lesão renal. SS-A/Ro - SS-B/La São anticorpos relacionados com uma classe de partículas de ribonucleoproteínas que são compostas por pequenos ácidos ribonucleicos. A detecção de auto-anticorpos SS-A/Ro é possível em aproximadamente 60 a 70% dos pacientes com síndrome de Sjögren, e com menor freqüência, na artrite reumatóide, nas vasculites associadas ao síndrome de Sjögren, noutras doenças do colágeno e em cerca de 5% da população hígida. Estão presentes em 40 a 50% de LES, em quase 100% dos casos de mães com filhos com lúpus neonatal e também nos casos da forma cutânea subaguda do lúpus. A presença de anti-ss-b/la dá-se em 40 a 50% dos casos de síndrome de Sjögren e em 6 a 15% dos casos de LES. No lúpus neonatal, quase sempre são detectados auto-anticorpos SS-A/Ro na mãe. Cerca de 2% de crianças nascidas de mães com auto-anticorpos SS-A/Ro apresentam a patologia. Na maioria das patologias em que se encontram presentes, os anticorpos anti- SSA/Ro são identificados com maior freqüência do que os anti-ssb/la. No síndrome de Sjögren, em cerca de 50% dos casos os auto-anticorpos SS-A/Ro estão acompanhados da presença de anti-ss-b/la. Scl 70 Na literatura actual, os anticorpos anti-scl 70 são identificados como antitopoisomerase I. Estão presentes em 64 a 75% de pacientes com ESP, mas só são vistos, raramente, na síndrome de CREST (calcinoses, dismotilidade esofagiana, fenómeno de Raynaud, esclerodactilia, telangicectasia), em poucos casos de fenómeno de Raynaud primário (10%), na síndrome de Sjögren (5%) e em cerca de 1% dos casos de DMTC e LES. É considerado marcador diagnóstico da ESP. A presença desses anticorpos aumenta em cerca de 17 vezes o risco de desenvolvimento de fibrose pulmonar em pacientes com quadro de esclerodermia. Esse risco implica a necessidade de monitorização mais frequente da função pulmonar. A positividade dos anticorpos anti-scl-70 não tem valor preditivo para a possibilidade de envolvimento cardíaco, renal ou sobrevida. Já a persistência de auto-anticorpos anti-scl-70 em pacientes com doença de Raynaud é indicativa da possibilidade de desenvolvimento de esclerose sistémica.
20 JO-1 Anticorpos contra o antigénio Jo-1 (sintetase-1,2-de histidil-trna) são encontrados em aproximadamente 30 a 50% dos pacientes adultos com miosites, incluindo polimiosite, dermatomiosite e as síndromes superpostas. Aparecem em cerca de 60% dos casos de miosite e de doença intersticial pulmonar. A presença de anticorpos anti-jo-1 em pacientes com polimiosite idiopática normalmente é acompanhada de doença grave, tendência a recidiva e mau prognóstico. Na miosite juvenil com presença de anti-jo-1, as manifestações clínicas e o curso de doença e resposta à terapia são semelhantes à evolução nos adultos. É considerado marcador diagnóstico de polimiosite. Anticentrómero Os anticorpos anticentrómero (AAC) são um subgrupo distinto dos anticorpos antinucleares detectáveis, utilizando como substrato células de cultura de tecidos. Os pacientes com anticentrómero-positivos não apresentam as características mais graves da esclerose sistémica progressiva, como a doença renal. Por isso, a positividade parece indicar um prognóstico mais favorável. São encontrados em cerca de 22% dos pacientes com esclerose sistémica progressiva e estão positivos em cerca de 70% dos casos de síndrome de CREST e em cerca de 12% dos pacientes com cirrose biliar primária, dos quais aproximadamente 50% apresentam características de esclerodermia. Por outro lado, a esclerodermia, sob a forma da síndrome de CREST, está presente em cerca de 4% dos casos de cirrose biliar primária. Os casos de esclerodermia limitados ao síndrome de CREST que cursam com AAC positivo apresentam, com mais frequência, calcinose e telangiectasias. Nestes casos, é menor a ocorrência de fibrose pulmonar intersticial. Os pacientes que apresentam fenómeno de Raynaud e AAC positivo sugerem a possibilidade de desenvolvimento do síndrome de CREST. Anticorpos Antitiroideus As doenças da tiróide de etiologia auto-imune são acompanhadas da presença de auto-anticorpos. A sua determinação está indicada na investigação diagnóstica das tiróidites auto-imunes, principalmente a doença de Hashimoto, doença de Graves, tiróidite pós-parto e mixedema idiopático. Na investigação diagnóstica, recomenda-se a utilização da pesquisa associada de mais de um anticorpo para avaliar, dessa forma, a presença de anticorpos contra os diferentes antígenos. Os anticorpos mais pesquisados são antitireoperoxidase (anti- TPO), antitireoglobulina (anti-trg) e os anticorpos anti-receptores de TSH (TRAB). Os anticorpos antimicrossomais foram durante muito tempo, em associação com os doseamentos das hormonas tiróideias, considerados o padrão para o diagnóstico das tiroidites auto-imunes. Hoje, podem ser substituídos pela pesquisa dos anticorpos antiperoxidase tiroideu. A tireoperoxidase (TPO), principal enzima envolvida no procedimento de síntese de hormona da tiróide, é uma glicoproteína, expressa apenas em células foliculares da tiróide. Ela é o principal antigénio na partícula microssomal da tiróide. Os anticorpos antitireoperoxidase estão presentes em 4 a 9% dos adultos normais, em 57-74% dos pacientes com doença de Graves, em % dos pacientes com
21 doença de Hashimoto ou mixedema idiopático, em 19% dos casos de tumores diferenciados de tiróide e, raramente, em pacientes com tiróidite subaguda. A prevalência de positividade em pacientes idosos (80 anos) é mais alta nas mulheres (10%) comparadas aos homens (2%). Os anticorpos antitireoglobulina estão presentes em títulos elevados em cerca de 25% dos casos de doença de Graves e em 55% dos pacientes com tiróidite de Hashimoto. Raramente se observam casos em que os anticorpos estão ausentes devido à produção de anticorpos restrita aos linfócitos intratiroideus. Eles podem ser detectados, com menor frequência, noutras patologias auto-imunes, em pacientes com carcinoma de tiróide e em percentagens ainda menores em mulheres e indivíduos idosos hígidos. Geralmente, as amostras apresentam-se positivas para anti -TRG e anti-tpo. A positividade isolada para os anticorpos antitireoglobulina é menos frequente que o achado isolado dos anticorpos antitireoperoxidase. Durante a gravidez, a presença de anticorpos anti-tpo e TRAB pode ser considerada fator preditivo de tiróidite pós-parto. Durante as fases precoces da tiróidite de Hashimoto, encontramos anticorpos antitireoglobulina significativamente elevados e níveis menos elevados de anti-tpo. Tardiamente, os anticorpos anti-trg podem desaparecer, enquanto os anti-tpo permanecem presentes por muitos anos. Pacientes que apresentam outras desordens auto-imunes, como síndrome de Sjögren, lúpus eritematoso sistémico, artrite reumatóide e anemia perniciosa, podem apresentar anticorpos antitireoglobulina positivos. Outro anticorpo utilizado na investigação clínica das patologias tiroideias são os anticorpos anti-receptores de TSH (TRAB), que podem actuar tanto estimulando como inibindo as funções tiroideias, ligando-se a diferentes epitopos. Encontram-se positivos na doença de Graves e nas tiroidites subagudas. Devido à sua capacidade de atravessar a barreira placentária, podem levar à doença de Graves neonatal por transferência passiva. A positividade do TRAB no soro sugere doença auto-imune em actividade, mas não define o estado funcional da glândula. O ensaio baseia-se na capacidade do soro que contém TRAB de impedir a ligação do TSH. Esse teste também é útil na avaliação de remissões ou recidivas da doença. Antiestreptolisina O Os Streptococcus beta-hemolíticos do grupo A causam infecções clínicas especialmente de orofaringe e pele, endocardites e quadros não-supurativos, como febre reumática e glomerulonefrite aguda. A estreptolisina O é uma das toxinas extracelulares libertadas pelo Streptococcus beta-hemolítico do grupo A. Ela é capaz de induzir o síntese de anticorpos específicos, os anticorpos antiestreptolisina O (ASO), em cerca de 80% das infecções. O uso de antibióticos, corticóides e drogas imunossupressoras pode inibir a produção de ASO. A ASO eleva-se na primeira semana, atingindo valores máximos em 2 a 4 semanas após a infecção estreptocócica e retornando aos valores normais após 6 a 12 meses.
22 A manutenção de títulos de ASO elevados de anticorpos ou a sua elevação em amostras seguidas são indicativas de infecção aguda, reinfecção ou lesões pósestreptocócicas. Apesar de níveis séricos de ASO serem encontrados na maioria dos pacientes com febre reumática e glomerulonefrite pós-estreptocócica, a sua maior indicação é no seguimento de pacientes com febre reumática, já que nesses casos os títulos de ASO se correlacionam melhor com a atividade da doença. Cerca de 80 a 85% dos casos de febre reumática cursam com títulos elevados. Antígeno Carcioembrionário (CEA) O antígeno carcioembrionário (CEA) é normalmente sintetizado e secretado pelas células que revestem o trato gastrointestinal do feto e em pequenas quantidades no adulto. Em situações normais, é eliminado pelo intestino. Em desordens benignas e malignas do trato gastrointestinal, pode ser detectado no sangue circulante. Não é um antigénio órgão-especifico. A detecção no soro associa-se a várias malignidades como as de estômago, pâncreas, gastrointestinais, mama, pulmão e ovário. O antigénio carcioembrionário está presente em doenças benignas como hepatopatias, pancreatites, enfisema pulmonar, doenças benignas da mama, colite ulcerosa, doença de Crohn e pólipo rectal. Níveis mais elevados são encontrados em tabagistas. O CEA é usado na monitorização de tumores gastrointestinais, particularmente no carcinoma colorrectal. Segundo o The National Cancer Institute, o CEA é o melhor método não-invasivo para acompanhamento do carcinoma colorrectal. Níveis pré-operatórios muito altos são prognósticos de altas taxas de recidiva e de baixas taxas de sobrevida. O CEA pode ser usado para monitorizar a eficácia do tratamento, a recidiva da doença local ou metastática. Elevações dos níveis de CEA são maiores nas metástases e menores na recidiva local. Os níveis mais altos são encontrados nas metástases ósseas e hepáticas. No decurso de quimioterapia ou de radioterapia, os níveis séricos podem elevar-se temporariamente. A avaliação pós-operatória deve ocorrer em torno da 4ª semana. A sua avaliação não é recomendada como screening, devido à incidência de elevação de CEA noutras patologias. Cerca de 63% dos pacientes com carcinoma colorretal têm elevações de CEA. As alterações correlacionam-se com o estadiamento do tumor. Apresenta-se alterado em 20% dos pacientes em Duke A, 58% em Duke B e 68% dos casos em Duke C. A avaliação bimensal é recomendada durante os primeiros 2 anos após a cirurgia; nos anos subsequentes, as avaliações podem ser mais espaçadas, até completar 5 anos. Noutros tipos de tumor em que o CEA é detectado, os níveis no pós-operatório podem ser úteis no acompanhamento da terapia e na identificação do aparecimento da doença metastática, especialmente nos carcinomas de mama associados com CA 15-3 e os de pâncreas associados ao CA 19-9.
23 Antimitocôndria A avaliação dos anticorpos antimitocondriais é importante na investigação diagnóstica das doenças hepáticas crónicas, em que está presente em 90% dos casos de cirrose biliar primária, especialmente no diagnóstico diferencial com outras colangites. Os anticorpos antimitocondriais (AMA) podem também estar presentes em 25% a 30% dos casos de hepatite crónica activa e mais raramente noutras doenças hepáticas, como obstrução biliar extra-hepática, hepatite vírica, cirrose de diferentes etiologias, hepatite induzida por drogas e neoplasia hepática. São encontrados em baixos títulos em cerca de 1% de adultos saudáveis e em doenças auto-imunes. Os níveis de anticorpos não se correlacionam com a gravidade e o tempo de evolução da doença, nem definem o prognóstico. Os AMA desaparecem aproximadamente 1 mês após o transplante hepático e diminuem com o uso de ciclosporina como tratamento. O diagnóstico da cirrose biliar primária deve-se basear nos achados clínicos, laboratoriais e histológicos. Aproximadamente 4% de pacientes com cirrose biliar primária têm esclerodermia, frequentemente como síndrome de CREST. Além disso, às vezes é encontrada reactividade para AMA nalguns pacientes com síndrome de CREST ou esclerodermia difusa, na ausência de doença hepática. Diferentes antigénios são encontrados na membrana mitocondrial, fazendo com que existam diferentes tipos de anticorpos antimitocondriais. A identificação dos diferentes tipos (M1, M2, M3, M4, M5, M6, M7, M8 e M9) é possível com o uso de antigénios recombinantes em ensaio imunoenzimático e permite um diagnóstico específico dos AMA. A cirrose biliar primária está relacionada a M2, e o tipo M9 pode ser encontrado em membros saudáveis da família. Os dos diferentes tipos restantes correlacionam-se com outras patologias, como doenças do colágeno (M5) e hepatite induzida por drogas (M6). A imunofluorescência indirecta usando células HEp-2 é 100% sensível e específica para identificação de AMA total. Antimúsculo Liso Os anticorpos antimúsculo liso (AML), ou (f-actina) são encontrados na maioria dos pacientes com hepatite crónica auto-imune. Em geral, a ausência de AML e anticorpos antinucleares são argumentos para o diagnóstico de formas não autoimunes de hepatites crónicas. Nas hepatites víricas crónicas, eles podem ser detectados em títulos mais baixos em cerca de 10% dos casos. Podem ser encontrados em aproximadamente 2% dos adultos normais, porém sempre em baixos títulos. A presença de anticorpos antinucleares pode interferir, levando à positividade com títulos baixos. Títulos elevados são característicos da hepatite crónica auto-imune. Quando presentes noutras patologias, normalmente apresentam-se com títulos baixos, <1/80. Cerca de 50% dos pacientes com cirrose biliar primária apresentam AML. Com menor frequência são encontrados nas uveítes, nas hepatites induzidas por drogas, na alopécia, na doença hepática alcoólica, nas neoplasias, na hipertensão pulmonar primária e transitoriamente em hepatites agudas e outras infecções
24 víricas, incluindo mononucleose infecciosa. A sua presença não tem valor preditivo para o desenvolvimento de doença hepática. O diagnóstico deve ser sempre acompanhado da avaliação de outros anticorpos como os anticorpos antinucleares e do perfil hepático. O achado isolado de AML não tem significado clínico. Apoliproteína A-I A apolipoproteína A (ApoA) é um dos principais componentes da lipoproteínas de alta densidade (HDL). Os seus dois componentes principais são a Apo-A-I e a Apo- A-II. A Apo-A-I é constituída por 245 aminoácidos e representa cerca de 75% da Apo-A nas HDL. É sintetizada no fígado e no intestino e responsável pela activação de uma enzima envolvida na esterificação do colesterol no plasma. O colesterol esterificado pode então ser removido dos tecidos extra-hepáticos e células periféricas e transportado até o fígado, para então ser metabolizado e excretado. A Apo-A-II representa cerca de 20% da Apo-A nas HDL. É constituída por 154 aminoácidos, e o seu papel fisiológico ainda é pouco conhecido. Valores da Apo-A-I elevam-se durante a gravidez, na doença hepática e na administração de estrogénios. Valores diminuídos são encontrados na colestase, na septicémia, na cirrose hepática aguda, em pacientes que consomem insulina, na aterosclerose e nos casos de deficiências hereditárias. A avaliação da Apo-A-I tem sido apontada como um bom parâmetro preditivo de risco de doença coronária. Os seus níveis são inversamente proporcionais ao risco de doença coronária prematura. Valores elevados de Apo-A-I (HDL) e baixos de Apo-B (LDL) correlacionam-se com baixo risco aterogénico. Avaliação da Função Gonadal DISTÚRBIOS DA REPRODUÇÃO FEMININA Puberdade Precoce A puberdade precoce caracteriza-se por aceleração da velocidade de crescimento, desenvolvimento das mamas e crescimento de pelos pubianos. Pode ser classificada como puberdade precoce verdadeira (dependente de GnRH), indicando activação precoce do eixo hipotalámico-hipofisário-gonadal, ou pseudopuberdade precoce (independente de GnRH), quando o aumento das hormonas esteróides ocorre sem o estímulo das gonadotrofinas. Ambas as condições podem estar relacionadas a doenças graves, sendo necessária cuidadosa anamnese, exame clínico e métodos de diagnóstico por imagem para descartar doenças do SNC, como tumores, traumatismo craniano ou encefalite, ou mesmo massa pélvica ou abdominal. A avaliação hormonal deve incluir função tiroideia (TSH, T4L), esteróides (estradiol, testosterona, progesterona, sulfato de deidroepiandrosterona (S-DHEA), androstenediona e 17 hidroxiprogesterona), FSH, LH, HCG e teste LH-RH. Na puberdade precoce verdadeira, os valores de LH, FSH e estrógenos são compatíveis com maturidade sexual, enquanto valores elevados de estrogénios e baixos de FSH e LH são geralmente observados na presença de tumores secretores
25 de estrogénios. Níveis elevados de HCG podem ser indicativos de teratoma ou de disgerminoma do ovário. Níveis elevados de 17-hidroxicorticosteróides, progesterona e androgénios adrenais confirmam o diagnóstico de hiperplasia adrenal por deficiência de 21-hidroxilase, enquanto o aumento do 11-desoxicortisol indica hiperplasia adrenal por deficiência de 11-hidroxilase. Suspeita-se de adenoma ou carcinoma do córtex adrenal quando o S-DHEA e/ou a androstenediona estão aumentados. Um aumento na testosterona sugere precocidade de origem ovariana. Outros testes úteis no diagnóstico da precocidade sexual são a ultra-sonografia dos ovários, a ressonância magnética (RM), a tomografia computadorizada (TC) ou a ultra-sonografia das adrenais, a determinação da idade óssea e RM ou TC de crânio. Amenorréia É definida como a ausência de menstruação por 3 meses ou mais em mulheres que já menstruaram anteriormente. Podem também ser consideradas amenorréicas as mulheres nas quais a menarca não ocorreu até os 16 anos, independentemente da presença ou ausência de caracteres sexuais secundários. Segundo Speroff, as causas de amenorréia podem ser classificadas em quatro grupos (compartimentos): GRUPO IV GRUPO III GRUPO II CLASSIFICAÇÃO ETIOLÓGICA DA AMENORRÉIA AMBIENTE SNC - HIPOTÁLAMO *GnRH-TRH HIPÓFISE ANTERIOR *TSH, FSH, LH, PROLACTINA OVÁRIO *ESTROGÊNIOS *PROGESTERONA *ANDROGÊNIOS Stress Aumento de Peso Distúrbios Psicológicos Exercícios físicos Tumor Hipofisário Insuficiência hipofisária Síndrome de Sheeham Perimenopausa Síndrome de Resistência Ovárica Insificiência Ovárica Anormalidades Cromossómicas GRUPO I ÚTERO, CERVICE E VAGINA Anomalia do Ducto de Müller Testículo Feminilizante Síndrome de Asheeman Amenorréia e infertilidade podem ser os primeiros sintomas de disfunção tiroidéia. Em casos de hipotiróidismo, o aumento de TSH induz a hiperprolactinémia.
26 Infertilidade Ocorre em 15% dos casais, e 50% dos casos devem-se a problemas na mulher. Dessas, 40% não ovulam, 10% têm fase lútea inadequada, 40% têm anomalias tubáricas e 10% têm factores cervicais ou tiroideios. Embora a causa da insuficiência não seja encontrada na maioria das mulheres, ela pode resultar de anomalias dos eixos hipotalámico-hipofisário ovárico, tiroideio ou adrenal. A avaliação laboratorial de não ovulação deve incluir FSH, LH, prolactina e progesterona. Em presença de sinais e sintomas de disfunção tiroideia ou de hiperandrogenismo, deve-se fazer avaliação de hormonas tiroideias, do S-DHEA e da testosterona. As disfunções da fase lútea podem ser avaliadas pelo doseamento de progesterona, cujos níveis de pg/ml ou mais, 5 a 10 dias antes do período menstrual seguinte, descartam uma fase lútea inadequada. A biópsia de endométrio realizada 2 a 3 dias antes da menstruação é útil no diagnóstico. Hirsutismo O aumento do crescimento de pelos (hirsutismo) ocorre por aumento da produção de androgénios (ováricos ou adrenais) ou aumento da sensibilidade da pele aos andrógenios circulantes. Mais de 90% das pacientes têm ovários poliquísticos ou hirsutismo idiopático. A avaliação hormonal deve incluir testosterona, androstenediona e S-DHEA. A sensibilidade da pele aos androgénios é modulada pela enzima 5-alfa-redutase, que converte a testosterona em deidrotestosterona, a hormona mais activa no crescimento dos pelos. O síndrome do ovário poliquístico envolve o eixo hipotálamo-hipófise-ovário e adrenal. Esses pacientes cursam com o aumento da produção de estrógenios e
27 androgénios, evidenciado pelo aumento dos níveis circulantes de testosterona, androstenediona, deidroepiandrosterona, S-DHEA, 17-hidroxiprogesterona e estrona. Deve-se avaliar ainda FSH, LH e hormonas tiroideios. A prolactina tende a estar ligeiramente elevada. DISTÚRBIOS DA REPRODUÇÃO MASCULINA Hipogonadismo/ Infertilidade O hipogonadismo masculino ou infertilidade pode ser classificado como prétesticular, testicular ou pós-testicular. As causas pré-testiculares (hipogonadismo secundário) são geralmente hipotalámicas ou hipofisárias, podendo ser congénitas ou adquiridas. As alterações hipotalámicas congénitas são mais frequentes do que as hipofisárias, e podem causar apenas puberdade atrasada ou hipogonadismo hipogonadotrófico idiopático. No geral, o crescimento progride sem sinais puberais e com testículos muito pequenos. A deficiência gonadotrófica hipofisária adquirida é mais frequente que a hipotalámica e, geralmente, causada por tumores. A disfunção eréctil ou impotência pode ser uma manifestação precoce, bem como a deficiência da hormona de crescimento (HGC). Tumores secretores de prolactina também podem causar sintomas de disfunção eréctil e infertilidade, uma vez que o aumento de prolactina suprime a produção de GnRH. Outras causas de hipogonadismo pré-testicular são: hipotiroidismo, síndrome de Cushing e cirrose alcoólica. As causas testiculares (hipogonadismo primário) podem ser congénitas ou adquiridas. As causas congénitas incluem síndrome de Klinefelter, criptorquidismo e hipoespermatogénese idiopática. As causas de insuficiência testicular adquiridas mais frequentes são orquite (que pode ser causada pela parotidite) e traumatismo físico. Outras causas são radiação e agentes antineoplásicos. As causas pós-testiculares devem-se geralmente ao bloqueio funcional ou à obstrução mecânica do transporte do esperma ou alterações funcionais do esperma. As manifestações clínicas incluem distribuição anormal de pelos faciais e corporais, distribuição anormal e diminuição da massa muscular, distribuição anormal da gordura corporal, aumento da proporção envergadura/altura ou diminuição da proporção tronco/membros inferiores, diminuição do volume testicular, diminuição ou ausência de olfacto e ginecomastia. É necessário investigar o desenvolvimento físico e a idade da puberdade, as alterações de líbido, disfunção eréctil, infertilidade e dificuldades conjugais relacionadas com o desempenho sexual. A síndrome de Kallmann caracteriza-se por ausência ou diminuição de olfacto, cegueira para cores, agenesia renal, surdez neurossensorial, fenda labial ou palatina, diminuição ou ausência das características sexuais secundárias em homens e testículos pequenos. No hipogonadismo devido à hiperprolactinemia, os pacientes podem apresentar galactorréia, disfunção eréctil e diminuição da líbido. A síndrome de Klinefelter após a puberdade caracteriza-se por aparência tipo eunuco, testículos firmes e pequenos, ginecomastia, azoospermia e por vezes
28 atraso mental. A avaliação laboratorial inclui os doeamentos séricas de testosterona, LH, FSH, prolactina e SHBG. No hipogonadismo primário, a testosterona sérica encontra-se baixa, com altos níveis de LH e FSH. No hipogonadismo secundário, a LH e a FSH encontram-se também diminuídos. A patologia hipofisária pode ser distinguida da patologia hipotalámica por meio de testes dinâmicos da função endócrina. O teste de estímulo com GnRH avalia a reserva de gonadotrofinas. O aumento da FSH e da LH após o teste indica patologia hipotalámica. No hipogonadismo primário (LH e FSH elevadas), um cariótipo alterado com genótipo masculino e azoospermia sugere síndrome de Klinefelter. O hipotiroidismo e a hiperprolactinemia podem ser excluídos com dosagens séricas de TSH e de prolactina, respectivamente. A pesquisa de tumores deve ser realizada com tomografia computadorizada e ressonância magnética. Infertilidade Geralmente, o único sinal de infertilidade é a incapacidade de engravidar a parceira. O paciente pode ter história de criptorquidismo e infecção do trato genito-urinário. O espermograma continua a ser o teste mais valioso na investigação da infertilidade masculina.testes especiais como anticorpos antiespermatozóides, interação com o muco cervical e testes de penetração do esperma só devem ser realizados após os exames de triagem. A azoospermia pode ocorrer devido a obstrução bilateral, ejaculação retrógrada ou ausência congénita dos vasos deferentes ou das vesículas seminais. Exames radiológicos dessas estruturas auxiliam o diagnóstico.
29 Disfunção Eréctil A disfunção eréctil é um síndrome complexo que envolve factores arteriais, venosos, sinusoidais, neurológicos, hormonais, bioquímicos, sociais e psicológicos. É definida como a incapacidade de obter uma erecção longa durante o tempo suficiente para uma relação plenamente satisfatória. Geralmente, ocorre uma disfunção eréctil parcial, mais frequentemente do que uma falta completa de rigidez
30 do pénis. A perda de erecção antes da ejaculação é a queixa mais comum. A disfunção eréctil pode ser classificada como fisiológica ou funcional. Uma disfunção neurogénica envolve incapacidade de iniciar a erecção devido à ausência dos neurotransmissores endógenos, e pode ser causada por diabetes, doenças da medula espinal, lesões da cauda da medula espinal, polineuropatia, mielopatia e esclerose múltipla, entre outras. Determinados medicamentos, estados de ansiedade e o uso de bebidas alcoólicas também podem acarretar problemas. Drogas que atuam no SNC ou no pico adrenérgico da ansiedade podem causar diminuição do fluxo sanguíneo do pénis, assim como drogas anti-hipertensivas (betabloqueadores, tiazidas, metildopa), cimetidina e alguns antilipémicos. O alcoolismo de longa duração e a cirrose hepática podem prejudicar os mecanismos de condução nervosa intrapenianos e acarretar atrofia testicular ou ginecomastia. A segunda classificação é baseada nas desordens vasculares. As principais causas são arteriosclerose, síndrome de Leriche, outras obstruções vasculares, microangiopatia, síndromes anginosas, insuficiência cardíaca congestiva e priapismo. A disfunção vascular pode ser arterial, venosa ou mista. Na disfunção arterial, não ocorre o enchimento do corpo cavernoso. Estes casos geralmente são provocados por hipertensão, diabetes, dislipidemias, angina e tabagismo. Na disfunção venosa, o corpo cavernoso não consegue reter o sangue, e isso deve-se, normalmente, a traumas ou à idade. As causas endócrinas da disfunção eréctil incluem a deficiência de testosterona por doença hipofisária ou testicular, o excesso de estrogénio e a hiperprolactinemia. Outras causas são o hipertiroidismo, o hipotiroidismo e o síndrome de Cushing. A avaliação laboratorial, portanto, deve incluir glicemia de jejum, perfil lipídico, avaliação hepática, renal e da tiróide, bem como doseamentos de prolactina, testosterona livre, LH e FSH. Prostatite O termo prostatite inclui inúmeras condições como prostatites bacterianas agudas e crónicas, não-bacterianas e prostatodinia. Nas prostatites bacterianas agudas, o início é abrupto, com febre e infecção do trato urinário, sintomas irritativos e obstrutivos, dor lombar baixa ou no períneo, astenia, mialgia e artralgia.
31 Geralmente, ocorre em pacientes jovens por bacilos Gram-negativos. O exame simples de urina geralmente revela piúria, indicativa de infecção urinária, e, à cultura, o Gram-negativo encontrado com mais frequência é Escherichia coli. A prostatite bacteriana crónica ocorre em pacientes mais velhos, com infecção urinária de repetição, geralmente por Gram-negativos. Muitos desses pacientes apresentam cálculos na próstata, o que facilita a cronicidade da infecção. A coleta após massagem prostática é aconselhável nesses casos. O tipo mais comum de prostatite é a não-bacteriana, geralmente causada por Chlamydia trachomatis, Ureaplasma urealyticum e Trichomonas vaginalis. Neoplasias Os tumores testiculares são raros e representam menos de 1% das mortes por cancro nos homens. Apesar da baixa prevalência, em alguns países é a neoplasia mais comum em homens entre os 29 e os 40 anos de idade. A maioria dos tumores testiculares (95%) é formada por células germinativas e divide-se em seminomas e não-seminomas. Entre os tumores não-seminomatosos estão o carcinoma de células embrionárias coriocarcinoma e o teratoma, que normalmente metastatizam por vias linfática e hemática, além de serem resistentes à radioterapia. As metástases dos tumores seminomatosos são, normalmente, apenas por via linfática, para linfonodos regionais, retroperitoneais, mediastinicos e supraclaviculares, e são sensíveis à radioterapia. Quarenta por cento dos tumores de células germinativas são formados por componentes seminomatosos e não-seminomatosos, mas a presença de qualquer componente não-seminomatoso classifica-o como tal. O sinal clínico mais comum da apresentação do tumor de testículo é o intumescimento indolor do órgão, que pode tornar-se doloroso por hemorragias no interior da neoplasia ou após traumatismos. Outros sintomas que podem ser encontrados são disúria, perda de peso, feminilização, ginecomastia e diminuição da libido. Paralelamente à realização de exames de imagem, os marcadores tumorais são de grande auxílio no diagnóstico desses tipos de cancro. A determinação sérica da hormona gonadotrófica coriónica (HCG) e de alfafetoproteína (AFP) é importante na investigação diagnóstica, especialmente se o método utilizado dosear o HCG total e a fracção beta livre. A presença de níveis aumentados de AFP indica a existência de um componente não-seminomatoso no tumor de testículo. Num estudo de pacientes com tumores não-seminomatosos, os níveis séricos de HCG e da fração beta livre estavam aumentados em 60% e em 40-70% dos casos, respectivamente. Apesar de poucos tumores seminomatosos estarem associados ao aumento de HCG, níveis elevados (acima de UI/L) estão ligados à presença de tumor não-seminomatoso. A avaliação conjunta dos dois analítos aumenta o valor preditivo dos testes em relação à dosagem isolada, pois permite a detecção de aproximadamente 90% dos tumores não-seminomatosos. Na investigação de seminoma, os níveis séricos de HCG estão aumentados somente em 7 a 16% dos pacientes, e os valores são inferiores a 200 UI/L. Porém, quando se utiliza a dosagem da fração beta livre, 20 a 50% dos pacientes com seminoma apresentam níveis séricos aumentados, mostrando a importância de se dosear essa fracção. Nesses casos, é necessário realizar o exame histológico do material de punção testicular para diferenciar seminomas de não-seminomas. Existem ainda os tumores testiculares de células de Sertoli ou células de Leydig,
32 que geralmente são benignos. Não existe um consenso entre os mais de 40 ensaios existentes hoje no mercado para as determinações de HCG ou das moléculas relacionadas. Variações entre os resultados encontrados entre ensaios são comuns, especialmente se a dosagem de HCG é para a investigação de gestações complicadas com aborto espontâneo, préeclâmpsia, doença trofoblástica, síndrome de Down ou neoplasias do testículo, da bexiga ou do ovário. Essas variações entre os resultados de HCG devem-se ao facto de que várias formas da molécula de HCG podem estar presentes no sangue e na urina de gestantes e de indivíduos com tumores: molécula de HCG intacta, fraccionada, hiperglicosilada, hipoglicosilada, sem a extensão C-terminal, sub-unidade livre, subunidade grande, sub-unidade beta livre, sub-unidade beta livre fraccionada e a fracção beta core. Muitas dessas sub-unidades são produtos de diferentes etapas de degradação do HCG que fazem parte de um processo de desativação da molécula. No início de uma gestação normal, a principal forma de HCG encontrada no sangue é a não-fraccionada, que aumenta exponencialmente no primeiro trimestre de gravidez. Em pacientes com cancro de testículo ou doença trofoblástica, as principais formas de HCG encontradas têm sido o HCG fraccionado e a fracção beta livre, que é indicada como o melhor marcador tumoral para o cancro de testículo. A metodologia que utiliza a associação HCG fraccionada, HCG não-fraccionada e fracção beta livre é a que melhor se aplica para a dosagem de HCG, seja na investigação de gravidez ou de cancro. A maioria das neoplasias de próstata é de adenocarcinomas, detectados quando se acha um nódulo de consistência difusa, por meio do toque retal. Em geral, o paciente não apresenta, até então, queixas clínicas. Alguns pacientes manifestam obstrução do trato urinário ou disfunção eréctil. O screening com dosagem do antigénio específico da prostata (PSA) tem facilitado, juntamente com o toque retal, o diagnóstico mais precoce. Perante as alterações desses parâmetros, exames complementares, como o ultra-som trans-rectal e a biópsia da próstata, tornam-se necessários para o diagnóstico.
33 AVALIAÇÃO LABORATORIAL Hormona Folículo-Estimulante (FSH) É uma hormona glicoproteica produzida pela hipófise e secretada de forma pulsátil, podendo ser doseada em pool. Eleva-se nas deficiências do ovário e testicular (hipogonadismo primário). É indicado no diagnóstico da menopausa. Encontra-se diminuída nas doenças hipotalámicas e hipofisárias, excepto em casos de tumores produtores de gonadotrofinas, quando se encontra elevada. Pode elevar-se também em casos de comprometimento da espermatogénese. A relação LH/FSH maior do que 2 pode sugerir o diagnóstico de ovário poliquístico. É útil também na avaliação da puberdade precoce. Hormona Luteínica (LH) É uma hormona glicoproteica produzida pela hipófise e secretada de forma pulsátil, podendo ser doseada em pool. O doseamento seriado é indicado no diagnóstico da ovulação. Eleva-se no hipogonadismo primário e encontra-se diminuída nas doenças hipotalámicas e hipofisárias, excepto em casos de tumores produtores de gonadotrofinas, quando se apresenta elevada. A sua relação com FSH é valorizada no diagnóstico do síndrome do ovário poliquístico. É útil também na avaliação da puberdade precoce. Testosterona É uma hormona esteróide androgénica secretada pelos ovários e gandulas suprarenais na mulher e pelos testículos nos homens. É útil no diagnóstico do hipogonadismo masculino, bem como na avaliação da puberdade. Na mulher, é indicado na avaliação do hirsutismo e da virilização. A testosterona circula ligada à SHBG (globulina ligada às hormonas sexuais), com uma pequena fracção que circula na forma livre. 3-Alfa-Androstenediol Glicuronídeo (3-Alfa-Diol) É o principal metabolito da deidrotestosterona. Nos casos de aumento da actividade da 5-alfa-reductase, ocorre aumento tanto da DHT quanto dos seus metabolitos. É importante no diagnóstico do hirsutismo idiopático, encontrando-se aumentado mesmo com níveis normais de testosterona. Estrona Provém principalmente da conversão periférica da androstenediona. É útil na avaliação dos tumores feminilizantes e da menopausa, bem como na avaliação da puberdade e do síndrome do ovário poliquístico. Estradiol (17-Beta-estradiol) É o estrogénio mais potente produzido pelas gonadas. Na mulher, é produzido pelos folículos ováricos, e nos homens, pelas células de Leydig e por conversão periférica da testosterona. É útil no diagnóstico da puberdade precoce e dos tumores feminilizantes no homem. No hipogonadismo feminino, encontra-se em níveis baixos, apesar de grande superposição com valores normais. No hipogonadismo masculino, dependendo da etiologia, os valores podem estar normais ou elevados. Nos tumores feminilizantes no homem (supra-renais ou testiculares) produtores de estrogénio, o estradiol estará elevado.
34 Estriol O estriol é produzido pela placenta a partir da conversão do sulfato de deidroepiandrosterona produzido pela supra-renal fetal. Por isso, o seu doseamento é útil na avaliação da integridade feto-placentária. Os seus valores elevam-se gradualmente durante a gestação normal. O seu doseamento seriado é utilizado como um marcador no acompanhamento das gestações de alto risco, visto que sua queda indica sofrimento fetal. Progesterona É um esteróide secretado pelas gonadas e glândulas supra-renais. É o principal marcador da ovulação. Para essa avaliação, devem ser colhidas amostras seriadas. A principal indicação desse doseamento é o diagnóstico de ciclos anovulatórios e a disfunção da fase lúctea. Testosterona Livre A testosterona livre é responsável pelo efeito metabólico da testosterona, uma vez que não sofre a influência dos níveis de SHBG. É importante no diagnóstico do hipogonadismo masculino e do hirsutismo feminino. Androstenediona É um androgénio produzido pelas supra-renais e gónadas. Útil na avaliação do hiperandrogenismo (hirsutismo, acne), no acompanhamento da hiperplasia congénita de supra-renal, tumores virilizantes de supra-renal e ovário. Deidrotestosterona (DHT) Provém da transformação periférica de testosterona no homem e da androstenediona na mulher, pela ação da 5-alfa-redutase. É útil na avaliação do hirsutismo feminino, sugerindo maior conversão periférica. Também é útil nas avaliações do defeito da 5-alfa-redutase, nos casos de pseudo-hermafroditismo masculino, quando as concentrações de DHT são desproporcionalmente baixas em relação às de testosterona. Eleva-se também na hiperplasia congénita da supra-renal e nos carcinomas do ovário e adrenais. Durante a gestação, grandes quantidades são produzidas pela placenta. Globulina Ligada às Hormonas Sexuais (SHBG) É uma glicoproteína sintetizada pelo fígado. A sua função é transportar as hormonas sexuais. É útil na avaliação complementar do hiperandrogenismo, uma vez que a sua elevação pode levar ao aumento dos níveis de testosterona total mas não dos de testosterona livre. Várias circunstâncias alteram seus valores, como estrógenios e hormonas tiroidéias (hipertiroidismo). Tamoxifen, fenitoína e cirrose hepática elevam os níveis de SHBG. Já os androgénios, os glicocorticóides, a hormona de crescimento, o hipotiroidismo, a obesidade e a acromegalia cursam com níveis diminuídos de SHBG.
35 Avaliação Dinâmica da Função Endócrina Muitas patologias endócrinas podem ser diagnosticadas por meio dos doseamentos dos níveis hormonais sérios ou urinários, em condições basais. Contudo, o doseamento isolado das hormonas nem sempre permite a distinção entre o normal e o patológico. Os valores de normalidade tão alargados para concentrações séricas de algumas hormonas tornam imprecisa a interpretação de valores individuais se o valor normal prévio para determinado paciente for desconhecido. Por exemplo, uma concentração sérica de tiroxina (T4) no limite máximo para a população em geral pode estar associada a hipertiroidismo num paciente cuja concentração, usualmente, estaria no limite mínimo da faixa de normalidade. Além disso, há pequenos níveis de disfunção endócrina que podem estar compensados em condições basais. Portanto, os níveis séricos de cortisol podem estar normais em pacientes com insuficiência adrenocortical parcial devido ao aumento de secreção de corticotrofina (ACTH). No diagnóstico de alterações parciais dos mecanismos de controlo endócrinos, podemos utilizar três tipos de testes funcionais: doseamentos hormonais seriados, doseamentos de várias hormonas e testes de reserva endócrina e retro-controlo endócrino. Todos os três são da máxima importância no diagnóstico, mas podem sofrer a influência de inúmeros factores que tornariam sua interpretação bastante complexa. Doseamentos Hormonais Seriados Nalgumas circunstâncias, a variação de secreção hormonal reflecte processos pouco compreendidos de exacerbação ou de remissão de patologias. Dessa forma, doseamentos seriados dos níveis de cálcio e PTH (paratormona) por períodos prolongados podem ser necessárias para diagnóstico de hiperparatiroidismo. Outras condições clínicas, como o síndrome de Cushing, podem apresentar o mesmo padrão de exacerbação/remissão. Noutras circunstâncias, a variação na secreção hormonal endócrina resulta de alterações rítmicas como uma secreção pulsátil ou um ritmo circadiano básico. A perda do ritmo circadiano de secreção de cortisol pode ser um sinal precoce de síndrome de Cushing. O ritmo circadiano da secreção hormonal pode ser alterado por inúmeros factores, como distúrbios do sono, drogas, doenças psiquiátricas e stres. A demonstração de uma variação diurna normal pode ser uma boa evidência de normalidade na sua função. No entanto, a sua ausência não indica necessariamente uma doença endócrina primária. Na verdade, alterações desse ritmo circadiano indicam a necessidade de testes diagnósticos adicionais. Doseamento de várias Hormonas Como o sistema endócrino funciona basicamente sob retro-regulação, o doseamento de várias hormonas (T4 e TSH, cálcio e PTH, testosterona e LH ) permite uma avaliação dos níveis individuais. Por exemplo, uma vez que a faixa de normalidade do T4 é ampla, os níveis de determinado paciente poderiam cair para a metade e ainda permanecer na faixa normal. Nesse caso, contudo, uma concentração de T4 próxima aos limites mínimos normais, associada a elevados níveis de TSH, indica o estadio inicial de uma falência tiroidiana compensada. Conforme observamos na tabela a seguir, baixos níveis de ambos os pares hormonais apontam deficiência da hormona trófica (ex: insuficiência hipofisária no caso de TSH e T4). Altos níveis da hormona-alvo com baixos níveis da hormona
36 trófica sugerem secreção autónoma do órgão-alvo (ex: adenomas adrenais hiperfuncionantes inibindo a secreção de ACTH). ALTO NORMAL BAIXO NÍVEL DA HORMONA DA GLÂNDULA BAIXO NORMAL ALTO Secreção autónoma de hormonas tróficas ou resistência à acção hormonal da glândula alvo Insuficiência Hipofisária Normal Secreção autónoma do órgão alvo Elevados níveis dos pares hormonais são compatíveis com os mecanismos de várias doenças. A secreção autónoma de uma hormona trófica pode ser tópica ou ectópica. Por exemplo, o síndrome de Cushing pode resultar da secreção hipofisária de ACTH ou da secreção de ACTH por tumores pulmonares. Outra possibilidade é a secreção de factores liberados a partir de tumores em órgãos periféricos, causando hipersecreção de hormonas hipofisárias, como por exemplo a acromegalia resultante da secreção ectópica de fatores liberadores da hormona de crescimento. Por outro lado, essa elevação combinada da hormona trófica e da hormona da glândula-alvo pode dever-se à resistência da acção da hormona da glândula-alvo. Essa resistência pode ser herdada (como nos casos de defeito de receptor de androgénios que causam resistência à acção da hormona e resultam em níveis elevados de LH e de testosterona), ou adquirida (como no caso de resistência insulínica da obesidade, que pode levar a hiperinsulinismo e hiperglicemia). Elevação de TSH e T4 pode indicar tanto secreção autónoma de TSH quanto à resistência da acção da T4. Contudo, doenças em estadio inicial podem tornar necessárias informações adicionais por meio de testes dinâmicos. Testes da Função Endócrina Os testes dinâmicos baseiam-se em estímulo ou em supressão da produção hormonal. Testes de Estimulação São utilizados na suspeita de hipofunção endócrina para avaliar a capacidade de reserva de síntese e secreção hormonal. Esses testes são realizados de duas maneiras: 1) Administração de uma hormona trófica para testar a capacidade do órgão-alvo de aumentar a produção hormonal. Essa hormona pode ser um factor liberador hipotalámico, como o TRH, ou uma hormona hipofisária, como o ACTH. Nesses casos, a capacidade do órgão-alvo é avaliada pelo doseamento dos níveis hormonais séricos - nos exemplos citados, o TSH e o cortisol. 2) Estimulação da secreção de uma hormona trófica endógena ou factor estimulador e medição do efeito desses estímulos antiestrogénicos em nível hipotalámico, diminuindo o retro-controlo negativo e causando um aumento na
37 secreção de gonadotrofinas, que pode ser seguido por ovulação e/ou aumento na formação de esteróides gonodais. Testes de Estimulção mais Frequentes ÓRGÃO/ SISTEMA ESTÍMULO RESPOSTA Hipotálamo-hipófise Hipoglicemia Metirapona Levodopa Anginina Citrato de clomifeno Exercício Restrição hídrica GH e ACTH (cortisol) ACTH (cortisol e 11-desoxicortisol) GH GH Gonodotrofinas GH Vasopresina Hipófise Tiróide Supra Renal RTH LHRH CRF GHRH TSH Pentagastrina Cálcio Certrosina Metirapona Mudança de postura TSH e prolactina Gonodotrofinas ACTH (cortisol) GH Captação de iodo radiotaivo Calcitonina Calcitonina Cortisol Cortisol e 11 desoxicortisol Renina e aldosterona Gónadas HCG Testosterona Ilhotas Pancreáticas Tolerância a glicose e libertação de Glicose insulina Paratiróide PTH AMPc e fósfatos urinários Balanço Hídrico Vasopresina Concentração urinária Metabolismo do Cálcio Sobrecarga de Cálcio Cálcio Urinário Testes de Supressão São utilizados em casos de suspeita de hiperfunção endócrina. Como nos testes de estimulação, são utilizadas hormonas exógenas ou factores reguladores conhecidos para avaliar a inibição da produção hormonal endógena, por exemplo, a administração de glicocorticóide (dexametasona) a pacientes com suspeita de síndrome de Cushing para avaliar a capacidade de inibição da secreção do ACTH e portanto da síntese adrenal de cortisol. A falência da supressão nesses testes indica a presença de secreção autónoma da hormona da glândula-alvo ou de hormonas tróficas (hipofisárias ou ectópicas) que não estão sob retro-regulação normal. Testes de Supressão Mais Frequentes ÓRGÃO/ SISTEMA ESTÍMULO RESPOSTA Hipotálamo-hipófise Glicose Dexametasona GH ACTH (cortisol) Tiróide T4 Captação de iodo radiotaivo Supra-renal Dexametasona Salina Clonidina Cortisol Renina e aldosterona Noradrenalina plasmática Ilhotas Pancreáticas Jejum Glicose e insulina
38 Interpretação dos Testes Funcionais São a melhor avaliação dos distúrbios endócrinos leves, como por exemplo o teste de estímulo com cortrosina para diagnosticar a insuficiência adrenocortical parcial com secreção de cortisol basal normal. Os testes dinâmicos também são úteis na determinação do defeito patogénico, tal como o estímulo com LHRH para diagnosticar se o hipogonadismo hipogonadotrófico ocorre em consequência de insuficiência hipofisária ou hipotalámica. Em pacientes com síndrome de Cushing, a supressão da produção de cortisol em resposta a altas doses de dexametasona sugere hipersecreção hipofisária de ACTH, uma vez que tumores adrenais ou secreção ectópica de ACTH não respondem ao teste de supressão. A principal dificuldade na interpretação dos testes é a definição adequada do que seja resposta normal em indivíduos normais que apresentam outras patologias. Por exemplo, os atletas têm uma resposta aumentada do ACTH e do cortisol ao estímulo com cortrosina. Além disso, inúmeros factores influenciam a resposta de um teste funcional, como idade, sexo, fumo, uso de determinadas drogas, obesidade, desnutrição, insuficiência renal crónica, cirrose hepática e outras patologias associadas. Por exemplo, a resposta do TSH ao estímulo com TRH diminui em homens com mais de 60 anos. Citamos ainda a resposta sub-normal do GH ao estímulo de hipoglicemia induzida por insulina e a administração de arginina e de levodopa em pacientes obesos, que normalizam após o retorno ao peso ideal. Por outro lado, pacientes com desnutrição grave, insuficiência renal crónica ou cirrose hepática costumam ter níveis de GH basal elevados, que não respondem à supressão ou respondem com um aumento paradoxal após sobrecarga de glicose. Na avaliação da baixa estatura, a realização de dois testes aumenta a sensibilidade de 80 para mais de 90%. Várias doenças psiquiátricas estão associadas a testes dinâmicos da função endócrina, alterados na ausência de patologia endócrina específica. A mais frequente é a depressão. Pacientes com depressão primária grave não apresentam supressão adequada do cortisol, após administração de dexametasona, normalizando essa resposta após o tratamento da depressão. Em 20% dos pacientes com doença psiquiátrica aguda, são encontradas concentrações elevadas de T4 e T4 livre sem evidência clínica de tireotoxicose. A resposta do TSH ao TRH apresenta-se subnormal ou ausente em cerca de 25% dos pacientes psiquiátricos sem doença tiroidéia, principalmente em casos de depressão unipolar ou bipolar. O uso de drogas também interfere nos testes dinâmicos. Glicocorticóides em doses farmacológicas, progestagénios, teofilina e cloropromazina bloqueiam a resposta do GH aos estímulos usuais. A ingestão crónica e excessiva de álcool diminui a resposta da prova de supressão do cortisol à dexametasona. O uso de levodopa, de dopamina e de aspirina em altas doses bloqueia a resposta do TSH ao TRH. A fenitoína aumenta a captação celular e o metabolismo do T4, levando a baixos níveis de T4 livre, além de diminuir em 50% a resposta do TSH ao TRH. Portanto, a avaliação da função tiridéia é prejudicada principalmente quando nos encontramos
39 diante de um paciente com uso dessa droga com níveis baixos de T4 e TSH normal. Deve ser considerada, ainda, a possível necessidade de estímulos repetidos para a obtenção de uma resposta normal. Por exemplo, pacientes com hipogonadismo hipogonadotrófico por doença hipotalámica com resposta subnormal do LH ao estímulo com LHRH podem normalizar a resposta ao teste após 1 semana de administração diária de LHRH. Esse protocolo permite a distinção entre hipogonadismo hipotalámico e hipofisário. Para melhor compreensão das provas funcionais, a figura acima esquematiza a regulação da secreção das hormonas hipofisárias por intermédio de hormonas hipotalámicas estimulantes e inibidores. Os Testes Mais Frequentes Estimulação da Hormona de Crescimento A maioria dos autores considera normal uma resposta superior a 7 ng/ml, embora outras escolas admitam valores > 10 ng/ml. - Após Exercício Colher a amostra basal em repouso, submeter o paciente a 20 minutos de exercício. Colocá-lo em repouso durante 10 minutos antes da colheita da amostra, após esforço. Aproximadamente 10% dos pacientes normais deixam de responder a esse estímulo. Portanto, a baixa resposta não faz o diagnóstico de deficiência de GH. A sua realização está contra-indicada nas doenças sistémicas nas quais o esforço possa desencadear ou agravar o quadro. - Após Clonidina Colher amostras nos tempos: basal, 60, 90 e 120 minutos. O paciente deverá permanecer deitado durante toda a prova e por mais 1 hora após a colheita da amostra de 120 minutos, prevenindo os efeitos da hipotensão causada pela droga. A pressão arterial deve ser monitorizada durante toda a prova. - Após Insulina São realizadas os doseamentos da GH e da glicemia nos tempos: basal, 30, 60, 90 e 120 minutos. É indispensável a monitorização médica contínua devido ao risco de hipoglicemia. A informação obtida nessa prova não parece superior à obtida com outros testes de libertação de GH. A sua realização é contra-indicada em pacientes com história de crises convulsivas, cardiopatias, insuficiência renal ou hepática, hipocortisolismo, em gestantes ou no uso concomitante de algumas drogas como hipoglicémicos orais e betabloqueadores. Para que o teste seja considerado válido, deve ocorrer queda da glicemia a valores abaixo de 40 mg/dl ou aparecimento de sinais clínicos de hipoglicemia. - Após Piridostigmina (Mestinon) Colher amostras para doseamento de GH nos tempos: basal, 60, 90 e 120 minutos. A sua realização é contra-indicada em pacientes com história de asma brônquica, diarréia e cólica intestinal.
40 - Após TRH Colher amostras para doseamento de GH nos tempos: basal, 30 e 60 minutos. Em indivíduos normais, não ocorre aumento dos níveis de GH, enquanto em muitos acromegálicos pode ocorrer um efeito paradoxal da droga com aumento da secreção de GH. Essa resposta não apresenta a mesma uniformidade que a resposta anormal à administração de glicose por via oral. A sua realização é contraindicada em pacientes com história de hipertensão arterial, doenças cerebrovasculares e glaucoma. Supressão da Hormona de Crescimento - Após Glicose São realizados os doseamentos de GH e de glicemia nos tempos: basal, 30, 60, 90, 120 e 180 minutos. Nos indivíduos normais, ocorre diminuição dos níveis de GH até valores inferiores a 2 ng/ml. Nos acromegálicos, pode ocorrer uma resposta paradoxal, com elevação dos níveis de GH. - Após Parlodel São realizados os doseamentos de GH nos tempos: basal, 60, 120, 180, 240 e 360 minutos. Indicado para determinar a possível resposta dos pacientes portadores de tumores produtores de GH à terapêutica medicamentosa com bromoergocriptina, devendo ocorrer queda expressiva (50% dos níveis basais). Estimulação da Prolactina - Após TRH São realizados os doseamentos de prolactina nos tempos: basal, 30 e 60 minutos. A pressão arterial deve ser monitorizada, pois pode ocorrer elevação dos níveis da PA. Em mulheres normais, deve ocorrer aumento de pelo menos três vezes o valor basal, enquanto nos homens se espera um aumento de pelo menos duas vezes o valor basal. Níveis elevados no doseamento basal e uma resposta reduzida ou ausente sugerem a presença de tumor, embora esse padrão de resposta não seja suficiente para diagnosticar ou excluir a possibilidade de prolactinoma. Níveis diminuídos no doseamento basal, com resposta baixa, são um achado raro, excepto quando associados à falência precoce da lactação no síndrome de Sheeham. Supressão da Prolactina - Após Parlodel Dosear a prolactina basal (8:00) e a cada 2 horas em quatro amostras (10,12,14 e 16 horas). Indicado para determinar a possível resposta dos pacientes portadores de tumor produtor de prolactina à terapêutica medicamentosa. Espera-se uma queda do nível basal de mais de 50% após 4 horas.
41 Estimulação da Hormona Tireotrófica - Após TRH É realizado o doseamento do TSH nos tempos: basal, 30 e 60 minutos, e se necessário, 90 e 120 minutos. Normalmente ocorre um pico de TSH entre 20 a 30 minutos após a administração do TRH. O incremento de TSH é de cinco a quinze vezes o nível basal, variando com o sexo (maior em mulheres) e com a idade (menor em idades avançadas). Em pacientes com hipotiroidismo primário, o TSH parte de valores basais altos, eleva-se mais ainda e não se normaliza aos 60 minutos. Já no hipotiroidismo secundário por deficiência hipofisária, o TSH encontra-se em níveis inferiores no doseamento basal e não responde ao TRH. No hipotiroidismo hipotalámico, a resposta do TSH ao TRH é tardia, registando-se elevação gradual do TSH até 60 minutos. Nos pacientes com hipertiroidismo, a secreção do TSH encontra-se bloqueada pelo excesso de T3 et4, não havendo resposta ao estímulo com o TRH. Estimulação das Gonadotrofinas Hipofisárias - Após LHRH São realizados os doseamentos de LH e de FSH nos tempos: basal, 15, 30 e 60 minutos. Em homens, ocorre um aumento de LH de duas a dez vezes o nível basal, e o aumento de FSH é de metade a duas vezes esse nível. Nas mulheres, o aumento de LH é de três a quatro vezes o nível basal na fase folicular e mais acentuado na fase lúctea, enquanto o aumento de FSH é de metade a duas vezes o basal. Estimulação Hipotálamo-Adreno-Hipofisária - Após Insulina Esse teste avalia o estímulo de ACTH e de cortisol. São realizados doseamentos de ACTH e de cortisol nos tempos: basal, 30, 60, 90 e 120 minutos. Para que o teste seja considerado válido, devem ocorrer queda da glicemia para valores abaixo de 40 mg/dl ou o aparecimento de sinais clínicos de hipoglicemia. É indispensável a monitorização médica contínua, devido ao risco de hipoglicemia. Esta prova deve ser precedida da prova de estímulo com ACTH, e só devem ser submetidos a ela os pacientes com estímulo positivo. Normalmente, o ACTH aumenta três vezes ou mais em relação ao nível basal, devendo exceder 150 ng/ml. O cortisol eleva-se a valores superiores a 200 ng/ml. - Após Cortrosina O teste de estimulação do cortisol - estimulação rápida com cortrosina simples. São realizadas os doseamentos de cortisol nos tempos: basal, 30, 60 e 90 minutos. A ausência de resposta do cortisol ao estímulo com cortrosina estabelece o diagnóstico de insuficiência adrenocortical parcial em pacientes com secreção de
42 cortisol basal normal. Níveis de cortisol iguais ou superiores a 200 ng/ml, em qualquer ponto da prova, indicam função adrenal normal. Avaliação Hipofisária Total São realizados doseamentos de TSH, prolactina, LH, FSH, cortisol, GH e glicose nos tempos: basal, 30, 60 minutos. Os doseamentos de FSH, GH, cortisol e glicose devem ser realizados também aos 90 minutos. A resposta de cada sector (tireotrófico, gonadotrófico, corticotrófico ou lactotrófico), bem como as contra-indicações, devem ser avaliadas isoladamente, como já foi descrito anteriormente. Betacaroteno O caroteno é um precursor lipossolúvel da vitamina A encontrado em gorduras, folhas e vegetais amarelos. Uma pequena porção do caroteno é absorvida pelo intestino, contribuindo para a cor amarela do soro. Com a participação das gorduras e dos sais biliares, a maior parte do caroteno é normalmente convertida em retinol no trato intestinal. A hipercarotenemia, isto é, a elevação do nível de caroteno, caracteriza-se por pigmentação amarela da pele, sem nenhuma mudança na cor da esclerótica, causada por ingestão excessiva de alimentos ou de complexos vitamínicos ricos em caroteno. O indivíduo também pode apresentar prurido e perda de peso. A doença é geralmente benigna e é tratada com mudanças na dieta. Valores diminuídos indicam ingestão insuficiente ou má absorção. O doseamento de caroteno é mais frequentemente utilizado como prova de triagem para a síndrome de má absorção e no diagnóstico diferencial de hiperbilirrubinemia Beta-2-Microglobulina A beta-2-microglobulina é uma pequena molécula presente na superfície das células nucleadas, principalmente linfócitos, que está relacionada com HLA (Human Leucocyte Antigen). A sua presença é necessária para a inserção da molécula de HLA na membrana celular, além de estabilizar a cadeia pesada do HLA. Ela parece actuar na regulação da função dos leucócitos, mas isso ainda não foi suficientemente definido. Está, normalmente, presente no plasma, urina e líquor. É libertada durante o processo de renovação das membranas celulares. Por ser uma proteína pequena, é filtrada pelos glomérulos. No entanto, a maior parte é reabsorvida e degradada pelas células epiteliais tubulares dos túbulos proximais. Por isso, a concentração plasmática de beta-2-microglobulina é um bom índice da taxa de filtração glomerular. É descrito um aumento progressivo dos valores normais acompanhando a idade. Níveis séricos elevados podem ocorrer em diversas patologias inflamatórias, como hepatites, artrite reumatóide, lúpus eritematoso sistémico, SIDA, sarcoidose e em pacientes com leucemias, linfomas e alguns tumores sólidos e patologias que cursam com a diminuição da filtração glomerular. Níveis urinários elevados podem ser encontrados em pacientes com desordens renais tubulo-intersticiais, como intoxicação por metais pesados, drogas quimioterápias, aminoglicosídeos, infecções urinárias altas e rejeição a
43 transplantes. Relatos recentes apontam a beta-2-microglobulina como o melhor marcador de prognóstico no mieloma múltiplo. Bilirrubina A bilirrubina é o principal produto do metabolismo do heme da hemoglobina. Cerca de 70% da bilirrubina são provenientes da destruição de eritrócitos velhos, 15% provêm de fontes hepáticas, e o restante é proveniente da destruição de células vermelhas defeituosas na medula óssea e nos citocromos. A hemoglobina é metabolizada no baço e no sistema reticuloendotelial, dando origem à biliverdina, que é reduzida a bilirrubina pela enzima biliverdina redutase. Essa bilirrubina recém-formada circula no sangue ligada à albumina sérica (forma não-conjugada). É transportada pelo sistema porta até o fígado, onde penetra no hepatócito por dois mecanismos distintos: difusão passiva e endocitose. Uma vez dentro do hepatócito, a bilirrubina desliga-se da albumina e forma um complexo protéico com as chamadas proteínas Y e Z. Logo depois, liga-se a um outro complexo chamado ligandina. É então transportada para o retículo endoplasmático liso, onde se forma um substrato da enzima glicuronil transferase, dando origem a um diglicuronídeo conjugado (mono- e triglicuronídeos também são formados). A bilirrubina, agora já conjugada, é transportada até a membrana celular. Na face oposta aos sinusóides e próxima aos canalículos biliares, ela é excretada directamente. Só consegue ultrapassar a membrana quando conjugada. Através dos canalículos biliares, alcança o trato intestinal, onde é metabolizada pelas bactérias da flora intestinal, formando os urobilinogénios. A maior parte dos urobilinogénios é absorvida e novamente excretada pelo fígado, e uma pequena fracção é excretada pelos rins. Existem portanto dois tipos de bilirrubina circulantes - a conjugada (bilirrubina directa) e a não-conjugada (bilirrubina indirecta). No entanto, existe um terceiro tipo de bilirrubina, chamada de bilirrubina delta, do tipo conjugada de reacção rápida e ligada à albumina permanentemente por uma reacção covalente. Pelas técnicas tradicionais, a bilirrubina delta era incluída nos resultados da bilirrubina directa (conjugada) e na bilirrubina total. Por estar fortemente ligada à albumina, a bilirrubina delta não é excretada pelos rins e permanece elevada por muitor tempo, na verdade, por períodos correspondentes à semi-vida da albumina (cerca de 19 dias), mesmo após a resolução da obstrução ou do período agudo da lesão hepática. Isso pode levar a falsas interpretações. Entretanto, actualmente, os métodos automatizados de última geração, especialmente a tecnologia de química seca, já separam a fracção delta, que não é incluída em nenhuma das demais frações, nem mesmo no valor da bilirrubina total. Acompanhando os mecanismos envolvidos no metabolismo da bilirrubina, é possível correlacionar o aumento de seus níveis séricos com alterações de uma dessas etapas. Os níveis séricos da bilirrubina não-conjugada (bilirrubina indirecta) são determinados pela velocidade de produção e pela velocidade de remoção dessa bilirrubina da circulação. Os distúrbios que alteram a capacidade de depuração do fígado estão ligados à captação e/ou conjugação hepática. Os aumentos de bilirrubina indirecta não levam ao aumento da bilirrubina na urina.
44 Os níveis séricos da bilirrubina conjugada (bilirrubina directa) são determinados pela capacidade de excreção da bilirrubina pelo fígado, ou seja, pela integridade fisiológica do hepatócito e da permeabilidade das vias biliares intra e extrahepáticas. Patologias que alterem essas funções cursam com aumento da bilirrubina directa, e muitas vezes da bilirrubina indirecta, e com a presença de bilirrubina na urina. Anemias hemolíticas (hereditárias e adquiridas, Produção excessiva reabsorção extravascular, eritropoiese ineficaz. Alterações da Síndrome de Gilbert, drogas, acidose metabólica e Captação estados carenciados com hipoalbuminémia. Alteração da Síndrome de Cligler-Najjar (tipos 1 e 2: deficiência Conjugação da actividade da glicuronil transferase total e parcial, respectivamente). Inibição da glicuronil transferase por fármacos, especialmente em recém nascidos. Alterações da excreção Obstruções das vias biliares Síndrome de Dubin-Johnson, síndrome de Rotor, colestase intra-hepática recorrente benigna, icterícia recorrente da gravidez, colestase por fármacos, icterícia pós-operatória, quadros de comprometimento da função hepática, como hepatites e cirrose. Lesões parciais ou completas dos ductos biliares por estenose, cálculos ou tumores. Brucelose A brucelose é uma zoonose, e a forma humana é causada por uma das quatro espécies: Brucella melitensis, a causa mais comum em todo o mundo, adquirida pelo contacto com cabras, carneiros e camelos; Brucella abortus, adquirida por contacto com bois; Brucella suis, adquirida por contacto com porcos; e Brucella canis, adquirida por contacto com cães. O contágio dá-se pelo contacto com a pele ou por ingestão de secreções contaminadas por esses animais. Tais bactérias mantêm-se viáveis em solo seco por cerca de 40 dias, e no caso de solo húmido esse prazo é ainda maior. São destruídas pela pasteurização e fervura, mas resistem ao congelamento. A contaminação relacionada com a ocupação profissional, como é o caso de agricultores, veterinários, processadores de carne, são a fonte mais frequente. Na população em geral, a fonte mais comum de contaminação é a ingestão de leite e derivados não-pasteurizados e o consumo de carne crua. Pode ser transmitida de pessoa a pessoa, pela placenta e durante a amamentação, e são citados casos raros de contaminação por actividade sexual. A infecção pode distribuir-se amplamente pelo organismo, causando lesões praticamente em qualquer órgão, com mais frequência no coração, ossos e articulações, aparelhos respiratório, gastrointestinal e geniturinário, globo ocular, pele, sistema nervoso central e sistema endócrino. O quadro clínico inicial é comum a outras doenças febris. O período de incubação dura em média de 1 a 3 semanas, podendo, em alguns casos, durar vários meses. A multiplicação intracelular do microrganismo ocorre nos gânglios linfáticos e sistema reticuloendotelial. A gravidade do quadro é variável, podendo apresentarse desde uma forma leve a grave. O quadro apresenta sintomas comuns como febre, mialgia, cefaléia, anorexia, artralgia e lombalgia. O exame clínico pode ser
45 pouco expressivo ou apresentar linfadenopatia, hepatoesplenomegalia, dor à palpação da coluna vertebral, dor abdominal e outras manifestações. O diagnóstico é feito mediante a associação de história compatível com probabilidade de infecção, sinais clínicos e deteccção de anticorpos por reacções de aglutinação (com ou sem cultura positiva de sangue e tecidos). O diagnóstico é de grande importância no período pré-natal, pois pode levar à morte fetal. Os antigénios bacterianos têm a capacidade de induzir a formação de anticorpos específicos, inicialmente da classe IgM e logo após das classes IgG e IgA. Esses anticorpos aparecem a partir da segunda semana da doença, com picos entre a terceira e sexta semanas. Títulos maiores ou iguais a 1/160 são considerados significativos quando encontrados numa região não-endémica. Em áreas endémicas e em profissionais de alto risco de contaminação, são considerados significativos títulos iguais ou acima de 1/320. Títulos altos de IgM indicam infecção aguda; altos títulos de IgG, infecção em actividade; quando mais baixos, podem significar infecção antiga. Recomenda-se a análise com intervalo de 2 semanas na avaliação dos casos duvidosos: variações de quatro vezes o título anterior são sugestivas de infecção aguda. Reacções com títulos baixos podem ser encontradas em pacientes vacinados contra a febre tifóide. Podem ser encontradas reações cruzadas por infecção por outras bactérias e após reacções intradérmicas, com antigénios de Brucella BTA O carcinoma da bexiga é um dos tipos de tumor de maior incidência na Europa. Afecta principalmente homens entre 50 e 70 anos de idade, fumadores e pessoas expostas a substâncias químicas, como tintas, couro e borracha. Segundo as estatísticas, 1 em cada 5 pacientes diagnosticados com este tipo de carcinoma tem expectativa de vida de cerca de 5 anos. No entanto, se o diagnóstico for precoce, a taxa de sobrevida nesse mesmo período sobe de 20 para 94%. Entre os sinais clínicos de carcinoma da bexiga, o mais frequente é a hematúria, mas outros sintomas - como aumento da frequência urinária, dor pélvica e suprapúbica, obstrução urinária e micro-hematúria, podem também manifestar-se. Aproximadamente 80% dos tumores da bexiga são de células de transicão e estão restritos, na sua maioria, à superfície mucosa, podendo ser resolvidos por meio de ressecções trans-uretrais. A detecção precoce do carcinoma da bexiga é essencial para se aumentar a sobrevida de pacientes portadores da entidade mórbida. A recorrencia desse tumor pode dar-se em cerca de 50% dos pacientes tratados, o que torna essencial a monitorização a longo prazo. A observação da recorrência do tumor em pacientes com diagnóstico prévio de carcinoma da bexiga tem sido feita por meio de cistoscopia, podendo ser suplementada, nalguns casos, pela citologia de amostra da urina ou do raspado da bexiga. Entretanto, no que diz respeito à monitorização, a citologia é um exame sensível para os tumores pouco diferenciados (alto grau) e pouco sensível para os bem diferenciados (baixo grau). Por esse motivo, têm-se procurado outros testes de maior sensibilidade que possam suplementar ou mesmo substituir os exames existentes.
46 O teste ideal para o diagnóstico e a monitorização de pacientes com carcinoma da bexiga deve ser rápido, de fácil realização, além de possuir sensibilidade e especificidade altas. Estudos recentes mostraram que a detecção do BTA (bladder tissue antigen) é significativamente mais sensível do que a citologia, não importando o estadio ou o grau do tumor da bexiga. O antigénio do tumor da bexiga reconhecido pelos anticorpos no teste BTA foi inicialmente isolado da urina de pacientes com neoplasia da bexiga confirmada histologicamente. Não é reconhecido na maioria dos indivíduos normais e em pessoas com outras patologias do aparelho urinário. A especificidade do teste mostrou-se equivalente à da citologia em indivíduos normais. Além de ser um teste não invasivo que utiliza como material apenas uma pequena amostra isolada de urina, estudos comprovaram que o BTA é significativamente mais sensível do que a citologia, sejam quais forem o estadio ou o grau do tumor. CA 125 O CA 125 é uma glicoproteína de alto peso molecular (>200 kd), de papel fisiológico ainda desconhecido, presente em diferentes condições benignas e malignas, sendo útil especialmente no acompanhamento dos carcinomas do ovário. A concentração sérica do CA 125 é superior a 35 U/mL em aproximadamente 80% das mulheres com carcinoma do ovário, 26% das mulheres com tumores benignos de ovário e em 66% de pacientes em condições não-neoplásicas, inclusive o primeiro trimestre da gravidez, fase folicular do ciclo menstrual, endometrioses, miomas uterinos, salpingites agudas, tuberculose pélvico-peritoneal, cirrose hepática, pancreatites e inflamações do peritoneu, do pericárdio e da pleura. Outros carcinomas não-ováricos podem elevar os níveis de CA 125 como os de endométrio, pâncreas, pulmão, mama e gastrointestinais. Sómente cerca de 3% das mulheres saudáveis têm concentração sérica de CA 125 acima de 35 U/mL, e apenas 0,8%, acima de 65 U/mL. Os níveis séricos correlacionam-se com o tamanho e o estadiamento do tumor. Em pacientes com carcinoma limitado ao ovário (estadio I), apenas 50% se apresentam positivas. Já 90% dos pacientes com carcinoma de ovário disseminado (estadios II, III e IV) apresentam concentrações séricas acima de 35 U/mL. A combinação da avaliação do CA 125 com o exame pélvico e a avaliação por ultrasom transvaginal aumenta a sensibilidade e a especificidade do exame como teste de triagem para o carcinoma do ovário. É útil também no diagnóstico diferencial de massas do ovário palpáveis. Quanto mais altos os níveis de CA 125, maior a probabilidade da sua associação ao carcinoma do foro ginecológico. O CA 125 é usado no acompanhamento dos carcinomas do ovário, na avaliação de lesões residuais, monitorização de recidivas e resposta à terapia. Na avaliação do aparecimento de metástases, tem a capacidade de detectar 75% dos casos. É útil também como marcador prognóstico. Um resultado negativo não exclui a presença da doença. Os valores diminuem em torno de 3 semanas após a conduta terapêutica. Os níveis
47 de CA 125 após a primeira etapa de quimioterapia ajudam a formulação do prognóstico. Pacientes com diminuição acima de 50% nas concentrações de CA 125 têm sobrevida de cerca de 2 anos em 45% dos casos, comparada com a previsão de 22% nos pacientes que apresentam diminuição do CA 125 inferior a 50%. Elevações acima de 60 U/mL, após o primeiro ciclo de quimioterapia, sugerem reincidência do tumor. CA 15-3 O antigénio CA 15-3 é uma glicoproteína presente no epitélio mamário, detectada em análises imunoenzimáticas utilizando-se anticorpos monoclonais específicos. Elevações das concentrações séricas do CA 15-3 podem ser encontradas em creca de 23% dos pacientes com carcinoma primário da mama e em cerca de 40 a 50% dos pacientes com metástases. Apenas 23% dos pacientes com doença precoce apresentam elevação da concentração do CA 15-3, e cerca de 16% dos pacientes com doença benigna da mama apresentam valores alterados. A sua utilização está indicada no acompanhamento da recorrência do carcinoma da mama, monitorização de metástases e também para monitorização da resposta à terapia. Os valores do CA 15-3 correlacionam-se com a extensão e o estágio da lesão. Entretanto, na prática, essa correlação é melhor observada na progressão do que na regressão. São encontrados percentadens de positividade com valores acima de 25 U/mL em 5% dos pacientes no estadio I, 29% no estadio II, 32% no estadio III e 95% no estadio IV. As pacientes que desenvolvem doença metastática têm aumento de CA 15-3, que pode preceder de 2 a 9 meses os sinais clínicos. As probabilidades de progressão são respectivamente 52%, 85% e 96% para 1, 3 e 6 meses após um teste positivo. A probabilidade de não-progressão após um teste negativo é de 91%. O CA 15-3 é mais sensível do que o CEA para monitorização de recidiva, e os dois marcadores devem ser utilizados em conjunto. Um aumento de 25% nos níveis séricos do CA 15-3 indica progressão do carcinoma em 95% dos pacientes. Uma diminuição de 25% dos níveis séricos do CA 15-3 está associada a resposta à terapia. Variações menores do que 25% são, frequentemente, associadas a doença estável. Uma elevação nos níveis de CA 15-3 pode acontecer nas primeiras semanas de tratamento e não deve ser confundida com falha terapêutica. Valores de CA 15-3 elevados correlacionam-se com a presença de metástase óssea, mas valores normais não excluem a possibilidade de sua existência. Utilizando-se como limite (cut-off) 26 U/mL, o CA 15-3 prediz recidivas em menor período de tempo do que os métodos radiológicos e os critérios clínicos. Como a maioria dos marcadores tumorais disponíveis, o CA 15-3 não pode ser utilizado como teste de rastreio na população em geral. Pode estar presente noutras patologias malignas do pâncreas, pulmão, ovário e fígado. Valores alterados podem ser encontrados numa pequena parcela da população hígida (2 a 5%), geralmente em concentrações baixas, bem próximas aos valores superiores de referência. Pacientes com condições benignas como hepatites crónicas, cirrose hepática, sarcoidose, tuberculose e lúpus eritematoso sistêmico podem apresentar concentrações séricas acima de 40 U/mL.
48 CA 19-9 O CA19-9, assim como o CA 242 e o CA 50, são marcadores tumorais de carcinoma colorrectal e pancreático. Estes três marcadores possuem um epítopo em comum, que os caracteriza como marcadores de carcinoma gastro-intestinal. O CA 19-9 (antígeno carboidrato 19-9) é uma glicoproteína do tipo mucina, de alto peso molecular (> 400 kd), que possui uma estrutura siálica originada do antigénio do grupo sanguíneo Lewis. Consequentemente, não se expressa nos indivíduos Le (a-, b-), levando a resultados falso-negativos em pessoas com esse perfil, aproximadamente 6% da população. É sintetizado normalmente pelas células dos ductos do pâncreas e da vesícula biliar humana e pelo epitélio gástrico, do cólon, endometrial e salivar. A concentração sérica do CA 19-9 encontra-se elevada em pacientes com carcinoma de pâncreas (80%), carcinoma hepatocelular (67%), carcinoma gástrico (40 a 50%) colorretal (30%) e alguns pacientes com carcinoma de mama (15%). Condições benignas como pancreatite e icterícia podem levar ao aumento dos níveis séricos (18%). A maioria dos pacientes com pancreatite tem valores séricos abaixo de 75 U/mL (96%). Os níveis séricos podem apresentar-se alterados também em pacientes com doenças como cirrose hepática, doenças intestinais inflamatórias e em condições auto-imunes como artrite reumatóide (33%), lúpus eritematoso sistémico (32%) e esclerodermia (33%). A baixa sensibilidade e especificidade e a falta de opções de tratamento impedem o uso de CA 19-9 como teste de triagem para carcinoma do pâncreas. Os níveis do CA 19-9 são úteis para avaliar a recidiva do tumor e a presença de metástases. A principal indicação para a utilização do CA 19-9 está na preparação para a conduta cirúrgica. Basicamente, todos os pacientes que apresentam valores séricos maiores do que U/mL têm um tumor maior que 5 centímetros de diâmetro, e apenas 5% dos pacientes desse grupo apresentam tumores ressecáveis. Porém, 50% dos pacientes pré-tratados com CA 19-9 abaixo de U/mL apresentam tumores ressecáveis. Outros estudos têm mostrado que a maioria dos pacientes com concentração maior do que 300 U/mL apresenta tumores irressecáveis. Apesar da sensibilidade diagnóstica do CA 19-9 para tumores do pâncreas ser maior do que a de outros marcadores, o diagnóstico precoce realizado por meio do seu uso tem sido bem limitado. Ou seja, a capacidade diagnóstica em casos iniciais é muito baixa. O CA-19-9 é utilizado na monitorização de carcinomas gastrointestinais, especialmente do pâncreas. É descrito como menos eficiente do que o CEA como marcador de carcinomas colorretais. O doseamento do CA 242 está indicada no acompanhamento de tumores pancreáticos e colorretais. Valores elevados de CA 242 são encontrados em 5 a 33% dos pacientes com doença benigna do cólon, estômago, fígado, pâncreas e vesícula biliar; 68 a 79% de pacientes com carcinoma do pâncreas; 55 a 85% de pacientes com carcinoma colorretal e 44% dos pacientes com carcinoma gástrico. O CA 242 é supostamente menos eficiente do que o CA 19-9 e o CA 50 na detecção do carcinoma pancreático. Níveis elevados de CA 50 são encontrados em até 46% das doenças benignas do
49 pâncreas, em 35 a 38% das patologias benignas do trato biliar e em 22 a 59% das patologias do fígado. Apresenta-se elevado entre 80 a 97% dos pacientes com carcinoma do pâncreas. No carcinoma do cólon, a frequência varia de 19% nos estadios mais iniciais até 73% nos estadios mais avançados. Este marcador encontra-se elevado no carcinoma de esófago (41 a 71%), estômago (41 a 78%), trato biliar (58 a 70%) e hepatocelular (14 a 78%). Cálcio No adulto, cerca de 98% do cálcio está localizado nos ossos, principalmente sob a forma de hidroxiapatita, uma rede composta por cálcio e fósforo. O restante, cerca de 2%, encontra-se no fluído extracelular e noutros tecidos, principalmente no músculo esquelético. O ião cálcio está entre os principais componentes minerais do organismo e desempenha um papel fundamental na mineralização óssea. Tem importância vital em vários processos fisiológicos, como o da coagulação sanguínea, a transmissão dos impulsos nervosos, a manutenção do mecanismo de contracção e relaxamento muscular esquelético e cardíaco, as activações enzimáticas, a regulação das glândulas endócrinas e exócrinas e a manutenção da integridade e da permeabilidade da membrana celular, principalmente em relação ao mecanismo de troca sódio /potássio. É absorvido de forma activa no duodeno e no jejuno superior. Cerca de 10 a 20% do cálcio consumido é absorvido. A absorção é estimulada principalmente pela vitamina D (estimula a absorção intestinal e a mineralização óssea), pelo meio ácido, pela hormona de crescimento e por uma dieta rica em proteínas. A relação cálcio/fósforo também é um factor importante na regulação da absorção. Coeficientes elevados levam à formação de complexos de fosfato de cálcio insolúveis. O ph alcalino, o teor de gordura do bolo alimentar e o cortisol inibem a absorção. A manutenção do equilíbrio dos níveis de cálcio no organismo envolve diferentes órgãos: intestino delgado, rins e esqueleto. Os seus níveis são regulados por diferentes hormonas: pela paratormona (que aumenta a reabsorção tubular e a mobilização do cálcio ósseo), por hormonas derivados do metabolismo da vitamina D3 e pela calcitonina (que actuam sobre a reabsorção óssea e nos túbulos renais). Outras hormonas que afectam o metabolismo do cálcio, mas que não têm a sua secreção alterada pelas alterações das concentracções do ião, são as hormonas tireoidéias, do crescimento, glicocorticóides adrenais e esteróides. Basicamente, os valores do cálcio dependem das taxas de absorção intestinal, reabsorção óssea e perda renal. Concentrações anormais do cálcio ósseo indicam distúrbios na função das glândulas paratiróides, doenças ósseas, neoplasias, síndrome de má absorção ou desnutrição, deficiência de vitamina D, excesso de antiácidos contendo cálcio e doenças renais. Actualmente, grande relevo tem sido dado à complementação de cálcio, especialmente nas mulheres após a menopausa, como meio de retardar ou evitar as manifestações de osteoporose. A excreção do cálcio dá-se principalmente por via urinária, e uma pequena parcela pela transpiração. A determinação do cálcio urinário é útil para o acompanhamento das terapias de reposição, nas investigações de litíase renal e no seguimento de patologias que envolvem o metabolismo do cálcio, como nas doenças ósseas primárias e metastáticas, intoxicação por vitamina D, hipercalciúrias idiopáticas,
50 sarcoidoise e doenças da paratiróide. O cálcio encontra-se no soro ou no plasma de três formas diferentes: 1. A forma fisiologicamente activa de cálcio livre e ionizado, que corresponde a 50% do cálcio total (difusível). 2. Em forma de complexos com outros iões, que correspondem a 5% do cálcio total (difusível). 3. Os 45% restantes, que se apresentam ligados a proteínas plasmáticas, especialmente à albumina (não-difusível). A distribuição dessas formas está directamente ligada ao ph do fluido extracelular e à concentração de proteínas. A acidose aumenta o cálcio ionizado, e a alcalose diminui a sua concentração. Já o aumento de proteínas leva a um aumento do cálcio ligado e também do cálcio total. O cálcio ionizado mantém os seus níveis fisiológicos, ou seja, a sua concentração é constante e independente do cálcio ligado. Portanto, a avaliação do cálcio ionizado é útil nalgumas situações clínicas, como distúrbios ácido-base, nos quais o cálcio ionizado está alterado sem que haja alteração do cálcio total. Esta situação pode ocorrer na hemodiálise, nas septicémias, mielomas, cirrose, transfusões, plasmaférese, distúrbios cardiovasculares, insuficiência renal e no diagnóstico do hiperparatiróidismo. Consultar Cálcio Ionizado. Cálcio Ionizado O cálcio é o quinto elemento mais comum no corpo humano. A distribuição desse elemento no corpo abrange três compartimentos: esqueleto (98%), tecidos moles e sangue (2%). No plasma, o cálcio está presente de três formas distintas: ligado à proteína, livre ou ionizado e formando complexos (principalmente com fosfato, bicarbonato e citrato). Aproximadamente 40% do cálcio plasmático está ligado de forma reversível às proteínas, e qualquer alteração na quantidade de proteína que se liga ao cálcio altera a quantidade de cálcio total. Cerca de 20% do cálcio ligado à proteína está ligado também à globulina. Em pacientes com mieloma múltiplo, a globulina em alta concentração pode ligar-se a uma grande quantidade de cálcio, provocando um aumento da quantidade de cálcio total. A quantidade de cálcio ionizado presente no plasma é de 50% do cálcio total. Apenas 10% do cálcio formam complexo com aniões. Além da concentração de proteína, o balanço ácido-base também pode afetar a fração ionizada. A alcalose causa redução na fracção de cálcio iónico circulante, e a acidose, aumento. Num estado de acidose crónica, por exemplo, os níveis séricos normais de cálcio total podem ocultar um aumento na concentração de cálcio ionizado. Portanto, os níveis séricos normais de cálcio ionizado são importantes na manutenção do metabolismo dependente de cálcio. O nível sérico de cálcio ionizado controla, por exemplo, a secreção de hormonas das paratiróides. Níveis baixos de cálcio ionizado estimulam a secreção de hormonas da paratiróide, e os níveis altos suprimem essa secreção. Finalmente, a determinação de cálcio ionizado é um indicador melhor do estado de cálcio plasmático do que o cálcio total, por ser metabolicamente activo e melhor regulado pelas hormonas reguladoras de cálcio
51 Cálculo Renal A análise físico-química do cálculo renal é de grande importância clínica na orientação preventiva da calculose. São avaliados os aspectos macroscópicos, como tamanho, cor, forma, consistência, além da análise bioquímica, na qual são identificados os elementos presentes. Os elementos frequentemente encontrados são oxalato de cálcio, ácido úrico, fosfato de magnésio e, mais raramente, cistina. TIPO DE CÁLCULO ÁCIDO ÚRICO CISTINA FOSFATO de MAGNÉSIO OXALATO OXALATO OU FOSFAFTO DE CALCIO CONDIÇÃO Hiperglicemia, Hiperparatiroidismo, Hipertiroidismo, Acidose tubular renal, etiologia desconhecida (comum), intoxicação por vitamina D Deficiência tubular renal Infecção por Proteus ssp e outras infecções das vias urinárias Anestesia com metaxiflurano, deficiência de vitamina B6 Gota, distúrbios linfoprolifarativos Capacidade Total de Fixação de Ferro A capacidade total de fixação do ferro sérico ou TIBC (Total Iron-Binding Capacity) representa uma estimativa aproximada de todas as proteínas transportadoras de ferro, em especial da transferrina. O teste consiste na adição de ferro em excesso ao soro, tentando a saturação das proteínas. A seguir, todo ferro excedente, nãoligado às proteínas é retirado, e logo após o ferro sérico é avaliado. Como a transferrina não é a única proteína fixadora de ferro, a avaliação da capacidade de fixação do ferro não representa exactamente a capacidade de fixação da transferrina. Entretanto, por ser a transferrina a maior proteína transportadora do ferro, a avaliação da capacidade total de fixação do ferro no soro representa de forma significativa a sua capacidade de ligação ao ferro. A anemia por deficiência de ferro é caracterizada por queda na concentração de ferro, aumento do TIBC e diminuição da saturação de transferrina. O TIBC do soro está aumentado na deficiência de ferro e diminuído na anemia por doenças crónicas. A redução da capacidade de fixação está associada à diminuição dos níveis séricos da transferrina. O inverso também acontece: níveis elevados de transferrina são seguidos pela elevação da capacidade de fixação do ferro. Na hepatite, ocorre um aumento da libertação da transferrina pela necrose do hepatócito, levando a um aumento da capacidade de combinação do ferro. CAPACIDADE TOTAL DE FIXAÇÃO DO FERRO AUMENTADA DIMINUÍDA Anemia ferropriva Síntese protéica diminuída Período da Infância Desnutrição grave Gravidez Neoplasias Hepatites e Insuficiência hepática Hemocromatose Anticontrceptivos orais Nefropatias
52 Carbamazepina É um fármaco antiepiléptico importante, utilizado no tratamento de crises convulsivas simples e complexas, parciais e generalizadas no adulto, e também no tratamento da nevralgia do trigémio, nevralgia glossofaringea e outras nevralgias como as neuropatias diabéticas. A carbamazepina é um composto tricíclico relacionado quimicamente com a imipramina (antidepressivo tricíclico). A acção antiepiléptica é diminuir o fluxo de sódio e de cálcio nos neurónios hiperexcitáveis. Uma redução da transmissão sináptica excitatória explicaria a sua acção sobre as nevralgias. A doseamento é importante para avaliar a eficácia do tratamento e impedir os efeitos tóxicos por meio da manutenção dos níveis séricos do range terapêutico. A concentração sérica terapêutica usual é de 4 a 12 mg/ml. Normalmente, alcançase um estado de estabilidade em 3 a 4 dias. Após a administração oral, a absorção é lenta e apresenta grandes variações individuais, atingindo o pico sérico em horas. A metabolização faz-se por via hepática, apresentando uma farmacocinética própria, com a capacidade de induzir as enzimas hepáticas responsáveis pela sua clearance (auto-indução). A clearance da carbamazepina aumenta com o tempo, e as enzimas estão completamente induzidas em cerca de 4 a 6 semanas, ocorrendo então o aumento da clearance e a consequente diminuição da semi-vida do fármaco, que cai de 25 a 40 horas para 15 a 25 horas, depois da auto-indução. Como o metabolismo é hepático, qualquer alteração da função hepática leva ao aumento da concentração sérica do fármaco. Cerca de 85% da carbamazepina está ligada às proteínas. A carbamazepina apresenta um metabolito activo que é potencialmente tóxico - a carbamazepina - 10,11 epóxido, que deve ser avaliado nos pacientes com sinais de intoxicação que apresentem níveis séricos normais da carbamazepina. Há a possibilidade de ocorrência de efeitos colaterais, como nistagmo, cefaléia, ataxia, visão dupla e, menos frequentemente, rash (erupção) cutâneo. Podem também ocorrer reacções hematológicas, sendo a mais comum a leucopenia. Em casos raros, regista-se a ocorrência de formas graves, como anemia aplástica, trombocitopenia e agranulocitose. Também podem surgir reacções de hipersensibilidade, incluindo síndrome de Steven Johnson, hiponatremia, especialmente em idosos, osteomalácia e efeitos sobre a condução cardíaca. O uso em mulheres no primeiro mês de gestação aumenta o risco de defeitos na formação do tubo neural. A carbamazepina aumenta o metabolismo do ácido valpróico, clonazepam, teofilina e warfarina. A sua concentração pode ser aumentada pelo uso concomitante de cimetidina, isoniazida, eritromicina, lítio, fluoxetina e ácido valpróico. Possui ainda um efeito antidiurético, reduzindo as concentrações da hormona antidiurética. Podem ser encontrados frequentemente níveis baixos, por falta de adesão ao tratamento. O uso de outras drogas anticonvulsivantes (politerapia) como fenobarbital, fenitoína e primidona pode diminuir a concentração sérica da carbamazepina sem levar a crises convulsivas. Normalmente, a colheita deve ser realizada em pacientes que estejam a fazer o medicamento há pelo menos 2 dias, e sempre cerca de 1 hora antes da próxima dose. Entretanto, nos casos de suspeita de intoxicação, pode ser realizada em
53 qualquer momento. Para facilitar a interpretação, é importante conhecer o horário da última dose ingerida. Ceruloplasmina A ceruloplasmina é uma glicoproteína produzida pelo fígado, responsável pelo transporte de 80 a 95% do cobre plasmático. É uma proteína de resposta de fase aguda, migrando na região alfa-2-globulina na electroforese das proteínas. Normalmente não é visível, mas apenas nas situações que levam a grandes elevações séricas. A sua principal utilização clínica é no diagnóstico diferencial entre várias doenças hepáticas e na doença de Wilson, que é classicamente acompanhada pela diminuição dos níveis séricos da ceruloplasmina. É uma doença autossómica recessiva, em que ocorre diminuição da capacidade de ligação do cobre à ceruloplasmina, resultando no aumento dos níveis de cobre livre no plasma e nos tecidos, especialmente fígado e cérebro. Outras patologias que levam a lesão hepática grave, desnutrição, síndrome nefrótica e enteropatias com perda de proteínas podem cursar com níveis diminuídos de ceruloplasmina. Níveis excessivos de zinco na dieta podem levar a um bloqueio da absorção intestinal de cobre, levando inicialmente a uma diminuição dos níveis de ceruloplasmina. O período necessário à eliminação do zinco supera o bloqueio à absorção do cobre, seguindo-se a um aumento do cobre sérico e da ceruloplasmina. Apresenta-se elevada em diferentes distúrbios que levam à reacção da fase aguda, como: carcinomas, leucemias, doença de Hodgkin, traumas, obstrução biliar, gravidez, intoxicação por cobre, uso de contraceptivos orais, fenitoína e terapia com estrogénios. Chlamydia O género Chlamydia compreende bactérias Gram-negativas desprovidas de motilidade, que se classificam nas espécies trachomatis, pneumoniae e psitacci. Incapazes de sintetizar o seu próprio DNA, são parasitas intracelulares obrigatórios de células eucarióticas, completando o seu ciclo de multiplicação em 48 a 72 horas. As espécies trachomatis e pneumoniae são reconhecidas como patogénios humanos, e a psitacci é reconhecida primariamente como patogénio animal. A psitacci infecta aves, bovinos e ovinos e pode desencadear em humanos uma doença respiratória por exposição ao material infeccioso (geralmente fezes de aves infectadas). A Chlamydia trachomatis possui 20 sorotipos diferentes já identificados. Os sorotipos L1,L2e L3 são responsáveis pelo síndrome linfogranulomatoso venéreo; os A, B, Ba e C são frequentemente associados ao tracoma, e os de D a K estão ligados a outras manifestações sexualmente transmitidas, sendo que os sorotipos D, E e F são os mais frequentes. A infecção por C. trachomatis pode perdurar por muitos anos de forma assintomática nos indivíduos infectados não-tratados. As infecções causadas por Chlamydia trachomatis incluem:
54 o Linfogranuloma venéreo - doença sistémica, sexualmente transmissível, causada por determinados serotipos da espécie; - o Tracoma - traduz-se por uma conjuntivite crónica que pode levar à cegueira. O contágio ocorre por transmissão directa, pessoa a pessoa; - as Infecções do trato genital - incluem cervicite, doenças inflamatórias pélvicas, uretrites, epididimite e proctite. Nos homens, cerca de 50% dos casos de uretrite não-gonocócica são causadas por Chlamydia trachomatis. Nas mulheres, 30% dos casos manifestam-se sob a forma de cervicite; porém, as infecções assintomáticas ocorrem em mais da metade dos casos e, em consequência, muitas não são detectadas; as Infecções neonatais - 60% das crianças nascidas de mães infectadas poderão contaminar-se no momento do parto, e 18 a 50% podem desenvolver a doença, nos primeiros dias de vida, uma conjuntivite; posteriormente, num período médio de 3 meses, em 3 a 15% poderá ocorrer uma pneumonia associada ou não à conjuntivite, com alteração do estado geral da criança. Cerca de 30% das pneumopatias em recém-nascidos são causadas por Chlamydia trachomatis. Nos homens, a C. Trachomatis é responsável por cerca de 50% dos casos de uretrite não-gonocócica e ainda por maior percentagem de uretrites pósgonocócicas. É a principal causa de epididimite em homens sexualmente activos acima dos 35 anos de idade. Nos casos assintomáticos, pode ser diagnosticada ao encontrar-se piúria ou queixa de disúria sem causa aparente. A infecção uretral é comum nas mulheres. Casos de piúrias sintomáticas ou assintomáticas sem causa aparente ou de cistites com cultura negativa são altamente sugestivos de uretrite por Chlamydia trachomatis. O endométrio é o órgão mais frequentemente infectado, e a maioria dos casos é assintomática. Além de causar uretrites, cervicites, endometrites e doença inflamatória pélvica nas mulheres, a infecção pode evoluir com complicações. As mais frequentes são a infertilidade (fibrose das trompas de Falópio), a gestação ectópica e, menos frequentemente, o chamado síndrome de Fitz-Hugh-Curtis (peri-hepatite). Estudos realizados entre estas pacientes com quadros de infertilidade por lesões tubáricas e gravidez ectópica demonstraram positividade três vezes maior para os anticorpos contra a C. trachomatis do que na população normal. As infecções do trato genital por Chlamydia trachomatis são consideradas as principais causas das doenças sexualmente transmissíveis na Europa e nos Estados Unidos, onde cerca de 3 a 4 milhões de casos são relatados por ano. Os índices de transmissão do agente patogénico, são superiores aos da gonorréia e da sífilis, e a sua ampla distribuição geográfica são preocupantes, justificando o uso de métodos diagnósticos sensíveis e rápidos para a sua identificação. Vários métodos estão disponíveis para a detecção de Chlamydia trachomatis em amostras de material biológico: coloração histológica, cultura de células, imunofluorescência e métodos imunoenzimáticos. Todos apresentam, porém, restrições de sensibilidade ou especificidade, ou exigem um tempo prolongado para a conclusão do diagnóstico. Até alguns anos, por apresentar alta especificidade, a cultura de células Maconkey era considerada o teste padrão para o diagnóstico da infecção por Chlamydia trachomatis. Apesar de sua alta especificidade, a cultura apresenta algumas restrições, como o longo tempo para obtenção do resultado e o facto de detectar apenas bactérias vivas. Portanto, o resultado pode ser prejudicado por situações
55 inadequadas de colheita, armazenamento e/ou transporte, o que diminui a sua sensibilidade em cerca de 70 a 80%. Outra técnica utilizada para a detecção de Chlamydia trachomatis era a imunofluorescência directa por anticorpos monoclonais específicos. Estsa técnica apresenta uma sensibilidade maior do que a cultura, tendo entretanto a desvantagem de apresentar reacções cruzadas, o que diminui a sua especificidade. Os métodos imunoenzimáticos ou de imunofluorescência indirecta para a pesquisa de anticorpos séricos, respectivamente, das classes IgG e IgM são menos sensíveis e menos específicos do que os métodos citados acima, além do facto de não permitirem a identificação das diferentes espécies do género Chlamydia nem serem capazes de detectar anticorpos anti-chlamydia pneumoniae. A reacção em cadeia da polimerase (PCR) é um método de especificidade e sensibilidade altas, que utiliza a amplificação do ácido nucléico da Chlamydia (DNAalvo), permitindo a sua detecção mesmo em concentrações ínfimas, da ordem de 1 a 10 microrganismos por mililitro de material biológico. Técnicas de PCR e de captura híbrida são os métodos de escolha para o diagnóstico da infecção por C. trachomatis. Podem ser realizadas em amostras endocervicais e uretrais colhidas com swabs, acondicionadas em tubos apropriados e também em amostras de urina (primeiro jacto). Devemos porém ressaltar que a metodologia de reacção em cadeia da polimerase pode se apresentar inconclusiva, especialmente na pesquisa em materiais endocervicais e uretrais. Isso ocorre em cerca de 5% dos casos analisados por PCR, pela presença de factores inibidores que interferem na reacção, inibindo a actividade enzimática. Ainda não se tem a certeza da origem desses inibidores. Acredita-se que se devam à presença de contaminantes bacterianos ou fúngicos. Citomegalovírus O citomegalovírus (CMV) é membro do grupo dos beta-herpesvírus. Hoje, é reconhecido como um patogénio que afecta todas as faixas etárias, tendo caráter endémico em todo o mundo e levando a graves lesões congénitas. A infecção pelo CMV causa um grande espectro de manifestações clínicas, variando de evoluções assintomáticas e infecções sublínicas a quadros de maior gravidade, dependendo da condição imunológica do paciente. Quando sintomática em pacientes imunocompetentes, geralmente evolui com um quadro semelhante ao de mononucleose, com febre, linfadenopatia, alterações hematológicas (leucopenia e trombocitopenia) e, muitas vezes, com sinais e sintomas hepáticos, pulmonares, gastrointestinais ou neurológicos. A transmissão pode dar-se por via transplacentária, respiratória, oral, venérea, por intermédio do aleitamento, de transplante de órgãos ou transfusão sanguínea. O antigénio pode ser detectado a partir da 4ª semana que se segue à infecção (período de incubação). Na fase aguda, o vírus pode ser identificado em diferentes secreções corporais. Os anticorpos da classe IgM aparecem logo no início da fase aguda, e os da classe IgG, uma semana mais tarde. Assim como no herpes simples e nos demais vírus do grupo herpes, a infecção pode permanecer latente por toda a vida ou evoluir com episódios de reactivação. Depois da primoinfecção, o vírus mantém-se de forma latente, com a virémia persistente
56 porém em níveis baixos. Os anticorpos desenvolvidos mantêm-se positivos por toda a vida (IgG). Em situações que levem à diminuição da condição imunológica, pode ocorrer a replicação viral com reactivação do quadro. A infecção pelo CMV apresenta maior significado clínico nas mulheres grávidas, em recém-nascidos (infecção congénita), nos imunossuprimidos, como os casos de pacientes transplantados, portadores de neoplasias, pós-operatório de cirurgia cardíaca, em curso de grandes agressões infecciosas e nos indivíduos com SIDA. Normalmente, em indivíduos saudáveis, há dificuldade de correlacionar a infecção por CMV ao episódio clínico da doença, pois a presença de anticorpos (IgG) específicos para CMV tem uma prevalência muito alta (>60% da população de adulto), e como já citado, as manifestações clínicas da infecção são muito variadas. Embora o isolamento do vírus seja ainda considerado o melhor, outras técnicas estão a ser desenvolvidas para a avaliação da virémia, que por ser intermitente, exige exame de amostras consecutivas para permitir um diagnóstico mais seguro. A colheita deve ser comparada entre amostra da fase aguda e da fase de convalescença. Isto quer dizer que devem ser colhidas com 10 a 14 dias de intervalo. A presença de anticorpos heterófilos e de factor reumatóide pode levar a resultados falso-positivos dos anticorpos IgM. Nos casos neonatais, a transferência transplacentária pode também induzir a falsa positividade. As pesquisas geralmente baseiam-se na presença de CMV (particularmente das inclusões virais). Aumentos significativos dos anticorpos IgG CMV específicos por IFI ou EIA sugerem, mas não comprovam, infecção aguda ou reactivação de uma infecção por CMV. Anticorpos de baixa avidez fazem a distinção entre a resposta imune primária e a reactivação da infecção por CMV (caracterizada por alta avidez de IgG). O teste de avidez de anticorpos é um procedimento laboratorial que permite estimar o período aproximado em que ocorreu a infecção.percentagens de avidez inferiores a 30% sugerem que a infecção ocorreu há menos de 2 meses. Percentagens superiores a 40% sugerem que a infecção ocorreu há mais de 3 meses e que os anticorpos IgM, caso presentes, são residuais e desprovidos de significado clínico.o achado de percentagens entre 30% e 40% é considerado indeterminado, já que não permite a definição do período provável da infecção. Quando a avaliação está a ser realizada em grávidas, o tempo de gestação deve ser considerado. Anticorpos IgM específicos para CMV podem ser detectados em adultos por Enzima imunoensaio (EIA), em ambas as infecções de CMV nas infecções primárias, em cerca de 93 a 100% dos casos, e nas infecções reactivadas, em aproximadamente 40% dos casos. Porém, a resposta de IgM pode estar reduzida ou ausente em pacientes imunocomprometidos com infecção activa. A maioria dos pacientes com SIDA (95%) já é seropositiva para CMV antes da infecção pelo HIV ser diagnosticada. Manifestações do sistema nervoso central e periférico causadas pela infecção por CMV são muito raras. Entretanto, nos casos de SIDA, comumente são diagnosticadas encefalites por CMV. Os índices dos anticorpos CMV podem ser usados para diferenciar síntese intratectal da infiltração da barreira hematoencefálica pelo CMV. Os métodos mais rápidos, sensíveis e específicos para diagnóstico de CMV são os de biologia molecular, a reacção em cadeia da polimerase (PCR) e a captura híbrida, especialmente em recém-nascidos infectados congenitamente, em amostras de medula óssea, análise de órgão sólidos para transplante, pacientes imunocomprometidos, indivíduos imunocompetentes com infecção activa e dadores de sangue. A evolução da PCR quantitativa para CMV tem monstrado que CMV DNA em líquor é mais elevado em pacientes com CMV relacionado à polirradiculopatia do
57 que nos que sofrem de encefalites, e que a quantificação do CMV pode ser útil na monitorização da terapia antiviral. Sendo assim, os métodos moleculares para a detecção do vírus são importantes aliados para identificar os pacientes com alto risco de desenvolvimento da doença. Neste sentido, a qualificação da carga viral para o CMV pela técnica de reações em cadeia de polimerase ou pela captura híbrida permite a definição da virémia e a monitorização da terapêutica. - Microscopia eletrónica do Citomegalovírus CK Total A creatinoquinase (CK), também chamada de creatina-fosfoquinase (CPK), é uma enzima com vasta distribuição tissular, que desempenha importante papel regulador no metabolismo intracelular dos tecidos contrácteis. Está presente principalmente no músculo estriado, no tecido cardíaco e no cérebro. Na electroforese, podem ser identificadas três isoenzimas, pela sua origem, e também de forma numérica, de acordo com a migração na eletroforese. A CK-BB - CK-1 - é a forma encontrada no cérebro; a CK-MB - CK-2 - é encontrada no miocárdio e a CK-MM - CK-3 - é encontrada no músculo estriado. A CK-MM está habitualmente presente no soro. AUMENTO CK - BB% CK - MB% CK - MM% MÚSCULO ESQUELÉTICO MIOCÁRIO CÉREBRO a 3 0 ESTÔMAGO, ÍLIO E CÓLON Também podem ser encontradas outras formas, ditas isoenzimas variantes. Não estão habitualmente presentes em indivíduos hígidos e não possuem tecido de origem determinada. As duas maiores variantes conhecidas são denominadas macro-ck, tipos 1 e 2. A macro-ck do tipo 1 é formada pela CK-BB, ou raramente pela CK-MB, que se liga a uma imunoglobulina G ou A (raramente) dando origem a macrocomplexos que correm electroforeticamente entre CK1 e CK2. É comum a sua presença em idosos, especialmente em mulheres. A do tipo 2 parece ser um complexo da CK mitocondrial, presente em pacientes que apresentam um quadro de metástases tumorais ou outras enfermidades de alta gravidade. Apesar de não serem doseadas, pois não existem ainda evidências de sua importância clínica, a sua presença poderá, em alguns casos, afectar a análise da CK-MB, interferindo no resultado final. A sua maior utilização está no diagnóstico das lesões e doenças do músculo
58 esquelético e no enfarte agudo do miocárdio. Encontra-se marcadamente elevada na distrofia muscular de Duchenne, com elevações que variam de 20 a 200 vezes o limite superior da normalidade, exercício físico intenso, polimiosite, dermatomiosites, miosites, miocardites, traumas musculares, injeções intramusculares recentes e após crises convulsivas. Valores muito elevados são encontrados também nas rabdomiólises, inclusive nas que têm como causa a intoxicação por uso de cocaína. Também pode encontrar-se elevada noutras situações, como acidente vascular cerebral, embolia, enfarte e edema pulmonar, após cardioversão com múltiplos choques, tosse grave, trabalho de parto, quadros de mixedema - hipotiroidismo, nas neoplasias da mama, próstata e trato gastrointestinal, e noutras neoplasias em estado avançado, no período pós-operatório imediato e na ingestão de grandes quantidades de bebidas alcóolicas. Os seus níveis séricos podem estar diminuídos em situações nas quais ocorra perda de massa muscular, nas hepatopatias alcoólicas, na gravidez ectópica, nas doenças do tecido conjuntivo, na artrite reumatóide, em pacientes idosos e acamados e na terapia com esteróides. O repouso nocturno diminui os níveis séricos de CK em 10 a 20%. No enfarte agudo do miocárdio (EAM), a CK total aumenta nas primeiras 4 a 6 horas após o início do quadro, apresentando um pico entre 18 a 24 horas e permanecendo alterada por 48 a 72 horas após o episódio. A CK total pode estar normal no período precoce pós-enfarte, quando a CK-MB já começa a elevar-se. Os valores da CK podem aumentar entre 3 a 20 vezes os valores normais, dependendo da localização e da extensão da área afectada. Os valores de referência para a CK total é bastante ampla, variando com a idade, estatura, actividade física e volume de massa muscular. No momento da interpretação do resultado, isto deve ser levado em conta, pois alguns pacientes podem ter, habitualmente, valores muito baixos, fazendo com que, nalguns casos, mesmo estando dentro dos limites superiores de referência, já represente uma elevação da CK total, na fase inicial do EAM. CK-MB Uma das isoenzimas da CK total, a CK-MB é considerada a análise de referência para comparação com outros marcadores de lesão miocárdica. Para o seu doseamento, utiliza-se um método no qual um anticorpo específico inibe a isoenzima MM e a fração restante corresponde basicamente à MB. O seu doseamento deve ser sempre acompanhado do doseamento de CK total. Para avaliar melhor os resultados obtidos, pode-se avaliar o índice obtido pela divisão de CK-MB/CK total x 100, que indica a percentagem de aumento da CK-MB em relação à CK total. Normalmente, a CK-MB representa 5 a 6% da CK total. Percentagens acima desses valores são indicativos de origem miocárdica e associados a doença. Índices superiores a 25% são raros, exigindo que se avaliem as interferências no método, tais como a presença de CK 1 e 2. É muito importante realizar a colheita de uma amostra de sangue logo no início dos sintomas, quando os valores ainda estarão normais. Dessa maneira, servirão como valores basais para estabelecer o ponto de partida da curva de acompanhamento.
59 The National Heart, Lung and Blood Institute recomenda a realização do doseamento da CK total e da CK-MB em períodos de 6 a 8 horas, durante as primeiras 24 horas após o episódio. Para estabelecer uma curva adequada de acompanhamento, outros autores recomendam a colheita das amostras numa sequência de horas, seguida de doseamentos seriados cada período de 6 a 8 horas. A evolução clássica da CK-MB durante a curva de dosagens seriadas é fundamental para o diagnóstico de enfarte do miocárdio. O aumento inicial ocorre entre 3 a 8 horas após o início dos sintomas, atingindo o seu pico entre 12 a 24 horas e declinando até a normalidade em 48 a 72 horas. Entretanto, o diagnóstico de doença miocárdica deve-se pautar por um conjunto de achados clínicos, alterações no electrocardiograma e dos marcadores bioquímicos cardíacos como CK, CK-MB, troponina, mioglobina, entre outros. Cerca de 10 a 15% dos pacientes - geralmente indivíduos com diminuição da massa muscular - evoluem com a CK-MB elevada mas com a CK total normal. Os valores encontrados no doseamento da CK-MB correlacionam-se com o tamanho da área enfartada. Entretanto, apesar de altamente sensível, o doseamento é incapaz de detectar pequenas áreas de necrose. Esta é a importância da realização de curvas evolutivas de mais de um marcador bioquímico para auxiliar o diagnóstico e o acompanhamento de possíveis complicações como o reenfarte. Algumas outras lesões da musculatura cardíaca que não o enfarte do miocárdio levam ao aumento dos níveis séricos da CK-MB, como as miocardites, cardiomiopatias, cirurgia cardíaca de revascularização, troca de válvulas e intervenções de defeitos congénitos. Outras condições que podem levar ao aumento da CK MB incluem dermatomiosite, distrofia muscular de Duchenne e a rabdomiólise. Nestes casos, os valores costumam elevar-se menos e não se comportam em curva crescente como no enfarte do miocárdio. Clearance da Creatinina A função renal normal depende da integridade de quatro aspectos da fisiologia renal: o fluxo sanguíneo, a filtração glomerular, a função tubular e a permeabilidade das vias urinárias. O rim tem como função básica a conservação de fluídos, ou, por outras palavras, a concentração da urina. Além dessa função básica, possui três importantes papéis, que são a depuração de substâncias tóxicas, a manutenção do equilíbrio hidroeletrolítico interno e a produção de hormonas. A função geral do rim pode ser avaliada pela clearance (depuração) renal de uma determinada substância. Por definição teórica, a clearance é o volume de plasma a partir do qual uma determinada substância pode ser totalmente depurada (eliminada) na urina numa determinada unidade de tempo. Esse processo depende da concentração sérica, da taxa de filtração glomerular e do fluxo plasmático renal. É calculado a partir dos valores sérico e urinário da substância e do volume urinário em 24 horas, sendo corrigido em relação à superfície corporal. A clearance de moléculas pequenas não-ligadas à proteína que são filtradas livremente pelos glomérulos, e não são secretadas ou reabsorvidas pelo sistema tubular, como a inulina, fornece uma avaliação fiel da taxa de filtração glomerular. Na prática, a clearance de creatinina é a escolhida para a avaliação da função renal.
60 A sua excreção não é influenciada pela dieta e é filtrada livremente pelos glomérulos. Entretanto, além da secreção glomerular, há também uma secreção tubular activa que é contrabalançada por um mecanismo de reabsorção tubular. Assim, é possível utilizar a clearance de creatinina para avaliar adequadamente a taxa de filtração glomerular, sendo um índice precoce da avaliação da função renal superior à avaliação sérica isolada dos níveis de uréia e de creatinina. Além de avaliar a função renal, são úteis também para o acompanhamento da evolução da lesão renal e da resposta a terapêuticas. A taxa de filtração glomerular é maior nos homens do que nas mulheres, já que os homens possuem uma massa renal maior. Durante a gravidez, a taxa de filtração aumenta em torno de 50%, retornando ao normal após o parto. Encontra-se diminuída nos recém-nascidos e nas crianças até 5 meses de idade, por uma imaturidade anatomofisiológica dos glomérulos. Os níveis da taxa de filtração glomerular começam a diminuir progressivamente a partir da meia-idade, em consequência da arterionefroesclerose, que leva à diminuição progressiva do número de glomérulos. A clearance estará diminuído quando aproximadamente 50% dos nefronios estiverem lesados, indicando comprometimento da filtração glomerular. A colheita de sangue deve ser realizada em jejum ao final da colheita da urina de 24 horas para a correlação dos níveis séricos e urinários. Clearance = Creatinina na urina (mg/dl) x Vol. (ml/min) / Creatinina no soro (mg/dl) Clearance Corrigida = Clearance x Factor (corrigida pela superfície corporal, calculada em função do peso e da altura). Cloro O cloro é o anião de maior concentração no meio extracelular e desempenha o principal papel na manutenção da neutralidade electroquímica do líquido extracelular, incluindo o plasma. A maior parte do cloro ingerido é absorvido, e o excesso é eliminado pelos rins. Existe uma discreta diminuição dos níveis séricos no período pós-prandial, por aumento da formação de ácido (HCl) pelas células parietais gástricas. Na maioria das vezes, a sua concentração é afectada pelas mesmas condições que afetam a concentração do sódio. O cloro sérico encontra-se aumentado na desidratação, nas perdas excessivas de bicarbonato por perdas gastrointestinais baixas, na acidose tubular renal, na insuficiência renal aguda, na alcalose respiratória, na excessiva reposição do íão por hidratação venosa ou alimentação parenteral, nas situações de hiperfunção adrenocortical, nalguns casos de hiperparatiroidismo primário e na intoxicação por salicilatos. O cloro sérico apresenta-se diminuído na hidratação acentuada, nas perdas excessivas de cloro por via gastrointestinal, na cetoacidose diabética, na acidose metabólica, nas nefropatias comperdas de sódio, no desvio do meio extracelular para o intracelular, como o que ocorre na acidose respiratória compensada e na alcalose metabólica. A hipocloremia é observada também na síndrome de Batten (defeito de reabsorção); na crise de addison e na secreção inapropriada da ADH - hormona antidiurética.
61 A determinação da concentração do cloro no suor é indicada na investigação da fibrose cística, onde se encontra aumentada. A excreção urinária está diminuída nas situações de grandes perdas gastrointestinais, diminuição da ingestão de sal na dieta, período de retenção prémenstrual, sudorese excessiva, hiperfunção adrenocortical, retenções hídricas, nos diferentes tipos de edema e na diabetes insipidus. A excreção urinária está aumentada nas situações de uso de diuréticos, aumento da ingestão de sal na dieta, diurese pós-menstrual, diurese maciça de qualquer etiologia, doença túbulo-intersticial, depleção de potássio e insuficiência adrenocortical. Colesterol Total É um esterol encontrado em todos os tecidos animais. Desempenha importantes funções fisiológicas, incluindo a síntese de ácidos biliares, vitamina D, hormonas esteróides e constituintes da dupla camada das membranas celulares. O colesterol está presente na parede intestinal, proveniente de três fontes: dieta, secreção biliar e intestinal e células. Alimentos de origem animal, em especial carne, gema de ovos, frutos do mar e lacticínios, aumentam a quantidade de colesterol na dieta. Praticamente todo o colesterol presente no intestino encontrase na forma livre, não-esterificado. Todo o colesterol esterificado proveniente da dieta é rapidamente hidrolisado pelas esterases secretadas pelo pâncreas no intestino delgado. Cerca de 30 a 60% do colesterol da dieta e do intestino são absorvidos. O colesterol total apresenta-se aumentado na hipercolesterolemia primária e secundariamente no síndrome nefrótico, no hipotiroidismo, na diabetes mellitus, na cirrose biliar primária e na hipoalbuminemia. Níveis baixos podem ser encontrados na desnutrição e no hipertiroidismo. A doença arterial coronária relaciona-se, em proporção direta e duplicada, com níveis de colesterol séricos. Diferentes estudos corroboram a hipótese de que cada 1% de redução dos níveis de colesterol está associado à queda de 2% de risco de doença arterial coronária. O doseamento isolado de colesterol necessita de jejum, visto que os valores de referência foram obtidos com jejum de 12 horas. Em pacientes que apresentem valores alterados em relação aos desejáveis para a idade, recomenda-se a validação com a repetição do doseamento dentro de um intervalo mínimo de 7 dias e máximo de 2 meses. Têm sido observadas variações sazonais do colesterol. Por exemplo, níveis séricos são mais elevados no outono e no inverno e mais baixos no verão e na primavera. Alguns factores podem interferir, como a postura antes e durante a colheita, stres e ciclo menstrual. Consultar Perfil Lipídico.
62 Colinesterase É uma enzima cujo papel fundamental é a regulação dos impulsos nervosos através da degradação da acetilcolina na junção neuromuscular e na sinapse nervosa. Existem duas categorias de colinesterases: a acetilcolinesterase (colinesterase verdadeira), que é encontrada nos eritrócitos, no pulmão e no tecido nervoso; e a colinesterase sérica, sintetizada no fígado, também chamada de pseudocolinesterase. A sua determinação é útil na avaliação e no acompanhamento de pacientes com intoxicação por organofosforados (inseticidas) que inibem a colinesterase eritrocitária e diminuem os níveis da colinesterase sérica. A colinesterase sérica está diminuída nas doenças parenquimatosas hepáticas (hepatites virícas, cirrose), na insuficiência cardíaca congestiva, nos abscessos e neoplasias. Os níveis baixos persistentes nos cirróticos têm sido apontados como marcador de mau prognóstico. Valores diminuídos também são encontrados em estados de desnutrição, infecções agudas, anemias, enfarte do miocárdio e dermatomiosite. Diversas drogas como estrogénios, testosterona e contraceptivos orais também podem interferir nos níveis da colinesterase sérica. A colinesterase pode estar aumentada em pacientes obesos, em diabéticos e no síndrome nefrótico. Contagem de Addis A contagem de Addis é realizada em amostras de urina de 12 ou 24 horas e permite caracterizar valores mais precisos dos elementos anormais presentes na urina, como aumento de eritrócitos e leucócitos e aumento das taxas de excreção de cilindros, que podem surgir em quantidades pequenas demais para serem detectadas numa amostra de urina aleatória de um exame de rotina. A contagem é realizada no sedimento por meio de leitura microscópica em câmara de Neubauer. É útil quando há suspeita de glomerulonefrite subclínica. São encontrados valores elevados principalmente nos quadros de hematúria e nas glomerulonefrites, em que apresentam um papel prognóstico. Coombs Directa O teste de Coombs directa é um exame que permite a identificação da presença de anticorpos fixados sobre as hemácias. Técnicamente, baseia-se no facto de que os anticorpos que recobrem as hemácias podem ser identificados pela adição de anticorpos antigamaglobulina humana. Quando positivo, ou seja, quando indica a presença de anticorpos aderidos às hemácias, formam-se pontes entre elas, levando ao fenómeno visível de aglutinação. O teste de Coombs contribui directamente para o diagnóstico da anemia autoimune, pois a sua positividade confirma que o anticorpo foi fixado in vivo à hemácia do paciente, auxiliando dessa forma o diagnóstico diferencial com outras anemias hemolíticas, como as causadas por alterações da hemoglobina ou da estrutura da hemácia. É importante também no diagnóstico das anemias hemolíticas do recémnascido e das anemias induzidas por drogas.
63 Embora o teste de Coombs seja extremamente sensível, um resultado negativo não exclui a presença de anticorpos ligados às hemácias. Coombs Indirecta O teste de Coombs indirecta permite a identificação de anticorpos antieritrocitários no soro. É importante para a avaliação de grávidas Rh (-) (avaliação de sensibilização), em pacientes com Rh (-) para avaliação da variante Du e nas fases pré-transfusionais, especialmente em pacientes já transfundidos, em que pode ter ocorrido sensibilização para Rh e outros sistemas. O teste indirecto identifica in vitro diferentes anticorpos, de acordo com a fase do teste que apresentou positividade. O teste é realizado em quatro diferentes etapas, conhecidas como: fase fria (à temperatura ambiente) - geralmente anticorpos da classe IgM; fase em meio protéico - identifica os anticorpos IgM e também anticorpos incompletos (da classe IgG); fase quente (à temperatura de 37 C) - detecta anticorpos que só reagem a essa temperatura (geralmente IgG); e a última etapa, que identifica aglutininas da classe IgG e anticorpos que fixam o complemento. A ocorrência de aglutinação e/ou de hemólise durante quaisquer das etapas indica a possibilidade da presença de anticorpos irregulares. Creatinina A creatinina não é formada pelo metabolismo corporal, sendo apenas um resultado do metabolismo da creatina e, portanto, relacionada com a massa muscular. A conversão da creatina em creatinina é praticamente constante, sendo que cerca de 2% da creatina total é convertida em creatinina em cada 24 horas. A concentração sérica em indivíduos normais é praticamente constante, apresentando uma variação em relação ao sexo e ao volume de massa muscular, sendo portanto maior nos homens e nos atletas do que nas mulheres, nas crianças e nos idosos. Normalmente, a sua excreção não é afectada pela dieta e pela velocidade do fluxo urinário. Os níveis séricos aumentam à medida que ocorre a diminuição da taxa de filtração glomerular. Por isso, é utilizada como marcador da função renal. Os aumentos tornam-se significativos quando existe uma perda de mais de 50% dos nefrónios funcionantes, com diminuição expressiva da filtração glomerular. Níveis séricos diminuídos podem ser encontrados em crianças e em condições em que ocorra uma redução significativa da massa muscular. A creatinina é filtrada livremente pelos glomérulos. Além da filtração glomerular, há também uma secreção tubular activa contrabalançada por um mecanismo de reabsorção tubular. Na doença renal, à medida que a taxa de filtração glomerular diminui, a secreção tubular activa conduz a uma proporção maior no volume de creatinina excretada pela urina, tornando a utilização da clearance para avaliação da taxa de filtração glomerular uma ferramenta menos precisa. Uma outra variável que deve ser levada em conta aquando da avaliação da clearance da creatinina é o uso de fármacos que possam interferir com a secreção tubular, como os salicilatos, a cimetidina e a espirinolactona, entre outros.
64 Crescimeto A hormona de crescimento é sintetizado pela hipófise anterior. É estimulada pela GHRH (growth hormone - releasing hormone) e é inibida pelo GHIH (growth hormone - inhibiting hormone) secretadas pelo hipotálamo. Actua em inúmeros tecidos, como tecido mole, cartilagem e osso. A principal acção é promover a síntese protéica e, consequentemente, o crescimento desses tecidos. Também mobiliza gordura do tecido adiposo, aumenta a absorção intestinal de cálcio, estimula a glicogenólise hepática e antagoniza os efeitos da insulina. Estas duas últimas acções resultam num aumento da glicemia. A GH induz à síntese hepática de somatomedinas (ou IGFs - insulin - like growth factors), que são os mediadores da acção da GH na cartilagem e no osso. A hipersecreção de GH deve-se a adenomas hipofisários, e os seus efeitos dependem da idade do paciente. Quando ocorre antes do fecho das epífises dos ossos longos, acarreta o crescimento desproporcional (gigantismo); quando ocorre depois, leva a um aumento de ossos da face e das extremidades (acromegalia), como também a um aumento de cartilagem e de tecidos moles. O diagnóstico laboratorial da hipersecreção de GH requer a utilização de provas funcionais, como o teste de supressão de GH com glicose para comprovação da não-supressibilidade normal dessa hormona pela glicose. O doseamento basal de GH é pouco útil nesse diagnóstico, em virtude de, nessa patologia, a secreção de GH ser episódica. A análise de IGF-I é um exame alternativo que tem melhor correlação com a actividade clínica da doença do que o doseamento de GH. O doseamento seriado dos dois é bastante útil na avaliação da eficácia terapêutica. A prolactina pode estar elevada em 30% dos casos, devido à hipersecreção do adenoma hipofisário. Portanto, os seus níveis séricos também devem ser avaliados. A deficiência de GH em crianças resulta na baixa estatura (nanismo hipofisário), definida como altura abaixo do terceiro percentil. Cursa com diminuição da velocidade de crescimento e atraso da idade óssea. Pode ser consequente a doença hipofisária primária ou a disfunção hipotalámica. A falência hipofisária primária resulta de doenças genéticas (hipoplasia hipofisária, aplasia hipofisária, hipopituitarismo familiar e deficiência familiar isolada de GH), trauma, tumores, doenças granulomatosas, radioterapia do sistema nervoso central. A maioria dos casos de deficiência de GH é de origem hipotalámica (traumas do parto, tumores ou infecções). O diagnóstico laboratorial da deficiência de GH requer a realização de provas de estimulação, uma vez que os níveis de GH são geralmente baixos em estado basal. Antes da realização dos testes de estimulação, é necessário investigar se o paciente é eutiroidéio, uma vez que o hipotiroidismo causa uma resposta abaixo do normal do GH ao estímulo. Os estímulos farmacológicos mais comuns são: clonidina, piridostigmina (mestinon) e insulina. O teste com insulina precisa ser cuidadosamente acompanhado com doseamentos de glicemia capilar, devido ao risco de hipoglicemia grave. Devido à possibilidade de ocorrência de resultados falso-negativos, geralmente são realizados dois testes, com estímulos diferentes. Crianças com deficiência discreta podem responder normalmente ao estímulo farmacológico. A dosagem de IGF-I
65 deve apoiar o diagnóstico, uma vez que níveis normais reduzem a possibilidade de deficiência de GH. GH (Hormona do Crescimento) Indicado no diagnóstico e no acompanhamento da acromegalia e do gigantismo, embora valores basais moderadamente elevados não confirmem o diagnóstico, que necessita de comprovação com provas funcionais. Na avaliação do déficite de crescimento, os testes de estimulação são fundamentais, pois níveis basais baixos ou indetectáveis não são úteis para o diagnóstico. A alimentação, o exercício e o stres de qualquer origem podem interferir nos resultados. IGFBP3 (Proteína Carregadora das IGFS) Entre as várias IGFBPs (IGF - binding proteins) descritas, a IGFBP3 é a principal proteína carregadora dos factores de crescimento insulina-like. Os níveis dependem do GH, e a IGFBP3 deve ser avaliada junto com a IGF1. Somatomedina C ou IGF1 (Insulin - Like Growth Factor I) É útil no diagnóstico e no seguimento dos pacientes com hipersomatotropismo (acromegalia e gigantismo), no acompanhamento de pacientes em tratamento com GH exógeno e no diagnóstico da deficiência da hormona de crescimento. A sua interpretação deve levar em consideração mais a idade óssea do que a idade cronológica. Crioglutininas As crioaglutininas são anticorpos capazes de aglutinar hemácias humanas. Acreditase que sejam formadas após exposição a microrganismos que apresentam grupos antigénicos semelhantes aos encontrados nas hemácias. Esses anticorpos necessitam da presença de complemento para a sua reacção. Aparecem na população normal em títulos até 1/32. Em condições normais, exigem refrigeração para que ocorra a reacção com as hemácias. Estas crioaglutininas apresentam-se elevadas em diferentes situações, como nas infecções por Mycoplasma pneumoniae, influenza, mononucleose infecciosa, doenças do colagénio, artrite reumatóide e linfomas. Quando em títulos altos, podem raramente, aglutinar hemácias em temperaturas próximas às do corpo humano, podendo levar à anemia hemolítica. A presença das crioaglutininas pode interferir na avaliação do grupo sanguíneo, na prova cruzada para transfusões, em análises hematológicas e em reacções imunológicas. A prova da crioaglutinina é utilizada para o diagnóstico de infecções pelo Mycoplasma pneumoniae. Não é específica, porém apresenta-se positiva em 34 a 68% dos pacientes com a infecção. Títulos iguais ou maiores do que 1/128, na presença de quadro clínico compatível, podem confirmar o diagnóstico. Em casos duvidosos, recomenda-se um segundo doseamento, após 10 a 15 dias. Crioglobulinas As crioglobulinas são imunoglobulinas que têm a característica de se precipitar em
66 temperaturas abaixo de 37º C (4º a 30º C). As crioglobulinas são classificadas em três tipos principais, de acordo com a sua composição, em tipos I, II e III. O mecanismo pelo qual são produzidas é ainda desconhecido. Quando presentes, os tipos I e II não apresentam sintomas clínicos importantes. Já o tipo III, composto pela associação entre crioglobulinas, cursa com manifestações importantes como fenômeno de Raynaud, artralgias, necrose de pele, púrpura vascular, petéquias e nefropatia. Nos três tipos de crioglobulinemia, é descrita a presença de neuropatia periférica e de concentração sérica de complemento diminuídas, especialmente de C3 e C4, (com maior frequência no tipo III). As doenças associadas incluem doenças virícas, bacterianas e parasitárias, lúpus eritematoso sistémico, poliartrite nodosa, síndrome de Sjögren, outras manifestações auto-imunes, desordens linfoproliferativas e hepatite C. Cryptococcus Neoformans A presença do antigénio capsular polissacarídico do Criptococcus neoformans é pesquisada por intermédio da aglutinação em látex, em amostras de soro e/ou líquor. O antigénio criptocóccico está presente em 87% dos soros e em 99% dos liquores de pacientes com Criptococose. É de grande importância no diagnóstico da criptococose sistémica. O método apresenta algumas limitações, como a reacção cruzada com antigénio de Trichosporum beigelii e a presença de interferência não-específica, resultante da presença de imunoglobulinas geradas por outras patologias como no caso da artrite reumatóide. Cultura de Anaeróbios Os materiais clínicos adequados para a realização da cultura de bactérias anaeróbias devem provir das cavidades fechadas do nosso organismo (coleções líquidas, abcessos, sangue e liquídos biológicos em geral) ou seja, locais estéreis, sem a presença da flora normal. As bactérias anaeróbias causam uma variedade de infecções humanas, incluindo peritonite, empiema, endocardite e artrite. As infecções anaeróbias são, geralmente, de fonte endógena, representada pela própria flora normal. Entretanto, apesar da grande variedade de anaeróbios da flora normal, as infecções são limitadas a uma pequena quantidade de microrganismos, na qual se destacam o isolamento do género Bacteroides spp. Estreptococcus spp., Prevotella spp. e Clostridium perfringens. Os materiais devem ser colhidos e inoculados em frascos anaeróbios de hemocultura, até ao volume máximo permitido, que é de 8 ml. Quando o material for sangue e liquídos biológicos, pode ser armazenado por um período de até 24 horas, à temperatura ambiente, em frascos anaeróbios. Não poderão ser utilizados para pesquisar microrganismos anaeróbios materiais
67 provenientes de locais que normalmente participem da flora normal ou transportados inadequadamente. Cultura de Fezes A coprocultura auxilia o clínico no diagnóstico da etiologia de diarréias bacterianas, por meio do isolamento de patogénios entéricos. As gastroenterites podem ser causadas por bactérias, vírus ou parasitas. Quando é solicitada uma rotina de coprocultura, são procurados os agentes etiológicos mais frequentes, tais como Shigella spp., Salmonela spp. e Escherichia coli enteropatogénica. A E. coli enteropatogénica é pesquisada nos casos de diarréias em crianças de até 4 anos de idade. A E.coli invasora é pesquisada em todas as faixas etárias. A sua toxicidade é dada pela toxina que produz, a qual penetra na mucosa intestinal, provocando diarréia aguda. Em casos mais específicos, como as pesquisas de Campylobacter spp. e Yersinia spp., o pedido médico deverá ser direcionado. Outros patogénios, como Aeromonas spp. e Plesiomonas spp., podem também ser isolados. Cabe lembrar que algumas espécies de Campylobacter spp. não crescem nas condições padronizadas para coprocultura. O crescimento abundante de germes como Pseudomonas aeruginosa, Candida spp., Staphylococcus aureus, entre outros, pode indicar pacientes tratados com antibióticos de amplo espectro. Apesar de seu papel ainda não estar claramente definido, sua presença é comunicada ao médico, indicando o seu predomínio. A cultura deve ser realizada de preferência a partir de fezes frescas. Caso não seja possível, pode-se enviar swab anal em gel de transporte ou fezes colhidas em meio de transporte (tampão glicerol). Para a pesquisa de Campylobacter spp., são adequadas apenas fezes frescas ou colhidas em gel de transporte. Os swabs com meio de transporte e as fezes conservadas em tampão glicerinado podem ser armazenados à temperatura ambiente até 24 horas. Cultura de Materiais do Aparelho Génito-Urinário Importante no diagnóstico laboratorial das uretrites, vaginites, endocervicites, doenças sexualmente transmitidas e agentes bacterianos associados às infecções do aparelho genital. Secreção uretral, vaginal, urina do 1º jacto, esperma, secreção endometrial, fundode-saco uterino e secreção prostática são consideradas amostras clínicas apropriadas. As amostras clínicas colhidas com meio de transporte podem ser armazenadas até 24 horas à temperatura ambiente. As urinas e swabs colhidos sem meio de transporte devem ser processados até 2 horas. São considerados como crescimento patológico: Neisseria gonorrheiae, Estreptococcus agalactiae, Haemophilus spp., Corynebacterium spp. e enterobactérias. A presença de Corynebacterium spp. e de enterobactérias é valorizada, principalmente em crianças, mas também em adultos, quando presentes em grandes quantidades e a critério do médico.
68 Cultura de Materiais do Aparelho Respiratório Inferior Embora as infecções do aparelho respiratório inferior estejam entre as causas de maior morbilidade e mortalidade dos pacientes, o diagnóstico dessas infecções é frequentemente complicado pela contaminação da espécie clínica com a flora normal. A expectoração é submetida inicialmente a culturas, a fim de determinar o agente etiológico das pneumonias. O material recebido no laboratório pode ser expectoração, expectorada e/ou induzida. Outros materiais clínicos incluindo aspirado traqueal, aspirado transtraqueal, lavado bronquico e lavado broncoalveolar protegido e não-protegido. A expectoração deve ser observada ao microscópio, para se avaliar a qualidade da amostra e se é representativa do aparelho respiratório inferior, ou se contém apenas saliva. O lavado broncoalveolar é obtido por meio de procedimentos invasivos, sendo recomendado na suspeita de pneumonias nasocomiais em pacientes com ventilação mecânica. Os resultados da cultura de expectoração são interpretados com base na avaliação da coloração de Gram preparada a partir da porção mais purulenta da amostra: se contém mais de 25 polimorfonucleares/campo ou até 10 células epiteliais/campo, observado através de objetiva de 10 vezes, o material é considerado satisfatório. A informação mais simples envolve a quantificação de um volume maior ou igual a 10 células epiteliais, com a objetiva de 40 vezes, o que seria inaceitável para a cultura. Nas culturas quantitativas, o volume do lavado broncoalveolar protegido colhido frequentemente é de 0,01 ml a 0,001mL de secreção. A contagem de 10 3 UFC/mL de um microrganismo corresponde a infecção. Para o lavado broncoalveolar (LBA), a contagem de UFC/mL ou mais de um microrganismo específico correlaciona-se com pneumonia. No lavado bronquico e no aspirado traqueal, a contagem de 10 6 colónias, ou seja, UFC/mL, sugere um processo infeccioso. Os microrganismos mais frequentemente isolados correspondem aos grupos dos bastonetes gram-negativos não-fermentadores ou entéricos, os estafilococos e enterococos. São eles: Staphylococcus aureus, Streptococcus pneumoniae, Streptococcus pyogenes, Enterococcus spp., Haemophilus influenza, Moraxella catarrhalis, Pseudomonas aeruginosa, Klebsiella pneumoniae e Rhodococcus equi. Cultura de Materiais do Aparelho Respiratório Superior Inclui as culturas de secreções da orofaringe, nasofaringe, ocular e do ouvido. Auxilia os clínicos no diagnóstico das faringites bacterianas. A causa mais comum de faringite é representada pelo Streptococcus pyogenes. Em 7% dos casos, as secreções da nasofaringe são úteis no diagnóstico de sinusites infecciosas e na detecção de portadores nasais de germes como Staphylococcus aureus MRSA (estafilococos aureus resistentes à meticilina) e Neisseria meningitidis. No caso da epiglotite, que têm evolução rápida e progressiva com celulite, apresentam um grande potencial de obstrução das vias
69 respiratórias, e os seus agentes etiológicos são Haemophilus influenzae, Streptococcus pneumoniae e Staphylococcus aureus. Nas secreções oculares e ouvido, por possuírem a mesma mucosa de revestimento do aparelho respiratório superior, são isolados os mesmos agentes e diagnosticadas conjuntivites purulentas e otites. Estas infecções são mais comuns na infância e na terceira idade. Para as culturas da orofaringe, os resultados reportados são a presença do crescimento de estreptococos beta-hemolíticos, Streptococcus pyogenes, outros não-pyogenes e a ausência de estreptococos beta-hemolítico. Nas secreções nasais, procura-se evidenciar a presença de Staphylococcus aureus, Streptococcus pneumoniae e Haemophilus influenzae. Nas secreções conjuntivais, a presença do crescimento bacteriano é avaliada, juntamente com os dados clínicos, a presença de cirurgias ou próteses. Os estafilococos coagulase-negativo e os bastonetes gram-negativos são os mais frequentemente isolados, juntamente com Staphylococcus aureus, Streptococcus pneumoniae e Haemophilus spp. No diagnóstico das otites médias e externas, são utilizados secreções ou fluidos do ouvido. As bactérias mais comunns são Pseudomonas spp. e outros microrganismos provenientes da microflora respiratória. Cultura de Micobactérias A realização da cultura de micobactérias utiliza como princípio biológico a detecção radiométrica do CO2 produzido pela actividade metabólica das micobactérias a partir de meios de cultura específicos marcados com C 14. É destinada ao diagnóstico da tuberculose e das micobacterioses. Pode ser realizada em expectoração, lavado bronquico, lavado broncoalveolar, líquido ascítico, líquido pleural, líquido peritoneal, líquido cefalorraquidiano, aspirado de medula óssea, sangue, fezes, biópsias e urina. O uso de antituberculostáticos, e a presença de micobactérias não-adaptadas ao crescimento em meio líquido ou à temperatura de 35ºC podem induzir a um resultado falso-negativo. Cultura de Outros Líquidos Biológicos A cultura dos líquidos biológicos é utilizada para determinar a presença de agentes infecciosos nos líquidos pleural, sinovial, ascítico e pericárdio, auxiliando no diagnóstico etiológico de infecções como as pneumonias com derrame pleural, pericardites e sinovites. Os fluidos biológicos normalmente são estéreis, e a presença de um microrganismo resulta quase sempre num agravamento do quadro clínico desses pacientes. O uso de próteses e a terapêutica com imunossupressores têm contribuído muito para o aumento da prevalência de positividade dessas amostras. As principais bactérias isoladas incluem Neisseria spp., Streptococcus pneumoniae, Streptococos betahemolíticos e Staphylococcus aureus, podendo também ser isolados bastonetes gram-negativos. A presença de crescimento bacteriano de qualquer microrganismo após a incubação é considerada patogénica, uma vez que esses líquidos são estéreis. Um número
70 pequeno de microrganismos na amostra enviada pode levar a um resultado falsonegativo. Os líquidos biológicos destinados a cultura devem ser transportados ao laboratório para sementeira em 2 horas após a colheita. Se esse tempo não puder ser respeitado, inocular até o volume de 8 ml num frasco de hemocultura aeróbio ou anaeróbio e enviar ao laboratório. Cultura de Secreções, Abcessos, Tecido Subcutâneo, Fragmento de Tecidos e Biópsias Microrganismos residentes na pele e nas mucosas humanas, assim como no ambiente, podem causar infecções quando inoculados em tecidos normalmente estéreis ou em mucosas íntegras. Nem sempre é necessário existirem mecanismos de virulência para o microrganismo causar a doença. O material de biópsia enviado ao laboratório com mais frequência são os de linfonodos, pulmão, fígado, fragmentos de tecidos obtidos por laparoscopia, fragmentos ósseos, secreções de ferida cirúrgica, furúnculos e punção de abscessos. A cultura desses espécimes permite diagnosticar as infecções dos tecidos cutâneos e subcutâneos e de órgãos mais profundos, tais como abscessos intra-abdominais (incluindo as diverticulites), abscessos peritonsilares, cutâneos e esplênicos, impetigo, foliculite, furúnculos, celulite, fasciite, erisipela e osteomielite. Permite também obter a sensibilidade do microrganismo isolado aos antimicrobianos. O material pode ser proveniente de secreções de pele, bolhosa, de impetigo, de abscessos em geral, ferida cirúrgica, punção de agulha fina de órgãos e fragmentos de tecidos. Os tecidos obtidos durante procedimento cirúrgico são os melhores espécimes, já que os microrganismos são os agentes etiológicos da infecção. Os materiais obtidos dessa forma devem ser enviados em frasco estéril contendo água estéril, soro fisiológico ou lactato de ringer. Normalmente, a flora normal não interfere com esta colheita de material. Em secreções purulentas e abscessos a colheita deve ser feita por aspiração com seringa. AUMENTO DA FORMAÇÃO DIMINUIÇÃO DA SECREÇÃO IMPETIGO Staphylococcus aureus, Staphylococcus pyogenes FOLICULITES Staphylococcus aureus FURÚNCULOS Staphylococcus aureus ERISIPELA Staphylococcus pyogenes CELULITES Staphylococcus pyogenes, Staphylococcus aureus, Esterobactérias, Aeromonas spp, Clostridium spp, Mycobacterium spp FASCIITE Staphylococcus pyogenes, ou infecções sinérgicas por bactérias facultativas e anaeróbias ABCESSOS Staphylococcus aureus, Propionebacterium spp. CUTÂNEOS ABCESSOS Staphylococcus aureus, Staphylococcus spp, Propionebacterium spp. PERINEAL, VULVOVAGINAL, ESCROTAL MIOSITES Staphylococcus aureus, Staphylococcus spp.
71 AUMENTO DA FORMAÇÃO DIMINUIÇÃO DA SECREÇÃO OSTEOMIELITES Staphylococcus aureus, Staphylococcus pyogenes, Streptococcus agalactiae, Candida spp., Pseudomonas aeruginosas, Pamonella spp INSUFICIÊNCIA Enterobactérias, Bactérias anaeróbias. VASCULAR TRAUMA Staphylococcus spp, Propionebacterium spp, Pseudomonas ssp, ASSOCIADO Staphylococcus aureus e Enterobactérias. Cultura de Urina Auxilia o clínico no diagnóstico das infecções urinárias. As urinas submetidas a cultura são provenientes de pacientes com sintomas ou algum factor de risco para o desenvolvimento de infecção urinária. As infecções do aparelho urinário têm frequentemente como agentes etiológicos, bactérias com características de crescimento rápido, como Escherichia coli, Enterococcus faecalis, Klebsiella pneumoniae, Enterobacter cloacae, Proteus mirabilis, Pseudomonas spp. e Staphylococcus saprophyticus, representando a maioria dos isolamentos em pacientes hospitalizados, assim como da comunidade. As culturas negativas são identificadas como ausência de crescimento bacteriano. As prováveis contaminações são definidas como difteróides, estreptococos alfahemolíticos, lactobacilos, Estafilococos Coagulase-Negativa, ou crescimento de três microrganismos diferentes. As culturas são consideradas positivas quando a contagem de colônias for igual ou superior a 10 5 UFC, com isolamento de um único agente etiológico, ou na presença de dois microrganismos, quando houver indicação clínica, ou ainda com contagens inferiores a 10 5 com o isolamento de um único microrganismo associado a um dado clínico e/ou laboratorial. Deve-se colher o 2º jacto urinário após higiene da genitália externa. Em crianças, que não controlam a micção, fazer a higiene e colocar o saco colector adesivo, que deve ser trocado a cada 30 minutos quando não tiver sido possível colher a urina. A urina do paciente em uso de sonda vesical deve ser colhida na válvula lateral do equipamento, após a desinfecção do mesmo. A urina do 2º jacto pode ser da primeira micção ou de qualquer amostra urinária, desde que o paciente retenha a urina por um período mínimo de 4 horas. A urina é um fluido normalmente estéril; por conseguinte, uma colheita inapropriada pode torná-la contaminada com a flora do períneo, da uretra ou da vagina. As amostras permanecem estáveis até 2 horas após a colheita ou em geladeira (2ºC - 8ºC). Cultura de Fungos O isolamento e a identificação de fungo em cultura são prova definitiva no diagnóstico de infecções fúngicas, permitindo a escolha do tratamento adequado. As diferentes amostras clínicas são semeadas nos meios de cultura apropriados para isolamento e identificação de fungos.
72 As amostras deverão ser colhidas de maneira asséptica em frasco estéril, conforme a natureza da amostra. Os materiais biológicos requeridos são: - escamas de pele, unhas, pêlos (micoses superficiais e cutâneas); - aspirado de lesão, secreções, biópsias de pele (micoses subcutâneas); - expectoração, lavado brônquico, aspirado brônquico, escovado brônquico (micoses sistémicas); - secreções: pulmonar, vaginal, traqueal, orotraqueal, de lesões cutâneas, abdominal, oral, de conjunctivas ou de qualquer outra localização (micoses sistémicas); - sangue, biópsia de qualquer órgão ou tecido, urina, líquor, líquidos sinovial, ascítico, amniótico ou outros líquidos orgânicos (micoses sistémicas). Os resultados serão interpretados de acordo com o tipo de material clínico semeado, o local da lesão e a indicação clínica. Alguns fungos são parte da flora normal, mas podem, ocasionalmente, causar doenças. Do mesmo modo, fungos oportunistas podem ser apenas contaminantes como os reais causadores da patologia em investigação. Muitas vezes, o médico prescritor deve ser consultado sobre a condição clínica do paciente, para que se possa concluir qual o real valor do isolamento de determinados fungos. A presença de microrganismos da flora normal ou de infecção bacteriana concomitante pode inibir o crescimento de fungos patogénicos. Curva Glicémica Também conhecida como prova de tolerância oral à glicose (PTOG), a curva glicémica consiste na administração de 75 g de glicose - em solução aquosa a 25% - por via oral, seguida de colheitas seriadas de sangue, nos tempos 0, 60 e 120 minutos, para o doseamento de glicose. Em crianças, administra-se 1,75 g/kg de peso até a dose máxima de 75 g. NORMAL INTOLERANTE (tolerância diminuída) DIABETES MELLITUS AUMENTO DA FORMAÇÃO Inferior a 140 mg/dl intolerante à sobrecarga entre 140 e 200 mg/dl Superior a 200 mg/dl Para garantir a fidelidade dos resultados de um teste de sobrecarga oral à glicose, devem ser tomados os seguintes cuidados: - nos 3 dias que antecedem a prova, o paciente deve ingerir, pelo menos, 150 g de carbohidratos por dia; - o paciente deve estar realizar as suas actividades físicas habituais, mantendo-se em regime alimentar normal, excepto pela adição da quantidade de carbohidratos indicada no item anterior; - o paciente não deve realizar medicação que interfira no metabolismo de carbohidratos; - durante o teste, o paciente deve manter-se em repouso e, se possível sem fumar; - a prova deve ser realizada pela manhã, com o paciente em jejum de 8 a 10 horas. Mesmo com todas essas precauções, é importante salientar que os resultados desta prova, em testes realizados em dias diferentes, podem mostrar-se com vários problemas. Assim, a interpretação deve ser feita sempre com cautela, por um médico que conheça a história clínica do paciente.
73 Triagem Gestacional O doseamento de glicose, os tempos de colheita e os critérios diagnósticos são ligeiramente diferentes para mulheres grávidas. Em grávidas entre a 24ª e a 28ª semana de gravidez, pode ser realizado um teste de rastreio em duas fases. Na primeira, faz-se a glicemia em jejum ou a glicemia de 1 hora após a ingestão oral de 50 g de glicose (sem necessidade de jejum prévio). Resultados de glicemia de jejum iguais ou acima de 85 mg/dl ou após sobrecarga maior ou iguais a 140 mg/dl são considerados positivos e com indicação de realização de PTOG. A segunda fase aplica-se nos casos em que se enquadrem nos critérios anteriores, e é realizado a PTOG com 75 g de glicose. As amostras de sangue são colhidas nos tempos basal, 60 e de 120 minutos. Os limites de 126 mg/dl para glicemia basal e de 140 mg/dl após 2 horas são considerados normais. O diagnóstico de diabetes gestacional será confirmado se pelo menos um dos limites estabelecidos como normais for ultrapassado. Consultar Glicose. CYFRA 21-1 O Cyfra 21-1 é um marcador tumoral cuja presença caracteriza um mau prognóstico nos carcinomas de células escamosas do pulmão. É o fragmento da citoqueratina 19 encontrado no soro. Dados da literatura revelam que o Cyfra 21-1 não é um bom marcador tumoral de carcinoma de pequenas células do pulmão; é porém um marcador de sensibilidade e especificidade melhores para outros carcinomas do pulmão, como carcinomas de células escamosas, adenocarcinomas e carcinomas de células grandes. Dengue Conhecida na literatura há cerca de 200 anos, caracteriza-se como doença infecciosa febril aguda, de etiologia viral e evolução benigna na maioria dos casos. A primeira epidemia foi relatada em ocorrências simultâneas nos três continentes em 1779/1780. Nos últimos 40 anos, mais de 3 milhões de casos de dengue foram registados no mundo, com cerca de 58 mil mortes nesse período. As regiões tropical e subtropical são as mais atingidas por esta doença que é causada por um vírus da família Flaviviridae e transmitida pelos mosquitos Aedes aegypti e A. albopictus. No Brasil e nas Américas, o A. aegypti é o mosquito epidemiologicamente mais importante. Proveniente de África e domesticado por acção antropofílica, o Aedes aegypti é, também, o vector responsável pela transmissão da febre amarela urbana. O mosquito, de cor escura com manchas brancas, adaptou-se muito bem à vida urbana. Possui hábitos diurnos, picando os indivíduos na parte da manhã e à tarde. As fêmeas depositam os ovos em água limpa, onde as larvas podem proliferar-se a partir de depósitos artificiais de água, como pneus e tanques. O vírus de dengue é dividido em quatro sorotipos distintos, com características antigénicas diferentes e isolados inicialmente de fontes diferentes: DEN-1, DEN-2, DEN-3, DEN-4. Na infecção humana, o quadro clínico pode ser assintomático, evoluir de forma
74 clássica, com febre, cefaléia de grande intensidade, artralgia, mialgia, rash cutâneo, insónia e anorexia ou determinar manifestações hemorrágicas fatais, sendo essa forma clínica denominada dengue hemorrágica, ocorrendo em menos de 0,2% dos casos de infeccção primária e em 90% dos casos que apresentam história prévia. A transmissão ao homem ocorre por meio da picada de mosquitos hematófagos infectados. Não ocorre transmissão de pessoa a pessoa. Os mecanismos que determinam a apresentação clínica da doença sob a forma clássica ou hemorrágica ainda são desconhecidos. Entre as hipóteses fisiopatogénicas da forma hemorrágica da doença, as mais aceitas são em função da presença de anticorpos anti-virais: duas infecções sequenciais, por diferentes sorotipos, com intervalo mínimo de 3 anos, são necessárias para que a resposta imunológica do indivíduo sensibilizado seja amplifica da pela segunda infecção. Outra hipótese aceite é a que relaciona as formas graves a uma maior virulência de determinadas cepas virais. No Brasil, as primeiras referências ao Dengue datam de 1916, em São Paulo, e em 1923 em Niterói, Rio de Janeiro. Entretanto, a primeira epidemia só foi relatada em 1982, em Roraima, em que foram registrados casos. Em 1986, uma grande epidemia ocorreu no estado do Rio de Janeiro, causada pelo serotipo DEN-1, até então o único serotipo encontrado no Brasil. Foram identificados então mais de casos em 1986 e casos em 1987, todos de dengue clássico. Na década de 1990, ocorreram vários casos de recrudescimento de DEN-1 no Rio de Janeiro e a introdução da DEN-2, com alta incidência no início da década. No ano de 1991, foram registados os primeiros casos de dengue hemorrágico no estado, com notificações e 8 óbitos. Os meses de maior incidência de dengue no Brasil nos últimos anos, segundo dados do Ministério da Saúde, são os cinco primeiros meses do ano, com pico de incidência nos meses de Março, Abril e Maio. Recentemente, foram relatados nos mídia (O Globo, 24 de março de 2001) casos de dengue causados pelo serotipo DEN-3 no Rio de Janeiro. A imunidade é serotipo-específica, ou seja, a infecção causada por um dos serotipos não confere imunidade aos outros. Além disso, como já citado, a probabilidade de ocorrência de formas mais graves da doença é maior em indivíduos que apresentam infecção prévia. Sugere-se que esses indivíduos desenvolvam anticorpos contra um dos serotipos que facilitariam a interacção vírus-célula numa nova infecção viral. Existe a tendência de pacientes que habitam regiões endémicas, quando diagnosticados, apresentarem não a infecção primária, mas sim a secundária. Portanto, a presença dos anticorpos é de grande importância, visto que na primeira reinfecção e nas infecções subsequentes aparece uma alta ocorrência de complicações. Actualmente, utilizam-se testes de ELISA, que determinam simultaneamente a presença de anticorpos IgM e IgG. A classificação da infecção como primária ou secundária é pela análise da presença ou ausência de IgM e pela avaliação dos títulos de IgG. Nos casos positivos, a detecção dos anticorpos IgM caracteriza a infecção aguda. Apresentam-se positivos por volta do terceiro ou quinto dia após o aparecimento da sintomatologia clínica, mantendo-se positivos cerca de 30 a 90 dias e declinando logo após, até níveis indetectáveis. Nalguns casos, mantêm-se detectáveis até 8 meses após o quadro. Os anticorpos IgG apresentam-se positivos
75 por volta da segunda semana após o início do quadro, mantendo-se detectáveis por toda a vida. Os casos secundários caracterizamse pela presença de altos títulos de IgG, podendo ou não apresentar níveis elevados de IgM. Recomenda-se que, nos casos clínicos sugestivos da doença que apresentam serologia negativa, esta seja repetida com intervalo de 1 semana, para afastar a possibilidade de não-detecção por níveis de anticorpos muito baixos, ou em consequência da fase da doença primária ou secundária em que a colheita foi realizada. Além dos exames laboratoriais específicos, devem também ser avaliados, no diagnóstico de dengue, exames complementares definindo trombocitopenia, aumento de hematócrito e hipoproteinémia. De grande utilidade são as aplicações recentes de testes imunocromatográficos, reação em cadeia da polimerase (PCR) e hibridização de ácidos nucleicos para o diagnóstico rápido, sensível e específico. O RNA viral pode ser detectado em soro, líquido cerebroespinhal e tecidos, e os subtipos virais determinados por hibridização dos produtos de reação em cadeia de polimerase (PCR) com sondas de oligonucleotídeos tipo-específicas. A variação de linhagem e subtipos virais pode ser identificada, em estudos de pesquisa, pela análise por RFLP (restriction fragment length polymorphism) ou pela sequência de nucleotídeos dos produtos de PCR. Estes ensaios encontram-se restristos, ainda não disponíveis para a maioria dos laboratórios clínicos. Desidrogenase Láctica É uma enzima intracelular responsável pela oxidação reversa do lactato em piruvato. É amplamente distribuída em todas as células do organismo, concentrando-se mais especialmente no miocárdio, rim, fígado, hemácias e músculos. Possui cinco formas de isoenzimas. Os seus valores encontram-se elevados em todas as situações em que ocorre grande destruição celular. Os níveis séricos elevados encontrados em diferentes condições como anemia megaloblástica e hemolítica, leucemias, linfoma, hemoglobinopatias, enfarte agudo do miocárdio, enfarte pulmonar, insuficiência cardíaca congestiva, insuficiência coronária, choque e hipóxia importantes, doenças musculares, lesões hepáticas, neoplasias primárias ou secundárias (metastáticas), hepatites, icterícias obstrutivas e cirrose.
76 Desordens das Supra-renais O par de glândulas supra-renais localiza-se na borda superior dos rins (suprarenais). Cada supra-renal consiste no córtex (porção mais externa) e na medula (porção mais interna). A medula secreta catecolaminas, em resposta ao estímulo de fibras nervosas simpáticas pré-ganglionares. O córtex compõe-se de três zonas: glomerular, fascicular e reticular. Secreta corticosteróides que, dependendo da função dos esteróides, são classificados como mineralocorticóides, glicocorticóides ou esteróides sexuais. REGIÕES DA SUPRA-RENAL E PRODUÇÃO HORMONAL CÓRTEX ZONA GLOMERULAR --> Mineralocorticóide ZONA FASCICULAR --> Glicocorticóides ZONA RETICULAR --> Esteróides sexuais MEDULA CATECOLAMINAS --> Epenefrina, Noraepinefrina, Dopamina Os glicocorticóides regulam o metabolismo dos carboidratos, das proteínas e das gorduras. O cortisol é o principal glicocorticóide. A hormona adrenocorticotrófica (ACTH) é a principal reguladora da produção e secreção de cortisol. A ACTH é secretada pela hipófise anterior em resposta à libertação, pelo hipotálamo, da hormona libertadora de corticotrofina (CRH). A hormona antidiurético (ADH), a ocitocina e as catecolaminas podem influenciar o ritmo diurno da ACTH. Febre, hipoglicemia, stres, distúrbios psicológicos podem disparar a libertação de ACTH. O cortisol circula na corrente sanguínea ligado a uma alfaglobulina chamada transcortina ou CBG (cortisol binding globulin). Apenas uma pequena fracção circula livre e é biologicamente activa. Possui um ritmo circadiano, com níveis elevados pela manhã, caindo ao final do dia. Actua como feedback negativo no hipotálamo e na hipófise anterior, diminuindo a libertação de CRH e de ACTH. É metabolizado principalmente no fígado e seus metabolitos são excretados na urina como 17- hidroxicorticosteróides (17-OH esteróides). As hormonas sexuais circulam ligados a proteínas plasmáticas, principalmente à SHBG (steroid hormone binding globulin). Apenas a fracção livre é biologicamente activa. As hormonas sexuais sofrem metabolização hepática. Os androgénios são excretados na urina como 17-cetosteróides (17-KS). A aldosterona é o principal mineralocorticóide. É regulada por vários mecanismos, sendo o principal o sistema renina-angiotensina. Em caso de depleção de volume, ocorre libertação de renina das células justa-glomerulares das arteríolas aferentes renais. A renina actua sobre o angiotensinogénio produzindo angiotensina I, por sua vez convertida em angiotensina II pela enzima conversora de angiotensina (ECA). A angiotensina II é convertida em angiotensina III, sendo ambas capazes de se ligar ao receptor na célula-alvo e de ativar o ciclo fosfatidil inositol que estimula a libertação do cálcio intracelular e a secreção de aldosterona. Outros estímulos para a secreção de aldosterona são aumento do potássio sérico, elevação dos estrogénios, redução do volume plasmático e redução do sódio sérico. A aldosterona circula ligada a proteínas plasmáticas. Após sofrer metabolização hepática, é excretada na urina como conjugados do ácido glicurónico.
77 Hipercortisolismo Caracterizado pelos elevados níveis de cortisol e pela perda do ritmo circadiano. O Síndrome de Cushing engloba as diversas causas de hipercortisolismo: a administração exógena de cortisol ou de ACTH; a secreção excessiva de ACTH pela hipófise anterior com consequente hiperplasia do córtex adrenal e aumento na secreção de cortisol (doença de Cushing); a secreção ectópica de ACTH ou de CRH por tumor não-hipofisário; a hipersecreção autónoma de cortisol por adenoma ou carcinoma de adrenal; a displasia nodular adrenocortical primária (com produção autónoma de glicocorticóide e ACTH em níveis baixos ou normais). A causa mais frequente do síndrome de Cushing é a terapia prolongada com glicocorticóide, denominado síndrome de Cushing iatrogénico. Dois terços dos pacientes com síndrome de Cushing endógeno têm doença de Cushing (adenoma hipofisário secretor de ACTH). Um terço dos casos do síndrome de Cushing por produção ectópica de ACTH devido a tumores malignos não-hipofisários é causado por carcinoma de pulmão tipo oat cell. Outras causas são: tumores de células das ilhotas pancreáticas, tumores renais, timomas e adenomas brônquicos. Menos de um terço das causas de síndrome de Cushing é de neoplasias adrenais. Carcinomas adrenais podem secretar também grandes quantidades de androgénios. As manifestações clínicas mais comuns do síndrome de Cushing são: acentuada fraqueza e perda muscular, intolerância à glicose, obesidade central, face em lua, pele fina, estrias violáceas, fragilidade capilar, atrazo de crescimento em crianças, osteoporose, cifose, hipertensão arterial e distúrbios psiquiátricos. Nas mulheres, podem ocorrer oligomenorréia, amenorréia, anovulação ou hirsutismo. Nos homens, podem ocorrer diminuição de libido e/ou ginecomastia. Laboratorialmente, o diagnóstico inicial é feito com a dosemento do cortisol basal, ritmo circadiano, teste de supressão nocturna e doseamento do cortisol livre urinário. A presença de hipercortisolismo deve ser confirmada pelo teste de supressão com dexametasona 2 mg, e o diagnóstico etiológico requer o teste de supressão com dexametasona 8 mg, além do doseamento de ACTH. O teste do CRH também é utilizado, apesar da dificuldade de obtenção desse medicamento. HIPERCORTISOLISMO DOENÇA DE ADENOMA CRACINOMA ACTH IATROGÉNICO CUSHING (ADENOMA HIPOFISÁRIO) SUPRA- RENAL SUPRA- RENAL ECTÓPICO Cortisol Basal (N) (N) Rítmo Circadiano A A A A A ACTH Cortisol Livre Urinário 17-OH Esteróides ou N 17 KS ou N ( ) elevado ( ) muito elevado ( )diminuído (A)ausente
78 Outros exames complementares são os testes dinamicos: a supressão nocturna pela dexametasona (1 mg); o teste de supressão com dexametasona (2 mg) (Liddle I); o teste de supressão com dexametasona (8 mg) (Liddle II); o teste de estimulação pelo CRH. Insuficiência Adrenal Caracteriza-se pela diminuição na produção de cortisol. Pode ser primária, com ACTH elevada, ou secundária, com ACTH diminuído. A insuficiência secundária geralmente resulta do uso prolongado de glicocorticóide como cortisona e prednisolona, mas também pode ser devido a um tumor hipofisário. Em caso de hipopituitarismo, outras hormonas podem estar comprometidos, como GH, TSH e LH. A insuficiência primária pode manifestar-se de forma aguda ou crónica. A forma aguda é rara e a causa mais frequente é a hemorragia adrenal em pacientes com terapia anticoagulante. Outras causas são: septicéemia, cirurgia, trauma, enfarte do miocárdio e gravidez. Clinicamente, é caracterizada por astenia intensa, dores graves na região lombar, pernas e abdómen, choque e insuficiência renal. A insuficiência adrenal crónica é denominada doença de Addison, e a causa mais comum é um processo de auto-imunidade. Outras causas são as infecções granulomatosas como tuberculose, histoplasmose e amiloidose, sarcoma de Kaposi e infiltração por outros patógenios como citomegalovírus. Clinicamente, a insuficiência adrenal prolongada caracteriza-se por hiperpigmentação da pele, especialmente nas cicatrizes e mucosa bucal, astenia, perda de peso, febre, mialgia e hipotensão. Os achados laboratoriais podem não ser muito expressivos, a menos que ocorra o choque, com hiponatremia, hipercalemia, hipoglicemia, hemoconcentração e uremia. Na insuficiência secundária devido a hiposecreção de ACTH, não ocorrem nem a hiperpigmentação, nem alteração tão grave de volume e eletrólitos, uma vez que a aldosterona não está sob controlo primário do ACTH. AVALIAÇÃO LABORATORIAL DO HIPOCORTISOLISMO PRIMÁRIO (Lesão Adrenal) SECUNDÁRIO (Lesão do Hipotálamo ou Hipófise) Cortisol (8HS) N ou Ritmo A A ACTH ( ) elevado ( )diminuído (A)ausente Em muitos casos de Insuficiência supra-renal moderada, os valores basais podem ser compatíveis com a normalidade, havendo necessidade da realização do teste de estímulo do cortisol com cortrosina (ACTH). O teste de estimulação do cortisol com insulina só deve ser realizado após a constatação de que a adrenal é capaz de responder ao estímulo com ACTH. A discriminação entre insuficiência adrenal hipofisária ou hipotalámica pode ser realizada com o teste do CRH. A resposta positiva sugere etiologia hipotalámica, e a falta de resposta sugere etiologia hipofisária.
79 Síndrome Adrenogenital Este síndrome engloba um grupo de patologias caracterizadas pelo excesso de corticosteróides adrenais: a Hiperplasia adrenal congénita; a Hiperplasia adrenal de início tardio; o Adenoma adrenal; o Carcinoma adrenal. Na maioria dos casos, ocorre hipersecreção de androgénios, que resulta em virilização. A hiperplasia adrenal congénita engloba inúmeros defeitos dos sistemas enzimáticos que envolvem a síntese do cortisol, cuja deficiência leva ao aumento de ACTH, com hiperplasia da adrenal e aumento de inúmeras hormonas intermediárias. O defeito de síntese mais frequente é a deficiência de 21-hidroxilase. Se o defeito é completo, o paciente sofre acentuada perda de sal pela deficiência de aldosterona com hipotensão arterial e insuficiência adrenal pela deficiência de glicorticóides. Pode haver urgência no diagnóstico devido aos graves quadros de desidratação e hipotensão em recém-nascidos. Pode ocorrer genitália externa ambígua no nascimento. Os sinais de virilização podem ocorrer mais tarde, dependendo do grau da deficiência enzimática. O principal exame diagnóstico é o doseamento de 17-OH progesterona. Casos atípicos ou heterozigotos necessitam da prova de estímulo com ACTH. Outros exames utilizados são sulfato de deidroepiandrosterona (S-DHEA), deidroepiandrosterona (DHEA), androstenediona, testosterona, renina e aldosterona. Outros defeitos de sistema enzimático são deficiência de 17-hidroxilase, 11- hidroxilase, 3-beta-hidroxiesteróide desidrogenase e colesterol desmolase. Na deficiência de 11-hidroxilase, além da virilização, ocorre hipertensão arterial devido à formação de 11-desoxicorticosterona, um potente retentor de sódio. Nestes casos, é importante o doseamento de 11-desoxicortisol. Tumores produtores de excesso de androgénios são raros e podem ocorrer em qualquer idade. Hiperaldosteronismo A aldosterona é secretada em resposta ao ACTH, à depleção de volume intravascular ou à hiponatremia. Actua nos rins, reabsorvendo sódio e água à custa da excreção de potássio, magnésio e hidrogénio, resultando em hipernatremia e hipervolemia. O hiperaldosteronismo primário ocorre quando há hipersecreção de aldosterona pela supra-renal. Pode ser causado por adenoma unilateral (síndrome de Conn), hiperplasia bilateral ou carcinoma. A principal manifestação clínica é a hipertensão arterial. Os níveis de potássio encontram-se baixos ou no limite inferior da normalidade e estão associados a fraqueza muscular, fadiga e poliúria nocturna; algumas vezes, também, a polidipsia e intolerância à glicose. A perda urinária de iões de hidrogénio pode acarretar alcalose metabólica. O hiperaldosteronismo secundário ocorre em condições como insuficiência cardíaca ou estenose da artéria renal, com consequente aumento da renina plasmática e da aldosterona. Alguns pacientes, nesse caso, apresentam hipertensão, embora a
80 maioria dos casos curse com edema e sem hipertensão, relacionados a patologias como síndrome nefrótico, cirrose com ascite e insuficiência cardíaca congestiva. Hipoaldosteronismo São raros os defeitos isolados na síntese de aldosterona. Defeitos parciais da síntese aparecem na hiperplasia adrenal congénita em virtude da deficiência de 21- hidroxilase. Existem duas formas de deficiência isolada de aldosterona: o hipoaldosteronismo idiopático e o hipoaldosteronismo hiporreninémico, sendo esste último o mais frequente e geralmente associado a doença renal crónica, com diminuição da libertação de renina por deficiência das células justaglomerulares, levando à diminuição da aldosterona, hipercaliémia e acidose metabólica. Os níveis de sódio geralmente estão normais ou baixos, e a restrição de sódio agrava as manifestações clínicas. A Diabetes é um achado comum nestes pacientes. Esta condição também é associada à deficiência de prostaglandina indometacina induzida e é agravada pelo uso de heparina, bloqueadores do canal de cálcio ou bloqueadores beta-adrenérgicos. O principal sintoma da deficiência de aldosterona é a hipotensão arterial. O hipoaldosteronismo idiopático é raro, e o paciente pode apresentar um quadro de bloqueio cardíaco secundário a hipercaliémia ou hipotensão postural secundária a hipovolemia. ACTH (Hormona Adrenocorticotrófica) Podem ocorrer picos de secreção pós-stres ou pós-alimentação. É indicado para o diagnóstico da doença de Addison, em que se encontra extremamente elevado, e no síndrome de Cushing, no qual ajuda no diagnóstico diferencial entre patologia adrenal primária (adenoma ou carcinoma) com valores muito baixos e com o hipercortisolismo ACTH dependente com níveis elevados. Colher entre as 7:00 e as 9:00 horas. Cortisol O seu doseamento é útil no diagnóstico de hipercortisolismo, sendo importante no teste de supressão com dexametasona e no diagnóstico de insuficiência adrenal primária (Addison) ou secundária, no qual o teste de cortirosina (ACTH) geralmente é necessário. Convém lembrar que valores normais não descartam nenhuma das patologias citadas. Deve ser dada atenção especial à possibilidade de outras situações que podem elevar os níveis séricos de cortisol, como stres, obesidade, alcoolismo, gravidez, uso de estrogénios e depressão endógena. Variações nas proteínas séricas (globulina ligada ao cortisol - CBG) podem elevar ou diminuir os níveis de cortisol. Colher entre as 7:00 e as 9:00 horas. Cortisol Urinário Livre Principal teste de triagem para hipercortisolismo. Detecta a fração de cortisol livre. Deve ser avaliado em paralelo com o doseamento de creatinina urinária, em urina de 24 horas, para validar a colheita.
81 11-Desoxicortisol Sérico (Composto S) Também chamado composto S. Eleva-se no bloqueio da enzima 11-hidroxilase por ser o precursor imediato do cortisol. Alguns pacientes com hirsutismo e níveis basais normais de 11 desoxicortisol podem evidenciar defeitos parciais de síntese no teste de estimulação com ACTH. Deidroepiandrosterona (DHEA) A deidroepiandrosterona, precursora da síntese de testosterona, é um androgénio de fraca atividade. A sua utilização está indicada na avaliação do hiperandrogenismo, como ocorre no hirsutismo, acne, hiperplasia congénita da supra-renal, carcinoma de supra-renal e puberdade precoce. A sua semi-vida é mais curta do que a do seu principal metabolito, o sulfato de deidroepiandrosterona (S-DHEA). Isto permite que seja utilizada na avaliação de respostas da supra-renal aos testes dinâmicos de estimulação e supressão. A hiperresposta do DHEA à estimulação com ACTH é utilizada para o diagnóstico de defeito de síntese da supra-renal. Os níveis séricos são significativamente alterados em condições de stres, variando com a idade, com um pico na fase puberal. Sulfato de Deidroepiandrosterona (S-DHEA) O sulfato de deidroepiandrosterona (SDHEA) é o metabolito da DHEA, e os seus níveis não sofrem grandes alterações com estimulação fisiológica, ao contrário do que ocorre com a DHEA. É encontrado em grande quantidade na circulação, e o seu doseamento pode substituir o doseamento sérico dos 17-cetosteróides urinários. A sua utilidade clínica está na avaliação do hiperandrogenismo, como ocorre no hirsutismo, no acne, no carcinoma de supra-renal e no diagnóstico e controle terapêutico da hiperplasia congénita da supra-renal. Androstenediona É um androgénio produzido pelas supra-renais e gonadas. Útil na avaliação do hiperandrogenismo (hirsutismo, acne), no acompanhamento da hiperplasia congénita da supra-renal e nos tumores virilizantes da supra-renal e ovário. 17-Hidroxiprogesterona (17-OHP) É produzido pelos ovários e supra-renais e sofre variações de acordo com a fase do ciclo menstrual. É importante na avaliação do hirsutismo e para diagnóstico e acompanhamento da hiperplasia congénita da supra-renal por defeito de síntese da 21-hidroxilase. Casos duvidosos podem ser confirmados pelo teste de estimulação com ACTH. 17-Cetosteróides (17-KS) Utilizado na avaliação do hiperandrogenismo, uma vez que representa vários metabolitos urinários de diferentes precursores. Nos homens, dois terços dos 17-KS são derivados do córtex da supra-renal, e um terço, dos testículos. Na mulher, são derivados praticamente da supra-renal. Os 17-KS elevam-se nos tumores adrenais e gonodais, no síndrome do ovário poliquístico e na hiperplasia supra-renal.
82 17-Hidroxicorticosteróides (17-OHS) Utilizado no diagnóstico de hipercortisolismo, uma vez que representa um grupo de esteróides secretados pela adrenal, incluindo cortisol, 11-desoxicortisol e outros. Várias situações podem elevar os seus níveis, como stres, obesidade e alcoolismo. Aldosterona Deve ser colhida após 1 hora de repouso em decúbito dorsal ou após 2 horas em posição ortostática. São interferências comuns o uso de hipotensores e de diuréticos, o teor de sódio na dieta e a postura. É útil na avaliação da hipertensão e/ou hipotensão arterial. Importante para diagnóstico de hiperaldosteronismo primário e secundário, hipoaldosteronismo, síndrome de Bartter e pseudo-hipoaldosteronismo. Para localização de tumores, podem ser colhidas amostras por cateterismo venoso. No hiperaldosteronismo primário, a aldosterona encontra-se elevada. Já os níveis de renina mostram-se baixos ou indetectáveis, associados com hipocaliémia. Renina elevada com aldosterona elevada sugere hiperaldosteronismo secundário (encontrado na hipertensão renovascular). No síndrome de Bartter, a aldosterona e a renina podem estar elevadas em pacientes normotensos, com potássio baixo. No hipoaldosteronismo, constatamos elevação de potássio com níveis baixos de aldosterona. Na síndrome de resistência à ação da aldosterona (pseudo-hipoaldosteronismo), encontra-se hipercaliémia com aldosterona em níveis elevados. Renina Deve ser colhida após 1 hora de repouso em decúbito dorsal ou após 2 horas em posição ortostática. Pode ser colhida por cateterismo das veias renais. Interferências comuns são o uso de diuréticos, de anti-hipertensivos e de estrogénios, assim como a postura e o teor de sódio na dieta. O seu doseamento é útil na avaliação da hipertensão e/ou hipotensão arterial. Tem um papel importante no diagnóstico de hiperaldosteronismo primário e secundário, hipoaldosteronismo e síndrome de Bartter, e no seguimento de portadores de defeito da 21-hidroxilase em tratamento. Encontra-se diminuída no hiperaldosteronismo primário e no hipoaldosteronismo hipo-reninémico, e elevada no hiperaldosteronismo secundário e no síndrome de Bartter. Deve ser avaliada em associação com os níveis de potássio e de aldosterona. Catecolaminas e Ácido Vanil Mandélico Utilizados na avaliação da hipertensão arterial. Úteis no diagnóstico de feocromocitoma, neuroblastoma, ganglioneuroma, ganglioneuroblastoma e gangliomas. Também empregues na monitorização do tratamento, para avaliar se houve remoção completa do tumor, assim como na avaliação da possibilidade de recidivas. Devido à secreção intermitente de catecolaminas por alguns tumores, várias colheitas devem ser realizadas num curto intervalo de tempo. Em 20 a 30% dos neuroblastomas, o doseamento de AVM pode ser normal. É necessário observar as inúmeras interferências causadas por drogas e pela dieta.
83 Ácido Vanil Mandélico (AVM) Realizado em amostra de urina de 24 h, colhida em frasco especial contendo ácido e após dieta especial. O uso de bebida alcoólica, de reserpina, de inibidores da MAO (monoamino oxidase) e de contrastes radiológicos pode interferir, diminuindo os seus valores. A ingestão de chocolate, chá, cafeína, banana, frutas cítricas, vegetais, baunilha e anfetaminas pode elevar os valores. Catecolaminas Urinárias Realizado em amostra de urina de 24 h, colhida em frasco especial contendo ácido e após dieta especial. O uso de guanetidinas e o uso crónico de inibidores da ECA (enzima conversora da angiotensina), reserpina e bromoergocriptina podem interferir e originar valores reduzidos. A ingestão de bebidas alcoólicas, chá, café, banana, nicotina, teofilina, anfetaminas, levodopa, aldomete e isoproterenol pode elevar os valores. Digoxina Os digitálicos são dos fármacos mais frequentemente prescritos na prática clínica. Devido à sua capacidade de aumentar a força de contracção cardíaca, são usados no controle de taquicardias supraventriculares e no tratamento da insuficiência cardíaca congestiva. A digoxina é um dos digitálicos mais usada. Tem uma semivida de 24 a 48 horas (com uma média de 35 horas). Como a digoxina é eliminada principalmente por meio de excreção renal, os pacientes com função renal reduzida apresentam uma semi-vida sérica mais longa. A digoxina deve ser avaliada até que o efeito terapêutico seja alcançado, no acompanhamento da estabilidade e no uso adequado do fármaco pelo paciente e ao primeiro sinal de aparecimento de efeito tóxico (como anorexia ou arritmia). O doseamento em crianças é aproximadamente 50% maior do que o usado em adultos, quando calculada em miligramas por quilograma de peso corporal. Doses mais altas são necessárias por causa da maior relação de massa cardíaca com a massa corporal em crianças. Estas doses mais altas refletem-se em concentrações séricas mais altas em crianças. A intoxicação digitálica acontece com frequência, já que o intervalo entre os níveis terapêuticos e tóxicos é muito pequeno. Os sintomas clínicos mais comuns de subredosagem são anorexia, náuseas e vômitos, visão turva e desorientação. A manifestação miocárdica mais importante e comum da intoxicação digitálica é a arritmia cardíaca. Frequentemente, o diagnóstico clínico de intoxicação digitálica torna-se difícil em pacientes com patologias cardíacas graves, pois a maioria das manifestações pode ser causada pela doença ou por farmacos. Por isso, o doseamento de digoxina sérica é especialmente útil na interpretação de arritmias. As maiores causas de intoxicação digitálica são a depleção de potássio e a diminuição da função renal com a idade. Alterações da função renal, hipercalcémia, alcalose, mixedema, hipomagnesemia, enfarte do miocárdio recente, hipóxia e hipocaliémia podem aumentar a sensibilidade aos efeitos tóxicos da digoxina. O uso de drogas como quinidina, verapamil, amiodarona, ciclosporina, espirinolactona, entre outras, pode aumentar os níveis séricos por diminuição da clearance da digoxina. Quando diante de níveis séricos abaixo do esperado, deve-se avaliar a presença de
84 doença tiroidiana, má absorção, diminuição do fluxo sanguíneo intestinal por arteriosclerose mesentérica e uso de drogas como laxantes, antiácidos, fenitoína, neomicina e metoclopramida, que podem diminuir a absorção. Outro dado a ser avaliado é o nível de adesão do paciente ao tratamento, tanto na frequência quanto nas doses prescritas. O tempo de colheita da amostra é um factor importante na determinação dos níveis séricos de digoxina. Os níveis séricos elevam-se nitidamente durante a primeira hora depois de uma dose oral. Isto é seguido por uma diminuição quando a digoxina é levada para o miocárdio e outros tecidos. Normalmente, para absorção e armazenamento, quando administrada por via oral, são necessárias 4 a 6 horas, e por via endovenosa, cerca de 30 minutos. Depois disso, os níveis de digoxina no soro tendem a estabilizar, passando a diminuir muito lentamente durante as 24 a 48 horas seguintes. Não é possível determinar com precisão os níveis de digoxina em pacientes em fase de troca de terapia de digitoxina para terapia com digoxina, visto que ambas as drogas podem estar presentes no soro. Os anticorpos anti-digoxina usados na maioria dos testes comerciais para doseamento de digoxina apresentam reacção cruzada significativa com digitoxina (2% a 6% de reação cruzada, com alguns casos que chegam a 40%) e outros digitálicos. O problema da reação cruzada é exacerbado pelo facto de que níveis terapêuticos de digitoxina são aproximadamente 10 vezes mais altos do que os da digoxina. O anticorpo antidigitoxina também apresenta reacção cruzada com digoxina (2% a 4% de reação cruzada), mas, por causa dos níveis terapêuticos mais altos, a interferência da digoxina é menos importante no doseamento de digitoxina. Obtém-se a maior precisão diagnóstica colhendo a amostra de sangue num momento padronizado durante a fase estável, quando os níveis de digoxina no soro reflectem as concentrações cardíacas usuais. Normalmente, o equilíbrio é alcançado num prazo de cerca de 5 dias, e a colheita é realizada imediatamente antes da próxima dose, ou a qualquer momento, aquando da suspeita de intoxicação. Doença de Chagas A tripanossomíase americana ou doença de Chagas é uma parasitose endémica causada pelo Trypanosoma cruzi. Pode cursar com infecções agudas ou crónicas. A forma aguda geralmente é uma doença febril discreta. Pode evoluir, especialmente em crianças, com um quadro mais exuberante, que é caracterizada por febre, anorexia, edema da face e dos membros inferiores, linfadenopatias e hepatoesplenomegalia discreta. Mais raramente ocorre miocardite. Após a fase aguda, o paciente, permanece infectado e passa para uma fase crónica assintomática. A doença crónica sintomática irá manisfestar-se anos ou mesmo décadas após a fase aguda. As clássicas manifestações crónicas relacionam-se com distúrbios de ritmo e condução cardíaca, tromboembolias, miocardiopatia de chagas, megaesófago e megacólon. Nas situações de imunossupressão, pode ocorrer a reactivação do quadro, que muitas vezes é fatal. A transmissão ocorre por vectores hematófagos, mas pode dar-se por via congénita, transfusional e outras formas menos frequentes, como a inoculação involuntária em laboratório. Os métodos serológicos para diagnóstico da doença de Chagas apresentam
85 sensibilidade e especificidade elevadas, sendo úteis para o diagnóstico nas fases aguda e crónica da doença. Entretanto, é possível a reacção positiva por reactividade cruzada com as leishmanioses, especialmente com a forma visceral e as formas cutaneo-mucosas da leishmaniose tegumentar, e com outros antigénios em comum. Por isso, é recomendável a realização de reacções por diferentes métodos como hemaglutinação, imunofluorescência e enzima imunoensaio. Devem ser realizados no mínimo dois métodos, para que se controlem mutuamente, visto que, em cada método, são utilizados diferentes antigénios e formas do parasita, o que permite diminuir a possibilidade de resultados falso-positivos. Resultados positivos devem ser encontrados nos dois métodos utilizados para confirmar o diagnóstico. Nos casos de apenas um método apresentar positividade, torna-se necessária a análise clínica da história epidemiológica, achados clínicos e outros exames diagnósticos complementares. Na fase aguda, anticorpos das classes IgM e IgG são detectáveis. Na fase crónica, são encontrados anticorpos da classe IgG. Os níveis de reactividade diferem para cada método e de acordo com a finalidade do diagnóstico. Os valores considerados para triagem de dadores de sangue são sempre inferiores aos considerados para o diagnóstico clínico. Electroforese da Hemoglobina A realização da electroforese da hemoglobina permite a identificação das diferentes fracções normais e patológicas da hemoglobina. A hemoglobina é separada, de acordo com a sua migração, num meio sólido (acetato de celulose), quando submetida a um campo eléctrico. A visualização das diferentes posições é evidenciada por coloração. É um método importante para investigar a presença das hemoglobinas anormais como a hemoglobina S e C e nas talassemias que podem cursar com aumento da HbA2 e com a presença da HbH. Permite também a quantificação das fracções normais da hemoglobina como A, A2 e Fetal. As fracções podem ser quantificadas por densitometria após eluição. A electroforese é realizada em ph alcalino e pode ser realizada, de forma complementar, também em ph ácido para melhorar a identificação de hemoglobinopatias, já que outras fracções anómalas podem migrar na mesma posição das hemoglobinas S e C como as HbD e HbE Electroforese das Proteínas O plasma humano contém mais de 500 proteínas identificáveis. Entre essas, estão presentes proteínas transportadoras, anticorpos, enzimas, inibidores enzimáticos, factores da coagulação e proteínas com outras funções. A avaliação das concentrações de proteínas séricas e as proporções das diferentes fracções de proteína têm considerável valor no diagnóstico de patologias agudas e crónicas. A electroforese das proteínas no soro é uma técnica simples para separar as proteínas do soro. É o teste de triagem mais utilizado para investigação de anomalias das proteínas séricas. Em condições normais, são separadas cinco bandas do soro: albumina, alfa-1, alfa-2, beta e gamaglobulinas. Eventualmente,
86 pode ser observada a presença da pré-albumina. O reconhecimento de paraproteínas, normalmente encontradas nas gamapatias benignas ou malignas é o uso diagnóstico mais importante para a electroforese das proteínas. Quando alteradas, as bandas apresentam-se com padrões conhecidos para importantes patologias. A banda de albumina é relativamente homogenea, porém as demais são compostas por uma mistura de diferentes proteínas. Informações adicionais podem ser encontradas nos títulos referentes às diferentes proteínas que compõem as bandas identificadas pela electoforese como: albumina, alfa-1-antitripsina, alfa-1-glicoproteína ácida, haptoglobina, ceruroplasmina, entre outras. Pré-Albumina Sintetizada pelo fígado, tem como função conhecida o transporte da tiroxina e desempenhar um papel significativo no metabolismo da vitamina A. Forma um complexo com o retinol, que se liga posteriormente à vitamina A. Devido à sua baixa concentração no soro, com frequência não se traduz na electroforese das proteínas séricas. Contudo, consegue ultrapassar a barreira hemato-encefálica e pode também ser sintetizada por células do plexo coróide, o que explica seu aparecimento frequente na electroforese do líquor cefalorraquidiano. Os níveis de pré-albumina estão significativamente diminuídos em diversas patologias hepáticas e aumentados em pacientes que usam esteróides, como também na falência renal e durante a gravidez. Por ter uma semi-vida muito curta e ser bastante sensível às variações do aporte alimentar e ao estado funcional hepático, é considerada um bom marcador do estado nutricional. Albumina É a proteína mais abundante no plasma, responsável por cerca de 60% da concentração total de proteínas. É sintetizada exclusivamente pelo fígado, aparecendo primeiro no citoplasma dos hepatócitos como um precursor chamado pré-albumina. Possui um papel muito importante em diversas funções do organismo, como o transporte de diferentes substâncias e em especial na manutenção da pressão oncótica. Foram descritas mais de 20 variantes genéticas de albumina. O tipo mais comum é chamado albumina A. Essas albuminas variantes podem resultar numa faixa de albumina larga na electroforese das proteína séricas ou podem dar origem a duas faixas distintas (bis-albuminémia). Nenhuma dessas variantes foi ainda associada a manifestações patológicas. Na rara síndrome de ausência congénita de albumina, os pacientes podem apresentar edema moderado, mas podem poupar as consequências hemodinámicas com a utilização de mecanismos compensatórios, como o aumento das globulinas do plasma, que assumem algumas das funções da albumina. O problema bioquímico principal nesses pacientes é uma alteração no metabolismo lipídico, como o aumento de colesterol, fosfolipídios e outras lipoproteínas. Alfa-1-Globulinas A alfa-1-antitripsina corresponde a cerca de 90% das proteínas que correm na faixa das alfa-1-globulinas. A deficiência da alfa-1-antitripsina está associada ao
87 enfisema pulmonar e à cirrose hepática. Só é detectável pela electroforese quando homozigótica; os estados heterozigóticos só podem ser identificados por técnicas imunoenzimáticas que também são utilizadas para confirmação das deficiências homozigóticas. É uma das proteínas de fase aguda e pode ser encontrada noutros fluidos orgânicos, como lágrimas, sémen, bile e líquido amniótico. Nos 10% restantes, estão a alfa-1-glicoproteína ácida, a alfafetoproteína e outras proteínas. Os níveis elevam-se nas doenças inflamatórias agudas e crónicas, neoplasias, após traumas ou cirurgias e durante a gravidez ou terapia com estrogénios. Nos carcinomas hepatocelulares, a elevação pode acontecer devido ao aumento da alfafetoproteína. Alfa-2-Globulinas Incluem a haptoglobina, a alfa-2-macroglobulina e a ceruloplasmina. Raramente se encontram alterações nessa banda electroforética, já que a diminuição de um componente é compensada pelos demais mesmo dentro dos valores de referência. Níveis elevados de alfa-2-macroglobulina associados à diminuição da albumina acontecem no síndrome nefrótico. Os níveis de haptoglobina e de ceruloplasmina podem apresentar-se elevados em numerosas situações que levam à reacção de fase aguda. Os níveis de haptoglobina apresentam-se diminuídos nas hepatopatias graves, na anemia megaloblástica, nas situações de aumento da hemoglobina livre, como na hemólise de eritrócitos ou na reabsorção de grandes hematomas e na terapia com estrogénios e corticóides. Os níveis de ceruloplasmina aumentam na terapia comestrogénios e encontram-se diminuídos na doença de Wilson, na desnutrição, no síndrome nefrótico e nas enteropatias com perda de proteínas. Betaglobulinas Composta pelas beta-lipoproteínas (LDL), transferrina, C3 e outros componentes do complemento, beta-2-microglobulina e antitrombina III. A redução dessa banda é rara. A anemia por défice de ferro leva ao aumento da transferrina. O hipotiroidismo, a cirrose biliar, as nefropatias e alguns casos de diabetes mellitus podem evidenciar-se pelo aumento de colesterol e consequente aumento das betalipoproteínas (LDL). A beta-globulina está elevada nos casos de icterícia obstrutiva e menos frequentemente nalguns casos de hepatite. Quase sempre, está elevada nos casos de cirrose hepática. Nesses casos, pode aparecer junto com sobreposição ou fusão das bandas beta e gama pelo aumento de IgA, que ocorre nas cirroses hepáticas, infecções de pele ou respiratórias e na artrite reumatóide. Elevações causadas normalmente pelo aumento dos componentes do complemento podem ocorrer na hipertensão maligna, doença de Cushing, poliartrite nodosa e carcinomas. Gamaglobulinas Composta pelas imunoglobulinas, predominantemente pela IgG. As imunoglobulinas A,M,D,E e proteína C reactiva encontram-se na área de junção beta-gama. A ausência ou a diminuição da banda gama indica imunodeficiências congénitas ou adquiridas. O aumento dessa banda sugere o aumento policlonal das gamaglobulinas associadas a doenças inflamatórias crónicas, reacções imunes, doenças hepáticas ou neoplasias disseminadas. Bandas oligoclonais podem eventualmente ser observadas em infecções víricas crónicas, nalgumas infecções bacterianas como as pneumonias por pneumococos e as hepatites crónicas activas.
88 Tuberculose, sarcoidose, linfogranuloma venéreo e sífilis terciária são doenças crónicas que levam ao aumento dessa banda. Artrite reumatóide, lúpus eritematoso sistémico e outras colagenoses podem apresentar níveis normais a acentuadamente aumentados, dependendo da fase de actividade da doença. Níveis aumentados também são encontrados em linfomas malignos, doença de Hodgkin e leucemia linfocítica crónica. Tipicamente, a macroglobulinemia de Waldenström e o mieloma múltiplo exibem um pico homogéneo, que pode ou não resultar do aumento total da banda gama. As hepatopatias cursam frequentemente com aumento da banda das gamaglobulinas. Na hepatite, verifica-se um aumento das beta e gamaglobulinas com redução da albumina. Nas cirroses, o padrão mais sugestivo consiste na elevação da gamaglobulina de base ampla, juntamente com a fusão da beta e da gamaglobulina, sem a individualização dos picos da chamada fusão beta-gama. Apenas cerca de 20% dos cirróticos apresentam a fusão completa, e cerca de 3% apresentam a fusão parcial. Alguns Padrões Electroforéticos Típicos A diminuição das bandas da albumina, alfa-1, beta e gamaglobulinas com a elevação da faixa alfa-2 é um padrão de perda seletiva de proteínas, como a que ocorre no síndrome nefrótico. Entretanto, convém lembrar que é necessário uma diminuição de pelo menos um terço na concentração da albumina para que seja possível a visualização na electroforese. A alteração característica das reacções de fase aguda consiste no aumento da alfa-1 e alfa-2-globulinas, quase sempre associado à diminuição da albumina. O aumento isolado da banda alfa-1 pode ser observado nas hepatites crónicas, nas reacções de fase aguda acompanhadas de hemólise, na gravidez e durante a terapia de estrogénios. O aumento predominante da banda alfa-2 pode ser observado em patologias que cursam com vasculites como a artrite reumatóide ou nas doenças por imunocomplexos. Podem aparecer faixas normalmente não-visualizadas, como um pico que pode surgir entre a albumina e a região alfa-1, como resultado de um aumento da alfafetoproteína. Um grande aumento de proteína C reactiva numa reacção de fase aguda severa pode gerar uma leve faixa na região gama. O aumento de lisozimas observadas na leucemia monocítica pode produzir uma faixa depois da região de gama. O pico monoclonal apresenta-se na região gama, menos frequentemente na faixa beta e, em raros casos, na região alfa-2. Consiste num pico alto e relativamente delgado, homogéneo e fusiforme, que normalmente está associado aos casos de mieloma ou são consequência de patologias como macroglobulinemia de Waldeström, gamapatias monoclonais secundárias e idiopáticas. Em contraste com os aumentos policlonais, as gamapatias monoclonais produzem um padrão muito específico. As bandas monoclonais ocorrem pelo aumento de clones de imunoglobulinas distintas, secretadas por uma proliferação monoclonal de células plasmáticas, acompanhada de quantidades progressivamente menores das imunoglobulinas policlonais, à medida que as células plasmáticas normais são substituídas pelos clones malignos.
89 AVALIAÇÃO LABORATORIAL DA ELECTROFORESE DAS PROTEÍNAS Electroforese da Urina A electroforese de proteínas da urina, assim como do soro, é uma técnica simples para separar as proteínas presentes na urina. A indicação mais importante da realização da electroforese de proteínas na urina é o reconhecimento de paraproteínas nas gamapatias benignas ou malignas, especialmente no mieloma múltiplo. Na presença de proteína de Bence Jones (cadeias leves), métodos específicos de identificação, como a análise de cadeias kappa e lambda, podem ser realizados para um diagnóstico mais específico. Electroforese do Líquor A realização da electroforese do líquido cefalorraquidiano (LCR) pode auxiliar na quantificação da proporção albumina/globulinas. A sua maior utilidade está na identificação de bandas oligoclonais presentes em 70 a 90% dos pacientes com esclerose múltipla. Entretanto, bandas oligoclonais de IgG também podem ser encontradas em diferentes situações como pan-encefalite esclerosante subaguda, encefalite por caxumba, em pacientes com infecção pelo HIV, meningite criptocócica, linfoma de Burkitt, neurossífilis, síndrome de Guillain-Barré, carcinomatose meníngia, toxoplasmose e meningoencefalites víricas e bacterianas. Na presença de lesões traumáticas do SNC, podem cursar nas fases iniciais com um aumento dos níveis de alfa-2-globulina. Como as alterações das imunoglobulinas podem ser derivadas de alterações séricas, é importante a realização concomitante da electroforese do soro e do líquor. Os casos duvidosos devem ser confirmados por outras técnicas, como a imunofixação. Enolase Neurónio-Específica (NSE) A enolase neurónio-específica (NSE) é uma enzima glicolítica que existe na forma de diversas isoenzimas diméricas: alfa-alfa, alfa-beta, beta-beta e gama-gama. Dessas subunidades, as isoenzimas alfa-gama e gama-gama são as enolases neurónio-específica que são encontradas principalmente nos neurónios e nas células neuroendócrinas.
90 É um marcador diagnóstico de relativa especificidade (85%) para carcinoma de pequenas células de pulmão. Pode ser usado para monitorizar os efeitos da terapia e indicar recidivas antes das evidências clínicas. É encontrado também noutras condições malignas como neuroblastoma, melanoma, carcinoma de células das ilhotas pancreáticas e hipernefroma. No neuroblastoma, o NSE correlaciona-se com o prognóstico, mas não é útil para o acompanhamento das recidivas. Epstein-Barr Vírus (EBV) O vírus Epstein-Barr (EBV) é um herpesvírus humano conhecido por causar a mononucleose infecciosa e também pela sua provável participação na etiologia de alguns carcinomas (nasofaríngeo), linfomas (linfoma de Burkitt) e doenças linfoproliferativas em pacientes imunodeprimidos. Recentemente, foi descrita o síndrome ativo crónica severo, no qual a linfoproliferação continua activa. Já o papel etiológico do EBV noutras patologias como artrites reumáticas, doença de Hodgkin e síndrome de fadiga crónica ainda não está bem definido. Na fase aguda da mononucleose infecciosa, anticorpos IgM e IgG para antigénios precoces do EBV (EA), antígénios da capsíde viral (VCA) e antigénios nucleares (EBNA) aparecem em sequência. A pesquisa mais utilizada é a de anticorpos IgM contra VCA por enzima imunoensaio. A positividade indica infecção aguda. Entretanto, a presença de anticorpos IgM para VCA ou IgM /IgG para EA, com ausência ou baixa concentração de anticorpos contra EBNA, indica infecção recente ou em curso. A presença de anticorpos contra VCA e a relação IgG/ IgM inferior a 1 podem auxiliar no diagnóstico de casos dificeis. A análise da avidez de anticorpos IgG contra VCA do EBV também é útil em casos de reactivação ou infecção recente. A persistência de EA e/ou VCA IgG em títulos altos indica infecção crónica pelo EBV. A pesquisa de anticorpos específicos para EBV deve ser realizada nos quadros de mononucleose para confirmação do diagnóstico ou nos casos de suspeita clínica que cursa com anticorpos heterófilos negativos, não sendo diagnosticada pelo métodos tradicionais, e também para o diagnóstico diferencial das patologias que podem mimetizar um quadro de mononucleose (mononucleose-like), como hepatites víricas agudas, colagenoses, síndrome de seroconversão do HIV-1, citomegália e toxoplasmose. A comparação de métodos de cultura de células e a amplificação genómica por PCR indica a maior sensibilidade da técnica molecular (PCR ) na detecção de EBV. A infecção crónica por EBV pode ser detectada pela presença do DNA-EBV em sangue periférico por PCR. Em pacientes em tratamento profilático com imunoglobulinas, o diagnóstico serológico pode acarretar problemas relativos a reacções falsopositivas. A técnica de PCR usando células mononucleares de sangue periférico pode ser usada para o diagnóstico preciso e precoce da infecção por EBV em pacientes altamente vulneráveis, com doenças linfoproliferativas, nos quais a PCR se apresenta altamente sensível, mesmo em amostras de saliva. A PCR é útil em detectar o EBV noutras patologias tais como pneumonia intertiscial, pericardite e miocardites a partir da análise de tecidos ou de líquidos. Entretanto, deve-se ter o cuidado de proceder à avaliação qualitativa e quantitativa em
91 amostras colhidas em diferentes datas, além da correlação clínica para a confirmação da relação entre os sintomas e a etiologia vírica. Consultar Mononucleose Infecciosa Eritropoietina A eritropoietina (EPO) é um factor regulador na formação dos glóbulos vermelhos do sangue. O rim é responsável por 90% da síntese da EPO circulante. Em situações anormais, pode ser produzida noutros órgãos, como ocorre nos casos de neoplasias. O seu doseamento está indicado na avaliação das anemias, policitemias, como marcador nalguns tumores e na monitorização dos níveis terapêuticos de EPOrecombinante. Os níveis séricos estão diminuídos na policitemia vera, na insuficiência renal crónica e na doença de Hodgkin. Níveis elevados podem ser encontrados em condições que cursem com hipóxia, como em grandes altitudes, presença de hemoglobinas anormais, cardiopatias e pneumopatias. Exame Directo para Fungos O exame microscópico directo de amostras clínicas tem como finalidade detectar a presença de fungos em material colhido de pacientes com suspeita de infecção fúngica. A presença de fungos pode ser detectada por meio de diferentes colorações, tais como: hidróxido de potássio 20%, isolado ou acrescido de tinta Parker ou de DMSO (dimetilsulfóxido) e Giemsa. A escolha da coloração varia conforme o tipo de material a ser analisado e a suspeita clínica. A visualização de estruturas fúngicas em material clínico é um importante instrumento diagnóstico. O exame directo pode fornecer identificação completa ou parcial do fungo (quando apenas o género ou o grupo pode ser identificado). Em ambos os casos, proporciona informação necessária para a escolha da conduta terapêutica. Em certos casos, a identificação pelo exame directo é o único exame necessário para o diagnóstico. São exemplos dessa situação a identificação dos agentes etiológicos de algumas micoses, como pitríase versicolor (Malassezia furfur), lobomicose (Loboa loboi), rinoesporodiose, adiaspiromicose. Noutras micoses, o agente pode ser identificado pelo exame directo, como por exemplo o Paracoccidioides brasiliensis e o Cryptococcus neoformans. Entretanto, é necessário proceder à realização da cultura para fungos. Trata-se de um exame indispensável, visto que os fungos podem permanecer presentes no exame directo por longo tempo, mesmo após o tratamento, sem no entanto serem viáveis. Portanto, não representa um bom parâmetro para controlo de cura. As amostras deverão ser colhidas em frasco estéril, de maneira asséptica. Os materiais biológicos necessários são: escamas de pele, unhas e pêlos (micoses superficiais e cutâneas); aspirado de lesões, secreções, biópsias de pele (micoses subcutâneas); expectoração, lavado brônquico, aspirado brônquico, escovado brônquico (micoses sistémicas); secreções: pulmonar, vaginal, traqueal, orotraqueal, de lesões cutâneas, abdominal, oral, de conjuntivas ou de qualquer outra localização (micoses
92 sistémicas); sangue, biópsia de qualquer órgão ou tecido, urina, líquor, líquido sinovial, ascítico, amniótico ou outros líquidos orgânicos (micoses sistémicas). As infecções fúngicas podem atingir qualquer órgão ou tecido do corpo humano. Portanto, qualquer material biológico pode ser analisado para a pesquisa de fungos. Os resultados devem ser interpretados de acordo com o tipo de material e o local da lesão. Muitas vezes, o fungo pode ser parte da flora local, não tendo significado clínico. Exame Microscópico Directo para Fungos com Tinta-da-China É utilizado para a pesquisa de leveduras do género Cryptococcus em qualquer material clínico. As amostras são coradas com tinta-da-china, com a finalidade de visualizar as leveduras encapsuladas. A tinta-da-china não é capaz de penetrar na cápsula dessas leveduras, mas é capaz de corar todo o material em negro, permitindo o fácil reconhecimento das leveduras encapsuladas, que permanecem claras. A sua presença é indicativa de criptococose, e o seu achado é fundamental para confirmação diagnóstica, embora não permita garantir que as leveduras sejam viáveis. A sua viabilidade terá que ser avaliada pela confirmação por realização da cultura para fungos, visto que podem permanecer presentes no exame directo por um longo tempo, mesmo após o tratamento, sem no entanto serem viáveis. Portanto, não representam um bom parâmetro para controlo de cura. Exame Parasitológico de Feses A investigação da presença de parasitas nas fezes é realizada pela pesquisa de ovos ou larvas de helmintas, e nas infecções por protozoários, quando se encontram cistos ou oocistos nas fezes. O exame parasitológico de fezes frescas possui uma excelente especificidade. Entretanto, a sua sensibilidade só será adequada (95%) se forem solicitados exames de pelo menos três amostras de fezes em dias distintos. Portanto, um resultado negativo numa única amostra não elimina a possibilidade de uma parasitose. A positividade vai depender de diferentes factores. O estadio da infecção, o ciclo do parasita, da eliminação intermitente de formas de resistências, da intensidade do parasitismo e o exame propriamente dito, que utiliza apenas uma pequena amostra de todo o material colhido, são alguns dos factores que interferem na possibilidade de o exame se revelar positivo. Além disso, algumas parasitoses necessitam de exames especiais para serem identificadas, como por exemplo o Enterobius vermicularis, sendo também o caso da investigação da presença de trofozoitos. São necessárias fezes frescas colhidas no frasco de plástico. No caso de fezes sólidas ou pastosas, a quantidade deverá corresponder a 5 colheres plásticas fornecidas com o frasco de colheita. Se as fezes estiverem liquefeitas, pelo menos 10 ml deverão ser fornecidos ao laboratório para análise. As fezes deverão ser colhidas originalmente num recipiente limpo e a seguir transferidas para o frasco fornecido pelo laboratório. O paciente não deve estar a fazer laxantes ou ter sido submetido a contrastes radiológicos nos 3 dias anteriores à colheita. Durante a colheita, é importante evitar a contaminação pela urina, pois a sua presença acelera a fermentação bacteriana, prejudicando a conservação.
93 ACHADOS PATOGÉNICOS MAIS FREQUENTES ACHADOS NÃO PATOGÉNICOS Ascaris lumbricoides Hymenolepis diminuta Chilomastix mesnillii Cryptosporidium sp. Hymenolepis nana Endolimax nana Dietamoeba fragilis Isospora beli Entamoeba coli Entamoeba Strongyloides histolytica stercolaris Iodamoeba butschlii Enterobios vermicularis Trichuris trichiura Giardia lamblia Schistosoma mansoni Exame Parasitológico de Feses/ MIF Como estão presentes amostras de fezes de 3 dias diferentes, a sensibilidade do exame aumenta. É útil na pesquisa de estrutura de resistência de helmintas (ovos e larvas) e protozoários (cistos e oocistos). As amostras de fezes são colhidas durante 3 dias consecutivos ou não (emissões diferentes), em líquido conservante MIF (Merthiolate-Iodo-Formol). No casos de fezes sólidas ou pastosas, deverá ser considerada como medida uma colher fornecida com o frasco de colheita de cada emissão. Se as fezes estiverem liquefeitas, deverão ser colhidos aproximadamente 2 ml de cada emissão. As fezes deverão ser colocadas num frasco com líquido conservante (MIF), tendo-se o cuidado de colocar pequenas porções de fezes de 3 emissões diferentes, misturando bem todas as fezes. Deve-se evitar encher demais o frasco, pois as fezes devem ficar totalmente cobertas pelo líquido conservante. Manter em local fresco. Contra-indicados laxantes e enemas. O paciente não deve ter sido submetido a contrastes radiológicos nos 3 dias anteriores à colheita. Factor Reumatóide O termo factor reumatóide (FR) engloba um grupo de auto-anticorpos das classes IgG, IgM e IgA que tem em comum a capacidade de reagir com diferentes epítopos da porção Fc da molécula da imunoglobulina G humana. Apesar da pequena evolução no conhecimento dos mecanismos de ligação do FR aos auto-antigénios e do seu envolvimento no processo patológico típico da artrite reumatóide (AR), o FR IgM pode servir como marcador precoce na AR, apoiando-se em dados que demonstram que o risco de desenvolvimento de AR aumenta de forma proporcional ao aumento da concentração de FR em indivíduos normais. Os pacientes com artrite que cursam com FR positivo, principalmente quando se encontram em concentrações elevadas, correm maior risco de apresentar complicações clínicas e uma menor resposta à terapia. O FR está presente em cerca de 50-90% dos casos de AR clássicos, alguns meses após o início da doença, e dessa percentagem, 17% em média apresentam-se negativos nas fases mais precoces da doença. Durante a fase activa, são encontradas concentrações mais elevadas, que começam a decair à medida que o paciente evolui para a remissão clínica, mantendo-se positivas em níveis baixos e estáveis e tornando a elevar-se nos períodos de reactivação da doença. O FR está aumentado também em 75 a 95% dos quadros de síndrome de Sjögren, em 50 a 60% dos pacientes com doença mista do tecido conjuntivo (DMTC), em 15 a 35% dos casos de lúpus eritematoso sistémico (LES), em 20 a 30% dos casos de
94 esclerodermia, noutros casos de colagenoses e noutras patologias, como nefropatia e crioglobulinemia. Sabe-se hoje que o FR não é produzido apenas sob condições patológicas, e uma pequena parcela da população normal, especialmente os idosos, pode apresentar positividade para FR. Essas percentagens de incidência, tanto nas patologias como nos pacientes normais, assim como a ocorrência de falsos positivos, variam de acordo com a sensibilidade e a especificidade do método utilizado. Os ensaios tradicionais para investigação do FR empregavam partículas de látex revestidas por imunoglobulina G humana (prova do látex) ou, na hemaglutinação indirecta, hemácias de carneiro, revestidas por imunoglobulina de coelho (reacção de Waller-Rose). A prova do látex era considerada mais sensível, e a reacção de Waller- Rose, mais específica. Realizadas em conjunto, forneciam dados complementares. Actualmente, o método de referência para a pesquisa do FR é a nefelometria, que fornece um resultado numérico em UI/mL, em vez dos resultados em títulos, resultantes de diluições fornecidas pelo método anterior (látex), o que permite um melhor acompanhamento dos pacientes. Com a nefelometria, podem ser identificadas três classes de auto-anticorpos, isto é o FR das classes IgG, IgM e IgA. A identificação e a quantificação da classe do FR que se encontra elevada podem ser realizadas pelo método de ensaio imunoenzimático. A utilidade clínica dessa individualização e quantificação tem sido cada vez mais explorada. Por exemplo, a presença de FR IgA nas manifestações extra-articulares da AR com ausência de FR IgM ou IgG; a predominância na AR de FR IgM, sendo que o FR IgG e IgA estão geralmente presentes, mas em baixa frequência e quantidade. É rara a detecção concomitante do FR das três classes noutra patologia que não a artrite reumatóide. Afoiçameto das Hemácias ou Faucização das Hemácias O teste de afoiçamento reproduz in vitro as condições de baixa tensão de oxigénio que levam as hemácias que contêm hemoglobina S a sofrerem falcização. Para isso, são utilizadas substâncias redutoras, como o metabissulfito de sódio. É importante lembrar que o teste é positivo para anemia falciforme, na presença de traço falcêmico e também para algumas outras variantes anormais da hemoglobina, como a Hb Bart e a HbC Harlem. O teste pode ser falsamente negativo em baixas concentrações de HbS e em altas concentrações de Hb fetal. Fenitoína Trata-se de uma droga anticonvulsivante, utilizada no tratamento da epilepsia, de outros estados convulsivos secundários e nalguns casos de intoxicação digitálica e arritmias cardíacas. Actua modulando o canal sináptico de sódio e prolongando a inactivação, o que reduz a habilidade do neurónio de responder à alta frequência. O efeito fisiológico dessa acção é a redução da transmissão sináptica central, ajudando ao controlo de excitabilidade dos neurónios anormal. A absorção do fármaco é lenta e por vezes incompleta. Cerca de 90% do fármaco está ligada a proteínas. Apenas a fracção livre (cerca de 10%) é biologicamente activa. É metabolizada no fígado, sendo a maior parte excretada na bilis na forma de metabolitos inactivos, que são reabsorvidos no intestino e excretados na urina.
95 Independentemente de estar nos níveis normais, a fenitoína pode interferir na ação de outros fármacos como anticoagulantes orais, ciclosporina, teofilina e contraceptivos orais. Pode diminuir a concentração sérica ou a eficácia de outras drogas, como a carbamazepina, ácido valpróico, primidona, corticosteróides, dopamina e cloranfenicol. Níveis baixos são encontrados, geralmente, nos casos de não-adesão ao tratamento ou de utilização inadequada pelo paciente. Os problemas de absorção são mais frequentes e importantes em crianças, especialmente até os primeiros 3 meses de vida. Níveis elevados encontrados em pacientes com uso crónico e adequadamente monitorizados, sem alteração da posologia, podem ocorrer por interacções medicamentosas ou infecções. As drogas que podem interagir, elevando os níveis séricos de fenitoína, são, entre outras, antidepressivos tricíclicos, cloranfenicol, cimetidina, amiodarona, sulfas, fenilbutazona, etanol, halotano e metronidazol. Os valores de pico normalmente aparecem entre 4 a 5 horas após a última dose. Entretanto, a grande variação inter-individual de metabolização faz com que os níveis do fármaco necessários para alcançar os níveis terapêuticos e os momentos de pico sejam extremamente variáveis. A semi-vida é de 20 a 40 horas nos adultos e de cerca de 10 horas nas crianças. São considerados níveis terapêuticos valores entre 10 a 20 mg/ml. Entretanto, como já citado, a grande variação individual tanto na absorção quanto na velocidade de metabolização do fármaco faz com que esses valores possam variar de paciente para paciente, sendo aceite como nível terapêutico ideal aquele que não apresente efeitos tóxicos e no qual não ocorram convulsões. Os efeitos tóxicos manifestam-se por sonolência, ataxia, nistagmo, diplopia, disartria e confusão mental. Apesar das variações individuais, raramente se observam sinais clínicos abaixo dos valores definidos como terapêuticos. O nistagmo geralmente apresenta-se com valores acima de 20 mg/ml. Já a ataxia é observada mais frequentemente em níveis entre de 25 a 30 mg/ml, e a disartria e a sonolência, em níveis de 40 mg/ml Recomenda-se que a colheita seja realizada imediatamente antes da dose seguinte e com níveis estáveis (cerca de 7 dias de tratamento), ou a qualquer hora, caso se suspeite de intoxicação. Fenobarbital É um barbitúrico de acção prolongada, frequentemente utilizado no tratamento dos quadros de convulsões tónico-clónicas generalizadas e convulsões parciais simples com sintomas motores, formas de epilepsia focal, bem como na ansiedade e na insónia. A monitorização dos níveis séricos é fundamental para se obterem os melhores níveis terapêuticos, evitando-se os efeitos colaterais. Ou seja, é importante para individualizar a posologia de cada paciente. Níveis baixos são encontrados frequentemente por não adesão ao tratamento. Porém, algumas interações medicamentosas também podem levar a concentrações séricas baixas. Níveis séricos elevados são encontrados com o uso concomitante de ácido valpróico, que inibe o metabolismo do fenobarbital, e nos casos de doses inadequadas.
96 O fenobarbital é metabolizado pelo fígado e tem uma semi-vida longa, de 50 a 140 horas, o que leva ao risco de doses cumulativas. Cerca de 40 a 50% está ligado à proteína. O fenobarbital pode afetar o metabolismo da fenitoína, acelerar a clearance de eliminação do cloranfenicol, teofilina, anticoagulantes orais, ciclosporina e contraceptivos orais. Pode diminuir a concentração sérica ou o efeito da fenilbutazona, griseofulvin, beta-bloqueadores, teofilina, corticóides, antidepressivos triciclícos, quinidina, haloperidol e propoxifeno. A furosemida, o ácido valpróico e os salicilatos podem inibir o metabolismo do fenobarbital, levando a um aumento de sua concentração sérica. A sua actividade é aumentada quando associada ao uso de bebidas alcoólicas, anti-histamínicos, neurolépticos e antidepressivos tricíclicos. O uso de fenobarbital acelera a degradação de outros agentes antiepilépticos, anticoagulantes orais, neurolépticos e contraceptivos orais. O uso de fenobarbital pode levar ao aumento da fosfatase alcalina, da gama GT e à diminuição da bilirrubina e do cálcio sérico. O fenobarbital aumenta o metabolismo da bilirrubina por indução enzimática e pode ser utilizado nos casos de hiperbilirrubinémia congénita (não- hemolítica, familiar, não-obstrutiva). Os pontos de equilíbrio são alcançados nos adultos em 10 a 25 dias e, em crianças, entre 7 a 17 dias. A média é de 14 a 21 dias. O pico é atingido entre 6 a 18 horas após a administração. Os efeitos colaterais mais frequentes são sonolência, nistagmo, ataxia e disartria. Em doses elevadas, pode provocar o aumento da frequência das convulsões. Recomenda-se que a colheita seja realizada imediatamente antes da dose seguinte e com níveis estáveis (cerca de 7 dias de tratamento), ou a qualquer hora caso se suspeite de intoxicação. Ferritina A ferritina é a mais importante proteína de reserva do ferro e é encontrada em todas as células, especialmente naquelas envolvidas na síntese de compostos férricos e no metabolismo e na reserva do ferro. O doseamento da ferritina é o mais fiel indicador da quantidade de ferro armazenada no organismo. A sua grande utilidade clínica está no diagnóstico diferencial entre as anemias hipocrómicas e microcíticas por deficiência de ferro de anemias por outras etiologias. Nesses casos, a ferritina diminui antes das alterações dos níveis de ferro sérico e das alterações morfológicas da série vermelha. Entretanto, por fazer parte do grupo de proteínas de fase aguda, a ferritina elevase em resposta a infecções, traumatismos e inflamações agudas. A elevação ocorre nas 24 a 48 horas iniciais, com um pico no terceiro dia, e mantém-se por algumas semanas, o que pode dificultar a sua interpretação. Os seus níveis podem elevar-se no excesso de ferro, em pacientes transfundidos e em neoplasias, especialmente nas leucemias e linfomas e nos carcinomas de mama, fígado, pulmão, cólon e próstata. Elevam-se também nas anemias hemolíticas e megaloblásticas e nas lesões hepáticas, especialmente as lesões alcoólicas. Cerca de 25% dos pacientes com hepatite crónica têm aumento da ferritina.
97 Ferro O ferro é absorvido principalmente na parte superior do duodeno e no jejuno. Uma vez absorvido, liga-se à transferrina plasmática. A maior parte do ferro circulante é captada pelos precursores eritróides na medula óssea para formar a hemoglobina. A hemoglobina utiliza cerca de 80% do ferro corporal. O restante é armazenado no interior das células reticulares da medula óssea, baço e fígado, 60% sob a forma de ferritina e cerca de 40% como hemossiderina. Portanto, a distribuição do ferro corporal é feita entre compartimentos: o funcional - hemoglobina, mioglobina, enzimas heme e não-heme, o de transporte - transferrina - e o de reserva - ferritina e hemossiderina. A maior parte do ferro corporal é proveniente da dieta. É ingerido no estado férrico e, para a sua absorção, precisa estar na forma reduzida (ferroso). Por isso, a absorção é influenciada por factores redutores gastrointestinais, ph gástrico e composição da dieta, como a presença de ácido ascórbico, que mantém o ferro no estado ferroso. Outra fonte do ferro é a proveniente do processo de degradação da hemoglobina, quando o ferro é libertado da hemoglobina e retorna à transferrina plasmática. Ao contrário de outros elementos, a homeostase do ferro é regulada pelo controlo da absorção, estando directamente relacionada às reservas de ferro e ao nível de eritropoiese. Quando as reservas de ferro diminuem ou o nível de eritropoiese aumenta, a taxa de absorção de ferro aumenta de forma compensatória. Os sinais clínicos da deficiência de ferro resultam de um longo período de desequilíbrio no balanço de ferro. Inicialmente ocorre uma depleção das reservas, sem alterações nos níveis de ferro sérico, o que pode ser evidenciado pela redução dos níveis de ferritina. Essa diminuição das reservas leva ao aumento da absorção intestinal de ferro. Num segundo momento, com as reservas já depletadas, mas com o nível de hemoglobina ainda normal, algumas alterações podem já ser evidenciadas, como a presença de hemácias microcíticas no exame do sangue periférico, mesmo com volume corpuscular médio (VCM) normal, presença de anisocitose, diminuição da saturação de transferrina e da ferritina e aumento do TIBC (capacidade total de combinação do ferro). Finalmente, os níveis de hemoglobina começam a cair, instalando-se um quadro clássico de anemia ferropriva, com diminuição do ferro sérico, da hemoglobina, do VCM, da saturação da transferrina e da ferritina. A deficiência de ferro pode ocorrer por diferentes mecanismos: - Por aumento das necessidades, como ocorre na gravidez, na lactação e na fase de rápido crescimento. - Por diminuição da ingestão, numa dieta pobre em proteínas animais. - Por diminuição da absorção, como nos casos de cirurgias ou de patologias que levem a má absorção. - Por perda excessiva, como sangramentos agudos ou crónicos. A perda sanguínea constitui a causa mais importante de deficiência de ferro em adultos. Nos homens e nas mulheres na pós-menopausa, quase sempre é consequência de perda sanguínea pelo tubo gastrointestinal, causada por patologias benignas e malignas. O uso crónico de medicamentos como antiinflamatórios, corticoesteróides, salicilatos e também o uso de álcool podem causar ou agravar os quadros gastrointestinais. Nas mulheres, a hemorragia vaginal é também um factor importante.
98 Quando a perda é aguda, leva a uma anemia normocrómica e normocítica, e, quando crónica, a uma anemia microcítica hipocrómica. A hemorragia crónica quase sempre esgota as reservas corporais de ferro, pelo esforço contínuo da medula em restaurar os níveis circulantes de hemoglobina. A pesquisa de sangue oculto é um exame importante na investigação dos pacientes com anemia ferropriva e deve ser realizada em amostras múltiplas para impedir a possibilidade de negatividade quando as perdas sanguíneas são intermitentes. A deficiência de ferro por ingestão inadequada quase sempre é subclínica. A infecção por ancilostomídeos é uma causa frequente de hemorragia. FERRO SÉRICO DIMINUÍDO Anemia Ferropriva Doenças Crónicas Neoplasias Hipermenoréia Hemorragias FERRO SÉRICO AUMENTADO Anemias Hemolíticas e Megaloblásticas Aplasias Medulares Necrose Hepática Maciça Hemocromatose - Hemossiderose Estrogenioterapia - Ferroterapia A única anemia microcítica e hipocrómica em que as reservas de ferro estão ausentes é a anemia ferropriva. Na maior parte dos casos, a avaliação dos indicadores como ferro baixo, TIBC aumentado, ferritina e saturação de transferrina diminuídas faz o diagnóstico. Entretanto, estes indicadores podem estar alterados na presença de neoplasias, infecções, processos inflamatórios, alcoolismo, desnutrição ou doença hepática, prejudicando a avaliação. A determinação concomitante do ferro sérico e da transferrina permite a avaliação da percentagem de saturação da transferrina, que é o melhor índice de avaliação do armazenamento do ferro. A avaliação da capacidade de fixação do ferro (TIBC) aumenta em resposta à diminuição do ião. Deficiência de ferro Infecções Crónicas Neoplasias Menstruação Gravidez Hepatites Nefropatias Talassemia FERRO TIBC Adaptado da tabela: Clinical Diagnosis and Management, by Laboratory Methods- 19º edição N SATURAÇÃO DA TRANSFERRINA, N Fibrinogénio O fibrinogénio (Factor I) é uma glicoproteína sintetizada no fígado e está envolvida na etapa final da coagulação, que consiste na sua conversão em fibrina, sob a acção da trombina. Além do seu papel na coagulação, é uma importante proteína na resposta de fase aguda. Portanto, pode estar elevado em diferentes patologias, como processos inflamatórios e infecciosos agudos, traumas, neoplasias, pós-operatório, uso de anticoncepcionais orais e síndrome nefrótico. Encontra-se também elevado por influências genéticas, na gravidez e no tabagismo. No entanto, pode estar reduzido
99 devido à diminuição da produção hepática, em doenças hepáticas graves, ou por aumento de consumo, com conversão excessiva do fibrinogénio em fibrina, sem tempo para reposição adequada, como nos quadros de coagulação intravascular disseminada. Pode também apresentar-se diminuído nos casos de fibrinólise primária e secundária e devido ao uso de agentes fibrinolíticos. Já foram identificadas diversas variantes hereditárias do fibrinogénio (disfibrinogenemia). Os quadros podem variar entre alterações hemorrágicas, tendência a distúrbios trombóticos ou indivíduos assintomáticos. A disfibrinogenemia adquirida está associada a doenças hepáticas ou renais. A sua avaliação tem um papel importante no diagnóstico diferencial das coagulopatias adquiridas, na coagulação intravascular disseminada, na fibrinólise primária e secundária, na disfibrinogenemia e na afibrinogenemia. Fosfatase Ácida As maiores concentrações da fosfatase ácida ocorrem na próstata, no fígado, na medula óssea, nos eritrócitos e nas plaquetas. Os pacientes com carcinoma da próstata confinados dentro da cápsula, normalmente apresentam níveis normais da fosfatase ácida sérica; já nos casos com metástases, mais da metade dos pacientes apresenta níveis elevados. Níveis alterados podem também ser observados em pacientes com hipertrofia benigna de próstata, retenção urinária e após manipulação prostática. A fracção não-prostática encontra-se fisiologicamente elevada nas crianças em fase de crescimento e patologicamente aumentada em condições em que existe um hipermetabolismo ósseo. Valores elevados são encontrados na doença de Paget e noutras patologias ósseas, no hiperparatiroidismo, nas metástases ósseas como no carcinoma da mama, do pulmão, da tiróide, nos mielomas e em situações de grande destruição de eritrócitos e de plaquetas. Elevam-se também em doenças metabólicas como doença de Gaucher, doença de Niemann-Pick e em leucemias e outras patologias hematológicas. Consultar Fosfatase Ácida Prostática. Fosfatase Ácida Prostática A fosfatase ácida de maior importância clínica é a derivada da próstata. Dada a importância clínica do aumento do nível sérico da fosfatase ácida no diagnóstico e na monitorizaação da resposta ao tratamento e no aparecimento de metástases no carcinoma da próstata, é necessário diferenciar-se especificamente entre aumentos nas concentrações das fosfatases de origem prostática das formas de origem nãoprostática. Certos inibidores podem aumentar a discriminação entre as duas formas. A fracção prostática é fortemente inibida pelo tartarato, e a fração não-prostática é resistente ao tartarato. Dessa forma, podemos obter valores mais específicos para o acompanhamento dos casos de carcinoma prostático. Devemos lembrar que a fosfatase ácida libertada pelas plaquetas apresenta resposta à inibição semelhante à de origem prostática. Os pacientes com carcinoma de próstata confinados dentro da cápsula normalmente apresentam níveis normais da fosfatase ácida sérica; já nos casos
100 com metástases, mais da metade dos pacientes apresenta níveis elevados. Níveis alterados podem ser observados em pacientes com hipertrofia benigna de próstata, retenção urinária de monta e após manipulação prostática. Fosfatase Alacalina É uma enzima presente em praticamente todos os tecidos do organismo, especialmente nas membranas das células dos túbulos renais, ossos (osteoblastos), placenta, trato intestinal e fígado. Portanto, a fosfatase alcalina encontrada no soro é resultado da presença de diferentes isoenzimas originadas em diferentes órgãos, com predomínio das fracções ósseas e hepáticas. Embora até hoje a sua função ainda não esteja bem definida, a fosfatase alcalina parece estar envolvida no transporte de lípidos no intestino e nos processos de calcificação óssea. A fosfatase alcalina óssea e a hepática partilham proteínas estruturais, codificadas por um mesmo gene. A fosfatase intestinal só se expressa em indivíduos dos grupos sanguíneos Lewis O e B. Além das isoenzimas conhecidas - óssea, hepática, intestinal e placentária -, podem ser encontradas isoformas patológicas, como a carcioplacentária ou Regan, que ocorre por uma depressão do gene da fosfatase placentária em neoplasias (do ovário, do pulmão, trofoblásticas, gastrointestinais, seminomas e doença de Hodgkin). Outras isoformas incomuns têm sido descritas em várias neoplasias. Na prática clínica, a grande utilidade está na investigação de doenças hepatobiliares e nas doenças ósseas que cursam com aumento da actividade osteoblástica. Como é totalmente excretada pela bilis, durante muito tempo pensou-se que sua elevação nas patologias hepatobiliares resultava da falência de excreção da enzima. Hoje sabe-se que a resposta hepática a qualquer tipo de agressão da árvore biliar é sintetizar a fosfatase alcalina principalmente nos canalículos biliares. Isto explica a sua marcada elevação nas patologias biliares. A elevação tende a ser maior nas obstruções extra-hepáticas (litíase e carcinoma da cabeça de pâncreas) do que nas intra-hepáticas (processos invasivos). Isto acontece devido a uma combinação do aumento de produção associado a uma diminuição da excreção. Por isso, é considerada um marcador importante para processos obstrutivos hepáticos. Níveis elevados podem ser também encontrados noutras lesões hepáticas activas e nas infiltrativas com níveis mais moderados de elevação. Está aumentada nos carcinomas hepáticos primários e secundários. Nas doenças ósseas, o maior aumento dos níveis séricos da fosfatase alcalina aparece na doença de Paget (valores de 10 a 25 vezes o normal). Níveis moderadamente elevados podem ser encontrados na osteomalácia, nalguns tumores ósseos e no hiperparatiroidismo primário e secundário. As fracturas ósseas levam a um aumento transitório, e na osteoporose os valores são normais. Nas neoplasias, os níveis da fosfatase alcalina são úteis para avaliar a presença de metástases envolvendo fígado e osso. Valores muito elevados são observados em pacientes com lesões osteoblásticas como as encontradas no carcinoma da próstata com metástases ósseas. Elevações menores são observadas quando as lesões são osteolíticas, como as encontradas no carcinoma metastático da mama. Outras condições malignas com infiltração hepática como leucemias, linfomas e sarcoma podem cursar também com elevação da fosfatase alcalina. Recém-nascidos e crianças, mas especialmente adolescentes, apresentam valores
101 significativamente mais elevados do que os adultos, devido ao crescimento ósseo. Durante a fase de crescimento rápido da adolescência (puberdade), são encontrados níveis extremamente elevados. Normalmente, os valores são discretamente mais elevados nos homens do que nas mulheres, e essa diferença desaparece durante e após a menopausa. Na população idosa, existe uma diminuição dos níveis séricos habitualmente encontrados, como consequência do aumento da incidência de osteoporose nessa faixa etária. Níveis elevados, duas a três vezes os valores de referência, podem ser encontrados durante a gravidez, especialmente no terceiro trimestre, devido à produção placentária. Níveis diminuídos podem ser encontrados no hipotiroidismo, na anemia perniciosa, nas hipofosfatémias e no uso de fármacos como contraceptivos orais. Aumento dos níveis séricos podem ser encontrados após uma refeição com alimentos ricos em gordura, especialmente em pacientes do grupo sanguíneo O ou B, devido à elevação da fracção intestinal. Recomenda-se portanto que seja avaliada sempre em jejum. ALGUMAS CAUSAS DE FOFATASE ALCALINA ELEVADA PUBERDADE GRAVIDEZ CRIANÇAS DOENÇA DE PAGET ACROMEGALIA SARCOMA HIPERPARATIROIDISMO OSTEOMALÁCIA MIELOFIBROSE HIPERNEFROMAS LEUCEMIAS MIELOMA ALCOOLISMO CIRROSE CIRROSE BILIAR PRIMÁRIA COLANGITES COLANGITES AUTO-IMUNES COLEDOCOLITÍASE CA DO PÂNCREAS COLECISTITES COLANGITES CA HEPÁTICO METÁSTASES HEPÁTICAS METÁSTASES ÓSSEAS SARCOIDOSE AMILOIDOSE ABCESSOS HEPÁTICOS HEPATITES DROGAS COLESTÁTICAS PANCREATITE Fosfatase Alacalina Óssea Os ossos encontram-se em constante processo metabólico de remodelação. Este, inclui a degradação e reabsorção ósseas, que são mediadas pelos osteoclastos, e os processos de estruturação e formação óssea mediada pela acção dos osteoblastos. A remodelação óssea é necessária para a manutenção da saúde global e da firmeza da trama óssea. Para isso, é importante um equilíbrio entre os processos de reabsorção e formação ósseas. Em estados de alteração do metabolismo ósseo, estses processos dissociam-se, ou seja, perdem o equilíbrio. Quando a reabsorção excede a formação, leva a uma perda de osso que pode conduzir a osteoporose ou a doenças do tecido ósseo, como as lesões da doença de Paget. A utilização de marcadores bioquímicos específicos para esses eventos de remodelação fornece dados analíticos em relação à taxa de metabolismo, ou seja, do turn-over ósseo. A fosfatase alcalina óssea é uma glicoproteína específica encontrada na superfície dos osteoblastos. A sua função ainda não é de todo conhecida, porém o seu papel na mineralização do esqueleto está confirmada. A avaliação da actividade sérica da fosfatase alcalina óssea é um marcador de turnover ósseo que fornece informações úteis da remodelação óssea na osteoporose, na doença de Paget e na monitorização de terapias preventivas e de reposição hormonal ou de outras terapias. A osteoporose é uma doença do metabolismo ósseo caracterizada pela remodelação
102 óssea anormal. Esta remodelação conduz a uma baixa da massa óssea e a uma deterioração da microarquitetura do tecido ósseo, com aumento consequente da suscetibilidade para fracturas. O tipo mais comum de osteoporose acontece nas mulheres na menopausa, como resultado da deficiência de estrogénio produzida pela cessação da função ovariana. A restauração dos níveis de estrogénio àqueles compatíveis com a fase pré-menopausa, através da terapia de reposição hormonal, previne a perda óssea e consequentemente a osteoporose. A osteoporose pode também resultar de um pico de ganho de massa óssea inadequado durante a fase de crescimento - um desequilíbrio ósseo relacionado à idade, que remodela com excesso de reabsorção - e várias condições clínicas e terapias que induzem a perda óssea ou a remodelamento ósseo desequilibrado, incluindo doenças endócrinas como hipogonadismo, hipertiroidismo, hiperparatiroidismo, hipercortisolismo, falência renal, metástases ósseas, doenças gastrointestinais relacionadas com a nutrição e metabolismo mineral, doenças do tecido conjuntivo, mieloma múltiplo, imobilização crónica, alcoolismo, tabagismo e terapia crónica com heparina e corticóides. A doença de Paget tem etiologia ainda desconhecida, porém hipóteses de etiologias envolvendo factores genéticos e víricos têm sido apontadas. É uma desordem óssea focal que produz dor e deformidade, com elevadas taxas de actividade de remodelação óssea. As lesões ocorrem principalmente no cránio, coluna vertebral, pelve e ossos longos, e podem resultar em fracturas e comprometimento neurológico. Fósforo O fósforo é um dos constituintes mais abundantes do organismo, presente em diferentes tecidos. Num adulto normal, a maior parte encontra-se no osso, e o restante, nos tecidos moles e ligados a proteínas, lìpidos e carbohidratos. Participa em diferentes processos metabólicos e está presente como fosfolípido em todas as membranas celulares. A sua homeostase depende basicamente do controle da absorção (intestino delgado), filtração e reabsorção renal e da reserva que é armazenada no osso. Cerca de 80 a 90% do fósforo ingerido é absorvido de forma activa no intestino. A absorção é aumentada na diminuição da ingestão de cálcio, na acidez do conteúdo intestinal e também pela acção da vitamina D e da hormona de crescimento. A maior parte do fósforo absorvido é excretada na urina. É filtrado pelos glomérulos e reabsorvido em grande parte pelo túbulo proximal, de modo que apenas cerca de 10 a 15% do fósforo filtrado alcança o túbulo distal. Nas situações em que há diminuição da filtração de fósforo, ocorre aumento da reabsorção tubular, e, ao contrário, quando aumenta a carga filtrada, diminui a reabsorção e aumenta a depuração. Nos casos de lesão renal, à medida que a taxa de filtração glomerular diminui, o fósforo é retido, reduzindo discretamente o nível de cálcio sérico, o que estimula as paratiróides a secretar a paratormona (PTH). A ação da PTH no sistema tubular reduz a reabsorção, na tentativa de restaurar os níveis normais de cálcio e de fósforo. Com a evolução da lesão renal, a fracção de fósforo reabsorvido pelo sistema tubular diminui, mantendo a depuração de fósforo constante, e por conseguinte os níveis séricos normais. Quando a taxa de filtração chega a níveis muito baixos, cerca de 20 ml/min, a excreção de fósforo não se mantém mais, devido a esse mecanismo de compensação, levando a uma elevação do fósforo sérico.
103 Os mecanismos de regulação do cálcio afetam também os níveis de fósforo, sendo os seus valores directamente relacionados: a elevação de um significa a diminuição do outro. Os níveis séricos de fósforo oscilam ao longo do dia: valores mínimos são observados entre as 9 e as 12 horas, aumentando gradualmente até atingir um platô à tarde, e apresentando um discreto pico em torno da meia-noite. Os níveis de fósforo são mais altos nas crianças, e tendem a elevar-se nas mulheres após a menopausa. Aumentam também com o exercício e na desidratação. Os valores séricos diminuem com a ingestão de carbohidratos e aumentam com a ingestão de fósforo, sendo portanto fundamental que a colheita seja realizada em jejum. O aumento do fósforo sérico ocorre pela diminuição da filtração glomerular, aumento da reabsorção tubular renal e aporte exógeno ou endógeno. A diminuição ocorre por doenças tubulares e aumento das perdas. Alterações nos níveis da hormona paratiroidéia afectam a reabsorção renal do fósforo. São causas de aumento dos níveis de fósforo no soro: desidratação, hipovolemia, acromegalia, hipoparatiroidismo, pseudo-hipoparatiroidismo, hipervitaminose D, metástases ósseas, sarcoidose, cirrose, embolia pulmonar, falência renal, após manobras de ressuscitação e cetoacidose diabética. Valores séricos diminuídos são encontrados no uso de diuréticos, antiácidos, hiperparatiroidismo primário, septicémia, deficiência de vitamina D, acidose tubular renal, síndrome de Fanconi, hemodialisados crónicos, após episódios de vómitos, osteomalácia e por outras causas que levem à elevação de cálcio no soro. Níveis urinários aumentados de fósforo podem ser encontrados no hiperparatiroidismo, na acidose tubular renal e no uso de diuréticos. Níveis diminuídos são encontrados no hipoparatiroidismo e no pseudo-hipoparatiroidismo. Fragilidade Osmótica Quando em meio hipotónico, os eritrócitos normais são capazes de resistir à hemólise, aumentando o seu volume. A variação da forma leva a variação da espessura das membranas dos eritrócitos, alterando a sua capacidade de resistir à lise celular por variações da pressão osmótica do meio onde se encontram. Os esferócitos têm fragilidade osmótica aumentada, pois apresentam uma membrana mais escassa do que a membrana de um eritrócito normal, o que os impede de acumular água no seu interior. Já os reticulócitos têm mais membrana, o que os torna capazes de resistir melhor à hemólise, mostrando assim menor grau de fragilidade osmótica. Na curva de fragilidade osmótica, os eritrócitos são submetidas a concentrações crescentes de cloreto de sódio. A percentagem de hemólise é avaliada pela quantidade de hemoglobina livre na solução. Frutosamina Além da HbA, a glicose pode ligar-se a outras proteínas e globulinas por meio de uma glicosilação não-enzimática. A proteína total, que após a ligação com a glicose, se transforma numa cetamina estável, é denominada genericamente frutosamina. Devido à sua semi-vida curta, de cerca de 30 dias, os resultados obtidos indicam a média das glicemias nas 2 últimas semanas (1 a 3).
104 Os valores podem ser alterados em situações de perda ou diminuição da semi-vida das proteínas. Não deve ser utilizada como diagnóstico e sim como monitorização do controle da diabetes mellitus. Os resultados dos doseamentos de frutosamina devem ser analisados juntamente com os resultados de glicose e da hemoglobina glicosilada. A frutosamina mostrase elevada em todos os casos de diabetes fora de controle metabólico, independentemente dos valores da glicemia de jejum. Os seus valores retornam aos níveis de referência 20 dias após a estabilização da glicemia em níveis adequados. É útil no acompanhamento de casos de pacientes portadores de hemoglobinopatias que interferem no doseamento da hemoglobina glicosilada. Gama Glutamil Tanspeptidase (GGT) A gama glutamil transpeptidase ou transferase (GGT) é uma enzima presente nas membranas celulares e nas fracções microssómicas envolvidas no transporte de aminoácidos através da membrana celular. Está presente em ordem decrescente de abundância no túbulo proximal renal, fígado, pâncreas e intestino. Os níveis séricos da GGT são principalmente de origem hepática. A sua semi-vida é de 7 a 10 dias, aumentando para 28 dias nas lesões hepáticas ligadas ao álcool. Os valores são aproximadamente 50% mais elevados nos homens do que nas mulheres, e são directamente proporcionais à massa corporal, ao consumo de álcool, ao fumo e ao nível de actividade física. Por mecanismos ainda não muito bem esclarecidos, pacientes com diabetes mellitus, hipertiroidismo, artrite reumatóide e doença pulmonar obstrutiva crónica frequentemente apresentam valores aumentados de GGT. Valores muito elevados são encontrados nos quadros de colestase crónica, como na cirrose biliar primária ou na colangite esclerosante e noutras patologias hepáticas e biliares. Apresenta-se elevada em alcoólatras, mesmo sem hepatopatia, na obesidade e no uso de fármacos como analgésicos, anticonvulsivantes, quimioterápios, estrogénio e contraceptivos orais. Nos períodos após enfarte agudo do miocárdio, a GGT pode permanecer alterada por semanas. Em estudos do gene humano, a GGT teve a sua sequência de nucleotídeos identificada. Deste modo, puderam ser identificadas três principais formas de GGT circulantes, que aparentemente, não são isoenzimas verdadeiras. Uma, de alto peso molecular, aparece nos soros normais, na obstrução biliar e, com mais frequência nos casos de neoplasia hepática. A segunda forma tem um peso molecular intermediário e apresenta duas fracções: uma detectável em hepatopatias, e a outra em obstruções das vias biliares. A terceira tem um baixo peso molecular e ainda não teve a sua função definida. Infelizmente, esses testes não estão disponíveis para uso clínico, pois o método ainda não apresenta sensibilidade e especificidade adequadas.
105 Gasimetria Arterial Para funcionarem normalmente, as actividades metabólicas necessitam de um ph mantido em condições ideais. Este factor depende da manutenção do equilíbrio ácido-base do organismo, obtido pela interacção dos mecanismos renais (controle de concentração de bicarbonato) e pulmonares (controle de concentração de CO 2 ). Consequentemente, o estado do equilíbrio metabólico depende de mecanismos respiratórios com uma troca gasosa adequada e boa oxigenação tecidual e um tamponamento fornecido pelo rins. Os distúrbios ácido-base que podem ocorrer são: acidose metabólica, acidose respiratória, alcalose metabólica e alcalose respiratória. Inicialmente, pode parecer que o conhecimento isolado da alteração da concentração de bicarbonato ou da concentração de pco 2 conduza, respectivamente, a um diagnóstico de alteração metabólica e respiratória. Entretanto, isto não é verdadeiro, visto que um distúrbio primário pode levar a uma alteração secundária compensatória, que no final leva à manutenção do ph para níveis adequados. Portanto, a análise do equilíbrio ácidobase depende da avaliação de um conjunto de diferentes parâmetros, que são representados pelo exame gasimetria arterial. Esses parâmetros são: - ph - pco 2 - bicarbonato - po 2 - saturação do O 2 - bases em excesso O primeiro parâmetro observado na análise da gasimetria arterial deve ser o ph. Independentemente dos demais parâmetros, o ph determina se o paciente se encontra em acidose ou alcalose. O valor limite do ph para essa definição é de 7,4. Valores abaixo deste são considerados acidose, e acima alcalose. Apenas após a avaliação desse parâmetro, outros, como bicarbonato e pco 2 poderão ser utilizados para diagnosticar se a origem dos distúrbio é metabólica ou respiratória. A concentração do bicarbonato, da pco 2 e do ph é interdependente. Portanto, a alteração de um dos parâmetros leva ao movimento compensatório dos demais, na busca do equilíbrio. Os níveis de bicarbonato associados aos mecanismos respiratórios de retenção e eliminação do CO 2 mantêm o equilíbrio ácido-base. SITUAÇÃO ph BIRCABONATO PCO 2 CAUSAS FREQUENTES Cetoacidose diabética, acidose láctica (sépsis por gramnegativos), insuficiência renal, Acidose <7.4 Baixo Baixa metabólica paragem cardio-respiratória e uso abusivos da aspirina. Acidose respiratória Acidose metabólica Acidose respiratória <7.4 Alto Alta >7.4 Alto Alta >7.4 Baixo Baixa DPCO, insuficiência respiratória, paralisia dos músculos respitetórios, pneumonia e lesões do SNC. Vómitos, outras causas de perda de ácido clorídrico e uso abusivo de diuréticos. Dor aguda e intensa, ansiedade, hiperventilação, estimulação não pulmonar do centro repirtório e uso de fármacos
106 Na acidose metabólica, a produção excessiva de ácido é tamponada pelo bicarbonato, que é consumido nesse processo, levando a um aumento da frequência respiratória para diminuir a pco 2 e compensar a perda de bicarbonato. Na alcalose metabólica, existe uma perda de ácido, com aumento da concentração do bicarbonato e de pco 2. Na acidose respiratória, o aumento da concentração de CO 2 leva a uma diminuição do ph, o que induz a uma retenção renal de bicarbonato para compensar a equação de equilíbrio. A avaliação da po 2 é importante para avaliação do estado de perfusão tecidual. Importante também é a determinação da percentagem de saturação da hemoglobina pelo O 2. Valores baixos de um ou de ambos os parâmetros acima referidos, são indicação de patologia subjacente. A queda da po 2 leva a acidose metabólica. As principais causas dessa condição são: embolia pulmonar, enfarte agudo do miocárdio, anóxia tecidual secundária a estados de hipoperfusão como situações cirúrgicas, septicémia, choque ou insuficiência cardíaca grave, entre outras. Outra causa de hipoxia, são as situações que levam à retenção do CO 2, como as lesões pulmonares e a DPCO. O excesso de bases representa o cálculo realizado a partir dos valores de ph, de pco 2 e da concentração da hemoglobina, que significa o excesso ou o déficite de bases, permitindo avaliar a gravidade do distúrbio metabólico. O excesso de bases é encontrado nas alcaloses, e o déficite nas acidoses. Gastrina É uma hormona produzida pelas células G localizadas principalmente no antro e duodeno proximal. Existem várias formas moleculares de gastrina. A principal forma de gastrina na mucosa antral é um heptadecapeptídeo com 17 resíduos de aminoácidos (G-17) que representa 90% da gastrina produzida nessa região. Já na circulação, dois terços da gastrina sérica são representados por uma molécula maior, com 34 aminoácidos (G-34). Embora a G-17 tenha uma semi-vida mais curta que a G-34, ambas têm a mesma intensidade de estimulação da secreção gástrica. A sua avaliação é útil no diagnóstico do síndrome de Zollinger-Ellison, caracterizado por ulceração péptica severa do trato gastrointestinal com hipersecreção ácida gástrica, consequente à excessiva secreção de gastrina. Valores superiores a pg/ml associados a hipercloridria são praticamente diagnóstico da presença desse síndrome. Além do síndrome de Zollinger-Ellison, níveis elevados podem ser detectados também em situações que cursam com acloridria ou hipocloridria, como nas anemias perniciosas, na gastrite atrófica e no carcinoma gástrico. Nestes casos, os níveis não se encontram tão elevados quanto no Síndrome de Zollinger-Ellison. O teste dinámico com infusão de cálcio ou secretina tem um papel importante no diagnóstico diferencial entre as possíveis etiologias. A ingestão de aminoácidos, drogas como carboneto, cloreto de cálcio e insulina podem elevar os níveis de gastrina. Já o uso de atropina diminui os seus níveis séricos.
107 Genotipagem da Hepatite C Os vírus da hepatite C são um grupo de isolados ou linhagens com alto grau de variabilidade. Esta heterogeneidade também pode ser observada no próprio hospedeiro, do qual um simples isolado pode abrigar variantes víricas de múltiplas sequências, as quais mostram apenas 92% de similaridade nas regiões que codificam proteínas do envólucro. Isolados de determinados subtipos exibem similaridades nucleotídicas em torno de 80% para o genoma completo ou regiões não-estruturais, enquanto um ou mais subtipos podem ser classificados em alguns tipos principais com similaridades em torno de 68%. Os seguintes genótipos são caracterizados como principais tipos de HCV: 1, 2, 3, 4, 5, 6, 7, 8, 9, 10 e11. Estes são subdivididos em diferentes subtipos possíveis de serem analisados pela genotipagem para HCV: - 1a, 1b, 1c - 2a, 2b, 2c - 3a, 3b - 4a, 4b, 4c, 4d, 4e - 5a - 6a - 7a, 7b - 8a, 8b - 9a - 10a - 11a Evidências substanciais têm demonstrado a grande importância da tipagem e subtipagem para a clínica. Estudos indicam que a infecção pelo HCV genótipo 1b não apresenta resposta eficiente ao tratamento com interferon alfa (10% dos pacientes tratados com resposta favorável), enquanto para os genótipos 1a, 2a, 2b e 3a respondem de forma favorável (50 a 80% de resposta). Tem sido demonstrado que infecções por HCV genótipo 1b evoluem rapidamente para formas crónicas de hepatites, cirrose e carcinoma hepatocelular. A rápida evolução da doença hepática crónica e cirrose em órgão transplantado é observada para o subtipo 1b. A genotipagem para HCV é obtida com a utilização de métodos de biologia molecular e de sequenciamento genómico, os quais são úteis para definir os genótipos e subtipos para estudos de epidemiologia molecular, estudos clínicos e monitorização da hepatite C. Genotipagem para HIV Recentes avanços nos estudos sobre o HIV-1 orientados, principalmente, para a quantificação da carga viral em plasma e células mononucleares do sangue periférico de pacientes nos diferentes estádios da síndrome de imunodeficiência adquirida (SIDA) têm evidenciado que a infecção pelo HIV-1 é um processo dinámico, em que ocorre um equilíbrio entre a produção e a eliminação de partículas virais. Este processo é observado, inclusive, na fase de lactência clínica, caracterizada por ausência de sintomas, altos níveis de anticorpos circulantes e níveis baixos ou não-detectados de virémia. A associação à elevada taxa de mutação genómica do HIV-1 resulta no desenvolvimento de linhagens virais mutantes, que são mais eficazmente selecionadas sob condições de pressão selectiva exercida pelo sistema imunológico ou pela intervenção farmacológica
108 prolongada. Essas variantes HIV-1 não são reconhecidas pelos mecanismos imunes efectores (anticorpos neutralizantes e/ou linfócitos T citotóxicos) e podem apresentar mutações nos genes codificantes para as enzimas protease ou transcriptase reversa. Estas resultam em mutações de aminoácidos nas enzimas, selecionando, desta forma, variantes resistentes aos anti-retrovirais. Mutações no genoma do HIV que conferem resistência aos agentes anti-retrovirais têm sido relatadas para todos os compostos usados no tratamento de pacientes infectados. O início da infecção está associado a uma população homogenea de HIV que é, usualmente, sensível aos anti-retrovirais. No entanto, as altas taxas de mutação podem resultar em 106 variantes genéticas, entre as quais podem estar presentes, em baixos níveis, as resistentes aos anti-retrovirais, antes do início da terapia. O significado clínico da resistência aos anti-retrovirais não está ainda totalmente elucidado, porém atribui-se a ocorrência ao decréscimo na eficiência da quimioterapia anti-retroviral. A enzima transcriptase reversa é estudada mais extensamente para a intervenção farmacológica. Ela é essencial para a replicação do HIV-1, uma vez que a expressão das proteínas virais e a progénie viral dependem da conversão da cadeia simples de RNA em cadeias duplas de DNA e a subsequente integração do cdna viral ao genoma da célula hospedeira. Análogos aos inibidores nucleosídicos da transcriptase reversa 3'-azido-3'- desoxitimidina (AZT; zidovudina); 2',3'-didesoxinosina (ddi; didanosina); 2',3'- didesoxicitidina (ddc; zalcitabina); (-)-b-l- 2',3'-didesoxi-3'-tiacitidina (3TC; lamivudina) e 2',3'-didesidro-3'-desoxitimidina (d4t; estavudina) são os fármacos actualmente aprovadas para o tratamento da SIDA. Estes compostos actuam de modo semelhante, após activação metabólica por fosforilação efectuada por quinases intracelulares. As formas trifosfato resultantes, podem inibir a enzima transcriptase reversa por competição pelo substrato ou podem actuar como cadeias finais da reacção de transcrição reversa, inibindo a síntese do cdna viral. As mutações de resistência são divididas em primárias e secundárias. As primárias devem ser analisadas em separado, já que são directamente responsáveis pela diminuição acentuada na sensibilidade ao fármaco. Para utilização adequada da genotipagem para HIV-1 é necessária uma avaliação criteriosa dos resultados. As alterações nos códons abaixo podem definir resistência total ou parcial às medicações anti-retrovirais. Inibidores de transcriptase reversa análogos de nucleosídeos - T215YF, M41L, K70R, D67N, L210W, K219Q, M184VI, V1181, E44D, K65R, L74V, Y115F. Inibidores de transcriptase reversa não-análogos de nucleosídeos - K103N, V106A, V1081, Y181CI, Y188CLH, G190AS, P236L, L1001. Inibidores de protease - M461L, V82AFTS, 184V, L10FIRV, K20MR, L24I, V32I, M36I, 154V, A71VT, G73AS, V77I, L90M, N88D, 147V. Uma única mutação pode resultar em diferentes graus de sensibilidade viral ao quimioterápio. A mutação na posição 184, com substituição de metionina por valina, resulta num decréscimo de cerca de mil vezes na sensibilidade ao 3TC (alto
109 nível de resistência) e de quatro a oito vezes ao ddi e ao ddc (baixo nível de resistência). Trabalhos desenvolvidos por alguns investigadores têm evidenciado que o desenvolvimento de mutações associadas à resistência viral à zidovudina segue um padrão transitório: a mutação pode ocorrer primeiro em qualquer códon, enquanto mutações adicionais acumulam-se lenta e progressivamente durante a terapia. Outros investigadores têm observado, entretanto, que a resistência do HIV-1 à zidovudina desenvolve-se de forma ordenada: em indivíduos assintomáticos em tratamento com zidovudina, a mutação no códon 70 ocorre primeiro, mas é substituída pela mutação, mais estável, no códon 215. Com o tratamento prolongado, outras mutações nos códons 41, 67 e novamente 70 desenvolvem-se, conferindo ao HIV maior resistência à zidovudina. Isto ocorre apenas com a progressão da doença, uma vez que vírus altamente resistentes não têm sido isolados de amostras biológicas de indivíduos assintomáticos. Vários métodos laboratoriais têm sido utilizados para a detecção de mutações associados à resistência à zidovudina, incluindo técnicas de clivagem por RNAse e sistemas de hibridização RNA/RNA. Porém, a maioria dos estudos usa métodos fundamentados na reacção em cadeia da polimerase (PCR), na qual o segmento do genoma do HIV-1, codificado para transcriptase reversa e protease, é amplificado e utilizado numa segunda reacção, empregando-se pares de primers especificamente definidos para a amplificação de sequências de mutantes ou selvagens em códons de interesse. Os segmentos amplificados por PCR são sequenciados directamente utilizando-se sequenciadores fluorescentes automatizados. Outro método para a análise genotípica consiste no ensaio de hibridização com sondas (LIPA), que se baseia na detecção de um sinal colorimétrico não-radioactivo, emitido pela hibridização do produto de PCR do HIV-1 com sondas oligonucleotídicas, imobilizadas em fitas de nitrocelulose. Entretanto, uma restrição ao seu emprego é polimorfismos muito próximos, que dificultam a hibridização, impedindo a obtenção de resultados. Glicose A glicose é essencial para a função do cérebro e dos eritrócitos. O excesso de glicose é armazenado na forma de glicogénio no fígado e nas células musculares. A determinação de glicose no sangue é um dos exames mais solicitados aos laboratórios clínicos e tem como finalidade diagnosticar e acompanhar o tratamento
110 de portadores de algum distúrbio no metabolismo de carbohidratos que levem a situações de hipo, ou hiperglicemia. Um dos problemas mais frequentes é a diabetes mellitus, que pode ser descrito como um grupo de doenças metabólicas de diversas etiologias, caracterizado por hiperglicemia, glicosúria e outras manifestações clínicas decorrentes do comprometimento, principalmente, do sistema vascular e do sistema nervoso, levando a lesões em múltiplos órgãos, em especial olhos, rins e coração. A prevalência da diabetes mellitus tem vindo a aumentar acentuadamente nos últimos anos. As causas apontadas para esse aumento são as mudanças de hábitos de vida ocasionados pela acelerada urbanização, levando a um sedentarismo cada vez maior, alimentação desequilibrada, obesidade e stres contínuo, que facilitam a manifestação da doença em indivíduos geneticamente predispostos. Outro dado importante é o aumento da esperança média de vida na população, que contribui também para o aumento da prevalência da doença. Estudos multicêntricos confirmam o aumento da prevalência e sugerem que os indivíduos obesos apresentam o dobro de risco de desenvolver a doença; já aqueles com parentes directos diabéticos apresentam risco triplicado. Outro dado importante oriundo desses estudos é que metade dos pacientes que tiveram o diagnóstico de diabetes confirmado desconhecia o facto e que 20% entre os que já conheciam o diagnóstico da doença não faziam nenhum tipo de tratamento. O dado de que metade dos pacientes diabéticos no nosso país vive com hiperglicemia levanos a um quadro desolador, no qual o risco de morbilidade e de mortalidade aumenta significativamente por complicações vasculares, renais, neurológicas, oftalmológicas e infecciosas. Uma nova classificação e novos critérios diagnósticos de diabetes mellitus foram propostos em maio de 2000 pela American Diabetes Association, e endossados pela Organização Mundial de Saúde. A classificação etiológica identifica quatro grupos distintos de diabetes DIABETES TIPO I Auto imunidade e idiopática DIABETES TIPO II OUTROS TIPOS ESPECÍFICOS Defeitos genéticos na acção da insulina, defeitos genéticos da células beta, doenças do pâncreas exócrino, endocrinopatias, induzido por fármacos, infecções, síndromes genéticos associados e formas imunomediadas incomuns DIABETES GESTACIONAL A diabetes tipo I apresenta duas formas clínicas. Uma, imunomediada, representa 90% dos casos e cursa com marcadores imunológicos de destruição das células beta pancreáticas, como os anticorpos anti-ilhota, anti-insulina e anti-gad, entre outros. A outra corresponde a 10% dos casos que, por não terem etiologia conhecida, são classificados como idiopáticos. Embora seja a principal endocrinopatia diagnosticada na infância e na juventude, o termo diabetes infantojuvenil não deve ser utilizado, uma vez que de forma menos frequente, pode também manifestar-se na idade adulta. O termo insulino-dependente também foi abandonado, já que qualquer tipo de diabetes pode, levar à dependência em relação à insulina, além do paciente apresentar grande tendência a cetoacidose e coma.
111 A diabetes tipo II caracteriza-se pela resistência periférica à acção da insulina, forte predisposição genética e familiar, e deficiência relativa de insulina, que aumenta com a evolução da doença. A maior parte dos pacientes é obeso clássico ou apresenta a chamada obesidade abdominal, que está associada ao aumento da produção de ácidos gordos livres, levando a um maior afluxo hepático e provocando hiperinsulinemia por diminuição da ligação e extração de insulina pelo fígado. Ambos os quadros cursam com a resistência periférica da insulina. A glicemia eleva-se de modo gradual e, durante os estágios iniciais, não induz a sintomas clínicos significativos. Com isso, o paciente permanece sem diagnóstico por muito tempo. A diabetes gestacional é definidao como uma intolerância à glicose diagnosticada durante a gravidez. A partir da sexta semana após o parto, nova avaliação deve ser realizada para reclassificação do estado da paciente. Os novos parâmetros diagnósticos para diabetes: - quadro clínico de diabetes associado a uma glicemia casual de 200 mg/dl; - glicemia de jejum superior a 126 mg/dl; - glicemia 2 horas após sobrecarga oral (PTGO) de 200 mg/dl. A avaliação do doseamento de glicose deve ser confirmada, pelo menos, em duas ocasiões diferentes. O grupo de intolerantes inclui os indivíduos que se afastam da normalidade (faixa de 110 a 125 mg/dl) mas não apresentam alterações suficientes para serem considerados diabéticos. Informações adicionais, consultar Curva glicémica. NOVOS CRITÉRIOS DIAGNÓSTICOS DE DIABETES MELLITUS GLICEMIS DE JEJUM GLICEMIA CASUAL PROVA DE TOLERÂNCIA ORAL À GLICOSE (AOS 120 MINUTOS) NORMAL até 109 mg/dl até 139 mg/dl Intolerante à INTOLERANTE intolerante em jejum sobrecarga entre (Tolerancia Diminuída) entre 110 e 125 mg/dl 140 e 200 mg/dl DIABETES MELLITUS Acima de 126 mg/dl > ou = 200 mg/dl Acima de 200 mg/dl. Mesmo a população aparentemente saudável deve ser submetida a exames, a fim de obter o diagnóstico precoce da diabetes, o que favorece o tratamento. Casos que devem ser investigados e/ou acompanhados: - pacientes obesos, - obesidade abdominal, - sedentários, - parentes de 1º grau de diabéticos, - história de diabetes gestacional, - história de macrossomia fetal e abortos de repetição, - hipertensão arterial sistémica, - resultados que indicam tolerancia diminuída à glicose, - níveis aumentados de triglicerídeos e diminuídos de HDL colesterol. Glicose-6-Fosfato Desidrogenase, Pesquisa Este erro inato é causado por mutações no gene codificante para a enzima glicose- 6-fosfato desidrogenase (G6PD) que se encontra localizado no cromossomo X,
112 sendo portanto uma doença hereditária ligada ao sexo. Como a deficiência, está ligada ao cromossomo feminino (X), para que ocorra a expressão total da doença o gene não deve ser antagonizado por um cromossoma X normal. Portanto, a manifestação é mais grave nos homens (XY) e num número reduzido de mulheres que apresentam ambos os X alterados. Mais de 400 mutações distintas já foram determinadas como responsáveis pela deficiência de G6PD. Afecta cerca de indivíduos no mundo. A deficiência da glicose-6-fosfato desidrogenase (G6PD) altera directamente a estabilidade das hemácias, tornando-as vulneráveis à desnaturação oxidativa da hemoglobina, o que por sua vez leva a episódios hemolíticos intermitentes e à presença de corpos de Heinz. A susceptibilidade à hemólise dos portadores da deficiência pode ser aumentada pela exposição a fármacos com propriedades oxidantes, em situações de agressões víricas ou bacterianas e na presença de distúrbios metabólicos. A apresentação clínica mais grave é a hemólise intravascular aguda, com hemoglobinúria e icterícia após quadros infecciosos ou exposição a fármacos com efeitos oxidantes (sulfonamidas, sulfonas, analgésicos, antipiréticos, antimaláricos etc.). As manifestações clínicas podem aparecer ao nascimento ou os pacientes podem permanecer assintomáticos por vários anos, conhecendo a doença após infecções ou exposição aos medicamentos supracitados. Quando o aparecimento dos sintomas é precoce, icterícia neonatal é comum e desenvolve-se em 1 a 4 dias após o nascimento. Pode apresentar-se de forma grave, evoluindo para comprometimento renal, sequelas cerebrais ou mesmo óbito. O rastreamento neonatal é pertinente por se considerar a alta frequência do gene defectivo na população e pela possibilidade de profilaxia de crises hemolíticas causadas por fármacos e pela opção de medidas terapêuticas consensuais, levando a um bom prognóstico. Gonodotrofina Coriónica Humana Os ensaios laboratoriais para o diagnóstico da gravidez doseiam a gonadotrofina coriónica humana (HCG), que é uma hormona glicoprotéica produzida pelas células do sinciciotrofoblasto da placenta. A molécula de HCG é composta por duas subunidades: alfa e beta. A subunidade beta é a que confere a especificidade, uma vez que a subunidade alfa é comum a outras hormonas como a LH, a FSH e o TSH. Além das subunidades livres, outras moléculas HCG-relacionadas podem estar presentes, tanto no soro como na urina de mulheres grávidas. Essas moléculas podem apresentar grandes variações estruturais e são reconhecidas de modo diferente por diversos imunoensaios para HCG. Alguns ensaios detectam apenas a molécula inteira, que é a hormona biologicamente activa, uma vez que, isoladamente, nenhuma das subunidades exerce efeito hormonal. Outros detectam tanto a molécula inteira quanto a fração beta livre. Outros, ainda, detectam, além das frações livres, todas as moléculas HCG-relacionadas. Esta é uma das razões para as variações passíveis de serem encontradas entre os diversos métodos para doseamento de HCG. A variação é menos significativa na gravidez normal e pode ser muito expressiva em gestações complicadas como aborto espontâneo, pré-eclâmpsia, doença trofoblástica, síndrome de Down e neoplasias do testículo, bexiga ou ovário. Nesses casos, a proporção de moléculas de HCG fragmentadas ou de fração beta livre pode ser muito maior.
113 O doseamento de beta HCG também é útil como marcador tumoral, especialmente no diagnóstico e no acompanhamento dos tumores trofoblásticos e testiculares. Os ensaios capazes de dosear a molécula de beta HCG total e as suas fracções livres são os mais indicados na detecção e na monitorização dessas patologias, já que alguns tumores secretam, além da molécula total da HCG, uma grande quantidade de fracções livres. O carcinoma testicular apresenta um pico de incidência em homens entre os 30 e 40 anos, sendo 10 vezes mais frequente em pacientes com história de criptorquidismo. Pode ser observada apenas a presença de nódulo indolor, ou ainda de dor, disúria, perda de peso, feminilização, ginecomastia e diminuição da líbido. Mais de 95% dos tumores testiculares originam-se nas células germinativas dos túbulos seminíferos. Geralmente são malignos. Os tumores de células germinativas podem ser divididos em seminomas e não-seminomas. Os não-seminomas mais comuns são os tumores de células embrionárias, o teratoma e o coriocarcinoma. A presença de alfafetoproteína (AFP) elevada indica a presença de um nãoseminoma, já que os seminomas não a secretam. Detectar HCG elevada sugere a presença de um coriocarcinoma ou tumor de células embrionárias, já que raramente a HCG é secretada por seminomas puros. Apenas 7 a 16% dos seminomas secretam HCG total, e cerca de 20 a 50% secreta também as suas fracções livres. Por isso, como já citado, a utilização de métodos capazes de detectar o HCG total e as suas frações aumenta a possibilidade diagnóstica. A realização do exame histológico do material de punção testicular é fundamental para diferenciar seminomas de não-seminomas. Na gravidez normal, a secreção de HCG é detectável entre 7 a 10 dias após a fertilização e eleva-se, alcançando níveis máximos nas 8 a 10 semanas de gestação. Após a 12ª semana, os seus níveis começam a diminuir, até alcançarem um platô. Níveis inferiores a 5 mui/ml podem ser encontrados em mulheres não-grávidas, enquanto níveis superiores a 25 mui/ml são interpretados como positivos. Os valores intermediários entre 5 e 25 mui/ml são considerados inconclusivos e devem ser confirmados após 2 a 3 dias, pois no caso de existir gravidez, os valores duplicam a cada 24 horas. Gestações múltiplas cursam com níveis mais elevados do que a gestação normal. Os níveis de HCG alcançados numa gestação normal são significativos, e a realização de doseamentos seriados é importante para elucidar casos de gravidez ectópica, que cursam com níveis bem menores. Grupo Sanguíneo e Factor RH A denominação grupos sanguíneos não se restringe apenas ao sistema de antigénios encontrados nas hemácias, podendo também ser expressa por outros constituintes sanguíneos como leucócitos, plaquetas e o próprio plasma. Esses antigénios são definidos geneticamente, e de acordo com as combinações das suas expressões na superfície das células sanguíneas, formam os sistemas que identificam os diferentes grupos sanguíneos. Os principais antigénios eritrocitários e os seus anticorpos correspondentes mais utilizados nas avaliações de imunohematologia de rotina são o sistema ABO e o Rhesus (Rh). O sistema ABO tem uma característica peculiar. A maioria dos indivíduos normais apresenta anticorpos (hemaglutininas potentes) contra os antigénios que não
114 possuem, e é nessa singularidade que os mecanismos de identificação do grupo ABO se baseiam. Portanto, para classificar os diferentes grupos, podemos realizar a chamada prova directa, em que são utilizados soros padrões que permitem identificar a presença de um determinado antigénio na superfície das hemácias. Uma outra forma é chamada prova reversa (confirmatória), na qual se utilizam células com antigénios conhecidos, permitindo a pesquisa de anticorpos livres no plasma ou no soro. É importante a realização das duas provas, para maior segurança da classificação do grupo sanguíneo. Os grupos A e B apresentam subgrupos de pouca importância clínica em relação às transfusões. Nalgumas situações, é possível encontrarmos discordância entre as duas técnicas e/ou dificuldades na classificação. Esses casos podem ser encontrados em subgrupos mais fracos, com fenótipos raros. Entre as diferentes causas de discordância na classificação ABO podemos citar os idosos e recém-nascidos, por baixa actividade do antigénio (aglutinina), presença de auto-anticorpos frios, imunossupressão, anticorpos ABO adquiridos passivamente ou, ainda mais raramente, alterações dos antigénios em patologias graves como a depressão antigénica observada em leucemias e noutras patologias, especialmente neoplasias. Encontra-se também o antigénio B adquirido, associado aos carcinomas do cólon e gástrico. Grupo ABO Antigénios Anticorpos % População % População presentes naturais branca negra O H anti-a e anti-b A A anti-b B B anti-a AB AB A explicação da expressão do factor Rh é complexa e envolve a manifestação dos diferentes antigénios em grupos de três. O sistema Rh foi assim denominado por Wiener logo no início de sua descoberta de diferentes antigénios eritrocitários D-ce-C-E, e é baseado na sua teoria de hereditariedade dos antigénios Rh. Posteriormente, outros autores propuseram a denominação sistema DCE, que terminou por não ser utilizada na rotina. Para simplificar a compreensão, consideremos que, do ponto de vista prático, apenas se utiliza o soro anti-d para classificação dos grupos Rh positivos, negativos e fracamente positivos (variante Du). Portanto, didáticamente, são indivíduos Rh(+) (85% da população) os que apresentam o antígeno D, e Rh(-) (15% da população) os que não apresentam o antígeno D. A variante Du é avaliada em todos os casos negativos. Quando positivo, o indivíduo será tratado como Rh(+). Haptoglobina É uma glicoproteína produzida pelo fígado, que migra na região alfa-2-globulina, na electroforese das proteínas, podendo ser identificados, pelo menos, três fenótipos diferentes (HAP1, HAP2-1, HAP1-1). A sua função é ligar-se à hemoglobina livre, libertada pela destruição intravascular das células vermelhas, conservando o ferro e prevenindo a possível nefrotoxidade causada pela hemoglobina durante a filtração glomerular. O complexo formado pela haptoglobina e pela hemoglobina livre é removido pelo sistema reticuloendotelial, no qual o grupo heme da hemoglobina é degradado em ferro e em bilirrubina.
115 Em estados de acelerada hemólise intravascular, a haptoglobina começa a diminuir, devido ao facto de estar a ser utilizada em maior velocidade do que a da reposição hepática, o que leva ao aparecimento de dímeros de hemoglobina livre que serão filtrados pelos rins. Uma vez filtrada, a hemoglobina livre é degradada pelas células epiteliais tubulares, levando à formação de hemossiderina. O rim possui capacidade limitada de filtração, em torno de 5 g de hemoglobina por dia. Quando ultrapassa esse nível, a hemoglobina livre começa a aparecer na urina. A hemoglobina livre pode ligar-se, também a uma outra proteína, a hemopexina, que por sua vez se liga ao heme, transportando-o para o fígado, onde o ferro é incorporado à ferritina e o heme segue a via metabólica das bilirrubinas. Assim como a haptoglobina, pode ser consumida em estados de hemólise acelerada. Os níveis de haptoglobina podem estar elevados em numerosas situações que levam à reacção de fase aguda como no síndrome nefrótico, em que, dependendo do fenótipo, podem aumentar de forma a compensar a perda de outras proteínas. A mesma elevação pode ocorrer no uso de corticóides. Apresentam-se diminuídos nas hepatopatias graves, nas situações de aumento da hemoglobina livre pela hemólise aumentada de eritrócitos, como em hemoglobinopatias, reacções transfusionais, anemia megaloblástica, eritropoiese ineficaz associada a destruição medular de células vermelhas, queimaduras extensas, coagulação intravascular disseminada, reabsorção de grandes hematomas, síndrome nefrótico em que, dependendo do fenótipo, podem diminuir os níveis séricos por perda urinária (geralmente fenótipo HAP1-1), e terapia com estrogénios e corticóides. Nas situações de hemólise severa aguda, a haptoglobina pode ser totalmente consumida, necessitando de cerca de 1 semana para retornar aos níveis normais. Já nos casos de hemólise crónica, como os que podem ser vistos em hemoglobinopatias e na hemólise causada por válvulas cardíacas mecânicas, os níveis séricos de haptoglobina decrescem mais lentamente, e o seu doseamento seriado pode ser um melhor indicador para o acompanhamento do nível de hemólise do que a avaliação isolada da hemoglobina. Por ser uma proteína de fase aguda, a presença conjunta de processos inflamatórios e de hemólise pode dificultar o diagnóstico em análises isoladas. Para facilitar o diagnóstico diferencial, recomenda-se a avaliação de outras proteínas de fase aguda, além do acompanhamento seriado. HDL-Colesterol O HDL-colesterol (colesterol contido nas HDL) é inversamente proporcional ao risco de desenvolvimento de doenças coronárias. Níveis superiores a 60 mg/dl são associados a um efeito protector, enquanto níveis séricos abaixo de 40 mg/dl relacionam-se a risco mais elevado de desenvolvimento de doença coronária. Esta capacidade protectora parece estar relacionada com o mecanismo de transporte reverso do colesterol, no qual o HDL está envolvido, captando colesterol não-esterificado dos tecidos periféricos pela acção enzimática da LCAT (lecitinacolesterol-acil-transferase) e formando as HDL maduras, que irão levar o colesterol até ao fígado de forma directa ou transferindo-o para outras lipoproteínas, as VLDL. No fígado, o colesterol é reutilizado em processos metabólicos ou excretado pela bilis.
116 Os valores séricos variam de acordo com a idade e o sexo. Algumas situações podem contribuir para a diminuição dos níveis séricos de HDL-colesterol, como sedentarismo, tabagismo, diabetes, factores genéticos, obesidade e diversos fármacos. O exercício e o uso moderado de flavonóides (contidos no vinho tinto) têm sido apontados como factores que ajudariam a elevar os níveis séricos do HDLcolesterol. Para cada redução de 5 mg/dl do HDL-colesterol abaixo da média, o risco de doença coronária aumenta em 25%. Nas hepatopatias, os níveis séricos do HDLcolesterol podem encontrar-se diminuídos. Consultar Perfil Lipídico Helicobacter pylori Em 1994, uma conferência de consenso declarou que a úlcera é uma doença infecciosa e recomendou que o tratamento dos sintomas com antiácidos deveria ser alterado para a erradiação antibiótica da infecção. A úlcera péptica é uma das doenças mais comuns, afectando, aproximadamente, 50% da população do mundo. O Helicobacter pylori está presente em quase 100% dos pacientes adultos com úlcera duodenal e em aproximadamente 80% dos pacientes com úlcera gástrica. A associação da úlcera gástrica com o carcinoma gástrico, suspeitada há muito tempo, está agora a ser confirmada. Em países em desenvolvimento, onde a maioria das crianças é infectada aos 10 anos de idade, as taxas de carcinoma gástrico são muito altas. Nos EUA e noutros países desenvolvidos, padrões de higiene e a melhoria socioeconómica crescente da população reduziram a incidência de infecção. Em paralelo, as taxas de úlcera péptica e de carcinoma gástrico baixaram. Os antagonistas H 2 receptores de histamina diminuem a secreção ácida a curto prazo, mas as taxas de recaída atingem 95% dos casos em 2 anos, determinando a retoma do tratamento. Recentes achados em gastrites crónicas e infecção por Helicobacter pylori em países desenvolvidos sugerem que: - Gastrites por Helicobacter pylori são adquiridas na infância e na adolescência (idade inferior a 20 anos) em mais de 50% dos casos; - Risco e taxa de aquisição são mais altos na infância; posteriormente, ocorre um declínio exponencial na taxa de aquisição; - Novas infecções acontecem na maior idade, mas são bastante raras (incidência anual de 0,4% em média); - A taxa e o risco de infecção pelo Helicobacter pylori são altos em nascidos no princípio do século XX, mas muito mais baixas entre os nascidos depois; - Este declínio deve-se à diminuição na taxa e no risco de aquisição de gastrites por Helicobacter pylori em particular na infância. Todas as espécies de Helicobacter causam algum grau de inflamação persistente no estômago dos mamíferos. São constatadas gastrites em praticamente todos os humanos infectados, embora a maioria não tenha nenhum sintoma; 1 em 10 desenvolve a úlcera. O desenvolvimento de adenocarcinoma gástrico é três a doze vezes mais provável em indivíduos infectados pelo Helicobacter pylori. A identificação do Helicobacter pylori pela coloração de Gram e a detecção de anticorpos anti-h. pylori por hemaglutinação ou fixação de complemento têm sensibilidade relativamente alta e especificidade como a do teste de biópsia/urease. Existe uma excelente correlação entre uma apresentação clínica clássica de
117 gastrites, a presença de Helicobacter pylori no estômago e a serologia alterada. A sensibilidade e a especificidade são de 90%, e o valor preditivo de um resultado negativo para anticorpos anti-helicobacter pylori por enzima imunoensaio (EIA) é elevado na infecção recente, excluindo-se uma população mais velha. Combinações de antigénios diferentes melhoram a sensibilidade sem perda de especificidade. Resultados positivos justificam uma tentativa empírica de curta terapia com antimicrobianos em gastrites de origem desconhecida. Pode ser esperada uma queda significativa das concentrações de anticorpos IgG anti-h. pylori depois de terapia antibacteriana adequada. Pacientes assintomáticos e sem tratamento continuam com seropositividade para IgG, mostrando a presença de H. pylori mesmo após a resolução histológica. A erradiação de H. pylori está associada à redução significativa do retorno de úlcera duodenal. A sua avaliação é útil na diferenciação entre gastrites por Helicobacter pylori e linfoma gástrico. Recentemente, surgiram testes imunoenzimáticos para a detecção de antigénios específicos de Helicobacter pylori. A investigação do antigénio Helicobacter pylori é um método não-invasivo para a identificação das bactérias em amostras. O teste tem altas sensibilidade (93,9%) e especificidade (96,3%), com uma precisão diagnóstica de 95%. Este ensaio pode simplificar o diagnóstico preciso da infecção por Helicobacter pylori. A PCR é uma técnica altamente sensível e rápida de identificação de Helicobacter pylori em espécimes clínicos. Hemocultura Quando uma bactéria vence as barreiras normais do hospedeiro e das células do sistema reticuloendotelial, ela invade a corrente circulatória ou os vasos linfáticos, podendo rapidamente disseminar-se e causar bacteriémia (presença de bactérias no sangue). A bacteriémia pode ocorrer de forma transitória, intermitente ou contínua. Além disso, os seus produtos metabólicos interagem com os mecanismos de resposta inflamatória, podendo levar à septicémia e ao choque, que é uma das mais sérias complicações das doenças infecciosas. A(s) bactéria(as) responsável(is) pode(m) ser identificada(s) pela realização da cultura do sangue (hemocultura) e é (são) útil (eis) no diagnóstico etiológico e na escolha da terapia. Para o diagnóstico, é importante a colheita de mais de uma amostra (mínimo de 2, ideal de 3), antes da administração de antimicrobianos. O número de amostras e o intervalo entre as colheitas dependem do quadro clínico investigado. Nas bacteriémias agudas e/ou contínuas, recomenda-se a colheita de 3 amostras com intervalo de 1 a 2 horas. Já nas intermitentes, recomenda-se a colheita em intervalos menores e antes ou imediatamente após o início do pico febril. Para a colheita, deve-se fazer anti-sépsia da pele, com álcool a 70%, 2 vezes, e esperar a acção do anti-séptico durante 2 minutos. Esta operação também pode ser realizada utilizando-se uma primeira anti-sépsia com álcool a 70%; posteriormente, utilizar álcool iodado. Puncionar a veia e colher o número de amostras no intervalo de tempo indicado. Deve-se evitar a colheita de sangue na região inguinal.
118 O material biológico utilizado pode ser sangue arterial ou venoso, aspirado de medula óssea ou de qualquer outro líquido biológico. Podem ser colhidos também líquidos de cavidades fechadas para cultura de anaeróbios. Quando o material for sangue, o volume colhido é um dos mais importantes parâmetros na detecção de bactérias na corrente sanguínea. Colher os seguintes volumes nas diferentes faixas etárias: - crianças até 1 ano: 0,5 ml a 1,5 ml em cada frasco de cultura; - crianças de 1 a 6 anos: 1,0 ml por cada ano de idade; - adultos: 20 ml de sangue para cada amostra de hemocultura. Quando for utilizada para cultura de líquidos biológicos, qualquer volume do espécime pode ser utilizado. O sangue colhido é acondicionado em frascos especiais com meio líquido e diferentes de acordo com o tipo de bactéria a ser investigada (aeróbia ou anaeróbia). A rapidez na identificação etiológica do agente bacteriano é essencial para a decisão precoce e adequada do tratamento específico. Os métodos modernos automatizados permitem a disponibilização rápida dos resultados. Nesses métodos, a presença de bactérias é detectada pelo CO 2 produzido durante o crescimento bacteriano, que irá modificar o sensor existente no fundo do frasco de cultura, proporcionando a emissão de fluorescência, por sua vez detectada pelo aparelho utilizado para leitura. A presença de crescimento bacteriano no sangue do paciente indica bacteriémia e/ou septicémia. Alguns agentes patogénios devem ser questionados quanto ao seu poder patogénico, como por exemplo o estafilococos coagulase-negativos numa única amostra, Propionebacterium acne e grupo Corynebacterium. Nas infecções hospitalares, os patogénios mais encontrados são Staphylococcus aureus, Escherichia coli, Klebsiella pneumoniae, Enterobacter spp., Pseudomonas aeruginosa, Enterococcus spp. e estafilococos coagulase-negativos. Nas endocardites, os agentes mais frequentemente isolados correspondem aos Estreptococcus spp. alfa-hemolíticos ou mesmo beta-hemoliticos, assim como aos Staphylococcus aureus e aos Stafilococcus coagulase-negativos. O anticoagulante utilizado no meio de cultura (SPS) inactiva o sistema do complemento, porém inibe o crescimento das Neisseria spp. e Gardnerella vaginalis. As bactérias com exigencias especiais, tais como Brucella spp., Leptospira spp., Bartonella spp., Legionella spp., Mycobacteria spp., não crescem nos meios tradicionalmente usados para hemoculturas. Hemocultura para Fungos O isolamento e a identificação de fungos em cultura são prova definitiva no diagnóstico de fungemia. O sangue venoso do paciente é inoculado num frasco especial, que contém os nutrientes necessários ao crescimento adequado dos fungos. Cada frasco contém um sensor capaz de detectar o decréscimo da concentração de oxigénio, resultante do metabolismo e do crescimento do fungo presente na amostra. Esse sensor é monitorizado por equipamento automatizado. No fundo de cada frasco existe um fluorocromo que produz uma fluorescência que é proporcional ao decréscimo do oxigénio na amostra. Na presença de fungos, ocorre consumo de oxigénio e, consequentemente, aumento da fluorescência, que provocará indicação de amostra positiva.
119 Os resultados devem ser interpretados correlacionando-se com o estado clínico do paciente. Alguns fungos podem provocar fungemia transitória, sendo isolados em amostra de hemocultura e com significado clínico duvidoso. Em caso de isolamento de fungo patogénico, o resultado é liberado para o médico o mais rápido possível. A presença de infecção bacteriana concomitante pode inibir o crescimento de fungos, assim como o uso de medicação sistémica. Os frascos utilizados não são selectivos para fungos e permitem também o crescimento de bactérias. Se presentes, as bactérias de crescimento rápido podem mascarar a detecção dos fungos. Alguns fungos, tais como Rodothorula rubra e Blastomyces dermatitidis, podem não ser detectados por esse método, necessitando, para a sua identificação, de outros métodos de cultura adicionais. A identificação de presença de leveduras pelo método automatizado exige uma espera de 7 dias, e os demais fungos, de 30 dias. Para colher a amostra, fazer anti-sépsia da pele com álcool a 70%, 2 vezes, e esperar a acção do anti-séptico durante 2 minutos. Puncionar a veia e colher o sangue. O número de amostras e o intervalo de tempo de colheita entre elas são determinados pelo próprio médico assistente. O volume recomendado é de 3 a 5 ml. Hemoglobina A2, Pesquisa A HbA2 é composta por dois pares de cadeias alfa e delta e é responsável por cerca de 3% da hemoglobina do adulto normal. O nível de HbA2 aumenta gradualmente durante o primeiro ano de vida, quando atinge os níveis de um adulto normal. Os seus níveis podem estar aumentados nalgumas beta-talassemias, doença da hemoglobina H e anemias megaloblásticas. A anemia por deficiência de ferro e as sideroblásticas podem levar à diminuição da sua síntese. Nos casos de beta-talassemias minor, a HbA2 está aumentada (>3,5%), com presença de microcitose e hipocromia eritrocitária e níveis séricos de ferritina normais. Hemoglobina Fetal, Pesquisa Cerca de 80% da hemoglobina do recém-nascido é constituída pela hemoglobina fetal. Ela é composta por 2 cadeias alfa e 2 cadeias gama. Essa hemoglobina possui uma maior afinidade para o oxigénio do que a do adulto. Por volta dos 6 meses após o nascimento, quase toda a hemoglobina fetal é substituída pela do adulto, a hemoglobina A (HbA), restando apenas cerca de 1 a 2% da fetal. Níveis aumentados no adulto podem ser encontrados na persistência hereditária da hemoglobina fetal, nas síndromes beta-talassémicas, na interação talassemia/outra hemoglobinopatia, na anemia falciforme e nas síndromes mieloproliferativas. Alterações discretas podem ser encontradas nas anemias aplásticas, na esferocitose hereditária e na anemia megaloblástica.
120 Hemoglobina Glicosilada O processo pelo qual a hemoglobina e outras proteínas se ligam à glicose é denominado glicosilação e corresponde à adição de forma não-enzimática de resíduos de açúcar a grupos de aminoácidos da proteína. A glicosilação da hemoglobina ocorre durante os 120 dias do período de sobrevida das hemácias. Entretanto, a glicose presente no sangue depende de um intervalo de tempo para glicosilar a hemoglobina. A glicemia dos últimos 30 dias antes do doseamento contribui com 50% da hemoglobina glicosilada doseada, e as glicemias dos últimos meses (2 a 4), com 25%. O doseamento final, portanto, corresponde à média ponderada dos níveis das glicemias das 6 a 8 últimas semanas antes do doseamento. No indivíduo adulto normal, a hemoglobina circulante é composta por 97% de HbA, 2,5% de HbA2 e 0,5% de HbF. A hemoglobina predominante, a hemoglobina A, é formada por 2 subunidades alfa e 2 subunidades beta. Por isso, as moléculas de açúcar podem ligar-se em diferentes sítios da hemoglobina, produzindo distintas formas de hemoglobinas glicadas ou glicosiladas. A hemoglobina glicosilada HbA1 é uma hemoglobina de migração rápida na electroforese, que tem um açúcar ligado ao local de maior reactividade para glicação, o aminoácido N-terminal da cadeia beta. É encontrada em níveis aumentados nos pacientes com hiperglicemia mantida e dentro dos limites de referência em indivíduos normais. De acordo com a metodologia empregue, podemos isolar apenas a HbA1 ou isolar as suas diferentes fracções, que são designadas como HbA1a, HbA1b HbA1c.Como a HbA1c representa cerca de 80% da HbA1, a sua avaliação reflete com fidelidade o grau de glicosilação da hemoglobina. Além disso, a HbA1c é a única irreversivelmente glicada e, portanto, suficientemente estável para ser utilizada para monitorização dos níveis glicémicos. A membrana da hemácia é totalmente permeável à glicose, expondo a hemoglobina a concentrações de glicose similares às plasmáticas. É com essa exposição que acontece a ligação da glicose com a valina N-terminal da cadeia beta da hemoglobina A. Embora existam diversos métodos para a quantificação da hemoglobina glicosilada, tais métodos podem ser divididos em dois grandes grupos, de acordo com o principio utilizado: a separa ção por diferenças estruturais (cromatografia HPLC/coluna e electroforese) e a separação por diferença de carga (cromatografia de troca iónica HPLC/coluna e método imunoenzimático). Os dois métodos mais utilizados são o cromatográfico por troca iónica e a cromatografia de afinidade. A cromatografia por troca iónica sofre a interferência de hemoglobinas variantes, como a HbS e HbC, e também por drogas ou substâncias que alterem a carga da hemoglobina. Já a cromatografia de afinidade não sofre a influência das hemoglobinas variantes, nem de medicamentos. No entanto, não consegue quantificar a fracção e sim o total de hemoglobinas glicosiladas. A literatura tem apontado a quantificação da HbA1c por HPLC como método de referência pelo DCCT (Diabetes Control and Complications Trial). Recomenda-se a monitorização a cada 3 meses em todos os pacientes diabéticos. Nalguns casos, como na diabetes gestacional ou com mudanças importantes do esquema terapêutico, a monitorização poderá ser mais frequente (a cada 4 semanas).
121 As principais interferências são as patologias que alteram a semi-vida da hemácias, hemoglobinopatias e nefropatias crónicas. Hemoglobina H, Pesquisa A hemoglobina H (HbH) pode ser encontrada na alfa-talassemia. É uma hemoglobina composta por 4 cadeias beta. A doença manifesta-se por anemia hemolítica crónica de grau moderado. A sua presença pode ser detectada pela electroforese da hemoglobina ou pela observação de corpos de inclusão que podem ser observados no sangue periférico por coloração especial. As inclusões de hemoglobina H ocorrem pela precipitação de cadeias em excesso. Está também descrita uma forma adquirida da doença da HbH observada nalguns pacientes com síndromes mieloproliferativos e mielodisplásicos. Hemoglobina S, Pesquisa A hemoglobina S pode apresentar-se de formas homozigótica (HbSS), heterozigótica, (HbAS), ou ainda associada a outras variantes de hemoglobinas, como a hemoglobina fetal e alfa ou beta-talassemia. É possível a detecção da hemoglobina S pela electroforese da hemoglobina. Entretanto, a presença necessita de ser confirmada por metodologias específicas, visto que é possível observar outras fracções de hemoglobina na mesma posição, como a HbD e a Hb Lepore, entre outras. Estão disponíveis diferentes métodos para confirmação da HbS, como a electroforese em ph ácido, a solubilidade e o teste de céluals falciformes. A electroforese em ph alcalino com avaliação da percentagem de HbS é útil na identificação e avaliação da concentração de HbS. Hemoglobina, Solubilidade Neste teste, investiga-se a presença de HbS, por meio da lise das hemácias e redução da possível hemoglobina S presente, pela acção do ditionito de sódio. Como a HbS é insolúvel em tampões inorgânicos concentrados, formam-se polímeros que produzem opacidade. O teste é útil como triagem para anemia falciforme, sendo positivo na presença de HbS e de outras hemoglobinas também insolúveis como HbC, HbC Harlem e Hb Bart. Reações falso-positivas podem ocorrer devido à turvação ocasionada pela presença de grande quantidade de corpos de Heinz e da presença de precipitação de proteínas plasmáticas. Podem ocorrer falso-negativos na presença de pequenas quantidades de HbS, alta concentração de hemoglobina fetal e anemia grave.
122 Hemoglobinas Instáveis As hemoglobinas chamadas instáveis constituem um grupo composto por cerca de 80 diferentes tipos de hemoglobinas anormais, que cursam, nos seus portadores, com anemias hemolíticas agudas ou crónicas. Podem ser identificadas pela instabilidade das suas cadeias polipeptídicas, que se precipitam quando submetidas ao calor, levando a uma reacção de floculação. Esta instabilidade deve-se a uma ligação anormal entre as cadeias alfa e beta ou na região do heme. A hemólise pode ser induzida por diferentes medicamentos e por processos infecciosos bacterianos ou víricos. Nestes pacientes, é frequente, após esplenectomia, a presença de corpos de Heinz nas hemácias, por colorações especiais. É também um achado laboratorial comum a presença de metaemoglobina proveniente da constante oxidação do heme. A presença de altas concentrações de hemoglobina fetal é uma limitação para essa investigação. Hemoglobinopatias A hemoglobina é uma proteína composta por dois pares de cadeias polipeptídicas e pelo heme (estrutura porfirínica que possui no interior um átomo de ferro mantido em estado ferroso). As cadeias polipeptídicas são compostas por combinações entre os diversos tipos de cadeias, resultando em hemoglobinas diferentes na sequência de seus aminoácidos. As cadeias são identificadas como a (alfa), b (beta),g (gama), d (delta) e as embrionárias e (épsílon) e z (zeta). Cerca de 80% da hemoglobina do recém-nascido é constituída pela hemoglobina fetal (duas cadeias a e duas cadeias g ). Essa hemoglobina possui maior afinidade com o oxigénio do que a do adulto. Por volta dos 6 meses após o nascimento, quase toda a hemoglobina fetal é substituída pela do adulto, a hemoglobina A (HbA), restando apenas cerca de 1 a 2% da fetal. A HbA é composta por dois pares de cadeias alfa e beta. Representa quase a totalidade da hemoglobina do adulto, que pode apresentar mínimas fracções da hemoglobina fetal e da chamada HbA2 (dois pares de cadeias alfa e delta). Existe um grupo de hemoglobinas chamadas de anormais porque diferem do ponto de vista estrutural e bioquímico da hemoglobina normal (HbA). As mutações são genéticas, podendo ter o caráter homozigótico ou heterozigótico, e são consequência de alterações dos genes estruturais (alterações qualitativas) ou dos genes reguladores (alterações quantitativas) que comandam a síntese das cadeias polipeptídicas. Portanto, as alterações ditas qualitativas são as que afectam estruturalmente a formação das cadeias, resultando em hemoglobinas bioquimicamente diferentes, denominadas anormais ou variantes. São causadas na sua maioria pela substituição de aminoácidos, sendo as mais comuns, no Ocidente, a hemoglobina falciforme (HbS), que decorre da substituição do ácido glutámico por valina na posição 6 da cadeia beta, e a hemoglobina C (HbC), decorrente da substituição do ácido glutámico por lisina, também na cadeia beta.
123 Existem mais de 300 tipos diferentes de hemoglobinas anormais descritos, mas apenas uma pequena parte delas está associada a manifestações clínicas e hematológicas. Elas podem ser identificadas pela mobilidade electroforética e são designadas por letras. A primeira a ser identificada foi a HbS, assim denominada pela aparência característica em foice da hemácia falciforme que, em inglês, é sickle (foice), o que explica a denominação HbS. Nos anos que se seguiram, foram descritas muitas outras variantes. A partir de 1962, durante o Congresso da Sociedade Internacional de Hematologia, estabeleceu-se a regra para a descrição das variantes reconhecidas a partir daquela data. Ficou estabelecido que passariam a receber designações seguindo o alfabeto (C, D, E, G, H) e que, quando com a mesma mobilidade electroforética porém com estruturas diferentes, seriam identificadas pela cidade onde foram descobertas. As mutações dos genes reguladores promovem alterações quantitativas que levam a anormalidades da síntese das hemoglobinas, com uma deficiência na produção de uma ou mais cadeias polipeptídicas da hemoglobina. Esta ocorrência dá origem às talassemias, classificadas de acordo com a cadeia que é produzida em taxa reduzida como a-tal e b-tal, as mais frequentes. São descritas também a b-d-tal, d- tal e a g d b -tal. Os quadros clínicos variam de assintomáticos a moderados, leves e muito graves. Mais informações de exames relacionados: Curva de fragilidade osmótica Electroforese de hemoglobina Hemoglobina A2, S, H, fetal Hemoglobinas instáveis Hemograma Hemoglobina, Solubilidade Hemograma O hemograma contempla diversas provas efectuadas, com a finalidade de avaliar quantitativa e qualitativamente os componentes celulares do sangue. Os itens avaliados incluem: eritrócitos, hemoglobina, hematócrito, índices hematimétricos, leucócitos totais, contagem diferencial de leucócitos, plaquetas e exame microscópico de esfregaço de sangue após coloração. A análise quantitativa dos eritrócitos, leucócitos totais, plaquetas e a avaliação dos índices hematimétricos são hoje realizados por meio de equipamentos automatizados que combinam diferentes métodos de avaliação de alta tecnologia e precisão à capacidade de análise de milhões de células, permitindo resultados mais precisos. A utilização desses equipamentos permite também a avaliação de índices hematológicos e a visualização em histogramas que demonstram a distribuição dos diferentes elementos analisados. Essa característica possibilita a identificação de alguns parâmetros antes impossíveis de serem avaliados ou que eram analisados subjetivamente, com a visualização do esfregaço em lámina. Entre esses parâmetros, temos o índice de anisocitose (RDW), a identificação de populações mistas de células, a anisocitose plaquetária e alertas para possíveis alterações presentes na amostra examinada. Esses alertas são específicos para alterações das séries vermelha, branca e das plaquetas, como presença de blastos, granulócitos imaturos, desvio à esquerda, linfocitos atípicos, agregados plaquetários, microcitose, hipocromia, entre outros. Realizam ainda, por uma combinação de métodos de análise celular e coloração, a
124 contagem diferencial de leucócitos, que serve de orientação para o hematologista, chamando a atenção para situações nas quais a avaliação deve ser mais cuidadosa. A análise qualitativa é realizada pela avaliação da lámina corada, associada aos resultados obtidos pela avaliação electrónica. A coloração das células diferencia em detalhes as estruturas nucleares e citoplasmáticas, permitindo a avaliação do tamanho das células, a relação núcleo/citoplasma, a forma do núcleo, a presença de nucléolos, o padrão da cromatina e a coloração do citoplasma, a presença de granulação, vacúolos e outras alterações morfológicas. Os resultados auxiliam a identificação de doenças de origem primária ou secundária de características agudas ou crónicas. São utilizados também para acompanhar a evolução de uma variedade de doenças e para monitorizar os efeitos colaterais decorrentes do uso de medicamentos. A avaliação eritrocitária pode identificar processos anémicos, policitémicos, alterações de forma e tamanho dos eritrócitos. A avaliação leucocitária pode identificar processos inflamatórios, infecciosos, alérgicos, parasitários e leucémicos. Pode também indicar a presença de elementos anormais e de linfocitos atípicos. A avaliação plaquetária identifica processos de trombocitopenias adquiridas ou hereditárias e trombocitoses. SÉRIE VERMELHA A contagem de eritrócitos é a primeira informação fornecida e é expressa em milhões por mm 3. Os níveis de eritrócitos iguais ou maiores que 6,20 milhões/mm 3 em homens e iguais ou maiores que 5,70 milhões/mm 3 em mulheres são considerados poliglobulia. A concentração de hemoglobina é expressa em g/dl, e a sua avaliação é de grande importância pelo papel no transporte de oxigénio e por estar directamente relacionada à anemia, sendo a melhor forma de avaliação laboratorial. O volume relativo dos eritrócitos dentro do volume de sangue é fornecido pela análise do hematócrito, que é expresso em percentagem. A relação entre esses diferentes parâmetros pode ser obtida pela análise dos índices hematimétricos que irão fornecer informações adicionais sobre as variações de volume e concentração da hemoglobina. Os achados morfológicos do esfregaço após coloração fornecem mais informações sobre conteúdo da hemoglobina, forma, tamanho e inclusões eritrocitárias. Índices Hematimétricos Volume Corpuscular Médio - VCM Avalia a média do tamanho (volume) dos eritrócitos, que estão no tamanho normal, e são denominados normocíticos, diminuídos (microcíticos) ou aumentados (macrocíticos). O achado de microcitose é comum em anemias por deficiência de ferro, nas doenças crónicas e nas talassemias. O aparecimento de macrocitose pode estar associado à presença de um grande número de reticulócitos, ao tabagismo e à deficiência de vitamina B12 e de ácido fólico.
125 ALTERAÇÃO DE TAMANHO ADULTOS CRIANÇAS ATÉ 3 ANOS CRIANÇAS DE 4 A 14 ANOS NORMOCITOSE 81,0 73,0 73,0 MICROCITOSE <ou = 81,0 <ou= 71,0 <ou= 73,0 MICROCITOSE DISCRETA 80 a 80,9 71 a 72,9 73 a 74,9 MICROCITOSE ACENTUADA < 60 < 60 < 60 MACROCITOSE > 90 > 99 > 99 MACROCITOSE ACENTUADA >120 > 120 > 120 ANISOCITOSE Presença de eritrócitos com volumes diferentes Hemoglobina Corpuscular Média (HCM) Índice hematimétrico que corresponde à média de hemoglobina por eritrócito. Pode estar elevado na presença de macrocitose e diminuído na presença de eritrócitos microcíticos. Concentração da Hemoglobina Corpuscular Média (CHCM) É a avaliação da hemoglobina encontrada em 100 ml de eritrócitos. Este índice permite a avaliação do grau de saturação de hemoglobina no eritrócito. A saturação da hemoglobina normal indica a presença de eritrócitos ditos normocrómicos. Quando diminuída, teremos eritrócitos denominados hipocrómicos e, quando aumentados, eritrócitos hipercrómicos. RDW (Red Cell Distribution Width) A variação do tamanho dos eritrócitos é analisada electronicamente pela variação de impulsos obtidos durante a leitura. A análise dessa variação permite a obtenção deste novo índice, que representa a amplitude de distribuição dos glóbulos vermelhos, servindo como um índice de anisocitose, que se altera precocemente na deficiência de ferro, mesmo antes da alteração de outros parâmetros, como a alteração do VCM e a diminuição da hemoglobina. Alterações da Cor (Características Tintoriais) A coloração dos eritrócitos reflecte a concentração da hemoglobina e pode ser ocasionada: - pela diminuição da concentração de hemoglobina e consequente redução da cor, que leva à chamada hipocromia; - pela presença de células com diferentes concentrações de hemoglobina chamada anisocromia; - pela presença de um grande número de reticulócitos que caracteristicamente têm uma cor azulada, que junto com a cor normal, produz a chamada policromasia. POIQUILOCITOSE Variação das formas dos eritrócitos que normalmente se apresentam numa forma circular e com uma halo central claro ELIPTÓCITOS/ Eritrócitos elípticos e ovalados, que ocorrem na ovolacitose hereditária OVALÓCITOSE (eliptocitóse) e podem também ser encontradas em anemias carenciadas e mais raramente nas talassemias e outras anemias ESFERÓCITOS Eritrócitos pequenos, de forma esférica e hipercorada que aparece na esfericitose hereditárias e nas animias hemolíticas auto-imunes DACRIÓCITOS Eritrócitos em forma de lágrima. Ocorrem provavelmente por atrazo da saída da medula óssea. Presente na metaplasia mielóide, na anemia megaloblástica, nas tatassemias e na esplenomegalia.
126 CODÓCITOS Células em forma de alvo. Ocorre um excesso de membrana, o que faz com que a heoglobina se distribua num anél periférico, com uma zona densa central. Encontradas nas talassemias, na hemoglobina C, icterícia obstrutiva e na doença hepática severa DREPANÓCITOS Eritrócitos em forma de foice, caracteristica da anemia falsiforme ACANTÓCITOS Eritrócitos pequenos com projeções irregulares. Célula peculiar da betalipoproteinemia hereditária, presente também noutras dislipidemias, na cirrose hepática, na hepatite do recám-nascido, na anemia hemolítica, após esplenectomia e após administração de heparina ESQUIZÓCIOTS Fragmentos de eritrócitos de tamanhos diferentes e com fromas bizarras. Observados em muitos casos de próteses valvulares e vasculares, microangiopatias, síndrome hemolítico-urêmico, nos casos de queimaduras graves e na coagulação intravascular disseminada. Inclusões e Outras Variações das Hemácias As inclusões que podem ser observadas nos eritrócitos estão relacionadas com diferentes patologias e são consequência do aumento ou de defeitos da eritropoiese. Dependem, também, da capacidade do baço de retirar da circulação as hemácias mal formadas. Outras alterações também podem ser observadas, como a presença de eritroblastos e a formação de rouleaux. ANEL DECABOT Figura em forma de anel observada na anemias megaloblásticas, podendo, nalguns casos, torcer-se, assuimindo um aspécto de oito (8). Pode também ser observada noutras situações de eritropoiese anormal. É um filamento fino, de cor vermelho-violeta, concêntrico em relaçãoa à membrana celular, que resulta de restos mitóticos de mitoses anomalas CORPÚSCULOS Corpúsculo de inclusão pequena, basófilo, restos nucleares de mitoses ano- DE HOWEL JOLLY malas. São observados em pacientes esplenectomizados, nas anemias hemolíticas e megaloblásticas PONTILHADO Granulações variáveis em número e tamanho, de cor azulada, agregados de BASÓFILO ribissomas remanescentes. podem ser encontradas na intoxicação por metais especialmente o chumbo, nas talassemias, e outras alterações da hemoglobina, nas mielodisplasias e noutras formas de anemia severa CORPOS Precipitados de hemoglobina desnaturada que podem ser encontrados aderidos DE HEINZ à membrana dos eritrócitos, em pacientes com anemia hemolítica por alguns fármacos, na deficiência da glicose-6-fosfato desidrogenase e nos síndromes das hemoglobinas instáveis. Para a sua visualização, é necessário coloração especial com azul de cresil brilhante CORPÚSCULO DE Associados a ribossomas remanescentes, apresentam-se como pontos PAPPENHEIMER enegrecidos, agrupados ou localizados nas anemias hemolíticas e sideroblásticas ROULEAUX Aglutinação dos eritrócitos que formam verdadeiras pilhas, podendo ser observadas em lámina corada, são decorrentes da concentração elevada de fibrinogénio ou de globulinas, especialmente nas gamapatias monoclonais. Levam ao aumento da velocidade de hemossedimentação ERITOBLASTOS São eritrócitos nucleados que podem aparecer no sangue periférico devido a grandes regenerações eritrocitárias, ou como consequências de infiltração medular. Aparecem na anemia hemolítica e nas reações leuco-eritroblásticas (fibrose e metástase medular). SÉRIE BRANCA A contagem global e diferencial de leucócitos e suas alterações quantitativas e qualitativas são as principais informações fornecidas na análise da série branca. Os leucócitos totais são expressos em mil/mm3. A contagem diferencial é de grande importância, podendo definir perfis patológicos, e é fornecida pela análise conjunta
127 dos equipamentos automáticos e pela leitura do esfregaço corado, que avalia as diferentes formas leucocitárias e as expressa de forma percentual (relativa) e em mm3 (absoluta). A análise das alterações morfológicas dos leucócitos também é realizada por observação microscópica do esfregaço corado. Os leucócitos podem ser divididos em granulócitos (mielócito, metamielócito, com forma de bastonete, neutrófilos, eosinófilos e basófilos), monócitos e linfócitos. Alterações Morfológicas dos Leucócitos Pelger-Hüet É uma alteração hereditária autossómica dominante rara, que se caracteriza pelao presença de neutrófilos hipossegmentados, sem que no entanto ocorra alteração da função da célula. Os neutrófilos aparecem na periferia com discreta segmentação (bilobulados) ou mesmo sem segmentação (como bastonetes). Como não conduz a alterações funcionais, não apresenta repercussões clínicas. O diagnóstico assume importância afim de evitar a sua interpretação como um desvio à esquerda. Pode também ser encontrada nos eosinófilos. Existe, ainda, um quadro chamado de pseudo-pelger-hüet, no qual esta alteração pode ser adquirida, sendo causada por reacções a fármacos e em alguns casos de mielodisplasias e leucemias. Alder-Reilly É uma alteração hereditária autossómica recessiva, que se caracteriza por grânulos grosseiros de cor púrpura, os quais podem ser encontrados em granulócitos, monócitos e linfócitos. May-Hegglin Alteração hereditária autossómica dominante rara, na qual os neutrófilos apresentam inclusão citoplasmática azulada de RNA, semelhante aos corpos de Döhle, associada a trombocitopenia leve e à presença de plaquetas gigantes. Chediak-Higashi Doença autossómica recessiva rara, em que os granulócitos, monócitos e linfócitos se apresentam com gránulos gigantes, associada a infecções piogénicas frequentes e anormalidade funcional dos leucócitos, geralmente com sobrevida curta. Alterações Adquiridas Entre as alterações adquiridas, pode ser destacada a presença de corpúsculos de Döhle, inclusões ovais azuladas encontradas na periferia do citoplasma. Geralmente, encontram-se isolados e são consequência de ribossomas que persistiram e costumam ser encontrados em infecções e grandes traumas. O achado de granulações grosseiras (tóxicas) no citoplasma dos neutrófilos pode acontecer em longos processos infecciosos. As vacuolizações citoplasmáticas acontecem em resultado da depleção dos gránulos azurófilos no processo de fagocitose. Plaquetas A avaliação das plaquetas pode ser feita de forma quantitativa, expressa em mm 3, e de modo qualitativo, pela avaliação das características analisadas no esfregaço corado, o que permite a identificação de alterações morfológicas das plaquetas.
128 A utilização de equipamentos automáticos, além de fornecer contagens mais precisas, permite que se obtenham informações em relação à presença de anisocitose e agregados plaquetários, e também de índices plaquetários, que na sua maioria ainda não são liberados para uso clínico. Entre eles, os que começam a ser utilizados são o MPV (Mean Platelet Volume), considerado um índice de anisocitose plaquetária, e o PDW (Platelet Distribution Width). Entretanto, ainda faltam maiores dados de correlação clínica. As alterações quantitativas podem ser tanto o aumento da quantidade de plaquetas, chamada hiperplaquetémia, quanto a diminuição, denominada plaquetopenia. Consultar Plaquetas. Hepatites A hepatite vírica consiste numa doença inflamatória, com quadro clínico infeccioso. São conhecidos vários tipos de vírus hepatotrópicos, com características físicoquímicas e epidemiológicas próprias para cada tipo e subtipos. As infecções desenvolvem-se de forma transitória ou persistente, favorecendo a evolução para a infecção aguda autolimitada, estado de portador crónico assintomático e doença crónica. Observa-se, com frequência, o desenvolvimento clínico associado às manifestações sistémicas, semelhantes àquelas observadas em diferentes infecções, não permitindo, dessa forma, o diagnóstico etiológico preciso. Os principais agentes víricos hepatotrópicos causadores de hepatite são designados como: vírus da hepatite A (HAV); vírus da hepatite B (HBV); vírus da hepatite C (HCV); vírus da hepatite Delta (HDV); vírus da hepatite E (HEV) e vírus GBV-C (HGV). Cada um apresenta características estruturais e genómicas que permitem diferenciá-los, detectadas por diferentes metodologias laboratoriais com sensibilidade e especificidade definidas. Infecções persistentes causadas por HBV, HCV e HDV estão sempre associadas a doença hepática crónica, podendo evoluir para cirrose e hepatocarcinoma. Hepatite A O vírus da hepatite A (HAV) classifica-se na família Picornaviridae e é transmitido por via fecal-oral, determinando formas esporádicas e epidémicas de hepatite aguda. Água e alimentos contaminados constituem as vias mais comuns em surtos epidémicos. O período de incubação da doença é de 4 semanas, com evolução clínica de forma branda a moderada e ausência de formas crónicas. A hepatite fulminante é descrita em 0,2 a 0,7% dos indivíduos infectados. Em crianças na faixa etária de 1 a 10 anos, a hepatite A é geralmente anictérica e assintomática. A presença da imunoglobulina M específica (IgM anti-hav) no sangue é quase sempre concomitante ao período sintomático da hepatite aguda. Títulos elevados, obtidos por metodologias de diluições seriadas ou por comparação aos valores limites (cut off), são detectados na fase aguda e no início da convalescença. Títulos menores são detectados 3 a 4 meses após o acometimento da doença e podem persistir por mais de 6 meses, em 20 a 30% dos indivíduos, e até por 1 ano em 5 a 10%. Nos casos em que os sintomas precedem por poucos dias, a detecção de IgM anti-hav, recomenda-se a serologia pareada. A segunda colheita, feita após 15 a
129 20 dias, é útil para a confirmação do resultado reactivo, definindo o laudo de positividade. Os métodos actuais para a pesquisa em soro e plasma permitem a detecção qualitativa e, eventualmente, um cálculo estimado, semiquantitativo, pela análise comparativa da reactividade do teste com o valor limite (cut-off). Anticorpos da classe IgG anti-hav permitem a definição de infecção passada. Resultados de seroconversão, traduzidos por anticorpos IgG não-reactivos numa primeira análise e reactivos na segunda colheita, com intervalos de 20 a 30 dias, estão associados a infecção recente. A resposta imune aos diferentes antigénios estruturais, proteínas do capsídeo viral, VP0, VP1 e VP3, ocorre a partir da quarta semana após a infecção, com títulos máximos de anticorpos após a sétima semana. A pesquisa do RNA-HAV em soro, plasma e suspensão fecal é um método pouco utilizado, embora permita a detecção do genoma viral a partir do segundo dia após a infecção, podendo prolongar-se até o 25º dia. A metodologia de PCR pode detectar períodos mais longos de virémia (várias semanas), em concentrações elevadas, de 104 a 106 partículas virais/ml de sangue. A heterogeneidade de sequências genómicas de isolados víricos obtidos em diferentes partes do mundo definiu, até ao momento, 7 genótipos e 1 sorotipo de HAV. Hepatite A Anticorpos totais anti- HAV (serologia) Anticorpos IgM anti- HAV (serologia) RNA-HAV (pesquisa em suspenção fecal Fase de Incubação Fase aguda sintomática ou assintomática Canvalecência Fase Crónica Sintomática ou Assintomática Resposta eficaz à vacinação Não há N N P comfirmação P de evolução para cronicidade. P P N São descritos N casos esporádicos de hepatite P P N fulminante e de N reagudização. Considerações gerais O HAV acomete população pediátrica com evolução assintomática e população adulta com sintomatologia evidente. P: Positivo. Resultado reactivo em primeira avaliação e comfirmado em segunda avaliação. N: Negativa. Resultado não-reactivo em primeira análise e confirmado em segunda avaliação. Hepatite B O vírus da hepatite B (HBV) pertence à família Hepadnaviridae e apresenta três formas distintas: partículas defectivas esféricas, tubulares e o vírião, constituído por um envólucro (antígeno de superfície do vírus da hepatite B - HBsAg), nucleocapsídeo (antígeno do core - HBcAg e antigénio e - HBeAg), DNA de cadeia dupla parcial e a enzima polimerase. A transmissão ocorre por via parenteral, com a presença obrigatória de sangue ou derivados. A transmissão sexual é eficaz, da mesma forma que a materno-fetal, sendo a eficácia definida pelo grau de replicação viral ou pela quantidade de vírus, avaliada pela concentração de DNA-HBV (carga viral) no sangue.
130 O HBV é detectado em sangue, saliva, leite materno, secreções vaginais, sémen e líquido ascítico. A transmissão homossexual tem diminuído em consequência da consciencialização e das acções efectuadas para controlar a epidemia de SIDA. A transmissão heterossexual responde por mais de um terço dos casos novos nos EUA. A taxa de portadores do HBV varia enormemente no mundo. A taxa global nos EUA é 0,3%; em zonas da África, Filipinas, e Ásia, alcança 20%. O risco de adquirir HBV após acidente com agulhas contaminadas varia de 20%, nos casos em que o paciente é positivo para HBsAg, a 66%, quando o paciente é positivo para HBsAg e HBeAg. Estima-se a existência mundial de 300 milhões de portadores crónicos do vírus da hepatite B (HBV). A história natural de infecção aguda por HBV varia de acordo com a idade do paciente e o tempo de infecção. Em adultos, 95% dos casos evoluem com vários graus de gravidade da doença aguda, havendo resolução espontânea na maioria. Cerca de 5% de adultos e 90% de recém-nascidos infectados desenvolvem hepatites crónicas. O período de incubação para HBV varia de 45 a 180 dias. As características clínicas da doença variam consideravelmente. A icterícia acontece em menos de 10% dos casos em crianças abaixo de 5 anos de idade. Porém, a icterícia manifesta-se em 50% de crianças mais velhas e em adultos. Os sintomas incluem anorexia, náusea, vómitos, queixas gripais e fadiga. Achados físicos variam de anormalidades inespecíficas mínimas a icterícia e hepatomegalia e, ocasionalmente, características extra-hepáticas que refletem fenômenos imunológicos, como vasculites, nefrites por imunocomplexos, artrites e poliarterite nodosa. A maioria dos adultos com infecção por HBV aguda apresenta recuperação total, e cerca de 5%, especialmente os homens, desenvolve infecção crónica, que é frequentemente assintomática. Dez a 20% desses pacientes podem progredir para cirrose ou carcinoma hepático. Três fases de replicação viral acontecem durante o curso da infecção por HBV, especialmente em pacientes com hepatites crónicas. Fase de Alta Replicação Está associada à presença de HBsAg, HBeAg e HBV DNA. Ocorrem aumentos nas aminotransferases, e, histologicamente, comprova-se a actividade inflamatória moderada. O risco de evolução para cirrose é alto. Fase de Baixa Replicação Associada a perda do HBeAg, a diminuição ou a não-detecção de concentrações de DNA-HBV. A soroconversão, com aparecimento de anti-hbe, pode indicar diminuição da actividade inflamatória, uma vez que indica diminuição da replicação vírica. Fase Não-Replicante Associada a ausência, a concentrações indetectáveis ou só detectáveis por meio de técnicas ultra-sensíveis de marcadores de replicação viral, a inflamação apresentase diminuída, e os achados histológicos não são significativos. O aumento das aminotransferases, especialmente da ALT (TGP), durante a hepatite aguda B, varia de um aumento médio a moderado a um aumento notável, superior
131 a 100 vezes o valor da normalidade. As concentrações de ALT são normalmente mais altas que as de AST. A concentração de bilirrubina sobe na maioria dos pacientes com infecção aguda. A icterícia clínica manifesta-se em 50% de adultos com concentrações de bilirrubina de 3,0 mg/dl. Concentrações maiores podem acontecer. Uma elevação leve da fosfatase alcalina também é evidente. Em pacientes que desenvolvem insuficiência hepática fulminante, uma queda rápida em ALT e AST (TGO) pode levar à conclusão errónea de que a infecção hepática está a melhorar, quando na realidade, há perda de hepatócitos. Aumentos nas concentrações de aminotransferases durante mais de 6 meses são indicativos de evolução para hepatite crónica. O HBV pode determinar uma variedade de doenças hepáticas, incluindo infecção aguda autolimitada, hepatite fulminante, hepatite crónica com progressão para cirrose e falência hepática, hepatocarcinoma e estado de portador crónico assintomático. Sistemas de antigénios e anticorpos específicos são definidos como marcadores biológicos e sorológicos do HBV e podem ser detectados por testes laboratoriais sorológicos que apresentam alta sensibilidade e especificidade. O HBsAg e a IgM anti-hbc são os principais marcadores em processos de infecção aguda, embora a IgM anti-hbc possa permanecer reactiva por alguns meses, em determinados indivíduos, após essa fase. O HBsAg pode ser detectado em soro e plasma, em períodos de 3 a 13 semanas após o início da infecção, dependendo da carga viral à qual o indivíduo foi exposto. Marcadores da Hepatite B HBsAg (antigénio de envólucro Anticorpo Anti-HBs Fase de Incubação Quando positivo, é indicativo de alta replicação viral e simultâneo ao HBsAg, com prognóstico HBeAg desfavorável. (antigénio de Negativo e nucleocapsídeo viral) simultâneo ao HBsAg com significado de baixa replicação, conferindo melhor prognóstico. P N Fase aguda sintomática ou assintomática P:em altas concentrações N P ou N Convalecência Baixa concentração ou N > 10 mu/ml evoluindo para superior a 100 mu/ml N Fase crónica sintomática ou assintomática P em alta concentração N P em altos títulos ou N: em casos de mutações da região pré-core. Resposta eficaz à Vacinação N 10 mu/ml após a 1ª dose 100 mu/ml após a 2ª dose 1000 mu/ml após a 3ª dose N
132 Anticorpo N ou P:baixa Anti-HBe concetração N ou P N ou P N N HBcAg (útil em pesquisa) P P N P N IgM anti-hbc N P N N N Ac totais anti- HBc N N P P N P: define replicação viral DNA-HBV activa com alta quantitativo produção de vírus. P N P N DNA-HBV Carga viral > cópias/ml > cópias/ml > N ou cópias/ml (sem <10.000cópias/ml tratamento) P: Positivo. Resultado reactivo na primeira avaliação e comfirmado na segunda avaliação. N: Negativa. Resultado não-reactivo em primeira análise e confirmado em segunda avaliação. A concentração máxima anterior ao desenvolvimento dos sintomas pode ser definida por alguns métodos quantitativos ou estimada por métodos semiquantitativos, quando comparada ao valor limite da reacção (cut-off). Estimase que 5 a 10% dos indivíduos infectados apresentem a IgM anti-hbc como único marcador de infecção aguda. Outro antigénio estrutural, HBeAg, deve ser pesquisado sempre após a confirmação do marcador HBsAg. A detecção do antigénio, que pode ocorrer antes do desenvolvimento dos sintomas, define o grau de infectividade e de replicação viral. A soroconversão para anti-hbe ocorre durante as 5 primeiras semanas da doença, definindo a diminuição da replicação viral e, consequentemente, do grau de infectividade. A persistência do HBsAg, em concentrações elevadas, da ordem de dez a cem vezes o valor limite, e a presença do HBeAg em análises seriadas, por períodos de até 4 meses, associam-se à evolução para a infecção crónica. Anticorpos contra o HBcAg, da classe IgG, são detectados de 12 a 20 dias após a fase aguda da doença, persistindo por muitos anos. Esses anticorpos podem indicar infecção passada, na ausência de HBsAg, ou infecção crónica, quando associados ao antigénio de superfície. Alguns estudos demonstram a presença de IgG anti-hbc como único marcador em até 10% dos indivíduos. Este resultado apresenta significados diferentes que devem ser analisados para determinadas situações: - Baixas concentrações de IgG anti-hbc, geralmente inferiores a 10 vezes o valor limite, sugerem infecção passada sem replicação viral; - Altas concentrações de IgG anti-hbc, superiores a 10 vezes o valor limite, sugerem infecção passada com replicação viral indetectável, sendo necessário, nesses casos, o acompanhamento por meio da pesquisa do DNA HBV por PCR qualitativo; - Valores de IgG anti-hbc próximos ao valor limite sugerem reactividade inespecífica. N
133 Em todos os casos mencionados, deve-se avaliar a necessidade de análises em novas colheitas, utilizando-se metodologias de diferentes procedências. A complementação dos resultados, por meio da análise do HBeAg e anti-hbe, deve ser realizada. Porém, a ausência do antigénio nem sempre está associada a diminuição da replicação viral. A não-detecção do HBeAg em portadores com elevada replicação viral é possível e associa-se às mutações do DNA HBV na região do pré-core/core. A detecção do DNA HBV em soro, plasma e tecido hepático auxilia na definição da replicação viral efectiva (indivíduos HBsAg-negativo) e no diagnóstico precoce (crianças nascidas de mães HBsAg-positivo). Após a detecção qualitativa, recomenda-se a análise quantitativa da carga viral (DNA HBV). Essa avaliação apresenta sensibilidade superior a 70% quando comparada à detecção do HBeAg, sendo indicada para a monitorização do tratamento. A pesquisa de anticorpos específicos para o HBsAg é indicada para definir a fase de convalescença e redução drástica da replicação viral, sugerindo imunidade. A recomendação para o diagnóstico laboratorial é a análise de pelo menos 2 amostras de material biológico, soro ou plasma, em períodos diferentes, seguindo metodologias tradicionais. Hepatite C O vírus da hepatite C (HCV) é classificado na família Flaviviridae. Apresenta RNA de cadeia simples, polaridade positiva, com cerca de nucleotídeos. Até a sua identificação e caracterização em 1989, por Choo e colaboradores, os casos clínicos não-diagnosticados sorologicamente para os vírus das hepatites A e B ou outros vírus hepatotrópicos conhecidos (Epstein-Barr, febre amarela, citomegalovírus, vírus da hepatite delta) eram rotulados como hepatite por vírus não-a e não-b. Sabe-se, actualmente, que o HCV é o principal agente etiológico, responsável por 90 a 95% dos casos de hepatite pós-transfusional não-a e não-b. A transmissão ocorre por via parenteral, por intermédio do sangue e derivados, pela utilização de agulhas e seringas contaminadas e transplantes de órgãos e tecidos. A transmissão sexual tem sido relatada, embora seja pouco frequente. Ocorrências esporádicas, sem história prévia de transfusão ou outra causa aparente, representam cerca de 40% dos casos de hepatite C. A infecção pelo HCV assemelha-se à causada pelo vírus B, e os sintomas iniciais da doença são inespecíficos e/ou gastrointestinais, seguindo-se a icterícia. Os níveis de alanina aminotransferase apresentam flutuações, com valores inferiores aos observados nas hepatites A e B. O curso clínico da hepatite C é menos severo que o da B, porém a evolução para a forma crónica da doença ocorre em 50% dos
134 pacientes infectados pelo vírus C, em comparação aos 5 a 10% dos casos de indivíduos infectados pelo vírus B. A detecção de anticorpos contra o HCV, em amostras de soro de pacientes infectados, pode ser feita por ensaios imunológicos específicos. Porém, esses anticorpos refletem a exposição prévia ao agente infeccioso e não podem ser considerados marcadores da infecção actual. Não estão, ainda disponíveis métodos imunológicos directos para a detecção de antigénios virais e métodos de cultura celular para o isolamento viral. A quantificação dos níveis de alanina aminotransferase, associada à sorologia, é utilizada como indicador auxiliar na avaliação da infecção pelo HCV, porém não constitui medida directa da virémia. A reacção em cadeia da polimerase (PCR), pela amplificação exponencial do ácido nucleico viral, permite a detecção e a quantificação em amostras de soro ou plasma, constituindo-se a medida directa para avaliação da virémia. A capacidade de detectar e de quantificar a carga viral é altamente desejável e será especificamente requerida nas seguintes condições: estabelecer o agente etiológico em casos de infecção aguda, quando ensaios imunodiagnósticos são negativos; identificação de indivíduos assintomáticos; monitorização da virémia em casos crónicos, com fins prognósticos ou quando o imunodiagnóstico resulta em dados inconsistentes; identificação de pacientes crónicos com elevada carga viral, que possuem, portanto, alto risco de desenvolvimento do carcinoma hepatocelular; monitorização da terapia antiviral; detecção do HCV em indivíduos anti-hcv positivos que tenham desenvolvido auto-anticorpos; detecção do HCV em dadores e receptores de transplantes hepáticos; avaliação da transmissão vertical do HCV. As técnicas de rt-pcr e PCR são utilizadas para a detecção e a quantificação do RNA viral ou do DNA pró-viral integrado ao genoma da célula hospedeira, em amostras de soro ou plasma, tecido hepático e células do sangue periférico. Rotineiramente, o método da rt-pcr é utilizado com boa sensibilidade e especificidade como teste qualitativo e quantitativo em análises de soro ou plasma. A metodologia utilizada permite a amplificação em quantidade do genoma viral (RNA-HCV). Marcadores da Hepatite C Fase da incubação Fase Aguda Sintomática ou Assintomática Convalecência Fase Crónica Sintomática ou Assintomática Anti-HCV N P P P RNA-HCV qualitativo P P N P RNA-HCV > > > N carga viral cópias/ml cópias/ml cópias/ml P: Positivo. Resultado reactivo na primeira avaliação e comfirmado na segunda avaliação. N: Negativa. Resultado não-reactivo na primeira análise e confirmado na segunda avaliação. Comparação de alterações enzimáticas e marcadores em diferentes estadios da hepatite C Estadios da Anticorpos Anticorpos HCV-RNA ALT (TGP) doença ELISA RIBA (rt-pcr) Hepatite Crónica Elevada Positivo Positivo Positivo Portador da Hepatite C Normal Positivo Positivo Positivo Hepatite C em recuperação Normal Positivo Positivo Negativo Falso-positivo para anti-hcv Normal Positivo Negativo Negativo
135 Os últimos estudos têm demonstrado que reacções contendo 10 ou mais cópias de RNA-HCV são positivas. Este valor é equivalente a cópias de RNA-HCV por mililitro de soro ou plasma. A genotipagem para HCV é obtida com a utilização de métodos em biologia molecular e de sequenciamento genómico, os quais são úteis para definir os genótipos e subtipos para estudos de epidemiologia molecular, estudo clínico e monitorização da hepatite C. Consultar Genotipagem para Hepatite C. Hepatite D O vírus da hepatite Delta (HDV), as co-infecções pelos vírus da hepatite B (HBV) e HDV e as superinfecções por HDV em portadores do HBV podem ocorrer em indivíduos procedentes de áreas endémicas. A presença (infecção aguda) ou a ausência (infecção crónica) de IgM anti-hdv deverá estar sempre associada a IgM anti-hbc ou a IgG anti-hbc, respectivamente. Baixas concentrações de HDAg podem ser detectadas na fase aguda, e anticorpos IgG anti-hdv, na fase crónica. A co-infecção HBV-HDV é diagnosticada pela detecção transitória, e em baixas concentrações, de anticorpos específicos para o HDV, principalmente da classe IgM, que poderão apresentar-se como os únicos marcadores da infecção no período de declínio de HDAg e desenvolvimento de anticorpos IgG. A presença constante de HBsAg e de IgG anti-hdv, em altos títulos, indica evolução para a infecção crónica, com detecção e quantificação do RNA HDV em soro ou plasma e detecção do HDAg em tecido hepático. Testes específicos são desenvolvidos para a detecção do HDAg e RNA HDV no soro, complementados pela maior sensibilidade do teste para IgM anti-hdv. A monitorização do tratamento deve ser feita por testes quantitativos, que permitem a detecção mínima de 10 cópias do genoma viral. O HDV apresenta diferentes genótipos: I, II e III, sem haver, entretanto, correlação definida com a evolução clínica. Hepatite E O vírus da hepatite E (HEV) é um dos agentes etiológicos de hepatites agudas por veiculação hídrica. São descritos casos de evolução aguda e fulminante. Partículas de HEV podem ser detectadas em suspensões fecais, na fase aguda da doença, por métodos aplicados à pesquisa. Anticorpos IgM e IgA são detectados em soro e plasma, por metodologias tradicionais, demonstrando percentagens variadas de grupos populacionais com infecção aguda. Anticorpos IgG específicos para HEV apresentam-se em altos títulos na fase aguda da doença, posteriormente ao declínio de IgM. O RNA HEV pode ser detectado por PCR em soro, plasma ou suspensão fecal até 40 a 50 dias após o início da doença, durante a fase aguda. A detecção no material fecal é, entretanto, menos frequente (até 70%) do que nos outros materiais biológicos (93%). Hepatite G A hepatite vírica é causada por diversos agentes, com seu próprio modo de transmissão e replicação, e as doenças causadas por esses vírus diferem significativamente em relação à severidade do dano hepático. Entretanto, várias evidências laboratoriais e epidemiológicas têm sugerido a existência de agentes adicionais, que podem ser transmitidos por via parenteral. Cerca de 10 a 20% de casos de doença hepática é de etiologia desconhecida. Um agente em potencial
136 está associado ao soro de um cirurgião (com as iniciais "GB"), que tinha desenvolvido hepatite aguda sem história epidemiológica conhecida. Estudos experimentais de Deinhardt e cols. (1967) de inoculação em primatas (Saguinus sp.) com o soro desse indivíduo mostraram que o material induziu hepatite nos animais, e o agente envolvido é mencionado como agente GB. Experiências adicionais de culturas de células levaram à caracterização de GB como agente viral. Entretanto, a variação de hospedeiros primatas e experiências crosschallenge sugeriram que o agente GB era distinto dos vírus das hepatites actualmente conhecidas, em humanos. Além disso, anticorpos específicos aos vírus das hepatites A,B,C,E não eram induzidos pela inoculação de GB em macacos, como não eram detectados em imunoensaios. Foi descrita a clonagem molecular de dois genomas, com características semelhantes a flavivirus de macacos experimentalmente infectados. Esses genomas representam dois vírus independentes: GB-vírus A (GBV-A) e GB-vírus B (GBV-B). Têm sido descritos estudos de PCR para a detecção de GBV-A e GBV-B RNA e o uso de imunoensaios para anticorpos específicos aos antigénios codificados pelos genomas dos agentes GB. Os genomas de GBV-A e GBV-B apresentam semelhança limitada na sequência de nucleotídeos entre si (27%) e com o vírus da hepatite C (28%), nas regiões NS3 (helicase) e NS5B (RNA-polimerase dependente de RNA). Os seus genomas apresentam respectivamente e nucleotídeos. Os genomas desses agentes estão organizados de forma bastante semelhante a pestivírus e flavivírus, com genes que codificam proteínas estruturais e não-estruturais em terminações 5' e 3', respectivamente. O grau de divergência na sequência entre GBV-A e GBV-B e outros membros da família Flaviviridae demonstra que os agentes GB representam dois novos géneros nessa família. Um terceiro agente viral, recentemente notificado, foi identificado no soro de vários pacientes com hepatite criptogénica (não A-E). Devido ao alto grau de identidade com GBV-A (59% em nível de nucleotídeos e 64% em nível de aminoácidos), esse vírus foi chamado GB-vírus C (GBV-C). Análises filogenéticas demonstraram que o GBV-C é um membro adicional dos Flaviviridae, distinto do grupo HCV e mais intimamente relacionado ao GBV-A.. A transmissão do HGV por meio de transfusões de sangue e por outras vias de exposição parenteral, tais como em usuários de drogas injectáveis, tem sido claramente estabelecida. A partir daí, conclui-se que muitos pacientes HGV-positivo tenham sido co-infectados com HBV ou HCV, provavelmente devido aos factores de risco compartilhados da infecção. O rastreio das doações de sangue para esses vírus também elimina as unidades de sangue infectadas por HGV, reduzindo dessa forma a incidência de hepatite pós-transfusional relacionada ao HGV. Estudos recente, demonstram que a infecção por HGV está associada a hepatite na maioria dos pacientes investigados. Há também pacientes com níveis normais de transaminases que requerem estudos adicionais de sequenciamento para determinar se são portadores ou pacientes em estado quiescente da doença. A associação do vírus com a doença hepática crónica e a sua presença em pacientes com dupla infecção por HBV ou HCV é irrefutável. Entretanto, a sua associação e potencial envolvimento na hepatite fulminante e carcinoma hepatocelular ainda estão a ser investigados.
137 Estudos retrospectivos evidenciaram os seguintes pontos: - a doença relacionada ao HGV é geralmente branda, com níveis pouco elevados de ALT (TGP); - a infecção por HGV pode ser persistente e acompanhada de hepatite crónica; - as infecções por HCV/HGV e HBV/HGV podem ocorrer simultaneamente e resultam em co-infecções persistentes; - a prevalência de HGV em dadores de sangue é maior do que HCV e não se relaciona aos níveis de ALT presentes nos doadores; - nas infecções duplas, os níveis de ALT são maiores e mais frequentemente aumentados; - indivíduos com infecções duplas crónicas podem apresentar severa necroinflamação hepática; - 6% e 10% de indivíduos com infecções crónicas respectivamente por HBV e HCV, apresentam positividade para HGV. A detecção do ácido nucléico viral a partir do soro de indivíduos infectados por HGV é, actualmente, o método disponível para a identificação dos casos. Comercialmente, existem kits que contêm primers dirigidos para o sequenciamento das regiões NS5 e NCR (non-coding region) do vírus da hepatite G. Intensos estudos que empregam peptídeos indicam que o uso de epítopos lineares não resulta em reconhecimento fiável da infecção pelo vírus da hepatite G por imunoensaios. Hepatite por TTV Partículas semelhantes a vírus são observadas com frequência em amostras biológicas humanas sem, necessariamente, apresentarem correlação com alguma patologia. Recentemente, uma dessas observações, originada num trabalho de pesquisa no Japão, por Nishizawa e colaboradores, originou o chamado Transmited Transfusion Vírus (TTV), caracterizado como uma partícula semelhante a vírus, extraída de um paciente com doença hepática crónica, adquirida, provavelmente, após transfusão sanguínea. O TTV, vírus associado à hepatite pós-transfusional não A-não G, apresenta estrutura genómica formada por DNA de cadeia simples e duas Open Reading Frame (ORF), sugerindo relações filogenéticas com outros vírus da família Circiniviridae e originando dois grupos genéticos com 16 genótipos distintos. A replicação do TTV parece ocorrer em hepatócitos, onde foram detectados DNA por métodos moleculares. Novas metodologias foram desenvolvidas, com diferentes sensibilidades, permitindo determinar altas prevalências de DNA-TTV em sangue de dadores sem doença hepática aparente e em pacientes com hepatites associadas a outras etiologias víricas - HCV e HBV, não havendo evidências de interferências na evolução da doença hepática por essas co-infecções. A via de transmissão parenteral parece ser a mais eficiente. Por outro lado, dados epidemiológicos de alta prevalência em países como Escócia (1,9%) e Japão (12%) sugerem a possibilidade de vias alternativas de transmissão. A detecção de DNA-TTV em amostras de fezes colhidas em pacientes com hepatite aguda e crónica demonstra a possibilidade de transmissão fecal-oral. No Brasil, alguns dados demonstram a prevalência de DNA-TTV em 62% dos indivíduos de uma casuística de 72 dadores de sangue e em 10% da população
138 geral. No Japão, 12% dos dadores de sangue avaliados apresentaram DNA-TTV detectável, 47% hepatites fulminantes não-a-g, 46% hepatopatias crónicas de etiologia desconhecida, 39% carcinoma hepatocelular e 48% cirroses. Embora a detecção de DNA-TTV tenha sido feita em tecidos hepáticos, não há confirmação de sua patogenicidade para o fígado. Outro estudos têm sido desenvolvidos para a definição de um novo agente hepatotrópico. Herpes Simplex A infecção pelos vírus Herpes simplex (HSV) está entre as infecções víricas com maior prevalência na população mundial. Existem dois sorotipos diferenciados: HSV1 e HSV2. São vírus DNA, da família Herpetoviridae, e reagem de forma cruzada, pois os sorotipos possuem cerca de 50% de sequência homóloga. O desenvolvimento, nas últimas décadas, de técnicas sorológicas que identificam e diferenciam os sorotipos tem aumentado não só a possibilidade de diagnosticar e tratar as infecções como também de compreender melhor a sua patogenia e meios de transmissão, em especial do herpes perinatal. A transmissão pode dar-se pelo contacto com superfícies mucosas infectadas por soluções de continuidade da pele e mucosas, relações sexuais e durante o parto. A disseminação do vírus ocorre pela migração centrífuga dos vírus através dos nervos sensoriais periféricos. Na porta de entrada, na derme e na epiderme, ocorre o processo de replicação, e as partículas virais são transportadas pela terminação nervosa retrogradamente ao núcleo dos neurónios sensoriais. Conhece-se menos a sucessão de eventos a partir deste ponto. Nalguns casos, ocorre a infecção com a replicação viral e morte celular ao nível mucocutâneo. Noutros, o vírus fica em estado de lactência. O detalhe dos mecanismos da persistência em lactência do HSV e sua reactivação periódica permanecem obscuros. O primeiro episódio de doença herpética, a primoinfecção, é normalmente acompanhado de sinais e sintomas envolvendo lesões mucosas e extramucosas. Apresenta longa duração dos sintomas e da permanência dos vírus na lesão e uma taxa maior de complicações do que os episódios de reagudização ou recorrentes. A gengivoestomatite aguda é a manifestação mais comum das primoinfecções. É mais frequente entre 1 e os 4 anos de idade. O herpes labial e as úlceras da córnea são as infecções sintomáticas recorrentes mais frequentes. As manifestações clínicas e a evolução da infecção dependem da idade, da localização, do estado imunológico do paciente e do tipo antigénico do vírus. A exposição ao sol (luz ultravioleta), imunossupressão e traumas cutâneos ou do gânglio podem levar à reactivação. Ocasionalmente, múltiplas linhagens do mesmo subtipo viral são detectadas no mesmo paciente, principalmente os imunodeprimidos. Este facto sugere a possibilidade de infecção exógena por diferentes linhagens de um mesmo subtipo. A infecção pelo tipo 1 émuitas vezes, adquirida mais cedo do que a do tipo 2. Cerca de 90% dos adultos apresentam anticorpos contra HSV1 por volta dos 50 anos de idade. Nas populações socioeconómicas desfavorecidas, a faixa etária decresce para 30 anos. Os anticorpos contra o tipo 2 não são normalmente detectados até à puberdade. As taxas de prevalência desses anticorpos correlacionam-se com a fase de vida sexual activa, o que distingue um grupo do outro. A percentagem aumentou 30 pontos nos
139 últimos 12 anos nos Estados Unidos. Numa avaliação obstétrica, 25% da população investigada tinham anticorpo positivo; entretanto, apenas 10% relatavam história de lesão genital. Cerca de 50% dos adultos heterossexuais, com vida sexual activa, apresenta anticorpos positivos, sendo a taxa 5% maior entre as mulheres. O HSV tipo 1 está associado a uma variedade de infecções envolvendo lesões mucocutâneas orolabiais, oftálmicas, meningoencefálicas, podendo eventualmente causar lesões viscerais e genitais, enquanto o HSV tipo 2 (HSV2) normalmente causa as infecções genitais sexualmente adquiridas. Ambos os tipos podem causar lesões nas diferentes localizações, e a infecção clínica é indistinguível. Tanto o HSV1 como o HSV2 podem ser responsáveis por lesões mucocutâneas primárias em qualquer localização. A duração e a intensidade da infecção são independentes do sorotipo envolvido. O tipo de vírus e a localização da primoinfecção afectam a frequência e a probabilidade de recidiva. Estudos recentes demonstram que tanto a frequência como a probabilidade são maiores quando a infecção é causada pelo HSV2. A infecção genital por HSV2 ocorre com frequência oito a dez vezes maior que a infecção genital por HSV1. Por outro lado, a infecção orolabial por HSV1 ocorre mais frequentemente do que a infecção orolabial por HSV2. A probabilidade de reactivação da infecção causada pelo HSV2 é duas vezes maior. Em indivíduos imunocompetentes, a infecção limita-se às localizações mucocutanêas e ao gânglio sensorial. Em indivíduos imunodeprimidos, as lesões causadas tanto pela primoinfecção como pelas reactivações tendem a ser mais extensas e persistir por muito mais tempo do que nos indivíduos imunocompetentes. Nesses pacientes, o quadro é grave, geralmente com comprometimento esofágico, pneumonite intersticial e doença disseminada com comprometimento visceral. A infecção pelo HSV2 é do tipo infecção oportunista importante em indivíduos infectados pelo HIV. Calcula-se que até 90% desses são co-infectados com HSV2. Num pequeno número de casos, a infecção pelo HSV leva a encefalite vírica e a um dano neurológico grave. O HSV, principalmente o tipo 1, pode causar encefalite em adultos pela reactivação de infecção latente. As infecções mais agressivas, com risco de vida, são a perinatal e as que ocorrem em indivíduos imunocomprometidos, incluindo pacientes com SIDA. Existem dados que demonstram que os pacientes que apresentam episódio primário intenso e não tratado têm índices mais elevados de recorrência a longo prazo. As respostas imune, humoral e celular manifestam-se nas primeiras semanas e persistem por toda a vida. Embora não possuam carácter imunizante, induzem a manifestações mais leves e apresentam reacção cruzada entre os dois subtipos. A sorologia permite a identificação de anticorpos IgM e IgG de forma qualitativa. A avaliação deve ser realizada em sorologia pareada para melhor interpretação dos resultados. O isolamento viral em cultura de tecidos era o método de escolha para o diagnóstico e tipagem do HSV. O HSV pode ser detectado em cultura depois de 2 a 8 dias, mas em vários casos, como nos de baixos títulos virais, cura das lesões ou lesões atípicas, o vírus não pode ser isolado. A sensibilidade do isolamento do HSV em cultura de tecido é de aproximadamente 105 vírus por ml. A reacção em cadeia da polimerase (PCR) é o método de escolha para o diagnóstico da infecção por HSV. É altamente sensível (até 5 vírus por ensaio), específica (98-
140 100%), e pode identificar o genótipo e a quantificação viral. A PCR quantitativa pode ser útil para monitorizar a resposta à terapia antivírica. Os ensaios mais usados para distinguir o tipo 1 do tipo 2 são os que utilizam a avaliação da presença de anticorpos contra glicoproteínas do HSV1 (gg1) e do HSV2 (gg2). Além disso, o ensaio realizado por PCR permite o diagnóstico utilizando-se diferentes materiais como sangue, líquor, líquido amniótico, vilosidades coriónicas e sangue fetal. O líquido amniótico pode ser colhido a partir da 12ª semana até o final da gestação. Porém, o período ideal para a colheita situa-se entre a 14ª e a 16ª semana. O período ideal para a colheita de vilosidades trofoblásticos situa-se entre a 10ª e a 12ª semana de gestação. No entanto, esse prazo poderá estender-se até à 14ª semana. O período ideal para a colheita de sangue fetal situa-se entre a 18ª e a 22ª semana de gestação. Hidroxiprolina Encontrada principalmente no colagénio da matriz óssea, a hidroxiprolina é o aminoácido utilizado como marcador bioquímico do metabolismo ósseo, mais especificamente da reabsorção óssea. A hidroxiprolina libertada do osso na degradação do colagénio é metabolizada pelo fígado (90%), e apenas 10% da hidroxiprolina são eliminados na urina. A sua excreção urinária reflecte o grau de catabolismo ósseo, aumentando nos momentos em que ocorre reabsorção óssea rápida. Níveis aumentados podem ser encontrados na doença de Paget, na osteomalacia, em fracturas extensas em fase de consolidação, nas neoplasias com metástase óssea, no hipertiroidismo, no hiperparatiroidismo primário e secundário, na osteomielite aguda, na acromegalia e na artrite reumatóide em actividade. Níveis normais ou ligeiramente alterados podem ser encontrados na gravidez, na osteoporose, na doença renal e em doenças inflamatórias cutâneas. A dieta influencia directamente a taxa de libertação urinária de hidroxiprolina. Para facilitar a colheita e evitar a realização de dieta preparatória, tem sido proposta a avaliação em amostra de urina de 2 horas colhida após um jejum nocturno de 12 horas. HIV 1 O síndrome da imunodeficiência adquirida (SIDA) é causado pelo vírus da imunodeficiência humana tipo 1 (HIV-1), um retrovírus da família Retroviridae, subfamília Lentivirinae, transmitido por contacto sexual, exposição a sangue contaminado e derivados e da mãe infectada para o feto. Na infecção inicial há, geralmente, um aumento significativo da virémia, posteriormente inibida pela activação da resposta imune. As subsequentes concentrações no plasma reflectem o equilíbrio alcançado entre vírus e hospedeiro, que pode durar alguns anos. Este nível de interacção varia de pessoa para pessoa e pode ser preditivo de um curso clínico de longa duração. Nessa fase clinicamente estável, indivíduos infectados apresentam geralmente níveis de virémia baixos e persistentes e uma depleção gradual de linfócitos T CD4(+) que pode levar a uma severa imunodeficiência, ao aparecimento de múltiplas infecções oportunistas, a neoplasias e à morte.
141 O diagnóstico laboratorial pode ser feito pela pesquisa de anticorpos contra o HIV-1 por técnicas imunoenzimáticas e Western-blot. Essas técnicas, embora precisas, apresentam limitações em determinados casos, tais como: crianças em idade até 15 meses, nas quais a permanência de anticorpos maternos, adquiridos na fase gestacional através da placenta, no momento do parto ou na fase pós-parto, através do colostro, pode determinar resultados falso-positivos; casos de infecção recente, em períodos inferiores a 2 ou 3 meses, nos quais não houve, ainda, a soroconversão, e casos que apresentam resultados indeterminados ou duvidosos. Sorologia Os testes sorológicos mais comuns são os imunoenzimáticos como ELISA (Enzyme Linked Immunosorbent Assay) e ELFA (Enzyme Linked Fluorescent Assay); esses testes que pesquisam anticorpos circulantes (anti-hiv) utilizam antigénios, adsorvidos em fases sólidas, que podem ser de origem sintética, peptídeos sintéticos (geralmente gp41 e p24 para o HIV-1 e gp36 para o HIV-2) ou o próprio vírus inactivado. O método ELFA apresenta uma versão para a detecção simultânea de anti-hiv e antígeno p24 (HIV-DUO), favorecendo o diagnóstico precoce de infecção por HIV, antecipando-o em até 7 dias, quando comparado a métodos que detectam apenas anti-hiv. Os métodos enzimáticos são, preferencialmente, utilizados para triagens de diferentes populações, em bancos de sangue e amostras sorológicas de indivíduos com sintomatologia sugestiva ou mesmo assintomáticos e com história de situação de risco. Os testes imunoenzimáticos, licenciados e comercializados actualmente, apresentam sensibilidade e especificidade que ultrapassam 98% a 99%. Segundo recomendações do OMS, a entrega de um resultado de um teste sorológico anti-hiv positivo só pode ser concretizada se pelo menos dois testes forem realizados em paralelo, com a mesma amostra, por metodologias diferentes (outro fabricante, outro tipo de antigénio ou diferente princípio metodológico) Se os resultos forem positivos ou discordantes (+/ -), é necessário a realização de um teste confirmatório, sendo o Western-blot o utilizado na rotina da maioria dos laboratórios privados. Caso após estas duas etapas o resultado final seja positivo, uma segunda amostra clínica deve ser solicitada para a repetição do procedimento realizado na primeira amostra. Havendo discordância entre os resultados da 1ª amostra com os obtidos na 2ª amostra, solicita-se uma nova colheita. O teste confirmatório para a presença de anticorpos anti-hiv indicado em crianças até dois anos de idade é a reacção em cadeia da polimerase (PCR) para a pesquisa do cdna-hiv. Em indivíduos com alto risco de exposição ao HIV, uma reactividade intensa pelo teste imunoenzimático apresenta um valor preditivo de 99%. Podem ocorrer reactividades falso-positivas em testes imunoenzimáticos, principalmente em pacientes com hepatite alcoólica, outras patologias em que ocorram anormalidades imunológicas, neoplasias, mulheres multíparas e indivíduos politransfundidos, os quais desenvolveram anticorpos contra antigénios HLA classe II, presentes em linhagens de células onde há a replicação do HIV. Os testes imunoenzimáticos para HIV-1 detectam 40% a 90% de infecções causadas por HIV-2, e testes de ELISA licenciados para HIV-2 têm uma sensibilidade de 99%. A opção mais utilizada actualmente são os testes imunoenzimáticos que detectam, simultaneamente, anticorpos contra HIV1 e HIV2.
142 A detecção de antigénio p24 do HIV-1 circulante por teste imunoenzimático é particularmente útil em determinadas situações. Nas primeiras semanas após a infecção, o antigénio p24 está presente no soro, antes da detecção dos anticorpos. Com o aparecimento destes, o antigénio p24 torna-se indetectável, permanecendo assim por meses ou anos. O reaparecimento da antigenémia durante o curso da infecção geralmente está associado a um prognóstico desfavorável. Métodos para a detecção de antigénio p24, principalmente aqueles que utilizam dissociação ácida, também têm sido utilizados para acompanhar pacientes em tratamento antiviral, conforme demonstrado durante ensaios clínicos. A sua eficácia porém é comprometida devido à baixa sensibilidade dos métodos actualmente disponíveis, sendo substituídos pela detecção da carga viral por metodologias de biologia molecular. Western-Blot O método de Western-Blot é amplamente utilizado como teste confirmatório dos resultados obtidos em testes imunoenzimáticos. Outros testes também são indicados, como imunofluorescência em células fixadas e o teste RIPA (Radio Immuno Precipitation Assay). O Western-Blot utiliza antigénios do HIV, obtidos em cultura de linhagem celular, separados eletroforecticamente em bandas distintas, posteriormente transferidas para membrana de nitrocelulose. A reacção ocorre entre os antigénios em contacto com os anticorpos, presentes no soro ou no plasma de indivíduos infectados. Padrões específicos de reacções podem ser identificados, e embora a definição de testes positivos seja controversaa, a ausência de reacções específicas para os diferentes antigénios do HIV confirma a reacção negativa. Padrões de positividade (presença de anticorpos) podem ser definidos no teste confirmatório de Western-Blot, pela visualização de bandas correspondentes às três principais proteínas virais: a proteína do núcleo, p24 ou p31 e duas proteínas do envólucro, gp41 e gp120/gp160. Alternativamente, o Centers for Diseases Control and Prevention-CDC recomenda que pelo menos uma das duas, p24 ou gp120/gp160, seja identificada. Outras bandas de antigénios do HIV são p17, p31, p51, p55, p66. Padrões definindo casos indeterminados, quando apenas uma das três principais bandas é visualizada no teste de Western-Blot, podem ocorrer, causando dúvidas quanto à real interpretação. Indivíduos infectados, em fase avançada de SIDA, podem não apresentar reactividade para p24, sugerindo resultado indeterminado. Alguns podem apresentar esse padrão por longo período de tempo, sem evidências de infecção por HIV. As interpretações mais correctas e apropriadas para os resultados de testes de ELISA reactivos e Western-blot indeterminados envolvem avaliações clínicas e acompanhamento laboratorial. Testes de Western-Blot são desenvolvidos por diferentes laboratórios de produção de kits e reagentes para diagnóstico. Isto origina a possibilidade de diferentes critérios de interpretação que devem estar sempre sujeitos a avaliações comparativas com aqueles recomendados por instituições de referência, tais como o CDC. A interpretação de resultados poderá acompanhar também os critérios complementares como se seguem: A presença ou a ausência de anticorpos contra HIV-1 em amostras de soro e/ou plasma e a identificação de anticorpos presentes são determinadas pela comparação de cada reacção com os controlos de reactividade baixa, alta e ausente. Deverão ser seguidas três fases de interpretação: primeira - cada banda
143 de reacção que aparece na fita de nitrocelulose da amostra deverá ser identificada comparativamente ao controlo padrão de alta reactividade; segunda - cada banda deverá ser avaliada com base na intensidade de reacção; terceira - a interpretação deverá ser finalizada pela associação dos padrões de reactividade. Proposta de interpretação alternativa seguindo-se os critérios de interpretação do Centers for Diseases Control and Prevention e da Association of State and Territorial Public Health Laboratory Directors (ASTPHLD): PADRÃO Ausência da bandas Presença de alguma banda sem atender ao critério de POSITIVO Duas ou mais bandas das seguintes alternativas: p24, gp41 e gp120/160. Cada banda com reactividade maior ou igual ao padrão positivo. Normalmente a banda para gp41 ou gp160 é difusa. Outras bandas poderão ou não estar presentes. INTERPRETAÇÃO NEGATIVO INDETERMINADO POSITIVO Nalgumas publicações, sugere-se que não há necessidade da presença de reactividade para p31. Outros estudos indicam como inadequada a interpretação de positividade para reacções em que estejam ausentes quaisquer duas das bandas para p24, gp41 ou gp 120/160 com padrão de reactividade igual ou maior do que controlo positivo. É reconhecido que indivíduos com soroconversão recente podem apresentar padrões distintos e incompletos de reacção mas que evoluirão para aumento de reactividade, em número e intensidade, quando acompanhados por períodos de 4 a 6 meses. Os resultados com interpretação de POSITIVO apresentarão as bandas p17, p31, p55, p66 e gp120. Reactividades inespecíficas, que persistem mas não evoluem para padrões completos, podem ocorrer, em particular nas regiões p17, p24, p55 e p66. As reactividades inespecíficas podem ser atribuídas a auto-anticorpos ou a reactividades com outros retrovirus humanos. Tem sido evidenciado que pacientes com SIDA perdem a reactividade para p24 e p31, e que em crianças pode haver falha de soroconversão e persistência de anticorpos maternos por vários meses.
144 Pacientes com doenças tumorais e em tratamento com imunossupressores podem falhar na resposta com padrão de positividade em Western-Blot. Bandas inespecíficas que não estejam acompanhadas das principais bandas de proteínas virais, p24 e gp41/120/160, podem estar relacionadas com constituintes celulares com pesos moleculares em torno de 70K, 51-55K (possivelmente originadas de HLA DR) e 43 K (de origem HLA-ABC). Carga Viral A quantificação de partículas virais no sangue periférico, que define a carga viral, pode ser estimada por níveis plasmáticos de antígeno p24, a principal proteína do nucleocapsídeo viral; por métodos quantitativos de cultura celular para HIV-1 ou pela quantificação directa do RNA viral no plasma, através de tecnologias de amplificação do ácido nucléico ou de amplificação de sondas marcadas. A utilização de testes quantitativos para antigénio p24 como parâmetro na avaliação da carga viral é de valor limitado, uma vez que apenas 20% de indivíduos assintomáticos e 40 a 50% de pacientes sintomáticos apresentam níveis antigénicos detectáveis, mesmo utilizando-se procedimentos de dissociação de imunocomplexos. As metodologias de biologia molecular (RT-PCR, b-dna, Nuclisens-NASBA) são metodologias quantitativas hoje recomendadas para a avaliação da carga viral. Elas permitem a quantificação directa do RNA viral em amostras de plasma. A carga viral, definida em número de cópias do genoma viral por mililitro de plasma, está correlacionada com o estadio da infecção, ao risco de evolução para SIDA e à eficácia do tratamento anti-retroviral. Vários estudos demonstram que níveis mais elevados de carga viral estão associados a maior risco de evolução da doença, enquanto níveis mais baixos correlacionam-se a risco diminuído de progressão clínica. A avaliação da carga viral, associada a dados clínicos e a outros parâmetros laboratoriais, permite ao clínico estabelecer condutas adequadas na monitorização do tratamento anti-retroviral. As metodologias de biologia molecular podem apresentar diferentes sensibilidades. A RT-PCR apresenta sensibilidade da ordem de 200 cópias de RNA viral, e a RT-PCR ultra-sensível, da ordem de 50 cópias. É recomendada a realização de duas avaliações, com intervalos de 15 dias, para o estabelecimento dos níveis de carga viral antes do tratamento. A eficácia do tratamento anti-retroviral é acompanhada por avaliação 4 semanas após o início da terapia. É esperado um declínio inicial rápido dos níveis da carga viral, que se segue a uma diminuição em ritmo mais lento e moderado no decurso dos meses subsequentes. A carga viral deve ser repetida rotineiramente a cada 3 ou 4 meses. Nos momentos de mudança terapêutica ou início de novos esquemas, recomendase uma avaliação em 2 a 4 semanas após a alteração e a cada 10 a 12 semanas. É indicado que a carga viral seja avaliada com o paciente em situação clínica estável. Em casos de imunização recente, recomenda-se um intervalo mínimo de 4 semanas para a colheita da amostr. Sugere-se também que sejam utilizadas as mesmas metodologias e o mesmo laboratório.
145 Homocisteína A aterosclerose é uma doença da actualidade, e a sua consequência mais drástica é a coronariopatia, uma das mais importantes causas de mortalidade nos países desenvolvidos. Vários factores já se encontram descritos como factores de risco para o aparecimento da doença, com inúmeras confirmações epidemiológicas. Dessa forma, o tabagismo, a hipercolesterolemia, o sedentarismo, a obesidade, a hipertensão arterial e a diabetes mellitus colaboram efectivamente para a instalação de doença aterosclerótica. De forma revolucionária, agentes infecciosos como Chlamydia pneumoniae, Helicobacter pylori e alguns vírus (herpes, citomegalovírus e vírus sincicial respiratório) passaram também a contribuir na causa de disfunções endoteliais e aterogénese. Recentemente, um novo factor tem sido aventado no desenvolvimento dessa doença: o aumento sérico de homocisteína (hiper-homocisteinémia). A hiperhomocisteinémia é, actualmente, considerada um factor de risco independente para doença arterial coronária, doença vascular periférica, doença cerebrovascular e tromboses. A evidência epidemiológica de que talvez esse aminoácido pudesse estar envolvido no desenvolvimento da aterosclerose veio da observação de que crianças com homocistinúria, um erro inato do metabolismo devido a um defeito monogénico autossómico recessivo que cursa com aumento de homocisteína plasmática e urinária, possuíam alto potencial aterogénico. A homocisteína é um pequeno aminoácido sulfidrílico que ocupa posição reguladora central no metabolismo da metionina. O plasma humano contém formas reduzidas (1%) e oxidadas de homocisteína (98 a 99%), sendo que de 80 a 90% da forma oxidada se encontram ligados a resíduos protéicos. A metileno tetraidrofolato redutase (MTHFR) é uma importante enzima no metabolismo da homocisteína. A sua actividade, quando diminuída, tem sido associada à hiper-homocisteinémia. Uma das principais causas de diminuição da actividade é uma mutação (Ala 677- >Val), que resulta na forma termolábil da enzima, que possui então 50% da actividade normal. Deficiências de vitaminas do complexo B, seja por insuficiência na dieta ou má absorção, estão associadas ao aumento de homocisteína sérica. O doseamento de homocisteína na população geral de adultos saudáveis revela concentrações que variam entre 5 a 15 mmol/l. Estudos recentes, demonstram que o nível desejável deve estar abaixo de 10 mmol/l. Concentrações situadas acima de 15 mmol/l são consideradas patológicas. Indivíduos com doença vascular
RESUMO DOS PRINCIPAIS AUTO-ANTICORPOS E MARCADORES REUMÁTICOS
 RESUMO DOS PRINCIPAIS AUTO-ANTICORPOS E MARCADORES REUMÁTICOS [ Índice ] Lúpus eritematoso sistêmico Esclerodermia Polimiosite/Dermatomiosite Doença mista do tecido conjuntivo Síndrome de Sjögren Vasculites
RESUMO DOS PRINCIPAIS AUTO-ANTICORPOS E MARCADORES REUMÁTICOS [ Índice ] Lúpus eritematoso sistêmico Esclerodermia Polimiosite/Dermatomiosite Doença mista do tecido conjuntivo Síndrome de Sjögren Vasculites
Interpretação de exames laboratoriais Lactato desidrogenase (LDH)
 Interpretação de exames laboratoriais Lactato desidrogenase (LDH) Nathália Krishna O que é? NAD+ está presente em quantidades somente catalíticas na célula e é um cofator essencial para a glicólise,dessa
Interpretação de exames laboratoriais Lactato desidrogenase (LDH) Nathália Krishna O que é? NAD+ está presente em quantidades somente catalíticas na célula e é um cofator essencial para a glicólise,dessa
Rejeição de Transplantes Doenças Auto-Imunes
 Rejeição de Transplantes Doenças Auto-Imunes Mecanismos da rejeição de transplantes Envolve várias reações de hipersensibilidade, tanto humoral quanto celular Habilidade cirúrgica dominada para vários
Rejeição de Transplantes Doenças Auto-Imunes Mecanismos da rejeição de transplantes Envolve várias reações de hipersensibilidade, tanto humoral quanto celular Habilidade cirúrgica dominada para vários
INTERPRETAÇÃO DE EXAMES LABORATORIAIS
 INTERPRETAÇÃO DE EXAMES LABORATORIAIS CINÉTICA DO FERRO Danni Wanderson Introdução A importância do ferro em nosso organismo está ligado desde as funções imune, até as inúmeras funções fisiológicas, como
INTERPRETAÇÃO DE EXAMES LABORATORIAIS CINÉTICA DO FERRO Danni Wanderson Introdução A importância do ferro em nosso organismo está ligado desde as funções imune, até as inúmeras funções fisiológicas, como
O que é Hemofilia? O que são os fatores de coagulação? A hemofilia tem cura?
 Volume1 O que é? O que é Hemofilia? Hemofilia é uma alteração hereditária da coagulação do sangue que causa hemorragias e é provocada por uma deficiência na quantidade ou qualidade dos fatores VIII (oito)
Volume1 O que é? O que é Hemofilia? Hemofilia é uma alteração hereditária da coagulação do sangue que causa hemorragias e é provocada por uma deficiência na quantidade ou qualidade dos fatores VIII (oito)
QUESTÕES DE HEMATOLOGIA E SUAS RESPOSTAS
 QUESTÕES DE HEMATOLOGIA E SUAS RESPOSTAS O QUE É VERDADEIRO E O QUE É FALSO? Questões 1 Anemia na deficiência de ferro a) Está geralmente associada com elevação do VCM. b) O HCM geralmente está diminuído.
QUESTÕES DE HEMATOLOGIA E SUAS RESPOSTAS O QUE É VERDADEIRO E O QUE É FALSO? Questões 1 Anemia na deficiência de ferro a) Está geralmente associada com elevação do VCM. b) O HCM geralmente está diminuído.
Hormonas e mensageiros secundários
 Hormonas e mensageiros secundários Interrelação entre os tecidos Comunicação entre os principais tecidos Fígado tecido adiposo hormonas sistema nervoso substratos em circulação músculo cérebro 1 Um exemplo
Hormonas e mensageiros secundários Interrelação entre os tecidos Comunicação entre os principais tecidos Fígado tecido adiposo hormonas sistema nervoso substratos em circulação músculo cérebro 1 Um exemplo
ÇÃO O DE EXAMES LABORATORIAIS
 INTERPRETAÇÃ ÇÃO O DE EXAMES LABORATORIAIS TRANSAMINASES HEPÁTICAS (TGO/TGP) Everton José Moreira Rodrigues Transaminases: enzimas que catalisam a transferência de um grupo alfa-amino de um aminoácido
INTERPRETAÇÃ ÇÃO O DE EXAMES LABORATORIAIS TRANSAMINASES HEPÁTICAS (TGO/TGP) Everton José Moreira Rodrigues Transaminases: enzimas que catalisam a transferência de um grupo alfa-amino de um aminoácido
Tipos de Diabetes. Diabetes Gestacional
 Tipos de Diabetes Diabetes Gestacional Na gravidez, duas situações envolvendo o diabetes podem acontecer: a mulher que já tinha diabetes e engravida e o diabetes gestacional. O diabetes gestacional é a
Tipos de Diabetes Diabetes Gestacional Na gravidez, duas situações envolvendo o diabetes podem acontecer: a mulher que já tinha diabetes e engravida e o diabetes gestacional. O diabetes gestacional é a
CAMPANHA PELA INCLUSÃO DA ANÁLISE MOLECULAR DO GENE RET EM PACIENTES COM CARCINOMA MEDULAR E SEUS FAMILIARES PELO SUS.
 Laura S. W ard CAMPANHA PELA INCLUSÃO DA ANÁLISE MOLECULAR DO GENE RET EM PACIENTES COM CARCINOMA MEDULAR E SEUS FAMILIARES PELO SUS. Nódulos da Tiróide e o Carcinoma Medular Nódulos da tiróide são um
Laura S. W ard CAMPANHA PELA INCLUSÃO DA ANÁLISE MOLECULAR DO GENE RET EM PACIENTES COM CARCINOMA MEDULAR E SEUS FAMILIARES PELO SUS. Nódulos da Tiróide e o Carcinoma Medular Nódulos da tiróide são um
Perguntas e respostas sobre imunodeficiências primárias
 Perguntas e respostas sobre imunodeficiências primárias Texto elaborado pelos Drs Pérsio Roxo Júnior e Tatiana Lawrence 1. O que é imunodeficiência? 2. Estas alterações do sistema imunológico são hereditárias?
Perguntas e respostas sobre imunodeficiências primárias Texto elaborado pelos Drs Pérsio Roxo Júnior e Tatiana Lawrence 1. O que é imunodeficiência? 2. Estas alterações do sistema imunológico são hereditárias?
EXERCÍCIO E DIABETES
 EXERCÍCIO E DIABETES Todos os dias ouvimos falar dos benefícios que os exercícios físicos proporcionam, de um modo geral, à nossa saúde. Pois bem, aproveitando a oportunidade, hoje falaremos sobre a Diabetes,
EXERCÍCIO E DIABETES Todos os dias ouvimos falar dos benefícios que os exercícios físicos proporcionam, de um modo geral, à nossa saúde. Pois bem, aproveitando a oportunidade, hoje falaremos sobre a Diabetes,
COAGULOPATIAS NO PACIENTE ONCOLÓGICO. Dra Carmen Helena Vasconcellos Hospital Veterinário Botafogo - RJ
 COAGULOPATIAS NO PACIENTE ONCOLÓGICO Dra Carmen Helena Vasconcellos Hospital Veterinário Botafogo - RJ HEMOSTASIA Conjunto de mecanismos que visa manter a fluidez do sangue no interior dos vasos no sistema
COAGULOPATIAS NO PACIENTE ONCOLÓGICO Dra Carmen Helena Vasconcellos Hospital Veterinário Botafogo - RJ HEMOSTASIA Conjunto de mecanismos que visa manter a fluidez do sangue no interior dos vasos no sistema
VIVER BEM OS RINS DO SEU FABRÍCIO AGENOR DOENÇAS RENAIS
 VIVER BEM OS RINS DO SEU FABRÍCIO AGENOR DOENÇAS RENAIS Leia o código e assista a história de seu Fabrício Agenor. Este é o seu Fabrício Agenor. Ele sempre gostou de comidas pesadas e com muito tempero
VIVER BEM OS RINS DO SEU FABRÍCIO AGENOR DOENÇAS RENAIS Leia o código e assista a história de seu Fabrício Agenor. Este é o seu Fabrício Agenor. Ele sempre gostou de comidas pesadas e com muito tempero
Patologia por imagem Abdome. ProfºClaudio Souza
 Patologia por imagem Abdome ProfºClaudio Souza Esplenomegalia Esplenomegalia ou megalosplenia é o aumento do volume do baço. O baço possui duas polpas que são constituídas por tecido mole, polpa branca
Patologia por imagem Abdome ProfºClaudio Souza Esplenomegalia Esplenomegalia ou megalosplenia é o aumento do volume do baço. O baço possui duas polpas que são constituídas por tecido mole, polpa branca
TROMBOCITOPENIA NA GRAVIDEZ
 TROMBOCITOPENIA NA GRAVIDEZ Ricardo Oliveira Santiago Francisco Herlânio Costa Carvalho INTRODUÇÃO: - Trombocitopenia pode resultar de uma variedade de condições fisiológicas e patológicas na gravidez.
TROMBOCITOPENIA NA GRAVIDEZ Ricardo Oliveira Santiago Francisco Herlânio Costa Carvalho INTRODUÇÃO: - Trombocitopenia pode resultar de uma variedade de condições fisiológicas e patológicas na gravidez.
Fibrose Cística. Triagem Neonatal
 Fibrose Cística Triagem Neonatal Fibrose cística Doença hereditária autossômica e recessiva, mais frequente na população branca; Distúrbio funcional das glândulas exócrinas acometendo principalmente os
Fibrose Cística Triagem Neonatal Fibrose cística Doença hereditária autossômica e recessiva, mais frequente na população branca; Distúrbio funcional das glândulas exócrinas acometendo principalmente os
DOENÇAS CARDÍACAS NA INSUFICIÊNCIA RENAL
 DOENÇAS CARDÍACAS NA INSUFICIÊNCIA RENAL As doenças do coração são muito freqüentes em pacientes com insuficiência renal. Assim, um cuidado especial deve ser tomado, principalmente, na prevenção e no controle
DOENÇAS CARDÍACAS NA INSUFICIÊNCIA RENAL As doenças do coração são muito freqüentes em pacientes com insuficiência renal. Assim, um cuidado especial deve ser tomado, principalmente, na prevenção e no controle
Adaptações Cardiovasculares da Gestante ao Exercício
 Desde as décadas de 60 e 70 o exercício promove Aumento do volume sanguíneo Aumento do volume cardíaco e suas câmaras Aumento do volume sistólico Aumento do débito cardíaco que pode ser alcançado Aumento
Desde as décadas de 60 e 70 o exercício promove Aumento do volume sanguíneo Aumento do volume cardíaco e suas câmaras Aumento do volume sistólico Aumento do débito cardíaco que pode ser alcançado Aumento
Trombofilias. Dr Alexandre Apa
 Trombofilias Dr Alexandre Apa TENDÊNCIA À TROMBOSE TRÍADE DE VIRCHOW Mudanças na parede do vaso Mudanças no fluxo sanguíneo Mudanças na coagulação do sangue ESTADOS DE HIPERCOAGULABILIDADE
Trombofilias Dr Alexandre Apa TENDÊNCIA À TROMBOSE TRÍADE DE VIRCHOW Mudanças na parede do vaso Mudanças no fluxo sanguíneo Mudanças na coagulação do sangue ESTADOS DE HIPERCOAGULABILIDADE
Litíase urinária- Identificação dos grupos de risco e tratamento. Humberto Lopes UFJF II Encontro de Urologia do Sudeste - BH
 - Identificação dos grupos de risco e tratamento Humberto Lopes UFJF II Encontro de Urologia do Sudeste - BH 11% homens X 5,6% mulheres Brancos X negros Oxalato de cálcio 80% Recorrência 40% 5 anos, 75%
- Identificação dos grupos de risco e tratamento Humberto Lopes UFJF II Encontro de Urologia do Sudeste - BH 11% homens X 5,6% mulheres Brancos X negros Oxalato de cálcio 80% Recorrência 40% 5 anos, 75%
Biomassa de Banana Verde Integral- BBVI
 Biomassa de Banana Verde Integral- BBVI INFORMAÇÕES NUTRICIONAIS Porção de 100g (1/2 copo) Quantidade por porção g %VD(*) Valor Energético (kcal) 64 3,20 Carboidratos 14,20 4,73 Proteínas 1,30 1,73 Gorduras
Biomassa de Banana Verde Integral- BBVI INFORMAÇÕES NUTRICIONAIS Porção de 100g (1/2 copo) Quantidade por porção g %VD(*) Valor Energético (kcal) 64 3,20 Carboidratos 14,20 4,73 Proteínas 1,30 1,73 Gorduras
Tome uma injeção de informação. Diabetes
 Tome uma injeção de informação. Diabetes DIABETES O diabetes é uma doença crônica, em que o pâncreas não produz insulina em quantidade suficiente, ou o organismo não a utiliza da forma adequada. Tipos
Tome uma injeção de informação. Diabetes DIABETES O diabetes é uma doença crônica, em que o pâncreas não produz insulina em quantidade suficiente, ou o organismo não a utiliza da forma adequada. Tipos
DIABETES MELLITUS. Ricardo Rodrigues Cardoso Educação Física e Ciências do DesportoPUC-RS
 DIABETES MELLITUS Ricardo Rodrigues Cardoso Educação Física e Ciências do DesportoPUC-RS Segundo a Organização Mundial da Saúde, existem atualmente cerca de 171 milhões de indivíduos diabéticos no mundo.
DIABETES MELLITUS Ricardo Rodrigues Cardoso Educação Física e Ciências do DesportoPUC-RS Segundo a Organização Mundial da Saúde, existem atualmente cerca de 171 milhões de indivíduos diabéticos no mundo.
GRUPO HOSPITALAR CONCEIÇÃO HOSPITAL NOSSA SENHORA DA CONCEIÇÃO LABORATÓRIO DE ANÁLISES CLÍNICAS
 POP n.º: I 22 Página 1 de 5 1. Sinonímia Beta 2 Microglobulina, b2m 2. Aplicabilidade Aos técnicos e bioquímicos do setor de imunologia 3. Aplicação clínica A beta-2-microglobulina é uma proteína presente
POP n.º: I 22 Página 1 de 5 1. Sinonímia Beta 2 Microglobulina, b2m 2. Aplicabilidade Aos técnicos e bioquímicos do setor de imunologia 3. Aplicação clínica A beta-2-microglobulina é uma proteína presente
PERFIL PANCREÁTICO. Prof. Dr. Fernando Ananias. MONOSSACARÍDEOS Séries das aldoses
 PERFIL PANCREÁTICO Prof. Dr. Fernando Ananias MONOSSACARÍDEOS Séries das aldoses 1 DISSACARÍDEO COMPOSIÇÃO FONTE Maltose Glicose + Glicose Cereais Sacarose Glicose + Frutose Cana-de-açúcar Lactose Glicose
PERFIL PANCREÁTICO Prof. Dr. Fernando Ananias MONOSSACARÍDEOS Séries das aldoses 1 DISSACARÍDEO COMPOSIÇÃO FONTE Maltose Glicose + Glicose Cereais Sacarose Glicose + Frutose Cana-de-açúcar Lactose Glicose
Retinopatia Diabética
 Retinopatia Diabética A diabetes mellitus é uma desordem metabólica crónica caracterizada pelo excesso de níveis de glicose no sangue. A causa da hiper glicemia (concentração de glicose igual ou superior
Retinopatia Diabética A diabetes mellitus é uma desordem metabólica crónica caracterizada pelo excesso de níveis de glicose no sangue. A causa da hiper glicemia (concentração de glicose igual ou superior
EXERCÍCIOS ON LINE DE CIÊNCIAS 8 AN0
 EXERCÍCIOS ON LINE DE CIÊNCIAS 8 AN0 1- Que órgão do sistema nervoso central controla nosso ritmo respiratório? Bulbo 2- Os alvéolos são formados por uma única camada de células muito finas. Explique como
EXERCÍCIOS ON LINE DE CIÊNCIAS 8 AN0 1- Que órgão do sistema nervoso central controla nosso ritmo respiratório? Bulbo 2- Os alvéolos são formados por uma única camada de células muito finas. Explique como
Diabetes Gestacional
 Diabetes Gestacional Introdução O diabetes é uma doença que faz com que o organismo tenha dificuldade para controlar o açúcar no sangue. O diabetes que se desenvolve durante a gestação é chamado de diabetes
Diabetes Gestacional Introdução O diabetes é uma doença que faz com que o organismo tenha dificuldade para controlar o açúcar no sangue. O diabetes que se desenvolve durante a gestação é chamado de diabetes
CENTRO DE APOIO OPERACIONAL DE DEFESA DA SAÚDE CESAU ORIENTAÇÃO TÉCNICA N.º 064 /2015 - CESAU
 ORIENTAÇÃO TÉCNICA N.º 064 /2015 - CESAU Salvador, 13 de abril de 2015 OBJETO: Parecer. - Centro de Apoio Operacional de Defesa da Saúde- CESAU REFERÊNCIA: 3 a promotoria de Justiça de Dias D'Àvila / Dispensação
ORIENTAÇÃO TÉCNICA N.º 064 /2015 - CESAU Salvador, 13 de abril de 2015 OBJETO: Parecer. - Centro de Apoio Operacional de Defesa da Saúde- CESAU REFERÊNCIA: 3 a promotoria de Justiça de Dias D'Àvila / Dispensação
Saiba quais são os diferentes tipos de diabetes
 Saiba quais são os diferentes tipos de diabetes Diabetes é uma doença ocasionada pela total falta de produção de insulina pelo pâncreas ou pela quantidade insuficiente da substância no corpo. A insulina
Saiba quais são os diferentes tipos de diabetes Diabetes é uma doença ocasionada pela total falta de produção de insulina pelo pâncreas ou pela quantidade insuficiente da substância no corpo. A insulina
ALTERAÇÕES METABÓLICAS NA GRAVIDEZ
 ALTERAÇÕES METABÓLICAS NA GRAVIDEZ CUSTO ENERGÉTICO DA GRAVIDEZ CRESCIMENTO E DESENVOLVIMENTO FETAL SÍNTESE DE TECIDO MATERNO 80.000 kcal ou 300 Kcal por dia 2/4 médios 390 Kcal depósito de gordura- fase
ALTERAÇÕES METABÓLICAS NA GRAVIDEZ CUSTO ENERGÉTICO DA GRAVIDEZ CRESCIMENTO E DESENVOLVIMENTO FETAL SÍNTESE DE TECIDO MATERNO 80.000 kcal ou 300 Kcal por dia 2/4 médios 390 Kcal depósito de gordura- fase
Câncer de Próstata. Fernando Magioni Enfermeiro do Trabalho
 Câncer de Próstata Fernando Magioni Enfermeiro do Trabalho O que é próstata? A próstata é uma glândula que só o homem possui e que se localiza na parte baixa do abdômen. Ela é um órgão muito pequeno, tem
Câncer de Próstata Fernando Magioni Enfermeiro do Trabalho O que é próstata? A próstata é uma glândula que só o homem possui e que se localiza na parte baixa do abdômen. Ela é um órgão muito pequeno, tem
SISTEMA URINÁRIO. Prof. Me. Leandro Parussolo
 SISTEMA URINÁRIO Prof. Me. Leandro Parussolo SISTEMA URINÁRIO Conjunto de órgãos e estruturas responsáveis pela filtração do sangue e consequente formação da urina; É o principal responsável pela eliminação
SISTEMA URINÁRIO Prof. Me. Leandro Parussolo SISTEMA URINÁRIO Conjunto de órgãos e estruturas responsáveis pela filtração do sangue e consequente formação da urina; É o principal responsável pela eliminação
Mônica H. C. Fernandes de Oliveira
 DISTÚRBIOS DA COAGULAÇÃO Mônica H. C. Fernandes de Oliveira Conceito A hemostasia é o processo fisiológico responsável pela manutenção do sangue em estado líquido e a integridade do envelope vascular.
DISTÚRBIOS DA COAGULAÇÃO Mônica H. C. Fernandes de Oliveira Conceito A hemostasia é o processo fisiológico responsável pela manutenção do sangue em estado líquido e a integridade do envelope vascular.
Epidemiologia DIABETES MELLITUS
 Epidemiologia DIABETES MELLITUS 300 milhões / mundo ( 5,9% população adulta) / Brasil : > 10 milhões Aumento progressivo : Longevidade, Síndrome metabólica Mortalidade anual : 3,8 milhões AVC, IAM... Amputação
Epidemiologia DIABETES MELLITUS 300 milhões / mundo ( 5,9% população adulta) / Brasil : > 10 milhões Aumento progressivo : Longevidade, Síndrome metabólica Mortalidade anual : 3,8 milhões AVC, IAM... Amputação
REGULAÇÃO HIDROELETROLÍTICA FUNÇÃO RENAL
 REGULAÇÃO HIDROELETROLÍTICA FUNÇÃO RENAL Bioquímica Profa. Dra. Celene Fernandes Bernardes Referências Bioquímica Clínica M A T Garcia e S Kanaan Bioquímica Mèdica J W Baynes e M H Dominiczack Fundamentos
REGULAÇÃO HIDROELETROLÍTICA FUNÇÃO RENAL Bioquímica Profa. Dra. Celene Fernandes Bernardes Referências Bioquímica Clínica M A T Garcia e S Kanaan Bioquímica Mèdica J W Baynes e M H Dominiczack Fundamentos
Roberto Satler Cetlin R2 CLN ANCP
 Roberto Satler Cetlin R2 CLN ANCP Aspectos Históricos Final do século XIX: primeiras descrições da associação entre SNC e anemia megaloblástica (Leichtenstern e Lichtheim). Início do séc. XX: descritas
Roberto Satler Cetlin R2 CLN ANCP Aspectos Históricos Final do século XIX: primeiras descrições da associação entre SNC e anemia megaloblástica (Leichtenstern e Lichtheim). Início do séc. XX: descritas
PROVA ESPECÍFICA Cargo 48. Na reação de hipersensibilidade imediata do tipo I, qual dos seguintes mediadores é neoformado nos tecidos?
 11 PROVA ESPECÍFICA Cargo 48 QUESTÃO 26 Na reação de hipersensibilidade imediata do tipo I, qual dos seguintes mediadores é neoformado nos tecidos? a) Heparina. b) Histamina. c) Fator ativador de plaquetas
11 PROVA ESPECÍFICA Cargo 48 QUESTÃO 26 Na reação de hipersensibilidade imediata do tipo I, qual dos seguintes mediadores é neoformado nos tecidos? a) Heparina. b) Histamina. c) Fator ativador de plaquetas
As principais causas de diabetes insípidus central são tumores que acometem a região hipotalâmica hipofisária, como por exemplo:
 Diabetes insípidus O que é Diabetes insípidus? Diabetes insípidus consiste em um distúrbio de controle da água no organismo, no qual os rins não conseguem reter adequadamente a água que é filtrada. Como
Diabetes insípidus O que é Diabetes insípidus? Diabetes insípidus consiste em um distúrbio de controle da água no organismo, no qual os rins não conseguem reter adequadamente a água que é filtrada. Como
Sistema circulatório. Componentes: - Vasos sanguíneos. - Sangue (elementos figurados e plasma) - Coração
 Fisiologia Humana Sistema circulatório Componentes: - Sangue (elementos figurados e plasma) - Vasos sanguíneos - Coração Vasos sanguíneos Artérias Vasos com paredes espessas e elásticas por onde circula
Fisiologia Humana Sistema circulatório Componentes: - Sangue (elementos figurados e plasma) - Vasos sanguíneos - Coração Vasos sanguíneos Artérias Vasos com paredes espessas e elásticas por onde circula
FISIOLOGIA RENAL EXERCÍCIOS DE APRENDIZAGEM
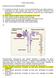 EXERCÍCIOS DE APRENDIZAGEM FISIOLOGIA RENAL 01. A sudorese (produção de suor) é um processo fisiológico que ajuda a baixar a temperatura do corpo quando está muito calor ou quando realizamos uma atividade
EXERCÍCIOS DE APRENDIZAGEM FISIOLOGIA RENAL 01. A sudorese (produção de suor) é um processo fisiológico que ajuda a baixar a temperatura do corpo quando está muito calor ou quando realizamos uma atividade
Conheça mais sobre. Diabetes
 Conheça mais sobre Diabetes O diabetes é caracterizado pelo alto nível de glicose no sangue (açúcar no sangue). A insulina, hormônio produzido pelo pâncreas, é responsável por fazer a glicose entrar para
Conheça mais sobre Diabetes O diabetes é caracterizado pelo alto nível de glicose no sangue (açúcar no sangue). A insulina, hormônio produzido pelo pâncreas, é responsável por fazer a glicose entrar para
Alterações Metabolismo Carboidratos DIABETES
 5.5.2009 Alterações Metabolismo Carboidratos DIABETES Introdução Diabetes Mellitus é uma doença metabólica, causada pelo aumento da quantidade de glicose sanguínea A glicose é a principal fonte de energia
5.5.2009 Alterações Metabolismo Carboidratos DIABETES Introdução Diabetes Mellitus é uma doença metabólica, causada pelo aumento da quantidade de glicose sanguínea A glicose é a principal fonte de energia
MARCADORES TUMORAIS EM DESTAQUE
 Adriana Helena Sedrez Farmacêutica Bioquímica Especialista em Microbiologia Clínica pela PUC-PR Coordenadora do setor de Hematologia Clínica, responsável pelo Atendimento ao Cliente e gerente de Recursos
Adriana Helena Sedrez Farmacêutica Bioquímica Especialista em Microbiologia Clínica pela PUC-PR Coordenadora do setor de Hematologia Clínica, responsável pelo Atendimento ao Cliente e gerente de Recursos
Faculdades Einstein de Limeira Biomedicina. SÍFILIS Diagnóstico Laboratorial
 Faculdades Einstein de Limeira Biomedicina SÍFILIS Diagnóstico Laboratorial SÍFILIS 1. CONCEITO Doença infecciosa, sistêmica, de evolução crônica 2. AGENTE ETIOLÓGICO espiroqueta Treponema pallidum. 3.
Faculdades Einstein de Limeira Biomedicina SÍFILIS Diagnóstico Laboratorial SÍFILIS 1. CONCEITO Doença infecciosa, sistêmica, de evolução crônica 2. AGENTE ETIOLÓGICO espiroqueta Treponema pallidum. 3.
Congresso do Desporto Desporto, Saúde e Segurança
 Congresso do Desporto Desporto, Saúde e Segurança Projecto Mexa-se em Bragança Organização: Pedro Miguel Queirós Pimenta Magalhães E-mail: mexaseembraganca@ipb.pt Web: http://www.mexaseembraganca.ipb.pt
Congresso do Desporto Desporto, Saúde e Segurança Projecto Mexa-se em Bragança Organização: Pedro Miguel Queirós Pimenta Magalhães E-mail: mexaseembraganca@ipb.pt Web: http://www.mexaseembraganca.ipb.pt
 Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Mensagem Química: Hormônios Os hormônios são substâncias químicas liberadas na corrente sanguínea
Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Sistema Endócrino Mensagem Química: Hormônios Os hormônios são substâncias químicas liberadas na corrente sanguínea
TRATAMENTO MEDICAMENTOSO DO DIABETES MELLITUS: SULFONILUREIAS E BIGUANIDAS
 UNIVERSIDADE DE UBERABA LIGA DE DIABETES 2013 TRATAMENTO MEDICAMENTOSO DO DIABETES MELLITUS: SULFONILUREIAS E BIGUANIDAS PALESTRANTES:FERNANDA FERREIRA AMUY LUCIANA SOUZA LIMA 2013/2 CRITÉRIOS PARA ESCOLHA
UNIVERSIDADE DE UBERABA LIGA DE DIABETES 2013 TRATAMENTO MEDICAMENTOSO DO DIABETES MELLITUS: SULFONILUREIAS E BIGUANIDAS PALESTRANTES:FERNANDA FERREIRA AMUY LUCIANA SOUZA LIMA 2013/2 CRITÉRIOS PARA ESCOLHA
RESPOSTA RÁPIDA 154/2014 Alfapoetina na IRC
 RESPOSTA RÁPIDA 154/2014 Alfapoetina na IRC SOLICITANTE Dra. Herilene de Oliveira Andrade Juíza de Direito Comarca de Itapecerica NÚMERO DO PROCESSO 0335.14.706-3 DATA 26/03/2014 SOLICITAÇÃO Solicito parecer
RESPOSTA RÁPIDA 154/2014 Alfapoetina na IRC SOLICITANTE Dra. Herilene de Oliveira Andrade Juíza de Direito Comarca de Itapecerica NÚMERO DO PROCESSO 0335.14.706-3 DATA 26/03/2014 SOLICITAÇÃO Solicito parecer
Cetoacidose Diabética. Prof. Gilberto Perez Cardoso Titular de Medicina Interna UFF
 Cetoacidose Diabética Prof. Gilberto Perez Cardoso Titular de Medicina Interna UFF Complicações Agudas do Diabetes Mellitus Cetoacidose diabética: 1 a 5% dos casos de DM1 Mortalidade de 5% Coma hiperglicêmico
Cetoacidose Diabética Prof. Gilberto Perez Cardoso Titular de Medicina Interna UFF Complicações Agudas do Diabetes Mellitus Cetoacidose diabética: 1 a 5% dos casos de DM1 Mortalidade de 5% Coma hiperglicêmico
SISTEMA EXCRETOR (URINÁRIO) RIO) Rins: morfologia e funcionamento Regulação hormonal Distúrbios mais comuns Excreção de compostos nitrogenados
 SISTEMA EXCRETOR (URINÁRIO) RIO) Rins: morfologia e funcionamento Regulação hormonal Distúrbios mais comuns Excreção de compostos nitrogenados Regulação osmótica SISTEMA URINÁRIO HUMANO adrenal Veia cava
SISTEMA EXCRETOR (URINÁRIO) RIO) Rins: morfologia e funcionamento Regulação hormonal Distúrbios mais comuns Excreção de compostos nitrogenados Regulação osmótica SISTEMA URINÁRIO HUMANO adrenal Veia cava
ORIENTAÇÕES PARA O PROFESSOR PRESENCIAL
 ORIENTAÇÕES PARA O PROFESSOR PRESENCIAL Componente Curriculares Educação Física Professores Ministrantes: Kim Raone e Marcus Marins Série/ Ano letivo: 2º ano/ 2014 Data: 26/03/2014 AULA 5.1 Conteúdo: Doenças
ORIENTAÇÕES PARA O PROFESSOR PRESENCIAL Componente Curriculares Educação Física Professores Ministrantes: Kim Raone e Marcus Marins Série/ Ano letivo: 2º ano/ 2014 Data: 26/03/2014 AULA 5.1 Conteúdo: Doenças
ALTERAÇÕES A INCLUIR NAS SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DOS MEDICAMENTOS QUE CONTENHAM NIMESULIDA (FORMULAÇÕES SISTÉMICAS)
 ANEXO III 58 ALTERAÇÕES A INCLUIR NAS SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DOS MEDICAMENTOS QUE CONTENHAM NIMESULIDA (FORMULAÇÕES SISTÉMICAS) Adições aparecem em itálico e sublinhado; rasuras
ANEXO III 58 ALTERAÇÕES A INCLUIR NAS SECÇÕES RELEVANTES DO RESUMO DAS CARACTERÍSTICAS DOS MEDICAMENTOS QUE CONTENHAM NIMESULIDA (FORMULAÇÕES SISTÉMICAS) Adições aparecem em itálico e sublinhado; rasuras
Diagnóstico Microbiológico
 Diagnóstico Microbiológico Identificação e Tipagem Bacteriana Prof. Vânia Lúcia Diagnóstico clínico Sinais (mensuráveis) e sintomas (subjetivos) Origem Etiologia Natureza Diagnóstico laboratorial Identificação
Diagnóstico Microbiológico Identificação e Tipagem Bacteriana Prof. Vânia Lúcia Diagnóstico clínico Sinais (mensuráveis) e sintomas (subjetivos) Origem Etiologia Natureza Diagnóstico laboratorial Identificação
Veículo: Jornal da Comunidade Data: 24 a 30/07/2010 Seção: Comunidade Vip Pág.: 4 Assunto: Diabetes
 Veículo: Jornal da Comunidade Data: 24 a 30/07/2010 Seção: Comunidade Vip Pág.: 4 Assunto: Diabetes Uma vida normal com diabetes Obesidade, histórico familiar e sedentarismo são alguns dos principais fatores
Veículo: Jornal da Comunidade Data: 24 a 30/07/2010 Seção: Comunidade Vip Pág.: 4 Assunto: Diabetes Uma vida normal com diabetes Obesidade, histórico familiar e sedentarismo são alguns dos principais fatores
ENOXALOW enoxaparina sódica. Forma farmacêutica e apresentações Solução injetável. Via de administração: IV/SC
 ENOXALOW enoxaparina sódica Forma farmacêutica e apresentações Solução injetável. Via de administração: IV/SC 20 mg/0,2 ml cartucho com 1 ou 10 seringas. 40 mg/0,4 ml cartucho com 1 ou 10 seringas. 60
ENOXALOW enoxaparina sódica Forma farmacêutica e apresentações Solução injetável. Via de administração: IV/SC 20 mg/0,2 ml cartucho com 1 ou 10 seringas. 40 mg/0,4 ml cartucho com 1 ou 10 seringas. 60
CITOLOGIA DA TALASSEMIA ALFA
 CITOLOGIA DA TALASSEMIA ALFA Foto 1: Talassemia Alfa Mínima em sangue periférico corado com azul de crezil brilhante. Comentários: A investigação laboratorial da talassemia alfa mínima se faz por meio
CITOLOGIA DA TALASSEMIA ALFA Foto 1: Talassemia Alfa Mínima em sangue periférico corado com azul de crezil brilhante. Comentários: A investigação laboratorial da talassemia alfa mínima se faz por meio
Alterações mecanismo sangramentos ou hemostático tromboses. púrpuras vasculares ou plaquetárias. Fase de coagulação e fibrinólise: coagulopatias
 DOENÇAS HEMORRÁGICAS INTRODUÇÃO Alterações mecanismo sangramentos ou hemostático tromboses Fase primária da hemostasia: púrpuras (alteração dos vasos ou plaquetas) púrpuras vasculares ou plaquetárias Fase
DOENÇAS HEMORRÁGICAS INTRODUÇÃO Alterações mecanismo sangramentos ou hemostático tromboses Fase primária da hemostasia: púrpuras (alteração dos vasos ou plaquetas) púrpuras vasculares ou plaquetárias Fase
Regulação dos níveis iônicos do sangue (Na +, K +, Ca 2+, Cl -, HPO 4. , K +, Mg 2+, etc...)
 Regulação dos níveis iônicos do sangue (Na +, K +, Ca 2+, Cl -, HPO 4 2-, K +, Mg 2+, etc...) Regulação do equilíbrio hidrossalino e da pressão arterial; Regulação do ph sanguíneo (H +, HCO 3- ); Síntese
Regulação dos níveis iônicos do sangue (Na +, K +, Ca 2+, Cl -, HPO 4 2-, K +, Mg 2+, etc...) Regulação do equilíbrio hidrossalino e da pressão arterial; Regulação do ph sanguíneo (H +, HCO 3- ); Síntese
LÍDER NO DESENVOLVIMENTO DA CRIOPRESERVAÇÃO. Garantir o futuro do seu filho com SEGURANÇA e INOVAÇÃO TECNOLÓGICA
 LÍDER NO DESENVOLVIMENTO DA CRIOPRESERVAÇÃO Garantir o futuro do seu filho com SEGURANÇA e INOVAÇÃO TECNOLÓGICA Apresentação de um serviço único na Europa na área da Biotecnologia Clínica As células estaminais
LÍDER NO DESENVOLVIMENTO DA CRIOPRESERVAÇÃO Garantir o futuro do seu filho com SEGURANÇA e INOVAÇÃO TECNOLÓGICA Apresentação de um serviço único na Europa na área da Biotecnologia Clínica As células estaminais
Abordagem Diagnóstica e Terapêutica da Diabete Melito Não Complicada em Cães
 Abordagem Diagnóstica e Terapêutica da Diabete Melito Não Complicada em Cães Cecilia Sartori Zarif Residente em Clínica e Cirurgia de Pequenos Animais da UFV Distúrbio do Pâncreas Endócrino Diabete Melito
Abordagem Diagnóstica e Terapêutica da Diabete Melito Não Complicada em Cães Cecilia Sartori Zarif Residente em Clínica e Cirurgia de Pequenos Animais da UFV Distúrbio do Pâncreas Endócrino Diabete Melito
Informação pode ser o melhor remédio. Hepatite
 Informação pode ser o melhor remédio. Hepatite HEPATITE A hepatite é uma inflamação do fígado provocada na maioria das vezes por um vírus. Diferentes tipos de vírus podem provocar hepatite aguda, que se
Informação pode ser o melhor remédio. Hepatite HEPATITE A hepatite é uma inflamação do fígado provocada na maioria das vezes por um vírus. Diferentes tipos de vírus podem provocar hepatite aguda, que se
DIABETES MELLITUS. Prof. Claudia Witzel
 DIABETES MELLITUS Diabetes mellitus Definição Aumento dos níveis de glicose no sangue, e diminuição da capacidade corpórea em responder à insulina e ou uma diminuição ou ausência de insulina produzida
DIABETES MELLITUS Diabetes mellitus Definição Aumento dos níveis de glicose no sangue, e diminuição da capacidade corpórea em responder à insulina e ou uma diminuição ou ausência de insulina produzida
Aparelho Gastrointestinal Dor Abdominal Aguda
 Aparelho Gastrointestinal Dor Abdominal Aguda Dor abdominal Difusa Localizada Abdome agudo Sem abdome agudo Exames específicos Tratamento específico Estabilizar paciente (vide algoritmo específico) Suspeita
Aparelho Gastrointestinal Dor Abdominal Aguda Dor abdominal Difusa Localizada Abdome agudo Sem abdome agudo Exames específicos Tratamento específico Estabilizar paciente (vide algoritmo específico) Suspeita
azul NOVEMBRO azul Saúde também é coisa de homem. Doenças Cardiovasculares (DCV)
 Doenças Cardiovasculares (DCV) O que são as Doenças Cardiovasculares? De um modo geral, são o conjunto de doenças que afetam o aparelho cardiovascular, designadamente o coração e os vasos sanguíneos. Quais
Doenças Cardiovasculares (DCV) O que são as Doenças Cardiovasculares? De um modo geral, são o conjunto de doenças que afetam o aparelho cardiovascular, designadamente o coração e os vasos sanguíneos. Quais
2 - Biodisponibilidade. Biodisponibilidade Velocidade e extensão de absorção de um fármaco a partir de uma forma de administração
 2 - Biodisponibilidade TOXICOCINÉTICA Biodisponibilidade Velocidade e extensão de absorção de um fármaco a partir de uma forma de administração Fator de Biodisponibilidade (F) Fração da dose administrada
2 - Biodisponibilidade TOXICOCINÉTICA Biodisponibilidade Velocidade e extensão de absorção de um fármaco a partir de uma forma de administração Fator de Biodisponibilidade (F) Fração da dose administrada
Que tipos de Diabetes existem?
 Que tipos de Diabetes existem? -Diabetes Tipo 1 -também conhecida como Diabetes Insulinodependente -Diabetes Tipo 2 - Diabetes Gestacional -Outros tipos de Diabetes Organismo Saudável As células utilizam
Que tipos de Diabetes existem? -Diabetes Tipo 1 -também conhecida como Diabetes Insulinodependente -Diabetes Tipo 2 - Diabetes Gestacional -Outros tipos de Diabetes Organismo Saudável As células utilizam
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores. 1º Ano ENSINO PRÁTICO DIABETES MELLITUS
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO DIABETES MELLITUS Diabetes Mellitus É a doença endócrina mais comum encontrada na clínica; - Caracterizada
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO DIABETES MELLITUS Diabetes Mellitus É a doença endócrina mais comum encontrada na clínica; - Caracterizada
Corticóides na Reumatologia
 Corticóides na Reumatologia Corticóides (CE) são hormônios esteróides produzidos no córtex (área mais externa) das glândulas suprarrenais que são dois pequenos órgãos localizados acima dos rins. São produzidos
Corticóides na Reumatologia Corticóides (CE) são hormônios esteróides produzidos no córtex (área mais externa) das glândulas suprarrenais que são dois pequenos órgãos localizados acima dos rins. São produzidos
Alelos múltiplos na determinação de um caráter
 Alelos múltiplos na determinação de um caráter Determinados gene pode sofrer ao longo do tempo diversas mutações e originar vários alelos esse fenômeno é chamado de polialelia. São bastante frequentes
Alelos múltiplos na determinação de um caráter Determinados gene pode sofrer ao longo do tempo diversas mutações e originar vários alelos esse fenômeno é chamado de polialelia. São bastante frequentes
Pâncreas. Pancreatite aguda. Escolha uma das opções abaixo para ler mais detalhes.
 Pâncreas Escolha uma das opções abaixo para ler mais detalhes. Pancreatite aguda Pancreatite crônica Cistos pancreáticos Câncer de Pancrêas Pancreatite aguda O pâncreas é um órgão com duas funções básicas:
Pâncreas Escolha uma das opções abaixo para ler mais detalhes. Pancreatite aguda Pancreatite crônica Cistos pancreáticos Câncer de Pancrêas Pancreatite aguda O pâncreas é um órgão com duas funções básicas:
Circulação sanguínea Intrapulmonar. V. Pulmonar leva sangue oxigenado do pulmão para o coração.
 DOENÇAS PULMONARES Árvore Brônquica Circulação sanguínea Intrapulmonar V. Pulmonar leva sangue oxigenado do pulmão para o coração. A. Pulmonar traz sangue venoso do coração para o pulmão. Trocas Histologia
DOENÇAS PULMONARES Árvore Brônquica Circulação sanguínea Intrapulmonar V. Pulmonar leva sangue oxigenado do pulmão para o coração. A. Pulmonar traz sangue venoso do coração para o pulmão. Trocas Histologia
TERAPÊUTICA DA HIPERTENSÃO ARTERIAL SISTÊMICA
 Disciplina: Farmacologia Curso: Enfermagem TERAPÊUTICA DA HIPERTENSÃO ARTERIAL SISTÊMICA Professora: Ms. Fernanda Cristina Ferrari Controle da Pressão Arterial Sistêmica Controle Neural estimulação dos
Disciplina: Farmacologia Curso: Enfermagem TERAPÊUTICA DA HIPERTENSÃO ARTERIAL SISTÊMICA Professora: Ms. Fernanda Cristina Ferrari Controle da Pressão Arterial Sistêmica Controle Neural estimulação dos
Papilomavírus Humano HPV
 Papilomavírus Humano HPV -BIOLOGIA- Alunos: André Aroeira, Antonio Lopes, Carlos Eduardo Rozário, João Marcos Fagundes, João Paulo Sobral e Hélio Gastão Prof.: Fragoso 1º Ano E.M. T. 13 Agente Causador
Papilomavírus Humano HPV -BIOLOGIA- Alunos: André Aroeira, Antonio Lopes, Carlos Eduardo Rozário, João Marcos Fagundes, João Paulo Sobral e Hélio Gastão Prof.: Fragoso 1º Ano E.M. T. 13 Agente Causador
CANCER DE MAMA FERNANDO CAMILO MAGIONI ENFERMEIRO DO TRABALHO
 CANCER DE MAMA FERNANDO CAMILO MAGIONI ENFERMEIRO DO TRABALHO OS TIPOS DE CANCER DE MAMA O câncer de mama ocorre quando as células deste órgão passam a se dividir e se reproduzir muito rápido e de forma
CANCER DE MAMA FERNANDO CAMILO MAGIONI ENFERMEIRO DO TRABALHO OS TIPOS DE CANCER DE MAMA O câncer de mama ocorre quando as células deste órgão passam a se dividir e se reproduzir muito rápido e de forma
5.1 Doenças do esôfago: acalasia, esofagite, hérnia hiatal, câncer de cabeça e pescoço, câncer de esôfago, cirurgias
 MÓDULO I NUTRIÇÃO CLÍNICA 1-Absorção, digestão, energia, água e álcool 2-Vitaminas e minerais 3-Proteínas, lipídios, carboidratos e fibras 4-Cálculo das necessidades energéticas 5-Doenças do aparelho digestivo
MÓDULO I NUTRIÇÃO CLÍNICA 1-Absorção, digestão, energia, água e álcool 2-Vitaminas e minerais 3-Proteínas, lipídios, carboidratos e fibras 4-Cálculo das necessidades energéticas 5-Doenças do aparelho digestivo
Exames Laboratoriais em Reumatologia
 Exames Laboratoriais em Reumatologia Kaline Medeiros Costa Pereira Disciplina de Reumatologia da Unifesp Fleury Medicina e Saúde Agenda Proteínas de fase aguda ASLO Complemento total e frações Antifosfolípides
Exames Laboratoriais em Reumatologia Kaline Medeiros Costa Pereira Disciplina de Reumatologia da Unifesp Fleury Medicina e Saúde Agenda Proteínas de fase aguda ASLO Complemento total e frações Antifosfolípides
O que é O que é. colesterol?
 O que é O que é colesterol? 1. O que é colesterol alto e por que ele é ruim? Apesar de a dislipidemia (colesterol alto) ser considerada uma doença extremamente prevalente no Brasil e no mundo, não existem
O que é O que é colesterol? 1. O que é colesterol alto e por que ele é ruim? Apesar de a dislipidemia (colesterol alto) ser considerada uma doença extremamente prevalente no Brasil e no mundo, não existem
Prof a Dr a Camila Souza Lemos IMUNOLOGIA. Prof a. Dr a. Camila Souza Lemos. camila.souzabiomedica@gmail.com AULA 4
 IMUNOLOGIA Prof a. Dr a. Camila Souza Lemos camila.souzabiomedica@gmail.com AULA 4 Imunidade contra tumores Linfócitos T-CD8 (azul) atacando uma célula tumoral (amarela) A imunologia tumoral é o estudo
IMUNOLOGIA Prof a. Dr a. Camila Souza Lemos camila.souzabiomedica@gmail.com AULA 4 Imunidade contra tumores Linfócitos T-CD8 (azul) atacando uma célula tumoral (amarela) A imunologia tumoral é o estudo
Introdução. Metabolismo dos pigmentos biliares: Hemoglobina Biliverdina Bilirrubina Indireta (BI) ou nãoconjugada
 Introdução Metabolismo dos pigmentos biliares: Hemoglobina Biliverdina Bilirrubina Indireta (BI) ou nãoconjugada BI + Albumina Hepatócitos Bilirrubina Direta (BD) ou conjugada Canalículos biliares Duodeno
Introdução Metabolismo dos pigmentos biliares: Hemoglobina Biliverdina Bilirrubina Indireta (BI) ou nãoconjugada BI + Albumina Hepatócitos Bilirrubina Direta (BD) ou conjugada Canalículos biliares Duodeno
Colesterol 3. Que tipos de colesterol existem? 3. Que factores afectam os níveis de colesterol? 4. Quando está o colesterol demasiado elevado?
 Colesterol Colesterol 3 Que tipos de colesterol existem? 3 Que factores afectam os níveis de colesterol? 4 Quando está o colesterol demasiado elevado? 4 Como reduzir o colesterol e o risco de doença cardiovascular?
Colesterol Colesterol 3 Que tipos de colesterol existem? 3 Que factores afectam os níveis de colesterol? 4 Quando está o colesterol demasiado elevado? 4 Como reduzir o colesterol e o risco de doença cardiovascular?
Como interpretar a Gasometria de Sangue Arterial
 Como interpretar a Gasometria de Sangue Arterial Sequência de interpretação e estratificação de risco 08/01/2013 Daniela Carvalho Objectivos da Tertúlia Sequência de interpretação da GSA - Método dos 3
Como interpretar a Gasometria de Sangue Arterial Sequência de interpretação e estratificação de risco 08/01/2013 Daniela Carvalho Objectivos da Tertúlia Sequência de interpretação da GSA - Método dos 3
47 Por que preciso de insulina?
 A U A UL LA Por que preciso de insulina? A Medicina e a Biologia conseguiram decifrar muitos dos processos químicos dos seres vivos. As descobertas que se referem ao corpo humano chamam mais a atenção
A U A UL LA Por que preciso de insulina? A Medicina e a Biologia conseguiram decifrar muitos dos processos químicos dos seres vivos. As descobertas que se referem ao corpo humano chamam mais a atenção
Sistema circulatório
 Sistema circulatório O que é: também conhecido como sistema cardiovascular é formado pelo coração e vasos sanguíneos. Tal sistema é responsável pelo transporte de nutrientes, gases, hormônios, excreções
Sistema circulatório O que é: também conhecido como sistema cardiovascular é formado pelo coração e vasos sanguíneos. Tal sistema é responsável pelo transporte de nutrientes, gases, hormônios, excreções
GASOMETRIA ARTERIAL GASOMETRIA. Indicações 11/09/2015. Gasometria Arterial
 GASOMETRIA ARTERIAL Processo pelo qual é feita a medição das pressões parciais dos gases sangüíneos, a partir do qual é possível o cálculo do PH sangüíneo, o que reflete o equilíbrio Ácido-Básico 2 GASOMETRIA
GASOMETRIA ARTERIAL Processo pelo qual é feita a medição das pressões parciais dos gases sangüíneos, a partir do qual é possível o cálculo do PH sangüíneo, o que reflete o equilíbrio Ácido-Básico 2 GASOMETRIA
GRUPO HOSPITALAR CONCEIÇÃO HOSPITAL NOSSA SENHORA DA CONCEIÇÃO LABORATÓRIO DE ANÁLISES CLÍNICAS
 POP n.º: I 29 Página 1 de 5 1. Sinonímia Pesquisa de anticorpos frios. 2. Aplicabilidade Bioquímicos e auxiliares de laboratório do setor de Imunologia. 3. Aplicação clínica As Crioaglutininas são anticorpos
POP n.º: I 29 Página 1 de 5 1. Sinonímia Pesquisa de anticorpos frios. 2. Aplicabilidade Bioquímicos e auxiliares de laboratório do setor de Imunologia. 3. Aplicação clínica As Crioaglutininas são anticorpos
Hipogonadismo. O que é Hipogonadismo? Causas 25/02/ 2015. Minhavida.com.br
 Hipogonadismo O que é Hipogonadismo? Hipogonadismo é uma doença na qual as gônadas (testículos nos homens e ovários nas mulheres) não produzem quantidades adequadas de hormônios sexuais, como a testosterona
Hipogonadismo O que é Hipogonadismo? Hipogonadismo é uma doença na qual as gônadas (testículos nos homens e ovários nas mulheres) não produzem quantidades adequadas de hormônios sexuais, como a testosterona
