Departamento de Química Fundamentos de Química I (Lic. Química e Bioquímica) 7.0 Converte: 2 ev para J
|
|
|
- Benedita Caetano Beretta
- 6 Há anos
- Visualizações:
Transcrição
1 Departamento de Química Fundamentos de Química I (Lic. Química e Bioquímica) 7.0 Converte: 2 ev para J 1eV = 1 e. 1 V (Carga de 1 electrão) x (1 Volt) = x10-19 C x 1V = 1.602x10-19 J (1 C.V = 1 J) 1eV = 1.60x10-19 J 7.2 n = c/l; [c = 3.00x10 8 ms -1 ] (a) λ > 800 nm ν < c/λ < 3.75x10 14 s -1 (b) λ > 3 mm ν < c/λ < 1.00x10 11 s -1 ν E/J E/kJmol E E E E E E E = hn [h = 6.63x10-34 J.s] ν = 2.0x10 18 s -1 E = hν = 1.33x10-15 J = 7.98x10 5 kjmol -1 ν E/J E/kJmol E E E E = h(n - n o ) = hn - hn o ) = E k + E I [h = 6.63x10-34 J.s] hν rad = E k + E I E min = E I = - hν o ν o = E min /h 6.90x10-19 J/6.63x10-34 Js = 1.04x10 15 s -1 λ max = c/ν o λ max = 288 nm E ν ν o λ λ max = λ o
2 Fundamentos de Química I Cap /12 Cálculo da velocidade do electrão ejectado (E k = ½ m e v 2 ) Energia mínima = 6.90x10-19 J = E I hc/λ rad = 6.63x10-34 x 3.00x10 8 / 250x10-9 = 7.95x10-19 J 7.95x10-19 J = E k x10-19 J E k = 1.05x10-19 J = ½ m e v 2 v 2 = 2. E k /m e = 2x1.05x10-19 J/m e (1 J = kg.m 2 s -2 ) v 2 = 2.31x10 11 m 2 s -2 v = 4.80x10 5 ms n = R H [(1/n 1 2 ) (1/n 2 2 )] R H = x10 15 s -1 1/l = R H [(1/n 1 2 ) (1/n 2 2 )] R H = x10 7 m - 1 R H = R H / c E n = h R H /n 2 a) E = hν = h c/ λ =? n 2 = 7 n 1 = 2 N 2 7 n 1 2 λ/nm E-09 ν/s E+14 E/J 5.005E -19 b) λ = nm c) Região do espectro: UV próximo 7.14 n 1 =? n 2 = 2 λ = nm (Violeta) 1/l = R H [(1/n 1 2 ) (1/n 2 2 )] R H = x10 7 m - 1 R H = R H / c n 1 = a) m = 5.0 Oz x g/oz = x10 2 g = 1.418x10-1 kg v = 92 mph (miles per hour) mile = km v = 92x(1/0.6214) = kmh -1 = x10 3 m/(60x60s) = ms -1
3 Fundamentos de Química I Cap /12 l = h/p = h/(mv) λ = 6.626x10-34 J.s/ (1.418x10-1 kg x ms -1 ) (1 J = kg.m 2 s -2 ) λ = 1.136x10-34 m = 1.136x10-25 nm v e = 2.2x10 3 km s -1 m e = 9.11x10-31 kg l = h/p = h/(mv) λ = 3.31x10-10 m = 3.31 Å = 33.1 nm (UV longínquo) 7.26 Uma camada com nº quântico principal n tem n 2 orbitais n 2 = Σ(2l+1)] l=0 n-1 Cada subcamada l tem 2l+1 orbitais n l m l nº de orbitais Designação s s 1-1, 0, 1 3 2p x, 2p y, 2p z s 1-1, 0, 1 3 3p x, 3p y, 3p z 2-2, -1, 0, 1, 2 5 3d xy, 3d yz, 3d xz, 3d x2-y2, 3d z2 n 3 -l, -l+1,.,0,.,l-1, l 2l+1 f n l+1 g n l+1 h 7.33 {n, l, m l, m s } {4, 4, -1, +½} Não permitida l = n {5, 0, -1, +½} Não permitida l = 0 m l = {n, l, m l, m s } {2, 2, -1, +½} Não permitida l = n {5, 4, +5, +½} Não permitida m l > l
4 Fundamentos de Química I Cap / Camadas: n = 1 < n = 2 < n = 3 < n = 4 Subcamadas da camada n = 4 l = 3, 2, 1, 0 0 < 1 < 2 < Distribuições radiais a) s > p > d > f (grau de penatração no núcleo) b) s > p > d > f (grau de blindagem aos electrões das subcamadas seguintes) Maior penetração menor energia Menor blindagem por parte de outros electrões menor energia mais ligados estão os electrões ao núcleo 7.44 Fe [Ar]4s 2 3d 6 Ga [Ar]3d 10 4s 2 4p 1 Zr [Kr]4d 2 5s 2 Na [He]3s 1
5 Fundamentos de Química I Cap / Relações diagonais (a) Não (b) Sim (c) Não (d) Não 7.86 n = R H [(1/n 1 2 ) (1/n 2 2 )] R H = x10 15 s -1 1/l = R H [(1/n 1 2 ) (1/n 2 2 )] R H = x10 7 m - 1 R H = R H / c DE = hn = h c/ l
6 Fundamentos de Química I Cap /12 a) 10 linhas Linha de maior energia n 2 = 5 n 1 = 1 n 2 = 4 n 1 = 1 n 2 = 3 n 1 = 1 Linha de menor energia n 2 = 2 n 1 = 1 Linha de maior energia n 2 = 5 n 1 = 2 n 2 = 4 n 1 = 2 Linha de menor energia n 2 = 3 n 1 = 2 Linha de maior energia n 2 = 5 n 1 = 3 Linha de menor energia n 2 = 4 n 1 = 3 Linha de maior energia n 2 = 5 n 1 = 4 1/λ = R H [(1/1) (1/5 2 )] l = nm 1/λ = R H [(1/1) (1/2 2 )] l = nm 1/λ = R H [(1/4 2 ) (1/5 2 )] l = 4050 nm l = 4050 nm l = nm Brackett Lyman Lyman (Ultravioleta) n Balmer (Visível) n Paschen (Infravermelho) n Brackett (Infravermelho) n Pfund (Infravermelho) n n Lyman (Ultravioleta) λ/nm Balmer (Visível) λ/nm Paschen (Infravermelho) λ/nm Brackett (Infravermelho) λ/nm Pfund (Infravermelho) λ/nm n 2 = n 2 > n 1 IR Vis UV n 1 = 3 n 1 = 2 n 1 = 1 Paschen Balmer Lyman
7 Fundamentos de Química I Cap / E = h(n - n o ) = hn - hn o ) = E k + E I hν = E k + E I E k = ½ m e v 2 hν = ½ m e v 2 + E I [h = 6.63x10-34 J.s] λ = 58.4 nm = 58.4x10-9 m v = 2450x10 3 ms -1 hc/l = ½ m e v 2 + E I (1 J = kg.m 2 s -2 ) hc/λ rad = 6.63x10-34 x 3.00x10 8 / 58.4x10-9 ½ m e v 2 = ½(9.109x10-31 kg)x(2450x10 3 ) 2 m 2 s -2 E I = hc/l - ½ m e v 2 E I = x10-19 J/átomo n = R H [(1/n 1 2 ) (1/n 2 2 )] R H = x10 15 s -1 1/l = R H [(1/n 1 2 ) (1/n 2 2 )] R H = x10 7 m - 1 R H = R H / c DE = hn = h c/ l a) n 1 = 2 n /λ = R H [(1/2 2 ) (1/100 2 )] 1/λ = x10 6 m -1 λ = x10-7 m l = 365 nm b) Série de Balmer c) 1/λ = R H [(1/100 2 ) (1/110 2 )] A transição é de menor energia do que a transição Maior λ
8 Fundamentos de Química I Cap / a) ν o = 508x1014 s -1 λ o = nm O valor de frequência liminar do césio é uma das menores entre os metais b) O césio é radioactivo H < He < N < O < F < Ne < Cl < Ar < Kr < Xe < Rn PV = nrt PV = (m/m M )RT PM M = (m/v)rt PM M = d.rt d = PM M /RT d=m/v d M M Em condições STP d = M M /V M = M M gmol -1 /22.41 Lmol NaCl(s) Na + (g) + Cl - (g) H =? Na(s) + ½Cl 2 (g) NaCl(s) H f (NaCl(s)) = kj/mol 1 NaCl(s) Na(s) + ½Cl 2 (g) H 1 = H r = 1x H f (NaCl(s)) = kj 2 Na(s) Na(g) H 2 = H r = kj 3 Na(g) Na + (g) + e - (g) H 3 = H r = kj 4 ½ (Cl 2 (g) Cl(g)) H 4 = ½ x H r = ½ x 242 kj 5 Cl(g) + e - (g) Cl - (g) H 5 = H r = kj H = H 1 + H 2 + H 3 + H 4 + H 5 H = = kj
9 Fundamentos de Química I Cap /12 Problemas suplementares 1 Um Dentista encontra-se a fazer um raios-x (λ =1.00 Å) a um paciente que está a ouvir uma estação de rádio (λ = 325 cm) e a observar o azul (λ = 473 nm) do céu através da janela. Qual é a frequência (em Hz e em s -1 ) e a energia (em kj) da radiação electromagnética emitida por cada uma das fontes. 2 Duas estações de rádio emitem, respectivamente em FM a 94 MHz e em AM a 860 khz. a) Calcule o comprimento de onda da radiação electromagnética emitida por cada estação b) Diga, justificando, qual das duas estações emite com maior energia. 3 Alguns diamantes parecem amarelos porque têm compostos de azoto na sua composição que absorvem a luz púrpura de frequência 7.23x10 14 Hz. Calcule o comprimento de onda (em nm e em Å) da radiação absorvida. 4 A ligação carbono-carbono é a base da estrutura de todas as moléculas orgânicas e biológicas. A energia média da ligação C-C é de 347 kjmol -1. a) Calcule a frequência e o comprimento de onda de um fotão capaz de quebrar esta ligação. b) A que região do espectro eletromagnético pertence esta radiação? 5 A seguinte figura ilustra gráficamente o elefeito fotoeléctico. É um gráfico da energia cinética dos electrões ejectados da superfície do metal indicado a diferentes frequências da luz incidente. E k (J) Ce Be Al ν (Hz) a) Porque razão as linhas não começam na origem, ponto (0,0)? b) Porque razão as duas linhas não começam no mesmo ponto? c) Qual dos metais requer luz de menor comprimento de onda para ejectar um electrão? d) Porque razão as linhas apresentam o mesmo declive?
10 Fundamentos de Química I Cap /12 Resolução: 1 Um Dentista encontra-se a fazer um raios-x (λ =1.00 Å) a um paciente que está a ouvir uma estação de rádio (λ = 325 cm) e a observar o azul (λ = 473 nm) do céu através da janela. Qual é a frequência (em Hz e em s -1 ) e a energia (em kj) da radiação electromagnética emitida por cada uma das fontes. Raios X ( s -1 ) Radio ( s -1 ) FM ( MHz) AM ( khz) Visível (7.4x x10 14 s -1 ) λ(r-x) = 1.00 Å = 1.00 x m ν =? λ(radio) = 325 cm = 325 x 10-2 m = 3.25 m ν =? λ(azul) = 473 nm = 473 x 10-9 m ν =? n = c/l; [c = 3.00x10 8 ms -1 ] ν(r-x) = (3.00x10 8 ms -1 )/(1.00x10-10 m) = 3.00x10 18 s -1 (Hz) ν(radio) = (3.00x10 8 ms -1 )/(3.25m) = 9.23x10 7 s -1 (Hz) ν(azul) = (3.00x10 8 ms -1 )/(473x10-9 m) = 6.34x10 14 s -1 (Hz) E = hn [h = 6.63x10-34 J.s] E(R-X) = (6.63x10-34 J.s)x(3.00x1018 s -1 ) = 1.99x10-15 J = 1.20x10 6 kj.mol -1 E(Radio) = (6.63x10-34 J.s)x(9.23x107 s -1 ) = 6.12x10-26 J = 3.68x10-5 kj.mol -1 E(Azul) = (6.63x10-34 J.s)x(6.34x1014 s -1 ) = 4.20x10-19 J = 2.53x10 2 kj.mol -1 Energia de fotões x N A 10-3 E = h n (J) fi (kjmol-1)
11 Fundamentos de Química I Cap /12 2 Duas estações de rádio emitem, respectivamente em FM a 94 MHz e em AM a 860 khz a) Calcule o comprimento de onda da radiação electromagnética emitida por cada estação n (FM) = 94 MHz = 94x106 s-1 n (AM) = 860 khz = 860x103 s-1 l = c/n; [c = 3.00x108 ms-1] E = hn b) Diga, justificando, qual das duas estações emite com maior energia. 3 Alguns diamantes parecem amarelos porque têm compostos de azoto na sua composição que absorvem a luz púrpura de frequência 7.23x10 14 Hz. Calcule o comprimento de onda (em nm e em Å) da radiação absorvida. l = c/n; [c = 3.00x10 8 ms -1 ] l = 4.15x10-7 m = 415 nm = 4.15x10 3 Å 4 A ligação carbono-carbono é a base da estrutura de todas as moléculas orgânicas e biológicas. A energia média da ligação C-C é de 347 kjmol -1. a) Calcule a frequência e o comprimento de onda de um fotão capaz de quebrar esta ligação. n = E / h = 347x10 3 J/mol C-C x(1mol/na)/ h = 8.70x1014 s -1 l = c/n; [c = x10 8 ms -1 ] l = 3.45x10-7 m = 345 nm b) A que região do espectro eletromagnético pertence esta radiação? 345 nm = Região do UV
12 Fundamentos de Química I Cap /12 5 A seguinte figura ilustra gráficamente o elefeito fotoeléctico. É um gráfico da energia cinética dos electrões ejectados da superfície do metal indicado a diferentes frequências da luz incidente. Ek (J) Ce Be Al ν (Hz) a) Porque razão as linhas não começam na origem, ponto (0,0)? E = n hν ; n = 1, 2,... A energia está quantificada. E = hν = Ek + El = ½mv2 + hν o Ek = ½mv2 Ek = hν hν o b) Porque razão as duas linhas não começam no mesmo ponto? Cada metal tem o seu valor de frequência limiar característico c) Qual dos metais requer luz de menor comprimento de onda para ejectar um electrão? λ = c/ν o d) Porque razão as linhas apresentam o mesmo declive? Ek = hν - hν o y = mx + b (m = h; b = hν o O declive é igual ao valor da constante de Plank
Teoria da ligação química
 FACULDADE DE CIÊNCIAS E TECNOLOGIA DEPARTAMENTO DE QUÍMICA E FARMÁCIA Caderno de problemas para as aulas teórico-práticas e tutoriais Teoria da ligação química 2009/2010 Radiação Electromagnética. Teoria
FACULDADE DE CIÊNCIAS E TECNOLOGIA DEPARTAMENTO DE QUÍMICA E FARMÁCIA Caderno de problemas para as aulas teórico-práticas e tutoriais Teoria da ligação química 2009/2010 Radiação Electromagnética. Teoria
EXERCÍCIOS ESTRUTURA ELETRONICA
 EXERCÍCIOS ESTRUTURA ELETRONICA Questão 1 O molibdênio metálico tem de absorver radiação com frequência mínima de 1,09 x 10 15 s -1 antes que ele emita um elétron de sua superfície via efeito fotoelétrico.
EXERCÍCIOS ESTRUTURA ELETRONICA Questão 1 O molibdênio metálico tem de absorver radiação com frequência mínima de 1,09 x 10 15 s -1 antes que ele emita um elétron de sua superfície via efeito fotoelétrico.
N P P N. Ciências de Materiais I Prof. Nilson C. Cruz. Aula 2 Ligação Química. Átomos. Diferença entre materiais = Diferença entre arranjos atômicos e
 Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Ciências de Materiais I Prof. Nilson C. Cruz Aula 2 Ligação Química Átomos Diferença entre materiais = Diferença entre arranjos atômicos e N P P N e N P e Carga (x 1,6x10-19 C) 0 1-1 Massa (x 1,673x10-24
Radiação electromagnetica
 Radiação electromagnetica A radiação eletromagnética é uma forma de energia absorvida e emitida por partículas com carga elétrica quando aceleradas por forças. Ao nível subatómico, a radiação eletromagnética
Radiação electromagnetica A radiação eletromagnética é uma forma de energia absorvida e emitida por partículas com carga elétrica quando aceleradas por forças. Ao nível subatómico, a radiação eletromagnética
Sumário. Espectros, Radiação e Energia
 Sumário Das Estrelas ao átomo Unidade temática 1 Radiação ionizante e radiação não ionizante.. E suas aplicações. APSA 5 Espectro eletromagnético.. Radiação não ionizante São radiações não ionizantes as
Sumário Das Estrelas ao átomo Unidade temática 1 Radiação ionizante e radiação não ionizante.. E suas aplicações. APSA 5 Espectro eletromagnético.. Radiação não ionizante São radiações não ionizantes as
QUÍMICA I. Teoria atômica Capítulo 6. Aula 2
 QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA Edição de junho de 2014 CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA ÍNDICE 3.1-
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA Edição de junho de 2014 CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA ÍNDICE 3.1-
Agrupamento de Escolas Madeira Torres Ficha de avaliação Física e Química A - VERSÃO 2 - Data: / /2013 Nome: Nº: Turma: 10ºF
 Agrupamento de Escolas Madeira Torres Ficha de avaliação Física e Química A - VERSÃO 2 - Data: / /2013 Nome: Nº: Turma: 10ºF CLASSIFICAÇÃO: Valores Prof. António Gonçalves: TABELA DE CONSTANTES Constante
Agrupamento de Escolas Madeira Torres Ficha de avaliação Física e Química A - VERSÃO 2 - Data: / /2013 Nome: Nº: Turma: 10ºF CLASSIFICAÇÃO: Valores Prof. António Gonçalves: TABELA DE CONSTANTES Constante
Revisão de Conceitos e Fundamentos de Física das Radiações (B)
 Revisão de Conceitos e Fundamentos de Física das Radiações (B) Augusto Oliveira adoliv@ctn.ist.utl.pt PSR WP4 ARIAS 2014 Resumo 1. A radiação 2. Energia 3. O jogo do lego da natureza 4. O átomo 5. Níveis
Revisão de Conceitos e Fundamentos de Física das Radiações (B) Augusto Oliveira adoliv@ctn.ist.utl.pt PSR WP4 ARIAS 2014 Resumo 1. A radiação 2. Energia 3. O jogo do lego da natureza 4. O átomo 5. Níveis
Lista de Exercício de Química - N o 6
 Lista de Exercício de Química - N o 6 Profa. Marcia Margarete Meier 1) Arranje em ordem crescente de energia, os seguintes tipos de fótons de radiação eletromagnética: raios X, luz visível, radiação ultravioleta,
Lista de Exercício de Química - N o 6 Profa. Marcia Margarete Meier 1) Arranje em ordem crescente de energia, os seguintes tipos de fótons de radiação eletromagnética: raios X, luz visível, radiação ultravioleta,
Ligação química em compostos de coordenação Espectros electrónicos. Livro Química Inorgânica Básica na página da cadeira, capítulo 10.
 Ligação química em compostos de coordenação spectros electrónicos Livro Química Inorgânica Básica na página da cadeira, capítulo 10 Cor 1 Cor e cor de complexos [Fe(H O) 6 ] + [Ni(H O) 6 ] + [Zn(H O) 6
Ligação química em compostos de coordenação spectros electrónicos Livro Química Inorgânica Básica na página da cadeira, capítulo 10 Cor 1 Cor e cor de complexos [Fe(H O) 6 ] + [Ni(H O) 6 ] + [Zn(H O) 6
Elementos sobre Física Atómica
 Elementos sobre Física Atómica Carla Silva Departamento de Física da Faculdade de Ciências e Tecnologia da Universidade do Algarve 1 ÍNDICE OS MODELOS ATÓMICOS O modelo de Pudim de Passas de Thomson O
Elementos sobre Física Atómica Carla Silva Departamento de Física da Faculdade de Ciências e Tecnologia da Universidade do Algarve 1 ÍNDICE OS MODELOS ATÓMICOS O modelo de Pudim de Passas de Thomson O
1ª e 2 ª Lista de Exercícios de Química Geral - Estrutura Atômica
 1ª e 2 ª Lista de Exercícios de Química Geral - Estrutura Atômica Prof. Dr. Newton Luiz Dias Filho 1) a) Qual é a frequência de radiação que tem um comprimento de onda de 0,452 pm? b) Qual é o comprimento
1ª e 2 ª Lista de Exercícios de Química Geral - Estrutura Atômica Prof. Dr. Newton Luiz Dias Filho 1) a) Qual é a frequência de radiação que tem um comprimento de onda de 0,452 pm? b) Qual é o comprimento
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 4 MODELOS ATÔMICOS Primeira Edição junho de 2005 CAPÍTULO 4 MODELOS ATÔMICOS ÍNDICE 4.1- Modelo de Thomson 4.2- Modelo de Rutherford 4.2.1-
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 4 MODELOS ATÔMICOS Primeira Edição junho de 2005 CAPÍTULO 4 MODELOS ATÔMICOS ÍNDICE 4.1- Modelo de Thomson 4.2- Modelo de Rutherford 4.2.1-
EXERCÍCIOS. Química 10. e problemas Exames Testes intermédios Professor Luís Gonçalves
 Química 10 EXERCÍCIOS e problemas Exames 2006 2007 2008 2009 2010 2011 Testes intermédios 2008 2009 2010 2011 Escola Técnica Liceal Salesiana do Estoril Professor Luís Gonçalves 2 3 4 UNIDADE 1 Das estrelas
Química 10 EXERCÍCIOS e problemas Exames 2006 2007 2008 2009 2010 2011 Testes intermédios 2008 2009 2010 2011 Escola Técnica Liceal Salesiana do Estoril Professor Luís Gonçalves 2 3 4 UNIDADE 1 Das estrelas
Determinação da constante de Planck: o efeito fotoeléctrico
 Determinação da constante de Planck: o efeito fotoeléctrico Objectivos: - Verificação experimental do efeito fotoeléctrico - Determinação da energia cinética dos fotoelectrões em função da frequência da
Determinação da constante de Planck: o efeito fotoeléctrico Objectivos: - Verificação experimental do efeito fotoeléctrico - Determinação da energia cinética dos fotoelectrões em função da frequência da
Espectros atômicos e níveis de energia Números quânticos Estrutura atômica do Hidrogênio e de. Energia dos orbitais e configurações eletrônicas
 Espectros atômicos e níveis de energia Números quânticos Estrutura atômica do Hidrogênio e de átomos com mais elétrons Energia dos orbitais e configurações eletrônicas Prof a. MarciaM. Meier UNIVERSIDADE
Espectros atômicos e níveis de energia Números quânticos Estrutura atômica do Hidrogênio e de átomos com mais elétrons Energia dos orbitais e configurações eletrônicas Prof a. MarciaM. Meier UNIVERSIDADE
Luz & Radiação. Roberto Ortiz EACH USP
 Luz & Radiação Roberto Ortiz EACH USP A luz é uma onda eletromagnética A figura acima ilustra os campos elétrico (E) e magnético (B) que compõem a luz Eles são perpendiculares entre si e perpendiculares
Luz & Radiação Roberto Ortiz EACH USP A luz é uma onda eletromagnética A figura acima ilustra os campos elétrico (E) e magnético (B) que compõem a luz Eles são perpendiculares entre si e perpendiculares
Modelos atômicos. Disciplina: Química Tecnológica Professora: Lukese Rosa Menegussi
 Modelos atômicos Disciplina: Química Tecnológica Professora: Lukese Rosa Menegussi Dalton Lei de Lavoisier Conservação da massa Lei de Proust Proporções constantes Balanceamento Excesso de reagente A natureza
Modelos atômicos Disciplina: Química Tecnológica Professora: Lukese Rosa Menegussi Dalton Lei de Lavoisier Conservação da massa Lei de Proust Proporções constantes Balanceamento Excesso de reagente A natureza
CURSO SUPERIOR DE TECNOLOGIA EM MECATRÔNICA INDUSTRIAL. Prof.: Cristiano Luiz Chostak Disciplina: Química Tecnológica (QMT12)
 CURSO SUPERIOR DE TECNOLOGIA EM MECATRÔNICA INDUSTRIAL Prof.: Cristiano Luiz Chostak Disciplina: Química Tecnológica (QMT12) Atomística: Estrutura atômica básica O modelo atômico de Dalton O modelo atômico
CURSO SUPERIOR DE TECNOLOGIA EM MECATRÔNICA INDUSTRIAL Prof.: Cristiano Luiz Chostak Disciplina: Química Tecnológica (QMT12) Atomística: Estrutura atômica básica O modelo atômico de Dalton O modelo atômico
Escola Secundária de Lagoa. Ficha de Trabalho 4. Física e Química A
 Escola Secundária de Lagoa Física e Química A 10º Ano Turmas A e B Paula Melo Silva e Emília Correia Ficha de Trabalho 4 Unidade Zero Materiais: diversidade e constituição Unidade Um Das estrelas ao átomo
Escola Secundária de Lagoa Física e Química A 10º Ano Turmas A e B Paula Melo Silva e Emília Correia Ficha de Trabalho 4 Unidade Zero Materiais: diversidade e constituição Unidade Um Das estrelas ao átomo
LISTA DE EXERCÍCIOS DE QUÍMICA GERAL
 LISTA DE EXERCÍCIOS DE QUÍMICA GERAL Prof. Mauricio Xavier Coutrim 1. O Newton (N) é a unidade do SI, derivada para força. Força é massa vezes aceleração e aceleração tem dimensão de distância dividida
LISTA DE EXERCÍCIOS DE QUÍMICA GERAL Prof. Mauricio Xavier Coutrim 1. O Newton (N) é a unidade do SI, derivada para força. Força é massa vezes aceleração e aceleração tem dimensão de distância dividida
LISTA 13 Ondas Eletromagnéticas
 LISTA 13 Ondas Eletromagnéticas 1. Não é radiação eletromagnética: a) infravermelho. b) ultravioleta. c) luz visível. d) ondas de rádio. e) ultra-som. 2. (UFRS) Das afirmações que se seguem: I. A velocidade
LISTA 13 Ondas Eletromagnéticas 1. Não é radiação eletromagnética: a) infravermelho. b) ultravioleta. c) luz visível. d) ondas de rádio. e) ultra-som. 2. (UFRS) Das afirmações que se seguem: I. A velocidade
Ficha formativa 10ªano-Química-unidade1 Nome: Nº Turma:
 ESCOLA SECUNDÁRIA DE LOUSADA Física Química A 11º Ano Ficha formativa 10ªano-Química-unidade1 Nome: Nº Turma: 1 Os astrónomos identificaram uma nova estrela, cuja luz demora 200 anos, 300 dias e 6 horas
ESCOLA SECUNDÁRIA DE LOUSADA Física Química A 11º Ano Ficha formativa 10ªano-Química-unidade1 Nome: Nº Turma: 1 Os astrónomos identificaram uma nova estrela, cuja luz demora 200 anos, 300 dias e 6 horas
Escola Secundária Alexandre Herculano 2009/2010
 Escola Secundária Alexandre Herculano 2009/2010 Curso Profissional de Programação e Gestão de Sistemas Informáticos Física e Química Teste de Avaliação - Módulo F3 11ºAno Turma M Número: Nome: Classificação:
Escola Secundária Alexandre Herculano 2009/2010 Curso Profissional de Programação e Gestão de Sistemas Informáticos Física e Química Teste de Avaliação - Módulo F3 11ºAno Turma M Número: Nome: Classificação:
Estrutura eletrônica da matéria - resumo
 Estrutura eletrônica da matéria - resumo A NATUREZA ONDULATÓRIA DA LUZ COMO A RADIAÇÃO ELETROMAGNÉTICA SE MOVE À VELOCIDADE DA LUZ, O COMPRIMENTO DE ONDA E A FREQUÊNCIA ESTÃO RELACIONADOS: νλ=c ONDE ν(ni)
Estrutura eletrônica da matéria - resumo A NATUREZA ONDULATÓRIA DA LUZ COMO A RADIAÇÃO ELETROMAGNÉTICA SE MOVE À VELOCIDADE DA LUZ, O COMPRIMENTO DE ONDA E A FREQUÊNCIA ESTÃO RELACIONADOS: νλ=c ONDE ν(ni)
Contextualização. O aparecimento da Física Atómica teve o contributo de diversas descobertas. Contam-se: 1) Os espectros de absorção e de emissão.
 Contextualização histórica No século XIX existiam as seguintes áreas da Física bem definidas: Mecânica Clássica Electromagnetismo Termodinâmica Física Estatística (tentava compreender a termodinâmica à
Contextualização histórica No século XIX existiam as seguintes áreas da Física bem definidas: Mecânica Clássica Electromagnetismo Termodinâmica Física Estatística (tentava compreender a termodinâmica à
O átomo de Rutherford
 O átomo de Rutherford ~10-14 m Núcleo de carga +Ze rodeado por Z elétrons (modelo planetário). Z é chamado número atômico (H: Z = 1, He: Z = 2, etc.). O número atômico determina as propriedades físicas
O átomo de Rutherford ~10-14 m Núcleo de carga +Ze rodeado por Z elétrons (modelo planetário). Z é chamado número atômico (H: Z = 1, He: Z = 2, etc.). O número atômico determina as propriedades físicas
13/Maio/2016 Aula 20. Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números quânticos. 11/Maio/2016 Aula 19
 11/Maio/2016 Aula 19 Aplicações: - nanotecnologias; - microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. 13/Maio/2016 Aula 20 Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números
11/Maio/2016 Aula 19 Aplicações: - nanotecnologias; - microscópio por efeito de túnel. Equação de Schrödinger a 3 dimensões. 13/Maio/2016 Aula 20 Átomo de hidrogénio Modelo de Bohr Modelo quântico. Números
Universidade Federal do Paraná Departamento de Física Laboratório de Física Moderna
 Universidade Federal do Paraná Departamento de Física Laboratório de Física Moderna Bloco 0: AS LINHAS DE BALMER Introdução A teoria quântica prevê uma estrutura de níveis de energia quantizados para os
Universidade Federal do Paraná Departamento de Física Laboratório de Física Moderna Bloco 0: AS LINHAS DE BALMER Introdução A teoria quântica prevê uma estrutura de níveis de energia quantizados para os
Introd. Física Médica
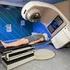 Introd. Física Médica O Efeito Foto Elétrico (EFE) Introdução a Física Médica O Efeito Foto Elétrico (EFE) Introdução a Fís sica Médica Heinrich HERTZ descobriu o Efeito FotoElétrico (1887): Quando a luz
Introd. Física Médica O Efeito Foto Elétrico (EFE) Introdução a Física Médica O Efeito Foto Elétrico (EFE) Introdução a Fís sica Médica Heinrich HERTZ descobriu o Efeito FotoElétrico (1887): Quando a luz
Problemas de Termodinâmica e Estrutura da Matéria
 Problemas de Termodinâmica e Estrutura da Matéria 5 a série 5.1) O filamento de tungsténio de uma lâmpada incandescente está à temperatura de 800 C. Determine o comprimento de onda da radiação emitida
Problemas de Termodinâmica e Estrutura da Matéria 5 a série 5.1) O filamento de tungsténio de uma lâmpada incandescente está à temperatura de 800 C. Determine o comprimento de onda da radiação emitida
Escola Secundária de Lagoa. Ficha de Trabalho 5. Física e Química A 11º Ano Paula Melo Silva. 1. Considere a molécula de metano.
 Escola Secundária de Lagoa Física e Química A 11º Ano Paula Melo Silva Ficha de Trabalho 5 Química 10ºano 1. Considere a molécula de metano. 1.1. Calcule o número de moléculas de metano, CH 4, presentes
Escola Secundária de Lagoa Física e Química A 11º Ano Paula Melo Silva Ficha de Trabalho 5 Química 10ºano 1. Considere a molécula de metano. 1.1. Calcule o número de moléculas de metano, CH 4, presentes
Introdução à Física Quântica
 17/Abr/2015 Aula 14 Introdução à Física Quântica Radiação do corpo negro; níveis discretos de energia. Efeito foto-eléctrico: - descrições clássica e quântica - experimental. Efeito de Compton. 1 Introdução
17/Abr/2015 Aula 14 Introdução à Física Quântica Radiação do corpo negro; níveis discretos de energia. Efeito foto-eléctrico: - descrições clássica e quântica - experimental. Efeito de Compton. 1 Introdução
Departamento de Zoologia da Universidade de Coimbra
 Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Caracterização de uma radiação electromagnética
 Caracterização de uma radiação electromagnética Todas as radiações electromagnéticas são caracterizadas pela sua frequência e comprimento de onda. A frequência é o número de vezes que uma onda se repete
Caracterização de uma radiação electromagnética Todas as radiações electromagnéticas são caracterizadas pela sua frequência e comprimento de onda. A frequência é o número de vezes que uma onda se repete
Velocidade. v= = t tempo necessário para completar 1 ciclo. d distância necessária para completar 1 ciclo. λ T. Ou seja
 Velocidade d distância necessária para completar 1 ciclo v= = t tempo necessário para completar 1 ciclo Ou seja f 1 λ v= = λ f = = T k kt No S.I. a velocidade de propagação da onda mede-se em m/s. Exercicios
Velocidade d distância necessária para completar 1 ciclo v= = t tempo necessário para completar 1 ciclo Ou seja f 1 λ v= = λ f = = T k kt No S.I. a velocidade de propagação da onda mede-se em m/s. Exercicios
Sensoriamento remoto 1. Prof. Dr. Jorge Antonio Silva Centeno Universidade Federal do Paraná 2016
 Sensoriamento remoto 1 Prof. Dr. Jorge Antonio Silva Centeno Universidade Federal do Paraná 2016 Súmula princípios e leis da radiação eletromagnética radiação solar conceito de corpo negro REM e sensoriamento
Sensoriamento remoto 1 Prof. Dr. Jorge Antonio Silva Centeno Universidade Federal do Paraná 2016 Súmula princípios e leis da radiação eletromagnética radiação solar conceito de corpo negro REM e sensoriamento
PROCESSOS DE DECAIMENTO
 PROCESSOS DE DECAIMENTO (Transformações Radioactivas) M Filomena Botelho Objectivos Compreender o que são transformações radioactivas Saber distinguir os diversos tipos de transformações radioactivas Transformações
PROCESSOS DE DECAIMENTO (Transformações Radioactivas) M Filomena Botelho Objectivos Compreender o que são transformações radioactivas Saber distinguir os diversos tipos de transformações radioactivas Transformações
Lista de Exercícios - Física Quântica - UNIDADE 1
 Lista de Exercícios - Física Quântica - UNIDADE 1 Problemas e questões baseados no D. Halliday, R. Resnick e J. Walker, Fundamentos de Física, 6ª ed. - Capítulos 39, 40 e 41. Questões 1. Como pode a energia
Lista de Exercícios - Física Quântica - UNIDADE 1 Problemas e questões baseados no D. Halliday, R. Resnick e J. Walker, Fundamentos de Física, 6ª ed. - Capítulos 39, 40 e 41. Questões 1. Como pode a energia
Absorção de Radiação por Gases na Atmosfera. Radiação I Primeiro semestre 2016
 Absorção de Radiação por Gases na Atmosfera Radiação I Primeiro semestre 2016 Constituintes gasosos da atmosfera N 2 ~ 78% O 2 ~ 21% ~ 99% da atmosfera seca vapor d água (0 a 4%) Argônio, CO 2, O 3, CH
Absorção de Radiação por Gases na Atmosfera Radiação I Primeiro semestre 2016 Constituintes gasosos da atmosfera N 2 ~ 78% O 2 ~ 21% ~ 99% da atmosfera seca vapor d água (0 a 4%) Argônio, CO 2, O 3, CH
TABELA PERIÓDICA E PROPRIEDADES PERIÓDICAS. Prof. Cristiano Torres Miranda Disciplina: Química Geral QM83A Turma Q33
 TABELA PERIÓDICA E PROPRIEDADES PERIÓDICAS Prof. Cristiano Torres Miranda Disciplina: Química Geral QM83A Turma Q33 Johann Wolfgang Döbereiner John Alexander Reina Newlands Tríades Döbereiner Lei das Oitavas
TABELA PERIÓDICA E PROPRIEDADES PERIÓDICAS Prof. Cristiano Torres Miranda Disciplina: Química Geral QM83A Turma Q33 Johann Wolfgang Döbereiner John Alexander Reina Newlands Tríades Döbereiner Lei das Oitavas
Descoberta o elétron século XIX por Thomsom. Próton - - século XX por Rutherford. Neutron 1932 por Chadwick
 Estrutura Atômica Átomo 3 partículas Quais são? Descoberta o elétron século XIX por Thomsom Próton - - século XX por Rutherford Neutron 1932 por Chadwick Modelo atômico Núcleo prótons e neutros Elétrons
Estrutura Atômica Átomo 3 partículas Quais são? Descoberta o elétron século XIX por Thomsom Próton - - século XX por Rutherford Neutron 1932 por Chadwick Modelo atômico Núcleo prótons e neutros Elétrons
ESCOLA SECUNDÁRIA PINHAL DO REI FICHA FORMATIVA 1ºTESTE
 Ano Letivo 206/207 ESCOLA SECUNDÁRIA PINHAL DO REI FICHA FORMATIVA ºTESTE Física e Química A 0ºAno Subdomínio.: Massa e tamanho dos átomos.. A tabela contém informações sobre cinco espécies químicas diferentes.
Ano Letivo 206/207 ESCOLA SECUNDÁRIA PINHAL DO REI FICHA FORMATIVA ºTESTE Física e Química A 0ºAno Subdomínio.: Massa e tamanho dos átomos.. A tabela contém informações sobre cinco espécies químicas diferentes.
A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos...
 Aula 02 - Tabela Periódica TABELA PERIÓDICA e Lothar Meyer A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos... Pode-se escrever a distribuição eletrônica de um elemento
Aula 02 - Tabela Periódica TABELA PERIÓDICA e Lothar Meyer A Tabela Periódica pode ser um guia para a ordem na qual os orbitais são preenchidos... Pode-se escrever a distribuição eletrônica de um elemento
UNIDADE I. Isótopos: São átomos do mesmo elemento que diferem no nº de neutrões.
 UNIDADE I Isótopos: São átomos do mesmo elemento que diferem no nº de neutrões. Espectro Eletromagnético: é o conjunto das radiações eletromagnéticas. Constituição do Espetro Eletromagnético: Ondas de
UNIDADE I Isótopos: São átomos do mesmo elemento que diferem no nº de neutrões. Espectro Eletromagnético: é o conjunto das radiações eletromagnéticas. Constituição do Espetro Eletromagnético: Ondas de
METAIS E COMPLEXOS. Um ácido de Lewis é uma espécie química que pode estabelecer uma ligação coordenada aceitando um par de eletrões de outra espécie.
 METAIS E COMPLEXOS BASE DE LEWIS Uma base e Lewis é uma espécie química que poe estabelecer uma ligação coorenaa oano um par e eletrões a outra espécie. ÁCIDO DE LEWIS Um ácio e Lewis é uma espécie química
METAIS E COMPLEXOS BASE DE LEWIS Uma base e Lewis é uma espécie química que poe estabelecer uma ligação coorenaa oano um par e eletrões a outra espécie. ÁCIDO DE LEWIS Um ácio e Lewis é uma espécie química
Affordable & Efficient Science Teacher In-service Training
 Affordable & Efficient Science Teacher In-service Training Financed partially by the European Commission under Comenius 2.1 Neither the Commission nor the Contractor nor the Partners may be held responsible
Affordable & Efficient Science Teacher In-service Training Financed partially by the European Commission under Comenius 2.1 Neither the Commission nor the Contractor nor the Partners may be held responsible
RAIOS-X (RAIOS RÖNTGEN)
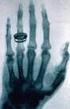 RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
O olho humano permite, com o ar limpo, perceber uma chama de vela em até 15 km e um objeto linear no mapa com dimensão de 0,2mm.
 A Visão é o sentido predileto do ser humano. É tão natural que não percebemos a sua complexidade. Os olhos transmitem imagens deformadas e incompletas do mundo exterior que o córtex filtra e o cérebro
A Visão é o sentido predileto do ser humano. É tão natural que não percebemos a sua complexidade. Os olhos transmitem imagens deformadas e incompletas do mundo exterior que o córtex filtra e o cérebro
O DESAFIO DOS SENSORES REMOTOS NO INVENTÁRIO DE BIOMASSA SÓLIDA. José Rafael M. Silva; Adélia Sousa; e Paulo Mesquita
 O DESAFIO DOS SENSORES REMOTOS NO INVENTÁRIO DE BIOMASSA SÓLIDA José Rafael M. Silva; Adélia Sousa; e Paulo Mesquita 1 A Detecção Remota e uma técnica que nos permite obter informação sobre um objecto
O DESAFIO DOS SENSORES REMOTOS NO INVENTÁRIO DE BIOMASSA SÓLIDA José Rafael M. Silva; Adélia Sousa; e Paulo Mesquita 1 A Detecção Remota e uma técnica que nos permite obter informação sobre um objecto
Fundamentos do. Sensoriamento Remoto. Metodologias de Aplicação. Mauricio A. Moreira -INPEe
 Fundamentos do Sensoriamento Remoto Mauricio A. Moreira mauricio@dsr.inpe.br -INPEe Metodologias de Aplicação Que importância tem o Sensoriamento Remoto nos dias atuais? * A Terra é um planeta finito e
Fundamentos do Sensoriamento Remoto Mauricio A. Moreira mauricio@dsr.inpe.br -INPEe Metodologias de Aplicação Que importância tem o Sensoriamento Remoto nos dias atuais? * A Terra é um planeta finito e
Correção da ficha de trabalho N.º3
 Correção da ficha de trabalho N.º3 1- Classifique as afirmações seguintes em verdadeiras ou falsas, corrigindo estas últimas: A. A passagem de um átomo de um estado excitado ao estado fundamental é acompanhada
Correção da ficha de trabalho N.º3 1- Classifique as afirmações seguintes em verdadeiras ou falsas, corrigindo estas últimas: A. A passagem de um átomo de um estado excitado ao estado fundamental é acompanhada
ÍNDICE. Prefácio... 5
 ÍNDICE Prefácio... 5 1. INTRODUÇÃO 1.1. Identificação de Estruturas Moleculares.... 1.2. Radiação Electromagnética. Regiões Características e Tipos de Interacção com a Materia.......... 7 9 2. ESPECTROSCOPIA
ÍNDICE Prefácio... 5 1. INTRODUÇÃO 1.1. Identificação de Estruturas Moleculares.... 1.2. Radiação Electromagnética. Regiões Características e Tipos de Interacção com a Materia.......... 7 9 2. ESPECTROSCOPIA
Radiação e Ionização. Proteção e higiene das Radiações I Profª: Marina de Carvalho CETEA
 Radiação e Ionização Proteção e higiene das Radiações I Profª: Marina de Carvalho CETEA Introdução O que é onda? Perturbação em um meio que se propaga transportando energia sem que haja transporte de matéria.
Radiação e Ionização Proteção e higiene das Radiações I Profª: Marina de Carvalho CETEA Introdução O que é onda? Perturbação em um meio que se propaga transportando energia sem que haja transporte de matéria.
EXAME NACIONAL DO ENSINO SECUNDÁRIO VERSÃO 2
 EXAME NACIONAL DO ENSINO SECUNDÁRIO 12.º Ano de Escolaridade (Decreto-Lei n.º 286/89, de 29 de Agosto) Cursos Gerais Agrupamentos 1 e 2 PROVA 142/12 Págs. Duração da prova: 120 minutos 2005 2.ª FASE PROVA
EXAME NACIONAL DO ENSINO SECUNDÁRIO 12.º Ano de Escolaridade (Decreto-Lei n.º 286/89, de 29 de Agosto) Cursos Gerais Agrupamentos 1 e 2 PROVA 142/12 Págs. Duração da prova: 120 minutos 2005 2.ª FASE PROVA
Séries de Lyman, Balmer, Paschen, etc. e Modelo de Bohr
 Séries de Lyman, Balmer, Paschen, etc. e Modelo de Bohr Problemas com a Física Clássica Fatos que a Física Clássica não podia explicar Observação de linhas nos espectros atômicos; A estrutura nuclear do
Séries de Lyman, Balmer, Paschen, etc. e Modelo de Bohr Problemas com a Física Clássica Fatos que a Física Clássica não podia explicar Observação de linhas nos espectros atômicos; A estrutura nuclear do
Universidade Federal do Tocantins
 Universidade Federal do Tocantins Modelos atômicos e configurações eletrônicas dos átomos enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com Prof. Dr. Edenilson dos Santos Niculau 2 Sumário ESTRUTURA
Universidade Federal do Tocantins Modelos atômicos e configurações eletrônicas dos átomos enicolau@uft.edu.br Blog: profedenilsonniculau.wordpress.com Prof. Dr. Edenilson dos Santos Niculau 2 Sumário ESTRUTURA
INSTITUTO POLITÉCNICO DE BRAGANÇA ESCOLA SUPERIOR DE TECNOLOGIA E DE GESTÃO FÍSICA III. Exercícios teórico-práticos FILIPE SANTOS MOREIRA
 INSTITUTO POLITÉCNICO DE BRAGANÇA ESCOLA SUPERIOR DE TECNOLOGIA E DE GESTÃO FÍSICA III Eercícios teórico-práticos FILIPE SANTOS MOREIRA Física 3 (EQ) Eercícios TP Índice Índice i Derivadas e integrais
INSTITUTO POLITÉCNICO DE BRAGANÇA ESCOLA SUPERIOR DE TECNOLOGIA E DE GESTÃO FÍSICA III Eercícios teórico-práticos FILIPE SANTOS MOREIRA Física 3 (EQ) Eercícios TP Índice Índice i Derivadas e integrais
ESCOLA SECUNDÁRIA DE CASQUILHOS
 ESCOLA SECUNDÁRIA DE CASQUILHOS 2.º teste sumativo de FQA 28. NOVEMBRO. 2014 Versão 1 10.º Ano Turma A Professor: Maria do Anjo Albuquerque Duração da prova: 90 minutos. Este teste é constituído por 10
ESCOLA SECUNDÁRIA DE CASQUILHOS 2.º teste sumativo de FQA 28. NOVEMBRO. 2014 Versão 1 10.º Ano Turma A Professor: Maria do Anjo Albuquerque Duração da prova: 90 minutos. Este teste é constituído por 10
8.2. Na extremidade de uma corda suficientemente longa é imposta uma perturbação com frequência f = 5 Hz que provoca uma onda de amplitude
 Constantes Velocidade do som no ar: v som = 344 m /s Velocidade da luz no vácuo c = 3 10 8 m/s 8.1. Considere uma corda de comprimento L e densidade linear µ = m/l, onde m é a massa da corda. Partindo
Constantes Velocidade do som no ar: v som = 344 m /s Velocidade da luz no vácuo c = 3 10 8 m/s 8.1. Considere uma corda de comprimento L e densidade linear µ = m/l, onde m é a massa da corda. Partindo
Agronomia Química Analítica Prof. Dr. Gustavo Rocha de Castro. As medidas baseadas na luz (radiação eletromagnética) são muito empregadas
 ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
Escola Básica e Secundária Gonçalves Zarco Física e Química A, 10º ano Ano lectivo 2007 / 2008
 Escola Básica e Secundária Gonçalves Zarco Física e Química A, 0º ano Ano lectivo 007 / 008 Correcção do teste de avaliação sumativa Nome: N.º aluno: Turma: Classificação : Professor: GRUPO I. Texto I
Escola Básica e Secundária Gonçalves Zarco Física e Química A, 0º ano Ano lectivo 007 / 008 Correcção do teste de avaliação sumativa Nome: N.º aluno: Turma: Classificação : Professor: GRUPO I. Texto I
Campos de forças: campos gravítico, magnético e eléctrico... Cargas em movimento e seus efeitos em termos de criação de campos...
 RADIAÇÃO 1 As radiações são ondas electromagnéticas. O que são ondas electromagnéticas? Quais os conceitos fundamentais que os alunos precisam de entender para lhes podermos explicar o que são ondas electromagnéticas?
RADIAÇÃO 1 As radiações são ondas electromagnéticas. O que são ondas electromagnéticas? Quais os conceitos fundamentais que os alunos precisam de entender para lhes podermos explicar o que são ondas electromagnéticas?
QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White
 QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White Natureza ondulatória da luz Todas as ondas têm um comprimento de onda característico, λ, e uma amplitude, A.
QUÍMICA A Ciência Central 9ª Edição Capítulo 6 Estrutura eletrônica dos átomos David P. White Natureza ondulatória da luz Todas as ondas têm um comprimento de onda característico, λ, e uma amplitude, A.
O Espaço: contínuo ou discreto? João Penedones
 O Espaço: contínuo ou discreto? João Penedones CERN Master Class Universidade do Porto, 15 de Março de 2014 O Espaço: plasticina ou Legos? Matéria contínua Matéria discreta Espaço discreto Espaço contínuo
O Espaço: contínuo ou discreto? João Penedones CERN Master Class Universidade do Porto, 15 de Março de 2014 O Espaço: plasticina ou Legos? Matéria contínua Matéria discreta Espaço discreto Espaço contínuo
Estrutura Eletrônica dos átomos
 Estrutura Eletrônica dos átomos 3- Os espectros de emissão dos gases Como a equação de Rydberg poderia ser explicada? Os estados de energia do átomo de hidrogênio Se n f é menor que n i, o e- move-se para
Estrutura Eletrônica dos átomos 3- Os espectros de emissão dos gases Como a equação de Rydberg poderia ser explicada? Os estados de energia do átomo de hidrogênio Se n f é menor que n i, o e- move-se para
Estimativa do Comprimento de Onda de um LED
 Universidade São Judas Tadeu Faculdade de Tecnologia e Ciências Exatas Cursos de Engenharia Laboratório de Física e Eletricidade: Estimativa do Comprimento de Onda de um LED Autor: Prof. Sandro Martini
Universidade São Judas Tadeu Faculdade de Tecnologia e Ciências Exatas Cursos de Engenharia Laboratório de Física e Eletricidade: Estimativa do Comprimento de Onda de um LED Autor: Prof. Sandro Martini
Tabela Periódica e Propriedades Periódicas dos Elementos. periódico permite fazer previsões gerais sobre seu comportamento químico e físico.
 Tabela Periódica e Propriedades Periódicas dos Elementos Agrupar os elementos num quadro Agrupar os elementos num quadro periódico permite fazer previsões gerais sobre seu comportamento químico e físico.
Tabela Periódica e Propriedades Periódicas dos Elementos Agrupar os elementos num quadro Agrupar os elementos num quadro periódico permite fazer previsões gerais sobre seu comportamento químico e físico.
8º ANO Ensino Fundamental
 E n s in o F o r t e e d e R e s u l t a do s Centro Educacio nal Juscelino K ub itschek APOSTILA G uar á e Valp ar aíso 3º Bimestre F Í S I C A 8º ANO Ensino Fundamental Data: / / Turno: Estudante: Turma:
E n s in o F o r t e e d e R e s u l t a do s Centro Educacio nal Juscelino K ub itschek APOSTILA G uar á e Valp ar aíso 3º Bimestre F Í S I C A 8º ANO Ensino Fundamental Data: / / Turno: Estudante: Turma:
Experimento 3A: A QUÍMICA DOS COMPOSTOS DE COORDENAÇÃO E A ESPECTROSCOPIA
 Universidade Federal do Paraná Departamento de Química Disciplina: Química Inorgânica e Experimental CQ071 Curso: Licenciatura e Bacharelado em Química Professor: Shirley Nakagaki Experimento 3A: A QUÍMICA
Universidade Federal do Paraná Departamento de Química Disciplina: Química Inorgânica e Experimental CQ071 Curso: Licenciatura e Bacharelado em Química Professor: Shirley Nakagaki Experimento 3A: A QUÍMICA
4ª Ficha de Avaliação de Conhecimentos Turma: 10ºA. Física e Química A - 10ºAno
 4ª Ficha de Avaliação de Conhecimentos Turma: 10ºA Física e Química A - 10ºAno Professora Paula Melo Silva Data: 7 de dezembro 2015 Ano Letivo: 2015/2016 135 + 15 min 1. Os espetros de absorção e de emissão
4ª Ficha de Avaliação de Conhecimentos Turma: 10ºA Física e Química A - 10ºAno Professora Paula Melo Silva Data: 7 de dezembro 2015 Ano Letivo: 2015/2016 135 + 15 min 1. Os espetros de absorção e de emissão
O Átomo e o Mundo Quântico
 O Átomo e o Mundo Quântico Surgimento da Mecânica Quântica: Século XX Natureza ondulatória da Luz Modelo de Bohr - 1913 Relacionou as idéias quânticas de Planck e Einstein e explicou os espectros dos átomos
O Átomo e o Mundo Quântico Surgimento da Mecânica Quântica: Século XX Natureza ondulatória da Luz Modelo de Bohr - 1913 Relacionou as idéias quânticas de Planck e Einstein e explicou os espectros dos átomos
Ficha de Trabalho n.º 4
 Ficha de Trabalho n.º 4 Disciplina: CFQ Componente de Química Ano/Turma Selecção de Conteúdos de Química 10 ano do exame 715 Data / / Professor: 1. (ENES 1ª Fase 2007) Leia atentamente o seguinte texto.
Ficha de Trabalho n.º 4 Disciplina: CFQ Componente de Química Ano/Turma Selecção de Conteúdos de Química 10 ano do exame 715 Data / / Professor: 1. (ENES 1ª Fase 2007) Leia atentamente o seguinte texto.
FUNDAMENTOS DE SENSORIAMENTO REMOTO
 FUNDAMENTOS DE SENSORIAMENTO REMOTO Elisabete Caria Moraes DSR/INPE bete@dsr.inpe.br Introdução O Sensoriamento Remoto pode ser entendido como um conjunto de atividades que permite a obtenção de informações
FUNDAMENTOS DE SENSORIAMENTO REMOTO Elisabete Caria Moraes DSR/INPE bete@dsr.inpe.br Introdução O Sensoriamento Remoto pode ser entendido como um conjunto de atividades que permite a obtenção de informações
Ondas e a radiação eletromagnética
 Ondas e a radiação eletromagnética Dark side of the Moon, album cover (1973), Pink Floyd Jorge Miguel Sampaio jmsampaio@fc.ul.pt 1. O que são ondas? São perturbações ou oscilações que se propagam no espaço
Ondas e a radiação eletromagnética Dark side of the Moon, album cover (1973), Pink Floyd Jorge Miguel Sampaio jmsampaio@fc.ul.pt 1. O que são ondas? São perturbações ou oscilações que se propagam no espaço
https://sites.google.com/site/estruturabc0102/
 Estrutura da Matéria Aula 4: Radiações clássicas E-mail da turma: emufabc@gmail.com Senha: ufabcsigma https://sites.google.com/site/estruturabc0102/ Radiações Clássicas 1899-1900: Rutherford e Villard
Estrutura da Matéria Aula 4: Radiações clássicas E-mail da turma: emufabc@gmail.com Senha: ufabcsigma https://sites.google.com/site/estruturabc0102/ Radiações Clássicas 1899-1900: Rutherford e Villard
FÍSICA. 2 a Etapa SÓ ABRA QUANDO AUTORIZADO. UNIVERSIDADE FEDERAL DE MINAS GERAIS. Duração desta prova: TRÊS HORAS. FAÇA LETRA LEGÍVEL.
 UNIVERSIDADE FEDERAL DE MINAS GERAIS FÍSICA 2 a Etapa SÓ ABRA QUANDO AUTORIZADO. Leia atentamente as instruções que se seguem. 1 - Este Caderno de Provas contém seis questões, constituídas de itens e subitens,
UNIVERSIDADE FEDERAL DE MINAS GERAIS FÍSICA 2 a Etapa SÓ ABRA QUANDO AUTORIZADO. Leia atentamente as instruções que se seguem. 1 - Este Caderno de Provas contém seis questões, constituídas de itens e subitens,
QUESTÕES DE FÍSICA MODERNA
 QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
Física Moderna. A quantização da energia. Dualidade onda-partícula. O efeito fotoelétrico.
 Física Moderna A quantização da energia. Dualidade onda-partícula. O efeito fotoelétrico. Efeito fotoelétrico Quando uma radiação eletromagnética incide sobre a superfície de um metal, elétrons podem ser
Física Moderna A quantização da energia. Dualidade onda-partícula. O efeito fotoelétrico. Efeito fotoelétrico Quando uma radiação eletromagnética incide sobre a superfície de um metal, elétrons podem ser
Graça Meireles. Física -10º ano. Física -10º ano 2
 Escola Secundária D. Afonso Sanches Energia do Sol para a Terra Graça Meireles Física -10º ano 1 Variação da Temperatura com a Altitude Física -10º ano 2 1 Sistemas Termodinâmicos Propriedades a ter em
Escola Secundária D. Afonso Sanches Energia do Sol para a Terra Graça Meireles Física -10º ano 1 Variação da Temperatura com a Altitude Física -10º ano 2 1 Sistemas Termodinâmicos Propriedades a ter em
PROPRIEDADES ATÔMICAS E TENDÊNCIAS PERIÓDICAS
 PROPRIEDADES ATÔMICAS E TENDÊNCIAS PERIÓDICAS TAMANHO ATÔMICO Pode ser definido como a distância entre os átomos em uma amostra do elemento. Cl Cl (Cl 2 ): 198 pm Raio covalente: 198/2 = 99 pm C-C no diamante
PROPRIEDADES ATÔMICAS E TENDÊNCIAS PERIÓDICAS TAMANHO ATÔMICO Pode ser definido como a distância entre os átomos em uma amostra do elemento. Cl Cl (Cl 2 ): 198 pm Raio covalente: 198/2 = 99 pm C-C no diamante
1318 Raios X / Espectro contínuo e característico Medida da razão h/e.
 1 Roteiro elaborado com base na documentação que acompanha o conjunto por: Máximo F. Silveira Instituto de Física UFRJ Tópicos Relacionados Raios-X, equação de Bragg, radiação contínua (bremstrahlung),
1 Roteiro elaborado com base na documentação que acompanha o conjunto por: Máximo F. Silveira Instituto de Física UFRJ Tópicos Relacionados Raios-X, equação de Bragg, radiação contínua (bremstrahlung),
Tubos de Crookes e a descoberta do elétron
 Tubos de Crookes e a descoberta do elétron (A) Efeito de um obstáculo no caminho dos raios catódicos. Raios Catódicos High voltage source of high voltage shadow Resultados independem do gás usado para
Tubos de Crookes e a descoberta do elétron (A) Efeito de um obstáculo no caminho dos raios catódicos. Raios Catódicos High voltage source of high voltage shadow Resultados independem do gás usado para
Escola Secundária de Lagoa. Correção da Ficha de Trabalho 14. Física e Química A pontos
 Escola Secundária de Lagoa Física e Química A 10º Ano Turmas A e B Paula Silva e Emília Correia Correção da Ficha de Trabalho 14 2014/2015 1. 1.1.. 12 pontos O buraco da camada de ozono consiste na baixa
Escola Secundária de Lagoa Física e Química A 10º Ano Turmas A e B Paula Silva e Emília Correia Correção da Ficha de Trabalho 14 2014/2015 1. 1.1.. 12 pontos O buraco da camada de ozono consiste na baixa
Ondas. Dark side of the Moon, album cover (1973), Pink Floyd. Jorge Miguel Sampaio
 Ondas Dark side of the Moon, album cover (1973), Pink Floyd Jorge Miguel Sampaio jmsampaio@fc.ul.pt 1. O que são ondas? São perturbações ou oscilações que se propagam no espaço e/ou no tempo acompanhadas
Ondas Dark side of the Moon, album cover (1973), Pink Floyd Jorge Miguel Sampaio jmsampaio@fc.ul.pt 1. O que são ondas? São perturbações ou oscilações que se propagam no espaço e/ou no tempo acompanhadas
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO Primeira Edição junho de 2005 CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO ÍNDICE 3.1- Efeito
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO Primeira Edição junho de 2005 CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO ÍNDICE 3.1- Efeito
Uma breve história do mundo dos quanta. Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso
 Uma breve história do mundo dos Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso Tópicos da Segunda Aula Abordagem histórica Radiação de corpo negro Efeito fotoelétrico Espalhamento Compton
Uma breve história do mundo dos Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso Tópicos da Segunda Aula Abordagem histórica Radiação de corpo negro Efeito fotoelétrico Espalhamento Compton
25/Mar/2015 Aula /Mar/2015 Aula 9
 20/Mar/2015 Aula 9 Processos Politrópicos Relações politrópicas num gás ideal Trabalho: aplicação aos gases perfeitos Calor: aplicação aos gases perfeitos Calor específico politrópico Variação de entropia
20/Mar/2015 Aula 9 Processos Politrópicos Relações politrópicas num gás ideal Trabalho: aplicação aos gases perfeitos Calor: aplicação aos gases perfeitos Calor específico politrópico Variação de entropia
Lista de Problemas rad.)
 Universidade Federal do Rio Grande do Sul Instituto de Física Departamento de Física FIS01044 UNIDADE III Difração Lista de Problemas Problemas extraídos de HALLIDAY, D., RESNICK, R., WALKER, J. Fundamentos
Universidade Federal do Rio Grande do Sul Instituto de Física Departamento de Física FIS01044 UNIDADE III Difração Lista de Problemas Problemas extraídos de HALLIDAY, D., RESNICK, R., WALKER, J. Fundamentos
Instituto de Física USP. Física V - Aula 15. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 15 Professora: Mazé Bechara Aula 15 Espectros de absorção e emissão atômica e modelo atômico de Thomson. 1. Evidências experimentais da existência de estrutura nos
Instituto de Física USP Física V - Aula 15 Professora: Mazé Bechara Aula 15 Espectros de absorção e emissão atômica e modelo atômico de Thomson. 1. Evidências experimentais da existência de estrutura nos
A fonte Solar de Energia da Terra
 A fonte Solar de Energia da Terra A energia solar é criada no núcleo do Sol quando os átomos de hidrogênio sofrem fusão nuclear para hélio. Em cada segundo deste processo nuclear, 700 milhões de toneladas
A fonte Solar de Energia da Terra A energia solar é criada no núcleo do Sol quando os átomos de hidrogênio sofrem fusão nuclear para hélio. Em cada segundo deste processo nuclear, 700 milhões de toneladas
RADIAÇÃO, ENERGIA E ESPECTROS. Maria do Anjo Albuquerque
 RADIAÇÃO, ENERGIA E ESPECTROS Maria do Anjo Albuquerque 19.Outubro.2010 Tínhamos visto que as estrelas são muitas vezes classificadas pela cor e, consequentemente, pelas suas temperaturas, usando uma escala
RADIAÇÃO, ENERGIA E ESPECTROS Maria do Anjo Albuquerque 19.Outubro.2010 Tínhamos visto que as estrelas são muitas vezes classificadas pela cor e, consequentemente, pelas suas temperaturas, usando uma escala
ESTRUTURA ATÔMICA - III
 ESTRUTURA ATÔMICA - III Elementos químicos emitem luz em diferentes comprimentos de onda. Esta emissão é descontínua e só ocorre para determinadas faixas de Prof. Bruno Gabriel Química 2ª Bimestre 2016
ESTRUTURA ATÔMICA - III Elementos químicos emitem luz em diferentes comprimentos de onda. Esta emissão é descontínua e só ocorre para determinadas faixas de Prof. Bruno Gabriel Química 2ª Bimestre 2016
O Átomo de hidrogénio
 O Átomo de hidrogénio O conceito de átomo como sendo a mais pequena porção indivisível de matéria foi introduzido no ano 450 antes de Cristo mas, só em 808, Dalton propôs um modelo atómico em que os átomos
O Átomo de hidrogénio O conceito de átomo como sendo a mais pequena porção indivisível de matéria foi introduzido no ano 450 antes de Cristo mas, só em 808, Dalton propôs um modelo atómico em que os átomos
O Átomo de Bohr. O Átomo de Bohr e o Espectro do Átomo Hidrogênio.
 O Átomo de Bohr UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL. Instituto de Física. Departamento de Física. Física do Século XXB (FIS1056). Prof. César Augusto Zen Vasconcellos. Lista 5 (Site: www.cesarzen.com)
O Átomo de Bohr UNIVERSIDADE FEDERAL DO RIO GRANDE DO SUL. Instituto de Física. Departamento de Física. Física do Século XXB (FIS1056). Prof. César Augusto Zen Vasconcellos. Lista 5 (Site: www.cesarzen.com)
Princípios da Interação da Luz com o tecido: Refração, Absorção e Espalhamento. Prof. Emery Lins Curso Eng. Biomédica
 Princípios da Interação da Luz com o tecido: Refração, Absorção e Espalhamento Prof. Emery Lins Curso Eng. Biomédica Introdução Breve revisão: Questões... O que é uma radiação? E uma partícula? Como elas
Princípios da Interação da Luz com o tecido: Refração, Absorção e Espalhamento Prof. Emery Lins Curso Eng. Biomédica Introdução Breve revisão: Questões... O que é uma radiação? E uma partícula? Como elas
Radiação: Considerações gerais
 Estuda-se radiação térmica, cujas origens estão ligadas à emissão da matéria a uma temperatura absoluta T>0 A emissão é devida oscilações e transições electrónicas dos muitos electrões que constituem a
Estuda-se radiação térmica, cujas origens estão ligadas à emissão da matéria a uma temperatura absoluta T>0 A emissão é devida oscilações e transições electrónicas dos muitos electrões que constituem a
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO Edição de janeiro de 2009 CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO ÍNDICE 3.1- Efeito
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO Edição de janeiro de 2009 CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO ÍNDICE 3.1- Efeito
Principais modelos atômicos. Principais modelos atômicos Modelo Atômico de Rutherford (1911)
 Principais modelos atômicos Modelo Atômico de Thomson (898) Com a descoberta dos prótons e elétrons, Thomson propôs um modelo de átomo no qual os elétrons e os prótons, estariam uniformemente distribuídos,
Principais modelos atômicos Modelo Atômico de Thomson (898) Com a descoberta dos prótons e elétrons, Thomson propôs um modelo de átomo no qual os elétrons e os prótons, estariam uniformemente distribuídos,
