Enzimas. 1.Maiores velocidades de reacção
|
|
|
- Eduarda Abreu Brás
- 6 Há anos
- Visualizações:
Transcrição
1 Enzimas
2 Enzimas Diferenças em relação aos catalisadores químicos: 1.Maiores velocidades de reacção P Com enzima reacção A P Sem enzima tempo
3 2. Condições de reacção mais suaves 3. Maior especificidade 3. Capacidade de regulação
4 História Anos: 1700 estudos sobre a digestão da carne por secreções do estômago Conversão do amido em açucar pela saliva e extractos de plantas (amilase)
5 1850 Pasteur a fermentação do açucar em álcool pelas leveduras era catalisada por fermentos, inseparáveis das células vivas vitalismo.
6 1893 Ostwald - enzima = catalisador Fischer: -teoria chave-fechadura 1897 Eduard Buchner as moléculas do extracto de levedura responsáveis pela conversão de açucar a etanol, continuavam a funcionar quando removidas das células. É uma molécula!?
7 1877 Kühne: in zyme enzima
8 Sumner: - urease cristal É uma proteína!
9 1905 Harden e Young: coenzima isolado(nad + ) 1909 Sorensen: escala de ph 1913 Michaelis e Menten: teoria cinética 1925 Briggs e Haldane: teoria cinética modificada
10 1931 Lineweaver e Burk determinação das constantes cinéticas Hirs, Moore e Stein ribonuclease (estrutura primária) 1962 Phillips lisozima (estrutura terciária) 1970 Chang e Cohen clonagem do gene do β-lactamase de Staphylococcus aureus em E. Coli 1982 produção de mutante de tirosil-rna sintetase por mutagénese dirigida
11 Mas todos os enzimas são realmente proteínas? Cech 1968 ribozimas - RNA com actividade catalítica Wade 1997 abzimas - anticorpo monoclonal com actividade catalítica.
12 Aplicações industriais de enzimas DISTRIBUIÇÃO DO MERCADO 29% 15% 10% 14% 32% p.lácteos deterg. texteis amido outros (2x) (2x) Godfrey,T., West, S.(eds)Industrial Enzimology, Macmillan, London(1990)
13 Indústria Função dos enzimas alimentos quebra do xarope de amido em xarope de glucose (osidases); isomerização de glucose em frutose, mais doce logo menor quantidade (isomerase); hidrólise da sacarose em glucose e frutose (hidrolases); fabrico de adoçantes artificiais; alimentos bébé sumos de frutos detergentes biológicos carne medicamentos início da digestão da comida (proteases e lipases) impedir turvação (pectinase) anti-nódoas (proteases para as proteinas e lipases para as gorduras); amaciadores (celulases quebram os borbotos ) tornar mais tenra cancro, produção de drogas sintéticas (penicilina)
14 Enzimas em medicina enfarte miocárdio (diagnóstico) terapêutica
15 Desenvolvimentos da última década Sobre-expressão Mutagénese dirigida Mais estruturas Mais sequências + Modificar e estudar propriedades Novos métodos de cálculo automático + desenho molecular Desenho de novos biocatalisadores enzimas artificiais
16 Enzimas artificiais maior estabilidade térmica Ex: subtilisina com 8 aa substituidos vida média a 100 o passa de 30s para 170min
17 A maioria dos enzimas são proteínas! MM
18 Classificação internacional de enzimas Nº Classe Tipo de reacção 1 Oxidoreductases Transferência de electrões 2 Transferases Reacções de transferência de grupos 3 Hidrolases Reacções de hidrólise (transferência de grupos para a água) 4 Liases Adição de grupos a ligações duplas ou formação de ligações duplas por remoção de grupos 5 Isomerases Transferência de grupos dentro da molécula para dar origem a formas isoméricas 6 Ligases Formação de ligações C-C, C-S, C-O e C-N, por reacções de condensação acopladas à hidrólise de ATP
19 Cada enzima tem um nome sistemático, um nº de classificação e um nome trivial Ex: O enzima que catalisa a reacção ATP + D-glucose ADP + D-glucose6-P Nome sistemático : ATP glucose fosfotransferase Nº de classificação: E.C E.C. Enzyme Commission 2- classe das transferases 7- subclasse fosfotransferase 1- fosfotransferase com um grupo hidroxilo como aceitador 1- D-glucose como aceitadora do grupo fosforilo Nome trivial : hexoquinase
20 Há enzimas que precisam de outras moléculas ou iões para a sua actividade Cofactores iões ou pequenas moléculas orgânicas (coenzimas) necessários à actividade enzimática. Os coenzimas podem estar transientemente ou permanentemente grupo prostético -ligados aos enzimas. Enzima + cofactor holoenzima Enzima sem cofactor apoenzima
21 Cofactores - iões inorgânicos Cu 2+ Ião Fe 2+ Fe 2+ K + Mg 2+ Mn 2+ Mo Ni 2+ Se Zn 2+ Citocromo oxidase Enzima Peroxidase, catalase, citocromo oxidase Piruvato cinase Hexocinase, 6-P-glucose fosfatase, piruvato cinase Arginase,ribonucleotido redutase Dinitrogenase Urease Glutationo peroxidase Anidrase carbónico, alcool desidrogenase, carboxipeptidases A e B
22 Coenzimas: moléculas orgânicas complexas ou organometálicas que transferem átomos específicos ou grupos funcionais coenzima Grupo transferido Precursor na dieta do mamífero Biocitina CO 2 biotina Coenzima A Grupos acilo Ácido pantoténico Coenzima B 12 H, grupos alquilo Vit B 12 FAD Electrões Riboflavina (Vit B 2 ) Lipoato Electrões, grupos acilo Não necess. na dieta NAD + Ião hidreto (:H - ) Ácido nicotínico Fosfato de piridoxal Grupos amina Piridoxina (Vit B 6 ) Tetrahidrofolato Grupos de 1C Folato Pirofosfato de tiamina Aldeídos Tiamina (Vit B 1 )
23 Os enzimas são altamente específicos: Estereoespecificidade reconhecem substratos quirais Especificidade geométrica são selectivos em relação aos grupos químicos dos substratos. Os enzimas variam no grau de especificidade geométrica
24 Regulação da actividade enzimática Controlo da quantidade de enzima Controlo da actividade enzimática
25 Funções termodinâmicas úteis para compreender o funcionamento dos enzimas Variação de energia livre de Gibbs entre os produtos e os reagentes Energia necessária para iniciar a conversão de reagentes em produtos
26 A variação da energia livre padrão de uma reacção está relacionada com a constante de equilíbrio Relação entre K eq e G o S P K eq = [P]/[S] G o = -RT lnk eq
27 Como é que os enzimas funcionam? Os enzimas fornecem um ambiente em que a reacção ocorre mais rapidamente. A reacção tem lugar no local activo do enzima. A molécula que se liga ao local activo é chamada substrato. Forma-se um complexo enzima-substrato
28 Os enzimas afectam as velocidades de reacção e não o equilibrio E + S ES EP E + P
29 Os catalisadores aumentam a velocidade das reacções baixando a energia de activação A reacção chega mais depressa ao equilíbrio
30 A velocidade de reacção é determinada pela concentração do(s) reagente(s) e pela constante de velocidade, k. v = k[s] A constante de velocidade de uma reacção está relacionada com a energia de activação: k = kt/h. e - G*/RT k constante de Boltzman h constante de Planck Uma energia de activação mais baixa significa uma maior velocidade de reacção para um reacção ser acelerada por um factor de 10, a energia de activação tem que baixar cerca de 5,7 kj/mole
31 2 H 2 O 2 2 H 2 O + O 2 Catalisador E activ (Jmol -1 ) Pt coloidal Catalase 8 400
32 Como é que os enzimas conseguem aumentar tanto as velocidades das reacções? Interacções covalentes entre enzimas e substratos baixam a energia de activação fornecendo uma via reaccional alternativa com energia mais baixa. Formação de um complexo específico enzima substrato em que são formadas muitas interacções fracas. A energia libertada aquando da formação destas ligações contribui para a especificidade e para a catálise. As ligações fracas são optimizadas no estado de transição. Os locais activos são complementares do estado de transição e não do substrato.
33 Formação de um complexo enzima-substrato. As interacções fracas entre o enzima e o substrato são optimizadas no estado de transição
34
35 Para baixar a energia de activação o sistema deve adquirir uma quantidade de energia equivalente à que diminui. Muita desta energia ( G B )vem da formação de ligações fracas entre o enzima e o substrato no estado de transição.
36 glucocinase PDB ID 2YHX
37 A catálise pode ser descrita formalmente em termos de estabilização do estado de transição através de ligação forte (tight binding) do reagente ao catalisador Jencks 1975 Ligação do reagente (substrato) ao centro activo do enzima(quimotripsina)
38 Aumentos de velocidade produzidos por enzimas: Ciclofilina Anidrase carbónico P-triose isomerase Carboxipeptidase A Fosfoglucomutase Succinil - coa transferase Urease Monofosfato de oritidina descarboxilase
39 O tamanho dos enzimas reflecte a necessidade de a superestrutura ter os grupos reactivos posicionados de modo correcto e de manter o local activo formado.
40 Os enzimas podem ser inibidos por moléculas específicas Inibição irreversível - os inibidores ligam-se covalentemente (ou não)ou destroiem um grupo funcional essencial para a actividade do enzima. A penicilina modifica por meio de ligações covalentes o enzima transpeptidase, impedindo a síntese das paredes bacterianas. A aspirina inibe o enzima que catalisa o 1º passo da síntese das prostaglandinas, compostos envolvidos nos processos de produção de dor.
41 Inactivadores-suicidas Compostos pouco reactivos que se ligam ao enzima no local activo, sofrem os primeiros passos da reacção normal mas não se transformam em produto. Convertem-se num composto muito reactivo que se combina irreversivelmente com o enzima. Design de fármacos Especificidade menos efeitos secundários
42 Inibição reversível Rápida dissociação do complexo enzima-inibidor. Inibição competitiva um inibidor competitivo compete com o substrato para o local activo do enzima. O inibidor é semelhante ao substrato. Substrato Inibidor competitivo Enzima Enzima
43 Ex. malonato (inibidor) e succinato (substrato da succinato desidrogenase) - OOCCH 2 COO - malonato - OOCCH 2 CH 2 COO - succinato
44 Metotrexato anticancerígeno Inibidor competitivo do dihidrofolato reductase Tratamento para a ingestão de metanol (solvente existente nos anticongelantes). Metanol formaldeído (provoca cegueira) desidrogenase alcoólica do fígado Etanol é inibidor competitivo do metanol e também é substrato para o enzima dando origem a acetaldeído.
45 Outros tipos de inibição reversível: Inibição incompetitiva o inibidor liga-se a um local diferente do local activo. Liga-se ao complexo ES Inibidor incompetitivo Substrato Inibição mista o inibidor também se liga a um local diferente do local activo. Liga-se a E ou a ES Enzima
46 Enzimas regulatórios Aumentam ou diminuem a sua actividade catalítica em resposta a sinais. Os enzimas alostéreos funcionam através de ligações reversíveis de compostos regulatórios. Outros enzimas são regulados por ligações covalentes reversíveis.
47 Regulação alostérea Forma activa Forma inactiva Substrato ligado ao local activo Inibidor ligado ao local alostéreo
48 Alguns enzimas são regulados por modificações covalentes reversíveis Modificação covalente (resíduos alvo) Fosforilação ( Tyr, Ser, Thr, His) Inactivo Activo
49 A actividade enzimática depende do ph Pepsina estômago G-6-P - hepatócitos Perfil da actividade enzimática vs ph de dois enzimas
50 Como estudar o mecanismo de acção dos enzimas? Cinética enzimática Estudos estruturais Química de proteínas Mutagénese dirigida
51 Efeito da concentração de substrato na velocidade inicial de uma reacção enzimática
52
53 O modelo de Michaelis - Menten A relação entre a concentração de substrato e a velocidade de reacção pode ser expressa quantitativamente Equação de Michaelis-Menten Vmax velocidade máxima; K M constante de Michaelis
54 Dependência da velocidade inicial da concentração de substrato
55 Quando [S] <<< K M, então v 0 = V max [S] /K M A velocidade é directamente proporcional a [S] Quando [S] >>> K M, então v 0 = V max A velocidade é independente de [S] Quando v 0 = V max /2, então K M = [S] K M é a conc. de substrato para a qual v 0 = V max /2
56 Transformações da equação de Michaelis- Menten a equação de Lineweaver-Burk (duplo recíproco)
57 Gráfico de Lineweaver-Burk
58 Os parâmetros cinéticos são usados para comparar actividades enzimáticas A equação de Michaelis descreve o comportamento cinético dos enzimas em que v 0 tem uma dependência hiperbólica de [S]. Estes enzimas seguem uma cinética de Michaelis-Menten. Excepções enzimas regulatórios. Parâmetros cinéticos: K M V max
59 Significado dos parâmetros cinéticos K M e V max K M Concentração de substrato para a qual a velocidade é igual a metade da V max. [S] necessária para ocorrer uma catálise significativa.
60 Consequência fisiológica do K M Fígado etanol acetaldeído desidrogenase alcoólica acetaldeído acetato desidrogenase do acetaldeído Desidrogenase do acetaldeído: Enzima mitocondrial baixo K M Enzima citosólico elevado K M Em pessoas susceptíveis ao etanol o enzima mitocondrial é menos activo.
61 O K M é muitas usado como indicador da afinidade do enzima para o substrato. O K M está relacionado com as constantes de velocidade: Se k 2 <<< k -1 Elevado K M substrato baixa afinidade do enzima para o Baixo K M elevada afinidade
62 V max V max = k cat [E t ] Representa o nº de moléculas de substrato convertidas em produto por uma molécula de enzima, numa unidade de tempo, quando o enzima está completamente saturado com o substrato. k cat Nº de turnover
63
64 Exemplo: Foi descoberto um enzima que catalisa a reacção Triste Contente Uma equipa de investigadores altamente motivados resolve estudar o enzima que chamaram contentase e verificaram que o k cat para este enzima era 600 s -1. Quando [E t ] = 20 nm e [Triste] = 40 µm, a velocidade da reacção V 0 é 9,6 µm s -1. Calcular o K M para o substrato Triste. R: 10 µm
65 Inibição competitiva A competição pode ser desviada para favorecer o substrato simplesmente adicionando mais substrato. Quando [S] >>> [I] a probabilidade do inibidor se ligar é minimizada e a reacção tem a V max normal. No entanto [S] para o qual V 0 =1/2 V max (K M ) aumenta. V max mantem o valor. K M - aumenta
66 Representação de Lineweaver-Burk para inibidores competitivos
67 Os investigadores a trabalhar na enzima contentase descobriram que o composto STRESS era um potente inibidor competitivo do enzima contentase. A adição de STRESS aumenta o valor de K M para o dobro. O que deverá ser feito para a reacção manter a sua velocidade máxima normal?
68 Os outros tipos de inibição reversível com diferentes variações dos parâmetros cinéticos (inibição anticompetitiva e mista) são observados em geral em reacções enzimáticas com mais que dois substratos.
69 Enzimas regulatórios Aumentam ou diminuem a sua actividade catalítica em resposta a sinais. Os enzimas alostéreos funcionam através de ligações reversíveis de compostos regulatórios. Outros enzimas são regulados por ligações covalentes reversíveis. Os enzimas alostéreos não obedecem à cinética de Michaelis-Menten
70 . Regulação da actividade enzimática Em muitas vias os passos de regulação são catalisados por enzimas alostéreos. Ex. Inibição por feed-back
71 Os enzimas alostéreos apresentam uma cinética sigmoidal que reflecte interacções cooperativas entre as subunidades da proteína
Enzimas - Sítio catalítico
 Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
Enzimas - Sítio catalítico Significado de cofator, grupo prostético e coenzima Enzima holozima Grupo prostético metal cofator coenzima Distinção entre cofator e coenzima depende da força de ligação com
Função proteica envolve a ligação reversível com outras moléculas O ligante se liga na proteína e um sítio específico, chamado SÍTIO DE LIGAÇÃO.
 Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
Estrutura Função 1. Função proteica envolve a ligação reversível com outras moléculas. A molécula que se liga reversivelmente à proteina LIGANTE 2. O ligante se liga na proteína e um sítio específico,
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2007/2008
 BIOQUÍMICA 1º ano de Medicina Ensino teórico 2007/2008 10ª aula teórica 23 Outubro 2007 Príncipios gerais de enzimologia Conceitos a relembrar: modo de acção das enzimas; cinética enzimática (Eq. Michaelis-Menten;
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2007/2008 10ª aula teórica 23 Outubro 2007 Príncipios gerais de enzimologia Conceitos a relembrar: modo de acção das enzimas; cinética enzimática (Eq. Michaelis-Menten;
Cinética enzimática. Cinética enzimática. Cinética enzimática 20/03/2012. Classificação sistemática das enzimas
 Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
Processo enzimático mais antigo conhecido é o da fermentação da glicose até etanol leveduras. (Pasteur, 1850). Enzima grego na levedura (Pasteur, 1877). Isolamento de todas as enzimas associadas a fermentação
Enzimas versus outros catalisadores
 Enzimas versus outros catalisadores Catalisadores proteicos Elevados factores de aceleração das reacções Grande especificidade para os substratos Estereo-especificidade (também absoluta) Reduzido número
Enzimas versus outros catalisadores Catalisadores proteicos Elevados factores de aceleração das reacções Grande especificidade para os substratos Estereo-especificidade (também absoluta) Reduzido número
São moléculas catalíticas protéicas (exceto algumas que são RNA) - Prefixo que designa a reação: lactato desidrogenase, catalase
 1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
1 5 Enzimas a) Conceito - O que são enzimas? São moléculas catalíticas protéicas (exceto algumas que são RNA) - Moléculas que aumentam a velocidade de reações sem se alterarem neste processo. - Catalisam
QBQ 0102 Educação Física. Carlos Hotta. Enzimas 17/03/15
 QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
QBQ 0102 Educação Física Carlos Hotta Enzimas 17/03/15 Previously... Proteínas são polímeros de aminoácidos A estrutura primária de uma proteína determina sua estrutura terciária e, portanto, sua função
Proteínas II. (Enzimas) Bioquímica Prof. Dr. Marcelo Soares
 Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
Proteínas II (Enzimas) Conceitos Gerais e Funções As enzimas são proteínas especializadas na catálise de reações biológicas Consideradas as biomoléculas mais notáveis devido a sua extraordinária especificidade
Enzimas e Actividade enzimática
 Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Enzimas e Actividade enzimática Energia de activação de uma reacção Em todas as células de um organismo vivo ocorre um número infindável de reacções químicas. Estas reacções implicam a quebra, e posteriormente,
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global.
 ENZIMAS Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global. Toda enzima é uma proteína, mas nem toda proteína é uma enzima! CARACTERÍSTICAS GERAIS:
ENZIMAS Proteínas catalisadoras que AUMENTAM a VELOCIDADE das reações, sem sofrerem alterações no processo global. Toda enzima é uma proteína, mas nem toda proteína é uma enzima! CARACTERÍSTICAS GERAIS:
ENZIMAS. Prof. Dr. Vagne Oliveira. Medicina Veterinária
 ENZIMAS Disciplina: Bioquímica, Prof. Dr. Vagne Oliveira Medicina Veterinária I. VISÃO GERAL A enzima B Cada traço representa uma enzima Catalizadores biológicos: substâncias de origem biológicas que aceleram
ENZIMAS Disciplina: Bioquímica, Prof. Dr. Vagne Oliveira Medicina Veterinária I. VISÃO GERAL A enzima B Cada traço representa uma enzima Catalizadores biológicos: substâncias de origem biológicas que aceleram
Aula 12: Enzimas Introdução e Cinética
 Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
Disciplina de Bioquímica Estrutural Curso de Biologia Aula 12: Enzimas Introdução e Cinética Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias de Jaboticabal
Enzimas. Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini
 Enzimas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Enzimas Proteínas especializadas em catalisar reações biológicas, ou seja aumentam a velocidade
Enzimas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Enzimas Proteínas especializadas em catalisar reações biológicas, ou seja aumentam a velocidade
Aula 4: Enzimas Cinética e Regulação
 Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Universidade Federal do Pampa Campus Itaqui Bioquímica. Profa. Dra. Marina Prigol
 Universidade Federal do Pampa Campus Itaqui Bioquímica Profa. Dra. Marina Prigol 1 1) O organismo deve ser capaz de se autoreplicar 2) O organismo deve ser capaz de catalisar reações químicas com eficiência
Universidade Federal do Pampa Campus Itaqui Bioquímica Profa. Dra. Marina Prigol 1 1) O organismo deve ser capaz de se autoreplicar 2) O organismo deve ser capaz de catalisar reações químicas com eficiência
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sítio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sítio ou centro ativo S + E
Introdução ao bloco II Enfermagem. Monica Montero Lomeli Sylvia Alquéres
 Introdução ao bloco II Enfermagem Monica Montero Lomeli Sylvia Alquéres Programação de aulas 16/set 21/set 23/set 28/set 30/set 05/out 07/out 12/out 14/out Apresentação do bloco + Enzimas I (cinéeca) Enzimas
Introdução ao bloco II Enfermagem Monica Montero Lomeli Sylvia Alquéres Programação de aulas 16/set 21/set 23/set 28/set 30/set 05/out 07/out 12/out 14/out Apresentação do bloco + Enzimas I (cinéeca) Enzimas
Aula 4: Enzimas Cinética e Regulação
 Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Disciplina de Engenharia de Proteínas Curso de Ciências Biológicas Aula 4: Enzimas Cinética e Regulação Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e Veterinárias
Enzimas. Bianca Zingales IQ - USP
 Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
Enzimas Bianca Zingales IQ - USP Enzimas As enzimas são catalisadores biológicos extremamente eficientes que aceleram 10 9 a 10 12 vezes (em média) a velocidade da reação. As enzimas chegam a transformar
1- Microrganismos e indústria alimentar 1.1 Fermentação e actividade enzimática
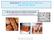 Unidade 4 Produção de alimentos e sustentabilidade 1- Microrganismos e indústria alimentar 1.1 1 Qual é a importância dos microrganismos na indústria alimentar? Queijo Os microrganismos são essenciais
Unidade 4 Produção de alimentos e sustentabilidade 1- Microrganismos e indústria alimentar 1.1 1 Qual é a importância dos microrganismos na indústria alimentar? Queijo Os microrganismos são essenciais
Enzimas. As enzimas são proteínas com exceção de um pequeno grupo de moléculas de RNA que tem ação catalítica.
 Enzimas As enzimas são proteínas com exceção de um pequeno grupo de moléculas de RNA que tem ação catalítica. Diferem dos catalisadores comuns em vários aspectos Velocidades de reações catalisadas por
Enzimas As enzimas são proteínas com exceção de um pequeno grupo de moléculas de RNA que tem ação catalítica. Diferem dos catalisadores comuns em vários aspectos Velocidades de reações catalisadas por
Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais
 O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
O que são enzimas? Catalizadores biológicos - Aceleram reações químicas específicas sem a formação de produtos colaterais Reagentes = substratos Local onde a reação ocorre = sitio ou centro ativo S + E
BIOQUÍMICA GERAL. Prof. Dr. Franciscleudo B. Costa UATA/CCTA/UFCG. Aula 6 Enzimas. Definição. Enzimas ENZIMAS PROTEÍNA
 Universidade Federal de Campina Grande Centro de Ciências e Tecnologia Agroalimentar Unidade Acadêmica de Tecnologia de Alimentos BIOQUÍMICA GERAL FRANCISCLEUDO BEZERRA DA COSTA PROFESSOR Campus Pombal
Universidade Federal de Campina Grande Centro de Ciências e Tecnologia Agroalimentar Unidade Acadêmica de Tecnologia de Alimentos BIOQUÍMICA GERAL FRANCISCLEUDO BEZERRA DA COSTA PROFESSOR Campus Pombal
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Como é que as células extraem energia e poder redutor do ambiente? Como é que as células sintetizam as unidades das macromoléculas?
 Metabolismo Como é que as células extraem energia e poder redutor do ambiente? Como é que as células sintetizam as unidades das macromoléculas? Os seres vivos precisam de energia para: Realização de trabalho
Metabolismo Como é que as células extraem energia e poder redutor do ambiente? Como é que as células sintetizam as unidades das macromoléculas? Os seres vivos precisam de energia para: Realização de trabalho
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008. Disciplina de BIOQUÍMICA I Curso de MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
ENZIMAS. Dra. Flávia Cristina Goulart. Bioquímica
 ENZIMAS Dra. Flávia Cristina Goulart Bioquímica ENZIMAS CONCEITO: São proteínas que catalisam reações químicas diferentes no organismo. Como proteínas, elas são moléculas grandes, constituídas de 20 AA.
ENZIMAS Dra. Flávia Cristina Goulart Bioquímica ENZIMAS CONCEITO: São proteínas que catalisam reações químicas diferentes no organismo. Como proteínas, elas são moléculas grandes, constituídas de 20 AA.
ENZIMAS. Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica. Prof.: Me.
 Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica ENZIMAS Prof.: Me. Allysson Haide 1 O que será abordado sobre as enzimas? Introdução às
Faculdade Maurício de Nassau Cursos de Biomedicina, Enfermagem, Farmácia e Fisioterapia Disciplina de Bioquímica ENZIMAS Prof.: Me. Allysson Haide 1 O que será abordado sobre as enzimas? Introdução às
Professora: Erika Liz. C i n é t i c a. E n z i m á t i c a
 rofessora: Erika Liz C i n é t i c a E n z i m á t i c a Elementos da Enzimologia Reações Químicas Termodinâmica estuda a viabilidade e a reversibilidade das reações, a partir da análise do conteúdo energético
rofessora: Erika Liz C i n é t i c a E n z i m á t i c a Elementos da Enzimologia Reações Químicas Termodinâmica estuda a viabilidade e a reversibilidade das reações, a partir da análise do conteúdo energético
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011 10ª aula teórica 19 Outubro 2010 Príncipios gerais de enzimologia. Modo de acção das enzimas. Cinética enzimática (Eq. Michaelis-Menten; K M e V max
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011 10ª aula teórica 19 Outubro 2010 Príncipios gerais de enzimologia. Modo de acção das enzimas. Cinética enzimática (Eq. Michaelis-Menten; K M e V max
Profa. Alessandra Barone
 Profa. Alessandra Barone www.profbio.com.br Enzimas São catalisadores biológicos de alta especificidade. Catalisar uma reação química é alterar a sua velocidade, ou seja, a quantidade de massa de reagentes
Profa. Alessandra Barone www.profbio.com.br Enzimas São catalisadores biológicos de alta especificidade. Catalisar uma reação química é alterar a sua velocidade, ou seja, a quantidade de massa de reagentes
Aula de Bioquímica I. Tema: Enzimas. Prof. Dr. Júlio César Borges
 Aula de Bioquímica I Tema: Enzimas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica I Tema: Enzimas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
A denominação das cínases não tem em linha de conta o sentido em que a reacção ocorre nos seres vivos
 A denominação das cínases não tem em linha de conta o sentido em que a reacção ocorre nos seres vivos mesmo quando (por razões de índole termodinâmica) apenas a reacção em que ocorre formação de ATP pode
A denominação das cínases não tem em linha de conta o sentido em que a reacção ocorre nos seres vivos mesmo quando (por razões de índole termodinâmica) apenas a reacção em que ocorre formação de ATP pode
Resumo esquemático da glicólise
 Resumo esquemático da glicólise Destino do piruvato em condições aeróbicas e anaeróbicas Glicólise Fermentação Oxidação completa Em condições aeróbicas o piruvato é oxidado a acetato que entra no ciclo
Resumo esquemático da glicólise Destino do piruvato em condições aeróbicas e anaeróbicas Glicólise Fermentação Oxidação completa Em condições aeróbicas o piruvato é oxidado a acetato que entra no ciclo
Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 581-
 Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
Degustação de trechos de livros sugeridos Enzimas Fonte: Wilson & Walker. Principles and Techniques of Biochemistry and Molecular Biology, 7ed. Página 58- Quando uma enzima é misturada com um excesso de
Aula de Bioquímica Avançada. Tema: Enzimas. Prof. Dr. Júlio César Borges
 Aula de Bioquímica Avançada Tema: Enzimas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica Avançada Tema: Enzimas Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Cinética das reacções enzimáticas
 Cinética das reacções enzimáticas Pioneiros da cinética enzimática: 1913 - L. Michaelis e M.L. Menten 1925 - Briggs e Haldane Leonor Michaelis Maud L. Menten v o = V max [S] K m + [S] Equação de Michaelis-Menten
Cinética das reacções enzimáticas Pioneiros da cinética enzimática: 1913 - L. Michaelis e M.L. Menten 1925 - Briggs e Haldane Leonor Michaelis Maud L. Menten v o = V max [S] K m + [S] Equação de Michaelis-Menten
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores
 Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
Que relação existe entre a atividade enzimática e a velocidade das reações? Catalisadores Que relação existe entre a atividade enzimática e a velocidade das reações? As enzimas diminuem a energia de ativação
Cinética em fase homogênea
 Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Cinética em fase homogênea Hipótese chave-fechadura Centro ativo complementar em tamanho, forma e natureza química à molécula do substrato, ou seja, uma cavidade geometricamente rígida. Emil Fischer (1894)
Fundamentos da Bioquímica II Aminoácidos Diferencia as propriedades físicoquímicas dos aminoácidos
 Fundamentos da Bioquímica II Aminoácidos Diferencia as propriedades físicoquímicas dos aminoácidos Amina R O α Carboxila N 2 C C O Na água: Zwitterion R O N + 3 α C C O - Carbono: Aspectos estruturais:
Fundamentos da Bioquímica II Aminoácidos Diferencia as propriedades físicoquímicas dos aminoácidos Amina R O α Carboxila N 2 C C O Na água: Zwitterion R O N + 3 α C C O - Carbono: Aspectos estruturais:
São catalisadores biológicos de alta especificidade. Catalisar uma reação química é alterar a sua
 Profa Alessandra Barone Enzimas São catalisadores biológicos de alta especificidade. Catalisar uma reação química é alterar a sua velocidade, ou seja, a quantidade de massa de reagentes (S) transformada
Profa Alessandra Barone Enzimas São catalisadores biológicos de alta especificidade. Catalisar uma reação química é alterar a sua velocidade, ou seja, a quantidade de massa de reagentes (S) transformada
Cinética Enzimática. Prof Karine P. Naidek Novembro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Cinética Enzimática Prof Karine P. Naidek Novembro/2016 Cinética das Reações Bioquímicas
Prof. Marcelo Langer. Curso de Biologia. Aula 38 Citologia
 Prof. Marcelo Langer Curso de Biologia Aula 38 Citologia ENZIMAS Apenas alguns grupos de moléculas de RNA que apresentam função biocatalisadora, todas as enzimas são proteínas. FUNÇÕES DAS ENZIMAS: Proteínas
Prof. Marcelo Langer Curso de Biologia Aula 38 Citologia ENZIMAS Apenas alguns grupos de moléculas de RNA que apresentam função biocatalisadora, todas as enzimas são proteínas. FUNÇÕES DAS ENZIMAS: Proteínas
ENZIMAS. Osmundo Brilhante
 ENZIMAS Osmundo Brilhante Introdução Condições Fundamentais para a Vida Auto replicação; O organismo deve ser capaz de catalisar as reações químicas; Metabolismo celular e manutenção da via Enzimas Doenças;
ENZIMAS Osmundo Brilhante Introdução Condições Fundamentais para a Vida Auto replicação; O organismo deve ser capaz de catalisar as reações químicas; Metabolismo celular e manutenção da via Enzimas Doenças;
Metabolismo e Regulação
 Metabolismo e Regulação PRBLEMAS - Série 1 Soluções 2009/2010 idratos de Carbono (Revisão) e Metabolismo Central 1 R: (α 1 4) (lineares) Ο (α1 6) (pontos de ramificação) 2. R: Locais de glicosilação são
Metabolismo e Regulação PRBLEMAS - Série 1 Soluções 2009/2010 idratos de Carbono (Revisão) e Metabolismo Central 1 R: (α 1 4) (lineares) Ο (α1 6) (pontos de ramificação) 2. R: Locais de glicosilação são
DETERMINAÇÃO DA ACTIVIDADE DE ENZIMAS DA GLICÓLISE EM EXTRACTOS DE CÉLULAS DE LEVEDURA. Glucose + 2Pi + 2ADP + 2NAD! 2CH COCOO " 2ATP " 2NADH " 2 H
 DETERMINAÇÃ DA ACTIVIDADE DE ENZIMAS DA GLICÓLISE EM EXTRACTS DE CÉLULAS DE LEVEDURA 1. Introdução A glicólise é um caminho metabólico quase universal no qual a glucose é convertida em piruvato com síntese
DETERMINAÇÃ DA ACTIVIDADE DE ENZIMAS DA GLICÓLISE EM EXTRACTS DE CÉLULAS DE LEVEDURA 1. Introdução A glicólise é um caminho metabólico quase universal no qual a glucose é convertida em piruvato com síntese
REAÇÕES ESPECÍFICAS PARA aa
 REAÇÕES ESPECÍFICAS PARA aa Organismo Desaminação não sintetiza Transaminação Descarboxilação TRANSAMINAÇÃO Ác.glutâmico Ceto-ácido ALANINA-piruvato ÁC. ASPÁRTICO- oxalacetato OBJETIVO : CENTRALIZAR TODOS
REAÇÕES ESPECÍFICAS PARA aa Organismo Desaminação não sintetiza Transaminação Descarboxilação TRANSAMINAÇÃO Ác.glutâmico Ceto-ácido ALANINA-piruvato ÁC. ASPÁRTICO- oxalacetato OBJETIVO : CENTRALIZAR TODOS
ENZIMAS. FCAV/UNESP Jaboticabal Dezembro de W.J.Melo
 ENZIMAS FCAV/UNESP Jaboticabal Dezembro de 1991 CONCEITO E EXEMPLOS!Conceito #São biomoléculas de natureza predominantemente protéica cuja função é catalisar reações termodinamicamente possíveis!exemplos
ENZIMAS FCAV/UNESP Jaboticabal Dezembro de 1991 CONCEITO E EXEMPLOS!Conceito #São biomoléculas de natureza predominantemente protéica cuja função é catalisar reações termodinamicamente possíveis!exemplos
Enzimas - Aspectos estruturais Parte 1. Informações gerais
 Enzimas - Aspectos estruturais Parte 1 Schpector São Carlos, 03 de junho de 2017 1 Informações gerais Enzimas que agem como catalizadores biológicos. 1. As enzimas tem um enorme poder catalítico. 2. São
Enzimas - Aspectos estruturais Parte 1 Schpector São Carlos, 03 de junho de 2017 1 Informações gerais Enzimas que agem como catalizadores biológicos. 1. As enzimas tem um enorme poder catalítico. 2. São
2- No dia estavam classificadas 4046 enzimas que podem ser consultadas em
 A maioria das enzimas são de natureza proteica e, relativamente aos outros catalisadores, têm uma grande especificidade em relação aos substratos e produtos da reacção. 1- A palavra enzima (do Grego: en,
A maioria das enzimas são de natureza proteica e, relativamente aos outros catalisadores, têm uma grande especificidade em relação aos substratos e produtos da reacção. 1- A palavra enzima (do Grego: en,
Enzimas Fermentos. Enzimologia: A ciência que estuda as enzimas
 Enzimas Fermentos As enzimas (ou fermentos), junto `as vitaminas e hormonas, constituem um grupo de substâncias cataliticamente activas nos organismos vivos Lazzaro Spallanzani (1783) Louis Pasteur (1857)
Enzimas Fermentos As enzimas (ou fermentos), junto `as vitaminas e hormonas, constituem um grupo de substâncias cataliticamente activas nos organismos vivos Lazzaro Spallanzani (1783) Louis Pasteur (1857)
[ A][ B] [ A] [ B] v {[A] }= Vmáx
![[ A][ B] [ A] [ B] v {[A] }= Vmáx [ A][ B] [ A] [ B] v {[A] }= Vmáx](/thumbs/75/72105322.jpg) Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
Reacções com Mais que um Substrato Equação de ase Experimental v = V máx S [ ][ ] [ ] [ ] [ ][ ] Quando [] ou [] toma valores muito elevados, por exemplo, reacções de hidrólise em solução aquosa podem
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias.
 UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
UNIVERSIDADE ESTADUAL PAULISTA JÚLIO DE MESQUITA FILHO Campus de Jaboticabal Faculdade de Ciências Agrárias e Veterinárias Enzimas Prof. Luciano Hauschild Plano de aula 1) Atuação das enzimas na cinética
Aula 2: Estrutura e Função de Proteínas
 Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
Disciplina de Mét. Purif. e Anál. Proteínas Curso de Ciências Biológicas Aula 2: Estrutura e Função de Proteínas Prof. Marcos Túlio de Oliveira mtoliveira@fcav.unesp.br Faculdade de Ciências Agrárias e
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS. Enzimas. Prof. Me. Cássio Resende de Morais
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Enzimas Prof. Me. Cássio Resende de Morais Enzimas Catalisadores biológicos: substâncias de origem biológica que aceleram
Enzimas revisões. v o = V max [S] K m + [S]
![Enzimas revisões. v o = V max [S] K m + [S] Enzimas revisões. v o = V max [S] K m + [S]](/thumbs/67/57975399.jpg) nzimas revisões k 1 k + 3 + S k 2 S P v o = V max [S] K m + [S] quação de Michaelis-Menten V max é o valor para o qual tende a velocidade à medida que se aumenta a concentração de substrato; corresponde
nzimas revisões k 1 k + 3 + S k 2 S P v o = V max [S] K m + [S] quação de Michaelis-Menten V max é o valor para o qual tende a velocidade à medida que se aumenta a concentração de substrato; corresponde
Acetil CoA e Ciclo de Krebs. Prof. Henning Ulrich
 Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich Glicose + Consumo de 2 ATP 2 Ácidos Pirúvicos + 4H + + Produção de 4 ATP (2C 3 H 4 O 3 ) 2H + são Transportados pelo NAD passando Para o estado reduzido
Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich Glicose + Consumo de 2 ATP 2 Ácidos Pirúvicos + 4H + + Produção de 4 ATP (2C 3 H 4 O 3 ) 2H + são Transportados pelo NAD passando Para o estado reduzido
QBQ-0230 Bioquímica do Metabolismo Biologia Noturno
 QBQ-0230 Bioquímica do Metabolismo Biologia Noturno A catálise na vida Um dos princípios da vida é que os organismos sejam capazes de extrair, transformar e utilizar a energia do ambiente. Para tal, sistemas
QBQ-0230 Bioquímica do Metabolismo Biologia Noturno A catálise na vida Um dos princípios da vida é que os organismos sejam capazes de extrair, transformar e utilizar a energia do ambiente. Para tal, sistemas
Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula!
 Aula: 20 Temática: Funções bioquímicas das proteínas parte II Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula! 1) Mediadores e reguladores metabólicos (continuação):
Aula: 20 Temática: Funções bioquímicas das proteínas parte II Na aula de hoje continuaremos a estudar as funções bioquímicas das proteínas. Boa aula! 1) Mediadores e reguladores metabólicos (continuação):
Os organismos necessitam de um constante fornecimento de energia livre
 Os organismos necessitam de um constante fornecimento de energia livre Por que? - Biossíntese de moléculas complexas; - Transporte ativo de moléculas e íons c através de membranas; - Realização de Trabalho
Os organismos necessitam de um constante fornecimento de energia livre Por que? - Biossíntese de moléculas complexas; - Transporte ativo de moléculas e íons c através de membranas; - Realização de Trabalho
Catálise Enzimática. Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química.
 Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Catálise Enzimática Um catalisador é uma substância que acelera uma reação sem sofrer, no processo, modificação de natureza química. O catalisador age fornecendo uma via reacional alternativa com menor
Biologia 12 Fermentação e actividade enzimática
 Biologia 12 Fermentação e actividade enzimática Uma elevada percentagem de produtos que consumimos é produzida, mantida ou degradada por microorganismos. O conhecimento do metabolismo microbiano permitirá
Biologia 12 Fermentação e actividade enzimática Uma elevada percentagem de produtos que consumimos é produzida, mantida ou degradada por microorganismos. O conhecimento do metabolismo microbiano permitirá
Mecanismo de reação de uma enzima com substrato único. A enzima (E) liga o substrato (S) e liberta o produto (P).
 CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
CINÉTICA ENZIMÁTICA Cinética Enzimática Estudo da velocidade de uma reação química que ocorre na presença de uma enzima a) Medir as velocidades das transformações que se processam; b) Estudar a influências
QBQ 0204 Bioquímica. Carlos Hotta. Glicólise 13/05/17
 QBQ 0204 Bioquímica Carlos Hotta Glicólise 13/05/17 Uma visão geral do metabolismo Ribose 5P (5) NUCLEOTÍDEOS Algumas reações são irreversíveis Vias de síntese e degradação precisam ser separadas Uma visão
QBQ 0204 Bioquímica Carlos Hotta Glicólise 13/05/17 Uma visão geral do metabolismo Ribose 5P (5) NUCLEOTÍDEOS Algumas reações são irreversíveis Vias de síntese e degradação precisam ser separadas Uma visão
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros
 Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Estudo da velocidade da reação enzimática e como ela se altera em função de diferentes parâmetros Importante abordagem para o entendimento do mecanismo de ação de uma enzima. Vários fatores afetam a atividade
Enzimas e Coenzimas. União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Enzimas e Coenzimas Prof. Dra. Narlize Silva Lira Cavalcante Março /2015 Enzimas Praticamente todas as
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Enzimas e Coenzimas Prof. Dra. Narlize Silva Lira Cavalcante Março /2015 Enzimas Praticamente todas as
Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13
 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8: Inibição por maltose (Ki) Execução e recolhimento dos exercícios 11 a 13 Prática 7: Caracterização da -glicosidase (Km e Vmax) Prática 8:
LIGAÇÃO PEPTÍDICA. ligação peptídica DIPEPTÍDEO AMINOÁCIDOS
 PROTEÍNAS PROTEÍNAS LIGAÇÃO PEPTÍDICA DIPEPTÍDEO AMINOÁCIDOS ligação peptídica PEPTÍDEO Resíduo N-terminal Resíduo C-terminal OLIGOPEPTÍDEOS: 2 a 10 resíduos de aminoácidos. Exemplos: dipeptídio (2 aminoácidos),
PROTEÍNAS PROTEÍNAS LIGAÇÃO PEPTÍDICA DIPEPTÍDEO AMINOÁCIDOS ligação peptídica PEPTÍDEO Resíduo N-terminal Resíduo C-terminal OLIGOPEPTÍDEOS: 2 a 10 resíduos de aminoácidos. Exemplos: dipeptídio (2 aminoácidos),
Processos catalíticos mediados por enzimas que contém metais
 Processos catalíticos mediados por enzimas que contém metais Shriver e Atkins, cap 26 Catálise ácido-base Pense: muitas reações catalisadas por ácidos ou bases requerem concentrações de H + ou de OH -
Processos catalíticos mediados por enzimas que contém metais Shriver e Atkins, cap 26 Catálise ácido-base Pense: muitas reações catalisadas por ácidos ou bases requerem concentrações de H + ou de OH -
Profª Eleonora Slide de aula. Metabolismo de Carboidratos
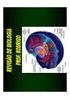 Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose 2 Etanol + 2 CO 2 Condições
Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose 2 Etanol + 2 CO 2 Condições
BIOENERGÉTICA INTRODUÇÃO
 INTRODUÇÃO BIOENERGÉTICA Hoje, mais do que nunca, estamos conscientes de que a energia, a capacidade de produzir trabalho, é vital para a nossa civilização moderna. Nas suas diversas formas (elétrica,
INTRODUÇÃO BIOENERGÉTICA Hoje, mais do que nunca, estamos conscientes de que a energia, a capacidade de produzir trabalho, é vital para a nossa civilização moderna. Nas suas diversas formas (elétrica,
Equipe de Biologia. Biologia
 Aluno (a): Série: 3ª Turma: TUTORIAL 4B Ensino Médio Equipe de Biologia Data: Biologia ENZIMAS CONCEITOS GERAIS E FUNÇÕES As enzimas são proteínas especializadas na catálise de reações biológicas. Elas
Aluno (a): Série: 3ª Turma: TUTORIAL 4B Ensino Médio Equipe de Biologia Data: Biologia ENZIMAS CONCEITOS GERAIS E FUNÇÕES As enzimas são proteínas especializadas na catálise de reações biológicas. Elas
12/11/2015. Disciplina: Bioquímica Prof. Dr. Vagne Oliveira
 Disciplina: Bioquímica Prof. Dr. Vagne Oliveira 2 1 ATP ADP Glicose (6C) C 6 H 12 O 6 ATP ADP P ~ 6 C ~ P 3 C ~ P 3 C ~ P Pi NAD NADH P ~ 3 C ~ P ADP P ~ 3 C ATP ADP ATP NAD Pi NADH P ~ 3 C ~ P ADP ATP
Disciplina: Bioquímica Prof. Dr. Vagne Oliveira 2 1 ATP ADP Glicose (6C) C 6 H 12 O 6 ATP ADP P ~ 6 C ~ P 3 C ~ P 3 C ~ P Pi NAD NADH P ~ 3 C ~ P ADP P ~ 3 C ATP ADP ATP NAD Pi NADH P ~ 3 C ~ P ADP ATP
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro)
 Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
Cinética e regulação enzímica (a velocidade das reacções enzímicas in vivo e in vitro) Conceitos de substrato de via metabólica, coenzima, grupo prostético e cofactor. Os conceitos de substrato da via
PRINCIPAIS VIAS METABÓLICAS
 PRINCIPAIS VIAS METABÓLICAS DEGRADAÇÃO DO GLIGOGÊNIO GLICÓLISE VIA DAS PENTOSES FOSFATO GLICONEOGÊNESE SÍNTESE DE CORPOS CETÔNICOS DEGRADAÇÃO DE AMINOÁCIDOS E CICLO DA URÉIA CICLO DE KREBS Β-OXIDAÇÃO DE
PRINCIPAIS VIAS METABÓLICAS DEGRADAÇÃO DO GLIGOGÊNIO GLICÓLISE VIA DAS PENTOSES FOSFATO GLICONEOGÊNESE SÍNTESE DE CORPOS CETÔNICOS DEGRADAÇÃO DE AMINOÁCIDOS E CICLO DA URÉIA CICLO DE KREBS Β-OXIDAÇÃO DE
Bibliografia. BIOQUÍMICA I 2010/2011 Ensino teórico - 1º ano Mestrado Integrado em Medicina. Stryer, Biochemistry, 5ª Ed, 2006, Capítulo 17
 BIOQUÍMICA I 2010/2011 Ensino teórico - 1º ano Mestrado Integrado em Medicina 14ª aula teórica Complexo da piruvato desidrogenase (PDH) e ciclo de Krebs. 15/11/2010 Bibliografia Stryer, Biochemistry, 5ª
BIOQUÍMICA I 2010/2011 Ensino teórico - 1º ano Mestrado Integrado em Medicina 14ª aula teórica Complexo da piruvato desidrogenase (PDH) e ciclo de Krebs. 15/11/2010 Bibliografia Stryer, Biochemistry, 5ª
Enzimas e Energia. Bases do metabolismo. Enzimas
 Enzimas e Energia Bases do metabolismo Enzimas 1 Enzimas - Proteínas. - Permitem que as reacções químicas ocorram à temperatura corporal - catalizadoras Enzimas catalizadoras: - Não se modificam na reacção
Enzimas e Energia Bases do metabolismo Enzimas 1 Enzimas - Proteínas. - Permitem que as reacções químicas ocorram à temperatura corporal - catalizadoras Enzimas catalizadoras: - Não se modificam na reacção
ENZIMAS ENZIMAS... 1 A. INTRODUÇÃO...3 B. CINÉTICA ENZIMÁTICA...7
 ENZIMAS ENZIMAS... 1 A. INTRODUÇÃO...3 1. CONCEITO... 3 2. PROPRIEDADES... 3 3. NOMENCLATURA E CLASSIFICAÇÃO... 4 4. COFACTORES... 5 4.a. Coenzimas...5 4.b. Iões Metálicos...5 4.c. Grupos Prostéticos...6
ENZIMAS ENZIMAS... 1 A. INTRODUÇÃO...3 1. CONCEITO... 3 2. PROPRIEDADES... 3 3. NOMENCLATURA E CLASSIFICAÇÃO... 4 4. COFACTORES... 5 4.a. Coenzimas...5 4.b. Iões Metálicos...5 4.c. Grupos Prostéticos...6
Enzimas. Prof Karine P. Naidek Outubro/2016
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Enzimas Prof Karine P. Naidek Outubro/2016 Enzimas Enzimas são proteínas com atividade
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Enzimas Prof Karine P. Naidek Outubro/2016 Enzimas Enzimas são proteínas com atividade
Oxidação parcial o que acontece com o piruvato?
 A glicólise ocorre no citosol das células transforma a glicose em duas moléculas de piruvato e é constituída por uma sequência de 10 reações (10 enzimas) divididas em duas fases. Fase preparatória (cinco
A glicólise ocorre no citosol das células transforma a glicose em duas moléculas de piruvato e é constituída por uma sequência de 10 reações (10 enzimas) divididas em duas fases. Fase preparatória (cinco
Macromoléculas. Biologia IV Aula 2 Bioquímica Proteínas
 Biologia IV Aula 2 Bioquímica Proteínas Carla Silva Martins 08 de agosto de 2016 Macromoléculas Água Carboidratos Aminoácidos (proteínas/enzimas) Lipídeos Ácidos nucléicos (Biologia Molecular) 1 Introdução
Biologia IV Aula 2 Bioquímica Proteínas Carla Silva Martins 08 de agosto de 2016 Macromoléculas Água Carboidratos Aminoácidos (proteínas/enzimas) Lipídeos Ácidos nucléicos (Biologia Molecular) 1 Introdução
CATÁLISE ENZIMÁTICA. CINÉTICA Controle da velocidade de reações. CINÉTICA Equilíbrio e Estado Estacionário
 CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
CATÁLISE ENZIMÁTICA Equilíbrio e Estado Estacionário P U T F M A Velocidade: período inicial Tempo As medidas de velocidade inicial (v 0 ) são obtidas com a variação da concentração de S btenção de várias
BIOQUÍMICA. Profº André Montillo
 BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
Página 1 de 8. 1 Elaborar um protocolo experimental adequado ao assunto em estudo estudo de uma enzima.
 Página 1 de 8 ACTIVIDADE LABORATORIAL BIOLOGIA 12º Ano O que se pretende 1 Elaborar um protocolo experimental adequado ao assunto em estudo estudo de uma enzima. 2 Seleccionar material adequado ao estudo
Página 1 de 8 ACTIVIDADE LABORATORIAL BIOLOGIA 12º Ano O que se pretende 1 Elaborar um protocolo experimental adequado ao assunto em estudo estudo de uma enzima. 2 Seleccionar material adequado ao estudo
Metabolismo e Regulação
 Metabolismo e Regulação PROBLEMAS - Série 1 Licenciatura em Bioquímica Licenciatura em Biologia Celular e Molecular Licenciatura em Química Aplicada Hidratos de Carbono e Metabolismo Central (Revisão)
Metabolismo e Regulação PROBLEMAS - Série 1 Licenciatura em Bioquímica Licenciatura em Biologia Celular e Molecular Licenciatura em Química Aplicada Hidratos de Carbono e Metabolismo Central (Revisão)
Hidrólise da ureia pela urease
 Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Hidrólise da ureia pela urease DQB Velocidade de uma reacção enzimática DQB Para cada case do utilização de um enzima para catálise de uma dada reacção é necessário conhecer a estequiometria da reacção
Introdução às reacções enzímicas. Equilíbrio químico, catálise e classificação funcional.
 Introdução às reacções enzímicas. Equilíbrio químico, catálise e classificação funcional. rui.fontes@mail.telepac.pt s vias metabólicas existem porque existem enzimas que têm especificidade para substratos
Introdução às reacções enzímicas. Equilíbrio químico, catálise e classificação funcional. rui.fontes@mail.telepac.pt s vias metabólicas existem porque existem enzimas que têm especificidade para substratos
As enzimas atuam ainda como reguladoras deste conjunto complexo de reações.
 ENZIMAS As enzimas são proteínas especializadas na catálise de reações biológicas. Elas estão entre as biomoléculas mais notáveis devido a sua extraordinária especificidade e poder catalítico, que são
ENZIMAS As enzimas são proteínas especializadas na catálise de reações biológicas. Elas estão entre as biomoléculas mais notáveis devido a sua extraordinária especificidade e poder catalítico, que são
ENZIMAS. Células podem sintetizar enzimas conforme a sua necessidade.
 ENZIMAS As enzimas são proteínas, catalisadores (aumenta a velocidade de uma determinada reação química) biológicos (proteínas) de alta especificidade. Praticamente todas as reações que caracterizam o
ENZIMAS As enzimas são proteínas, catalisadores (aumenta a velocidade de uma determinada reação química) biológicos (proteínas) de alta especificidade. Praticamente todas as reações que caracterizam o
Mecanismos de catálise enzimática
 Mecanismos de catálise enzimática Guilherme Menegon Arantes garantes@iq.usp.br http://gaznevada.iq.usp.br Universidade de São Paulo Resumo da aula de hoje Relembrando a equação de Michaelis-Mentem Reação
Mecanismos de catálise enzimática Guilherme Menegon Arantes garantes@iq.usp.br http://gaznevada.iq.usp.br Universidade de São Paulo Resumo da aula de hoje Relembrando a equação de Michaelis-Mentem Reação
BIOLOGIA. Moléculas, células e tecidos. A química da vida Parte 5. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos A química da vida Parte 5 Professor: Alex Santos Tópicos em abordagem: Enzimas: I Conceitos fundamentais II Propriedades das enzimas III Nomenclatura de enzimas IV
BIOLOGIA Moléculas, células e tecidos A química da vida Parte 5 Professor: Alex Santos Tópicos em abordagem: Enzimas: I Conceitos fundamentais II Propriedades das enzimas III Nomenclatura de enzimas IV
Engenharia Bioquímica
 Engenharia Bioquímica Cinética Enzimática Mestrando: Mateus Vinícius Casagrande da Silva Professor Doutor João Batista de Almeida e Silva Conceitos e revisão sobre Enzimas O que são enzimas? Definições
Engenharia Bioquímica Cinética Enzimática Mestrando: Mateus Vinícius Casagrande da Silva Professor Doutor João Batista de Almeida e Silva Conceitos e revisão sobre Enzimas O que são enzimas? Definições
Glória Braz GLICÓLISE
 Glória Braz GLICÓLISE Utilização de glicose pelas células A glicólise é a via metabólica mais conservada nos sistemas biológicos A glicose é o combustível preferencial e mais versátil disponível nas células
Glória Braz GLICÓLISE Utilização de glicose pelas células A glicólise é a via metabólica mais conservada nos sistemas biológicos A glicose é o combustível preferencial e mais versátil disponível nas células
Metabolismo e Endocrinologia
 Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
Metabolismo e Endocrinologia Teórica-Pratica: 1 Tema: 1.Enzimologia 1.1 Noções de termodinâmica 1.2 Cinética 1.3 Inibição 2. Tópicos de resposta para a primeira teórico-prática Data: 30.03.2011 1 ENZIMOLOGIA
ENZIMAS ENZIMAS ENZIMAS 19/02/17 DEFINIÇÃO CLASSIFICAÇÃO ESTRUTURAL. ativa. inativa
 DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
DFNÇÃO nzimas são proteínas que atuam como catalisadores biológicos o Aceleram a velocidade das reações químicas o Não alteram os produtos finais das reações o Zimogênio (inativas) / nzima (ativas) Composto
C 6 H 12 O O 2 6 CO H 2 O
 O que os seres vivos sabem fazer melhor é comer ingerir substâncias no estado reduzido que vão ser oxidadas a e respirar inspirar O 2, o oxidante último dos nutrientes e expirar o produto da oxidação dos
O que os seres vivos sabem fazer melhor é comer ingerir substâncias no estado reduzido que vão ser oxidadas a e respirar inspirar O 2, o oxidante último dos nutrientes e expirar o produto da oxidação dos
Inibidores Enzimáticos
 Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
Inibidores Enzimáticos BIOQUÍMICA - INIBIÇÃO ENZIMÁTICA NOÇÕES BÁSICAS SOBRE ENZIMAS CONCEITO As enzimas são proteínas especializadas na catálise de reações biológicas MECANISMO DE AÇÃO As enzimas aceleram
