Teoria Cinética dos Gases
|
|
|
- William Bentes Cesário
- 6 Há anos
- Visualizações:
Transcrição
1 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 1 Teora Cnétca dos Gases 19.1 Introdução Um gás consste em átomos que preenchem o volume de seu recpente. As varáves volume, pressão e temperatura, são conseqüêncas do movmento dos átomos. olume resultado da lberdade dos átomos; Pressão resultado das colsões dos átomos com as paredes do recpente; Temperatura relaconada com a energa cnétca dos átomos. 19. Número de Avogadro mol número de átomos em uma amostra de 1g do carbono-1. Num mol de qualquer substânca exstem 3 1 N A 6,0x10 mol NÚMERO DE AOGADRO O número de moles n contdos em uma amostra de qualquer substânca é gual a razão entre o número de moléculas N na amostra e o número de moléculas N A em 1mol: N n O número de moles n pode ser encontrado dvdndo a massa M am da amostra pela sua massa molar M. M am M am n M mn A onde m é a massa de uma molécula. N A
2 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 19.3 Gases Ideas Expermentos mostraram que, para densdades sufcentemente baxas, todos os gases tendem a obedecer à relação: p nrt LEI DOS GASES IDEAIS Onde p é a pressão absoluta (não manométrca), n é o número de moles do gás confnado e T é a temperatura em kelvns. R é a constante dos gases deas. R 8,31J / mol. K Em termos da constante de Boltzmann, temos: k R N A 8,31J / mol. K 3 1,38x10 J / K 3 1 6,0x10 mol Podemos escrever, R kn A o que nos permte usar a equação e obtermos nr Nk n N / N, Substtundo na equação dos gases deas temos p NkT Trabalho Realzado por um Gás Ideal a Temperatura Constante Em um dagrama p, uma soterma é uma curva que conecta pontos que possuem a mesma temperatura. Para n moles de um gás deal, ela é o gráfco da equação 1 1 p nrt ( cons tan te) A
3 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 3 Para encontrar o trabalho realzado durante qualquer varação de volume de qualquer gás, podemos usar p nrt para substtur p, W f nrt W W f d nrt f pd 1 d nrtln f nrt ln GÁS IDEAL, PROCESSO ISOTÉRMICO. Trabalho Realzado a olume Constante e a Pressão Constante Se o volume do gás é constante, a equação anteror nos fornece W 0 PROCESSO ISOCÓRICO Se o volume vara enquanto a pressão é mentda constante, a equação f W pd nos dá W f p d p( ) PROCESSO ISOBÁRICO f f p Exercíco Um clndro contém 1L de oxgêno a 0 o C e 15atm. A temperatura é aumentada para 35 o C e o volume é reduzdo para 8,5L. Qual é a pressão fnal do gás em atmosferas? Suponha que o gás seja deal.,3atm.
4 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 4 Exercíco: Um mol de oxgêno (suponha deal) se expande a uma temperatura constante de 310K de um volume ncal =1L até um volume fnal f =19L. Que trabalho é realzado pelo gás durante a expansão? (1183J) 19.4 Pressão, Temperatura e elocdade Méda Quadrátca. Consdera n moles de um gás deal confnado numa caxa cúbca de volume. As paredes da caxa são mantdas a temperatura T. Qual a lgação entre a pressão p exercda pelo gás sobre as paredes e as velocdades das moléculas? Quando a molécula da fgura coldr com a parede, a varação do momento ao longo do exo x é dada por: p ( mv ) ( mv ) mv x x x x A molécula va atngr a parede váras vezes. O tempo entre duas colsões na mesma parede será dado por L t A taxa méda com que o momento é transmtdo para a parede sombreada é v x
5 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 5 px mvx mvx t L / vx L De acordo com a ª le de Newton ( F dp / dt ), a taxa com a qual o momento é transferdo para a parede é a força que atua sobre a mesma. A pressão exercda devdo a contrbução de todas as moléculas na parede do cubo é Fx mvx 1 / L mvx / L... mvxn / L p L L m p ( v 1... ), 3 x vx vxn L onde N é o número de moléculas na caxa. Como N nn A, exstem nn A termos no segundo conjunto entre parêntess da equação anteror. Substtundo esta quantdade por nn A( v x ) méd, onde ( v x ) méd é o valor médo do quadrado da componente x de todas as velocdades moleculares. A equação da pressão torna-se então nmn p A ( v x ) 3 méd L Como há mutas moléculas, v vx v y vz, os valores médos dos quadrados das componentes da velocdade são guas, 1 de modo que vx v. Consderando que mn M 3 A, L 3 e substtundo na equação teremos: nm p ( v ) méd 3 A raz quadrada de ( v ) méd vrms é uma velocdade conhecda como velocdade méda quadrátca, smbolzada por v rms. Assm nm p v rms 3
6 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 6 A equação anteror pode ser Algumas elocdades RMS à nvertda para se calcular a Temperatura Ambente (T=300K) Massa Molar Gás v (10-3 rms kg/mol) (m/s) velocdade quadrátca méda. 3p 3RT v rms nm M sendo que p nrt. Exercíco: (a) Encontre o valor médo dos números: 5, 11, 3, 67, e 89 (resp 40,8) n médo 40,8 5 (b) Encontre o valor rms destes números n rms , Energa Cnétca Translaconal Consderando uma molécula coldndo com outras moléculas do gás no nteror da caxa, sua energa cnétca translaconal méda será dada por K méd 1 mv méd 1 m( v ) méd 1 mv rms que pode ser escrta na forma 1 3RT K méd m M K méd mas M mn A, logo 3RT N, sendo k R / N A A m 1 M 3 K méd kt Hdrogêno,0 190 (H ) Hélo (He) 4, apor d água (H O) Ntrogêno (N ) Oxgêno (O ) Dóxdo de carbono (CO ) Dóxdo de enxofre (SO ) 64,1 34 Em uma dada temperatura T, todas as moléculas de um gás deal, ndependentemente de suas massas, têm a mesma energa cnétca translaconal méda, 3 kt. N A
7 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr Camnho Lvre Médo O Camnho lvre médo descreve o movmento aleatóro que ndca a dstânca méda percorrda por uma molécula entre colsões. Espera-se que este parâmetro vare nversamente com N/, o número de moléculas por undade de volume ( densdade de moléculas). Quanto maor for N/, maor o número de colsões e menor o camnho lvre médo. Esperase também que vare nversamente com o tamanho das moléculas. A expressão para o camnho lvre médo é: 1 d N / Na fgura ao lado, (a) ocorre uma colsão quando os centros de duas moléculas estverem a uma dstânca d. Se consderarmos nossa molécula (b) com rao d e as demas como sendo puntformes, o crtéro para colsão não muda. Entre uma colsão e outra, a molécula varre uma dstânca compreendda por um clndro de área de seção d. Num tempo t a molécula percorre uma dstânca v t, e o volume do clndro será dado por ( d )( vt).
8 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 8 O número de colsões que ocorrem num ntervalo de tempo t é gual ao número de moléculas puntformes que estão no volume do clndro. Como N / é o número de moléculas por undade de volume, ( N / )( d vt), que é o número de colsões que ocorrem neste ntervalo de tempo. O camnho lvre médo será o comprmento da trajetóra (do clndro) dvddo por este número. vt 1 d vtn / d N / Esta equação leva em conta que somente uma das moléculas do gás está em movmento. Se consderarmos o movmento das outra, ela se transforma em. 1 d N / Consderando as moléculas do ar: 0, 1m ao nível do mar; 16cm 100km de alttude; 0km 300km de alttude. Exercíco: (a) Qual é o camnho lvre médo para moléculas de oxgêno na temperatura T 300K e pressão p 1, 0atm? Suponha que o dâmetro molecular seja d 90 pm e que o gás seja deal. (b) Suponha que a velocdade méda das moléculas de oxgêno é v 450m / s. Qual é o tempo médo t entre colsões sucessvas para qualquer molécula? A que taxa as moléculas coldem, ou seja, qual a freqüênca f das colsões? (resp. 1,1 x10 m ;,44x10 s ; 4,1x 10 s )
9 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr A dstrbução de elocdades Moleculares A fgura (a) mostra uma dstrbução para as moléculas de oxgêno na temperatura ambente (T=300K). A fgura (b) compara este resultado com a dstrbução a T=80K. Le da Dstrbução de elocdades de Maxwell (185) - Encontra a dstrbução das velocdades moleculares de um gás. P(v) M Mv / RT P( v) 4 v e RT é a função dstrbução de probabldade de velocdade A área sob a curva será 0 P( v) dv 1 A fração (fr) das moléculas com velocdades em um ntervalo de v1 a v será. 3 / fr v v 1 P( v) dv
10 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 10 elocdades Méda, RMS e Mas Provável. A velocdade méda v méd, é obtda multplcando-se v pela fração P ( v) dv das moléculas com velocdades em um ntervalo dferencal dv centrado em v. Adconando todos estes valores, de vp ( v) dv. Substtundo P (v) por P( v) 4 M RT 3 / v e Mv / RT v méd 0 vp( v) dv e usando o resultado genérco da ntegral (0 apêndce E) para encontrar, 8RT v méd M ELOCIDADE MÉDIA Para encontrar a méda dos quadrados da velocdades fazse: 0 ( ) v P( v) dv v méd Substtundo P (v) e resolvendo através da ntegral (16 em apêndce), encontramos: 3RT ( v ) méd M A raz quadrada de ( v ) méd é a velocdade méda quadrátca v rms : M v rms 3RT ELOCIDADE RMS
11 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 11 A velocdade mas provável vp é aquela na qual P(v) é máxma. Fazendo dp / dt 0 temos um valor máxmo na curva e então, RT v p M ELOCIDADE MAIS PROÁEL Exercíco: Um recpente com gás oxgêno é mantdo na temperatura ambente de (300K). Qual é a fração das moléculas que possuem velocdades no ntervalo de 599 a 601 m/s? A massa molar M do oxgêno é 0,030 kg/mol. Resp.,6x10-3. A massa molar M do oxgêno é 0,030kg/mol. (a) Qual a velocdade méda vméd das moléculas do gás oxgêno a T=300K? (b) Qual é a velocdade méda quadrátca rms em v T=300K? (c) Qual a velocdade mas provável Resp. 445m/s; 483m/s; 395m/s. vp a 300K? 19.8 Os Calores Específcos Molares de um Gás Ideal Energa Interna E nt - Supondo um gás deal monoatômco (hélo, neôno, argôno...), cuja energa nterna esteja assocada apenas as energas de cnétcas de translação de seus átomos, teremos: 3 E nt ( nn A ) K méd ( nn A )( kt )
12 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 1 Usando k R / N A, teremos: E nt 3 nrt GÁS IDEAL MONOATÔMICO A energa nterna de um gás deal é função apenas da temperatura do gás; ela não depende de qualquer outra varável. Calor Específco Molar a olume Constante Na fgura ao lado, o gás é elevada lentamente de T a T T, enquanto a pressão passa de p para p p em um processo a volume constante. O calor é adconado, mas nenhum trabalho é realzado, como mostra o dagrama p-. Neste caso, o calor Q está relaconado com a varação da temperatura por: Q nc v T C v é uma constante chamada calor específco molar a volume constante. Usando a 1ª le da termodnâmca e substtundo Q, teremos: nt E ncvt W
13 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 13 Como o volume é mantdo constante, W 0 e então: E 3 C v nrt Ent nt Sabemos que, de modo que a varação da energa nterna seja da forma E nt 3 nrt nt, logo: 3/ nrt 3 C v R nt, assm, C v 1,5J / mol. K Gás monoatômco Generalzando para qualquer gás deal temos, E nc T nt v, o que nos leva a uma varação de energa do tpo: E nc nt v T Gás deal, qualquer processo. Uma varação na energa nterna Ent de um gás deal confnado depende apenas da varação na temperatura do gás; ela não depende do tpo de processo que produz a varação de temperatura Calores Específcos Molares a olume Constante Molécula Exemplo ( J / mol. K) Monoatômca Datômca Polatômcas Na fgura acma, os três processo, volume constante (1), pressão constante() e sem troca de colar com o meo (3), A varação da energa nterna é a mesma, pos ad temperaturas ncal e fnal são as mesmas. C v Ideal 3 R 1, 5 Real He 1,5 Ar 1,6 Ideal 5 R 0, 8 Real N 0,7 O 0,8 Ideal 3R 4, 9 Real NH 4 9,0 CO 9,7
14 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 14 Calor Específco Molar a Pressão Constante Nesta stuação, a temperatura de um gás deal é elevada de T para T T em um processo a pressão p constante. Calor é adconado e trabalho é realzado levantando o pstão carregado. Este processo é mostrado no dagrama p- abaxo. O valor de Q está assocado com a varação de temperatura T por: Q nc p C p é uma constante chamada calor específco molar a pressão constante. T Usando a 1ª le da termodnâmca, temos: E nt Q W mas E nc nt v T, Q ncpt e W p, logo: ncv T nc pt p, como C e p nrt, chegamos a uma relação entre p C v nc C v v T nc C p R logo: p T nrt C p C v R
15 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 15 Exercíco: Uma bolha de 5,00mol de hélo está submersa a uma certa profunddade na água quando a água (e, portanto o hélo) sofre um aumento de temperatura de 0 0 C a pressão constante. Como resultado, a bolha se expande. O hélo é monoatômco e deal. (a) Quanta energa é adconada ao hélo sob a forma de calor durante esta expansão com o aumento de temperatura? (b) Qual é a varação Ent do hélo durante o aumento de temperatura? (c) Que trabalho W é realzado pelo hélo quando ele se expande contra a pressão da água ao seu redor durante o aumento de temperatura? Respostas: Q 077, 5J ; Ent 146, 5J ; W 831J 19.9 Graus de Lberdade e Calores Específcos Molares. 3 Na últma tabela, verfcou-se que C v R concorda para gases monoatômco, mas falha para gases datômcos e polatômcos. Isto ocorre porque as moléculas com mas de um átomo armazenam energa numa forma dferente do que a cnétca translaconal Teorema da equpartção da energa de James Clerk Maxwell Todo tpo de molécula tem um certo número f de graus de lberdade, que são maneras ndependentes pelas quas uma molécula pode armazenar energa. Cada grau de lberdade tem a ele assocada 1 na méda uma energa de kt por molécula (ou por mol).
16 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 16 Para os gases datômcos e polatômcos, é necessáro 3 refazer os cálculos. Prmero, trocamos a equação Ent nrt por E nt ( f / ) nrt, onde f é o número de graus de lberdade lstado na tabela abaxo. Graus de Lberdade Para áras Moléculas Calores Específcos Graus de Lberdade Molares Prevstos f Molécula Exemplo Translação Rotação Total ( f ) C v R C C Monoatômca He R Datômca O 3 5 R Fazendo sto, podemos prever que: f C v R 4,16 f ( J Gás datômco e polatômco / mol. K) Exercíco: Uma cabana de volume está preenchda com ar (que vamos consderar um gás deal datômco) em uma temperatura ncal T 1. Após acender uma larera, a temperatura do ar aumenta para T. Qual é a varação resultante E na energa nterna do ar na cabana? Resposta: 0 nt p v R 3 5 R 5 7 R Polatômca CH R 4R
17 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr Uma Sugestão da Teora Quântca. Se a temperatura do gás for sufcentemente alta, outro movmento (outro grau de lberdade) pode aparecer, o osclatóro. No caso do O, os átomos começaram a osclar um em relação ao outro, como se conectados por uma mola A Expansão Adabátca de um Gás Ideal Este processo ocorre sem troca de calor entre o sstema e o meo, ou seja, Q 0. Na fgura, o volume de um gás deal é expanddo removendo-se massa do pstão processo adabátco de para f - como mostra o dagrama p-. Neste caso, podemos escrever, p const. Processo Adabátco Onde C / C p.
18 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 18 nrt Num processo adabátco, p p ff. Usando p, podemos elmnar p, fcando com; nrt const. Como nr são constantes, podemos escrever: 1 T const. Processo Adabátco Quando o gás va de um estado ncal até um estado fnal: T 1 1 Tf f Processo Adabátco Expansões Lvres: É um processo adabátco que não envolve trabalho realzado pelo gás ou sobre o gás e nem vara sua energa nterna. Logo as equações anterores não se aplcam. As temperaturas ncal e fnal devem ser a mesma, ou seja, o processo ocorre sobre uma soterma. T T f Expansão Lvre Se não há varação na temperatura, não pode haver varação no produto p, logo: p p Expansão Lvre Exercíco: No segundo exercíco, 1 mol de oxgêno (por hpótese, um gás deal) se expande sotermcamente (a 310K) a partr de um volume ncal 1L a um volume fnal 19L. (a) Qual sera a temperatura fnal se o gás tvesse expanddo adabatcamente até este mesmo volume fnal? O oxgêno é datômco e aqu possu rotação, mas não oscla. (b) Qual sera a temperatura fnal e a pressão fnal se, em vez dsso, o gás tvesse expanddo lvremente para o novo volume a partr de uma pressão de,0pa? Resp. 58K; 310K e 1,3Pa. f f
19 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 19 Resumndo, os quatro processos em gases: 1- Isobárco - Isotérmco 3- Adabátco 4- Isocórco (sovolumétrco) Quatro Processos Especas Trajetóra do gráfco acma Grandeza constante 1 p 3 4 T 1 p, T Tpo de processo Isobárco Alguns resultados especas Ent Q W Ent ncvt (para todas as trajetóras) Q nc pt W p Isotérmco Q W nrt ln Adabátco Isocórco E nt 0 Q 0 W E nt Q Ent ncv W 0 f T
20 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 0 Exercícos do Cap 19 1) Encontre a massa em qulograma de 7,50x10 4 átomos de arsênco, que tem uma massa molecular de 74,9g/mol. 3) Calcule (a) o número de moles e (b) o número de moléculas em 1,00cm 3 de um gás deal numa pressão de 100Pa e numa temperatura de 0K. 5) Uma amostra de gás oxgêno tendo volume de 1000cm 3 a 40 o C e 1,01x10 5 Pa se expande até que seu volume seja de 1500cm 3 e sua pressão seja de 1,06x10 5 Pa. Encontre (a) o número de moles do oxgêno presente e (b) a temperatura fnal da amostra. 7) Uma certa quantdade de um gás deal a 10,0 o C e 100kPa ocupa um volume de,50m 3. (a) Quantos moles do gás estão presentes? (b) Se a pressão for aumentada para 300kPa e a temperatura elevada para 30,0 o C, que volume o gás passará a ocupar? Suponha que não há vazamento. 11) No ntervalo de temperatura de 310K para 330K, a pressão p de um certo gás não deal está relaconada com seu volume e temperatura T por T T p ( 4,9J / K) (0,0066J / K ). Que trabalho é realzado pelo gás se a sua temperatura aumentar de 315K para 35K a pressão constante? 17) A menor temperatura possível no espaço sderal é,7k. Qual é a velocdade rms de moléculas de hdrogêno nesta temperatura? (A massa molar das moléculas de hdrogêno (H ) é dada na tabela 19-1). 19) (a) calcule a velocdade rms de uma molécula de ntrogêno a 0,0 o C. A massa molar das moléculas de (N ) é dada na tabela Em que temperatura a velocdade rms será (b) metade desse valor e (c) o dobro desse valor? 1) Um fexe de moléculas de hdrogêno (H ) está dreconado para uma parede, em um ângulo de 55 o com a normal à parede.
21 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 1 Cada molécula no fexe tem uma velocdade de 1,0km/s e uma massa de 3,3x10-4 g. O fexe atnge a parede sobre uma área de cm, a uma taxa de 10 3 moléculas por segundo. Qual é a pressão do fexe sobre a parede? 4) Determne o valor médo da energa cnétca de translação das moléculas de um gás deal a (a) 0,00 o C e (b) 100 o C. Qual é a energa cnétca de translação méda por mol de um gás deal a (c) 0,00 o C e (d) 100 o C? 7) A densdade atmosférca em uma alttude de 500km está em torno de uma molécula/cm 3. (a) Supondo que o dâmetro da molécula seja de,0x10-8 cm, determne o camnho lvre médo 1 prevsto por. (b)explque se o valor prevsto é sgnfcatvo. d N / 30) A 0 o C e a uma pressão de 750torr, os camnhos lvres médos para o gás argôno (Ar) e o gás ntrogêno (N ) são 6 6 Ar 9,9x10 cm e N 7,5x10 cm. (a) Encontre a razão entre o dâmetro de um átomo de Ar e o de uma molécula de N. Qual é o camnho lvre médo do argôno a (b) 0 o C e 150torr, e (c) 40 o C e 750torr? 3) As velocdades de partículas são as seguntes (N representa o número de partículas que têm velocdade v ): N (m/s) 1,0,0 3,0 4,0 5,0 Quas são (a) v méd, (b) v rms, (c) v p? 39) A fgura abaxo mostra uma dstrbução de velocdades hpotétca para uma a mostra de um gás com N partículas (note que P( v) 0 para velocdades v v0 ). Quas são os valores de (a) av v 0, (b) méd v e (c) rms, (d) qual a v 0 v 0 fração das partículas que têm velocdades entre 1,5v 0 e,0v 0?
22 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 41) A temperatura de,00mol de um gás deal monoatômco aumenta de 15,0K a volume constante. Quas são (a) o trabalho realzado pelo gás, (b) a energa transferda como calor, (c) a varação da energa nterna do gás e (d) a varação da energa cnétca méda por átomo. 44) Quando 0,9J foram adconados como calor a um gás deal partcular, o volume do gás varou de 50,0cm 3 para 100cm 3 enquanto a pressão permaneceu em 1,00atm. (a) De quanto varo a energa nterna do gás? Se a quantdade de gás presente era de,00x10-3 mol, encontre (b) C p e (c) C v. 46) Um mol de um gás deal datômco va de a para c ao longo da trajetóra dagonal na fgura abaxo. Durante a transção, (a) qual é a varação na energa nterna do gás e (b) quanta energa é adconada ao gás como calor? (c) Que calor é necessáro se o gás va de a para c ao longo da trajetóra abc? 49) Quando 1 mol de gás oxgêno (O ) é aquecdo a pressão constante ncando a 0 o C, quanta energa deve ser adconada ao gás como calor para dobrar seu volume? 51) Suponha que 4,00 mol de um gás deal datômco, com rotação molecular, mas sem osclação, sofrem um aumento de temperatura de 60,0K sob pressão constante. Quas são (a) a energa transferda como calor Q, (b) a varação Ent na energa nterna do gás, (c) o trabalho realzado pelo gás e (d) a varação K na energa cnétca translaconal total do gás? 53) Um certo gás ocupa um volume de 4,3L na pressão de 1,atm e uma temperatura de 310K. Ele é comprmdo adabatcamente para um volume de 0,76L. Determne (a) sua pressão fnal e (b) a temperatura fnal, supondo que o gás é deal e que 1, 4.
23 Cap 19: Teora Cnétca dos Gases - Prof. Wladmr 3 55) A fgura abaxo mostra duas trajetóras que podem ser segudas por um gás de um ponto ncal até um ponto fnal f. A trajetóra 1 consste em uma expansão sotérmca (o trabalho tem módulo de 50J), uma expansão adabátca (trabalho com módulo de 40J), uma compressão sotérmca (trabalho 30J em módulo) e então uma compressão adabátca (o trabalho tem módulo de 5J). Qual é a varação na energa nterna do gás se ele for do ponto para o ponto f segundo a trajetóra?
Capítulo 19. A teoria cinética dos gases
 Capítulo 19 A teora cnétca dos gases Neste capítulo, a ntroduzr a teora cnétca dos gases que relacona o momento dos átomos e moléculas com olume, pressão e temperatura do gás. Os seguntes tópcos serão
Capítulo 19 A teora cnétca dos gases Neste capítulo, a ntroduzr a teora cnétca dos gases que relacona o momento dos átomos e moléculas com olume, pressão e temperatura do gás. Os seguntes tópcos serão
19.2 Número de Avogadro mol número de átomos em uma amostra de 12g do carbono-12. Num mol de qualquer substância existem
 Cap. 19 Um gás consiste em átomos que preenchem o volume de seu recipiente. As variáveis volume, pressão e temperatura, são conseqüências do movimento dos átomos. Volume resultado da liberdade dos átomos;
Cap. 19 Um gás consiste em átomos que preenchem o volume de seu recipiente. As variáveis volume, pressão e temperatura, são conseqüências do movimento dos átomos. Volume resultado da liberdade dos átomos;
γ = C P C V = C V + R = q = 2 γ 1 = 2 S gas = dw = W isotermico
 Q1 Um clndro feto de materal com alta condutvdade térmca e de capacdade térmca desprezível possu um êmbolo móvel de massa desprezível ncalmente fxo por um pno. O rao nterno do clndro é r = 10 cm, a altura
Q1 Um clndro feto de materal com alta condutvdade térmca e de capacdade térmca desprezível possu um êmbolo móvel de massa desprezível ncalmente fxo por um pno. O rao nterno do clndro é r = 10 cm, a altura
TEORIA CINÉTICA DOS GASES
 TEORIA CIÉTICA DOS GASES Hpóteses: y t A z ; V ta q = m de uma molécula antes da colsão q = -m depos da colsão q m De todas as moléculas V taˆ V m Atˆ p F A A q t V m ou que pv m em todas as moléculas
TEORIA CIÉTICA DOS GASES Hpóteses: y t A z ; V ta q = m de uma molécula antes da colsão q = -m depos da colsão q m De todas as moléculas V taˆ V m Atˆ p F A A q t V m ou que pv m em todas as moléculas
Unidade II 1. Estudo dos gases e primeira Lei da Termodinâmica
 Governo do Estado do Ro Grande do Norte Secretara de Estado da Educação e da Cultura - SEEC UNIERSIDADE DO ESTADO DO RIO GRANDE DO NORTE - UERN Pró-Retora de Ensno de Graduação PROEG Home Page: http://www.uern.br
Governo do Estado do Ro Grande do Norte Secretara de Estado da Educação e da Cultura - SEEC UNIERSIDADE DO ESTADO DO RIO GRANDE DO NORTE - UERN Pró-Retora de Ensno de Graduação PROEG Home Page: http://www.uern.br
Física do Calor Licenciatura: 6ª Aula (19/08/2015)
 Físca do Calor Lcencatura: 6ª Aula (9/08/05) Pro. Alaro annucc mos, na últma aula: Se um gás sore uma transormação sotérmca, então o trabalho é calculado por: W F I Pd usando que P = KT: W n K T d W( T
Físca do Calor Lcencatura: 6ª Aula (9/08/05) Pro. Alaro annucc mos, na últma aula: Se um gás sore uma transormação sotérmca, então o trabalho é calculado por: W F I Pd usando que P = KT: W n K T d W( T
Parênteses termodinâmico
 Parênteses termodnâmco Lembrando de 1 dos lmtes de valdade da dstrbução de Maxwell-Boltzmann: λ
Parênteses termodnâmco Lembrando de 1 dos lmtes de valdade da dstrbução de Maxwell-Boltzmann: λ
Instituto de Física. FEP112 - FÍSICA II para o Instituto Oceanográfico 1º Semestre de 2009
 .. Unersdade de São aulo Insttuto de Físca FE11 - FÍSIA II para o Insttuto Oceanográco 1º Semestre de 009 Qunta Lsta de Exercícos Temperatura, alor, 1ª Le da Termodnâmca e ropredades dos Gases 1) Um relógo
.. Unersdade de São aulo Insttuto de Físca FE11 - FÍSIA II para o Insttuto Oceanográco 1º Semestre de 009 Qunta Lsta de Exercícos Temperatura, alor, 1ª Le da Termodnâmca e ropredades dos Gases 1) Um relógo
AULA 10 Entropia e a Segunda Lei da Termodinâmica
 UFABC - BC0205 - Prof. Germán Lugones AULA 10 Entropa e a Segunda Le da ermodnâmca Sad Carnot [1796-1832] R. Clausus [1822-1888] W. homson (Lord Kelvn) [1824-1907] Quando um saco de ppocas é aquecdo em
UFABC - BC0205 - Prof. Germán Lugones AULA 10 Entropa e a Segunda Le da ermodnâmca Sad Carnot [1796-1832] R. Clausus [1822-1888] W. homson (Lord Kelvn) [1824-1907] Quando um saco de ppocas é aquecdo em
Gabarito para a prova de 1º Ano e 8ª serie (atual 9º Ano)
 Gabarto para a prova de 1º Ano e 8ª sere (atual 9º Ano) 1. t t c F 5 3 9 ; t c 451 3 5 9 o ; tc 33 C ΔS. a) Δ t 5 s V 4, 1 mnuto possu 6 s, portanto, dos 5 s temos: 8 mnutos (equvale a 48 s) e sobram segundos.
Gabarto para a prova de 1º Ano e 8ª sere (atual 9º Ano) 1. t t c F 5 3 9 ; t c 451 3 5 9 o ; tc 33 C ΔS. a) Δ t 5 s V 4, 1 mnuto possu 6 s, portanto, dos 5 s temos: 8 mnutos (equvale a 48 s) e sobram segundos.
Problemas Propostos. Frações mássicas, volúmicas ou molares. Estequiometria.
 Elementos de Engenhara Químca I II. Frações e Estequometra (problemas resolvdos) Problemas Propostos. Frações másscas, volúmcas ou molares. Estequometra.. Em 5 moles de Benzeno (C 6 H 6 ) quanto é que
Elementos de Engenhara Químca I II. Frações e Estequometra (problemas resolvdos) Problemas Propostos. Frações másscas, volúmcas ou molares. Estequometra.. Em 5 moles de Benzeno (C 6 H 6 ) quanto é que
Dinâmica do Movimento de Rotação
 Dnâmca do Movmento de Rotação - ntrodução Neste Capítulo vamos defnr uma nova grandeza físca, o torque, que descreve a ação gratóra ou o efeto de rotação de uma força. Verfcaremos que o torque efetvo que
Dnâmca do Movmento de Rotação - ntrodução Neste Capítulo vamos defnr uma nova grandeza físca, o torque, que descreve a ação gratóra ou o efeto de rotação de uma força. Verfcaremos que o torque efetvo que
Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a. o resultado do movimento dos átomos e moléculas.
 TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
TEORIA CINÉTICA Neste modelo o gás é estudado de uma forma microscópica, onde a temperatura, a pressão e a energia interna são interpretadas como o resultado do movimento dos átomos e moléculas. Pressão
FIS01183 Turma C/CC Prova da área 2 07/05/2010. Nome: Matrícula: Explicite seu raciocínio e os cálculos realizados em cada passo!
 FIS8 urma C/CC rova da área 7/5/ Nome: Matrícula: Em todas as questões: Cudado com as undades! Explcte seu racocíno e os cálculos realzados em cada passo! BOA ROA! uestão - Laboratóro (, pontos) Na aula
FIS8 urma C/CC rova da área 7/5/ Nome: Matrícula: Em todas as questões: Cudado com as undades! Explcte seu racocíno e os cálculos realzados em cada passo! BOA ROA! uestão - Laboratóro (, pontos) Na aula
F r. PASES 2 a ETAPA TRIÊNIO o DIA GAB. 1 5 FÍSICA QUESTÕES DE 11 A 20
 PSES 2 a ETP TRIÊNIO 2004-2006 1 o DI G. 1 5 FÍSI QUESTÕES DE 11 20 11. onsdere um sstema consttuído por duas partículas. Uma das partículas está ncalmente se movendo e colde nelastcamente com a outra
PSES 2 a ETP TRIÊNIO 2004-2006 1 o DI G. 1 5 FÍSI QUESTÕES DE 11 20 11. onsdere um sstema consttuído por duas partículas. Uma das partículas está ncalmente se movendo e colde nelastcamente com a outra
Cap. 6 - Energia Potencial e Conservação da Energia Mecânica
 Unversdade Federal do Ro de Janero Insttuto de Físca Físca I IGM1 014/1 Cap. 6 - Energa Potencal e Conservação da Energa Mecânca Prof. Elvs Soares 1 Energa Potencal A energa potencal é o nome dado a forma
Unversdade Federal do Ro de Janero Insttuto de Físca Físca I IGM1 014/1 Cap. 6 - Energa Potencal e Conservação da Energa Mecânca Prof. Elvs Soares 1 Energa Potencal A energa potencal é o nome dado a forma
Física do Calor Licenciatura: 14ª Aula (02/10/2015)
 Físca do Calor Lcencatura: 4ª ula (2//25) Pro. lvaro annucc mos, na últma aula: Conceto de Entropa (S): exprme a tendênca de todos os sstemas íscos de evoluírem espontaneamente para uma stuação de maor
Físca do Calor Lcencatura: 4ª ula (2//25) Pro. lvaro annucc mos, na últma aula: Conceto de Entropa (S): exprme a tendênca de todos os sstemas íscos de evoluírem espontaneamente para uma stuação de maor
QiD 6 3ª SÉRIE/PRÉ - VESTIBULAR PARTE 3 QUÍMICA
 PARA A VALIDADE DO QD, AS RESPOSTAS DEVEM SER APRESENTADAS EM FOLHA PRÓPRIA, FORNECIDA PELO COLÉGIO, COM DESENVOLVIMENTO E SEMPRE A TINTA. TODAS AS QUESTÕES DE MÚLTIPLA ESCOLHA DEVEM SER JUSTIFICADAS.
PARA A VALIDADE DO QD, AS RESPOSTAS DEVEM SER APRESENTADAS EM FOLHA PRÓPRIA, FORNECIDA PELO COLÉGIO, COM DESENVOLVIMENTO E SEMPRE A TINTA. TODAS AS QUESTÕES DE MÚLTIPLA ESCOLHA DEVEM SER JUSTIFICADAS.
Física 10 Questões [Difícil]
![Física 10 Questões [Difícil] Física 10 Questões [Difícil]](/thumbs/71/65281624.jpg) Físca Questões [Dfícl] - (UF MG) Um líqudo encontra-se, ncalmente, à temperatura T o, pressão P o e volume o, em um recpente fechado e solado termcamente do ambente, conforme lustra a fgura ao lado. Após
Físca Questões [Dfícl] - (UF MG) Um líqudo encontra-se, ncalmente, à temperatura T o, pressão P o e volume o, em um recpente fechado e solado termcamente do ambente, conforme lustra a fgura ao lado. Após
F-128 Física Geral I. Aula exploratória-11a UNICAMP IFGW
 F-18 Físca Geral I Aula exploratóra-11a UNICAMP IFGW username@f.uncamp.br Momento Angular O momento angular em relação ao ponto O é: r p de uma partícula de momento (Note que a partícula não precsa estar
F-18 Físca Geral I Aula exploratóra-11a UNICAMP IFGW username@f.uncamp.br Momento Angular O momento angular em relação ao ponto O é: r p de uma partícula de momento (Note que a partícula não precsa estar
A teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II A teoria Cinética dos Gases Prof. Bruno Farias Gases Um gás é formado de átomos (isolados
4 Sistemas de partículas
 4 Sstemas de partículas Nota: será feta a segunte convenção: uma letra em bold representa um vector,.e. b b Nesta secção estudaremos a generalzação das les de Newton a um sstema de váras partículas e as
4 Sstemas de partículas Nota: será feta a segunte convenção: uma letra em bold representa um vector,.e. b b Nesta secção estudaremos a generalzação das les de Newton a um sstema de váras partículas e as
Universidade Estadual do Sudoeste da Bahia
 Unversdade Estadual do Sudoeste da Baha Departamento de Cêncas Exatas e Naturas 5 - Rotações, Centro de Massa, Momento, Colsões, Impulso e Torque Físca I Ferrera Índce 1. Movmento Crcular Unformemente
Unversdade Estadual do Sudoeste da Baha Departamento de Cêncas Exatas e Naturas 5 - Rotações, Centro de Massa, Momento, Colsões, Impulso e Torque Físca I Ferrera Índce 1. Movmento Crcular Unformemente
Curso de extensão, MMQ IFUSP, fevereiro/2014. Alguns exercício básicos
 Curso de extensão, MMQ IFUSP, feverero/4 Alguns exercíco báscos I Exercícos (MMQ) Uma grandeza cujo valor verdadero x é desconhecdo, fo medda três vezes, com procedmentos expermentas dêntcos e, portanto,
Curso de extensão, MMQ IFUSP, feverero/4 Alguns exercíco báscos I Exercícos (MMQ) Uma grandeza cujo valor verdadero x é desconhecdo, fo medda três vezes, com procedmentos expermentas dêntcos e, portanto,
Expectativa de respostas da prova de Física Vestibular 2003 FÍSICA. C) Usando a lei das malhas de Kirchhoff temos para a malha mais externa:
 QUESTÃO 1 FÍSICA A) Usando a le dos nós de Krchhoff temos, prmero no nó X: 0 1 0 0 1 50 6 Em seguda, temos no nó Y: 4 5 0 5 4. 188mA como 0 50 5 15 ma. 15 5 B) A le da conseração da carga. C) Usando a
QUESTÃO 1 FÍSICA A) Usando a le dos nós de Krchhoff temos, prmero no nó X: 0 1 0 0 1 50 6 Em seguda, temos no nó Y: 4 5 0 5 4. 188mA como 0 50 5 15 ma. 15 5 B) A le da conseração da carga. C) Usando a
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PC1. [D] Condções ncas do balão: V1 = 10,0 L P1 = 1,00 atm T1 = 27 C + 273 = 300K Condções fnas na troposfera: V2 =? P2 = 0,25 atm T2 = -50,0 C + 273 = 223K SOLUÇÃO PRATIQUE E CASA De acordo com
SOLUÇÃO PC1. [D] Condções ncas do balão: V1 = 10,0 L P1 = 1,00 atm T1 = 27 C + 273 = 300K Condções fnas na troposfera: V2 =? P2 = 0,25 atm T2 = -50,0 C + 273 = 223K SOLUÇÃO PRATIQUE E CASA De acordo com
Cálculo de variações de entropia
 álculo de varações de entropa I stema de um corpo em nteracção com uma onte de calor quecmento rreversível, a volume constante m, c c onte F F onte onte entropa é uma unção de estado e a sua varação é
álculo de varações de entropa I stema de um corpo em nteracção com uma onte de calor quecmento rreversível, a volume constante m, c c onte F F onte onte entropa é uma unção de estado e a sua varação é
18 e 20/Abr/2016 Aulas 12 e 13. Introdução à Física Estatística Postulados Equilíbrio térmico Função de Partição; propriedades termodinâmicas
 01/Abr/2016 Aula 11 Potencas termodnâmcos Energa nterna total Entalpa Energas lvres de Helmholtz e de Gbbs Relações de Maxwell 18 e 20/Abr/2016 Aulas 12 e 13 Introdução à Físca Estatístca Postulados Equlíbro
01/Abr/2016 Aula 11 Potencas termodnâmcos Energa nterna total Entalpa Energas lvres de Helmholtz e de Gbbs Relações de Maxwell 18 e 20/Abr/2016 Aulas 12 e 13 Introdução à Físca Estatístca Postulados Equlíbro
X = 1, se ocorre : VB ou BV (vermelha e branca ou branca e vermelha)
 Estatístca p/ Admnstração II - Profª Ana Cláuda Melo Undade : Probabldade Aula: 3 Varável Aleatóra. Varáves Aleatóras Ao descrever um espaço amostral de um expermento, não especfcamos que um resultado
Estatístca p/ Admnstração II - Profª Ana Cláuda Melo Undade : Probabldade Aula: 3 Varável Aleatóra. Varáves Aleatóras Ao descrever um espaço amostral de um expermento, não especfcamos que um resultado
Universidade Federal do Pampa UNIPAMPA. Teoria Cinética do Gases
 Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
Universidade Federal do Pampa UNIPAMPA Teoria Cinética do Gases Introdução A descrição de um gás por inteiro (descrição macroscópica) pode ser feito estabelecendo as grandezas macroscópicas que caracterizam
3. Um protão move-se numa órbita circular de raio 14 cm quando se encontra. b) Qual o valor da velocidade linear e da frequência ciclotrónica do
 Electromagnetsmo e Óptca Prmero Semestre 007 Sére. O campo magnétco numa dada regão do espaço é dado por B = 4 e x + e y (Tesla. Um electrão (q e =.6 0 9 C entra nesta regão com velocdade v = e x + 3 e
Electromagnetsmo e Óptca Prmero Semestre 007 Sére. O campo magnétco numa dada regão do espaço é dado por B = 4 e x + e y (Tesla. Um electrão (q e =.6 0 9 C entra nesta regão com velocdade v = e x + 3 e
Física Moderna II - FNC376
 Unversdade de São Paulo Insttuto de Físca Físca Moderna II - FNC376 Profa. Márca de Almeda Rzzutto 1o. Semestre de 008 FNC0376 - Fsca Moderna 1 Revsão A organzação da tabela peródca reflete a dstrbução
Unversdade de São Paulo Insttuto de Físca Físca Moderna II - FNC376 Profa. Márca de Almeda Rzzutto 1o. Semestre de 008 FNC0376 - Fsca Moderna 1 Revsão A organzação da tabela peródca reflete a dstrbução
PROVA 2 Cálculo Numérico. Q1. (2.0) (20 min)
 PROVA Cálculo Numérco Q. (.0) (0 mn) Seja f a função dada pelo gráfco abaxo. Para claro entendmento da fgura, foram marcados todos os pontos que são: () raízes; () pontos crítcos; () pontos de nflexão.
PROVA Cálculo Numérco Q. (.0) (0 mn) Seja f a função dada pelo gráfco abaxo. Para claro entendmento da fgura, foram marcados todos os pontos que são: () raízes; () pontos crítcos; () pontos de nflexão.
SC de Física I Nota Q Nota Q2 Nota Q3 NOME: DRE Teste 1
 SC de Físca I - 2017-2 Nota Q1 88888 Nota Q2 Nota Q3 NOME: DRE Teste 1 Assnatura: Questão 1 - [3,5 pontos] Uma partícula de massa m se move sobre uma calha horzontal lsa com velocdade constante de módulo
SC de Físca I - 2017-2 Nota Q1 88888 Nota Q2 Nota Q3 NOME: DRE Teste 1 Assnatura: Questão 1 - [3,5 pontos] Uma partícula de massa m se move sobre uma calha horzontal lsa com velocdade constante de módulo
Teoria Cinética dos Gases
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II Teoria Cinética dos Gases Prof. Bruno Farias Introdução Termodinâmica é o estudo das transformações
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS DISCIPLINA: FÍSICA II Teoria Cinética dos Gases Prof. Bruno Farias Introdução Termodinâmica é o estudo das transformações
CQ110 : Princípios de FQ
 CQ 110 Prncípos de Físco Químca Curso: Farmáca Prof. Dr. Marco Vdott mvdott@ufpr.br 1 soluções eletrolítcas Qual a dferença entre uma solução 1,0 mol L -1 de glcose e outra de NaCl de mesma concentração?
CQ 110 Prncípos de Físco Químca Curso: Farmáca Prof. Dr. Marco Vdott mvdott@ufpr.br 1 soluções eletrolítcas Qual a dferença entre uma solução 1,0 mol L -1 de glcose e outra de NaCl de mesma concentração?
Prof. Oscar. Cap. 20 ENTROPIA E SEGUNDA LEI DA TERMODINÂMICA
 Pro. Oscar Cap. 20 ENROPIA E SEGUNDA LEI DA ERMODINÂMICA 20.1 INRODUÇÃO Os processos que ocorrem num únco sentdo são chamados de rreversíves. A chave para a compreensão de por que processos undreconas
Pro. Oscar Cap. 20 ENROPIA E SEGUNDA LEI DA ERMODINÂMICA 20.1 INRODUÇÃO Os processos que ocorrem num únco sentdo são chamados de rreversíves. A chave para a compreensão de por que processos undreconas
Termo-Estatística Licenciatura: 4ª Aula (08/03/2013)
 Termo-Estatístca Lcencatura: 4ª Aula (08/03/013) Prof. Alvaro Vannucc RELEMBRADO Dstrbução dscreta (hstogramas) x contínua (curvas de dstrbução): Dada uma Função de Dstrbução de Densdade de Probabldade,
Termo-Estatístca Lcencatura: 4ª Aula (08/03/013) Prof. Alvaro Vannucc RELEMBRADO Dstrbução dscreta (hstogramas) x contínua (curvas de dstrbução): Dada uma Função de Dstrbução de Densdade de Probabldade,
Algarismos Significativos Propagação de Erros ou Desvios
 Algarsmos Sgnfcatvos Propagação de Erros ou Desvos L1 = 1,35 cm; L = 1,3 cm; L3 = 1,30 cm L4 = 1,4 cm; L5 = 1,7 cm. Qual destas meddas está correta? Qual apresenta algarsmos com sgnfcado? O nstrumento
Algarsmos Sgnfcatvos Propagação de Erros ou Desvos L1 = 1,35 cm; L = 1,3 cm; L3 = 1,30 cm L4 = 1,4 cm; L5 = 1,7 cm. Qual destas meddas está correta? Qual apresenta algarsmos com sgnfcado? O nstrumento
AEP FISCAL ESTATÍSTICA
 AEP FISCAL ESTATÍSTICA Módulo 11: Varáves Aleatóras (webercampos@gmal.com) VARIÁVEIS ALEATÓRIAS 1. Conceto de Varáves Aleatóras Exemplo: O expermento consste no lançamento de duas moedas: X: nº de caras
AEP FISCAL ESTATÍSTICA Módulo 11: Varáves Aleatóras (webercampos@gmal.com) VARIÁVEIS ALEATÓRIAS 1. Conceto de Varáves Aleatóras Exemplo: O expermento consste no lançamento de duas moedas: X: nº de caras
É o grau de associação entre duas ou mais variáveis. Pode ser: correlacional ou experimental.
 Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Trabalho e Energia. Curso de Física Básica - Mecânica J.R. Kaschny (2005)
 Trabalho e Energa Curso de Físca Básca - Mecânca J.R. Kaschny (5) Lembrando nosso epermento de queda lvre... z z 1 v t 1 z = z - v t - gt ( ) z- z v = g = t Contudo, se consderarmos obtemos: v z z 1 t
Trabalho e Energa Curso de Físca Básca - Mecânca J.R. Kaschny (5) Lembrando nosso epermento de queda lvre... z z 1 v t 1 z = z - v t - gt ( ) z- z v = g = t Contudo, se consderarmos obtemos: v z z 1 t
F-128 Física Geral I. Aula exploratória-11b UNICAMP IFGW
 F-18 Físca Geral I Aula exploratóra-11b UNICAMP IFGW username@f.uncamp.br Momento Angular = r p O momento angular de uma partícula de momento em relação ao ponto O é: p (Note que a partícula não precsa
F-18 Físca Geral I Aula exploratóra-11b UNICAMP IFGW username@f.uncamp.br Momento Angular = r p O momento angular de uma partícula de momento em relação ao ponto O é: p (Note que a partícula não precsa
Ajuste de um modelo linear aos dados:
 Propagação de erros Suponhamos que se pretende determnar uma quantdade Z, a partr da medda drecta das grandezas A, B, C,, com as quas se relacona através de Z = f(a,b,c, ). Se os erros assocados a A, B,
Propagação de erros Suponhamos que se pretende determnar uma quantdade Z, a partr da medda drecta das grandezas A, B, C,, com as quas se relacona através de Z = f(a,b,c, ). Se os erros assocados a A, B,
Física I p/ IO FEP111 ( )
 ísca I p/ IO EP (4300) º Semestre de 00 Insttuto de ísca Unversdade de São Paulo Proessor: Antono Domngues dos Santos E-mal: adsantos@.usp.br one: 309.6886 4 e 6 de setembro Trabalho e Energa Cnétca º
ísca I p/ IO EP (4300) º Semestre de 00 Insttuto de ísca Unversdade de São Paulo Proessor: Antono Domngues dos Santos E-mal: adsantos@.usp.br one: 309.6886 4 e 6 de setembro Trabalho e Energa Cnétca º
Entropia e Segunda Lei da Termodinâmica.
 Cap 20: Entropa e Segunda Le da ermodnâmca - Pro. Wladmr 1 Entropa e Segunda Le da ermodnâmca. 20.1 Introdução Os processos que ocorrem num únco sentdo são chamados de rreversíves. chave para a compreensão
Cap 20: Entropa e Segunda Le da ermodnâmca - Pro. Wladmr 1 Entropa e Segunda Le da ermodnâmca. 20.1 Introdução Os processos que ocorrem num únco sentdo são chamados de rreversíves. chave para a compreensão
Física Geral I - F Aula 12 Momento Angular e sua Conservação. 2º semestre, 2012
 Físca Geral I - F -18 Aula 1 Momento Angular e sua Conservação º semestre, 01 Momento Angular Como vmos anterormente, as varáves angulares de um corpo rígdo grando em torno de um exo fxo têm sempre correspondentes
Físca Geral I - F -18 Aula 1 Momento Angular e sua Conservação º semestre, 01 Momento Angular Como vmos anterormente, as varáves angulares de um corpo rígdo grando em torno de um exo fxo têm sempre correspondentes
Termodinâmica dos Sistemas Abertos Sistemas heterogêneos: Potencial Químico. Grandezas Molares.
 Termoâmca dos Sstemas Abertos Sstemas heterogêneos: Potencal Químco. Grandezas Molares. A aplcação da função Energa Lvre de Gbbs aos sstemas de um únco componente permte a construção dos Dagramas de Fases
Termoâmca dos Sstemas Abertos Sstemas heterogêneos: Potencal Químco. Grandezas Molares. A aplcação da função Energa Lvre de Gbbs aos sstemas de um únco componente permte a construção dos Dagramas de Fases
Fone:
 Prof. Valdr Gumarães Físca para Engenhara FEP111 (4300111) 1º Semestre de 013 nsttuto de Físca- Unversdade de São Paulo Aula 8 Rotação, momento nérca e torque Professor: Valdr Gumarães E-mal: valdrg@f.usp.br
Prof. Valdr Gumarães Físca para Engenhara FEP111 (4300111) 1º Semestre de 013 nsttuto de Físca- Unversdade de São Paulo Aula 8 Rotação, momento nérca e torque Professor: Valdr Gumarães E-mal: valdrg@f.usp.br
Mecânica Estatística. - Leis da Física Macroscópica - Propriedades dos sistemas macroscópicos
 Mecânca Estatístca Tal como a Termodnâmca Clássca, também a Mecânca Estatístca se dedca ao estudo das propredades físcas dos sstemas macroscópcos. Tratase de sstemas com um número muto elevado de partículas
Mecânca Estatístca Tal como a Termodnâmca Clássca, também a Mecânca Estatístca se dedca ao estudo das propredades físcas dos sstemas macroscópcos. Tratase de sstemas com um número muto elevado de partículas
do Semi-Árido - UFERSA
 Unversdade Federal Rural do Sem-Árdo - UFERSA Temperatura e Calor Subêna Karne de Mederos Mossoró, Outubro de 2009 Defnção: A Termodnâmca explca as prncpas propredades damatéra e a correlação entre estas
Unversdade Federal Rural do Sem-Árdo - UFERSA Temperatura e Calor Subêna Karne de Mederos Mossoró, Outubro de 2009 Defnção: A Termodnâmca explca as prncpas propredades damatéra e a correlação entre estas
F-328 Física Geral III
 F-328 Físca Geral III Aula Exploratóra Cap. 26 UNICAMP IFGW F328 1S2014 1 Corrente elétrca e resstênca Defnção de corrente: Δq = dq = t+δt Undade de corrente: 1 Ampère = 1 C/s A corrente tem a mesma ntensdade
F-328 Físca Geral III Aula Exploratóra Cap. 26 UNICAMP IFGW F328 1S2014 1 Corrente elétrca e resstênca Defnção de corrente: Δq = dq = t+δt Undade de corrente: 1 Ampère = 1 C/s A corrente tem a mesma ntensdade
2/Mar/2016 Aula 4. 26/Fev/2016 Aula 3
 6/Fev/016 Aula 3 Calor e Primeira Lei da Termodinâmica Calor e energia térmica Capacidade calorífica e calor específico Calor latente Diagrama de fases para a água Primeira Lei da Termodinâmica Trabalho
6/Fev/016 Aula 3 Calor e Primeira Lei da Termodinâmica Calor e energia térmica Capacidade calorífica e calor específico Calor latente Diagrama de fases para a água Primeira Lei da Termodinâmica Trabalho
4 Critérios para Avaliação dos Cenários
 Crtéros para Avalação dos Cenáros É desejável que um modelo de geração de séres sntétcas preserve as prncpas característcas da sére hstórca. Isto quer dzer que a utldade de um modelo pode ser verfcada
Crtéros para Avalação dos Cenáros É desejável que um modelo de geração de séres sntétcas preserve as prncpas característcas da sére hstórca. Isto quer dzer que a utldade de um modelo pode ser verfcada
Prof. Lorí Viali, Dr.
 Prof. Lorí Val, Dr. vall@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ Em mutas stuações duas ou mas varáves estão relaconadas e surge então a necessdade de determnar a natureza deste relaconamento. A análse
Prof. Lorí Val, Dr. vall@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ Em mutas stuações duas ou mas varáves estão relaconadas e surge então a necessdade de determnar a natureza deste relaconamento. A análse
EXERCÍCIOS DE RECUPERAÇÃO PARALELA 4º BIMESTRE
 EXERCÍCIOS DE RECUERAÇÃO ARALELA 4º BIMESTRE NOME Nº SÉRIE : 2º EM DATA : / / BIMESTRE 4º ROFESSOR: Renato DISCILINA: Físca 1 VISTO COORDENAÇÃO ORIENTAÇÕES: 1. O trabalho deverá ser feto em papel almaço
EXERCÍCIOS DE RECUERAÇÃO ARALELA 4º BIMESTRE NOME Nº SÉRIE : 2º EM DATA : / / BIMESTRE 4º ROFESSOR: Renato DISCILINA: Físca 1 VISTO COORDENAÇÃO ORIENTAÇÕES: 1. O trabalho deverá ser feto em papel almaço
Módulo I Ondas Planas. Reflexão e Transmissão com incidência normal Reflexão e Transmissão com incidência oblíqua
 Módulo I Ondas Planas Reflexão e Transmssão com ncdênca normal Reflexão e Transmssão com ncdênca oblíqua Equações de Maxwell Teorema de Poyntng Reflexão e Transmssão com ncdênca normal Temos consderado
Módulo I Ondas Planas Reflexão e Transmssão com ncdênca normal Reflexão e Transmssão com ncdênca oblíqua Equações de Maxwell Teorema de Poyntng Reflexão e Transmssão com ncdênca normal Temos consderado
( ) ( ) ( ) ( ) Algumas consequências do Primeiro Princípio. Método das misturas (utilizado para determinar calores específicos, em calorimetria)
 Método das msturas (utlzado para determnar calores especícos, em calormetra) Joseph lack (sec. XIII) ( ) ( ) ( ) ( ) W W W W ª Le aplcada a cada um dos subsstemas: No nteror de uma parede adabátca (calorímetro),
Método das msturas (utlzado para determnar calores especícos, em calormetra) Joseph lack (sec. XIII) ( ) ( ) ( ) ( ) W W W W ª Le aplcada a cada um dos subsstemas: No nteror de uma parede adabátca (calorímetro),
GABARITO ERP19. impedância total em pu. impedância linha em pu; impedância carga em pu; tensão no gerador em pu.
 GABARITO ERP9 Questão mpedânca total em pu. mpedânca lnha em pu; mpedânca carga em pu; tensão no gerador em pu. Assm, tem-se que: ( ). Mas, ou seja: : ( ).. Logo: pu. () A mpedânca da carga em pu,, tem
GABARITO ERP9 Questão mpedânca total em pu. mpedânca lnha em pu; mpedânca carga em pu; tensão no gerador em pu. Assm, tem-se que: ( ). Mas, ou seja: : ( ).. Logo: pu. () A mpedânca da carga em pu,, tem
EXPANSÃO TÉRMICA DOS LÍQUIDOS
 Físca II Protocolos das Aulas Prátcas 01 DF - Unversdade do Algarve EXPANSÃO ÉRMICA DOS ÍQUIDOS 1 Resumo Estuda-se a expansão térmca da água destlada e do glcerol utlzando um pcnómetro. Ao aquecer-se,
Físca II Protocolos das Aulas Prátcas 01 DF - Unversdade do Algarve EXPANSÃO ÉRMICA DOS ÍQUIDOS 1 Resumo Estuda-se a expansão térmca da água destlada e do glcerol utlzando um pcnómetro. Ao aquecer-se,
Capítulo 24: Potencial Elétrico
 Capítulo 24: Potencal Energa Potencal Elétrca Potencal Superfíces Equpotencas Cálculo do Potencal a Partr do Campo Potencal Produzdo por uma Carga Pontual Potencal Produzdo por um Grupo de Cargas Pontuas
Capítulo 24: Potencal Energa Potencal Elétrca Potencal Superfíces Equpotencas Cálculo do Potencal a Partr do Campo Potencal Produzdo por uma Carga Pontual Potencal Produzdo por um Grupo de Cargas Pontuas
Calor Específico Molar, Transformações Adiabáticas e Expansão Livre
 Calor Específico Molar, Transformações Adiabáticas e Expansão Livre Revisando Deduzimos que a temperatura determina a energia cinética média (via a velocidade média). O modelo de gás ideal não considera
Calor Específico Molar, Transformações Adiabáticas e Expansão Livre Revisando Deduzimos que a temperatura determina a energia cinética média (via a velocidade média). O modelo de gás ideal não considera
AULA 8 Teoria Cinética dos Gases II
 UFABC - BC0205 Prof. Germán Lugones AULA 8 Teoria Cinética dos Gases II James Clerk Maxwell 1831-1879 A Distribuição de Velocidades Moleculares A velocidade média quadrática V rms nos fornece uma ideia
UFABC - BC0205 Prof. Germán Lugones AULA 8 Teoria Cinética dos Gases II James Clerk Maxwell 1831-1879 A Distribuição de Velocidades Moleculares A velocidade média quadrática V rms nos fornece uma ideia
Física E Semiextensivo V. 3
 Físca E emextensvo V. 3 Exercícos 0) D É mpossível um dspostvo operando em cclos converter ntegralmente calor em trabalho. 0) A segunda le também se aplca aos refrgeradores, pos estes também são máqunas
Físca E emextensvo V. 3 Exercícos 0) D É mpossível um dspostvo operando em cclos converter ntegralmente calor em trabalho. 0) A segunda le também se aplca aos refrgeradores, pos estes também são máqunas
FÍSICO-QUÍMICA I Termodinâmica do Equilíbrio
 UNIVERSIDADE FEDERAL DE MINAS GERAIS Departamento de Químca, ICEx, Setor de Físco-Químca FÍSICO-QUÍMICA I Termodnâmca do Equlíbro Prof. Wellngton Ferrera de MAGALHÃES, Departamento de Químca, e-mal: welmag@ufmg.br
UNIVERSIDADE FEDERAL DE MINAS GERAIS Departamento de Químca, ICEx, Setor de Físco-Químca FÍSICO-QUÍMICA I Termodnâmca do Equlíbro Prof. Wellngton Ferrera de MAGALHÃES, Departamento de Químca, e-mal: welmag@ufmg.br
Expansão livre de um gás ideal
 Expansão lvre de um gás deal (processo não quase-estátco, logo, rreversível) W=0 na expansão lvre (P e = 0) Paredes adabátcas a separar o gás das vznhanças Q = 0 ª Le U gás = Q + W = 0 U = U Para um gás
Expansão lvre de um gás deal (processo não quase-estátco, logo, rreversível) W=0 na expansão lvre (P e = 0) Paredes adabátcas a separar o gás das vznhanças Q = 0 ª Le U gás = Q + W = 0 U = U Para um gás
Termodinâmica dos Sistemas Abertos Sistemas heterogêneos: Potencial Químico. Grandezas Molares.
 Termodnâmca dos Sstemas Abertos Sstemas heterogêneos: Potencal Químco. Grandezas Molares. A aplcação da função Energa Lvre de Gbbs aos sstemas de um únco componente permte a construção dos Dagramas de
Termodnâmca dos Sstemas Abertos Sstemas heterogêneos: Potencal Químco. Grandezas Molares. A aplcação da função Energa Lvre de Gbbs aos sstemas de um únco componente permte a construção dos Dagramas de
Leis de conservação em forma integral
 Les de conservação em forma ntegral J. L. Balño Departamento de Engenhara Mecânca Escola Poltécnca - Unversdade de São Paulo Apostla de aula Rev. 10/08/2017 Les de conservação em forma ntegral 1 / 26 Sumáro
Les de conservação em forma ntegral J. L. Balño Departamento de Engenhara Mecânca Escola Poltécnca - Unversdade de São Paulo Apostla de aula Rev. 10/08/2017 Les de conservação em forma ntegral 1 / 26 Sumáro
1. Obtenha o modelo de ½ carro:
 Lsta Aulas Prátcas de Sclab 1 Suspensão vecular Modelo de ½ de carro 1. Obtenha o modelo de ½ carro: v H A v A l A l M, J v M = 200 kg; J = 512 kgm 2 ; l A = 0,8 m; l = 0,8 m; k A = 10.000 N/m; k = 10.000
Lsta Aulas Prátcas de Sclab 1 Suspensão vecular Modelo de ½ de carro 1. Obtenha o modelo de ½ carro: v H A v A l A l M, J v M = 200 kg; J = 512 kgm 2 ; l A = 0,8 m; l = 0,8 m; k A = 10.000 N/m; k = 10.000
Radiação Térmica Processos, Propriedades e Troca de Radiação entre Superfícies (Parte 2)
 Radação Térmca Processos, Propredades e Troca de Radação entre Superfíces (Parte ) Obetvo: calcular a troca por radação entre duas ou mas superfíces. Essa troca depende das geometras e orentações das superfíces,
Radação Térmca Processos, Propredades e Troca de Radação entre Superfíces (Parte ) Obetvo: calcular a troca por radação entre duas ou mas superfíces. Essa troca depende das geometras e orentações das superfíces,
TERMODINÂMICA QUÍMICA
 TERMODINÂMICA QUÍMICA CAPÍTULO DA QUÍMICA FÍSICA QUE ESTUDA A VARIAÇÃO DE ENERGIA DOS SISTEMAS ENVOLVIDOS EM REACÇÕES QUÍMICAS QUALQUER SISTEMA EVOLUI ESPONTANEAMENTE DE UM ESTADO DE MAIOR ENERGIA PARA
TERMODINÂMICA QUÍMICA CAPÍTULO DA QUÍMICA FÍSICA QUE ESTUDA A VARIAÇÃO DE ENERGIA DOS SISTEMAS ENVOLVIDOS EM REACÇÕES QUÍMICAS QUALQUER SISTEMA EVOLUI ESPONTANEAMENTE DE UM ESTADO DE MAIOR ENERGIA PARA
1º Exame de Mecânica Aplicada II
 1º Exame de Mecânca Aplcada II Este exame é consttuído por 4 perguntas e tem a duração de três horas. Justfque convenentemente todas as respostas apresentando cálculos ntermédos. Responda a cada pergunta
1º Exame de Mecânca Aplcada II Este exame é consttuído por 4 perguntas e tem a duração de três horas. Justfque convenentemente todas as respostas apresentando cálculos ntermédos. Responda a cada pergunta
6/Mar/2013 Aula 7 Entropia Variação da entropia em processos reversíveis Entropia e os gases ideais
 6/Mar/01 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
6/Mar/01 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
Prof. Lorí Viali, Dr.
 Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ 1 É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Prof. Lorí Val, Dr. val@mat.ufrgs.br http://www.mat.ufrgs.br/~val/ 1 É o grau de assocação entre duas ou mas varáves. Pode ser: correlaconal ou expermental. Numa relação expermental os valores de uma das
Física II FEP 112 ( ) 1º Semestre de Instituto de Física - Universidade de São Paulo. Professor: Valdir Guimarães
 Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
Física II FEP 11 (4300110) 1º Semestre de 01 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104(05) Aula 1 Temperatura e Teoria
TEORIA DE ERROS * ERRO é a diferença entre um valor obtido ao se medir uma grandeza e o valor real ou correto da mesma.
 UNIVERSIDADE FEDERAL DO ESPÍRITO SANTO CENTRO DE CIÊNCIAS EXATAS DEPARTAMENTO DE FÍSICA AV. FERNANDO FERRARI, 514 - GOIABEIRAS 29075-910 VITÓRIA - ES PROF. ANDERSON COSER GAUDIO FONE: 4009.7820 FAX: 4009.2823
UNIVERSIDADE FEDERAL DO ESPÍRITO SANTO CENTRO DE CIÊNCIAS EXATAS DEPARTAMENTO DE FÍSICA AV. FERNANDO FERRARI, 514 - GOIABEIRAS 29075-910 VITÓRIA - ES PROF. ANDERSON COSER GAUDIO FONE: 4009.7820 FAX: 4009.2823
Interpretação Molecular da Temperatura de um Gás Ideal
 Interpretação Molecular da Temperatura de um Gás Ideal Já vimos que a pressão está relacionada com a energia cinética média das moléculas. Agora relacionaremos a temperatura à uma descrição microscópica
Interpretação Molecular da Temperatura de um Gás Ideal Já vimos que a pressão está relacionada com a energia cinética média das moléculas. Agora relacionaremos a temperatura à uma descrição microscópica
UFABC - BC Prof. Germán Lugones. AULA 9 Teoria Cinética dos Gases III
 UFABC - BC0205 - Prof. Germán Lugones AULA 9 Teoria Cinética dos Gases III Graus de liberdade e Calores Específicos Molares A previsão de que c v = 3/2 R concorda com o experimento para gases monoatômicos,
UFABC - BC0205 - Prof. Germán Lugones AULA 9 Teoria Cinética dos Gases III Graus de liberdade e Calores Específicos Molares A previsão de que c v = 3/2 R concorda com o experimento para gases monoatômicos,
Flambagem. Cálculo da carga crítica via MDF
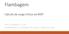 Flambagem Cálculo da carga crítca va MDF ROF. ALEXANDRE A. CURY DEARTAMENTO DE MECÂNICA ALICADA E COMUTACIONAL Flambagem - Cálculo da carga crítca va MDF Nas aulas anterores, vmos como avalar a carga crítca
Flambagem Cálculo da carga crítca va MDF ROF. ALEXANDRE A. CURY DEARTAMENTO DE MECÂNICA ALICADA E COMUTACIONAL Flambagem - Cálculo da carga crítca va MDF Nas aulas anterores, vmos como avalar a carga crítca
Eventos coletivamente exaustivos: A união dos eventos é o espaço amostral.
 DEFINIÇÕES ADICIONAIS: PROBABILIDADE Espaço amostral (Ω) é o conjunto de todos os possíves resultados de um expermento. Evento é qualquer subconjunto do espaço amostral. Evento combnado: Possu duas ou
DEFINIÇÕES ADICIONAIS: PROBABILIDADE Espaço amostral (Ω) é o conjunto de todos os possíves resultados de um expermento. Evento é qualquer subconjunto do espaço amostral. Evento combnado: Possu duas ou
Física Geral II. Aula 1 - Teoria cinética dos gases. D. Valin 1. Universidade do Estado de Mato Grosso. Sinop-MT, April 25, 2017
 Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
Física Geral II Aula 1 - Teoria cinética dos gases D. Valin 1 1 Faculdade de Ciências Exatas - FACET Universidade do Estado de Mato Grosso Sinop-MT, April 25, 2017 D. Valin (Universidade do Estado de Mato
Capítulo 26: Corrente e Resistência
 Capítulo 6: Corrente e esstênca Cap. 6: Corrente e esstênca Índce Corrente Elétrca Densdade de Corrente Elétrca esstênca e esstvdade Le de Ohm Uma Vsão Mcroscópca da Le de Ohm Potênca em Crcutos Elétrcos
Capítulo 6: Corrente e esstênca Cap. 6: Corrente e esstênca Índce Corrente Elétrca Densdade de Corrente Elétrca esstênca e esstvdade Le de Ohm Uma Vsão Mcroscópca da Le de Ohm Potênca em Crcutos Elétrcos
Um mol é o número de átomos em uma amostra de 12 g de carbono 12.
 NOTA DE AULA 07 UNIVERSIDADE CATÓLICA DE GOIÁS DEPARTAMENTO DE MATEMÁTICA E FÍSICA Disciplina: FÍSICA GERAL E EXPERIMENTAL II (MAF 0) Coordenação: Prof. Dr. Elias Calixto Carrijo CAPÍTULO 0 A TEORIA CINÉTICA
NOTA DE AULA 07 UNIVERSIDADE CATÓLICA DE GOIÁS DEPARTAMENTO DE MATEMÁTICA E FÍSICA Disciplina: FÍSICA GERAL E EXPERIMENTAL II (MAF 0) Coordenação: Prof. Dr. Elias Calixto Carrijo CAPÍTULO 0 A TEORIA CINÉTICA
V.1. Introdução. Reações Químicas.
 V.1. Introdução. Reações Químcas. V. Balanços Materas a Processos com Reação Químca Uma equação químca acertada ornece muta normação. Por exemplo, a reação de síntese do metanol: CO (g) + 3H (g) CH 3 OH
V.1. Introdução. Reações Químcas. V. Balanços Materas a Processos com Reação Químca Uma equação químca acertada ornece muta normação. Por exemplo, a reação de síntese do metanol: CO (g) + 3H (g) CH 3 OH
Isostática 2. Noções Básicas da Estática
 Isostátca. Noções Báscas da Estátca Rogéro de Olvera Rodrgues .1. Força Força desgna um agente capa de modfcar o estado de repouso ou de movmento de um determnado corpo. É uma grandea vetoral e, como tal,
Isostátca. Noções Báscas da Estátca Rogéro de Olvera Rodrgues .1. Força Força desgna um agente capa de modfcar o estado de repouso ou de movmento de um determnado corpo. É uma grandea vetoral e, como tal,
Figura 8.1: Distribuição uniforme de pontos em uma malha uni-dimensional. A notação empregada neste capítulo para avaliação da derivada de uma
 Capítulo 8 Dferencação Numérca Quase todos os métodos numércos utlzados atualmente para obtenção de soluções de equações erencas ordnáras e parcas utlzam algum tpo de aproxmação para as dervadas contínuas
Capítulo 8 Dferencação Numérca Quase todos os métodos numércos utlzados atualmente para obtenção de soluções de equações erencas ordnáras e parcas utlzam algum tpo de aproxmação para as dervadas contínuas
Regressão Múltipla. Parte I: Modelo Geral e Estimação
 Regressão Múltpla Parte I: Modelo Geral e Estmação Regressão lnear múltpla Exemplos: Num estudo sobre a produtvdade de trabalhadores ( em aeronave, navos) o pesqusador deseja controlar o número desses
Regressão Múltpla Parte I: Modelo Geral e Estmação Regressão lnear múltpla Exemplos: Num estudo sobre a produtvdade de trabalhadores ( em aeronave, navos) o pesqusador deseja controlar o número desses
2 - Análise de circuitos em corrente contínua
 - Análse de crcutos em corrente contínua.-corrente eléctrca.-le de Ohm.3-Sentdos da corrente: real e convenconal.4-fontes ndependentes e fontes dependentes.5-assocação de resstêncas; Dvsores de tensão;
- Análse de crcutos em corrente contínua.-corrente eléctrca.-le de Ohm.3-Sentdos da corrente: real e convenconal.4-fontes ndependentes e fontes dependentes.5-assocação de resstêncas; Dvsores de tensão;
11/Mar/2016 Aula 7 Entropia Variação da entropia em processos reversíveis Entropia e os gases ideais
 11/Mar/016 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
11/Mar/016 Aula 7 Entropia ariação da entropia em processos reversíveis Entropia e os gases ideais Entropia no ciclo de Carnot e em qualquer ciclo reversível ariação da entropia em processos irreversíveis
3 Animação de fluidos com SPH
 3 Anmação de fludos com SPH O SPH (Smoothed Partcle Hydrodynamcs) é um método Lagrangeano baseado em partículas, proposto orgnalmente para smulação de problemas astrofíscos por Gngold e Monaghan (1977)
3 Anmação de fludos com SPH O SPH (Smoothed Partcle Hydrodynamcs) é um método Lagrangeano baseado em partículas, proposto orgnalmente para smulação de problemas astrofíscos por Gngold e Monaghan (1977)
CONCEITOS INICIAIS DE ESTATÍSTICA MÓDULO 2 DISTRIBUIÇÃO DE FREQÜÊNCIA - ELEMENTOS Prof. Rogério Rodrigues
 CONCEITOS INICIAIS DE ESTATÍSTICA MÓDULO DISTRIBUIÇÃO DE FREQÜÊNCIA - ELEMENTOS Prof. Rogéro Rodrgues I) TABELA PRIMITIVA E DISTRIBUIÇÃO DE FREQÜÊNCIA : No processo de amostragem, a forma de regstro mas
CONCEITOS INICIAIS DE ESTATÍSTICA MÓDULO DISTRIBUIÇÃO DE FREQÜÊNCIA - ELEMENTOS Prof. Rogéro Rodrgues I) TABELA PRIMITIVA E DISTRIBUIÇÃO DE FREQÜÊNCIA : No processo de amostragem, a forma de regstro mas
% Al 48 b) Alumínio que fica em solução. Precisamos calcular o equilíbrio da alumina com Al e O no aço:
 1a Verfcação Refno dos s I EEIMVR-UFF, Setembro de 11 Prova A 1. Calcule o valor de γ no ferro, a 17 o C, com os dados fornecdos na prova. Vmos em aula que o 1% G e o γ estão relaconados através de 1%
1a Verfcação Refno dos s I EEIMVR-UFF, Setembro de 11 Prova A 1. Calcule o valor de γ no ferro, a 17 o C, com os dados fornecdos na prova. Vmos em aula que o 1% G e o γ estão relaconados através de 1%
Capítulo 21 Teoria Cinética dos Gases
 apítulo eora nétca dos Gases Hallyday Resnck a Edção Eercícos e robleas oléculas de ar estão contnuaente atngndo esta págna Estas bolas de têns eculares são tão pequenas que sera precso cerca de delas
apítulo eora nétca dos Gases Hallyday Resnck a Edção Eercícos e robleas oléculas de ar estão contnuaente atngndo esta págna Estas bolas de têns eculares são tão pequenas que sera precso cerca de delas
Dinâmica Estocástica. Instituto de Física, outubro de Tânia Tomé - Din Estoc
 Dnâmca Estocástca Insttuto de Físca, outubro de 2016 1 Dnâmcas estocástcas para o modelos defndos em redes Sstema defndo em um retculado em um espaço de d dmensões Exemplo: rede quadrada d=2 em que cada
Dnâmca Estocástca Insttuto de Físca, outubro de 2016 1 Dnâmcas estocástcas para o modelos defndos em redes Sstema defndo em um retculado em um espaço de d dmensões Exemplo: rede quadrada d=2 em que cada
Nenhum desses processos violaria a Lei de Conservação de Energia se ocorresse no sentido inverso.
 SEGUNDA LEI E ENROPIA Processos rreversíves e entroa Alguns rocessos termodnâmcos num só sentdo. Exemlos: - grão de mlho se transformando em oca; - caneca de café esfrando - exansão lvre de um gás. ocorrem
SEGUNDA LEI E ENROPIA Processos rreversíves e entroa Alguns rocessos termodnâmcos num só sentdo. Exemlos: - grão de mlho se transformando em oca; - caneca de café esfrando - exansão lvre de um gás. ocorrem
CAPÍTULO 2 - Estatística Descritiva
 INF 16 Prof. Luz Alexandre Peternell CAPÍTULO - Estatístca Descrtva Exercícos Propostos 1) Consderando os dados amostras abaxo, calcular: méda artmétca, varânca, desvo padrão, erro padrão da méda e coefcente
INF 16 Prof. Luz Alexandre Peternell CAPÍTULO - Estatístca Descrtva Exercícos Propostos 1) Consderando os dados amostras abaxo, calcular: méda artmétca, varânca, desvo padrão, erro padrão da méda e coefcente
25/Fev/2015 Aula 2. 20/Fev/2015 Aula 1
 /Fe/15 Aula 1 Temperatura e a Lei Zero da Termodinâmica Sistema Termodinâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação dos gases ideais 5/Fe/15 Aula Teoria Cinética
/Fe/15 Aula 1 Temperatura e a Lei Zero da Termodinâmica Sistema Termodinâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação dos gases ideais 5/Fe/15 Aula Teoria Cinética
Estatística II Antonio Roque Aula 18. Regressão Linear
 Estatístca II Antono Roque Aula 18 Regressão Lnear Quando se consderam duas varáves aleatóras ao mesmo tempo, X e Y, as técncas estatístcas aplcadas são as de regressão e correlação. As duas técncas estão
Estatístca II Antono Roque Aula 18 Regressão Lnear Quando se consderam duas varáves aleatóras ao mesmo tempo, X e Y, as técncas estatístcas aplcadas são as de regressão e correlação. As duas técncas estão
Capítulo 9. Colisões. Recursos com copyright incluídos nesta apresentação:
 Capítulo 9 Colsões Recursos com copyrght ncluídos nesta apresentação: http://phet.colorado.edu Denremos colsão como uma nteração com duração lmtada entre dos corpos. Em uma colsão, a orça externa resultante
Capítulo 9 Colsões Recursos com copyrght ncluídos nesta apresentação: http://phet.colorado.edu Denremos colsão como uma nteração com duração lmtada entre dos corpos. Em uma colsão, a orça externa resultante
