Distúrbios Ácido Básicos
|
|
|
- Augusto Guimarães Chagas
- 6 Há anos
- Visualizações:
Transcrição
1 Distúrbios Ácido Básicos Prof. Vinicius Coca Fisioterapeuta Especialista em Pneumofuncional Mestre em Terapia Intensiva - SOBRATI Mestre em Ensino na Saúde - UGF
2 Equilíbrio Acidobásico O Equilíbrio acidobásico refere- se aos mecanismos fisiológicos que mantêm a concentração de ions hidrogênio nos líquidos corpóreos Ação conjunta dos sistemas tampão, pulmões e rins
3 Formação e Tamponamento do H + Ácidos Substâncias capazes de doar ions H + Base Substâncias capazes de aceitar os H + de outras substâncias
4 Potencial Hidrogeniônio O ph de uma solução é o logarikmo negakvo da akvidade dos ions H +. Representa, na maioria dos casos, a medida da concetração dos ions H + ph = -log(h + ) ou seja quanto H +, ph e quanto H +, ph
5 Ácidos Fixos Ácidos Sulfúrico Ácido Fosfórico Ácido Clorídrico Ácido Lático
6 Ácido Carbônico Ácidos Voláteis METABOLISMO AERÓBIO CO 2 + H 2 O H 2 CO 3 HCO 3- + H +
7 Sistema Tampão Em condições agudas, o ph arterial acima de 7,8 e abaixo de 6,9 são incompakveis com a vida Solução tampão é uma mistura de componentes ácidos e básicos que anula as alterações do ph quando um ácido ou uma base é adicionado a ela
8 Tamponamento Isoídrico TECIDO Hb + H + H + Hb H + Hb Hb H 2 CO 3 VASOS SANGUINEOS H + + HCO 3 -
9 Tamponamento Isoídrico H 2 CO 3 CO 2 H 2 O PULMÃO
10 Equação de Handerson- Hasselbalch Considera a proporção entre as moleculas ácidas não dissociadas (H 2 CO 3 ) e os ânions básicos (HCO 3- ) ph = 6,1 + log [HCO 3- ] PCO 2 x 0,03
11 Papel dos pulmões no equilíbrio A/B Excreção do CO 2 e H 2 O por meio da ventilação Eliminação diária de cerca de a mmol/l
12 Papel dos rins no equilíbrio A/B Excreção direta de H + Retenção ou excreção de HCO 3 -
13 Distúrbios Acidobásicos Os rins mantém uma concentração arterial de bicarbonato em torno de 24mEq/L. A venklação mantem uma PaCO 2 de aproximadamente 40mmHg phα = controle renal da [HCO 3 ] controle pulmonar da PaCO 2
14 Interpretação da GSA em 3 passos!"#"$%&'(&)*+",-./!,$"!"#$%&'()$*+,-".+'*%/,/0'"1/* 20',.'()$*3'*0$,4&.'*/*5.3%'1'()$* 2"1/+.6'()$*3$7*3/70.$7* /76/%'3$7*!!!" "$2@'(61"0&"<$A=>:?;!$"&B31B(&'"1"0+"!=/=<;$>$" CD"=E(F12&)*+"" GD"H5(0+#I&61" JD"!816" CD",= G CD"M16%(+" KB(N@B(+! CD"AO0(+!!!" "!0123(4(5&)*+"01"6(37&)816"01" 9:;!<="!>!/:/?:" 85$9:/* ;'< = *>*?@&&AB* 2+.3/&.'*B%'0/*C6A*>*DEFG* ;$1H77.$*>*=E?*$:*I*D&&$,JK* L' M *>*FF?*$:*I*FN@&&$,JKE*7."1$&H1.+$* 8' MM *.$".O'3$*IFE?&&$,JK** GD"<B&0(1231"$#&! JD";16K+63&"&+"" "0&"L(= G! GD,+NK126&)816! JD"<&K"$2(O2(5+! GD"9+3@66(+! JD",@'5(+" (+2(P&0+!
15 Padrões de Normalidade ph Sanguíneo 7,35 a 7,45 PaCO 2 35 a 45 HCO 3 22 a 26
16 Distúrbios Acidobásicos Distúrbios Simples Acidose Respiratória Acidose Metabólica Alcalose Respiratória Alcalose Metabólica Distúrbios Duplos Acidose Mista Alcalose Mista Distúrbios Mistos
17 Distúrbio Simples Componente Respiratório Componente não Respiratório CO 2 HCO 3 - ph Acidose Metabólica
18 Distúrbio Simples Componente Respiratório Componente não Respiratório CO 2 HCO 3 - ph Alcalose Metabólica
19 Distúrbio Simples Componente Respiratório Componente não Respiratório CO 2 HCO 3 - ph Acidose Respiratoria
20 Distúrbio Simples Componente Respiratório Componente não Respiratório CO 2 HCO 3 - ph Alcalose Respiratória
21 Causas de acidose respiratória Pulmões normais Depressão do SNC (anestesias, narcókcos, sedação, analgésicos) Doenças neuromusculares (poliomielite, miastenia, Guillain- Barré) TRM, TCE ou trauma torácico Distúrbios restrikvos extrapulmonares graves (obesidade, cifoescolises) Pulmões anormais DPOC Obstruções agudas de vias aéreas
22 Causas de alcalose respiratória Ansiedade / Dor Sepse / Febre Drogas eskmulantes Lesão SNC Hipobarismo Pulmões normais Pulmões anormais Asma Aguda EsKmulação de recptores irritantes do parênquima pulmonar (pneumonia, EAP) Doença Vascular Pulmonar Outras HipervenKlação iatrogênica (VM)
23 Causas de acidose metabólica Hiato aniônico elevado Ganho de ácido produzido metabólicamente (acidose lakca, cetoacidose, insuficiência renal) Ingestão de ácidos (intoxicação AAS, metanol, eklenoglicerol, etc) Hiato aniônico normal Perda gastrointesknal de HCO 3 - (diarreia, fistula pancreákca) Perda tubular renal Ingestão de cloreto de amônia Hiperalimentação intravenosa
24 Hiato Aniônio A lei da eletroneutralidade estabelece que o número total de cargas posikvas deve ser igual ao numero total de cargas negakvas nos líquidos corpóreos Porém as concentrações plasmáticas dos cátions (Na + e K + ) são superiores as dos ânions (Cl - e HCO 3- ) Hiato aniônico = [Na + ] ([Cl - ] + [HCO 3- ]) Normalidade de 9 a 14mEq/L
25 Causas de alcalose metabólica Vômitos Uso diurékcos Hipocloremia Hipovolemia Perda de ions H + Retenção de ions HCO 3 - Infusão ou ingestão de bicarbonato de sódio ou outras bases (ankácidos)
26 Distúrbios Duplos Componente Respiratório Componente não Respiratório CO 2 HCO 3 - ph Alcalose Mista
27 Distúrbios Duplos Componente Respiratório Componente não Respiratório CO 2 HCO 3 - ph Acidose Mista
28 Respostas Compensatórias Na presença de um distúrbio acidobásico, o organismo desencadeia uma resposta compensatória com o objekvo de normalizar o ph
29 Respostas Compensatórias Distúrbio respiratória Metabolica CO 2 ph HCO 3 CO 2 ph HCO 3 HCO 3 ph CO 2 HCO 3 ph CO 2 Compensação renal respiratória
30 Passo a passo Categorização do ph entre alcalose, acidose, ou normalidade; Determinar se existe alteração respiratória ou metabólica, se é aguda ou crônica, compensatória ou mista; Avaliar o componente causal do distúrbio do ph; Checar o grau de compensação por parte do componente não causal, e verificar se a compensação encontra-se dentro da resposta esperada, ou se é um distúrbio acidobásico misto;
31 Graus de compensação acidobásica Componente não causal ph Classificação Dentro da faixa normal Anormal Distúrbio não compensado Fora da faixa normal, na direção esperada Anormal Distúrbio parcialmente compensado Fora da faixa normal, na direção esperada Normal Distúrbio compensado
32 Regra Prática Nos casos de compensação, se o ph estiver no lado ácido, ou seja entre 7,35 a 7,39, o componente que seria o causador da acidose geralmente é a causa primária do distúrbio. Nos casos de compensação, se o ph estiver no lado alcalino, ou seja entre 7,41 e 7,45, o componente que seria o causador da alcalose geralmente é a causa primária do distúrbio.
33 Resposta compensatória esperada na Ac.Resp.Aguda Na acidose respiratória aguda é possivel quankficar a resposta compensatória esperada uklizando- se a regra do 1 para 10 O HCO 3 - irá aumentar 1mlEq/L para cada elevação de 10mmHg na PaCO 2 acima de 40mmHg [HCO 3- ]esperada = 24 + {(PaCO 2 atual 40)/10}
34 Resposta compensatória esperada na Ac.Resp.Aguda Paciente com acidose respiratória aguda PaCO 2 = 60mmHg HCO 3 - = 31mEq/L Se colocarmos os dados na fórmula, veremos que o HCO 3 - esperado para compensar a desordem respiratória é de 26mEq/L. O valor atual é 31mEq/L, ou seja, mais elevado. Este resultado indica que alem da acidose respiratória, também há um alcaloe metabólica, caracterizando um distúrbio acidobásico misto
35 Resposta compensatória esperada na Ac.Resp.Crônica Na acidose respiratória aguda é possivel quankficar a resposta compensatória esperada uklizando- se a regra do 4 para 10 O HCO 3 - irá aumentar 4mlEq/L para cada elevação de 10mmHg na PaCO 2 acima de 40mmHg [HCO 3- ]esperada = {(PaCO 2 atual 40)/10}
36 Resposta compensatória esperada na Ac.Resp.Crônica Paciente com acidose respiratória crônica PaCO 2 = 60mmHg HCO 3 - = 31mEq/L Se colocarmos os dados na fórmula, veremos que o HCO 3 - esperado para compensar a desordem respiratória é de 32mEq/L. O valor atual é 31mEq/L, ou seja, extremamente próximo do valor esperado, evidneciando que a compensação renal esta correta, e não há evidência de distúrbio acidobásico secundário
37 Resposta compensatória esperada na Al.Resp.Aguda Na alcalose respiratória aguda é possivel quankficar a resposta compensatória esperada uklizando- se a regra do 2 para 10 O HCO 3 - irá diminuir 2mlEq/L para cada diminuição de 10mmHg na PaCO 2 abaixo de 40mmHg [HCO 3- ]esperada = 24 2 x {(40 PaCO 2 atual)/10}
38 Resposta compensatória esperada na Al.Resp.Aguda Na prákca essa mudança fisico- quimica raramente resulta em uma HCO 3 - menor que 18mEq/L, pois não há valores negakvos de PaCO2. Dessa forma, qualquer valor de HCO 3 - menor que 18mEq/L indica a coexistência de acidose metabólica
39 Resposta compensatória esperada na Al.Resp.Crônica Na alcalose respiratória crônica é possivel quankficar a resposta compensatória esperada uklizando- se a regra do 5 para 10 O HCO 3 - irá diminuir 5mlEq/L para cada diminuição de 10mmHg na PaCO 2 abaixo de 40mmHg [HCO 3- ]esperada = 24 5 x {(40 PaCO 2 atual)/10} Aceita- se uma variação de +/ 2
40 Resposta compensatória esperada na acidose metabólica PaCO 2 esperada = (1,5 x [HCO 3- ]) + 8 Aceita variação de +/- 2
41 Resposta compensatória esperada na alcalose metabólica PaCO 2 esperada = (0,7 x [HCO 3- ]) + 20 Aceita variação de +/- 5
42 Excesso de base Consiste no número de meq de ácido ou base necessário para Ktular 1 litro de sangue a um ph de 7,4, a 37 o C, se a PaCO 2 eskver em 40mmHg dessa forma é preciso considerar que: O EB normal varia entre 2 e +2mEq/L; EB > +2mEq/L indica ganho de base ou perda de ácido por causas não respiratórias; EB < 2mEq/L indica diminuição de base ou excesso de ácido por causas não respiratórias;
43 PaCO2 aumentada? Sim Não G(A-a) aumentado? G(A-a) aumentado? Não Sim Sim Boa resposta ao O2? Não ;"< =- Não 0&.&12")345"$-678-9:2'(- Sim!"#$%&'(")*+,$-".$)*/*-!"#$%&'(")*+,$-
Profª Allana dos Reis Corrêa Enfermeira SAMU BH Mestranda em Enfermagem UFMG
 Gasometria Arterial Profª Allana dos Reis Corrêa Enfermeira SAMU BH Mestranda em Enfermagem UFMG Gasometria arterial Por quê a Gasometria se temos o Oxímetro de pulso e Capnógrafo? Gasometria Arterial
Gasometria Arterial Profª Allana dos Reis Corrêa Enfermeira SAMU BH Mestranda em Enfermagem UFMG Gasometria arterial Por quê a Gasometria se temos o Oxímetro de pulso e Capnógrafo? Gasometria Arterial
Petr Soares de Alencar DISTÚRBIOS DO EQUILÍBRIO ÁCIDO BASE
 Petr Soares de Alencar DISTÚRBIOS DO EQUILÍBRIO ÁCIDO BASE GASOMETRIA ARTERIAL GASOMETRIA ARTERIAL Paciente com os seguintes valores na gasometria arterial: ph = 7,08; HCO - 3 = 10mEq/litro; PCO 2 = 35
Petr Soares de Alencar DISTÚRBIOS DO EQUILÍBRIO ÁCIDO BASE GASOMETRIA ARTERIAL GASOMETRIA ARTERIAL Paciente com os seguintes valores na gasometria arterial: ph = 7,08; HCO - 3 = 10mEq/litro; PCO 2 = 35
Lembrando. Ácidos são quaisquer substâncias capazes de ceder H+ Exemplos: ácido clorídrico, ácido lático, ácido úrico
 GASOMETRIA Lembrando Ácidos são quaisquer substâncias capazes de ceder H+ Exemplos: ácido clorídrico, ácido lático, ácido úrico Lembrando Bases são quaisquer substâncias capazes de captar H+ Exemplos:
GASOMETRIA Lembrando Ácidos são quaisquer substâncias capazes de ceder H+ Exemplos: ácido clorídrico, ácido lático, ácido úrico Lembrando Bases são quaisquer substâncias capazes de captar H+ Exemplos:
21/07/14. Processos metabólicos. Conceitos Básicos. Respiração. Catabolismo de proteínas e ácidos nucleicos. Catabolismo de glicídios
 Prof. Dr. Adriano Bonfim Carregaro Medicina Veterinária FZEA USP www.anestesia.vet.br Processos metabólicos Respiração Catabolismo de proteínas e ácidos nucleicos Ácidos acético, sulfúrico, fosfórico e
Prof. Dr. Adriano Bonfim Carregaro Medicina Veterinária FZEA USP www.anestesia.vet.br Processos metabólicos Respiração Catabolismo de proteínas e ácidos nucleicos Ácidos acético, sulfúrico, fosfórico e
Equilíbrio ácido-básico. Monitor: Tarcísio Alves Teixeira Professor: Guilherme Soares Fisiologia Veterinária / MFL / IB / UFF
 Equilíbrio ácido-básico Monitor: Tarcísio Alves Teixeira Professor: Guilherme Soares Fisiologia Veterinária / MFL / IB / UFF O que são Ácidos e Bases Ácido: substância que, em solução, é capaz de doar
Equilíbrio ácido-básico Monitor: Tarcísio Alves Teixeira Professor: Guilherme Soares Fisiologia Veterinária / MFL / IB / UFF O que são Ácidos e Bases Ácido: substância que, em solução, é capaz de doar
EXAMES COMPLEMENTARES GASOMETRIA GASOMETRIA ARTERIAL EQUILÍBRIO ÁCIDO - BÁSICO EQUILÍBRIO ÁCIDO - BÁSICO
 GASOMETRIA ARTERIAL EXAMES COMPLEMENTARES GASOMETRIA A gasometria arterial é um exame invasivo que mede as concentrações de oxigênio, a ventilação e o estado ácido-básico. Prof. Carlos Cezar I. S. Ovalle
GASOMETRIA ARTERIAL EXAMES COMPLEMENTARES GASOMETRIA A gasometria arterial é um exame invasivo que mede as concentrações de oxigênio, a ventilação e o estado ácido-básico. Prof. Carlos Cezar I. S. Ovalle
Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent
![Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent](/thumbs/50/27125458.jpg) Equilíbrio ácido-básico A concentração de H no FEC é mantida dentro de um limite extremamente estreito: 40 nmol/l = 1.000.000 menor que a Concentração dos outros íons!! [H] tem profundo efeito nos eventos
Equilíbrio ácido-básico A concentração de H no FEC é mantida dentro de um limite extremamente estreito: 40 nmol/l = 1.000.000 menor que a Concentração dos outros íons!! [H] tem profundo efeito nos eventos
SISTEMA TAMPÃO NOS ORGANISMOS ANIMAIS
 SISTEMA TAMPÃO NOS ORGANISMOS ANIMAIS Regulação do Equilíbrio Ácido-Básico ph = Potencial Hidrogeniônico Concentração de H + Quanto mais ácida uma solução maior sua concentração de H + e menor o seu ph
SISTEMA TAMPÃO NOS ORGANISMOS ANIMAIS Regulação do Equilíbrio Ácido-Básico ph = Potencial Hidrogeniônico Concentração de H + Quanto mais ácida uma solução maior sua concentração de H + e menor o seu ph
ph do sangue arterial = 7.4
 Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
Distúrbios do equilíbrio ácido básico. Fisiologia do equilíbrio ácido básico (6,80) 7,35 7,45 (7,80)
 Renato Ribeiro Nogueira Ferraz Mestre e Doutor em Nefrologia pela Universidade Federal de São Paulo UNIFESP, com Pós Doutorado também em Nefrologia pela mesma Universidade. Organizador do livro Nefrologia:
Renato Ribeiro Nogueira Ferraz Mestre e Doutor em Nefrologia pela Universidade Federal de São Paulo UNIFESP, com Pós Doutorado também em Nefrologia pela mesma Universidade. Organizador do livro Nefrologia:
ALCALOSES 1. Introdução HA H + +A -.
 ALCALOSES 1 Introdução Acidose e alcalose referem-se aos mecanismos fisiopatológicos que causam acúmulo de ácido ou base no organismo. Os termos acidemia e alcalemia referem-se ao ph no fluido extracelular.
ALCALOSES 1 Introdução Acidose e alcalose referem-se aos mecanismos fisiopatológicos que causam acúmulo de ácido ou base no organismo. Os termos acidemia e alcalemia referem-se ao ph no fluido extracelular.
GASOMETRIA ARTERIAL- ARTIGO DE REVISÃO. interpretação
 TRABALHO DE CONCLUSÃO DE CURSO GASOMETRIA ARTERIAL- ARTIGO DE REVISÃO interpretação Dra Leticia Godoy Dias Sanderson Porto Ferreira, fevereiro 2012 Resumo O objetivo do estudo é identificar na literatura
TRABALHO DE CONCLUSÃO DE CURSO GASOMETRIA ARTERIAL- ARTIGO DE REVISÃO interpretação Dra Leticia Godoy Dias Sanderson Porto Ferreira, fevereiro 2012 Resumo O objetivo do estudo é identificar na literatura
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012. Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICOPRÁTICO 5ª AULA TEÓRICOPRÁTICA RESOLUÇÃO
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICOPRÁTICO 5ª AULA TEÓRICOPRÁTICA RESOLUÇÃO
Manutenção do ph do sangue
 Manutenção do ph do sangue Muitos dos fluidos biológicos, quer no interior, quer no exterior das células, apresentam intervalos de ph muito apertados, ou seja um valor de ph praticamente constante, uma
Manutenção do ph do sangue Muitos dos fluidos biológicos, quer no interior, quer no exterior das células, apresentam intervalos de ph muito apertados, ou seja um valor de ph praticamente constante, uma
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA EQUILÍBRIO ÁCIDO-BASE NO ORGANISMO HUMANO REGULAÇÃO DA CONCENTRAÇÃO HIDROGENIÓNICA - IMPORTÂNCIA
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA EQUILÍBRIO ÁCIDO-BASE NO ORGANISMO HUMANO REGULAÇÃO DA CONCENTRAÇÃO HIDROGENIÓNICA - IMPORTÂNCIA
ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões
![ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões](/thumbs/60/44575873.jpg) Regulação do ph dos líquidos Regulação do ph dos líquidos ph = log[ ] LEC =, ±, (, mm) ph , Alcalose Ojetivo: Manutenção do ph sistêmico na faixa de normalidade. ph arterial entre, e, [H]
Regulação do ph dos líquidos Regulação do ph dos líquidos ph = log[ ] LEC =, ±, (, mm) ph , Alcalose Ojetivo: Manutenção do ph sistêmico na faixa de normalidade. ph arterial entre, e, [H]
Tampão. O que é? MISTURA DE UM ÁCIDO FRACO COM SUA BASE CONJUGADA, QUE ESTABILIZA O P H DE UMA SOLUÇÃO
 Tampões biológicos Relembrar os conceitos de ácido e base (Brönsted-Lowry), ph, pka; Compreender a importância do ph na manutenção da estrutura tridimensional das biomoléculas; Conhecer os valores de ph
Tampões biológicos Relembrar os conceitos de ácido e base (Brönsted-Lowry), ph, pka; Compreender a importância do ph na manutenção da estrutura tridimensional das biomoléculas; Conhecer os valores de ph
D) Como seria a correção desse distúrbio? A correção seria atuar na causa e proporcionar eliminação de CO2 por aumento da ventilação alveolar.
 Exercícios de Gasometria Arterial - Gabarito Docente responsável: Profª Paula C Nogueira Para as situações abaixo, responda às seguintes questões: Considere os seguintes valores de referência: ph: 7,35-7,45
Exercícios de Gasometria Arterial - Gabarito Docente responsável: Profª Paula C Nogueira Para as situações abaixo, responda às seguintes questões: Considere os seguintes valores de referência: ph: 7,35-7,45
DISTÚRBIO HIDRO- ELETROLÍTICO E ÁCIDO-BÁSICO. Prof. Fernando Ramos Gonçalves -Msc
 DISTÚRBIO HIDRO- ELETROLÍTICO E ÁCIDO-BÁSICO Prof. Fernando Ramos Gonçalves -Msc Distúrbio hidro-eletrolítico e ácido-básico Distúrbios da regulação da água; Disnatremias; Alterações do potássio; Acidoses
DISTÚRBIO HIDRO- ELETROLÍTICO E ÁCIDO-BÁSICO Prof. Fernando Ramos Gonçalves -Msc Distúrbio hidro-eletrolítico e ácido-básico Distúrbios da regulação da água; Disnatremias; Alterações do potássio; Acidoses
Regulação renal do equilíbrio ácido base
 Universidade de São Paulo Faculdade de Medicina de Ribeirão Preto Informática Biomédica Regulação renal do equilíbrio ácido base Gabriela Silva Borges O que é ácido e base? Função Química conjunto de compostos
Universidade de São Paulo Faculdade de Medicina de Ribeirão Preto Informática Biomédica Regulação renal do equilíbrio ácido base Gabriela Silva Borges O que é ácido e base? Função Química conjunto de compostos
Homeostase do ph. Ácidos e Bases. HA H + + A - HCl H + + Cl - H 2 CO 3 H + + HCO H + + NH 3. Escala de ph
 Frederico Gueiros Filho Formação: Bacharelado em Biologia - UERJ Mestrado em Genética - UFRJ Doutorado - Harvard Medical School - EUA Pós-doutorado - Harvard, Depto. MCB - EUA Interesse de pesquisa: Mecanismo
Frederico Gueiros Filho Formação: Bacharelado em Biologia - UERJ Mestrado em Genética - UFRJ Doutorado - Harvard Medical School - EUA Pós-doutorado - Harvard, Depto. MCB - EUA Interesse de pesquisa: Mecanismo
Alterações do equilíbrio hídrico Alterações do equilíbrio hídrico Desidratação Regulação do volume hídrico
 Regulação do volume hídrico Alteração do equilíbrio hídrico em que a perda de líquidos do organismo é maior que o líquido ingerido Diminuição do volume sanguíneo Alterações do equilíbrio Hídrico 1. Consumo
Regulação do volume hídrico Alteração do equilíbrio hídrico em que a perda de líquidos do organismo é maior que o líquido ingerido Diminuição do volume sanguíneo Alterações do equilíbrio Hídrico 1. Consumo
Fisiologia do Sistema Urinário
 Sistema Urinário Fisiologia do Sistema Urinário Funções do sistema urinário Anatomia fisiológica do aparelho urinário Formação de urina pelos rins Filtração glomerular Reabsorção e secreção tubular Equilíbrio
Sistema Urinário Fisiologia do Sistema Urinário Funções do sistema urinário Anatomia fisiológica do aparelho urinário Formação de urina pelos rins Filtração glomerular Reabsorção e secreção tubular Equilíbrio
Universidade Federal Rural de Pernambuco
 Universidade Federal Rural de Pernambuco Departamento de Morfologia e Fisiologia Animal Área de Biofísica Medindo o potencial Hidrogeniônico Prof. Romildo Nogueira 1. Entendendo as bases A manutenção da
Universidade Federal Rural de Pernambuco Departamento de Morfologia e Fisiologia Animal Área de Biofísica Medindo o potencial Hidrogeniônico Prof. Romildo Nogueira 1. Entendendo as bases A manutenção da
Fisioterapia em Terapia Intensiva
 Ácidos e Bases Fisioterapia em Terapia Intensiva ÁCIDO moléculas que contem átomos de hidrogênio capazes de liberar íons de hidrogênio. HCl H + + Cl BASE molécula que pode aceitar um íon de hidrogênio
Ácidos e Bases Fisioterapia em Terapia Intensiva ÁCIDO moléculas que contem átomos de hidrogênio capazes de liberar íons de hidrogênio. HCl H + + Cl BASE molécula que pode aceitar um íon de hidrogênio
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO. Profa. Dra. Celene Fernandes Bernardes
 TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
TRANSTORNOS ÁCIDOS-BÁSICOS
 TRANSTORNOS ÁCIDOS-BÁSICOS Marcos Mendes Disciplina de Fisiologia FMABC Conceitos ph = 7,40 0,04 (compatível com a vida 6,8 a 7,8) ph < 7,36 ACIDEMIA ph > 7,44 ALCALEMIA pco2 (a) = (40 4) mmhg TRANST.
TRANSTORNOS ÁCIDOS-BÁSICOS Marcos Mendes Disciplina de Fisiologia FMABC Conceitos ph = 7,40 0,04 (compatível com a vida 6,8 a 7,8) ph < 7,36 ACIDEMIA ph > 7,44 ALCALEMIA pco2 (a) = (40 4) mmhg TRANST.
BIOQUÍMICA II SISTEMAS TAMPÃO NOS ORGANISMOS ANIMAIS 3/1/2012
 BIOQUÍMICA II Professora: Ms. Renata Fontes Medicina Veterinária 3º Período O conteúdo de Bioquímica II utiliza os conhecimentos adquiridos referentes ao estudo do metabolismo celular e fenômenos físicos
BIOQUÍMICA II Professora: Ms. Renata Fontes Medicina Veterinária 3º Período O conteúdo de Bioquímica II utiliza os conhecimentos adquiridos referentes ao estudo do metabolismo celular e fenômenos físicos
Considerações Gerais sobre Hemogasometria
 Considerações Gerais sobre Hemogasometria Exame hemogasométrico Grande importância na avaliação do equilíbrio ácido-básico Diagnóstico e prognóstico de inúmeras enfermidades Cuidados importantes para obtenção
Considerações Gerais sobre Hemogasometria Exame hemogasométrico Grande importância na avaliação do equilíbrio ácido-básico Diagnóstico e prognóstico de inúmeras enfermidades Cuidados importantes para obtenção
GASOMETRIA ARTERIAL GASOMETRIA. Indicações 11/09/2015. Gasometria Arterial
 GASOMETRIA ARTERIAL Processo pelo qual é feita a medição das pressões parciais dos gases sangüíneos, a partir do qual é possível o cálculo do PH sangüíneo, o que reflete o equilíbrio Ácido-Básico 2 GASOMETRIA
GASOMETRIA ARTERIAL Processo pelo qual é feita a medição das pressões parciais dos gases sangüíneos, a partir do qual é possível o cálculo do PH sangüíneo, o que reflete o equilíbrio Ácido-Básico 2 GASOMETRIA
Reconhecendo os agravos clínicos em urgência e emergência. Prof.º Enfº. Diógenes Trevizan
 Reconhecendo os agravos clínicos em urgência e emergência Prof.º Enfº. Diógenes Trevizan Cuidando do cliente com agravos respiratórios em urgência e emergência Introdução Em atenção às urgências, a insuficiência
Reconhecendo os agravos clínicos em urgência e emergência Prof.º Enfº. Diógenes Trevizan Cuidando do cliente com agravos respiratórios em urgência e emergência Introdução Em atenção às urgências, a insuficiência
GASOMETRIA ph E GASES SANGUÍNEOS
 GASOMETRIA ph E GASES SANGUÍNEOS CBHPM 4.03.0.01-6 AMB 8.01.096-5 CBHPM 4.14.01.16-6 Sinonímia: Gasometria de Siggaard-Andersen. Teste de exercício em ergômetro com realização de gasometria arterial. Gasometria
GASOMETRIA ph E GASES SANGUÍNEOS CBHPM 4.03.0.01-6 AMB 8.01.096-5 CBHPM 4.14.01.16-6 Sinonímia: Gasometria de Siggaard-Andersen. Teste de exercício em ergômetro com realização de gasometria arterial. Gasometria
INSUFICIÊNCIA RESPIRATÓRIA
 Clínica Médica e Cirúrgica I INSUFICIÊNCIA RESPIRATÓRIA João Adriano de Barros Disciplina de Pneumologia Universidade Federal do Paraná Objetivos da Aula... Importância da IRA devido a sua alta mortalidade
Clínica Médica e Cirúrgica I INSUFICIÊNCIA RESPIRATÓRIA João Adriano de Barros Disciplina de Pneumologia Universidade Federal do Paraná Objetivos da Aula... Importância da IRA devido a sua alta mortalidade
Testes de Consumo máximo de Oxigênio (Vo 2 máx) Fisiologia Do Esforço Prof.Dra. Bruna Oneda 2016
 Testes de Consumo máximo de Oxigênio (Vo 2 máx) Fisiologia Do Esforço Prof.Dra. Bruna Oneda 2016 Tamponamento Substâncias que se dissociam em solução e liberam H + são denominadas ácidos Compostos que
Testes de Consumo máximo de Oxigênio (Vo 2 máx) Fisiologia Do Esforço Prof.Dra. Bruna Oneda 2016 Tamponamento Substâncias que se dissociam em solução e liberam H + são denominadas ácidos Compostos que
QUÍMICA ANALÍTICA APLICADA - QUI 111 SOLUÇÃO TAMPÃO Natal/RN SOLUÇÃO TAMPÃO
 QUÍMICA ANALÍTICA APLICADA - QUI 111 SOLUÇÃO TAMPÃO Prof a. Nedja Suely Fernandes 2014.1 Natal/RN SOLUÇÃO TAMPÃO É uma solução que resiste a uma modificação da concentração de íon hidrogênio ou de ph,
QUÍMICA ANALÍTICA APLICADA - QUI 111 SOLUÇÃO TAMPÃO Prof a. Nedja Suely Fernandes 2014.1 Natal/RN SOLUÇÃO TAMPÃO É uma solução que resiste a uma modificação da concentração de íon hidrogênio ou de ph,
Livro Eletrônico Aula 00 Questões Comentadas de Fisioterapia - Terapia Intensiva
 Livro Eletrônico Questões Comentadas de Fisioterapia - Terapia Intensiva Professor: Fábio Cardoso 1 APRESENTAÇÃO.... 2 2 -QUESTÕES COMENTADAS...5 RESUMO....7 LISTA DE QUESTÕES SEM COMENTÁRIOS... 7 GABARITO...8
Livro Eletrônico Questões Comentadas de Fisioterapia - Terapia Intensiva Professor: Fábio Cardoso 1 APRESENTAÇÃO.... 2 2 -QUESTÕES COMENTADAS...5 RESUMO....7 LISTA DE QUESTÕES SEM COMENTÁRIOS... 7 GABARITO...8
Sistema Respiratório. Superior. Língua. Inferior
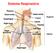 Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
BIOQUÍMICA PARA ODONTO
 BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
Fundamentos de Química Profa. Janete Yariwake. Equilíbrio químico em solução aquosa. Soluções-tampão. Soluções tampão
 Equilíbrio químico em solução aquosa Soluções-tampão 1 Soluções tampão Definição: soluções que podem resistir a variações significativas de ph. (se adicionamos quantidades pequenas de ácidos fortes ou
Equilíbrio químico em solução aquosa Soluções-tampão 1 Soluções tampão Definição: soluções que podem resistir a variações significativas de ph. (se adicionamos quantidades pequenas de ácidos fortes ou
Equilíbrio Ácido básico Enfa. Profa. Dra. Paula C Nogueira
 UNIVERSIDADE DE SÃO PAULO Escola de Enfermagem Departamento de Enfermagem Médico-Cirúrgica Equilíbrio Ácido básico Enfa. Profa. Dra. Paula C Nogueira Objetivos Conhecer e identificar os distúrbios ácido-básico
UNIVERSIDADE DE SÃO PAULO Escola de Enfermagem Departamento de Enfermagem Médico-Cirúrgica Equilíbrio Ácido básico Enfa. Profa. Dra. Paula C Nogueira Objetivos Conhecer e identificar os distúrbios ácido-básico
Profa Maria Clorinda EV/UFG
 Escola de Veterinária e Zootecnia da UFG Departamento de Medicina Veterinária Maria Clorinda Soares Fioravanti (clorinda@vet.ufg.br) Disciplina: Clínica Médica de Pequenos Animais Profa Maria Clorinda
Escola de Veterinária e Zootecnia da UFG Departamento de Medicina Veterinária Maria Clorinda Soares Fioravanti (clorinda@vet.ufg.br) Disciplina: Clínica Médica de Pequenos Animais Profa Maria Clorinda
Fisiologia Renal. Mecanismos tubulares I ESQUEMAS SOBRE FISIOLOGIA RENAL. Profa. Ms Ana Maria da Silva Curado Lins Universidade Católica de Goiás
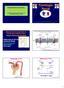 ESQUEMAS SOBRE FISIOLOGIA RENAL. Mecanismos tubulares I Fisiologia Renal Profa. Ms Ana Maria da Silva Curado Lins Universidade Católica de Goiás Mecanismos de manipulação do filtrado pelos túbulos renais:
ESQUEMAS SOBRE FISIOLOGIA RENAL. Mecanismos tubulares I Fisiologia Renal Profa. Ms Ana Maria da Silva Curado Lins Universidade Católica de Goiás Mecanismos de manipulação do filtrado pelos túbulos renais:
ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes
 ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes ph = potencial hidrogeniônico ph = -log [H + ] Sorenson 1909 A escala de ph é logarítma; portanto, quando duas
ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes ph = potencial hidrogeniônico ph = -log [H + ] Sorenson 1909 A escala de ph é logarítma; portanto, quando duas
VI SEMINÁRIO. Tema: BIOQUÍMICA DO EQUILÍBRIO ÁCIDO-BASE. Subtemas: Bioquímica do equilíbrio ácido-base Acidoses e alcaloses.
 EQUILÍBRIO ÁCIDOBASE Actas Bioq. 2007, 8: 185192 VI SEMINÁRIO Tema: BIOQUÍMICA DO EQUILÍBRIO ÁCIDOBASE Subtemas: Bioquímica do equilíbrio ácidobase Acidoses e alcaloses Intervenientes: Docentes convidados:
EQUILÍBRIO ÁCIDOBASE Actas Bioq. 2007, 8: 185192 VI SEMINÁRIO Tema: BIOQUÍMICA DO EQUILÍBRIO ÁCIDOBASE Subtemas: Bioquímica do equilíbrio ácidobase Acidoses e alcaloses Intervenientes: Docentes convidados:
Aula-8Gasometria Arterial. Profª Tatiani
 Aula-8Gasometria Arterial Profª Tatiani Gasometria Arterial A gasometria arterial é um exame invasivo que mede as concentrações de oxigênio, a ventilação e o estado ácido-básico. Tipicamente, os valores
Aula-8Gasometria Arterial Profª Tatiani Gasometria Arterial A gasometria arterial é um exame invasivo que mede as concentrações de oxigênio, a ventilação e o estado ácido-básico. Tipicamente, os valores
Sistema tampão. Um sistema tampão é constituído por um ácido fraco e sua base conjugada HA A - + H +
 Sistema tampão Um sistema tampão é constituído por um ácido fraco e sua base conjugada HA A - + H + Quando se adiciona um ácido forte na solução de ácido fraco HX X - + H + HA A - H + X - H + H + HA A
Sistema tampão Um sistema tampão é constituído por um ácido fraco e sua base conjugada HA A - + H + Quando se adiciona um ácido forte na solução de ácido fraco HX X - + H + HA A - H + X - H + H + HA A
Desequilíbrio Ácido básico Enfa. Profa. Dra. Paula C Nogueira
 UNIVERSIDADE DE SÃO PAULO Escola de Enfermagem Departamento de Enfermagem Médico-Cirúrgica Desequilíbrio Ácido básico Enfa. Profa. Dra. Paula C Nogueira Objetivos Conhecer e identificar os distúrbios ácido-básico
UNIVERSIDADE DE SÃO PAULO Escola de Enfermagem Departamento de Enfermagem Médico-Cirúrgica Desequilíbrio Ácido básico Enfa. Profa. Dra. Paula C Nogueira Objetivos Conhecer e identificar os distúrbios ácido-básico
Interpretação da Gasometria Arterial. Dra Isabel Cristina Machado Carvalho
 Interpretação da Gasometria Arterial Dra Isabel Cristina Machado Carvalho Distúrbios Ácido-Base O reconhecimento dos mecanismos homeostáticos que controlam o equilíbrio ácido-base é fundamental, pois os
Interpretação da Gasometria Arterial Dra Isabel Cristina Machado Carvalho Distúrbios Ácido-Base O reconhecimento dos mecanismos homeostáticos que controlam o equilíbrio ácido-base é fundamental, pois os
Avaliação e tratamento das alterações do equilibrio ácido-base
 Avaliação e tratamento das alterações do equilibrio ácido-base - Regras práticas - Prof. Doutor António Vaz Carneiro Disciplina de Introdução à Clínica Disciplina de Medicina I Centro de Estudos de Medicina
Avaliação e tratamento das alterações do equilibrio ácido-base - Regras práticas - Prof. Doutor António Vaz Carneiro Disciplina de Introdução à Clínica Disciplina de Medicina I Centro de Estudos de Medicina
Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária. Pelotas, 11 de novembro de 2015
 Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Pelotas, 11 de novembro de 2015 Carlos Loures Pires Josiane de Oliveira Feijó Escolha do artigo Cálcio Homeostase Hormônios
Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Pelotas, 11 de novembro de 2015 Carlos Loures Pires Josiane de Oliveira Feijó Escolha do artigo Cálcio Homeostase Hormônios
ESTUDO DIRIGIDO SOBRE FISIOLOGIA RENAL. Abaixo, encontram-se os pontos que precisam ser estudados na área de Fisiologia Renal.
 1 ESTUDO DIRIGIDO SOBRE FISIOLOGIA RENAL Abaixo, encontram-se os pontos que precisam ser estudados na área de Fisiologia Renal. Anatomia funcional do rim As diferenças entre a circulação cortical e medular
1 ESTUDO DIRIGIDO SOBRE FISIOLOGIA RENAL Abaixo, encontram-se os pontos que precisam ser estudados na área de Fisiologia Renal. Anatomia funcional do rim As diferenças entre a circulação cortical e medular
Soluções. Prof a. Jennifer
 Soluções Prof a. Jennifer Conceito Qualitativo Uma solução é formada por dois componentes, denominados dispersante (ou solvente) e o componente disperso (ou soluto). Sólidos em líquidos Líquidos em líquidos
Soluções Prof a. Jennifer Conceito Qualitativo Uma solução é formada por dois componentes, denominados dispersante (ou solvente) e o componente disperso (ou soluto). Sólidos em líquidos Líquidos em líquidos
Experimento 1: Efeito do íon comum equilíbrio de ionização da amônia
 Experimento Deslocamento de equilíbrios químicos (Princípio de Le Chatelier) Objetivo: Estudar e compreender alguns fatores que deslocam equilíbrios químicos. Experimento 1: Efeito do íon comum equilíbrio
Experimento Deslocamento de equilíbrios químicos (Princípio de Le Chatelier) Objetivo: Estudar e compreender alguns fatores que deslocam equilíbrios químicos. Experimento 1: Efeito do íon comum equilíbrio
Ácidos, bases e sistemas tampão
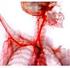 Ácidos, bases e sistemas tampão Ionização da água A água pura tem uma baixa concentração de iões hidrónio (H 3 O + ) e uma igual concentração de iões hidróxido (OH - ) Os ácidos são dadores de protões
Ácidos, bases e sistemas tampão Ionização da água A água pura tem uma baixa concentração de iões hidrónio (H 3 O + ) e uma igual concentração de iões hidróxido (OH - ) Os ácidos são dadores de protões
Biologia. Identidade dos Seres Vivos. Sistema Respiratório Humano. Prof.ª Daniele Duó
 Biologia Identidade dos Seres Vivos Prof.ª Daniele Duó Fisiologia do Sistema Respiratório Pode ser interpretada como um processo de trocas gasosas entre o organismo e o meio, ou conjunto de reações químicas
Biologia Identidade dos Seres Vivos Prof.ª Daniele Duó Fisiologia do Sistema Respiratório Pode ser interpretada como um processo de trocas gasosas entre o organismo e o meio, ou conjunto de reações químicas
Biofísica renal. Estrutura e função dos rins
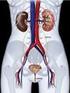 Biofísica renal Estrutura e função dos rins Múltiplas funções do sistema renal Regulação do balanço hídrico e eletrolítico (volume e osmolaridade) Regulação do equilíbrio ácidobásico (ph) Excreção de produtos
Biofísica renal Estrutura e função dos rins Múltiplas funções do sistema renal Regulação do balanço hídrico e eletrolítico (volume e osmolaridade) Regulação do equilíbrio ácidobásico (ph) Excreção de produtos
Como interpretar a Gasometria de Sangue Arterial
 Como interpretar a Gasometria de Sangue Arterial Sequência de interpretação e estratificação de risco 08/01/2013 Daniela Carvalho Objectivos da Tertúlia Sequência de interpretação da GSA - Método dos 3
Como interpretar a Gasometria de Sangue Arterial Sequência de interpretação e estratificação de risco 08/01/2013 Daniela Carvalho Objectivos da Tertúlia Sequência de interpretação da GSA - Método dos 3
DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BÁSICO REVISÃO DE LITERATURA
 DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BÁSICO REVISÃO DE LITERATURA SOUZA, Camila Carolina Discente do Curso de Medicina Veterinária da FAMED Garça SACCO, Soraya Regina ZAPPA, Vanessa Docente do Curso de Medicina
DISTÚRBIOS DO EQUILÍBRIO ÁCIDO-BÁSICO REVISÃO DE LITERATURA SOUZA, Camila Carolina Discente do Curso de Medicina Veterinária da FAMED Garça SACCO, Soraya Regina ZAPPA, Vanessa Docente do Curso de Medicina
Ciclo Respiratório Normal. Como Respiramos? Prova de Função Pulmonar. Que diz a espirometria? Espirômetro. Sensível ao volume.
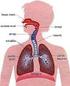 Ciclo Respiratório Normal Como Respiramos? Prova de Função Pulmonar Que diz a espirometria? Espirômetro Sensível ao volume Sensível ao fluxo 1 FEV1 / FVC % Visão Geral da Hematose O índice espirométrico
Ciclo Respiratório Normal Como Respiramos? Prova de Função Pulmonar Que diz a espirometria? Espirômetro Sensível ao volume Sensível ao fluxo 1 FEV1 / FVC % Visão Geral da Hematose O índice espirométrico
Equilíbrio Ácido-base. Controle de ph por meio de soluções tampão
 Equilíbrio Ácido-base Controle de ph por meio de soluções tampão Conceitos Soluções tampão = são sistemas aquosos que tendem a resistir a mudanças no seu ph quando pequenas quantidades de ácido ( H + )
Equilíbrio Ácido-base Controle de ph por meio de soluções tampão Conceitos Soluções tampão = são sistemas aquosos que tendem a resistir a mudanças no seu ph quando pequenas quantidades de ácido ( H + )
tampão Prof a Alessandra Smaniotto QMC Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B
 Cap 3: Equilíbrio Químico Soluções tampão Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Água:excepcional habilidade em dissolver grande
Cap 3: Equilíbrio Químico Soluções tampão Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Água:excepcional habilidade em dissolver grande
EQÚILÍBRIO ÁCIDO-BÁSICO E ACIFICAÇÃO URINÁRIA. Profa. Dra. Monica Akemi Sato
 EQÚILÍBRIO ÁCIDO-BÁSICO E ACIFICAÇÃO URINÁRIA Profa. Dra. Monica Akemi Sato Introdução Homeostasia: constância do meio interno Claude Bernard Parâmetros fisiológicos constantes: temperatura, volume, pressão,
EQÚILÍBRIO ÁCIDO-BÁSICO E ACIFICAÇÃO URINÁRIA Profa. Dra. Monica Akemi Sato Introdução Homeostasia: constância do meio interno Claude Bernard Parâmetros fisiológicos constantes: temperatura, volume, pressão,
Soluções. Prof a. Jennifer
 Soluções Prof a. Jennifer Conceito Qualitativo Uma solução é formada por dois componentes, denominados dispersante (ou solvente) e o componente disperso (ou soluto). Sólidos em líquidos Líquidos em líquidos
Soluções Prof a. Jennifer Conceito Qualitativo Uma solução é formada por dois componentes, denominados dispersante (ou solvente) e o componente disperso (ou soluto). Sólidos em líquidos Líquidos em líquidos
Gabaritos Resolvidos Energia Química Semiextensivo V4 Frente C
 01) E Quanto maior a constante ácida, maior a força do ácido (acidez). Assim, HF < HCl < HBr < HI Ordem crescente de acidez (mais fraco para o mais forte) a) Errada é o HI (ácido mais forte); b) Errada
01) E Quanto maior a constante ácida, maior a força do ácido (acidez). Assim, HF < HCl < HBr < HI Ordem crescente de acidez (mais fraco para o mais forte) a) Errada é o HI (ácido mais forte); b) Errada
As alterações são grandes para que haja sustentação das necessidades maternas e para o desenvolvimento do feto
 ALTERAÇÕES CARDIORRESPIRATÓRIAS NA GESTAÇÃO Gestação e Exercício dois fatores que alteram o sistema cardiorrespiratório Gestacionais devido aos hormônios do feto e da placenta Exercício devido ao estresse
ALTERAÇÕES CARDIORRESPIRATÓRIAS NA GESTAÇÃO Gestação e Exercício dois fatores que alteram o sistema cardiorrespiratório Gestacionais devido aos hormônios do feto e da placenta Exercício devido ao estresse
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
FISIOLOGIA RESPIRATÓRIA REVISÃO
 FISIOLOGIA RESPIRATÓRIA REVISÃO Fisioterapia FMRPUSP Paulo Evora Revisão Anatômica O sistema respiratório consiste no nariz, faringe, laringe, traquéia, brônquios e pulmões. A pleura visceral cobre a superfície
FISIOLOGIA RESPIRATÓRIA REVISÃO Fisioterapia FMRPUSP Paulo Evora Revisão Anatômica O sistema respiratório consiste no nariz, faringe, laringe, traquéia, brônquios e pulmões. A pleura visceral cobre a superfície
Solução Fisiológica de Ringer com Lactato
 Solução Fisiológica de Ringer com Lactato Bula para paciente Solução injetável 6 mg/ml + 0,3 mg/ml + 0,2 mg/ml + 3 mg/ml Solução de Ringer com Lactato cloreto de sódio (6 mg/ml) + cloreto de potássio (0,3
Solução Fisiológica de Ringer com Lactato Bula para paciente Solução injetável 6 mg/ml + 0,3 mg/ml + 0,2 mg/ml + 3 mg/ml Solução de Ringer com Lactato cloreto de sódio (6 mg/ml) + cloreto de potássio (0,3
Aula 1: Introdução à Bioquímica. A Água
 Aula 1: Introdução à Bioquímica A Água 1 A Célula Composição de uma célula PROTEÍNAS 15% LIPÍDIOS 2% CARBOIDRATOS 3% ÁC. NUCLEICOS 7% Sais Minerais 1% Água 70% 2 DISTRIBUIÇÃO CORPORAL DA ÁGUA EM ADULTOS
Aula 1: Introdução à Bioquímica A Água 1 A Célula Composição de uma célula PROTEÍNAS 15% LIPÍDIOS 2% CARBOIDRATOS 3% ÁC. NUCLEICOS 7% Sais Minerais 1% Água 70% 2 DISTRIBUIÇÃO CORPORAL DA ÁGUA EM ADULTOS
CAPÍTULO 3 SISTEMA TAMPÃO
 17 CAPÍTULO 3 SISTEMA TAMPÃO Introdução: As reações químicas no organismo estão sujeitas a certas limitações como faixas estreitas de ph e temperatura, devido à necessidade de se preservar o ambiente fisiológico.
17 CAPÍTULO 3 SISTEMA TAMPÃO Introdução: As reações químicas no organismo estão sujeitas a certas limitações como faixas estreitas de ph e temperatura, devido à necessidade de se preservar o ambiente fisiológico.
INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS
 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS 2016 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO PROFESSOR:
INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS 2016 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO PROFESSOR:
Hidroclorotiazida. Diurético - tiazídico.
 Hidroclorotiazida Diurético - tiazídico Índice 1. Definição 2. Indicação 3. Posologia 4. Contraindicação 5. Interação medicamentosa 1. Definição A Hidroclorotiazida age diretamente sobre os rins atuando
Hidroclorotiazida Diurético - tiazídico Índice 1. Definição 2. Indicação 3. Posologia 4. Contraindicação 5. Interação medicamentosa 1. Definição A Hidroclorotiazida age diretamente sobre os rins atuando
DISTÚRBIO HIDRO- ELETROLÍTICO E ÁCIDO-BÁSICO. Prof. Fernando Ramos Gonçalves -Msc
 DISTÚRBIO HIDRO- ELETROLÍTICO E ÁCIDO-BÁSICO Prof. Fernando Ramos Gonçalves -Msc Distúrbio hidro-eletrolítico e ácido-básico Distúrbios da regulação da água; Disnatremias; Alterações do potássio; Acidoses
DISTÚRBIO HIDRO- ELETROLÍTICO E ÁCIDO-BÁSICO Prof. Fernando Ramos Gonçalves -Msc Distúrbio hidro-eletrolítico e ácido-básico Distúrbios da regulação da água; Disnatremias; Alterações do potássio; Acidoses
FISIOLOGIA GERAL INTRODUÇÃO
 FISIOLOGIA GERAL INTRODUÇÃO FISIOLOGIA Fisiologia (do grego physis = natureza, função ou funcionamento; e logos =estudo) A fisiologia: - estuda as funções mecânicas, físicas e bioquímicas nos seres vivos.
FISIOLOGIA GERAL INTRODUÇÃO FISIOLOGIA Fisiologia (do grego physis = natureza, função ou funcionamento; e logos =estudo) A fisiologia: - estuda as funções mecânicas, físicas e bioquímicas nos seres vivos.
ALCALOSES 1. Introdução
 ALCALOSES 1 Introdução O organismo é responsável por manter em equilíbrio o ph dos fluidos corpóreos presentes nos espaços extracelulares e intracelular através de diversos sistemas e mecanismos compensatórios
ALCALOSES 1 Introdução O organismo é responsável por manter em equilíbrio o ph dos fluidos corpóreos presentes nos espaços extracelulares e intracelular através de diversos sistemas e mecanismos compensatórios
FISIOTERAPIA PREVENTIVA
 FISIOTERAPIA PREVENTIVA DIABETES MELLITUS APOSTILA 5 DEFINIÇÃO É um distúrbio crônico, caracterizado pelo comprometimento do metabolismo da glicose e de outras substâncias produtoras de energia, bem como
FISIOTERAPIA PREVENTIVA DIABETES MELLITUS APOSTILA 5 DEFINIÇÃO É um distúrbio crônico, caracterizado pelo comprometimento do metabolismo da glicose e de outras substâncias produtoras de energia, bem como
Sistema Urinário. Patrícia Dupim
 Sistema Urinário Patrícia Dupim Insuficiência Renal Ocorre quando os rins não conseguem remover os resíduos metabólicos do corpo. As substância normalmente eliminadas na urina acumulam-se nos líquidos
Sistema Urinário Patrícia Dupim Insuficiência Renal Ocorre quando os rins não conseguem remover os resíduos metabólicos do corpo. As substância normalmente eliminadas na urina acumulam-se nos líquidos
Homeostase do potássio, cálcio e fosfato
 Homeostase do potássio, cálcio e fosfato Regulação dos eletrólitos Homeostase do potássio Intracellular ADP ATP P Extracellular Hipocalemia: baixo Repolarização mais lenta do potencial de membrana. - Fraqueza
Homeostase do potássio, cálcio e fosfato Regulação dos eletrólitos Homeostase do potássio Intracellular ADP ATP P Extracellular Hipocalemia: baixo Repolarização mais lenta do potencial de membrana. - Fraqueza
Equilíbrio ácido-básico 2010
 Iuri Marques de Oliveira & Renato Moreira Rosa O grau de acidez é uma propriedade química importante do sangue e outros líquidos corpóreos. A acidez é expressa na escala de ph e o valor de ph fisiológico
Iuri Marques de Oliveira & Renato Moreira Rosa O grau de acidez é uma propriedade química importante do sangue e outros líquidos corpóreos. A acidez é expressa na escala de ph e o valor de ph fisiológico
Profª:EnfªDarlene Carvalho Diálise : Aula I
 FISIOLOGIA RENAL E INSUFICIÊNCIA RENAL Profª:EnfªDarlene Carvalho Diálise : Aula I (DARLLENECARVALHO@YAHOO.COM.BR Anatomia Renal Funções do rim Excreção de produtos de degradação do metabolismo e de substâncias
FISIOLOGIA RENAL E INSUFICIÊNCIA RENAL Profª:EnfªDarlene Carvalho Diálise : Aula I (DARLLENECARVALHO@YAHOO.COM.BR Anatomia Renal Funções do rim Excreção de produtos de degradação do metabolismo e de substâncias
CINÉTICA QUÍMICA Folha 15 Prof.: João Roberto Mazzei
 01. (UNIRIO-RJ) Uma solução-tampão é preparada a partir de 6,4g de NH 4 NO 3 e 0,10L de solução aquosa 0,080mol/L de NH 4 OH. Sendo assim, A) determine o ph desta solução. B) o ph após adição de 700 ml
01. (UNIRIO-RJ) Uma solução-tampão é preparada a partir de 6,4g de NH 4 NO 3 e 0,10L de solução aquosa 0,080mol/L de NH 4 OH. Sendo assim, A) determine o ph desta solução. B) o ph após adição de 700 ml
CONHECIMENTO ESPERADO
 REPOSIÇÃO VOLÊMICA GABRIEL MAGALHÃES NUNES GUIMARÃES, GABRIEL@GABRIEL.MED.BR DISPONÍVEL EM WWW.ANESTESIOLOGIAUNB.COM.BR AULA DA DISCIPLINA BASES DA ANESTESIOLOGIA UNIVERSIDADE DE BRASÍLIA, 2017 CONHECIMENTO
REPOSIÇÃO VOLÊMICA GABRIEL MAGALHÃES NUNES GUIMARÃES, GABRIEL@GABRIEL.MED.BR DISPONÍVEL EM WWW.ANESTESIOLOGIAUNB.COM.BR AULA DA DISCIPLINA BASES DA ANESTESIOLOGIA UNIVERSIDADE DE BRASÍLIA, 2017 CONHECIMENTO
Docente: Prof a. Dr a. Luciana M. Saran
 FCAV/ UNESP Jaboticabal Disciplina: Química Geral Assunto: Solução Tampão Docente: Prof a. Dr a. Luciana M. Saran 1 1. INTRODUÇÃO Por que a adição de 0,01 mol de HCl à 1L de sangue humano, altera o ph
FCAV/ UNESP Jaboticabal Disciplina: Química Geral Assunto: Solução Tampão Docente: Prof a. Dr a. Luciana M. Saran 1 1. INTRODUÇÃO Por que a adição de 0,01 mol de HCl à 1L de sangue humano, altera o ph
Universidade Federal Rural de Pernambuco
 Universidade Federal Rural de Pernambuco 1 SISTEMAS RESTAURADORES Prof. Romildo Nogueira 1. Mecanismos de retroalimentação (feedback) Existem nos seres vivos sistemas (sistemas de controle), nos quais
Universidade Federal Rural de Pernambuco 1 SISTEMAS RESTAURADORES Prof. Romildo Nogueira 1. Mecanismos de retroalimentação (feedback) Existem nos seres vivos sistemas (sistemas de controle), nos quais
28/10/2016.
 alexandre.personal@hotmail.com www.professoralexandrerocha.com.br 1 O exercício é um grade desafio para as vias energéticas! Exercício intenso: 15 a 25X o gasto energético em repouso Os músculos aumentam
alexandre.personal@hotmail.com www.professoralexandrerocha.com.br 1 O exercício é um grade desafio para as vias energéticas! Exercício intenso: 15 a 25X o gasto energético em repouso Os músculos aumentam
AVALIAÇÃO LABORATORIAL DA FUNÇÃO RENAL
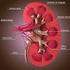 AVALIAÇÃO LABORATORIAL DA FUNÇÃO RENAL AVALIAÇÃO LABORATORIAL DA FUNÇÃO RENAL 1. EXAME DE URINA Cor Aspecto Densidade urinária ph Glicosúria Proteinúria Pigmentos e Sais biliares Hemoglobinúria e Mioglobinúria
AVALIAÇÃO LABORATORIAL DA FUNÇÃO RENAL AVALIAÇÃO LABORATORIAL DA FUNÇÃO RENAL 1. EXAME DE URINA Cor Aspecto Densidade urinária ph Glicosúria Proteinúria Pigmentos e Sais biliares Hemoglobinúria e Mioglobinúria
Principais exames bioquímicos de. tratamento do paciente intoxicado
 Universidade Estadual de Londrina Centro de Ciências da Saúde Departamento de Patologia e Análises Clínicas e Toxicológicas Principais exames bioquímicos de importância no diagnóstico e tratamento do paciente
Universidade Estadual de Londrina Centro de Ciências da Saúde Departamento de Patologia e Análises Clínicas e Toxicológicas Principais exames bioquímicos de importância no diagnóstico e tratamento do paciente
FCAV/ UNESP Jaboticabal. Disciplina: Química Geral Assunto: Solução Tampão. Docente: Prof a. Dr a. Luciana M. Saran
 FCAV/ UNESP Jaboticabal Disciplina: Química Geral Assunto: Solução Tampão Docente: Prof a. Dr a. Luciana M. Saran 1 1. SOLUÇÃO TAMPÃO Um tampão ou solução tampão é uma solução cujo ph varia muito pouco
FCAV/ UNESP Jaboticabal Disciplina: Química Geral Assunto: Solução Tampão Docente: Prof a. Dr a. Luciana M. Saran 1 1. SOLUÇÃO TAMPÃO Um tampão ou solução tampão é uma solução cujo ph varia muito pouco
MODELO DE BULA (Profissionais de Saúde)
 MODELO DE BULA (Profissionais de Saúde) CPHD SMP 35 FRAÇÃO ÁCIDA cloreto de sódio + cloreto de potássio + associações APRESENTAÇÃO E FORMA FARMACÊUTICA Solução para hemodiálise bombona plástica de 5 ou
MODELO DE BULA (Profissionais de Saúde) CPHD SMP 35 FRAÇÃO ÁCIDA cloreto de sódio + cloreto de potássio + associações APRESENTAÇÃO E FORMA FARMACÊUTICA Solução para hemodiálise bombona plástica de 5 ou
São exemplos de órgãos que realizam excreção em nosso corpo: Rins (exemplo de substância excretada = uréia);
 O sistema excretor é formado pelo conjunto de órgãos que permitem a eliminação de substâncias encontradas em excesso no corpo ou algumas são nocivas à saúde humana; Muitos metabólitos (Ex: uréia, H +,
O sistema excretor é formado pelo conjunto de órgãos que permitem a eliminação de substâncias encontradas em excesso no corpo ou algumas são nocivas à saúde humana; Muitos metabólitos (Ex: uréia, H +,
FISIOTERAPIA RESPIRATÓRIA NO AVE FT RAFAELA DE ALMEIDA SILVA APAE-BAURU
 FISIOTERAPIA RESPIRATÓRIA NO AVE FT RAFAELA DE ALMEIDA SILVA APAE-BAURU INTERNAÇÃO HOSPITALAR Toda pessoa com quadro suspeito de AVE deve ser levada imediatamente ao serviço de urgência para avaliação
FISIOTERAPIA RESPIRATÓRIA NO AVE FT RAFAELA DE ALMEIDA SILVA APAE-BAURU INTERNAÇÃO HOSPITALAR Toda pessoa com quadro suspeito de AVE deve ser levada imediatamente ao serviço de urgência para avaliação
Abordagem de íons fortes no equilíbrio ácido-básico 1
 Abordagem de íons fortes no equilíbrio ácido-básico 1 Introdução O controle do equilíbrio ácido-base se refere ao controle da concentração de H + nos líquidos corporais, que nas mesmas proporções devem
Abordagem de íons fortes no equilíbrio ácido-básico 1 Introdução O controle do equilíbrio ácido-base se refere ao controle da concentração de H + nos líquidos corporais, que nas mesmas proporções devem
c) Escreva a equação da reação de combustão completa, devidamente equilibrada, para o composto de fórmula molecular C 5 H 10 O.
 Questão 1 O esquema abaixo mostra compostos que podem ser obtidos a partir de um alceno de fórmula molecular C 5 H 10. A seguir, responda às questões relacionadas a esse esquema, considerando sempre o
Questão 1 O esquema abaixo mostra compostos que podem ser obtidos a partir de um alceno de fórmula molecular C 5 H 10. A seguir, responda às questões relacionadas a esse esquema, considerando sempre o
Química C Semiextensivo V. 4
 Química C Semiextensivo V. Exercícios 01) E 02) B 0) D 0) C 05) B Quanto maior a constante ácida, maior a força do ácido (acidez). Assim, HF
Química C Semiextensivo V. Exercícios 01) E 02) B 0) D 0) C 05) B Quanto maior a constante ácida, maior a força do ácido (acidez). Assim, HF
EQUILIBRIO HIDRICO. Prof. Dr. Rodolfo C. Araujo Berber Médico Veterinário, MSc. PhD. UFMT-Sinop
 EQUILIBRIO HIDRICO Prof. Dr. Rodolfo C. Araujo Berber Médico Veterinário, MSc. PhD. UFMT-Sinop Porque os organismos de mamíferos possuem grande quantidade de água? Alto ponto de ebulição (controle da temperatura);
EQUILIBRIO HIDRICO Prof. Dr. Rodolfo C. Araujo Berber Médico Veterinário, MSc. PhD. UFMT-Sinop Porque os organismos de mamíferos possuem grande quantidade de água? Alto ponto de ebulição (controle da temperatura);
MECANISMOS DE ACIDIFICAÇÃO URINÁRIA. Carlos Balda UNIFESP
 MECANISMOS DE ACIDIFICAÇÃO URINÁRIA Carlos Balda UNIFESP - 2012 Steady State Equilíbrio Dinâmico VALORES NORMAIS ph H+ (nanoeq/l) pco 2 (mmhg) HCO 3 (meq/l) ARTERIAL 7,37-7,43 37-43 36-44 22-26 VENOSO
MECANISMOS DE ACIDIFICAÇÃO URINÁRIA Carlos Balda UNIFESP - 2012 Steady State Equilíbrio Dinâmico VALORES NORMAIS ph H+ (nanoeq/l) pco 2 (mmhg) HCO 3 (meq/l) ARTERIAL 7,37-7,43 37-43 36-44 22-26 VENOSO
Ácidos e Bases. a) Produto iônico da água
 1 Ácidos e Bases a) Produto iônico da água A água é anfiprótica. Ou seja, ela tanto doa, com aceita prótons Reação direta: 2H 2O(l) H 3O + (aq) + OH (aq) autoprotólise: uma molécula transfere um próton
1 Ácidos e Bases a) Produto iônico da água A água é anfiprótica. Ou seja, ela tanto doa, com aceita prótons Reação direta: 2H 2O(l) H 3O + (aq) + OH (aq) autoprotólise: uma molécula transfere um próton
