Unidade VII Métodos moleculares de identificação de leveduras do vinho
|
|
|
- Mikaela Coelho Meneses
- 6 Há anos
- Visualizações:
Transcrição
1 Unidade VII Métodos moleculares de identificação de leveduras do vinho Margarida Casal, Dorit Schuller e Célia Pais 1. Fermentação à escala laboratorial 4 2. Identificação de organismos por métodos moleculares 7 3. Isolamento de DNA de leveduras Preparação da reacção de PCR Sequenciação automática 14
2 2 Unidade VII A transformação do mosto em vinho é um processo microbiológico muito complexo, caracterizado pela predominância sequencial de diferentes espécies de leveduras, bactérias lácticas e fungos filamentosos. A qualidade e as características sensoriais do vinho estão intimamente associadas com a biodiversidade da flora de leveduras. As leveduras envolvidas na vinificação originam-se da microflora na superfície da uva e da flora secundária que coloniza as superfícies de equipamentos e utensílios aplicados no fabrico de vinhos. A flora indígena inclui espécies dos géneros Kloeckera /Hanseniaspora, Candida, Pichia, Kluyveromyces ou Metschnikovia, que se encontram em elevada concentração na superfície de uvas sãs ( células/cm 2 ), e são responsáveis pelo arranque da fermentação alcoólica. Comparativamente, a levedura fermentativa por excelência, Saccharomyces cerevisiae, encontra-se em concentração muito baixa no início da fermentação, mas devido à sua elevada tolerância ao etanol consegue rapidamente predominar após os primeiros dias do processo, sendo geralmente a única espécie de levedura encontrada no final da fermentação, como se verifica na figura 7.1. A fermentação espontânea baseada unicamente na flora indígena pode produzir vinhos de qualidade excepcional, mas devido a variações na biodiversidade da microflora de um ano para outro, este processo torna-se por vezes pouco eficaz traduzindo-se na dificuldade de produzir em anos seguidos vinho com a mesma personalidade, e que reflicta as características desejadas. Por este motivo, a enologia moderna recorre ao uso de leveduras starter que são estirpes de S. cerevisiae seleccionadas de variadas regiões com tradição vitivinícola. Estas estirpes foram intensamente estudadas quanto às suas características fermentativas e são comercializadas na forma de leveduras secas activas (LSA). A estirpe inoculada predomina e reprime a flora indígena, permitindo um melhor controlo da microbiologia do processo, e consequentemente uma fermentação rápida e previsível, que se traduz na qualidade reprodutível do produto final, o vinho. Esta prática evita também paragens ( amuos ) da fermentação, que se verificam por vezes em fermentações espontâneas, por exemplo em consequência do uso excessivo de fungicidas durante a maturação das uvas. No presente trabalho vai ser realizada uma fermentação espontânea em escala reduzida a partir do mosto de uvas. O desenrolar da fermentação será acompanhado ao longo do tempo pelo registo da diminuição do peso do mosto devido à libertação de CO 2, que está associada à fermentação dos açúcares do sumo de uva. Na fase final da fermentação o mosto será inoculado em meios de cultura apropriados, permitindo o isolamento de colónias de leveduras. Após enriquecimento, e extracção do DNA de
3 Unidade VII 3 alguns isolados, será realizada a sua caracterização recorrendo a uma técnica baseada na reacção em cadeia da polimerase (polymerase chain reaction - PCR). População de leveduras (células/ml) 1 x x x x Teor em açúcares redutores (g/l) Dias Candida stellata Hanseniaspora uvarum Pichia membranifaciens Metschnikowia pulcherrima Saccharomyces cerevisiae Figura Dinâmica populacional de leveduras e teor em açúcares redutores no mosto ao longo da fermentação.
4 4 Unidade VII 1. Fermentação à escala laboratorial Realizar os passos que se seguem. 1. Recolher uvas (ca. 2 kg) num saco de plástico previamente esterilizado e proceder ao seu esmagamento no laboratório. É importante que as uvas não tenham sofrido recentemente tratamentos químicos com fungicidas. 2. Verter o mosto num balão de Erlenmeyer (previamente pesado). Encher o balão completamente para evitar a oxidação do mosto. 3. Retirar uma alíquota de 10 ml de mosto e determinar o seu ph. Opcionalmente, realizar diluições decimais e plaquear 0,1 ml das diluições 10-4 e 10-5 em meio YEPD. Incubar 1-2 dias à temperatura ambiente e registar as observações.
5 Unidade VII 5 4. Fechar o recipiente com uma rolha de plástico ou borracha. Introduzir uma agulha de seringa na parte lateral da rolha de modo que a ponta da agulha se encontre no interior do frasco Deste modo é possível a libertação de CO2 resultante da fermentação alcoólica. A seguir, selar a rolha com parafilm. 5. Realizar a fermentação numa estufa de temperatura controlada (20ºC). 6. Monitorizar o progresso da fermentação por pesagens diárias. O arranque da fermentação pode ser muito variável e depende de numerosos factores como o estado sanitário das uvas ou o uso de fungicidas. Geralmente, após 3-7 dias verifica-se o início da fermentação, perceptível através do aparecimento de bolhas de CO2. Recolher uma amostra de mosto quando se verificar a diminuição do peso do mosto correspondente a 70 g/l (fase final da fermentação). Preparar diluições decimais e inocular 0,1 ml das diluições 10-4 e10-5 em meio YEPD.
6 6 Unidade VII 7. Após 2 dias de incubação, contar as unidades formadoras de colónias. A fim de obter maior biomassa, estender 8 colónias em diferentes secções de uma nova placa com meio YEPD e incubar novamente 1a 2 dias. Interpretação dos resultados Interpretar os resultados apresentados nas figuras 7.2 e Perda de peso (g/l) Fermentação tardia com paragem Sem fermentação -100 Fermentação completa Tempo (dias) Figura 7.2 Perfis de fermentação espontânea de mosto de uva.
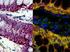
7 Unidade VII 7 A B Figura 7.3. Isolamento de microrganismos do mosto em fermentação. (A) Mosto na fase inicial da fermentação: verifica-se a presença de fungos filamentosos (manchas translúcidas), bactérias (colónias mais pequenas) e leveduras (colónias maiores). (B) Na fase final da fermentação o mosto contém quase exclusivamente a levedura S. cerevisiae. 2. Identificação de organismos por métodos moleculares - Estudos de reassociação DNA-DNA A comparação da totalidade do genoma de organismos diferentes, realizada por técnicas de reassociação DNA-DNA, tem permitido a determinação da homologia genética existente entre esses mesmos organismos. A utilização desta metodologia é um reafirmar ao nível molecular do princípio evolutivo da ascendência comum. Ou seja, se dois organismos estão relacionados, devem reter nos seus genomas sequências de bases que descendem de um ancestral comum e os organismos mais relacionados conservarão maior proporção dessas sequências de bases do que organismos com maior divergência. A grande confirmação da validade deste tipo de estudos, relativamente à delimitação de espécies, resultou do paralelismo encontrado entre esses resultados e os obtidos por estudos de interfertilidade entre estirpes, os quais se correlacionam com o conceito biológico de espécie. Assim, foram estabelecidas as seguintes correlações entre os resultados da complementaridade do DNA e as relações biológicas entre as estirpes: 1) estirpes conspecíficas, em geral apresentam valores de homologia de DNA superior a 70%; 2) relações varietais podem ser atribuídas a estirpes que apresentem valores entre 40 e 70% de complementaridade do DNA, a não ser que cruzamentos genéticos mostrem ausência de interfertilidade; 3) estirpes apresentando
8 8 Unidade VII menos de 40% de homologia de DNA, são quase sempre isoladas geneticamente, representando espécies independentes. Quando sujeitos a um campo eléctrico, os cromossomas formam um perfil de bandas, considerado característico de cada espécie. No entanto, têm sido observadas bastantes variações de perfis intraspecíficos, devidas a polimorfismos associados ao tamanho dos cromossomas, a rearranjos dos cromossomas e a fenómenos de aneuploidia, o que dificulta a interpretação taxonómica de cariótipos. Para além disso, moléculas do mesmo tamanho podem migrar como dupletos, não havendo também relação linear estrita entre o tamanho molecular e a distância de migração, sobretudo para os cromossomas maiores. - Análise de polimorfismos de restrição (RFLP) Uma outra técnica bastante empregue na análise do DNA e RNA, principalmente antes do desenvolvimento da técnica de PCR, foi o polimorfismo do tamanho de fragmentos de restrição (RFLP - restriction fragment length polymorphism). A técnica compreende a quebra do DNA por enzimas de restrição em regiões com determinadas sequências de bases e a separação dos fragmentos resultantes por electroforese. Diferentes perfis de bandas, ou polimorfismos, podem ser observados directamente sob luz ultravioleta após coloração do gel com brometo de etídio, ou indirectamente após transferência das bandas para membranas, sobre as quais se faz hibridação com sondas específicas de DNA ou RNA marcado. A detecção da hibridação poderá ser efectuada posteriormente por película de raios-x ou por quimioluminescência, consoante a marcação utilizada. O facto do rdna ocorrer em cópias múltiplas, reflectindo a necessidade de produção de quantidades elevadas pelas células destes genes, tem facilitado a sua análise por RFLP, tendo os polimorfismos obtidos permitido a diferenciação tanto de espécies, como de estirpes de leveduras. De referir que quase todos os sítios de restrição que permitiram a discriminação de estirpes individuais se encontravam localizados na região hipervariável dos espaçadores intergénicos. Este tipo de análise possibilitou também a elaboração de mapas de restrição e a estimativa das relações filogenéticas. A análise de restrição do DNA mitocondrial tem tido uma grande aplicação no estudo de leveduras, dado por um lado originar um pequeno número de fragmentos (quando comparado com o DNA genómico) conduzindo a electroforegramas pouco
9 Unidade VII 9 complexos, e por outro, devido ao elevado polimorfismo dos perfis obtidos. Este último aspecto tem-se revelado bastante útil na diferenciação de estirpes, nomeadamente enológicas. - Técnicas baseadas em PCR Pode afirmar-se que a técnica de reacção em cadeia da polimerase (PCR - polimerase chain reaction), constitui uma ferramenta básica para inúmeras metodologias de análise do DNA, consistindo fundamentalmente na amplificação de determinados segmentos de DNA. O processo é iniciado com a desnaturação da molécula de DNA de dupla hélice por aplicação de temperatura elevada. Após o abaixamento da temperatura, dois oligonucleótidos de cadeia simples, complementares às regiões flanqueadoras do segmento que se quer amplificar e que funcionam como iniciadores ou primers, ligam-se a essas regiões, dando-se início à síntese do DNA por acção de uma DNA polimerase termostável. Ciclos de desnaturação, de ligação dos primers e de extensão (elongamento) dos mesmos por acção da DNA polimerase, são repetidos várias vezes resultando na amplificação do segmento alvo. A grande vantagem da utilização da técnica de PCR baseia-se na necessidade de uma pequena quantidade de DNA para efectuar a análise, o qual não necessita de estar muito purificado. A amplificação pode mesmo ser efectuada a partir de células lisadas sem posterior extracção ou purificação do DNA. Uma das utilizações mais directas da PCR é a técnica de análise de polimorfismo de DNA amplificado aleatoriamente (RAPD). O DNA é amplificado numa reacção de PCR, usando um só primer com uma sequência arbitrária. O primer hibrida aleatoriamente com sequências homólogas ao DNA em estudo, originando fragmentos amplificados. O produto é sujeito a electroforese e, após coloração com brometo de etídio, é visualizado sob luz ultravioleta. Perfis de bandas diferentes indicam sequências diferentes nas moléculas originais de DNA. Em diversos trabalhos de aplicação da técnica de RAPD em leveduras, foi obtida discriminação ao nível da espécie, mas pequenas diferenças nos perfis de diferentes estirpes da mesma espécie, indicam que é possível discriminar ao nível de subespécie. Um dos problemas da análise de RAPD é que os perfis obtidos, quer num mesmo laboratório, quer inter-laboratórios, nem sempre são reprodutíveis. A resolução do problema passa pelo uso de condições muito restritas dos perfis de temperatura usados.
10 10 Unidade VII Uma abordagem relacionada com a técnica de RAPD é a amplificação de fragmentos usando como primers, oligonucleótidos específicos para sequências de DNA repetitivas, ou primers microssatélite, a qual tem permitido a discriminação ao nível da espécie e subespécie. Este método é mais robusto do que o RAPD dado que a temperatura de emparelhamento das bases é superior. Um alternativa que oferece maior segurança no caso da amplificação por PCR não ser suficientemente específica, é o chamado "nested PCR" (PCR encaixado). No "nested PCR" são usados um primeiro par de primers para amplificar um determinado fragmento do DNA original, seguindo-se nova reacção de PCR com um segundo par de primers, os quais são complementares a sequências existentes no primeiro produto amplificado. Caso este corresponda ao fragmento que se pretendia amplificar, esta estratégia funciona como um passo de confirmação. No genoma de S. cerevisiae existem cerca de sequências repetidas com tamanho de 300 pb, designadas por sequências δ. Pela ultilização de primers adequados é amplificado o DNA localizado nas regiões entre duas sequências δ adjacentes. O resultado da reacção de PCR é uma mistura de fragmentos de tamanhos entre 200 a 2000 pb. Uma vez que o perfil de distribuição de sequências δ é muito variável entre diferentes estirpes de S. cerevisiae, este método de tipagem molecular tem sido utilizado para distinguir estirpes enológicas. 3. Isolamento de DNA de leveduras Para a obtenção de resultados credíveis e reprodutíveis, certas regras devem ser respeitadas ao manusear o DNA: Verificar que todo o material que entra em contacto directo com o DNA genómico está estéril, para que não haja contaminações com DNases ou por outros ácidos nucleícos. Usar luvas durante as manipulações do DNA, para evitar que as DNases presentes nas mãos contaminem as amostras de DNA. Verificar a perigosidade dos produtos químicos que se usam.
11 Unidade VII 11 Procedimento 1. Inocular uma colónia de S. cerevisiae num tubo Eppendorf contendo 1 ml de YPD. 2. Agitar o tubo fortemente num vortex até que as células dispersem completamente. Furar a tampa com a agulha de uma seringa. 3. Crescer durante a noite a 28-30ºC, numa incubadora com agitação (200 rpm). 4. Centrifugar as células brevemente (30 s, rpm) numa centrifuga de bancada. Desprezar o sobrenadante. 5. Lavar o sedimento com água: ressuspender as células em 100 µl de água esterilizada, centrifugar as células brevemente (30 seg., rpm) numa centrifuga de bancada e desprezar o sobrenadante. 6. Ressuspender o sedimento em 100 µl de uma solução contendo sorbitol (1M) e EDTA (100mM), ph 7,5. 7. Adicionar 5 µl da enzima liticase (5 U/µl) que provoca a degradação da parede celular. 8. Proceder a uma incubação de 20 minutos a 37ºC. 9. Adicionar 100 µl do tampão Tris HCl (50mM) EDTA (20 mm), ph Adicionar 5,0 µl de SDS 10 % (p/v). 11. Incubar 5 minutos a 65ºC. A adição do detergente SDS em combinação com a temperatura elevada provoca a lise das células e a libertação dos compostos celulares. 12. Adicionar 80 µl de acetato de potássio (5M). 13. Colocar imediatamente no gelo e incubar durante 5 minutos. O acetato de potássio e a temperatura baixa provocam a desnaturação e precipitação da proteína celular. 14. Centrifugar durante 15 minutos, a uma velocidade de rpm, numa microcentrífuga refrigerada (4ºC). No sedimento no fundo do tubo Eppendorf encontram-se agora os restos celulares bem como a proteína precipitada, enquanto o DNA permanece no sobrenadante 15. Transferir o sobrenadante para um novo tubo Eppendorf. 16. Adicionar volume igual de isopropanol e agitar ligeiramente (inverter o tubo 2-3 vezes). Incubar durante 5 minutos à temperatura ambiente. Verificar a formação de nuvens do DNA precipitado pelo isopropanol.
12 12 Unidade VII 17. Centrifugar 45 segundos a rpm numa microcentrífuga para sedimentar o DNA precipitado. 18. Rejeitar o sobrenadante. 19. Lavar o sedimento com 1 ml de etanol 70%, (v/v). A lavagem consiste na adição de etanol, breve agitação, centrifugação e remoção do etanol. 20. Deixar o DNA secar no tubo de Eppendorf com a tampa aberta à temperatura ambiente. Ressuspender o sedimento em 0,1 ml de tampão TE. Guardar a -20 C. 4. Preparação da reacção de PCR Procedimento 1. Num suporte adequado, colocado sobre gelo, dispor um tubo de PCR (0,2 ml) para cada isolado a testar. Os tubos devem estar devidamente identificados. 2. Num tubo de Eppendorf preparar a mistura de reacção de acordo com o número de reacções a realizar (os valores estão calculados para uma reacção). Manter a mistura no gelo. Volume (µl) H2O 15,7 -- Concentração final para um volume de 25 µl Tampão 10x 2,5 1x MgCl2 (25 mm) 3 3 mm Mistura de dntps (10 mm cada) 1 0,4 mm Primer δf (50 pmol//µl) 0,8 40 pmol Primer δr (50 pmol//µl) 0,8 40 pmol Taq DNA polimerase (5U/µl) 0,2 1U Sequência dos primers: δf : 5 -CAAAATTCACCTATATCT-3 δr : 5 -GTGGATTTTTATTCCAAC-3
13 Unidade VII Distribuir 50 ng de DNA genómico (1 µl) de cada isolado a identificar nos respectivos tubos de PCR. 4. Distribuir 24 µl da mistura para cada tubo de PCR já com o DNA. Manter os tubos no gelo. 5. Programar o aparelho de PCR: Passo Temperatura Tempo Nº de ciclos Desnaturação inicial 95ºC 2 Desnaturação 95ºC 30 Emparelhamento 43,2ºC Extensão 72ºC 60 Extensão Final 72ºC Colocar os tubos no aparelho de PCR e iniciar o programa. 7. Preparar o gel de agarose 1,5 % (p/v) em tampão TAE 1x e acrescentar 5 µl de uma solução de brometo de etídeo (10 mg/ml). Nota importante: O brometo de etídeo é um agente mutagénico poderoso. Pode ser prejudicial por inalação, ingestão e absorção através da pele. Desta forma, deve ser manipulado com luvas apropriadas e o trabalho realizado na hotte. O brometo de etídeo é também irritante para as mucosas e para o tracto respiratório. Dado o seu carácter mutagénico está classificado como uma substância perigosa, pelo que os seus resíduos devem ser incluídos na linha de tratamento de resíduos perigosos. 8. Quando a reacção de PCR terminar, retirar as amostras do aparelho e juntar 2 µl tampão de aplicação. 9. Aplicar no primeiro poço do gel um marcador de DNA com fragmentos de peso molecular conhecidos. 10. Colocar 10 µl de cada reacção de PCR (já com o tampão de aplicação) em cada poço do gel e iniciar a electroforese a 3 V/cm. Utilizar tampão de electroforese TAE 1x. 11. Desligar a fonte de energia após a electroforese, visualizar o gel num transiluminador de UV e fotografar. 12. Analisar e comparar os padrões obtidos para cada isolado.
14 14 Unidade VII Interpretação dos resultados Comparar os perfis obtidos e concluir sobre a identidade das estirpes analisadas. Marcador (pb) Pista 1 e 4: estirpe A Pista 2: estirpe B Pista 3,7 e 8: estirpe C Pista 5 estirpe D Pista 6 estirpe E 200 Figura 7.4. Análise do perfil de amplificação de sequências inter-δ em estirpes de S. cerevisiae distintas isoladas do mosto de uva em fermentação, através de uma electroforese em gel de agarose. 5. Sequenciação automática Muita informação sobre a estrutura e expressão génica pode ser obtida pela determinação directa da sequência de bases numa molécula de DNA. A utilização de sequenciadores automáticos (Figura 7.5) é essencial quando se deseja realizar sequenciação em larga escala, como por exemplo em projectos genoma. O desenvolvimento e utilização de sequenciadores automáticos torna mais eficiente e rápida a sequenciação de DNA na medida em que as etapas de leitura do gel e o processamento de sequências são realizadas através de computadores. Alguns sequenciadores conseguem ler cerca de 1000 bases numa separação. A reacção de sequenciação é baseada no método de Sanger, do mesmo modo que a manual que utiliza ddntps (di-desoxinucleotídeo-tri-fosfatos) que impedem a síntese nos respectivos nucleotídeos (ddgtp, ddatp, ddttp, ddctp). Assim, por exemplo, as reacções com ddgtp terão fragmentos de diferentes tamanhos todos eles com o ddg no final, correspondendo a regiões onde existam Cs no DNA. A análise dos fragmentos em
15 Unidade VII 15 eletroforese permite a identificação das posições dos Cs. Do mesmo modo é executado o processo para os demais nucleótidos. O método original utiliza marcação radioactiva enquanto que novos métodos utilizam marcação fluorescente. O sequenciador a laser permite que todas as reacções (A, C, G, T) sejam corridas juntas pois utiliza-se uma cor fluorescente diferente para cada base. São utilizados quatro fluorocromos diferentes e uma vez excitados por um feixe de laser emitem luz em comprimentos de onda distintos. É possível marcar com estes fluorocromos o primer universal M13 ou então cada um dos nucleotídeos (terminadores). Assim, uma vez que em cada uma das reacções (A, T, C, G) é empregue um fluorocromo diferente é possível juntar estes produtos e realizar uma corrida num único gel. Os produtos da reacção de sequenciação, marcados com os fluorocromos, ao serem submetidos a eletroforese passam pelo feixe de laser, que promove a excitação dos fluorocromos. A luz emitida pelos fluorocromos é detectada por um fotomultiplicador e a informação é processada através de um computador (Figura 7.6). Figura 7.5 Aparelho de sequenciação automática (ABI Prism 310).
16 16 Unidade VII Figura 7.2- Registo de uma sequenciação automática. N representa uma base que não pode ser determinada. Figura Electroferograma obtido num sequenciador automático recorrendo ao uso de nucleótidos marcados com fluorescência (N representa uma base que não foi identificada nesta reacção). Purificação do produto de PCR Para purificar os ácidos nucleicos devem usar-se colunas com resinas apropriadas (Amersham Bioscience MicroSpin columns) e seguir as instruções do fabricante. Preparação das amostras para o sequenciador Reacção de sequenciação A reacção de sequenciação é realizada com base no protocolo do Big Dye Terminator Cycle sequencing Ready reaction Kit da Applied Biosystems. 1. Colocar 2,5 µl de amostra de DNA purificada num tubo de PCR. 2. Adicionar 2 µl de Terminator ready reactions MIX.
17 Unidade VII 17 Terminator ready reactions MIX é uma solução constituída por: Terminadores marcados (A-[RGG]; C-[ROX]; G-[R110] e T-[TAMRA]), datp, dctp, DITP, dutp, AmplitTaq DNA Polimerase FS, MgCl2 e tampão Tris-HCl (ph 9,0). Esta solução vem completamente preparada no Kit de sequenciação utilizado. 3. Terminar a mistura com a adição de 0,5 µl de uma solução contendo os respectivos primers na concentração de 2,5 µm. 4. Misturar bem e colocar no termociclador previamente programado com o seguinte programa: Passo Temperatura Tempo Nº de ciclos Desnaturação inicial 96ºC 4 Desnaturação 96ºC 10 Emparelhamento 58ºC 5 35 Extensão 60ºC 4 Extensão Final 60ºC 10 Purificação dos produtos de extensão após reacção de sequenciação Após a reacção de sequenciação as amostras são purificadas em colunas de purificação AutoSeq 50 da Amersham Biosciences. O objectivo desta purificação é essencialmente a remoção de terminadores não incorporados que poderão interferir na obtenção de um bom perfil de nucleótidos. As amostras quando não são purificadas imediatamente após a reacção de sequenciação, devem ser conservadas a 4ºC. 1. Agitar as colunas no vortex de modo a ressupender a resina. Cortar a ponta e inserir em tubos de Eppendorf. 2. Abrir ligeiramente as tampas e centrifugar a 2000 g durante 1 minuto. 3. Remover o excedente dos tubos, limpar a parte inferior de cada coluna, colocar as colunas em tubos novos e retirar as tampas. 4. Aplicar a amostra (produtos da extensão) no centro da coluna e centrifugar a 2000 g durante 1 minuto. 5. Descartar as colunas. Os produtos purificados ficam no fundo do tubo.
18 18 Unidade VII Sequenciação A 5 µl de produto extenso purificado, adicionar 15 µl de formamida, transferir para um tubo de sequenciação e desnaturar a 95ºC durante 2 minutos. Após a desnaturação, colocar em gelo pelo menos 5 minutos. Proceder à sequenciação no Genetic Analizer 310 ABI PRISM (Figura 7.6). Soluções Tampão TAE 50 x (solução Stock) Tris Base 242 g Ácido acético glacial 57,1 ml EDTA Na2 2 H2O 37,2 g Dissolver o Tris em 800 ml de água desionizada, e juntar a seguir o EDTA e o ácido acético glacial. Perfazer o volume a 1000 ml. Verificar o ph da solução que deve estar a 8,5. Para preparar 1 l de tampão TAE, adicionar 20 ml de TAE 50x a 980 ml de água desionizada. Tampão TE Tris HCl EDTA Ajustar o ph a 8,0. 10mM 1 mm Tampão de aplicação de amostras em geles de agarose 10 x Ficoll 20 g Azul de bromofenol 0,05 g TAE 10 X 2 ml EDTA 0,4 g Dissolver os compostos em 100 ml de água desionizada. Meio YPD (Yeast Extract Peptone Dextrose Agar) Extracto de levedura 10 g/l Peptona 20 g/l Glucose 20 g/l Agar 20 g/l
19 Unidade VII 19 Bibliografia Ciani, M.Biodiversity and biotechnology of wine yeast Research Signpost. Griffin, H V e Griffin, A M PCR technology: current innovations. CRC Press, Inc. Fleet, G.H. Wine: Microbiology and biotechnology Harword Academic Fugelsang, K.C. Wine microbiology Chapman and Hall. New York Pascal Ribéreau-GayonT, P. Glories, Y., Maujean, A., Dubourdieu, D The Handbook of Enology: Microbiology of Wine, Volume 1, The Microbiology of Wine and Vinifications. John Wiley and Sons. Schuller, D., Valero, E., Dequin, S. e Casal, M. (2003) Survey of molecular methods for the typing of wine yeast strains. FEMS Letters, 11366: 1-8. WWW
Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM)
 Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM) Ana Luísa Carvalho Departamento de Zoologia, Universidade de Coimbra Introdução: Neste trabalho pretende-se analisar um polimorfismo
Estudo de um Polimorfismo no Gene da Cadeia Pesada β da Miosina (CPβM) Ana Luísa Carvalho Departamento de Zoologia, Universidade de Coimbra Introdução: Neste trabalho pretende-se analisar um polimorfismo
Extracção de ADN de mancha de sangue por Chelex 100. Protocolo experimental:
 Extracção de ADN de mancha de sangue por Chelex 100 1. Num tubo eppendorf misturar 1ml de água desionizada estéril com uma mancha de sangue com aproximadamente 3mm²; 2. Incubar à temperatura ambiente no
Extracção de ADN de mancha de sangue por Chelex 100 1. Num tubo eppendorf misturar 1ml de água desionizada estéril com uma mancha de sangue com aproximadamente 3mm²; 2. Incubar à temperatura ambiente no
GENÉTICA HUMANA LICENCIATURA EM CIÊNCIAS DA SAÚDE
 GENÉTICA HUMANA LICENCIATURA EM CIÊNCIAS DA SAÚDE PROTOCOLOS LABORATORIAIS 3º Ano - 1º Semestre 2013 / 2014 1 EXTRACÇÃO DE DNA GENÓMICO ESFREGAÇO BUCAL Citogene Buccal Kit Esfregar 10 vezes a mucosa bucal
GENÉTICA HUMANA LICENCIATURA EM CIÊNCIAS DA SAÚDE PROTOCOLOS LABORATORIAIS 3º Ano - 1º Semestre 2013 / 2014 1 EXTRACÇÃO DE DNA GENÓMICO ESFREGAÇO BUCAL Citogene Buccal Kit Esfregar 10 vezes a mucosa bucal
Apostila de aula prática REAÇÃO EM CADEIA PELA POLIMERASE (PCR)
 1 Universidade Federal Fluminense Instituto Biomédico Departamento de Microbiologia e Parasitologia Curso: Medicina Veterinária Disciplina: Virologia III (MIP00071) Apostila de aula prática REAÇÃO EM CADEIA
1 Universidade Federal Fluminense Instituto Biomédico Departamento de Microbiologia e Parasitologia Curso: Medicina Veterinária Disciplina: Virologia III (MIP00071) Apostila de aula prática REAÇÃO EM CADEIA
acompanhamento científico
 acompanhamento científico tipagem molecular de leveduras: caracterização da colecção enológica porto dorit-elisabeth th schuller 12 abril 2007 comissão de viticultura da região dos vinhos verdes A evolução
acompanhamento científico tipagem molecular de leveduras: caracterização da colecção enológica porto dorit-elisabeth th schuller 12 abril 2007 comissão de viticultura da região dos vinhos verdes A evolução
Para 1L de meio triptona ou peptona 16g (1,6%) extrato de levedura 10g (1%) NaCl 5g (0,5%)
 Preparação de meio líquido - triptona ou peptona - extrato de levedura 1º Dissolver a triptona e o extrato; 2º Acrescentar o cloreto de sódio e acertar o volume; 3º Após tudo dissolvido e com volume correto,
Preparação de meio líquido - triptona ou peptona - extrato de levedura 1º Dissolver a triptona e o extrato; 2º Acrescentar o cloreto de sódio e acertar o volume; 3º Após tudo dissolvido e com volume correto,
Universidade de Évora ICAAM Laboratório de Microbiologia do Solo 18/07/ /07/2011
 Universidade de Évora ICAAM Laboratório de Microbiologia do Solo Ana Neves José Neto 18/07/2011-22/07/2011 Responsável: Solange Oliveira Investigadoras: Marta Laranjo Ana Alexandre Rizóbios são bactérias
Universidade de Évora ICAAM Laboratório de Microbiologia do Solo Ana Neves José Neto 18/07/2011-22/07/2011 Responsável: Solange Oliveira Investigadoras: Marta Laranjo Ana Alexandre Rizóbios são bactérias
Departamento de Biologia. Mestrado em Bioempreendedorismo e Biotecnologia de PAM
 Departamento de Biologia Mestrado em Bioempreendedorismo e Biotecnologia de PAM Protocolos das aulas práticas Docente: Rui Oliveira Construção de um plasmídeo com o gene da GFP sob regulação do promotor
Departamento de Biologia Mestrado em Bioempreendedorismo e Biotecnologia de PAM Protocolos das aulas práticas Docente: Rui Oliveira Construção de um plasmídeo com o gene da GFP sob regulação do promotor
PCR Reação de Polimerase em Cadeia. Termociclador
 PCR Reação de Polimerase em Cadeia Termociclador REAÇÃO EM CADEIA DA POLIMERASE (PCR) Técnica que permite a amplificação da quantidade de DNA específico utilizando a enzima Taq DNA polimerase, sequências
PCR Reação de Polimerase em Cadeia Termociclador REAÇÃO EM CADEIA DA POLIMERASE (PCR) Técnica que permite a amplificação da quantidade de DNA específico utilizando a enzima Taq DNA polimerase, sequências
EXTRAÇÃO DE DNA DE SANGUE (LEUCÓCITOS)
 EXTRAÇÃO DE DNA DE SANGUE (LEUCÓCITOS) A) Obtenção de Leucócitos 1. Coletar 5mL de sangue em tubos contendo EDTA potássio (50uL de EDTA (k 3) a 15%). O EDTA é uma substância anticoagulante. Existem outras
EXTRAÇÃO DE DNA DE SANGUE (LEUCÓCITOS) A) Obtenção de Leucócitos 1. Coletar 5mL de sangue em tubos contendo EDTA potássio (50uL de EDTA (k 3) a 15%). O EDTA é uma substância anticoagulante. Existem outras
PCR Prof. Dr. Fábio Gregori
 PCR Prof. Dr. Fábio Gregori Laboratório de Biologia Molecular Aplicada e Sorologia VPS-FMVZ-USP 1 Reação em Cadeia pela Polimerase Amplificação in vitro de DNA BANDA DNA (amplificado) DNA Agente infeccioso
PCR Prof. Dr. Fábio Gregori Laboratório de Biologia Molecular Aplicada e Sorologia VPS-FMVZ-USP 1 Reação em Cadeia pela Polimerase Amplificação in vitro de DNA BANDA DNA (amplificado) DNA Agente infeccioso
Procedimento Operacional Padrão - POP
 Página 1 de 10 Biobanco Procedimento Operacional Padrão para: Extração de RNA total de sangue POP: V. 1.0 Nome: Extração de RNA total de sangue Efetiva: dezembro, 22 autora: Erika Regina Manuli Aprovação
Página 1 de 10 Biobanco Procedimento Operacional Padrão para: Extração de RNA total de sangue POP: V. 1.0 Nome: Extração de RNA total de sangue Efetiva: dezembro, 22 autora: Erika Regina Manuli Aprovação
Tecnologia do DNA recombinante. John Wiley & Sons, Inc.
 Tecnologia do DNA recombinante John Wiley & Sons, Inc. Tópicos Técnicas básicas usadas para identificar, amplificar e clonar genes Construção e triagem de bibliotecas de DNA Análise molecular de DNA, RNA
Tecnologia do DNA recombinante John Wiley & Sons, Inc. Tópicos Técnicas básicas usadas para identificar, amplificar e clonar genes Construção e triagem de bibliotecas de DNA Análise molecular de DNA, RNA
IDENTIFICAÇÃO DE SEQUÊNCIAS POR HIBRIDIZAÇÃO E SEQUENCIAMENTO. Aula 5. Maria Carolina Quecine Departamento de Genética
 IDENTIFICAÇÃO DE SEQUÊNCIAS POR HIBRIDIZAÇÃO E SEQUENCIAMENTO Aula 5 LGN232 Genética Molecular Maria Carolina Quecine Departamento de Genética mquecine@usp.br LEMBRANDO O DOGMA CENTRAL DA BIOLOGIA MOLECULAR
IDENTIFICAÇÃO DE SEQUÊNCIAS POR HIBRIDIZAÇÃO E SEQUENCIAMENTO Aula 5 LGN232 Genética Molecular Maria Carolina Quecine Departamento de Genética mquecine@usp.br LEMBRANDO O DOGMA CENTRAL DA BIOLOGIA MOLECULAR
Actividade prática: Constrói os teus Kits de Genética!
 Actividade prática: Constrói os teus Kits de Genética! Mais uma vez vais vestir a tua bata de cientista e investigador e preparar o teu dia a dia no laboratório. Hoje é um dia especial, vais receber a
Actividade prática: Constrói os teus Kits de Genética! Mais uma vez vais vestir a tua bata de cientista e investigador e preparar o teu dia a dia no laboratório. Hoje é um dia especial, vais receber a
Conceitos Básico sobre Biologia molecular
 Conceitos Básico sobre Biologia molecular UFMS Mestre: Paula Cristhina Niz Xavier INTRODUÇÃO A biologia molecular tem aplicação expressiva na pesquisa de marcadores genéticos úteis no diagnóstico laboratorial.
Conceitos Básico sobre Biologia molecular UFMS Mestre: Paula Cristhina Niz Xavier INTRODUÇÃO A biologia molecular tem aplicação expressiva na pesquisa de marcadores genéticos úteis no diagnóstico laboratorial.
Identificação de sementes de soja geneticamente modificadas utilizando a técnica de PCR convencional
 Identificação de sementes de soja geneticamente modificadas utilizando a técnica de PCR convencional HONNA,P.T. 1 ; GIROTTO, L. 2 ; SOLDERA, M.C.A. 2 ; KANAMORI, N. 3 ;MARCELINO-GUIMARAES, F. C. 4 ; YAMAGUCHI-SHINOZAKI,
Identificação de sementes de soja geneticamente modificadas utilizando a técnica de PCR convencional HONNA,P.T. 1 ; GIROTTO, L. 2 ; SOLDERA, M.C.A. 2 ; KANAMORI, N. 3 ;MARCELINO-GUIMARAES, F. C. 4 ; YAMAGUCHI-SHINOZAKI,
CATÁLOGO DE KITS DE EXTRAÇÃO
 CATÁLOGO DE KITS DE EXTRAÇÃO KITS DE EXTRAÇÃO BIOPUR A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
CATÁLOGO DE KITS DE EXTRAÇÃO KITS DE EXTRAÇÃO BIOPUR A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
- HIBRIDAÇÃO DE SOUTHERN UTILIZANDO SONDAS NÃO RADIOACTIVAS 1ª
 TP3 e TP4 - HIBRIDAÇÃO DE SOUTHERN UTILIZANDO SONDAS NÃO RADIOACTIVAS 1ª Parte: A- Separação em gel de agarose e visualização do DNA cromossómico de S. elodea ATCC 31461 após hidrólise com BamHI, EcoRI,
TP3 e TP4 - HIBRIDAÇÃO DE SOUTHERN UTILIZANDO SONDAS NÃO RADIOACTIVAS 1ª Parte: A- Separação em gel de agarose e visualização do DNA cromossómico de S. elodea ATCC 31461 após hidrólise com BamHI, EcoRI,
Kit de Clonagem Flex-C
 Kit de Clonagem Flex-C Instruções de Uso DESCRIÇÃO O Kit de Clonagem Flex-C é altamente eficiente, rápido e de fácil uso para clonagem por PCR. A enzima Flex-C permite a clonagem direta de qualquer fragmento
Kit de Clonagem Flex-C Instruções de Uso DESCRIÇÃO O Kit de Clonagem Flex-C é altamente eficiente, rápido e de fácil uso para clonagem por PCR. A enzima Flex-C permite a clonagem direta de qualquer fragmento
Catálogo de Kits de Extração
 Catálogo de Kits de Extração Kits de Extração Biopur A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
Catálogo de Kits de Extração Kits de Extração Biopur A extração de DNA é o primeiro passo para diferentes procedimentos na Biologia Molecular. Este processo é parte fundamental para se obter alta eficiência
PROTOCOLO OPERACIONAL PARA TRANSFERÊNCIA DE CÉLULAS BACTERIANAS PARA MEIO LÍQUIDO
 Ministério da Agricultura e do Abastecimento Empresa Brasileira de Pesquisa Agropecuária-EMBRAPA Centro Nacional de Pesquisa de Agrobiologia-CNPAB ISSN 0104-6187 PROTOCOLO OPERACIONAL PARA TRANSFERÊNCIA
Ministério da Agricultura e do Abastecimento Empresa Brasileira de Pesquisa Agropecuária-EMBRAPA Centro Nacional de Pesquisa de Agrobiologia-CNPAB ISSN 0104-6187 PROTOCOLO OPERACIONAL PARA TRANSFERÊNCIA
BacBio. Crescimento, Renovação Celular e Reprodução: da teoria à prática. Coimbra, 2012/2013. Sandra Gamboa Andreia Quaresma Fernando Delgado
 BacBio Crescimento, Renovação Celular e Reprodução: da teoria à prática Coimbra, 2012/2013 Sandra Gamboa Andreia Quaresma Fernando Delgado Escolher Ciência PEC282 ESCOLA SUPERIOR AGRÁRIA DE COIMBRA BacBio
BacBio Crescimento, Renovação Celular e Reprodução: da teoria à prática Coimbra, 2012/2013 Sandra Gamboa Andreia Quaresma Fernando Delgado Escolher Ciência PEC282 ESCOLA SUPERIOR AGRÁRIA DE COIMBRA BacBio
Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio.
 ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
ATIVIDADE 2 - CÁLCULO DE CONCENTRAÇÃO Exercício 1. Calcule a concentração dos reagentes listados abaixo em mol L -1 Tabela 1. Propriedades de ácidos inorgânicos e hidróxido de amônio. Exercício 2. Calcule
Análises moleculares - DNA
 Análises moleculares - DNA Como o mapeamento genético contribui para a genética médica? A caracterização de um gene e suas mutações aumenta a compreensão da doença Aplicações: -Desenvolvimento de diagnóstico
Análises moleculares - DNA Como o mapeamento genético contribui para a genética médica? A caracterização de um gene e suas mutações aumenta a compreensão da doença Aplicações: -Desenvolvimento de diagnóstico
DISSEMINAÇÃO DE LEVEDURAS COMERCIAIS EM ECOSSISTEMAS VITIVINÍCOLAS
 DISSEMINAÇÃO DE LEVEDURAS COMERCIAIS EM ECOSSISTEMAS VITIVINÍCOLAS D. Schuller 1*, H. Alves 1, S. Dequin 2 e M. Casal 1 1 Centro de Biologia Universidade do Minho Portugal 2 Institut Nacional de la Recherche
DISSEMINAÇÃO DE LEVEDURAS COMERCIAIS EM ECOSSISTEMAS VITIVINÍCOLAS D. Schuller 1*, H. Alves 1, S. Dequin 2 e M. Casal 1 1 Centro de Biologia Universidade do Minho Portugal 2 Institut Nacional de la Recherche
Hibridação in situ por fluorescência FISH
 Universidade Estadual de Londrina Departamento de Biologia Geral Laboratório de Citogenética Animal - LACA Hibridação in situ por fluorescência FISH O protocolo descrito a seguir foi baseado nos procedimentos
Universidade Estadual de Londrina Departamento de Biologia Geral Laboratório de Citogenética Animal - LACA Hibridação in situ por fluorescência FISH O protocolo descrito a seguir foi baseado nos procedimentos
Em nossos experimento serão utilizadas células SH SY5Y, uma sublinhagem de células de neuroblastoma SK-N-SH, figura 1.
 Procedimentos Em nossos experimento serão utilizadas células SH SY5Y, uma sublinhagem de células de neuroblastoma SK-N-SH, figura 1. As células serão submetidas a estresse oxidativo por meio do tratamento
Procedimentos Em nossos experimento serão utilizadas células SH SY5Y, uma sublinhagem de células de neuroblastoma SK-N-SH, figura 1. As células serão submetidas a estresse oxidativo por meio do tratamento
NextGeneration ECO One-Step RT-qPCR Kit
 DNA EXPRESS BIOTECNOLOGIA NextGeneration ECO One-Step RT-qPCR Kit Kit para uso em RT-PCR em tempo real quantitativo (RT-qPCR) em único tubo contendo NextGeneration Transcriptase Reversa M-MLV RNAse Minus
DNA EXPRESS BIOTECNOLOGIA NextGeneration ECO One-Step RT-qPCR Kit Kit para uso em RT-PCR em tempo real quantitativo (RT-qPCR) em único tubo contendo NextGeneration Transcriptase Reversa M-MLV RNAse Minus
HEMOCENTRO RP TÉCNICA
 P. 1/9 1. OBJETIVO Genotipar os Alelos HLA em alta resolução. 2. APLICAÇÃO Aplica-se a amostras de DNA de pacientes e doadores. 3. RESPONSABILIDADE Assistentes de Laboratório, Técnicos, Aprimorandos, Bolsistas
P. 1/9 1. OBJETIVO Genotipar os Alelos HLA em alta resolução. 2. APLICAÇÃO Aplica-se a amostras de DNA de pacientes e doadores. 3. RESPONSABILIDADE Assistentes de Laboratório, Técnicos, Aprimorandos, Bolsistas
Polimerase Chain Reaction PCR
 Polimerase Chain Reaction PCR Reação em cadeia da polimerase Técnica in vitro utilizada para sintetizar muitas cópias de DNA Amplificar uma seqüência alvo específica Termociclador DNA molde dntp DNA polimerase
Polimerase Chain Reaction PCR Reação em cadeia da polimerase Técnica in vitro utilizada para sintetizar muitas cópias de DNA Amplificar uma seqüência alvo específica Termociclador DNA molde dntp DNA polimerase
Departamento de Biologia. Mestrado em Bioempreendedorismo e Biotecnologia de PAM
 Departamento de Biologia Mestrado em Bioempreendedorismo e Biotecnologia de PAM Protocolos das aulas práticas Docente: Rui Oliveira P1-Análise da actividade do promotor CTA1 com o gene repórter GFP Ligação
Departamento de Biologia Mestrado em Bioempreendedorismo e Biotecnologia de PAM Protocolos das aulas práticas Docente: Rui Oliveira P1-Análise da actividade do promotor CTA1 com o gene repórter GFP Ligação
RELAÇÃO DOS GENES ADH1 E ADH2 COM A TOLERÂNCIA AO ETANOL EM SACCHAROMYCES CEREVISIAE BY4741.
 RELAÇÃO DOS GENES ADH1 E ADH2 COM A TOLERÂNCIA AO ETANOL EM SACCHAROMYCES CEREVISIAE BY4741. P. S. COSTA 1,2,3, L. G. FIETTO 3 1 Universidade Estadual de Campinas, Faculdade de Engenharia Química 2 Centro
RELAÇÃO DOS GENES ADH1 E ADH2 COM A TOLERÂNCIA AO ETANOL EM SACCHAROMYCES CEREVISIAE BY4741. P. S. COSTA 1,2,3, L. G. FIETTO 3 1 Universidade Estadual de Campinas, Faculdade de Engenharia Química 2 Centro
4 O anticoagulante mais utilizado na coleta de sangue para a extração de DNA é:
 CONCURSO PARA VAGA DE TÉCNICO DE LABORATÓRIO PROVA ESPECÍFICA 1ª FASE NOME: RG: DATA: 1 A extração de DNA é possível na seguinte condição: 2 - Um rastro fragmentado de DNA em gel de agarose indica: 3 A
CONCURSO PARA VAGA DE TÉCNICO DE LABORATÓRIO PROVA ESPECÍFICA 1ª FASE NOME: RG: DATA: 1 A extração de DNA é possível na seguinte condição: 2 - Um rastro fragmentado de DNA em gel de agarose indica: 3 A
mundo inteiro com uma variedade de aplicações como clonagem, genotipagem e sequenciamento.
 mundo inteiro com uma variedade de aplicações como clonagem, genotipagem e sequenciamento. necessária para que você possa alcançar o melhor desempenho nesta técnica. AGAROSE A agarose é um polissacarídeo
mundo inteiro com uma variedade de aplicações como clonagem, genotipagem e sequenciamento. necessária para que você possa alcançar o melhor desempenho nesta técnica. AGAROSE A agarose é um polissacarídeo
Extração de DNA/RNA Viral. Instruções de uso K204
 Extração de DNA/RNA Viral Instruções de uso K204 Revisão: Novembro/2018 ÍNDICE Finalidade... 3 Princípio de Ação... 3 Apresentação... 3 Reagentes... 4 Equipamentos e Insumos Operacionais... 4 Condições
Extração de DNA/RNA Viral Instruções de uso K204 Revisão: Novembro/2018 ÍNDICE Finalidade... 3 Princípio de Ação... 3 Apresentação... 3 Reagentes... 4 Equipamentos e Insumos Operacionais... 4 Condições
Sequenciamento de DNA e PCR 2018 s1
 Sequenciamento de DNA e PCR 2018 s1 Prof. João Carlos Setubal DNA é microscópico como saber a composição de DNA? não existe microscópio suficientemente poderoso que permita simplesmente ler a molécula,
Sequenciamento de DNA e PCR 2018 s1 Prof. João Carlos Setubal DNA é microscópico como saber a composição de DNA? não existe microscópio suficientemente poderoso que permita simplesmente ler a molécula,
Procedimento Operacional Padrão - POP
 Página 1 de 10 IMT-POP-BB-0 Biobanco Procedimento Operacional Padrão para: Extração de DNA de sangue total POP: V. 1.0 Nome: Extração de DNA em sangue total Efetiva: dezembro, 22 autora: Erika Regina Manuli
Página 1 de 10 IMT-POP-BB-0 Biobanco Procedimento Operacional Padrão para: Extração de DNA de sangue total POP: V. 1.0 Nome: Extração de DNA em sangue total Efetiva: dezembro, 22 autora: Erika Regina Manuli
BIOQUÍMICA EXPERIMENTAL
 Departamento de Bioquímica Instituto de Química USP Apostila de protocolos Parte A BIOQUÍMICA EXPERIMENTAL QBQ 036N 05 Professores Carlos T. Hotta Ronaldo B. Quaggio Esta apostila foi desenvolvida originalmente
Departamento de Bioquímica Instituto de Química USP Apostila de protocolos Parte A BIOQUÍMICA EXPERIMENTAL QBQ 036N 05 Professores Carlos T. Hotta Ronaldo B. Quaggio Esta apostila foi desenvolvida originalmente
BETA - GLOBIN oligomix Alert kit controlo externo de qualidade do DNA extraído
 ÍNDICE USO PREVISTO pág. 1 APRESENTAÇÃO DO KIT pág. 1 CARACTERÍSTICAS DO KIT pág. 2 OUTROS PRODUTOS REQUERIDO pág. 2 MATERIAL INCLUÍDO NO KIT pág. 2 MATERIAL NECESSÁRIO NÃO INCLUÍDO NO KIT pág. 2 ADVERTÊNCIAS
ÍNDICE USO PREVISTO pág. 1 APRESENTAÇÃO DO KIT pág. 1 CARACTERÍSTICAS DO KIT pág. 2 OUTROS PRODUTOS REQUERIDO pág. 2 MATERIAL INCLUÍDO NO KIT pág. 2 MATERIAL NECESSÁRIO NÃO INCLUÍDO NO KIT pág. 2 ADVERTÊNCIAS
Sessão 1: Os Princípios e as Técnicas da Biologia Molecular do Séc XXI
 Sessão 1: Os Princípios e as Técnicas da Biologia Molecular do Séc XXI Menu do dia: -DNA RNA proteína - Sequenciação de genomas (Clonagem, electroforese em gel) - Transcritoma (Microarrays) - Organismos
Sessão 1: Os Princípios e as Técnicas da Biologia Molecular do Séc XXI Menu do dia: -DNA RNA proteína - Sequenciação de genomas (Clonagem, electroforese em gel) - Transcritoma (Microarrays) - Organismos
1 º Exame Engenharia Genética 11 de Janeiro de 2013 Duração: 2h30min.
 Nome: Curso: Nº 1 º Exame Engenharia Genética 11 de Janeiro de 2013 Duração: 2h30min. A bactéria Edwardsiella tarda causa septicémia hemorrágica em peixes bem como infecções gastrointestinais em humanos.
Nome: Curso: Nº 1 º Exame Engenharia Genética 11 de Janeiro de 2013 Duração: 2h30min. A bactéria Edwardsiella tarda causa septicémia hemorrágica em peixes bem como infecções gastrointestinais em humanos.
Princípios e Aplicações da Técnica de PCR
 Universidade Federal de Santa Catarina Centro de Ciências Biológicas XVIII Semana Acadêmica da Biologia- UFSC Curso teórico-prático Princípios e Aplicações da Técnica de PCR Prof. Dr. Rafael D Rosa Departamento
Universidade Federal de Santa Catarina Centro de Ciências Biológicas XVIII Semana Acadêmica da Biologia- UFSC Curso teórico-prático Princípios e Aplicações da Técnica de PCR Prof. Dr. Rafael D Rosa Departamento
II - ELECTROFORESE DE AMINOÁCIDOS
 II - ELECTROFORESE DE AMINOÁCIDOS Introdução Muitas moléculas biológicas apresentam carga eléctrica cujo valor e sinal depende das suas características e também do ph e da composição do meio em que se
II - ELECTROFORESE DE AMINOÁCIDOS Introdução Muitas moléculas biológicas apresentam carga eléctrica cujo valor e sinal depende das suas características e também do ph e da composição do meio em que se
UNIVERSIDADE FEDERAL DE SANTA CATARINA DEPARTAMENTO DE BIOLOGIA CELULAR, EMBRIOLOGIA E GENÉTICA LABORATÓRIO DE IMUNOLOGIA APLICADA À AQUICULTURA
 UNIVERSIDADE FEDERAL DE SANTA CATARINA DEPARTAMENTO DE BIOLOGIA CELULAR, EMBRIOLOGIA E GENÉTICA LABORATÓRIO DE IMUNOLOGIA APLICADA À AQUICULTURA ELETROFORESE DE DNA Nicolas Argenta da Conceição Email:
UNIVERSIDADE FEDERAL DE SANTA CATARINA DEPARTAMENTO DE BIOLOGIA CELULAR, EMBRIOLOGIA E GENÉTICA LABORATÓRIO DE IMUNOLOGIA APLICADA À AQUICULTURA ELETROFORESE DE DNA Nicolas Argenta da Conceição Email:
BIBLIOTECAS DE DNA E HIBRIDIZAÇÃO. FABIANA SEIXAS
 BIBLIOTECAS DE DNA E HIBRIDIZAÇÃO FABIANA SEIXAS email: fabianak@ufpel.edu.br ABORDAGENS... BIBLIOTECAS DE DNA -Bibliotecas de DNA Genômico -Bibliotecas de cdna TÉCNICAS DE HIBIDIZAÇÃO -Hibidização em
BIBLIOTECAS DE DNA E HIBRIDIZAÇÃO FABIANA SEIXAS email: fabianak@ufpel.edu.br ABORDAGENS... BIBLIOTECAS DE DNA -Bibliotecas de DNA Genômico -Bibliotecas de cdna TÉCNICAS DE HIBIDIZAÇÃO -Hibidização em
MARCADORES MOLECULARES
 ESALQ/USP MARCADORES MOLECULARES Base genética dos marcadores e usos no melhoramento de plantas e em estudos de diversidade genética e conservação Departamento de Genética ESTUDO DIRIGIDO 1. O que são
ESALQ/USP MARCADORES MOLECULARES Base genética dos marcadores e usos no melhoramento de plantas e em estudos de diversidade genética e conservação Departamento de Genética ESTUDO DIRIGIDO 1. O que são
no ensino da Microbiologia e da Genética: Estratégias de e-learning Uma abordagem prática com aplicação nos ensinos Básico B
 Estratégias de e-learning no ensino da Microbiologia e da Genética: Uma abordagem prática com aplicação nos ensinos Básico B e Secundário Teresa Vieira 2, Dorit Schuller 1 e Margarida Casal 1 1 Departamento
Estratégias de e-learning no ensino da Microbiologia e da Genética: Uma abordagem prática com aplicação nos ensinos Básico B e Secundário Teresa Vieira 2, Dorit Schuller 1 e Margarida Casal 1 1 Departamento
Funcional de Saccharomyces cerevisiae durante fermentação
 Bioenergética e Genética Funcional de Saccharomyces cerevisiae durante fermentação vinária durante a (Functional Genomics and Bioenergetics of Saccharomyces cerevisiae during winemaking) 100º Curso de
Bioenergética e Genética Funcional de Saccharomyces cerevisiae durante fermentação vinária durante a (Functional Genomics and Bioenergetics of Saccharomyces cerevisiae during winemaking) 100º Curso de
Recursos Genéticos Vegetais
 Recursos Genéticos Vegetais Caracterização x Avaliação Caracterização Alta herdabilidade Pouca influência ambiental Avaliação Baixa herdabilidade Muita influência ambiental Caracterização: Caracterização
Recursos Genéticos Vegetais Caracterização x Avaliação Caracterização Alta herdabilidade Pouca influência ambiental Avaliação Baixa herdabilidade Muita influência ambiental Caracterização: Caracterização
Extração de DNA do pinhão manso (Jatropha curcas L.) para análises de marcador AFLP
 Extração de DNA do pinhão manso (Jatropha curcas L.) para análises de marcador DNA extraction of physic nut (Jatropha curcas L.) for analyses of marker Tuany Priscila P. Costa 1 ; Carlos Antônio F. Santos
Extração de DNA do pinhão manso (Jatropha curcas L.) para análises de marcador DNA extraction of physic nut (Jatropha curcas L.) for analyses of marker Tuany Priscila P. Costa 1 ; Carlos Antônio F. Santos
Sequenciamento de DNA e PCR QBQ 102 Aula 6 (biomol)
 Sequenciamento de DNA e PCR QBQ 102 Aula 6 (biomol) Prof. João Carlos Setubal Replicação de DNA 5ʹ 3ʹ Se um dos nucleotídeos for defeituoso A replicação pára Reação da DNA Polimerase com dntps síntese
Sequenciamento de DNA e PCR QBQ 102 Aula 6 (biomol) Prof. João Carlos Setubal Replicação de DNA 5ʹ 3ʹ Se um dos nucleotídeos for defeituoso A replicação pára Reação da DNA Polimerase com dntps síntese
Prof. João Carlos Setubal
 Prof. João Carlos Setubal QBQ 204 Aula 6 (biomol) Sequenciamento de DNA e PCR Replicação de DNA 5ʹ 3ʹ Se um dos nucleotídeos for defeituoso A replicação pára Reação da DNA Polimerase com dntps síntese
Prof. João Carlos Setubal QBQ 204 Aula 6 (biomol) Sequenciamento de DNA e PCR Replicação de DNA 5ʹ 3ʹ Se um dos nucleotídeos for defeituoso A replicação pára Reação da DNA Polimerase com dntps síntese
Ficha de protocolo do QIAsymphony SP
 Fevereiro de 2017 Ficha de protocolo do QIAsymphony SP circdna_2000_dsp_v1 e circdna_4000_dsp_v1 Este documento é a ficha de protocolo do QIAsymphony circdna_2000_dsp_v1 e circdna_4000_dsp_v1, versão 1,
Fevereiro de 2017 Ficha de protocolo do QIAsymphony SP circdna_2000_dsp_v1 e circdna_4000_dsp_v1 Este documento é a ficha de protocolo do QIAsymphony circdna_2000_dsp_v1 e circdna_4000_dsp_v1, versão 1,
MARCADORES MOLECULARES: DO MELHORAMENTO A CONSERVAÇÃO. Aula 10. Maria Carolina Quecine Departamento de Genética
 MARCADORES MOLECULARES: DO MELHORAMENTO A CONSERVAÇÃO Aula 10 LGN232 Genética Molecular Maria Carolina Quecine Departamento de Genética mquecine@usp.br RELEMBRANDO. kit de genética molecular ENZIMAS DE
MARCADORES MOLECULARES: DO MELHORAMENTO A CONSERVAÇÃO Aula 10 LGN232 Genética Molecular Maria Carolina Quecine Departamento de Genética mquecine@usp.br RELEMBRANDO. kit de genética molecular ENZIMAS DE
PNEUMOCYSTIS JIROVECI oligomix Alert kit
 PNEUMOCYSTIS JIROVECI oligomix Alert kit pesquisa do DNA de Pneumocystis jiroveci ÍNDICE USO PREVISTO pág. 1 APRESENTAÇÃO DO KIT pág. 1 CARACTERÍSTICAS DO KIT pág. 2 OUTROS PRODUTOS REQUERIDO pág. 2 MATERIAL
PNEUMOCYSTIS JIROVECI oligomix Alert kit pesquisa do DNA de Pneumocystis jiroveci ÍNDICE USO PREVISTO pág. 1 APRESENTAÇÃO DO KIT pág. 1 CARACTERÍSTICAS DO KIT pág. 2 OUTROS PRODUTOS REQUERIDO pág. 2 MATERIAL
Departamento de Biologia da Universidade do Minho
 Departamento de Biologia da Universidade do Minho Mestrado em Bioempreendedorismo e Biotecnologia em Plantas Aromáticas e Medicinais Ano lectivo de 2007/2008 Protocolos das aulas práticas Rui Oliveira
Departamento de Biologia da Universidade do Minho Mestrado em Bioempreendedorismo e Biotecnologia em Plantas Aromáticas e Medicinais Ano lectivo de 2007/2008 Protocolos das aulas práticas Rui Oliveira
Amplificação, Detecção e Quantificação. Daniela Cochicho Luís Martins
 Amplificação, Detecção e Quantificação PCR em Tempo Real Daniela Cochicho Luís Martins I curso de Virologia Molecular em Oncologia PCR Clássico The polymerase chain reaction (PCR) is one of the most powerful
Amplificação, Detecção e Quantificação PCR em Tempo Real Daniela Cochicho Luís Martins I curso de Virologia Molecular em Oncologia PCR Clássico The polymerase chain reaction (PCR) is one of the most powerful
SEQUENCIAMENTO DE DNA
 Universidade Federal de Santa Catarina Centro de Ciências Biológicas Programa de Pós Graduação em Biotecnologia e Biociências SEQUENCIAMENTO DE DNA Patrícia H. Stoco Edmundo C. Grisard Sequenciamento DNA:
Universidade Federal de Santa Catarina Centro de Ciências Biológicas Programa de Pós Graduação em Biotecnologia e Biociências SEQUENCIAMENTO DE DNA Patrícia H. Stoco Edmundo C. Grisard Sequenciamento DNA:
Indicadores microbiológicos para qualidade do solo
 Universidade Federal Rural de Pernambuco Programa de Pós-Graduação em Ciência do Solo Disciplina: Seminário II Professor: Mario de Andrade Lira Junior Indicadores microbiológicos para qualidade do solo
Universidade Federal Rural de Pernambuco Programa de Pós-Graduação em Ciência do Solo Disciplina: Seminário II Professor: Mario de Andrade Lira Junior Indicadores microbiológicos para qualidade do solo
EXTRAÇÃO DE DNA E ELETROFORESE
 EXTRAÇÃO DE DNA E ELETROFORESE Isolamento de ácidos nucléicos de células e tecidos Extração de ácidos nucléicos Obtenção do material: Vírus Bactérias; fungos Célula vegetal / célula animal Extração de
EXTRAÇÃO DE DNA E ELETROFORESE Isolamento de ácidos nucléicos de células e tecidos Extração de ácidos nucléicos Obtenção do material: Vírus Bactérias; fungos Célula vegetal / célula animal Extração de
VARIABILIDADE GENÉTICA ENTRE GENITORES PARA O MAPEAMENTO MOLECULAR DO ALGODOEIRO
 VARIABILIDADE GENÉTICA ENTRE GENITORES PARA O MAPEAMENTO MOLECULAR DO ALGODOEIRO Jair Moisés de Sousa (UFRN / jair.moises@hotmail.com), Ivandilson P. Pinto de Meneze (UFRN), Milena Ferreira Alves (UFRN),
VARIABILIDADE GENÉTICA ENTRE GENITORES PARA O MAPEAMENTO MOLECULAR DO ALGODOEIRO Jair Moisés de Sousa (UFRN / jair.moises@hotmail.com), Ivandilson P. Pinto de Meneze (UFRN), Milena Ferreira Alves (UFRN),
PARVOVIRUS B19 oligomix Alert kit
 CARACTERÍSTICAS DO KIT pesquisa do DNA de Parvovirus B19 ÍNDICE USO PREVISTO pág. 1 APRESENTAÇÃO DO KIT pág. 1 CARACTERÍSTICAS DO KIT pág. 2 OUTROS PRODUTOS REQUERIDO pág. 2 MATERIAL INCLUÍDO NO KIT pág.
CARACTERÍSTICAS DO KIT pesquisa do DNA de Parvovirus B19 ÍNDICE USO PREVISTO pág. 1 APRESENTAÇÃO DO KIT pág. 1 CARACTERÍSTICAS DO KIT pág. 2 OUTROS PRODUTOS REQUERIDO pág. 2 MATERIAL INCLUÍDO NO KIT pág.
CONSTRUÇÃO DE BACTÉRIAS VERDES FLUORESCENTES PARA USO DIDÁTICO
 UNIVERSIDADE FEDERAL DE MINAS GERAIS INSTITUTO DE CIENCIAS BIOLOGICAS PROJETO DE BIOLOGIA MOLECULAR CONSTRUÇÃO DE BACTÉRIAS VERDES FLUORESCENTES PARA USO DIDÁTICO Débora do Vale Gabriela Modenesi Gabriela
UNIVERSIDADE FEDERAL DE MINAS GERAIS INSTITUTO DE CIENCIAS BIOLOGICAS PROJETO DE BIOLOGIA MOLECULAR CONSTRUÇÃO DE BACTÉRIAS VERDES FLUORESCENTES PARA USO DIDÁTICO Débora do Vale Gabriela Modenesi Gabriela
MEIOS DE CULTURA PARA LEVEDURAS
 MONITORAMENTO TEÓRICO E PRÁTICO DA FERMENTAÇÃO ETANÓLICA MEIOS DE CULTURA PARA LEVEDURAS COORDENADORES: Profa. Dra. Dejanira Franceschi de Angelis Prof. Dr. Octávio Antonio Valsechi RIO CLARO 2006 MEIOS
MONITORAMENTO TEÓRICO E PRÁTICO DA FERMENTAÇÃO ETANÓLICA MEIOS DE CULTURA PARA LEVEDURAS COORDENADORES: Profa. Dra. Dejanira Franceschi de Angelis Prof. Dr. Octávio Antonio Valsechi RIO CLARO 2006 MEIOS
ACÇÃO DE FORMAÇÃO GUIÃO DE ACTIVIDADE PRÁTICA. (Versão Professor)
 Escola Secundária Marques de Castilho ÁGUEDA ACÇÃO DE FORMAÇÃO UTILIZAÇÃO DOS NOVOS LABORATÓRIOS ESCOLARES GUIÃO DE ACTIVIDADE PRÁTICA FUNCIONAMENTO DE UM SISTEMA TAMPÃO (Versão Professor) Formando: Henrique
Escola Secundária Marques de Castilho ÁGUEDA ACÇÃO DE FORMAÇÃO UTILIZAÇÃO DOS NOVOS LABORATÓRIOS ESCOLARES GUIÃO DE ACTIVIDADE PRÁTICA FUNCIONAMENTO DE UM SISTEMA TAMPÃO (Versão Professor) Formando: Henrique
Microbiologia alimentar Medronho. Maria João de Almeida Pessoa Trigo. Escola Secundária Fonseca de Benevides, Lisboa 4 de Fevereiro de 2014
 Microbiologia alimentar Medronho Maria João de Almeida Pessoa Trigo Escola Secundária Fonseca de Benevides, Lisboa 4 de Fevereiro de 2014 NORMAS DE SEGURANÇA Principais Normas de Segurança em Laboratório
Microbiologia alimentar Medronho Maria João de Almeida Pessoa Trigo Escola Secundária Fonseca de Benevides, Lisboa 4 de Fevereiro de 2014 NORMAS DE SEGURANÇA Principais Normas de Segurança em Laboratório
BORRELIA spp. oligomix Alert kit
 BORRELIA spp. oligomix Alert kit ÍNDICE USO PREVISTO pág. 1 APRESENTAÇÃO DO KIT pág. 1 CARACTERÍSTICAS DO KIT pág. 2 OUTROS PRODUTOS REQUERIDO pág. 2 MATERIAL INCLUÍDO NO KIT pág. 2 MATERIAL NECESSÁRIO
BORRELIA spp. oligomix Alert kit ÍNDICE USO PREVISTO pág. 1 APRESENTAÇÃO DO KIT pág. 1 CARACTERÍSTICAS DO KIT pág. 2 OUTROS PRODUTOS REQUERIDO pág. 2 MATERIAL INCLUÍDO NO KIT pág. 2 MATERIAL NECESSÁRIO
Identificação de leveduras. Métodos moleculares
 Identificação de leveduras Métodos moleculares DNA ribossomal Os genes de RNA ribossomal de fungos existem como uma família de genes com múltiplas cópias compostas de sequências de DNA altamente similares
Identificação de leveduras Métodos moleculares DNA ribossomal Os genes de RNA ribossomal de fungos existem como uma família de genes com múltiplas cópias compostas de sequências de DNA altamente similares
2 Contexto Biológico Genômica
 15 2 Contexto Biológico Neste capítulo abordaremos o contexto biológico para o entendimento deste trabalho. Serão abordados os aspectos gerais da genômica, expostos os processos do sequenciamento genético
15 2 Contexto Biológico Neste capítulo abordaremos o contexto biológico para o entendimento deste trabalho. Serão abordados os aspectos gerais da genômica, expostos os processos do sequenciamento genético
Eletroforese de DNA. Gabriel M. Matos Nicolas Conceição
 Eletroforese de DNA Gabriel M. Matos Nicolas Conceição Eletroforese Usada para separar, identificar e purificar fragmentos de DNA; Bastante sensível, capaz de detectar até 20 pg de DNA; Permite a recuperação
Eletroforese de DNA Gabriel M. Matos Nicolas Conceição Eletroforese Usada para separar, identificar e purificar fragmentos de DNA; Bastante sensível, capaz de detectar até 20 pg de DNA; Permite a recuperação
PCR em Tempo Real / PCR quantitativa (qpcr)
 em Tempo Real / quantitativa (q) Dra. Elisabet Marti Serrano emartiserrano@gmail.com (Polymerase Chain Reaction) Amplificação in vitro de uma sequência específica de DNA - Primers o iniciadores - DNA polimerase
em Tempo Real / quantitativa (q) Dra. Elisabet Marti Serrano emartiserrano@gmail.com (Polymerase Chain Reaction) Amplificação in vitro de uma sequência específica de DNA - Primers o iniciadores - DNA polimerase
Departamento de Zoologia da Universidade de Coimbra
 Departamento de Zoologia da Universidade de Coimbra Ana Luísa Carvalho Amplificação de um fragmento de DNA por PCR Numa reacção em cadeia catalizada pela DNA polimerase (Polymerase Chain Reaction - PCR),
Departamento de Zoologia da Universidade de Coimbra Ana Luísa Carvalho Amplificação de um fragmento de DNA por PCR Numa reacção em cadeia catalizada pela DNA polimerase (Polymerase Chain Reaction - PCR),
Biologia Celular e Molecular
 DEPARTAMENTO DE ZOOLOGIA FACULDADE DE CIÊNCIAS E TECNOLOGIA UNIVERSIDADE DE COIMBRA Biologia Celular e Molecular Detecção da presença de organismos geneticamente modificados em alimento por PCR 2007-2008
DEPARTAMENTO DE ZOOLOGIA FACULDADE DE CIÊNCIAS E TECNOLOGIA UNIVERSIDADE DE COIMBRA Biologia Celular e Molecular Detecção da presença de organismos geneticamente modificados em alimento por PCR 2007-2008
HEMOCENTRO RP TÉCNICA
 P. 1/6 1. OBJETIVO Amplificar os genes HLA-A, B, C, DRB1, e DQA1/DQB1 para posterior identificação dos seus respectivos grupos alélicos. *1 2. APLICAÇÃO Aplica-se às amostras de DNA genômico de doadores
P. 1/6 1. OBJETIVO Amplificar os genes HLA-A, B, C, DRB1, e DQA1/DQB1 para posterior identificação dos seus respectivos grupos alélicos. *1 2. APLICAÇÃO Aplica-se às amostras de DNA genômico de doadores
Instrução normativa 62/2003: Contagem de coliformes pela técnica do NMP e em placas
 Instrução normativa 62/2003: Contagem de coliformes pela técnica do NMP e em placas CAPÍTULO IX NÚMERO MAIS PROVÁVEL DE COLIFORMES TOTAIS E COLIFORMES TERMOTOLERANTES EM ÁGUA E GELO 1. OBJETIVOS E ALCANCE
Instrução normativa 62/2003: Contagem de coliformes pela técnica do NMP e em placas CAPÍTULO IX NÚMERO MAIS PROVÁVEL DE COLIFORMES TOTAIS E COLIFORMES TERMOTOLERANTES EM ÁGUA E GELO 1. OBJETIVOS E ALCANCE
Paulo no Departamento de Triagem de doadores e no Departamento de. As amostras de plasma e PBMC de dois grupos de indivíduos
 MATERIAIS E MÉTODOS 54 4. MATERIAIS E MÉTODOS 4.1. COLETA DE AMOSTRAS 4.1.1. Local do estudo O Estudo foi realizado na Fundação Pró-Sangue Hemocentro de São Paulo no Departamento de Triagem de doadores
MATERIAIS E MÉTODOS 54 4. MATERIAIS E MÉTODOS 4.1. COLETA DE AMOSTRAS 4.1.1. Local do estudo O Estudo foi realizado na Fundação Pró-Sangue Hemocentro de São Paulo no Departamento de Triagem de doadores
Marcadores Moleculares
 Marcadores Moleculares Marcadores Moleculares Marcadores Genéticos Características polimórficas: marcadores de variabilidade genética entre indivíduos, populações, espécies e taxons superiores. Marcadores
Marcadores Moleculares Marcadores Moleculares Marcadores Genéticos Características polimórficas: marcadores de variabilidade genética entre indivíduos, populações, espécies e taxons superiores. Marcadores
PREPARAÇÃO DE CÉLULAS COMPETENTES DE Escherichia coli HB101
 PREPARAÇÃO DE CÉLULAS COMPETENTES DE Escherichia coli HB101 OBJECTIVO Obtenção de células competentes de Escherichia coli através de um método químico, para transformação de DNA plasmídico INTRODUÇÃO O
PREPARAÇÃO DE CÉLULAS COMPETENTES DE Escherichia coli HB101 OBJECTIVO Obtenção de células competentes de Escherichia coli através de um método químico, para transformação de DNA plasmídico INTRODUÇÃO O
- Sequenciamento de genomas nada mais é que a determinação da ordem linear dos nucleotídeos ou bases nitrogenadas de um genoma.
 Sequenciamento de genomas - Sequenciamento de genomas nada mais é que a determinação da ordem linear dos nucleotídeos ou bases nitrogenadas de um genoma. O sequenciamento de um genoma é geralmente referido
Sequenciamento de genomas - Sequenciamento de genomas nada mais é que a determinação da ordem linear dos nucleotídeos ou bases nitrogenadas de um genoma. O sequenciamento de um genoma é geralmente referido
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012. Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA EXTRACÇÃO
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA EXTRACÇÃO
Preparação do gel de poliacrilamida
 Preparação do gel de poliacrilamida Materiais: - álcool 70% (limpeza) - SDS 10% - água Milli-Q - APS 10% - acrilamida/ bisacrilamida 40% - TEMED - tampão Tris-HCl, ph 8,8 e 6,8 - vidros 1º Limpar os vidros
Preparação do gel de poliacrilamida Materiais: - álcool 70% (limpeza) - SDS 10% - água Milli-Q - APS 10% - acrilamida/ bisacrilamida 40% - TEMED - tampão Tris-HCl, ph 8,8 e 6,8 - vidros 1º Limpar os vidros
PCR (Polymerase chain reaction) Reação em cadeia da DNA polimerase. e suas aplicações
 PCR (Polymerase chain reaction) Reação em cadeia da DNA polimerase e suas aplicações Bianca Zingales zingales@iq.usp.br PCR é uma Técnica - Desenvolvida por Kary Mullis e colaboradores em 1983 - É um método
PCR (Polymerase chain reaction) Reação em cadeia da DNA polimerase e suas aplicações Bianca Zingales zingales@iq.usp.br PCR é uma Técnica - Desenvolvida por Kary Mullis e colaboradores em 1983 - É um método
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010. Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA PRÁTICA Determinação
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA PRÁTICA Determinação
MARCADORES MOLECULARES: AFLP E RFLP
 Universidade Federal de Pelotas Programa de Pós Graduação em Agronomia Disciplina de Biotecnologia Aplicada ao Melhoramento MARCADORES MOLECULARES: AFLP E RFLP Prof. PhD. Antonio Costa de Oliveira Gabriela
Universidade Federal de Pelotas Programa de Pós Graduação em Agronomia Disciplina de Biotecnologia Aplicada ao Melhoramento MARCADORES MOLECULARES: AFLP E RFLP Prof. PhD. Antonio Costa de Oliveira Gabriela
DNA recombinante. Nilce M. Martinez Rossi Depto de Genética
 DNA recombinante Nilce M. Martinez Rossi Depto de Genética Descobertas marcantes 1962 Arber, Nathans e Smith Enzimas de restrição 1966 Niremberg, Ochoa e Khorana Elucidaram o código genético 1961 Marmur
DNA recombinante Nilce M. Martinez Rossi Depto de Genética Descobertas marcantes 1962 Arber, Nathans e Smith Enzimas de restrição 1966 Niremberg, Ochoa e Khorana Elucidaram o código genético 1961 Marmur
Como obter uma planta transgénica à boleia do. Agrobacterium tumefaciens
 Como obter uma planta transgénica à boleia do Agrobacterium tumefaciens Participantes Adilson Vaz (Lisboa) Ana Rita Araújo (Aveiro) Ana Sofia Martins (Vila Real) André Pereira (Lisboa) Entidade: Universidade
Como obter uma planta transgénica à boleia do Agrobacterium tumefaciens Participantes Adilson Vaz (Lisboa) Ana Rita Araújo (Aveiro) Ana Sofia Martins (Vila Real) André Pereira (Lisboa) Entidade: Universidade
BIOPUR KIT Extração Mini Mag SLNB96
 BIOPUR KIT Extração Mini Mag SLNB96 Instruções de Uso 1. USO PRETENDIDO O BIOPUR Kit Mini Mag SLNB96 é destinado para extração de DNA genômico de alta qualidade a partir de 200µl de sangue total. O procedimento
BIOPUR KIT Extração Mini Mag SLNB96 Instruções de Uso 1. USO PRETENDIDO O BIOPUR Kit Mini Mag SLNB96 é destinado para extração de DNA genômico de alta qualidade a partir de 200µl de sangue total. O procedimento
AMPLIFICAÇÃO DO GENE DA PROTEÍNA E DO VÍRUS DENV ATRAVÉS DA TÉCNICA DE REAÇÃO EM CADEIA DA POLIMERASE (PCR)
 AMPLIFICAÇÃO DO GENE DA PROTEÍNA E DO VÍRUS DENV ATRAVÉS DA TÉCNICA DE REAÇÃO EM CADEIA DA POLIMERASE (PCR) Beatriz Dantas Guimarães (1); Lucas Linhares de Locio (2); Herbert Crisóstomo dos Santos Araújo
AMPLIFICAÇÃO DO GENE DA PROTEÍNA E DO VÍRUS DENV ATRAVÉS DA TÉCNICA DE REAÇÃO EM CADEIA DA POLIMERASE (PCR) Beatriz Dantas Guimarães (1); Lucas Linhares de Locio (2); Herbert Crisóstomo dos Santos Araújo
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata)
 Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
Alunos: Carlos Guilherme Reis, Roberta Silveira Professora: Fabiana Seixas Disciplina: Biologia Molecular
 Alunos: Carlos Guilherme Reis, Roberta Silveira Professora: Fabiana Seixas Disciplina: Biologia Molecular O que é PCR? Aplicações Técnicas: -Nested-PCR e artigos relacionados -PCR-Elisa e artigos relacionados
Alunos: Carlos Guilherme Reis, Roberta Silveira Professora: Fabiana Seixas Disciplina: Biologia Molecular O que é PCR? Aplicações Técnicas: -Nested-PCR e artigos relacionados -PCR-Elisa e artigos relacionados
Estudos das ômicas: Genômica; Transcriptomica; Metagenômica. Aula 7
 Estudos das ômicas: Genômica; Transcriptomica; Metagenômica Aula 7 DOGMA DA GENÉTICA MOLECULAR Genoma Transcriptoma Proteoma DOGMA DA GENÉTICA MOLECULAR Genômica Transcriptômica Proteômica Regiões codantes,
Estudos das ômicas: Genômica; Transcriptomica; Metagenômica Aula 7 DOGMA DA GENÉTICA MOLECULAR Genoma Transcriptoma Proteoma DOGMA DA GENÉTICA MOLECULAR Genômica Transcriptômica Proteômica Regiões codantes,
Contagem Padrão em Placas. Profa. Leila Larisa Medeiros Marques
 Contagem Padrão em Placas Profa. Leila Larisa Medeiros Marques 1. OBJETIVOS E ALCANCE Estabelecer procedimento para a contagem padrão de microrganismos mesófilos aeróbios estritos e facultativos viáveis.
Contagem Padrão em Placas Profa. Leila Larisa Medeiros Marques 1. OBJETIVOS E ALCANCE Estabelecer procedimento para a contagem padrão de microrganismos mesófilos aeróbios estritos e facultativos viáveis.
Departamento de Biologia da Universidade do Minho
 Departamento de Biologia da Universidade do Minho Mestrado em Genética Molecular Ano lectivo de 2004/2005, edição de 2004-2006 Estudo da regulação do gene STL1 codificando o sistema de simporte H + /glicerol
Departamento de Biologia da Universidade do Minho Mestrado em Genética Molecular Ano lectivo de 2004/2005, edição de 2004-2006 Estudo da regulação do gene STL1 codificando o sistema de simporte H + /glicerol
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata)
 Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
Hibridação in situ fluorescente em corte histológico (Câncer de Próstata) FISH em tecido incluído em parafina: Four Colour PTEN Deletion Probe O protocolo de FISH descrito abaixo é recomendado para cortes
TEÓRICA 10 DOCENTES: Prof. Helena Galvão (responsável componente teórico) Prof. Margarida Reis (componente prático)
 TEÓRICA 10 DOCENTES: Prof. Helena Galvão (responsável componente teórico) Prof. Margarida Reis (componente prático) TAXONOMIA BACTERIANA Conceitos e Definições Conceito de espécie bacteriana é complexo.
TEÓRICA 10 DOCENTES: Prof. Helena Galvão (responsável componente teórico) Prof. Margarida Reis (componente prático) TAXONOMIA BACTERIANA Conceitos e Definições Conceito de espécie bacteriana é complexo.
Cargo: D-41 Técnico Laboratório - Biotecnologia - Análise de Proteínas
 da Prova Prática QUESTÃO 1: Cargo: D-41 Técnico Laboratório - Biotecnologia - Análise de Proteínas Apresenta-se abaixo um protocolo para preparação de géis SDS-PAGE a ser utilizado em uma análise de confirmação
da Prova Prática QUESTÃO 1: Cargo: D-41 Técnico Laboratório - Biotecnologia - Análise de Proteínas Apresenta-se abaixo um protocolo para preparação de géis SDS-PAGE a ser utilizado em uma análise de confirmação
Teoria da Prática: Transporte de Glicídios
 Teoria da Prática: Transporte de Glicídios INTRODUÇÃO Os estudos dos fatores que afetam a síntese enzimática nos microrganismos levaram à hipótese de que há duas classes de enzimas: as constitutivas e
Teoria da Prática: Transporte de Glicídios INTRODUÇÃO Os estudos dos fatores que afetam a síntese enzimática nos microrganismos levaram à hipótese de que há duas classes de enzimas: as constitutivas e
