Alunos: Fredson de Araujo Vasconcelos, Alexandre Bergantini de Souza, Will Robson M. Rocha, Victor Bonfim
|
|
|
- Rafael Palha Garrido
- 8 Há anos
- Visualizações:
Transcrição
1 Astroquímica Mestrado e Doutorado em Física e Astronomia Prof. Dr. Sergio Pilling Alunos: Fredson de Araujo Vasconcelos, Alexandre Bergantini de Souza, Will Robson M. Rocha, Victor Bonfim AULA 4 - MOLÉCULAS ORGÂNICAS NO MEIO INTERESTELAR. MOLÉCULAS ORGÂNICAS COMPLEXAS. 1. INTRODUÇÃO 1.1 O Meio Interestelar O Meio Interestelar (MI) compreende todo o material (gás, poeira e radiação) entre as estrelas. Grande parte do material do MI foi ejetado por estrelas mortas e antigas. O meio interestelar é composta principalmente por gás (99%) e poeira (1%). Do gás presente no MI, 90 % é constituído por hidrogênio molecular ou atômico, 9% de hélio e menos de 1% formado por átomos tais como C, N e O e traços de outras moléculas. Figura 1. Imagens ópticas revelando nuvens de gás e poeira na nebulosa de Órion. A imagem de infravermelhos (direita) mostra as estrelas de formação recente brilhando na nebulosa. Crédito: C. R. O'Dell-Universidade Vanderbilt, NASA/ ESA. A poeira interestelar, por outro lado, é composta basicamente por silicatos, óxidos e espécies carbonáceas diversas (grafite, carbono amorfo, PAHs, SiC), gelo (H2O), Fe, Mg, etc,). Acredita-se que um grão de poeira típico tenha o diâmetro de 10-7 metros e seja composto por carbono com uma estrutura cristalina tipo grafite, misturado com silicatos como, por exemplo, a olivina - MgSiO3- ( Essa poeira circunda algumas estrelas, refletindo sua luz e formando uma nebulosa de reflexão, de cor predominantemente azulada. Figura 2. Nebulosa de reflexão NGC1999, constelação de Orion. Credito: NASA and The Hubble Heritage Team (STScI). A temperatura média do meio interestelar, em uma região escura, é cerca de 100 K. A densidade do meio 1
2 interestelar também é muito baixa sendo, em média, de 1 a 10 átomos por centímetro cúbico. Diversas regiões integram o meio interestelar como as Nuvens Difusas (quentes e rarefeitas) com densidade menor que 1, Regiões ionizadas (HII, T~10 4 K), Nuvens Densas (N~10 5 ), Nuvens Moleculares ( T~104 K ), Glóbulos de Bock, Discos Protoplanetários, Envoltórios Circunstelares, Nebulosas Planetárias entre outras. 1.2 MOLÉCULAS INTERESTELARES Várias moléculas diferentes foram identificadas em regiões interstelares circunsestelares e a maior parte deles são orgânicas na natureza. Essas moléculas estão concentradas principalmente na nuvens densas, ou nuvens moleculares. São geralmente moléculas orgânicas e apresentam uma grande variedade, compreendendo hidretos, óxidos simples, sulfetos, derivados do acetileno, aldeídos, álcoois, éteres, moléculas cíclicas e radicais (Maciel, 2002). A Tabela 1 mostra as várias moléculas encontradas no Meio Interestelar e circunstelar. Tabela 1. Moléculas interestelares e circumestelares como compilado por Al Wootten. Fonte: Ehrenfreund and Charnley, As moléculas são detectadas a partir de suas linhas espectrais. Estas linhas são geradas a partir de transições entre os diferentes níveis eletrônicos ou de transições entre diferentes níveis de rotação. A detecção ocorre nas faixas do infravermelho, micro-ondas ou de rádio do espectro. A primeira molécula interestelar (CH) foi identificada em 1937 (Swings e Rosenfeld, 1937). As moléculas interestelares são formadas em nuvens moleculares interestelares ou circunstelares. Em geral ocorre quando uma molécula é ionizada, geralmente quando um raio cósmico a atinge. A molécula normalmente adquire uma carga positiva e é atraída eletrostaticamente por elétrons a partir de outra molécula neutra nas proximidades. Os compostos também podem ser gerados a partir de reações entre átomos e moléculas neutras, embora este processo seja muito lento. 2
3 A presença de íons dentro das nuvens moleculares é assegurada pela radiação UV ou pela propagação de partículas energéticas - os raios cósmicos, e a carga elétrica de um dos reagentes resultam em uma força de atração, que favorece a reação. Exemplos dos principais processos são (Maciel, 2002): C + hν C + + e (1) H 2 + r.c. H e + r.c. (2) onde r.c. significa raios cósmicos. Nas nuvens interestelares as reações íon-molécula frequentemente envolvem o H 2. Por exemplo, o íon H 2 + produzido pela reação 2 pode desencadear as seguintes reações em nuvens densas (Maciel, 2002): H H 2 H H (3) H O OH + + H 2 (4) OH + + H 2 H 2 O + + H (5) H 2 O + + H 2 H 3 O + + H (6) H 3 O + + e H 2 O + H (7) Com a produção de H 2 O na reação de recombinação dissociativa 7. Essa reação pode ser substituída pela formação de OH, como por exemplo H 3 O + + e OH + H 2 (8) O mesmo resultado, isto é, a formação de H 2 O e OH, pode resultar da reação: O + + H 2 OH + + H (9) seguindo-se, então, as reações 5 a MOLÉCULAS ORGÂNICAS NO MEIO INTERESTELAR O carbono é encontrado no espaço em todas as suas formas alotrópicas: diamante, grafite e fulereno (Cataldo et al., 2004). Observações astronômicas na última década mostraram que compostos carbonáceos (moléculas gasosas e sólidas) são onipresentes em nossa própria galáxia, bem como em galáxias distantes (Ehrenfreund et al. 2006a). O primeiro enriquecimento químico do universo podem provavelmente ser ligado à primeira geração de estrelas (SPAANS 2004). As grandes abundâncias de carbono já estão extrapolados a partir de observações das linhas forte do C [II] e CO para os mais distantes quasares (Bertoldi et al., 2003). Carbono no espaço foi produzido pela primeira vez no interior das estrelas em reações de fusão e, posteriormente, foi lançada ao espaço interestelar e intergaláctico durante o colapso estelar e de explosões de supernovas (Ehrenfreund and Cami, 2010). Nas regiões mais densas do espaço interestelar, as chamadas nuvens interestelares, via química ativa, forma moléculas de carbono simples e complexos (van Dishoeck e Blake, 1998 ). Envelopes circumestelar são considerados como os maiores fábricas de química do carbono no espaço (Kwok, 2009). 2.1 Moléculas orgânicas em densas nuvens Densas nuvens são os locais de nascimento de estrelas de todas as massas e seus sistemas planetários (Ehrenfreund and Charnley,2000). Essas regiões do MI apresentam várias classes orgânicas tais como 3
4 nitrilas, os aldeídos, álcoois, ácidos, cetonas, éteres, aminas e amidas, assim como muitos compostos de hidrocarbonetos de cadeia longa. A química do carbono nas nuvens interestelares densas é também baseada nas reações íon-molécula, em especial a formação de CO. A partir do íon H 3 + formado em 3 e de maneira semelhante as reações 4 a 6, temos: H C CH + + H 2 (10) CH + + H 2 CH H (11) CH H 2 CH H (12) A formação do CO é feita, então, pelas reações: CH O HCO + + H 2 (13) HCO + + e CO + H (14) As reações íon - molécula estão, em geral, envolvidas na formação das moléculas mais abundantes que são observadas no meio interestelar, e têm também um papel importante na síntese de moléculas longas, como os cianopoliacetilenos HC 9 N e HC 11 N. De fato, acredita-se que reações íon-molécula envolvendo NH 3 ou NH 2 levem à produção de HCN, a partir do qual são formadas as moléculas mais complexas por incremento de pares de átomos de carbono (Maciel, 2002). Nas densas nuvens interestelares detecções ou verificações de identificações anteriores possíveis incluem o íon H 3 O +, que é um intermediário na produção de H 2 O e O 2, o radical CCO, que é isoeletrônico com HCCN, o íon SO +, HCCNC, CCCNH, H 2 C 3 e H 2 C 4 ( Irvine, 1995). 2.2 Moléculas Orgânicas em Nuvens Difusas Regiões difusas do MI têm densidades de gás na faixa cm -3, temperaturas em fase gasosa de K, e as temperaturas de superfície de grãos de talvez 20 K. Radiação Ultravioleta e visível de estrelas tendem a penetrar através de material difuso, e processos de fotodissociação e fotoionização são importantes para reduzir as concentrações de moléculas. Com efeito, o gás é composto principalmente de material atômico, exceto para o caso de hidrogênio, o elemento dominante, que é igualmente dividida em átomos e moléculas neutras (Herbst E, 2005). Desde a descoberta inicial de moléculas diatômicas simples no espaço interestelar, CH, CN e CH + (Swings & Rosenfeld 1937, McKellar 1940, Douglas & Herzberg 1941), muitas outras moléculas foram detectados no meio difuso dominado por fótons, embora em abundância menor do que a encontrada em nuvens densas. Espécies detectadas incluem HCO +, CO, OH, C 2, HCN, HNC, CN, CS e H 2 CO (Lucas & Liszt 1997). Lucas & Liszt (2000) detectaram C 2 H and c-c 3 H 2 em várias nuvens extragalácticas difusas e os limites máximos obtidos na coluna densidades l-c 3 H e C 4 H. A abundância C 2 H varia pouco de nuvens densas para difusas enquanto a abundância c-c 3 H 2 é marcadamente maior em densas nuvens. Reações das moléculas neutras CH e CH 2 com C + podem levar à formação e acumulação de hidrocarbonetos poliatômicos. Moléculas diatômicas (eg CH, CH +, OH, NH, C 2, CO) e duas espécies triatômicas (H + 3, C 3 ) foram detectados na absorção de infravermelho, óptico e ultravioleta usando estrelas de fundo como lâmpadas. As moléculas orgânicas presentes no meio difuso pode ter origem de três maneiras: (i) através de reações em fase gasosa, onde cálculos de modelo de nuvens dispersantes permitem a formação de moléculas de até 64 átomos de carbono com reações íon-molécula e reações neutro -neutro (Bettens & Herbst 1996); (ii) por reações em envelopes circunestelares e posterior mistura para o meio difuso (somente espécie fotoresistente) e (3) a partir de poeira carbonácea por reações fotoquímicas e colisões de grãos (Ehrenfreund and Charnley, 2000). Reações de superfície de grãos também foram sugeridas, mas estes só são esperados para produzir hidretos simples, por exemplo, NH (Wagenblast et al 1993). Nas nuvens difusas, o principal meio de destruição de moléculas é a fotodissociação, como na reação a seguir: 4
5 OH + hν O + H. Em nuvens difusas a penetração da radiação produz íons reativos como o C +, que se associa radiativamente com H 2. C + + H 2 CH hν (15) O produto (CH 2 + ) pode sofrer reações como nas equações 12 a 14 ou formar CH ou CH 2 pelas reações CH e CH + H 2 (16) CH e CH 2 + H (17) As moléculas em nuvens interestelares não protegidas pelos grãos de poeira podem ser destruídas pela radiação ultravioleta em escalas de tempo relativamente curtas, da ordem de algumas centenas de anos (Maciel, 2002). 2.3 Moléculas Orgânicas Formadas na Superfície de Grãos As partículas de poeira presentes em nuvens moleculares frias são catalisadores químicos importantes porque podem agregar mantos de grãos de gelo com a acreção e reação de átomos e moléculas do gás (Ehrenfreund and Charnley, 2000). Dados mostram que as principais espécies orgânicas em gelos interestelares são CO, CO 2, e CH 3 OH. Formação das moléculas mais simples no manto de gelo (H 2 O, NH 3, CH 4, etc) pode ser explicado por meio de reações de adição de hidrogénio. No entanto, a presença de moléculas complexas, tais como CH 3 OH e vários compostos orgânicos não identificados indica que outros processos de reação também operam nos mantos de gelo. Em nuvens densas, a superfície dos grãos é revestida com um manto de gelo que contém uma variedade de moléculas como H2O e outras moléculas simples (CH 3 OH, CO, CO 2, NH 3, CH 4, H 2 CO, etc ). A radiação de alta energia pode converter alguns destes materiais geladas em compostos orgânicos mais complexos como pode ser visto na Figura 3. Figura 3. Diagrama esquemático mostrando a formação de moléculas a partir da interação da radiação UV com a superfície congelada de grão interestelar. As temperaturas em densas nuvens interestelares são baixas o suficiente para que a maioria das moléculas na fase gasosa congele em mantos de gelo sobre grãos de poeira (Crédito: php). 5
6 A adsorção de CO sobre a superfície de gelo proporciona uma fonte de carbono para iniciar a síntese orgânica, por exemplo, na sequência de reacções simples (Shaw, 2006): CO + H HCO (18) HCO + H H 2 CO (19) H 2 CO + H H 3 CO (20) H 3 CO + H CH 3 OH (21) O esquema de reação passa através da formação de HCO, formaldeído e, finalmente, para a formação de metanol. É difícil ver como a formação de metanol previamente visto no ISM poderia resultar de uma série de reações em fase gasosa, e assim por dessorção de metanol a partir da superfície do grão podem ser responsáveis para a concentração de metanol no MI. 2.4 Núcleos Moleculares Quentes Núcleos moleculares quente são regiões com temperaturas de K, encontrados na vizinhança da formação de estrela de alta massa, onde a abundância de espécies orgânicas, tais como etanol, formato de metila e éter dimetílico são detectados (Herbst E, 2005). São ricos em moléculas orgânicas complexas e caracterizados por grandes abundâncias de H 2 O e NH 3, com presença de CO, HCN, e acetileno. Nessas regiões ocorrem a evaporação e sputtering de mantos de grãos de gelo. Reações de superfície dos grãos produzem compostos saturados simples tais como água e amoníaco, HDO, NH 2 D, DCN, D 2 CO, CH 2 DOH. Evaporação de gelos ricos em metanol e etanol devem produzir vários éteres puros e mistos (Charnley et al, 1995). A formação de moléculas grandes em núcleos quentes é principalmente devido ao NH 3 e CH 3 OH, que após a aquisição de um próton do H +3, H 3 O + ou + HCO, podem formar cadeias. As moléculas de HCN e C 2 H 5 OH poderiam desempenhar funções semelhantes, mas até agora, apenas limites máximos de suas abundâncias de estado sólido têm sido obtidos. Um determinante importante da química é, por conseguinte, a competição de prótons entre NH 3 e CH 3 OH, os quais têm uma elevada afinidade de prótons. Rodgers & Charnley (2001) mostram resultados de modelo para vários valores de razão de NH 3 /CH 3 OH, que observações ainda não especifcam bem (Van der Tak, 2003). Diversidade química também pode ser o resultado da alta temperatura e reações neutro-neutro. Em temperaturas ~ > 300 K, as reações de O e OH com H 2 conduzir todo o oxigênio disponível em H 2 O. Núcleos em altas temperaturas são, portanto, esperado para ser rico em compostos contendo nitrogênio (Rodgers & Charnley 2001). 3. MOLÉCULAS ORGÂNICAS COMPLEXAS 3.1 Fulerenos A geometria poliédrica de C 60 foi discutido pela primeira vez por Kroto et al (1985). Em 1990, C 60 foi eficientemente sintetizados em quantidades macroscópicas por Kraetschmer et al (1990). A presença de material fuligem em estrelas ricas em carbono, juntamente com a formação espontânea e estabilidade notável da cadeia de fulereno sugerem a presença de compostos de fulereno no espaço interestelar (ver Ehrenfreund & Foing 1997, para uma revisão). Os fulerenos podem ser formados em pequenas quantidades em envelopes de estrelas R Coronae Borealis (Goeres & Sedlmayr 1992). Os modelos teóricos mostram a possível formação de fulerenos no gás interestelar difusa através da formação de cadeias de C 2 -C 10 de inserção C +, reações íon-molécula, e reações neutro - neutro (Bettens & Herbst 1996, 1997). Impressões digitais do íon 6
7 recentes foram descobertas no infravermelho próximo, que indicam que os fulerenos podem desempenhar um papel importante na química interestelar. C 60 + Figura 4. Representação do fulereno C 60. Fonte: Iglesias and Groth, Fulerenos foram detectados em meteoritos do tipo condrito carbonáceo. Estes meteoritos provavelmente se formaram no início do Sistema Solar (Iglesias and Groth, 2012). A espectroscopia de massa do meteorito Allende (México 1969), o meteorito Murchinson (Austrália 1969) e o meteorito Tagish Lake (Canadá) relataram abundâncias de fulereno da ordem de 0,1 ppm (Vries et al. 1993; Becker et al. 1994, 1997,1999; Pizzarello et al., 2000). Na Terra, os fulerenos foram detectados em camadas sedimentares do Cretáceo- Terciário (KTB) fronteira da China e Bulgária e em minerais shunghite da Região Carelia (Rússia). 3.2 Hidrocarbonetos Aromáticos Policíclicos ( PAH's ) Os Hidrocarbonetos Aromáticos Policíclicos (Policiclic Aromatic Hidrocarbons PAH's) são moléculas grandes que contêm anéis aromáticos. No ecossistema terrestre eles são produzidos pela queima de combustíveis fósseis. No meio interestelar, que é o foco desse trabalho, eles estão associados com emissões no infravermelho médio, e já foram detectadas por telescópios espaciais. Os Hidrocarbonetos Aromáticos Policíclicos pertencem à família das moléculas planares, contendo átomos de carbono arranjados em uma estrutura semelhante à uma colmeia e ligações com átomos de carbono. A Figura 5 mostra alguns exemplos de PAH's com ligações de até quatro átomos de hidrogênio. Essa Figura mostra também a molécula de antraceno, que é do tipo catacondensado e a molécula de coroneno, do tipo pericondensado. Figura 5. Estrutura de quatro PAH's mostrando ligações com um a quatro átomos de hidrogênio. Fonte: Draine
8 PAHs são consideradas as moléculas orgânicas mais abundantes no espaço. Cálculos teóricos implicam que PAHs com átomos de carbono < 50 podem ser destruídos ou fragmentados em regiões dominadas por UV (Allain et al 1996a). Em seu ciclo evolutivo, as moléculas de PAHs podem congelar-se para grãos em nuvens densas, uma idéia que é suportada por observações da ISO recentes em direção a M17 (Verstraete et al 1996). As bandas de emissão das moléculas de PAH passaram quase uma década sem seremdeterminadas. Inicialmente eram chamadas de unidentified infrared band (UIR). No entanto, após telescópios espaciais como o IRAS e o ISO (Infrared Space Observatory) essas bandas foram identificadas. As bandas mais conhecidas no infravermelho médio relacionadas aos PAH's são: 3.3, 6.2, e 11.3 μm. No entanto, outras menos intensas que as anteriores foram detectadas, como: , 6.9, μm. A Figura 6 mostra dois exemplos de regiões que contêm os perfis de emissão dos PAH's. Figura 6. Espectro de PDR's associadas com a NGC7027 e a Barra de Órion, mostrando as características de emissão no infravermelho médio (sombreadas). As linhas estreitas são linhas de recombinação de HI, linhas rotacionais e ro-vibracionais de H 2 puro, e linhas atômicas da estrutura fina. O painel de cima indica os modos vibracionais associados à PAH's. Fonte: Tielens Eles são as moléculas orgânicas mais abundantes na fase de gás além do CO. A Figura 7 mostra exemplos de várias estruturas de PHAs que podem estar presentes no meio interestelar. Sua área de superfície, razoavelmente grande, pode facilitar a síntese molecular. 8
9 Figura 7. Alguns exemplos de estruturas de PHA que pode estar presente no Meio Interestelar. Fonte: Cold Spring Harb Perspect Biol2010; 2:a No meio interestelar difuso, PAHs supostamente estão presentes na forma ionizada. Alguns PAH foram identificados de forma inequívoca. No entanto, a banda de emissão de infravermelho observada no meio interestelar pode representar famílias de moléculas de HAP com um intervalo de distribuição, um número de diferentes estruturas diferentes e estados de ionização (Cold Spring Harb Perspect Biol2010; 2:a ) REFERÊNCIAS Bertoldi F, Carilli CL, Cox P, Fan X, Strauss MA, Beelen A, Omont A, Zylka R Dust emission from the most distant quasars. Astronomy and Astrophysics 406: L55 L58. Brown, Laurie M.; Pais, Abraham; Pippard, AB (1995). «A física do meio interestelar».século XX Física (2ª edición). CRC Press. p ISBN DL Lambert, Y. Sheffer, SR Federman (1995). «observações do telescópio espacial Hubble de moléculas de C 2 em nuvens interestelares difusas». Astrophysical Journal 438 : Cataldo F From Elemental Carbon to Complex Macromolecular Networks in Space. InAstrobiology: Future Perspectives (eds Ehrenfreund P., Becker L., and Blank J.) Astrophysics and Space Science Library, Vol. 305, pp Kluwer Academic Publishers: Dordrecht, The Netherlands. Ehrenfreund P, Charnley SB Organic molecules in the interstellar medium, comets, and meteorites: A voyage from dark clouds to the early Earth. Ann Rev Astron Astrophys 38: Ehrenfreund P, Rasmussen S, Cleaves JH, Chen L 2006a. Experimentally tracing the key steps in the origin of life: The aromatic world. Astrobiology 6/3: [PubMed]. Irvine WM. Organic molecules in the gas phase of dense interstellar clouds. Adv Space Res Mar;15(3): Kwok S Delivery of complex organic compounds from planetary nebulae to the solar system.intern. J Astrobiol 8/3: Maciel, Walter. Astrofísica do Meio Interestelar. São Paulo, Edusp, Spaans M The synthesis of the elements and the formation of stars. In Astrobiology: Future Perspectives (eds Ehrenfreund P., Becker L., and Blank J.) Astrophysics and Space Science Library, Vol. 305, pp Kluwer Academic Publishers: Dordrecht, The Netherlands. Van Dishoeck EF, Blake G Chemical evolution of star-forming regions. Ann Rev of Astronomy and Astrophysics 36: 317 [PubMed]. 9
01 Processos Químicos. Prof. Dr. Sergio Pilling Aluno: Will Robson Monteiro Rocha
 Física e a Química do Meio Interestelar Mestrado e Doutorado em Física e Astronomia Livro texto: Physics and chemistry of the interestellar medium A. G. G. M. Tielens (2004) Prof. Dr. Sergio Pilling Aluno:
Física e a Química do Meio Interestelar Mestrado e Doutorado em Física e Astronomia Livro texto: Physics and chemistry of the interestellar medium A. G. G. M. Tielens (2004) Prof. Dr. Sergio Pilling Aluno:
Qual o nosso lugar no Universo?
 Qual o nosso lugar no Universo? Acredita-se que no Universo existam cerca de 100 000 milhões de galáxias. As galáxias são enormes grupos de estrelas, gás e poeira. Nem todas são iguais e diferenciam-se
Qual o nosso lugar no Universo? Acredita-se que no Universo existam cerca de 100 000 milhões de galáxias. As galáxias são enormes grupos de estrelas, gás e poeira. Nem todas são iguais e diferenciam-se
Formação estelar e Estágios finais da evolução estelar
 Elementos de Astronomia Formação estelar e Estágios finais da evolução estelar Rogemar A. Riffel Formação estelar - Estrelas se formam dentro de concentrações relativamente densas de gás e poeira interestelar
Elementos de Astronomia Formação estelar e Estágios finais da evolução estelar Rogemar A. Riffel Formação estelar - Estrelas se formam dentro de concentrações relativamente densas de gás e poeira interestelar
05 Nuvens Moleculares. Prof. Dr. Sergio Pilling Aluno: Will Robson Monteiro Rocha
 Física e a Química do Meio Interestelar Mestrado e Doutorado em Física e Astronomia Livro texto: Physics and chemistry of the interestellar medium A. G. G. M. Tielens (2004) Prof. Dr. Sergio Pilling Aluno:
Física e a Química do Meio Interestelar Mestrado e Doutorado em Física e Astronomia Livro texto: Physics and chemistry of the interestellar medium A. G. G. M. Tielens (2004) Prof. Dr. Sergio Pilling Aluno:
Uma estrela-bebê de 10 mil anos
 1 Uma estrela-bebê de 10 mil anos Jane Gregorio-Hetem (IAG/USP) Email: jane@astro.iag.usp.br A versão original deste texto foi divulgada no CD-ROM da 48ª Reunião Anual da SBPC, na qual a conferência Estrelas
1 Uma estrela-bebê de 10 mil anos Jane Gregorio-Hetem (IAG/USP) Email: jane@astro.iag.usp.br A versão original deste texto foi divulgada no CD-ROM da 48ª Reunião Anual da SBPC, na qual a conferência Estrelas
Observatórios Virtuais Fundamentos de Astronomia Cap. 14 (C. Oliveira & V.Jatenco-Pereira) Capítulo 14 O MEIO INTERESTELAR
 150 Capítulo 14 O MEIO INTERESTELAR Nós dedicaremos esse capítulo ao estudo do meio entre as estrelas ou meio interestelar, usualmente rico em gás, poeira e outros materiais, sendo um local prolífico para
150 Capítulo 14 O MEIO INTERESTELAR Nós dedicaremos esse capítulo ao estudo do meio entre as estrelas ou meio interestelar, usualmente rico em gás, poeira e outros materiais, sendo um local prolífico para
ÇÃO À ASTRONOMIA (AGA-210) Notas de aula INTRODUÇÃ. Estrelas: do nascimento à Seqüê. üência Principal. Enos Picazzio IAGUSP, Maio/2006
 INTRODUÇÃ ÇÃO À ASTRONOMIA (AGA-210) Notas de aula Estrelas: do nascimento à Seqüê üência Principal Enos Picazzio IAGUSP, Maio/2006 De que são formadas as estrelas? Átomo: elemento básico b da matéria
INTRODUÇÃ ÇÃO À ASTRONOMIA (AGA-210) Notas de aula Estrelas: do nascimento à Seqüê üência Principal Enos Picazzio IAGUSP, Maio/2006 De que são formadas as estrelas? Átomo: elemento básico b da matéria
A Via-Láctea. Prof. Fabricio Ferrari Unipampa. adaptado da apresentação The Milky Way, Dr. Helen Bryce,University of Iowa
 A Via-Láctea Prof. Fabricio Ferrari Unipampa adaptado da apresentação The Milky Way, Dr. Helen Bryce,University of Iowa Aparência da Via Láctea no céu noturno Imagem de todo o céu em luz visível Nossa
A Via-Láctea Prof. Fabricio Ferrari Unipampa adaptado da apresentação The Milky Way, Dr. Helen Bryce,University of Iowa Aparência da Via Láctea no céu noturno Imagem de todo o céu em luz visível Nossa
Astroquímica. Aula 10 Orbitais Moleculares e outros aspectos da Formação das moléculas de H 2, de H 2 O e de PAH s no espaço. Prof. Dr.
 Astroquímica Mestrado e Doutorado em Física e Astronomia Prof. Dr. Sergio Pilling Alunos: Víctor de Souza Bonfim Aula 10 Orbitais Moleculares e outros aspectos da Formação das moléculas de H 2, de H 2
Astroquímica Mestrado e Doutorado em Física e Astronomia Prof. Dr. Sergio Pilling Alunos: Víctor de Souza Bonfim Aula 10 Orbitais Moleculares e outros aspectos da Formação das moléculas de H 2, de H 2
A VIA LÁCTEA, NOSSA GALÁXIA
 A VIA LÁCTEA, NOSSA GALÁXIA A Via Láctea é uma faixa de luz tênue e esbranquiçada que percorre todo o céu, formando um anel à nossa volta. É conhecida desde a antiguidade. Somente com o uso do telescópio
A VIA LÁCTEA, NOSSA GALÁXIA A Via Láctea é uma faixa de luz tênue e esbranquiçada que percorre todo o céu, formando um anel à nossa volta. É conhecida desde a antiguidade. Somente com o uso do telescópio
GEOLOGIA. Prof. Dr. Adilson Soares E- mail: adilson.soares@unifesp.br Site: www.geologia.wiki.br
 GEOLOGIA Prof. Dr. Adilson Soares E- mail: adilson.soares@unifesp.br Site: www.geologia.wiki.br Origem do Universo e Sistema Solar Origem do Universo e Sistema Solar Teoria do Big Bang - o universo surgiu
GEOLOGIA Prof. Dr. Adilson Soares E- mail: adilson.soares@unifesp.br Site: www.geologia.wiki.br Origem do Universo e Sistema Solar Origem do Universo e Sistema Solar Teoria do Big Bang - o universo surgiu
INTERAÇÃO DOS RAIOS-X COM A MATÉRIA
 INTERAÇÃO DOS RAIOS-X COM A MATÉRIA RAIOS-X + MATÉRIA CONSEQUÊNCIAS BIOLÓGICAS EFEITOS DAZS RADIAÇÕES NA H2O A molécula da água é a mais abundante em um organismo biológico, a água participa praticamente
INTERAÇÃO DOS RAIOS-X COM A MATÉRIA RAIOS-X + MATÉRIA CONSEQUÊNCIAS BIOLÓGICAS EFEITOS DAZS RADIAÇÕES NA H2O A molécula da água é a mais abundante em um organismo biológico, a água participa praticamente
Interacção da Radiação com a Matéria
 Interacção da Radiação com a Matéria Já sabemos que: As radiações eletromagnéticas têm comportamento ondulatório e corpuscular. Cada radiação apresenta as suas características individuais; Os corpúsculos
Interacção da Radiação com a Matéria Já sabemos que: As radiações eletromagnéticas têm comportamento ondulatório e corpuscular. Cada radiação apresenta as suas características individuais; Os corpúsculos
Mary Santiago Silva 05/05/2010
 Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
Universidade Federal do Rio Grande do Sul Instituto de Física Departamento de Astronomia. Estrelas. Prof. Tibério B. Vale
 Universidade Federal do Rio Grande do Sul Instituto de Física Departamento de Astronomia Estrelas Prof. Tibério B. Vale Propriedades Estrelas são esferas autogravitantes de gás ionizado, cuja fonte de
Universidade Federal do Rio Grande do Sul Instituto de Física Departamento de Astronomia Estrelas Prof. Tibério B. Vale Propriedades Estrelas são esferas autogravitantes de gás ionizado, cuja fonte de
QUÍMICA QUESTÃO 41 QUESTÃO 42
 Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
ENSINO FUNDAMENTAL - CIÊNCIAS 9ºANO- UNIDADE 3 - CAPÍTULO 1
 ENSINO FUNDAMENTAL - CIÊNCIAS 9ºANO- UNIDADE 3 - CAPÍTULO 1 questão 01. O que é Astrofísica? questão 02. O que são constelações? questão 03. Como era o calendário Lunar? questão 04. Qual era diferença
ENSINO FUNDAMENTAL - CIÊNCIAS 9ºANO- UNIDADE 3 - CAPÍTULO 1 questão 01. O que é Astrofísica? questão 02. O que são constelações? questão 03. Como era o calendário Lunar? questão 04. Qual era diferença
Aula 1. 1. Introdução
 Aula 1 Nesta aula, iniciaremos nosso estudo sobre a física básica dos plasmas, onde iremos definir o que é plasma, mostraremos alguns exemplos e discutiremos, brevemente a evolução das pesquisas na área.
Aula 1 Nesta aula, iniciaremos nosso estudo sobre a física básica dos plasmas, onde iremos definir o que é plasma, mostraremos alguns exemplos e discutiremos, brevemente a evolução das pesquisas na área.
Astor João Schönell Júnior
 Astor João Schönell Júnior As galáxias são classificadas morfologicamente (Hubble Sequence): -Espirais -Elípticas -Irregulares - Galáxias SO As galáxias espirais consistem em um disco com braços espirais
Astor João Schönell Júnior As galáxias são classificadas morfologicamente (Hubble Sequence): -Espirais -Elípticas -Irregulares - Galáxias SO As galáxias espirais consistem em um disco com braços espirais
Sua Conexão Cósmica com os Elementos
 Sua Conexão Cósmica com os Elementos James Lochner (USRA) & Suzanne Pleau Kinnison (AESP), NASA/GSFC Traduzido por Paulo Marcelo Pontes, pmarcelopontes@gmail.com Conexões Elementares O Big Bang A Cosmologia
Sua Conexão Cósmica com os Elementos James Lochner (USRA) & Suzanne Pleau Kinnison (AESP), NASA/GSFC Traduzido por Paulo Marcelo Pontes, pmarcelopontes@gmail.com Conexões Elementares O Big Bang A Cosmologia
Efeito estufa: como acontece, por que acontece e como influencia o clima do nosso planeta
 XXII Encontro Sergipano de Física Efeito estufa: como acontece, por que acontece e como influencia o clima do nosso planeta Prof. Dr. Milan Lalic Departamento de Física Universidade Federal de Sergipe
XXII Encontro Sergipano de Física Efeito estufa: como acontece, por que acontece e como influencia o clima do nosso planeta Prof. Dr. Milan Lalic Departamento de Física Universidade Federal de Sergipe
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é:
 01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
CURSO AVANÇADO EM ASTRONOMIA E ASTROFÍSICA OBSERVATÓRIO ASTRONÓMICO DE LISBOA VIDA E MORTE DAS ESTRELAS. Rui Jorge Agostinho MÓDULO CAOAL VME
 CURSO AVANÇADO EM ASTRONOMIA E ASTROFÍSICA DO OBSERVATÓRIO ASTRONÓMICO DE LISBOA VIDA E MORTE DAS ESTRELAS MÓDULO CAOAL VME Rui Jorge Agostinho Outubro de 2013 Conteúdo Objectivos e Estrutura do Curso..............................
CURSO AVANÇADO EM ASTRONOMIA E ASTROFÍSICA DO OBSERVATÓRIO ASTRONÓMICO DE LISBOA VIDA E MORTE DAS ESTRELAS MÓDULO CAOAL VME Rui Jorge Agostinho Outubro de 2013 Conteúdo Objectivos e Estrutura do Curso..............................
Elementos do bloco p
 Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Astroquímica. Aula 14 - Modelos de evolução química em ambientes astrofísicos: meio interestelar, nuvens moleculares, atmosferas planetárias.
 Astroquímica Mestrado e Doutorado em Física e Astronomia Prof. Dr. Sergio Pilling Aluno: Víctor de Souza Bonfim Aula 14 - Modelos de evolução química em ambientes astrofísicos: meio interestelar, nuvens
Astroquímica Mestrado e Doutorado em Física e Astronomia Prof. Dr. Sergio Pilling Aluno: Víctor de Souza Bonfim Aula 14 - Modelos de evolução química em ambientes astrofísicos: meio interestelar, nuvens
A) a existência do oceano líquido é uma hipótese possível, pois um sal solúvel só forma uma mistura homogênea com a água, quando ela está líquida.
 TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
TEXTO PARA A QUESTÃO 1. Sonda espacial detecta sal de cozinha em lua de Saturno A análise da composição química do anel mais externo de Saturno revelou a presença de 98% de água, 1% de cloreto de sódio,
Universidade Federal Fluminense
 Universidade Federal Fluminense Curso de Formação continuada em Astronomia Para professores de Educação Básica Prof. Dr. Tibério Borges Vale Projeto de Extensão O uso da Astronomia como elemento didático
Universidade Federal Fluminense Curso de Formação continuada em Astronomia Para professores de Educação Básica Prof. Dr. Tibério Borges Vale Projeto de Extensão O uso da Astronomia como elemento didático
ANO LETIVO 2013/2014 PROVAS DE ACESSO AO ENSINO SUPERIOR PARA CANDIDATOS MAIORES DE 23 ANOS EXAME DE QUÍMICA CONTEÚDOS PROGRAMÁTICOS
 ANO LETIVO 2013/2014 PROVAS DE ACESSO AO ENSINO SUPERIOR PARA CANDIDATOS MAIORES DE 23 ANOS EXAME DE QUÍMICA CONTEÚDOS PROGRAMÁTICOS 1. MATERIAIS: DIVERSIDADE E CONSTITUIÇÃO 1.1 Materiais 1.1.1 Materiais
ANO LETIVO 2013/2014 PROVAS DE ACESSO AO ENSINO SUPERIOR PARA CANDIDATOS MAIORES DE 23 ANOS EXAME DE QUÍMICA CONTEÚDOS PROGRAMÁTICOS 1. MATERIAIS: DIVERSIDADE E CONSTITUIÇÃO 1.1 Materiais 1.1.1 Materiais
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves
 Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
http://www.quimica.net/emiliano 1
 Resolução da Prova de Química Vestibular Verão UPF 2004 Professor Emiliano hemello www.quimica.net/emiliano emiliano@quimica.net Questões Resolução: B Resoluções Em 1875, rookes colocou gases muito rarefeitos
Resolução da Prova de Química Vestibular Verão UPF 2004 Professor Emiliano hemello www.quimica.net/emiliano emiliano@quimica.net Questões Resolução: B Resoluções Em 1875, rookes colocou gases muito rarefeitos
a) Qual a configuração eletrônica do cátion do alumínio isoeletrônico ao gás nobre neônio?
 Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Física e a Química do Meio Interestelar
 Física e a Química do Meio Interestelar Mestrado e Doutorado em Física e Astronomia Livro texto: Physics and chemistry of the interestellar medium A. G. G. M. Tielens (2004) Prof. Dr. Sergio Pilling Aluno:
Física e a Química do Meio Interestelar Mestrado e Doutorado em Física e Astronomia Livro texto: Physics and chemistry of the interestellar medium A. G. G. M. Tielens (2004) Prof. Dr. Sergio Pilling Aluno:
Fundamentos de Astronomia e Astrofísica. Galáxias. Tibério B. Vale. http://astro.if.ufrgs.br/
 Fundamentos de Astronomia e Astrofísica Galáxias Tibério B. Vale http://astro.if.ufrgs.br/ A descoberta das galáxias Kant (1755): hipótese dos "universos-ilha": a Via Láctea é apenas uma galáxia a mais
Fundamentos de Astronomia e Astrofísica Galáxias Tibério B. Vale http://astro.if.ufrgs.br/ A descoberta das galáxias Kant (1755): hipótese dos "universos-ilha": a Via Láctea é apenas uma galáxia a mais
O olho humano permite, com o ar limpo, perceber uma chama de vela em até 15 km e um objeto linear no mapa com dimensão de 0,2mm.
 A Visão é o sentido predileto do ser humano. É tão natural que não percebemos a sua complexidade. Os olhos transmitem imagens deformadas e incompletas do mundo exterior que o córtex filtra e o cérebro
A Visão é o sentido predileto do ser humano. É tão natural que não percebemos a sua complexidade. Os olhos transmitem imagens deformadas e incompletas do mundo exterior que o córtex filtra e o cérebro
por espécies monoatômicas H, He, O, alcalinos e alcalinos terrosos, e possui pressão superficial menor que 10-12 bar. A atmosfera de Vênus é
 1 Introdução Aproximadamente, 90% de toda matéria do universo é constituída de corpos como estrelas e planetas, e apenas cerca de 10% representa o meio interestelar, e este é constituído por aproximadamente
1 Introdução Aproximadamente, 90% de toda matéria do universo é constituída de corpos como estrelas e planetas, e apenas cerca de 10% representa o meio interestelar, e este é constituído por aproximadamente
Ligações Químicas Ligação Iônica Ligação Metálica
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Ligações Químicas Ligação Iônica Ligação Metálica Periodicidade O átomo é visto como uma esfera, onde só as
COLÉGIO SANTA TERESINHA R. Madre Beatriz 135 centro Tel. (33) 3341-1244 www.colegiosantateresinha.com.br
 PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
LIGAÇÕES QUÍMICAS TEORIA CORPUSCULAR
 LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron:
 Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
Astroquímica. 3 - O meio interestelar e as estrelas. a) b) Prof. Dr. Sergio Pilling Aluno: Will Robson M. Rocha
 Astroquímica Mestrado e Doutorado em Física e Astronomia Prof. Dr. Sergio Pilling Aluno: Will Robson M. Rocha 3 - O meio interestelar e as estrelas 1. Introdução Ao olhar para o céu noturno em um local
Astroquímica Mestrado e Doutorado em Física e Astronomia Prof. Dr. Sergio Pilling Aluno: Will Robson M. Rocha 3 - O meio interestelar e as estrelas 1. Introdução Ao olhar para o céu noturno em um local
Transições de Fase de Substâncias Simples
 Transições de Fase de Substâncias Simples Como exemplo de transição de fase, vamos discutir a liquefação de uma amostra de gás por um processo de redução de volume a temperatura constante. Consideremos,
Transições de Fase de Substâncias Simples Como exemplo de transição de fase, vamos discutir a liquefação de uma amostra de gás por um processo de redução de volume a temperatura constante. Consideremos,
Quando esses temas são compreendidos, o aprendizado da química orgânica se torna muito mais fácil, diminuindo a necessidade de memorização.
 REAÇÕES ORGÂNIAS A primeira vista, a química orgânica pode ser observada como uma coleção confusa de milhões de compostos, dezenas de grupos funcionais e um número infinito de reações químicas. Ao estudá-la,
REAÇÕES ORGÂNIAS A primeira vista, a química orgânica pode ser observada como uma coleção confusa de milhões de compostos, dezenas de grupos funcionais e um número infinito de reações químicas. Ao estudá-la,
Todas as reações dos Compostos de Grignard
 Todas as reações dos Compostos de Grignard Primeiramente vamos relembrar os compostos de Gringnard. Compostos de Grignard são os principais compostos organometálicos da química orgânica, onde o metal é
Todas as reações dos Compostos de Grignard Primeiramente vamos relembrar os compostos de Gringnard. Compostos de Grignard são os principais compostos organometálicos da química orgânica, onde o metal é
06-01-2012. Sumário. O Sistema Solar. Principais características dos planetas do Sistema Solar 05/01/2012. 23 e 24
 Sumário Os planetas do Sistema Solar e as suas principais características. (BI dos Planetas do Sistema Solar). Atividade Prática de Sala de Aula Características dos planetas. Preenchimento de tabelas,
Sumário Os planetas do Sistema Solar e as suas principais características. (BI dos Planetas do Sistema Solar). Atividade Prática de Sala de Aula Características dos planetas. Preenchimento de tabelas,
Separação de Isótopos de Terras Raras usando Laser. Nicolau A.S.Rodrigues Instituto de Estudos Avançados
 Separação de Isótopos de Terras Raras usando Laser Nicolau A.S.Rodrigues Instituto de Estudos Avançados Roteiro 1. Motivação: - Isótopos: o que são porque um determinado isótopo é mais interessantes que
Separação de Isótopos de Terras Raras usando Laser Nicolau A.S.Rodrigues Instituto de Estudos Avançados Roteiro 1. Motivação: - Isótopos: o que são porque um determinado isótopo é mais interessantes que
Unidade IV Ser Humano e saúde. Aula 17.1
 Unidade IV Ser Humano e saúde. Aula 17.1 Conteúdo: O efeito estufa. Habilidade: Demonstrar uma postura crítica diante do uso do petróleo. REVISÃO Reações de aldeídos e cetonas. A redução de um composto
Unidade IV Ser Humano e saúde. Aula 17.1 Conteúdo: O efeito estufa. Habilidade: Demonstrar uma postura crítica diante do uso do petróleo. REVISÃO Reações de aldeídos e cetonas. A redução de um composto
5. Resultados e Análises
 66 5. Resultados e Análises Neste capítulo é importante ressaltar que as medições foram feitas com uma velocidade constante de 1800 RPM, para uma freqüência de 60 Hz e uma voltagem de 220 V, entre as linhas
66 5. Resultados e Análises Neste capítulo é importante ressaltar que as medições foram feitas com uma velocidade constante de 1800 RPM, para uma freqüência de 60 Hz e uma voltagem de 220 V, entre as linhas
PROVA DE QUÍMICA - 1998 Segunda Etapa
 PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
TEORIA DO ORBITAL MOLECULAR PARA MOLÉCULAS POLIATÔMICAS
 UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA FUNDAMENTAL TEORIA DO ORBITAL MOLECULAR PARA MOLÉCULAS POLIATÔMICAS Prof. Fabio da Silva Miranda
UNIVERSIDADE FEDERAL FLUMINENSE INSTITUTO DE QUÍMICA DEPARTAMENTO DE QUÍMICA INORGÂNICA QUÍMICA INORGÂNICA FUNDAMENTAL TEORIA DO ORBITAL MOLECULAR PARA MOLÉCULAS POLIATÔMICAS Prof. Fabio da Silva Miranda
Estudo da emissão veicular de Gases de Efeito Estufa (GEE) em veículos movidos à DIESEL. Prof. Dr. Ariston da Silva Melo Júnior
 Estudo da emissão veicular de Gases de Efeito Estufa (GEE) em veículos movidos à DIESEL Prof. Dr. Ariston da Silva Melo Júnior INTRODUÇÃO Durante milhões de anos a Terra passou por ciclos naturais de aquecimento
Estudo da emissão veicular de Gases de Efeito Estufa (GEE) em veículos movidos à DIESEL Prof. Dr. Ariston da Silva Melo Júnior INTRODUÇÃO Durante milhões de anos a Terra passou por ciclos naturais de aquecimento
Química 1 Química Geral 1
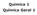 α α = 2 3 2 2 34 2 2 34 56787 977 7 767 34 2 56787 97657 23456789 9 24869 234869 + 567 7657 23456789 24869 24869 2 3 4 35 4 34 + = = Química Geral A Lei Periódica é estabelecida nestes termos: As
α α = 2 3 2 2 34 2 2 34 56787 977 7 767 34 2 56787 97657 23456789 9 24869 234869 + 567 7657 23456789 24869 24869 2 3 4 35 4 34 + = = Química Geral A Lei Periódica é estabelecida nestes termos: As
UNIVERSIDADE ESTADUAL DE PONTA GROSSA PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO PROGRAMA DE PÓS-GRADUAÇÃO QUÍMICA APLICADA - MESTRADO
 strado em Química Aplicada Seleção 2007 1/6 1 a etapa do Processo de Seleção 2007 - Parte 1 Questão 01: (A) Arranje, em ordem crescente de comprimento de onda, os seguintes tipos de fótons de radiação
strado em Química Aplicada Seleção 2007 1/6 1 a etapa do Processo de Seleção 2007 - Parte 1 Questão 01: (A) Arranje, em ordem crescente de comprimento de onda, os seguintes tipos de fótons de radiação
Química Atomística Profª: Bruna Villas Bôas. Exercícios
 NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
NÚMERO ATÔMICO (Z) Os diferentes tipos de átomos (elementos químicos) são identificados pela quantidade de prótons (P) que possui. Esta quantidade de prótons recebe o nome de número atômico e é representado
Projeto Embuá Unidade de Aprendizagem: ENERGIA
 Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Projeto Embuá Unidade de Aprendizagem: ENERGIA Energia para realizar reações químicas: eletrólise do iodeto de potássio aquoso Existem reações químicas não espontâneas, mas que são realizadas com rapidez
Próton Nêutron Elétron
 Próton Nêutron Elétron ARNOLD SOMMERFELD MODELO ATÔMICO DE ARNOLD SOMMERFELD - 1916 Ao pesquisar o átomo, Sommerfeld concluiu que os elétrons de um mesmo nível, ocupam órbitas de trajetórias diferentes
Próton Nêutron Elétron ARNOLD SOMMERFELD MODELO ATÔMICO DE ARNOLD SOMMERFELD - 1916 Ao pesquisar o átomo, Sommerfeld concluiu que os elétrons de um mesmo nível, ocupam órbitas de trajetórias diferentes
Química. Resolução das atividades complementares. Q42 Ligação metálica
 Resolução das atividades complementares 3 Química Q42 Ligação metálica p. 59 1 (Cefet-PR) Analise as afirmações a seguir: I. O metal X é leve, sofre pouca corrosão e é bastante utilizado na construção
Resolução das atividades complementares 3 Química Q42 Ligação metálica p. 59 1 (Cefet-PR) Analise as afirmações a seguir: I. O metal X é leve, sofre pouca corrosão e é bastante utilizado na construção
POLÍMEROS POLIETILENO DE BAIXA DENSIDADE
 POLÍMEROS Os polímeros são macromoléculas formada pela união de pequenas unidades que se repetem, os monômeros. Existem basicamente dois tipos de polimerização: adição e condensação. Na polimeirzação por
POLÍMEROS Os polímeros são macromoléculas formada pela união de pequenas unidades que se repetem, os monômeros. Existem basicamente dois tipos de polimerização: adição e condensação. Na polimeirzação por
Aspectos ambientais da energia aplicada em reações químicas
 Aspectos ambientais da energia aplicada em reações químicas Sumário As cargas ambientais resultantes da utilização de energias térmicas ou elétricas são particularmente importantes. Freqüentemente, o impacto
Aspectos ambientais da energia aplicada em reações químicas Sumário As cargas ambientais resultantes da utilização de energias térmicas ou elétricas são particularmente importantes. Freqüentemente, o impacto
Qualidade Ambiental Química
 Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
EXAME GERAL EM QUÍMICA EDITAL N 118/2009. Seleção para o 1º Semestre de 2010 07 de Dezembro de 2009 CANDIDATO: Assinatura: INSTRUÇÕES
 UNIVERSIDADE ESTADUAL DO SUDOESTE DA BAHIA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA R. José Moreira Sobrinho, s/n, CEP: 45506-191 Jequié-BA Tel / FAX: 73 3528-9630 e-mail: mestrado.quimica@uesb.br Reservado
UNIVERSIDADE ESTADUAL DO SUDOESTE DA BAHIA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA R. José Moreira Sobrinho, s/n, CEP: 45506-191 Jequié-BA Tel / FAX: 73 3528-9630 e-mail: mestrado.quimica@uesb.br Reservado
Como as estrelas se formam?
 EAD - Astrofísica Geral 2013 Home Informações Gerais Cronograma do Curso Contato Inscrições Como as estrelas se formam? Nada no Universo existe para sempre, talvez nem mesmo o próprio Universo. Todas as
EAD - Astrofísica Geral 2013 Home Informações Gerais Cronograma do Curso Contato Inscrições Como as estrelas se formam? Nada no Universo existe para sempre, talvez nem mesmo o próprio Universo. Todas as
Departamento de Astronomia - Universidade Federal do Rio Grande do Sul
 Departamento de Astronomia - Universidade Federal do Rio Grande do Sul FIS02010-A - FUNDAMENTOS DE ASTRONOMIA E ASTROFÍSICA A 3.a PROVA - 2012/1 - Turma C NOME: I.Nas questões de 1 a 20, escolhe a alternativa
Departamento de Astronomia - Universidade Federal do Rio Grande do Sul FIS02010-A - FUNDAMENTOS DE ASTRONOMIA E ASTROFÍSICA A 3.a PROVA - 2012/1 - Turma C NOME: I.Nas questões de 1 a 20, escolhe a alternativa
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo
 Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
EXOPLANETAS EIXO PRINCIPAL
 EXOPLANETAS Antes mesmo de eles serem detectados, poucos astrônomos duvidavam da existência de outros sistemas planetários além do Solar. Mas como detectar planetas fora do Sistema Solar? Às suas grandes
EXOPLANETAS Antes mesmo de eles serem detectados, poucos astrônomos duvidavam da existência de outros sistemas planetários além do Solar. Mas como detectar planetas fora do Sistema Solar? Às suas grandes
Considera-se que o Sistema Solar teve origem há cerca de 5 mil milhões de anos.
 19 e 20 17/11/2011 Sumário Correção do TPC. Como se formou o Sistema Solar? Constituição do Sistema Solar. Os planetas do Sistema Solar. Principais características dos planetas do Sistema Solar. Outros
19 e 20 17/11/2011 Sumário Correção do TPC. Como se formou o Sistema Solar? Constituição do Sistema Solar. Os planetas do Sistema Solar. Principais características dos planetas do Sistema Solar. Outros
nome de Química do C1. De uma maneira geral é possível dividir estes produtos em três categorias:
 ,1752'8d 2 O gás natural é composto, principalmente, de metano (até 98%) e por alguns hidrocarbonetos de maior peso molecular (de C 2 a C 6 ) além dos diluentes N 2 e CO 2. Com o uso crescente de petróleo
,1752'8d 2 O gás natural é composto, principalmente, de metano (até 98%) e por alguns hidrocarbonetos de maior peso molecular (de C 2 a C 6 ) além dos diluentes N 2 e CO 2. Com o uso crescente de petróleo
5 as Olimpíadas Nacionais de Astronomia
 5 as Olimpíadas Nacionais de Astronomia Prova da eliminatória regional 14 de Abril de 2010 15:00 Duração máxima 120 minutos Nota: Ler atentamente todas as questões. Existe uma tabela com dados no final
5 as Olimpíadas Nacionais de Astronomia Prova da eliminatória regional 14 de Abril de 2010 15:00 Duração máxima 120 minutos Nota: Ler atentamente todas as questões. Existe uma tabela com dados no final
Gabarito -Funções Orgânicas 2015
 Gabarito: Resposta da questão 1: [Resposta do ponto de vista da disciplina de Química] As cenouras de coloração laranja podem ter sido trazidas a Pernambuco durante a invasão holandesa e contêm um pigmento
Gabarito: Resposta da questão 1: [Resposta do ponto de vista da disciplina de Química] As cenouras de coloração laranja podem ter sido trazidas a Pernambuco durante a invasão holandesa e contêm um pigmento
ESPECTRO ELETROMAGNÉTICO
 COLÉGIO ESTADUAL RAINHA DA PAZ, ENSINO MÉDIO REPOSIÇÃO DAS AULAS DO DIA 02 e 03/07/2012 DAS 1 ª SÉRIES: A,B,C,D,E e F. Professor MSc. Elaine Sugauara Disciplina de Química ESPECTRO ELETROMAGNÉTICO As ondas
COLÉGIO ESTADUAL RAINHA DA PAZ, ENSINO MÉDIO REPOSIÇÃO DAS AULAS DO DIA 02 e 03/07/2012 DAS 1 ª SÉRIES: A,B,C,D,E e F. Professor MSc. Elaine Sugauara Disciplina de Química ESPECTRO ELETROMAGNÉTICO As ondas
A Via LácteaMassa da Galáxia
 Fundamentos de Astronomia e Astrofísica A Via LácteaMassa da Galáxia Tibério B. Vale http://astro.if.ufrgs.br Meio Interestelar O meio entre as estrelas não é completamente vazio. Tem gás: principalmente
Fundamentos de Astronomia e Astrofísica A Via LácteaMassa da Galáxia Tibério B. Vale http://astro.if.ufrgs.br Meio Interestelar O meio entre as estrelas não é completamente vazio. Tem gás: principalmente
Cromatografia Gasosa. Principles of Instrumental Analysis Skoog, West, Holler, Nieman. Thomson Learning; ISBN: 0030020786. Departamento de Química
 Capítulo X-5 Cromatografia Gasosa Principles of Instrumental Analysis Skoog, West, Holler, Nieman Thomson Learning; ISBN: 0030020786 1 Na cromatografia de fase gasosa (GC) a amostra é volatizada e injectada
Capítulo X-5 Cromatografia Gasosa Principles of Instrumental Analysis Skoog, West, Holler, Nieman Thomson Learning; ISBN: 0030020786 1 Na cromatografia de fase gasosa (GC) a amostra é volatizada e injectada
FCVA/ UNESP JABOTICABAL ESPECTROSCOPIA DE ABSORÇÃO ATÔMICA. Prof a. Dr a. Luciana Maria Saran
 FCVA/ UNESP JABOTICABAL ESPECTROSCOPIA DE ABSORÇÃO ATÔMICA Prof a. Dr a. Luciana Maria Saran 1. INTRODUÇÃO Átomos ou Íons: têm estados de energia característicos, nos quais os elétrons podem permanecer.
FCVA/ UNESP JABOTICABAL ESPECTROSCOPIA DE ABSORÇÃO ATÔMICA Prof a. Dr a. Luciana Maria Saran 1. INTRODUÇÃO Átomos ou Íons: têm estados de energia característicos, nos quais os elétrons podem permanecer.
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
 CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS EXERCÍCIOS Questão 01) O correto uso da tabela periódica permite determinar os elementos químicos a partir de algumas de suas características. Recorra a tabela periódica
Tabela periódica e propriedades periódicas
 Tabela periódica e propriedades periódicas Mendeleev Vários cientistas procuravam agrupar os átomos de acordo com algum tipo de semelhança, mas o químico russo Dmitri Ivanovich Mendeleev foi o primeiro
Tabela periódica e propriedades periódicas Mendeleev Vários cientistas procuravam agrupar os átomos de acordo com algum tipo de semelhança, mas o químico russo Dmitri Ivanovich Mendeleev foi o primeiro
Capítulo 5 Distribuição de Energia e Linhas Espectrais
 Capítulo 5 Distribuição de Energia e Linhas Espectrais As transições atômicas individuais (das quais falaremos mais adiante) são responsáveis pela produção de linhas espectrais. O alargamento das linhas
Capítulo 5 Distribuição de Energia e Linhas Espectrais As transições atômicas individuais (das quais falaremos mais adiante) são responsáveis pela produção de linhas espectrais. O alargamento das linhas
De um ponto negro a um ponto azul: geosfera, atmosfera e vida
 De um ponto negro a um ponto azul: geosfera, atmosfera e vida E. Ivo Alves Instituto Geofísico, Centro de Geofísica e Departamento de Ciências da Terra Faculdade de Ciências e Tecnologia da Universidade
De um ponto negro a um ponto azul: geosfera, atmosfera e vida E. Ivo Alves Instituto Geofísico, Centro de Geofísica e Departamento de Ciências da Terra Faculdade de Ciências e Tecnologia da Universidade
GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES. Professor Cristiano
 GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES Professor Cristiano GEOMETRIA MOLECULAR É o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Dependendo dos átomos que a
GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES Professor Cristiano GEOMETRIA MOLECULAR É o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Dependendo dos átomos que a
Esse grupo já foi conhecido como gases raros e gases inertes.
 GASES NOBRES GRUPO 18 OU VIIIA Esse grupo já foi conhecido como gases raros e gases inertes. Gases raros não é apropriado porque o argônio (Ar) não é raro (é mais abundante que o CO 2 no ar). Gases Inertes
GASES NOBRES GRUPO 18 OU VIIIA Esse grupo já foi conhecido como gases raros e gases inertes. Gases raros não é apropriado porque o argônio (Ar) não é raro (é mais abundante que o CO 2 no ar). Gases Inertes
 A Via Láctea Curso de Extensão Universitária Astronomia: Uma Visão Geral 12 a 17 de janeiro de 2004 Histórico Sec. XVII Galileu: descobriu que a Via-Láctea consistia de uma coleção de estrelas. Sec. XVIII/XIX
A Via Láctea Curso de Extensão Universitária Astronomia: Uma Visão Geral 12 a 17 de janeiro de 2004 Histórico Sec. XVII Galileu: descobriu que a Via-Láctea consistia de uma coleção de estrelas. Sec. XVIII/XIX
Radiação Solar como forçante climática
 Radiação Solar como forçante climática O Sol fornece 99,97 % Emite 2,34 x10 22 MJ/min. Terra intercepta apenas 1,06 x 10 13 MJ (milionésimo) Milhares de vezes maior que consumo anual de energia no planeta.
Radiação Solar como forçante climática O Sol fornece 99,97 % Emite 2,34 x10 22 MJ/min. Terra intercepta apenas 1,06 x 10 13 MJ (milionésimo) Milhares de vezes maior que consumo anual de energia no planeta.
Emissão Veicular de Gases de Efeito Estufa (GEE) Em Automotivos Movidos a Diesel
 Emissão Veicular de Gases de Efeito Estufa (GEE) Em Automotivos Movidos a Diesel *MELO JUNIOR, A. S a.;gatti, L. b.; FERREIRA, P. G c.; FRUGOLLI, A. d a.universidade de São Paulo (USP)/Universidade Paulista,
Emissão Veicular de Gases de Efeito Estufa (GEE) Em Automotivos Movidos a Diesel *MELO JUNIOR, A. S a.;gatti, L. b.; FERREIRA, P. G c.; FRUGOLLI, A. d a.universidade de São Paulo (USP)/Universidade Paulista,
Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2
 11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
28-02-2015. Sumário. Atmosfera da Terra. Interação Radiação-Matéria 23/02/2015
 Sumário Na : Radiação, Matéria e Estrutura Unidade temática 2. O ozono como filtro protetor da Terra. Formação e decomposição do ozono na atmosfera. Filtros solares. Alternativas aos CFC. Como se mede
Sumário Na : Radiação, Matéria e Estrutura Unidade temática 2. O ozono como filtro protetor da Terra. Formação e decomposição do ozono na atmosfera. Filtros solares. Alternativas aos CFC. Como se mede
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Disciplina: Físico-Química II Professora: Claudia
 Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Disciplina: Físico-Química II Professora: Claudia Aluno: Julys Pablo Atayde Fernandes Células a Combustível:
Universidade Federal da Paraíba Centro de Ciências Exatas e da Natureza Departamento de Química Disciplina: Físico-Química II Professora: Claudia Aluno: Julys Pablo Atayde Fernandes Células a Combustível:
Radiação Solar e Vento Solar
 INPE Instituto Nacional de Pesquisas Espaciais CMC-213-3 Modelagem de Sensores e Atuadores em Controle de Atitude e Órbita Radiação Solar e Vento Solar Professor: Mário César Ricci Aluno: Delfim Pinto
INPE Instituto Nacional de Pesquisas Espaciais CMC-213-3 Modelagem de Sensores e Atuadores em Controle de Atitude e Órbita Radiação Solar e Vento Solar Professor: Mário César Ricci Aluno: Delfim Pinto
Gabarito Química - Grupo A. 1 a QUESTÃO: (1,0 ponto) Avaliador Revisor
 VESTIB LAR Gabarito Química - Grupo A 1 a QUESTÃO: (1,0 ponto) Avaliador Revisor Muitos álcoois, como o butanol (C 4 H 10 O), têm importância comercial como solventes e matériasprimas na produção industrial
VESTIB LAR Gabarito Química - Grupo A 1 a QUESTÃO: (1,0 ponto) Avaliador Revisor Muitos álcoois, como o butanol (C 4 H 10 O), têm importância comercial como solventes e matériasprimas na produção industrial
2. (Ifsc 2014) A reação abaixo representa este processo: CO 3H H COH H O ΔH 12 kcal/mol
 1. (Uel 2014) A gasolina é uma mistura de vários compostos. Sua qualidade é medida em octanas, que definem sua capacidade de ser comprimida com o ar, sem detonar, apenas em contato com uma faísca elétrica
1. (Uel 2014) A gasolina é uma mistura de vários compostos. Sua qualidade é medida em octanas, que definem sua capacidade de ser comprimida com o ar, sem detonar, apenas em contato com uma faísca elétrica
Astronomia fora do visível Beatriz García, Ricardo Moreno, Rosa M. Ros
 Astronomia fora do visível Beatriz García, Ricardo Moreno, Rosa M. Ros União Astronómica Internacional Universidade Tecnológica Nacional, Argentina Colégio Retamar de Madrid, Espanha Universidade Politécnica
Astronomia fora do visível Beatriz García, Ricardo Moreno, Rosa M. Ros União Astronómica Internacional Universidade Tecnológica Nacional, Argentina Colégio Retamar de Madrid, Espanha Universidade Politécnica
Atmosfera terrestre: Descrição física e química; emissões atmosféricas naturais e antropogênicas; suas transformações. Transporte atmosférico.
 Atmosfera terrestre: Descrição física e química; emissões atmosféricas naturais e antropogênicas; suas transformações. Transporte atmosférico. Por: Vânia Palmeira Campos UFBA IQ -Dpto Química Analítica
Atmosfera terrestre: Descrição física e química; emissões atmosféricas naturais e antropogênicas; suas transformações. Transporte atmosférico. Por: Vânia Palmeira Campos UFBA IQ -Dpto Química Analítica
MÁQUINAS TÉRMICAS AT-101
 Universidade Federal do Paraná Curso de Engenharia Industrial Madeireira MÁQUINAS TÉRMICAS AT-101 M.Sc. Alan Sulato de Andrade alansulato@ufpr.br INTRODUÇÃO: Uma das formas mais empregadas para produção
Universidade Federal do Paraná Curso de Engenharia Industrial Madeireira MÁQUINAS TÉRMICAS AT-101 M.Sc. Alan Sulato de Andrade alansulato@ufpr.br INTRODUÇÃO: Uma das formas mais empregadas para produção
RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011
 RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011 Questão 26 Como a questão pede a separação do sólido solúvel do líquido, o único processo recomendado é a destilação simples. Lembrando que filtração e decantação
RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011 Questão 26 Como a questão pede a separação do sólido solúvel do líquido, o único processo recomendado é a destilação simples. Lembrando que filtração e decantação
Meio interestelar. Roberto Ortiz EACH/USP
 Meio interestelar Roberto Ortiz EACH/USP Noções intuitivas A observação do céu noturno a olho nu propicia a detecção de cerca de 6000 estrelas. Diversas regiões parecem estar desprovidas de estrelas. Essas
Meio interestelar Roberto Ortiz EACH/USP Noções intuitivas A observação do céu noturno a olho nu propicia a detecção de cerca de 6000 estrelas. Diversas regiões parecem estar desprovidas de estrelas. Essas
ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos
 Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
Nova Friburgo, de de 2014. Aluno (a): Gabarito Professor(a): ATIVIDADES EM QUÍMICA Recuperação paralela de conteúdos Nº: Turma:100 Assuntos: Estrutura atômica; Tabela Periódica; Propriedades periódicas;
Sabemos hoje em dia que os anéis são formados por mil milhões de partículas de gelo, misturadas com rocha e silicatos, algumas do tamanho de LU11
 SATURNO Se existe outro planeta, para além da Terra, que todos conseguem reconhecer instantaneamente, é certamente Saturno, o sexto membro da família solar. Apesar de agora sabermos que Júpiter, Úrano
SATURNO Se existe outro planeta, para além da Terra, que todos conseguem reconhecer instantaneamente, é certamente Saturno, o sexto membro da família solar. Apesar de agora sabermos que Júpiter, Úrano
O MUNDO QUE VIVEMOS CAPITULO 1 DO VIANELLO E ALVES METEOROLOGIA BÁSICA E APLICAÇÕES
 O MUNDO QUE VIVEMOS CAPITULO 1 DO VIANELLO E ALVES METEOROLOGIA BÁSICA E APLICAÇÕES O SOL E O SISTEMA SOLAR SE ENCONTRA NA VIA-LÁCTEA SIMPLES GRAUM DE AREIA ENTRE AS INCONTAVEIS GALÁXIAS DO UNIVERSO VISÍVEL
O MUNDO QUE VIVEMOS CAPITULO 1 DO VIANELLO E ALVES METEOROLOGIA BÁSICA E APLICAÇÕES O SOL E O SISTEMA SOLAR SE ENCONTRA NA VIA-LÁCTEA SIMPLES GRAUM DE AREIA ENTRE AS INCONTAVEIS GALÁXIAS DO UNIVERSO VISÍVEL
Teoria Ácido-Base e Reações Químicas
 Aula ao Vivo Teoria Ácido-Base e Reações Químicas Química Allan Rodrigues 27.04.2015 Existem várias teorias sobre ácidos e bases. Dentre elas, temos a teoria do químico sueco Svante August Arrhenius, que
Aula ao Vivo Teoria Ácido-Base e Reações Químicas Química Allan Rodrigues 27.04.2015 Existem várias teorias sobre ácidos e bases. Dentre elas, temos a teoria do químico sueco Svante August Arrhenius, que
Evolução Estelar e A Via-Láctea
 Introdução à Astronomia Evolução Estelar e A Via-Láctea Rogério Riffel http://astro.if.ufrgs.br Formação estelar - Estrelas se formam dentro de concentrações relativamente densas de gás e poeira interestelar
Introdução à Astronomia Evolução Estelar e A Via-Láctea Rogério Riffel http://astro.if.ufrgs.br Formação estelar - Estrelas se formam dentro de concentrações relativamente densas de gás e poeira interestelar
5 as Olimpíadas Nacionais de Astronomia
 5 as Olimpíadas Nacionais de Astronomia Prova da eliminatória regional 14 de Abril de 2009 15:00 Duração máxima 120 minutos Nota: Ler atentamente todas as questões. Existe uma tabela com dados no final
5 as Olimpíadas Nacionais de Astronomia Prova da eliminatória regional 14 de Abril de 2009 15:00 Duração máxima 120 minutos Nota: Ler atentamente todas as questões. Existe uma tabela com dados no final
LIGAÇÕES INTERATÔMICAS
 UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
A resposta correta deve ser a letra B.
 ITA - 1999 1- (ITA-99) Assinale a opção CORRETA em relação à comparação das temperaturas de ebulição dos seguintes pares de substâncias: a) Éter dimetílico > etanol; Propanona > ácido etanóico; Naftaleno
ITA - 1999 1- (ITA-99) Assinale a opção CORRETA em relação à comparação das temperaturas de ebulição dos seguintes pares de substâncias: a) Éter dimetílico > etanol; Propanona > ácido etanóico; Naftaleno
