Introdução aos Materiais Imperfeições em Sólidos Metais DEMEC TM229 Prof Adriano Scheid
|
|
|
- Regina Mangueira Figueiroa
- 7 Há anos
- Visualizações:
Transcrição
1 Introdução aos Materiais Imperfeições em Sólidos Metais DEMEC TM229 Prof Adriano Scheid
2 Introdução Os sólidos contém inúmeras imperfeições nas estruturas cristalinas e muitas propriedades são alteradas significativamente pela presença dos defeitos. Os defeitos cristalinos são classificados conforme a sua geometria. Neste capítulo, serão estudados: - Defeitos Pontuais - Defeitos Lineares -Defeitos de Superície (ou de contorno).
3 Vazios ou Auto-Intersticiais O defeito mais simples é o vazio ou posição do reticulado vazio, que ocorre quando existe a falta de um átomo na posição do reticulado. A presença dos vazios eleva a entropia do material. O número de vazios em equilíbrio (N v ) depende da temperatura e aumenta com o aumento desta. N nº total de posições de átomos Q v Energia para a formação do vazio T Temperatura absoluta K Constante de Boltzmann Auto-Intersticial Vazio
4 Vazios ou Auto-Intersticiais O número e vazios aumenta exponencialmente com a temperatura. Para metais, logo abaixo da temperatura de fusão, o valor N v /N é de 10-4, o que corresponde a um vazio a cada posições no reticulado. Auto-Intersticial Defeito que ocorre quando um átomo do material é forçado a ocupar um interstício, um pequeno espaço que não está preenchido em condições normais. O resultado é a geração de um campo de tensão, pois o átomo é maior que o espaço intersticial. Assim, a formação deste tipo de defeito é menos freqüente que os vazios.
5 : Impurezas em Sólidos Ligas Metálicas Um metal puro com 99,9999% apresenta entre a átomos de impureza presentes por m³ de material. A maior parte dos metais são ligas, em que as impurezas são adicionadas intencionalmente a fim de conferir propriedades e características específicas ao material. Na maior parte dos casos, o objetivo de adicionar elementos de liga é aumentar a resistência mecânica e resistência à corrosão. Solução Sólida A adição de impurezas a um sólido resulta na formação de soluções sólidas ou uma segunda fase, conforme o elemento adicionado, a concentração do elemento e a temperatura.
6 : Impurezas em Sólidos Soluto e Solvente Para as ligas metálicas, os termos soluto e solvente são usados. O primeiro representa o elemento em menor teor e o segundo diz respeito ao elemento majoritátio. Soluções Sólidas Uma solução sólida é formada quando os átomos são adicionados ao material formado pelo elemento majoritário, a estrutura cristalina é mantida e não são formadas novas estruturas. Átomo de impureza Substitucional Átomo de impureza Intersticial
7 : Impurezas em Sólidos Defeitos pontuais de impurezas são encontradas na forma Substitucional e Intersticial. Existem alguns fatores que determinam a formação de Solução Sólida Substitucional, conforme segue: - Tamanho Atômico Uma quantidade apreciável de elementos pode ser adicionado desde que a razão de diâmetros atômicos não ultrapasse 15%. Quando a diferença é superada, criam-se distorções na estrutura cristalina e uma nova fase é formada. - Estrutura Cristalina Para maior solubilidade, as estruturas cristalinas dos dois metais devem ser as mesmas.
8 : Impurezas em Sólidos - Eletronegatividade Quando dois tipos de átomos são misturados, quanto mais para os extremos da tabela periódica estiverem os elementos (maior a eletropositividade de um e eletronegatividade do outro), maior a tendência à formação de Intermetálicos ao invés de solução sólida substitucional. - Valência Átomos de um solvente apresentam maior tendência em dissolver um soluto que apresente maior valência. Exemplo: Na solução sólida substitucional de Cobre em Níquel, a solubilidade é total, com raios atômicos de 0,128 e 0,125nm, ambos com estrutura cristalina Cúbica de Faces Centradas, eletronegatividades de 1,9 e 1,8, com valências +1 (podendo ser +2) para o Cobre e +2 para o Níquel.
9 : Impurezas em Sólidos Solução Sólida Intersticial Neste tipo de solução, os átomos de soluto ocupam os espaços vazios que existem entre os átomos de solvente. Uma vez que os metais apresentam elevados fatores de empacotamento atômico, o tamanho dos interstícios é pequeno, podendo alojar elementos de pequeno tamanho, muito menores que os átomos de solvente. - A solubilidade intersticial é geralmente menor que 10%. - Os átomos destes elementos pequenos são maiores que os espaços intersticiais, resultando em distorção no reticulado cristalino. Exemplo: Solução sólida de Carbono em Ferro, cujos raios atômicos são 0,071 e 0,124nm, com limite de solubilidade máxima de 2% em peso.
10 Defeitos Lineares - Discordâncias Uma discordância é um defeito linear unidimensional, ao longo do qual os átomos estão desalinhados. Esta é chamada discordância em linha ou em cunha e é como um plano extra de átomos. Vetor de Burgers Os átomos estão distorcidos ao redor do defeito e esta distorção é reduzida à medida que se afasta da mesma. Linha da discordância em cunha
11 Defeitos Lineares - Discordâncias Um outro tipo de discordância, chamada discordância helicoidal, pode ser gerada pela aplicação de tensões de cisalhamento. Linha da discordância Vetor de Burgers
12 Defeitos Lineares - Discordâncias Vetor de Burgers A magnitude e direção associada à distorção do reticulado causada por uma discordância pode ser expressa em termos do vetor de Burgers, representado pela letra b. Discordâncias observadas em uma liga de Titânio a partir de Microscopia Eletrônica de Transmissão. As discordâncias surgem a partir de processos de solidificação, deformação plástica e tensões térmicas resultantes de rápido resfriamento.
13 Defeitos Interfaciais Os defeitos interfaciais são contornos que apresentam duas dimensões e normalmente separam regiões dentro do material que apresentam diferentes estruturas cristalinas ou orientações cristalográficas. Estas imperfeições incluem: a superfície externa, os contornos de grão, os contornos de macla, defeitos de empilhamento, e contornos de fases. Superfícies Externas Os átomos da superfície externa estão ligados a um número menor de vizinhos mais próximos quando comparados aos átomos do interior do material. Estes átomos apresentam energia mais elevada, relacionada à energia das ligações não regulares.
14 : Superfícies Externas Os materiais tendem a minimizar esta energia pela redução da área superficial. Um bom exemplo ocorre nos líquidos, que assumem formas de mínima área superficial. Um exemplo disto são as gotas de água, que assume a forma esférica. Uma limitação ocorre para os materiais sólidos, haja visto a rigidez mecânica. Contornos de Grão Ângulo de Desalinhamento Outro exemplo de defeito de superfície são os contornos de grão. Nesta região, existe uma largura equivalente a alguns espaçamentos atômicos e apresenta um desencontro devido à diferente orientação cristalina. Contorno de grão de alto ângulo Contorno de grão de baixo ângulo Ângulo de Desalinhamento
15 : Contornos de Grão O grau de desalinhamento pode variar, conforme segue: - Contorno de grão de baixo ângulo, ocorre quando a diferença de orientação é pequena. Podem ser considerados como arranjos de discordâncias e são chamados contornos inclinados cujo ângulo de desalinhamento é indicado na figura como. Quando o ângulo de desalinhamento é maior, chamamos este de contorno de alto ângulo. A energia dos contornos é função do ângulo formado de desalinhamento e apresenta maiores valores para os contornos de alto ângulo.
16 : Contornos de Grão A energia dos contornos é mais elevada em função das ligações mais irregulares formadas, podendo ser comparada de forma similar à energia da superfície externa. Em elevadas temperaturas, os contornos tendem a migrar, promovendo o crescimento dos grãos, como resultado da minimização da energia total de contorno de grão do material. Os átomos de impureza são segregadas ao longo dos contornos dos grãos, devido à energia mais elevada. Apesar da desordem e falta de regularidade dos contornos, um material policristalino é muito resistente e apresenta forças de coesão dentro e através dos contornos de grão.
17 : Contornos de Macla Os contornos de macla são um tipo especial de contorno de grão, em que existe uma simetria específica de espelho no reticulado. A macla surge a partir da aplicação de deformação por forças cisalhantes (HCP e CCC) e também por tratamento térmico seguido de deformação (CFC). A macla ocorre em planos definidos da estrutura cristalina e em direções específicas. Contorno do plano de macla Superfície polida e com ataque químico
18 : Outros Defeitos de Interface Outros defeitos de interface são os defeitos de empilhamento e contornos de fase. Os defeitos de empilhamento ocorrem em metais quando há falha no empilhamento de planos compactos. Os contornos de fase existem em materiais multifásicos e resultam da interface entre fases com propriedades físicas e químicas diferentes. Defeitos de Volume Estes defeitos são maiores em relação aos anteriormente discutidos. Entre eles estão os poros, trincas, inclusões.
19 : Vibrações Atômicas As vibrações atômicas em sólidos podem ser pensadas como imperfeições cristalinas. É importante destacar a relação entre: Temperatura x Defeitos Cristalinos Para Vazios:
20 Exercício - Aula dia 06/10/2010 Preparar apresentação para seminário (15 ) sobre os seguintes itens: a- Mecamismos de Crescimento de Grão b- Mecanismos de formação de Macla
21 Introdução aos Materiais Imperfeições em Sólidos Cerâmicas DEMEC TM229 Prof Adriano Scheid
22 Defeitos Pontuais Assim como nos metais, vazios e intersticiais podem existir, entretanto, como nas Cerâmicas contém pelo menos dois tipos de íons, defeitos de cada tipo de íon são possíveis. Exemplo: Para o NaCl, vazios e intersticiais de cada um dos elementos (Na e Cl) pode ocorrer. Existe baixa probabilidade de ocorrer intersticiais de ânions, uma vez que estes são grandes e tensões de distorção são geradas. Vazio de ânion Vazio de Cátion Cátion Intersticial
23 Defeitos da Estrutura A expressão Defeitos da Estrutura é usada para designar os tipos e concentrações dos defeitos atômicos nas Cerâmicas. Eletroneutralidade Uma vez que os átomos são considerados como íons carregados, quando existem defeitos na estrutura, torna-se importante manter a eletroneutralidade. O material apresenta eletroneutralidade quando o número de cargas positivas e negativas é igual.
24 Defeito de Frenkel O defeito de Frenkel envolve um par, um vazio de cátion e um cátion intersticial. Pode ser pensado como o deslocamento de um cátion da sua posição normal para um interstício. Há balanço de carga uma vez que o número total de cátions é o mesmo. Defeito de Schottky Defeito de Frenkel
25 Defeito de Schottky O defeito de Schottky ocorre em materiais Cerâmicos do tipo AX, e consiste de um vazio de um cátion e de um ânion. Uma vez que cátions e ânions apresentam a mesma carga, a neutralidade de carga do cristal é mantida. Defeito de Schottky Defeito de Frenkel
26 Estequiometria A razão de cátions e ânions não é alterada pela formação dos defeitos de Frenkel e Schottky e, neste caso, o material Cerâmico é dito estequiométrico. Um material estequiométrico pode ser definido como sendo um estado para compostos iônicos onde existe a exata razão entre cátions e ânions. Exemplo: NaCl é um composto estequiométrico, uma vez que a razão de cátions e ânions é 1:1.
27 Estequiometria Um material é dito Não-Estequiométrico quando existe algum desvio da exata razão 1:1. A não-estequiometria envolve os materiais Cerâmicos com dois estados de valência para o mesmo ion. Exemplo: FeO (Wüstita), onde os íons de Ferro podem ocorrer como Fe +2 e Fe +3. O número destes tipos de íon depende da temperatura e da pressão de Oxigênio. A presença de Fe +3 interrompe a eletroneutralidade do cristal pela introdução de uma carga +1 em excesso, podendo gerar vazios de cátions Fe 2+.
28 Estequiometria O material é não-estequiométrico uma vez que o Oxigênio apresenta um íon em excesso em relação aos íons de Ferro. Apesar disso, o cristal permanece eletricamente neutro. Vazio de Fe 2+
29 Equilíbrio de Defeitos O número de defeitos de Frenkel e Schottky é dependente e aumenta com a temperatura, conforme segue: Defeitos de Frenkel N fr é o número de cátion-vazio / cátion-intersticial e N é o número total de locais no reticulado, Q fr é a energia necessária para a formação de um defeito de Frenkel, T é a temperatura absoluta e k é a constante de Boltzmann. Defeitos de Schottky N s é o número de vazios de par de íons e N é o número total de locais no reticulado para com postos tipo AX, Q s é a energia necessária para a formação de um defeito de Schottky, T é a temperatura absoluta e k é a constante de Boltzmann.
30 Impurezas em Cerâmicas A adição de elementos às Cerâmicas pode levar à formação de soluções sólidas substitucionais ou intersticiais. Soluções Sólidas Intersticiais Podem se formar soluções sólidas Intersticiais quando o íon apresenta tamanho pequeno em relação ao ânion. Soluções Sólidas Substitucionais Uma vez que o material é formado por cátions e ânions, o átomo de soluto substituirá o íon de solvente mais eletricamente similar.
31 Impurezas em Cerâmicas Por exemplo, no Cerâmico NaCl, os íons Ca 2+ substituirão preferencialmente os íons Na + e o átomo de O 2- substituirá preferencialmente os íons Cl -. Para que ocorra apreciável solubilidade substitucional, o tamanho do íon e a carga devem ser similares ao do íon de solvente. Ions de impureza intersticial Ions de impureza substitucional
32 Introdução aos Materiais Imperfeições em Sólidos Polímeros DEMEC TM229 Prof Adriano Scheid
33 Defeitos em Polímeros Uma vez que os Polímeros apresentam estruturas formadas por cadeias carbônicas e que o conceito de cristalinidade é diferente em relação aos Metais e Cerâmicos, o conceito de defeito pontual também é diferente. Em regiões cristalinas nos Polímeros são observados defeitos pontuais similares aos encontrados nos metais, como vazios e intersticiais (átomos ou íons). As extremidades das cadeias são consideradas defeitos, uma vez que apresentam configurações diferentes em relação à região média da cadeia. Os vazios são relacionados às extremidades das cadeias. Defeitos adicionais são gerados a partir de ramificações nas cadeias.
34 Defeitos em Polímeros Discordâncias helicoidais ocorrem em polímeros, assim como átomos ou íons de impurezas ou ainda grupos de átomos ou íons podem ser incorporados às moléculas dos Polímeros como intersticiais. Discordância Espiral Defeitos aparecem nas interfaces entre as regiões cristalinas e não cristalinas e nas regiões dobradas das cadeias. Contorno de cristalito Cadeias Pendentes Região Não- Cristalina Impureza Pontas das Cadeias Vazio Ramificação Discordância em cunha (plano extra) Cadeias Frouxas
4- IMPERFEIÇÕES CRISTALINAS
 ASSUNTO 4- IMPERFEIÇÕES CRISTALINAS - Defeitos pontuais - Defeitos de linha (discordâncias) - Defeitos de interface (grão e maclas) - Defeitos volumétricos (inclusões, precipitados) Eleani Maria da Costa
ASSUNTO 4- IMPERFEIÇÕES CRISTALINAS - Defeitos pontuais - Defeitos de linha (discordâncias) - Defeitos de interface (grão e maclas) - Defeitos volumétricos (inclusões, precipitados) Eleani Maria da Costa
DEFEITOS CRISTALINOS
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais DEFEITOS CRISTALINOS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia 2º Semestre de 2005
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais DEFEITOS CRISTALINOS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia 2º Semestre de 2005
AULA 04 IMPERFEIÇÕES CRISTALINAS Capítulo 04
 AULA 04 IMPERFEIÇÕES CRISTALINAS Capítulo 04 1 IMPERFEIÇÕES CRISTALINAS Estrutura perfeita no arranjo atômico, existe?? Material Cristalino 2 IMPERFEIÇÕES CRISTALINAS 3 Imagem representagva de um plano
AULA 04 IMPERFEIÇÕES CRISTALINAS Capítulo 04 1 IMPERFEIÇÕES CRISTALINAS Estrutura perfeita no arranjo atômico, existe?? Material Cristalino 2 IMPERFEIÇÕES CRISTALINAS 3 Imagem representagva de um plano
IMPERFEIÇÕES EM SÓLIDOS. Bento Gonçalves, 2014.
 IMPERFEIÇÕES EM SÓLIDOS Bento Gonçalves, 2014. O QUE É UM DEFEITO? É uma imperfeição ou um "erro" no arranjo cristalino dos átomos em um cristal. Podem envolver uma irregularidade: Na posição dos átomos
IMPERFEIÇÕES EM SÓLIDOS Bento Gonçalves, 2014. O QUE É UM DEFEITO? É uma imperfeição ou um "erro" no arranjo cristalino dos átomos em um cristal. Podem envolver uma irregularidade: Na posição dos átomos
ESTADOS EXCITADOS: fonões, electrões livres
 Capítulo III.1 DEFEITOS (IMPERFEIÇÕES) NOS SÓLIDOS CRISTALINOS ESTADOS EXCITADOS: fonões, electrões livres DEFEITOS TRANSIENTES: fotões, electrões, neutrões tõ IMPERFEIÇÕES ESTRUTURAIS IMPORTÂNCIA DEFEITOS
Capítulo III.1 DEFEITOS (IMPERFEIÇÕES) NOS SÓLIDOS CRISTALINOS ESTADOS EXCITADOS: fonões, electrões livres DEFEITOS TRANSIENTES: fotões, electrões, neutrões tõ IMPERFEIÇÕES ESTRUTURAIS IMPORTÂNCIA DEFEITOS
Fundamentos de Ciência e Engenharia de Materiais. DEFEITOS CRISTALINOS Prof. Dr. André Paulo Tschiptschin
 Fundamentos de Ciência e Engenharia de Materiais DEFEITOS CRISTALINOS Prof. Dr. André Paulo Tschiptschin Defeitos cristalinos Defeito cristalino: imperfeição do reticulado cristalino Classificação dos
Fundamentos de Ciência e Engenharia de Materiais DEFEITOS CRISTALINOS Prof. Dr. André Paulo Tschiptschin Defeitos cristalinos Defeito cristalino: imperfeição do reticulado cristalino Classificação dos
DEFEITOS CRISTALINOS. Conceitos Gerais
 DEFEITOS CRISTALINOS Conceitos Gerais CAPA 1 CAPA 2 1 Defeitos atômicos usados para reduzir a emissão de poluentes 2 Conversor catalítico poluente é retido pelo material que tem esta capacidade em função
DEFEITOS CRISTALINOS Conceitos Gerais CAPA 1 CAPA 2 1 Defeitos atômicos usados para reduzir a emissão de poluentes 2 Conversor catalítico poluente é retido pelo material que tem esta capacidade em função
Materiais e sua propriedades Aula 5
 Materiais e sua propriedades Aula 5 Prof a. Dr a. Vânia Trombini Hernandes Imperfeições nos sólidos cristalinos 2 º Q - 2017 Defeitos Cristalinos Até agora, ao estudar os materiais cristalinos, tem-se
Materiais e sua propriedades Aula 5 Prof a. Dr a. Vânia Trombini Hernandes Imperfeições nos sólidos cristalinos 2 º Q - 2017 Defeitos Cristalinos Até agora, ao estudar os materiais cristalinos, tem-se
IMPERFEIÇÕES EM SÓLIDOS
 IMPERFEIÇÕES EM SÓLIDOS INTRODUÇÃO Ao estudar os materiais cristalinos, tem-se admitido que existe uma perfeita ordem em escala atômica Contudo esse tipo de sólido idealizado não existe, todos os materiais
IMPERFEIÇÕES EM SÓLIDOS INTRODUÇÃO Ao estudar os materiais cristalinos, tem-se admitido que existe uma perfeita ordem em escala atômica Contudo esse tipo de sólido idealizado não existe, todos os materiais
ESTRUTURA CRISTALINA E IMPERFEIÇÕES NOS SÓLIDOS ESTRUTURA CRISTALINA E IMPERFEIÇÕES NOS SÓLIDOS
 ESTRUTURA CRISTALINA E IMPERFEIÇÕES NOS SÓLIDOS Prof. M.Sc.: Anael Krelling 1 CONCEITOS FUNDAMENTAIS Materiais sólidos podem ser classificados de acordo com a regularidade com que os seus átomos ou íons
ESTRUTURA CRISTALINA E IMPERFEIÇÕES NOS SÓLIDOS Prof. M.Sc.: Anael Krelling 1 CONCEITOS FUNDAMENTAIS Materiais sólidos podem ser classificados de acordo com a regularidade com que os seus átomos ou íons
APONTAMENTOS PRIMEIRA PROVA DE MATERIAIS DE CONSTRUÇÃO I
 APONTAMENTOS PRIMEIRA PROVA DE MATERIAIS DE CONSTRUÇÃO I Normalização na construção civil Normalizar: É padronizar atividades específicas e repetitivas. Normas técnicas: Documentos aprovados por instituições
APONTAMENTOS PRIMEIRA PROVA DE MATERIAIS DE CONSTRUÇÃO I Normalização na construção civil Normalizar: É padronizar atividades específicas e repetitivas. Normas técnicas: Documentos aprovados por instituições
Ligações químicas e estrutura dos materiais
 Disciplina : - MFI Professores: Guilherme Ourique Verran - Dr. Eng. Metalúrgica Aula 02 Revisão de alguns conceitos fundamentais da Ciência dos Materiais Ligações químicas e estrutura dos materiais Conceitos
Disciplina : - MFI Professores: Guilherme Ourique Verran - Dr. Eng. Metalúrgica Aula 02 Revisão de alguns conceitos fundamentais da Ciência dos Materiais Ligações químicas e estrutura dos materiais Conceitos
Defeitos cristalinos. (monocristais) Ponto. Superfície
 [7] Defeitos cristalinos 1> Ligações atômicas propriedades resistência teórica (monocristais) causa da discrepância > resistência experimental defeitos cristalinos Ponto Defeitos cristalinos Linha Superfície
[7] Defeitos cristalinos 1> Ligações atômicas propriedades resistência teórica (monocristais) causa da discrepância > resistência experimental defeitos cristalinos Ponto Defeitos cristalinos Linha Superfície
Aula 5. Defeitos cristalinos
 Aula 5 Defeitos cristalinos 1 DEFEITOS - Defeitos pontuais - Defeitos de linha (discordâncias) - Defeitos de interface (grão e maclas) - Defeitos volumétricos (inclusões, precipitados) 2 O QUE É UM DEFEITO?
Aula 5 Defeitos cristalinos 1 DEFEITOS - Defeitos pontuais - Defeitos de linha (discordâncias) - Defeitos de interface (grão e maclas) - Defeitos volumétricos (inclusões, precipitados) 2 O QUE É UM DEFEITO?
ESTRUTURA CRISTALINA E IMPERFEIÇÕES NOS SÓLIDOS ESTRUTURA CRISTALINA E IMPERFEIÇÕES NOS SÓLIDOS
 ESTRUTURA CRISTALINA E IMPERFEIÇÕES NOS SÓLIDOS Prof. Dr.: Anael Krelling 1 CONCEITOS FUNDAMENTAIS Materiais sólidos podem ser classificados de acordo com a regularidade com que os seus átomos ou íons
ESTRUTURA CRISTALINA E IMPERFEIÇÕES NOS SÓLIDOS Prof. Dr.: Anael Krelling 1 CONCEITOS FUNDAMENTAIS Materiais sólidos podem ser classificados de acordo com a regularidade com que os seus átomos ou íons
Sugestões de estudo para a P1
 Sugestões de estudo para a P1 1) Considere a curva de energia potencial da ligação entre dois átomos (E) apresentada ao lado, e as três afirmações a Seguir: I. Na distância interatômica r o as forças de
Sugestões de estudo para a P1 1) Considere a curva de energia potencial da ligação entre dois átomos (E) apresentada ao lado, e as três afirmações a Seguir: I. Na distância interatômica r o as forças de
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais UNIDADE 6 DEFEITOS DO SÓLIDO CRISTALINO
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais UNIDADE 6 DEFEITOS DO SÓLIDO CRISTALINO PMT 3110 - Introdução à Ciência dos Materiais para Engenharia
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais UNIDADE 6 DEFEITOS DO SÓLIDO CRISTALINO PMT 3110 - Introdução à Ciência dos Materiais para Engenharia
Universidade Estadual de Ponta Grossa Departamento de Engenharia de Materiais Disciplina: Ciência dos Materiais 1. Imperfeições nos sólidos
 Universidade Estadual de Ponta Grossa Departamento de Engenharia de Materiais Disciplina: Ciência dos Materiais 1 Imperfeições nos sólidos 1º semestre / 2016 Imperfeições nos Sólidos ASSUNTOS ABORDADOS...
Universidade Estadual de Ponta Grossa Departamento de Engenharia de Materiais Disciplina: Ciência dos Materiais 1 Imperfeições nos sólidos 1º semestre / 2016 Imperfeições nos Sólidos ASSUNTOS ABORDADOS...
Aula 7: Cristais 0,0,1 1/2,1/2,1/2 0,0,0 0,1/2,0 0,1,0 1/2,1/2,0 1,0,0. Aula 7 - Profa. Adélia
 Aula 7: Cristais Para poder descrever a estrutura cristalina é necessário escolher uma notação para posições, direções e planos As posições são definidas dentro de um cubo com lado unitário. 0,0,1 1/2,1/2,1/2
Aula 7: Cristais Para poder descrever a estrutura cristalina é necessário escolher uma notação para posições, direções e planos As posições são definidas dentro de um cubo com lado unitário. 0,0,1 1/2,1/2,1/2
ESTRUTURA DOS SÓLIDOS CRISTALINOS. Mestranda: Marindia Decol
 ESTRUTURA DOS SÓLIDOS CRISTALINOS Mestranda: Marindia Decol Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
ESTRUTURA DOS SÓLIDOS CRISTALINOS Mestranda: Marindia Decol Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
MATERIAIS ELÉTRICOS - MEL
 MATERIAIS ELÉTRICOS - MEL Unidade 1 Diagramas de Fases Roteiro da Aula Importância do Tema Revisão: impurezas nos sólidos Definições: componente, sistema, fase e equilíbrio Sistemas Unários e Binários
MATERIAIS ELÉTRICOS - MEL Unidade 1 Diagramas de Fases Roteiro da Aula Importância do Tema Revisão: impurezas nos sólidos Definições: componente, sistema, fase e equilíbrio Sistemas Unários e Binários
TM229 - Introdução aos Materiais
 TM229 - Introdução aos Materiais 2009.2 Ana Sofia C. M. D Oliveira Introdução aos materiais O que determina o comportamento/propriedades dos materiais? Composição química e microestrutura Cada uma destas
TM229 - Introdução aos Materiais 2009.2 Ana Sofia C. M. D Oliveira Introdução aos materiais O que determina o comportamento/propriedades dos materiais? Composição química e microestrutura Cada uma destas
DEFEITOS DO SÓLIDO CRISTALINO DIFUSÃO NO ESTADO SÓLIDO
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais DEFEITOS DO SÓLIDO CRISTALINO DIFUSÃO NO ESTADO SÓLIDO PMT 3100 - Fundamentos de Ciência e Engenharia
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais DEFEITOS DO SÓLIDO CRISTALINO DIFUSÃO NO ESTADO SÓLIDO PMT 3100 - Fundamentos de Ciência e Engenharia
Fundamentos de Ciência e Engenharia de Materiais Prof. Dr. André Paulo Tschiptschin
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Fundamentos de Ciência e Engenharia de Materiais Prof. Dr. André Paulo Tschiptschin CONCEITUAÇÃO Difusão:
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Fundamentos de Ciência e Engenharia de Materiais Prof. Dr. André Paulo Tschiptschin CONCEITUAÇÃO Difusão:
Estruturas cristalinas - Reticulado cristalino
 Página 1 de 9 MENU PRINCIPAL CONTEUDO TÉCNICO DOWNLOAD CONTATO ENTRETENIMENTO LOGIN search.... Home PAINEL Ciência dos Materiais Estruturas cristalinas - Reticulado cristalino Estruturas cristalinas -
Página 1 de 9 MENU PRINCIPAL CONTEUDO TÉCNICO DOWNLOAD CONTATO ENTRETENIMENTO LOGIN search.... Home PAINEL Ciência dos Materiais Estruturas cristalinas - Reticulado cristalino Estruturas cristalinas -
Materiais e Reciclagem. 4 Estruturas Cristalinas com Defeitos
 Instituto de Ciência e Tecnologia de Sorocaba Materiais e Reciclagem 4 Estruturas Cristalinas com Defeitos Professor Sandro Donnini Mancini Sorocaba, Fevereiro de 2019. Mesmo em materiais considerados
Instituto de Ciência e Tecnologia de Sorocaba Materiais e Reciclagem 4 Estruturas Cristalinas com Defeitos Professor Sandro Donnini Mancini Sorocaba, Fevereiro de 2019. Mesmo em materiais considerados
Ligação iônica Ligação covalente Ligação metálica
 Principais Tipos de Ligações Químicas Ligação iônica Ligação covalente Ligação metálica Iônicas Covalentes Metálicas Ligações químicas A maioria dos compostos situa-se dentro do triângulo Representações
Principais Tipos de Ligações Químicas Ligação iônica Ligação covalente Ligação metálica Iônicas Covalentes Metálicas Ligações químicas A maioria dos compostos situa-se dentro do triângulo Representações
Estrutura de Sólidos Cristalinos. Profa. Dra Daniela Becker
 Estrutura de Sólidos Cristalinos Profa. Dra Daniela Becker Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
Estrutura de Sólidos Cristalinos Profa. Dra Daniela Becker Bibliografia Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 3, 2002. Shackelford, J.F. Ciências dos Materiais,
Ciências dos materiais- 232
 Aula 1 1 1 Ciências dos materiais- 232 2 a aula - Imperfeições em Sólidos - Propriedades Mecânicas dos Metais - Falhas em Materiais Terça Semana par 19:00 às 20:40 21:00 às 22:40 Professor: Luis Gustavo
Aula 1 1 1 Ciências dos materiais- 232 2 a aula - Imperfeições em Sólidos - Propriedades Mecânicas dos Metais - Falhas em Materiais Terça Semana par 19:00 às 20:40 21:00 às 22:40 Professor: Luis Gustavo
DIFUSÃO. Conceitos Gerais
 DIFUSÃO Conceitos Gerais CAPA Os tratamentos térmicos são um conjunto de operações que têm por objetivo modificar as propriedades dos aços e de outros materiais através de um conjunto de operações que
DIFUSÃO Conceitos Gerais CAPA Os tratamentos térmicos são um conjunto de operações que têm por objetivo modificar as propriedades dos aços e de outros materiais através de um conjunto de operações que
Professora: Daniela Becker Mestranda: Jéssica de Aguiar
 Professora: Daniela Becker Mestranda: Jéssica de Aguiar JOINVILLE SC BRASIL 2016 Estruturas Cerâmicas São compostas por pelo menos dois elementos; Em geral são mais complexas do que a dos metais; Ex.:
Professora: Daniela Becker Mestranda: Jéssica de Aguiar JOINVILLE SC BRASIL 2016 Estruturas Cerâmicas São compostas por pelo menos dois elementos; Em geral são mais complexas do que a dos metais; Ex.:
Ciências dos materiais- 232
 1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
1 Ciências dos materiais- 232 2 a aula - Ligações químicas - Estruturas Cristalinas Quinta Quinzenal Semana par 10/03/2015 1 Professor: Luis Gustavo Sigward Ericsson Curso: Engenharia Mecânica Série: 5º/
A5 Estrutura nãocristalina. -imperfeição. Materiais são preparados com algum grau de impurezas químicas
 A5 Estrutura nãocristalina -imperfeição Materiais são preparados com algum grau de impurezas químicas Além das impurezas, existem numerosos tipos de defeitos estruturais que representam uma perda da perfeição
A5 Estrutura nãocristalina -imperfeição Materiais são preparados com algum grau de impurezas químicas Além das impurezas, existem numerosos tipos de defeitos estruturais que representam uma perda da perfeição
30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
 IFRS - Mestrado em Tecnologia e Engenharia de Materiais DISCIPLINA: Ciência dos Materiais PROFESSOR: Juliano Toniollo ALUNO: PAULO CESAR FRITZEN 30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
IFRS - Mestrado em Tecnologia e Engenharia de Materiais DISCIPLINA: Ciência dos Materiais PROFESSOR: Juliano Toniollo ALUNO: PAULO CESAR FRITZEN 30 Exercícios Resolvidos CAPÍTULO 3 ESTRUTURA CRISTALINA
31/3/2006 CM I 1. Imperfeições em Arranjos Atômicos
 31/3/2006 CM I 1 Imperfeições em Arranjos Atômicos 31/3/2006 CM I 2 Por quê o rubi é vermelho? A adição de 1% de óxido de cromo em alumina cria defeitos; Uma transição entre os níveis destes defeitos tornam
31/3/2006 CM I 1 Imperfeições em Arranjos Atômicos 31/3/2006 CM I 2 Por quê o rubi é vermelho? A adição de 1% de óxido de cromo em alumina cria defeitos; Uma transição entre os níveis destes defeitos tornam
Defeitos em Cristais Iônicos. Prof Ubirajara Pereira Rodrigues Filho
 Defeitos em Cristais Iônicos Prof Ubirajara Pereira Rodrigues Filho Defeitos Os defeitos perturbam a ordem a longa distância da rede cristalina e afetam as propriedades dos compostos cristalinos que dependem
Defeitos em Cristais Iônicos Prof Ubirajara Pereira Rodrigues Filho Defeitos Os defeitos perturbam a ordem a longa distância da rede cristalina e afetam as propriedades dos compostos cristalinos que dependem
TM229 - Introdução aos Materiais
 TM229 - Introdução aos Materiais 2009.1 Ana Sofia C. M. D Oliveira Interação entre imperfeições cristalinas Importância dos defeitos cristalinos para o comportamento dos materiais: Interação entre defeitos
TM229 - Introdução aos Materiais 2009.1 Ana Sofia C. M. D Oliveira Interação entre imperfeições cristalinas Importância dos defeitos cristalinos para o comportamento dos materiais: Interação entre defeitos
COMPORTAMENTO MECÂNICO DOS MATERIAIS: DEFEITOS CRISTALINOS E DEFORMAÇÃO PLÁSTICA
 UNIVERSIDADE FEDERAL DO ABC Centro de Engenharia, Modelagem e Ciências Sociais Aplicadas (CECS) BC-1105: MATERIAIS E SUAS PROPRIEDADES COMPORTAMENTO MECÂNICO DOS MATERIAIS: DEFEITOS CRISTALINOS E DEFORMAÇÃO
UNIVERSIDADE FEDERAL DO ABC Centro de Engenharia, Modelagem e Ciências Sociais Aplicadas (CECS) BC-1105: MATERIAIS E SUAS PROPRIEDADES COMPORTAMENTO MECÂNICO DOS MATERIAIS: DEFEITOS CRISTALINOS E DEFORMAÇÃO
Sólidos. Prof. Fernando R. Xavier
 Sólidos Prof. Fernando R. Xavier UDESC 2015 Sólidos Sob um aspecto simples e prático, é dito sólido o estado da matéria onde seu volume e forma são bem definidos. Dentro de um sólido, os átomos ou moléculas
Sólidos Prof. Fernando R. Xavier UDESC 2015 Sólidos Sob um aspecto simples e prático, é dito sólido o estado da matéria onde seu volume e forma são bem definidos. Dentro de um sólido, os átomos ou moléculas
Introdução a Engenharia e Ciência dos Materiais
 Introdução a Engenharia e Ciência dos Materiais Estrutura Cristalina Prof. Vera L Arantes 2014 25/3/2014 ESTRUTURA CRISTALINA 2 ARRANJO ATÔMICO Por que estudar? As propriedades de alguns materiais estão
Introdução a Engenharia e Ciência dos Materiais Estrutura Cristalina Prof. Vera L Arantes 2014 25/3/2014 ESTRUTURA CRISTALINA 2 ARRANJO ATÔMICO Por que estudar? As propriedades de alguns materiais estão
CTM P OBS: Esta prova contém 7 páginas e 6 questões. Verifique antes de começar. VOCÊ DEVE ESCOLHER APENAS 5 QUESTÕES PARA RESOLVER.
 Nome: Assinatura: CTM P1 2014.2 Matrícula: Turma: OBS: Esta prova contém 7 páginas e 6 questões. Verifique antes de começar. VOCÊ DEVE ESCOLHER APENAS 5 QUESTÕES PARA RESOLVER. VOCÊ DEVE RISCAR NA TABELA
Nome: Assinatura: CTM P1 2014.2 Matrícula: Turma: OBS: Esta prova contém 7 páginas e 6 questões. Verifique antes de começar. VOCÊ DEVE ESCOLHER APENAS 5 QUESTÕES PARA RESOLVER. VOCÊ DEVE RISCAR NA TABELA
Deformação e Mecanismos de Endurecimento Metais DEMEC TM242-B Prof Adriano Scheid
 Deformação e Mecanismos de Endurecimento Metais DEMEC TM242-B Prof Adriano Scheid Tensão Propriedades Mecânicas: Tensão e Deformação Deformação Elástica Comportamento tensão-deformação O grau com o qual
Deformação e Mecanismos de Endurecimento Metais DEMEC TM242-B Prof Adriano Scheid Tensão Propriedades Mecânicas: Tensão e Deformação Deformação Elástica Comportamento tensão-deformação O grau com o qual
ARRANJOS ATÔMICOS. Química Aplicada. Profº Vitor de Almeida Silva
 ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
ARRANJOS ATÔMICOS Química Aplicada Profº Vitor de Almeida Silva 1. Arranjo Periódico de Átomos SÓLIDO: Constituído por átomos (ou grupo de átomos) que se distribuem de acordo com um ordenamento bem definido;
Difusão em Sólidos TM229 - DEMEC Prof Adriano Scheid
 Difusão em Sólidos TM229 - DEMEC Prof Adriano Scheid O que é Difusão? É o fenômeno de transporte de material pelo movimento de átomos. Importância? Diversas reações e processos que ocorrem nos materiais
Difusão em Sólidos TM229 - DEMEC Prof Adriano Scheid O que é Difusão? É o fenômeno de transporte de material pelo movimento de átomos. Importância? Diversas reações e processos que ocorrem nos materiais
Materiais e Reciclagem. 4 Estruturas Cristalinas com Defeitos
 Instituto de Ciência e Tecnologia de Sorocaba Materiais e Reciclagem 4 Estruturas Cristalinas com Defeitos Professor Sandro Donnini Mancini Sorocaba, Março de 2017. Mesmo em materiais considerados 100%
Instituto de Ciência e Tecnologia de Sorocaba Materiais e Reciclagem 4 Estruturas Cristalinas com Defeitos Professor Sandro Donnini Mancini Sorocaba, Março de 2017. Mesmo em materiais considerados 100%
Aula 02 (Revisão): Ligação Química e Estruturas Cristalinas
 Aula 02 (Revisão): Ligação Química e Estruturas Cristalinas Prof. Dr. André Luiz Molisani Curso de Engenharia de Materiais e-mail: andre.molisani@fsa.br 2017 1 MATERIAL RECOMENDADO PARA ESTUDO: Capítulo
Aula 02 (Revisão): Ligação Química e Estruturas Cristalinas Prof. Dr. André Luiz Molisani Curso de Engenharia de Materiais e-mail: andre.molisani@fsa.br 2017 1 MATERIAL RECOMENDADO PARA ESTUDO: Capítulo
Estruturas dos Materiais
 Sumário Conceitos 1 Constituição de um átomo.......................... 1 Propriedade dos átomos........................... 1 Ligações químicas 2 Ligações Primárias............................... 2 Ligação
Sumário Conceitos 1 Constituição de um átomo.......................... 1 Propriedade dos átomos........................... 1 Ligações químicas 2 Ligações Primárias............................... 2 Ligação
DEFEITOS CRISTALINOS E DEFORMAÇÃO PLÁSTICA
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais DEFEITOS CRISTALINOS E DEFORMAÇÃO PLÁSTICA PMT 2100 - Introdução à Ciência dos Materiais para Engenharia
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais DEFEITOS CRISTALINOS E DEFORMAÇÃO PLÁSTICA PMT 2100 - Introdução à Ciência dos Materiais para Engenharia
O mais simples dos defeitos pontuais é a lacuna. Posição atômica na qual falta um átomo; Todo sólido cristalino contém lacunas; Aumento da entropia.
 O mais simples dos defeitos pontuais é a lacuna Posição atômica na qual falta um átomo; Todo sólido cristalino contém lacunas; Aumento da entropia. O número de lacunas em equilíbrio depende da temperatura
O mais simples dos defeitos pontuais é a lacuna Posição atômica na qual falta um átomo; Todo sólido cristalino contém lacunas; Aumento da entropia. O número de lacunas em equilíbrio depende da temperatura
Equilíbrio de fases e fortalecimento por solução sólida e por dispersão na solidificação
 UNIVESIDADE DE SÃO PAULO EESC SCM5757 Ciência dos materiais I Equilíbrio de fases e fortalecimento por solução sólida e por dispersão na solidificação Prof. Dra. Lauralice Canale 1º. Semestre - 2017 1
UNIVESIDADE DE SÃO PAULO EESC SCM5757 Ciência dos materiais I Equilíbrio de fases e fortalecimento por solução sólida e por dispersão na solidificação Prof. Dra. Lauralice Canale 1º. Semestre - 2017 1
28/09/2017. Ewaldo Luiz de Mattos Mehl. Departamento de Engenharia Elétrica
 Ewaldo Luiz de Mattos Mehl Departamento de Engenharia Elétrica mehl@ufpr.br 1 Agenda: Arranjos atômicos Estrutura cristalina Tipos de estruturas Influência nas propriedades Defeitos na estrutura cristalina
Ewaldo Luiz de Mattos Mehl Departamento de Engenharia Elétrica mehl@ufpr.br 1 Agenda: Arranjos atômicos Estrutura cristalina Tipos de estruturas Influência nas propriedades Defeitos na estrutura cristalina
Produto amolecido. Produto moldado. moléculas
 ω PROVA FINAL - PMT-5783 FUNDAMENTOS DE CIÊNCIA E ENGENHARIA DE MATERIAIS 1) A respeito dos materiais poliméricos elastoméricos (elastômeros) é errado afirmar que: a) Quando submetidos a tensão, os elastômeros
ω PROVA FINAL - PMT-5783 FUNDAMENTOS DE CIÊNCIA E ENGENHARIA DE MATERIAIS 1) A respeito dos materiais poliméricos elastoméricos (elastômeros) é errado afirmar que: a) Quando submetidos a tensão, os elastômeros
PROVA FINAL - PMT-5783 FUNDAMENTOS DE CIÊNCIA E ENGENHARIA DE MATERIAIS
 PROVA FINAL - PMT-5783 FUNDAMENTOS DE CIÊNCIA E ENGENHARIA DE MATERIAIS 1) Em relação aos defeitos cristalinos qual das seguintes afirmações é incorreta: a) Numa discordância em cunha o vetor de Burgers
PROVA FINAL - PMT-5783 FUNDAMENTOS DE CIÊNCIA E ENGENHARIA DE MATERIAIS 1) Em relação aos defeitos cristalinos qual das seguintes afirmações é incorreta: a) Numa discordância em cunha o vetor de Burgers
MECANISMOS DE ENDURECIMENTO DE METAIS
 1 MECANISMOS DE ENDURECIMENTO DE METAIS Eng. os metalurgistas e Eng. os de materiais visam o "projeto" de ligas com elevadas resistência mecânica (S E 0,2% ), ductilidade (A% e RA%) e tenacidade (resistência
1 MECANISMOS DE ENDURECIMENTO DE METAIS Eng. os metalurgistas e Eng. os de materiais visam o "projeto" de ligas com elevadas resistência mecânica (S E 0,2% ), ductilidade (A% e RA%) e tenacidade (resistência
LISTA DE EXERCÍCIOS 6 1 (UNIDADE III INTRODUÇÃO À CIÊNCIA DOS MATERIAIS)
 UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO CENTRO DE ENGENHARIAS DEPARTAMENTO DE ENGENHARIA E TECNOLOGIA DISCIPLINA: QUÍMICA APLICADA À ENGENHARIA PROFESSOR: FREDERICO RIBEIRO DO CARMO Estrutura cristalina
UNIVERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO CENTRO DE ENGENHARIAS DEPARTAMENTO DE ENGENHARIA E TECNOLOGIA DISCIPLINA: QUÍMICA APLICADA À ENGENHARIA PROFESSOR: FREDERICO RIBEIRO DO CARMO Estrutura cristalina
Microestrutura (Fases) Parte 2
 Microestrutura (Fases) Parte 2 1. MICROESTRUTURA 1-4 SOLUBILIDADE 1-5 FORMAÇÃO DE FASE EM SÓLIDOS 1 1-44 SOLUBILIDADE Um material pode ser resultado da combinação de diferentes componentes: - por formação
Microestrutura (Fases) Parte 2 1. MICROESTRUTURA 1-4 SOLUBILIDADE 1-5 FORMAÇÃO DE FASE EM SÓLIDOS 1 1-44 SOLUBILIDADE Um material pode ser resultado da combinação de diferentes componentes: - por formação
Ligação metálica corrente elétrica
 Ligações Metálicas Ligação metálica É o tipo de ligação que ocorre entre os átomos de metais. Quando muitos destes átomos estão juntos num cristal metálico, estes perdem seus elétrons da última camada.
Ligações Metálicas Ligação metálica É o tipo de ligação que ocorre entre os átomos de metais. Quando muitos destes átomos estão juntos num cristal metálico, estes perdem seus elétrons da última camada.
Líquido Sólido Amorfo Sólido Cristalino
 INTRODUÇÃO AOS MATERIAIS METÁLICOS Os processos de fabricação que se encarregam de dar forma à matéria-prima, entre outras coisas, modificam a estrutura interna da mesma apresentada em cada etapa do processamento,
INTRODUÇÃO AOS MATERIAIS METÁLICOS Os processos de fabricação que se encarregam de dar forma à matéria-prima, entre outras coisas, modificam a estrutura interna da mesma apresentada em cada etapa do processamento,
UNIDADE 6 Defeitos do Sólido Cristalino
 UNIDADE 6 Defeitos do Sólido Cristalino 1. Em condições de equilíbrio, qual é o número de lacunas em 1 m de cobre a 1000 o C? Dados: N: número de átomos por unidade de volume N L : número de lacunas por
UNIDADE 6 Defeitos do Sólido Cristalino 1. Em condições de equilíbrio, qual é o número de lacunas em 1 m de cobre a 1000 o C? Dados: N: número de átomos por unidade de volume N L : número de lacunas por
Universidade Estadual de Ponta Grossa PRÓ-REITORIA DE GRADUAÇÃO DIVISÃO DE ENSINO
 Universidade Estadual de Ponta Grossa PRÓ-REITORIA DE GRADUAÇÃO DIVISÃO DE ENSINO PROGRAMA DE DISCIPLINA SETOR: Ciências Agrárias e de Tecnologia DEPARTAMENTO: Engenharia de Materiais DISCIPLINA: Ciência
Universidade Estadual de Ponta Grossa PRÓ-REITORIA DE GRADUAÇÃO DIVISÃO DE ENSINO PROGRAMA DE DISCIPLINA SETOR: Ciências Agrárias e de Tecnologia DEPARTAMENTO: Engenharia de Materiais DISCIPLINA: Ciência
ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03 CMA CIÊNCIA DOS MATERIAIS 2º Semestre de 2014 Prof.
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03 CMA CIÊNCIA DOS MATERIAIS 2º Semestre de 2014 Prof.
Física dos Materiais FMT0502 ( )
 Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
Estrutura de cristais iônicos. Regras de Pauling
 Estrutura de cristais iônicos Regras de Pauling Estabilidade energética Por que os íons preferem ficar juntos, formando um cristal, do que moléculas isoladas? formar A Constante de Madelung é uma definição
Estrutura de cristais iônicos Regras de Pauling Estabilidade energética Por que os íons preferem ficar juntos, formando um cristal, do que moléculas isoladas? formar A Constante de Madelung é uma definição
TP064 - CIÊNCIA DOS MATERIAIS PARA EP. FABIANO OSCAR DROZDA
 TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 03 ESTRUTURA DOS SÓLIDOS CRISTALINOS 2 BREVE REVISÃO AULA PASSADA LIGAÇÕES QUÍMICAS Ligações primárias ou fortes
TP064 - CIÊNCIA DOS MATERIAIS PARA EP FABIANO OSCAR DROZDA fabiano.drozda@ufpr.br 1 AULA 03 ESTRUTURA DOS SÓLIDOS CRISTALINOS 2 BREVE REVISÃO AULA PASSADA LIGAÇÕES QUÍMICAS Ligações primárias ou fortes
Aula 17 - Transformações no estado sólido. Transformações Estruturais a nível de tamanho e formato dos grãos
 Aula 17 - Transformações no estado sólido Transformações Estruturais a nível de tamanho e formato dos grãos Encruamento Recristalização Crescimento de Grão Encruamento Aumento de dureza ou da resistência
Aula 17 - Transformações no estado sólido Transformações Estruturais a nível de tamanho e formato dos grãos Encruamento Recristalização Crescimento de Grão Encruamento Aumento de dureza ou da resistência
ESTRUTURA DOS SÓLIDOS CRISTALINOS CAP. 03 Parte II
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIA E ENGENHARIA DE MATERIAIS - PGCEM ESTRUTURA DOS SÓLIDOS
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE ENGENHARIA MECÂNICA PROGRAMA DE PÓS-GRADUAÇÃO EM CIÊNCIA E ENGENHARIA DE MATERIAIS - PGCEM ESTRUTURA DOS SÓLIDOS
Física dos Materiais
 Física dos Materiais 4300502 1º Semestre de 2016 Instituto de Física Universidade de São Paulo Professor: Luiz C. C. M. Nagamine E-mail: nagamine@if.usp.br Fone: 3091.6877 homepage: http://disciplinas.stoa.usp.br/course/view.php?id=10070
Física dos Materiais 4300502 1º Semestre de 2016 Instituto de Física Universidade de São Paulo Professor: Luiz C. C. M. Nagamine E-mail: nagamine@if.usp.br Fone: 3091.6877 homepage: http://disciplinas.stoa.usp.br/course/view.php?id=10070
Física dos Materiais FMT0502 ( )
 Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
Física dos Materiais FMT0502 (4300502) 1º Semestre de 2010 Instituto de Física Universidade de São Paulo Professor: Antonio Dominguesdos Santos E-mail: adsantos@if.usp.br Fone: 3091.6886 http://plato.if.usp.br/~fmt0502n/
ESTRUTURA DOS SÓLIDOS
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais ESTRUTURA DOS SÓLIDOS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia 2º semestre de
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais ESTRUTURA DOS SÓLIDOS PMT 2100 - Introdução à Ciência dos Materiais para Engenharia 2º semestre de
Principais Tipos de Ligações Químicas. Iônicas Covalentes Metálicas
 Principais Tipos de Ligações Químicas Iônicas Covalentes Metálicas Principais Tipos de Ligações Químicas Ligações químicas A maioria dos compostos situa-se dentro do triângulo Representações de Lewis Numa
Principais Tipos de Ligações Químicas Iônicas Covalentes Metálicas Principais Tipos de Ligações Químicas Ligações químicas A maioria dos compostos situa-se dentro do triângulo Representações de Lewis Numa
Difusão em sólidos. Defeitos Pontuais em Cristais. Prof. Rodrigo Perito Cardoso
 Universidade Federal do Paraná Setor de Tecnologia Departamento de Engenharia Mecânica Difusão em sólidos Defeitos Pontuais em Cristais Prof. Rodrigo Perito Cardoso Introdução Frenkel em 1926 -> introduziu
Universidade Federal do Paraná Setor de Tecnologia Departamento de Engenharia Mecânica Difusão em sólidos Defeitos Pontuais em Cristais Prof. Rodrigo Perito Cardoso Introdução Frenkel em 1926 -> introduziu
A6 Estrutura não cristalina imperfeição: defeitos lineares, planares e em volume
 A6 Estrutura não cristalina imperfeição: defeitos lineares, planares e em volume Deslocações no KCl. O KCl é transparente e as deslocações (linhas brancas) foram decoradas com impurezas para as tornar
A6 Estrutura não cristalina imperfeição: defeitos lineares, planares e em volume Deslocações no KCl. O KCl é transparente e as deslocações (linhas brancas) foram decoradas com impurezas para as tornar
Centro Universitário da Fundação Educacional de Barretos. Princípio de Ciências dos Materiais Prof.: Luciano H. de Almeida
 Centro Universitário da Fundação Educacional de Barretos Princípio de Ciências dos Materiais Prof.: Luciano H. de Almeida Porque estudar estrutura atômica? Ligação atômica e as propriedades dos materiais
Centro Universitário da Fundação Educacional de Barretos Princípio de Ciências dos Materiais Prof.: Luciano H. de Almeida Porque estudar estrutura atômica? Ligação atômica e as propriedades dos materiais
Estrutura Cristalina dos Sólidos (Arranjos Atômicos)
 Estrutura Cristalina dos Sólidos (Arranjos Atômicos) INTRODUÇÃO As propriedades dos materiais dependem dos arranjos dos seus átomos. Esses arranjos podem ser classificados em: Estruturas moleculares: agrupamento
Estrutura Cristalina dos Sólidos (Arranjos Atômicos) INTRODUÇÃO As propriedades dos materiais dependem dos arranjos dos seus átomos. Esses arranjos podem ser classificados em: Estruturas moleculares: agrupamento
TRATAMENTO TÉRMICO PARTE 2
 TRATAMENTO TÉRMICO PARTE 2 Antes de falarmos sobre tratamento térmico, devemos conhecer estruturas cristalinas Estrutura Cristalina O que é uma Estrutura Cristalina? É a maneira segundo a qual os átomos,
TRATAMENTO TÉRMICO PARTE 2 Antes de falarmos sobre tratamento térmico, devemos conhecer estruturas cristalinas Estrutura Cristalina O que é uma Estrutura Cristalina? É a maneira segundo a qual os átomos,
Materiais de Engenharia Michel Ashby e David Jones Copyright Elsevier, 2018
 Lista de Exercícios Por Prof. Pedro Nascente (Revisor Técnico) 1. Considere um fio de uma liga de níquel com 5 m de comprimento e diâmetro de 0,75 mm. Os valores do módulo de Young e do coeficiente de
Lista de Exercícios Por Prof. Pedro Nascente (Revisor Técnico) 1. Considere um fio de uma liga de níquel com 5 m de comprimento e diâmetro de 0,75 mm. Os valores do módulo de Young e do coeficiente de
ES 542 Tratamentos Térmicos. Professor: Felipe Bertelli Site :
 ES 542 Tratamentos Térmicos Professor: Felipe Bertelli E-mail: febertelli@fem.unicamp.br Site : www.gps.dema.fem.unicamp.br Pré-requisito para a disciplina: ter cursado a disciplina ES 242 Materiais de
ES 542 Tratamentos Térmicos Professor: Felipe Bertelli E-mail: febertelli@fem.unicamp.br Site : www.gps.dema.fem.unicamp.br Pré-requisito para a disciplina: ter cursado a disciplina ES 242 Materiais de
Introdução aos Materiais A Estrutura em Sólidos Cristalinos Metais DEMEC TM229 Prof. Adriano Scheid
 Introdução aos Materiais A Estrutura em Sólidos Cristalinos Metais DEMEC TM229 Prof. Adriano Scheid Introdução: Diversas propriedades dos sólidos estão relacionadas à Estrutura Cristalina. Não somente
Introdução aos Materiais A Estrutura em Sólidos Cristalinos Metais DEMEC TM229 Prof. Adriano Scheid Introdução: Diversas propriedades dos sólidos estão relacionadas à Estrutura Cristalina. Não somente
UNIDADE 6 - VIBRAÇÕES ATÔMICAS E DIFUSÃO NO ESTADO SÓLIDO
 UNIDADE 6 - VIBRAÇÕES ATÔMICAS E DIFUSÃO NO ESTADO SÓLIDO 6.1. TAXA DE UM PROCESSO Um grande número de processos que tem a temperatura como força motriz são regidos pela Equação de Arrhenius Q / RT (6.1)
UNIDADE 6 - VIBRAÇÕES ATÔMICAS E DIFUSÃO NO ESTADO SÓLIDO 6.1. TAXA DE UM PROCESSO Um grande número de processos que tem a temperatura como força motriz são regidos pela Equação de Arrhenius Q / RT (6.1)
P1 de CTM Nome: Matrícula: Assinatura: Turma:
 P1 de CTM 2012.1 Nome: Assinatura: Matrícula: Turma: 1) (1,5) Uma liga de cobre tem limite de escoamento igual a 300 MPa e módulo de elasticidade de 100 GPa. a. (0,5) Qual é a máxima carga (em N) que pode
P1 de CTM 2012.1 Nome: Assinatura: Matrícula: Turma: 1) (1,5) Uma liga de cobre tem limite de escoamento igual a 300 MPa e módulo de elasticidade de 100 GPa. a. (0,5) Qual é a máxima carga (em N) que pode
Difusão Prof. C. Brunetti
 Difusão Prof. C. Brunetti Conceitos fundamentais Definição: Mecanismo pelo qual a matéria é transportada através da matéria. Os átomos, em gases, líquidos e sólidos, estão em movimento constante e migram
Difusão Prof. C. Brunetti Conceitos fundamentais Definição: Mecanismo pelo qual a matéria é transportada através da matéria. Os átomos, em gases, líquidos e sólidos, estão em movimento constante e migram
Ligação iônica = transfere elétrons (um doa outro recebe) 1, 2, 3 e - c.v. 5, 6, 7 e - c.v. Doar e - Receber e - Íon+ Íon - Cl - : NaCl.
 LIGAÇÕES QUÍMICAS Os gases nobres aparecem isolados na natureza, ou seja, são estáveis na forma atômica. Isso ocorre em razão de possuírem 8 elétrons na última camada (exceção do hélio, que possui 2 elétrons
LIGAÇÕES QUÍMICAS Os gases nobres aparecem isolados na natureza, ou seja, são estáveis na forma atômica. Isso ocorre em razão de possuírem 8 elétrons na última camada (exceção do hélio, que possui 2 elétrons
AULA 07 DEFORMAÇÃO PLÁSTICA DOS METAIS
 AULA 07 DEFORMAÇÃO PLÁSTICA DOS METAIS Conceitos fundamentais σ Os materiais experimentam dois tipos de deformação: elástica e plástica. Elástica: retornável. Plástica: permanente. ε Em uma escala microscópica:
AULA 07 DEFORMAÇÃO PLÁSTICA DOS METAIS Conceitos fundamentais σ Os materiais experimentam dois tipos de deformação: elástica e plástica. Elástica: retornável. Plástica: permanente. ε Em uma escala microscópica:
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais. Unidade 4 ESTRUTURA DOS SÓLIDOS CRISTALINOS
 ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Unidade 4 ESTRUTURA DOS SÓLIDOS CRISTALINOS PMT 3100 - Fundamentos de Ciência e Engenharia dos Materiais
ESCOLA POLITÉCNICA DA UNIVERSIDADE DE SÃO PAULO Departamento de Engenharia Metalúrgica e de Materiais Unidade 4 ESTRUTURA DOS SÓLIDOS CRISTALINOS PMT 3100 - Fundamentos de Ciência e Engenharia dos Materiais
Disciplina: Ciência dos Materiais. Prof. Alex Bernardi
 Disciplina: Ciência dos Materiais Prof. Alex Bernardi 1 Aula Atividade Tele Aula 1 Questão 1. A Ciência dos Materiais é definida como o estudo das relações entre as estruturas e propriedades dos materiais
Disciplina: Ciência dos Materiais Prof. Alex Bernardi 1 Aula Atividade Tele Aula 1 Questão 1. A Ciência dos Materiais é definida como o estudo das relações entre as estruturas e propriedades dos materiais
P1 de CTM VOCÊ DEVE ESCOLHER APENAS 5 QUESTÕES PARA RESOLVER. VOCÊ DEVE RISCAR NA TABELA ABAIXO A QUESTÃO QUE NÃO SERÁ CORRIGIDA
 P1 de CTM 2014.1 Nome: Assinatura: Matrícula: Turma: OBS: Esta prova contém 7 páginas e 6 questões. Verifique antes de começar. VOCÊ DEVE ESCOLHER APENAS 5 QUESTÕES PARA RESOLVER. VOCÊ DEVE RISCAR NA TABELA
P1 de CTM 2014.1 Nome: Assinatura: Matrícula: Turma: OBS: Esta prova contém 7 páginas e 6 questões. Verifique antes de começar. VOCÊ DEVE ESCOLHER APENAS 5 QUESTÕES PARA RESOLVER. VOCÊ DEVE RISCAR NA TABELA
Desordem Atômica nos Sólidos Imperfeições Cristalinas
 Desordem Atômica nos Sólidos Imperfeições Cristalinas O que se entende por defeito ouimperfeição cristalina? Denomina se dedefeito defeito ouimperfeição as irregularidades quepodemocorrernos ocorrer arranjos
Desordem Atômica nos Sólidos Imperfeições Cristalinas O que se entende por defeito ouimperfeição cristalina? Denomina se dedefeito defeito ouimperfeição as irregularidades quepodemocorrernos ocorrer arranjos
6 - Microestrutura Fases
 24 6 - Microestrutura 6-1. Fases Um cubo de gelo flutuando na água e a atmosfera que os envolve são exemplos dos três estados da matéria, sem dúvida, mas também são exemplos de fases (Figura 6-1). Uma
24 6 - Microestrutura 6-1. Fases Um cubo de gelo flutuando na água e a atmosfera que os envolve são exemplos dos três estados da matéria, sem dúvida, mas também são exemplos de fases (Figura 6-1). Uma
P1 de CTM Energia Direcionalidade Troca ou Compartilhamento. Covalente Alta Sim Compartilhamento. Metálica Alta Não Compartilhamento
 P1 de CTM 2012.2 Nome: Assinatura: Matrícula: Turma: 1) (1,5) Liste e classifique as ligações químicas em termos de a. Energia de ligação b. Direcionalidade c. Troca ou compartilhamento de elétrons COLOQUE
P1 de CTM 2012.2 Nome: Assinatura: Matrícula: Turma: 1) (1,5) Liste e classifique as ligações químicas em termos de a. Energia de ligação b. Direcionalidade c. Troca ou compartilhamento de elétrons COLOQUE
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2014 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 2º semestre de 2014 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Crescimento de Cristais - Diagrama de Fases
 Crescimento de Cristais - Diagrama de Fases Recapitulando a aula 2: NUCLEAÇÃO E CRESCIMENTO DE FASES Nucleação Redução da Temperatura Líquido - Desorganização Cristalina Formação de clusters ou embriões
Crescimento de Cristais - Diagrama de Fases Recapitulando a aula 2: NUCLEAÇÃO E CRESCIMENTO DE FASES Nucleação Redução da Temperatura Líquido - Desorganização Cristalina Formação de clusters ou embriões
Física dos Materiais
 4300502 1º Semestre de 2014 Instituto de Física Universidade de São Paulo Professor: Luiz C C M Nagamine E-mail: nagamine@if.usp.br Fone: 3091.6877 homepage: http://disciplinas.stoa.usp.br/course/view.php?id=10070
4300502 1º Semestre de 2014 Instituto de Física Universidade de São Paulo Professor: Luiz C C M Nagamine E-mail: nagamine@if.usp.br Fone: 3091.6877 homepage: http://disciplinas.stoa.usp.br/course/view.php?id=10070
Sólidos. Prof. Fernando R. Xavier
 Sólidos Prof. Fernando R. Xavier UDESC 2013 Sólidos Sob um aspecto simples e prático, é dito sólido o estado da matéria onde seu volume e forma são bem definidos. Dentro de um sólido, os átomos ou moléculas
Sólidos Prof. Fernando R. Xavier UDESC 2013 Sólidos Sob um aspecto simples e prático, é dito sólido o estado da matéria onde seu volume e forma são bem definidos. Dentro de um sólido, os átomos ou moléculas
Estrutura atômica e ligação interatômica. Profa. Daniela Becker
 Estrutura atômica e ligação interatômica Profa. Daniela Becker Referências Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 2, 2002. Shackelford, J.F. Ciências dos
Estrutura atômica e ligação interatômica Profa. Daniela Becker Referências Callister Jr., W. D. Ciência e engenharia de materiais: Uma introdução. LTC, 5ed., cap 2, 2002. Shackelford, J.F. Ciências dos
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS
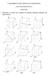 FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
FUNDAMENTOS DE CIÊNCIA DOS MATERIAIS LISTA DE EXERCÍCIOS CRISTAIS 1 Determine os índices e/ou desenhe as direções cristalinas indicadas nas figuras abaixo. 2 Determineos índices dos planos cristalinos
Os processos de fabricação mecânica podem ser agrupados em 5 grupos principais.
 Os processos de fabricação mecânica podem ser agrupados em 5 grupos principais. a) Fundição d) Metalurgia do pó b) Usinagem c) Soldagem E) CONFORMAÇÃO MECÂNICA Esquema geral dos processos de conformação
Os processos de fabricação mecânica podem ser agrupados em 5 grupos principais. a) Fundição d) Metalurgia do pó b) Usinagem c) Soldagem E) CONFORMAÇÃO MECÂNICA Esquema geral dos processos de conformação
SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I
 SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I Ligação química Estrutura cristalina de cerâmicas cristalinas 2 Ligação química Ligação química 3 % de caráter iônico = {1-exp[-(0,25)(X A -X B ) 2 ]}.100
SMM-0194 ENGENHARIA E CIÊNCIA DOS MATERIAIS II I Ligação química Estrutura cristalina de cerâmicas cristalinas 2 Ligação química Ligação química 3 % de caráter iônico = {1-exp[-(0,25)(X A -X B ) 2 ]}.100
Introdução a Ciência dos Materiais IMPERFEIÇÕES NO SÓLIDO. Professora: Maria Ismenia Sodero
 Introdução a Ciência dos Materiais IMPERFEIÇÕES NO SÓLIDO Professora: Maria Ismenia Sodero maria.ismenia@usp.br Tópicos abordados. Quais os tipos de defeitos podem ocorrer nos sólidos? 2. Como é possível
Introdução a Ciência dos Materiais IMPERFEIÇÕES NO SÓLIDO Professora: Maria Ismenia Sodero maria.ismenia@usp.br Tópicos abordados. Quais os tipos de defeitos podem ocorrer nos sólidos? 2. Como é possível
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de Informações e instruções para a resolução da prova
 Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2013 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
Programa de Pós-graduação em Ciência e Tecnologia de Materiais 1º semestre de 2013 Informações e instruções para a resolução da prova 1. A prova deve ser realizada sem consulta; 2. A duração da prova é
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DE PELOTAS PRÓ-REITORIA DE GRADUAÇÃO
 MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DE PELOTAS PRÓ-REITORIA DE GRADUAÇÃO PLANO DE ENSINO Ano Semestre letivo 2016 1 o 1. Identificação Código 1.1 Disciplina: Ciência dos Materiais 0950003 1.2 Unidade:
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DE PELOTAS PRÓ-REITORIA DE GRADUAÇÃO PLANO DE ENSINO Ano Semestre letivo 2016 1 o 1. Identificação Código 1.1 Disciplina: Ciência dos Materiais 0950003 1.2 Unidade:
