Aula 3 AMINOÁCIDOS. André Luís Bacelar Silva Barreiros Marizeth Libório Barreiros. META Introduzir o aluno ao estudo dos aminoácidos.
|
|
|
- Armando Moreira Vilalobos
- 7 Há anos
- Visualizações:
Transcrição
1 Aula 3 AMINOÁCIDOS META Introduzir o aluno ao estudo dos aminoácidos. OBJETIVOS Ao final desta aula, o aluno deverá: Saber definir, classificar e dar o nome a um aminoácido. Conhecer suas propriedades ácido-base. Conhecer os métodos de separação dos aminoácidos. Conhecer as reações dos aminoácidos e seus mecanismos. PRÉ-REQUISITOS Nomenclatura e função dos compostos Orgânicos. Estereoquímica e reações dos compostos orgânicos. André Luís Bacelar Silva Barreiros Marizeth Libório Barreiros
2 Química de Biomoléculas Olá, nesta aula vamos começar com o estudo dos aminoácidos. Os aminoácidos são ácidos carboxílicos que possuem uma função anima como podemos ver na figura 2. Uma ligação amida entre a função do ácido carboxílico de um aminoácido e o nitrogênio do grupo amino de outro aminoácido é chamada de ligação peptídica. Os aminoácidos se unem através de ligações peptídicas para formar os peptídeos e as proteínas. Figura 2 - Estrutura de alfa-aminoácidos. Fonte: CAREY, F. A. Química Orgânica, v.2, 7ª. Ed, 2011, pg Uma molécula formada pela união de dois aminoácidos através de uma ligação peptídica é chamada de dipeptídeo. Um tripeptídeo é formado por três aminoácidos unidos por ligações peptídicas, e um tetrapeptídeo tem quatro aminoácidos e assim por diante. Os peptídeos com mais de 30 a 50 aminoácidos são polipeptídeos. As proteínas são polipeptídeos que têm alguma função biológica. Os peptídeos e as proteínas são polímeros de aminoácidos unidos por uma ligação amida. CLASSIFICAÇÃO E NOMENCLATURA DOS AMINOÁCIDODOS Os aminoácidos são classificados de acordo com a localização do grupo amino na cadeia carbônica que contém a função ácido arboxílico em α, β, γ e assim por diante (Figura 3). A forma mais importante dos aminoácidos, são os α-aminoácidos, os quais são constituintes das proteínas e dos peptídeos. 58
3 Aminoácidos Aula 3 Figura 3 - Estrutura de α, β e γ aminoácidos. Fonte: CAREY, F. A. Química Orgânica, v.2, 7ª. Ed, 2011, pg Embora sejam conhecidos mais de 700 aminoácidos naturais diferentes, apenas o grupo de 20 aminoácidos chamados de aminoácidos padrões, listados na tabela, merece atenção especial. Tabela 1 Os 20 aminoácidos mais comuns de ocorrência natural. Todos os aminoácidos são mostrados na forma que predominam no ph (7,3) 59
4 Química de Biomoléculas Todos são α-aminoácidos e contêm uma função amina primária, com exceção da prolina, uma amina secundária onde o nitrogênio amínico está incorporado em um anel de 5 membros. Todos eles possuem um grupo carboxil e um grupo amino ligados ao mesmo átomo de carbono (o carbono α). Os aminoácidos podem ser divididos em essenciais e os não essenciais; os aminoácidos essenciais são aqueles que os seres humanos não são capazes de sintetizar ou sintetizam em quantidades insuficientes para suprir as necessidades, portanto, devem ser obtidos pela dieta. Os aminoácidos essenciais são: valina, leucina, isoleucina, treonina, metionina, lisina, triptofano, fenilalanina, histidina e arginina, sendo que estes dois últimos só são essenciais na infância. Os aminoácidos não essenciais são aqueles que podemos sintetizar. Encontramos aminoácidos nas proteínas de alguns alimentos, como carnes vermelhas, frango, peixes, ovos, queijos, proteínas da soja, feijão, lentilha, amêndoas, amendoim, castanha do Pará, aveia, granola, arroz. O nome sistemático dos aminoácidos é obtido de acordo com as regras da IUPAC para ácidos carboxílicos que vocês estudaram em Fundamentos de Química Orgânica, como os exemplos da figura 3. Todos os aminoácidos possuem nomes simples ou comuns, em alguns casos derivados da fonte da qual eles foram inicialmente isolados. Como por exemplo, a asparagina foi encontrada no aspargo, e o glutamato no glúten de trigo; a tirosina foi primeiramente isolada do queijo (derivado do grego tyros, queijo ); a glicina recebeu seu nome por seu gosto doce (do grego glycos, doce ); tirosina e triptofano (do inglês tyrosine, twiptophan). 60
5 Aminoácidos Aula 3 Os aminoácidos podem ser classificados de acordo com a polaridade da cadeia lateral em: apolares, polares neutros e polares carregados. Fazem parte dos apolares: alanina, valina, glicina, prolina, leucina, isoleucina, metionina, fenilalanina e triptofano. Os polares neutros são: serina, treonina, aspargina, glutanina, tirosina, histidina e cisteína. No grupo dos polares garregados estão: aspartato, glutamato, lisina e arginina. ESTEREOQUÍMICA DOS AMINOÁCIDOS Dos 20 aminoácidos, a glicina, é o único que é aquiral. Todos os outros 19 são quirais, consequentemente são possíveis dois enantiômeros de cada um, mais a natureza usa apenas um para sintetizar as proteínas. Todos os aminoácidos naturais são L, ao contrário dos carboidratos que são D. As designações D e L indicam a configuração do carbono α e são atribuídas da mesma forma que nos carboidratos que vocês acabaram de estudar. Assim, um aminoácido que tem em uma projeção de Fischer o grupo amino para esquerda é L, enquanto o que tem o grupo amino para direita é D conforme mostrado na figura 4. Figura 4 - Estrutura da (L)-alamina e (D)-alanina. Fonte: NELSON, D. L.; COX, M.M. Princípios de Bioquímica de Lehninger, 5ª. Ed, 2011, pg.74. PROPRIEDADES ÁCIDO-BASE DE AMINOÁCIDOS Como todo aminoácido tem um grupo carboxila e um grupo amino, eles podem ser classificados de acordo com a estrutura da cadeia lateral em neutros, ácidos ou básicos. A lisina, arginina e histidina são aminoácidos básicos. O glutamato e o aspartato aminoácidos ácidos e os demais são aminoácidos neutros. Os aminoácidos existem em ph fisiológico (7,3), como íons dipolares, chamados de zwitterions, uma forma na qual o grupo carboxila está presente como um íon carboxilato, - CO 2 -, e o grupo amino está presente como um íon amínio, - NH 3 +. Já em solução aquosa, existe um equilíbrio entre o íon dipolar e as formas aniônica e catiônica dependendo do ph da solução (Figura 5). 61
6 Química de Biomoléculas Figura 5 - Equilíbrio ácido-base dos aminoácidos. Fonte: Fonte: BRUICE, P. Y. Química Orgânica, v.2, 4ª. Ed., 2006, pg.379. A forma predominante do aminoácido presente em solução vai depender do ph da solução e da natureza do aminoácido. Nas soluções fortementes ácidas todos os aminoácidos estão presentes como cátions, enquanto em soluções fortemente básicas eles estão presentes como ânions. Em um ph intermediário, chamado de ponto isoelétrico (pi), a concentração do íon dipolar está no seu máximo e as concentrações dos ânions e cátions são iguais, portanto se anulam, ou seja, o ponto isoelétrico de um aminoácido é o valor de ph em que ele não tem carga líquida, a carga do aminoácido é zero. Podemos ver como exemplo (Figura 6) a alanina, um aminoácido simples com um grupo carboxíla e um grupo amina, o pi será a média aritmética de seus dois valores de pka. Isso ocorre porque em ph = 2,34 metade das moléculas está com o grupo carboxila carregado negativamente e metade tem o grupo carboxila não carregado; e em ph = 9,69, metade das moléculas tem um grupo amino carregado positivamente e metade tem um grupo amino não carregado. Quando o ph é maior que 2,34, o grupo carboxila com mais moléculas torna-se negativamente carregado. Quando o ph é menor que 9,69, o grupo amino com mais moléculas torna-se positivamente carregado. O ponto isoelétrico, é a média dos dois valores de pka, e nesse ponto, o número de grupos negativamente carregados se iguala ao número de grupos positivamente carregados e o aminoácido tem carga zero. Figura 6 -Cálculo do ponto isoelétrico da alanina. Fonte: Fonte: BRUICE, P. Y. Química Orgânica, v.2, 4ª. Ed., 2006, pg
7 Aminoácidos Aula 3 Para os aminoácidos com grupos ácidos ou básicos na cadeia lateral, o ponto isoelétrico é a média dos valores de pka dos grupos semelhantes. Por exemplo, o pi da lisina é a média dos valores de pka dos dois grupos que estão carregados positivamente em sua forma ácida e não estão carregados em sua forma básica. O pi do glutamato, por outro lado, é a média dos valores de pka dos dois grupos que estão carregados negativamente em sua forma básica (Figura 7). Figura 7 - Cálculo do ponto isoelétrico da lisina e do glutamato. Fonte: Fonte: BRUICE, P. Y. Química Orgânica, v.2, 4ª. Ed., 2006, pg.381. Observe que um aminoácido nunca pode existir como uma substância não-carregada, a despeito do ph da solução. Para estar sem carga, um aminoácido teria de perder um próton de um grupo +NH3 com um pka de aproximadamente 9, antes de perder um próton de um grupo COOH com um pka de aproximadamente 2. O que é impossível: um ácido fraco não pode ser mais ácido que um ácido forte. A tabela 2 mostra os valores de pka dos aminoácidos. Tabela 2 Valores de pka de aminoácidos. 63
8 Química de Biomoléculas SÍNTESE DOS AMINOÁCIDOS Um α-aminoácido pode ser preparado no laboratório usando como substrato um ácido α-halocarboxílico e amônia aquosa como nucleófilo através de uma reação de substituição nucleofílica. O ácido halocarboxílico é preparado a partir da reação de Hell-Velhard-Zelinsky que vocês viram na Química dos Compostos Orgânicos II (Figura 8). Figura 8 - Síntese de α-aminoácido. Fonte: SOLOMONS, T. W. G; FRYHLE, C. B. Química Orgânica, v.2, 7ª. Ed., 2002, pg.114/ CAREY, F. A. Química Orgânica, v.2, 7ª. Ed, 2011, pg Outro método de preparar um α-aminoácido é através da síntese de Strecker, onde um aldeído é convertido a um α-aminoácido com um átomo de carbono a mais. A reação pode ser vista na figura 9. Figura 9 - Síntese de α-aminoácido pela reação de Strecker. Fonte: CAREY, F. A. Química Orgânica, v.2, 7ª. Ed, 2011, pg
9 Aminoácidos Aula 3 Um terceiro método para a preparação dos α-aminoácidos é a aminação redutiva de um α-cetoácido com amônia e um agente redutor. Podemos ver como exemplo (Figura 10) a síntese da alanina a partir do ácido pirúvico com amônia na presença do NaBH 4. Figura 10 - Síntese da alanina pela aminação redutiva. Fonte: Mc MURRY, Química Orgânica, v.2/combo, 7ª. Ed., 2011, pg REAÇÕES DOS AMINOÁCIDOS Os aminoácidos têm um grupo amino e um grupo ácido carboxílico, portanto sofrem reações características desses grupos. Um aminoácido pode reagir com um álcool formando um éster, como por exemplo, a alanina pode reagir com etanol para formar o hidrocloreto do éster etílico da alanina conforme mostrado na figura 11. O mecanismo é o mesmo da esterificação de ácidos carboxílicos que vocês viram na Química dos Compostos Orgânicos II. Figura 11 - Formação do éster da alanina. Fonte: CAREY, F. A. Química Orgânica, v.2, 7ª. Ed, 2011, pg
10 Química de Biomoléculas A outra reação dos aminoácidos é a acilação, um aminoácido reage com o anidrido acético para formar uma amida (Figura 12). Essa é uma reação típica do grupo amino. O mecanismo é o mesmo da reação do anidrido acético com amina e análogo ao da reação do anidrido acético com álcool que vocês estudaram na Química dos Compostos Orgânicos II. Figura 12 - Formação da N-Acetilglicina Fonte: CAREY, F. A. Química Orgânica, v.2, 7ª. Ed, 2011, pg.1147./ BRUICE, P. Y. Química Orgânica, v.2, 4ª. Ed., 2006, pg.100. SEPARAÇÃO DE AMINOÁCIDOS Agora vamos aprender como separar os aminoácidos. Uma mistura de aminoácidos pode ser separada através de várias técnicas diferentes como: a eletroforese, a cromatografia em papel, a cromatografia em camada delgada e a cromatografia de troca iônica. Eletroforese A eletroforese é uma técnica de separação de uma mistura de moléculas que envolve a migração de partículas carregadas eletricamente em um determinado gel ou papel quando se aplica uma diferença de potencial. Uma mistura de aminoácidos é separada na eletroforese com base em seus valores de ponto isoéletrico (pi). Para fazer a separação algumas gotas de uma solução da mistura de aminoácidos são aplicadas em um papel de filtro ou em um gel (Figura 13). Quando o papel ou o gel é colocado entre dois eletrodos em uma solução tamponada e é aplicado um campo elétrico, o aminoácido com pi maior do que o ph da solução terá uma carga global positiva e migrará na direção do catodo (o eletrodo eletronegativo). Quanto maior for a diferença do pi do aminoácido do ph da solução, mais positivo estará o aminoácido e mais rápido ele migrará na direção do catodo. 66
11 Aminoácidos Aula 3 Um aminoácido com pi menor do que o pi do ph da solução do tampão terá uma carga global negativa e migrará em direção ao anodo (o eletrodo positivo). Quando duas moléculas têm cargas iguais, a separação se dá por tamanho, pois a molécula maior se moverá mais lentamente. Para fazer a detecção dos aminoácidos após sua separação, o papel de filtro é borrifado com ninhidrina e seco em forno quente. A maioria dos aminoácidos forma um produto de cor púrpura. Figura 13 - Separação de uma mistura de aminoácidos por eletroforese. Fonte: Fonte: BRUICE, P. Y. Química Orgânica, v.2, 4ª. Ed., 2006, pg.382. Comatografia em papel A cromatografia em papel é uma técnica de separação bastante simples. A técnica de cromatografia em papel separa os aminoácidos com base em sua polaridade. Para fazer a separação algumas gotas da solução que contém a mistura de aminoácidos são aplicadas na parte inferior da tira de papel de filtro. O papel é colocado em uma cuba contendo o solvente (fase móvel), em geral uma mistura de água, ácido acético e butanol. O solvente sobe pelo papel por ação de capilaridade, arrastando os aminoácidos (Figura 14). Dependendo de suas polaridades, os aminoácidos têm diferentes afinidades pelas fases móvel (solvente) e estacionária (papel) e conseqüentemente se deslocarão pelo papel com diferentes velocidades. Quanto mais polar for o aminoácido, mais fortemente ele será adsorvido no papel, que é uma fase estacionária polar, e se deslocarão mais lentamente pelo papel. Ao contrário, os aminoácidos menos polares se deslocarão pelo papel mais rapidamente, pois têm uma afinidade maior pela fase móvel. 67
12 Química de Biomoléculas Figura 14 - Separação do glutamato, alanina e leucina por cromatografia em papel. Fonte: BRUICE, P. Y. Química Orgânica, v.2, 4ª. Ed., 2006, pg.383. Cromatografia em camada delgada A cromatografia em camada delgada (CCD) difere da cromatografia em papel porque a fase estacionária é um sólido em vez de papel. O modo de separação da cromatografia em camada delgada é o mesmo da cromatografia em papel, separa os aminoácidos por polaridade. Na CCD usa-se uma placa de vidro como suporte para o sólido (fase estacionária). Para fazer a separação dos aminoácidos segue o mesmo procedimento da cromatografia em papel. O mecanismo de separação também é por polaridade dos aminoácidos, ou seja, por afinidade com as fases móvel (solvente) e a fase estacionária (sólido), os aminoácidos que tiverem maior afinidade pela fase estacionária ficarão retidos por mais tempo, enquanto os que tiverem maior afinidade pela fase móvel serão arrastados primeiro. A separação vai depender do material sólido e do solvente escolhido para a fase móvel. Cromatografia de troca iônica A cromatografia de troca iônica é uma técnica em que a separação baseia-se na interação eletrostática (força iônica) entre o soluto e a fase es- 68
13 Aminoácidos Aula 3 tacionária. Essa técnica emprega uma coluna empacotada com uma resina carregada (fase estacionária). Essa resina pode ser carregada positivamente denominada de resina de troca aniônica ou carregada negativamente denominada de resina de troca catiônica. Uma resina muito empregada é a do copolímero de estireno e divinil-benzeno (Figura 15), com um grupo ácido sulfônico negativamente carregado em alguns dos anéis benzênicos. A fase móvel geralmente é um tampão. Podemos ver como exemplo, a mistura de lisina e glutamato: o glutamato tem uma cadeia lateral negativamente carregada e desceria pela coluna mais rádido. Por outro lado, a lisina tem uma cadeia lateral carregada positivamente e ficaria retida na coluna por mais tempo. Figura 15 - Resina de troca catiônica. Fonte: BRUICE, P. Y. Química Orgânica, v.2, 4ª. Ed., 2006, pg.384. CONCLUSÃO Nesta aula aprendemos que os aminoácidos são ácidos α-aminocarboxílicos e vimos também que eles se ligam através de uma ligação amida para formar os peptídeos e as proteínas. As proteínas são as macromoléculas biológicas mais abundantes, ocorrendo em todas as partes das células. Encontramos aminoácidos nas proteínas de alguns alimentos, como carnes vermelhas, frango, peixes, ovos, queijos, proteínas da soja, feijão, lentilha, amêndoas, amendoim, castanha do Pará, aveia, granola e arroz. Observamos que um aminoácido nunca pode existir como uma substância não-carregada. Além disso, aprendemos que os aminoácidos sofrem reações características de ácidos carboxílicos e do grupo amino. 69
14 Química de Biomoléculas RESUMO Nesta aula estudamos os aminoácidos, os quais são ácidos carboxílicos que possuem uma função anima. Os aminoácidos se unem atrevés da ligação peptídica para formar os peptídeos e as proteínas. Os aminoácidos são classificados de acordo com a localização do grupo amino na cadeia carbônica que contém a função ácido arboxílico em α, β, γ e assim por diante. Os aminoácidos podem ser divididos em essencias e os não essencias; os aminoácidos essencias são aqueles que os seres humanos não são capazes de sintetizar e os não essencias são os que sintetizamos. Todos os vinte aminoácidos construtores das proteínas são α-aminoácidos, e todos, exceto a glicina, possuem estereoquímica L. Os aminoácidos podem ser classificados de acordo com a estrutura da cadeia lateral em neutros, ácidos ou básicos. Em solução neutra; os aminoácidos existem como zwitterions dipolares. O ph de uma solução aquosa na qual a concentração do zwitterion atinge o máximo é chamada de ponto isoelétrico (pi). Os aminoácidos podem ser sintetizados em laboratório a partir das reações de um haloácido com amônia; reação de um aldeído com amônia e o íon cianeto (Síntese de Strecker). Os aminoácidos sofrem reações características dos grupos funcionais que eles contém, assim o grupo ácido reage com álcool para formar um éster (esterificação) e o grupo amina reage com anidrido acético para formar uma amida. Uma mistura de aminoácidos pode ser separada com base em seus pontos isoéletricos por eletroforese ou com base em suas polaridades por cromatografia em papel ou cromatografia em camada delgada ou ainda com base na força iônica através da cromatografia de troca iônica. ATIVIDADES 1. Desenhe uma estrutura de Fischer para o enantiômero da L-isoleucina: 70
15 Aminoácidos Aula 3 COMENTÁRIOS SOBRE AS ATIVIDADES Como a D-isoleucina é o enantiômero da L-isoleucina, apenas olhe para a estrutura da L-isoleucina e reverta a configuração em cada centro de quiralidade conforme figura 16. Figura 16 - Projeção de Fischer para a L-isoleucina e D-isoleucina. Fonte: CAREY, F. A. Química Orgânica, v.2, 7ª. Ed, 2011, pg ATIVIDADES Desenhe a forma na qual o ácido aspártico existe predominantemente em ph fisiológico (7,3): COMENTÁRIOS SOBRE AS ATIVIDADES Olhando para a estrutura do ácido aspártico na tabela 1 verifica-se que ambos os grupos carboxílas estão em suas formas básicas, uma vez o ph é maior que seus valores de pka conforme mostrado na tabela 2. Já o grupo amino protonado está na sua forma ácida, porque o ph é menor que seu pka, logo o ácido aspártico existe no ph (7,3) como mostrado na figura 17. Figura 17 - Fórmula do ácido aspártico no ph (7,3). Fonte: BRUICE, P. Y. Química Orgânica, v.2, 4ª. Ed., 2006, pg
16 Química de Biomoléculas 1. Calcule o pi da arginina: ATIVIDADES COMENTÁRIOS SOBRE AS ATIVIDADES Primeiro pegue os valores de pka na tabela 2. O pi da arginina é a média dos valores de pka dos dois grupos que estão carregados positivamente na sua forma ácida, ou seja dos dois grupos semelhantes, conforme figura abaixo. Para calcular o pi some esses dois valores e tire a média. pka = 12,48 + pka = 2,17 NH 2 O H 2 NCNHCH 2 CH 2 CH 2 + CHCOH NH 3 pka = 9,04 pi = 9, ,48 =10,76 2 ATIVIDADES 1. Qual forma do ácido glutâmico você esperaria ser predominante em: a) uma solução fortemente ácida, b) uma solução fortemente básica e c) no seu ponto isoelétrico (PI = 3,22). 72
17 Aminoácidos Aula 3 COMENTÁRIOS SOBRE AS ATIVIDADES a) Em uma solução muito ácida nenhum hidrogênio ainda foi doado, então o ácido encontra-se na sua forma mais ácida. b) Enquanto em uma solução básica todos os hidrogênios ácidos já foram doados. c) No ponto isoelétrico as cargas se anulam, então somente o hidrogênio mais ácido foi doado. O O O O a) HO OH b) - O - O + NH 3 NH 2 O O c) HO - O + NH 3 AUTO-AVALIAÇÃO 1- Quantos dos 20 aminoácidos α mostrados na tabela 1 contêm anéis aromáticos? Quantos contêm enxofre? Quantos contêm álcoois? 2- Desenhe as projeções de Fischer da L-treonina e L-valina e de seus enantiômeros. 3- Quais aminoácidos listados na tabela 1 tem mais de um carbono assimétrido? OBS: Carbono assimétrico é aquele ligado a quatro grupos diferentes. 4- Calcule o pi da asparagina e do ácido aspártico? Os valores de pka estão na tabela Desenhe a forma na qual a alanina e valina existem predominantemente em ph: 7,3; 0 e 11? 6- Uma mistura de três aminoácidos (glicina, isoleucina e ácido glutâmico) é separada por CCD utilizando sílica como fase estacionária. Explique a ordem de eluição de cada aminoácido. A sílica é uma fase estacionária polar. Lembre que o mecanismo de separação na CCD é igual na cromatografia em papel. 73
18 Química de Biomoléculas PRÓXIMA AULA Na próxima aula estudaremos os peptídeos e as proteínas. Vamos ver como os aminoácidos se ligam para formar os peptídeos e as proteínas. Conheceremos as estruturas primárias, secundárias, terciárias e quaternárias das proteínas. REFERÊNCIAS BRUICE, P. Y. Química Orgânica, 4ª. Ed., v. 2, São Paulo, Pearson Prentice Hall, CAREY, F. A. Química Orgânica, 7ª. Ed., v.2, Porto Alegre, Boockman, Mc MURRY, J. Química Orgânica, 7ª. Ed., v.2, São Paulo, Cengage, NELSON, D. L., COX, M. M. Princípios de Bioquímica de Lehninger, 5ª. Ed., Porto Alegre, Artmed, SOLOMONS, T. W. G. Química Orgânica, 9ª. Ed., v.2, São Paulo, Gen/ LTC,
Rafael Mesquita. Aminoácidos
 Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA. Aminoácidos. Prof. Willame Bezerra
 CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
Aminoácidos e peptídeos. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
1. INTRODUÇÃO. Polímeros biológicos. Polissacarídeos Proteínas Ácidos Nucléicos. Reservas de energia. Armazenamento e Transmissão de informações
 AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas
 Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Macromolécula mais abundante nas células
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
Aminoácidos. Bioquímica Prof. Dr. Marcelo Soares
 Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
PROTEÍNAS. A palavra proteína derivada de proteos, (grego = primeira ou a mais importante)
 PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
1164 BIOLOGIA ESTRUTURAL Aula 1 Prof. Dr. Valmir Fadel
 H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
Origem grego (protos) primeira, mais importante
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
Carla Bittar Bioquímica e Metabolismo Animal
 Carla Bittar Bioquímica e Metabolismo Animal Compostos orgânicos Unidades formadoras de PROTEÍNAS Ligações covalentes com perda de água Moléculas pequenas PM de aproximadamente 130 Estrutura da célula
Carla Bittar Bioquímica e Metabolismo Animal Compostos orgânicos Unidades formadoras de PROTEÍNAS Ligações covalentes com perda de água Moléculas pequenas PM de aproximadamente 130 Estrutura da célula
13/08/2018. Escala de ph. Escala de ph. Crescimento básico. Crescimento ácido. Neutro. básico
 Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
 Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
Aminoácidos e Peptideos
 Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
Aminoácidos e Peptídeos. Profa. Alana Cecília
 Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
Aminoácidos não-essenciais: alanina, ácido aspártico, ácido glutâmico, cisteína, glicina, glutamina, hidroxiprolina, prolina, serina e tirosina.
 AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
AMINOÁCIDOS. - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos;
 1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
MACRONUTRIENTES III PROTEÍNAS
 MACRONUTRIENTES III PROTEÍNAS 1 PROTEÍNAS As proteínas são compostos orgânicos de estrutura complexa e massa molecular elevada, elas são sintetizadas pelos organismos vivos através da condensação de um
MACRONUTRIENTES III PROTEÍNAS 1 PROTEÍNAS As proteínas são compostos orgânicos de estrutura complexa e massa molecular elevada, elas são sintetizadas pelos organismos vivos através da condensação de um
Aminoácidos. Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP.
 Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
13/03/2016. Profª. Drª. Andréa Fontes Garcia E -mail:
 Profª. Drª. Andréa Fontes Garcia E -mail: andrea@salesiano-ata.br 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
Profª. Drª. Andréa Fontes Garcia E -mail: andrea@salesiano-ata.br 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
AMINOÁCIDOS. Dra. Flávia Cristina Goulart. Bioquímica
 AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
Introdução. Estrutura dos Aminoácidos e Proteínas. Aminoácidos componentes de proteínas. Aminoácidos componentes de proteínas 10/02/2012.
 Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila
 Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
Aula 1. Referência. Bancos de Dados. Linguagem x Informação. Introdução a Bioquímica: Biomoléculas. Introdução ao Curso: Aminoácidos.
 Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
Programa de Pós-Graduação em Química
 1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
Introdução aos aminoácidos
 MÓDULO 2 - AULA 8 Aminoácidos não essenciais Aminoácidos essenciais Glicina 11355 mg Lisina 1958 mg Prolina 6808 mg Leucina 1569 mg Hidroxiprolina 5789 mg Valina 1223 mg Ácido Glutâmico 5065 mg Fenilalanina
MÓDULO 2 - AULA 8 Aminoácidos não essenciais Aminoácidos essenciais Glicina 11355 mg Lisina 1958 mg Prolina 6808 mg Leucina 1569 mg Hidroxiprolina 5789 mg Valina 1223 mg Ácido Glutâmico 5065 mg Fenilalanina
Aminoácidos peptídeos e proteínas
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
BÁSICA EM IMAGENS. Aminoácidos, peptídeos e proteínas
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
BC 0307 Transformações Químicas
 BC 0307 Transformações Químicas ANDERSON ORZARI RIBEIRO Anderson.ribeiro@ufabc.edu.br Bloco B, 10º andar - Sala 1043 BC 0307 Transformações Químicas AULA 5 Compostos de carbono e interações intermoleculares
BC 0307 Transformações Químicas ANDERSON ORZARI RIBEIRO Anderson.ribeiro@ufabc.edu.br Bloco B, 10º andar - Sala 1043 BC 0307 Transformações Químicas AULA 5 Compostos de carbono e interações intermoleculares
AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES
 UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
Aminoácidos, Péptidos e Proteínas
 Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
ANDERSON ORZARI RIBEIRO
 Transformações Químicas ANDERSON ORZARI RIBEIRO Anderson.ribeiro@ufabc.edu.br Bloco B, 10º andar - Sala 1043 Transformações Químicas AULA 5 Compostos de carbono e interações intermoleculares CAPÍTULO 3
Transformações Químicas ANDERSON ORZARI RIBEIRO Anderson.ribeiro@ufabc.edu.br Bloco B, 10º andar - Sala 1043 Transformações Químicas AULA 5 Compostos de carbono e interações intermoleculares CAPÍTULO 3
REVISÃO: ENADE BIOQUÍMICA - 1
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
Aminoácidos e Peptídeos
 Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Faculdade Anhanguera Curso de Graduação em Educação Física
 Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: Amabile.arias@anhanguera.com 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: Amabile.arias@anhanguera.com 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos
 Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Lista de Exercícios de Bioquímica
 Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Aminoácidos. subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes
 . Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
. Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs
 Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
- Apresentam uma fórmula básica: um átomo central de carbono onde se ligam:
 1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
BIOQUÍMICA. Profº André Montillo
 BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
ATIVIDADE - 3 ARTIGO: Proteínas: Hidrólise, Precipitação e um Tema para o Ensino de Química RESUMO: Questão 1:
 ATIVIDADE - 3 ARTIGO: FRANCISCO JUNIOR, W. E.; FRANCISCO, W. Proteínas: Hidrólise, Precipitação e um Tema para o Ensino de Química. 2006. Disponível em: .
ATIVIDADE - 3 ARTIGO: FRANCISCO JUNIOR, W. E.; FRANCISCO, W. Proteínas: Hidrólise, Precipitação e um Tema para o Ensino de Química. 2006. Disponível em: .
Estrutura das Proteínas pode ser descrita em 4 níveis de organização
 PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
AMINOÁCIDOS.! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico NH2 I R - C - C = 0O I I H OH
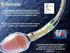 Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
Biologia Molecular (Parte I)
 Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES
 Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
UNIFESO Engenharia Ambiental Prof.: Edson R. Fernandes dos Santos Aminoácidos
 UNIFESO Engenharia Ambiental Prof.: Edson R. Fernandes dos Santos Aminoácidos Clique para editar o estilo do subtítulo mestre α-aminoácidos Variações possíveis Estrutura básica Amina Ácido Carboxílico
UNIFESO Engenharia Ambiental Prof.: Edson R. Fernandes dos Santos Aminoácidos Clique para editar o estilo do subtítulo mestre α-aminoácidos Variações possíveis Estrutura básica Amina Ácido Carboxílico
Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
3 LIGANTES. 3.1 Aspectos biológicos
 LIGANTES 38 3 LIGANTES Serão descritos os principais aspectos químicos e biológicos dos ligantes estudados neste trabalho. A importância desse capítulo fundamenta-se no fato de que os aminoácidos são as
LIGANTES 38 3 LIGANTES Serão descritos os principais aspectos químicos e biológicos dos ligantes estudados neste trabalho. A importância desse capítulo fundamenta-se no fato de que os aminoácidos são as
Aminoácidos FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
5. Reações de Adição Nucleofílica
 5. Reações de Adição Nucleofílica 5.1. Aspectos Gerais das Reações de Adição Nucleofílica 5.2. Adição de Água 5.3. Adição de Álcoois 5.4. Reação de Aldeídos e de Cetonas com Aminas 5.5. Adição de HCN 5.6.
5. Reações de Adição Nucleofílica 5.1. Aspectos Gerais das Reações de Adição Nucleofílica 5.2. Adição de Água 5.3. Adição de Álcoois 5.4. Reação de Aldeídos e de Cetonas com Aminas 5.5. Adição de HCN 5.6.
Professor Antônio Ruas
 Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Gliconeogênese. Gliconeogênese. Órgãos e gliconeogênese. Fontes de Glicose. Gliconeogênese. Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia
 Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia Gliconeogênese Alexandre Havt Gliconeogênese Fontes de Energia para as Células Definição Via anabólica que ocorre no fígado e, excepcionalmente
Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia Gliconeogênese Alexandre Havt Gliconeogênese Fontes de Energia para as Células Definição Via anabólica que ocorre no fígado e, excepcionalmente
Prof. Marcelo Langer. Curso de Biologia. Aula Genética
 Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
DIGESTÃO E ABSORÇÃO DAS PROTEÍNAS
 DIGESTÃO E ABSORÇÃO DAS PROTEÍNAS 1 Fenilalanina Valina Aa essenciais Treonina Triptofano Isoleucina Metionina Histidina Lisina Arginina Leucina PROTEÍNAS Alanina Asparagina Aspartato Cisteína Glutamato
DIGESTÃO E ABSORÇÃO DAS PROTEÍNAS 1 Fenilalanina Valina Aa essenciais Treonina Triptofano Isoleucina Metionina Histidina Lisina Arginina Leucina PROTEÍNAS Alanina Asparagina Aspartato Cisteína Glutamato
Profº Lásaro Henrique
 Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
A QUÍMICA DOS AMINOÁCIDOS E PEPTÍDEOS
 A QUÍMICA DOS AMINOÁCIDOS E PEPTÍDEOS META Introduzir o estudo do conhecimento das estruturas e das propriedades químicas dos aminoácidos e peptídeos. OBJETIVOS Ao final desta aula, o aluno deverá: reconhecer
A QUÍMICA DOS AMINOÁCIDOS E PEPTÍDEOS META Introduzir o estudo do conhecimento das estruturas e das propriedades químicas dos aminoácidos e peptídeos. OBJETIVOS Ao final desta aula, o aluno deverá: reconhecer
5. Reações de Adição Nucleofílica
 5. Reações de Adição Nucleofílica 5.1. Aspectos Gerais das Reações de Adição Nucleofílica 5.2. Adição de Água 5.3. Adição de Álcoois 5.4. Reação de Aldeídos e de Cetonas com Aminas 5.5. Adição de HCN 5.6.
5. Reações de Adição Nucleofílica 5.1. Aspectos Gerais das Reações de Adição Nucleofílica 5.2. Adição de Água 5.3. Adição de Álcoois 5.4. Reação de Aldeídos e de Cetonas com Aminas 5.5. Adição de HCN 5.6.
Componentes Químicos das Células
 Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Bioquímica: Componentes orgânicos e inorgânicos necessários à vida. Leandro Pereira Canuto
 Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Estrutura Primária de Proteínas: Sequenciamento de Aminoácidos
 UNIVERSIDADE DE SÃO PAULO USP FARMÁCIA BIOQUÍMICA 015N Reatividade de Compostos Orgânicos II Estrutura Primária de Proteínas: Sequenciamento de Aminoácidos Beatriz In Soon Chang (9328183) João Gabriel
UNIVERSIDADE DE SÃO PAULO USP FARMÁCIA BIOQUÍMICA 015N Reatividade de Compostos Orgânicos II Estrutura Primária de Proteínas: Sequenciamento de Aminoácidos Beatriz In Soon Chang (9328183) João Gabriel
Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos. Referência: Stryer ou Lehninger
 Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos Referência: Stryer ou Lehninger Deoxi-hemoglobina Slide - Lehninger 5a edição Estrutura de proteínas
Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos Referência: Stryer ou Lehninger Deoxi-hemoglobina Slide - Lehninger 5a edição Estrutura de proteínas
Aula 5 Estrutura e função de proteínas
 Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
Alcoóis. -Nomenclatura IUPAC: Quantidade de C + tipo de ligação entre C + ol. Ex: Butan-2-ol. Fenóis
 Ácidos e Base -Numa reação entre um ácido e uma base, o ácido atua como o doador de prótons e a base como o aceptor de prótons. O íon H + é considerado um próton, então na reação o ácido perde um H + e
Ácidos e Base -Numa reação entre um ácido e uma base, o ácido atua como o doador de prótons e a base como o aceptor de prótons. O íon H + é considerado um próton, então na reação o ácido perde um H + e
Professor Antônio Ruas
 Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS
 PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
Proteínas. Proteínas são polímeros de aminoácidos
 Proteínas Estrutura & Propriedades Proteínas são polímeros de aminoácidos Existem 20 tipos diferentes de aminoácidos Aminoácidos são ácidos fracos A carga elétrica do aminoácido varia de acordo com o ph
Proteínas Estrutura & Propriedades Proteínas são polímeros de aminoácidos Existem 20 tipos diferentes de aminoácidos Aminoácidos são ácidos fracos A carga elétrica do aminoácido varia de acordo com o ph
Composição química celular
 Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
O DIAMANTE POSSUI HIBRIDIZAÇÃO
 QUÍMICA ORGÂNICA Pode-se afirmar com certeza que se não fosse pelo Carbono você não estaria lendo essa breve descrição agora. A química orgânica se preocupa com o entendimento da vida dada pelo Carbono
QUÍMICA ORGÂNICA Pode-se afirmar com certeza que se não fosse pelo Carbono você não estaria lendo essa breve descrição agora. A química orgânica se preocupa com o entendimento da vida dada pelo Carbono
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas.
 São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS CAMPUS POMBAL - PB
 CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS CAMPUS POMBAL - PB DISCIPLINA: Química Orgânica PRÉ-REQUISITO: Química Geral CRÉDITOS: 04 CARGA HORÁRIA: 60 horas
CENTRO DE CIÊNCIAS E TECNOLOGIA AGROALIMENTAR UNIDADE ACADÊMICA DE TECNOLOGIA DE ALIMENTOS CAMPUS POMBAL - PB DISCIPLINA: Química Orgânica PRÉ-REQUISITO: Química Geral CRÉDITOS: 04 CARGA HORÁRIA: 60 horas
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS
 UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Parte escrita do seminário referente à disciplina Reatividade de Compostos Orgânicos II e Biomoléculas
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Parte escrita do seminário referente à disciplina Reatividade de Compostos Orgânicos II e Biomoléculas
Purificação de Proteínas
 Purificação de Proteínas Propriedades usadas na purificação de proteínas através de cromatografia líquida Na separação a amostra contendo a mistura de proteínas é preparada em solução aquosa, a solução
Purificação de Proteínas Propriedades usadas na purificação de proteínas através de cromatografia líquida Na separação a amostra contendo a mistura de proteínas é preparada em solução aquosa, a solução
Peptídeos e Proteínas: Estrutura de Proteínas
 Peptídeos e Proteínas: Estrutura de Proteínas QFL0343 - REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS Adriana Uehara 9820384 Janaína Novais 9819722 Aminoácidos Estruturas carbônicas que possuem
Peptídeos e Proteínas: Estrutura de Proteínas QFL0343 - REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS Adriana Uehara 9820384 Janaína Novais 9819722 Aminoácidos Estruturas carbônicas que possuem
QUÍMICA (A) (B) (C) (D) (E)
 QUÍMICA A octanagem é uma medida da resistência à compressão da gasolina. O isoctano é utilizado como padrão de índice de octanagem por ser o composto que mais resiste à compressão sem explodir. A respeito
QUÍMICA A octanagem é uma medida da resistência à compressão da gasolina. O isoctano é utilizado como padrão de índice de octanagem por ser o composto que mais resiste à compressão sem explodir. A respeito
BIOQUÍMICA PARA ODONTO
 BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
Aminoácidos e Proteínas
 Aminoácidos e Proteínas PROTEÍNAS As proteínas são as macromoléculas mais abundantes nas células vivas. Ocorrem em todas as células e em todas as partes das mesmas. FUNÇÕES DAS PROTEÍNAS Formam estruturas
Aminoácidos e Proteínas PROTEÍNAS As proteínas são as macromoléculas mais abundantes nas células vivas. Ocorrem em todas as células e em todas as partes das mesmas. FUNÇÕES DAS PROTEÍNAS Formam estruturas
RESPOSTAS DAS TAREFAS 2ª SÉRIE. Química - Setor A. Aulas 43 e 44. Aula 43. Aula 44 ENSINO MÉDIO 1. D 2. C
 ESI MÉDI RESPSTAS DAS TAREFAS 2ª SÉRIE 16 Química - Setor A Aulas 43 e 44 Aula 43 1. D 2. 3. a) idrólise alcalina ou saponificação b) Sais de ácidos carboxílicos Aula 44 1. A interação intermolecular que
ESI MÉDI RESPSTAS DAS TAREFAS 2ª SÉRIE 16 Química - Setor A Aulas 43 e 44 Aula 43 1. D 2. 3. a) idrólise alcalina ou saponificação b) Sais de ácidos carboxílicos Aula 44 1. A interação intermolecular que
Purificação de Proteínas
 Purificação de Proteínas Recuperação da atividade enzimática Etapa de purificação 100 mu 80 mu 2ml de lisado contendo 50 mu/ml 10ml de material contendo 8 mu/ml Recuperação = 80% = 80 mu/100 mu Recuperação:
Purificação de Proteínas Recuperação da atividade enzimática Etapa de purificação 100 mu 80 mu 2ml de lisado contendo 50 mu/ml 10ml de material contendo 8 mu/ml Recuperação = 80% = 80 mu/100 mu Recuperação:
EXPERIÊNCIA 6 CROMATOGRAFIA
 EXPERIÊNCIA 6 CROMATOGRAFIA 1. OBJETIVOS No final desta experiência espera-se que o aluno seja capaz de: Entender os princípios e as principais aplicações da cromatografia. Separar e identificar os componentes
EXPERIÊNCIA 6 CROMATOGRAFIA 1. OBJETIVOS No final desta experiência espera-se que o aluno seja capaz de: Entender os princípios e as principais aplicações da cromatografia. Separar e identificar os componentes
Reações de Substituição Nucleofílica em Carbono Saturado. Aula 11
 Universidade Federal de Ouro Preto Reações de Substituição Nucleofílica em Carbono Saturado Aula 11 Flaviane Francisco Hilário 1 1 - Reação de Substituição Nucleofílica e Reação de Eliminação SUBSTITUIÇÃO
Universidade Federal de Ouro Preto Reações de Substituição Nucleofílica em Carbono Saturado Aula 11 Flaviane Francisco Hilário 1 1 - Reação de Substituição Nucleofílica e Reação de Eliminação SUBSTITUIÇÃO
1. 1. Polímeros de adição: Para que ocorra polímero de adição é necessário que o monômero possua ligação PI.
 Bioquímica. Polímeros Alguns tipos de moléculas pequenas, camadas monômeros, podem ligar-se umas com as outras, dando origem a macromoléculas, denominadas polímeros (do grego poli = muitos; meros = partes)
Bioquímica. Polímeros Alguns tipos de moléculas pequenas, camadas monômeros, podem ligar-se umas com as outras, dando origem a macromoléculas, denominadas polímeros (do grego poli = muitos; meros = partes)
Ácidos Carboxílicos e Derivados Reações de Substituição Nucleofílica no Grupo Acil
 Ácidos arboxílicos e Derivados eações de Substituição Nucleofílica no Grupo Acil N307 - Química rgânica II Prof. Dr. José Nunes da Silva Jr. bjetivos da Unidade Analisar as estruturas dos ácidos carboxílicos
Ácidos arboxílicos e Derivados eações de Substituição Nucleofílica no Grupo Acil N307 - Química rgânica II Prof. Dr. José Nunes da Silva Jr. bjetivos da Unidade Analisar as estruturas dos ácidos carboxílicos
UFSC. Resposta: 76. Comentário. 01. Incorreta. É formado pela reação de neutralização entre o hidróxido de potássio e ácido carbônico.
 Resposta: 76 01. Incorreta. É formado pela reação de neutralização entre o hidróxido de potássio e ácido carbônico. H 2 CO 3 + KOH = K 2 CO 3 + H 2 0 02. Incorreta. O nox do carbono é +4. 04. Correta.
Resposta: 76 01. Incorreta. É formado pela reação de neutralização entre o hidróxido de potássio e ácido carbônico. H 2 CO 3 + KOH = K 2 CO 3 + H 2 0 02. Incorreta. O nox do carbono é +4. 04. Correta.
Pré UFSC Química. Química Orgânica. Alcinos. Funções Orgânicas. Alcadienos. Hidrocarbonetos. Alcanos. Cicloalcanos. Alcenos.
 Química Orgânica Estuda as propriedades e composição dos compostos que apresentam o carbono como principal elemento químico. Alcinos São hidrocarbonetos acíclicos contendo uma única ligação tripla entre
Química Orgânica Estuda as propriedades e composição dos compostos que apresentam o carbono como principal elemento químico. Alcinos São hidrocarbonetos acíclicos contendo uma única ligação tripla entre
Funções orgânicas oxigenadas e nitrogenadas.
 Funções orgânicas oxigenadas e nitrogenadas Funções que possuem ou derivam do grupo funcional hidroxila ( OH) Ex: a) Etanol Álcool b) Prop 2 en 1 ol Ex:... estiver ligado a um carbono saturado...... estiver
Funções orgânicas oxigenadas e nitrogenadas Funções que possuem ou derivam do grupo funcional hidroxila ( OH) Ex: a) Etanol Álcool b) Prop 2 en 1 ol Ex:... estiver ligado a um carbono saturado...... estiver
Q.02 Considere uma solução aquosa diluída de dicromato de potássio, a 25 ºC. Dentre os equilíbrios que estão presentes nessa solução, destacam-se:
 Q.01 Íons indesejáveis podem ser removidos da água, tratando-a com resinas de troca iônica, que são constituídas por uma matriz polimérica, à qual estão ligados grupos que podem reter cátions ou ânions.
Q.01 Íons indesejáveis podem ser removidos da água, tratando-a com resinas de troca iônica, que são constituídas por uma matriz polimérica, à qual estão ligados grupos que podem reter cátions ou ânions.
UFSC. Química (Amarela) Resposta: = 05
 Resposta: 01 + 04 = 05 01. Correto. Apresenta carboxila e grupamento amino no carbono alfa. 02. Incorreto. Com a elevação do ph ocorre a desprotonação da carboxila formando carga negativa. 04. Correto.
Resposta: 01 + 04 = 05 01. Correto. Apresenta carboxila e grupamento amino no carbono alfa. 02. Incorreto. Com a elevação do ph ocorre a desprotonação da carboxila formando carga negativa. 04. Correto.
Substituição Nucleofílica em Ácidos Carboxílicos e Derivados
 Substituição Nucleofílica em Ácidos Carboxílicos e Derivados Estrutura, Nomenclatura, ocorrência natural, aplicação, propriedades físicas,preparação e reatividade. 2- Estrutura dos ácidos carboxílicos
Substituição Nucleofílica em Ácidos Carboxílicos e Derivados Estrutura, Nomenclatura, ocorrência natural, aplicação, propriedades físicas,preparação e reatividade. 2- Estrutura dos ácidos carboxílicos
Carla Bittar Bioquímica e Metabolismo Animal
 Carla Bittar Bioquímica e Metabolismo Animal Biosfera rica em N2 Microrganismos reduzem N2 formando NH3 Plantas e microrganismos absorvem NH3 e NO3- para síntese de biomoléculas Animais dependem da dieta
Carla Bittar Bioquímica e Metabolismo Animal Biosfera rica em N2 Microrganismos reduzem N2 formando NH3 Plantas e microrganismos absorvem NH3 e NO3- para síntese de biomoléculas Animais dependem da dieta
FERTILIZANTE ORGÂNICO COMPOSTO CLASSE A
 FERTILIZANTE ORGÂNICO COMPOSTO CLASSE A REGISTRADO NO MAPA SOB O Nº PA-07526 10001-7 GARANTIAS DE REGISTRO 11% Nitrogênio Total (N) 20% Carbono Orgânico Total (COT) É um fertilizante fluido com alta concentração
FERTILIZANTE ORGÂNICO COMPOSTO CLASSE A REGISTRADO NO MAPA SOB O Nº PA-07526 10001-7 GARANTIAS DE REGISTRO 11% Nitrogênio Total (N) 20% Carbono Orgânico Total (COT) É um fertilizante fluido com alta concentração
Proteínas A U L A 04 - TEÓRICA PROF. DÉBORA CHRISTINA
 Proteínas A U L A 04 - TEÓRICA 04-09- 17 PROF. DÉBORA CHRISTINA CONCEITO As proteínas apresentam funções e estruturas diversificadas e são sintetizadas a partir de apenas 20 aminoácidos diferentes; São
Proteínas A U L A 04 - TEÓRICA 04-09- 17 PROF. DÉBORA CHRISTINA CONCEITO As proteínas apresentam funções e estruturas diversificadas e são sintetizadas a partir de apenas 20 aminoácidos diferentes; São
RMN em proteínas pequenas
 COSY COrrelated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) mais simples Primeiro experimento 2D proposto (Jeener, 1971) Período de mistura: 1 único pulso de 90 Transferência da coerência entre
COSY COrrelated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) mais simples Primeiro experimento 2D proposto (Jeener, 1971) Período de mistura: 1 único pulso de 90 Transferência da coerência entre
UDESC 2016/2 QUÍMICA. Comentário. I. Verdadeira. 0,07 mg 1 kg x mg 14 kg. Na 2 PO 3. F 144 g 19 g 7,58 mg x mg. x = 0,98 (limite de ingestão diária)
 QUÍMICA I. Verdadeira. 0,07 mg 1 kg x mg 14 kg x = 0,98 (limite de ingestão diária) Na PO 3 F 144 g 19 g 7,58 mg x mg x = 1 mg (que já é maior que o limite de ingestão diária) 1 II. Verdadeira. 0,07 mg
QUÍMICA I. Verdadeira. 0,07 mg 1 kg x mg 14 kg x = 0,98 (limite de ingestão diária) Na PO 3 F 144 g 19 g 7,58 mg x mg x = 1 mg (que já é maior que o limite de ingestão diária) 1 II. Verdadeira. 0,07 mg
Você deve desenhar o aminoácido com o grupo amino protonado (pka > 7) e o grupo carboxílico desprotonado (pka <7).
 QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
Universidade Federal do Ceará Centro de Ciências Departamento de Química Orgânica e Inorgânica
 Universidade Federal do Ceará Centro de Ciências Departamento de Química Orgânica e Inorgânica PLANO DE ENSINO DE DISCIPLINA Ano/Semestre 2015.1 1. Identificação 1.1. Unidade Acadêmica: Centro de Ciências
Universidade Federal do Ceará Centro de Ciências Departamento de Química Orgânica e Inorgânica PLANO DE ENSINO DE DISCIPLINA Ano/Semestre 2015.1 1. Identificação 1.1. Unidade Acadêmica: Centro de Ciências
1 a Lista de Exercícios de Técnicas Cromatográficas (2 a parte)
 1 a Lista de Exercícios de Técnicas Cromatográficas (2 a parte) Prof. Mauricio Xavier Coutrim 1. Explique porquê apenas um dentre os seguintes procedimentos a ser adotados para a melhora da separação de
1 a Lista de Exercícios de Técnicas Cromatográficas (2 a parte) Prof. Mauricio Xavier Coutrim 1. Explique porquê apenas um dentre os seguintes procedimentos a ser adotados para a melhora da separação de
