Introdução ao Metabolismo
|
|
|
- João Lucas Cavalheiro Castelhano
- 7 Há anos
- Visualizações:
Transcrição
1 Introdução ao Metabolismo
2 Mapa 1 Alimentos Polissacarídeos Lipídios Proteínas glicose aminoácidos ácido graxo CO 2 NADH FADH 2 O 2 NAD + FAD ADP+P i CO 2 ATP
3 Mapa 2 Polissacarídeos Proteínas Lipídeos glicose aminoácidos ácido graxo Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Piruvato CO 2 Acetil-CoA CO 2 Oxaloacetato(4) Citrato(6) Malato(4) Isocitrato(6) CO 2 Fumarato(4) -cetoglutaratoato(5) Succinato(4) CO 2
4 METABOLISMO- Conceitos fundamentais e estudos dirigidos M1 INTRODUÇÃO AO METABOLISMO A - MAPA I: DEGRADAÇÃO (OXIDAÇÃO) DE ALIMENTOS: 1. Qual a finalidade biológica dos processos descritos no mapa? 2. Analisar a função das coenzimas e do oxigênio na oxidação dos alimentos. 3. Quais os compostos aceptores de hidrogênio? Quais os compostos necessários para a conversão da forma reduzida das coenzimas na forma oxidada? B - DISCUTIR AS SEGUINTES AFIRMAÇÕES: 4. A energia dos alimentos é obtida por oxidação. A oxidação biológica consiste na retirada de hidrogênio (H 2 ) do substrato. 5. Os processos celulares que requerem energia utilizam a energia térmica proveniente da oxidação dos alimentos. 6. Uma parte da energia derivada da oxidação de alimentos é usada para sintetizar um composto rico em energia, o ATP. A única função dos alimentos é fornecer energia. 7. Os compostos característicos de um dado organismo devem ser supridos pela dieta. C - MAPA II: 8. Quais são os passos irreversíveis que aparecem no mapa anexo? Qual o primeiro composto comum à degradação de proteínas, lipídios e carboidratos? 9. Animais de laboratório foram submetidos a dietas compostas exclusivamente de carboidratos, lipídios, ou proteínas. Estes três tipos de compostos são essenciais para a sobrevivência. Não havendo outras restrições na dieta, prever que grupo de animais sobreviveria, verificando se é possível sintetizar: a) ácido graxo a partir de glicose b) proteína a partir de glicose c) glicose a partir de ácido graxo d) proteína a partir de ácido graxo e) glicose a partir de proteína f) ácido graxo a partir de proteína Indicar no mapa a via utilizada em cada item. O SENTIDO DAS REAÇÕES Conceitos Fundamentais Energia Livre de Gibbs - Mede a quantidade de energia utilizada pelos seres vivos para realizar trabalho em condições de temperaturas e pressão constantes. É representada pelo símbolo G. Variação de Energia Livre (de uma reação química)- Se refere à diferença entre o conteúdo de energia de reagentes e produtos, que acompanha qualquer reação química.
5 G - O sinal atribuído ao G indica o sentido em que a reação tende a ocorrer em condições padrão (ph 7,0; concentração de reagentes e produtos de 1M; temperatura de 273 K, pressão de 1 atmosfera). Nas células, reações com G>0, que não aconteceriam espontaneamente, passam a acontecer se forem acopladas a reações com G<0 e a somatória das duas reações produzir um G<0. Compostos ricos em energia são compostos que contém uma ligação química (muitas vezes a ligação da qual faz parte o grupamento fosfato), cuja hidrólise (quebra) é acompanhada de uma grande liberação de energia. Quando o G da reação de hidrólise de dado composto é negativo e tem valor absoluto maior que 25 kj/mol o composto é classificado como rico em energia. Procurar no livro texto uma tabela de compostos ricos em energia. Nas reações de óxido-redução, para um composto ser oxidado (perder elétrons ou átomos de hidrogênio) algum outro composto tem que necessariamente ser reduzido (ganhar elétrons ou átomos de hidrogênio). A tendência de um par redox ganhar ou perder elétrons é determinada pelo valor do potencial de óxido-redução padrão (E ) de cada par. Questões 1. Desenhe a estrutura do ATP. Aponte na estrutura química da molécula de ATP, os componentes responsáveis por seu nome: adenosina trifosfato. Explique porquê o ATP é um composto rico em energia. 2. Leia sobre variação de energia livre em reações de óxido-redução e explique como se pode medir o potencial redox de determinada reação. 3. A uma solução com concentração 1M de NAD +, NADH, piruvato e lactato, adicionou-se lactato desidrogenase. O potencial de óxido-redução padrão (E ) dos sistemas NAD + /NADH e piruvato/lactato é igual a 0,32V e 0,19V, respectivamente. a) Em que sentido ocorrerá a reação? b) Como variam os potenciais de óxido-redução dos sistemas à medida que a reação ocorre? c) Em que condições a reação atingirá o equilíbrio? Qual o valor do potencial de óxido-redução dos dois sistemas nesta situação? d) Qual o valor G da reação? M2 GLICÓLISE / DESTINOS DO PIRUVATO Conceitos fundamentais Glicose: principal substrato oxidável para a maioria dos organismos; única fonte de energia utilizável pelas hemácias e tecido nervoso. A glicólise é uma via de degradação da glicose que ocorre no citossol de células procarióticas e eucarióticas. A glicólise é uma seqüência de 10 reações catalisadas por enzimas, por meio das quais uma molécula de glicose (6C) é convertida a duas moléculas de piruvato (3C), com a produção líquida de dois ATPs e a redução de dois NAD + a dois NADH. No primeiro estágio da glicólise, a glicose é fosforilada pela hexoquinase originando glicose-6-fosfato; esta é isomerizada pela fosfoglicose-isomerase produzindo
6 frutose-6-fosfato que é então fosforilada pela fosfofrutoquinase formando frutose- 1,6-bisfosfato. Sua clivagem pela aldolase produz duas trioses: gliceraldeído-3- fosfato e diidroxiacetona-fosfato, que são interconvertidas pela triose-fosfatoisomerase. Essas reações consomem 2 ATP por glicose. No segundo estágio da glicólise, o gliceraldeído-3-fosfato é fosforilado pela gliceraldeído-3-fosfato-desidrogenase, formando o 1,3-bisfosfoglicerato que é defosforilado pela fosfoglicerato-quinase para produzir ATP. O 3-fosfoglicerato é isomerizado pela fosfoglicerato-mutase produzindo 2-fosfoglicerato que é desidratado pela enolase levando à formação de fosfoenolpiruvato, que sofre defosforilação pela piruvato-quinase produzindo um segundo ATP e um piruvato. Esse estágio produz 4 ATP por glicose, entretanto, descontando os ATP usados para as fosforilações iniciais da via, houve um rendimento líquido de 2 ATP por glicose. Em condições anaeróbicas (fermentação), o piruvato é reduzido pelo NADH a lactato regenerando NAD + para prosseguimento da glicólise (fermentação lática). Na fermentação alcoólica, o piruvato é descarboxilado formando acetaldeído e este recebe os elétrons provenientes do NADH. O acetaldeído é reduzido a etanol recebendo o hidrogênio do NADH que se reoxida. As reações da via glicolítica catalisadas pela hexoquinase, fosfofrutoquinase e piruvato-quinase são irreversíveis. Os possíveis destinos do piruvato são: 1) via aeróbica completa após descarboxilação oxidativa e formação de acetil-coa para entrada em Krebs; 2) fermentação lática (músculo); 3) fermentação alcoólica (leveduras ou bactérias). Questões 1. Escreva as reações da glicólise mostrando as fórmulas estruturais dos intermediários e os nomes das enzimas que catalisam as reações. 2. Baseado no mapa da glicólise, responda as seguintes questões: a. Qual a finalidade da via glicolítica? b. Escreva a reação de oxidação da coenzima NADH (nicotinamida-adeninadinucleotídeo) apresentando as estruturas químicas completas. c. Qual(is) o(s) composto(s) que aceitam os átomos de hidrogênio na via glicolítica? d. Escrever as reações de óxido-redução que ocorrem na via glicolítica identificando os pares redox, compostos oxidados e compostos reduzidos nessas reações. e. Associar formação de ATP e reações de óxido-redução. f. Quais são os passos irreversíveis da glicólise? 3. Indicar os compostos ricos em energia formados na glicólise. 4. Descrever os três possíveis destinos do piruvato. 5. Indicar os principais tipos de reação encontrados na via glicolítica. Esses tipos serão comuns a diversas vias metabólicas que serão estudadas mais adiante. 6. Discutir se é verdadeiro ou falso: ( ) A quantidade de NAD + é um dos limitantes da glicólise. ( ) Quando a razão ATP/ADP está baixa, a via glicolítica está inibida. 7. Quantas moléculas de piruvato se formam a partir de uma molécula de glicose? 8. Verificar na via metabólica os compostos que apresentam ligações do tipo: a) fosfoenol, b) anidrido fosfórico, c) éster fosfórico.
7 9. Identificar também as reações catalisadas pelas seguintes enzimas: a) quinase, b) mutase, c) isomerase, d) aldolase, e) desidrogenase. 10. Considerando o número de moléculas de ATP consumidas e formadas, estabelecer o saldo final de ATP na oxidação de uma molécula de glicose pela via glicolítica. 11. Citar os compostos que devem ser fornecidos à via glicolítica para haver formação de lactato (iniciar a via) ou mantê-la em funcionamento. 12. Esquematizar as reações de fermentação alcoólica que possibilitam a obtenção de NAD+ na forma oxidada. Citar exemplos de tecidos ou organismos onde ocorrem fermentação lática e alcoólica. Em que condições o músculo oxida glicose a lactato? Formação de Acetil-CoA 13. Escrever a reação de formação de acetil-coa a partir de piruvato e indicar: a) as 5 coenzimas necessárias, b) as vitaminas envolvidas e c) a sua localização celular 14. Esquematizar as reações que permitem a oxidação de etanol a acetil-coa. 15. Quando glicose é metabolizada a acetil-coa, citar o número de moléculas de ATP, NADH e CO2 formadas. Sentido das reações da via glicolítica em condições fisiológicas e regulação da via 1. Reações irreversíveis possuem G Reações reversíveis possuem G ~ O controle de uma via metabólica ocorre sempre através do controle das etapas irreversíveis dessa via. 4. Para controlar dada reação irreversível deve-se controlar a enzima que a catalisa. 5. As enzimas podem aumentar ou diminuir suas atividades de acordo com o meio ambiente onde se encontram. Por exemplo, a fosfofrutoquinase torna-se praticamente inativa quando há abundância de ATP na célula. Estudo dirigido 1. Determinar o sentido das reações da via glicolítica. 2. Discutir porque etapas irreversíveis em geral estão acopladas ao gasto de ATP. 3. Como fatores alostéricos regulam enzimas?quais as enzimas que são reguladas por fatores alostéricos na via glicolítica? 4. Discutir como a glicólise é regulada a partir do mapa metabólico geral. M3 GLICONEOGÊNESE E CICLO DE CORI Conceitos fundamentais Os principais reagentes que irão produzir glicose pela gliconeogênese são: 1)lactato; 2)aminoácidos conversíveis a piruvato; 2) aminoácidos conversíveis a oxaloacetato; 3) glicerol conversível a dihidroxicetona fosfato. A conversão dos reagentes da gliconeogênese a glicose requer substituição de enzimas da glicólise que catalisam etapas irreversíveis. A piruvato-carboxilase e a fosfoenolpiruvato-carboxiquinase substituem a piruvato-quinase. A frutose-
8 1,6-bisfosfatase substitui a fosfofrutoquinase. A glicose-6-fosfatase substitui a hexoquinase. A regulação da glicólise e da gliconeogênese é recíproca: se uma via está ativada a outra estará desativada. A gliconeogênese é favorecida e a glicólise é desfavorecida, quando a célula está com carga energética alta. A gliconeogênese é regulada por alterações na síntese das enzimas e por efetuadores alostéricos, incluindo a frutose-2,6-bisfosfato, que inibe a frutose-1,6-bisfosfatase (enzima da gliconeogênese) e ativa a fosfofrutoquinase (enzima da glicólise). Estudo dirigido 1. Definir gliconeogênese. Citar o tecido responsável pela gliconeogênese. 2. Observar a Figura com o esquema da lançadeira malato-aspartato. Identificar na capa da apostila a mesma lançadeira. Porque a lançadeira malatoaspartato é importante para a gliconeogênese? Qual o nome das enzimas importantes para a conversão de aminoácidos como o aspartato em piruvato? 3. Comparar as três reações irreversíveis da glicólise com as reações da gliconeogênese que as substituem, quanto a reagentes, produtos, enzimas e coenzimas. 4. Porque o fosfoenolpiruvato é um composto rico em energia? Dar a base estrutural para a ocorrência de ligação altamente energética. 5. Comparar a estequiometria da glicólise e a da gliconeogênese e explicar porquê uma simples reversão da glicólise não foi o esquema adotado pela natureza para obtenção de glicose. Explicar através de energética das vias. 6. O que é o ciclo de Cori? M4 VIA DAS PENTOSES Conceitos Fundamentais Muitas funções celulares que envolvem reações endergônicas são efetuadas graças à hidrólise exergônica de ATP. Outras reações endergônicas, como a síntese de ácidos graxos e colesterol e a fotossíntese, requerem NADPH, que tem um grande poder redutor. O grupo fosforila no carbono 2 de uma das unidades de ribose do NADPH o diferencia de NADH. NADH é oxidado pela cadeia respiratória para gerar ATP, enquanto que NADPH serve como um doador de elétrons em reações biossintéticas redutoras. Na via das pentoses, NADPH é gerado quando a glicose-6-fosfato é oxidada a ribose-5-fosfato, que é um açúcar de 5 carbonos, componente de vários compostos importantes, como ATP, CoA, NAD+, FAD, RNA e DNA. A via das pentoses também catalisa a interconversão de açúcares de 3, 4, 5, 6 e 7 carbonos, em uma série de reações não oxidativas que ocorrem no citosol. As reações da via das pentoses são as seguintes: glicose-6-fosfato é desidrogenado e convertido a ribulose-5-fosfato, em três reações, produzindo 2 NADPH + H+. ribulose-5-fosfato é isomerizada a ribose-5-fosfato. Nestas reações, 2 NADPH + H+ e uma ribose-5-fosfato são gerados para cada glicose- 6-fosfato oxidada.
9 ribose-5-fosfato é convertida a gliceraldeído-3-fosfato e frutose-6-fosfato pela transcetolase e transaldolase. A transcetolase catalisa a transferência de unidades de C2 de uma cetose para uma aldose. A transaldolase transfere unidades de C3 de uma aldose para uma cetose. As reações de transcetolase e transaldolase criam uma ligação reversível entre a via das pentoses e a via glicolítica. O resultado dessas reações é a formação de 2 hexoses e 1 triose a partir de 3 pentoses: C5 + C5 C3 + C7 Transcetolase C7 + C3 C4 + C6 Transaldolase C5 + C4 C3 + C6 Transcetolase O excesso de ribose-5-fosfato formado pela vias das pentoses pode ser completamente convertido em intermediários da via glicolítica. A primeira reação da via das pentoses, a desidrogenação da glicose-6-fosfato, é praticamente irreversível. E é essa a reação em que a via das pentoses é controlada. O fator regulatório mais importante é o nível de NADP+, o receptor de elétrons na oxidação da glicose-6-fosfato a 6-fosfogluconolactona. Além disso, NADPH compete com NADP+ pela ligação à enzima. A parte não oxidativa da via das pentoses é controlada principalmente pela disponibilidade de substratos. A via percorrida pela glicose-6-fosfato depende da necessidade celular de NADPH + H+, ribose-5-fosfato e ATP: Quando muito mais ribose-5-fosfato é requerida que NADPH + H+, a maior parte de glicose-6-fosfato é convertida a frutose-6-fostato e gliceraldeído-3-fosfato pela via glicolítica, a transaldolase e a transcetolase convertem esses em ribose-3- fosfato. Quando a necessidade de NADPH + H+ e ribose-5-fosfato estão balanceadas, a reação predominante é a formação de 2 NADPH e uma ribose-5-fosfato de glicose-6-fosfato pela fase oxidativa da via das pentoses. Quando muito mais NADPH + H+ é requerido que ribose-5-fosfato, a glicose-6- fosfato é completamente oxidada a CO2, ou convertida a piruvato. Estudo dirigido 1.Mostre a parte oxidativa do ciclo das pentoses com as equações das reações envolvidas, indicando os agentes oxidantes e a origem do carbono presente no CO2 liberado. 2.Compare NADH e NADPH, indicando suas funções no metabolismo de carboidratos. Explique porque a via da pentose-fosfato é muito mais ativa no tecido adiposo que no músculo. 3.Quando há necessidade de NADPH, o ciclo das pentoses pode funcionar dando um resultado líquido que equivale à oxidação total de glicose a CO2. Explique este processo através das respectivas reações estequiometricamente equilibradas. 4. Ribose 5-fosfato pode ser obtida para a síntese de nucleotídeos através da via das pentoses, com ou sem oxidação da glicose. Mostre como isso é possível com as respectivas equações químicas.
10 5.Explique como a via da pentose fosfato é controlada, tendo em vista que grande parte das reações dessa via é reversível. 6.Compare as reações catalisadas por transaldolases e transcetolases, indicando reagentes, produtos e a natureza das reações. M5 Metabolismo de ácidos graxos Biosíntese de ácidos graxos Conceitos Básicos 1. Na síntese de ácidos graxos, a acetil-coa mitocondrial é translocada ao citosol via sistema de transporte de tricarboxilato e ativada a malonil-coa pela ação de acetil- CoA-carboxilase. 2. Uma série de atividades enzimáticas, que em mamíferos estão contidas em uma enzima homodimérica multifuncional, estende cadeias acil-acp (ACP é o grupo carreador de acila) em dois carbonos por vez. Um grupo acila ligado à enzima e uma malonil-coa condensam-se para formar um intermediário -cetoacil e CO2. Duas reduções e uma desidratação fornecem uma acil-acp em uma série de reações similares ao reverso da -oxidação, mas são catalisadas por enzimas distintas no citosol. O palmitato (C16), o produto normal da biossíntese de ácidos graxos, é sintetizado em sete desses ciclos de reações, sendo, então, hidrolisados da ACP por uma tioeterase. 3. As rotas opostas de degradação e síntese de ácidos graxos são reguladas por hormônios. O glucagon e a epinefrina ativam a lípase sensível a hormônio no tecido adiposo, aumentando o suprimento de substrato para a acil-coa-carboxilase. A insulina tem o efeito oposto. Os hormônios também regulam os níveis de acetil- CoA-carboxilase e do ácido graxo sintase controlando a taxa de biosíntese dessas enzimas. Estudo dirigido Síntese de ácidos graxos 01. Relacionar o nível de citrato com o nível de ATP na mitocôndria. 02. Esquematizar a reação catalisada pela citrato liase. 03. Esquematizar as reações que permitem a transferência de acetil-coa da mitocôndria para o citossol, mostrando a regeneração do oxaloacetato mitocondrial, com participação da enzima málica. 04. Escrever a reação catalisada pela acetil-coa carboxilase. Citar as coenzimas envolvidas na reação e os efetuadores alostéricos dessa enzima. 05. Citar as proteínas componentes do complexo multienzimático de síntese de ácidos graxos. 06. Definir ACP e comparar sua função com a da coenzima A. 07. Analisar as reações que levam à formação de um ácido graxo a partir de acetil-coa e malonil-coa no complexo multienzimático. 08. Citar o agente redutor na biossíntese de ácidos graxos e as suas fontes. 09. Indicar a localização celular da biossíntese de ácidos graxos.
11 10. Citar tecidos onde ocorre essa biossíntese. 11. Indicar o composto presente nos depósitos do tecido adiposo e as reações que levam à sua síntese. 12. Esquematizar a via de síntese do glicerol-fosfato, precursor de triacilgliceróis. 13. Definir ácido graxo essencial. Citar exemplos indicando o número de insaturações. 14. Escrever a estrutura química dos corpos cetônicos, o órgão e as condições que determinam sua síntese. 15. Analisar as reações que levam à sua produção. 16. Esquematizar as reações que permitem o aproveitamento dos corpos cetônicos. Citar os tecidos onde ocorrem essas reações. 17. Indicar as condições metabólicas que levam a um aumento na produção de corpos cetônicos. 18. Citar as consequências de uma produção excessiva de corpos cetônicos. 19. Descrever as alterações metabólicas decorrentes da falta de insulina (diabetes). 20. Citar o precursor básico e as coenzimas necessárias para a síntese de colesterol. Analisar a regulação desta via. 21. Citar compostos derivados do colesterol. 22. Verificar a ação do glucagon e adrenalina no metabolismo de triacilgliceróis. 22. A insulina estimula a síntese de triacilgliceróis. Explicar porque. Beta-oxidação de ácidos graxos Conceitos Fundamentais A digestão de triacilgliceróis depende da atividade emulsificante dos ácidos biliares e da ativação de lipases na interface lipídeo-água. Depois de serem absorvidos, os produtos da digestão de lipídeos são arranjados em lipoproteínas para transporte aos tecidos pela corrente sanguínea. Triacilgliceróis são lipídeos formados pela esterificação dos ácidos graxos pelo glicerol, são muito abundantes na dieta e constituem a forma de armazenamento de todo o excesso de nutrientes. A vantagem de se armazenar lipídeos (na forma de triacilgliceróis) ao invés de carboidratos é que a oxidação de lípides tem um rendimento energético muito maior. Os ácidos graxos são liberados dos triacilgliceróis nos seus sítios de armazenamento no tecido adiposo pela triacilglicerol-lipase sensível a hormônio, e são carregados pelo sangue aos seus sítios de oxidação complexados com albumina. A oxidação de ácidos graxos é a principal fonte de energia liberada na degradação de lipídeos. Depois da ativação no citossol, essa degradação tem lugar na matriz mitocondrial através de um processo chamado -oxidação ou ciclo de Lynen. A oxidação de ácidos graxos inicia-se com a ação da enzima acil-coa sintetase que transformam ácidos graxos em acil-coa. Como a membrana interna da mitocôndria é impermeável a esta molécula, os radicais acila dos ácidos graxos são ligados à carnitina e desta forma transportados para a mitocôndria. Neste processo, unidades de dois carbonos são sucessivamente removidas a partir do terminal carboxílico do ácido graxo para produzir acetil-coa. A -oxidação ocorre em quatro reações: (1) formação de uma ligação dupla, ; (2) hidratação da ligação dupla; (3) desidrogenação para formar uma -
12 cetoacil-coa; (4) tiólise pela CoA para produzir acetil-coa e uma acil-coa encurtada em dois carbonos. Esse processo é repetido até que os ácidos graxos com número par de carbonos sejam convertidos em acetil-coa e uma molécula de propionil-coa. A acetil-coa é oxidada pelo ciclo de Krebs e pela fosforilação oxidativa para geração de ATP. Propionil-CoA é convertida em succinil-coa, um intermediário do ciclo de Krebs. A oxidação de ácidos graxos insaturados requer uma isomerase para converter as ligações duplas 3 para ligações duplas 2 e uma redutase para remover ligações duplas 4. A oxidação de ácidos graxos de cadeia ímpar fornece propionil-coa, que é convertida em succinil-coa através da rota dependente de cobalamina (B 12 ). Os ácidos graxos de cadeia muito longa são parcialmente oxidados por um sistema de três enzimas nos peroxissomas. O fígado utiliza o excesso de acetil-coa para sintetizar acetoacetato e - hidroxibutirato, que são liberados na circulação sanguínea. Os tecidos que usam estes corpos cetônicos como combustível os convertem de volta em acetil-coa. A degradação de triacilgliceróis é estimulada por glucagon e adrenalina e inibida por insulina. Estudo dirigido 1. Esquematizar a reação catalisada por lipases de tecido adiposo. 2. Esquematizar as reações de conversão de glicerol a compostos intermediários da via glicolítica. 3. Esquematizar o primeiro passo necessário para a degradação de um ácido graxo (ativação). 4. Indicar o papel da carnitina na oxidação dos ácidos graxos. 5. Citar os compostos formados no fim de cada volta do ciclo de Lynen. 6. Citar as enzimas envolvidas na -oxidação. 7. Citar as vitaminas que participam do ciclo de Lynen. 8. Quantas moléculas de ATP são necessárias para degradar uma molécula de ácido graxo? 9. Indicar a reação irreversível do ciclo de Lynen e a enzima que catalisa essa reação. 10. Citar a localização celular da beta-oxidação. Explicar a origem da denominação beta-oxidação para a via de degradação de ácidos graxos. 11. Citar os tecidos que não oxidam ácidos graxos. 12. Escrever a equação geral da beta-oxidação do derivado acila do ácido palmítico a acetil-coa. M6 CICLO DE KREBS Conceitos Fundamentais O ciclo de Krebs é a via metabólica final comum para a oxidação de carboidratos, lipídeos e proteínas. Ocorre na membrana interna da mitocôndria e é conhecido também como Ciclo do Ácido Cítrico.
13 As reações do ciclo de Krebs estão relacionadas à cadeia de transporte de elétrons e a fosforilação oxidativa, que conduzem ao oxigênio. Os receptores de elétrons nas reações de oxidação são o NAD + e o FAD. As oito enzimas do ciclo de Krebs funcionam em ciclo catalítico de múltiplas etapas, promovendo a oxidação um grupo acetil-coa a duas moléculas de CO 2, com geração concomitante de três NADH, um FADH 2 e um GTP. A energia livre sintetizar ATP. Os grupos acetila entram no ciclo como acetil-coa. O complexo multienzimático da piruvato-desidrogenase, que contém três enzimas e cinco coenzimas, produz acetil- CoA a partir do piruvato. A citrato sintase catalisa a condensação da acetil-coa e do oxaloacetato em uma reação altamente exergônica. A aconitase catalisa a isomerização do citrato a isocitrato, e a isocitratodesidrogenase catalisa a descarboxilação oxidativa do isocitrato a -cetoglutarato e produz o primeiro CO 2 e NADH do ciclo de Krebs. A -cetoglutarato desidrogenase catalisa a descarboxilação oxidativa do - cetoglutarato, produzindo succinil-coa e a segunda molécula de CO 2 e NADH do ciclo. A succinil-coa sintetase acopla a clivagem da succinil-coa à síntese da GTP. No ciclo de Krebs ocorrem ainda mais três reações catalisadas pela succinatodesidrogenase (succinato fumarato), pela fumarase (fumarato malato) e pela malato desidrogenase (malato oxaloacetato), que regeneram o oxaloacetato para a continuação do ciclo. A entrada de acetil-coa no ciclo de Krebs é regulada pela carga energética da célula, pois o ATP funciona como efetuador alostérico negativo do complexo piruvato desidrogenase na etapa de conversão de piruvato a acetil-coa. O ciclo de Krebs é regulado fundamentalmente pela carga energética da célula uma vez que o ATP é efetuador alostérico negativo das enzimas citrato sintase e isocitrato desidrogenase NAD + -dependente e -cetoglutarato desidrogenase. Além disso, ocorre ainda regulação pela disponibilidade de substrato, inibição pelo produto e inibição por retroalimentação. O ciclo do glioxilato, que ocorre apenas em plantas e em algumas bactérias, necessita de duas enzimas para ocorrer, a isocitrato liase e a malato sintase. Essa variação no ciclo de Krebs permite a síntese de glicose a partir da acetil-coa. Estudo dirigido 1. Descreva as cinco reações do complexo multienzimático da piruvato-desidrogenase. 2. Desenhe a estrutura dos oito intermediários do ciclo de Krebs e o nome das enzimas que catalisam as suas interconversões. Consultar em livros de Bioquímica o valor da variação de energia livre de cada reação em condições padrão. 3. Citar as funções do Ciclo de Krebs. 4. Citar as vitaminas que participam do Ciclo de Krebs. 5. Indicar a localização celular do Ciclo de Krebs. 6. A isomerização do citrato a cis-aconitato possui variação de energia livre em condições padrão positiva. Discutir as implicações da inibição do ciclo por alta carga energética quanto ao deslocamento dessa reação de isomerização. 7. Escreva a equação resultante da soma de todas as reações de: 1)glicose a CO 2 ; 2) glicose a piruvato; 3) piruvato a acetilcoa; 4) acetilcoa a CO 2.
14 8. Compare a energética de reações do ciclo de Krebs envolvendo FAD ou NAD Na oxidação de uma molécula de acetil-coa no Ciclo de Krebs, indicar a enzima que catalisa a reação onde há produção ou consumo de: a) CO 2, b) GTP, c) NADH, d) FADH 2, e) H 2 O. REGULAÇÃO DO CICLO DE KREBS O controle do ciclo de Krebs é exercido em três pontos, ou seja, três enzimas do ciclo exercem papel regulatório. Os pontos de controle são as reações catalisadas pela citrato sintase, pela isocitrato desidrogenase e pelo complexo -cetoglutarato desidrogenase. A citrato sintase é uma enzima inibida por ATP, NADH e succinil-coa. Há também inibição pelo produto, neste caso, o citrato. ADP e NAD + são ativadores alostéricos da isocitrato desidrogenase; ATP e NADH são inibidores. O complexo -cetoglutarato desidrogenase é inibido por ATP e por NADH e ativado por ADP e NAD +. Células em estado metabólico de repouso necessitam e usam pouca energia; alto nível de ATP, baixo nível de ADP (ATP/ADP alto); alto nível de NADH e baixo nível de NAD + (alto NADH/NAD + ). Células em estado metabólico ativo necessitam e usam mais energia do que células em repouso; baixo nível de ATP e alto nível de ADP (ATP/ADP baixo); baixo nível de NADH, alto nível de NAD + (NADH/NAD + baixo). Estudo dirigido 1. Determinar o sentido das reações do ciclo de Krebs e verificar G destas reações. 2. De que modo um aumento na relação ADP/ATP influencia a atividade da isocitrato desidrogenase? 3. Você esperaria que o ciclo de Krebs fosse mais ou menos ativo quando uma célula tem uma relação de ATP/ADP e de NADH/NAD + alta? Justifique. M7 CADEIA RESPIRATÓRIA e FOSFORILAÇÃO OXIDATIVA Conceitos Fundamentais Todas as coenzimas reduzidas obtidas pelo catabolismo são reoxidadas graças à cadeia de transporte de elétrons. Então, as moléculas de NADH e FADH 2, em uma série de reações, transferem os elétrons para o oxigênio, sendo este o aceptor final. Essas reações ocorrem na cadeia transportadora de elétrons, cuja localização é a membrana mitocondrial interna.
15 A cadeia de transporte de elétrons corresponde a uma organização estratégica de biomoléculas na membrana mitocondrial interna dispostas segundo seu potencial de óxido-redução. O transporte de elétrons das coenzimas até o O 2 requer quatro complexos ligados à membrana. São eles: complexo I (NADH-CoQ oxidoredutase); complexo II (succinato-coq oxidoredutase); complexo III (CoQH 2 - citocromo c oxidoredutase e complexo IV (citocromo c oxidase). A operação da cadeia transportadora de elétrons conduz ao bombeamento de prótons (íons hidrogênio), criando um gradiente de ph (também chamado de gradiente de prótons) entre o espaço intermembranas mitocondriais e a matriz mitocondrial. O gradiente de prótons é dissipado através de um canal que existe na ATPsintase da membrana mitocondrial interna. Essa variação de energia potencial é convertida parcialmente em energia de ligação química da molécula de ATP que é sintetizada por essa mesma enzima. Em resumo, a energia liberada pela oxidação dos nutrientes é usada pelos organismos sob a forma de energia química contida no ATP. A produção de ATP na mitocôndria é o resultado da fosforilação oxidativa, no qual o ADP é fosforilado obtendo-se ATP. A cadeia transportadora de elétrons e a fosforilação oxidativa são processos acoplados. O acoplamento quimiosmótico é o mecanismo mais amplamente utilizado para explicar o modo pelo qual o transporte de elétrons e a fosforilação oxidativa estão acoplados. A maneira pela qual o gradiente de prótons leva à produção de ATP depende de canais iônicos, que atravessam a membrana mitocondrial interna; esses canais são uma característica estrutural da ATP-sintase. A síntese de ATP depende da cadeia transportadora de elétrons. O fluxo de elétrons só ocorre enquanto houver a síntese de ATP. A oxidação dos substratos é impedida sempre que a concentração de ATP tem níveis compatíveis com a demanda. A velocidade de produção de ATP é determinada pela concentração de ADP e P i, substratos da ATP-sintase. A síntese de ATP processa-se em velocidade paralela à sua oxidação. Estudo dirigido 1. Citar os compostos que fazem parte da cadeia de transporte de elétrons e caracterizá-los quimicamente. 2. Esquematizar a seqüência dos compostos da cadeia de transporte de elétrons, indicando os transportadores de elétrons e os transportadores de prótons e elétrons.
16 3. Citar a localização celular da cadeia de transporte de elétrons. 4. Citar 3 inibidores da cadeia de transporte de elétrons, indicando os transportadores sobre os quais atuam. 5. Verificar se é possível a oxidação de malato e de succinato em presença de rotenona. 6. Qual seria o estado de oxidação (oxidado/reduzido) dos componentes da cadeia de transporte de elétrons em presença de malato e de antimicina A? 7. Definir fosforilação oxidativa. 8. Descrever a hipótese do acoplamento quimiosmótico para a fosforilação oxidativa. 9. Indicar o número de ATP sintetizados para cada NADH e FADH 2 oxidados. Citar exemplos de processos biológicos que utilizam ATP. 10. Definir desacoplador e citar um exemplo. 11. Definir inibidor de fosforilação oxidativa e citar um exemplo. 12. Definir controle respiratório. a) Definir fosforilação ao nível do substrato e citar as reações onde ocorre esta fosforilação. 13. Dinitrofenol acelera o consumo de oxigênio pela cadeia de transporte de elétrons. Justifique. 14. Citar as conseqüências dos seguintes fatores para o funcionamento da cadeia de transporte de elétrons e da fosforilação oxidativa: a) presença de CN - ou CO b) carência de P i c) carência de ADP d) presença de DNP (dinitrofenol) e) carência de P i e/ou ADP em presença de DNP f) presença de oligomicina g) presença de oligomicina + DNP 15. Calcular o saldo de ATP formado na oxidação total de glicose.qual o destino da energia não armazenada sob a forma de ATP? Qual seria o resultado na presença de dinitrofenol? M8 METABOLISMO DO GLICOGÊNIO E SUA REGULAÇÃO Conceitos Fundamentais O glicogênio é um polissacarídeo de glicose que funciona como forma de reserva de energia em animais e microrganismos. Em animais, o glicogênio está depositado no fígado, um órgão central de reserva de energia, e, também, nos músculos, onde é degradado localmente. O glicogênio hepático é exportado para manter a glicemia. A natureza polimérica e semi-solúvel do glicogênio constitui-se numa maneira perfeita de armazenar energia na forma de glicose. O estoque de glicogênio do fígado na forma de glicose causaria tamanha pressão osmótica, que a viabilidade do hepatócito seria impossível. O glicogênio é um polímero de -D-glico-piranose altamente ramificado. Na cadeia os monômeros são interligados por ligações glicosídicas (14); nos pontos de ramificação a ligação também é glicosídica, mas (16). A glicose, na forma de glicose-1-p, é liberada da reserva de glicogênio pela fosforólise da ligação (14) da extremidade não redutora do polímero. Esta reação é catalisada pela glicogênio fosforilase.
17 A glicogênio fosforilase degrada até restarem 4 resíduos antes de uma ramificação até que a enzima desramificadora transfere 3 dos 4 resíduos para outra extremidade da cadeia de glicogênio formando uma nova ligação (14). O resíduo restante está ligado a cadeia pela ligação (16) que é hidrolisada pela enzima desramificadora através de sua atividade (16) glicosidase. Glicose-1-fosfato é convertida a glicose-6-fosfato pela fosfoglicomutase, esta pode ser liberada pela circulação no fígado pela ação da glicose-6-fosfatase ou degradada pelo músculo. A síntese do glicogênio se dá através de via uma diferente da de degradação. A glicose-1-p é primeiro ativada à uridinadifosfato-glicose, ou simplesmente UDP-G. UDP-G é o substrato da glicogênio sintase que catalisa a adição de um resíduo de glicose ao carbono 4 da glicose de uma extremidade não redutora do glicogênio, liberando ainda como produto UDP. Esta reação necessita de cadeias glicogênicas pré-existentes que funcionam como PRIMER da reação, oferecendo extremidades não redutoras para reagir com UDP-G. Gli 6-P Glicose 1-P Gli 1-P + UTP UDP-Gli + PP I (1-fosfato uridil transferase) UDP-Gli + glicogênio (n) UDP + glicogênio (n + 1) O UDP é convertido a UTP às custas da utilização de ATP: PP I + H 2 O 2 P I (pirofosfatase) UDP + ATP UTP + ATP (nucleosídeo difosfato quinase) A glicogênio fosforilase e glicogênio sintase formam um ciclo que, respectivamente, libera e deposita glicose-1-p a partir do estoque de glicogênio: Glicose-1P UTP + H 2 O UDPG 2 P i Glicogênio n Fosforilase Sintase I P i Glicogênio n+1 UDP É fácil notar que se estas enzimas funcionarem concomitantemente o ciclo será fútil, cujo único resultado líquido será dissipação de energia através da reação: UTP + H 2 O UDP + P i Conclui-se que, necessariamente, no hepatócito estas enzimas são coordenadamente reguladas, isto é, quando a fosforilase é ativada para mobilizar glicose-1-p, a sintase é desativada, e viceversa, conforme a necessidade celular. Ambas fosforilase e sintase são reguladas por fosforilação (modificação covalente) em resíduos específicos de serina, reações catalisadas pela mesma proteína-quinase que possui dupla especificidade, sendo por isso chamada de sintase-fosforilase quinase. A fosforilase e a sintase são espécies fosforiladas, portanto a fosforilação, catalisada pela sintase-fosforilase quinase, causa ativação da fosforilase e inativação da sintase. A fosforilase a e a sintase I (formas ativas), por um lado, e a fosforilase b e a sintase D (formas não ativas), por outro, são, respectivamente interconversíveis. Para tanto é necessário que fosforilase a e a sintase I sejam desfosforiladas, através de uma reação que requer catálise. A principal enzima, catalisadora comum destas desfosforilações, é a fosfoproteína fosfatase 1. Hormônios específicos regulam a síntese e a degradação de glicogênio no músculo e no fígado. A adrenalina aumenta degradação no músculo enquanto que o glucagon faz o mesmo no fígado. A insulina aumenta a síntese de glicogênio tanto no músculo quanto no fígado. Os hormônios mencionados são hidrosolúveis e atuam via segundo mensageiro com ativação da adenilato ciclase e formação de AMP-cíclico. Isso porque os hormônios não conseguem penetrar no interior das células. A degradação e a síntese de glicogênio possuem regulação recíproca, ou seja, quando a degradação está ativada, a síntese está inibida. Essa regulação é feita através dos hormônios e de
18 fosforilações estratégicas que culminam na fosforilação final da fosforilase com sua ativação e na fosforilação final da sintetase com sua inibição. A liberação de Ca 2+ no músculo juntamente com a regulação hormonal são responsáveis pela degradação de glicogênio no músculo. Estudo dirigido 1. Definir polissacarídeo. Citar exemplos de polissacarídeos estruturais e de reserva. 2. Descrever a estrutura do glicogênio. 3. Esquematizar as reações de degradação do glicogênio a glicose 1-fosfato. 4. Citar os hormônios que estimulam a degradação do glicogênio no fígado e no músculo e mostrar seu modo de ação. 5. Esquematizar as reações de síntese do glicogênio a partir de glicose. 6. Esquematizar as reações de conversão de glicose 1-fosfato a glicose. Citar os tecidos onde estas reações ocorrem. 7. Esquematizar as reações de síntese de glicogênio a partir de glicose. 8. Mostrar a relação entre AMP cíclico e a síntese de glicogênio. 9. Descrever a ação de insulina sobre o metabolismo de carboidratos quanto à: a) permeabilidade da célula à glicose. b) síntese de glicogênio. c) síntese de glicoquinase (fígado). 10. Citar a função do glicogênio hepático e do glicogênio muscular. 11. Indicar os efeitos da adrenalina e insulina no músculo sobre o metabolismo do glicogênio muscular. Idem para o glucagon e insulina no fígado. M9 Metabolismo de aminoácidos DEGRADAÇÃO DE PROTEÍNAS E AMINOÁCIDOS/ CICLO DA URÉIA Conceitos fundamentais As proteínas intracelulares são degradadas por proteínas lisossomais ou, após serem ubiquitinizadas, pela ação de proteossomos. A degradação de um aminoácido quase sempre se inicia com a remoção de seu grupo amino em uma reação de transaminação que consiste na transferência de um grupo amino para um alfa-cetoácido. Por desaminação oxidativa envolvendo NAD +, o grupo amino transferido é convertido em íon amônio. Ocorre ainda a transformação dos esqueletos de C em intermediários da glicólise e do ciclo de Krebs. Duas reações principais permitem a eliminação do amino grupo. Diversos aminoácidos podem transferir o grupo amino para o alfa-cetoglutarato numa reação catalisada por transaminases: aspartato + alfa-cetoglutarato oxalacetato + glutamato Por outro lado, glutamina e glutamato podem ser desaminados em reações catalisadas pela glutaminase e desidrogenase glutâmica, respectivamente: + glutamina + H 2 O glutamato + NH 4 glutamato + NAD + (ou NADP + ) + H 2 O NH alfa-cetoglutarato + NADH (ou NADPH) + H + O cátion amônio é tóxico, sendo utilizado para a síntese de glutamina ou convertido em uréia no ciclo correspondente, para fins de excreção. O grupo prostético das transaminases é a vitamina B6 (piridoxina) na forma de piridoxal fosfato ou PLP.
19 No ciclo da uréia, um átomo de nitrogênio desse íon amônio (um produto da desaminação oxidativa de glutamato) e um átomo de nitrogênio do aspartato combinam-se com HCO - 3 para formar uréia para a excreção. O passo limitante da velocidade desse processo é catalisado pela carbamoil-fosfato-sintetase. Os 20 aminoácidos-padrão são degradados para formar: 1) compostos intermediários da glicólise, 2) corpos cetônicos, 3) ácidos graxos. Exemplos de compostos formados pela degradação: piruvato, -cetoglutarato, succinil-coa, fumarato, oxaloacetato, acetil-coa ou acetoacetato. Aminoácidos como alanina, aspartato e glutamato são ditos glicogênicos porque podem ser convertidos em, respectivamente, piruvato, oxalacetato e alfacetoglutarato, que, por sua vez, podem ser transformados em fosfoenolpiruvato para síntese de glicose. Já os aminoácidos leucina e lisina são chamados cetogênicos por produzirem exclusivamente acetil-coa como produto de degradação, portanto servindo à síntese de corpos cetônicos, mas não de glicose. Ciclo da Uréia Estudo dirigido 1. Escrever as três reações que levam à desaminação de um alfa-aminoácido com formação do íon amônio. Incluir as enzimas envolvidas. 2. Comente sobre o papel essencial das vitaminas no metabolismo. Escreva a estrutura química da vitamina B6 e do piridoxal fosfato.
20 3. Explique por que a degradação de proteínas pelo proteossomos requer ATP, apesar da proteólise ser um processo exergônico. 4. Explique por que uma alta concentração de amônia diminui a taxa do ciclo de Krebs. 5. Quais dos 20 aminoácidos-padrão são (a) puramente glicogênicos, (b) puramente cetogênicos e (c) tanto glicogênicos como cetogênicos? 6. Desenhe o ciclo da uréia e escreva a reação geral do ciclo. 7. Faça um esquema geral mostrando os destinos dos esqueletos de carbono dos aminoácidos glicogênicos e cetogênicos. 8. Analisar o destino da cadeia carbônica dos aminoácidos e o balanço de nitrogênio que ocorrem com as seguintes dietas: a) normal em carboidratos, lipídios e proteínas b) rica em proteínas e normal nos demais componentes c) pobre em carboidratos e normal nos demais componentes d) pobre em proteínas e normal nos demais componentes BIOSSÍNTESE DE AMINOÁCIDOS Conceitos fundamentais Os gases mais abundantes no ar atmosférico, O 2 e N 2, são essenciais para a existência da vida biológica no planeta Terra, mas divergem quanto à reatividade química. O O 2 tem propriedades de radical livre reagindo com relativa facilidade, daí servir muito bem como oxidante final na respiração de todos os organismos. Já o N 2 possui uma tripla ligação altamente estável que lhe confere baixíssima reatividade química. Apesar disso, o N 2 gasoso da atmosfera é a fonte do elemento N que garante a vida na Terra. Por essas razões físico-químicas a redução do N 2 atmosférico pelos sistemas biológicos tem características muito peculiares. A redução química do N 2 a NH 3 exige condições drásticas, 500 graus Celsius de temperatura e 300 atm de pressão, certamente incompatíveis com a vida biológica. Mas bactérias especializadas do gênero Rhyzobium, que são simbiontes de plantas leguminosas, reduzem eficientemente N 2 a NH + 4, uma espécie química totalmente compatível com o metabolismo de todos os organismos. Portanto, o N 2 fixado por essa simbiose entre planta e bactéria garante a disponibilidade do elemento N para todas as formas de vida terrestre. As bactérias fixadoras de N 2 possuem um complexo enzimático singular, a nitrogenase. A reação de redução do N 2 a NH + 4 (fixação de nitrogênio), qual envolve um redutor poderoso a grande investimento de energia na forma de ATP, é catalisado pela nitrogenase, qual usa NADPH + H + como doador de elétrons: N H e ATP + 16 H 2 O 2 NH 3 + H ADP +16 P i A volatilidade do NH + 4 (NH 3 + H + ) não favorece sua permanência no solo, mas existem bactérias autotróficas de vida livre, muito abundantes e largamente disseminadas, que são especializadas na oxidação do cátion amônio a nitrito e nitrato para fins de obtenção de energia metabólica. Desta maneira o elemento N é estavelmente depositado no solo na forma de espécies químicas, sais de nitrito e nitrato, que são eficientemente absorvidas pelas raízes das plantas e prontamente reduzidas a NH + 4 no interior da célula vegetal.
21 As etapas sumariamente mencionadas compreendem o ciclo do nitrogênio na natureza: a) redução do N 2 a NH + 4 ; b) oxidação de NH + 4 a nitrito e nitrato; c) redução de nitrito e nitrato a NH + 4 e d) transformação do elemento N de inorgânico para orgânico com a síntese de aminoácidos a partir de NH + 4, reação possível em todas a formas de organismos biológicos. Em animais, o N do grupo amino dos aminoácidos é eficientemente obtido a partir de NH + 4 pelas reações catalisadas pelas enzimas desidrogenase glutâmica e glutamina sintetase, fornecendo, respectivamente, glutamato e glutamina. Ainda em animais de forma geral, os aminoácidos alanina e aspartato podem ser obtidos a partir de, respectivamente, piruvato e oxalacetato, através da reação de transaminação tendo glutamato como doador de grupo amino. Outros aminoácidos exigem reações adicionais, além da transaminação para sua síntese final. Mas, como regra, os esqueletos de C dos aminoácidos são obtidos a partir dos intermediários da glicólise, do ciclo de Krebs e do ciclo das pentoses. Há, no entanto, aminoácidos que não podem ser sintetizados por animais devido a falta do precursor que fornece o esqueleto de C. Estes são ditos aminoácidos essenciais e tem que ser obtidos na dieta. Por exemplo, humanos tem que conseguir da dieta 9 aminoácidos essenciais. Estudo Dirigido 1. Defina fixação do nitrogênio. 2. Equacione a reação da nitrogenase e mostre aonde ocorre. 3. Definir aminoácido essencial e citar os aminoácidos essenciais para o organismo humano. 4. Qual a importância dos aminoácidos para os organismos? 5. Verificar por que a glutamina e o glutamato são doadores de nitrogênio para a síntese de aminoácidos M10 INTEGRAÇÃO METABÓLICA E REGULAÇÃO HORMONAL DO METABOLISMO Conceitos Fundamentais A regulação metabólica é feita de interferência direta de determinadas reações químicas que compõem o metabolismo, aumentando ou reduzindo sua velocidade. O resultado direto deste processo é a maior oferta de substratos ou acúmulo de metabólitos que acabará por influenciar outras vidas dependentes destes compostos e a forma mais eficiente de regulação desta rede é aumentar a concentração ou alterar a eficiência da enzima. Pode se controlar a síntese ou degradação enzimática; também se pode modular a atividade enzimática através de mudanças conformacionais da própria enzima provocada através da ligação de compostos ou grupos na cadeia peptídica: regulação alostérica e regulação por modificação covalente. A concentração enzimática também pode variar conforme a oferta do substrato; alteração mediada através de hormônios. Os hormônios estão envolvidos no metabolismo em dois níveis: indução ou repressão gênica de determinadas enzimas ou através da modificação covalente: A fosforilação é mediada pelas proteínas quinases que transferem o grupo
22 fosfato do ATP para resíduos específicos de serina, treonina e tirosina, formando uma ligação éster fosfórico ou a retirada do grupo fosfato é catalisada pela ação de fosfoproteínas fosfatases através da hidrólise. Os hormônios transmitem sinais regulatórios para os tecidos-alvo por meio da ligação a receptores que traduz o sinal em respostas no interior da célula. A insulina e o glucagon pancreáticos e a adrenalina e noradrenalina da medula adrenal são os principais hormônios envolvidos no metabolismo energético dos mamíferos. Dois hormônios são os principais responsáveis pelo equilíbrio da concentração da glicose circulante: Glucagon e insulina. O glucagon é um hormônio que tem efeitos equivalentes ao da adrenalina no controle do metabolismo do glicogênio: possui um receptor da família dos receptores acoplados a proteína-g e ativa a cascata que se inicia com camp/pka. Este é liberado em condições de hipoglicemia ativando processos degradativos para manutenção da glicemia sanguínea. A PKA (proteína quinase ativada por camp) fosforila a fosforilase quinase tornando-a ativa. A fosforilase quinase fosforila agora glicogênio fosforilase. A glicogênio fosforilase ativada (quando fosforilada, glicogênio fosforilase b a) catalisa a hidrólise de resíduos de glicose do glicogênio liberando grupos de glicose-1-fosfato. No mesmo tempo, a fosforilase quinase, ativada pela cascata do receptor de glucagon-proteína-g, camp/pka, fosforila a glicogênio síntase, a qual se torna inativa quando fosforilada (síntase I sintase D). A insulina tem efeito oposto, promove a absorção de glicose pelo fígado e músculos e usa deposição nas reservas de glicogênio. Mas é importante notar que a insulina tem mecanismos de ação totalmente diferentes da adrenalina e do glucagon. Os receptores de insulina não pertencem à família dos receptores acoplados a proteína-g e não têm ação sobre a adenilato ciclase. Seus receptores são do grupo de receptores cujo domínio intracelular apresenta atividade intrínseca de proteína-quinase de tirosina. A insulina estimula fosfoproteínas fosfatases. Para reverter a ação do glucagon, a insulina promove a ativação da fosfoproteína fosfatase que catalisa a desfosforilação da glicogênio fosforilase e da glicogênio sintase, levando a inativação da primeira (fosforilase a b) e ativação da segunda (síntase D sintase I). Desta forma o fluxo glicoseglicogênio é favorecido. O transporte da glicose no interior das células com a atuação da insulina é um processo passivo mediado por uma família de permeases denominadas GLUT (glicose transporter). Respostas celulares rápidas desencadeadas por hormônios só podem ser obtidas através da ativação, ou da inibição, de enzimas pré-existentes. Hormônios esteróides (por exemplo, cortisol) quando secretados difundem-se pela membrana citoplasmática e ligam-se ao seus receptores intracelulares os quais, quando ativados, promovem no núcleo a regulação do metabolismo pela indução da transcrição de genes que codificam enzimas específicas, levando à síntese de novo das proteínas correspondentes, fenômeno conhecido como indução enzimática. Mas o mecanismo de indução enzimática desencadeado por hormônios resulta necessariamente numa resposta celular lenta, uma vez que os RNAs mensageiros (mrnas) precisam ser transcritos, processados, transportados para o citoplasma e finalmente traduzidos para produzir as proteínas enzimáticas exigidas. A adrenalina estimula uma resposta local no músculo. A liberação de adrenalina é induzida por estímulo nervoso autônomo em situações de perigo, exercício
MANUAL DA DISCIPLINA DE BIOQUÍMICA CURSO DE FISIOTERAPIA
 MANUAL DA DISCIPLINA DE BIOQUÍMICA CURSO DE FISIOTERAPIA 2017 MÓDULO 2 METABOLISMO 1 Introdução ao Metabolismo METABOLISMO Tópicos para estudo (em casa): 1- Dê as principais características do ser vivo.
MANUAL DA DISCIPLINA DE BIOQUÍMICA CURSO DE FISIOTERAPIA 2017 MÓDULO 2 METABOLISMO 1 Introdução ao Metabolismo METABOLISMO Tópicos para estudo (em casa): 1- Dê as principais características do ser vivo.
Acetil CoA e Ciclo de Krebs. Prof. Henning Ulrich
 Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich Glicose + Consumo de 2 ATP 2 Ácidos Pirúvicos + 4H + + Produção de 4 ATP (2C 3 H 4 O 3 ) 2H + são Transportados pelo NAD passando Para o estado reduzido
Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich Glicose + Consumo de 2 ATP 2 Ácidos Pirúvicos + 4H + + Produção de 4 ATP (2C 3 H 4 O 3 ) 2H + são Transportados pelo NAD passando Para o estado reduzido
Profª Eleonora Slide de aula. Metabolismo de Carboidratos
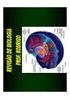 Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose 2 Etanol + 2 CO 2 Condições
Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose 2 Etanol + 2 CO 2 Condições
Funções do Metabolismo
 Universidade Federal de Mato Grosso Disciplina de Bioquímica Conceito de Metabolismo METABOLISMO DOS CARBOIDRATOS Prof. Msc. Reginaldo Vicente Ribeiro Atividade celular altamente dirigida e coordenada,
Universidade Federal de Mato Grosso Disciplina de Bioquímica Conceito de Metabolismo METABOLISMO DOS CARBOIDRATOS Prof. Msc. Reginaldo Vicente Ribeiro Atividade celular altamente dirigida e coordenada,
MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS. Leu Ile Lys Phe. Gly Ala Ser Cys. Fosfoenolpiruvato (3) Piruvato (3)
 Ciclo de Krebs MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Piruvato (3) CO 2 Acetil-CoA (2) CO 2 Oxaloacetato
Ciclo de Krebs MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Piruvato (3) CO 2 Acetil-CoA (2) CO 2 Oxaloacetato
Doenças Metabólicas. Revisão Bioquímica. Bruna Mion
 Doenças Metabólicas Revisão Bioquímica Bruna Mion GLICÓLISE Glicólise GLICOSE Armazenamento Polissacarídeo Sacarose Glicólise Piruvato ATP Intermediários Via das Pentoses Fosfato Ribose 5 fosfato NADPH
Doenças Metabólicas Revisão Bioquímica Bruna Mion GLICÓLISE Glicólise GLICOSE Armazenamento Polissacarídeo Sacarose Glicólise Piruvato ATP Intermediários Via das Pentoses Fosfato Ribose 5 fosfato NADPH
PRINCIPAIS VIAS METABÓLICAS
 PRINCIPAIS VIAS METABÓLICAS DEGRADAÇÃO DO GLIGOGÊNIO GLICÓLISE VIA DAS PENTOSES FOSFATO GLICONEOGÊNESE SÍNTESE DE CORPOS CETÔNICOS DEGRADAÇÃO DE AMINOÁCIDOS E CICLO DA URÉIA CICLO DE KREBS Β-OXIDAÇÃO DE
PRINCIPAIS VIAS METABÓLICAS DEGRADAÇÃO DO GLIGOGÊNIO GLICÓLISE VIA DAS PENTOSES FOSFATO GLICONEOGÊNESE SÍNTESE DE CORPOS CETÔNICOS DEGRADAÇÃO DE AMINOÁCIDOS E CICLO DA URÉIA CICLO DE KREBS Β-OXIDAÇÃO DE
Glicólise. Professora Liza Felicori
 Glicólise Professora Liza Felicori Glicose Glicose (combustível metabólico) Fígado: Serve como tampão para manter o nível de glicose no sangue (liberação controlada de glicose) Glicose GLICOGÊNIO Estoque
Glicólise Professora Liza Felicori Glicose Glicose (combustível metabólico) Fígado: Serve como tampão para manter o nível de glicose no sangue (liberação controlada de glicose) Glicose GLICOGÊNIO Estoque
Corpos cetônicos. Quais são? A partir de qual composto se formam? Como se formam? Quando se formam? Efeitos de corpos cetônicos elevados?
 Corpos cetônicos Quais são? A partir de qual composto se formam? Como se formam? Quando se formam? Efeitos de corpos cetônicos elevados? Importante saber!!!!!!!!!!!! A partir de qual composto se formam?
Corpos cetônicos Quais são? A partir de qual composto se formam? Como se formam? Quando se formam? Efeitos de corpos cetônicos elevados? Importante saber!!!!!!!!!!!! A partir de qual composto se formam?
Gliconeogênese. Gliconeogênese. Órgãos e gliconeogênese. Fontes de Glicose. Gliconeogênese. Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia
 Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia Gliconeogênese Alexandre Havt Gliconeogênese Fontes de Energia para as Células Definição Via anabólica que ocorre no fígado e, excepcionalmente
Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia Gliconeogênese Alexandre Havt Gliconeogênese Fontes de Energia para as Células Definição Via anabólica que ocorre no fígado e, excepcionalmente
BIOSSÍNTESE DE ÁCIDOS GRAXOS E TRIACILGLICERÓIS. Bianca Zingales IQ-USP
 BIOSSÍNTESE DE ÁCIDOS GRAXOS E TRIACILGLICERÓIS Bianca Zingales IQ-USP Importância dos Lipídios 1. A maior fonte de armazenamento de Energia dos mamíferos 2. Componente de todas as membranas biológicas
BIOSSÍNTESE DE ÁCIDOS GRAXOS E TRIACILGLICERÓIS Bianca Zingales IQ-USP Importância dos Lipídios 1. A maior fonte de armazenamento de Energia dos mamíferos 2. Componente de todas as membranas biológicas
FISIOLOGIA VEGETAL 24/10/2012. Respiração. Respiração. Respiração. Substratos para a respiração. Mas o que é respiração?
 Respiração Mas o que é respiração? FISIOLOGIA VEGETAL Respiração É o processo pelo qual compostos orgânicos reduzidos são mobilizados e subsequentemente oxidados de maneira controlada É um processo de
Respiração Mas o que é respiração? FISIOLOGIA VEGETAL Respiração É o processo pelo qual compostos orgânicos reduzidos são mobilizados e subsequentemente oxidados de maneira controlada É um processo de
Universidade Federal do Pampa Campus Itaqui Bioquímica GLICÓLISE AERÓBICA. Ciclo de Krebs e Fosforilação Oxidativa. Profa.
 Universidade Federal do Pampa Campus Itaqui Bioquímica GLICÓLISE AERÓBICA Ciclo de Krebs e Fosforilação Oxidativa Profa. Marina Prigol 1 Glicólise Anaeróbica RESPIRAÇÃO CELULAR ou GLICÓLISE AERÓBICA:
Universidade Federal do Pampa Campus Itaqui Bioquímica GLICÓLISE AERÓBICA Ciclo de Krebs e Fosforilação Oxidativa Profa. Marina Prigol 1 Glicólise Anaeróbica RESPIRAÇÃO CELULAR ou GLICÓLISE AERÓBICA:
METABOLISMO DOS CARBOIDRATOS - GLICÓLISE
 Após a absorção dos carboidratos no intestino, a veia porta hepática fornece glicose ao fígado, que vai para o sangue para suprir as necessidades energéticas das células do organismo. GLICÓLISE principal
Após a absorção dos carboidratos no intestino, a veia porta hepática fornece glicose ao fígado, que vai para o sangue para suprir as necessidades energéticas das células do organismo. GLICÓLISE principal
5/4/2011. Metabolismo. Vias Metabólicas. Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos).
 Metabolismo Vias Metabólicas Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos). 1 Endergônico Exergônico Catabolismo Durante o catabolismo de carboidratos,
Metabolismo Vias Metabólicas Séries de reações consecutivas catalisadas enzimaticamente, que produzem produtos específicos (metabólitos). 1 Endergônico Exergônico Catabolismo Durante o catabolismo de carboidratos,
Ciclo do Ácido Cítrico ou Ciclo de Krebs ou Ciclo dos Ácidos Tricarboxílicos
 Ciclo do Ácido Cítrico ou Ciclo de Krebs ou Ciclo dos Ácidos Tricarboxílicos Vias da Respiração Celular NADH Glicólise NADH 2 Ciclo de Krebs Mitocôndria Cadeia transp. elétrons Glicose Piruvato Citosol
Ciclo do Ácido Cítrico ou Ciclo de Krebs ou Ciclo dos Ácidos Tricarboxílicos Vias da Respiração Celular NADH Glicólise NADH 2 Ciclo de Krebs Mitocôndria Cadeia transp. elétrons Glicose Piruvato Citosol
Ciclo de Krebs ou Ciclo do ácido cítrico. Prof. Liza Felicori
 Ciclo de Krebs ou Ciclo do ácido cítrico Prof. Liza Felicori VISÃO GERAL Em circunstâncias aeróbicas piruvato é descarboxilado CO 2 C4 + C2 C6 C6 C6 C6 C5 CO 2 CO 2 C5 C4 C4 C4 C4 NAD+ & FAD 3 Íons H-
Ciclo de Krebs ou Ciclo do ácido cítrico Prof. Liza Felicori VISÃO GERAL Em circunstâncias aeróbicas piruvato é descarboxilado CO 2 C4 + C2 C6 C6 C6 C6 C5 CO 2 CO 2 C5 C4 C4 C4 C4 NAD+ & FAD 3 Íons H-
BIOSSÍNTESE DE ÁCIDOS GRAXOS E REGULAÇÃO DO METABOLISMO DE GORDURAS
 BIOSSÍNTESE DE ÁCIDOS GRAXOS E REGULAÇÃO DO METABOLISMO DE GORDURAS Se carboidratos, gorduras e proteínas são consumidas em quantidades que excedam as necessidades energéticas, o excesso será armazenado
BIOSSÍNTESE DE ÁCIDOS GRAXOS E REGULAÇÃO DO METABOLISMO DE GORDURAS Se carboidratos, gorduras e proteínas são consumidas em quantidades que excedam as necessidades energéticas, o excesso será armazenado
12/11/2015. Disciplina: Bioquímica Prof. Dr. Vagne Oliveira
 Disciplina: Bioquímica Prof. Dr. Vagne Oliveira 2 1 ATP ADP Glicose (6C) C 6 H 12 O 6 ATP ADP P ~ 6 C ~ P 3 C ~ P 3 C ~ P Pi NAD NADH P ~ 3 C ~ P ADP P ~ 3 C ATP ADP ATP NAD Pi NADH P ~ 3 C ~ P ADP ATP
Disciplina: Bioquímica Prof. Dr. Vagne Oliveira 2 1 ATP ADP Glicose (6C) C 6 H 12 O 6 ATP ADP P ~ 6 C ~ P 3 C ~ P 3 C ~ P Pi NAD NADH P ~ 3 C ~ P ADP P ~ 3 C ATP ADP ATP NAD Pi NADH P ~ 3 C ~ P ADP ATP
METABOLISMO DE CARBOIDRATOS METABOLISMO DOS LIPÍDIOS METABOLISMO DE PROTEÍNAS
 METABOLISMO DE CARBOIDRATOS METABOLISMO DOS LIPÍDIOS METABOLISMO DE PROTEÍNAS METABOLISMO DE CARBOIDRATOS GLICÓLISE Transporte da Glicose para dentro das Células: Glicose não difunde diretamente para
METABOLISMO DE CARBOIDRATOS METABOLISMO DOS LIPÍDIOS METABOLISMO DE PROTEÍNAS METABOLISMO DE CARBOIDRATOS GLICÓLISE Transporte da Glicose para dentro das Células: Glicose não difunde diretamente para
Glicogênese, Glicogenólise e Gliconeogênese. Profa. Alessandra Barone
 Glicogênese, Glicogenólise e Gliconeogênese Profa. Alessandra Barone www.profbio.com.br Polissacarídeo de reserva animal Constituído por moléculas de α-d-glicose ligadas entre si por ligações glicosídicas
Glicogênese, Glicogenólise e Gliconeogênese Profa. Alessandra Barone www.profbio.com.br Polissacarídeo de reserva animal Constituído por moléculas de α-d-glicose ligadas entre si por ligações glicosídicas
QBQ 0204 Bioquímica. Carlos Hotta. Glicólise 13/05/17
 QBQ 0204 Bioquímica Carlos Hotta Glicólise 13/05/17 Uma visão geral do metabolismo Ribose 5P (5) NUCLEOTÍDEOS Algumas reações são irreversíveis Vias de síntese e degradação precisam ser separadas Uma visão
QBQ 0204 Bioquímica Carlos Hotta Glicólise 13/05/17 Uma visão geral do metabolismo Ribose 5P (5) NUCLEOTÍDEOS Algumas reações são irreversíveis Vias de síntese e degradação precisam ser separadas Uma visão
30/05/2017. Metabolismo: soma de todas as transformações químicas que ocorrem em uma célula ou organismo por meio de reações catalisadas por enzimas
 Metabolismo: soma de todas as transformações químicas que ocorrem em uma célula ou organismo por meio de reações catalisadas por enzimas Metabolismo energético: vias metabólicas de fornecimento de energia
Metabolismo: soma de todas as transformações químicas que ocorrem em uma célula ou organismo por meio de reações catalisadas por enzimas Metabolismo energético: vias metabólicas de fornecimento de energia
Aula de Bioquímica II SQM Gliconeogênese Glicogênio: Glicogenólise, Síntese e Regulação
 Aula de Bioquímica II SQM04242015201 Bacharelado em Ciências Físicas e Biomoleculares Temas: Gliconeogênese Glicogênio: Glicogenólise, Síntese e Regulação Prof. Dr. Júlio César Borges Depto. de Química
Aula de Bioquímica II SQM04242015201 Bacharelado em Ciências Físicas e Biomoleculares Temas: Gliconeogênese Glicogênio: Glicogenólise, Síntese e Regulação Prof. Dr. Júlio César Borges Depto. de Química
Corpos cetônicos e Biossíntese de Triacilglicerois
 Corpos cetônicos e Biossíntese de Triacilglicerois Formação de Corpos Cetônicos Precursor: Acetil-CoA Importante saber!!!!!!!!!!!! http://bloglowcarb.blogspot.com.br/2011/06/o-que-acontece-com-os-lipidios.html
Corpos cetônicos e Biossíntese de Triacilglicerois Formação de Corpos Cetônicos Precursor: Acetil-CoA Importante saber!!!!!!!!!!!! http://bloglowcarb.blogspot.com.br/2011/06/o-que-acontece-com-os-lipidios.html
Aula de Bioquímica II SQM Ciclo do Ácido Cítrico
 Aula de Bioquímica II SQM04242015201 Bacharelado em Ciências Físicas e Biomoleculares Tema: Ciclo do Ácido Cítrico Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química
Aula de Bioquímica II SQM04242015201 Bacharelado em Ciências Físicas e Biomoleculares Tema: Ciclo do Ácido Cítrico Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química
26/4/2011. Beta-Oxidação de Ácidos Graxos. Principal fonte de Ácidos Graxos são os TRIGLICÉRIDES
 Beta-Oxidação de Ácidos Graxos Principal fonte de Ácidos Graxos são os TRIGLICÉRIDES 1 TG constituem mais de 90 % dos lipídios da dieta... TG são sintetizados no FÍGADO e estocados no TECIDO ADIPOSO 2
Beta-Oxidação de Ácidos Graxos Principal fonte de Ácidos Graxos são os TRIGLICÉRIDES 1 TG constituem mais de 90 % dos lipídios da dieta... TG são sintetizados no FÍGADO e estocados no TECIDO ADIPOSO 2
1. Produção de Acetil-CoA. 2. Oxidação de Acetil-CoA. 3. Transferência de elétrons e fosforilação oxidativa
 CICLO DE KREBS OU DO ÁCIDO CÍTRICO 1. Produção de Acetil-CoA 2. Oxidação de Acetil-CoA 3. Transferência de elétrons e fosforilação oxidativa CICLO DE KREBS OU DO ÁCIDO CÍTRICO 1. Produção de Acetil-CoA
CICLO DE KREBS OU DO ÁCIDO CÍTRICO 1. Produção de Acetil-CoA 2. Oxidação de Acetil-CoA 3. Transferência de elétrons e fosforilação oxidativa CICLO DE KREBS OU DO ÁCIDO CÍTRICO 1. Produção de Acetil-CoA
Metabolismo e vias metabólicas
 Fases: Metabolismo e vias metabólicas I. Catabolismo (degradação) II. Anabolismo (biossíntese) Combustíveis Metabólicos durante o estado alimentado Catabolismo de proteínas, gorduras e carboidratos nos
Fases: Metabolismo e vias metabólicas I. Catabolismo (degradação) II. Anabolismo (biossíntese) Combustíveis Metabólicos durante o estado alimentado Catabolismo de proteínas, gorduras e carboidratos nos
Profª Eleonora Slide de aula. Metabolismo de Carboidratos
 Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Fermentação alcoólica Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose Condições
Metabolismo de Carboidratos Metabolismo de Carboidratos Profª Eleonora Slide de aula Condições de anaerobiose Fermentação alcoólica Glicose 2 Piruvato Ciclo do ácido cítrico Condições de anaerobiose Condições
CICLO DE KREBS. Bianca Zingales IQ-USP
 CICLO DE KREBS https://www.youtube.com/watch?v=ubzwpqpqm Bianca Zingales IQ-USP G L IC O S E A M IN O Á C ID O S Á C ID O S G R A X O S A sp G ly L eu G lu A la Ile F o sfo e n o lp iru v a to ( ) S er
CICLO DE KREBS https://www.youtube.com/watch?v=ubzwpqpqm Bianca Zingales IQ-USP G L IC O S E A M IN O Á C ID O S Á C ID O S G R A X O S A sp G ly L eu G lu A la Ile F o sfo e n o lp iru v a to ( ) S er
OXIDAÇÃO DOS AMINOÁCIDOS E PRODUÇÃO DE URÉIA
 Universidade Federal de Pelotas Programa de Pós-Graduação em Veterinária Disciplina de Doenças metabólicas OXIDAÇÃO DOS AMINOÁCIDOS E PRODUÇÃO DE URÉIA Doutoranda Lourdes Caruccio Hirschmann Orientador:
Universidade Federal de Pelotas Programa de Pós-Graduação em Veterinária Disciplina de Doenças metabólicas OXIDAÇÃO DOS AMINOÁCIDOS E PRODUÇÃO DE URÉIA Doutoranda Lourdes Caruccio Hirschmann Orientador:
Aula Neoglicogênese Gliconeogênese
 Aula 22.10.09 Neoglicogênese Gliconeogênese Metabolismo de açúcares Visão Geral Galactose Frutose Ácido láctico Fermentação Glicólise Glicose Piruvato Glicogenólise Gliconeogênese Glicogênese Glicogênio
Aula 22.10.09 Neoglicogênese Gliconeogênese Metabolismo de açúcares Visão Geral Galactose Frutose Ácido láctico Fermentação Glicólise Glicose Piruvato Glicogenólise Gliconeogênese Glicogênese Glicogênio
Fontes de Ácidos Graxos. Dieta Estoque de gorduras Síntese de outras fontes
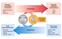 Acetil CoA ATP Fontes de Ácidos Graxos Dieta Estoque de gorduras Síntese de outras fontes Lipídios ingeridos da dieta L i Emulsificação Sais biliares Lipases intestinais degradam TCG Mucosa intestinal
Acetil CoA ATP Fontes de Ácidos Graxos Dieta Estoque de gorduras Síntese de outras fontes Lipídios ingeridos da dieta L i Emulsificação Sais biliares Lipases intestinais degradam TCG Mucosa intestinal
Lipídeos e ácidos graxos
 Lipídeos e ácidos graxos Tópicos de Estudo Lipídeos Lipoproteínas Passos da -oxidação Regulação em estados absortivos, fome e exercício Lipídeos que contem ácidos graxos Ácidos graxos e triacilgliceróis
Lipídeos e ácidos graxos Tópicos de Estudo Lipídeos Lipoproteínas Passos da -oxidação Regulação em estados absortivos, fome e exercício Lipídeos que contem ácidos graxos Ácidos graxos e triacilgliceróis
BIOLOGIA. Moléculas, células e tecidos. Respiração celular e fermentação Parte 1. Professor: Alex Santos
 BIOLOGIA Moléculas, células e tecidos Parte 1 Professor: Alex Santos Tópicos em abordagem: Parte 1 Respiração celular I Conceitos fundamentais; II Etapas da respiração celular; Parte 2 Respiração celular
BIOLOGIA Moléculas, células e tecidos Parte 1 Professor: Alex Santos Tópicos em abordagem: Parte 1 Respiração celular I Conceitos fundamentais; II Etapas da respiração celular; Parte 2 Respiração celular
Cérebro e hemácias utilizam a glicose como fonte exclusiva de energia. Cerca de 75% da oxidadação da glicose / dia é feita pelo cérebro (adulto).
 Gliconeogênese Cérebro e hemácias utilizam a glicose como fonte exclusiva de energia Cerca de 75% da oxidadação da glicose / dia é feita pelo cérebro (adulto). Desta forma o organismo deve ter mecanismos
Gliconeogênese Cérebro e hemácias utilizam a glicose como fonte exclusiva de energia Cerca de 75% da oxidadação da glicose / dia é feita pelo cérebro (adulto). Desta forma o organismo deve ter mecanismos
Utilização de glicose pelas células. A glicólise é a via metabólica mais conservada nos sistemas biológicos
 Utilização de glicose pelas células A glicólise é a via metabólica mais conservada nos sistemas biológicos A glicose é o combustível preferencial e mais versátil disponível nas células vivas. Principais
Utilização de glicose pelas células A glicólise é a via metabólica mais conservada nos sistemas biológicos A glicose é o combustível preferencial e mais versátil disponível nas células vivas. Principais
MÓDULO 2 - METABOLISMO. Bianca Zingales IQ-USP
 MÓDULO 2 - METABOLISMO Bianca Zingales IQ-USP INTRODUÇÃO AO METABOLISMO CARACTERÍSTICAS DO SER VIVO 1- AUTO-REPLICAÇÃO Capacidade de perpetuação da espécie 2- TRANSFORMAÇÃO DE ENERGIA O ser vivo extrai
MÓDULO 2 - METABOLISMO Bianca Zingales IQ-USP INTRODUÇÃO AO METABOLISMO CARACTERÍSTICAS DO SER VIVO 1- AUTO-REPLICAÇÃO Capacidade de perpetuação da espécie 2- TRANSFORMAÇÃO DE ENERGIA O ser vivo extrai
Introdução ao Metabolismo. Profª Eleonora Slide de aula
 Introdução ao Metabolismo Profª Eleonora Slide de aula Metabolismo Profª Eleonora Slide de aula Relacionamento energético entre as vias catabólicas e as vias anabólicas Nutrientes que liberam energia Carboidratos
Introdução ao Metabolismo Profª Eleonora Slide de aula Metabolismo Profª Eleonora Slide de aula Relacionamento energético entre as vias catabólicas e as vias anabólicas Nutrientes que liberam energia Carboidratos
Metabolismo de Carboidratos. Profa.Dra. Leticia Labriola Abril 2011
 Metabolismo de Carboidratos. Profa.Dra. Leticia Labriola Abril 2011 Funções da Via Glicolítica Gerar ATP (rápido); Gerar intermediários para síntese; Regenerar NADH; 2 ATP em anaerobiose Rendimento
Metabolismo de Carboidratos. Profa.Dra. Leticia Labriola Abril 2011 Funções da Via Glicolítica Gerar ATP (rápido); Gerar intermediários para síntese; Regenerar NADH; 2 ATP em anaerobiose Rendimento
Obtenção de Energia. Obtenção de Energia. Obtenção de Energia. Oxidação de Carboidratos. Obtenção de energia por oxidação 19/08/2014
 , Cadeia de Transporte de Elétrons e Fosforilação Oxidativa Prof. Dr. Bruno Lazzari de Lima Para que um organismo possa realizar suas funções básicas: Obtenção de nutrientes. Crescimento. Multiplicação.
, Cadeia de Transporte de Elétrons e Fosforilação Oxidativa Prof. Dr. Bruno Lazzari de Lima Para que um organismo possa realizar suas funções básicas: Obtenção de nutrientes. Crescimento. Multiplicação.
Hoje iremos conhecer o ciclo de Krebs e qual a sua importância no metabolismo aeróbio. Acompanhe!
 Aula: 13 Temática: Metabolismo aeróbio parte I Hoje iremos conhecer o ciclo de Krebs e qual a sua importância no metabolismo aeróbio. Acompanhe! O Ciclo de Krebs ou Ciclo do Ácido Cítrico A molécula de
Aula: 13 Temática: Metabolismo aeróbio parte I Hoje iremos conhecer o ciclo de Krebs e qual a sua importância no metabolismo aeróbio. Acompanhe! O Ciclo de Krebs ou Ciclo do Ácido Cítrico A molécula de
Oxidação parcial o que acontece com o piruvato?
 A glicólise ocorre no citosol das células transforma a glicose em duas moléculas de piruvato e é constituída por uma sequência de 10 reações (10 enzimas) divididas em duas fases. Fase preparatória (cinco
A glicólise ocorre no citosol das células transforma a glicose em duas moléculas de piruvato e é constituída por uma sequência de 10 reações (10 enzimas) divididas em duas fases. Fase preparatória (cinco
Prof André Montillo
 Prof André Montillo www.montillo.com.br Definição: É a soma de todas as reações químicas envolvidas na manutenção do estado dinâmico das células, onde milhares de reações ocorrem ao mesmo tempo, determinando
Prof André Montillo www.montillo.com.br Definição: É a soma de todas as reações químicas envolvidas na manutenção do estado dinâmico das células, onde milhares de reações ocorrem ao mesmo tempo, determinando
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Pontifícia Universidade Católica de Goiás Departamento de Biologia Bioquímica Metabólica ENZIMAS Origem das proteínas e de suas estruturas Níveis de Estrutura Protéica Estrutura das proteínas Conformação
Metabolismo de Glicídeos
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica Metabolismo de Glicídeos Professora Ana Chaves Introdução Boca Enzima Ligação Substrato Produto α-amilase (glândulas
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica Metabolismo de Glicídeos Professora Ana Chaves Introdução Boca Enzima Ligação Substrato Produto α-amilase (glândulas
QBQ 0230 Bioquímica. Carlos Hotta. Metabolismo integrado do corpo 17/11/17
 QBQ 0230 Bioquímica Carlos Hotta Metabolismo integrado do corpo 17/11/17 Órgãos especializados: fígado - Garante a síntese de substrato energético para os demais tecidos - Sintetiza e armazena glicogênio
QBQ 0230 Bioquímica Carlos Hotta Metabolismo integrado do corpo 17/11/17 Órgãos especializados: fígado - Garante a síntese de substrato energético para os demais tecidos - Sintetiza e armazena glicogênio
Metabolismo de Lipídeos
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Curso Engenharia Química Disciplina Bioquimica Metabolismo Energético de Lipídeos Oxidação Completa: Combustível +
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Curso Engenharia Química Disciplina Bioquimica Metabolismo Energético de Lipídeos Oxidação Completa: Combustível +
Faculdade de Tecnologia de Araçatuba. Curso Superior de Tecnologia em Bioenergia Sucroalcooleira
 Faculdade de Tecnologia de Araçatuba Curso Superior de Tecnologia em Bioenergia Sucroalcooleira SÍNTESE DE CARBOIDRATOS Gliconeogênese Biossíntese de glicogênio, amido e sacarose Glicose sanguínea glicogênio
Faculdade de Tecnologia de Araçatuba Curso Superior de Tecnologia em Bioenergia Sucroalcooleira SÍNTESE DE CARBOIDRATOS Gliconeogênese Biossíntese de glicogênio, amido e sacarose Glicose sanguínea glicogênio
Dra. Kátia R. P. de Araújo Sgrillo.
 Dra. Kátia R. P. de Araújo Sgrillo Sgrillo.ita@ftc.br Processo pelo qual os organismos vivos adquirem e usam energia livre para realizar suas funções. É tradicionalmente dividido em: CATABOLISMO ou degradação
Dra. Kátia R. P. de Araújo Sgrillo Sgrillo.ita@ftc.br Processo pelo qual os organismos vivos adquirem e usam energia livre para realizar suas funções. É tradicionalmente dividido em: CATABOLISMO ou degradação
Revisão do Metabolismo da Glicose
 Gliconeogênese Revisão do Metabolismo da Glicose Esquema Geral da Glicólise lise 1 açúcar de 6 C 2 açúcares de 3 C A partir deste ponto as reações são duplicadas 2 moléculas de Piruvato (3C) Saldo 2 moléculas
Gliconeogênese Revisão do Metabolismo da Glicose Esquema Geral da Glicólise lise 1 açúcar de 6 C 2 açúcares de 3 C A partir deste ponto as reações são duplicadas 2 moléculas de Piruvato (3C) Saldo 2 moléculas
Metabolismo energético das células
 Metabolismo energético das células Medicina Veterinária Bioquímica I 2º período Professora: Ms. Fernanda Cristina Ferrari Como a célula produz energia? Fotossíntese Quimiossíntese Respiração Adenosina
Metabolismo energético das células Medicina Veterinária Bioquímica I 2º período Professora: Ms. Fernanda Cristina Ferrari Como a célula produz energia? Fotossíntese Quimiossíntese Respiração Adenosina
objetivo Ciclo da uréia Pré-requisito Ao final desta aula, você deverá ser capaz de: Entender as etapas de formação da uréia.
 Ciclo da uréia A U L A 18 objetivo Ao final desta aula, você deverá ser capaz de: Entender as etapas de formação da uréia. Pré-requisito Conhecimentos adquiridos na Aula 17. BIOQUÍMICA II Ciclo da uréia
Ciclo da uréia A U L A 18 objetivo Ao final desta aula, você deverá ser capaz de: Entender as etapas de formação da uréia. Pré-requisito Conhecimentos adquiridos na Aula 17. BIOQUÍMICA II Ciclo da uréia
Profa. Alessandra Barone.
 Profa. Alessandra Barone www.profbio.com.br Quando é acionada a lipólise no organismo? ATP? Glicose? Glicólise? Glicogênese? Gliconeogênese? Via das pentoses? Lipídeo: reserva energética em forma de triacilglicerol
Profa. Alessandra Barone www.profbio.com.br Quando é acionada a lipólise no organismo? ATP? Glicose? Glicólise? Glicogênese? Gliconeogênese? Via das pentoses? Lipídeo: reserva energética em forma de triacilglicerol
QBQ 0230 Bioquímica. Carlos Hotta. Metabolismo de aminoácidos 10/11/17
 QBQ 0230 Bioquímica Carlos Hotta Metabolismo de aminoácidos 10/11/17 Estrutura geral dos aminoácidos Aminoácidos são a unidade básica das proteínas -> heteropolímeros lineares de aminoácidos 20 aminoácidos
QBQ 0230 Bioquímica Carlos Hotta Metabolismo de aminoácidos 10/11/17 Estrutura geral dos aminoácidos Aminoácidos são a unidade básica das proteínas -> heteropolímeros lineares de aminoácidos 20 aminoácidos
Carla Bittar Bioquímica e Metabolismo Animal
 Carla Bittar Bioquímica e Metabolismo Animal Biosfera rica em N2 Microrganismos reduzem N2 formando NH3 Plantas e microrganismos absorvem NH3 e NO3- para síntese de biomoléculas Animais dependem da dieta
Carla Bittar Bioquímica e Metabolismo Animal Biosfera rica em N2 Microrganismos reduzem N2 formando NH3 Plantas e microrganismos absorvem NH3 e NO3- para síntese de biomoléculas Animais dependem da dieta
Gliconeogénese e Metabolismo do Glicogénio
 Página 1 de 5 Aulas de grupo 2001-02; Rui Fontes Gliconeogénese e Metabolismo do Glicogénio 1- Gliconeogénese 1- A gliconeogénese é um termo usado para incluir o conjunto de processos pelos quais o organismo
Página 1 de 5 Aulas de grupo 2001-02; Rui Fontes Gliconeogénese e Metabolismo do Glicogénio 1- Gliconeogénese 1- A gliconeogénese é um termo usado para incluir o conjunto de processos pelos quais o organismo
Processo de obtenção de energia das células respiração celular
 Processo de obtenção de energia das células respiração celular Lipídeos de armazenamento (Gorduras e óleos) Substâncias que originam ácidos graxos e usadas como moléculas que armazenam energia nos seres
Processo de obtenção de energia das células respiração celular Lipídeos de armazenamento (Gorduras e óleos) Substâncias que originam ácidos graxos e usadas como moléculas que armazenam energia nos seres
Metabolismo de Lipídeos
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Curso Engenharia Química Disciplina Bioquimica Metabolismo Energético de Lipídeos Oxidação Completa: Combustível +
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Curso Engenharia Química Disciplina Bioquimica Metabolismo Energético de Lipídeos Oxidação Completa: Combustível +
Acetil CoA e Ciclo de Krebs. Prof. Henning Ulrich
 Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich No citossol Na mitocôndria Descarboxilação do piruvato: H 3 C- Piruvato Coenzima A Acetil CoA Redução de 1 NAD + Formação de acetil CoA (rica em energia)
Acetil CoA e Ciclo de Krebs Prof. Henning Ulrich No citossol Na mitocôndria Descarboxilação do piruvato: H 3 C- Piruvato Coenzima A Acetil CoA Redução de 1 NAD + Formação de acetil CoA (rica em energia)
Aula de Bioquímica II. Ciclo do Ácido Cítrico
 Aula de Bioquímica II Tema: Ciclo do Ácido Cítrico Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica II Tema: Ciclo do Ácido Cítrico Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Resumo esquemático da glicólise
 Resumo esquemático da glicólise Destino do piruvato em condições aeróbicas e anaeróbicas Glicólise Fermentação Oxidação completa Em condições aeróbicas o piruvato é oxidado a acetato que entra no ciclo
Resumo esquemático da glicólise Destino do piruvato em condições aeróbicas e anaeróbicas Glicólise Fermentação Oxidação completa Em condições aeróbicas o piruvato é oxidado a acetato que entra no ciclo
Metabolismo de Lipídeos
 Outros Exemplos de Mecanismos de Regulação Glicose X Gliconeogênese Regulação da Frutose 6P pela Frutose 2,6 bifosfato FBPase: bifosfatofosfatase (Gliconeogênese) PFK : fosfofrutoquinase (Glicólise) Universidade
Outros Exemplos de Mecanismos de Regulação Glicose X Gliconeogênese Regulação da Frutose 6P pela Frutose 2,6 bifosfato FBPase: bifosfatofosfatase (Gliconeogênese) PFK : fosfofrutoquinase (Glicólise) Universidade
METABOLISMO DOS AMINOÁCIDOS. Prof. Henning Ulrich
 METABOLISMO DOS AMINOÁCIDOS Prof. Henning Ulrich CATABOLISMO DOS AMINOÁCIDOS EM MAMÍFEROS CATABOLISMO DOS GRUPOS AMINO CATABOLISMO DOS GRUPOS AMINO PORÇÃO DO TRATO DIGESTIVO HUMANO TRANSAMINAÇÕES CATALISADAS
METABOLISMO DOS AMINOÁCIDOS Prof. Henning Ulrich CATABOLISMO DOS AMINOÁCIDOS EM MAMÍFEROS CATABOLISMO DOS GRUPOS AMINO CATABOLISMO DOS GRUPOS AMINO PORÇÃO DO TRATO DIGESTIVO HUMANO TRANSAMINAÇÕES CATALISADAS
A energética celular:
 A energética celular: o papel das mitocôndrias e cloroplastos Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular Como já vimos anteriormente
A energética celular: o papel das mitocôndrias e cloroplastos Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular Como já vimos anteriormente
Cadeia de transporte de elétrons e fosforilação oxidativa
 Cadeia de transporte de elétrons e fosforilação oxidativa MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Piruvato
Cadeia de transporte de elétrons e fosforilação oxidativa MAPA II POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Piruvato
CICLO DE KREBS. 1. Em condições aeróbicas, o destino do piruvato produzido na glicólise é sofrer uma
 CICLO DE KREBS 1. Em condições aeróbicas, o destino do piruvato produzido na glicólise é sofrer uma descarboxilação oxidativa catalisada pela piruvato desidrogenase, que é um complexo multienzimático existente
CICLO DE KREBS 1. Em condições aeróbicas, o destino do piruvato produzido na glicólise é sofrer uma descarboxilação oxidativa catalisada pela piruvato desidrogenase, que é um complexo multienzimático existente
MAPA II Vias metabólicas degradativas
 GLIÓLISE MAPA II Vias metabólicas degradativas PLISSAARÍDIS PRTEÍNAS LIPÍDIS GLISE AMINÁIDS ÁIDS GRAXS Glicólise Fosfoenolpiruvato (3) Asp Gly Ala Ser ys Leu Ile Lys Phe Glu Piruvato (3) 2 Acetil-oA (2)
GLIÓLISE MAPA II Vias metabólicas degradativas PLISSAARÍDIS PRTEÍNAS LIPÍDIS GLISE AMINÁIDS ÁIDS GRAXS Glicólise Fosfoenolpiruvato (3) Asp Gly Ala Ser ys Leu Ile Lys Phe Glu Piruvato (3) 2 Acetil-oA (2)
Graxos. Metabolismo dos Lipídios. Oxidação. Degradação dos Triacilgliceróis is (TG) do Tecido Adiposo. Tecido Adiposo. Tecido Adiposo.
 Lipóle (β-oxida( oxidação) Cetogênese Síntese de Ácidos Graxos Alexandre Havt Metabolmo dos Lipídios Fonte de obtenção Dieta Triacilgliceró Síntese endógena Transporte Excesso de Carboidratos, Proteínas
Lipóle (β-oxida( oxidação) Cetogênese Síntese de Ácidos Graxos Alexandre Havt Metabolmo dos Lipídios Fonte de obtenção Dieta Triacilgliceró Síntese endógena Transporte Excesso de Carboidratos, Proteínas
Aulas Multimídias Santa Cecília Profª Renata Coelho Disciplina: Biologia Série: 9º ano EF
 Aulas Multimídias Santa Cecília Profª Renata Coelho Disciplina: Biologia Série: 9º ano EF QUAIS SÃO OS PROCESSOS METABÓLICOS QUE LIBERAM ENERGIA DO ALIMENTO DENTRO DAS CÉLULAS HUMANAS? ONDE, NAS CÉLULAS
Aulas Multimídias Santa Cecília Profª Renata Coelho Disciplina: Biologia Série: 9º ano EF QUAIS SÃO OS PROCESSOS METABÓLICOS QUE LIBERAM ENERGIA DO ALIMENTO DENTRO DAS CÉLULAS HUMANAS? ONDE, NAS CÉLULAS
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa
 OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
OXIDAÇÕES BIOLÓGICAS: Cadeia respiratória e fosforilação oxidativa Metabolismo: integração entre catabolismo e anabolismo Assimilação ou processamento da mat. Orgânica Síntese de Substâncias Estágio 1
Organelas e suas funções. A energética celular:
 Organelas e suas funções Capitulo 15- Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular: Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição
Organelas e suas funções Capitulo 15- Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular: Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição
Metabolismo de Glicídios
 Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Doenças Metabólicas Metabolismo de Glicídios Lucas Balinhas Mozer Ávila Patrícia Mattei Uriel Londero Pelotas, abril 2015
Universidade Federal de Pelotas Núcleo de Pesquisa, Ensino e Extensão em Pecuária Doenças Metabólicas Metabolismo de Glicídios Lucas Balinhas Mozer Ávila Patrícia Mattei Uriel Londero Pelotas, abril 2015
GLICONEOGÊNESE ou NEOGLICOGÊNESE
 GLICONEOGÊNESE ou NEOGLICOGÊNESE GLICONEOGÊNESE OU NEOGLICOGÊNESE Definição: é a via de biossíntese de Glicose a partir de Piruvato Esta via faz parte do ANABOLISMO A Gliconeogênese ocorre no CITOSSOL
GLICONEOGÊNESE ou NEOGLICOGÊNESE GLICONEOGÊNESE OU NEOGLICOGÊNESE Definição: é a via de biossíntese de Glicose a partir de Piruvato Esta via faz parte do ANABOLISMO A Gliconeogênese ocorre no CITOSSOL
Biologia. Respiração Celular. Professor Enrico Blota.
 Biologia Respiração Celular Professor Enrico Blota www.acasadoconcurseiro.com.br Biologia RESPIRAÇÃO CELULAR A bioenergética é o estudo dos processos do metabolismo celular de produção e quebra de energia
Biologia Respiração Celular Professor Enrico Blota www.acasadoconcurseiro.com.br Biologia RESPIRAÇÃO CELULAR A bioenergética é o estudo dos processos do metabolismo celular de produção e quebra de energia
Abaixo estão notas de aula Sugiro visualizar o vídeo disposto neste link:
 3. Metabolismo Abaixo estão notas de aula Sugiro visualizar o vídeo disposto neste link: http://www.youtube.com/watch?v=5emw4b29rg&feature=related Fermentação alcoólica Em aulas anteriores vimos como a
3. Metabolismo Abaixo estão notas de aula Sugiro visualizar o vídeo disposto neste link: http://www.youtube.com/watch?v=5emw4b29rg&feature=related Fermentação alcoólica Em aulas anteriores vimos como a
Processo de obtenção de energia das células respiração celular
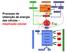 Processo de obtenção de energia das células respiração celular Lipídeos de armazenamento (Gorduras e óleos) Os lipideos de armazenamento são constituidos por ácidos graxos esterificados ao glicerol - triglicerídeos
Processo de obtenção de energia das células respiração celular Lipídeos de armazenamento (Gorduras e óleos) Os lipideos de armazenamento são constituidos por ácidos graxos esterificados ao glicerol - triglicerídeos
Metabolismo de Carboidratos
 Metabolismo de Carboidratos Curso de Bioqímica para Saúde Coletiva- UFRJ Profa. Dra. Mônica Santos de Freitas 1 Carboidratos Três maiores classes de carboidratos Monossacarídeos- são carboidratos não polimerizados;
Metabolismo de Carboidratos Curso de Bioqímica para Saúde Coletiva- UFRJ Profa. Dra. Mônica Santos de Freitas 1 Carboidratos Três maiores classes de carboidratos Monossacarídeos- são carboidratos não polimerizados;
A energética celular:
 A energética celular: o papel das mitocôndrias e cloroplastos Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular Como já vimos anteriormente
A energética celular: o papel das mitocôndrias e cloroplastos Capitulo 13 (p 427 a 444) e Capitulo 14 Fundamentos da Biologia Celular- Alberts- 2ª edição A energética celular Como já vimos anteriormente
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA COMO AS CÉLULAS SINTETIZAM ATP
 CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
17/3/2014. Metabolismo Microbiano. Definição FUNÇÕES ESPECÍFICAS
 Definição UNIDADE ACADÊMICA DE CIÊNCIAS AGRÁRIAS CURSO DE GRADUAÇÃO EM AGRONOMIA DISCIPLINA: BIOQUÍMICA GERAL PROFESSORAS: Adriana Silva Lima e Márcia Aparecida Cezar Metabolismo Microbiano Chama-se metabolismo
Definição UNIDADE ACADÊMICA DE CIÊNCIAS AGRÁRIAS CURSO DE GRADUAÇÃO EM AGRONOMIA DISCIPLINA: BIOQUÍMICA GERAL PROFESSORAS: Adriana Silva Lima e Márcia Aparecida Cezar Metabolismo Microbiano Chama-se metabolismo
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA COMO AS CÉLULAS SINTETIZAM ATP
 CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
CADEIA DE TRANSPORTE DE ELÉTRONS E FOSFORILAÇÃO OXIDATIVA OU COMO AS CÉLULAS SINTETIZAM ATP SINTETIZAM ATP ÀS CUSTAS DA OXIDAÇÃO DAS COENZIMAS NADH E FADH 2 PELO OXIGÊNIO AS COENZIMAS REDUZIDAS SÃO PRODUZIDAS
Via das pentoses-fosfato
 Via das pentoses-fosfato A U L A 24 objetivos Nesta aula, você vai conhecer a via das pentoses-fosfato, um desvio da via glicolítica necessário às células que realizam reações de biossíntese redutoras.
Via das pentoses-fosfato A U L A 24 objetivos Nesta aula, você vai conhecer a via das pentoses-fosfato, um desvio da via glicolítica necessário às células que realizam reações de biossíntese redutoras.
Matéria: Biologia Assunto: Respiração celular Prof. Enrico blota
 Matéria: Biologia Assunto: Respiração celular Prof. Enrico blota Biologia 1. Moléculas, células e tecidos - Fotossíntese e respiração - Respiração celular Fermentação Organismos que só vivem na presença
Matéria: Biologia Assunto: Respiração celular Prof. Enrico blota Biologia 1. Moléculas, células e tecidos - Fotossíntese e respiração - Respiração celular Fermentação Organismos que só vivem na presença
Aula de Bioquímica Avançada. Gliconeogênese Glicogênio: Glicogenólise, Síntese e Regulação
 Aula de Bioquímica Avançada Temas: Gliconeogênese Glicogênio: Glicogenólise, Síntese e Regulação Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos
Aula de Bioquímica Avançada Temas: Gliconeogênese Glicogênio: Glicogenólise, Síntese e Regulação Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos
Organelas Transdutoras de Energia: Mitocôndria - Respiração
 Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Curso: Engenharia
Universidade de São Paulo Escola de Engenharia de Lorena Departamento de Biotecnologia Organelas: Cloroplasto e Mitocôndria Obtenção de energia para a célula a partir diferentes fontes: Curso: Engenharia
Glória Braz GLICÓLISE
 Glória Braz GLICÓLISE Utilização de glicose pelas células A glicólise é a via metabólica mais conservada nos sistemas biológicos A glicose é o combustível preferencial e mais versátil disponível nas células
Glória Braz GLICÓLISE Utilização de glicose pelas células A glicólise é a via metabólica mais conservada nos sistemas biológicos A glicose é o combustível preferencial e mais versátil disponível nas células
Processo de obtenção de energia das células respiração celular
 Processo de obtenção de energia das células respiração celular Macromolécula mais abundante nas células Grande variedade (tamanho e função) Pequenos peptídeos a grandes cadeias com PM alto Diversidade
Processo de obtenção de energia das células respiração celular Macromolécula mais abundante nas células Grande variedade (tamanho e função) Pequenos peptídeos a grandes cadeias com PM alto Diversidade
β-oxidação de lipídios Ciclo de Lynen
 β-oxidação de lipídios Ciclo de Lynen POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Lactato Piruvato (3) CO 2 Acetil-CoA
β-oxidação de lipídios Ciclo de Lynen POLISSACARÍDIOS PROTEÍNAS LIPÍDIOS GLICOSE AMINOÁCIDOS ÁCIDOS GRAXOS Fosfoenolpiruvato (3) Asp Gly Ala Ser Cys Leu Ile Lys Phe Glu Lactato Piruvato (3) CO 2 Acetil-CoA
Oxidação parcial o que acontece com o piruvato?
 A glicólise ocorre no citosol das células transforma a glicose em duas moléculas de piruvato e é constituída por uma sequência de 10 reações (10 enzimas) divididas em duas fases. Fase preparatória (cinco
A glicólise ocorre no citosol das células transforma a glicose em duas moléculas de piruvato e é constituída por uma sequência de 10 reações (10 enzimas) divididas em duas fases. Fase preparatória (cinco
Metabolismo de Carboidratos
 Metabolismo de Carboidratos Curso de Bioqímica para Saúde Coletiva- UFRJ Profa. Dra. Mônica Santos de Freitas 1 Gliconeogênese - Ocorre principalmente no fígado; - Algumas das enzimas utilizadas na síntese
Metabolismo de Carboidratos Curso de Bioqímica para Saúde Coletiva- UFRJ Profa. Dra. Mônica Santos de Freitas 1 Gliconeogênese - Ocorre principalmente no fígado; - Algumas das enzimas utilizadas na síntese
Respiração Celular. Ciclo de Krebs Ciclo do ácido Tricarboxílico Ciclo do ácido Cítrico. Prof. Ana Paula Jacobus
 Respiração Celular Ciclo de Krebs Ciclo do ácido Tricarboxílico Ciclo do ácido Cítrico Prof. Ana Paula Jacobus GLICOSE VIAS LINEARES (glicólise e gliconeogênese) PIRUVATO Ciclo do ácido cítrico ou
Respiração Celular Ciclo de Krebs Ciclo do ácido Tricarboxílico Ciclo do ácido Cítrico Prof. Ana Paula Jacobus GLICOSE VIAS LINEARES (glicólise e gliconeogênese) PIRUVATO Ciclo do ácido cítrico ou
Ciclo de Calvin. Síntese de glicose a partir de CO 2. ATP e NADPH + H+ sintetizados na fase clara são utilizados para reduzir CO 2 a glicose
 Ciclo de Calvin Síntese de glicose a partir de CO 2 ATP e NADPH + H+ sintetizados na fase clara são utilizados para reduzir CO 2 a glicose Síntese de carboidratos ATP e NADPH + H + produzidos na reação
Ciclo de Calvin Síntese de glicose a partir de CO 2 ATP e NADPH + H+ sintetizados na fase clara são utilizados para reduzir CO 2 a glicose Síntese de carboidratos ATP e NADPH + H + produzidos na reação
Metabolismo de Lipídios
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica Metabolismo de Lipídios Professora Ana Chaves Classificação Ácidos graxos Lipídeos Complexos Lipídeos Simples
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica Metabolismo de Lipídios Professora Ana Chaves Classificação Ácidos graxos Lipídeos Complexos Lipídeos Simples
Introdução ao Metabolismo Microbiano
 Introdução ao Metabolismo Microbiano METABOLISMO DEFINIÇÃO: Grego: metabole = mudança, transformação; Toda atividade química realizada pelos organismos; São de dois tipos: Envolvem a liberação de energia:
Introdução ao Metabolismo Microbiano METABOLISMO DEFINIÇÃO: Grego: metabole = mudança, transformação; Toda atividade química realizada pelos organismos; São de dois tipos: Envolvem a liberação de energia:
Universidade Federal do Pampa Campus Itaqui Bioquímica GLICONEOGÊNESE. Profa. Dra. Marina Prigol
 Universidade Federal do Pampa Campus Itaqui Bioquímica GLICONEOGÊNESE Profa. Dra. Marina Prigol GLICONEOGÊNESE PROCESSO DE SÍNTESE DE GLICOSE A PARTIR DE COMPOSTOS NÃO GLICÍDICOS OCORRÊNCIA: Citosol do
Universidade Federal do Pampa Campus Itaqui Bioquímica GLICONEOGÊNESE Profa. Dra. Marina Prigol GLICONEOGÊNESE PROCESSO DE SÍNTESE DE GLICOSE A PARTIR DE COMPOSTOS NÃO GLICÍDICOS OCORRÊNCIA: Citosol do
Visão geral do metabolismo glicídico
 Visão geral do metabolismo glicídico 1. Todas as células do organismo podem usar glicose oxidando-a (processo exergónico) de forma acoplada com a formação de (processo endergónico). a) O catabolismo da
Visão geral do metabolismo glicídico 1. Todas as células do organismo podem usar glicose oxidando-a (processo exergónico) de forma acoplada com a formação de (processo endergónico). a) O catabolismo da
Semana 12 Respiração Celular
 Semana 12 Respiração Celular Prof. Saul Carvalho Respiração Celular Extração de energia química de substâncias orgânicas (carboidratos e lipídios) Principalmente quebra da Glicose Gera energia celular
Semana 12 Respiração Celular Prof. Saul Carvalho Respiração Celular Extração de energia química de substâncias orgânicas (carboidratos e lipídios) Principalmente quebra da Glicose Gera energia celular
