BIOQUÍMICA GERAL. Prof. Dr. Franciscleudo B. Costa UATA/CCTA/UFCG. Aula 4 Aminoácidos. Origem dos aminoácidos. Estrutura Química Geral
|
|
|
- Ana Carolina Azenha Bastos
- 7 Há anos
- Visualizações:
Transcrição
1 Universidade Federal de Campina Grande Centro de Ciências e Tecnologia Agroalimentar Unidade Acadêmica de Tecnologia de Alimentos BIOQUÍMICA GERAL FRANCISCLEUDO BEZERRA DA COSTA PROFESSOR Câmpus de Pombal Pombal - PB Aula 4 Aminoácidos Origem dos AA Estrutura e fórmula química geral de AA Propriedades ópticas dos AA Características físicas dos AA Funções biológicas Classificação quanto a natureza do grupo R Aminoácidos essenciais Aminoácidos não essenciais Destino final dos AA pelo metabolismo animal Ligação peptídica Peptídeos fisiologicamente ativos Origem dos aminoácidos O primeiro aminoácido descoberto foi a Asparagina, em O último, dos mais comuns, foi a Treonina, em Todos os aminoácidos possuem nomes comuns, sendo, na maioria das vezes, retirados das fontes de onde foram isolados pela 1ª vez. Asparagina Ác. Glutâmico Tirosina Aspargo Glúten do Trigo Queijo (Tyros = Queijo) Glicina sabor doce GlyKos Mais de 300 AA diferentes foram descritos, porém apenas 20 são encontrados em constituintes de proteínas em mamíferos. Aminoácidos mais importantes sãos os α. Apresentam carbono assimétrico O carbono liga-se a 4 grupos substituintes diferentes Apresentam: Um grupo amina: NH2 Um grupo carboxila: COOH Um hidrogênio H Estrutura Química Geral O carbono α é um centro quiral (opticamnte ativo) Uma cadeia lateral R (determina a identidade de um aa específico). Exceção: Glicina, com o R formado por um H. H 3 N + COO _ C Portanto, as moléculas com centros quirais são opticamente ativas. R H Propriedades ópticas dos AA Devido à geometria tetraédrica em torno do carbono-α, os vários grupos podem ocupar dois arranjos espaciais diferentes (L- e D- aminoácidos); O carbono-α é, portanto, um centro quiral (o que implica que é opticamente ativo); Como as duas formas não podem ser sobrepostas, designam-se enantiómeros; Formam dois esterioisômeros: L e D L Levorrotatório (esquerda) D Destrorrotatório (direita) Estereoisómeros da alanina 1
2 Nome Símbolo Abreviação Nomenclatura Observações importantes: Os aminoácidos nas moléculas protéicas são sempre L-estereisômeros Os D aminoácidos foram encontrados apenas em pequenos peptídeos de parede celular bacteriana e alguns peptídeos que têm função antibiótica. Glicina ou Glicocola Gly, Gli G Ácido 2-aminoacético ou Ácido 2-amino-etanóico Alanina Ala A Ácido 2-aminopropiônico ou Ácido 2-amino-propanóico Leucina Leu L Ácido 2-aminoisocapróico ou Ácido 2-amino-4-metil-pentanóico Valina Val V Ácido 2-aminovalérico ou Ácido 2-amino-3-metil-butanóico Isoleucina Ile I Ácido 2-amino-3-metil-n-valérico ou ácido 2-amino-3-metilpentanóico Prolina Pro P Ácido pirrolidino-2-carboxílíco Fenilalanina Phe ou Fen F Ácido 2-amino-3-fenil-propiônico ou Ácido 2-amino-3-fenil-propanóico Serina Ser S Ácido 2-amino-3-hidroxi-propiônico ou Ácido 2-amino-3-hidroxipropanóico Treonina Thr, The T Ácido 2-amino-3-hidroxi-n-butírico Cisteina Cys, Cis C Ácido 2-bis-(2-amino-propiônico)-3-dissulfeto ou Ácido 3-tiol-2-aminopropanóico Tirosina Tyr, Tir Y Ácido 2-amino-3-(p-hidroxifenil)propiônico ou paraidroxifenilalanina Asparagina Asn N Ácido 2-aminossuccionâmico Glutamina Gln Q Ácido 2-aminoglutarâmico Aspartato ou Ác. Aspártico Asp D Ácido 2-aminossuccínico ou Ácido 2-amino-butanodióico Glutamato ou Ác. glutâmico Glu E Ácido 2-aminoglutárico Arginina Arg R Ácido 2-amino-4-guanidina-n-valérico Lisina Lys, Lis K Ácido 2,6-diaminocapróico ou Ácido 2, 6-diaminoexanóico Histidina His H Ácido 2-amino-3-imidazolpropiônico Triptofano Trp, Tri W Ácido 2-amino-3-indolpropiônico Metionina Met M Ácido 2-amino-3-metiltio-n-butírico Características Físicas Compostos sólidos, cristalinos e se fundem a alta temperatura; Incolores; A maioria apresenta sabor adocicado; Alguns insípidos; E outros amargos; Com exceção da glicina, que é solúvel em água, os demais apresentam solubilidade variável; Insolúveis em solventes orgânicos; Em soluções aquosas apresentam alto momento dipolar. FUNÇÕES BIOLÓGICAS Estrutura da célula Funcionam como sistema tampão, ou seja, atuam no controle do ph das células; Hormônios Receptores de proteínas e hormônios Transporte de metabólitos e íons Atividade enzimática Imunidade Gliconeogênese no jejum e diabetes Propriedades Químicas Característica ácida (presença do grupo carboxila); Característica básica (presença do grupo amino); Interação intramolecular, originando um "sal interno": Propriedades Químicas Caráter anfótero - reagem tanto em ácidos quanto em bases, produzindo sais : Solúveis em água; Insolúveis em solventes orgânicos; PF e PE altos (características dos sais). 2
3 Propriedades Ácido-Base Quando em solução aquosa, um aminoácido existe sob a forma de um íon dipolar (zwitterion, do alemão íon híbrido ); Zwitterion "sal interno" ou "íon dipolar, composto químico eletricamente neutro, mas que possui cargas opostas em diferentes átomos. Podem se comportar como ácidos ou bases, portanto são anfóteros. Curvas de Titulação pka do grupo carboxilo ~2 pka do grupo amina ~9 Curva de titulação da glicina. Curva de titulação do glutamato. Os aminoácidos têm várias regiões tampão. Curva de titulação de um Aminoácido I ph ácido: grupos COOH e NH 3 + protonados devido ao excesso de prótons (H + ). Ex.: estômago. II ph neutro: a medida que o ph aumenta (7 a 7,4), ocorre dissociação primeiro do H + no. O grupo NH 3 + ainda está protonado (íon dipolar). Ex.: sangue, saliva, meio intracelular. III ph básico: há dissociação do H + no NH 3+. Os grupos Grupo NH 2 e ficam desprotonados. Ex.: duodeno. Titulação de um Aminoácido Na titulação de um AA com uma base, iniciando-se em ph=1 observa-se que o ph da solução aumenta até cerca de ph=2, quando o grupo COOH começa a liberar íons H + para o meio, originando água. Titulação de um Aminoácido Continuando a adição de base o ph irá progressivamente se elevando até que o grupo NH 3 + tenha condições de liberar seu íon H +, o que ocorre próximo ao ph 9. COOH H- C - NH OH - R H 2 O H- C - NH pk 1 R NH 3 + íon dipolar H-C-NH OH - R íon dipolar H 2 O pk 2 H-C-NH 2 R 3
4 COOH H- C - NH CH 3 Titulação de um Aminoácido NH + 3 pk 1 H-C-NH CH 3 NH + 3 pk 2 H-C-NH 2 CH 3 Ponto Isoelétrico Compreende o ph no qual a molécula de aminoácido apresenta igual número de cargas positivas e negativas; O AA encontra-se eletricamente neutro; Região de tamponamento devida ao grupo -COOH Região de tamponamento devida ao grupo -NH 2 COOH + H 3 N- C -H + H 3 N- C- H H 2 N- C- H R pk 1 R pk 2 R A+ Forma A- Isoelétrica Formando um íon dipolar ou zwitterion; O cálculo do pi baseia-se nas formas de dissociação do aminoácido utilizando os pk anterior e posterior à forma isoelétrica do aminoácido. AMINOÁCIDOS- ESTRUTURA Cadeias laterais (R) Propriedades das cadeias laterais em diferentes aminoácidos afinidade ou não pela água, cargas elétricas importantes na conformação e função das proteínas. Aminoácidos classificados de acordo com a polaridade do grupo R Apolares grupo R hidrofóbico Polares grupo R hidrofílico Aminoácidos Apolares (Hidrofóbicos) Grupos R constituídos de hidrocarbonetos que não interagem com a água. Tem uma localização mais interna na molécula Aminoácidos incapazes de receber ou doar prótons, de formar ligações iônicas ou pontes de hidrogênio Aminoácidos Polares (Hidrofílicos) Aminoácidos com cadeias laterais polares, desprovidas de cargas elétricas (não ionizáveis) Aminoácidos Polares (Hidrofílicos) Aminoácidos com cargas negativas Aminoácidos com cadeias laterais ácidas cadeias laterais ionizadas, com grupo carboxilato (-coo - ) carregado negativamente Aminoácidos doadores de prótons 4
5 Aminoácidos Polares (Hidrofílicos) Aminoácidos com cargas positivas Aminoácidos com cadeias laterais ácidas cadeias laterais ionizadas, com carga positiva As cadeias laterais dos aminoácidos básicos são aceptoras de prótons 5
6 AMINOÁCIDOS Em soluções aquosas, cadeias laterais apolares se agrupam no interior da proteína; A hidrofobicidade dos grupos R apolares, funcionam como gotículas de óleo em ambiente aquoso Em proteínas localizadas em ambientes hidrofóbicos (interior da membranas)- grupos R são encontrados na superfície da proteína interagindo com o ambiente lipídico. Cadeias laterais polares (hidrofílicas) Cadeias laterais apolares (hidrofóbicas) Proteínas em solução Classificação dos Aminoácidos Aminoácidos ESSENCIAIS: aa que não podem ser sintetizados pelos animais. Aminoácidos NÃO ESSENCIAIS: aa que podem ser sintetizados pelos animais, cerca de 10 a 12, encontrados em suas proteínas. Para os vegetais, todos os aminoácidos são do tipo não essenciais; Para classificar um aminoácido em não essencial ou essencial depende da espécie estudada; Um mesmo AA pode ser essencial para um organismo e não essencial para outro. 1. Arginina, Arg (A): Precursor do óxido nítrico, que tem sido associado à redução da pressão arterial, redução da coagulação sanguínea e proteção contra enfarte do miocárdio e ataque cardíaco. O sumo de melancia é uma fonte deste precursor metabólico da arginina. 2. Fenilalanina, Phe ou Fen (F): A fenilalanina é um aminoácido encontrado em proteínas vegetais ou animais, sendo fundamental para o bom funcionamento do organismo. Porém, seu consumo pode ser perigoso para quem sofre de fenilcetonúria, uma alteração genética que ocorre em um a cada 10 mil nascimentos. 6
7 3. Isoleucina, Ile (I): A L-isoleucina, a L-leucina e a L-valina são os aminoácidos de cadeia ramificada que atuam em conjunto, desempenhando diversas funções no organismo. Protegem os músculos de lesões por esforço excessivo, por meio da síntese de proteínas e da redução do catabolismo protéico. 4. Lisina, Lys ou Lis (K): No organismo, a L-lisina desempenha diversas funções como participação na síntese de proteínas e de compostos precursores à produção de energia, como por exemplo, a D-glicose, glicogênio e lipídios. Além disso, está presente na composição do colágeno e da elastina na forma de L-hidroxilisina. 5. Metionina, Met (M): A L-metionina pode atuar na formação de compostos essenciais à produção de energia, D-glicose e glicogênio; reduz os efeitos tóxicos de certas hepatotoxinas (substâncias tóxicas ao fígado); E, pode atuar com atividade antioxidante, inibindo a formação de radicais livres, substâncias que podem provocar diversos tipos de doenças. 6. Serina, Ser (S): A L-serina atua em rotas biossintéticas das pirimidinas, purinas, creatina e porfirinas. Encontra-se na porção ativa das enzimas proteases de serina, que incluem a tripsina e a quimotripsina. Estas enzimas catalisam a hidrólise das ligações peptídicas em polipeptídios e em proteínas, importante no processo digestivo. Fontes: Arroz, ovos, leite são ricos em serina. 7. Treonina, Thr ou The (T): A L-treonina desempenha um papel importante, junto com a glicina e a serina, no metabolismo de porfirina. A treonina representa cerca de 4% dos aminoácidos das proteínas do nosso organismo. Os ovos são ricos em treonina. 8. Triptofano, Trp ou Tri (W): O L-triptofano aumenta a produção de serotonina que é o neurotransmissor capaz de reduzir a sensação de dor, diminuir o apetite, relaxar e até induzir e melhorar o sono. Fontes: carnes magras, peixes, leite e iogurtes desnatados, queijos brancos e magros, nozes e leguminosas, arroz, feijão, lentilha, castanhas, abacate, soja e derivados. 7
8 9. Histidina, His (H): A L-histidina atua na síntese de proteínas, é precursora do alfacetoglutarato (molécula que participa da produção de energia), bem como do composto antioxidante ergotionina, da histamina (mediador químico liberado nas reações de hipersensibilidade imediata e nas respostas alérgicas) e do ácido transurocânico, substância filtrante dos raios ultravioleta encontrada na epiderme. 10. Valina, Val (V): A L-valina está em maior concentração na musculatura esquelética, mas pode também ser encontrado no cérebro e rins. Destino final de AA no metabolismo animal produto gerado no metabolismo Classificação dos aminoácidos em relação aos produtos gerados Glucogênicos: transformados em glicose (alanina, arginina, metionina, cisteína, cistina, histidina, treonina e valina). Glucocetogênicos: transformados em glicose ou em corpos cetônicos (fenilalanina, tirosina, triptofano, isoleucina e lisina). Cetogênicos: transformados em corpos cetônicos (leucina). Metabolismo dos aminoácidos : Produtos gerados a partir da degradação dos aas síntese de glicose, lipídeos, produção de energia. Aminoácidos glicogênicos- aas cujo catabolismo produz piruvato, - cetoglutarato, succinil-coa, fumarato, oxalacetato (intermediários do ciclo Krebs). Esses intermediários são substratos para gliconeogênese e podem originar glicose ou glicogênio no fígado e glicogênio no músculo Aminoácidos cetogênicos: Aas que são degradados a Acetil-CoAa ou Acetoacetil- CoAaas cujo catabolismo produz acetoacetato,acetona, b-hidroxibutirato (corpos cetônicos- produtos derivados da quebra dos ácidos graxos para fornecimento de energia) 8
9 AMINOÁCIDOS: COMPONENTES DAS PROTEÍNAS Existem 300 AAs diferentes descritos na natureza. Apenas 20 AAs são encontrados como constituintes de proteínas; Proteínas compostas por uma seqüência de AAs; Cada aminoácido pode estar presente mais de uma vez em uma proteína; Número pequeno de aminoácidos-? Geração de inúmeras proteínas com estruturas e funções diferentes 2 aminoácidos livres LIGAÇÃO PEPTÍDICA Interação para formação da ligação peptídica Os AAs podem formar polímeros pela ligação do grupo carboxílico de um aminoácido com o grupo amino de outro AA. Ligação peptídica: ligação química entre 2 moléculas, quando o grupo carboxílico de uma molécula reage com o grupo amina de outra molécula, liberando 1 molécula de H 2 O (Reação de síntese por desidratação que ocorre entre moléculas de aminoácidos). Formação da ligação peptídica com liberação de H 2 O 9
10 FORMAÇÃO DE UMA LIGAÇÃO PEPTÍDICA DIPEPTÍDEO Cadeia polipeptídica, 2 a milhares AAs: extremidade amino (N-terminal)- à esquerda extremidade carboxila (C-terminal)- à direita As seqüências de aminoácidos são lidas da esquerda pra direita (extremidade N-terminal para C- terminal) 2 AAs - Dipeptídeo 3 AAs - Tripeptídeo 4 a 10 AAs - Oligopeptídeo 11 a 100 Aas - Polipeptídeo CADEIA POLIPEPTÍDICA PEPTIDEOS DE IMPORTANCIA FISIOLOGICA Aspartame Cadeias laterais- grupo R Grupo carboxila Grupo amina Peptídios de importância biológica Vasopressina Ocitocina Cys Cys Phe Ile Cys Arg Cys Leu 10
11 Peptídios de importância biológica Vasopressina- hormônio antidiurético Ocitocina- hormônio que atua no sistema reprodutor feminino Estimula a freqüência e a amplitude das contrações da musculatura uterina no fim da gestação Desempenha um papel durante a lactação 11
Aminoácidos e Peptídeos. Profa. Alana Cecília
 Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
AMINOÁCIDOS. Dra. Flávia Cristina Goulart. Bioquímica
 AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
Rafael Mesquita. Aminoácidos
 Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
13/08/2018. Escala de ph. Escala de ph. Crescimento básico. Crescimento ácido. Neutro. básico
 Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs
 Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA. Aminoácidos. Prof. Willame Bezerra
 CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
Aminoácidos não-essenciais: alanina, ácido aspártico, ácido glutâmico, cisteína, glicina, glutamina, hidroxiprolina, prolina, serina e tirosina.
 AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
BÁSICA EM IMAGENS. Aminoácidos, peptídeos e proteínas
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
- Apresentam uma fórmula básica: um átomo central de carbono onde se ligam:
 1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
Aminoácidos FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
Carla Bittar Bioquímica e Metabolismo Animal
 Carla Bittar Bioquímica e Metabolismo Animal Compostos orgânicos Unidades formadoras de PROTEÍNAS Ligações covalentes com perda de água Moléculas pequenas PM de aproximadamente 130 Estrutura da célula
Carla Bittar Bioquímica e Metabolismo Animal Compostos orgânicos Unidades formadoras de PROTEÍNAS Ligações covalentes com perda de água Moléculas pequenas PM de aproximadamente 130 Estrutura da célula
Aminoácidos. Bioquímica Prof. Dr. Marcelo Soares
 Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
 Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
Aminoácidos. Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP.
 Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aminoácidos peptídeos e proteínas
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas
 Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
Aminoácidos e peptídeos. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
REVISÃO: ENADE BIOQUÍMICA - 1
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
Macromolécula mais abundante nas células
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
3 LIGANTES. 3.1 Aspectos biológicos
 LIGANTES 38 3 LIGANTES Serão descritos os principais aspectos químicos e biológicos dos ligantes estudados neste trabalho. A importância desse capítulo fundamenta-se no fato de que os aminoácidos são as
LIGANTES 38 3 LIGANTES Serão descritos os principais aspectos químicos e biológicos dos ligantes estudados neste trabalho. A importância desse capítulo fundamenta-se no fato de que os aminoácidos são as
13/03/2016. Profª. Drª. Andréa Fontes Garcia E -mail:
 Profª. Drª. Andréa Fontes Garcia E -mail: andrea@salesiano-ata.br 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
Profª. Drª. Andréa Fontes Garcia E -mail: andrea@salesiano-ata.br 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
AMINOÁCIDOS. - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos;
 1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
Origem grego (protos) primeira, mais importante
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
1. INTRODUÇÃO. Polímeros biológicos. Polissacarídeos Proteínas Ácidos Nucléicos. Reservas de energia. Armazenamento e Transmissão de informações
 AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
Gliconeogênese. Gliconeogênese. Órgãos e gliconeogênese. Fontes de Glicose. Gliconeogênese. Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia
 Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia Gliconeogênese Alexandre Havt Gliconeogênese Fontes de Energia para as Células Definição Via anabólica que ocorre no fígado e, excepcionalmente
Gliconeogênese Metabolismo dos aminoácidos Ciclo da Uréia Gliconeogênese Alexandre Havt Gliconeogênese Fontes de Energia para as Células Definição Via anabólica que ocorre no fígado e, excepcionalmente
Introdução. Estrutura dos Aminoácidos e Proteínas. Aminoácidos componentes de proteínas. Aminoácidos componentes de proteínas 10/02/2012.
 Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Programa de Pós-Graduação em Química
 1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila
 Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
BÁSICA EM IMAGENS. Aminoácidos, peptídeos e proteínas
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Hierarquia estrutural
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Hierarquia estrutural
Aminoácidos e Peptídeos
 Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Aula 1. Referência. Bancos de Dados. Linguagem x Informação. Introdução a Bioquímica: Biomoléculas. Introdução ao Curso: Aminoácidos.
 Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES
 UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
AMINOÁCIDOS AMINOÁCIDOS AMINOÁCIDOS AMINOÁCIDOS. Estrutura Básica de um Aminoácido
 AMINOÁCIDOS AMINOÁCIDOS São ácidos orgânicos formados por átomos de carbono, hidrogênio, oxigênio e nitrogênio. Alguns tipos de aminoácidos contêm também átomos de enxofre e fósforo que aparecem, portanto
AMINOÁCIDOS AMINOÁCIDOS São ácidos orgânicos formados por átomos de carbono, hidrogênio, oxigênio e nitrogênio. Alguns tipos de aminoácidos contêm também átomos de enxofre e fósforo que aparecem, portanto
PROTEÍNAS. A palavra proteína derivada de proteos, (grego = primeira ou a mais importante)
 PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
Aminoácidos. subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes
 . Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
. Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
Composição química celular
 Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos
 Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Estrutura das Proteínas pode ser descrita em 4 níveis de organização
 PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
Aminoácidos, Péptidos e Proteínas
 Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
MACRONUTRIENTES III PROTEÍNAS
 MACRONUTRIENTES III PROTEÍNAS 1 PROTEÍNAS As proteínas são compostos orgânicos de estrutura complexa e massa molecular elevada, elas são sintetizadas pelos organismos vivos através da condensação de um
MACRONUTRIENTES III PROTEÍNAS 1 PROTEÍNAS As proteínas são compostos orgânicos de estrutura complexa e massa molecular elevada, elas são sintetizadas pelos organismos vivos através da condensação de um
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
Profº Lásaro Henrique
 Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Catabolismo de Aminoácidos em Mamíferos
 Catabolismo de Aminoácidos em Mamíferos O grupo amino e o esqueleto de carbono seguem vias separadas. A amônia é tóxica para os animais As bases moleculares não são totalmente esclarecidas Em humanos,
Catabolismo de Aminoácidos em Mamíferos O grupo amino e o esqueleto de carbono seguem vias separadas. A amônia é tóxica para os animais As bases moleculares não são totalmente esclarecidas Em humanos,
ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial. Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica
 ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica Prof. Diogo Schott diogo.schott@yahoo.com Substâncias orgânicas
ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica Prof. Diogo Schott diogo.schott@yahoo.com Substâncias orgânicas
Aminoácidos e Peptideos
 Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
1164 BIOLOGIA ESTRUTURAL Aula 1 Prof. Dr. Valmir Fadel
 H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
Soluções de Conjunto de Problemas 1
 Soluções de 7.012 Conjunto de Problemas 1 Questão 1 a) Quais são os quatro tipos principais de moléculas biológicas discutidos na aula? Cite uma função importante de cada tipo de molécula biológica na
Soluções de 7.012 Conjunto de Problemas 1 Questão 1 a) Quais são os quatro tipos principais de moléculas biológicas discutidos na aula? Cite uma função importante de cada tipo de molécula biológica na
Você deve desenhar o aminoácido com o grupo amino protonado (pka > 7) e o grupo carboxílico desprotonado (pka <7).
 QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
Introdução aos aminoácidos
 MÓDULO 2 - AULA 8 Aminoácidos não essenciais Aminoácidos essenciais Glicina 11355 mg Lisina 1958 mg Prolina 6808 mg Leucina 1569 mg Hidroxiprolina 5789 mg Valina 1223 mg Ácido Glutâmico 5065 mg Fenilalanina
MÓDULO 2 - AULA 8 Aminoácidos não essenciais Aminoácidos essenciais Glicina 11355 mg Lisina 1958 mg Prolina 6808 mg Leucina 1569 mg Hidroxiprolina 5789 mg Valina 1223 mg Ácido Glutâmico 5065 mg Fenilalanina
RMN em proteínas pequenas
 COSY COrrelated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) mais simples Primeiro experimento 2D proposto (Jeener, 1971) Período de mistura: 1 único pulso de 90 Transferência da coerência entre
COSY COrrelated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) mais simples Primeiro experimento 2D proposto (Jeener, 1971) Período de mistura: 1 único pulso de 90 Transferência da coerência entre
Metabolismo de PROTEÍNAS
 FACULDADE DE CIÊNCIAS E TECNOLOGIA Departamento de Educação Física Metabolismo de PROTEÍNAS Disciplina Nutrição aplicada à Educação Física e ao Esporte Prof. Dr. Ismael Forte Freitas Júnior FORMAÇÃO DAS
FACULDADE DE CIÊNCIAS E TECNOLOGIA Departamento de Educação Física Metabolismo de PROTEÍNAS Disciplina Nutrição aplicada à Educação Física e ao Esporte Prof. Dr. Ismael Forte Freitas Júnior FORMAÇÃO DAS
DIGESTÃO E ABSORÇÃO DAS PROTEÍNAS
 DIGESTÃO E ABSORÇÃO DAS PROTEÍNAS 1 Fenilalanina Valina Aa essenciais Treonina Triptofano Isoleucina Metionina Histidina Lisina Arginina Leucina PROTEÍNAS Alanina Asparagina Aspartato Cisteína Glutamato
DIGESTÃO E ABSORÇÃO DAS PROTEÍNAS 1 Fenilalanina Valina Aa essenciais Treonina Triptofano Isoleucina Metionina Histidina Lisina Arginina Leucina PROTEÍNAS Alanina Asparagina Aspartato Cisteína Glutamato
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III
 Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
Proteínas: aspectos gerais
 Proteínas: aspectos gerais As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (mais de 50% do seu peso seco) As proteínas são omnipresentes na célula, pois estão ligadas a todos
Proteínas: aspectos gerais As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (mais de 50% do seu peso seco) As proteínas são omnipresentes na célula, pois estão ligadas a todos
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
Metabolismo de Proteínas. Tiago Fernandes 2014
 Metabolismo de Proteínas Tiago Fernandes 2014 Proteínas (do grego de primordial importância ) - aa acoplados formam proteínas. - 10 a 12 kg de proteína em um adulto saudável - maior proporção no músculo
Metabolismo de Proteínas Tiago Fernandes 2014 Proteínas (do grego de primordial importância ) - aa acoplados formam proteínas. - 10 a 12 kg de proteína em um adulto saudável - maior proporção no músculo
Graduação em Biotecnologia Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia Aminoácidos Grupos funcionais em bioquímica Propriedades químicas da água Estrutura e
Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia Aminoácidos Grupos funcionais em bioquímica Propriedades químicas da água Estrutura e
Biologia Molecular (Parte I)
 Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
BIOQUÍMICA PARA ODONTO
 BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
A QUÍMICA DOS AMINOÁCIDOS E PEPTÍDEOS
 A QUÍMICA DOS AMINOÁCIDOS E PEPTÍDEOS META Introduzir o estudo do conhecimento das estruturas e das propriedades químicas dos aminoácidos e peptídeos. OBJETIVOS Ao final desta aula, o aluno deverá: reconhecer
A QUÍMICA DOS AMINOÁCIDOS E PEPTÍDEOS META Introduzir o estudo do conhecimento das estruturas e das propriedades químicas dos aminoácidos e peptídeos. OBJETIVOS Ao final desta aula, o aluno deverá: reconhecer
Aminoácidos e proteínas
 Aminoácidos e proteínas Visão geral 2 https://www.youtube.com/watch?v=qbrfimcxznm Importância dessa aula Serina Fosfoserina Treonina Fosfotreonina Fosforilação de resíduos de aa modifica a atividade enzimática
Aminoácidos e proteínas Visão geral 2 https://www.youtube.com/watch?v=qbrfimcxznm Importância dessa aula Serina Fosfoserina Treonina Fosfotreonina Fosforilação de resíduos de aa modifica a atividade enzimática
Aminoácidos e Proteínas
 Aminoácidos e Proteínas PROTEÍNAS As proteínas são as macromoléculas mais abundantes nas células vivas. Ocorrem em todas as células e em todas as partes das mesmas. FUNÇÕES DAS PROTEÍNAS Formam estruturas
Aminoácidos e Proteínas PROTEÍNAS As proteínas são as macromoléculas mais abundantes nas células vivas. Ocorrem em todas as células e em todas as partes das mesmas. FUNÇÕES DAS PROTEÍNAS Formam estruturas
Faculdade Anhanguera Curso de Graduação em Educação Física
 Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: Amabile.arias@anhanguera.com 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
Faculdade Anhanguera Curso de Graduação em Educação Física Profa. Dra. Amabile Vessoni Arias E-mail: Amabile.arias@anhanguera.com 2016-2 Mês de agosto Conteúdo 9 Unidade 1 16 Unidade 1 23 Unidade 1 30
14/02/2017. Genética. Professora Catarina
 14/02/2017 Genética Professora Catarina 1 A espécie humana Ácidos nucleicos Tipos DNA ácido desoxirribonucleico RNA ácido ribonucleico São formados pela união de nucleotídeos. 2 Composição dos nucleotídeos
14/02/2017 Genética Professora Catarina 1 A espécie humana Ácidos nucleicos Tipos DNA ácido desoxirribonucleico RNA ácido ribonucleico São formados pela união de nucleotídeos. 2 Composição dos nucleotídeos
Bioquímica: Componentes orgânicos e inorgânicos necessários à vida. Leandro Pereira Canuto
 Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS
 UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Parte escrita do seminário referente à disciplina Reatividade de Compostos Orgânicos II e Biomoléculas
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Parte escrita do seminário referente à disciplina Reatividade de Compostos Orgânicos II e Biomoléculas
AMINOÁCIDOS.! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico NH2 I R - C - C = 0O I I H OH
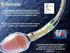 Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
Componentes Químicos das Células
 Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
BIOQUÍMICA. Profº André Montillo
 BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
UNIVERSIDADE FEDERAL DE ALAGOAS ENGENHARIA DE PESCA DISCIPLINA: BIOQUÍMICA AMINOÁCIDOS II SÍNTESE
 UNIVERSIDADE FEDERAL DE ALAGOAS ENGENHARIA DE PESCA DISCIPLINA: BIOQUÍMICA AMINOÁCIDOS II SÍNTESE Dra. Talita Espósito BIOSSINTESE DE AA amônia + H 3 N COO - C H Esqueleto carbônico NH 4 + R COO - aminoácidos
UNIVERSIDADE FEDERAL DE ALAGOAS ENGENHARIA DE PESCA DISCIPLINA: BIOQUÍMICA AMINOÁCIDOS II SÍNTESE Dra. Talita Espósito BIOSSINTESE DE AA amônia + H 3 N COO - C H Esqueleto carbônico NH 4 + R COO - aminoácidos
Metabolismo de aminoácidos de proteínas
 Metabolismo de aminoácidos de proteínas Profa Dra Mônica Santos de Freitas 12.09.2012 1 transporte DE AMINOÁCIDOS DENTRO DA CÉLULA O metabolismo de aminoácidos ocorre dentro da célula; A concentração intracelular
Metabolismo de aminoácidos de proteínas Profa Dra Mônica Santos de Freitas 12.09.2012 1 transporte DE AMINOÁCIDOS DENTRO DA CÉLULA O metabolismo de aminoácidos ocorre dentro da célula; A concentração intracelular
Carla Bittar Bioquímica e Metabolismo Animal
 Carla Bittar Bioquímica e Metabolismo Animal Biosfera rica em N2 Microrganismos reduzem N2 formando NH3 Plantas e microrganismos absorvem NH3 e NO3- para síntese de biomoléculas Animais dependem da dieta
Carla Bittar Bioquímica e Metabolismo Animal Biosfera rica em N2 Microrganismos reduzem N2 formando NH3 Plantas e microrganismos absorvem NH3 e NO3- para síntese de biomoléculas Animais dependem da dieta
Me. Aylan Kener Meneghine Doutorando em Microbiologia Agropecuária
 Me. Aylan Kener Meneghine Doutorando em Microbiologia Agropecuária Setembro - 2013 O ciclo de energia nos seres vivos... Como ocorre a produção de ATP pela oxidação dos diferentes compostos? A oxidação
Me. Aylan Kener Meneghine Doutorando em Microbiologia Agropecuária Setembro - 2013 O ciclo de energia nos seres vivos... Como ocorre a produção de ATP pela oxidação dos diferentes compostos? A oxidação
Aminoácidos. Estrutura e Função das Proteínas UNIDADE I I. VISÃO GERAL II. ESTRUTURA DOS AMINOÁCIDOS COOH C H R
 UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
METABOLISMO DOS AMINOÁCIDOS
 METABOLISMO DOS AMINOÁCIDOS As proteínas ingeridas na dieta são degradadas por enzimas digestivas (pepsina, tripsina, quimotripsina, etc.) até aminoácidos Os aminoácidos são absorvidos pela mucosa intestinal,
METABOLISMO DOS AMINOÁCIDOS As proteínas ingeridas na dieta são degradadas por enzimas digestivas (pepsina, tripsina, quimotripsina, etc.) até aminoácidos Os aminoácidos são absorvidos pela mucosa intestinal,
METABOLISMO DOS AMINOÁCIDOS. Prof. Henning Ulrich
 METABOLISMO DOS AMINOÁCIDOS Prof. Henning Ulrich CATABOLISMO DOS AMINOÁCIDOS EM MAMÍFEROS CATABOLISMO DOS GRUPOS AMINO CATABOLISMO DOS GRUPOS AMINO PORÇÃO DO TRATO DIGESTIVO HUMANO TRANSAMINAÇÕES CATALISADAS
METABOLISMO DOS AMINOÁCIDOS Prof. Henning Ulrich CATABOLISMO DOS AMINOÁCIDOS EM MAMÍFEROS CATABOLISMO DOS GRUPOS AMINO CATABOLISMO DOS GRUPOS AMINO PORÇÃO DO TRATO DIGESTIVO HUMANO TRANSAMINAÇÕES CATALISADAS
Proteínas A U L A 04 - TEÓRICA PROF. DÉBORA CHRISTINA
 Proteínas A U L A 04 - TEÓRICA 04-09- 17 PROF. DÉBORA CHRISTINA CONCEITO As proteínas apresentam funções e estruturas diversificadas e são sintetizadas a partir de apenas 20 aminoácidos diferentes; São
Proteínas A U L A 04 - TEÓRICA 04-09- 17 PROF. DÉBORA CHRISTINA CONCEITO As proteínas apresentam funções e estruturas diversificadas e são sintetizadas a partir de apenas 20 aminoácidos diferentes; São
Prof. Marcelo Langer. Curso de Biologia. Aula Genética
 Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
Bioquímica Celular (parte II) Lipídios Proteínas Vitaminas Ácidos Nucléicos
 Bioquímica Celular (parte II) Lipídios Proteínas Vitaminas Ácidos Nucléicos Lipídios Possuem função energética e estrutural. 2ª fonte de energia do organismo. Apresentam maior quantidade de energia que
Bioquímica Celular (parte II) Lipídios Proteínas Vitaminas Ácidos Nucléicos Lipídios Possuem função energética e estrutural. 2ª fonte de energia do organismo. Apresentam maior quantidade de energia que
Aula 5 Estrutura e função de proteínas
 Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
COMPONENTES ORGÂNICOS: CARBOIDRATOS. Glicídios ou Açúcares
 COMPONENTES ORGÂNICOS: CARBOIDRATOS Glicídios ou Açúcares COMPOSIÇÃO DOS CARBOIDRATOS Compostos constituídos principalmente de: Carbono, Hidrogênio Oxigênio Principal fonte de energia para os seres vivos.
COMPONENTES ORGÂNICOS: CARBOIDRATOS Glicídios ou Açúcares COMPOSIÇÃO DOS CARBOIDRATOS Compostos constituídos principalmente de: Carbono, Hidrogênio Oxigênio Principal fonte de energia para os seres vivos.
Aminoácidos AMINOÁCIDOS, PEPTÍDEOS E PROTEÍNAS. Universidade Federal de Mato Grosso Disciplina de Bioquímica H2N C COOH
 1 2 Universidade Federal de Mato Grosso Disciplina de Bioquímica AMINOÁCIDOS, PEPTÍDEOS E PROTEÍNAS Vagalume (fireflies) Prof. Ms. Reginaldo Vicente Ribeiro Eritrócitos Luciferina Rinoceronte Queratina
1 2 Universidade Federal de Mato Grosso Disciplina de Bioquímica AMINOÁCIDOS, PEPTÍDEOS E PROTEÍNAS Vagalume (fireflies) Prof. Ms. Reginaldo Vicente Ribeiro Eritrócitos Luciferina Rinoceronte Queratina
Aminoácidos. UNIDADE I Estrutura e Função das Proteínas COOH I. VISÃO GERAL II. ESTRUTURA DOS AMINOÁCIDOS. Aminoácido livre
 UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
UNIVERSO TERRA SERES VIVOS ORIGEM
 UNIVERSO TERRA SERES VIVOS ORIGEM BIOLOGIA Surgiu da observação, da curiosidade de se compreender a vida e da utilização da natureza em benefício humano Grande salto com Aristóteles Baseada na observação
UNIVERSO TERRA SERES VIVOS ORIGEM BIOLOGIA Surgiu da observação, da curiosidade de se compreender a vida e da utilização da natureza em benefício humano Grande salto com Aristóteles Baseada na observação
CÓDIGO GENÉTICO E SÍNTESE PROTEICA
 Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA 1. Síntese de proteínas pelos ribossomos a partir do RNAm. a) RNAm: molécula de RNA que contem a informação genética necessária para
Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA 1. Síntese de proteínas pelos ribossomos a partir do RNAm. a) RNAm: molécula de RNA que contem a informação genética necessária para
Corpos cetônicos. Quais são? A partir de qual composto se formam? Como se formam? Quando se formam? Efeitos de corpos cetônicos elevados?
 Corpos cetônicos Quais são? A partir de qual composto se formam? Como se formam? Quando se formam? Efeitos de corpos cetônicos elevados? Importante saber!!!!!!!!!!!! A partir de qual composto se formam?
Corpos cetônicos Quais são? A partir de qual composto se formam? Como se formam? Quando se formam? Efeitos de corpos cetônicos elevados? Importante saber!!!!!!!!!!!! A partir de qual composto se formam?
Proteínas. - Revisão - Prof a. Dr a. Elisa d Avila Costa Cavalcanti. Bromatologia EN/UNIRIO
 Proteínas - Revisão - Prof a. Dr a. Elisa d Avila Costa Cavalcanti Bromatologia EN/UNIRIO 2018.2 O que são proteínas? Aminoácidos α 21 tipos Grupos R Tendência de interagir com a água em ph intracelular
Proteínas - Revisão - Prof a. Dr a. Elisa d Avila Costa Cavalcanti Bromatologia EN/UNIRIO 2018.2 O que são proteínas? Aminoácidos α 21 tipos Grupos R Tendência de interagir com a água em ph intracelular
29/08/2015 QUÍMICA DE PROTEÍNAS. Medicina Veterinária IBGM - IBS. Medicina Veterinária IBGM - IBS
 QUÍMICA DE PROTEÍNAS D i s c i p l i n a : b i o q u í m i c a, p r o f. D r. Va g n e O l i v e i ra E-mail: vagne_melo_oliveira@outlook.com Medicina Veterinária IBGM - IBS Medicina Veterinária IBGM -
QUÍMICA DE PROTEÍNAS D i s c i p l i n a : b i o q u í m i c a, p r o f. D r. Va g n e O l i v e i ra E-mail: vagne_melo_oliveira@outlook.com Medicina Veterinária IBGM - IBS Medicina Veterinária IBGM -
Bioinformática Estrutural Aula 1
 Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária Paula.kuser-falcao@embrapa.br Pratique Atividade Física Paula
Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária Paula.kuser-falcao@embrapa.br Pratique Atividade Física Paula
AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES
 Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
COLÉGIO PEDRO II CAMPUS TIJUCA II. DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI
 COLÉGIO PEDRO II CAMPUS TIJUCA II DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI 1º & 2º TURNOS 3ª SÉRIE / ENSINO MÉDIO REGULAR & INTEGRADO ANO LETIVO 2015 PROFESSORES: FRED & PEDRO
COLÉGIO PEDRO II CAMPUS TIJUCA II DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI 1º & 2º TURNOS 3ª SÉRIE / ENSINO MÉDIO REGULAR & INTEGRADO ANO LETIVO 2015 PROFESSORES: FRED & PEDRO
Lista de Exercícios de Bioquímica
 Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Professor Antônio Ruas
 Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Entendem-se por compostos heterocíclicos, aqueles compostos orgânicos cíclicos estáveis, que contem no seu anel um ou mais átomos diferentes do
 1 2 3 Entendem-se por compostos heterocíclicos, aqueles compostos orgânicos cíclicos estáveis, que contem no seu anel um ou mais átomos diferentes do carbono. 4 5 O prefixo ribo também é aceitável para
1 2 3 Entendem-se por compostos heterocíclicos, aqueles compostos orgânicos cíclicos estáveis, que contem no seu anel um ou mais átomos diferentes do carbono. 4 5 O prefixo ribo também é aceitável para
HNT 130 Nutrição Normal
 PROTEÍNAS definição, classificação, avaliação da qualidade protéica, funções e metabolismo. HNT 130 Nutrição Normal NUTRIÇÃO NORMAL Combinação dos processos pelos quais os organismos vivos recebem e utilizam
PROTEÍNAS definição, classificação, avaliação da qualidade protéica, funções e metabolismo. HNT 130 Nutrição Normal NUTRIÇÃO NORMAL Combinação dos processos pelos quais os organismos vivos recebem e utilizam
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
