9.1 O ESPECTRO ELETROMAGNÉTICO E A EXCITAÇÃO MOLECULAR
|
|
|
- Bruno Affonso Covalski
- 7 Há anos
- Visualizações:
Transcrição
1 O ESPECTRO ELETROMAGNÉTICO E A EXCITAÇÃO MOLECULAR A radiação infravermelha corresponde à parte do espectro eletromagnético entre as regiões do visível e das microondas (figura 9.01). A porção de maior utilidade para a análise de grupos funcionais de estruturas orgânicas, esta situada entre 4000 e 400 cm -1. A espectroscopia no infravermelho, fornece evidencias da presença de vários grupos funcionais na estrutura orgânica devido à interação das moléculas ou átomos com a radiação eletromagnética em um processo de vibração molecular (figura 9.01). As ligações covalentes que constituem as moléculas orgânicas estão em constantes movimentos axiais e angulares. A radiação no infravermelho faz com que átomos e grupos de átomos de compostos orgânicos vibrem com amplitude aumentada ao redor das ligações covalentes que os ligam. O processo é quantizado, porém o espectro vibracional costuma aparecer como uma serie de bandas, porque a cada mudança de nível de energia vibracional corresponde uma série de mudanças de níveis de energia rotacional, desta forma, as linhas se sobrepõem dando origem às bandas observadas no espectro. As posições das bandas no espectro podem ser apresentadas em número de ondas, utilizando a unidade centímetro inverso ( cm -1 ) ou em micrômetros (2,5-16 µm).
2 ESPECTRÔMETRO A radiação no infravermelho atravessa a amostra a ser analisada, a radiação transmitida é comparada com aquela transmitida na ausência de amostra. O espectrômetro (figura 9.02) registra o resultado na forma de uma banda de absorção. Um espectrômetro de grande sensibilidade é o espectrômetro com transformada de Fourier (FTIR), que empregam um interferômetro de Michelson, que tem a finalidade de dividir o feixe da radiação da fonte de infravermelho de tal forma que ele reflita simultaneamente a partir de um espelho em movimento e de um espelho fixo. Os feixes refletidos voltam a se combinar e passam através da amostra para o detector e são reproduzidos na forma de um gráfico de tempo contra a intensidade do sinal denominado de interferograma. Figura 9.02 Espectrômetro com transformada de Fourier.(Solomons, 2005)
3 FORMA DO ESPECTRO A radiação infravermelha quando absorvida por uma molécula orgânica, converte-se em energia de vibração molecular. O espectro reflete o movimento vibracional e costuma aparecer em forma de bandas. Energia incidente Radiação infravermelha E I Molécula absorve a energia e a converte em energia de vibração molecular E T Energia transmitida Energia transmitida Transmitância = Energia incidente A localização de uma banda de absorção no infravermelho pode ser especificada em unidades relacionadas com a freqüência ( ) pelo seu comprimento de onda ( ) medidos em centímetro ou através de seu comprimento de onda ( ) medidos em micrômeros: = 1/ ( em cm) ou = 10000/ ( em m). A intensidade da banda é medida pela transmitância ou pela absorvância. A transmitância é definida pela razão entre a energia transmitida e a energia incidente na amostra analisada e a absorvância é o logaritmo na base dez do recíproco da transmitância: T = Et / Ei A = log 1 / T A possibilidade de dois compostos diferentes terem o mesmo espectro no infravermelho é improvável, é por este motivo, que cada função orgânica apresenta no espectro a região de impressão digital na faixa de cm -1. A figura 9.3 mostra o espectro do octano, perceba que a intensidade da banda esta vinculada à transmitância (eixo das ordenadas) enquanto que a localização da banda é percebida no eixo das abicissas e é apresentada em número de onda (figura 9.03). Figura 9.03 espectro do octano. (Solomons, 2005).
4 VIBRAÇÕES MOLECULARES A energia fornecida pela radiação no infravermelho é da ordem de 2 a 15 Kcal e tende a afetar os níveis vibracionais de uma ligação química. As vibrações moleculares (figura 9.04) podem ser de dois tipos: deformações axiais e deformações angulares. Quando a deformação ocorre na direção do eixo da molécula, à distância interatômica aumenta e diminui alternadamente e o modo de vibração é denominado estiramento ou deformação axial. As vibrações de deformação angular correspondem ao movimento de um grupo de átomos em relação ao resto da molécula, sem que as posições relativas dos átomos do grupo se alterem. Essa de formações recebem a denominação de deformação angular simétrica e assimétrica no plano e deformação angular simétrica e assimétrica fora do plano cm cm -1 Deformação axial simétrica do CO 2 Deformação axial assimétrica do CO 2 Aumentando a distancia interatômica Diminuindo e aumentando a distancia interatômica 1465 cm cm -1 Deformação angular simétrica no plano do CH 2 denominada de tesoura Deformação angular assimétrica no plano do CH 2 denominada de balanço Figura 9.04.Deformações angulares. 9.5 ESTIMATIVA MATEMÁTICA PARA FREQÜÊNCIA DE ABSORÇÃO A rigidez das ligações é medida pela constante de força K. Esta é a mesma constante da lei de Hooke para força de restauração de uma mola. Força = K x deslocamento. Em suas vibrações, as ligações covalentes comportam-se como se fossem molas minúsculas conectando os átomos, quando os átomos vibram, elas podem vibrar apenas em determinadas freqüências, como se as ligações estivessem sintonizadas. Em função disso, os átomos ligados covalentemente têm apenas níveis de energia vibracionais específicos. A excitação de uma molécula de um nível de energia vibracional para outro ocorre apenas quando o composto absorve a radiação no infravermelho de uma energia específica, significando um comprimento de onda ou freqüência específico, desde que: E = h. v
5 191 A freqüência de uma determinada vibração de estiramento em um espectro no infravermelho pode estar relacionada aos seguintes fatores: massa relativa dos átomos; constante de força das ligações; geometria dos átomos. Átomos leves vibram a freqüências mais altas do que os átomos mais pesados. As ligações triplas são mais rígidas do que as duplas, que são mais rígidas que as ligações simples, logo as ligações triplas vibram a freqüências mais altas. O valor numérico da freqüência de absorção pode ser estimado através da equação matemática derivada da lei de Hooke. = 1 2 C f M x. M y M x.+m y 1 2 frequência vibracional em cm -1 C velocidade da luz em cm / seg f constante de força da ligação em dinas/cm M x e M y massas dos átomos X e Y em gramas 9.6 FREQÜÊNCIA DOS MODOS DE VIBRAÇÃO DE ALGUMAS LIGAÇÕES Observe a freqüência de estiramento de alguns grupos envolvendo o hidrogênio (átomo leve), ocorrem a freqüências relativamente altas. As ligações formadas por carbonos com hibridação sp ocorrem na faixa de cm -1 (figura 9.05). Ligação Função Faixa de absorção(cm -1 ) O H Acool, fenol, enol, acido carboxilico , aguda aberta R2NH Aminas secundarias, 1 banda , media NH2 Amina primarias. 2 bandas , media C H Em alcanos , forte C H Em alcenos CO C H Em aldeidos , C C, C N Alcinos e nitrilas R2C=O Em carbonilas H2C=CH2 Em alcenos C=C Em aromáticos , Figura Freqüência de absorção de alguns grupos funcionais Região de estiramento axial, cm -1. Bandas fortes nesta região indicam a presença do grupo OH, NH e Carbono-Hidrogênio. Bandas fracas são na região de cm -1 podem indicar o estiramento axial da ligação CH do grupo formila de aldeídos. Bandas fortes em torno de 2900 cm -1 aparecem em quase todos os espectros de compostos orgânicos, pois são decorrentes da presença do estiramento C H. Região de estiramento da carbonila, cm -1 (figura 9.05).
6 192 Bandas fortes nesta região indicam a presença do grupo carbonila dos diversos compostos carbonilados. Essas absorções são deslocadas de 30 40cm -1 para freqüências mais baixas em sistemas α,β insaturados. Região de absorção de núcleos aromáticos, cm -1. Bandas fortes nesta região indicam a presença da vibração angular fora do plano de C H de aromáticos. A confirmação do anel aromático é feita na região de cm -1, através da banda de absorção da ligação C=C do anel.região de Nitrilas e alcinos, cm -1. Bandas fortes ou medias nesta região indicam a presença da absorção da ligação C C e C N de alcinos e nitrilas respectivamente. Região de estiramento de C O, Bandas fortes nesta região indicam presença da ligação C O de álcool, éteres e etc GRUPOS FUNCIONAIS CARBONILADOS Um grupo que fornece um pico de absorção notável nos espectros no IV é o grupo carbonila. Esse grupo está presente nos aldeídos, nas cetonas, nos éteres, nos ácidos carboxílicos, nas amidas, assim por diante. A freqüência de estiramento da ligação dupla carbono-oxigênio dá um pico forte entre 1630 e 1850 cm -1. A localização exata do pico depende-se se ele é originário de uma cetona, de um aldeído, de um acido carboxílico, e assim por diante (figura 9.06). O O O R H O R R O R OH Aldeído Cetona Ácido carboxílico 1725 cm -1 R OR 1715 cm -1 R NH cm -1 Éster Amida 1735 cm cm -1 Figura 9.06.Banda de absorção de carbonila de algumas funções. 9.7 ESPECTRO DE ALGUMAS FUNÇÕES ORGÂNICAS As regiões mais importantes do espectro de infravermelho estão envolvendo o início e o final do espectro, e compreendem as faixas de cm -1 (2,5-7,7 µm) e cm -1 (11-15,4 µm). A região inicial, de alta energia é chamada região dos grupamentos funcionais, aqui se encontra as absorções de hidroxila de álcool, acido carboxílico, fenol, enol, vibrações de NH de aminas primárias e secundárias, grupo carbonila e outros. A ausência de bandas fortes na região de cm -1 (11-15,4 µm) indica ausência de esqueleto aromático na estrutura. A região intermediária, que compreende a faixa de cm -1 (7,7-11µm) é conhecida como região de impressão digital por ser muito importante para a determinação da estrutura.
7 COMPOSTOS AROMÁTICOS O espectro de compostos aromáticos apresenta na região de 5-6 micrometros as chamadas bandas de combinação. Na região de cm -1 aparecem as bandas de absorção de CH angular fora do plano, essas bandas mostram informações a respeito da posição dos substituintes no anel. Na faixa de cm -1 estão localizadas as bandas de C = C do anel. Bandas de combinação Deformação angular no plano da ligação -CH 7,70-10 m ou cm-1 Estiramento ou deformação axial,c = C do anel Figura Espectro do tolueno. (Pavia, 1996). -CH angular fora do plano Espectro de composto aromático dissubstituído (posição orto). Banda de -CH angular fora do plano de aromático com substituinte em posição orto. R R As ligações carbono-hidrogênio do anel são responsáveis por uma banda intensa de absorção angular fora do plano de -CH, na região cm -1
8 194 Bandas de combinação -C = C do anel -CH angular fora do plano Figura Espectro do 1,2-dimetilbenzeno.(Pavia, 1996). Composto aromático dissubstituído (posição meta). Bandas de combinação C = C do anel -CH angular fora do plano Figura Espectro do 1,3-dimetilbenzeno. (Pavia, 1996). Banda de -CH angular fora do plano de aromático com substituintes em meta. R As ligações carbono-hidrogênio do anel são responsáveis por três bandas de absorção angular fora do plano de -CH, na região cm -1 R Finalmente o composto aromático dissubstituído (posição para) apresenta uma única banda de absorção no infravermelho.
9 R Espectroscopia na Região do Infravermelho Banda de -CH angular fora do plano de aromático dissubstituído. 195 As ligações carbono-hidrogênio do anel são responsáveis por uma banda intensa, de absorção angular fora do plano de -CH, na região cm -1 R Bandas de combinação C = C do anel -CH angular fora do plano Figura Espectro do 1,4-dimetilbenzeno. (Pavia,1996) ÁLCOOIS E FENÓIS Os grupos hidroxila de álcoois e fenóis são também fáceis de reconhecer nos espectros no infravermelho através de suas absorções de estiramento O H (figura 9.11). Essas ligações fornecem também evidencias diretas para a ligação de hidrogênio.
10 196 Figura Espectro do 2-butanol. (Pavia, 1996). Se um álcool ou fenol está presente como uma solução muito diluída em um solvente que não pode contribuir para a ligação de hidrogênio, a absorção O H ocorre como um pico muito pronunciado na região cm -1. As vibrações de estiramento axial da ligação C O em álcoois e fenóis se encontram na região de cm -1 (7,93-10 µm). A vibração angular no plano da ligação O H aparece na região de cm -1 (7,93-10 µm). Figura 9.12.Espectro do p-hidróxitolueno. (Pavia, 1996). Figura Espectro do hexanol (Brown, 1995).
11 197 OH C-H de Csp 3 C-O Figura Espectro do metanol. (McMurry, 2005). OH CH de Csp 3 C-O Figura Espectro do Ciclopentanol (Fessenden, 1982) ESPECTRO DE ÁCIDOS CARBOXÍLICOS Os dímeros de ácidos carboxílicos produzem uma absorção de deformação axial do grupo hidroxila de forma intensa e muito larga na região de cm -1. As bandas de estiramento ou deformação axial aparecem superpostas com a banda da hidroxila.a banda de estiramento axial de carbonila, para ácidos carboxílicos alifáticos saturados é cerca de 1760 cm -1.
12 198 Figura Espectro do ácido propanóico. (Solomons, 2005) Figura 9.17.Espectro do ácido pentanóico. (Bruice, 2006). Figura Ácido heptanóico.(silverstein, 1979) ALDEÍDOS E CETONAS As cetonas normalmente mostram uma freqüência de absorção de carbonila por volta de1715 cm -1 enquanto que a carbonila de aldeído se apresenta em torno de 1725cm -1. O espectro da butanona apresenta a vibração de estiramento axial da ligação C- H por volta de 3000 cm -1. O grupo carbonila mostra vibração molecular em torno de 1715 cm -1.
13 199 -CH de Csp 3 Vibração axial e angular de C-CO-C Vibração angular de -CH Figura Espectro da butanona. (Fessenden, 1982). O grupo carbonila de aldeído mostra banda de absorção na região de cm -1. A substituição de hidrogênio alfa por um átomo eletronegativo aumenta a freqüência de absorção. O acetaldeído absorve em 1730 cm -1 e o tricloroacetaldeído em 1768 cm -1. A presença de insaturação em aldeídos α, β insaturados desloca a absorção de carbonila para 1685 cm -1. Os aldeídos apresentam duas bandas de deformação axial de CH do grupo formila na região de cm -1. Quando existe a ocorrência de espectros de isômeros de função, esta banda por ser característica de aldeído, serve para diferenciar um aldeído de uma cetona. Figura Espectro do butiraldeído. (Fessenden, 1982) AMINAS Soluções muito diluídas de aminas primárias e secundárias também fornecem picos pronunciados na região de cm -1 originários de vibrações de estiramento N H livres. A amina primaria fornece dois picos pronunciados originários do estiramento simétrico e assimétrico das duas ligações
14 200 N H; a amina secundaria origina apenas uma absorção de estiramento. A amina terciária, uma vez que não têm ligação N H, não absorve nessa região. O espectro no infravermelho das aminas primária, secundária e terciária estão nas figuras 8.21, 8.22, 8.23 e Deformação axial de -NH Deformação angular simétrica de -NH Estiramento axial de -CH de Csp 3 Vibração angular simétrica de -CH 2 Figura Espectro da propilamina. (Fessenden, 1982). As aminas secundárias apresentam uma única banda fraca na região cm -1 (2,98 3,02 µm). A formação de ligação hidrogênio desloca estas bandas de absorção para comprimentos de onda maiores. Deformação axial de -NH Estiramento de -CH de Csp 3 Deformação angular simétrica de -CH 2 Figura Espectro da dipropilamina. (Fessenden, 1982). A amina terciária não mostra banda na região de cm -1. As bandas de absorção da ligação C-N não conjugada, em aminas primária, secundaria e terciária costumam aparecer na região entre cm -1 e são bandas de intensidade média a fraca.
15 201 Figura Tripropilamina. (Fessenden, 1982). Figura Isopentilamina.(Bruice, 2006). Sugestão de leitura SOLOMONS, Graham; FRYHLE, Craig. Química Orgánica. Tradução da 10 a edição americana, vols 1 e 2. Rio de Janeiro: Livros Técnicos e Científicos Editora S. A., p. BRUICE, Paula. Química Orgânica. Tradução da quarta edição. São Paulo: Pearson Prentice Hall, p.
Espectroscopia no IV
 Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Espectroscopia no IV Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Região do Infravermelho na
Espectroscopia no Infravermelho (IR)
 Espectroscopia no Infravermelho (IR) INFRARED (IR) 0,78 µm a 1000 µm 12800 cm -1 a 10 cm -1 Região Comprimento de onda (µm) Número de onda (cm -1 ) Frequência (Hz) Próximo 0,78 a 2,5 12800 a 4000 3,8 x
Espectroscopia no Infravermelho (IR) INFRARED (IR) 0,78 µm a 1000 µm 12800 cm -1 a 10 cm -1 Região Comprimento de onda (µm) Número de onda (cm -1 ) Frequência (Hz) Próximo 0,78 a 2,5 12800 a 4000 3,8 x
TABELA DE VALORES DE ABSORÇÃO NO INFRAVERMELHO PARA COMPOSTOS ORGÂNICOS
 TABELA DE VALORES DE ABSORÇÃO NO INFRAVERMELHO PARA COMPOSTOS ORGÂNICOS 1) 3.600-2.700 cm -1 A absorção nesta região é associada às vibrações de deformação axial nos átomos de hidrogênio ligados a carbono,
TABELA DE VALORES DE ABSORÇÃO NO INFRAVERMELHO PARA COMPOSTOS ORGÂNICOS 1) 3.600-2.700 cm -1 A absorção nesta região é associada às vibrações de deformação axial nos átomos de hidrogênio ligados a carbono,
Análise Estrutural. José Carlos Marques Departamento de Química Universidade da Madeira
 Análise Estrutural José Carlos Marques Departamento de Química Universidade da Madeira Programa Espectroscopia interacção luz /átomos-moléculas Espectroscopia UV-vis transições electrónicas determinação
Análise Estrutural José Carlos Marques Departamento de Química Universidade da Madeira Programa Espectroscopia interacção luz /átomos-moléculas Espectroscopia UV-vis transições electrónicas determinação
Aula 2. Organic Chemistry. Espectroscopia UV-VIS e Infravermelho. 4 th Edition Paula Yurkanis Bruice
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 2 Espectroscopia UV-VIS e Infravermelho Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Radiação Eletromagnética E
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 2 Espectroscopia UV-VIS e Infravermelho Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Radiação Eletromagnética E
Prof. Aloísio J.B. Cotta
 Prof. Aloísio J.B. Cotta e-mail: acotta@ceunes.ufes.br Bibliografia: Cap 26 do SKOOG ou Cap 16 Princípios de Análise Instrumental Cap 18 Infravermelho Todos os comprimentos de onda do espectro eletromagnético
Prof. Aloísio J.B. Cotta e-mail: acotta@ceunes.ufes.br Bibliografia: Cap 26 do SKOOG ou Cap 16 Princípios de Análise Instrumental Cap 18 Infravermelho Todos os comprimentos de onda do espectro eletromagnético
Região do Espectro Eletromagnético
 Região do Espectro Eletromagnético Região do Espectro Eletromagnético Raios X UV / V Infravermelho Microonda Radiofrequência Transição Quebra de ligação Eletrônica Vibracional Rotacional Spin nuclear (RMN),
Região do Espectro Eletromagnético Região do Espectro Eletromagnético Raios X UV / V Infravermelho Microonda Radiofrequência Transição Quebra de ligação Eletrônica Vibracional Rotacional Spin nuclear (RMN),
Espectroscopia Vibracional
 Espectroscopia Vibracional Infravermelho (IV) Difusão de Raman (R) Vibrações moleculares Transições vibracionais Região do Infravermelho 12820 4000 400 Número de onda (cm -1 ) 33 IVP IVM IVL IVP IV próximo;
Espectroscopia Vibracional Infravermelho (IV) Difusão de Raman (R) Vibrações moleculares Transições vibracionais Região do Infravermelho 12820 4000 400 Número de onda (cm -1 ) 33 IVP IVM IVL IVP IV próximo;
Química Orgânica. Profª Drª Cristiane de Abreu Dias
 Química Orgânica Profª Drª Cristiane de Abreu Dias Composição dos Compostos Orgânicos Características Gerais dos Compostos Orgânicos Capacidade de formar Cadeias Representação usual das Cadeias Carbônicas
Química Orgânica Profª Drª Cristiane de Abreu Dias Composição dos Compostos Orgânicos Características Gerais dos Compostos Orgânicos Capacidade de formar Cadeias Representação usual das Cadeias Carbônicas
QUÍMICA Prof. Alison Cosme Souza Gomes. Funções Orgânicas Resumo UERJ
 QUÍMICA Prof. Alison Cosme Souza Gomes Funções Orgânicas Resumo UERJ A Química Orgânica é a parte da química que estuda os diversos compostos de carbonos existentes. São compostos com sua base nos átomos
QUÍMICA Prof. Alison Cosme Souza Gomes Funções Orgânicas Resumo UERJ A Química Orgânica é a parte da química que estuda os diversos compostos de carbonos existentes. São compostos com sua base nos átomos
Espectrometria de massas
 Espectrometria de massas Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Espectrometria de Massas
Espectrometria de massas Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Espectrometria de Massas
Métodos Físicos de Análise - ESPECTROFOTOMETRIA NO INFRAVERMELHO
 Métodos Físicos de Análise - ESPECTROFOTOMETRIA NO INFRAVERMELHO Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos
Métodos Físicos de Análise - ESPECTROFOTOMETRIA NO INFRAVERMELHO Prof. Dr. Leonardo Lucchetti Mestre e Doutor em Ciências Química de Produtos Naturais NPPN/UFRJ Depto. de Química de Produtos Naturais Farmanguinhos
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA CONCEITOS BÁSICOS DE ESPECTROSCOPIA
 QFL5947-1onceitos Básicos de Espectroscopia 2011-2 UNIVERIDADE DE Ã PAUL INTITUT DE QUÍMIA Programa de Pós-Graduação em Química NEIT BÁI DE EPETRPIA QFL5947-1 3 a Prova de I.V.-Raman-2011 ETR AGUILAR VITRIN
QFL5947-1onceitos Básicos de Espectroscopia 2011-2 UNIVERIDADE DE Ã PAUL INTITUT DE QUÍMIA Programa de Pós-Graduação em Química NEIT BÁI DE EPETRPIA QFL5947-1 3 a Prova de I.V.-Raman-2011 ETR AGUILAR VITRIN
Absorções de grupos funcionais na região do Infravermelho
 Intensidade Deformação/Observação Grupo requência cm -1 Alcanos 2840-3000 C-H axial -CH 3 2970-2950 C-H axial assimétrica ( as ) -CH 3 2880-2860 C-H axial simétrica ( s ) -CH 3 1735 C-H angular simétrica
Intensidade Deformação/Observação Grupo requência cm -1 Alcanos 2840-3000 C-H axial -CH 3 2970-2950 C-H axial assimétrica ( as ) -CH 3 2880-2860 C-H axial simétrica ( s ) -CH 3 1735 C-H angular simétrica
Pré UFSC Química. Química Orgânica. Alcinos. Funções Orgânicas. Alcadienos. Hidrocarbonetos. Alcanos. Cicloalcanos. Alcenos.
 Química Orgânica Estuda as propriedades e composição dos compostos que apresentam o carbono como principal elemento químico. Alcinos São hidrocarbonetos acíclicos contendo uma única ligação tripla entre
Química Orgânica Estuda as propriedades e composição dos compostos que apresentam o carbono como principal elemento químico. Alcinos São hidrocarbonetos acíclicos contendo uma única ligação tripla entre
Análise de Alimentos II Espectroscopia de Absorção Molecular
 Análise de Alimentos II Espectroscopia de Absorção Molecular Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 2 Introdução A absorção de radiação no UV/Vis por uma espécie química (M) pode
Análise de Alimentos II Espectroscopia de Absorção Molecular Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 2 Introdução A absorção de radiação no UV/Vis por uma espécie química (M) pode
Introdução à Química Orgânica. Ana Clara Vasconcelos Helber Cardoso Heloísa Miranda Edirley Maruzo Costa Michelle Rodrigues Thaís Andrade
 Introdução à Química Orgânica Ana Clara Vasconcelos Helber Cardoso Heloísa Miranda Edirley Maruzo Costa Michelle Rodrigues Thaís Andrade Química Orgânica é o ramo da Química que estuda os compostos de
Introdução à Química Orgânica Ana Clara Vasconcelos Helber Cardoso Heloísa Miranda Edirley Maruzo Costa Michelle Rodrigues Thaís Andrade Química Orgânica é o ramo da Química que estuda os compostos de
Estrutura de moléculas orgânicas e biológicas
 Hidrocarbonetos Os hidrocarbonetos são compostos orgânicos formados exclusivamente por átomos de carbono e hidrogénio, ligados por ligações covalentes simples (C H e C C), duplas (C = C) ou triplas (C
Hidrocarbonetos Os hidrocarbonetos são compostos orgânicos formados exclusivamente por átomos de carbono e hidrogénio, ligados por ligações covalentes simples (C H e C C), duplas (C = C) ou triplas (C
Química Orgânica. Química orgânica: Estrutura das moléculas. Grupos funcionais. Estereoquímica. Reatividade..
 Química Orgânica X Química orgânica: Estrutura das moléculas. Grupos funcionais. Estereoquímica. Reatividade.. Química Orgânica Os compostos orgânicos são as substâncias químicas que contêm carbono e hidrogénio,
Química Orgânica X Química orgânica: Estrutura das moléculas. Grupos funcionais. Estereoquímica. Reatividade.. Química Orgânica Os compostos orgânicos são as substâncias químicas que contêm carbono e hidrogénio,
Questão 01 - Em qual região do espectro você encontraria uma banda C=C?
 Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Diretoria de Graduação e Educação Profissional Departamento Acadêmico de Química e Biologia Segunda Lista de Exercícios
Ministério da Educação Universidade Tecnológica Federal do Paraná Campus de Curitiba Diretoria de Graduação e Educação Profissional Departamento Acadêmico de Química e Biologia Segunda Lista de Exercícios
Espetroscopia Molecular (QT)
 Espetroscopia Molecular (QT) Exercícios 1. Considere duas ondas com λ=700 nm e 450 nm, respetivamente. Calcule: a) as frequências de cada uma em s -1. b) os seus números de onda. c) os seus períodos associados
Espetroscopia Molecular (QT) Exercícios 1. Considere duas ondas com λ=700 nm e 450 nm, respetivamente. Calcule: a) as frequências de cada uma em s -1. b) os seus números de onda. c) os seus períodos associados
QUÍMICA ORGÂNICA parte 1
 QUÍMICA ORGÂNICA parte 1 1 QUÍMICA ORGÂNICA Cafeína Vinagre Glicose (É o ramo da Química que estuda os compostos do CARBONO) 2 CLASSIFICAÇÃO DO CARBONO Carbono primário Ligado diretamente, no máximo, a
QUÍMICA ORGÂNICA parte 1 1 QUÍMICA ORGÂNICA Cafeína Vinagre Glicose (É o ramo da Química que estuda os compostos do CARBONO) 2 CLASSIFICAÇÃO DO CARBONO Carbono primário Ligado diretamente, no máximo, a
ia p sco ctro e sp E
 Espectroscopia Onda electromagnética A onda electromagnética resulta da associação de um campo eléctrico alternado com um campo magnético(em planos perpendiculares) a componente eléctrica é responsável
Espectroscopia Onda electromagnética A onda electromagnética resulta da associação de um campo eléctrico alternado com um campo magnético(em planos perpendiculares) a componente eléctrica é responsável
Gabaritos Resolvidos Energia Química Semiextensivo V4 Frente E
 01) D A preferência de substituição obedece a ordem: C terciário C secundário C primário. A halogenação de um alcano se dá por substituição de um átomo de hidrogênio por um halogênio, resultando em um
01) D A preferência de substituição obedece a ordem: C terciário C secundário C primário. A halogenação de um alcano se dá por substituição de um átomo de hidrogênio por um halogênio, resultando em um
Interpretação de Espectros de Infravermelho
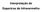 Interpretação de Espectros de Infravermelho Frequências aproximadas de Absorção no Infravermelho correspondentes aos movimentos de Stretching de ligações X-H (cm -1 ) B-H 2400 C-H 3000 N-H 3400 O-H 3600
Interpretação de Espectros de Infravermelho Frequências aproximadas de Absorção no Infravermelho correspondentes aos movimentos de Stretching de ligações X-H (cm -1 ) B-H 2400 C-H 3000 N-H 3400 O-H 3600
Gabaritos Resolvidos Energia Química Semiextensivo V3 Frente D
 01) B Composto A: éter Composto B: fenol Composto C: álcool Fórmula molecular dos 3 compostos: C 7 H 8 O Compostos de mesma fórmula molecular e função química diferente isomeria de função. 02) B I. Álcool
01) B Composto A: éter Composto B: fenol Composto C: álcool Fórmula molecular dos 3 compostos: C 7 H 8 O Compostos de mesma fórmula molecular e função química diferente isomeria de função. 02) B I. Álcool
Análise Estrutural. José Carlos Marques Departamento de Química Universidade da Madeira
 Análise Estrutural José Carlos Marques Departamento de Química Universidade da Madeira Programa Espectroscopia interacção luz /átomos-moléculas Espectroscopia UV-vis transições electrónicas determinação
Análise Estrutural José Carlos Marques Departamento de Química Universidade da Madeira Programa Espectroscopia interacção luz /átomos-moléculas Espectroscopia UV-vis transições electrónicas determinação
LICENCIATURA EM QUÍMICA QUÍMICA ORGÂNICA I SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira
 LICENCIATURA EM QUÍMICA QUÍMICA ORGÂNICA I SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira EMENTA QUÍMICA ORGÂNICA I Introdução a química orgânica: teoria estrutural e o átomo de carbono
LICENCIATURA EM QUÍMICA QUÍMICA ORGÂNICA I SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira EMENTA QUÍMICA ORGÂNICA I Introdução a química orgânica: teoria estrutural e o átomo de carbono
FUNÇÕES ORGÂNICAS. É um conjunto de compostos que apresentam propriedades químicas semelhantes.
 FUNÇÕES RGÂNIAS É um conjunto de compostos que apresentam propriedades químicas semelhantes. Hidrocarbonetos ompostos formados por somente hidrogênio e carbono. São apolares, portanto: Insolúveis em água
FUNÇÕES RGÂNIAS É um conjunto de compostos que apresentam propriedades químicas semelhantes. Hidrocarbonetos ompostos formados por somente hidrogênio e carbono. São apolares, portanto: Insolúveis em água
Espectroscopia no Inf n ra r v a e v r e m r e m l e h l o
 Espectroscopia no Infravermelho A chamada radiação no infravermelho (IV) A chamada radiação no infravermelho (IV) corresponde aproximadamente a parte do espectro eletromagnético situado entre as regiões
Espectroscopia no Infravermelho A chamada radiação no infravermelho (IV) A chamada radiação no infravermelho (IV) corresponde aproximadamente a parte do espectro eletromagnético situado entre as regiões
Química D Intensivo V. 1
 Química D Intensivo V. 1 Exercícios 01) A 07) B Na síntese de Wöhler, o cianato de amônio (inorgânico) foi transformado em ureia (orgânica). 02) 63 01. Certa. 02. Certa. 04. Certa. 08. Certa. 16. Certa.
Química D Intensivo V. 1 Exercícios 01) A 07) B Na síntese de Wöhler, o cianato de amônio (inorgânico) foi transformado em ureia (orgânica). 02) 63 01. Certa. 02. Certa. 04. Certa. 08. Certa. 16. Certa.
Química D Semiextensivo V. 2
 GABARIT Semiextensivo V. Exercícios 0) A Etanol: Et: dois carbonos. an: ligações simples entre os carbonos. ol: terminação característica do grupo dos álcoois. 0) 0. Errada. Se a hidroxila () estiver em
GABARIT Semiextensivo V. Exercícios 0) A Etanol: Et: dois carbonos. an: ligações simples entre os carbonos. ol: terminação característica do grupo dos álcoois. 0) 0. Errada. Se a hidroxila () estiver em
Espectroscopia de IV. Para que um modo vibracional seja activo no IV tem que estar associado a variações do momento dipolar da molécula.
 A espectroscopia de infravermelhos (IV) baseia-se na observação de que as ligações químicas apresentam frequências específicas às quais vibram, a níveis de energia bem definidos. Estas frequências de vibração,
A espectroscopia de infravermelhos (IV) baseia-se na observação de que as ligações químicas apresentam frequências específicas às quais vibram, a níveis de energia bem definidos. Estas frequências de vibração,
QUÍMICA ORGÂNICA PARTE1 PROFESSOR: JOÃO RODRIGO ESCALARI QUINTILIANO
 QUÍMICA ORGÂNICA PARTE1 PROFESSOR: JOÃO RODRIGO ESCALARI QUINTILIANO 1 QUÍMICA ORGÂNICA Cafeína Vinagre Glicose (É o ramo da Química que estuda os compostos do CARBONO) 2 CLASSIFICAÇÃO DO CARBONO Carbono
QUÍMICA ORGÂNICA PARTE1 PROFESSOR: JOÃO RODRIGO ESCALARI QUINTILIANO 1 QUÍMICA ORGÂNICA Cafeína Vinagre Glicose (É o ramo da Química que estuda os compostos do CARBONO) 2 CLASSIFICAÇÃO DO CARBONO Carbono
Ressonância Magnética Nuclear
 Ressonância Magnética Nuclear Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Raios-X são as radiações
Ressonância Magnética Nuclear Bibliografia: Pavia, D.L. et al., Introdução à Espectroscopia, Ed. Cengage Learning, 2010. Bruice, P.Y. et al., Química Orgânica, Ed. Prendice Hall, 2004. Raios-X são as radiações
O DIAMANTE POSSUI HIBRIDIZAÇÃO
 QUÍMICA ORGÂNICA Pode-se afirmar com certeza que se não fosse pelo Carbono você não estaria lendo essa breve descrição agora. A química orgânica se preocupa com o entendimento da vida dada pelo Carbono
QUÍMICA ORGÂNICA Pode-se afirmar com certeza que se não fosse pelo Carbono você não estaria lendo essa breve descrição agora. A química orgânica se preocupa com o entendimento da vida dada pelo Carbono
Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da
 Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da função. REVISÃO DE ISOMERIA PLANA E GEOMETRICA 1) Indique
Exercíciosde Funções Orgânicas 1) Identifique as funções químicas presentes em cada uma das estruturas seguintes. Faça um círculo e dê o nome da função. REVISÃO DE ISOMERIA PLANA E GEOMETRICA 1) Indique
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA
 UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA LOQ4001 ANÁLISE INSTRUMENTAL - ESPECTROMETRIA NO INFRAVERMELHO (FTIR) - ESPECTROMETRIA DE RESSONÂNCIA MAGNÉTICA NUCLEAR (RMN) PROFA. TALITA M. LACERDA
UNIVERSIDADE DE SÃO PAULO ESCOLA DE ENGENHARIA DE LORENA LOQ4001 ANÁLISE INSTRUMENTAL - ESPECTROMETRIA NO INFRAVERMELHO (FTIR) - ESPECTROMETRIA DE RESSONÂNCIA MAGNÉTICA NUCLEAR (RMN) PROFA. TALITA M. LACERDA
NORMAL: RAMIFICADA: H H H C C
 C4 OBS.: C Carbono primário: Se o átomo de carbono estiver ligado a um átomo de carbono. Carbono secundário: se um átomo de carbono estiver ligado a dois átomos de carbono. Carbono terciário: se estiver
C4 OBS.: C Carbono primário: Se o átomo de carbono estiver ligado a um átomo de carbono. Carbono secundário: se um átomo de carbono estiver ligado a dois átomos de carbono. Carbono terciário: se estiver
SETOR 1301 AULA 11 NOMENCLATURA DOS COMPOSTOS ORGÂNICOS
 SETOR 1301 AULA 11 NOMENCLATURA DOS COMPOSTOS ORGÂNICOS ÁLCOOL São compostos orgânicos que apresentam o grupo funcional hidroxila ( OH) ligado a carbono saturado. ÁLCOOL Classificação Quanto ao número
SETOR 1301 AULA 11 NOMENCLATURA DOS COMPOSTOS ORGÂNICOS ÁLCOOL São compostos orgânicos que apresentam o grupo funcional hidroxila ( OH) ligado a carbono saturado. ÁLCOOL Classificação Quanto ao número
LISTA DE EXERCÍCIOS 2º ANO
 Dentre os compostos apresentados, os dois que proporcionam melhor qualidade para os óleos de cozinha são os ácidos linolênico (três duplas entre carbonos) e linoleico (duas duplas entre carbonos). Carbono
Dentre os compostos apresentados, os dois que proporcionam melhor qualidade para os óleos de cozinha são os ácidos linolênico (três duplas entre carbonos) e linoleico (duas duplas entre carbonos). Carbono
LISTA DAS FUNÇÕES ORGÂNICAS
 Orgânica Na pré-história, o ser humano se limitava a usar materiais que encontrava na natureza, sem provocar neles grandes modificações. A descoberta do fogo trouxe ao ser humano a primeira maneira efetiva
Orgânica Na pré-história, o ser humano se limitava a usar materiais que encontrava na natureza, sem provocar neles grandes modificações. A descoberta do fogo trouxe ao ser humano a primeira maneira efetiva
Profº André Montillo
 Profº André Montillo www.montillo.com.br Definição: É o ramo da química que estuda os composto formados pelo arbono. São os compostos encontrados nos organismos vivos e representam 60% da massa do organismo:
Profº André Montillo www.montillo.com.br Definição: É o ramo da química que estuda os composto formados pelo arbono. São os compostos encontrados nos organismos vivos e representam 60% da massa do organismo:
PSVS/UFES 2014 MATEMÁTICA 1ª QUESTÃO. O valor do limite 2ª QUESTÃO. O domínio da função real definida por 3ª QUESTÃO
 MATEMÁTICA 1ª QUESTÃO O valor do limite 3 x 8 lim é x 2 x 2 2ª QUESTÃO O domínio da função real definida por é 3ª QUESTÃO A imagem da função real definida por, para todo, é GRUPO 2 PROVA DE MATEMÁTICA
MATEMÁTICA 1ª QUESTÃO O valor do limite 3 x 8 lim é x 2 x 2 2ª QUESTÃO O domínio da função real definida por é 3ª QUESTÃO A imagem da função real definida por, para todo, é GRUPO 2 PROVA DE MATEMÁTICA
PROVA DE INGRESSO ANO LETIVO 2018/2019 PROVA DE QUÍMICA OBJETIVOS
 UNIVERSIDADE DE CABO VERDE PROVA DE INGRESSO ANO LETIVO 2018/2019 PROVA DE QUÍMICA OBJETIVOS OBJETIVOS Reconhecer o átomo de hidrogénio como átomo mais simples. Conhecer o espetro de emissão de hidrogénio.
UNIVERSIDADE DE CABO VERDE PROVA DE INGRESSO ANO LETIVO 2018/2019 PROVA DE QUÍMICA OBJETIVOS OBJETIVOS Reconhecer o átomo de hidrogénio como átomo mais simples. Conhecer o espetro de emissão de hidrogénio.
2.1 COMPOSTOS AROMÁTICOS: LEI DE HUCKEL
 47 2.1 COMPOSTOS AROMÁTICOS: LEI DE HUCKEL O anel aromático (benzeno) é formado pela conexão de seis carbonos sp 2. No interior do anel aromático, existem seis elétrons pi, ocupando seis orbitais p, e
47 2.1 COMPOSTOS AROMÁTICOS: LEI DE HUCKEL O anel aromático (benzeno) é formado pela conexão de seis carbonos sp 2. No interior do anel aromático, existem seis elétrons pi, ocupando seis orbitais p, e
E = h. c / λ 10.1 INTRODUÇÃO
 10.1 INTRODUÇÃO A espectroscopia na região do ultravioleta e do visível fornece informações a respeito da interação entre a matéria e a radiação eletromagnética. Essa radiação apresenta tanto as propriedades
10.1 INTRODUÇÃO A espectroscopia na região do ultravioleta e do visível fornece informações a respeito da interação entre a matéria e a radiação eletromagnética. Essa radiação apresenta tanto as propriedades
Química E Extensivo V. 3
 Química E Extensivo V. 3 01) Alternativa correta: A Exercícios O clorofórmio, nome usual do Triclorometano fórmula CHCl 3. É um polialeto, pois possui 3 átomos de Cloro. 02) Respostas: Pentaclorofenol
Química E Extensivo V. 3 01) Alternativa correta: A Exercícios O clorofórmio, nome usual do Triclorometano fórmula CHCl 3. É um polialeto, pois possui 3 átomos de Cloro. 02) Respostas: Pentaclorofenol
Funções orgânicas oxigenadas e nitrogenadas.
 Funções orgânicas oxigenadas e nitrogenadas Funções que possuem ou derivam do grupo funcional hidroxila ( OH) Ex: a) Etanol Álcool b) Prop 2 en 1 ol Ex:... estiver ligado a um carbono saturado...... estiver
Funções orgânicas oxigenadas e nitrogenadas Funções que possuem ou derivam do grupo funcional hidroxila ( OH) Ex: a) Etanol Álcool b) Prop 2 en 1 ol Ex:... estiver ligado a um carbono saturado...... estiver
Alcoóis. -Nomenclatura IUPAC: Quantidade de C + tipo de ligação entre C + ol. Ex: Butan-2-ol. Fenóis
 Ácidos e Base -Numa reação entre um ácido e uma base, o ácido atua como o doador de prótons e a base como o aceptor de prótons. O íon H + é considerado um próton, então na reação o ácido perde um H + e
Ácidos e Base -Numa reação entre um ácido e uma base, o ácido atua como o doador de prótons e a base como o aceptor de prótons. O íon H + é considerado um próton, então na reação o ácido perde um H + e
HIDROCARBONETOS FUNÇÕES ORGÂNICAS
 HIDROCARBONETOS FUNÇÕES ORGÂNICAS FUNÇÕES ORGÂNICAS O átomo de carbono: Apresenta capacidade singular de compartilhar elétrons com outros átomos de carbono formando ligações carbono-carbono estáveis. Permite
HIDROCARBONETOS FUNÇÕES ORGÂNICAS FUNÇÕES ORGÂNICAS O átomo de carbono: Apresenta capacidade singular de compartilhar elétrons com outros átomos de carbono formando ligações carbono-carbono estáveis. Permite
UFSC. Resposta: 76. Comentário. 01. Incorreta. É formado pela reação de neutralização entre o hidróxido de potássio e ácido carbônico.
 Resposta: 76 01. Incorreta. É formado pela reação de neutralização entre o hidróxido de potássio e ácido carbônico. H 2 CO 3 + KOH = K 2 CO 3 + H 2 0 02. Incorreta. O nox do carbono é +4. 04. Correta.
Resposta: 76 01. Incorreta. É formado pela reação de neutralização entre o hidróxido de potássio e ácido carbônico. H 2 CO 3 + KOH = K 2 CO 3 + H 2 0 02. Incorreta. O nox do carbono é +4. 04. Correta.
Espectroscopia no infravermelho e Raman
 Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 21/03/2017 Espectroscopia no infravermelho ACIK, M., LEE, G.,
Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Uberlândia, 21/03/2017 Espectroscopia no infravermelho ACIK, M., LEE, G.,
Ciência que estuda a química da vida (características dos seres vivos)
 Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos 1 - Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande
Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos 1 - Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande
Luis Eduardo C. Aleotti. Química. Aula 61 - Propriedades Físicas dos Compostos Orgânicos
 Luis Eduardo C. Aleotti Química Aula 61 - Propriedades Físicas dos Compostos Orgânicos PROPRIEDADES FÍSICAS O que é? - Características da matéria, determinadas de forma experimental. - Não são alteradas,
Luis Eduardo C. Aleotti Química Aula 61 - Propriedades Físicas dos Compostos Orgânicos PROPRIEDADES FÍSICAS O que é? - Características da matéria, determinadas de forma experimental. - Não são alteradas,
Prof. Luiz F. Silva Jr - IQ-USP
 Leitura Recomendada: 1) Organic Chemistry Structure and Function, K. P. C. Vollhardt e N. E. Schore, 3 a ed., Freeman, New York, 2000, cap. 2, p. 61-64, 213-214, 285-288, 343-347, 446-447, 732-733, 828-830,
Leitura Recomendada: 1) Organic Chemistry Structure and Function, K. P. C. Vollhardt e N. E. Schore, 3 a ed., Freeman, New York, 2000, cap. 2, p. 61-64, 213-214, 285-288, 343-347, 446-447, 732-733, 828-830,
UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008.
 UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008. Espectroscopia de Infravermelho (IR) Issac Newton Feixe de luz; A luz violeta é a que mais é deslocada
UNIVERSIDADE FEDERAL DE PELOTAS INSPEÇÃO DE LEITE E DERIVADOS ESPECTROSCOPIA DENISE HENTGES PELOTAS, 2008. Espectroscopia de Infravermelho (IR) Issac Newton Feixe de luz; A luz violeta é a que mais é deslocada
PPGQTA. Prof. MGM D Oca
 PPGQTA Prof. Compostos Carbonílicos O grupo carbonila é um dos mais importantes grupos funcionais e está envolvido em muitas reações. Reações envolvendo grupos carbonila também são particularmente importantes
PPGQTA Prof. Compostos Carbonílicos O grupo carbonila é um dos mais importantes grupos funcionais e está envolvido em muitas reações. Reações envolvendo grupos carbonila também são particularmente importantes
ESTUDANTE: Química Orgânica Básica
 ESTUDANTE: Química Orgânica Básica Professor André Calaça QUÍMICA ORGÂNICA O carbono é um elemento que está sempre presente no nosso cotidiano. Ele pode ser encontrado no ar na forma de moléculas de gás
ESTUDANTE: Química Orgânica Básica Professor André Calaça QUÍMICA ORGÂNICA O carbono é um elemento que está sempre presente no nosso cotidiano. Ele pode ser encontrado no ar na forma de moléculas de gás
6.1 CLASSIFICAÇÃO DAS REAÇÕES ORGÂNICAS
 131 6.1 CLASSIFICAÇÃO DAS REAÇÕES ORGÂNICAS Quando a ligação pi estiver entre dois carbonos, formando alcenos, a reação será de adição eletrofílica. Substratos que apresentam a ligação pi formada entre
131 6.1 CLASSIFICAÇÃO DAS REAÇÕES ORGÂNICAS Quando a ligação pi estiver entre dois carbonos, formando alcenos, a reação será de adição eletrofílica. Substratos que apresentam a ligação pi formada entre
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS
 PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS As propriedades físicas dos compostos orgânicos podem ser interpretadas, e muitas vezes até previstas, a partir do conhecimento das ligações químicas que unem
FCAV/UNESP. DISCIPLINA: Química Fisiológica. ASSUNTO: Noções de Química Orgânica
 FCAV/UNESP DISCIPLINA: Química Fisiológica ASSUNTO: Noções de Química Orgânica 1 QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos
FCAV/UNESP DISCIPLINA: Química Fisiológica ASSUNTO: Noções de Química Orgânica 1 QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos
QUÍ MÍCA: ORGA NÍCA ÍV (REAÇO ES)
 QUÍ MÍCA: ORGA NÍCA ÍV (REAÇO ES) REAÇÕES DE SUBSTITUIÇÃO São assim denominadas porque um hidrogênio da molécula orgânica é substituído por um átomo de halogênio, por um grupo nitro (NO 2 ) ou um grupo
QUÍ MÍCA: ORGA NÍCA ÍV (REAÇO ES) REAÇÕES DE SUBSTITUIÇÃO São assim denominadas porque um hidrogênio da molécula orgânica é substituído por um átomo de halogênio, por um grupo nitro (NO 2 ) ou um grupo
ROTEIRO DE ESTUDOS III TRIMESTRE. Hidrocarbonetos
 RTEIR DE ESTUDS III TRIMESTRE Nome: nº: Ano: 2º E.M. Professor: assio Pacheco 1- Dê a nomenclatura dos compostos orgânicos. Hidrocarbonetos H Álcool H Enol H Fenol Aldeído H H H etona H3 Ácidos arboxílicos
RTEIR DE ESTUDS III TRIMESTRE Nome: nº: Ano: 2º E.M. Professor: assio Pacheco 1- Dê a nomenclatura dos compostos orgânicos. Hidrocarbonetos H Álcool H Enol H Fenol Aldeído H H H etona H3 Ácidos arboxílicos
Química E Intensivo V. 1
 GABARIT Química E Intensivo V. Exercícios 0 adeia carbônica normal é a cadeia não ramificada. Nesse tipo de cadeia, existirão apenas carbonos primários e secundários. 0 99 Na cadeia carbônica saturada,
GABARIT Química E Intensivo V. Exercícios 0 adeia carbônica normal é a cadeia não ramificada. Nesse tipo de cadeia, existirão apenas carbonos primários e secundários. 0 99 Na cadeia carbônica saturada,
Química D Extensivo V. 5
 Química D Extensivo V. 5 Exercícios 01) D H 3 C O 02) D éter H 3 C OH álcool C 2 H 6 O (isômeros) Funções diferentes isomeria de função. 06) D I. C 3 O P III. C 3 H 6 O O II. C 3 O P IV. C 3 O P Isômeros
Química D Extensivo V. 5 Exercícios 01) D H 3 C O 02) D éter H 3 C OH álcool C 2 H 6 O (isômeros) Funções diferentes isomeria de função. 06) D I. C 3 O P III. C 3 H 6 O O II. C 3 O P IV. C 3 O P Isômeros
Química D Semiextensivo V. 3
 GABARIT Química D Semiextensivo V 3 Exercícios 01) B 02) B 03) E omposto A: éter omposto B: fenol omposto : álcool Fórmula molecular dos três compostos: 7 8 éter fenol 2 álcool ompostos de mesma fórmula
GABARIT Química D Semiextensivo V 3 Exercícios 01) B 02) B 03) E omposto A: éter omposto B: fenol omposto : álcool Fórmula molecular dos três compostos: 7 8 éter fenol 2 álcool ompostos de mesma fórmula
Ciências Físico-Químicas 9ºAno Prof. Carla Bastos
 Ciências Físico-Químicas 9ºAno Prof. Carla Bastos O que são? Compostos orgânicos Compostos que contêm carbono e hidrogénio, podendo ainda conter outros elementos. Isómeros Compostos com a mesma fórmula
Ciências Físico-Químicas 9ºAno Prof. Carla Bastos O que são? Compostos orgânicos Compostos que contêm carbono e hidrogénio, podendo ainda conter outros elementos. Isómeros Compostos com a mesma fórmula
QFL-306 Prof. Luiz F. Silva Jr 1. Aldeídos e Cetonas - Parte 1
 10. Aldeídos e Cetonas 10.1. Introdução Grupo Carbonílico: provavelmente o grupo funcional mais importante Aldeídos e Cetonas são responsáveis por aromas e sabores. Além disso, são empregados como solventes,
10. Aldeídos e Cetonas 10.1. Introdução Grupo Carbonílico: provavelmente o grupo funcional mais importante Aldeídos e Cetonas são responsáveis por aromas e sabores. Além disso, são empregados como solventes,
Carbonos Hidrogênios Oxigênios C 2 H 6 O
 Prof. Edson Cruz ISOMERIA Carbonos Hidrogênios Oxigênios H H H C C O H H C O C H H H H H H H C 2 H 6 O C 2 H 6 O Os compostos H 3 C CH 2 OH e H 3 C O CH 3 são ISÔMEROS. ISÔMEROS são compostos diferentes
Prof. Edson Cruz ISOMERIA Carbonos Hidrogênios Oxigênios H H H C C O H H C O C H H H H H H H C 2 H 6 O C 2 H 6 O Os compostos H 3 C CH 2 OH e H 3 C O CH 3 são ISÔMEROS. ISÔMEROS são compostos diferentes
Funções Orgânicas, Isomeria e Propriedades
 Ensino Médio QUÍMICA Data: / / 2012 Atividade: Exercícios de Recuperação Paralela e Anual aula 3 Nome : n o Classe: 2 2MA Funções Orgânicas, Isomeria e Propriedades 1. (Espcex (Aman) 2013) A tabela abaixo
Ensino Médio QUÍMICA Data: / / 2012 Atividade: Exercícios de Recuperação Paralela e Anual aula 3 Nome : n o Classe: 2 2MA Funções Orgânicas, Isomeria e Propriedades 1. (Espcex (Aman) 2013) A tabela abaixo
FCAV/UNESP. DISCIPLINA: Química Orgânica. ASSUNTO: Introdução à Química Orgânica
 FCAV/UNESP DISCIPLINA: Química Orgânica ASSUNTO: Introdução à Química Orgânica 1 QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos
FCAV/UNESP DISCIPLINA: Química Orgânica ASSUNTO: Introdução à Química Orgânica 1 QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos
FCAV/UNESP. DISCIPLINA: Química Fisiológica. ASSUNTO: Noções de Química Orgânica
 FCAV/UNESP DISCIPLINA: Química Fisiológica ASSUNTO: Noções de Química Orgânica 1 QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos
FCAV/UNESP DISCIPLINA: Química Fisiológica ASSUNTO: Noções de Química Orgânica 1 QUÍMICA ORGÂNICA Química Orgânica é a área da Química que estuda os compostos que contêm carbono, chamados de compostos
7.1 CISÃO E FORMAÇÃO DE LIGAÇÃO NO MECANISMO POLAR
 163 7.1 CISÃO E FORMAÇÃO DE LIGAÇÃO NO MECANISMO POLAR Para que uma reação orgânica ocorra, é necessário que haja rompimento nas ligações químicas envolvidas na estrutura das moléculas do substrato e do
163 7.1 CISÃO E FORMAÇÃO DE LIGAÇÃO NO MECANISMO POLAR Para que uma reação orgânica ocorra, é necessário que haja rompimento nas ligações químicas envolvidas na estrutura das moléculas do substrato e do
Química E Extensivo V. 1
 Química E Extensivo V. 1 Exercícios 01) B 02) D 03) C 04) D 05) C 06) E a) Errada. Cada ligação dupla possui dois elétrons pi. Como existem 11 ligações duplas, segue que o número de elétrons pi é 22. b)
Química E Extensivo V. 1 Exercícios 01) B 02) D 03) C 04) D 05) C 06) E a) Errada. Cada ligação dupla possui dois elétrons pi. Como existem 11 ligações duplas, segue que o número de elétrons pi é 22. b)
Ciência que estuda a química da vida
 Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física que regem
Ciência que estuda a química da vida Mostra como o conjunto de moléculas inanimadas que constituem os seres vivos interagem para manter e perpetuar a vida seguindo as leis da química e da física que regem
Ciência que estuda a química da vida (características dos seres vivos)
 Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande diversidade
Ciência que estuda a química da vida (características dos seres vivos) Características dos seres vivos Complexidade química e organização microscópica Elementos químicos comuns C, O, N, H e P Grande diversidade
Curso Científico-Humanístico de Ciências e Tecnologias Disciplina de Física e Química A 10ºAno
 Agrupamento de Escolas João da Silva Correia DEPARTAMENTO DE CIÊNCIAS NATURAIS E EXPERIMENTAIS Curso Científico-Humanístico de Ciências e Tecnologias Disciplina de Física e Química A 10ºAno FICHA DE TRABALHO
Agrupamento de Escolas João da Silva Correia DEPARTAMENTO DE CIÊNCIAS NATURAIS E EXPERIMENTAIS Curso Científico-Humanístico de Ciências e Tecnologias Disciplina de Física e Química A 10ºAno FICHA DE TRABALHO
Isomeria h Quantas vezes caiu no ENEM. Complexidade. Tempo de estudo a dedicar. Videoaulas para estudar. Exercícios por resolver
 TEMAS VESTIBULARES Q1 Isomeria Quantas vezes caiu no ENEM Complexidade Tempo de estudo a dedicar Videoaulas para estudar Exercícios por resolver 8 3 8h 10 20 Isomeria 05 out EXERCÍCIOS DE AULA 1. A isomerização
TEMAS VESTIBULARES Q1 Isomeria Quantas vezes caiu no ENEM Complexidade Tempo de estudo a dedicar Videoaulas para estudar Exercícios por resolver 8 3 8h 10 20 Isomeria 05 out EXERCÍCIOS DE AULA 1. A isomerização
Lista de Exercícios Prova Trimestral. Hidrocarbonetos
 Lista de Exercícios Prova Trimestral Nome: nº: Ano: 2º E.M. Professor: assio Pacheco 1- Dê a nomenclatura dos compostos orgânicos. Hidrocarbonetos H Álcool H H H H H H H H Unidade I: Av. Mascote, 913 -
Lista de Exercícios Prova Trimestral Nome: nº: Ano: 2º E.M. Professor: assio Pacheco 1- Dê a nomenclatura dos compostos orgânicos. Hidrocarbonetos H Álcool H H H H H H H H Unidade I: Av. Mascote, 913 -
AULA 17. Reações Orgânicas. Prof Taynara Oliveira
 AULA 17 Reações Orgânicas Prof Taynara Oliveira Para que ocorra uma reação química, é necessário que as ligações existentes entre os átomos de uma molécula se rompam e esses átomos se rearranjem, formando
AULA 17 Reações Orgânicas Prof Taynara Oliveira Para que ocorra uma reação química, é necessário que as ligações existentes entre os átomos de uma molécula se rompam e esses átomos se rearranjem, formando
Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução
 Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução Emissão Atômica Absorção no Infravermelho Espectrometria de Massas Detector Espectrométrico de Massas (MSD) Acoplamento de GC com um
Detectores Espectrométricos em Cromatografia Gasosa de Alta Resolução Emissão Atômica Absorção no Infravermelho Espectrometria de Massas Detector Espectrométrico de Massas (MSD) Acoplamento de GC com um
A função orgânica caracteriza o composto, agrupando e facilitando os estudos na química, pois ela leva em consideração as suas propriedades físicas e
 Professor: Bob A função orgânica caracteriza o composto, agrupando e facilitando os estudos na química, pois ela leva em consideração as suas propriedades físicas e químicas. Hidrocarbonetos- Compostos
Professor: Bob A função orgânica caracteriza o composto, agrupando e facilitando os estudos na química, pois ela leva em consideração as suas propriedades físicas e químicas. Hidrocarbonetos- Compostos
DISCIPLINA: Química Fisiológica ASSUNTO: Fundamentos de Química Orgânica
 Universidade Estadual Paulista UNESP Faculdade de Ciências Agrárias e Veterinárias - FCAV DISCIPLINA: Química Fisiológica ASSUNTO: Fundamentos de Química Orgânica 1 1ª Semana 21/02/2019: Composição e estrutura
Universidade Estadual Paulista UNESP Faculdade de Ciências Agrárias e Veterinárias - FCAV DISCIPLINA: Química Fisiológica ASSUNTO: Fundamentos de Química Orgânica 1 1ª Semana 21/02/2019: Composição e estrutura
Química Orgânica 2016
 Gabarito: Resposta da questão 1: [E] [Resposta do ponto de vista da disciplina de Química] As cenouras de coloração laranja podem ter sido trazidas a Pernambuco durante a invasão holandesa e contêm um
Gabarito: Resposta da questão 1: [E] [Resposta do ponto de vista da disciplina de Química] As cenouras de coloração laranja podem ter sido trazidas a Pernambuco durante a invasão holandesa e contêm um
- TEMPERATURA DE EBULIÇÃO - SOLUBILIDADE
 PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS - TEMPERATURA DE EBULIÇÃO - SOLUBILIDADE TEMPERATURA DE EBULIÇÃO Depende do tipo de -LIGAÇÃO INTERMOLECULAR e do - TAMANHO DAS MOLÉCULAS LIGAÇÕES INTERMOLECULARES
PROPRIEDADES FÍSICAS DOS COMPOSTOS ORGÂNICOS - TEMPERATURA DE EBULIÇÃO - SOLUBILIDADE TEMPERATURA DE EBULIÇÃO Depende do tipo de -LIGAÇÃO INTERMOLECULAR e do - TAMANHO DAS MOLÉCULAS LIGAÇÕES INTERMOLECULARES
CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de , DOU de PLANO DE CURSO
 CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de 01.11.12, DOU de 06.11.12 Componente Curricular: Química Orgânica Farmacêutica I Código: FAR 202 Pré-requisito: Química Geral e Inorgânica Período
CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de 01.11.12, DOU de 06.11.12 Componente Curricular: Química Orgânica Farmacêutica I Código: FAR 202 Pré-requisito: Química Geral e Inorgânica Período
Estrutura de moléculas orgânicas e biológicas
 Estrutura de moléculas orgânicas e biológicas Adaptado pelo Prof. Luís Perna 1 Compostos orgânicos Os compostos orgânicos formam um grupo enorme de substâncias que inclui a maioria daquelas que contêm
Estrutura de moléculas orgânicas e biológicas Adaptado pelo Prof. Luís Perna 1 Compostos orgânicos Os compostos orgânicos formam um grupo enorme de substâncias que inclui a maioria daquelas que contêm
Componente Curricular: Química Orgânica Farmacêutica II PLANO DE CURSO
 CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de 01.11.12, DOU de 06.11.12 Componente Curricular: Química Orgânica Farmacêutica II Código: FAR 204 Pré-requisito: Química Orgânica Farmacêutica
CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de 01.11.12, DOU de 06.11.12 Componente Curricular: Química Orgânica Farmacêutica II Código: FAR 204 Pré-requisito: Química Orgânica Farmacêutica
Química 12.º Ano Unidade 2 Combustíveis, Energia e Ambiente Carlos Alberto da Silva Ribeiro de Melo
 Química 12.º Ano Unidade 2 Combustíveis, Energia e Ambiente Carlos Alberto da Silva Ribeiro de Melo Lição n.º 54 Sumário: Continuação da aula anterior. Hidrocarbonetos: grupos funcionais. Isomeria. COMPETÊNCIAS
Química 12.º Ano Unidade 2 Combustíveis, Energia e Ambiente Carlos Alberto da Silva Ribeiro de Melo Lição n.º 54 Sumário: Continuação da aula anterior. Hidrocarbonetos: grupos funcionais. Isomeria. COMPETÊNCIAS
IDENTIFICAÇÃO DE UMA ESTRUTURA MOLECULAR A PARTIR
 Licenciatura em Ciências da Saúde Métodos Instrumentais de Análise IDENTIFICAÇÃO DE UMA ESTRUTURA MOLECULAR A PARTIR DE GRÁFICOS DE ESPECTROMETRIA DE MASSA, RESSONÂNCIA MAGNÉTICA NUCLEAR E INFRAVERMELHOS
Licenciatura em Ciências da Saúde Métodos Instrumentais de Análise IDENTIFICAÇÃO DE UMA ESTRUTURA MOLECULAR A PARTIR DE GRÁFICOS DE ESPECTROMETRIA DE MASSA, RESSONÂNCIA MAGNÉTICA NUCLEAR E INFRAVERMELHOS
Parte do espectro electromagnético tico da luz
 Parte do espectro electromagnético tico da luz U.V. Visível I.V. R.M.N. Electrónicas Vibracionais Rotacionais Tipo de transições observadas Spin nuclear (Res.Mag.Nuclear) 1 Espectroscopia de Infravermelho
Parte do espectro electromagnético tico da luz U.V. Visível I.V. R.M.N. Electrónicas Vibracionais Rotacionais Tipo de transições observadas Spin nuclear (Res.Mag.Nuclear) 1 Espectroscopia de Infravermelho
Espectroscopia no infravermelho e Raman
 Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Espectroscopia no infravermelho ACIK, M., LEE, G., MATTEVI, C., CHHOWALLA,
Espectroscopia no infravermelho e Raman Tópicos Especiais em Química XII Métodos Físicos em Química Inorgânica Prof. Edson Nossol Espectroscopia no infravermelho ACIK, M., LEE, G., MATTEVI, C., CHHOWALLA,
Estudo do átomo de carbono (Hibridização), Estrutura de Lewis, Carga formal. Aula 2
 Universidade Federal de Ouro Preto Estudo do átomo de carbono (Hibridização), Estrutura de Lewis, Carga formal Aula 2 Flaviane Francisco Hilário 1 1 Estudo do átomo de carbono 1.1 - Configuração eletrônica
Universidade Federal de Ouro Preto Estudo do átomo de carbono (Hibridização), Estrutura de Lewis, Carga formal Aula 2 Flaviane Francisco Hilário 1 1 Estudo do átomo de carbono 1.1 - Configuração eletrônica
Aula 1. Organic Chemistry 4 th Edition Paula Yurkanis Bruice. Espectroscopia de RMN
 Aula 1 Espectroscopia de RMN Organic Chemistry 4 th Edition Paula Yurkanis Bruice Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Ressonância Magnética Nuclear (RMN) Identifica
Aula 1 Espectroscopia de RMN Organic Chemistry 4 th Edition Paula Yurkanis Bruice Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall Ressonância Magnética Nuclear (RMN) Identifica
Colégio Ressurreição Nossa Senhora
 Colégio Ressurreição Nossa Senhora 3º ano do Ensino Médio Isomeria: plana, geométrica e óptica Prof. Enio S. Santos Isomeria vem do grego e significa "mesma composição" (iso = mesma(s); meros = partes).
Colégio Ressurreição Nossa Senhora 3º ano do Ensino Médio Isomeria: plana, geométrica e óptica Prof. Enio S. Santos Isomeria vem do grego e significa "mesma composição" (iso = mesma(s); meros = partes).
ÁCIDO DE ARRHENIUS. Hidrácidos HCl + H 2 O H + + Cl - HCl, HBr, HI ---- Fortes. HF ---- Moderado Demais ---- Fracos. Prof.
 ÁCIDO DE ARRHENIUS Hidrácidos HCl + H 2 O H + + Cl - HCl, HBr, HI ---- Fortes HF ---- Moderado Demais ---- Fracos ÁCIDO DE ARRHENIUS Oxiácidos HNO 3 + H 2 O H + + NO 3 - ÁCIDOS DE ARRHENIUS Não Como Bolo
ÁCIDO DE ARRHENIUS Hidrácidos HCl + H 2 O H + + Cl - HCl, HBr, HI ---- Fortes HF ---- Moderado Demais ---- Fracos ÁCIDO DE ARRHENIUS Oxiácidos HNO 3 + H 2 O H + + NO 3 - ÁCIDOS DE ARRHENIUS Não Como Bolo
Química E Extensivo V. 5
 Química E Extensivo V. 5 Exercícios 01) a) b) 02) F V V F a) Errada. Existem séries homólogas em qualquer função. b) Certa. Na série homóloga, cada membro tem um CH 2 a mais. Massa molecular: 14µ. c) Certa.
Química E Extensivo V. 5 Exercícios 01) a) b) 02) F V V F a) Errada. Existem séries homólogas em qualquer função. b) Certa. Na série homóloga, cada membro tem um CH 2 a mais. Massa molecular: 14µ. c) Certa.
ESTRUTURA E REATIVIDADE DOS COMPOSTOS ORGÂNICOS ENGENHARIA QUÍMICA/ SEGUNDO SEMESTRE 2014 PLANO DE CURSO. Professora: Ana Júlia Silveira
 ESTRUTURA E REATIVIDADE DOS COMPOSTOS ORGÂNICOS ENGENHARIA QUÍMICA/ SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira EMENTA: Introdução a Química Orgânica. Nomenclatura das Funções Orgânicas.
ESTRUTURA E REATIVIDADE DOS COMPOSTOS ORGÂNICOS ENGENHARIA QUÍMICA/ SEGUNDO SEMESTRE 2014 PLANO DE CURSO Professora: Ana Júlia Silveira EMENTA: Introdução a Química Orgânica. Nomenclatura das Funções Orgânicas.
