A IMPORTÂNCIA DA ÁGUA
|
|
|
- Natália Leveck Escobar
- 7 Há anos
- Visualizações:
Transcrição
1 A ÁGUA
2 A IMPORTÂNCIA DA ÁGUA A água é a substância mais abundante nos sistemas vivos, prefazendo 70% ou mais do peso da maioria dos organismos. Os primeiros organismos vivos iniciaram a sua vida num ambiente aquoso, e o curso da evolução tem sido modelado pelas propriedades do meio aquoso onde a vida começou.
3 INTERAÇÕES FRACAS EM SISTEMAS AQUOSOS As ligações de hidrogénio entre as moléculas de água são forças coesivas que tornam a água líquida à temperatura ambiente. As biomoléculas polares dissolvem-se em água porque estas trocam as interações água-água com interações água-soluto energeticamente favoráveis. As biomoléculas apolares interferem nas interações água-água mas não conseguem formar interações água-soluto, as moléculas apolares são pouco solúveis na água. Nas soluções aquosas, as moléculas apolares tendem a formar clusters entre elas. As ligações de hidrogénio são interações fracas individuais, quando existem um grande número deste tipo de ligações, estas, têm uma grande influência nas estruturas tridimensionais das proteínas, ácidos nucleicos, polissacarídeos e lípidos membranares.
4 PROPRIEDADES FÍSICAS DE SOLVENTES
5 ESTRUTURA DA ÁGUA A polaridade das moléculas de água é devida aos ângulos que os átomos de hidrogénio formam quando se ligam ao átomo de oxigénio (104,5º), tornando o átomo de oxigénio eletronegativo. A distribuição espacial dos eletrões resultante da ligação covalente entre os átomos de hidrogénio e o átomo de oxigénio determina que a molécula da água seja um dipolo elétrico.
6 ESTRUTURA DA ÁGUA NO GELO No gelo, cada molécula de água forma no máximo quatro ligações de hidrogénio, criando uma estrutura regular de cristal. À temperatura ambiente e à pressão atmosférica normal, cada molécula de água forma em média 3,4 ligações de hidrogénio. A estrutura de cristal no gelo é menos densa do que a água fazendo com que este flutue na água líquida.
7 ÁGUA FORMA LIGAÇÕES DE HIDROGÉNIO COM SOLUTOS POLARES As ligações de hidrogénio também se dão entre átomos eletronegativos (Azoto, oxigénio com pares de eletrões livres)
8 ÁGUA INTERAGE ELETROSTATICAMENTE COM SOLUTOS IONIZADOS A água é um solvente polar. Dissolve a maioria das biomoléculas, que estão ionizadas ou que são compostos polares. Os compostos que se dissolvem facilmente na água são hidrofílicos (gostam de água). Os solventes não polares (clorofórmio e benzeno) são maus solventes para as biomoléculas polares mas dissolvem facilmente aquelas que são hidrofóbicas (medo da água), como por exemplo os lípidos. A água dissolve o NaCl por hidratação formando os iões Na + e Cl - enfraquecendo as interações eletrostáticas entre os iões. O mesmo acontece às biomoléculas ionizadas, compostos com grupos funcionais tais como ácidos carboxílicos (-COO - ), aminas portonadas (-NH3 + ), e estéres fosfatados.
9 ÁGUA COMO SOLVENTE
10 Os ácidos gordos de longa cadeia possuem cadeias muito hidrofóbicas onde são circundados por uma camada muito bem ordenada de moléculas de água.
11
12 BIOMOLÉCULAS POLARES E APOLARES
13 GASES APOLARES SÃO INSOLÚVEIS NA ÁGUA As moléculas de gases biologicamente importantes CO 2, O 2, e N 2 são apolares. O transporte de O 2 é realizado por proteínas solúveis em água: Hemoglobina - proteína que transporta o O 2 para os tecidos e remove o CO 2 e protões para os pulmões. Mioglobina - proteína monomérica dos músculos, armazena oxigénio como reserva contra a falta do mesmo.
14
15
16 AÇÃO DA ÁGUA NA CATÁLISE ENZIMÁTICA Quando separados, o enzima e o substrato forçam as moléculas de água a fazerem uma espécie de cobertura à volta dos dois. Quando os dois se aproximam, a água afasta-se para se ligarem, resultando num aumento de entropia fazendo com que o substrato se agarre para a formação do complexo enzima-substrato.
17 IONIZAÇÃO DA ÁGUA, ÁCIDOS E BASES FRACOS Tal como todas as reações reversíveis, a ionização da água pode ser descrita por uma constante e equilíbrio (Kw). Quando ácidos fracos são dissolvidos na água, estes contribuem na reação libertando um grupo H +. As bases fracas consumem H + tornando-se bases protonadas. Estes processos também possuem constantes de equilíbrio (Ka e Kb). A concentração total de H + numa solução dá o ph da solução.
18 Ionização da água
19 CONSTANTE DE EQUILÍBRIO DA ÁGUA E ph
20 Equação de Anderson-Hasselbalch HA + H 2 O A - + H 3 O + A equação Henderson-Hasselbalch permite: 1) O cálculo do pka, quando dado o ph e a razão molar do aceitador e do doador de protões. 2) Calcular o ph e a fração molar quando todos os outros dados são indicados.
21 TITULAÇÃO DO ÁCIDO ACÉTICO COM NaOH
22
23 ÁGUA COMO REAGENTE A formação do ATP a partir do ADP e do fosfato inorgânico (P) é uma reação de condensação (os elementos da água são eliminados). Na reação inversa existe uma adição dos elementos da água Reação de Hidrólise. As reações de hidrólise são responsáveis pela despolimerização enzimática de proteínas, carbohidratos e ácidos nucleicos (exergónicas). A formação de polímeros celulares por reações de condensação deverão ser endergónicas por isso não ocorrem.
24 INALTERAÇÕES DE ph NOS SISTEMAS BIOLÓGICOS Quase todos os processos biológicos são dependentes do ph, uma pequena alteração do ph produz uma grande mudança no procedimento dum processo. Isto é verdade para reações onde há troca de iões H + como participante direto, mas também para outro tipo de reações. Os enzimas que catalisam as reações celulares e muitas das moléculas onde os enzimas atuam, contêm grupos ionizáveis com valores de pka caraterísticos.
25 Cont. Os grupos amino e carboxílicos protonados dos aminoácidos e os grupos fosfato dos nucleótidos, funcionam como ácidos fracos; o seu estado iónico depende do ph do meio circundante. As células e organismos mantêm um valor específico e constante de ph no citosol, mantendo as biomoléculas no seu estado iónico otímo, perto de ph = 7. Nos organismos multicelulares, o ph dos fluidos extracelulares também é extremamente controlado. Este estado constante é alcançado com misturas de ácidos fracos e suas bases conjugadas.
26 O plasma do sangue humano normalmente tem o ph perto de 7,4. Se os mecanismos de regulação do ph falharem, como acontece nos diabetes não controlados, havendo um produção excessiva de ácidos metalólicos causando acidose, o ph do sangue poderá cair para o valor de 6,8 ou menos, poderá levar à destruição irreparável das células causando a morte. Noutras doenças o ph poderá aumentar o seu valor para níveis letais. Os enzimas normalmente apresentam uma atividade catalítica máxima a um ph caraterístico, chamado ph óptimo. Uma pequena mudança no ph óptimo pode causar uma grande diferença na velocidade de importantes reações catalisadas por enzimas. O controlo biológico do ph nas células e nos fluidos corporais é de central importância em todos os aspetos do metalolismo e atividades celulares.
27 FLUIDOS CORPORAIS
28 FLUIDOS CORPORAIS Há em média cerca de 42 litros de fluidos (adulto) Intracelular Fluido existente dentro das células Extracelular Intersticial Plasma Fluido localizado no exterior das células Fluido que rodeia os tecidos individuais Parte líquida do sangue Intracelular Citoplasma Meio para as reações de manutenção da vida Extracelular Plasma Linfa Fluido cerebrospinal Urina Transporte de nutrientes, de produtos de excreção e de informação Sucos digestivos Degradação dos alimentos
29 TRANSPORTE DE O 2 E CO 2 98% do oxigénio é transportado pela hemoglobina dos glóbulos vermelhos. Oxi-hemoglobina Forma oxigenada. Desoxi-hemoglobina Forma desoxigenada. Uma pessoa tem em média 15 g de hemoglobina por 100 ml de sangue.
30 HEMOGLOBINA E O TRANSPORTE DE O 2 e CO 2 Nos pulmões há abundância de O 2 o oxigénio passa para a hemoglobina Hb 4 O Hb( O ) Quando o sangue chega às células, ocorre a reação inversa (cedência do oxigénio às células) A hemoglobina desempenha um papel pequeno no transporte de CO 2 para os pulmões 25% é transportado como um complexo de hemoglobina - Carbaminohemoglobina HB CO HBCO 2 2 5% é transportado dissolvido no plasma. Os outros 70% são conduzidos aos pulmões sob a forma de bicarbonato (HCO 3- )
31 TRANSPORTE QUÍMICO PARAS AS CÉLULAS As substâncias químicas transportadas pelo corpo movem via corrente sanguínea. Dissolvidos na água plasma (iões, aminoácidos, açúcares) Ligados aos componentes celulares (oxigénio, dióxido de carbono) Deslocando-se em suspensão lípidos. Quando transportados pelo sangue, as substâncias devem: Passar através da parede dos capilares; Entrar no fluido intersticial; Passar através da membrana celular.
32 Cont. Os produtos de excreção deslocam-se na direção oposta. A parede capilar atua como uma membrana semipermeável, controlando o fluxo de materiais. Os níveis de proteína são mais elevados no sangue. A pressão diminui à medida que o sangue passa através do capilar. Na extremidade venosa do capilar há um fluxo de lixo (substâncias de excreção) para o capilar.
33 URINA A urina serve para remover o excesso de água, azoto e iões. É constituída por 96% de água, 4% de lixo orgânico e inorgânico. Componentes g (excretada 24h) Aminoácidos 0,80 Ureia 25,0 Creatina 1,5 Na + 3,0 K + 1,7 NH + 4 0,8 Ca 2+ 0,2 Componentes g (excretada 24h) Mg 2+ 0,15 Cl - 6,3 SO H 2 PO 2-4 1,2 HCO Outros 2-3 ph 4,5-8,0
34 A urina é um bom meio (não invasivo) para testar algumas condições do organismo. Constituinte Condição Causa Glucose (alta) Glucosúria Diabetes mellitus, diabetes renal, glicosúria Proteína Pigmentos biliares Proteinúria ou albuminúria Icterícia Danos dos rins, infeção na bexiga, nefrite Bloqueio do ducto biliar, hepatite, cirrose Corpos cetónicos Cetonúria Diabetes mellitus, dietas com alto teor de gordura, fome
35 FLUIDO E EQUILÍBRIO ELETROLÍTICO O equilíbrio fluido e eletrolítico São ambos interdependentes Devem ser controlados para uma saúde perfeita Os seus níveis são geralmente medidos Entram no corpo com a comida e bebida Saem do corpo principalmente pela urina, pulmões, pele e intestinos Os rins desempenham um papel fundamental na manutenção dos níveis apropriados de fluido e eletrólito. Entrada (ml) Saída (ml) Fluidos ingeridos 1500 Rins (Urina) 1400 Água em alimentos 700 Pulmões (ar) 350 Água formada pelo catabolismo 200 Difusão (pele) 350 Transpiração 100 Intestinos (fezes) 200 Os níveis de entrada e saída devem ser os mesmos
36 VASOPRESSINA Manutenção do nível de fluido constante Hormona anti-diurética utilizada pelo corpo para controlar a função renal. Afeta a permeabilidade dos túbulos renais à água. À medida que os níveis sobem, mais água é reabsorvida para a corrente sanguínea. Se os níveis de água caem tornando-se perigosamente baixos devido a: Transpiração excessiva; Falta ou deficiência de água (bebida). As glândulas supra-renais segregam algoesterona. Hormona que provoca a reabsorção do sódio dos túbulos renais para o sangue. Evita a perda excessiva de eletrólitos e ajuda a reter fluidos.
37 CONTROLO RESPIRATÓRIO e URINÁRIO DO ph DO SANGUE O ph do sangue pode ser mantido controlando o nível de CO 2 expirado. CO H O H CO HCO H Hiper-ventilação Aumenta o rácio e a profundidade da respiração. Reduz o CO 2 no sangue, aumentando o ph. Hipo-ventilação Reduz o rácio e a profundidade da respiração. Aumenta o CO 2 no sangue, diminuindo o ph. Os rins podem excretar várias quantidades de ácidos e de bases para a urina. Condições ácidas O excesso de iões de hidrogénio pode ser excretado. Resultando uma maior produção de bicarbonato aumentando o ph do sangue. Condições básicas O bicarbonato pode ser eliminado, baixando o ph do sangue.
38 ACIDOSE E ALCALOSE Quando os padrões respiratórios são inadequados pode ocorrer: Alcalose respiratória Provocada por hiper-ventilação. Tratamento inspirar ar ou administrar CO 2 Acidose respiratória Provocada por respiração inadequada. Tratamento administrar HCO 3 - Várias condições metabólicas podem criar níveis de ph inadequados no sangue. Acidose metabólica causada por descontrole a diabetes, diarreia, overdose de aspirina e depois de exercício violento. Alcalose metabólica causada por vómitos prolongados, uso excessivo de bicarbonato para tratar problemas estomacais.
ph do sangue arterial = 7.4
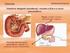 Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
Regulação do Equilíbrio Ácido Base ph do sangue arterial = 7.4 < 6.9 ou > 7.7 = MORTE 1 Importância do ph nos processos biológicos Protonação ou desprotonação de radicais proteicos Variação da carga total
ÁGUA. Planeta Terra ou planeta Água? 71% da supergcie é de água. Composição dos seres vivos:
 ÁGUA Planeta Terra ou planeta Água? 71% da supergcie é de água Composição dos seres vivos: 1% de sais minerais 1% de carboidratos 2 a 3% de lipídios 10 a 15% de proteínas 1% de cidos nucléicos 75 a 85%
ÁGUA Planeta Terra ou planeta Água? 71% da supergcie é de água Composição dos seres vivos: 1% de sais minerais 1% de carboidratos 2 a 3% de lipídios 10 a 15% de proteínas 1% de cidos nucléicos 75 a 85%
A molécula de água A ÁGUA 2
 A água A maior parte da superfície do planeta terra está coberto com água. A água é também a substância mais abundante dos sistemas vivos, perfazendo cerca de 70% ou mais do peso dos mesmos. A água influência
A água A maior parte da superfície do planeta terra está coberto com água. A água é também a substância mais abundante dos sistemas vivos, perfazendo cerca de 70% ou mais do peso dos mesmos. A água influência
SISTEMA TAMPÃO NOS ORGANISMOS ANIMAIS
 SISTEMA TAMPÃO NOS ORGANISMOS ANIMAIS Regulação do Equilíbrio Ácido-Básico ph = Potencial Hidrogeniônico Concentração de H + Quanto mais ácida uma solução maior sua concentração de H + e menor o seu ph
SISTEMA TAMPÃO NOS ORGANISMOS ANIMAIS Regulação do Equilíbrio Ácido-Básico ph = Potencial Hidrogeniônico Concentração de H + Quanto mais ácida uma solução maior sua concentração de H + e menor o seu ph
Aula: 03 Temática: Componentes Inorgânicos das Células Parte I
 Aula: 03 Temática: Componentes Inorgânicos das Células Parte I As substâncias inorgânicas existem na natureza, independentemente dos seres vivos, mas algumas delas podem ser encontradas nas células. Acompanhe!
Aula: 03 Temática: Componentes Inorgânicos das Células Parte I As substâncias inorgânicas existem na natureza, independentemente dos seres vivos, mas algumas delas podem ser encontradas nas células. Acompanhe!
Água, ph e tampão. Profa. Alana Cecília
 Água, ph e tampão Profa. Alana Cecília Água: Estrutura e Propriedades Físico-químicas A água é o principal componente da maioria das células; Permeia todas as porções de todas as células; Importância em
Água, ph e tampão Profa. Alana Cecília Água: Estrutura e Propriedades Físico-químicas A água é o principal componente da maioria das células; Permeia todas as porções de todas as células; Importância em
Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent
![Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent Conceito de ph ph = - Log [H + ] Aumento [H + ] => diminuição do ph => acidose Diminuição [H + ] => aumento do ph => alcalose Alterações são dependent](/thumbs/50/27125458.jpg) Equilíbrio ácido-básico A concentração de H no FEC é mantida dentro de um limite extremamente estreito: 40 nmol/l = 1.000.000 menor que a Concentração dos outros íons!! [H] tem profundo efeito nos eventos
Equilíbrio ácido-básico A concentração de H no FEC é mantida dentro de um limite extremamente estreito: 40 nmol/l = 1.000.000 menor que a Concentração dos outros íons!! [H] tem profundo efeito nos eventos
UNIVERSIDADE PAULISTA UNIP MEDICINA VETERINÁRIA PROFA. DRA. VIVIAN C. C. HYODO. Aula 1 Água
 UNIVERSIDADE PAULISTA UNIP MEDICINA VETERINÁRIA PROFA. DRA. VIVIAN C. C. HYODO Aula 1 Água COMPOSIÇÃO QUÍMICA DE MATÉRIA VIVA Principais átomos C, H, O, N, P, S. Principais Moléculas 70% a 80% Água 10%
UNIVERSIDADE PAULISTA UNIP MEDICINA VETERINÁRIA PROFA. DRA. VIVIAN C. C. HYODO Aula 1 Água COMPOSIÇÃO QUÍMICA DE MATÉRIA VIVA Principais átomos C, H, O, N, P, S. Principais Moléculas 70% a 80% Água 10%
Ácidos, bases e sistemas tampão
 Ácidos, bases e sistemas tampão Ionização da água A água pura tem uma baixa concentração de iões hidrónio (H 3 O + ) e uma igual concentração de iões hidróxido (OH - ) Os ácidos são dadores de protões
Ácidos, bases e sistemas tampão Ionização da água A água pura tem uma baixa concentração de iões hidrónio (H 3 O + ) e uma igual concentração de iões hidróxido (OH - ) Os ácidos são dadores de protões
BIOQUÍMICA PARA ODONTO
 BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
BIOQUÍMICA PARA ODONTO Aula 1: ph, pk a e Sistemas tampão Aminoácidos Autoria: Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade Federal do Rio de Janeiro Reprodução
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes
 ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes ph = potencial hidrogeniônico ph = -log [H + ] Sorenson 1909 A escala de ph é logarítma; portanto, quando duas
ph SISTEMAS TAMPÕES Faculdade de Medicina PUC-Campinas Profa. Dra. Celene Fernandes Bernardes ph = potencial hidrogeniônico ph = -log [H + ] Sorenson 1909 A escala de ph é logarítma; portanto, quando duas
Cerca de 99% dos átomos no corpo humano são de H, O, C e N. Oxigenio 63% Hidrogenio 25.2% Carbono 9.5% Azoto 1.4%
 Cerca de 99% dos átomos no corpo humano são de H, O, C e N Oxigenio 63% Hidrogenio 25.2% Carbono 9.5% Azoto 1.4% Tipos de ligação covalente mais comuns em biomoleculas As reacções bioquímicas utilizam
Cerca de 99% dos átomos no corpo humano são de H, O, C e N Oxigenio 63% Hidrogenio 25.2% Carbono 9.5% Azoto 1.4% Tipos de ligação covalente mais comuns em biomoleculas As reacções bioquímicas utilizam
ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões
![ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões ph arterial entre 7,35 e 7,45 [H+] ~ 40 nanomoles/l (10-9) CO2 (Ácido volátil) O CO 2 não se acumula no organismo, é eliminado pelos pulmões](/thumbs/60/44575873.jpg) Regulação do ph dos líquidos Regulação do ph dos líquidos ph = log[ ] LEC =, ±, (, mm) ph , Alcalose Ojetivo: Manutenção do ph sistêmico na faixa de normalidade. ph arterial entre, e, [H]
Regulação do ph dos líquidos Regulação do ph dos líquidos ph = log[ ] LEC =, ±, (, mm) ph , Alcalose Ojetivo: Manutenção do ph sistêmico na faixa de normalidade. ph arterial entre, e, [H]
Sistema Respiratório. Superior. Língua. Inferior
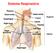 Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
Sistema Respiratório Língua Superior Inferior Funções 1. Troca de gases entre a atmosfera e o sangue. 2. Regulação homeostática do ph corporal 3. Proteção contra substâncias irritantes e patógenos 4. Vocalização
Tampão. O que é? MISTURA DE UM ÁCIDO FRACO COM SUA BASE CONJUGADA, QUE ESTABILIZA O P H DE UMA SOLUÇÃO
 Tampões biológicos Relembrar os conceitos de ácido e base (Brönsted-Lowry), ph, pka; Compreender a importância do ph na manutenção da estrutura tridimensional das biomoléculas; Conhecer os valores de ph
Tampões biológicos Relembrar os conceitos de ácido e base (Brönsted-Lowry), ph, pka; Compreender a importância do ph na manutenção da estrutura tridimensional das biomoléculas; Conhecer os valores de ph
Biomoléculas. * Este esquema não está a incluir as Vitaminas que são classificadas no grupo de moléculas orgânicas. Biomoléculas
 Biomoléculas Biomoléculas Inorgânicas Orgânicas Água Sais Minerais Glícidos Lípidos Prótidos Ácidos Nucléicos * Este esquema não está a incluir as Vitaminas que são classificadas no grupo de moléculas
Biomoléculas Biomoléculas Inorgânicas Orgânicas Água Sais Minerais Glícidos Lípidos Prótidos Ácidos Nucléicos * Este esquema não está a incluir as Vitaminas que são classificadas no grupo de moléculas
Aspectos Bioquímicos da Água
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Aspectos Bioquímicos da Água Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com A concentração de água varia entre os organismos
Pontifícia Universidade Católica de Goiás Departamento de Biologia Aspectos Bioquímicos da Água Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com A concentração de água varia entre os organismos
INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS
 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS 2016 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO PROFESSOR:
INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO ARINOS MINAS GERAIS 2016 INSTITUTO FEDERAL DO NORTE DE MINAS GERAIS KAMILA MARCIANO DE SOUZA SOLUÇÃO TAMPÃO PROFESSOR:
Introdução à Bioquímica
 Introdução à Bioquímica Água Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. A água é fundamental para os seres vivos, atua como solvente
Introdução à Bioquímica Água Dra. Fernanda Canduri Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. A água é fundamental para os seres vivos, atua como solvente
FISIOLOGIA DO EXERCÍCIO
 FISIOLOGIA DO EXERCÍCIO 1 Ventilação e metabolismo energético Equivalente ventilatório de oxigênio: Relação entre volume de ar ventilado (VaV) e a quantidade de oxigênio consumida pelos tecidos (VO2) indica
FISIOLOGIA DO EXERCÍCIO 1 Ventilação e metabolismo energético Equivalente ventilatório de oxigênio: Relação entre volume de ar ventilado (VaV) e a quantidade de oxigênio consumida pelos tecidos (VO2) indica
Regulação renal do equilíbrio ácido base
 Universidade de São Paulo Faculdade de Medicina de Ribeirão Preto Informática Biomédica Regulação renal do equilíbrio ácido base Gabriela Silva Borges O que é ácido e base? Função Química conjunto de compostos
Universidade de São Paulo Faculdade de Medicina de Ribeirão Preto Informática Biomédica Regulação renal do equilíbrio ácido base Gabriela Silva Borges O que é ácido e base? Função Química conjunto de compostos
Aula de Bioquímica I. Tema: Água. Prof. Dr. Júlio César Borges
 Aula de Bioquímica I Tema: Água Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Aula de Bioquímica I Tema: Água Prof. Dr. Júlio César Borges Depto. de Química e Física Molecular DQFM Instituto de Química de São Carlos IQSC Universidade de São Paulo USP E-mail: borgesjc@iqsc.usp.br
Constituintes básicos de uma célula - Biomoléculas. Biomoléculas
 Biomoléculas Todas as moléculas que fazem parte da constituição dos seres vivos são designadas biomoléculas. Formam-se a partir da união de bioelementos. Biomoléculas Os bioelementos combinam-se entre
Biomoléculas Todas as moléculas que fazem parte da constituição dos seres vivos são designadas biomoléculas. Formam-se a partir da união de bioelementos. Biomoléculas Os bioelementos combinam-se entre
FISIOLOGIA GERAL INTRODUÇÃO
 FISIOLOGIA GERAL INTRODUÇÃO FISIOLOGIA Fisiologia (do grego physis = natureza, função ou funcionamento; e logos =estudo) A fisiologia: - estuda as funções mecânicas, físicas e bioquímicas nos seres vivos.
FISIOLOGIA GERAL INTRODUÇÃO FISIOLOGIA Fisiologia (do grego physis = natureza, função ou funcionamento; e logos =estudo) A fisiologia: - estuda as funções mecânicas, físicas e bioquímicas nos seres vivos.
08/08/2017. Objetivos da aula
 Objetivos da aula Desenvolver a capacidade de preparar uma solução em diferentes unidades de expressão de concentração. Compreender o mecanismo de dissolução de uma substância e os fatores que afetam a
Objetivos da aula Desenvolver a capacidade de preparar uma solução em diferentes unidades de expressão de concentração. Compreender o mecanismo de dissolução de uma substância e os fatores que afetam a
Disciplina Fisiologia veterinária I (VET 302)
 Disciplina Fisiologia veterinária I (VET 302) Prof. Bruna Waddington de Freitas Médica Veterinária bruna.freitas@ufv.br 1 Bibliografia Básica REECE, W. O. Dukes Fisiologia dos Animais Domésticos. 12 a
Disciplina Fisiologia veterinária I (VET 302) Prof. Bruna Waddington de Freitas Médica Veterinária bruna.freitas@ufv.br 1 Bibliografia Básica REECE, W. O. Dukes Fisiologia dos Animais Domésticos. 12 a
Composição Química das Células: Água e Sais Minerais
 Composição Química das Células: Água e Sais Minerais Uma das evidências da evolução biológica e da ancestralidade comum dos seres vivos é que todas as formas de vida possuem composição química semelhante.
Composição Química das Células: Água e Sais Minerais Uma das evidências da evolução biológica e da ancestralidade comum dos seres vivos é que todas as formas de vida possuem composição química semelhante.
Metais no Organismo Humano
 Metais no Organismo Humano Relativamente à necessidade biológica podem classificar-se Metais Essenciais: Metais Tóxicos: sódio, potássio, cálcio, magnésio, ferro, crómio, zinco, cobalto, manganês e níquel.
Metais no Organismo Humano Relativamente à necessidade biológica podem classificar-se Metais Essenciais: Metais Tóxicos: sódio, potássio, cálcio, magnésio, ferro, crómio, zinco, cobalto, manganês e níquel.
Homeostase do potássio, cálcio e fosfato
 Homeostase do potássio, cálcio e fosfato Regulação dos eletrólitos Homeostase do potássio Intracellular ADP ATP P Extracellular Hipocalemia: baixo Repolarização mais lenta do potencial de membrana. - Fraqueza
Homeostase do potássio, cálcio e fosfato Regulação dos eletrólitos Homeostase do potássio Intracellular ADP ATP P Extracellular Hipocalemia: baixo Repolarização mais lenta do potencial de membrana. - Fraqueza
As bases bioquímicas da vida
 As bases bioquímicas da vida Água, Sais Minerais, Carboidratos, Lipídios, Proteínas e Vitaminas 1º Ano Profª Priscila F Binatto Constituintes Bioquímicos da Célula Água e Minerais Carboidratos Lipídios
As bases bioquímicas da vida Água, Sais Minerais, Carboidratos, Lipídios, Proteínas e Vitaminas 1º Ano Profª Priscila F Binatto Constituintes Bioquímicos da Célula Água e Minerais Carboidratos Lipídios
INTRODUÇÃO. As reacções bioquímicas requerem, muitas vezes, energia. A fonte mais vulgar de energia química é a adenosina trifosfato (ATP).
 INTRODUÇÃO Célula é a unidade básica dos organismos - tem a área limitada por uma membrana Todas as células são compostas por moléculas pequenas, macromoléculas e organelos. 70% da célula é Água Há quatro
INTRODUÇÃO Célula é a unidade básica dos organismos - tem a área limitada por uma membrana Todas as células são compostas por moléculas pequenas, macromoléculas e organelos. 70% da célula é Água Há quatro
INTRODUÇÃO. As reacções bioquímicas requerem, muitas vezes, energia. A fonte mais vulgar de energia química é a adenosina trifosfato (ATP).
 INTRODUÇÃO Célula é a unidade básica dos organismos - tem a área limitada por uma membrana Todas as células são compostas por moléculas pequenas, macromoléculas e organelos. 70% da célula é Água Há quatro
INTRODUÇÃO Célula é a unidade básica dos organismos - tem a área limitada por uma membrana Todas as células são compostas por moléculas pequenas, macromoléculas e organelos. 70% da célula é Água Há quatro
- Molécula polar, devido à elevada electronegatividade do átomo de oxigénio e à própria estrutura da molécula.
 Água A água é a substância mais abundante dos organismos vivos, correspondendo a 70% ou mais da sua composição. Os primeiros organismos vivos surgiram certamente no meio aquoso, e o curso da evolução foi
Água A água é a substância mais abundante dos organismos vivos, correspondendo a 70% ou mais da sua composição. Os primeiros organismos vivos surgiram certamente no meio aquoso, e o curso da evolução foi
ÁGUA, SOLUBILIDADE E PH
 Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia ÁGUA, SOLUBILIDADE E PH ÁGUA: UM COMPONENTE E SOLVENTE UNIVERSAL A ÁGUA
Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia ÁGUA, SOLUBILIDADE E PH ÁGUA: UM COMPONENTE E SOLVENTE UNIVERSAL A ÁGUA
Trabalho de Recuperação 1º SEMESTRE
 Curso: ENSINO FUNDAMENTAL 2 Trabalho de Recuperação 1º SEMESTRE Foco, Força e Fé Turma: 9º Ano Data: / /2019 Valor: 12,0 Nota: Disciplina: BIOLOGIA Professor(a) NIZE G.CHAGAS PAVINATO Nome do Aluno(a):
Curso: ENSINO FUNDAMENTAL 2 Trabalho de Recuperação 1º SEMESTRE Foco, Força e Fé Turma: 9º Ano Data: / /2019 Valor: 12,0 Nota: Disciplina: BIOLOGIA Professor(a) NIZE G.CHAGAS PAVINATO Nome do Aluno(a):
BIOQUÍMICA CELULAR. Ramo das ciências naturais que estuda a química da vida. Prof. Adaianne L. Teixeira
 BIOQUÍMICA CELULAR Ramo das ciências naturais que estuda a química da vida Prof. Adaianne L. Teixeira Principais elementos químicos dos seres vivos CARBONO (C) (Essencial) HIDROGÊNIO (H) OXIGÊNIO (O) NITROGÊNIO
BIOQUÍMICA CELULAR Ramo das ciências naturais que estuda a química da vida Prof. Adaianne L. Teixeira Principais elementos químicos dos seres vivos CARBONO (C) (Essencial) HIDROGÊNIO (H) OXIGÊNIO (O) NITROGÊNIO
LIPOFILIA LIPOFILIA COEFICIENTE DE PARTIÇÃO.
 LIPOFILIA A lipofilia de um composto é comumente estimada usando Log P a partir da partição de um sistema octanol/água aandrico@ifsc.usp.br A lipofilia é uma das propriedades mais importantes relacionadas
LIPOFILIA A lipofilia de um composto é comumente estimada usando Log P a partir da partição de um sistema octanol/água aandrico@ifsc.usp.br A lipofilia é uma das propriedades mais importantes relacionadas
Objetivo: Estudar os mecanismos fisiológicos responsáveis pelas trocas gasosas e pelo controle do transporte de gases Roteiro:
 TROCAS GASOSAS E CONTROLE DO TRANSPORTE DE GASES Objetivo: Estudar os mecanismos fisiológicos responsáveis pelas trocas gasosas e pelo controle do transporte de gases Roteiro: 1. Trocas gasosas 1.1. Locais
TROCAS GASOSAS E CONTROLE DO TRANSPORTE DE GASES Objetivo: Estudar os mecanismos fisiológicos responsáveis pelas trocas gasosas e pelo controle do transporte de gases Roteiro: 1. Trocas gasosas 1.1. Locais
Equilíbrio ácido-básico. Monitor: Tarcísio Alves Teixeira Professor: Guilherme Soares Fisiologia Veterinária / MFL / IB / UFF
 Equilíbrio ácido-básico Monitor: Tarcísio Alves Teixeira Professor: Guilherme Soares Fisiologia Veterinária / MFL / IB / UFF O que são Ácidos e Bases Ácido: substância que, em solução, é capaz de doar
Equilíbrio ácido-básico Monitor: Tarcísio Alves Teixeira Professor: Guilherme Soares Fisiologia Veterinária / MFL / IB / UFF O que são Ácidos e Bases Ácido: substância que, em solução, é capaz de doar
Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa
 Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa edisousa@if.usp.br Metabolismo Celular Cada reação que ocorre em um organismo vivo requer o uso de energia
Universidade de São Paulo Instituto de Física Energia em Sistemas Biológicos Edi Carlos Sousa edisousa@if.usp.br Metabolismo Celular Cada reação que ocorre em um organismo vivo requer o uso de energia
Todos os seres vivos são constituídos por células unidade estrutural.
 Prof. Ana Rita Rainho Biomoléculas Todos os seres vivos são constituídos por células unidade estrutural. Para além da unidade estrutural também existe uma unidade bioquímica todos os seres vivos são constituídos
Prof. Ana Rita Rainho Biomoléculas Todos os seres vivos são constituídos por células unidade estrutural. Para além da unidade estrutural também existe uma unidade bioquímica todos os seres vivos são constituídos
Membranas Biológicas
 UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Membranas Biológicas Prof Karine P. Naidek Outubro/2016 Membranas Biológicas Membranas
UNIVERSIDADE DO ESTADO DE SANTA CATARINA CENTRO DE CIÊNCIAS TECNOLÓGICAS DEPARTAMENTO DE QUÍMICA DQMC BIOQUÍMICA BIO0001 Membranas Biológicas Prof Karine P. Naidek Outubro/2016 Membranas Biológicas Membranas
Alterações do equilíbrio hídrico Alterações do equilíbrio hídrico Desidratação Regulação do volume hídrico
 Regulação do volume hídrico Alteração do equilíbrio hídrico em que a perda de líquidos do organismo é maior que o líquido ingerido Diminuição do volume sanguíneo Alterações do equilíbrio Hídrico 1. Consumo
Regulação do volume hídrico Alteração do equilíbrio hídrico em que a perda de líquidos do organismo é maior que o líquido ingerido Diminuição do volume sanguíneo Alterações do equilíbrio Hídrico 1. Consumo
artéria renal arteríola aferente capilares glomerulares artéria renal capilares glomerulares veia renal
 FUNÇÕES DOS RINS Controle da osmolaridade dos fluidos corporais Regulação do volume dos fluidos corporais (controle a longo prazo da pressão arterial) Regulação da concentração de eletrólitos: Na +, K
FUNÇÕES DOS RINS Controle da osmolaridade dos fluidos corporais Regulação do volume dos fluidos corporais (controle a longo prazo da pressão arterial) Regulação da concentração de eletrólitos: Na +, K
Bioquímica: Componentes orgânicos e inorgânicos necessários à vida. Leandro Pereira Canuto
 Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
BIOQUÍMICA II SISTEMAS TAMPÃO NOS ORGANISMOS ANIMAIS 3/1/2012
 BIOQUÍMICA II Professora: Ms. Renata Fontes Medicina Veterinária 3º Período O conteúdo de Bioquímica II utiliza os conhecimentos adquiridos referentes ao estudo do metabolismo celular e fenômenos físicos
BIOQUÍMICA II Professora: Ms. Renata Fontes Medicina Veterinária 3º Período O conteúdo de Bioquímica II utiliza os conhecimentos adquiridos referentes ao estudo do metabolismo celular e fenômenos físicos
Biomoléculas e processos Passivos/Ativos na célula
 Biomoléculas e processos Passivos/Ativos na célula ICB Dep. Mofologia Disciplina: Biologia Celular Bases moleculares e Macromoleculares Substâncias Inorgânicas/Orgânicas Processos Celulares Passivos/Ativos
Biomoléculas e processos Passivos/Ativos na célula ICB Dep. Mofologia Disciplina: Biologia Celular Bases moleculares e Macromoleculares Substâncias Inorgânicas/Orgânicas Processos Celulares Passivos/Ativos
Manutenção do ph do sangue
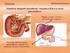 Manutenção do ph do sangue Muitos dos fluidos biológicos, quer no interior, quer no exterior das células, apresentam intervalos de ph muito apertados, ou seja um valor de ph praticamente constante, uma
Manutenção do ph do sangue Muitos dos fluidos biológicos, quer no interior, quer no exterior das células, apresentam intervalos de ph muito apertados, ou seja um valor de ph praticamente constante, uma
Água A água é uma substância química cujas moléculas são formadas por dois átomos de hidrogênio e um de oxigênio (H2O). É abundante no planeta Terra,
 A Química da Vida Água A água é uma substância química cujas moléculas são formadas por dois átomos de hidrogênio e um de oxigênio (H2O). É abundante no planeta Terra, onde cobre grande parte de sua superfície
A Química da Vida Água A água é uma substância química cujas moléculas são formadas por dois átomos de hidrogênio e um de oxigênio (H2O). É abundante no planeta Terra, onde cobre grande parte de sua superfície
A ÁGUA NO METABOLISMO DOS ANIMAIS
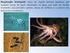 A ÁGUA NO METABOLISMO DOS ANIMAIS Estrutura molecular da água A água se assume um tetraedro irregular. Lado do oxigênio = rico em elétrons Lado do hidrogênio = rico em prótons 1 Características da Molécula
A ÁGUA NO METABOLISMO DOS ANIMAIS Estrutura molecular da água A água se assume um tetraedro irregular. Lado do oxigênio = rico em elétrons Lado do hidrogênio = rico em prótons 1 Características da Molécula
Vamos iniciar o estudo da unidade fundamental que constitui todos os organismos vivos: a célula.
 Aula 01 Composição química de uma célula O que é uma célula? Vamos iniciar o estudo da unidade fundamental que constitui todos os organismos vivos: a célula. Toda célula possui a capacidade de crescer,
Aula 01 Composição química de uma célula O que é uma célula? Vamos iniciar o estudo da unidade fundamental que constitui todos os organismos vivos: a célula. Toda célula possui a capacidade de crescer,
QBQ 0204 Bioquímica. Carlos Hotta e Glaucia Souza. Introdução à disciplina 11/03/17
 QBQ 0204 Bioquímica Introdução à disciplina Carlos Hotta e Glaucia Souza 11/03/17 Organização do curso Os tópicos serão tratados em aulas expositivas e resolução de exercícios. Material disponível em http://carloshotta.com.br/qbq0304
QBQ 0204 Bioquímica Introdução à disciplina Carlos Hotta e Glaucia Souza 11/03/17 Organização do curso Os tópicos serão tratados em aulas expositivas e resolução de exercícios. Material disponível em http://carloshotta.com.br/qbq0304
02/03/2012. Rodrigo Borges, M.Sc. Absorção Distribuição Metabolização ou biotransformação Excreção
 Rodrigo Borges, M.Sc 2012 Movimento dos fármacos no organismo O que o organismo faz sobre a droga É o estudo da velocidade com que os fármacos atingem o sítio de ação e são eliminados do organismo, bem
Rodrigo Borges, M.Sc 2012 Movimento dos fármacos no organismo O que o organismo faz sobre a droga É o estudo da velocidade com que os fármacos atingem o sítio de ação e são eliminados do organismo, bem
Propriedades Físicas e Químicas dos Compostos Orgânicos
 Aumenta Propriedades das Moléculas Orgânicas Propriedades Físicas e Químicas dos Compostos Orgânicos A partir das ligações químicas que unem os átomos de suas moléculas, e das forças que agem entre elas
Aumenta Propriedades das Moléculas Orgânicas Propriedades Físicas e Químicas dos Compostos Orgânicos A partir das ligações químicas que unem os átomos de suas moléculas, e das forças que agem entre elas
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA EQUILÍBRIO ÁCIDO-BASE NO ORGANISMO HUMANO REGULAÇÃO DA CONCENTRAÇÃO HIDROGENIÓNICA - IMPORTÂNCIA
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA EQUILÍBRIO ÁCIDO-BASE NO ORGANISMO HUMANO REGULAÇÃO DA CONCENTRAÇÃO HIDROGENIÓNICA - IMPORTÂNCIA
Fisiologia do Sistema Urinário
 Sistema Urinário Fisiologia do Sistema Urinário Funções do sistema urinário Anatomia fisiológica do aparelho urinário Formação de urina pelos rins Filtração glomerular Reabsorção e secreção tubular Equilíbrio
Sistema Urinário Fisiologia do Sistema Urinário Funções do sistema urinário Anatomia fisiológica do aparelho urinário Formação de urina pelos rins Filtração glomerular Reabsorção e secreção tubular Equilíbrio
artéria renal arteríola aferente capilares glomerulares artéria renal capilares glomerulares veia renal
 FUNÇÕES DOS RINS Controle da osmolaridade dos fluidos corporais Regulação do volume dos fluidos corporais (controle a longo prazo da pressão arterial) Regulação da concentração de eletrólitos: Na +, K
FUNÇÕES DOS RINS Controle da osmolaridade dos fluidos corporais Regulação do volume dos fluidos corporais (controle a longo prazo da pressão arterial) Regulação da concentração de eletrólitos: Na +, K
A análise da matéria que constitui os seres vivos revela abundância de água. Os demais constituintes moleculares estão representados pelos sais
 1 2 A análise da matéria que constitui os seres vivos revela abundância de água. Os demais constituintes moleculares estão representados pelos sais minerais e pelas substâncias orgânicas como proteínas,
1 2 A análise da matéria que constitui os seres vivos revela abundância de água. Os demais constituintes moleculares estão representados pelos sais minerais e pelas substâncias orgânicas como proteínas,
artéria renal arteríola aferente capilares glomerulares artéria renal capilares glomerulares veia renal
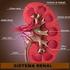 FUNÇÕES DOS RINS Controle da osmolaridade dos fluidos corporais Regulação do volume dos fluidos corporais (controle a longo prazo da pressão arterial) Regulação da concentração de eletrólitos: Na +, K
FUNÇÕES DOS RINS Controle da osmolaridade dos fluidos corporais Regulação do volume dos fluidos corporais (controle a longo prazo da pressão arterial) Regulação da concentração de eletrólitos: Na +, K
Composição química da célula
 Composição química da célula Introdução Evidência da evolução Todas as formas de vida tem a mesma composição química! Substâncias inorgânicas Substâncias orgânicas Água e sais minerais Carboidratos, lipídios,
Composição química da célula Introdução Evidência da evolução Todas as formas de vida tem a mesma composição química! Substâncias inorgânicas Substâncias orgânicas Água e sais minerais Carboidratos, lipídios,
Transporte através de membranas celulares. Tipos de transporte. Exemplos. Importância fisiológica
 Transporte através de membranas celulares Tipos de transporte Exemplos Importância fisiológica Transporte através de membranas celulares (32 D) (44 D) Bicamada lipídica é permeável a gases e moléculas
Transporte através de membranas celulares Tipos de transporte Exemplos Importância fisiológica Transporte através de membranas celulares (32 D) (44 D) Bicamada lipídica é permeável a gases e moléculas
Soluções. Prof a. Jennifer
 Soluções Prof a. Jennifer Conceito Qualitativo Uma solução é formada por dois componentes, denominados dispersante (ou solvente) e o componente disperso (ou soluto). Sólidos em líquidos Líquidos em líquidos
Soluções Prof a. Jennifer Conceito Qualitativo Uma solução é formada por dois componentes, denominados dispersante (ou solvente) e o componente disperso (ou soluto). Sólidos em líquidos Líquidos em líquidos
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO. Profa. Dra. Celene Fernandes Bernardes
 TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
TROCAS GASOSAS TRANSPORTE DE O 2 E CO 2 FUNÇOES DA HEMOGLOBINA QUÍMICA DA RESPIRAÇÃO Profa. Dra. Celene Fernandes Bernardes Plasma sanguíneo ph normal Acidose Alcalose Líquido extracelular Sangue arterial
tampão Prof a Alessandra Smaniotto QMC Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B
 Cap 3: Equilíbrio Químico Soluções tampão Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Água:excepcional habilidade em dissolver grande
Cap 3: Equilíbrio Químico Soluções tampão Prof a Alessandra Smaniotto QMC 5325 - Química Analítica Curso de Graduação em Farmácia Turmas 02102A e 02102B Água:excepcional habilidade em dissolver grande
Transporte através de membranas celulares. Tipos de transporte. Exemplos. Importância fisiológica
 Transporte através de membranas celulares Tipos de transporte Exemplos Importância fisiológica Transporte através de membranas celulares (32 D) (44 D) Bicamada lipídica é permeável a gases e moléculas
Transporte através de membranas celulares Tipos de transporte Exemplos Importância fisiológica Transporte através de membranas celulares (32 D) (44 D) Bicamada lipídica é permeável a gases e moléculas
INTRODUÇÃO À BIOQUÍMICA DA CÉLULA. Bioquímica Celular Prof. Júnior
 INTRODUÇÃO À BIOQUÍMICA DA CÉLULA Histórico INTRODUÇÃO 1665: Robert Hooke Compartimentos (Células) 1840: Theodor Schwann Teoria Celular 1. Todos os organismos são constituídos de uma ou mais células 2.
INTRODUÇÃO À BIOQUÍMICA DA CÉLULA Histórico INTRODUÇÃO 1665: Robert Hooke Compartimentos (Células) 1840: Theodor Schwann Teoria Celular 1. Todos os organismos são constituídos de uma ou mais células 2.
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
Biologia e Geologia 10º ano. Natércia Charruadas 2011
 Biologia e Geologia 10º ano Natércia Charruadas 2011 Todos os seres vivos, logo todas as células, são constituídos por moléculas orgânicas de grandes dimensões macromoléculas. Estas são formadas por um
Biologia e Geologia 10º ano Natércia Charruadas 2011 Todos os seres vivos, logo todas as células, são constituídos por moléculas orgânicas de grandes dimensões macromoléculas. Estas são formadas por um
Homeostase do ph. Ácidos e Bases. HA H + + A - HCl H + + Cl - H 2 CO 3 H + + HCO H + + NH 3. Escala de ph
 Frederico Gueiros Filho Formação: Bacharelado em Biologia - UERJ Mestrado em Genética - UFRJ Doutorado - Harvard Medical School - EUA Pós-doutorado - Harvard, Depto. MCB - EUA Interesse de pesquisa: Mecanismo
Frederico Gueiros Filho Formação: Bacharelado em Biologia - UERJ Mestrado em Genética - UFRJ Doutorado - Harvard Medical School - EUA Pós-doutorado - Harvard, Depto. MCB - EUA Interesse de pesquisa: Mecanismo
PROTEÍNAS GLOBULARES E
 Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia PROTEÍNAS GLOBULARES E TRANSPORTE DE O 2 TRANSPORTE DE O 2 O 2 é pouco
Universidade Federal do Rio de Janeiro Centro de Ciências da Saúde Instituto de Bioquímica Médica Curso: Enfermagem e Obstetrícia PROTEÍNAS GLOBULARES E TRANSPORTE DE O 2 TRANSPORTE DE O 2 O 2 é pouco
Biomoléculas e processos Passivos/Ativos na célula
 Biomoléculas e processos Passivos/Ativos na célula ICB Dep. Mofologia Disciplina: Biologia Celular Prof: Dr. Cleverson Agner Ramos Bases moleculares e Macromoleculares Substâncias Inorgânicas/Orgânicas
Biomoléculas e processos Passivos/Ativos na célula ICB Dep. Mofologia Disciplina: Biologia Celular Prof: Dr. Cleverson Agner Ramos Bases moleculares e Macromoleculares Substâncias Inorgânicas/Orgânicas
TRABALHO DE BIOLOGIA QUÍMICA DA VIDA
 TRABALHO DE BIOLOGIA QUÍMICA DA VIDA Água Sais minerais Vitaminas Carboidratos Lipídios Proteínas Enzimas Ácidos Núcleos Arthur Renan Doebber, Eduardo Grehs Água A água é uma substância química composta
TRABALHO DE BIOLOGIA QUÍMICA DA VIDA Água Sais minerais Vitaminas Carboidratos Lipídios Proteínas Enzimas Ácidos Núcleos Arthur Renan Doebber, Eduardo Grehs Água A água é uma substância química composta
ARTIGO SOBRE OS PERSONAGENS MARCANTES DA HISTÓRIA DA FISIOLOGIA
 ARTIGO SOBRE OS PERSONAGENS MARCANTES DA HISTÓRIA DA FISIOLOGIA Adaptação Ponto de vista evolutivo Exemplos: gado Zebu X gado europeu Aclimatação Alteração fisiológica, bioquímica ou anatômica a partir
ARTIGO SOBRE OS PERSONAGENS MARCANTES DA HISTÓRIA DA FISIOLOGIA Adaptação Ponto de vista evolutivo Exemplos: gado Zebu X gado europeu Aclimatação Alteração fisiológica, bioquímica ou anatômica a partir
Todos tem uma grande importância para o organismo.
 A Química da Vida ÁGUA A água é um composto químico formado por dois átomos de hidrogênio e um de oxigênio. Sua fórmula química é H2O. A água pura não possui cheiro nem cor. Ela pode ser transformada em
A Química da Vida ÁGUA A água é um composto químico formado por dois átomos de hidrogênio e um de oxigênio. Sua fórmula química é H2O. A água pura não possui cheiro nem cor. Ela pode ser transformada em
Fisiologia do Exercício
 Fisiologia do Exercício REAÇÕES QUÍMICAS Metabolismo inclui vias metabólicas que resultam na síntese de moléculas Metabolismo inclui vias metabólicas que resultam na degradação de moléculas Reações anabólicas
Fisiologia do Exercício REAÇÕES QUÍMICAS Metabolismo inclui vias metabólicas que resultam na síntese de moléculas Metabolismo inclui vias metabólicas que resultam na degradação de moléculas Reações anabólicas
Nos diferentes tecidos do corpo, um dos produtos da degradação das proteínas e dos ácidos nucléicos é a amônia, substância muito solúvel e
 SISTEMA EXCRETOR 1 Nos diferentes tecidos do corpo, um dos produtos da degradação das proteínas e dos ácidos nucléicos é a amônia, substância muito solúvel e extremamente tóxica para as células, esmo em
SISTEMA EXCRETOR 1 Nos diferentes tecidos do corpo, um dos produtos da degradação das proteínas e dos ácidos nucléicos é a amônia, substância muito solúvel e extremamente tóxica para as células, esmo em
Colheita e manuseamento de fluidos biológicos
 Colheita e manuseamento de fluidos biológicos Na aula de hoje, vamos falar de: 1. Importância da análise de amostras biológicas como ferramentas de diagnóstico 2. Composição dos dois fluidos mais analisados:
Colheita e manuseamento de fluidos biológicos Na aula de hoje, vamos falar de: 1. Importância da análise de amostras biológicas como ferramentas de diagnóstico 2. Composição dos dois fluidos mais analisados:
TRANSPORTE ATRAVÉS DA MEMBRANA
 TRANSPORTE ATRAVÉS DA MEMBRANA LÍQUIDOS INTRA E EXTRA CELULARES MEMBRANA CELULAR: manutenção das # / seletividade das proteínas transportadoras para íons ou moléculas; SELETIVIDADE E ABERTURAS DAS COMPORTAS
TRANSPORTE ATRAVÉS DA MEMBRANA LÍQUIDOS INTRA E EXTRA CELULARES MEMBRANA CELULAR: manutenção das # / seletividade das proteínas transportadoras para íons ou moléculas; SELETIVIDADE E ABERTURAS DAS COMPORTAS
Avaliação da Capacidade para Frequência do Ensino Superior de Candidatos Maiores de 23 anos
 Avaliação da Capacidade para Frequência do Ensino Superior de Candidatos Maiores de 23 anos 2016 QUÍMICA Conteúdos Programáticos MATERIAIS - Origem - Constituição e composição dos materiais: - Constituição
Avaliação da Capacidade para Frequência do Ensino Superior de Candidatos Maiores de 23 anos 2016 QUÍMICA Conteúdos Programáticos MATERIAIS - Origem - Constituição e composição dos materiais: - Constituição
objetivo Ciclo da uréia Pré-requisito Ao final desta aula, você deverá ser capaz de: Entender as etapas de formação da uréia.
 Ciclo da uréia A U L A 18 objetivo Ao final desta aula, você deverá ser capaz de: Entender as etapas de formação da uréia. Pré-requisito Conhecimentos adquiridos na Aula 17. BIOQUÍMICA II Ciclo da uréia
Ciclo da uréia A U L A 18 objetivo Ao final desta aula, você deverá ser capaz de: Entender as etapas de formação da uréia. Pré-requisito Conhecimentos adquiridos na Aula 17. BIOQUÍMICA II Ciclo da uréia
Biologia Molecular ÁGUA
 Biologia Molecular ÁGUA Direitos autorais reservados. INTRODUÇÃO A vida depende de reações químicas que ocorrem dentro das células reações bioquímicas do metabolismo. Constituição da matéria viva: água,
Biologia Molecular ÁGUA Direitos autorais reservados. INTRODUÇÃO A vida depende de reações químicas que ocorrem dentro das células reações bioquímicas do metabolismo. Constituição da matéria viva: água,
MEMBRANAS BIOLÓGICAS E TRANSPORTE
 MEMBRANAS BIOLÓGICAS E TRANSPORTE Funções das membranas celulares Definem limites externos das células Dividem compartimentos Regulam o trânsito das moléculas Manutenção do equilíbrio com o meio Participam
MEMBRANAS BIOLÓGICAS E TRANSPORTE Funções das membranas celulares Definem limites externos das células Dividem compartimentos Regulam o trânsito das moléculas Manutenção do equilíbrio com o meio Participam
BIOLOGIA MOLECULAR. Água, Sais Minerais, Glicídios e Lipídios. Biologia Frente A Laís Oya
 BIOLOGIA MOLECULAR Água, Sais Minerais, Glicídios e Lipídios Biologia Frente A Laís Oya E-mail: laisfernandabio@gmail.com Composição dos seres vivos: 99% da massa corporal dos seres vivos é composta por
BIOLOGIA MOLECULAR Água, Sais Minerais, Glicídios e Lipídios Biologia Frente A Laís Oya E-mail: laisfernandabio@gmail.com Composição dos seres vivos: 99% da massa corporal dos seres vivos é composta por
COMPOSIÇÃO QUÍMICA DA CÉLULA. Prof.(a):Monyke Lucena
 COMPOSIÇÃO QUÍMICA DA CÉLULA Prof.(a):Monyke Lucena Composição Química da Célula Substâncias Inorgânicas Substâncias Orgânicas Água Sais Minerais Carboidratos Lipídios Proteínas Ácidos Nucléicos Composição
COMPOSIÇÃO QUÍMICA DA CÉLULA Prof.(a):Monyke Lucena Composição Química da Célula Substâncias Inorgânicas Substâncias Orgânicas Água Sais Minerais Carboidratos Lipídios Proteínas Ácidos Nucléicos Composição
Profº Lásaro Henrique
 Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
O sangue e seus constituintes. Juliana Aquino. O sangue executa tantas funções que, sem ele, de nada valeria a complexa organização do corpo humano
 O sangue e seus constituintes Juliana Aquino O sangue executa tantas funções que, sem ele, de nada valeria a complexa organização do corpo humano O sangue e seus constituintes É através da circulação sanguínea
O sangue e seus constituintes Juliana Aquino O sangue executa tantas funções que, sem ele, de nada valeria a complexa organização do corpo humano O sangue e seus constituintes É através da circulação sanguínea
Excreção. Expulsão de produtos residuais da actividade celular e de outras substâncias presentes em excesso no sangue.
 Sistema Urinário Excreção Expulsão de produtos residuais da actividade celular e de outras substâncias presentes em excesso no sangue. Como eliminar os produtos tóxicos que se formam nas células? Vias
Sistema Urinário Excreção Expulsão de produtos residuais da actividade celular e de outras substâncias presentes em excesso no sangue. Como eliminar os produtos tóxicos que se formam nas células? Vias
Fundamentos de Química Profa. Janete Yariwake
 Soluções. Equilíbrio químico em solução aquosa Equilíbrio químico: ácidos e bases 1 ácidos e bases cf. Arrhenius Exemplo: Preparo de uma solução de HCl em água HCl (aq) + H 2 O H 3 O + (aq) + Cl (aq) íon
Soluções. Equilíbrio químico em solução aquosa Equilíbrio químico: ácidos e bases 1 ácidos e bases cf. Arrhenius Exemplo: Preparo de uma solução de HCl em água HCl (aq) + H 2 O H 3 O + (aq) + Cl (aq) íon
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012. Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICOPRÁTICO 5ª AULA TEÓRICOPRÁTICA RESOLUÇÃO
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICOPRÁTICO 5ª AULA TEÓRICOPRÁTICA RESOLUÇÃO
13/08/2018. Escala de ph. Escala de ph. Crescimento básico. Crescimento ácido. Neutro. básico
 Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
COVEST/UFPE ª ETAPA
 COVEST/UFPE 2000 2ª ETAPA. A partir das entalpias padrão das reações de oxidação do ferro dadas abaixo: determine a quantidade de calor liberada a 298K e 1 atm na reação:. Iguais volumes de amônia e cloreto
COVEST/UFPE 2000 2ª ETAPA. A partir das entalpias padrão das reações de oxidação do ferro dadas abaixo: determine a quantidade de calor liberada a 298K e 1 atm na reação:. Iguais volumes de amônia e cloreto
Composição e Estrutura Molecular dos Sistemas Biológicos
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica Composição e Estrutura Molecular dos Sistemas Biológicos Átomos e Moléculas Hierarquia
Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica Composição e Estrutura Molecular dos Sistemas Biológicos Átomos e Moléculas Hierarquia
Número atômico de A = número atômico de B = 18
 61 e QUÍMICA O elemento químico B possui 20 nêutrons, é isótopo do elemento químico A, que possui 18 prótons, e isóbaro do elemento químico C, que tem 16 nêutrons Com base nessas informações, pode-se afirmar
61 e QUÍMICA O elemento químico B possui 20 nêutrons, é isótopo do elemento químico A, que possui 18 prótons, e isóbaro do elemento químico C, que tem 16 nêutrons Com base nessas informações, pode-se afirmar
Solução Comentada Prova de Química
 34. Considere duas soluções de ácido clorídrico (HCl), um ácido forte, (solução I), e ácido acético (CH 3 COOH), um ácido fraco, k a =1,8 x 10-5, (solução II). Ambas as soluções com concentração 0,02 mol.
34. Considere duas soluções de ácido clorídrico (HCl), um ácido forte, (solução I), e ácido acético (CH 3 COOH), um ácido fraco, k a =1,8 x 10-5, (solução II). Ambas as soluções com concentração 0,02 mol.
UNIVERSIDADE FEDERAL DE CAMPINA GRANDE CENTRO DE TECNOLOGIA AGROALIMENTAR CURSO DE GRADUAÇÃO EM AGRONOMIA DISCIPLINA: BIOQUÍMICA GERAL PROFESSOR:
 Aula 4: água UNIVERSIDADE FEDERAL DE CAMPINA GRANDE CENTRO DE TECNOLOGIA AGROALIMENTAR CURSO DE GRADUAÇÃO EM AGRONOMIA DISCIPLINA: BIOQUÍMICA GERAL PROFESSOR: Adriana Silva Lima Água A água é a substância
Aula 4: água UNIVERSIDADE FEDERAL DE CAMPINA GRANDE CENTRO DE TECNOLOGIA AGROALIMENTAR CURSO DE GRADUAÇÃO EM AGRONOMIA DISCIPLINA: BIOQUÍMICA GERAL PROFESSOR: Adriana Silva Lima Água A água é a substância
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas.
 São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
Unidade: Natal Curso: Fisioterapia Disciplina: Bioquímica Docente: Drª Valeska Santana de Sena Pereira.
 Unidade: Natal Curso: Fisioterapia Disciplina: Bioquímica Docente: Drª Valeska Santana de Sena Pereira valeska_sena@hotmail.com 11/08/2016 Apresentação da disciplina. Introdução à bioquímica. 18/08/2016
Unidade: Natal Curso: Fisioterapia Disciplina: Bioquímica Docente: Drª Valeska Santana de Sena Pereira valeska_sena@hotmail.com 11/08/2016 Apresentação da disciplina. Introdução à bioquímica. 18/08/2016
