FILOSOFANDO EM TORNO DA MATÉRIA. Ao longo dos séculos o homem utiliza as propriedades químicas da matéria para obtenção de produtos de seu interesse.
|
|
|
- Miguel Fraga Silva
- 8 Há anos
- Visualizações:
Transcrição
1 FILOSOFANDO EM TORNO DA MATÉRIA A constituição da matéria Ao longo dos séculos o homem utiliza as propriedades químicas da matéria para obtenção de produtos de seu interesse. Metais (a partir de minérios) Cerâmicas (a partir de argilas) Vinho (a partir da uva) Cosméticos e fármacos ( obtidos através da matéria-prima animal e vegetal)
2 Há muito tempo o também se questiona a respeito da constituição da matéria. Por exemplo: Se um pedaço de madeira após sua queima pode se transformar em cinzas e fumaças, do que essa matéria é constituída? Esses são alguns dos questionamentos para os quais, há muito tempo, buscamos respostas por meio de diversas formas de pensar. O pensamento mágico e mitológico é uma das formas mais antigas de respostas a essas questões. Assim foram, por exemplo, muitas explicações atribuídas à origem e a natureza do fogo, tido como um fenômeno divino.
3 Um grande avanço na evolução da nossa civilização foi contudo, quando esse pensamento mágico começou a ser substituído pelo pensamento racional, como o da Filosofia, que busca respostas para as questões que tanto intrigam o homem. Essa discursão (sobre a origem da matéria) e o por que das suas transformações começou com os primeiros filósofos gregos. Eles buscavam as questões enigmáticas que até hoje persistem: De onde viemos? Para que existimos? Como tudo funciona? Vários filósofos tentaram responder esses questionamentos.
4 Os primeiros modelos de constituição da matéria: Tales de mileto ( A.C) As primeiras especulações relativas à constituição são devidas ao filósofo grego TALES, que viveu na cidade de Mileto. Tales deduzia que teria a água como princípio (ou substrato) único, ou seja: TODO UNIVERSO teria a água como origem. Demócrito ( A.C) e Leucipo ( A.C) Esses dois filósofos gregos, baseados apenas no raciocínio (sem a realização de experimentos), consideravam que toda a matéria do universo era constituída por átomos (não divisível, em grego), existindo um único tipo de átomo, eterno e imperecível, que se movimentaria no vazio.
5 Os primeiros modelos de constituição da matéria: Aristóteles ( A.C) Aristóteles foi o sistematizador da teoria dos quatro elementos. Para ele, cada elemento seria formado por duas de quatro possíveis qualidades (QUENTE, ÚMIDO, FRIO e SECO), e o conjunto, disposto em dois pares antagônicos (TERRA/AR e FOGO e ÁGUA), seria da seguinte forma: QUALIDADES Quente + úmido Frio + seco Úmido + frio Seco + quente AR TERRA ÁGUA FOGO ELEMENTO
6 Os primeiros modelos de constituição da matéria: Aristóteles ( A.C) As mudanças da matéria viriam das mudanças de qualidades e de formas. A transmutação do fogo em terra se resumiria em alterar uma das suas qualidades, isto é, quente para frio. Para Aristóteles, a matéria era contínua (não atômica) e suas ideias terminaram prevalecendo entre a maioria dos pensadores até o século XVI, quando outros estudiosos, rompendo com a filosofia aristotélica, passaram a defender o atomismo e adotar o empirismo como prática para o estabelecimento da verdade científica.
7 O método científico e o nascimento da Ciência Moderna. Muitos cientistas, a partir do século XVII, começaram a realizar experimentos com base num moderno método experimental, centrado em observações rigorosamente controladas que pudessem desenvolver teorias demonstráveis matematicamente. Vários pensadores contribuíram para o estabelecimento desse modo de pensar: O MÉTODO CIENTÍFICO. O físico italiano Galileu Galilei ( ) e o químico Robert Boyle ( ) estão entre os primeiros estudiosos a fazer uso dessa metodologia.
8 O método científico e o nascimento da Ciência Moderna Robert Boyle Os resultados do trabalho do físico e químico Irlandês Robert Boyle, publicados em 1661, foram decisivos para a retomada do atomismo. Nesses trabalhos, ele concluiu que todos os objetos eram compostos por átomos, que seriam as unidades fundamentais da matéria. Boyle concluiu que: os átomos existiam e eram diferentes para cada tipo de elemento; combinações de tipos diferentes de átomos formavam os compostos; Toda a matéria era formada por um pequeno número de substâncias simples (ou elementos) combinados de formas diferentes.
9 O método científico e o nascimento da Ciência Moderna. Boyle adotou o termo elemento, que era usado na Grécia Antiga, para designar cada substância simples. Parecia, portanto, que a existência do átomo já era irrefutável., mais ainda faltava descrevê-lo detalhadamente, fato que vem evoluindo até os dias de hoje. O nascimento da Química Moderna Não há uma data que possamos estabelecer como início da Química moderna. Alguns cientistas que viveram nos séculos XVII e XVIII deram uma grande contribuição para o estabelecimento dessa ciência. Entre esses cientistas, um dos mais relevantes foi o francês Antonie Laurent Lavoisier. Seus trabalhos, realizados no século XVIII, foram tão importantes que alguns consideraram o pai da Química. Dentre as suas contribuições, a mais conhecida e relevante é a LEI DA CONSERVAÇÃO DA MASSA.
10 LEI DA CONSERVAÇÃO DA MASSA DE LAVOISIER O nascimento da Química Moderna No final do século XVII, o cientista Antonie Lavoisier realizou uma série de experiências em recipientes fechados e efetuando pesagens com balanças bem precisas, concluiu: No interior de um recipiente fechado, a massa total não varia, quaisquer que sejam as transformações que venham ocorrer nesse espaço. Tal alternativa é uma lei da natureza, descoberta por Lavoisier e que, por esse motivo, ficou conhecida como lei de Lavoisier (ou lei de conservação da massa). Exemplo: Verifica-se que três gramas de carbono reagem com oito gramas de oxigênio, produzindo onze gras de gás carbônico. Como 3 g + 8 g = 11 g, conclui-se que nada se perdeu.
11 O nascimento da Química Moderna LEI DE PROUST Quase na mesma época de Lavoisier, Joseph Louis Proust, efetuando também uma grande série de pesagens em inúmeras experiências, chegou a seguinte conclusão: A proporção em massa das substâncias que reagem e que são produzidas em uma reaçãoquímica é sempre constante e invariável. Exemplo: Verifica-se que o gás carbônico é sempre formado por carbono e oxigênio, e verificase também que: 3 g de carbono se unem a 8 g de oxigênio, produzindo-se 11 g de gás carbônico. 6 g de carbono se unem a 16 g de oxigênio, produzindo 22 g de gás carbônico. Nas duas experiências a proporção entre as massa dos participantes da reação é a mesma. Essa conclusão é chamada de LEI DE PROUST ou LEI DAS PROPORÇÕES CONSTANTES.
12 O nascimento da Química Moderna 1803 John Dalton As duas leis enunciadas são chamadas LEIS PONDERAIS, porque falam em massa das substâncias envolvidas. São leis importantíssimas, pois marcam o início da química como ciência. Em 1803, buscando explicações dos fatos experimentais observados nas duas leis ponderais, o inglês John Dalton desenvolveu uma teoria sobre a estrutura da matéria defendendo a antiga ideia de átomo imaginada pelos filósofos gregos Demócrito e Leucipo retomada por Boyle.
13 O modelo atômico elaborado por Dalton baseava-se nas seguintes hipóteses: 1) A matéria é constituída de pequenas partículas esféricas maciças e indivisíveis denominadas átomos. 2) Um conjunto de átomos com as mesmas massas e tamanhos apresenta as mesmas propriedades e constitui um elemento químico. 3) Elementos químicos diferentes apresentam átomos com massas, tamanhos e propriedades diferentes. 4) A combinação de átomos de elementos diferentes, numa proporção de números inteiros, origina substâncias diferentes. 5) Os átomos não são criados nem destruídos: são simplesmente rearranjados, originando novas substâncias.
14 O modelo atômico de Dalton
15 Explicando as Leis ponderais utilizando a teoria atômica de Dalton O modelo atômico proposto por Dalton explicou adequadamente as leis ponderais da seguinte forma: Lei de Lavoisier: Como os átomos eram esferas indestrutíveis, em uma reação a sua quantidade total permanece constante. Uma reação química seria um rearranjo de átomos formando novas substâncias. Lei de Proust: Se dobrássemos o número de átomos dos reagentes, teríamos de dobrar o número de átomos dos produtos.
16 Com o modelo atômico de Dalton, foi possível estabelecer um critério para uma classificação ampla das substâncias puras, que foram divididas em: 1) Substância simples: Formadas por átomos de mesmo elemento químico. Não podem ser decompostas em outras substâncias mais simples. Exemplos: gás oxigênio (O2), gás hidrogênio (H2) 2) Substâncias compostas: Formadas por átomos de diferentes elementos químicos. Podem ser decompostas em duas ou mais substâncias Exemplos: água (H2O), gás carbônico (CO2) e cloreto de sódio (NaCl)
17 A linguagem química Como toda ciência, além de seus métodos investigativos e suas estruturas e modelos, a Química apresenta uma linguagem própria, ricas em símbolos e regras diferentes da linguagem comum. Para facilitar a comunicação entre os cientistas de todo o mundo, os elementos químicos são representados por símbolos que derivam dos seus nomes em latim. Elemento químico Símbolo Hidrogênio H Cálcio Ca Carbono C ( são usadas duas letras para não confundir com o carbono) Potássio K ( do latim kalium) Chumbo Pb ( do latim plumbum )
18 A linguagem química Enquanto os elementos químicos são representados por símbolos, as substâncias são representadas por fórmulas. Nas fórmulas, representamos os símbolos dos elementos que são constituintes de cada substância, e por meio de índices numéricos colocados um pouco abaixo do elemento, indicando o número de átomos que compõem a substância. FÓRMULAS QUÍMICAS DE ALGUMAS SUBSTÂNCIAS Substância Elemento químico Fórmula Hidrogênio H H2 Nitrogênio N N2 Oxigênio O O2 Água H e O H2O Metano Ferro H e C Fe CH4 Fe
19 Alotropia A classificação das substâncias em simples e compostas permitiu aos cientistas um aprimoramento no estudo das propriedades de cada substância em particular, o que acabou levando à constatação de um fenômeno: algumas substâncias simples com propriedades físicas totalmente diferentes tinham um comportamento químico muito semelhante Esse fenômeno foi denominado ALOTROPIA e as substâncias que sofrem esse fenômeno são denominadas variedades alotrópicas. Vários elementos sofrem alotropia. Os exemplos mais comuns ocorrem com o carbono, o oxigênio, o fósforo e o enxofre.
20 Alotropia Carbono O elemento carbono apresenta duas variedades alotrópicas naturais que diferem quanto à distribuição dos átomos no espaço (ARRANJO CRISTALINO). O diamante formado por átomos de carbono que se unem posicionando-se nos vértices e no centro de um tetraédrico. O grafite formado por átomos de carbono, só que ligados formando camadas paralelas de hexágonos como podemos ver nas figuras a seguir:
21 Alotropia A grafita (encontrada no lápis de escrever) e o diamante apresentam propriedades físicas bastante distintas. Grafita d = 2,26 g/cm 3 cinza escuro Diamante d = 3,51 g/cm 3 incolor quando puro dureza baixa conduz eletricidade dureza alta não conduz corrente elétrica Em relação às propriedades químicas, porém, a grafita e o diamante se comportam praticamente da mesma maneira, isto é, reagem com as mesmas substâncias, dando origem ao mesmo produto. Exemplo: Cgrafita + O2 CO2 Cdiamante + O2 CO2
22 Alotropia Quando duas ou mais substâncias sofrem alotropia, uma das formas alotrópicas sempre é mais estável que a (as) outra (as). A forma mais instável (mais energética) tende a se transformar espontaneamente na forma mais estável num processo que ocorre com liberação de energia. A grafita tem um arranjo cristalino mais estável, portanto menos energético. Os cristais de diamante tendem a se transformar em grafita espontaneamente, embora isso, leve milhões de anos para ocorrer. O diamante só é formado na natureza nas camadas mais externas da Terra onde existem condições propícias, como altas pressão e temperatura. O carbono também apresenta outras variedades alotrópicas sintéticas, sintéticas como o BUCKMINSTERFULERENO e os NANOTUBOS DE CARBONO.
23 Alotropia Oxigênio Forma as substâncias simples oxigênio (O2) e ozônio (O3). A diferença entre as variedades alotrópicas ocorre no número de átomos que compõem cada molécula.
24 Alotropia Enxofre: Possui várias formas alotrópicas, sendo as mais comuns o enxofre rômbico e o enxofre monoclínico, que diferem quanto à distribuição dos átomos no espaço (arranjo cristalino). Substância P.F P.E Cor Estabilidade Enxofre rômbico 112,8 ºC 444,6 ºC amarelo estável Enxofre monoclínico 119 ºC 444,6 ºC amarelo instável
25 Alotropia Fósforo: Forma os alotrópicos fósforo branco e fósforo vermelho, cuja diferença entre as variedades alotrópicas se verifica na atomicidade. Substância P.F P.E Cor Estabilidade Fósforo vermelho 593 ºC 725 ºC vermelho estável P- branco Fósforo branco 44,1 ºC 280 ºC branco avermelhado instável P- vermelho
uma divisão da História da Química
 1. Introdução: Conceitos e cálculos fundamentais 1 uma divisão da História da Química 1. Protoquímica desde a descoberta do fogo até o início da era cristã 2. Alquimia ~ entre o início da era cristã até
1. Introdução: Conceitos e cálculos fundamentais 1 uma divisão da História da Química 1. Protoquímica desde a descoberta do fogo até o início da era cristã 2. Alquimia ~ entre o início da era cristã até
Leis Históricas da Estequiometria
 Estequiometria A proporção correta da mistura ar-combustível para o motor de uma carro de corrida pode ser tão importante quanto a habilidade do piloto para ganhar a corrida. As substâncias químicas, como
Estequiometria A proporção correta da mistura ar-combustível para o motor de uma carro de corrida pode ser tão importante quanto a habilidade do piloto para ganhar a corrida. As substâncias químicas, como
São Mateus ES, Novembro de 1998 SUMÁRIO. I Introdução. II Desenvolvimento. 2.1 Leis da reações químicas. III Conclusão.
 São Mateus ES, Novembro de 1998 SUMÁRIO I Introdução II Desenvolvimento 2.1 Leis da reações químicas III Conclusão IV Bibliografia I Introdução Tentar-se-à mostrar nesta obra uma pesquisa sobre a Lei das
São Mateus ES, Novembro de 1998 SUMÁRIO I Introdução II Desenvolvimento 2.1 Leis da reações químicas III Conclusão IV Bibliografia I Introdução Tentar-se-à mostrar nesta obra uma pesquisa sobre a Lei das
478 a.c. Leucipo e seu discípulo Demócrito
 MODELOS ATÔMICOS 478 a.c. Leucipo e seu discípulo Demócrito - A matéria após sofrer várias subdivisões, chegaria a uma partícula indivisível a que chamaram de átomo. - ÁTOMO a = sem tomos = divisão - Esta
MODELOS ATÔMICOS 478 a.c. Leucipo e seu discípulo Demócrito - A matéria após sofrer várias subdivisões, chegaria a uma partícula indivisível a que chamaram de átomo. - ÁTOMO a = sem tomos = divisão - Esta
Teoria Atômica. Constituição da matéria. Raízes históricas da composição da matéria. Modelos atômicos. Composição de um átomo.
 Teoria Atômica Constituição da matéria Raízes históricas da composição da matéria Modelos atômicos Composição de um átomo Tabela periódica Raízes Históricas 6000 a.c.: descoberta do fogo 4000 a.c.: vidros,
Teoria Atômica Constituição da matéria Raízes históricas da composição da matéria Modelos atômicos Composição de um átomo Tabela periódica Raízes Históricas 6000 a.c.: descoberta do fogo 4000 a.c.: vidros,
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL
 RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
Aula 2: O estudo da matéria
 KROTON S.A. UNIC EDUCACIONAL LTDA. ENGENHARIA DE PRODUÇÃO 2015/1 Aula 2: O estudo da matéria A Matéria Conceitos; Tudo que tem massa e ocupa lugar no espaço. - O que é massa? - Como se afere a massa de
KROTON S.A. UNIC EDUCACIONAL LTDA. ENGENHARIA DE PRODUÇÃO 2015/1 Aula 2: O estudo da matéria A Matéria Conceitos; Tudo que tem massa e ocupa lugar no espaço. - O que é massa? - Como se afere a massa de
Evolução do Modelo Atómico
 Evolução do Modelo Atómico Desde a antiguidade que os homens se preocupavam em saber de que é que as «coisas» são feitas. No entanto, existiam perspectivas diversas sobre o assunto, a mais conhecida das
Evolução do Modelo Atómico Desde a antiguidade que os homens se preocupavam em saber de que é que as «coisas» são feitas. No entanto, existiam perspectivas diversas sobre o assunto, a mais conhecida das
1 - Etapas do método científico.
 1 - Etapas do método científico. Realizar experimentos apropriados para responder a questões; A partir da observação, estabelecer relações. Princípios: Proposições ou generalizações de regularidades, semelhanças
1 - Etapas do método científico. Realizar experimentos apropriados para responder a questões; A partir da observação, estabelecer relações. Princípios: Proposições ou generalizações de regularidades, semelhanças
MODELOS ATÔMICOS. Química Professora: Raquel Malta 3ª série Ensino Médio
 MODELOS ATÔMICOS Química Professora: Raquel Malta 3ª série Ensino Médio PRIMEIRA IDEIA DO ÁTOMO 546 a.c. Tales de Mileto: propriedade da atração e repulsão de objetos após atrito; 500 a.c. Empédocles:
MODELOS ATÔMICOS Química Professora: Raquel Malta 3ª série Ensino Médio PRIMEIRA IDEIA DO ÁTOMO 546 a.c. Tales de Mileto: propriedade da atração e repulsão de objetos após atrito; 500 a.c. Empédocles:
Leis Ponderais e Cálculo Estequiométrico
 Leis Ponderais e Cálculo Estequiométrico 1. (UFF 2009) Desde a Antiguidade, diversos povos obtiveram metais, vidro, tecidos, bebidas alcoólicas, sabões, perfumes, ligas metálicas, descobriram elementos
Leis Ponderais e Cálculo Estequiométrico 1. (UFF 2009) Desde a Antiguidade, diversos povos obtiveram metais, vidro, tecidos, bebidas alcoólicas, sabões, perfumes, ligas metálicas, descobriram elementos
Química SUBSTÂNCIAS, MISTURAS E PROCESSO DE SEPARAÇÃO DE MISTURAS
 SUBSTÂNCIAS, MISTURAS E PROCESSO DE SEPARAÇÃO DE MISTURAS SUBSTÂNCIAS QUÍMICAS Átomos ligados entre si são chamados de moléculas, e representam substâncias químicas. Cada molécula é identificada por uma
SUBSTÂNCIAS, MISTURAS E PROCESSO DE SEPARAÇÃO DE MISTURAS SUBSTÂNCIAS QUÍMICAS Átomos ligados entre si são chamados de moléculas, e representam substâncias químicas. Cada molécula é identificada por uma
Variação de entalpia nas mudanças de estado físico. Prof. Msc.. João Neto
 Variação de entalpia nas mudanças de estado físico Prof. Msc.. João Neto Processo Endotérmico Sólido Líquido Gasoso Processo Exotérmico 2 3 Processo inverso: Solidificação da água A variação de entalpia
Variação de entalpia nas mudanças de estado físico Prof. Msc.. João Neto Processo Endotérmico Sólido Líquido Gasoso Processo Exotérmico 2 3 Processo inverso: Solidificação da água A variação de entalpia
A Matéria Química Geral
 Química Geral A Matéria Tudo o que ocupa lugar no espaço e tem massa. A matéria nem sempre é visível Noções Preliminares Prof. Patrícia Andrade Mestre em Agricultura Tropical Massa, Inércia e Peso Massa:
Química Geral A Matéria Tudo o que ocupa lugar no espaço e tem massa. A matéria nem sempre é visível Noções Preliminares Prof. Patrícia Andrade Mestre em Agricultura Tropical Massa, Inércia e Peso Massa:
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09
 Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 2ºTeste Sumativo 1ºPeríodo Duração do Teste:60 minutos Data: 05 / 12 / 08 Prof. Dulce Godinho
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 2ºTeste Sumativo 1ºPeríodo Duração do Teste:60 minutos Data: 05 / 12 / 08 Prof. Dulce Godinho
Átomo e Modelos Atómicos
 Átomo e Modelos Atómicos Demócrito (Sec. V a.c.) defendeu a ideia de que a matéria era composta por pequeníssimas partículas. Átomo Demócrito (460 370 A.C.) Modelo baseado apenas na intuição e na lógica.
Átomo e Modelos Atómicos Demócrito (Sec. V a.c.) defendeu a ideia de que a matéria era composta por pequeníssimas partículas. Átomo Demócrito (460 370 A.C.) Modelo baseado apenas na intuição e na lógica.
MATÉRIA- PROPRIEDADES DA MATÉRIA- SUBSTÂNICAS (Pura e Composta)- MISTURAS- ANÁLISE IMEDIATA.
 ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
ATENÇÃO: Não sou o detentor dos direitos e também não tenho a intenção de violá-los de nenhuma imagem, exemplo prático ou material de terceiros que porventura venham a ser utilizados neste ou em qualquer
A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas.
 A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas. Não há reação química que ocorra sem variação de energia! A energia é conservativa. Não pode ser criada
A Termoquímica tem como objetivo o estudo das variações de energia que acompanham as reações químicas. Não há reação química que ocorra sem variação de energia! A energia é conservativa. Não pode ser criada
A origem dos filósofos e suas filosofias
 A Grécia e o nascimento da filosofia A origem dos filósofos e suas filosofias Você certamente já ouviu falar de algo chamado Filosofia. Talvez conheça alguém com fama de filósofo, ou quem sabe a expressão
A Grécia e o nascimento da filosofia A origem dos filósofos e suas filosofias Você certamente já ouviu falar de algo chamado Filosofia. Talvez conheça alguém com fama de filósofo, ou quem sabe a expressão
Introdução à Química Inorgânica
 Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
Introdução à Química Inorgânica Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira Química A Química é uma ciência que está diretamente ligada à nossa vida cotidiana. A produção do pão,
Átomo e Modelos Atô t m ô ic i o c s o
 Átomo e Modelos Atômicos Demócrito (Sec. V a.c.) defendeu a idéia de que a matéria era composta por pequeníssimas partículas. Átomo Demócrito (460 370 A.C.) Modelo baseado apenas na intuição e na lógica.
Átomo e Modelos Atômicos Demócrito (Sec. V a.c.) defendeu a idéia de que a matéria era composta por pequeníssimas partículas. Átomo Demócrito (460 370 A.C.) Modelo baseado apenas na intuição e na lógica.
Leucipo de Mileto e Demócrito de Abdera. Pércio Augusto Mardini Farias
 Pércio Augusto Mardini Farias Este documento tem nível de compartilhamento de acordo com a licença 2.5 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by/2.5/br/
Pércio Augusto Mardini Farias Este documento tem nível de compartilhamento de acordo com a licença 2.5 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by/2.5/br/
Propriedades da Matéria
 Professor: Robinho AULA 1 QMC E Propriedades da Matéria Matéria Massa Volume AR Matéria/Propriedades Pág. 263 DENSIDADE d = m V Matéria/Propriedades Pág. 263 Med (UFSC 2011)Uma medalha, supostamente de
Professor: Robinho AULA 1 QMC E Propriedades da Matéria Matéria Massa Volume AR Matéria/Propriedades Pág. 263 DENSIDADE d = m V Matéria/Propriedades Pág. 263 Med (UFSC 2011)Uma medalha, supostamente de
Escola Básica da Gafanha da Encarnação Físico-Química 8º ano Ficha de trabalho 2014/2015 Nome N.º Turma Data: Enc. Educação Professora
 Escola Básica da Gafanha da Encarnação Físico-Química 8º ano Ficha de trabalho 2014/2015 Nome N.º Turma Data: Enc. Educação Professora 1. A Maria adicionou uma colher de chocolate em pó a um copo com Leite
Escola Básica da Gafanha da Encarnação Físico-Química 8º ano Ficha de trabalho 2014/2015 Nome N.º Turma Data: Enc. Educação Professora 1. A Maria adicionou uma colher de chocolate em pó a um copo com Leite
3. Elemento Químico Elemento Químico é um conjunto de átomos iguais (do mesmo tipo). E na linguagem dos químicos eles são representados por Símbolos.
 Química Profª SIMONE MORGADO Aula 1 Elemento, substância e mistura 1. Conceito de Química A Química é uma ciência que busca compreender os mistérios da matéria, sua organização e transformações, bem como
Química Profª SIMONE MORGADO Aula 1 Elemento, substância e mistura 1. Conceito de Química A Química é uma ciência que busca compreender os mistérios da matéria, sua organização e transformações, bem como
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014
 RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
RESOLUÇÃO COMENTADA DA PROVA DA UNESP DE 2014 1-Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo
Uma breve história da Química
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Uma breve história da Química Professor: José Tiago Pereira Barbosa 1 História da Química A história da química tem início há aproximadamente
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Uma breve história da Química Professor: José Tiago Pereira Barbosa 1 História da Química A história da química tem início há aproximadamente
Estão corretos: a) apenas I, II e V. b) apenas I, III e IV. c) apenas II, III e V. d) I, II, III, IV e V. e) apenas I, II, III, IV.
 1. (Ufpr 2014) As teorias atômicas vêm se desenvolvendo ao longo da história. Até o início do século XIX, não se tinha um modelo claro da constituição da matéria. De lá até a atualidade, a ideia de como
1. (Ufpr 2014) As teorias atômicas vêm se desenvolvendo ao longo da história. Até o início do século XIX, não se tinha um modelo claro da constituição da matéria. De lá até a atualidade, a ideia de como
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09
 Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 1ºTeste Sumativo 1ºPeríodo Duração do Teste: 90 minutos Data: 07 / 11 / 08 Prof. Dulce Godinho
Escola Secundária Anselmo de Andrade Teste Sumativo de Ciências Físico - Químicas 9º Ano Ano Lectivo 08/09 1ºTeste Sumativo 1ºPeríodo Duração do Teste: 90 minutos Data: 07 / 11 / 08 Prof. Dulce Godinho
LINGUAGEM, LÍNGUA, LINGÜÍSTICA MARGARIDA PETTER
 LINGUAGEM, LÍNGUA, LINGÜÍSTICA MARGARIDA PETTER Duas explicações da Origem do mundo palavra (a linguagem verbal) associada ao poder mágico de criar. Atributo reservado a Deus. Através dela ele criou as
LINGUAGEM, LÍNGUA, LINGÜÍSTICA MARGARIDA PETTER Duas explicações da Origem do mundo palavra (a linguagem verbal) associada ao poder mágico de criar. Atributo reservado a Deus. Através dela ele criou as
IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS. Aluno(a): Turma:
 IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS Aluno(a): Turma: Querido (a) aluno (a), Este estudo dirigido foi realizado para que você revise
IESA-ESTUDO DIRIGIDO 1º SEMESTRE 8º ANO - MANHÃ E TARDE- DISCIPLINA: CIÊNCIAS PROFESSORAS: CELIDE E IGNÊS Aluno(a): Turma: Querido (a) aluno (a), Este estudo dirigido foi realizado para que você revise
dóxa e epistéme. sensível e inteligível. fé e razaão.
 dóxa e epistéme. sensível e inteligível. fé e razaão. Senso comum... aranha caranguejeira ou aranha-marrom? Epistemologia Moderna e Contemporânea EPISTEMOLOGIA investiga o conhecimento. limites. possibilidades.
dóxa e epistéme. sensível e inteligível. fé e razaão. Senso comum... aranha caranguejeira ou aranha-marrom? Epistemologia Moderna e Contemporânea EPISTEMOLOGIA investiga o conhecimento. limites. possibilidades.
A MATÉRIA E SEUS ESTADOS FÍSICOS I TRIMESTRE CIÊNCIAS NATURAIS SABRINA PARENTE
 A MATÉRIA E SEUS ESTADOS FÍSICOS I TRIMESTRE CIÊNCIAS NATURAIS SABRINA PARENTE Matéria é tudo em que você puder pensar, destas páginas que você está lendo até a cadeira que você está sentado, a água que
A MATÉRIA E SEUS ESTADOS FÍSICOS I TRIMESTRE CIÊNCIAS NATURAIS SABRINA PARENTE Matéria é tudo em que você puder pensar, destas páginas que você está lendo até a cadeira que você está sentado, a água que
AS LEIS DE NEWTON PROFESSOR ANDERSON VIEIRA
 CAPÍTULO 1 AS LEIS DE NEWTON PROFESSOR ANDERSON VIEIRA Talvez o conceito físico mais intuitivo que carregamos conosco, seja a noção do que é uma força. Muito embora, formalmente, seja algo bastante complicado
CAPÍTULO 1 AS LEIS DE NEWTON PROFESSOR ANDERSON VIEIRA Talvez o conceito físico mais intuitivo que carregamos conosco, seja a noção do que é uma força. Muito embora, formalmente, seja algo bastante complicado
Juliana Cerqueira de Paiva. Modelos Atômicos Aula 2
 Juliana Cerqueira de Paiva Modelos Atômicos Aula 2 2 Modelo Atômico de Thomson Joseph John Thomson (1856 1940) Por volta de 1897, realizou experimentos estudando descargas elétricas em tubos semelhantes
Juliana Cerqueira de Paiva Modelos Atômicos Aula 2 2 Modelo Atômico de Thomson Joseph John Thomson (1856 1940) Por volta de 1897, realizou experimentos estudando descargas elétricas em tubos semelhantes
QUÍMICA QUESTÃO 41 QUESTÃO 42
 Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Processo Seletivo/UNIFAL- janeiro 2008-1ª Prova Comum TIPO 1 QUÍMICA QUESTÃO 41 Diferentes modelos foram propostos ao longo da história para explicar o mundo invisível da matéria. A respeito desses modelos
Como surgiu o universo
 Como surgiu o universo Modelos para o universo Desde os tempos remotos o ser humano observa o céu, buscando nele pistas para compreender o mundo em que vive. Nessa busca incansável, percebeu fenômenos
Como surgiu o universo Modelos para o universo Desde os tempos remotos o ser humano observa o céu, buscando nele pistas para compreender o mundo em que vive. Nessa busca incansável, percebeu fenômenos
ESTEQUIOMETRIA. Prof. João Neto
 ESTEQUIOMETRIA Prof. João Neto 1 Lei de Lavoisier Leis Ponderais Lei de Dalton Lei de Proust 2 Fórmula molecular Fórmula mínima Tipos de Fórmulas Fórmula eletrônica ou de Lewis Fórmula Centesimal Fórmula
ESTEQUIOMETRIA Prof. João Neto 1 Lei de Lavoisier Leis Ponderais Lei de Dalton Lei de Proust 2 Fórmula molecular Fórmula mínima Tipos de Fórmulas Fórmula eletrônica ou de Lewis Fórmula Centesimal Fórmula
Apostila de Química Geral
 Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Tecnologia Mecânica MATERIAIS. Roda de aço. Mapa do Brasil em cobre. Prof. Marcio Gomes
 Alumínio Tecnologia Mecânica Ferro fundido MATERIAIS Roda de aço Mapa do Brasil em cobre Introdução Átomo: modelo de Bohr Tecnologia Mecânica O átomo, que não dá para a gente ver nem com um microscópio,
Alumínio Tecnologia Mecânica Ferro fundido MATERIAIS Roda de aço Mapa do Brasil em cobre Introdução Átomo: modelo de Bohr Tecnologia Mecânica O átomo, que não dá para a gente ver nem com um microscópio,
marcelo@sombraealegria.com.br Aula 03 Filosofia 3 Colegial
 Aula 03 Filosofia 3 Colegial Os Primeiros Filósofos Busca por uma explicação racional do mundo Filósofos Físicos Explicação na própria natureza Substância básica que formariam todas as coisas: Arkhé A
Aula 03 Filosofia 3 Colegial Os Primeiros Filósofos Busca por uma explicação racional do mundo Filósofos Físicos Explicação na própria natureza Substância básica que formariam todas as coisas: Arkhé A
PROVA DE QUÍMICA - 1998 Segunda Etapa
 PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
PROVA DE QUÍMICA - 1998 Segunda Etapa QUESTÃO 01 Num laboratório químico, havia três frascos que continham, respectivamente, um alcano, um álcool e um alqueno. Foram realizados experimentos que envolviam
TERMOQUÍMICA. Desta forma podemos dizer que qualquer mudança química geralmente envolve energia.
 TERMOQUÍMICA 1 Introdução A sociedade moderna depende das mais diversas formas de energia para sua existência. Quase toda a energia de que dependemos é obtida a partir de reações químicas, como a queima
TERMOQUÍMICA 1 Introdução A sociedade moderna depende das mais diversas formas de energia para sua existência. Quase toda a energia de que dependemos é obtida a partir de reações químicas, como a queima
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves
 Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
Material Extra: Modelos atômicos e atomística Química professor Cicero # Modelos Atômicos e atomística - Palavras chaves Evolução da ideia do átomo 1) Partícula maciça, indivisível e indestrutível; 2)
Adaptado de Professora: Miwa Yoshida. www.colegionobel.com.br/2004quimica1oano/atomo.ppt
 Adaptado de Professora: Miwa Yoshida www.colegionobel.com.br/2004quimica1oano/atomo.ppt Leucipo de Mileto ( 440 a.c.) & Demócrito (460 a.c. - 370 a.c. ) A ideia de dividirmos uma porção qualquer de matéria
Adaptado de Professora: Miwa Yoshida www.colegionobel.com.br/2004quimica1oano/atomo.ppt Leucipo de Mileto ( 440 a.c.) & Demócrito (460 a.c. - 370 a.c. ) A ideia de dividirmos uma porção qualquer de matéria
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA
 SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
SÉRIE: 2º ano EM Exercícios de recuperação final DATA / / DISCIPLINA: QUÍMICA PROFESSOR: FLÁVIO QUESTÕES DE MÚLTIPLA ESCOLHA QUESTÃO 01 Em uma determinada transformação foi constatado que poderia ser representada
Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron:
 Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
Introduzir o estudo das fórmulas químicas e seus diversos tipos, além de mostrar as fórmulas de determinados compostos.
 INTRODUÇÃO AO ESTUDO DAS FÓRMULAS QUÍMICAS Aula 8 META Introduzir o estudo das fórmulas químicas e seus diversos tipos, além de mostrar as fórmulas de determinados compostos. OBJETIVOS Ao final desta aula,
INTRODUÇÃO AO ESTUDO DAS FÓRMULAS QUÍMICAS Aula 8 META Introduzir o estudo das fórmulas químicas e seus diversos tipos, além de mostrar as fórmulas de determinados compostos. OBJETIVOS Ao final desta aula,
Qualidade Ambiental Química
 Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
Qualidade Ambiental Química Programa Revisão dos Conceitos Básicos de Química e Estatística Poluição o Ar e a Química da Troposfera Reações Químicas ligadas à Emissão de Poluentes da Atmosfera Bibliografia
Matriz - Prova de recuperação modular- Cursos profissionais Física e Química- Módulo Q3- Reações Químicas Duração da Prova: 90 min (prova escrita)
 Matriz - Prova de recuperação modular- Cursos profissionais Física e Química- Módulo Q3- Reações Químicas Duração da Prova: 90 min (prova escrita) O presente documento divulga informação relativa à prova
Matriz - Prova de recuperação modular- Cursos profissionais Física e Química- Módulo Q3- Reações Químicas Duração da Prova: 90 min (prova escrita) O presente documento divulga informação relativa à prova
Química - Profa. GRAÇA PORTO
 Disciplina: Química Química - Profa. GRAÇA PORTO ESTUDO DAS SUBSTÂNCIAS E MISTURAS Você sabe caracterizar a quanto ao sabor, a cor e ao cheiro? E o sal? Quais são as características do açúcar? Agora, tente
Disciplina: Química Química - Profa. GRAÇA PORTO ESTUDO DAS SUBSTÂNCIAS E MISTURAS Você sabe caracterizar a quanto ao sabor, a cor e ao cheiro? E o sal? Quais são as características do açúcar? Agora, tente
TEORIA GERAL DOS SISTEMAS
 TEORIA GERAL DOS SISTEMAS 2 HISTÓRICO Gottfried Leibniz (1646-1716) chamava de Sistema: Repertório de conhecimentos que não se limitasse a ser um simples inventário, mas que contivesse suas razões ou provas
TEORIA GERAL DOS SISTEMAS 2 HISTÓRICO Gottfried Leibniz (1646-1716) chamava de Sistema: Repertório de conhecimentos que não se limitasse a ser um simples inventário, mas que contivesse suas razões ou provas
PARA A CIÊNCIA PARA A TECNOLOGIA PARA A SOCIEDADE
 PARA A CIÊNCIA PARA A TECNOLOGIA PARA A SOCIEDADE Essas são atividades de grande influência no desenvolvimento humano. Procura entender os fenômenos e criar teorias adequadas que possam explicar os acontecimentos.
PARA A CIÊNCIA PARA A TECNOLOGIA PARA A SOCIEDADE Essas são atividades de grande influência no desenvolvimento humano. Procura entender os fenômenos e criar teorias adequadas que possam explicar os acontecimentos.
ESTRUTURAS CRISTALINAS - TEORIA
 ESTRUTURAS CRISTALINAS - TEORIA Introdução Sólidos são compostos que apresentam uma alta regularidade estrutural. Com exceção dos sólidos amorfos, nos quais essa regularidade só existe em um curto espaço,
ESTRUTURAS CRISTALINAS - TEORIA Introdução Sólidos são compostos que apresentam uma alta regularidade estrutural. Com exceção dos sólidos amorfos, nos quais essa regularidade só existe em um curto espaço,
MOTIVAÇÃO 1: Reflexão e discussão do grupo sobre a frase
 TÍTULO: Transformando e Conservando MOTIVAÇÃO 1: Reflexão e discussão do grupo sobre a frase Figura 1: Disponível em: http://portaleliomar.opovo.com.br/wpcontent/uploads/2014/05/frases-lavoisier.jpg acessado
TÍTULO: Transformando e Conservando MOTIVAÇÃO 1: Reflexão e discussão do grupo sobre a frase Figura 1: Disponível em: http://portaleliomar.opovo.com.br/wpcontent/uploads/2014/05/frases-lavoisier.jpg acessado
PROF. KELTON WADSON OLIMPÍADA 8º SÉRIE ASSUNTO: TRANSFORMAÇÕES DE ESTADOS DA MATÉRIA.
 PROF. KELTON WADSON OLIMPÍADA 8º SÉRIE ASSUNTO: TRANSFORMAÇÕES DE ESTADOS DA MATÉRIA. 1)Considere os seguintes dados obtidos sobre propriedades de amostras de alguns materiais. Com respeito a estes materiais,
PROF. KELTON WADSON OLIMPÍADA 8º SÉRIE ASSUNTO: TRANSFORMAÇÕES DE ESTADOS DA MATÉRIA. 1)Considere os seguintes dados obtidos sobre propriedades de amostras de alguns materiais. Com respeito a estes materiais,
Tabel e a l P rió dica
 Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
Tabela Periódica Desenvolvimento histórico da Tabela Periódica Dmitri Mendeleev (1834-1907 ) Escreveu em fichas separadas as propriedades (estado físico, massa, etc) dos elementos químicos. Enquanto arruma
Prova de Recuperação Bimestral de Ciências Nome Completo: Data: / /2010
 COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
COLÉGIO MARIA IMACULADA QI 05 ch. 72 LAGO SUL BRASÍLIA DF E-MAIL: cmidf@cmidf.com.br FONE: 248 4768 SITE: www.cmidf.com.br VALOR:10 pontos. NOTA: 9ºano 2º PERÍODO Prova de Recuperação Bimestral de Ciências
 Termos Técnicos Ácidos Classe de substâncias que têm ph igual ou maior que 1 e menor que 7. Exemplo: sumo do limão. Átomos Todos os materiais são formados por pequenas partículas. Estas partículas chamam-se
Termos Técnicos Ácidos Classe de substâncias que têm ph igual ou maior que 1 e menor que 7. Exemplo: sumo do limão. Átomos Todos os materiais são formados por pequenas partículas. Estas partículas chamam-se
IX Olimpíada Catarinense de Química 2013. Etapa I - Colégios
 I Olimpíada Catarinense de Química - 2013 I Olimpíada Catarinense de Química 2013 Etapa I - Colégios Imagem: Oxidação Fonte:Gilson Rocha Reynaldo, 2013 Primeiro Ano Conselho Regional de Química CRQ III
I Olimpíada Catarinense de Química - 2013 I Olimpíada Catarinense de Química 2013 Etapa I - Colégios Imagem: Oxidação Fonte:Gilson Rocha Reynaldo, 2013 Primeiro Ano Conselho Regional de Química CRQ III
Características do conhecimento científico
 Características Racional Objetivo Factual Transcende os fatos Analítico Claro e preciso Comunicável Verificável Depende de investigação metódica Sistemático Acumulativo Falível Geral Explicativo Preditivo
Características Racional Objetivo Factual Transcende os fatos Analítico Claro e preciso Comunicável Verificável Depende de investigação metódica Sistemático Acumulativo Falível Geral Explicativo Preditivo
15-09-2015. Química 12º Ano. Marília Peres Esc. Sec. José Saramago - Mafra. Chemistry is all about you! http://www.youtube.com/watch?
 12º Ano Esc. Sec. José Saramago - Mafra O que é a? Chemistry is all about you! http://www.youtube.com/watch?v=9ith8us-uju 2 1 O que é a? Orgânica Física Inorgânica Bioquímica Analítica... 3 O que é a?
12º Ano Esc. Sec. José Saramago - Mafra O que é a? Chemistry is all about you! http://www.youtube.com/watch?v=9ith8us-uju 2 1 O que é a? Orgânica Física Inorgânica Bioquímica Analítica... 3 O que é a?
TERMOQUÍMICA. O que é o CALOR? Energia térmica em transito
 TERMOQUÍMICA Termoquímica PROF. Prof. DAVID David TERMOQUÍMICA O que é o CALOR? Energia térmica em transito TERMOQUÍMICA Estuda as quantidades de calor liberadas ou absorvidas durante as reações químicas
TERMOQUÍMICA Termoquímica PROF. Prof. DAVID David TERMOQUÍMICA O que é o CALOR? Energia térmica em transito TERMOQUÍMICA Estuda as quantidades de calor liberadas ou absorvidas durante as reações químicas
ORIGEM DA VIDA. Pró Madá 1º ano
 ORIGEM DA VIDA NA TERRA Pró Madá 1º ano A Terra primitiva Estima-se que o planeta Terra surgiu há aproximadamente 4,6 bilhões de anos Durante muito tempo, permaneceu como um ambiente inóspito (80% de gás
ORIGEM DA VIDA NA TERRA Pró Madá 1º ano A Terra primitiva Estima-se que o planeta Terra surgiu há aproximadamente 4,6 bilhões de anos Durante muito tempo, permaneceu como um ambiente inóspito (80% de gás
Diferentes padrões para uma mesma medida.
 Diferentes padrões para uma mesma medida. Antes de iniciarmos o assunto desta atividade, veremos como se deu a evolução das medidas utilizadas pelo homem e depois trataremos das proporções do Homem Vitruviano.
Diferentes padrões para uma mesma medida. Antes de iniciarmos o assunto desta atividade, veremos como se deu a evolução das medidas utilizadas pelo homem e depois trataremos das proporções do Homem Vitruviano.
Valor verdadeiro, precisão e exatidão. O valor verdadeiro de uma grandeza física experimental às vezes pode ser considerado
 UNIDADE I Fundamentos de Metrologia Valor verdadeiro, precisão e exatidão O valor verdadeiro de uma grandeza física experimental às vezes pode ser considerado o objetivo final do processo de medição. Por
UNIDADE I Fundamentos de Metrologia Valor verdadeiro, precisão e exatidão O valor verdadeiro de uma grandeza física experimental às vezes pode ser considerado o objetivo final do processo de medição. Por
Os Sólidos de Platão. Colégio Santa Maria Matemática III Geometria Espacial Sólidos Geométricos Prof.º Wladimir
 Sólidos Geométricos As figuras geométricas espaciais também recebem o nome de sólidos geométricos, que são divididos em: poliedros e corpos redondos. Vamos abordar as definições e propriedades dos poliedros.
Sólidos Geométricos As figuras geométricas espaciais também recebem o nome de sólidos geométricos, que são divididos em: poliedros e corpos redondos. Vamos abordar as definições e propriedades dos poliedros.
CADERNO DE EXERCÍCIOS 1D
 CADERNO DE EXERCÍCIOS 1D Ensino Fundamental Ciências da Natureza II Questão Conteúdo Habilidade da Matriz da EJA/FB 01 Propriedades e aplicação dos materiais H55/H56 02 Propriedades específicas, físicas
CADERNO DE EXERCÍCIOS 1D Ensino Fundamental Ciências da Natureza II Questão Conteúdo Habilidade da Matriz da EJA/FB 01 Propriedades e aplicação dos materiais H55/H56 02 Propriedades específicas, físicas
15 O sistema solar e seus planetas
 A U A UL LA Atenção O sistema solar e seus planetas Leia com atenção as notícias abaixo, que apareceram em jornais de diferentes épocas. ANO DE 1781 CIENTISTAS DESCOBREM NOVO PLANETA De há quase 2.000
A U A UL LA Atenção O sistema solar e seus planetas Leia com atenção as notícias abaixo, que apareceram em jornais de diferentes épocas. ANO DE 1781 CIENTISTAS DESCOBREM NOVO PLANETA De há quase 2.000
1 O número concreto. Como surgiu o número? Contando objetos com outros objetos Construindo o conceito de número
 Página 1 de 5 1 O número concreto Como surgiu o número? Contando objetos com outros objetos Construindo o conceito de número Como surgiu o número? Alguma vez você parou para pensar nisso? Certamente você
Página 1 de 5 1 O número concreto Como surgiu o número? Contando objetos com outros objetos Construindo o conceito de número Como surgiu o número? Alguma vez você parou para pensar nisso? Certamente você
Ligações Químicas. Profª. Drª Narlize Silva Lira. Agosto /2014
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Ligações Químicas Profª. Drª Narlize Silva Lira Agosto /2014 A Química Orgânica e a Vida A química orgânica
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Ligações Químicas Profª. Drª Narlize Silva Lira Agosto /2014 A Química Orgânica e a Vida A química orgânica
3ª Filosofia Antiga (Pensadores antigos)
 3ª Filosofia Antiga (Pensadores antigos) Questão (1) - A filosofia se constitui, a partir das concepções de Sócrates, Platão e Aristóteles, como o pensamento que investiga: a) A questão da dívida externa.
3ª Filosofia Antiga (Pensadores antigos) Questão (1) - A filosofia se constitui, a partir das concepções de Sócrates, Platão e Aristóteles, como o pensamento que investiga: a) A questão da dívida externa.
ESTUDO DA MATÉRIA. QUÍMICA - Prof. Marcelo Uchida -
 ESTUDO DA MATÉRIA QUÍMICA - Prof. Marcelo Uchida - Matéria Material ou matéria é tudo aquilo que tem massa e ocupa lugar no espaço. Água Ar Madeira Ouro Corpo Porção limitada da matéria Barra de Ouro Tronco
ESTUDO DA MATÉRIA QUÍMICA - Prof. Marcelo Uchida - Matéria Material ou matéria é tudo aquilo que tem massa e ocupa lugar no espaço. Água Ar Madeira Ouro Corpo Porção limitada da matéria Barra de Ouro Tronco
INTRODUÇÃO AO ESTUDO DA DOUTRINA ESPÍRITA ESPÍRITA E ESPIRITISMO
 INTRODUÇÃO AO ESTUDO DA DOUTRINA ESPÍRITA 1 ESPÍRITA E ESPIRITISMO Para designar coisas novas, são necessárias palavras novas. A clareza de uma língua assim exige, a fim de evitar que uma mesma palavra
INTRODUÇÃO AO ESTUDO DA DOUTRINA ESPÍRITA 1 ESPÍRITA E ESPIRITISMO Para designar coisas novas, são necessárias palavras novas. A clareza de uma língua assim exige, a fim de evitar que uma mesma palavra
Exercícios Sobre LigaÇões iônicas
 Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
Tecnol. Mecânica: Produção do Gusa Introdução: conhecimentos tecnológicos que faltavam ao homem da antiguidade:
 Introdução Você já parou para imaginar um mundo sem coisas simples como facas, agulhas de costura, chaves, fechaduras, alfinetes lâminas de barbear? Pois é, não faz muito tempo, na verdade cerca de 500
Introdução Você já parou para imaginar um mundo sem coisas simples como facas, agulhas de costura, chaves, fechaduras, alfinetes lâminas de barbear? Pois é, não faz muito tempo, na verdade cerca de 500
MÉTODO CIENTÍFICO. BENEFÍCIOS DO MÉTODO: execução de atividade de forma mais segura, mais econômica e mais perfeita;
 MÉTODO CIENTÍFICO CONCEITO: palavra de origem grega, significa o conjunto de etapas e processos a serem vencidos ordenadamente na investigação da verdade; IMPORTÃNCIA DO MÉTODO: pode validar ou invalidar
MÉTODO CIENTÍFICO CONCEITO: palavra de origem grega, significa o conjunto de etapas e processos a serem vencidos ordenadamente na investigação da verdade; IMPORTÃNCIA DO MÉTODO: pode validar ou invalidar
QUÍMICA TECNOLÓGICA I
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG QUÍMICA TECNOLÓGICA I Prof a. Dr a. Flaviana Tavares Vieira flaviana.tavares@ufvjm.edu.br Alquimia
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG QUÍMICA TECNOLÓGICA I Prof a. Dr a. Flaviana Tavares Vieira flaviana.tavares@ufvjm.edu.br Alquimia
Introdução à Química. Prof. Fernando R. Xavier
 Introdução à Química Prof. Fernando R. Xavier UDESC 2013 Qual a idade da química? É possível identificar a presença da química desde a idade do bronze (3,300 a.c.). Ex.: Agricultura, conserva de alimentos,
Introdução à Química Prof. Fernando R. Xavier UDESC 2013 Qual a idade da química? É possível identificar a presença da química desde a idade do bronze (3,300 a.c.). Ex.: Agricultura, conserva de alimentos,
Quando esses temas são compreendidos, o aprendizado da química orgânica se torna muito mais fácil, diminuindo a necessidade de memorização.
 REAÇÕES ORGÂNIAS A primeira vista, a química orgânica pode ser observada como uma coleção confusa de milhões de compostos, dezenas de grupos funcionais e um número infinito de reações químicas. Ao estudá-la,
REAÇÕES ORGÂNIAS A primeira vista, a química orgânica pode ser observada como uma coleção confusa de milhões de compostos, dezenas de grupos funcionais e um número infinito de reações químicas. Ao estudá-la,
A Música na Antiguidade
 A Música na Antiguidade Josemar Bessa A palavra música deriva de arte das musas em uma referência à mitologia grega, marca fundamental da cultura da antigüidade ocidental. No entanto muitos estudiosos
A Música na Antiguidade Josemar Bessa A palavra música deriva de arte das musas em uma referência à mitologia grega, marca fundamental da cultura da antigüidade ocidental. No entanto muitos estudiosos
QUÍMICA. 3. (FCC BA) A reação abaixo pode ser classificada como endotérmica ou exotérmica? Justifique H2(g) + ½ O2(g) H2O(g) + 242kJ
 QUÍMICA Prof. Arthur LISTA DE EXERCÍCIOS - 2.8: TERMOQUÍMICA 1. (UFMG-MG) O gás natural (metano) é um combustível utilizado, em usinas termelétricas, na geração de eletricidade, a partir da energia liberada
QUÍMICA Prof. Arthur LISTA DE EXERCÍCIOS - 2.8: TERMOQUÍMICA 1. (UFMG-MG) O gás natural (metano) é um combustível utilizado, em usinas termelétricas, na geração de eletricidade, a partir da energia liberada
ESTADOS DA MATÉRIA. O átomo é composto por outras partículas ainda menores.
 ESTADOS DA MATÉRIA A matéria que temos a nossa volta é formada de moléculas que são constituídas por átomos. Uma combinação destes átomos forma as substâncias que conhecemos, porém, devemos salientar que
ESTADOS DA MATÉRIA A matéria que temos a nossa volta é formada de moléculas que são constituídas por átomos. Uma combinação destes átomos forma as substâncias que conhecemos, porém, devemos salientar que
Joseph Priestley. Camila Welikson. Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons.
 Camila Welikson Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode Mudança
Camila Welikson Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode Mudança
ESTUDO DO ÁTOMO. Palavras-chave: átomo. Nuclear. Radiação.
 ESTUDO DO ÁTOMO Isaias Jose dos Santos ISE - santosisaiasjose@yahoo.com.br Rodrigo dos Santos ISE.- antos.rodrigo10@hotmail.com Orientador: Francisco de Assis Andrade Resumo Desde o princípio da humanidade
ESTUDO DO ÁTOMO Isaias Jose dos Santos ISE - santosisaiasjose@yahoo.com.br Rodrigo dos Santos ISE.- antos.rodrigo10@hotmail.com Orientador: Francisco de Assis Andrade Resumo Desde o princípio da humanidade
De onde vêm as lágrimas?
 De onde vêm as lágrimas? É toda substância que, em solução aquosa, sofre dissociação, liberado pelo menos um cátion diferente de H + e um ânion diferente de OH -. a) Presença de oxigênio b) Sal não oxigenado
De onde vêm as lágrimas? É toda substância que, em solução aquosa, sofre dissociação, liberado pelo menos um cátion diferente de H + e um ânion diferente de OH -. a) Presença de oxigênio b) Sal não oxigenado
COLÉGIO NOSSA SENHORA DA PIEDADE. Programa de Recuperação Paralela. 2ª Etapa 2014. 1ª série Turma: FG
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 2ª Etapa 2014 Disciplina: QUÍMICA Professora: Maria Luiza 1ª série Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
DATA: 17/11/2015. 2. (ENEM) Discutindo sobre a intensificação do efeito estufa, Francisco Mendonça afirmava:
 EXERCÍCIOS REVISÃO QUÍMICA AMBIENTAL (EFEITO ESTUFA, DESTRUIÇÃO DA CAMADA DE OZÔNIO E CHUVA ÁCIDA) e EQUILÍBRIO QUÍMICO DATA: 17/11/2015 PROF. ANA 1. Na década de 70, alguns cientistas descobriram quais
EXERCÍCIOS REVISÃO QUÍMICA AMBIENTAL (EFEITO ESTUFA, DESTRUIÇÃO DA CAMADA DE OZÔNIO E CHUVA ÁCIDA) e EQUILÍBRIO QUÍMICO DATA: 17/11/2015 PROF. ANA 1. Na década de 70, alguns cientistas descobriram quais
Introdução. Gerais. Funcionais. Propriedades. da Matéria Organolépticas. Específicas. Químicas. Físicas. Química. Rômulo
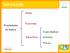 Introdução Gerais Propriedades Funcionais da Matéria Organolépticas Específicas s Físicas Propriedades Gerais São propriedades comuns a todo tipo de matéria massa extensão impenetrabilidade divisibilidade
Introdução Gerais Propriedades Funcionais da Matéria Organolépticas Específicas s Físicas Propriedades Gerais São propriedades comuns a todo tipo de matéria massa extensão impenetrabilidade divisibilidade
COLÉGIO SANTA TERESINHA R. Madre Beatriz 135 centro Tel. (33) 3341-1244 www.colegiosantateresinha.com.br
 PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
EQUAÇÕES E INEQUAÇÕES DE 1º GRAU
 1 EQUAÇÕES E INEQUAÇÕES DE 1º GRAU Equação do 1º grau Chamamos de equação do 1º grau em uma incógnita x, a qualquer expressão matemática que pode ser escrita sob a forma: em que a e b são números reais,
1 EQUAÇÕES E INEQUAÇÕES DE 1º GRAU Equação do 1º grau Chamamos de equação do 1º grau em uma incógnita x, a qualquer expressão matemática que pode ser escrita sob a forma: em que a e b são números reais,
O SOM E SEUS PARÂMETROS
 O SOM E SEUS PARÂMETROS Você já percebeu como o mundo está cheio de sons? Mas você já parou para pensar o que é o SOM? Pois bem, som é tudo o que nossos ouvidos podem ouvir, sejam barulhos, pessoas falando
O SOM E SEUS PARÂMETROS Você já percebeu como o mundo está cheio de sons? Mas você já parou para pensar o que é o SOM? Pois bem, som é tudo o que nossos ouvidos podem ouvir, sejam barulhos, pessoas falando
Estequiometria. Prof a. Dr a. Flaviana Tavares Vieira
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Estequiometria Prof a. Dr a. Flaviana Tavares Vieira -A palavra estequiometria deriva das palavras
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Diamantina - MG Estequiometria Prof a. Dr a. Flaviana Tavares Vieira -A palavra estequiometria deriva das palavras
Aluno (a): Professor:
 3º BIM P1 LISTA DE EXERCÍCIOS CIÊNCIAS 6º ANO Aluno (a): Professor: Turma: Turno: Data: / / Unidade: ( ) Asa Norte ( ) Águas Lindas ( )Ceilândia ( ) Gama ( )Guará ( ) Pistão Norte ( ) Recanto das Emas
3º BIM P1 LISTA DE EXERCÍCIOS CIÊNCIAS 6º ANO Aluno (a): Professor: Turma: Turno: Data: / / Unidade: ( ) Asa Norte ( ) Águas Lindas ( )Ceilândia ( ) Gama ( )Guará ( ) Pistão Norte ( ) Recanto das Emas
Equações do segundo grau
 Módulo 1 Unidade 4 Equações do segundo grau Para início de conversa... Nesta unidade, vamos avançar um pouco mais nas resoluções de equações. Na unidade anterior, você estudou sobre as equações de primeiro
Módulo 1 Unidade 4 Equações do segundo grau Para início de conversa... Nesta unidade, vamos avançar um pouco mais nas resoluções de equações. Na unidade anterior, você estudou sobre as equações de primeiro
UFU 2014 VESTIBULAR DE MAIO 1ª FASE
 UFU 2014 VESTIBULAR DE MAIO 1ª FASE 1-O iodo-132, devido à sua emissão de partículas beta e radiação gama, tem sido muito empregado no tratamento de problemas na tireoide. A curva abaixo ilustra o decaimento
UFU 2014 VESTIBULAR DE MAIO 1ª FASE 1-O iodo-132, devido à sua emissão de partículas beta e radiação gama, tem sido muito empregado no tratamento de problemas na tireoide. A curva abaixo ilustra o decaimento
OLIMPÍADA BRASILEIRA DE MATEMÁTICA DAS ESCOLAS PÚBLICAS (OBMEP): EXPERIÊNCIAS VIVENCIADAS A PARTIR DO PIBID UEPB MONTEIRO
 OLIMPÍADA BRASILEIRA DE MATEMÁTICA DAS ESCOLAS PÚBLICAS (OBMEP): EXPERIÊNCIAS VIVENCIADAS A PARTIR DO PIBID UEPB MONTEIRO Cícero Félix da Silva; Izailma Nunes de Lima; Ricardo Bandeira de Souza; Manoela
OLIMPÍADA BRASILEIRA DE MATEMÁTICA DAS ESCOLAS PÚBLICAS (OBMEP): EXPERIÊNCIAS VIVENCIADAS A PARTIR DO PIBID UEPB MONTEIRO Cícero Félix da Silva; Izailma Nunes de Lima; Ricardo Bandeira de Souza; Manoela
INTRODUÇÃO AO ESTUDO DO DIREITO - IED AULAS ABRIL E MAIO
 INTRODUÇÃO AO ESTUDO DO DIREITO - IED AULAS ABRIL E MAIO Docente: TIAGO CLEMENTE SOUZA E-mail: tiago_csouza@hotmail.com 2. Direito como objeto de conhecimento. Conforme pudemos observar nas aulas iniciais
INTRODUÇÃO AO ESTUDO DO DIREITO - IED AULAS ABRIL E MAIO Docente: TIAGO CLEMENTE SOUZA E-mail: tiago_csouza@hotmail.com 2. Direito como objeto de conhecimento. Conforme pudemos observar nas aulas iniciais
Transições de Fase de Substâncias Simples
 Transições de Fase de Substâncias Simples Como exemplo de transição de fase, vamos discutir a liquefação de uma amostra de gás por um processo de redução de volume a temperatura constante. Consideremos,
Transições de Fase de Substâncias Simples Como exemplo de transição de fase, vamos discutir a liquefação de uma amostra de gás por um processo de redução de volume a temperatura constante. Consideremos,
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007
 Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
Escola Básica e Secundária Gonçalves Zarco Ciências Físico-Químicas, 9º ano Ano lectivo 2006 / 2007 Ficha de Trabalho, nº 2 CORRECÇÃO Nome: n.º aluno: Turma: 1. Nas frases seguintes, risca as palavras
