2015 Dr. Walter F. de Azevedo Jr. Produção e Propriedades dos Raios X
|
|
|
- Kátia Aldeia Franco
- 7 Há anos
- Visualizações:
Transcrição
1 2015 Dr. Walter F. de Azevedo Jr Produção e Propriedades dos Raios X 1
2 Espectro de Emissão de Luz No experimento abaixo temos o gás hidrogênio introduzido num tubo de vidro. No tubo temos dois eletrodos, que são submetidos a uma diferença de potencial (E). Tal diferença de potencial é alta o suficiente para ionizar o gás hidrogênio (arrancar elétrons do átomo) gerando luz. No diagrama abaixo, a luz incide sobre um anteparo com uma fenda, que por sua vez incide sobre um prisma. O prisma decompõe a luz, gerando o espectro de emissão do gás. Espectro de emissão E Prisma Gás excitado Anteparo 2
3 Espectro de Emissão de Luz Experimentos, como o descrito anteriormente, foram realizados para diferentes gases, gerando padrões de espectro de emissão distintos. Cada gás apresenta um padrão característico, que o identifica, como nossas impressões digitais. A observação do espectro de emissão discreto, como o mostrado ao lado, não tem explicação a partir da física clássica. Os conhecimentos da física do final do século XIX, indicavam que o gás deveria produzir um espectro contínuo, com todas as cores do arco-íris. A visualização de um espectro de emissão discreto (com raias definidas), levantou novas questões sobre o átomo e como este absorve e emite a luz. Ao lado temos os espectros de emissão dos gases hidrogênio e hélio. Espectro de emissão do hidrogênio Espectro de emissão do hélio Espectro de emissão do hidrogênio. Disponível em: < > Espectro de emissão do hélio. Disponível em: < > Acesso em: 16 de junho de
4 Espectro de Absorção de Luz No experimento ilustrado abaixo, temos uma luz branca incidindo sobre um anteparo com uma fenda, que permite que a luz incida sobre um prisma gerando a decomposição da luz branca nas cores do arco-íris. Luz branca Prisma Anteparo 4
5 Espectro de Absorção de Luz Inserimos, entre a fonte de luz branca e o anteparo, um tubo com gás hidrogênio. Nenhuma descarga elétrica é aplicada ao tubo e deixamos a luz passar por ele. O resultado é o aparecimento de raias de absorção, as linhas pretas da figura, tais linhas indicam que o gás está absorvendo a luz para aqueles comprimentos de onda. O que observamos é o espectro de absorção, que não pode ser explicado pela física clássica. Luz branca Prisma Tubo de vidro com gás Anteparo 5
6 Modelo de Bohr O primeiro modelo satisfatório para o átomo, foi proposto por Neils Bohr em Para superar o problema da instabilidade do elétron em sua órbita, Bohr introduziu um postulado, conhecido como primeiro postulado de Bohr. As órbitas dos elétrons são não irradiantes. Assim, os elétrons nos átomos, não podem ter qualquer órbita, somente órbitas não irradiantes. O átomo de Bohr apresenta um conjunto de órbitas permitidas para o elétron. Ao passar de uma órbita para outra o elétron irradia, ou absorve radiação. Postulado (segundo o dicionário Houaiss): substantivo masculino 1 o que se considera como fato reconhecido e ponto de partida, implícito ou explícito, de uma argumentação; premissa 2 afirmação ou fato admitido sem necessidade de demonstração Fonte: =k (acesso em 16/05/2015) Representação artística da órbita de um elétron em torno do núcleo (não mostrado na figura). O modelo atômico de Bohr prevê que os elétrons não podem ter qualquer órbita em torno do núcleo, só órbitas permitidas. Uma vez nestas órbitas os elétrons não emitem energia, gerando um modelo estável do ponto de vista energético. Fonte da imagem: < > Acesso em: 16 de junho de
7 Modelo de Bohr Quando um elétron muda para uma órbita permitida de mais alta energia ele absorve um fóton. Quando vai para uma órbita de mais baixa energia ele emite fótons. O segundo postulado de Bohr prevê que a energia do fóton é dada pela conservação da energia, como segue: Ei E f f onde E i e E f são energias inicial e final, respectivamente, h a constante de Planck (h = 6, J.s) e f a frequência do fóton (em Hertz). Fótons são partículas de luz, que tem energia (E), dada pela equação abaixo: h Representação artística gerada por computador da emissão de um fóton de luz amarela. O modelo de Bohr prevê que essa emissão ocorre quando um elétron passa de uma órbita de alta energia para uma órbita de energia mais baixa. O excesso da energia é convertido em energia luminosa, um fóton. E = h.f Fonte da imagem: < > Acesso em: 16 de junho de
8 Modelo de Bohr A constante de Planck é usada para vários cálculos relacionados ao modelo atômico. No sistema internacional (SI) ela é dada em unidades de J.s e tem o seguinte valor: h = 6, J.s Esta grandeza pode ser expressa em uma unidade muito usada em análise de sistemas atômicos, chamada ev. Temos que 1 ev = 1, J, assim podemos converter de J.s para ev.s, dividindo-se h por 1, , nesta unidade temos: E = h.f Fóton emitido n 1 n 2 n 3 h = 4, ev.s. Usaremos a constante de Planck em ev.s, toda vez que a energia for expressa em ev, caso contrário usaremos em J.s. Representação de um átomo de Bohr. O elétron no átomo sofre uma transição do nível 3 para o nível 2, emitindo um fóton com energia igual a h.f, onde h é a constante de Planck e f a frequência do fóton emitido. 8
9 Modelo de Bohr O modelo de Bohr, para um átomo de número atômico Z, representa o núcleo com carga positiva (+Z), e elétrons girando em volta do núcleo em órbitas não irradiantes, conforme a figura ao lado. No modelo de Bohr o elétron está submetido a uma força centrípeta, de origem elétrica, devido à atração entre o elétron negativo e o núcleo positivo. Aplicando-se os postulados de Bohr e a atração elétrica entre o elétron e o núcleo, chegamos a um conjunto de equações simples, que mostram que o elétron no átomo não pode ter qualquer energia, ou seja, a energia do átomo é quantizada. O termo quantizado significa não contínuo, ou seja, não pode apresentar qualquer valor, e sim valores discretos. +Ze Modelo de Bohr para um átomo com número de prótons (Z) e um elétron girando em torno de núcleo. r F -e v 9
10 Modelo de Bohr O raio da órbita do elétron (r n ) no nível n é dado pela seguinte equação: r n = n 2 r 1 onde r 1 = 0,53 Å. Para a primeira órbita, o estado fundamental do átomo, temos (n=1): r 3 r 2 r 1 r 1 = 0,53 Å Para a segunda órbita (n=2): r 2 = n 2.0,53 Å = 2 2.0,53 Å = 4.0,53 Å = 2,12 Å Fóton é emitido com energia E = hf E assim podemos determinar o raio para qualquer órbita, é só substituir o número n, chamado número quântico principal, na equação acima. 10 Modelo de Bohr para um átomo, onde vemos as 3 primeiras órbitas e uma transição do elétron da segunda (n = 2) para a primeira órbita (n = 1).
11 Modelo de Bohr A energia do elétron (E m ) no nível n é dada por: E n 13,6 ev n 2 r 3 r 2 Para o nível 1 (estado fundamental do átomo) temos (n=1) e, r 1 13,6 ev En ,6 ev 13,6 ev 1 Fóton é emitido com energia E = hf e assim podemos calcular para qualquer nível. 11
12 Modelo de Bohr No diagrama abaixo temos a transição do nível de energia 2 (E 2 ) para o nível de energia 1 (E 1 ) (estado fundamental). Na transição o átomo perde energia, que é transformada em luz. A luz manifesta-se na forma de um fóton de frequência (f), dada pela equação: E i E f hf f E i E h f E i 13,6 ev n 2 i E 2 E = h.f, onde h é constante de Planck e f a freqüência. E f 13,6 ev n 2 f E 1 12
13 Energia (ev) Modelo de Bohr Diagrama de níveis de energia para o átomo de H n n 4 n 3 n 2 Energia do elétron no nível n (E n ) para o átomo de H: E n 13,6 ev 2 n Para n = 1 temos: 13,6 ev En ,6 ev 13,6 ev 1-13,6 n 1 Usaremos a equação acima para determinar os 4 primeiros níveis do átomo de hidrogênio, mostrado nos próximos slides. 13
14 Energia (ev) Modelo de Bohr Diagrama de níveis de energia para o átomo de H -3,40 n n 4 n 3 n 2 Energia do elétron no nível n (E n ) para o átomo de H: E n 13,6 ev 2 n Para n = 2 temos: 13,6 ev En 2 2 3,4 ev 13,6 ev 4-13,6 n 1 14
15 Energia (ev) Modelo de Bohr Diagrama de níveis de energia para o átomo de H -1,51-3,40 n n 4 n 3 n 2 Energia do elétron no nível n (E n ) para o átomo de H: E n 13,6 ev 2 n Para n = 3 temos: 13,6 ev En 2 3 1,51eV 13,6 ev 9-13,6 n 1 15
16 Energia (ev) Modelo de Bohr Diagrama de níveis de energia para o átomo de H -0,85-1,51-3,40 n n 4 n 3 n 2 Energia do elétron no nível n (E n ) para o átomo de H: E n 13,6 ev 2 n Para n = 4 temos: 13,6 ev En 2 4 0,85 ev 13,6 ev 16-13,6 n 1 16
17 Energia (ev) Modelo de Bohr Diagrama de níveis de energia para o átomo de H 0-0,85-1,51-3,40 n n 4 n 3 n 2 Aplicando-se sucessivamente a equação abaixo, montamos o diagrama de níveis de energia do átomo de H. 13,6 ev En 2 n -13,6 n 1 Quando n tende a infinito temos que a energia tende a zero. E n 0 ev O gráfico ao lado é chamado diagrama de níveis de energia, nele vemos os níveis de energia de um átomo, o que facilita a visualização de transições entre níveis de energia. 17
18 Energia (ev) Modelo de Bohr Diagrama de níveis de energia para o átomo de H 0-0,85-1,51-3,40 n n 4 n 3 n 2 Um elétron com energia zero indica que o elétron não está mais ligado ao átomo, ou seja, energias maiores que zero indicam que o elétron saiu do átomo. Para ionizar um átomo, temos que adicionar energia para que o mesmo apresente pelo menos energia zero. Assim, se um elétron apresenta energia -13,6 ev, temos que adicionar + 13,6 ev para ionizá-lo, ou seja, arrancá-lo do átomo de hidrogênio. -13,6 n 1 18
19 Energia (ev) Modelo de Bohr Diagrama de níveis de energia para o átomo de H 0-0,85-1,51-3,40 n n 4 n 3 n 2 Uma transição entre níveis de energia pode ser indicada por setas entre os níveis energéticos. Como exemplo vamos considerar uma transição entre os níveis 2 e 1, indicada pela seta vertical. A seta indica que o elétron estava no nível 2 (n 2 ), com energia -3,4 ev, e sofreu uma transição para o nível 1 (n 1 ), chamado estado fundamental, com -13,6 ev de energia. Na transição há liberação de 10,2 ev de energia na forma de fóton. Pelo diagrama de níveis de energia fica clara a transição. -13,6 n 1 19
20 Energia (ev) Modelo de Bohr Diagrama de níveis de energia para o átomo de H 0-0,85-1,51-3,40-13,6 n n 4 n 3 n 2 n 1 Vejamos agora uma transição entre os níveis 1 e 3, indicada pela seta vertical. A seta indica que o elétron estava no nível 1 (n 1 ), com energia -13,6 ev, e sofreu uma transição para o nível 3 (n 3 ), com -1,51 ev de energia. Na transição há absorção de 12,09 ev de energia, na forma de fóton. No diagrama de níveis de energia vemos a transição. Segundo o modelo atômico de Bohr, a radiação eletromagnética é emitida ou absorvida, quando um elétron faz uma transição de uma órbita para outra. Todos átomos ou moléculas apresentam um diagrama de níveis de energia, o que facilita a representação de transições no átomo ou molécula. 20
21 Modelo de Bohr O diagrama ao lado indica o núcleo positivo do átomo de hidrogênio e as órbitas para os 3 primeiros níveis ( n =1, n =2 e n = 3). Do lado direito temos o diagrama de níveis de energia (E), indicando as transições que ocorrem. Na animação temos a simulação da transição do nível 3 para o nível 1 (emissão do fóton) e a transição do nível 1 para o nível 3 (absorção do fóton). Fim Início Energia (ev) 0-1,51-3,40-13,6 Distância (Å) Imagem disponível em:< welcome.html > Acesso em: 16 de junho de
22 Modelo de Bohr (Exemplo 1) Exemplo 1. Calcule o comprimento de onda () da radiação emitida quando o elétron do átomo de hidrogênio efetua uma transição de n i =2 para n f =1. Sabemos que a energia do fóton é dada por: E = hf. Solução Vimos no estudo de ondas que a frequência (f) e o comprimento de onda () relacionam-se pela equação:.f = c, onde c é a velocidade da luz. n 1 n 2 n 3 Fóton é emitido com comprimento de onda () Assim, a frequência (f) pode ser dada por: Substituindo a equação acima na equação da energia temos: f E c λ hf hc Se a energia E for a energia perdida na transição teremos: hc E 2 E 1 hc E 22
23 Modelo de Bohr (Exemplo 1, continuação) Sabemos que a energia do nível 2 do átomo de hidrogênio é -3,4 ev e a energia do estado fundamental (nível 1) é -13,6 ev. Usando-se a constante de Planck 4, ev.s, a velocidade da luz c = m/s, temos: hc E 2 E 1 n 1 n 2 n 3 15 (4,14.10 )(3.10 λ 3,4 13, (12, ) 10,2 1, , nm m 1,22.10 Å Å ) (12, , Å ) Fóton é emitido com energia E 23
24 Modelo de Bohr (Exemplo 2) Exemplo 2. Calcule o comprimento de onda da radiação emitida quando o elétron do átomo de hidrogênio efetua uma transição de n i =3 para n f =1. Solução h=6, J.s = 4, ev.s n 1 n 2 n 3 hc E 3 E 1 0, , ( 4, )( , 85 ( 13, 6) 15 ( 12, , m , ) Å 8 ) ( 12, , , ) -7 1 m = Å m 9, Å 974, 1 Å -8 m Fóton é emitido com comprimento de onda () 24
25 Modelo de Bohr (Exemplo 3) Exemplo 3. Calcule a energia em elétron-volts (ev) de um fóton emitido por um pointer de laser de cor vermelha, com comprimento de onda de 671 nm (1 nm = 10-9 m). Solução E hc 15 4,14.10 ev. s m 8 m / s E 12, , ev E 1,85eV 25
26 Interação da Radiação com a Matéria Partículas como elétrons, pósitrons ou partículas alfa e radiações como gama e raios X são geradas durante o decaimento radioativo ou por meio da desaceleração e/ou aceleração de partículas carregadas. Essas radiações interagem com a matéria, por meio de transferência de energia. Esses processos envolvem transições dos elétrons e são importantes para aplicações médicas e biológicas, bem como para as bases da dosimetria e detecção de radiação Os principais processos, onde há interação da radiação com a matéria, são indicados ao lado. Ionização Excitação Captura 26
27 Interação da Radiação com a Matéria Quando uma partícula, ou um fóton, de energia suficiente, incide sobre um átomo, ocorre a ejeção de um elétron desse átomo, ou seja, temos a ionização do átomo. A condição para que isto ocorra, é que a energia da partícula ou fóton incidente, seja maior ou igual à energia do nível onde se encontra o elétron. Temos como resultado, um átomo com carga positiva e um elétron livre com energia cinética. O elétron pode ionizar outro átomo. Elétron incidente Elétron ejetado K L K L Átomo no estado fundamental Átomo sem 1 elétron na camada K 27
28 Interação da Radiação com a Matéria Um átomo ionizado, quando absorve um elétron, emite o excesso de energia na forma de um fóton, este processo é chamado captura, como indicado no diagrama abaixo. Elétron livre Emissão de fóton K L K L Átomo ionizado Átomo sem 1 elétron na camada K 28
29 Interação da Radiação com a Matéria Outra forma de interação da radiação com a matéria, é por meio da absorção da energia de uma partícula ou de um fóton por um elétron de um átomo, onde esse elétron salta para uma camada de mais alta energia (como na figura abaixo), chamamos a este processo de excitação. Essa transição leva o átomo a um estado excitado, onde haverá a emissão do excesso de energia na forma de um fóton. A condição para que ocorra a transição, é que a energia incidente seja igual à diferença de energia entre dois níveis. Radiação incidente Elétron num estado de mais alta energia (excitado) Emissão de fóton K L K L K L Átomo no estado fundamental Átomo no estado excitado Átomo no estado fundamental 29
30 Interação da Radiação com a Matéria As radiações podem ser classificadas considerando-se suas características majoritárias, assim temos a seguinte divisão: Eletromagnética: 1) Ultravioleta 2) Raios X e 2) gama Corpuscular: 1) Alfa, 2) Beta e 3) Nêutrons Emissão de partícula alfa. Imagem disponível em: Acesso em: 6 de maio de
31 Interação da Radiação com a Matéria Radiação gama ou raios gama. É uma radiação eletromagnética de alta energia. É produzida em processos nucleares, tais como aniquilação de pares elétronpósitron. A radiação gama forma a parte mais energética do espectro eletromagnético (localizada à esquerda do gráfico abaixo). Raios X. É a segunda radiação mais energética, pode ser produzida pela aceleração de partículas carregadas. Espectro de radiação eletromagnética, com escala de comprimento de onda em metros. 31
32 Interação da Radiação com a Matéria Radiação alfa ou partícula alfa. É formada por um núcleo do átomo Hélio, ou seja, dois prótons e dois nêutrons. É uma radiação de baixa penetração. É produzida pelo decaimento radioativo de elementos químicos, como urânio e rádio. Radiação beta ou partícula beta. É composta por elétrons ou pósitrons de alta energia e são emitidos por núcleos atômicos como o potássio 40. Possui um poder de penetração maior que das partículas alfa. A produção de partículas beta é chamada decaimento beta. Nêutrons. É um feixe de nêutrons, pode ser produzido em aceleradores de partículas, ou em reatores nucleares. Representação artística da emissão de partícula alfa de um núcleo. Prótons são esferas amarelas e laranjas. Em azul temos os nêutrons. Imagem disponível em: < 32 Acesso em: 6 de maio de 2015.
33 Produção de Raios X Os raios X foram descobertos em 1895 de forma quase acidental. O físico alemão Wilhelm Conrad Roentgen realizava experimentos com um tudo de vidro, onde foi feito vácuo. Nesse tubo de vidro havia dois eletrodos, e uma diferença de potencial de milhares de volts foi aplicada. Tal diferença de potencial levou elétrons migrarem de um eletrodo para outro, gerando uma radiação desconhecida até então, que Roentgen chamou de raios X. Diversos testes foram feitos, e num dos experimentos Roentgen descobriu a radiografia médica de raios X (mostrada ao lado). Roentgen usou a mão de sua esposa (Anna Bertha Ludwig) para registrar a radiografia. Foto disponível em: < > Acesso em: 6 de maio de
34 Raios X Considere um tubo de vidro onde foi feito vácuo, onde temos dois eletrodos inseridos, conforme o esquema abaixo. O catodo apresenta um filamento que ao ser aquecido, devido à passagem da corrente elétrica I, gera uma nuvem de elétrons. O anodo apresenta uma diferença de potencial (V2) em relação ao catodo. Tal ddp promove a aceleração dos elétrons do catodo para o anodo. 34
35 Raios X Os elétrons são acelerados e colidem com o anodo. Esta colisão converte a energia cinética em energia térmica, que aquece o anodo, e em radiação eletromagnética, na forma de raios X. Com uma ddp da ordem de algumas dezenas de kv teremos a geração de raios X. Este espectro de raios X é chamado radiação branca, que se sobrepõe ao espectro característico, devido à retirada de elétrons dos átomos do anodo. 35
36 Raios X Característicos O modelo de Bohr é suficiente para entendermos os principais aspectos do espectro característico de raios X. Considere que os átomos do anodo são bombardeados com elétrons com energia cinética. Esses elétrons apresentam energia suficiente para arrancar elétrons da camada K do átomo, como mostrado na figura abaixo. Elétron incidente Elétron ejetado K L K L Átomo no estado fundamental Átomo sem 1 elétron na camada K 36
37 Raios X Característicos O átomo sem um elétron é instável e tende a absorver um elétron de uma camada mais externa. Ao absorver este elétron, o excesso de energia é emitido na forma de um fóton de raios X. Elétron ejetado Emissão de um fóton de raios X K L K L Átomo sem 1 elétron na camada K Átomo sem 1 elétron na camada K 37
38 Raios X Característicos A energia cinética dos elétrons é perdida no impacto com o anodo. Boa parte desta energia é convertida em calor, tanto é que nos tubos de raios X comerciais temos um sistema de refrigeração para dissipar o calor gerado com o choque do feixe de elétrons. Devido à diferença de potencial V, existente entre o anodo e catodo, os elétrons apresentam energia potencial U = ev, onde e é a carga do elétron. Do eletromagnetismo clássico sabemos que toda partícula carregada acelerada ou desacelerada emite radiação, os elétrons que chocam-se o anodo e perdem toda sua energia no impacto, produzem raios X com a mais alta energia possível, ou seja, com o menor comprimento de onda ( min ), vamos determiná-lo, como segue: ev min min hf hc min hc ev 12,4.10 V 3 onde h é constante de Plack, c a velocidade da luz. (Esta equação já retorna o comprimento de onda em Å) 38
39 Intensidade (unidades arbitrárias) Raios X Característicos A radiação X devida à desaceleração dos elétrons produz o que chamamos de espectro contínuo, ou radiação branca. A voltagem necessária para produção de raios X é da ordem de dezenas de kilovolts. A figura ao lado ilustra a variação da intensidade em função do comprimento de onda, para voltagens no tubo de 5, 10, 15, 20 e 25 kv. A posição em destaque SWL indica o comprimento de onda mínino (short wavelength limit), a partir do qual começa a produção de raios X. Devemos pensar que nem todos os elétrons perdem sua energia cinética em um choque. Muitos elétrons sobre uma sequência de choques onde vão perdendo frações da sua energia inicial, esses elétrons resultam em fótons menos energéticos. K K 25 kv 20 kv 15 kv 10 kv Comprimento de onda (Å) 5 kv Fonte: Modificado de Cullity, B. D. & Stock, S. R. Elements of X-Ray diffraction. 3rd ed. Pg
40 Intensidade (unidades arbitrárias) Raios X Característicos Até 20 kv os espectros de raios X apresentam o mesmo comportamento, ou seja, apesar do aumento da intensidade dos raios X, conforme aumentamos a voltagem, a curva do espectro é suave. A partir de 25 kv temos pelo menos dois picos claros, sobrepondo-se ao espectro contínuo, indicados na figura como K e K. K K 25 kv 20 kv 15 kv 10 kv 5 kv Comprimento de onda (Å) Fonte: Modificado de Cullity, B. D. & Stock, S. R. Elements of X-Ray diffraction. 3rd ed. Pg
41 Intensidade (unidades arbitrárias) Raios X Característicos Os novos picos observados são chamados de espectro característico, sua formação ocorre devido à geração de lacunas na camada K ou L do metal do anodo. Essas lacunas geradas levam os átomos do alvo a um estado energeticamente instável, nessa situação o átomo tende a absorver um elétron, emitindo no processo um fóton de raios X. Ao emitir o fóton de raios X o átomo diminui sua energia total. As lacunas são geradas devido ao choque dos elétrons do feixe, que apresentam energia cinética suficiente para arrancar elétrons das camadas mais internas do átomos. K K 25 kv 20 kv 15 kv 10 kv Comprimento de onda (Å) 5 kv Fonte: Modificado de Cullity, B. D. & Stock, S. R. Elements of X-Ray diffraction. 3rd ed. Pg
42 Raios X Característicos Na figura ao lado temos o modelo de Bohr, para um átomo do metal que compõe o anodo do tubo de raios X. Neste diagrama vemos que transições da camada L para K produzem o pico de K, da camada M para K produzem o pico de K e da camada M para L o pico L. O pico K é o mais energético, como podemos ver na figura anterior, mas tem intensidade de raios X menor que o K. K K Núcleo L K L M 42
43 Raios X Característicos As camadas podem na verdade apresentar diversos subníveis, no caso da camada L temos 3 subníveis, indicados por L 1, L 2 e L 3. As transições permitidas entre as camadas K e L envolvem transições entre as camadas L 2 e K 1 e L 3 e K 1, dando origem a dois picos próximos, chamados de K 1 e K 2. Esses picos próximos são chamados de dupletos. 43
44 Produção de Raios X A figura abaixo mostra uma seção de um tubo de raios X de anodo fixo. Fonte: 44
45 Produção de Raios X A figura abaixo uma foto de um tubo de raios X. Fonte: 45
46 Produção de Raios X A incidência do feixe de elétrons num ponto gera calor, que pode levar o anodo a derreter. Para conseguir maior intensidade, sem fundir o anodo, podemos colocar o mesmo girando, de forma que o ponto de incidência do feixe varia. Tal sistema é chamado fonte de anodo rotatório. Imagem disponível em: < > Acesso em: 16 de junho de
47 Produção de Raios X Do eletromagnetismo clássico sabemos que toda partícula com carga elétrica, quando acelerada emite radiação. Ao acelerarmos um elétron, ou pósitron, e confinarmos esta partícula em um toróide, onde foi feito vácuo, teremos produção de radiação. Tal sistema de produção de radiação é chamado síncrotron. A radiação produzida é chamada radiação síncrotron, inclui radiação visível, ultravioleta e raios X. Diagrama esquemático do Laboratório Nacional de Luz Síncrotron (LNLS). Fonte: 47
48 Produção de Raios X O Laboratório Nacional de Luz Síncrotron (LNLS) é o primeiro laboratório desse tipo a ser construído no hemisfério Sul. O LNLS produz radiação intensa que tem sido usado para experimentos de cristalografia, espectroscopia e outras técnicas. Foto. Cortesia da Dra. Ana Luiza Vivan. 48
49 O LNLS foi inaugurado em junho de 1997, e desde então tem sido usado de forma intensa pela comunidade científica brasileira e internacional. 49 Foto. Cortesia de Anne Villela
50 LNLS 50 Foto. Cortesia de Anne Villela
51 LNLS 51 Foto. Cortesia de Anne Villela
52 Síncrotron Principais aplicações biológicas 1) Estudo da estrutura quaternária de macromoléculas biológicas (Técnica de espalhamento de raios X a baixo ângulo) (Small-angle X-ray Scattering, SAXS). Nesta técnica uma macromolécula dissolvida em tampão é submetida à intensa radiação do síncrotron (na faixa de comprimento de onda dos raios X). Os raios X, ao interagirem com a solução da macromolécula dissolvida, produzem uma curva de espalhamento, de onde é possível inferir informações sobre a topologia da molécula. Figura A. Gráfico da função de distribuição de distâncias, obtidas a partir da análise das curvas de espalhamento de raios X a baixo ângulo (SAXS). B. Modelo da proteína referente à curva à esquerda. Fonte: Vivan AL et al. (2008) Proteins, 72(4): , DOI: /prot
53 Síncrotron 2) Elucidação da estrutura tridimensional da macromoléculas biológicas (Cristalografia por difração de raios X). Nesta técnica cristais de proteínas são submetidos à intensa radiação produzida pelo síncrotron (raios X). Esses raios X interagem com o cristal e produzem um padrão de difração de raios X, que é usado para a elucidação da estrutura tridimensional de proteínas. Estrutural cristalográfica de chiquimato quinase de Mycobacterium tuberculosis. Pereira JH, de Oliveira JS, Canduri F, Dias MV, Palma MS, Basso LA, Santos DS, de Azevedo WF Jr. Structure of shikimate kinase from Mycobacterium tuberculosis reveals the binding of shikimic acid. Acta Crystallogr D Biol Crystallogr Dec;60(Pt 12 Pt 2):
54 Referências Drenth, J. (1994). Principles of Protein X-ray Crystallography. Verlag. New York: Springer- Rhodes, G. (2000). Crystallography Made Crystal Clear. 2 nd ed.san Diego: Academic Press. Stout, G. H. & Jensen, L. H. (1989). X-Ray Structure Determination. A Practical Guide. 2nd ed. New York: John Wiley & Sons. 54
2018 Dr. Walter F. de Azevedo Jr.
 2018 Dr. Walter F. de Azevedo Jr. 000000000000000000000000000000000000000 000000000000000000000000000000000000000 000000000000111111111110001100000000000 000000000001111111111111111111000000001 000000000111111111111111111111111000000
2018 Dr. Walter F. de Azevedo Jr. 000000000000000000000000000000000000000 000000000000000000000000000000000000000 000000000000111111111110001100000000000 000000000001111111111111111111000000001 000000000111111111111111111111111000000
2018 Dr. Walter F. de Azevedo Jr. Produção e Propriedades dos Raios X
 2018 Dr. Walter F. de Azevedo Jr. 000000000000000000000000000000000000000 000000000000000000000000000000000000000 000000000000111111111110001100000000000 000000000001111111111111111111000000001 000000000111111111111111111111111000000
2018 Dr. Walter F. de Azevedo Jr. 000000000000000000000000000000000000000 000000000000000000000000000000000000000 000000000000111111111110001100000000000 000000000001111111111111111111000000001 000000000111111111111111111111111000000
Introd. Física Médica
 Introd. Física Médica O Efeito Foto Elétrico (EFE) Introdução a Física Médica O Efeito Foto Elétrico (EFE) Introdução a Fís sica Médica Heinrich HERTZ descobriu o Efeito FotoElétrico (1887): Quando a luz
Introd. Física Médica O Efeito Foto Elétrico (EFE) Introdução a Física Médica O Efeito Foto Elétrico (EFE) Introdução a Fís sica Médica Heinrich HERTZ descobriu o Efeito FotoElétrico (1887): Quando a luz
QUESTÕES DE FÍSICA MODERNA
 QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
QUESTÕES DE FÍSICA MODERNA 1) Em diodos emissores de luz, conhecidos como LEDs, a emissão de luz ocorre quando elétrons passam de um nível de maior energia para um outro de menor energia. Dois tipos comuns
Física D Extensivo V. 8
 Física D Extensivo V. 8 Exercícios 0) C f R X > f WZ 0) B 03) E 04) E raios X > luz Raios X são radiações eletromagnéticas com um comprimento de onda muito curto, aproximadamente de 0,06 até 0 Å. Formam-se
Física D Extensivo V. 8 Exercícios 0) C f R X > f WZ 0) B 03) E 04) E raios X > luz Raios X são radiações eletromagnéticas com um comprimento de onda muito curto, aproximadamente de 0,06 até 0 Å. Formam-se
Prof. Dr. Lucas Barboza Sarno da Silva
 Prof. Dr. Lucas Barboza Sarno da Silva O Efeito Compton Einstein, em 1919, concluiu que um fóton de energia E se desloca em uma única direção (diferentemente de uma onda esférica) e é portador de um momento
Prof. Dr. Lucas Barboza Sarno da Silva O Efeito Compton Einstein, em 1919, concluiu que um fóton de energia E se desloca em uma única direção (diferentemente de uma onda esférica) e é portador de um momento
RAIOS-X (RAIOS RÖNTGEN)
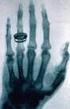 RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
RAIOS-X (RAIOS RÖNTGEN)
 RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
RAIOS-X (RAIOS RÖNTGEN) Descobertos por Wilhelm Röntgen (1895) Primeiro prêmio Nobel em física (1901) Radiação extremamente penetrante (
Uma breve história do mundo dos quanta. Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso
 Uma breve história do mundo dos Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso Tópicos da Segunda Aula Abordagem histórica Radiação de corpo negro Efeito fotoelétrico Espalhamento Compton
Uma breve história do mundo dos Érica Polycarpo Equipe de Física Coordenação: Prof. Marta Barroso Tópicos da Segunda Aula Abordagem histórica Radiação de corpo negro Efeito fotoelétrico Espalhamento Compton
INTERPRETAÇÃO DO EXPERIMENTO DE FRANCK E HERTZ EM CONTRAPOSIÇÃO À INTERPRETAÇÃO DE NEILS BOHR E ALBERT EINSTEIN
 INTERPRETAÇÃO DO EXPERIMENTO DE FRANCK E HERTZ EM CONTRAPOSIÇÃO À INTERPRETAÇÃO DE NEILS BOHR E ALBERT EINSTEIN LUIZ CARLOS DE ALMEIDA O experimento e suas interpretações dentro de uma visão da quantização
INTERPRETAÇÃO DO EXPERIMENTO DE FRANCK E HERTZ EM CONTRAPOSIÇÃO À INTERPRETAÇÃO DE NEILS BOHR E ALBERT EINSTEIN LUIZ CARLOS DE ALMEIDA O experimento e suas interpretações dentro de uma visão da quantização
2. Propriedades Corpusculares das Ondas
 2. Propriedades Corpusculares das Ondas Sumário Revisão sobre ondas eletromagnéticas Radiação térmica Hipótese dos quanta de Planck Efeito Fotoelétrico Geração de raios-x Absorção de raios-x Ondas eletromagnéticas
2. Propriedades Corpusculares das Ondas Sumário Revisão sobre ondas eletromagnéticas Radiação térmica Hipótese dos quanta de Planck Efeito Fotoelétrico Geração de raios-x Absorção de raios-x Ondas eletromagnéticas
Prof. Dr. Lucas Barboza Sarno da Silva
 Prof. Dr. Lucas Barboza Sarno da Silva Espectros atômicos Toda substância a uma certa temperatura emite radiação térmica, caracterizada por uma distribuição contínua de comprimentos de onda. A forma da
Prof. Dr. Lucas Barboza Sarno da Silva Espectros atômicos Toda substância a uma certa temperatura emite radiação térmica, caracterizada por uma distribuição contínua de comprimentos de onda. A forma da
Disciplina: Física IV Física Moderna
 Disciplina: Física IV Física Moderna Instrutor: Prof. Carlos Eduardo Souza - Cadu Sala: A2-15 (IF, andar 1P) Email: carloseduardosouza@id.uff.br Site do curso: http://cursos.if.uff.br/fisicaiv_xxi_0216/
Disciplina: Física IV Física Moderna Instrutor: Prof. Carlos Eduardo Souza - Cadu Sala: A2-15 (IF, andar 1P) Email: carloseduardosouza@id.uff.br Site do curso: http://cursos.if.uff.br/fisicaiv_xxi_0216/
Principais modelos atômicos. Principais modelos atômicos Modelo Atômico de Rutherford (1911)
 Principais modelos atômicos Modelo Atômico de Thomson (898) Com a descoberta dos prótons e elétrons, Thomson propôs um modelo de átomo no qual os elétrons e os prótons, estariam uniformemente distribuídos,
Principais modelos atômicos Modelo Atômico de Thomson (898) Com a descoberta dos prótons e elétrons, Thomson propôs um modelo de átomo no qual os elétrons e os prótons, estariam uniformemente distribuídos,
PRODUÇÃO DE RAIOS X. Produção de raios X Tubo de raios X. Produção de raio x Tubo de raios X
 PRODUÇÃO DE RAIOS X Prof. André L. C. Conceição DAFIS Curitiba, 17 de abril de 2015 Produção de raios X Tubo de raios X Os raios X são uma das maiores ferramentas médicas de diagnóstico desde sua descoberta
PRODUÇÃO DE RAIOS X Prof. André L. C. Conceição DAFIS Curitiba, 17 de abril de 2015 Produção de raios X Tubo de raios X Os raios X são uma das maiores ferramentas médicas de diagnóstico desde sua descoberta
Instituto de Física USP. Física V - Aula 13. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 13 Professora: Mazé Bechara Convite Amanhã, às 18h, tem um colóiquio com o título A mecânica quântica em exemplos simples, do prof. Amir Caldeira da Unicamp, pode
Instituto de Física USP Física V - Aula 13 Professora: Mazé Bechara Convite Amanhã, às 18h, tem um colóiquio com o título A mecânica quântica em exemplos simples, do prof. Amir Caldeira da Unicamp, pode
CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS
 CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS Walter Siqueira Paes DIVISÃO DE HIGIENE, SEGURANÇA E MEDICINA DO TRABALHO SETOR DE PROTEÇÃO RADIOLÓGICA PROGRAMAÇÃO
CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS Walter Siqueira Paes DIVISÃO DE HIGIENE, SEGURANÇA E MEDICINA DO TRABALHO SETOR DE PROTEÇÃO RADIOLÓGICA PROGRAMAÇÃO
ELÉTRONS EM ÁTOMOS. Depois do modelo de Rutherford: Como é o comportamento dos elétrons nos átomos? Rutherford: estrutura planetária, com o
 ELÉTRONS EM ÁTOMOS Depois do modelo de Rutherford: Como é o comportamento dos elétrons nos átomos? Rutherford: estrutura planetária, com o núcleo correspondendo ao sol no nosso sistema solar e os elétrons
ELÉTRONS EM ÁTOMOS Depois do modelo de Rutherford: Como é o comportamento dos elétrons nos átomos? Rutherford: estrutura planetária, com o núcleo correspondendo ao sol no nosso sistema solar e os elétrons
QUÍMICA I. Teoria atômica Capítulo 6. Aula 2
 QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
QUÍMICA I Teoria atômica Capítulo 6 Aula 2 Natureza ondulatória da luz A teoria atômica moderna surgiu a partir de estudos sobre a interação da radiação com a matéria. A radiação eletromagnética se movimenta
MODELOS ATÔMICOS BIK0102: ESTRUTURA DA MATÉRIA. Professor Hugo Barbosa Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace MODELOS ATÔMICOS Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Ondas (uma breve revisão...) Uma onda é uma perturbação
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace MODELOS ATÔMICOS Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Ondas (uma breve revisão...) Uma onda é uma perturbação
Biologia Estrutural. Ondas e Lei de Bragg. Prof. Dr. Walter Filgueira de Azevedo Jr. wfdaj.sites.uol.com.br Dr. Walter F. de Azevedo Jr.
 Biologia Estrutural Ondas e Lei de Bragg Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Fenômenos Ondulatórios Pulso de Ondas Ondas Onda Eletromagnética Radiação Eletromagnética Interferência Representação
Biologia Estrutural Ondas e Lei de Bragg Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Fenômenos Ondulatórios Pulso de Ondas Ondas Onda Eletromagnética Radiação Eletromagnética Interferência Representação
O ÂTOMO TIPOS DE RADIAÇÕES. TIPOS DE RADIAÇÕES As radiações podem ser classificadas da seguinte forma: Quanto à composição
 O ÂTOMO Prof. André L. C. Conceição DAFIS Curitiba, 27 de março de 2015 TIPOS DE RADIAÇÕES Radiação é energia em trânsito (emitida e transferida por um espaço). Do mesmo jeito que o calor (energia térmica
O ÂTOMO Prof. André L. C. Conceição DAFIS Curitiba, 27 de março de 2015 TIPOS DE RADIAÇÕES Radiação é energia em trânsito (emitida e transferida por um espaço). Do mesmo jeito que o calor (energia térmica
Biologia Estrutural. Espaço Recíproco e a Esfera de Ewald. Prof. Dr. Walter Filgueira de Azevedo Jr. wfdaj.sites.uol.com.br
 Biologia Estrutural Espaço Recíproco e a Esfera de Ewald Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Índices de Miller Índices de Direções Espaço Recíproco Esfera de Ewald Esfera Limite Número de
Biologia Estrutural Espaço Recíproco e a Esfera de Ewald Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Índices de Miller Índices de Direções Espaço Recíproco Esfera de Ewald Esfera Limite Número de
Estrutura da Matéria BIK Prof. Fernando Carlos Giacomelli (Turma A)
 Estrutura da Matéria BIK0102-15 Prof. Fernando Carlos Giacomelli (Turma A) fernando.giacomelli@ufabc.edu.br Bloco A - Sala 613-3 Torre 3 - CCNH - Santo André Dualidade Onda-Partícula: Descrição Clássica
Estrutura da Matéria BIK0102-15 Prof. Fernando Carlos Giacomelli (Turma A) fernando.giacomelli@ufabc.edu.br Bloco A - Sala 613-3 Torre 3 - CCNH - Santo André Dualidade Onda-Partícula: Descrição Clássica
Aula 1 Conceitos Básicos sobre Radiação. F 107 Física para Biologia 1º Semestre de 2010 Prof.Dr. Edmilson JT Manganote
 Aula 1 Conceitos Básicos sobre Radiação Introdução O que vamos discutir? Tipos e características das radiações Teoria dos quanta Dualidade onda-partícula Microscópio eletrônico A radiação é a propagação
Aula 1 Conceitos Básicos sobre Radiação Introdução O que vamos discutir? Tipos e características das radiações Teoria dos quanta Dualidade onda-partícula Microscópio eletrônico A radiação é a propagação
Física Moderna- Exercícios
 Física Moderna- Exercícios Professor Walescko 19 de dezembro de 2005 Sumário 1 Exercícios 1 2 Vestibulares UFRGS 4 3 Gabarito 10 1 Exercícios 1. Uma superfície está sendo iluminda por uma lâmpada. Nesse
Física Moderna- Exercícios Professor Walescko 19 de dezembro de 2005 Sumário 1 Exercícios 1 2 Vestibulares UFRGS 4 3 Gabarito 10 1 Exercícios 1. Uma superfície está sendo iluminda por uma lâmpada. Nesse
SEL PRINCÍPIOS FÍSICOS DE FORMAÇÃO DE IMAGENS MÉDICAS. Prof. Homero Schiabel
 SEL 397 - PRINCÍPIOS FÍSICOS DE FORMAÇÃO DE IMAGENS MÉDICAS Prof. Homero Schiabel Max Planck (1901): teoria dos quanta E depende da freqüência de radiação (ou de λ): E = h ν ν = c / λ E = h c / λ 4. PRODUÇÃO
SEL 397 - PRINCÍPIOS FÍSICOS DE FORMAÇÃO DE IMAGENS MÉDICAS Prof. Homero Schiabel Max Planck (1901): teoria dos quanta E depende da freqüência de radiação (ou de λ): E = h ν ν = c / λ E = h c / λ 4. PRODUÇÃO
FÍSICA MODERNA I AULA 06
 Universidade de São Paulo Instituto de Física FÍSICA MODERNA I AULA 06 Profa. Márcia de Almeida Rizzutto Pelletron sala 220 rizzutto@if.usp.br 1o. Semestre de 2015 Monitor: Gabriel M. de Souza Santos Página
Universidade de São Paulo Instituto de Física FÍSICA MODERNA I AULA 06 Profa. Márcia de Almeida Rizzutto Pelletron sala 220 rizzutto@if.usp.br 1o. Semestre de 2015 Monitor: Gabriel M. de Souza Santos Página
Raios-x. Proteção e higiene das Radiações Profª: Marina de Carvalho CETEA
 Raios-x Proteção e higiene das Radiações Profª: Marina de Carvalho CETEA Materiais Radioativos 1896 o físico Francês Becquerel descobriu que sais de Urânio emitia radiação capaz de produzir sombras de
Raios-x Proteção e higiene das Radiações Profª: Marina de Carvalho CETEA Materiais Radioativos 1896 o físico Francês Becquerel descobriu que sais de Urânio emitia radiação capaz de produzir sombras de
Modelos atômicos (quânticos) Bohr Sommerfeld Professor: Hugo Cesário
 Modelos atômicos (quânticos) Bohr Sommerfeld Professor: Hugo Cesário Rutherford Niels Bohr Max Planck Sommerfeld Modelos atômicos quânticos Problemas de Rutherford: Modelo entrou em choque com os conceitos
Modelos atômicos (quânticos) Bohr Sommerfeld Professor: Hugo Cesário Rutherford Niels Bohr Max Planck Sommerfeld Modelos atômicos quânticos Problemas de Rutherford: Modelo entrou em choque com os conceitos
Dosimetria e Proteção Radiológica
 Dosimetria e Proteção Radiológica Prof. Dr. André L. C. Conceição Departamento Acadêmico de Física (DAFIS) Programa de Pós-Graduação em Engenharia Elétrica e Informática Industrial (CPGEI) Universidade
Dosimetria e Proteção Radiológica Prof. Dr. André L. C. Conceição Departamento Acadêmico de Física (DAFIS) Programa de Pós-Graduação em Engenharia Elétrica e Informática Industrial (CPGEI) Universidade
Prof. Dr. Lucas Barboza Sarno da Silva
 Prof. Dr. Lucas Barboza Sarno da Silva O Efeito Compton Einstein, em 1919, concluiu que um fóton de energia E se desloca em uma única direção (diferentemente de uma onda esférica) e é portador de um momento
Prof. Dr. Lucas Barboza Sarno da Silva O Efeito Compton Einstein, em 1919, concluiu que um fóton de energia E se desloca em uma única direção (diferentemente de uma onda esférica) e é portador de um momento
Estrutura eletrônica da matéria - resumo
 Estrutura eletrônica da matéria - resumo A NATUREZA ONDULATÓRIA DA LUZ COMO A RADIAÇÃO ELETROMAGNÉTICA SE MOVE À VELOCIDADE DA LUZ, O COMPRIMENTO DE ONDA E A FREQUÊNCIA ESTÃO RELACIONADOS: νλ=c ONDE ν(ni)
Estrutura eletrônica da matéria - resumo A NATUREZA ONDULATÓRIA DA LUZ COMO A RADIAÇÃO ELETROMAGNÉTICA SE MOVE À VELOCIDADE DA LUZ, O COMPRIMENTO DE ONDA E A FREQUÊNCIA ESTÃO RELACIONADOS: νλ=c ONDE ν(ni)
Análise de alimentos II Introdução aos Métodos Espectrométricos
 Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
Análise de alimentos II Introdução aos Métodos Espectrométricos Profª Drª Rosemary Aparecida de Carvalho Pirassununga/SP 2018 Introdução Métodos espectrométricos Abrangem um grupo de métodos analíticos
Energia certa significa: quando a energia do fóton corresponde à diferença nos níveis de energia entre as duas órbitas permitidas do átomo de H.
 ESPECTROSCOPIA II A relação da luz com as linhas espectrais O que acontece se átomos de H forem bombardeados por fótons? R. Existem três possibilidades: 1) a maioria dos fótons passa sem nenhuma interação
ESPECTROSCOPIA II A relação da luz com as linhas espectrais O que acontece se átomos de H forem bombardeados por fótons? R. Existem três possibilidades: 1) a maioria dos fótons passa sem nenhuma interação
O Efeito Fotoelétrico
 O Efeito Fotoelétrico O efeito fotoelétrico é a emissão de elétrons por um material, geralmente metálico, quando exposto a uma radiação eletromagnética (como a luz) suficientemente energética, ou seja,
O Efeito Fotoelétrico O efeito fotoelétrico é a emissão de elétrons por um material, geralmente metálico, quando exposto a uma radiação eletromagnética (como a luz) suficientemente energética, ou seja,
Aula 7 INTERAÇÃO DA RADIAÇÃO COM A MATÉRIA
 INTERAÇÃO DA RADIAÇÃO COM A MATÉRIA Aula 7 META Neta aula o aluno aprenderá os mecanismos envolvidos quando a radiação eletromagnética ou corpuscular interage com a matéria. Os conceitos contidos nesta
INTERAÇÃO DA RADIAÇÃO COM A MATÉRIA Aula 7 META Neta aula o aluno aprenderá os mecanismos envolvidos quando a radiação eletromagnética ou corpuscular interage com a matéria. Os conceitos contidos nesta
Distribuição da radiação* ESPECTRO
 ESPECTROSCOPIA intensidade INFORMAÇÃO Distribuição da radiação* ESPECTRO Através do espectro de um objeto astronômico pode-se conhecer informações sobre temperatura, pressão, densidade, composição química,
ESPECTROSCOPIA intensidade INFORMAÇÃO Distribuição da radiação* ESPECTRO Através do espectro de um objeto astronômico pode-se conhecer informações sobre temperatura, pressão, densidade, composição química,
Introdução à Astrofísica. Espectroscopia. Rogemar A. Riffel
 Introdução à Astrofísica Espectroscopia Rogemar A. Riffel Radiação de Corpo Negro Corpo negro: corpo que absorve toda a radiação que incide sobre ele, sem refletir nada; - Toda a radiação emitida pelo
Introdução à Astrofísica Espectroscopia Rogemar A. Riffel Radiação de Corpo Negro Corpo negro: corpo que absorve toda a radiação que incide sobre ele, sem refletir nada; - Toda a radiação emitida pelo
01. (ITA ) A tabela abaixo mostra os níveis de energia de um átomo do elemento X que se encontra no estado gasoso.
 01. (ITA - 1999) A tabela abaixo mostra os níveis de energia de um átomo do elemento X que se encontra no estado gasoso. E 0 0 E 1 7,0 ev E 2 13,0 ev E 3 17,4 ev Ionização 21,4 ev Dentro das possibilidades
01. (ITA - 1999) A tabela abaixo mostra os níveis de energia de um átomo do elemento X que se encontra no estado gasoso. E 0 0 E 1 7,0 ev E 2 13,0 ev E 3 17,4 ev Ionização 21,4 ev Dentro das possibilidades
O átomo de Rutherford
 O átomo de Rutherford ~10-14 m Núcleo de carga +Ze rodeado por Z elétrons (modelo planetário). Z é chamado número atômico (H: Z = 1, He: Z = 2, etc.). O número atômico determina as propriedades físicas
O átomo de Rutherford ~10-14 m Núcleo de carga +Ze rodeado por Z elétrons (modelo planetário). Z é chamado número atômico (H: Z = 1, He: Z = 2, etc.). O número atômico determina as propriedades físicas
4º bimestre - Volume 3, Capítulo 19
 Página 1 de 7 4º bimestre - Volume 3, Capítulo 19 Testes propostos 4º bimestre 1 (Uneb-BA) De acordo com o físico Max Planck, que introduziu o conceito de energia quantizada, a luz, elemento imprescindível
Página 1 de 7 4º bimestre - Volume 3, Capítulo 19 Testes propostos 4º bimestre 1 (Uneb-BA) De acordo com o físico Max Planck, que introduziu o conceito de energia quantizada, a luz, elemento imprescindível
Luz & Radiação. Roberto Ortiz EACH USP
 Luz & Radiação Roberto Ortiz EACH USP A luz é uma onda eletromagnética A figura acima ilustra os campos elétrico (E) e magnético (B) que compõem a luz Eles são perpendiculares entre si e perpendiculares
Luz & Radiação Roberto Ortiz EACH USP A luz é uma onda eletromagnética A figura acima ilustra os campos elétrico (E) e magnético (B) que compõem a luz Eles são perpendiculares entre si e perpendiculares
Fundamentos de Física Capítulo 39 Mais Ondas de Matéria Questões Múltipla escolha cap. 39 Fundamentos de Física Halliday Resnick Walker 1) Qual das
 Fundamentos de Física Capítulo 39 Mais Ondas de Matéria Questões Múltipla escolha cap. 39 Fundamentos de Física Halliday Resnick Walker 1) Qual das frases abaixo descreve corretamente a menor energia possível
Fundamentos de Física Capítulo 39 Mais Ondas de Matéria Questões Múltipla escolha cap. 39 Fundamentos de Física Halliday Resnick Walker 1) Qual das frases abaixo descreve corretamente a menor energia possível
Lista de Exercícios - Física Quântica - UNIDADE 1
 Lista de Exercícios - Física Quântica - UNIDADE 1 Problemas e questões baseados no D. Halliday, R. Resnick e J. Walker, Fundamentos de Física, 6ª ed. - Capítulos 39, 40 e 41. Questões 1. Como pode a energia
Lista de Exercícios - Física Quântica - UNIDADE 1 Problemas e questões baseados no D. Halliday, R. Resnick e J. Walker, Fundamentos de Física, 6ª ed. - Capítulos 39, 40 e 41. Questões 1. Como pode a energia
Biofísica Bacharelado em Biologia
 Biofísica Bacharelado em Biologia Prof. Dr. Sergio Pilling PARTE B Capítulo 6 Conceitos basicos sobre radiação. Modelos atómico e niveis de energia. Radiaoatividade. Objetivos: Nesta aula veremos alguns
Biofísica Bacharelado em Biologia Prof. Dr. Sergio Pilling PARTE B Capítulo 6 Conceitos basicos sobre radiação. Modelos atómico e niveis de energia. Radiaoatividade. Objetivos: Nesta aula veremos alguns
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. QUÍMICA estudo
Biologia Estrutural. Cálculo dos Fatores de Estrutura. Prof. Dr. Walter Filgueira de Azevedo Jr. wfdaj.sites.uol.com.br
 Biologia Estrutural Cálculo dos Fatores de Estrutura Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Extinção Sistemática para Cela Unitária de Face Centrada (F) Fator de Estrutura na Forma Complexa Cálculo
Biologia Estrutural Cálculo dos Fatores de Estrutura Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Extinção Sistemática para Cela Unitária de Face Centrada (F) Fator de Estrutura na Forma Complexa Cálculo
CLIMATOLOGIA. Radiação solar. Professor: D. Sc. João Paulo Bestete de Oliveira
 CLIMATOLOGIA Radiação solar Professor: D. Sc. João Paulo Bestete de Oliveira Sistema Solar Componente Massa (%) Sol 99,85 Júpiter 0,10 Demais planetas 0,04 Sol x Terra massa 332.900 vezes maior volume
CLIMATOLOGIA Radiação solar Professor: D. Sc. João Paulo Bestete de Oliveira Sistema Solar Componente Massa (%) Sol 99,85 Júpiter 0,10 Demais planetas 0,04 Sol x Terra massa 332.900 vezes maior volume
SUGESTÕES DE EXERCÍCIOS PARA A SEGUNDA AVALIAÇÃO
 FÍSICA IV PROF. DR. DURVAL RODRIGUES JUNIOR SUGESTÕES DE EXERCÍCIOS PARA A SEGUNDA AVALIAÇÃO Como na Biblioteca do Campus I e do Campus II temos bom número de cópias do Halliday e poucas do Serway, os
FÍSICA IV PROF. DR. DURVAL RODRIGUES JUNIOR SUGESTÕES DE EXERCÍCIOS PARA A SEGUNDA AVALIAÇÃO Como na Biblioteca do Campus I e do Campus II temos bom número de cópias do Halliday e poucas do Serway, os
CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS
 CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS COORDENADORIA DE ADMINISTRAÇÃO GERAL DIVISÃO DE SAÚDE OCUPACIONAL SEÇÃO TÉCNICA DE PROTEÇÃO RADIOLÓGICA PROGRAMAÇÃO
CURSO DE RADIOPROTEÇÃO COM ÊNFASE NO USO, PREPARO E MANUSEIO DE FONTES RADIOATIVAS NÃO SELADAS COORDENADORIA DE ADMINISTRAÇÃO GERAL DIVISÃO DE SAÚDE OCUPACIONAL SEÇÃO TÉCNICA DE PROTEÇÃO RADIOLÓGICA PROGRAMAÇÃO
Radiações e Radioatividade
 Radiações e Radioatividade 2015 Dr. Walter F. de Azevedo Jr. Objetivos Visualizar o espectro de emissão do hidrogênio. Estudar o decaimento radioativo e a datação por carbono 14. Materiais 1. Computador
Radiações e Radioatividade 2015 Dr. Walter F. de Azevedo Jr. Objetivos Visualizar o espectro de emissão do hidrogênio. Estudar o decaimento radioativo e a datação por carbono 14. Materiais 1. Computador
interação feixe de elétrons-amostra [3] Propriedades do elétron:
![interação feixe de elétrons-amostra [3] Propriedades do elétron: interação feixe de elétrons-amostra [3] Propriedades do elétron:](/thumbs/70/63114313.jpg) [3] Propriedades do elétron: 1> Comprimento de onda do feixe de elétrons (λ): V [kv] λ [pm] 1 38,7 5 17,3 10 12,2 15 9,9 20 8,6 25 30 120 200 7,6 6,9 3,3 2,5 λ = λ = 2 e V m 1,5 h e 2 + ( ) 6 2 V + 10
[3] Propriedades do elétron: 1> Comprimento de onda do feixe de elétrons (λ): V [kv] λ [pm] 1 38,7 5 17,3 10 12,2 15 9,9 20 8,6 25 30 120 200 7,6 6,9 3,3 2,5 λ = λ = 2 e V m 1,5 h e 2 + ( ) 6 2 V + 10
Agronomia Química Analítica Prof. Dr. Gustavo Rocha de Castro. As medidas baseadas na luz (radiação eletromagnética) são muito empregadas
 ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
ESPECTROMETRIA DE ABSORÇÃO ATÔMICA Introdução As medidas baseadas na luz (radiação eletromagnética) são muito empregadas na química analítica. Estes métodos são baseados na quantidade de radiação emitida
EFEITO FOTOELÉTRICO. Propriedade corpuscular da radiação eletromagnética Reforço à teoria quântica de Planck (quanta de energia)
 EFEITO FOTOELÉTRICO Elétrons são emitidos da matéria após absorverem a energia de uma radiação eletromagnética (de baixos comprimentos de onda visível ou UV) que incida sobre ela. Descoberto acidentalmente
EFEITO FOTOELÉTRICO Elétrons são emitidos da matéria após absorverem a energia de uma radiação eletromagnética (de baixos comprimentos de onda visível ou UV) que incida sobre ela. Descoberto acidentalmente
AULA 01 TEORIA ATÔMICA COMPLETA
 AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
AULA 01 TEORIA ATÔMICA COMPLETA - ESTRUTURA ATÔMICA; - MODELOS ATÔMICOS; - ESPECTROSCOPIA ATÔMICA; - PROPRIEDADES ONDULATÓRIAS DOS ELÉTRONS; - NÚMEROS QUÂNTICOS E DISTRIBUIÇÃO ELETRÔNICA. Estrutura Eletrônica
Física Moderna I Aula 05. Marcelo G Munhoz Edifício HEPIC, sala 212, ramal
 Física Moderna I Aula 05 Marcelo G Munhoz Edifício HEPIC, sala 212, ramal 916940 munhoz@if.usp.br 1 Röntgen descobre os raios-x (1895) Röntgen trabalhava com tubos de raios catódicos Durante seus estudos
Física Moderna I Aula 05 Marcelo G Munhoz Edifício HEPIC, sala 212, ramal 916940 munhoz@if.usp.br 1 Röntgen descobre os raios-x (1895) Röntgen trabalhava com tubos de raios catódicos Durante seus estudos
5. Modelo atômico de Bohr
 5. Modelo atômico de Bohr Sumário Espectros atômicos Modelo de Bohr para o átomo de hidrogênio Níveis de energia e raias espectrais Experiência de Franck-Hertz O princípio da correspondência Correção do
5. Modelo atômico de Bohr Sumário Espectros atômicos Modelo de Bohr para o átomo de hidrogênio Níveis de energia e raias espectrais Experiência de Franck-Hertz O princípio da correspondência Correção do
MODELOS ATÔMICOS BIK0102: ESTRUTURA DA MATÉRIA. Professor Hugo Barbosa Suffredini Site:
 BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace MODELOS ATÔMICOS Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Ondas (uma breve revisão...) Uma onda é uma perturbação
BIK0102: ESTRUTURA DA MATÉRIA Crédito: Sprace MODELOS ATÔMICOS Professor Hugo Barbosa Suffredini hugo.suffredini@ufabc.edu.br Site: www.suffredini.com.br Ondas (uma breve revisão...) Uma onda é uma perturbação
FÍSICA IV PROF. PIERRE VILAR DANTAS AULA 11-04/11/2017 TURMA: A HORÁRIO: 7M PIERREDANTASBLOG.WORDPRESS.COM
 FÍSICA IV PROF. PIERRE VILAR DANTAS AULA 11-04/11/2017 TURMA: 0053- A HORÁRIO: 7M PIERREDANTASBLOG.WORDPRESS.COM 1 Introdução à Física Moderna 2 Objetivos do Aprendizado Explicar a absorção e emissão da
FÍSICA IV PROF. PIERRE VILAR DANTAS AULA 11-04/11/2017 TURMA: 0053- A HORÁRIO: 7M PIERREDANTASBLOG.WORDPRESS.COM 1 Introdução à Física Moderna 2 Objetivos do Aprendizado Explicar a absorção e emissão da
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 4 MODELOS ATÔMICOS Primeira Edição junho de 2005 CAPÍTULO 4 MODELOS ATÔMICOS ÍNDICE 4.1- Modelo de Thomson 4.2- Modelo de Rutherford 4.2.1-
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 4 MODELOS ATÔMICOS Primeira Edição junho de 2005 CAPÍTULO 4 MODELOS ATÔMICOS ÍNDICE 4.1- Modelo de Thomson 4.2- Modelo de Rutherford 4.2.1-
AS RADIAÇÕES NUCLEARES 4 AULA
 AS RADIAÇÕES NUCLEARES 4 AULA Nesta Aula: Caracterização das radiações Nucleares Caracterização das radiações Nucleares UM POUCO DE HISTÓRIA... O físico francês Henri Becquerel (1852-1908), em 1896, acidentalmente
AS RADIAÇÕES NUCLEARES 4 AULA Nesta Aula: Caracterização das radiações Nucleares Caracterização das radiações Nucleares UM POUCO DE HISTÓRIA... O físico francês Henri Becquerel (1852-1908), em 1896, acidentalmente
Universidade Federal do Rio de Janeiro Instituto de Física Física IV 2019/1 Lista de Exercícios do Capítulo 5 Origens da Teoria Quântica
 Universidade Federal do Rio de Janeiro Instituto de Física Física IV 2019/1 Lista de Exercícios do Capítulo 5 Origens da Teoria Quântica 1) Calcule a energia de um quantum de luz de comprimento de onda
Universidade Federal do Rio de Janeiro Instituto de Física Física IV 2019/1 Lista de Exercícios do Capítulo 5 Origens da Teoria Quântica 1) Calcule a energia de um quantum de luz de comprimento de onda
Física Nuclear: Radioatividade
 Física Nuclear: Radioatividade Descoberta da Radioatividade Becquerel, estudando fenômenos de fluorescência e raios-x Observava fluorescência no Urânio quando exposto ao Sol. Becquerel protegia uma chapa
Física Nuclear: Radioatividade Descoberta da Radioatividade Becquerel, estudando fenômenos de fluorescência e raios-x Observava fluorescência no Urânio quando exposto ao Sol. Becquerel protegia uma chapa
Física Nuclear: Radioatividade
 Física Nuclear: Radioatividade Descoberta da Radioatividade Becquerel, estudando fenômenos de fluorescência e raios-x Observava fluorescência no Urânio quando exposto ao Sol. Becquerel protegia uma chapa
Física Nuclear: Radioatividade Descoberta da Radioatividade Becquerel, estudando fenômenos de fluorescência e raios-x Observava fluorescência no Urânio quando exposto ao Sol. Becquerel protegia uma chapa
Capítulo 2: Postulados de Bohr
 Material laborado por Caio Guimarães Física Moderna: Análise da Aplicação da Teoria nos xercícios do ITA Capítulo : Postulados de Bor Rydberg e Balmer No final dos século XIX, início do século XX a física
Material laborado por Caio Guimarães Física Moderna: Análise da Aplicação da Teoria nos xercícios do ITA Capítulo : Postulados de Bor Rydberg e Balmer No final dos século XIX, início do século XX a física
Aula 15 Mais sobre Ondas de Matéria
 Aula 15 Mais sobre Ondas de Matéria Física 4 Ref. Halliday Volume4 Sumário...relembrando... Relembrando... Elétrons e Ondas de Matéria Em 1924, Louis de Broglie propôs um novo raciocínio: Se um feixe luminoso
Aula 15 Mais sobre Ondas de Matéria Física 4 Ref. Halliday Volume4 Sumário...relembrando... Relembrando... Elétrons e Ondas de Matéria Em 1924, Louis de Broglie propôs um novo raciocínio: Se um feixe luminoso
Instituto de Física USP. Física V - Aula 11. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 11 Professora: Mazé Bechara AVISOS 1. A aula de 21/3, quinta-feira será uma aula de aplicações. Excepcionalmente não haverá a sessão monitoria às 13h. 2. Na página
Instituto de Física USP Física V - Aula 11 Professora: Mazé Bechara AVISOS 1. A aula de 21/3, quinta-feira será uma aula de aplicações. Excepcionalmente não haverá a sessão monitoria às 13h. 2. Na página
Instituto de Física USP. Física V - Aula 15. Professora: Mazé Bechara
 Instituto de Física USP Física V - Aula 15 Professora: Mazé Bechara Aula 15 Espectros de absorção e emissão atômica e modelo atômico de Thomson. 1. Evidências experimentais da existência de estrutura nos
Instituto de Física USP Física V - Aula 15 Professora: Mazé Bechara Aula 15 Espectros de absorção e emissão atômica e modelo atômico de Thomson. 1. Evidências experimentais da existência de estrutura nos
AULA 21 INTRODUÇÃO À RADIAÇÃO TÉRMICA
 Notas de aula de PME 3361 Processos de Transferência de Calor 180 AULA 1 INTRODUÇÃO À RADIAÇÃO TÉRMICA A radiação térmica é a terceira e última forma de transferência de calor existente. Das três formas,
Notas de aula de PME 3361 Processos de Transferência de Calor 180 AULA 1 INTRODUÇÃO À RADIAÇÃO TÉRMICA A radiação térmica é a terceira e última forma de transferência de calor existente. Das três formas,
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA Edição de junho de 2014 CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA ÍNDICE 3.1-
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA Edição de junho de 2014 CAPÍTULO 3 MODELOS ATÔMICOS E A VELHA TEORIA QUÂNTICA ÍNDICE 3.1-
A radiação do corpo negro
 A radiação do corpo negro Um corpo em qualquer temperatura emite radiações eletromagnéticas. Por estarem relacionadas com a temperatura em que o corpo se encontra, freqüentemente são chamadas radiações
A radiação do corpo negro Um corpo em qualquer temperatura emite radiações eletromagnéticas. Por estarem relacionadas com a temperatura em que o corpo se encontra, freqüentemente são chamadas radiações
UFABC - Física Quântica - Curso Prof. Germán Lugones. Aula 4. O modelo atômico de Bohr
 UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 4 O modelo atômico de Bohr 1 O modelo de Bohr Em 1913, Niels Bohr propôs um modelo do átomo de hidrogênio que combinava o trabalho de Planck,
UFABC - Física Quântica - Curso 2017.3 Prof. Germán Lugones Aula 4 O modelo atômico de Bohr 1 O modelo de Bohr Em 1913, Niels Bohr propôs um modelo do átomo de hidrogênio que combinava o trabalho de Planck,
2. A ORIGEM DA CONSTANTE DE NEGRO
 QUANTIZAÇÃO . INTRODUÇÃO O No final do século XIX acreditava-se, em geral, que todos os fenômenos naturais poderiam ser descritos mediante: Leis de Newton, Leis da Termodinâmica, e Leis do Eletromagnetismo.
QUANTIZAÇÃO . INTRODUÇÃO O No final do século XIX acreditava-se, em geral, que todos os fenômenos naturais poderiam ser descritos mediante: Leis de Newton, Leis da Termodinâmica, e Leis do Eletromagnetismo.
Max Planck Pai da Física Quantica
 A Mecânica Quântica é a parte da física que estuda o movimento dos corpos microscópicos em altas velocidades. As principais conclusões da Física Quântica são que, em estados ligados, a energia não se troca
A Mecânica Quântica é a parte da física que estuda o movimento dos corpos microscópicos em altas velocidades. As principais conclusões da Física Quântica são que, em estados ligados, a energia não se troca
Professor Edson Cruz
 Professor Edson Cruz A RADIOATIVIDADE E A NECESSIDADE DE NOVAS PESQUISAS Wilhelm RÖNTGEN (1845-1923) Estudava raios emitidos pela ampola de Crookes. Repentinamente, notou que raios desconhecidos saíam
Professor Edson Cruz A RADIOATIVIDADE E A NECESSIDADE DE NOVAS PESQUISAS Wilhelm RÖNTGEN (1845-1923) Estudava raios emitidos pela ampola de Crookes. Repentinamente, notou que raios desconhecidos saíam
O espectro eletromagnético
 Difração de Raios X O espectro eletromagnético luz visível raios-x microondas raios gama UV infravermelho ondas de rádio Comprimento de onda (nm) Raios Absorção, um fóton de energia é absorvido promovendo
Difração de Raios X O espectro eletromagnético luz visível raios-x microondas raios gama UV infravermelho ondas de rádio Comprimento de onda (nm) Raios Absorção, um fóton de energia é absorvido promovendo
Capítulo 38 Fótons e Ondas de Matéria Questões Múltipla escolha cap. 38 Fundamentos de Física Halliday Resnick Walker
 Capítulo 38 Fótons e Ondas de Matéria Questões Múltipla escolha cap. 38 Fundamentos de Física Halliday Resnick Walker 1) Qual é o nome das partículas associadas ao campo eletromagnético? a) Fônons. b)
Capítulo 38 Fótons e Ondas de Matéria Questões Múltipla escolha cap. 38 Fundamentos de Física Halliday Resnick Walker 1) Qual é o nome das partículas associadas ao campo eletromagnético? a) Fônons. b)
Universidade Federal do Paraná Departamento de Física Laboratório de Física Moderna
 Universidade Federal do Paraná Departamento de Física Laboratório de Física Moderna Bloco 0: AS LINHAS DE BALMER Introdução A teoria quântica prevê uma estrutura de níveis de energia quantizados para os
Universidade Federal do Paraná Departamento de Física Laboratório de Física Moderna Bloco 0: AS LINHAS DE BALMER Introdução A teoria quântica prevê uma estrutura de níveis de energia quantizados para os
Física Aplicada Aula 13
 Universidade de São Paulo Instituto de Física Física Aplicada Aula 13 Profa. Márcia de Almeida Rizzutto Edifício Oscar Sala sala 220 rizzutto@if.usp.br http://disciplinas.stoa.usp.br/course/view.php?id=24279
Universidade de São Paulo Instituto de Física Física Aplicada Aula 13 Profa. Márcia de Almeida Rizzutto Edifício Oscar Sala sala 220 rizzutto@if.usp.br http://disciplinas.stoa.usp.br/course/view.php?id=24279
Sumário. O átomo de H e a estrutura atómica
 Sumário Das Estrelas ao átomo Unidade temática 1 O átomo de hidrogénio e a estrutura atómica. Quantização de energia. APSA 6 Espectro atómico do átomo de hidrogénio. Porque é que o espectro do átomo de
Sumário Das Estrelas ao átomo Unidade temática 1 O átomo de hidrogénio e a estrutura atómica. Quantização de energia. APSA 6 Espectro atómico do átomo de hidrogénio. Porque é que o espectro do átomo de
Introdução às interações de partículas carregadas Parte 1. FÍSICA DAS RADIAÇÕES I Paulo R. Costa
 Introdução às interações de partículas carregadas Parte 1 FÍSICA DAS RADIAÇÕES I Paulo R. Costa Sumário Introdução Radiação diretamente ionizante Partículas carregadas rápidas pesadas Partículas carregadas
Introdução às interações de partículas carregadas Parte 1 FÍSICA DAS RADIAÇÕES I Paulo R. Costa Sumário Introdução Radiação diretamente ionizante Partículas carregadas rápidas pesadas Partículas carregadas
Noções básicas de quântica. Prof. Ms. Vanderlei Inácio de Paula
 Noções básicas de quântica Prof. Ms. Vanderlei Inácio de Paula Noções de quântica O professor recomenda: Estude pelos seguintes livros/páginas sobre a Ligações químicas e faça os exercícios! Shriver Ed
Noções básicas de quântica Prof. Ms. Vanderlei Inácio de Paula Noções de quântica O professor recomenda: Estude pelos seguintes livros/páginas sobre a Ligações químicas e faça os exercícios! Shriver Ed
Física Moderna. A quantização da energia. Dualidade onda-partícula. O efeito fotoelétrico.
 Física Moderna A quantização da energia. Dualidade onda-partícula. O efeito fotoelétrico. Efeito fotoelétrico Quando uma radiação eletromagnética incide sobre a superfície de um metal, elétrons podem ser
Física Moderna A quantização da energia. Dualidade onda-partícula. O efeito fotoelétrico. Efeito fotoelétrico Quando uma radiação eletromagnética incide sobre a superfície de um metal, elétrons podem ser
NOTAS DE AULAS DE FÍSICA MODERNA
 NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO Primeira Edição junho de 2005 CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO ÍNDICE 3.1- Efeito
NOTAS DE AULAS DE FÍSICA MODERNA Prof. Carlos R. A. Lima CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO Primeira Edição junho de 2005 CAPÍTULO 3 PROPRIEDADES CORPUSCULARES DA RADIAÇÃO ÍNDICE 3.1- Efeito
2015 Dr. Walter F. de Azevedo Jr.
 015 Dr. Walter F. de Azevedo Jr. 000000000000000000000000000000000000000 000000000000000000000000000000000000000 000000000000111111111110001100000000000 000000000001111111111111111111000000001 000000000111111111111111111111111000000
015 Dr. Walter F. de Azevedo Jr. 000000000000000000000000000000000000000 000000000000000000000000000000000000000 000000000000111111111110001100000000000 000000000001111111111111111111000000001 000000000111111111111111111111111000000
Biofísica Espectrofotometria Prof. Dr. Walter F. de Azevedo Jr.
 Biofísica Espectrofotometria Prof. Dr. Walter F. de Azevedo Jr. 1 2018 Dr. Walter F. de Azevedo Espectro de Emissão de Luz No experimento abaixo temos o gás hidrogênio introduzido num tubo de vidro. No
Biofísica Espectrofotometria Prof. Dr. Walter F. de Azevedo Jr. 1 2018 Dr. Walter F. de Azevedo Espectro de Emissão de Luz No experimento abaixo temos o gás hidrogênio introduzido num tubo de vidro. No
Biologia Estrutural. Cálculo da Densidade Eletrônica. Prof. Dr. Walter Filgueira de Azevedo Jr. wfdaj.sites.uol.com.br
 Biologia Estrutural Cálculo da Densidade Eletrônica Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Introdução Cálculo da densidade eletrônica Densidade eletrônica de um cristal unidimensional Densidade
Biologia Estrutural Cálculo da Densidade Eletrônica Prof. Dr. Walter Filgueira de Azevedo Jr. Resumo Introdução Cálculo da densidade eletrônica Densidade eletrônica de um cristal unidimensional Densidade
Principais Postulados de Dalton (1803)
 Teoria Atômica da Matéria Breve Histórico Leucipo e Demócrito ( 400 a.c.) descontinuidade da matéria (átomo). Alquimia ( 300 a.c. 1500 d.c.) civilizações árabes e gregas. Paracelsus ( 1500 d.c.) Iatroquímica.
Teoria Atômica da Matéria Breve Histórico Leucipo e Demócrito ( 400 a.c.) descontinuidade da matéria (átomo). Alquimia ( 300 a.c. 1500 d.c.) civilizações árabes e gregas. Paracelsus ( 1500 d.c.) Iatroquímica.
Sumário. Espectros, Radiação e Energia
 Sumário Das Estrelas ao átomo Unidade temática 1 Radiação ionizante e radiação não ionizante.. E suas aplicações. APSA 5 Espectro eletromagnético.. Radiação não ionizante São radiações não ionizantes as
Sumário Das Estrelas ao átomo Unidade temática 1 Radiação ionizante e radiação não ionizante.. E suas aplicações. APSA 5 Espectro eletromagnético.. Radiação não ionizante São radiações não ionizantes as
Radiação electromagnetica
 Radiação electromagnetica A radiação eletromagnética é uma forma de energia absorvida e emitida por partículas com carga elétrica quando aceleradas por forças. Ao nível subatómico, a radiação eletromagnética
Radiação electromagnetica A radiação eletromagnética é uma forma de energia absorvida e emitida por partículas com carga elétrica quando aceleradas por forças. Ao nível subatómico, a radiação eletromagnética
Física VIII Ondas eletromagnéticas e Física Moderna
 Física VIII Ondas eletromagnéticas e Física Moderna Aula 5: Difração Parte II 1 Baseado no material preparado por Sandro Fonseca de Souza Helena Malbouisson Redes de difração Grande número de fendas (ranhuras)
Física VIII Ondas eletromagnéticas e Física Moderna Aula 5: Difração Parte II 1 Baseado no material preparado por Sandro Fonseca de Souza Helena Malbouisson Redes de difração Grande número de fendas (ranhuras)
FÍSICA IV PROF. PIERRE VILAR DANTAS AULA 10-28/10/2017 TURMA: A HORÁRIO: 7M PIERREDANTASBLOG.WORDPRESS.COM
 FÍSICA IV PROF. PIERRE VILAR DANTAS AULA 10-28/10/2017 TURMA: 0053- A HORÁRIO: 7M PIERREDANTASBLOG.WORDPRESS.COM 1 Introdução à Física Moderna 2 Objetivos do Aprendizado Explicar a absorção e emissão da
FÍSICA IV PROF. PIERRE VILAR DANTAS AULA 10-28/10/2017 TURMA: 0053- A HORÁRIO: 7M PIERREDANTASBLOG.WORDPRESS.COM 1 Introdução à Física Moderna 2 Objetivos do Aprendizado Explicar a absorção e emissão da
Prof. Dr. Lucas Barboza Sarno da Silva
 Prof. Dr. Lucas Barboza Sarno da Silva A radiação do corpo negro e as hipóteses de Planck Um corpo, em qualquer temperatura emite radiação, algumas vezes denominada radiação térmica. O estudo minucioso
Prof. Dr. Lucas Barboza Sarno da Silva A radiação do corpo negro e as hipóteses de Planck Um corpo, em qualquer temperatura emite radiação, algumas vezes denominada radiação térmica. O estudo minucioso
1. (Fuvest-SP) Resolução
 1. (Fuvest-SP) Na estratosfera, há um ciclo constante de criação e destruição do ozônio. A equação que representa a destruição do ozônio pela ação da luz ultravioleta solar (UV) é O gráfico representa
1. (Fuvest-SP) Na estratosfera, há um ciclo constante de criação e destruição do ozônio. A equação que representa a destruição do ozônio pela ação da luz ultravioleta solar (UV) é O gráfico representa
Disciplina: NMA-103. Prof. Dr. Jose Antonio Souza
 Disciplina: NMA-103 Prof. Dr. Jose Antonio Souza 02/2015 Física Clássica Tudo resolvido no final do século XIX Maxwell (1865) Formulação elegante e concisa Fundamentos da Eletricidade e Magnetismo Matematização
Disciplina: NMA-103 Prof. Dr. Jose Antonio Souza 02/2015 Física Clássica Tudo resolvido no final do século XIX Maxwell (1865) Formulação elegante e concisa Fundamentos da Eletricidade e Magnetismo Matematização
A experiência das Linhas de Balmer
 A experiência das Linhas de Balmer 1 Introdução Conforme vemos nos cursos que tratam sobre física quântica, podemos excitar elétrons presos aos seus núcleos atômicos apenas quando utilizamos energias corretas,
A experiência das Linhas de Balmer 1 Introdução Conforme vemos nos cursos que tratam sobre física quântica, podemos excitar elétrons presos aos seus núcleos atômicos apenas quando utilizamos energias corretas,
