ESTUDO EPIDEMIOLÓGICO DA LEISHMANIOSE NO MUNICÍPIO DE PIRENÓPOLIS GOIÁS BRASIL, NOS ANOS DE 2005 a 2010
|
|
|
- João Vítor Valente Balsemão
- 7 Há anos
- Visualizações:
Transcrição
1 UNIVERSIDADE ESTADUAL DE GOIÁS UNIDADE UNIVERSITÁRIA DE CIÊNCIAS EXATAS E TECNOLÓGICAS CURSO DE FARMÁCIA FERNANDA FELICIANO DA SILVA RENATA DE LIMA CASTRO ESTUDO EPIDEMIOLÓGICO DA LEISHMANIOSE NO MUNICÍPIO DE PIRENÓPOLIS GOIÁS BRASIL, NOS ANOS DE 2005 a 2010 Anápolis, Junho/2011.
2 FERNANDA FELICIANO DA SILVA RENATA DE LIMA CASTRO ESTUDO EPIDEMIOLÓGICO DA LEISHMANIOSE NO MUNICÍPIO DE PIRENÓPOLIS GOIÁS BRASIL, NOS ANOS DE 2005 a 2010 Trabalho de Conclusão de Curso apresentado ao Curso de Farmácia da Universidade Estadual de Goiás como exigência parcial à obtenção do título de Bacharel em Farmácia. Orientador: Prof. MSc. Ricardo Carvalho Silva Co-orietador: Profº. MSc. Marc Gigonzac Anápolis, Junho/2011.
3
4 Dedicamos este trabalho a Deus, nosso Senhor, Pai bondoso, que até aqui nos abençoou, cuidou e nos amou.
5 AGRADECIMENTOS Fernanda Feliciano da Silva Agradeço primeiramente a Deus, por as bênçãos derramadas em minha vida, em especial por mais essa conquista, que só foi possível, porque o Senhor permitiu. Agradeço aos meus amados pais, João e Josefa, por todo amor, carinho e dedicação, pelo esforço, pela educação e pela pessoa que hoje sou. Obrigada, eu amo vocês! Agradeço a minha mana querida Flavinha, que é o meu xodó, e que mesmo morando fora, sempre esteve presente no meu coração, no meu pensamento e nas minhas orações. Agradeço ao meu namorado Gabriel, pelo amor, pela compreensão, pelo companheirismo, pela preocupação e por estar sempre ao meu lado me confortando e tranquilizando com palavras de carinho. Agradeço a minha amiga Ana Paula, pelos telefonemas preocupados, querendo notícias da amiga estressada, cansada, sumida, e sempre me dizendo Acaba essa monografia logo, eu quero minha melhor amiga de volta!. Obrigada filha! Agradeço também aos meus colegas de faculdade, por esses 4 anos de convivência que não foram fáceis, mas que com certeza irei me lembrar com saudade. Em especial, a melhor comissão de formatura de todos os tempos, as minhas amigas Camila, Hallana e Letícia, pela amizade sincera, pelos momentos de alegria, de trabalho (que foram muitos), de comilança, e até de nervosismo, obrigada meninas. Sem me esquecer é claro, do bendito é o fruto entre as mulheres Gilmar, obrigada pela paciência, porque afinal de contas, não é fácil conviver com tantas mulheres. Quero agradecer a minha companheira ingrata Renata, especialmente, pela parceria tão harmoniosa, pela amizade, pelos lanchinhos gostosos e até pelos cansativos corujões. A minha xará preferida Fer Rocha, pelo carinho e também a Dani, pelas caronas tão importantes. Obrigada meninas! E aos meus professores Ricardo Carvalho e Marc Gigonzac, pela orientação, pela paciência e por terem aceitado nos ajudar nessa etapa tão importante. Obrigada professores!
6 Renata de Lima Castro Agradeço a Deus, Aquele que sempre me ouviu, confortou-me, deu-me sabedoria e me capacitou. Obrigada Senhor! Aos professores Ricardo Carvalho e Marc Gigonzac, pela paciência, atenção e valiosas colaborações ao nosso trabalho. Obrigada professores! Aos meus pais Edmilson e Rosana exemplos em minha vida - pelo apoio, dedicação e todo amor. Obrigada papai e mamãe! Ao meu namorado Neylismar, por ter tornado esta caminhada mais leve, com seu companheirismo, compreensão e carinho. Obrigada amor! A todos os meus amigos que me apoiarem nos momentos de angústia e compartilharam os momentos de alegria. Muito obrigada amigos! O meu muitíssimo obrigada a todos que colaboraram de forma direta ou indireta para a realização deste trabalho.
7 É melhor tentar e falhar, que preocupar-se e ver a vida passar; é melhor tentar, ainda que em vão, que sentar-se fazendo nada até o final. Eu prefiro na chuva caminhar, que em dias tristes em casa me esconder. Prefiro ser feliz, embora louco, que em conformidade ver... Martin Luther King
8 RESUMO As leishmanioses são zoonoses provocadas por protozoários do gênero Leishmania, que apresentam ciclo biológico heteroxênico, com duas formas evolutivas, as amastigotas e as promastigotas. A transmissão dessa infecção crônica ocorre pela picada das fêmeas dos flebotomíneos, do gênero Lutzomyia. A Leishmaniose Tegumentar Americana caracteriza-se por diferentes manifestações clínicas que acometem pele e mucosas. A Leishmaniose Visceral trata-se de uma doença grave, com alta letalidade, sendo os principais sintomas a hepatomegalia e esplenomegalia associadas à febre. Foram notificados no município de Pirenópolis casos de Leishmaniose Tegumentar Americana e Visceral. O objetivo desta pesquisa foi estudar a situação epidemiológica da leishmaniose em Pirenópolis, no Estado de Goiás, nos anos de 2005 a Os dados dos casos ocorridos em 2005 e 2006, foram retirados do Trabalho de Conclusão de Curso do acadêmico Piêrro Kristtóferson Carizzio Assunção, da Universidade Estadual de Goiás. E os dados referentes aos anos de 2007 a 2010, foram coletados junto a Secretaria Municipal de Saúde e Saneamento de Pirenópolis. Foram registrados 17 casos de leishmaniose, nas notificações da tegumentar americana observou-se somente a presença de lesões cutâneas e nas de visceral, verificou-se a presença de manifestações clínicas características da parasitose. Quanto ao diagnóstico laboratorial, foram realizados exames parasitológicos, imunológicos e histopatológicos. Constatou-se que as principais espécies de flebotomíneos encontradas no município foram Lutzmyia whitmani e Lutzomyia longipalpis e que a Leishmania (Viannia) braziliensis e Leishmania (Leishmania) chagasi foram os principais agentes etiológicos envolvidos na transmissão. Os pacientes, em sua maioria, foram submetidos a tratamento com os antimoniais pentavelentes, a droga de primeira escolha. A cidade de Pirenópolis apresenta características epidemiológicas de um local endêmico, o que requer acompanhamento constante da região, para detectar precocemente quaisquer alterações na epidemiologia. Palavras-chave: Leishmaniose. Pirenópolis. Leishmania.
9 ABSTRACT The leishmaniasis are zoonoses caused by protozoans the genus Leishmania, which have heteroxenic biological cycle, with two evolutionary forms, the amastigotes and promastigotes. The transmission of chronic infection happens through the bite of female sandflies of, the genus Lutzomyia. The Cutaneous Leishmaniasis is characterized by clinical manifestations affecting skin and mucous membranes. The Visceral Leishmaniasis is a serious disease with high fatality, and the main symptoms associated with hepatomegaly and splenomegaly with fever. Were reported in county of Pirenópolis cases Cutaneous and Visceral Leishmaniasis. The goal of this research was to study the epidemiological situation of leishmaniasis in Pirenópolis, in State of Goias, during the years 2005 to The data of the cases occurred in 2005 and 2006, were removed from the graduation work at the Piêrro Kristtóferson Carizzio Assunção at the Universidade Estadual de Goiás and the data for the years 2007 to 2010, were collected from the Secretaria Municipal de Saúde e Saneamento de Pirenópolis. Were recorded 17 cases of leishmaniasis, in reports of American cutaneous was observed only the presence of skin lesions and in the visceral, it was the presence of characteristic clinical manifestations of parasitic disease. The laboratory diagnostic tests were carried out parasitological, immunological and histopathological findings. It was found that the main species of sand flies were found in county Lutzmyia whitmani and Lutzomyia longipalpis and the Leishmania (Viannia) braziliensis and Leishmania (Leishmania) chagasi were the main etiological agents involved in transmission. The patients, most of them were treated with antimonials pentavelente, the drug of first choice. The Pirenópolis county shows epidemiological characteristics of a endemic local, which requires constant monitoring of the region, to early detect any changes in epidemiology. Keywords: Leishmaniasi. Pirenopolis. Leishmania.
10 LISTA DE ILUSTRAÇÕES Figura 1 Agente etiológico, causador da leishmaniose, pertencente ao gênero Leishmania Figura 2 Agente transmissor da leishmaniose, inseto pertencente ao gênero Lutzomyia Figura 3 Ciclo Biológico heteroxênico do parasito Figura 4 Lesão ulcerada franca, única, arredondadas, com bordas elevadas, infiltradas e fundo granuloso Figura 5 Forma cutânea difusa Polimorfismo lesional Figura 6 Paciente com Leishmaniose Visceral (fase aguda) Figura 7 Planta baixa do município de Pirenópolis Figura 8 Gráfico do número total de pacientes com LTA e com LV em porcentagem Figura 9 Gráfico do número de casos de LTA e LV nos anos de 2005 à Figura 10 Gráfico com as principais manifestações clínicas nos pacientes diagnosticados com LV de 2007 a Figura 11 Exames laboratorias realizados pelos pacientes com LTA Figura 12 Exames laboratorias realizados pelos pacientes com LV Figura 13 Mapa de Pirenópolis com os bairros e suas respectivas incidências de LTA e LV, nos anos de 2007 a Figura 14 Fotos dos bairros endêmicos de Pirenópolis Figura 15 Gráfico do percentual dos pacientes que sucederam à cura e dos que foram a óbito 52 Figura 16 Informativos divulgados pela Secretaria de Saúde e Saneamento Básico de Pirenópolis, sobre a leishmaniose e ações realizadas para o controle dos vetores... 54
11 LISTA DE TABELAS Tabela 1 Taxa de incidência de casos de Leishmaniose Tegumentar Americana por habitantes, nos anos de 2005 a Tabela 2 Relação dos casos estudados segundo idade e sexo, referentes aos anos de 2007 a
12 LISTA DE ABREVIAÇÕES DNA- Ácido Desoxirribonucléico ELISA- Enzyme Linked Immunosorbent Assay FLAB- Formulações Lipídicas da Anfotericina B HDT Hospital de Doenças Tropicais HIV- Human Immunodeficiency Virus IBGE- Instituto Brasileiro de Geografia e Estatística IDRM Intradermorreação de Montenegro IFI Imunofluorescência Indireta IFN- Interferon LACEN-GO Laboratório Central de Goiás LTA Leishmaniose Tegumentar Americana LV Leishmaniose Visceral NK- Natural Killer NNN- Novy-MacNeal-Nicolle PCR Polimerase Chain Reaction SbV- Antimoniato pentavalente SFM - Sistema Fagocitário Mononuclear SINAN- Sistema de Informação de Agravos de Notificação SMSS Secretaria Municipal de Saúde e Saneamento
13 SUMÁRIO 1. INTRODUÇÃO OBJETIVOS OBJETIVO GERAL OBJETIVOS ESPECÍFICOS REFERENCIAL TEÓRICO LEISHMANIOSE TEGUMENTAR AMERICANA Epidemiologia Situação Epidemiológica Agente etiológico Vetor Reservatórios e hospedeiros Ciclo Biológico Modo de transmissão e período de incubação Fisiopatogenia Diagnóstico clínico Leishmaniose Cutânea Leishmaniose Mucosa Leishmaniose Cutânea Difusa Diagnóstico Laboratorial Diagnóstico Parasitológico Diagnóstico Imunológico Exames Molecurales: reação em cadeia de polimerase (PCR) LEISHMANIOSE VISCERAL Epidemiologia Situação epidemiológica Agente etiológico Vetor Reservatórios Ciclo Biológico Modo de transmissão e período de incubação Outros mecanismos de transmissão... 30
14 3.2.2 Diagnóstico Clínico Diagnóstico Laboratorial Diagnóstico Parasitológico Diagnóstico Imunológico Exames Moleculares TRATAMENTO DAS LEISHMANIOSES Drogas de primeira escolha Antimoniais pentavalentes Drogas de segunda escolha Anfotericina B desoxicolato Pentamidina Outras alternativas terapêuticas Formulações lipídicas da anfotericina B (FLAB) Miltefosina MATERIAIS E MÉTODOS DESCRIÇÃO DA ÁREA DE ESTUDO METODOLOGIA RESULTADOS E DISCUSSÃO INCIDÊNCIAS DE CASOS DE LTA E LV FAIXA ETÁRIA E SEXO DOS PACIENTES DIAGNÓSTICO CLÍNICO DOS PACIENTES DIAGNÓSTICOS LABORATORIAIS BAIRROS ENDÊMICOS DO MUNICÍPIO ESPÉCIES DE FLEBOTOMÍNEOS ECONTRADAS NA CIDADE POPULAÇÃO CANINA TRATAMENTO REALIZADO PELOS PACIENTES EVOLUÇÃO DOS CASOS MEDIDAS PREVENTIVAS E DE CONTROLE CONCLUSÃO REFERÊNCIAS BIBLIOGRÁFICAS... 58
15 13 1. INTRODUÇÃO As leishmanioses são infecções crônicas, provocadas por protozoários do gênero Leishmania, família Trypanosomatidae, ordem Kinetoplastida. Durante o seu ciclo biológico apresentam duas formas evolutivas, as amastigotas que parasitam células do Sistema Fagocitário Mononuclear (SFM) de hospedeiros vertebrados e as promastigotas que se desenvolvem no aparelho digestivo dos vetores, denominados genericamente de flebotomíneos (CASTRO et al., 2002; LESSA et al., 2007; SECRETARIA DE ESTADO DA SAÚDE DE SÃO PAULO, 2004). A principal forma de transmissão do parasito para homem e outros hospedeiros ocorre por meio da picada das fêmeas dos flebotomíneos, que são insetos pertencentes à família Psychodidae, subfamília Phlebotominae e do gênero Lutzomyia (GONTIJO; MELO, 2004; LESSA et al., 2007). A Leishmaniose Tegumentar Americana (LTA) é uma endemia com elevada ocorrência no Brasil, em constante expansão territorial e diferentes padrões de transmissão em diversas áreas. Caracteriza-se por manifestações clínicas polimórficas de pele e mucosa, provocadas por protozoários do gênero Leishmania, sendo Leishmania (Viannia) braziliensis, Leishmania (Leishmania) amazonensis e Leishmania (Viannia) guyanensis, as mais encontradas no país (KAWA et al., 2010; MURBACK et al., 2011). A Leishmaniose Visceral (LV) apresenta-se em franca expansão geográfica, especialmente no meio urbano. No Brasil, é causada pelo protozoário Leishmania (Leishmania) chagasi, trata-se de uma doença grave, cujas apresentações clínicas podem ser desde assintomáticas até o quadro clássico, caracterizado principalmente por febre, hepatomegalia e esplenomegalia. Possui escassos recursos terapêuticos, além de alta letalidade quando não tratada corretamente e em tempo adequado (DANTAS-TORRES; BRANDÃO-FILHO, 2006; PASTORINO et al., 2002; WERNECK, 2010). Em casos de suspeita da doença, o diagnóstico deve fundamentar-se em dados epidemiológicos, assim como nos sintomas e métodos laboratoriais. Para a confirmação de LTA, utiliza-se métodos parasitológicos como a pesquisa direta, além de Reação em Cadeia de Polimerase (PCR), exames histopatológicos e imunológicos, como por exemplo, o de Intradermorreação de Montenegro (IDRM) e Imunofluorescência Indireta (IFI). No diagnóstico laboratorial de LV, empregam-se também as técnicas de PCR, parasitológicas,
16 14 exames imunológicos como IFI e Ensaio Imunoenzimético (ELISA) (GONTIJO; MELO, 2004; MURBACK et al., 2011; PASTORINO et al., 2002). A droga mais utilizada no tratamento das leishmanioses desde 1945 são os antimoniais pentavalentes, que são administrados por via endovenosa e o esquema terapêutico aconselhado pela Organização Mundial da Saúde é calculado em mg/sbv/kg/dia. O antimoniato comercializado no Brasil é o N-metilglucamina (Glucantime ), este medicamento apresenta diversos efeitos colaterais como náuseas, dor abdominal, prurido, febre, fraqueza, cefaléia, tontura, insônia, sendo o principal a cardiotoxicidade, relacionada a altas doses e a duração do tratamento. Em caso de contra-indicações, resistência e intolerância ao antimonial, são utilizadas drogas de segunda escolha, como pentamidina e anfotericina B, que também são tóxicas, podem não ser eficazes e apresentarem resistência (BRASIL, 2007; LIMA et al., 2007a; LIMA et al., 2007b). O município de Pirenópolis, localizado na região leste do estado de Goiás, é uma cidade turística, devido à diversidade de atrativos naturais existentes no local, como cachoeiras, reservas ecológicas, parques e mirantes. Apresenta-se em ampla expansão urbana, onde a derrubada de matas para construção de loteamentos é uma prática bastante comum. Observou-se que a cidade notificou casos de Leishmaniose Tegumentar Americana e Visceral nos últimos seis anos e que alguns destes evoluíram ao óbito. Por isso, a relevância deste estudo quanto à investigação da situação epidemiológica do município, já que se trata de uma doença grave e pouco divulgada, em uma cidade pequena e com a sua economia voltada para o ecoturismo.
17 15 2. OBJETIVOS 2.1 OBJETIVO GERAL Estudar a situação epidemiológica no município de Pirenópolis Goiás Brasil, nos anos de 2005 a OBJETIVOS ESPECÍFICOS I Determinar a incidência de casos de leishmaniose no período de 2005 a 2010; II Descrever as principais espécies de flebotomíneos encontradas no município; III Verificar as principais metodologias utilizadas nos diagnósticos laboratoriais das leishmanioses; IV Relatar os principais sintomas apresentados nos pacientes positivos; V Destacar os principais fármacos utilizados no tratamento da doença; VI Comparar os dados de Pirenópolis com os de outros municípios.
18 16 3. REFERENCIAL TEÓRICO 3.1 LEISHMANIOSE TEGUMENTAR AMERICANA A Leishmaniose Tegumentar Americana (LTA) é uma doença infecciosa, não contagiosa, caracteriza-se por diferentes manifestações clínicas, que envolve desde pequenos nódulos à destruição da mucosa. É causada por várias espécies de protozoários do gênero Leishmania, sendo primariamente, uma zoonose que afeta várias espécies de animais silvestres e domésticos, mas que secundariamente pode afetar o homem (BRASIL, 2006a; MARTINS; ALEXANDRINO; GUIMARÃES, 2010) Epidemiologia Situação Epidemiológica A leishmaniose tegumentar é considerada um problema de saúde pública, que afeta 88 países em quatro continentes, Américas, África, Ásia e Europa, são registrados de 1 a 1,5 milhões de novos casos por ano. É considerada pela Organização Mundial de Saúde (OMS), como uma das seis doenças infecciosas mais importantes, pelo seu alto coeficiente de detecção e sua capacidade de causar deformidades (BRASIL, 2000; BRASIL, 2007). A LTA, também é conhecida no Brasil, como úlcera de baurú e ferida brava, e caracteriza-se como uma afecção dermatológica de significativa relevância, devido à magnitude da doença, e também pelo envolvimento psicológico do paciente, com reflexos no campo social e econômico (BRASIL, 2007; MOREIRA et al., 2002). A doença apresenta ampla distribuição, com registro de casos em todas as regiões brasileiras, a partir da década de 80, observou-se um aumento do número de notificações, variando de (1980) a (1995). No período de 1985 a 2005, verificou-se uma média anual de casos autóctones registrados. E somente no ano de 2003 foram detectados casos, sendo: 45% dos casos na Região Norte (principalmente nos estados do Pará, Amazonas e Rondônia), 26% dos casos na Região Nordeste (predominantemente no Maranhão, Bahia e Ceará), 15% dos casos na Região Centro-Oeste (prevalecendo no Mato Grosso), 11% dos casos na Região Sudeste (destacando-se Minas Gerais) e finalmente a Região Sul com 3% dos casos (com maior frequência no Paraná) (BRASIL, 2006a; BRASIL, 2007).
19 Agente etiológico O gênero Leishmania compreende protozoários parasitos, que apresentam ciclo biológico heteroxênico, sendo as suas principais formas, conforme Figura 1: promastigota ou flagelada, a qual é alongada, detectada no tubo digestivo do inseto vetor, e amastigota ou aflagelada que é arredondada e imóvel, encontrada nas células do Sistema Fagocitário Mononuclear (SFM), nos tecidos dos hospedeiros vertebrados (GONTIJO; CARVALHO, 2003; NEVES et al., 2004). Figura 1- Agente etiológico, causador da leishmaniose, pertencente ao gênero Leishmania. (A) Forma promastigota; (B) Forma amastigota. Fonte: BRASIL, Atualmente são conhecidas nas Américas onze espécies de Leishmania causadoras de doenças humanas e oito espécies observadas somente em animais. No Brasil, já foram identificadas sete espécies que causam a LTA humana, pertencentes aos subgêneros Leishmania e Viannia. Admite-se a inexistência de imunidade cruzada entre os parasitos do subgênero Leishmania, e a imunidade pode ocorrer entre os parasitos do subgênero Viannia, porém é incompleta. (BRASIL 2000; BRITO et al., 2008). Entre as espécies de Leishmania envolvidas na etiologia da LTA no Brasil, pode-se destacar a Leishmania (Viannia) brasiliensis, que é a espécie encontrada com maior frequência no homem, causa lesões cutâneas e mucosas metastáticas e se distribui amplamente no Brasil, em todas as zonas endêmicas. Sua transmissão está associada a diferentes espécies de flebotomíneos, como Lu. whitmani, Lu. wellcomei e Lu. intermedia (BRITO et al., 2008; BASANO; CAMARGO, 2004; GUERRA et al., 2003).
20 18 A Leishmania (Viannia) guyanensis que causa, sobretudo, lesões ulceradas cutâneas, ocorre predominantemente na calha norte da Amazônia, em áreas de colonização recente. Está associada ao habitat de animais silvestres, como a preguiça, os marsupiais, os roedores, o tamanduá. Os flebotomíneos envolvidos na transmissão são Lu. anduzei, Lu. whitmani, Lu. umbratilis (BASANO; CAMARGO, 2004; GONTIJO; CARVALHO, 2003). A Leishmania (Viannia) lainsoni, a qual ocorre apenas na Amazônia, sendo a paca um reservatório natural suspeito e tem como vetor Lu. Biquitalis (BASANO; CAMARGO, 2004; GONTIJO; CARVALHO, 2003). A Leishmania (Viannia) naiffi que causa a LTA de evolução benigna, registrado na Amazônia, principalmente nos estados do Pará e do Amazonas, sendo o tau o reservatório natural. Os vetores são Lu. squamiventris, Lu. paraenses, Lu. ayrozai (BASANO; CAMARGO, 2004; GONTIJO; CARVALHO, 2003). A Leishmania (Viannia) shawi que é responsável por casos de LTA não tão frequentes no Amazonas e Pará, os reservatórios são animais silvestres, como macacos e preguiças. O principal vetor é Lu. whitmani (BASANO; CAMARGO, 2004; GONTIJO; CARVALHO, 2003). E finalmente, a Leishmania (Leishmania) amazonensis que causa úlceras cutâneas localizadas, e ocasionalmente a forma cutânea difusa anérgica, em pacientes imunodeprimidos. Distribui-se na Amazônia, particularmente em áreas de igapó e de florestas tipo várzea, no Nordeste, Sudeste e Centro-Oeste (Goiás). Os reservatórios são marsupiais e roedores silvestres e os vetores são Lu. flaviscutellata, Lu. reducta e Lu. olmeca nociva (BASANO; CAMARGO, 2004; GUERRA et al., 2003; GONTIGO; CARVALHO,2003) Vetor Os agentes transmissores da LTA são insetos chamados flebotomíneos, pertencentes ao gênero Lutzomyia e são popularmente conhecidos, dependendo da região do Brasil, como mosquito palha, birigui, tatuquira (Figura 2) (BASANO; CAMARGO, 2004; DIAS et al., 2006).
21 19 Figura 2- Agente transmissor da leishmaniose, inseto pertencente ao gênero Lutzomyia. Fonte: BRASIL, Reservatórios e hospedeiros Reservatório é uma espécie ou um conjunto de espécies de animais que participam da circulação da Leishmania na natureza, em um determinado tempo e espaço. Infecções causadas por esse parasito foram identificadas em animais silvestres e domésticos, sendo o cão, considerado como o principal reservatório doméstico da doença (BRASIL, 2007; LOPES et al., 2010; ZANZARINE et al., 2005). Na natureza ocorrem ciclos silvestres, nos quais o parasito circula entre os flebotomíneos, do gênero Lutzomyia, e os animais silvestres, incluindo algumas espécies de roedores, marsupiais, canídeos e edentados. O homem se infecta, em sua maioria, ao mudar o ambiente, interpondo-se ao ciclo quando penetra nesse ecossistema, comportando-se como hospedeiro acidental. Os animais domésticos além de reservatórios, também podem ser considerados hospedeiros acidentais e a LTA nesses animais manifesta-se cronicamente, semelhante à doença humana (GUERRA et al., 2006; NEVES et al, 2004; ZANZARINE et al., 2005) Ciclo Biológico Nos flebotomíneos as fêmeas possuem exclusivamente o hábito da hematofagia, porque necessitam do sangue para maturação dos ovários. Ao realizar a hematofagia, as fêmeas podem adquirir ou transmitir as Leishmanias, que são parasitos dimórficos, entre os
22 20 mamíferos, em determinados ambientes (Figura 3) (BRASIL, 2006a; OLIVEIRA-PEREIRA, 2008). O vetor ao picar um reservatório infectado, adquire as formas amastigotas do protozoário e no trato digestivo os macrófagos se rompem liberando-as. As mesmas sofrem divisão binária e posteriormente se transformam nas formas promastigotas, que também se reproduzem por divisão binária. Essas formas livres podem seguir por dois caminhos, no primeiro os parasitos do subgênero Viannia, migram para o intestino, local da transformação das promastigotas em paramastigotas, as quais permanecem aderidas pelo flagelo ao epitélio intestinal através de hemidesmossomas, onde ainda se dividem (BASANO; CAMARGO, 2004; BRASIL, 2006a; NEVES et al, 2004). Novamente ocorre a transformação em promastigotas, que migram através do estômago em direção a faringe do inseto. Durante esse trajeto ocorre a metaciclogênese, na qual as formas flageladas sofrem modificações bioquímicas em sua superfície, perdendo a capacidade de adesão e se tornando formas metacíclicas infectantes (BRASIL, 2006a; NEVES et al, 2004;). No segundo as formas flageladas do subgênero Leishmania, reproduzem se livres ou aderidos às paredes do estômago, onde se transformam em paramastigotas colonizando o esôfago e faringe. Então ocorre novamente a diferenciação em pequenas promastigotas metacíclicas. O tempo necessário para que o ciclo se complete varia entre 3 a 5 dias para as diferentes espécies (NEVES et al, 2004). No vertebrado, as formas promastigotas (infectantes), interagem com as células do Sistema Fagocitário Mononuclear, perdem o flagelo e na forma amastigota, passam a multiplicar-se no interior das células por divisão binária. Resistem à ação destruidora dos lisossomas, passando a ocupar todo o citoplasma. Quando a membrana do macrófago se esgota, ela é rompida liberando amastigotas no tecido, que são novamente fagocitadas, iniciando no local uma reação inflamatória (BASANO; CAMARGO, 2004; NEVES et al, 2004; OLIVEIRA-PEREIRA, 2008).
23 21 Figura 3- Ciclo Biológico Heteroxênico do parasito. Fonte: < Modo de transmissão e período de incubação A transmissão do parasito ocorre através da picada das fêmeas de flebotomíneos infectados, que representam a ligação entre os reservatórios e os hospedeiros, e uma pessoa infectada não transmite a outra. Os participantes da transmissão de LTA mudam dependendo da região geográfica, pois envolvem diversas espécies de parasitos, reservatórios, vetores e hospedeiros. O período de incubação dura aproximadamente de dois a três meses, mas pode variar de duas semanas a dois anos (BRASIL, 2007; ZANZARINE et al., 2005) Fisiopatogenia Quando as formas promastigotas são inoculadas na pele, inicia-se uma complexa interação entre o parasito e a resposta imunológica do hospedeiro, que será determinante para a caracterização da forma clínica da LTA. Vários segmentos do sistema imunológico são
24 22 ativados, mas a resposta imune celular, própria para Leishamania, tem um importante papel no controle final à infecção (BRASIL, 2006a; BRITO et al., 2008). Inicialmente as promastigotas introduzidas na pele, encontram no local células do sistema imune como as células natural killer (NK), polimorfonucleares (neutrófilos, eosinófilos e macrófagos) e sistema complemento. As formas flageladas que ficam fora das células, são rapidamente destruídas. E as que aderem à superfície dos macrófagos e das células de Langerhans passam para o meio intracelular, por meio de fagocitose mediada por receptores, os lisossomas dessas células fundem-se aos vacúolos parasitóforos, o que causa uma modificação do microambiente, e estimulam a transformação em amastigotas. Isso facilita a sobrevivência do parasito que fica mais resistente e desencadeia uma menor resposta oxidativa da célula parasitada (BRASIL, 2006a; BRASIL, 2007). As células NK são muito importantes no controle da infecção, pois além de sua ação citotóxica, é fonte primária de interferon-gama (IFN-γ), o que determina um potencial para desenvolver resposta imune adequada, induzindo à resistência na primeira semana de infecção (BRASIL, 2006a; BRASIL, 2007). A imunidade específica à leishmaniose é basicamente mediada por células TCD4+ e para iniciar a resposta imune, as células de Langerhans transportam os parasitos e seus antígenos aos linfonodos, para apresentarem os antígenos às células TCD4+, as quais liberam citocinas chamadas IFN-γ, que ativam os macrófagos, tornando-os capazes de destruírem as amastigotas (BRASIL, 2006a; BRASIL, 2007). Os mecanismos de eliminação envolvem síntese de óxido nítrico. Os macrófagos são simultaneamente, células hospedeiras apresentadoras de antígenos para o sistema imune e efetoras para a eliminação do parasito (BRASIL, 2007) Diagnóstico clínico Leishmaniose Cutânea A leishmaniose cutânea apresenta-se como lesões na pele, nos locais onde foram inoculadas as formas promastigotas metacíclicas do parasito pelo vetor. A úlcera, via de regra, é única, típica, costuma ser indolor, tem formato arredondado ou ovalado, bordas elevadas com fundo avermelhado e granulações grosseiras, pode medir desde alguns milímetros até
25 23 centímetros, normalmente localiza-se nas partes expostas da pele (Figura 4). As lesões apresentam polimorfismos, sendo encontradas formas impetigóide, liquenóide, tuberculosa ou lupóide, nodular, vegetante e ectimatóide (GONTIJO; CARVALHO 2003, MURBACK, et al., 2011). Figura 4 - Lesão ulcerada franca, única, arredondada, com bordas elevadas, infiltradas e fundo granuloso. Fonte: BRASIL, O período de incubação dura cerca de 10 dias a 3 meses, o quadro geralmente não apresenta sintomas, e em alguns casos a infecção se desenvolve como uma pápula eritematosa que progride para nódulo, depois de um tempo de latência. Isso devido à disseminação linfática e/ou hematogênica do parasito (BRASIL, 2007; GONTIJO; CARVALHO, 2003). Essa forma é causada principalmente pelas espécies L. (Viannia) braziliensis, L.(Viannia) guyanensis, L. (Viannia) lainsoni e L.(Leishmania) amazonensis (MURBACK et al., 2011) Quando não tratadas, as lesões podem evoluir para cura espontânea dentre de meses a alguns anos, ou podem continuar ativas e coexistir com lesões mucosas de surgimento posterior. As lesões cutâneas podem deixar cicatrizes atróficas com superfície lisa, deprimida e áreas de hipo ou hiperpigmentação (BRASIL, 2007) Leishmaniose Mucosa Estima-se que cerca de 3 a 5% dos casos de leishmaniose cutânea evoluam para lesão mucosa, que se apresenta como lesões destrutivas na mucosa orofaríngea, nasal, palatos, lábios, língua, laringe e mais raramente, traquéia e vias respiratórias superiores (BRASIL, 2007; LESSA et al., 2007).
26 24 O acometimento mucoso pode acontecer com a lesão cutânea primária ainda ativa ou algum tempo após a cicatrização, devido a metástase hematogênica. Isso provavelmente acontece, por causa da demora na cicatrização da lesão e tratamento inicial inadequado. Geralmente, a úlcera é indolor e inicia-se no septo nasal anterior cartilaginoso, próximo a cavidade nasal, sendo de fácil visualização (GONTIJO; CARVALHO, 2003; LESSA et al., 2007; MURBACK, et al, 2011). Dentre os pacientes com leishmaniose cutânea que evoluem para a mucosa, 90% ocorrem nos primeiros 10 anos, destes 50% ocorrem nos dois primeiros anos após a cicatrização (BRASIL, 2007) Leishmaniose Cutânea Difusa A leishmaniose cutânea difusa caracteriza-se por lesões nodulares não ulceradas, múltiplas, espalhadas pela pele e distantes do sítio de inoculação (Figura 5). Inicia-se como lesões localizadas típicas (ulceradas, com bordas expressas e fundos granulosos). Então provavelmente ocorre o fenômeno da disseminação do parasito por via hemática ou linfática, aguda em maior ou menor intensidade, que se instala em poucos dias ou em até 24 horas, causando lesão distante do local do repasto sanguíneo do vetor. Esta forma encontra-se vinculada a uma resposta imune celular deprimida, que leva o paciente a um estado de anergia imunológica (BRASIL 2007; LESSA et al., 2007; MURBACK et al., 2011). Figura 5 - Forma cutânea difusa Polimorfismo lesional. Fonte: BRASIL, 2007.
27 Diagnóstico Laboratorial Os métodos diagnósticos laboratoriais têm como objetivos, confirmar o diagnóstico clínico e fornecer informações epidemiológicas, como caracterização da espécie encontrada, e propor o tratamento e as medidas de profilaxia adequadas a fim de evitar o agravo e o surgimento de novos casos (BRASIL, 2007) Diagnóstico Parasitológico O diagnóstico parasitológico apresenta técnicas de pesquisa direta e indireta. A demonstração direta das formas amastigotas do parasito é o exame de primeira escolha, por ser o mais simples e rápido. O material é retirado da úlcera por biópsia da borda, escarificação ou aspiração e corado utilizando Giemsa ou Leishman. A capacidade de encontrar o parasito é inversamente proporcional ao tempo de permanência da lesão e a sensibilidade dos métodos. Quanto menor o tempo de evolução da L. braziliensis, por exemplo, maior a probabilidade de se encontrar o parasito, sendo de 100% nos primeiros meses, 75% aos seis meses e 20% acima de 12 meses (BASANO; CAMARGO, 2004; BRASIL 2007; PASSOS et al., 2001). Já os métodos de pesquisa indireta como isolamento em cultivo in vitro, é um método de confirmação do agente etiológico, o que torna possível a identificação da espécie de Leishmania envolvida. O meio de cultura mais utilizado para o isolamento é o ágar-sangue, no qual entre 24 e 26 C ocorre o crescimento do parasito. Outro método indireto utilizado é o isolamento in vivo, o material retirado da lesão é inoculado nas patas posteriores e focinho de animais de laboratório, como hamster (Mesocricetusauratus), porém gasta-se um longo período para o desenvolvimento da lesão (de 2 a 9 meses) e o isolamento apresenta variação dependendo da espécie (BASANO; CAMARGO, 2004; GONTIJO; CARVALHO, 2003; PASSOS, et al., 2001) Diagnóstico Imunológico Como exemplo de diagnóstico imunológico, existe a Intradermoreação de Montenegro (IDRM) que detecta a resposta de hipersensibilidade celular a LTA, já que o paciente desenvolve uma memória imunológica durante a doença e após a cura. A IDRM pode ser negativa durante as primeiras 4 a 6 semanas após o início da lesão. Apresenta relevante
28 26 importância no diagnóstico dos casos em que o agente etiológico é escasso ou ausente, sendo utilizado também nos inquéritos de áreas endêmicas. A positividade fica cerca de 84% para formas cutâneas e 100% para mucocutânea (BASANO; CAMARGO, 2004; BRASIL, 2007; CASTRO et al., 2002). Além da IDRM, as reações sorológicas são utilizadas para detectar anticorpos anti- Leishmania circulantes no soro do paciente. A técnica de Ensaio Imuno Enzimático (ELISA), não está disponível para comercialização, sendo utilizada restritamente em caso de pesquisa. A reação de imunofluorescência indireta (IFI) é a mais utilizada, entretanto pode apresentar reação cruzada com a Doença de Chagas. Sua capacidade de detecção varia entre 71% nos casos da forma cutânea e 100% na mucosa, sendo negativo para difusa (BRASIL, 2007; GONTIJO; CARVALHO, 2003) Exames Molecurales: reação em cadeia de polimerase (PCR) Uma das técnicas que possui maior eficiência e sensibilidade, em relação as outras técnicas utilizadas para diagnóstico é a polimerase chain reaction (PCR), e vem sendo muito utilizada para realização de pesquisas. Apresenta algumas vantagens, como maior chance de se encontrar o DNA do parasito no sangue do indivíduo, diagnóstico rápido que pode ser feito em várias amostras, maior sensibilidade, já que pesquisas mostram que a técnica foi capaz de identificar o DNA de Leishmania em amostras negativas para outros testes. Enfim, o PCR é capaz de identificar o parasito, tanto em material de biópsia, quanto em sangue venoso. (MARTINS; ALEXANDRINO; GUIMARÃES, 2010). 3.2 LEISHMANIOSE VISCERAL A leishmaniose visceral (LV) é uma enfermidade infecciosa generalizada, crônica grave, potencialmente fatal para o homem quando não se institui o tratamento adequado. No Brasil, é conhecida também como calazar, barriga d água e outras denominações (GONTIJO; MELO, 2004). O protozoário causador da LV nas Américas é um parasita intracelular obrigatório e a espécie é Leishmania (Leishmania) chagasi (FIGUEREDO et al. 2010; PASTORINO et al., 2002).
29 27 Dada a sua incidência e alta letalidade, principalmente em indivíduos não tratados e crianças desnutridas, é também considerada uma doença oportunista em indivíduos portadores da infecção pelo vírus da imunodeficiência adquirida (HIV), tornando-se uma das doenças mais importantes da atualidade (CARRANZA-TAMAYO et al., 2009) Epidemiologia Situação epidemiológica Os principais surtos epidêmicos relatados no mundo foram na Índia em 1994, no Estado Bihar, onde 250 mil pessoas encontraram-se infectadas, e no Sudão, onde, recentemente, ocorreram 100 mil mortes atribuídas a LV (NEVES et al., 2004). Segundo Alencar & Dietze (1991) o registro do primeiro caso da doença no Brasil ocorreu em 1913, quando Migone, no Paraguai, descreveu o caso em material de necropsia, do paciente oriundo de Boa Esperança, Mato Grosso. Nos últimos anos, a letalidade da LV vem aumentando gradativamente, passando de 3,6% no ano de 1994 para 6,7% em 2003, o que representa um aumento de 85% (WERNECK et al., 2003). Dois surtos epidêmicos foram registrados no período de 1994 a 1996 nas cidades de Teresina (PI) e São Luis (MA), inicialmente, a doença tinha um caráter eminentemente rural, porém, hoje, vem se expandindo para as áreas urbanas de médio e grande porte (TURETZ et al., 2002). Segundo o Ministério da Saúde, em dezenove anos de notificação, do ano de 1984 a 2002, no Brasil os casos de LV somaram casos. Nos últimos dez anos, a média anual de casos no País foi de casos, e a incidência de dois casos em cada habitantes (BRASIL, 2006b; COSTA et al., 2004). A doença é mais freqüente em crianças menores de dez anos, devido à maior susceptibilidade explicada pelo estado de relativa imaturidade imunológica celular agravada pela desnutrição, tão comum nas áreas endêmicas, além de uma maior exposição ao vetor no peridomicílio. Já o envolvimento do adulto, tem repercussão significativa na epidemiologia da LV, pelas formas oligossintomáticas ou assintomáticas, além das formas com expressão clínica (CARRANZA-TAMAYO et al., 2009; LOPES et al., 2010; TURETZ et al., 2002).
30 28 Ambientes de baixo nível socioeconômico, pobreza, são característicos e propícios à ocorrência da doença, são aqueles prevalentes em grande medida no meio rural e na periferia das grandes cidades. Entretanto, estas características vêm se modificando, principalmente, nos estados das regiões Sudeste e Centro-Oeste, onde a LV se encontra urbanizada (BRASIL, 2006b; CAMARGO-NEVES et al., 2001) Agente etiológico Os parasitos responsáveis pela LV estão agrupados no complexo donovani, onde são reconhecidos atualmente três espécies como agente etiológico da doença: Leishmania (Leishmania) donovani; Leishmania (Leishmania) infantum e Leishmania (Leishmania) chagasi. Em alguns estudos recentes consideram a L. (L.) chagasi como espécie idêntica à L. (L.) infantum, estas espécies apresentam distribuição geográfica definida, afetando principalmente regiões tropicais e subtropicais. Assim, Leishmania (Leishmania) donovani acomete indivíduos na Ásia e no leste da África, a Leishmania (Leishmania) infantum afeta principalmente a bacia do Mediterrâneo, compreendendo países da Europa e norte da África, nordeste da China e sul da Rússia. Enquanto, nas Américas, ocorre uma única espécie representante deste complexo, a Leishmania (Leishmania) chagasi (DANTAS-TORRES, 2006; KURLS, et al., 2005; SHAW, 2006) Vetor Os insetos flebotomíneos são também vetores da leishmaniose visceral. No Brasil, duas espécies, até o momento, estão relacionadas com a transmissão da doença Lutzomyia longipalpis e Lutzomyia cruzi. A primeira espécie é considerada a principal espécie transmissora da Leishmania (Leishmania) chagasi no país, sendo ela encontrada em quatro das cinco regiões geográficas: Nordeste, Norte, Sudeste e Centro-Oeste (MISSAWA; BORBA, 2009; PETERSON; SHAW, 2003). Ao final da década de 80, verificou-se a adaptação deste vetor aos ambientes urbanos, em periferias de grandes centros, podendo ser encontrados no peridomicílio, em galinheiros, chiqueiro, canil, paiol, entre outros ambientes e também no intradomicílio (BRASIL, 2006; COSTA et al., 2004).
31 Reservatórios Na área urbana a principal fonte de infecção é o cão. A enzootia canina tem precedido a ocorrência de casos humanos e a infecção em cães tem sido mais prevalente do que no homem. No ambiente silvestre, os reservatórios são as raposas e os marsupiais (CAMARGO- NEVES et al., 2001; BRASIL, 2006b) Ciclo Biológico O ciclo biológico da Leishmania (L.) chagasi é do tipo heteroxênico, envolvendo como transmissor as fêmeas da L. longipalpis, este ciclo ocorre no ambiente terrestre e compreende-se em quatro fases de desenvolvimento: ovo, larva (com quatro estadios), pupa e adulto. Após a cópula as fêmeas colocam seus ovos sobre um substrato úmido no solo e com alto teor de matéria orgânica, para garantir a alimentação das larvas (BRASIL, 2006b; MAIA- ELKHOURY et al., 2008). O desenvolvimento do ovo ao inseto adulto decorre um período de aproximadamente 30 a 40 dias de acordo com a temperatura. As fêmeas são hematófagas obrigatórias, apresentam hábitos ecléticos podendo realizar o repasto sangüíneo em várias espécies de animais vertebrados, inclusive em humanos, em áreas urbanas, o cão parece ser a principal fonte de alimentação (BRASIL, 2006b; TURETZ et al., 2002). A atividade dos flebotomíneos é crepuscular e noturna. No intra e peridomicílio, a L. longipalpis é encontrada, principalmente, próximas a uma fonte de alimento. Durante o dia, estes insetos ficam em repouso, em lugares sombreados e úmidos, protegidos do vento e de predatores naturais (COSTA et al., 2004; RANGEL; RALPH, 2003). A infecção do vetor ocorre quando as fêmeas, ao sugarem o sangue de mamíferos infectados, ingerem macrófagos parasitados por formas amastigotas da Leishmania e no trato digestivo anterior ocorre o rompimento dos macrófagos liberando essas formas. Reproduzemse por divisão binária e diferenciam-se rapidamente em formas flageladas (promastigotas), que também se reproduzem por processos sucessivos de divisão binária. Essas formas transformam-se em paramastigotas, as quais colonizam o esôfago e a faringe do vetor e permanecem aderidas ao epitélio pelo flagelo, diferenciando-se em formas infectantes promastigotas metacíclicas (DIAS; LOROSA; REBELO, 2003; TAUIL, 2006).
32 30 O ciclo do parasito no inseto se completa em torno de 72 horas, após este período, as fêmeas infectantes, ao realizarem um novo repasto sangüíneo em um hospedeiro vertebrado não infectado o homem ou outro reservatório - liberam as promastigotas metacíclicas juntamente com a saliva do inseto (NEVES et al., 2004). Na epiderme do hospedeiro, estas formas são fagocitadas por células do Sistema Mononuclear Fagocitário (SMF) e no interior dos macrófagos, diferenciam-se em amastigotas e multiplicam-se intensamente até o rompimento dos mesmos, ocorrendo à liberação destas formas que serão fagocitadas por novos macrófagos num processo contínuo, havendo, portanto, a disseminação hematogênica para outros tecidos ricos em células do SMF, como linfonodos, fígado, baço e medula óssea (NEVES et al., 2004) Modo de transmissão e período de incubação A forma de transmissão é através da picada dos vetores L. longipalpis ou L. cruzi, infectados pela Leishmania (Leishmania) chagasi (DIAS; LOROSA; REBELO, 2003; NEVES et al., 2004). Alguns autores admitem a hipótese da transmissão entre a população canina através da ingestão de carrapatos infectados e mesmo através de mordeduras, cópula, ingestão de vísceras contaminadas, porém não existem evidências sobre a importância epidemiológica destes mecanismos de transmissão para humanos ou na manutenção da enzootia (CAMARGO-NEVES et al., 2004; COSTA et al., 2004). O período de incubação é bastante variável tanto para o homem como para o cão. No homem pode variar de 10 dias a 24 meses, com média entre 2 a 6 meses, enquanto no cão, de 3 meses a vários anos com média de 3 a 7 meses (COSTA et al., 2004) Outros mecanismos de transmissão Pode também ocorrer, eventualmente, a transmissão da doença através de acidentes laboratoriais quando há auto-inoculação por meio de material perfurocortante contaminado; em transfusão sanguínea, na qual o processo de transmissão requer que o parasito esteja presente no sangue periférico do doador e que sobreviva ao processo de estocagem no banco de sangue e infecte o receptor. Embora não seja tão conhecida a real situação deste tipo de transmissão no Brasil, sete casos foram descritos na literatura. Através do uso de drogas
33 31 injetáveis - no compartilhamento de seringas e agulhas contaminadas e também por meio de transmissão congênita - em que se acredita ocorrer através de células do SFM infectadas por amastigotas que atravessariam a membrana que separa a circulação fetal materna ou por contato do sangue da mãe com o do filho no momento do parto (NEVES et al., 2004) Diagnóstico Clínico A infecção pela Leishmania (L.) chagasi caracteriza-se por um amplo espectro clínico, que pode variar desde as manifestações clínicas discretas (oligossintomáticas), moderadas e graves e que se não tratadas podem levar o paciente à morte. As rotinas de diagnóstico, tratamento e acompanhamento dos pacientes necessitam ser implantadas obrigatoriamente em todas as áreas com transmissão ou em risco de transmissão (GONTIJO; MELO, 2004). O diagnóstico clínico da leishmaniose visceral deve ser suspeitado quando o paciente apresentar febre, esplenomegalia e hepatomegalia. A identificação precoce dos pacientes que poderão evoluir o mal, é de fundamental importância para se reduzir a letalidade por meio da instituição de medidas terapêuticas e profiláticas eficazes (CARRANZA-TAMAYO et al., 2010; CARVALHO, 2000; RIGO; RIGO; RONER, 2009). Considerando a evolução clínica da doença (Figura 6), optou-se em dividi-la em períodos: período inicial: o início da sintomatologia que pode variar de paciente para paciente, mas na maioria dos casos inclui febre com duração inferior a quatro semanas, palidez cutâneo-mucosa e hepatoesplenomegalia; período de estado: caracteriza-se por febre irregular, geralmente associada a emagrecimento progressivo, palidez cutâneo-mucosa e aumento da hepatoesplenomegalia. Apresenta um quadro clínico arrastado geralmente com mais de dois meses de evolução, na maioria das vezes, associado a comprometimento do estado geral; período final: caso não seja feito o diagnóstico e tratamento, a doença evolui progressivamente para o período final, com febre contínua e comprometimento mais intenso do estado geral. Instala-se a desnutrição, edema dos membros inferiores que pode evoluir para anasarca, outras manifestações importantes incluem hemorragias, icterícia e ascite (BRASIL, 2006b; OLIVEIRA et al., 2010).
34 32 Figura 6- Paciente com Leishmaniose Visceral (fase aguda). Fonte: BRASIL, Diagnóstico Laboratorial Diagnóstico Parasitológico A punção aspirativa esplênica é o método que oferece maior sensibilidade para demonstração do parasita, seguida pelo o aspirado de medula óssea, biópsia hepática e a aspiração de linfonodos. Por tratar-se de um procedimento mais seguro, recomenda-se a punção aspirativa da medula óssea. O material aspirado deverá ser examinado e submetido a pelo menos uma das técnicas de exame direto, isolamento em meio de cultura in vitro ou isolamento em aninais (BRASIL, 2006b; DOURADO et al., 2007). No Exame Direto, formas amastigotas do parasita podem ser visualizadas em lâminas pelas colorações de Giemsa ou Wright, Leishman, Panóptico. O encontro de parasitas no material examinado depende do número de campos observados, deve-se analisar cerca de duzentos, antes de considerar uma lâmina como negativa (DOURADO et al., 2007). No isolamento em meio de cultura in vitro, formas amastigotas do parasita, inoculadas em meios de cultura especiais, contendoágar e sangue de coelho, transformam-se em formas promastigotas. O clássico meio de NNN (Novy-MacNeal-Nicolle) é o mais comumente empregado e a presença de meio líquido sobre o NNN, comoo LIT ou de Drosophila de Schneider, aumenta e acelera a positividade da cultura (RIGO; RIGO; RONER, 2009). O isolamento em animais susceptíveis in vivo é feita através de uma inoculação experimental em hamsters, de amostras de tecidos de pacientes com suspeita de LV, não tem
35 33 valor prático no diagnósticoda doença devido ao seu demorado tempo de positividade, de 1 a 3 meses (DOURADO et al., 2007; RIGO; RIGO; RONER, 2009) Diagnóstico Imunológico No Brasil, os exames imunológicos mais utilizados são a IFI e os ensaios imunoenzimáticos. O teste ELISA tem o seu resultado expresso em unidades de absorvância a um raio de luz ou, mais comumente, apenas como reagente ou não. Na presença de dados clínicos e laboratoriais, um teste sorológico reagente, reforça o diagnóstico de LV. Entretanto, um teste reagente, na ausência de manifestações clínicas sugestivas da doença, não autoriza o início do tratamento (OLIVEIRA, et al.,2010; RIGO; RIGO; RONER, 2009). A IDRM, ao contrário do que ocorre na LTA, é sempre negativa durante o período de estado da doença, não sendo assim, utilizado para o diagnóstico. Ela torna-se positiva após a cura clínica na maioria dos pacientes em um período de seis meses a três anos após o término do tratamento (DOURADO et al., 2007) Exames Moleculares O método do PCR, que se constitui na amplificação do DNA do parasita, trata-se de uma nova perspectiva para o diagnóstico da LV, pois apresenta alta sensibilidade. Entretanto, os seus resultados dependem de algumas variáveis envolvidas, como: área endêmica, o tipo de amostra, o alvo do DNA utilizado para amplificação e o método de extração do DNA (KUHLS et al., 2005; MURBACK et al., 2011). 3.3 TRATAMENTO DAS LEISHMANIOSES Drogas de primeira escolha Antimoniais pentavalentes A Organização Mundial da Saúde e o Ministério da Saúde do Brasil, recomendam para o tratamento das leishmanioses em humanos, os antimoniais pentavalentes (SbV) como drogas de primeira escolha. O primeiro antimônio pentavalente sintetizado foi o
36 34 estibogluconato de sódio, com nome comercial de Pentostam, em 1945, neste mesmo ano, ocorreu a síntese de outro composto pentavalente, o antimoniato de N-metil glucamina, conhecido comercialmente como Glucantime (AMATO, 2006; BRASIL, 2004; BRASIL, 2006b; GILMAN et al., 2001). Os antimoniais pentavalentes parecem atuar no mecanismo bioenergético das formas amastigotas da Leishmania, por meio de glicólise e beta-oxidação, que ocorrem nas organelas denominadas glicossomas. Outro mecanismo cogitado é o de ligação com sítios sulfidrílicos, provocando a morte destes protozoários (ROMERO et al., 2001a). As recomendações terapêuticas para o tratamento da LTA, segundo o Ministério da Saúde, são: em lesões cutâneas localizadas e disseminadas: 15 mg/sbv/kg/dia, durante 20 dias seguidos. Na forma cutânea difusa, embora as recidivas sejam invariavelmente freqüentes, a dose é de 20 mg/sbv/kg/dia, durante 20 dias seguidos. Em lesões mucosas, 20 mg/sbv/kg/dia, durante 30 dias seguidos (BRASIL, 2006a; BRASIL, 2007; LIMA et al., 2007a). E recomenda-se o tratamento da LV com a dose de 20mg/SbV/kg/dia, por no mínimo 20 e no máximo 40 dias, utilizando-se o limite máximo de 2 a 3 ampolas/dia do produto com bons índices de cura. A aplicação dessas drogas deve ser realizada por via intramuscular (IM) ou endovenosa (EV) (BERMAN, 2003). Antes da utilização do antimonial e durante o tratamento, devem ser realizados eletrocardiograma, dosagem sérica de uréia e creatinina, enzimas hepáticas e leucograma. O eletrocardiograma deve ser realizado duas vezes por semana e os demais exames ao menos uma vez por semana (RATH et al., 2003). As contra-indicações ao uso dos antimoniais são para gestantes, portadores de cardiopatias, nefropatias e hepatopatias. Quanto às nefropatias, deve ser ressaltado que os antimoniais pentavalentes não são dialisáveis, ocorrendo acúmulo em indivíduos com clearance de creatinina rebaixado e, portanto, podendo levar a arritmias graves (PASSOS et al., 2001). As variações da eficácia terapêutica dessas drogas, tanto na LTA quanto na LV, podem ser consequência de diferentes esquemas posológicos utilizados nos diversos estudos; resultados terapêuticos não homogêneos em diferentes regiões geográficas e falta de padronização do conteúdo de SbV em cada lote do antimoniato de N-metil glucamina. Outros
37 35 fatores relacionados à eficácia terapêutica estariam relacionados ao agente causal e à imunidade do hospedeiro (MAIA-ELKHOURY et al., 2008; RATH et al., 2003). A terapia com os antimoniais pode apresentar falha, na forma cutânea. Embora os estudos não possam ser absolutamente comparáveis, devido a diferentes esquemas posológicos utilizados, insucesso terapêutico ou recidivas podem ocorrer com estes medicamentos na LTA. Nos casos mais avançados de LV, onde a resposta clínica nos primeiros 20 dias não é evidente, o tempo mínimo de tratamento deverá ser estendido para 30 dias, tempo necessário para lograr índices de cura satisfatórios (ROMERO et al., 2001b; PASSOS et al., 2001). Em caso de falha terapêutica ao antimonial usado isoladamente, foi demonstrado que a associação com um inibidor do fator de necrose tumoral, a pentoxifilina, pode produzir bons resultados. A posologia nestes casos é de 20 mg/sbv/kg/dia de antimônio pentavalente com 400 mg de pentoxifilina três vezes ao dia, por 30 dias (LESSA et al., 2001). Os efeitos adversos mais freqüentes dos antimoniais são: artralgia, mialgia, náusea, vômito, cefaléia, anorexia, aumento de transaminases, fosfatase alcalina, lípase e amilase, leucopenia, cardiotoxicidade. Outros efeitos colaterais menos freqüentes são: aumento de uréia e creatinina, arritmia cardíaca, morte súbita e herpes zoster (BRASIL, 2000; BRASIL, 2004; BRASIL, 2006b) Drogas de segunda escolha Anfotericina B desoxicolato Os primeiros relatos da eficiência da anfotericina B no tratamento da LTA ocorreram no final da década de 1950 e início dos anos Posteriormente, outros estudos analisaram a utilização da anfotericina B no tratamento da LTA, demonstrando pequeno número de recidivas e melhor ação sobre as lesões mucosas em comparação aos antimoniais (BROWN et al., 2005; LIMA et al., 2007a). A anfotericina B interage especificamente com o ergosterol, esteróide da membrana das Leishmanias, causando aumento de permeabilidade e morte do parasito, ela é aplicada por via endovenosa, diluída em soro glicosado 5% e infundida em quatro horas. A posologia de anfotericina B desoxicolato para o tratamento da LTA, deve ser de 1 a 4 mg/kg/dia diariamente por infusão venosa, em dose única, sem limite de dose diária até atingir doses
38 36 totais de 1 a 1,5 g em formas cutâneas e na forma mucosa e cutaneomucosa de 2,5 a 3g. E para o tratamento da LV, a dose recomendada é de 1,0 a 1,5 mg/kg/dia durante 21 dias, ou como alternativa a dose de 3,0 mg/kg/dia durante 10 dias (CARVALHO, 2000; BERMAN, 2003; ROMERO et al., 2001b). A anfotericina B desoxicolato é contra-indicada em gestantes e em indivíduos com cardiopatias e nefropatias, seus efeitos colaterais são: febre, calafrios cefaléia, hipocalemia, hipomagnesemia, anemia, leucopenia, flebite, nefrotoxicidade e arritmias. Deve-se dosar duas vezes por semana níveis séricos de sódio, potássio, magnésio, uréia e creatinina, além de realizar hemograma e eletrocardiograma. (AMATO et al., 2006, BRASIL, 2000; BRASIL, 2004) Pentamidina A pentamidina é comercializada sob a forma de isotionato e mesilato, em frascos que contêm 300 mg de droga, a dosagem utilizada é de 4mg/kg/dia em dias alternados no total de 15 doses, não ultrapassando a 2g como dose total. Sua eficácia é inferior a dos antimoniais pentavalentes e anfotericina B e seus paraefeitos maiores (PAULA et al., 2003). A droga, provavelmente, age interferindo na síntese do DNA, alterando morfologicamente o cinetoplasto e fragmentando a membrana mitocondrial. A administração pode ser realizada por via EV ou IM, administra-se a pentamidina diluída em soro glicosado a 10%, em infusão lenta (TURETZ, et al., 2002). As contra-indicações são gravidez, diabetes, nefropatias com insuficiência renal e cardiopatias, podendo causar náuseas, vômitos, cefaléia, hipoglicemia, hipotensão durante a infusão, aumento de uréia e creatinina, síncope, leucopenia, pancreatite e alterações inespecíficas do segmento ST e da onda T.E durante a terapia com a droga, deve-se realizar duas vezes por semana exames de glicemia de jejum, creatinina, uréia e eletrocardiograma e pacientes que receberam doses superiores a 1 g devem ter a glicemia monitorizada por seis meses após o término do tratamento (BRASIL, 2004). A pentamidina é droga extremamente eficaz no tratamento da LTA, especialmente em lesões cutâneas, cuja dose acumulada aparentemente não necessita ser tão expressiva. Esta droga pode ser eficaz na forma cutânea, seja causada por Leishmania (Viannia) braziliensis
39 37 ou por Leishmania (Viannia) gyuanensis, doses maiores, embora aumentem o risco de toxicidade pancreática, evidenciam um expressivo sucesso terapêutico na forma mucosa da LTA (PAULA et al., 2003) Outras alternativas terapêuticas Alguns esquemas terapêuticos são utilizados como alternativas para casos refratários ou com contra-indicação aos esquemas clássicos. Entre os esquemas mais utilizados, destacam-se a associação de antimonial pentavalente + pentoxifilina, ou antimonial pentavalente + alopurinol, antimonial pentavalente + sulfato de aminosidina, antimonial pentavalente + sulfato de paramomicina, antimonial pentavalente + imunoterápicos. Apesar dessas indicações fazerem sentido, não foram documentadas por ensaios clínicos controlados, o que possam respaldar sua aprovação (CARVALHO, 2000; LESSA, et al., 2001) Formulações lipídicas da anfotericina B (FLAB) O emprego das FLAB no tratamento da leishmaniose constitui-se em alternativa terapêutica nos casos de falha ou contra-indicações dos antimoniais, e medicações de segunda escolha (AMATO et al., 2004; BROWN et al., 2005). As FLAB têm sido utilizadas esporadicamente no tratamento das formas cutâneas e mucosas da LTA, seja em pacientes imunocompetentes ou com alguma forma de imunossupressão, incluindo indivíduos infectados pelo vírus da imunodeficiência humana. Estas formulações têm apresentado resultados promissores, embora estudos com maior casuística sejam necessários, especialmente para se determinar a dose adequada para cada forma de leishmaniose (AMATO et al., 2000) Miltefosina A miltefosina foi a primeira droga de uso oral usada no tratamento da LV. Na LV causada por L. donovani, na Índia, os resultados foram bastante promissores. Os mecanismos
40 38 de ação da miltefosina contra a Leishmania ainda não são bem entendidos. Sabe-se que esta droga é capaz de bloquear a síntese e alterar a composição da membrana do parasita e que existem poucos efeitos adversos, tais como vômito e diarréia. Em relação à LTA, estudos utilizando a miltefosina no tratamento da forma cutânea da doença resultaram em boa eficácia contra Leishmania (Viannia) panamensis, mas para Leishmania (Viannia) braziliensis, não houve eficiência adequada (SOTO et al., 2004).
41 39 4. MATERIAIS E MÉTODOS 4.1 DESCRIÇÃO DA ÁREA DE ESTUDO O município de Pirenópolis localiza-se no leste goiano, abrangendo uma área de km 2, a120 km de distância da capital Goiânia, pela rodovia BR 153. Faz limite com: ao Norte, com o município de Vila Propício; ao Sul, com os municípios de Anápolis e Petrolina de Goiás; a Leste, com os municípios de Cocalzinho, Corumbá de Goiás, Abadiânia; e a oeste com os municípios de São Francisco de Goiás, Jaraguá e Goianésia. Suas coordenadas geográficas são latitude (S): 15,8525 e longitude (W): 48,9591 (CARVALHO, 2001; IBGE 2010). Possui um total de habitantes, sendo que (67,59%) pertencem a população urbana e (32,41%) a população rural. Do número total de habitantes, (51, 27%) são do sexo masculino e (48,73%) do sexo feminino (IBGE, 2010). Segundo Goiás (2002) o perímetro urbano consiste nos seguintes bairros ou localidades (Figura 7): Centro: compreende o Centro Histórico, as vilas Couro e Anduzeiro e o entorno sul do campo das cavalhadas, incluindo o Jardim Kubitscheck I. A população estimada é de, aproximadamente, habitantes, em uma área estimada de 82,28 hectares com densidade de 54 habitantes por hectare. Alto do Carmo: constitui-se pelo Bairro do Carmo e Vilas Pompeu I e II, ocupando uma área de 35,57 hectares, com uma população de habitantes, caracterizando uma densidade de 46 habitantes por hectare. Vilas Matutina I e II, Pireneus e Pequizeiro: esse grupo de vilas localiza-se no entorno do Centro Histórico. Compreendendo uma área de 18,68 hectares, com uma população estimada de habitantes, caracterizando uma densidade de 55 habitantes por hectare. Alto da Lapa: é uma continuação do Centro Histórico. Apresenta uma das mais altas densidades populacionais da cidade. Possui uma área total de 15,98 hectares e sua população habitantes. São, portanto, 91 habitantes por hectare.
42 40 Alto do Bonfim: é constituído pelo Jardim Santa Bárbara, Jardim Pireneus, as vilas José Aires, Nenen Jayme, Nhonho Godinho, Santa Bárbara, João Figueiredo, Pratinha, o Alto do Bonfim e o Setor Meia Ponte. Essa área encontra-se densamente povoada, abrigando cerca de habitantes. Sua densidade demográfica é de 27 habitantes por hectare. Área do eixo Benjamin Constant: é formada pelas Vilas Oliveira e Estrela D alva e casario lideiro à Avenida Benjamin Constant. O conjunto localiza-se a leste dessa avenida até o córrego Pratinha. Vilas Zizito Pompeu, Marília, Teodoro de Oliveira, Cintra e Jardim Kubitschek I e II encontram-se a oeste da avenida Benjamin Constan, tendo como limite o córrego Lava-pés. Esse conjunto de Bairros forma uma área de 49,24 hectares onde está assentada uma população de habitantes em uma densidade de 46,51 habitantes por hectare.
43 41 Figura 7 Planta baixa do município de Pirenópolis. Fonte: <
44 METODOLOGIA Os dados dos casos de leishmaniose ocorridos no Município de Pirenópolis nos anos de 2005 e 2006 foram extraídos do Trabalho de Conclusão de Curso de Biologia, da Universidade Estadual de Goiás, do acadêmico Piêrro Kristtóferson Carizzio Assunção, no ano de 2007, cujo título é Ocorrência de Leishmaniose Tegumentar Americana e Leishmaniose Visceral no Município de Pirenópolis, Goiás, Brasil. E os casos confirmados referentes aos anos de 2007 a 2010, foram coletados junto a Secretaria Municipal de Saúde e Saneamento (SMSS) de Pirenópolis. As informações necessárias para o estudo foram retiradas do Sistema de Informação de Agravos de Notificação (SINAN), o qual entrou em vigência no ano de 2007.
45 43 5. RESULTADOS E DISCUSSÃO 5.1 INCIDÊNCIAS DE CASOS DE LTA E LV O município de Pirenópolis pode ser classificado como endêmico para leishmaniose, pois apresentou um ou mais casos autóctones nos últimos 10 anos (BRASIL, 2007). Segundo os registros da SMSS foram notificados no período de 2005 a 2010 um total de 17 casos autóctones da parasitose, sendo 6 casos (35%) de LTA e 11 casos (65%) de LV (Figura 8). Percentual de casos de LTA e LV 65% 35% LTA LV Figura 8 - Gráfico do número total de pacientes com LTA e com LV em porcentagem. A taxa de incidência por habitantes de LV nesse período, apresentou uma variação de 6,41 a 25,66 casos, incidência que comparada a do município de Várzea Grande, no Estado de Mato Grosso, que variou de 0 a 11,7 casos, entre 1998 a 2007, é relativamente alta (MESTRE; FONTES, 2007). Quanto à incidência de LTA no período, houve uma variação de 0 a 12,83 casos, com uma média de 6,415. Com base nos dados do Ministério da Saúde, quanto às taxas de incidência por ano, de alguns Estados brasileiros, calculou-se as médias das taxas entre o período de 2005 a 2009 (Tabela 1). O Estado de Goiás apresentou neste período uma média de 7,42 casos, isso mostra que a média de Pirenópolis, está bem próxima a do Estado.
46 44 Comparando a média da taxa de incidência de Goiás com a média de 3.834,8 casos do Estado do Pará, no mesmo período, pôde-se notar o quanto a situação neste Estado é crítica, pela discrepância dos valores das médias observadas. Já Minas Gerais, apresentou uma média bem próxima a de Goiás, com 7,28 casos, enquanto que na Bahia, essa média foi de 17,82, maior que o dobro dos outros dois Estados. Ao correlacionar o valor da média de incidência de Goiás com a do Rio Grande do Sul, que foi de 0,1 casos, notou-se a que a do primeiro Estado é relativamente alta. Na Região Centro-Oeste do país, o Mato Grosso é o Estado que apresentou a maior média da taxa de incidência, de 109,9 casos, quando comparado com os demais. Tabela 1 Taxa de incidência de casos de Leishmaniose Tegumentar Americana por habitantes, nos anos de 2005 a Região e UF Média Norte Pará ,8 Rondônia ,8 Tocantins ,6 Nordeste Bahia 14,5 16,7 13,6 20,8 23,5 17,82 Ceará 24,4 12,2 11,2 8,3 11,6 13,54 Maranhão 55,6 35,2 37,3 26,3 25,5 35,94 Sudeste São Paulo 1,2 1,2 0,8 0,8 0,9 0,98 Rio de Janeiro 12,1 11,8 0,8 0,3 0,6 5,12 Minas Gerais 9,4 9,5 6,7 5,7 5,1 7,28 Sul Paraná 4,3 3,9 4,2 5,0 3,8 4,24 Rio Grande do Sul 0,1 0,1 0,1 0,1 0,1 0,1 Santa Catarina 1,4 2,7 1,1 1,4 0,7 1,46 Centro-Oeste Mato Grosso 129,8 111,3 93,3 85,2 129,9 109,9 Goiás 10,3 8,8 4,2 6,0 7,8 7,42 Distrito Federal 1,4 2,1 1,4 0,6 1,0 1,3 Fonte: Ministério da Saúde, Do número total de casos, 4 foram notificados no ano de 2005, sendo estes somente LV, enquanto que em 2006 foram registrados 2 ocorrências tanto de LTA quanto de LV. O ano de 2007 apresentou apenas 1 caso de LV, já em 2008 ocorreram 2 casos, um de cada tipo
47 45 de leishmaniose. Em 2009 totalizou-se 3 notificações, 2 de LTA e 1 de LV e no ano de 2010 também houve o mesmo número de casos, porém, 1 de LTA e 2 de LV, conforme Figura 9. Número de casos por ano 4 LTA LV Figura 9 - Gráfico do número de casos de LTA e LV nos anos de 2005 à FAIXA ETÁRIA E SEXO DOS PACIENTES Segundo demonstra a Tabela 2, observou-se que os pacientes apresentaram uma ampla faixa etária, variando de 1 a 62 anos de idade, havendo predominância do sexo feminino, isto corrobora com Missawa & Borba (2009) nos levantamentos feitos em Várzea Grande, Mato Grosso. Apesar de a literatura apontar o sexo masculino como o mais afetado pela LV, devido maior exposição aos vetores flebotomíneos (DANTAS-TORRES; BRANDÃO-FILHO, 2006).
48 46 Tabela 2 Relação dos casos estudados segundo idade e sexo, referentes aos anos de 2007 a 2010 Idade (anos) Sexo F M Total > Total Legenda: F - feminino; M - masculino. Verificou-se que os pacientes com faixa etária entre 1 a 15 anos, pertencem ao sexo feminino e que todos foram notificados com LV, o que caracteriza uma maior ocorrência deste tipo de Leishmaniose em crianças e adolescentes. Isso mostra que a pouca idade na LV é um fator de risco, pois a susceptibilidade é maior devido imaturidade imunológica, geralmente agravada pela desnutrição (BEVILACQUA et al., 2001; MESTRE; FONTES, 2007). A elevada ocorrência da enfermidade nesta faixa propõe que a infecção aconteça nos ambientes peridomiciliar e intradomiciliar (MESTRE; FONTES, 2007; SILVA et al., 2001).No sexo masculino não houve pacientes na faixa etária de 1 a 15 anos, predominando indivíduos com idade maior que 45 anos (50%). 5.3 DIAGNÓSTICO CLÍNICO DOS PACIENTES Quanto ao diagnóstico clínico, em todos os casos de LTA foram observados somente a presença característica de lesões cutâneas. No estudo realizado por Murback et al. (2011) no Hospital Universitário de Campo Grande, esta também foi a forma mais encontrada, em 68,1% dos casos, e em menor percentual verificou-se a presença das formas mucosa (27,7%) e cutaneomucosa (4,3%).
49 47 Enquanto na LV, as principais manifestações clínicas apresentadas foram febre, hepatomegalia, esplenomegalia, tosse, diarréia, palidez e fraqueza (Figura 10) Sintomas da LV Figura 10 - Gráfico com as principais manifestações clínicas nos pacientes diagnosticados com LV de 2007 a Estes são sintomas clássicos da doença e estão em consonância com estudos de outros autores (OLIVEIRA et al., 2010; PEDROSA; ROCHA, 2004; PASTORINO et al., 2002; CARRANZA-TAMAYO et al., 2010). Ocorreram ainda, em menor freqüência icterícia, hemorragia, emagrecimento, edema, quadro infeccioso, e outros sintomas como náusea, vômito, dispnéia e dor abdominal. 5.4 DIAGNÓSTICOS LABORATORIAIS A Figura 11 e Figura 12, apresentam os exames aos quais os 4 pacientes com suspeita de LTA e os 5 de LV foram submetidos, podendo estes terem realizado mais de um exame diferente. Para a confirmação da LTA, 1 indivíduo realizou o exame parasitológico direto, cujo resultado foi negativo e 3 não realizaram. Quanto a IDRM, 3 pacientes foram sujeitos ao exame, apresentando 2 resultados positivos e 1 negativo, entretanto em 1 paciente o exame não foi realizado. Além dos exames parasitológicos e imunológicos, foi feito a histopatologia
50 48 em todos os suspeitos, apresentando resultado compatível para a presença de formas amastigotas do parasito, em 100% dos casos (Figura 11). Diagnóstico Laboratorial de LTA Positivo Negativo Não realizado Parasitológico Direto Intradermorreação de Montenegro Figura 11 Exames laboratoriais realizados pelos pacientes com LTA. Dos exames realizados para confirmação de LTA, a pesquisa direta apresenta uma diminuição da sensibilidade com o aumento do tempo de evolução da doença. A mesma é praticamente 100% positivo nos casos de infecções recentes e progressivamente negativa com a duração da lesão. Contudo, os exames de IDRM e IFI podem ser vantajosos em casos de escassez de parasitos nas lesões e no diagnóstico de turistas em áreas endêmicas, pois é comum esses testes apresentarem positividade mesmo em pacientes sem lesão ativa ou cicatricial (MURBACK et al., 2011; PASSOS et al., 2001; RODRIGUES, 2000). Assim como o exame parasitológico direto, o histopatológico possuiu um maior percentual de confirmações em lesões recentes, já que há uma diminuição do número de parasitos à medida que o processo crônico granulomatoso se organiza. Isso aumenta a quantidade de exames sugestivos, como constatado nesse estudo (MURBACK et al., 2011; PASSOS et al., 2001; RODRIGUES, 2000). Nos casos de LV, para sua confirmação, foi realizado o diagnóstico parasitológico em todos os suspeitos, apresentando 3 resultados positivos e 2 negativos (Figura 12). O material no qual as informações foram coletadas, não especificou qual o tipo de diagnóstico parasitológico o paciente foi submetido. Se foi por pesquisa direta do parasito em lâminas ou esfregaço, isolamento em meio de cultura ou inoculação em hamster (GONTIJO; MELO, 2004; MURBACK, 2011).
51 49 Diagnóstico Laboratorial para LV Positivo Negativo Não realizado Parasitológico Direto Imunofluorescência Indireta Outros Figura 12 Exames laboratorias realizados pelos pacientes com LV. Quanto ao diagnóstico imunológico apenas 2 pacientes foram submetidos a IFI, sendo 1 positivo e 1 negativo. E em 3 pacientes foram realizados outros testes imunológicos, apresentando resultados positivos. O paciente negativo para IFI também realizou outro teste que apresentou o mesmo resultado do anterior, neste caso o critério de confirmação foi clínico epidemiológico. Referindo-se aos exames para diagnóstico de LV, o parasitológico direto possui uma alta especificidade, porém uma sensibilidade bastante variável, devido à falta de homogeneidade na distribuição dos parasitos no tecido. A LV apresenta uma característica estimulação policlonal de linfócitos B, resultando em elevada produção de anticorpos, o que facilita os testes sorológicos e evita os parasitológicos, que são métodos invasivos. No Brasil, os exames sorológicos mais usados são a IFI e ELISA, os quais utilizam antígenos brutos e são limitados quanto à especificidade (GONTIJO; MELO, 2004; SUNDAR, 2002). 5.5 BAIRROS ENDÊMICOS DO MUNICÍPIO A Figura 13 apresenta a ocorrência de leishmaniose nos bairros de Pirenópolis, sendo que dos 4 casos de LTA, 3 (75%) ocorreram no bairro Alto da Lapa e 1 (25%) no Alto do Carmo, enquanto na LV todos os 5 casos (100%) registrados foram no bairro Alto do Bonfim, apresentando notificações nos anos 2007, 2008, 2009 e Esses dados indicam que a
52 50 distribuição dos casos de leishmaniose no município não foi aleatória, caracterizando-se um padrão de agregação no local, o que pode estar relacionado às condições sócio-econômicas da população (MISSAWA; BORBA, 2009). Figura 13 Mapa de Pirenópolis com os bairros e suas respectivas incidências de LTA e LV, nos anos de 2007 a Fonte: < Notou-se que os bairros com maiores incidências de casos de leishmaniose apresentam fatores que facilitam a propagação dos vetores, como residências localizadas bem próximas às matas, locais úmidos e sombreados, presença de eqüinos, suínos e aves perto do ambiente domiciliar. Esses animais podem atrair vetores da doença, além de contribuírem juntamente com os lixos espalhados pelos moradores, para o aumento de matéria orgânica no solo, deixando-o favorável ao desenvolvimento das larvas de flebotomíneos. Constatou-se também a existência de cães, que são hospedeiros por servirem como fonte de alimento ao mosquito palha. Esses fatores se assemelham aos apresentados pela Secretaria de Estado da Saúde de São Paulo (2007) e Mestre & Fontes (2007). A Figura 14 ilustra alguns locais dos bairros mais acometidos por LTA e LV, sendo possível observar nos bairros Alto do Carmo, Alto do Bonfim e Alto da Lapa a presença de residências bem próximas às matas e serras, animais como cavalos, galinhas e cachorros nos quintais, lixos espalhados no peridomicílio. Esses fatores contribuem para a presença de flebotomíneos, bem como de outros insetos que podem ser transmissores de doenças.
53 51 Figura 14 - Fotos dos bairros endêmicos de Pirenópolis. (A) Bairro Alto do Carmo; (B) Bairro Alto do Bonfim; (C) e (D) Bairro Alto da Lapa. 5.6 ESPÉCIES DE FLEBOTOMÍNEOS ECONTRADAS NA CIDADE Segundo a SMSS, as espécies de Lutzomyia até hoje encontradas na cidade são Lu. whitmani, Lu. longipalpis, Lu. lenti, Lu. sallesi, Lu. sordelli, Lu. aragaoi, Brumptomyia sp, Lu. baculus, Lu. oliveirai. Sendo Lu. whitmani e Lu. longipalpis, potenciais vetores da leishmaniose, as espécies mais abundantes, o que também foi constatado por Assunção (2007) em seu trabalho realizado em Pirenópolis. Diversos estudos entomológicos, como o de Martins et al. (2002), realizado no Estado de Goiás, em áreas de ocorrência de LTA, verificaram um número considerável de Lu. whitmani infectados por Leishmania (Viannia) brasiliensis, sendo portanto, apontados como transmissores da LTA (OLIVEIRA-PEREIRA, 2008).
54 52 A Lu. whitmani, espécie do flebotomíneo relacionada à transmissão de LTA no município, é também a espécie encontrada com maior frequência no Distrito Federal, que foi coletada no peridomicílio (59,2%), no intradomicílio (4,1%) e no cerrado (36,7%). Já em São João, Manaus, a espécie prevalente foi a Lu. umbratilis (32,3%) (GUERRA et al., 2006; SAMPAIO et al., 2009). Relatos demonstram uma significativa associação dos casos de LV e a presença de Lu. longipalpis, principal vetor da Leishmania (Leishmania) chagasi, agente etilógico dessa doença. Em pesquisa realizada nos anos de 2005 a 2009 no Distrito Federal, observou-se que essa espécie foi frequentemente encontrada na casa ou no bairro de pacientes com LV (MARTINS et al., 2002; CARRANZA-TAMAYO et al., 2010). 5.7 POPULAÇÃO CANINA Ocorreu no município, entre os anos de 2005 e 2006, uma Campanha Sorológica para Leishmaniose Canina, onde amostras de sangue foram coletadas de cães, tanto da zona urbana quanto da zona rural, e submetidos à IFI no Laboratório Central de Goiás (LACEN), localizado na capital Goiânia. Os cães soropositivos foram sacrificados por eutanásia utilizando-se cloreto de potássio intravenoso, visto a proibição do tratamento em cães pelos Ministérios da Saúde e da Agricultura, Pecuária e Abastecimento, conforme a Portaria IM nº que regulamenta o Decreto nº Alguns estudos explicam essa proibição por apresentarem evidências de que os cães tratados mantêm a capacidade de infectar os flebotomíneos (MIRET et al., 2008; RIBEIRO et al., 2008). A leishmaniose tem apresentado mudanças na sua epidemiologia com notificações de casos em meio urbano, sendo que o cão possui um papel importante nessa expansão, especialmente em áreas endêmicas, uma vez que é considerado como o principal reservatório doméstico. Pesquisas apontam que elevadas taxas de prevalência canina, estão ligadas à ocorrência de casos humanos. Isso confirma a necessidade de realização de inquéritos sorológicos caninos, para o planejamento antecipado de ações profiláticas (ALMEIDA, 2009; LOPES et al., 2010).
55 TRATAMENTO REALIZADO PELOS PACIENTES Oito pacientes notificados entre 2007 e 2010, foram submetidos a tratamento com a droga de primeira escolha, o antimonial pentavalente e apenas um utilizou anfotericina B. No entanto, a utilização destas drogas é questionável, devido à eficácia variável entre as diferentes espécies de Leishmania, alta toxicidade com relatos de óbitos, indução de resistência do parasito, administração via parenteral e custo elevado (BEZERRA et al., 2006; PEDROSA; ROCHA, 2004). 5.9 EVOLUÇÃO DOS CASOS Dos casos analisados, certificou-se que todos os referentes à LTA evoluíram para a cura após o período de tratamento. Quanto à evolução dos casos de LV, nem todos sucederam para a cura, tendo esta um percentual de 73%, e 27% para o óbito, que totaliza 3 crianças, duas notificadas em 2005 com idades de 3 meses e 4 anos e uma em 2009 com 1 ano de idade (Figura 15). Já na pesquisa de Oliveira, et al. (2010) a letalidade por LV foi maior em pacientes adultos acima de 40 anos (69%), o que caracteriza esses grupos como de risco, provavelmente devido queda imunológica nessas faixas etárias. Evolução dos casos de LV Óbito 27% Cura 73% Figura 15 Gráfico do percentual dos pacientes que sucederam à cura e dos que foram a óbito.
Leishmaniose. Família: Trypanosomatidae (da mesma família que o Trypanosoma cruzi, causador de Chagas).
 Leishmaniose Parasito Reino: Protozoa Filo: Sarcomastigophora (porque possui flagelo) Ordem: Kinetoplastida (porque tem cinetoplasto) Família: Trypanosomatidae (da mesma família que o Trypanosoma cruzi,
Leishmaniose Parasito Reino: Protozoa Filo: Sarcomastigophora (porque possui flagelo) Ordem: Kinetoplastida (porque tem cinetoplasto) Família: Trypanosomatidae (da mesma família que o Trypanosoma cruzi,
FAMÍLIA TRYPANOSOMATIDAE
 FAMÍLIA TRYPANOSOMATIDAE CLASSIFICAÇÃO: FILO SARCOMASTIGOPHORA(flagelos, pseudópodes ou ambos) SUBFILO MASTIGOPHORA (protozoários com 1 ou + flagelos) FAMÍLIA TRYPANOSOMATIDAE: São nove gêneros que parasitam
FAMÍLIA TRYPANOSOMATIDAE CLASSIFICAÇÃO: FILO SARCOMASTIGOPHORA(flagelos, pseudópodes ou ambos) SUBFILO MASTIGOPHORA (protozoários com 1 ou + flagelos) FAMÍLIA TRYPANOSOMATIDAE: São nove gêneros que parasitam
Gênero Leishmania. século XIX a febre negra ou Kala-azar era temida na Índia. doença semelhante matava crianças no Mediterrâneo
 Leishmaniose Leishmaniose é um espectro de doenças produzidas por Leishmania sp. cuja manifestação clínica varia de infecção assintomática tica à morte Gênero Leishmania Histórico século XIX a febre negra
Leishmaniose Leishmaniose é um espectro de doenças produzidas por Leishmania sp. cuja manifestação clínica varia de infecção assintomática tica à morte Gênero Leishmania Histórico século XIX a febre negra
Universidade Federal Rural do Rio de Janeiro Instituto de Veterinária Departamento de Epidemiologia e Saúde Pública
 Universidade Federal Rural do Rio de Janeiro Instituto de Veterinária Departamento de Epidemiologia e Saúde Pública LEISHMANIOSE CANINA Leishmanose Tegumentar America LTA Leishmania Visceral - LV Adivaldo
Universidade Federal Rural do Rio de Janeiro Instituto de Veterinária Departamento de Epidemiologia e Saúde Pública LEISHMANIOSE CANINA Leishmanose Tegumentar America LTA Leishmania Visceral - LV Adivaldo
Leishmaniose Tegumentar Americana
 Leishmaniose Tegumentar Americana (Leishmania) Prfª. M.Sc. Yara Bandeira Azevedo UNIFAN Leishmania Filo: Sarcomastigophora Subfilo: Mastigophora Ordem: Kinetoplastida Família: Trypanosomatidae Gênero:
Leishmaniose Tegumentar Americana (Leishmania) Prfª. M.Sc. Yara Bandeira Azevedo UNIFAN Leishmania Filo: Sarcomastigophora Subfilo: Mastigophora Ordem: Kinetoplastida Família: Trypanosomatidae Gênero:
Complexo Leishmania donovani Forte tendência a visceralização (baço, fígado, medula óssea e órgãos linfóides).
 ORDEM: KINETOPLASTIDA FAMÍLIA: TRYPANOSOMATIDAE GÊNERO: Leishmania Classificações: A) SUBGÊNEROS: Leishmania Viannia B) COMPLEXOS: Parasitologia (Nutrição) Aula 4 (26/03) Leishmania Profa. Adriana Pittella
ORDEM: KINETOPLASTIDA FAMÍLIA: TRYPANOSOMATIDAE GÊNERO: Leishmania Classificações: A) SUBGÊNEROS: Leishmania Viannia B) COMPLEXOS: Parasitologia (Nutrição) Aula 4 (26/03) Leishmania Profa. Adriana Pittella
Agente etiológico. Leishmania brasiliensis
 Leishmaniose Agente etiológico A leishmaniose é causada por protozoários flagelados chamados Leishmania brasiliensis e Leishmania chagasi, que invadem e se reproduzem dentro das células que fazem parte
Leishmaniose Agente etiológico A leishmaniose é causada por protozoários flagelados chamados Leishmania brasiliensis e Leishmania chagasi, que invadem e se reproduzem dentro das células que fazem parte
Módulo: Nível Superior Dezembro/2014 GVDATA
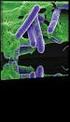 Módulo: Nível Superior Dezembro/2014 GVDATA Classificada no grupo de doenças extremamente negligenciadas Leishmanioses Volta Redonda Barra Mansa Rio de Janeiro Niterói Definição de Caso suspeito Todo individuo
Módulo: Nível Superior Dezembro/2014 GVDATA Classificada no grupo de doenças extremamente negligenciadas Leishmanioses Volta Redonda Barra Mansa Rio de Janeiro Niterói Definição de Caso suspeito Todo individuo
Universidade de São Paulo -USP. Leishmanioses. Luciana Benevides. Ribeirão Preto- 2013
 Universidade de São Paulo -USP Leishmanioses Luciana Benevides Ribeirão Preto- 2013 Tópicos abordados Definição Leishmaniose Vetores Parasita Manifestações clínicas Epidemiologia Classificação das doenças
Universidade de São Paulo -USP Leishmanioses Luciana Benevides Ribeirão Preto- 2013 Tópicos abordados Definição Leishmaniose Vetores Parasita Manifestações clínicas Epidemiologia Classificação das doenças
Relações Parasitas e Hospedeiros. Aula 06 Profº Ricardo Dalla Zanna
 Relações Parasitas e Hospedeiros Aula 06 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 2 Hemoparasitoses o Seção 2.1 Toxoplasmose e Doença de Chagas o Seção 2.2 Leishmaniose oseção 2.3 Malária
Relações Parasitas e Hospedeiros Aula 06 Profº Ricardo Dalla Zanna Conteúdo Programático Unidade 2 Hemoparasitoses o Seção 2.1 Toxoplasmose e Doença de Chagas o Seção 2.2 Leishmaniose oseção 2.3 Malária
Leishmanioses. Zoonoses e Administração em Saúde Pública Universidade Federal de Pelotas. Prof. Fábio Raphael Pascoti Bruhn
 Leishmanioses Zoonoses e Administração em Saúde Pública Universidade Federal de Pelotas Prof. Fábio Raphael Pascoti Bruhn Porque estudar a leishmaniose? Leishmaniose visceral Doença negligenciada associada
Leishmanioses Zoonoses e Administração em Saúde Pública Universidade Federal de Pelotas Prof. Fábio Raphael Pascoti Bruhn Porque estudar a leishmaniose? Leishmaniose visceral Doença negligenciada associada
Leishmanioses. Silvia Reni B. Uliana ICB - USP
 Leishmanioses Silvia Reni B. Uliana ICB - USP Síndromes clínicas Localizada L. braziliensis L. amazonensis etc. Leishmaniose tegumentar Mucocutânea Disseminada L. braziliensis L. braziliensis Difusa L.
Leishmanioses Silvia Reni B. Uliana ICB - USP Síndromes clínicas Localizada L. braziliensis L. amazonensis etc. Leishmaniose tegumentar Mucocutânea Disseminada L. braziliensis L. braziliensis Difusa L.
Levantamento epidemiológico da leishmaniose tegumentar na região Nordeste, Brasil, de 2001 a 2010
 Levantamento epidemiológico da leishmaniose tegumentar na região Nordeste, Brasil, de 2001 a 2010 1 Médico Veterinário UFRPE. E-mail: vagne_melo@hotmail.com Vagne de Melo Oliveira 1 Resumo: Doença parasitária
Levantamento epidemiológico da leishmaniose tegumentar na região Nordeste, Brasil, de 2001 a 2010 1 Médico Veterinário UFRPE. E-mail: vagne_melo@hotmail.com Vagne de Melo Oliveira 1 Resumo: Doença parasitária
Manual de Vigilância e Controle das Leishmanioses
 Secretaria Estadual de Saúde de Mato Grosso Superintendência de Vigilância em Saúde Coordenadoria de Vigilância em Saúde Ambiental Gerência de Vigilância de Vetores e Antropozoonoses Manual de Vigilância
Secretaria Estadual de Saúde de Mato Grosso Superintendência de Vigilância em Saúde Coordenadoria de Vigilância em Saúde Ambiental Gerência de Vigilância de Vetores e Antropozoonoses Manual de Vigilância
Trypanosoma cruzi Doença de Chagas
 Disciplina de Parasitologia Trypanosoma cruzi Doença de Chagas Profa. Joyce Fonteles Histórico Histórico 1908- Carlos Chagas MG encontrou o parasito no intestino de triatomíneos. 1909- descrição do primeiro
Disciplina de Parasitologia Trypanosoma cruzi Doença de Chagas Profa. Joyce Fonteles Histórico Histórico 1908- Carlos Chagas MG encontrou o parasito no intestino de triatomíneos. 1909- descrição do primeiro
ESTUDO DO PERFIL EPIDEMIOLÓGICO DA LEISHMANIOSE VISCERAL NA REGIÃO NORDESTE
 ESTUDO DO PERFIL EPIDEMIOLÓGICO DA LEISHMANIOSE VISCERAL NA REGIÃO NORDESTE Raquel Costa e Silva 1 ; Karla Gomes Cunha 2 ; Gerlane Guedes Delfino da Silva³; Lucas Ermando Ricardo da Silva 4 ; Josimar dos
ESTUDO DO PERFIL EPIDEMIOLÓGICO DA LEISHMANIOSE VISCERAL NA REGIÃO NORDESTE Raquel Costa e Silva 1 ; Karla Gomes Cunha 2 ; Gerlane Guedes Delfino da Silva³; Lucas Ermando Ricardo da Silva 4 ; Josimar dos
ENFERMAGEM DOENÇAS INFECCIOSAS E PARASITÁRIAS. OUTRAS DOENÇAS INFECCIOSAS E PARASITÁRIAS Aula 3. Profª. Tatiane da Silva Campos
 ENFERMAGEM DOENÇAS INFECCIOSAS E PARASITÁRIAS Aula 3 Profª. Tatiane da Silva Campos Poliomielite Doença viral aguda; paralisia flácida de início súbito; déficit motor instala-se subitamente e a evolução
ENFERMAGEM DOENÇAS INFECCIOSAS E PARASITÁRIAS Aula 3 Profª. Tatiane da Silva Campos Poliomielite Doença viral aguda; paralisia flácida de início súbito; déficit motor instala-se subitamente e a evolução
LEISHMANIOSES 31/08/2015. Leishmanioses: etiologia. Leishmanioses: distribuição mundial
 LEISHMANIOSES L E I S H M A N I O S E T E G U M E N T A R A M E R I C A N A L E I S H M A N I O S E V I S C E R A L http://www.zoonoses.org.br/ Fonte: http://www.mdsaude.com/ Fonte: http://www.wspabrasil.org/
LEISHMANIOSES L E I S H M A N I O S E T E G U M E N T A R A M E R I C A N A L E I S H M A N I O S E V I S C E R A L http://www.zoonoses.org.br/ Fonte: http://www.mdsaude.com/ Fonte: http://www.wspabrasil.org/
BIOLOGIA. Qualidade de Vida das Populações Humanas. Principais doenças endêmicas no Brasil. Prof. ª Daniele Duó.
 BIOLOGIA Qualidade de Vida das Populações Humanas Principais doenças endêmicas no Brasil Prof. ª Daniele Duó - História da Epidemiologia Hipócrates (mais de 2000 anos) fatores ambientais influenciam a
BIOLOGIA Qualidade de Vida das Populações Humanas Principais doenças endêmicas no Brasil Prof. ª Daniele Duó - História da Epidemiologia Hipócrates (mais de 2000 anos) fatores ambientais influenciam a
TÍTULO: OCORRÊNCIA DE LEISHMANIA SP DETECTADA POR PCR EM LABORATÓRIO DE PATOLOGIA CLÍNICA PARTICULAR DE SP
 Anais do Conic-Semesp. Volume 1, 2013 - Faculdade Anhanguera de Campinas - Unidade 3. ISSN 2357-8904 TÍTULO: OCORRÊNCIA DE LEISHMANIA SP DETECTADA POR PCR EM LABORATÓRIO DE PATOLOGIA CLÍNICA PARTICULAR
Anais do Conic-Semesp. Volume 1, 2013 - Faculdade Anhanguera de Campinas - Unidade 3. ISSN 2357-8904 TÍTULO: OCORRÊNCIA DE LEISHMANIA SP DETECTADA POR PCR EM LABORATÓRIO DE PATOLOGIA CLÍNICA PARTICULAR
SITUAÇÃO ATUAL DA LEISHMANIOSE VISCERAL NO ESTADO DO CEARÁ
 SITUAÇÃO ATUAL DA LEISHMANIOSE VISCERAL NO ESTADO DO CEARÁ Ana Paula Cunha Gomes Bouty Médica Veterinária Assessora Técnica GT-Leishmanioses NUVET/COVIG/SESA Leishmaniose Visceral A leishmaniose visceral
SITUAÇÃO ATUAL DA LEISHMANIOSE VISCERAL NO ESTADO DO CEARÁ Ana Paula Cunha Gomes Bouty Médica Veterinária Assessora Técnica GT-Leishmanioses NUVET/COVIG/SESA Leishmaniose Visceral A leishmaniose visceral
do Vale do Araguaia UNIVAR - LEISHMANIOSE TEGUMENTAR AMERICANA HUMANA NO MUNICÍPIO DE GENERAL CARNEIRO MATO GROSSO
 1 JORDANA BELOS DOS SANTOS 1, ANDRÉ LUIZ FERNANDES DA SILVA 2, PATRÍCIA GELLI FERES DE MARCHI 2, ISABELLA RODRIGUES DA SILVA CONDE 1 1 Acadêmicas do Curso de Medicina Veterinária das Faculdades Unidas
1 JORDANA BELOS DOS SANTOS 1, ANDRÉ LUIZ FERNANDES DA SILVA 2, PATRÍCIA GELLI FERES DE MARCHI 2, ISABELLA RODRIGUES DA SILVA CONDE 1 1 Acadêmicas do Curso de Medicina Veterinária das Faculdades Unidas
Palavras-chaves: Doença cutânea, mosquito-palha, doenças tropicais, Leishmania.
 HISTÓRIA DA LEISHMANIOSE TEGUMENTAR AMERICANA NO ESTADO DE GOIÁS JANINE VARGAS RESUMO O presente projeto visa realizar o levantamento histórico da doença leishmaniose tegumentar americana no Brasil, especificamente
HISTÓRIA DA LEISHMANIOSE TEGUMENTAR AMERICANA NO ESTADO DE GOIÁS JANINE VARGAS RESUMO O presente projeto visa realizar o levantamento histórico da doença leishmaniose tegumentar americana no Brasil, especificamente
AVALIAÇÃO EPIDEMIOLOGICA DA LEISHMANIOSE VISCERAL NA CIDADE DE IMPERATRIZ, MARANHÃO. Natã Silva dos Santos 1 Graduando em Enfermagem
 AVALIAÇÃO EPIDEMIOLOGICA DA LEISHMANIOSE VISCERAL NA CIDADE DE IMPERATRIZ, MARANHÃO. Natã Silva dos Santos 1 Graduando em Enfermagem Universidade Federal do Maranhão-natan.silva0@gmail.com Gustavo de Almeida
AVALIAÇÃO EPIDEMIOLOGICA DA LEISHMANIOSE VISCERAL NA CIDADE DE IMPERATRIZ, MARANHÃO. Natã Silva dos Santos 1 Graduando em Enfermagem Universidade Federal do Maranhão-natan.silva0@gmail.com Gustavo de Almeida
NOVO CONCEITO. Nova proposta para a prevenção da Leishmaniose Visceral Canina UMA DUPLA PROTEÇÃO PARA OS CÃES. CONTRA O VETOR E O PATÓGENO!
 NOVO CONCEITO Nova proposta para a prevenção da Leishmaniose Visceral Canina UMA DUPLA PROTEÇÃO PARA OS CÃES. CONTRA O VETOR E O PATÓGENO! Repelente de uso tópico para cães Vacina recombinante contra Leishmaniose
NOVO CONCEITO Nova proposta para a prevenção da Leishmaniose Visceral Canina UMA DUPLA PROTEÇÃO PARA OS CÃES. CONTRA O VETOR E O PATÓGENO! Repelente de uso tópico para cães Vacina recombinante contra Leishmaniose
LEISHMANIOSE LEISHMANIOSE LEISHMANIOSE LEISHMANIOSE. Protista SUB-REINO: REINO: Protozoa FILO: Sarcomastigophora SUBFILO: Mastigophora CLASSE:
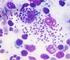 PROTOZOÁRIOS Sarcomastigophora Apicomplexa Ciliophora Mastigophora Sarcodina Babesia Balantidium Trypanosoma Giardia Entamoeba Acanthamoeba Naegleria Eimeria Isospora Sarcocystis Trichomonas Endolimax
PROTOZOÁRIOS Sarcomastigophora Apicomplexa Ciliophora Mastigophora Sarcodina Babesia Balantidium Trypanosoma Giardia Entamoeba Acanthamoeba Naegleria Eimeria Isospora Sarcocystis Trichomonas Endolimax
Vigilância da Leishmaniose Tegumentar Americana no estado do Rio de Janeiro 01/01/2007 a 07/11/2017
 SECRETARIA DE ESTADO DE SAÚDE DO RIO DE JANEIRO SUBSECRETARIA DE VIGILÂNCIA EM SAÚDE SUPERINTENDÊNCIA DE VIGILÂNCIA EPIDEMIOLÓGICA E AMBIENTAL COORDENAÇÃO DE VIGILÂNCIA EPIDEMIOLÓGICA GERÊNCIA DE DOENÇAS
SECRETARIA DE ESTADO DE SAÚDE DO RIO DE JANEIRO SUBSECRETARIA DE VIGILÂNCIA EM SAÚDE SUPERINTENDÊNCIA DE VIGILÂNCIA EPIDEMIOLÓGICA E AMBIENTAL COORDENAÇÃO DE VIGILÂNCIA EPIDEMIOLÓGICA GERÊNCIA DE DOENÇAS
Unir forças para não expandir
 Alerta à População A leishmaniose visceral (LV) é uma doença grave, causada por um parasito transmitido para pessoas e cães por meio da picada de um inseto (vetor) muito pequeno, conhecido como mosquito
Alerta à População A leishmaniose visceral (LV) é uma doença grave, causada por um parasito transmitido para pessoas e cães por meio da picada de um inseto (vetor) muito pequeno, conhecido como mosquito
ALERTA EPIDEMIOLÓGICO
 ALERTA EPIDEMIOLÓGICO Gerência de Vigilância Epidemiológica - Diretoria de Vigilância em Saúde SMS Florianópolis, SC 13 de dezembro de 2017 Leishmaniose Visceral Humana Em 08/12/2017 foi confirmado mais
ALERTA EPIDEMIOLÓGICO Gerência de Vigilância Epidemiológica - Diretoria de Vigilância em Saúde SMS Florianópolis, SC 13 de dezembro de 2017 Leishmaniose Visceral Humana Em 08/12/2017 foi confirmado mais
Aula Prática II: Protozoários - Família Trypanosomatidae.
 UFF Universidade Federal Fluminense. PUNF - Polo Universitário de Nova Friburgo. Curso de Biomedicina. Disciplina: Parasitologia Professora: Aline Caseca Volotão. Monitora: Lorraine Herdy Heggendornn.
UFF Universidade Federal Fluminense. PUNF - Polo Universitário de Nova Friburgo. Curso de Biomedicina. Disciplina: Parasitologia Professora: Aline Caseca Volotão. Monitora: Lorraine Herdy Heggendornn.
14/06/12. Esta palestra não poderá ser reproduzida sem a referência do autor
 14/06/12 Esta palestra não poderá ser reproduzida sem a referência do autor ESTA PALESTRA NÃO PODERÁ SER REPRODUZIDA SEM A REFÊNCIA DO AUTOR. LEISHMANIOSE VISCERAL TRANSMISSÃO EM BANCO DE SANGUE Dra. Margarida
14/06/12 Esta palestra não poderá ser reproduzida sem a referência do autor ESTA PALESTRA NÃO PODERÁ SER REPRODUZIDA SEM A REFÊNCIA DO AUTOR. LEISHMANIOSE VISCERAL TRANSMISSÃO EM BANCO DE SANGUE Dra. Margarida
Disciplina de Parasitologia
 Disciplina de Parasitologia Curso de Medicina 2018 Tema: Leishmanioses Profa. Dra. Juliana Quero Reimão Generalidades O que é Leishmaniose? Doença infecciosa, de manifestação cutânea ou visceral, causada
Disciplina de Parasitologia Curso de Medicina 2018 Tema: Leishmanioses Profa. Dra. Juliana Quero Reimão Generalidades O que é Leishmaniose? Doença infecciosa, de manifestação cutânea ou visceral, causada
Instituto de Pesquisas em Patologias Tropicais IPEPATRO/FIOCRUZ. Ferida Brava (Leishmaniose): Conheça e Aprenda a se proteger
 Instituto de Pesquisas em Patologias Tropicais IPEPATRO/FIOCRUZ Ferida Brava (Leishmaniose): Conheça e Aprenda a se proteger Janeiro de 2013 O que é? É uma doença infecciosa, não contagiosa, que afeta
Instituto de Pesquisas em Patologias Tropicais IPEPATRO/FIOCRUZ Ferida Brava (Leishmaniose): Conheça e Aprenda a se proteger Janeiro de 2013 O que é? É uma doença infecciosa, não contagiosa, que afeta
11 a 14 de dezembro de 2012 Campus de Palmas
 SENSIBILIDADE E ESPECIFICIDADE DA IMUNOFLUORESCÊNCIA INDIRETA UTILIZANDO CEPA DE LEISHMANIA SPP. ISOLADA DE CÃO DA CIDADE DE ARAGUAÍNA-TO NO DIAGNÓSTICO DA LEISHMANIOSE VISCERAL CANINA. Emerson Danillo
SENSIBILIDADE E ESPECIFICIDADE DA IMUNOFLUORESCÊNCIA INDIRETA UTILIZANDO CEPA DE LEISHMANIA SPP. ISOLADA DE CÃO DA CIDADE DE ARAGUAÍNA-TO NO DIAGNÓSTICO DA LEISHMANIOSE VISCERAL CANINA. Emerson Danillo
LEISHMANIOSE CANINA Prof. Rafael Fighera
 LEISHMANIOSE CANINA Prof. Rafael Fighera Serviço de Consultoria Diagnóstica Veterinária Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria Leishmaniose
LEISHMANIOSE CANINA Prof. Rafael Fighera Serviço de Consultoria Diagnóstica Veterinária Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria Leishmaniose
REGINA LUNARDI ROCHA. Departamento de Pediatria FM/UFMG Serviço DIP-HC/UFMG
 REGINA LUNARDI ROCHA Departamento de Pediatria FM/UFMG Serviço DIP-HC/UFMG LEISHMANIOSE VISIERAL Antropozoonose de áreas tropicais Febre, hepatoesplenomegalia, palidez, emagrecimento Hipoalbuminemia, hipergamaglobulinemia,
REGINA LUNARDI ROCHA Departamento de Pediatria FM/UFMG Serviço DIP-HC/UFMG LEISHMANIOSE VISIERAL Antropozoonose de áreas tropicais Febre, hepatoesplenomegalia, palidez, emagrecimento Hipoalbuminemia, hipergamaglobulinemia,
LEISHMANIOSE: Uma Grande Endemia. Beatriz S Stolf Depto de Parasitologia ICB II- USP
 LEISHMANIOSE: Uma Grande Endemia Beatriz S Stolf Depto de Parasitologia ICB II- USP Endêmica em 98 países ~12 milhões de pessoas infectadas 2 milhões de casos novos / ano 350 milhões de pessoas ameaçadas
LEISHMANIOSE: Uma Grande Endemia Beatriz S Stolf Depto de Parasitologia ICB II- USP Endêmica em 98 países ~12 milhões de pessoas infectadas 2 milhões de casos novos / ano 350 milhões de pessoas ameaçadas
Classificação ALGAS PROTOZOÁRIOS
 Reino Protista Classificação PROTOZOÁRIOS ALGAS Antigamente, estes organismos eram agrupados nos reinos Animal e Vegetal, respectivamente. Hoje em dia, sabemos que fazem parte dos protistas devido a características
Reino Protista Classificação PROTOZOÁRIOS ALGAS Antigamente, estes organismos eram agrupados nos reinos Animal e Vegetal, respectivamente. Hoje em dia, sabemos que fazem parte dos protistas devido a características
Leishmaniose Tegumentar Americana no Estado de São Paulo: Situação Epidemiológica
 Leishmaniose Tegumentar Americana no Estado de São Paulo: Situação Epidemiológica 2001 2002 Vera Lucia Fonseca de Camargo-Neves¹ e Mitie Tada L.R.F Brasil² No Estado de São Paulo a Leishmaniose Tegumentar
Leishmaniose Tegumentar Americana no Estado de São Paulo: Situação Epidemiológica 2001 2002 Vera Lucia Fonseca de Camargo-Neves¹ e Mitie Tada L.R.F Brasil² No Estado de São Paulo a Leishmaniose Tegumentar
Nota Técnica nº 13 LEISHIMANIOSE VICERAL
 CENTRO DE INFORMAÇÕES ESTRATÉGICAS E RESPOSTA EM VIGILÂNCIA EM SAÚDE Nota Técnica nº 13 LEISHIMANIOSE VICERAL Centro de Informações Estratégicas e Resposta em Vigilância em Saúde Departamento de Epidemiologia/
CENTRO DE INFORMAÇÕES ESTRATÉGICAS E RESPOSTA EM VIGILÂNCIA EM SAÚDE Nota Técnica nº 13 LEISHIMANIOSE VICERAL Centro de Informações Estratégicas e Resposta em Vigilância em Saúde Departamento de Epidemiologia/
SITUAÇÃO EPIDEMIOLÓGICA DA LEISHMANIOSE VISCERAL NA PARAÍBA: UMA QUESTÃO DE SAÚDE PÚBLICA
 SITUAÇÃO EPIDEMIOLÓGICA DA LEISHMANIOSE VISCERAL NA PARAÍBA: UMA QUESTÃO DE SAÚDE PÚBLICA EPIDEMIOLOGICAL SITUATION OF VISCERAL LEISHMANIASIS IN PARAÍBA: A PUBLIC HEALTH QUESTION Suzanna Cavalcante LINS
SITUAÇÃO EPIDEMIOLÓGICA DA LEISHMANIOSE VISCERAL NA PARAÍBA: UMA QUESTÃO DE SAÚDE PÚBLICA EPIDEMIOLOGICAL SITUATION OF VISCERAL LEISHMANIASIS IN PARAÍBA: A PUBLIC HEALTH QUESTION Suzanna Cavalcante LINS
SECRETARIA DE ESTADO DE SAÚDE - DF HOSPITAL REGIONAL DA ASA SUL PROGRAMA DE RESIDÊNCIA MÉDICA M CALAZAR GERMANO DA SILVA DE SOUZA R 2
 SECRETARIA DE ESTADO DE SAÚDE - DF HOSPITAL REGIONAL DA ASA SUL PROGRAMA DE RESIDÊNCIA MÉDICA M EM PEDIATRIA CALAZAR GERMANO DA SILVA DE SOUZA R 2 www.paulomargotto.com.br CALAZAR DEFINIÇÃO ÃO: Zoonose
SECRETARIA DE ESTADO DE SAÚDE - DF HOSPITAL REGIONAL DA ASA SUL PROGRAMA DE RESIDÊNCIA MÉDICA M EM PEDIATRIA CALAZAR GERMANO DA SILVA DE SOUZA R 2 www.paulomargotto.com.br CALAZAR DEFINIÇÃO ÃO: Zoonose
Vestibular1 A melhor ajuda ao vestibulando na Internet Acesse Agora! Leishmaniose
 Leishmaniose Sob a denominação genérica de leishmaniose, a ciência médica descreve um grupo de doenças infecciosas causadas por protozoários do gênero Leishmania, transmitidos ao homem por mosquitos do
Leishmaniose Sob a denominação genérica de leishmaniose, a ciência médica descreve um grupo de doenças infecciosas causadas por protozoários do gênero Leishmania, transmitidos ao homem por mosquitos do
LEISHMANIOSE HUMANA E CANINA
 LEISHMANIOSE HUMANA E CANINA O QUE É LEISHMANIOSE? É uma doença CAUSADA por protozoários do gênero Leishmania No Brasil existem atualmente seis espécies de protozoários responsáveis por causar doença humana.
LEISHMANIOSE HUMANA E CANINA O QUE É LEISHMANIOSE? É uma doença CAUSADA por protozoários do gênero Leishmania No Brasil existem atualmente seis espécies de protozoários responsáveis por causar doença humana.
MALÁRIA. Agentes etiológicos (Protozoários) Plasmodium vivax Plasmodium falciparum Plasmodium malariae Plasmodium ovale
 MALÁRIA Agentes etiológicos (Protozoários) Plasmodium vivax Plasmodium falciparum Plasmodium malariae Plasmodium ovale Vetores (Insetos) Culicidae gênero Anopheles A. (Nyssorhincus) darlingi A. (N) aquasalis
MALÁRIA Agentes etiológicos (Protozoários) Plasmodium vivax Plasmodium falciparum Plasmodium malariae Plasmodium ovale Vetores (Insetos) Culicidae gênero Anopheles A. (Nyssorhincus) darlingi A. (N) aquasalis
PROJETO TURMINHA DA SAÚDE. Ronaldo Kroeff Daghlawi. São Luís-MA
 PROJETO TURMINHA DA SAÚDE Ronaldo Kroeff Daghlawi São Luís-MA Janeiro/2014 PROJETO TURMINHA DA SAÚDE Estamos lançando em todo o Maranhão a Revista Turminha da Saúde na qual serão abordados variados temas
PROJETO TURMINHA DA SAÚDE Ronaldo Kroeff Daghlawi São Luís-MA Janeiro/2014 PROJETO TURMINHA DA SAÚDE Estamos lançando em todo o Maranhão a Revista Turminha da Saúde na qual serão abordados variados temas
MORTALIDADE E LETALIDADE POR LEISHMANIOSE VISCERAL NA REGIÃO NORDESTE DO BRASIL
 MORTALIDADE E LETALIDADE POR LEISHMANIOSE VISCERAL NA REGIÃO NORDESTE DO BRASIL Allan Batista Silva 1, Ana Carolina da Silva Monteiro 2, Waldner Gomes Barbosa Filho 3, Mirian Marques Vieira 4, Caliandra
MORTALIDADE E LETALIDADE POR LEISHMANIOSE VISCERAL NA REGIÃO NORDESTE DO BRASIL Allan Batista Silva 1, Ana Carolina da Silva Monteiro 2, Waldner Gomes Barbosa Filho 3, Mirian Marques Vieira 4, Caliandra
LEISHMANIOSE VISCERAL E TEGUMENTAR AMERICANA VISCERAL AND CUTANEOUS LEISHMANIASIS
 40 LEISHMANIOSE VISCERAL E TEGUMENTAR AMERICANA VISCERAL AND CUTANEOUS LEISHMANIASIS Gustavo Pereira da Rocha¹ Tatiane Ferreira Petroni¹ RESUMO: A leishmaniose é causada por parasitas do gênero Leishmania
40 LEISHMANIOSE VISCERAL E TEGUMENTAR AMERICANA VISCERAL AND CUTANEOUS LEISHMANIASIS Gustavo Pereira da Rocha¹ Tatiane Ferreira Petroni¹ RESUMO: A leishmaniose é causada por parasitas do gênero Leishmania
Febre Amarela: O que você precisa saber sobre a doença
 Febre Amarela: O que você precisa saber sobre a doença A febre amarela vem preocupando a sociedade brasileira. O número de casos no Brasil é o maior desde 1980. A OMS (Organização Mundial de Saúde) incluiu
Febre Amarela: O que você precisa saber sobre a doença A febre amarela vem preocupando a sociedade brasileira. O número de casos no Brasil é o maior desde 1980. A OMS (Organização Mundial de Saúde) incluiu
CAPACITAÇÃO AGENTE COMUNITÁRIOS
 CAPACITAÇÃO AGENTE COMUNITÁRIOS Prefeitura Municipal de Corumbá Paulo Roberto Duarte Secretária Municipal de Saúde Dinaci Vieira Ranzi Gerência de Vigilância em Saúde Viviane Campos Ametlla Coordenação
CAPACITAÇÃO AGENTE COMUNITÁRIOS Prefeitura Municipal de Corumbá Paulo Roberto Duarte Secretária Municipal de Saúde Dinaci Vieira Ranzi Gerência de Vigilância em Saúde Viviane Campos Ametlla Coordenação
Leishmaniose Visceral
 Leishmaniose Visceral Introdução As Leishmanioses são protozooses de grande importância em nosso meio Causadas por protozoários do gênero Leishmania São zoonoses e que afetam o homem acidentalmente Trasmitidas
Leishmaniose Visceral Introdução As Leishmanioses são protozooses de grande importância em nosso meio Causadas por protozoários do gênero Leishmania São zoonoses e que afetam o homem acidentalmente Trasmitidas
DIAGNÓSTICOS SOROLÓGICO NAS INFECÇÕES BACTERIANAS. Sífilis
 DIAGNÓSTICOS SOROLÓGICO NAS INFECÇÕES BACTERIANAS Sífilis Sífilis Agente Etiológico Doença crônica sistêmica Família Spirochaetaceae Espiroqueta: Treponema pallidum, sub espécie pallidum Motilidade Característica:
DIAGNÓSTICOS SOROLÓGICO NAS INFECÇÕES BACTERIANAS Sífilis Sífilis Agente Etiológico Doença crônica sistêmica Família Spirochaetaceae Espiroqueta: Treponema pallidum, sub espécie pallidum Motilidade Característica:
MÉTODOS DE DIAGNÓSTICO DA LEISHMANIOSE VISCERAL CANINA
 MÉTODOS DE DIAGNÓSTICO DA LEISHMANIOSE VISCERAL CANINA DOTTA, Silvia Cristina Nardy Discente do Curso de Medicina Veterinária da FAMED Garça LOT, Rômulo Francis Estangari ZAPPA, Vanessa Docentes da Associação
MÉTODOS DE DIAGNÓSTICO DA LEISHMANIOSE VISCERAL CANINA DOTTA, Silvia Cristina Nardy Discente do Curso de Medicina Veterinária da FAMED Garça LOT, Rômulo Francis Estangari ZAPPA, Vanessa Docentes da Associação
RESPONSABILIDADE NA CONDUTA TERAPÊUTICA EM CASOS DE LVC. Dra Liliane Carneiro Diretora do CENP/IEC/MS CRMV/PA Nº 1715
 RESPONSABILIDADE NA CONDUTA TERAPÊUTICA EM CASOS DE LVC Dra Liliane Carneiro Diretora do CENP/IEC/MS CRMV/PA Nº 1715 A leishmaniose visceral canina (LVC) é uma doença infecciosa provocada pelo protozoário
RESPONSABILIDADE NA CONDUTA TERAPÊUTICA EM CASOS DE LVC Dra Liliane Carneiro Diretora do CENP/IEC/MS CRMV/PA Nº 1715 A leishmaniose visceral canina (LVC) é uma doença infecciosa provocada pelo protozoário
1º EM BIOLOGIA PROFESSOR JOÃO C5, 8 H19, 29, 30 PROTOZOOSES. Biologia Professor João
 1º EM BIOLOGIA PROFESSOR JOÃO PROTOZOOSES Biologia Professor João DOENÇA DE CHAGAS Sinônimo: Tripanossomíase americana Agente Etiológico: Trypanosoma cruzi (protozoário flagelado) Vetor (transmissor):
1º EM BIOLOGIA PROFESSOR JOÃO PROTOZOOSES Biologia Professor João DOENÇA DE CHAGAS Sinônimo: Tripanossomíase americana Agente Etiológico: Trypanosoma cruzi (protozoário flagelado) Vetor (transmissor):
CARACTERÍSTICAS EPIDEMIOLÓGICAS DA LEISHMANIOSE TEGUMENTAR AMERICANA NA PARAÍBA
 CARACTERÍSTICAS EPIDEMIOLÓGICAS DA LEISHMANIOSE TEGUMENTAR AMERICANA NA PARAÍBA Allan Batista Silva 1, Ana Carolina da Silva Monteiro 2, Waldner Gomes Barbosa Filho 3, Caliandra Maria Bezerra Luna Lima
CARACTERÍSTICAS EPIDEMIOLÓGICAS DA LEISHMANIOSE TEGUMENTAR AMERICANA NA PARAÍBA Allan Batista Silva 1, Ana Carolina da Silva Monteiro 2, Waldner Gomes Barbosa Filho 3, Caliandra Maria Bezerra Luna Lima
ARTIGO ORIGINAL. Resumo INTRODUÇÃO. Waneska Alexandra Alves 1. anteriormente de caráter rural, se expandiu para zonas urbanas,
 ARTIGO ORIGINAL Waneska Alexandra Alves 1 Resumo : INTRODUÇÃO A Leishmaniose Visceral (LV) é uma doença sistêmica que afeta tanto animais quanto o homem, sendo o cão o protozoários heteroxênicos e intracelulares
ARTIGO ORIGINAL Waneska Alexandra Alves 1 Resumo : INTRODUÇÃO A Leishmaniose Visceral (LV) é uma doença sistêmica que afeta tanto animais quanto o homem, sendo o cão o protozoários heteroxênicos e intracelulares
Febre maculosa febre carrapato
 A febre maculosa, também conhecida como febre do carrapato é uma doença infecciosa aguda causada pela bactéria Rickettsia rickettsii, que é intracelular obrigatória e tem como vetor biológico o carrapato
A febre maculosa, também conhecida como febre do carrapato é uma doença infecciosa aguda causada pela bactéria Rickettsia rickettsii, que é intracelular obrigatória e tem como vetor biológico o carrapato
Interdisciplinar: Revista Eletrônica da UNIVAR X Ano de publicação: 2014 N.:11 Vol.:1 Págs.
 Interdisciplinar: Revista Eletrônica da UNIVAR http://revista.univar.edu.br 1984-431X Ano de publicação: 2014 N.:11 Vol.:1 Págs.:71-76 ISSN PREVALÊNCIA DE LEISHMANIOSE TEGUMENTAR AMERICANA NO MUNICÍPIO
Interdisciplinar: Revista Eletrônica da UNIVAR http://revista.univar.edu.br 1984-431X Ano de publicação: 2014 N.:11 Vol.:1 Págs.:71-76 ISSN PREVALÊNCIA DE LEISHMANIOSE TEGUMENTAR AMERICANA NO MUNICÍPIO
Profa. Carolina G. P. Beyrodt
 Profa. Carolina G. P. Beyrodt Agente etiológico: Toxoplasma gondii (Protozoário coccídeo do Filo Apicomplexa) Histórico Isolado em 1908 de um roedor do deserto: Ctenodactylus gondii 1923 descrição do primeiro
Profa. Carolina G. P. Beyrodt Agente etiológico: Toxoplasma gondii (Protozoário coccídeo do Filo Apicomplexa) Histórico Isolado em 1908 de um roedor do deserto: Ctenodactylus gondii 1923 descrição do primeiro
Vigilância da Leishmaniose Visceral. (calazar, esplenomegalia tropical, febre Dundun)
 Vigilância da Leishmaniose Visceral (calazar, esplenomegalia tropical, febre Dundun) LEISHMANIOSE VISCERAL Doença infecciosa causada por Leishmania infantum e transmitida pela picada de fêmeas de Lutzomyia
Vigilância da Leishmaniose Visceral (calazar, esplenomegalia tropical, febre Dundun) LEISHMANIOSE VISCERAL Doença infecciosa causada por Leishmania infantum e transmitida pela picada de fêmeas de Lutzomyia
LEISHMANIOSE TEGUMENTAR AMERICANA HUMANA NOS MUNICÍPIOS DE CAMPINÁPOLIS, GENERAL CARNEIRO, NOVA XAVANTINA E NOVO SÃO JOAQUIM EM MATO GROSSO
 LEISHMANIOSE TEGUMENTAR AMERICANA HUMANA NOS MUNICÍPIOS DE CAMPINÁPOLIS, GENERAL CARNEIRO, NOVA XAVANTINA E NOVO SÃO JOAQUIM EM MATO GROSSO Jordana Belos dos SANTOS 1, André Luiz Fernandes da SILVA 1,
LEISHMANIOSE TEGUMENTAR AMERICANA HUMANA NOS MUNICÍPIOS DE CAMPINÁPOLIS, GENERAL CARNEIRO, NOVA XAVANTINA E NOVO SÃO JOAQUIM EM MATO GROSSO Jordana Belos dos SANTOS 1, André Luiz Fernandes da SILVA 1,
O REINO PROTISTA II. Biodiversidade Prof. Thafarel
 O REINO PROTISTA II Biodiversidade Prof. Thafarel Introdução: Na aula anterior, vimos um pouco da estrutura e fisiologia dos chamados protozoa, ou, em outras palavras, dos protozoários que apresentam mobilidade.
O REINO PROTISTA II Biodiversidade Prof. Thafarel Introdução: Na aula anterior, vimos um pouco da estrutura e fisiologia dos chamados protozoa, ou, em outras palavras, dos protozoários que apresentam mobilidade.
Doenças causadas por vírus. Professora: Elyka Fernanda
 Doenças causadas por vírus Professora: Elyka Fernanda Herpes labial Transmissão Causador: HSV 1 (vírus do herpes simples tipo 1) Sintomas A infecção inicial pode não causar sintomas ou surgimento de bolhas
Doenças causadas por vírus Professora: Elyka Fernanda Herpes labial Transmissão Causador: HSV 1 (vírus do herpes simples tipo 1) Sintomas A infecção inicial pode não causar sintomas ou surgimento de bolhas
LEISHMANIOSE VISCERAL REVISÃO DE LITERATURA VISCERAL LEISHMANIASIS REVIEW
 LEISHMANIOSE VISCERAL REVISÃO DE LITERATURA VISCERAL LEISHMANIASIS REVIEW BRANDÃO, Talita Galvão Evaristo Acadêmica do curso de Medicina Veterinária da Faculdade de Medicina Veterinária e Zootecnia de
LEISHMANIOSE VISCERAL REVISÃO DE LITERATURA VISCERAL LEISHMANIASIS REVIEW BRANDÃO, Talita Galvão Evaristo Acadêmica do curso de Medicina Veterinária da Faculdade de Medicina Veterinária e Zootecnia de
Palavras-chave: Diagnostico molecular; Mosquito-palha; Epidemiologia; Leishmania spp.
 IMPLEMENTAÇÃO DE REAÇÃO EM CADEIA DA POLIMERASE EM TEMPO REAL PARA DETECÇÃO E QUANTIFICAÇÃO DE LEISHMANIOSE VISCERAL Resumo Vinicius Proença da Silveira 1 Patrícia de Freitas Salla 2 Nilo Ikuta 3 Vagner
IMPLEMENTAÇÃO DE REAÇÃO EM CADEIA DA POLIMERASE EM TEMPO REAL PARA DETECÇÃO E QUANTIFICAÇÃO DE LEISHMANIOSE VISCERAL Resumo Vinicius Proença da Silveira 1 Patrícia de Freitas Salla 2 Nilo Ikuta 3 Vagner
INFORME TÉCNICO PARA MÉDICOS VETERINÁRIOS LEISHMANIOSE VISCERAL AMERICANA
 PREFEITURA MUNICIPAL DE CAMPINAS SECRETARIA MUNICIPAL DE SAÚDE COORDENADORIA DE VIGILÂNCIA EM SAÚDE Avenida Anchieta, 200 11º andar Centro CEP: 13015-904 Tel. (19) 2116-0187 / 0286 E-mail: covisa@campinas.sp.gov.br
PREFEITURA MUNICIPAL DE CAMPINAS SECRETARIA MUNICIPAL DE SAÚDE COORDENADORIA DE VIGILÂNCIA EM SAÚDE Avenida Anchieta, 200 11º andar Centro CEP: 13015-904 Tel. (19) 2116-0187 / 0286 E-mail: covisa@campinas.sp.gov.br
LEISHMANIOSE VISCERAL EM ANIMAIS E HUMANOS
 LEISHMANIOSE VISCERAL EM ANIMAIS E HUMANOS Mayara Barbosa Santiago Graduanda em Medicina Veterinária, Faculdades Integradas de Três Lagoas - FITL/AEMS Íria Maria Abel Santos Graduanda em Medicina Veterinária,
LEISHMANIOSE VISCERAL EM ANIMAIS E HUMANOS Mayara Barbosa Santiago Graduanda em Medicina Veterinária, Faculdades Integradas de Três Lagoas - FITL/AEMS Íria Maria Abel Santos Graduanda em Medicina Veterinária,
Febre Amarela Informações (18/01/2018)
 Febre Amarela Informações (18/01/2018) Segundo o Ministério da Saúde, O Brasil enfrentou em 2016/2017 um grande surto de febre amarela, envolvendo principalmente os estados da região Sudeste, com destaque
Febre Amarela Informações (18/01/2018) Segundo o Ministério da Saúde, O Brasil enfrentou em 2016/2017 um grande surto de febre amarela, envolvendo principalmente os estados da região Sudeste, com destaque
Toxoplasmose. Zoonose causada por protozoário Toxoplasma gondii. Único agente causal da toxoplasmose. Distribuição geográfica: Mundial
 Toxoplasmose Zoonose causada por protozoário Toxoplasma gondii Único agente causal da toxoplasmose Distribuição geográfica: Mundial Hospedeiros: a) Hospedeiros finais ou definitivos: - felideos (gato doméstico
Toxoplasmose Zoonose causada por protozoário Toxoplasma gondii Único agente causal da toxoplasmose Distribuição geográfica: Mundial Hospedeiros: a) Hospedeiros finais ou definitivos: - felideos (gato doméstico
COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA
 COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA INFORME Nº 33/2017 MONITORAMENTO DOS CASOS E ÓBITOS DE FEBRE AMARELA NO BRASIL INÍCIO DO EVENTO: Dezembro de 2016
COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA INFORME Nº 33/2017 MONITORAMENTO DOS CASOS E ÓBITOS DE FEBRE AMARELA NO BRASIL INÍCIO DO EVENTO: Dezembro de 2016
RESUMOS DE PROJETOS
 181 RESUMOS DE PROJETOS... 182 RESUMOS DE PROJETOS 182 ATIVIDADE ANTIPARASITÁRIA DE BYRSONIMA INTERMEDIA SOBRE FORMAS EPIMASTIGOTAS DE TRYPANOSOMA CRUZI... 183 EFEITO IN VITRO DE INIBIDORES DE PROTEASES
181 RESUMOS DE PROJETOS... 182 RESUMOS DE PROJETOS 182 ATIVIDADE ANTIPARASITÁRIA DE BYRSONIMA INTERMEDIA SOBRE FORMAS EPIMASTIGOTAS DE TRYPANOSOMA CRUZI... 183 EFEITO IN VITRO DE INIBIDORES DE PROTEASES
LEISHMANIOSES Dra. Cristiana de Melo Trinconi Tronco
 LEISHMANIOSES Dra. Cristiana de Melo Trinconi Tronco Laboratório de Leishmanioses Instituto de Ciências Biomédicas II Universidade de São Paulo USP Leishmanioses Leishmanioses - Ciclo de vida - Leishmanioses
LEISHMANIOSES Dra. Cristiana de Melo Trinconi Tronco Laboratório de Leishmanioses Instituto de Ciências Biomédicas II Universidade de São Paulo USP Leishmanioses Leishmanioses - Ciclo de vida - Leishmanioses
PROGRAMA DE PG EM BIOLOGIA EXPERIMENTAL - PGBIOEXP
 QUESTÕES ESPECÍFICAS Questão 5 Observou-se recentemente, nos anos de 2017 e 2018, uns dos eventos epidêmicos de febre amarela mais graves no Brasil, considerando-se a série histórica de 1980-2018. O vírus
QUESTÕES ESPECÍFICAS Questão 5 Observou-se recentemente, nos anos de 2017 e 2018, uns dos eventos epidêmicos de febre amarela mais graves no Brasil, considerando-se a série histórica de 1980-2018. O vírus
COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA
 COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA INFORME Nº 34/2017 MONITORAMENTO DOS CASOS E ÓBITOS DE FEBRE AMARELA NO BRASIL INÍCIO DO EVENTO: Dezembro de 2016
COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA INFORME Nº 34/2017 MONITORAMENTO DOS CASOS E ÓBITOS DE FEBRE AMARELA NO BRASIL INÍCIO DO EVENTO: Dezembro de 2016
Diagnóstico Laboratorial de Infecções Virais. Profa. Claudia Vitral
 Diagnóstico Laboratorial de Infecções Virais Profa. Claudia Vitral Importância do diagnóstico laboratorial virológico Determinar a etiologia e acompanhar o curso de uma infecção viral Avaliar a eficácia
Diagnóstico Laboratorial de Infecções Virais Profa. Claudia Vitral Importância do diagnóstico laboratorial virológico Determinar a etiologia e acompanhar o curso de uma infecção viral Avaliar a eficácia
UNIVERSIDADE FEDERAL DE MINAS GERAIS CURSO DE ESPECIALIZAÇÃO EM ATENÇÃO BÁSICA EM SAÚDE DA FAMÍLIA
 UNIVERSIDADE FEDERAL DE MINAS GERAIS CURSO DE ESPECIALIZAÇÃO EM ATENÇÃO BÁSICA EM SAÚDE DA FAMÍLIA GLEICIENE CORREIA DE OLIVEIRA PROPOSTA DE INTERVENÇÂO EM LEISHMANIOSE TEGUMENTAR NO MUNICÍPIO DE PEDRA
UNIVERSIDADE FEDERAL DE MINAS GERAIS CURSO DE ESPECIALIZAÇÃO EM ATENÇÃO BÁSICA EM SAÚDE DA FAMÍLIA GLEICIENE CORREIA DE OLIVEIRA PROPOSTA DE INTERVENÇÂO EM LEISHMANIOSE TEGUMENTAR NO MUNICÍPIO DE PEDRA
Cerca de 6000 espécies conhecidas - ~10000 são parasitas. Eucariotos unicelulares
 Cerca de 6000 espécies conhecidas - ~10000 são parasitas. Eucariotos unicelulares Apresentam variadas formas, processo de alimentação, reprodução e locomoção De acordo com a estrutura de locomoção Sarcodina
Cerca de 6000 espécies conhecidas - ~10000 são parasitas. Eucariotos unicelulares Apresentam variadas formas, processo de alimentação, reprodução e locomoção De acordo com a estrutura de locomoção Sarcodina
Vigilância Epidemiológica das Doenças Negligenciadas e das Doenças relacionadas à pobreza 2017
 Vigilância Epidemiológica das Doenças Negligenciadas e das Doenças relacionadas à pobreza 2017 OMS doenças tropicais negligenciadas Bouba Doença de Chagas Dengue Dracunculíase Equinococose (Hidatidose)
Vigilância Epidemiológica das Doenças Negligenciadas e das Doenças relacionadas à pobreza 2017 OMS doenças tropicais negligenciadas Bouba Doença de Chagas Dengue Dracunculíase Equinococose (Hidatidose)
Classe Nematoda. Ascaridíase
 Classe Nematoda - Os parasitos pertencentes a essa classe possuem características em comum, como: - São pseudocelomados; - Possuem sistema digestório completo; - Alguns são geo-helmintos (verdadeiros),
Classe Nematoda - Os parasitos pertencentes a essa classe possuem características em comum, como: - São pseudocelomados; - Possuem sistema digestório completo; - Alguns são geo-helmintos (verdadeiros),
Este estudo teve o objetivo de conhecer aspectos epidemiológicos dos casos de leishmaniose visceral notificados em Sobral,
 PERFIL EPIDEMIOLÓGICO DOS CASOS DE LEISHMANIOSE VISCERAL EM SOBRAL, CEARÁ NO PERÍODO DE 2001 A 2010 * EPIDEMIOLOGICAL PROFILE OF CASES OF VISCERAL LEISHMANIASIS IN SOBRAL, CEARÁ THE PERIOD 2001 TO 2010
PERFIL EPIDEMIOLÓGICO DOS CASOS DE LEISHMANIOSE VISCERAL EM SOBRAL, CEARÁ NO PERÍODO DE 2001 A 2010 * EPIDEMIOLOGICAL PROFILE OF CASES OF VISCERAL LEISHMANIASIS IN SOBRAL, CEARÁ THE PERIOD 2001 TO 2010
PERFIL EPIDEMIOLÓGICO DA LEISHMANIOSE TEGUMENTAR AMERICANA NO MUNICÍPIO DE CACOAL-RO DO ANO DE 2007 A 2015
 PERFIL EPIDEMIOLÓGICO DA LEISHMANIOSE TEGUMENTAR AMERICANA NO MUNICÍPIO DE CACOAL-RO DO ANO DE 2007 A 2015 EPIDEMIOLOGICAL PROFILE OF AMERICAN TEGUMENTARY LEISHMANIASIS IN CACOAL-RO FROMYEAR 2007 TO 2015
PERFIL EPIDEMIOLÓGICO DA LEISHMANIOSE TEGUMENTAR AMERICANA NO MUNICÍPIO DE CACOAL-RO DO ANO DE 2007 A 2015 EPIDEMIOLOGICAL PROFILE OF AMERICAN TEGUMENTARY LEISHMANIASIS IN CACOAL-RO FROMYEAR 2007 TO 2015
HIMENOLEPÍASE RA:
 HIMENOLEPÍASE Grupo 12 Nomes: Amanda Chelala Manuela de Queiroz Belardi Bianca Zorge Vasconcelos Bruna Moraes Camargo Fernanda Sayuri Watanabe Nakakogue RA: 1801038 1801163 1801165 1801170 1801171 CARACTERÍSTICAS
HIMENOLEPÍASE Grupo 12 Nomes: Amanda Chelala Manuela de Queiroz Belardi Bianca Zorge Vasconcelos Bruna Moraes Camargo Fernanda Sayuri Watanabe Nakakogue RA: 1801038 1801163 1801165 1801170 1801171 CARACTERÍSTICAS
ASSOCIAÇÃO DA CARGA PARASITÁRIA NO EXAME CITOLÓGICO DE PUNÇÃO BIÓPSIA ASPIRATIVA DE LINFONODO COM O PERFIL CLÍNICO DE CÃES COM LEISHMANIOSE VISCERAL.
 ASSOCIAÇÃO DA CARGA PARASITÁRIA NO EXAME CITOLÓGICO DE PUNÇÃO BIÓPSIA ASPIRATIVA DE LINFONODO COM O PERFIL CLÍNICO DE CÃES COM LEISHMANIOSE VISCERAL. WALESSON DE ARAUJO ABREU 1 ; HELCILEIA DIAS SANTOS
ASSOCIAÇÃO DA CARGA PARASITÁRIA NO EXAME CITOLÓGICO DE PUNÇÃO BIÓPSIA ASPIRATIVA DE LINFONODO COM O PERFIL CLÍNICO DE CÃES COM LEISHMANIOSE VISCERAL. WALESSON DE ARAUJO ABREU 1 ; HELCILEIA DIAS SANTOS
COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA
 COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA INFORME Nº 35/2017 MONITORAMENTO DOS CASOS E ÓBITOS DE FEBRE AMARELA NO BRASIL INÍCIO DO EVENTO: Dezembro de 2016
COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA INFORME Nº 35/2017 MONITORAMENTO DOS CASOS E ÓBITOS DE FEBRE AMARELA NO BRASIL INÍCIO DO EVENTO: Dezembro de 2016
LEISHMANIOSE VISCERAL
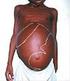 LEISHMANIOSE VISCERAL BLAU, Diego Dias OLIVEIRA, Karla Henrique de Acadêmicos do Curso de Medicina Veterinária FAIT Itapeva/SP NAKAGHI, Andréa C. Higa Prof. Drª. Fait Itapeva/SP Faculdade de Ciências Sociais
LEISHMANIOSE VISCERAL BLAU, Diego Dias OLIVEIRA, Karla Henrique de Acadêmicos do Curso de Medicina Veterinária FAIT Itapeva/SP NAKAGHI, Andréa C. Higa Prof. Drª. Fait Itapeva/SP Faculdade de Ciências Sociais
INFECÇÃO SIMULTÂNEA POR Leishmania chagasi E Ehrlichia canis EM CÃES NATURALMENTE INFECTADOS EM SÃO LUÍS, MARANHÃO, BRASIL
 INFECÇÃO SIMULTÂNEA POR Leishmania chagasi E Ehrlichia canis EM CÃES NATURALMENTE INFECTADOS EM SÃO LUÍS, MARANHÃO, BRASIL SIMULTANEOUS INFECTION BY Leishmania chagasi AND Ehrlichia canis IN NATURALLY
INFECÇÃO SIMULTÂNEA POR Leishmania chagasi E Ehrlichia canis EM CÃES NATURALMENTE INFECTADOS EM SÃO LUÍS, MARANHÃO, BRASIL SIMULTANEOUS INFECTION BY Leishmania chagasi AND Ehrlichia canis IN NATURALLY
LEISHMANIOSE CANINA (continuação...)
 LEISHMANIOSE CANINA (continuação...) Prof. Rafael Fighera Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria CRITÉRIOS CLÍNICOS PARA SUSPEITA DE
LEISHMANIOSE CANINA (continuação...) Prof. Rafael Fighera Laboratório de Patologia Veterinária Hospital Veterinário Universitário Universidade Federal de Santa Maria CRITÉRIOS CLÍNICOS PARA SUSPEITA DE
Leishmaniose. Profa Alessandra Barone Prof. Archangelo Fernandes
 Leishmaniose Profa Alessandra Barone Prof. Archangelo Fernandes www.profbio.com.br Taxonomia Reino: Protozoa Filo: Sarcomastigophora Classe: Zoomastigophorea Ordem: Kinetoplastida Família: Trypanosomatidae
Leishmaniose Profa Alessandra Barone Prof. Archangelo Fernandes www.profbio.com.br Taxonomia Reino: Protozoa Filo: Sarcomastigophora Classe: Zoomastigophorea Ordem: Kinetoplastida Família: Trypanosomatidae
2.Introdução A Doença Descrição...11
 Índice 1.Apresentação... 05 2.Introdução...07 3.A Doença... 11 3.1. Descrição...11 3.2. Epidemiologia... 11 3.2.1. Agente Etiológico e Ciclo Evolutivo...11 3.2.2. Reservatórios / Hospedeiros Intermediários...
Índice 1.Apresentação... 05 2.Introdução...07 3.A Doença... 11 3.1. Descrição...11 3.2. Epidemiologia... 11 3.2.1. Agente Etiológico e Ciclo Evolutivo...11 3.2.2. Reservatórios / Hospedeiros Intermediários...
Semi-Árido (UFERSA). 2 Farmacêutico bioquímico, Mestre em Ciência Animal. UFERSA 3
 DIAGNÓSTICO CITOPATOLÓGICO DE LEISHMANIOSE VISCERAL CANINA EM REGIÃO ENDÊMICA DO NORDESTE DO BRASIL CITOPATHOLOGICAL DIAGNOSIS OF CANINE VISCERAL LEISHMANIOSIS IN NORTHEAST BRAZIL'S ENDEMIC REGION Yannara
DIAGNÓSTICO CITOPATOLÓGICO DE LEISHMANIOSE VISCERAL CANINA EM REGIÃO ENDÊMICA DO NORDESTE DO BRASIL CITOPATHOLOGICAL DIAGNOSIS OF CANINE VISCERAL LEISHMANIOSIS IN NORTHEAST BRAZIL'S ENDEMIC REGION Yannara
Audiência Pública 17/08/2015. Projeto de Lei 1.738/2011
 Audiência Pública 17/08/2015 Projeto de Lei 1.738/2011 Prof. Vitor Márcio Ribeiro PUC Minas A LEISHMANIOSE VISCERAL NO BRASIL O primeiro caso no Brasil foi descrito por Migone L.E.,em 1913 O paciente era
Audiência Pública 17/08/2015 Projeto de Lei 1.738/2011 Prof. Vitor Márcio Ribeiro PUC Minas A LEISHMANIOSE VISCERAL NO BRASIL O primeiro caso no Brasil foi descrito por Migone L.E.,em 1913 O paciente era
UNIVERSIDADE DE BRASÍLIA FACULDADE DE MEDICINA PROGRAMA DE PÓS-GRADUAÇÃO EM MEDICINA TROPICAL GETÚLIO BERNARDO MORATO FILHO
 UNIVERSIDADE DE BRASÍLIA FACULDADE DE MEDICINA PROGRAMA DE PÓS-GRADUAÇÃO EM MEDICINA TROPICAL GETÚLIO BERNARDO MORATO FILHO INFLUÊNCIA DA IDADE SOBRE O PROGNÓSTICO DA LEISHMANIOSE CUTÂNEA TRATADA COM ANTIMONIAL
UNIVERSIDADE DE BRASÍLIA FACULDADE DE MEDICINA PROGRAMA DE PÓS-GRADUAÇÃO EM MEDICINA TROPICAL GETÚLIO BERNARDO MORATO FILHO INFLUÊNCIA DA IDADE SOBRE O PROGNÓSTICO DA LEISHMANIOSE CUTÂNEA TRATADA COM ANTIMONIAL
Leishmaniose Visceral Americana no Hospital Materno Infantil de Brasília DF
 Leishmaniose Visceral Americana no HMI Leishmaniose Visceral Americana no Hospital Materno Infantil de Brasília DF Jaqueline de Deus Costa 1 Marco Túlio A. García-Zapata 2 RESUMO - Através de ficha padronizada,
Leishmaniose Visceral Americana no HMI Leishmaniose Visceral Americana no Hospital Materno Infantil de Brasília DF Jaqueline de Deus Costa 1 Marco Túlio A. García-Zapata 2 RESUMO - Através de ficha padronizada,
Diagnóstico Laboratorial de Infecções Virais. Profa. Claudia Vitral
 Diagnóstico Laboratorial de Infecções Virais Profa. Claudia Vitral Importância do diagnóstico laboratorial virológico Determinar a etiologia e acompanhar o curso de uma infecção viral Avaliar a eficácia
Diagnóstico Laboratorial de Infecções Virais Profa. Claudia Vitral Importância do diagnóstico laboratorial virológico Determinar a etiologia e acompanhar o curso de uma infecção viral Avaliar a eficácia
SITUAÇÃO EPIDEMIOLÓGICA DA LEISHMANIOSE EM CÃES ERRANTES NO MUNICÍPIO DE IJUÍ RIO GRANDE DO SUL 1
 SITUAÇÃO EPIDEMIOLÓGICA DA LEISHMANIOSE EM CÃES ERRANTES NO MUNICÍPIO DE IJUÍ RIO GRANDE DO SUL 1 Franciele Ceratti Dortzbacher 2, Francini Palha 3, Leonardo Sasso Bernardi 4, Luciana Mori Viero 5, Cristiane
SITUAÇÃO EPIDEMIOLÓGICA DA LEISHMANIOSE EM CÃES ERRANTES NO MUNICÍPIO DE IJUÍ RIO GRANDE DO SUL 1 Franciele Ceratti Dortzbacher 2, Francini Palha 3, Leonardo Sasso Bernardi 4, Luciana Mori Viero 5, Cristiane
COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA
 COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA INFORME Nº 39/2017 MONITORAMENTO DOS CASOS E ÓBITOS DE FEBRE AMARELA NO BRASIL INÍCIO DO EVENTO: Dezembro de 2016
COES Febre Amarela CENTRO DE OPERAÇÕES DE EMERGÊNCIAS EM SAÚDE PÚBLICA SOBRE FEBRE AMARELA INFORME Nº 39/2017 MONITORAMENTO DOS CASOS E ÓBITOS DE FEBRE AMARELA NO BRASIL INÍCIO DO EVENTO: Dezembro de 2016
PUBVET, Publicações em Medicina Veterinária e Zootecnia.
 PUBVET, Publicações em Medicina Veterinária e Zootecnia. O papel do Rhipicephalus sanguineus na transmissão da Leishmaniose Visceral Canina: aspectos epidemiológicos. Otamires Alves da Silva 1 e Geovania
PUBVET, Publicações em Medicina Veterinária e Zootecnia. O papel do Rhipicephalus sanguineus na transmissão da Leishmaniose Visceral Canina: aspectos epidemiológicos. Otamires Alves da Silva 1 e Geovania
Lamentável caso de Mormo, em Minas Gerais
 Lamentável caso de Mormo, em Minas Gerais O Mormo é uma doença infecto-contagiosa que acomete os Equinos e Asininos e tem como agente causador a bactéria Burkholderia mallei; Mormo é uma Zoonose porque
Lamentável caso de Mormo, em Minas Gerais O Mormo é uma doença infecto-contagiosa que acomete os Equinos e Asininos e tem como agente causador a bactéria Burkholderia mallei; Mormo é uma Zoonose porque
ENFERMAGEM SAÚDE DA MULHER. Doenças Sexualmente Transmissíveis Parte 2. Profª. Lívia Bahia
 ENFERMAGEM SAÚDE DA MULHER Doenças Sexualmente Transmissíveis Parte 2 Profª. Lívia Bahia Sífilis Agente Etiológico: Treponema pallidum Morfologicamente o Treponema pallidum é uma bactéria espiral fina
ENFERMAGEM SAÚDE DA MULHER Doenças Sexualmente Transmissíveis Parte 2 Profª. Lívia Bahia Sífilis Agente Etiológico: Treponema pallidum Morfologicamente o Treponema pallidum é uma bactéria espiral fina
