FENÔMENOS DE TRANSPORTE TERMODINÂMICA
|
|
|
- Marina Carneiro de Santarém
- 7 Há anos
- Visualizações:
Transcrição
1 UNIERSIDADE FEDERAL RURAL DO SEMI-ÁRIDO DEPARTAMENTO DE CIÊNCIAS AMBIENTAIS FENÔMENOS DE TRANSPORTE TERMODINÂMICA CICLO DE POTÊNCIA E DE REFRIGERAÇÃO CALOR E TRABALHO Prof. Roberto ieira Pordeus Mossoró-RN 008
2 CICLO DE POTÊNCIA E DE REFRIGERAÇÃO Os ciclos de geração de potêcia retiram calor de uma fote à alta temperatura. Cosideremos como sistema o gás cotido um cilidro com êmbolo, como mostrado a Fig. amos tirar um dos pequeos pesos do êmbolo provocado um movimeto para cima deste, de uma distâcia dx. Podemos cosiderar este pequeo deslocameto de um processo quase-estático e calcular o trabalho, dw, realizado pelo sistema durate este processo. A força total sobre o êmbolo é P. A, ode P é a pressão do gás e A é a área do êmbolo. Portato o trabalho dw é: δ W P.A.dx ( ) δ W Pd ( ) Figura - Exemplo de trabalho efetuado pelo movimeto de froteira de um sistema um processo quase-estático - A relação etre P e é dada em termos de dados experimetais ou a forma gráfica (como, por exemplo, o traço em um osciloscópio) Neste caso podemos determiar a itegral da Eq., por itegração gráfica ou umérica. - A relação etre P e é tal que seja possível ajustar uma relação aalítica etre eles, e podemos etão, fazer diretamete a itegração. Um exemplo comum desse segudo tipo de relação é o caso de um processo chamado politrópico, o qual P costate, através de todo o processo. O expoete "" pode tomar qualquer valor etre - e + depededo do processo particular sob aálise. P cos ta te P cos ta te P P P P Para esse tipo de processo, podemos itegrar a Eq., resultado em: Pd cos ta te d + cos ta te + cos ta te ( ) P P P P Pd ( )
3 Note-se que este resultado, Eq., é válido para qualquer valor do expoete, exceto. No caso ode, tem-se; Pd P P l ( 4 ) P Costate P P, e portato, d O processo politrópico coforme já descrito, expõe uma relação fucioal especial etre P e durate um processo. Há muitas relações possíveis, algumas das quais serão examiadas os problemas apresetados o fial deste capítulo. Exemplo. Cosidere como sistema o gás cotido o cojuto cilidro - êmbolo mostrado a figura abaixo. Observe que vários pesos pequeos estão colocados sobro o êmbolo. A pressão iicial é igual a 00 kpa e o volume iicial do gás é 0,040 m. a) Coloquemos um bico de Buse embaixo do cilidro e deixemos que o volume do gás aumete para 0, m, equato a pressão permaece costate. Calcular o trabalho realizado pelo sistema durate esse processo. Como a pressão, este caso é costate, cocluímos pela Eq. ; ( ) W 00 kpa x ( 0, 0,04) m,0 kj W P d P b) Cosideremos o mesmo sistema e as mesmas codições iiciais e fiais, porém, ao mesmo tempo que o bico de Buse está sob o cilidro e o êmbolo se levata, removamos os pesos deste, de tal maeira que durate o processo a temperatura se matém costate. Se admitirmos que o gás se comporta como gás ideal, obtemos: P mrt e otamos que este processo é politrópico com o expoete, pois a massa, m, do sistema é costate, R é a costate do gás e sedo T costate, mrt costate. Da ossa aálise aterior, cocluímos que o trabalho é dado pela Eq. 4, Portato: 0, W P d P l 00 kpa x 0, 04 m x l 7, kj 0, 04 c) Cosideremos o mesmo sistema, porém, durate a troca de calor removamos os pesos de tal maeira que a expressão P, costate, descreva a relação etre a pressão e o volume durate o processo. Novamete o volume fial é 0, m. Calcular o trabalho.
4 Esse processo é politrópico, o qual,. Aalisado o processo, cocluímos ovamete que o trabalho é dado pela Eq., assim: P,, 0, 04 P 00, 0, kpa P P 60, 77 x 0, 00 x 0, 04 W P d 6, 4 kj, d) Cosideremos o sistema e o estado iicial dado os três primeiros exemplos, porém matehamos o êmbolo preso por meio de um pio, de modo que o volume permaeça costate. Além disso, façamos com que o calor seja trasferido do sistema para o meio até que a pressão caia a 00 kpa. Calcular o trabalho. Como dw P.d, para um processo quase-estático, o trabalho é igual a zero porque, este caso, ão há variação do volume, isto é, d0. O processo em cada um dos quatro exemplos está mostrado a Figura abaixo. O processo -a é um processo a pressão costate e a área -a-f-e- represeta o respectivo trabalho. Aalogamete, a liha -b represeta o processo em que P costate, a liha -c represeta o processo em que P, costate e a liha -d represeta o processo a volume costate. O estudate deve comparar as áreas relativas sob cada curva com os resultados uméricos obtidos acima. 4
5 EXERCICIOS DE APLICAÇÃO 4.. Problema. Um cilidro, provido de um êmbolo sem atrito, cotém 5 kg de vapor de refrigerate R-4a a 000 kpa e 40 ºC. O sistema é resfriado a pressão costate, até que o refrigerate apresete um título igual a 5%. Calcular o trabalho realizado durate esse processo. Solução: P costate e trabalho de froteiras W Pd p ( ) m p( v v), pois v m m v ( 0, , 0495) 9 75 kj W 5 x 000, (realizado sobre o sistema) 4.9. Problema. O cojuto cilidro-pistão, mostrado a Figura abaixo, cotém, iicialmete, 0, m de dióxido de carboo a 00 kpa e 00ºC. Os pesos são, etão, adicioados a uma velocidade tal que o gás é comprimido segudo a relação p, costate. Admitido que a temperatura fial seja igual a 00ºC, determie o trabalho realizado durate esse processo. Solução: Da equação 4.4 p/ P costate ( ) temperatura variou W Pd P P Assumido um gás ideal: P mrt mr P T ( T ) mrt mrt mr T W, mas, P 00 x 0, mr 0, 6 m T 7, ( 47, 7, ) 0, 608 W 80, 40, kj 5
6 4.. Problema. Um cojuto cilidro-pistão cotém, iicialmete, 0, m de um gás a MPa e 500ºC. O gás é etão expadido um processo ode p costate. Admitido que a pressão fial seja igual a 00 kpa, determie o trabalho evolvido este processo. Solução: Como P costate, etão é válido: P cte. (politrópico) à T cte. W Pd C d C l P 0, x 000 P P m P 00 W P l 000 x 0, l 0, kj 0, 4.5. Problema 4. O espaço localizado acima do ível d água um taque fechado de armazeameto cotém itrogêio a 5ºC e 00 kpa. O taque tem um volume total de 4 m e cotém 500 kg de água a 5ºC. Uma quatidade adicioal de 500 kg de água é etão letamete forçada para detro do taque. Admitido que a temperatura permaeça costate o processo, calcular a pressão fial do itrogêio e o trabalho realizado sobre o mesmo durate o processo. Solução: H 500 x O,, m N 4, 0 0, 505, 4985 m N, , 505, 997m, 4985 Cosiderado gás ideal T costate P N 00 x 6, 7 kpa, 997 W W N P d N N N P l, x,4985 x l 54, kj,4985 6
7 4.. Problema 5. O cojuto cilidro-pistão mostrado a figura abaixo, cotém ar e iicialmete está a 50 kpa e 400ºC. O cojuto é etão resfriado até 0ºC. Pergutase: a ) O pistão está ecostado os esbarros o estado fial? Qual é a pressão fial o ar? b ) Qual o trabalho realizado o processo? Solução P 50 kpa; T 400ºC 67, K T T 0 0ºC 9, K a ) Se o pistão para em ; x Cosiderado gás ideal: P T P T P P x T x T 9, 50 x x 0, 7 kpa < P 67, O pistão esbarra o fial, pois, se P > P a pressão extera P, resposável pelo movimeto do pistão ão seria suficiete para movimetá-lo. b ) O trabalho realizado quado o pistão está se movedo a Pext costate P ( ) W Pext d P P mrt m R T P T P mr T W R RT W m RT 0,87 x x 67, x 96,6 kj kg - 7
8 4.7. Problema 6. Um cojuto cilidro-pistão cotém kg de ar a 0ºC e 00 kpa. O cojuto é etão aquecido em um processo a pressão costate até 600 K. a. Determie o volume fial. b. Trace um gráfico da liha do processo em um diagrama P-v. c. Determie o trabalho o processo Problema 7. Um cilidro com êmbolo móvel, como mostrado a figura, cotém kg d água o estado de vapor úmido com título igual a 5% e pressão de,0 bar (estado ). Esse sistema é aquecido à pressão costate até se obter o título igual a 85% (estado ). Pede-se: a) Represetar o processo em um diagrama P-. b) Calcular o trabalho realizado pelo vapor durate o processo. Resposta a) Resposta b) Da defiição de Trabalho termodiâmico devido ao movimeto de froteira, e sedo a massa do sistema costate, temos: Assim, para calcularmos o W precisamos determiar o valor do volume específico e. Cosiderado a tabela de propriedades da água saturada para P,0 bar temos: L 0, m kg - 0,8857 m kg - Da defiição de título e da relação etre título e uma propriedade qualquer a região de vapor úmido temos: L + X ( - L ) 8
9 0, ,5 ( 0,8857-0, ) 0,756 m kg - 0, ,85 ( 0,8857-0,000605) 0,750 m kg - Substituido a expressão do trabalho, Eq.() temos: W,0.0 5 x x (0,750-0,756) [ J ] W, [ J ] ou W 7,5 [ kj ] Problema 8.Um cilidro com êmbolo móvel, como mostrado a figura, cotém 5 kg d água o estado de vapor úmido com título igual a 0% e pressão de 5,0 bar (estado ). Esse sistema é aquecido à pressão costate até se obter a temperatura de 00ºC (estado ). Pede-se: a) Represetar o processo em um diagrama P- b) Determiar o trabalho realizado pela substâcia de trabalho cotra o êmbolo, em kj Solução Resposta a) b) O trabalho devido ao movimeto de froteira é: W Pd como P costate, etão W m P dv m P ( v v) Da tabela de propriedades de saturação, para o estado, P 5,0 bar (500 kpa) obtemos ls 0,00096 m kg -, vs 0,749 m kg - ls + X ( vs - ls ) 0, , ( 0,749-0,00096) 0,0759 m kg - Da tabela de vapor superaquecido para P 5,0 bar e T 00 o C, obtemos 0,449 m kg - 9
10 Assim o trabalho etre o estado e resulta m W 5,0 Kg x 500 kpa 87 kg x ( 0,449 0,0759) kj A PRIMEIRA LEI DA TERMODINÂMICA PARA MUDANÇA DE ESTADO DE UM SISTEMA A primeira lei da termodiâmica é comumete chamada de "lei da coservação da eergia". Nos cursos elemetares de física, o estudo da coservação de eergia dá êfase às trasformações de eergia ciética e potecial e suas relações com o trabalho. Uma forma mais geral de coservação de eergia iclui os efeitos de trasferêcia de calor e a variação de eergia itera. Esta forma mais geral é chamada de "Primeira Lei da Termodiâmica". Outras formas de eergia podem também serem icluídas, tais como: eergia eletrostática, eergia de campos magéticos tesão superficial etc. A idéia básica, aqui, é que a eergia pode ser armazeada detro de um sistema, trasformada de uma para outra forma de eergia e trasferida etre sistemas. Para o sistema fechado a eergia pode ser trasferida através do trabalho e da trasferêcia de calor. A quatidade total de eergia é coservada em todas as trasformações e trasferêcias. Primeira Lei para Um Sistema Percorredo Um Ciclo A primeira lei da termodiâmica estabelece que, durate um processo cíclico qualquer, percorrido por um sistema, a itegral cíclica (somatório sobre todo o ciclo), do calor é proporcioal à itegral cíclica do trabalho, matematicamete δ Q J δ W ( ) Q J ciclo Ou ciclo W A uidade de calor e trabalho, para o sistema iteracioal, SI, é o joule ou seus múltiplos. Outras uidades são freqüetemete usadas, tais como aquelas do sistema prático iglês e do sistema prático métrico, respectivamete, BTU (British thermal uits) e a kcal (quilocaloria). kcal 4,868 kj BTU,05506 kj kcal,96744 BTU kw 860 kcal 4 BTU / h hp 64, kcal / h 545 BTU / h 0
11 Primeira Lei para Mudaça de Estado de um Sistema A Eq. estabelece a primeira lei da termodiâmica para um sistema operado em um ciclo. Muitas vezes, etretato, estamos mais iteressados a respeito de um processo que em um ciclo. Assim é iteressate obter uma expressão da primeira lei da termodiâmica para um processo. Isto pode ser feito itroduzido-se uma ova propriedade, a eergia total, a qual é represetada pelo símbolo E. Cosidere-se um sistema que percorre um ciclo, mudado do estado ao estado pelo processo A e voltado do estado ao estado pelo processo B. Este ciclo está mostrado a Fig.. Da primeira lei da termodiâmica temos; δ Q δ W Figura cosiderado os dois processo que costituem o ciclo separadamete obtemos; QA + δ QB δ W A + δ δ W ( ) B Agora, cosideremos outro ciclo, com o sistema mudado do estado ao estado pelo mesmo processo A e voltado ao estado pelo processo C como idicado a Fig. Para este ciclo podemos escrever: δ Q + + A δ Q C δ W A δ W C Subtraido a seguda (Eq. ) destas equações da primeira, temos, Q B δ Q C δ W B δ δ W ou reordeado temos, C ( Q δ W ) ( ) B δ Q δ W C δ ( ) isto que B e C represetam camihos arbitrários etre os estados e cocluímos que a quatidade ( δ Q δ W ) é a mesma para qualquer processo etre o estado e o estado. Em coseqüêcia, ( δ Q δ W ) depede somete dos estados iicial e fial ão depededo do camiho percorrido etre os dois estados. Isto os faz cocluir que a quatidade, ( δ Q δ W ), é uma fução de poto, e, portato, é a diferecial exata de
12 uma propriedade do sistema. Essa propriedade é a eergia total do sistema e é represetada pelo símbolo E. Assim podemos escrever. δ Q δ W d E ou δ Q d E + δ W ( 4 ) Observe-se que, sedo E uma propriedade, sua diferecial é escrita Eq. 4 é itegrada, de um estado iicial a um estado fial, temos d E. Quado a Q E E + W ( 5 ) ode, Q é o calor trasferido para o sistema durate o processo do estado para o estado, E e E são os valores iicial e fial da eergia total do sistema e W é o trabalho efetuado pelo sistema durate o processo. O sigificado físico da propriedade E é o de represetar toda a eergia de um sistema em um dado estado. Essa eergia pode estar presete em uma multiplicidade de formas, tais como; eergia ciética, eergia potecial, eergia associada à estrutura do átomo, eergia química, etc. No estudo da termodiâmica é coveiete cosiderar-se separadamete as eergias ciética e potecial, as demais formas de eergia do sistema são agrupadas em uma úica variável, já defiida, a eergia itera, represetada pelo símbolo U. Assim, E U + EC + EP ( 6 ) Sedo EC m e EP m gz ( 7 ) ode, m é a massa do sistema, é a velocidade, g a aceleração gravitacioal e Z a elevação em relação ao referecial adotado para o sistema termodiâmico. A razão para trabalhar separadamete é que a eergia ciética, (EC), e a eergia potecial, (EP), estão associadas a um sistema de coordeadas que escolhemos, e podem ser determiadas pelos parâmetros macroscópicos de massa, velocidade e elevação. A eergia itera U está associada ao estado termodiâmico do sistema. Como cada uma das parcelas é uma fução de poto, podemos escrever, de du + d(ec) + d(ep) ( 8 ) A primeira lei da termodiâmica para uma mudaça de estado de um sistema pode, etão, ser escrita como;
13 ( EC ) + d( EP) δw δ Q du + d + ( 9 ) Itegrado a Equação 9 e admitido que g é costate, obtemos ( ) + m g( Z Z) W m Q + U U + ( 0 ) EXEMPLO. Um automóvel, com massa igual a 00 kg, se desloca com uma velocidade tal que sua eergia ciética é 400 kj (veja Figura). Nesta codição, determie a velocidade do automóvel. Admita que o mesmo automóvel é levatado por um guidaste. A que altura o automóvel deve ser içado para que sua eergia potecial se tore igual a eergia ciética especificada o problema. Cosidere que o campo gravitacioal é o padrão. Solução: A eergia ciética do automóvel é defiida por EC m 400 kj A velocidade do automóvel pode ser calculada a partir da eergia ciética, ou seja, EC x 400 x 0 00 m A eergia potecial é defiida por EP m gh 7,0 m s - Admitido que o valor da eergia potecial é igual aquele forecido para a eergia ciética o euciado do problema, H EC m g 400 x 0 7, m 00 x 9,8
14 EXEMPLO. Um sistema iicialmete em repouso sofre um processo o qual recebe uma quatidade de trabalho igual a 00 kj. Durate o processo o sistema trasfere para o meio ambiete uma quatidade de calor igual a 0 kj. Ao fial do processo o sistema tem velocidade de 60 m s - e uma elevação de 50 m. A massa do sistema é de 5 kg, e a aceleração gravitacioal local é de 9,78 m s -. Determie a variação de eergia itera do sistema durate o processo, em kj. Solução: Cohecemos: Um sistema de massa cohecida sofre um processo recebedo uma quatidade de trabalho e trasferido uma quatidade de calor cohecidos. O sistema está iicialmete em repouso e o estado fial tem velocidade de 60 m s - e elevação de 50 m. Obter: Determiar a variação de eergia itera do sistema. Hipótese: - O sistema sob aálise é um sistema fechado, costituído da massa de 5 kg - No estado fial o sistema está em equilíbrio (velocidade uiforme) aálise: a primeira lei da termodiâmica (balaço de eergia) para o sistema fechado é Q Δ E + W ou Q ΔU + ΔEC + ΔEP + W a variação de eergia ciética e potecial é: ΔEC m ΔEP mg - ( ) ΔEC ( 5 kg)( 60 0 ) m s ΔEC J - ( Z Z ) ΔEP ( 5 kg)( 9,78 m s )( 50 0) m ΔEP 5 J substituido os valores uméricos a expressão da Primeira Lei obtemos o valor de ΔU, ΔU Q ΔEC ΔEP W ΔU ( 0 kj ) ( 45,0) (,5 kj ) ( 00 kj ) ΔU 87,5 + 00,775 kj 4
15 EXEMPLO. O fluido cotido um taque é movimetado por um agitador. O trabalho forecido ao agitador é kj e o calor trasferido do taque é 500 kj. Cosiderado o taque e o fluido como sistema, determie a variação da eergia do sistema este processo. A primeira lei da termodiâmica é (Eq. 0) ( ) + m g( Z Z) W m Q U U + + Como ão há variação de eergia ciética ou de potecial, essa equação fica reduzido a Q U U + W ( 5090) 590 kj U U 500 Eergia Itera Uma Propriedade Termodiâmica A eergia itera é uma propriedade extesiva, vista que ela depede da massa do sistema. As eergias ciética e potecial, pelo mesmo motivo, também são propriedades extesivas. O símbolo U desiga a eergia itera de uma dada massa de uma substâcia. Segudo a coveção usada para as outras propriedades extesivas, o símbolo u desiga a eergia itera por uidade de massa. Pode-se dizer que u é a eergia itera específica, coforme fizemos o caso do volume específico. U U liq + U vap ou m u mliq ul + mvap uv Dividido por m e itroduzido o título x, temos ( x) ul x uv u + u u + x l u lv EXEMPLO 4. A eergia itera específica do vapor d água saturado a pressão de 0,6 MPa e com título de 95% é calculada do seguite modo: ( 897, 5) 47 5 kj/kg u ul + x ulv 669, 9 + 0, 95, A Tab. A.. apreseta os valores de u para a região ode o vapor está superaquecido, a A..4 os valores referetes a região do líquido comprimido e a A..5 os valores referetes aos estados ode o sólido e o vapor coexistem em equilíbrio. EXEMPLO 5. Determie, para a água e os estados idicados, as propriedades que faltam (p, T, x e v): a). T 00ºC, u 780 kj kg - b). P 000 kpa, u 000 kj kg - 5
16 Solução: As propriedades forecidas os dois estados são idepedetes e, assim, determiam completamete o estado termodiâmico. Observe que ós precisamos idetificar a fase da água os estados forecidos e isto pode ser utilizado comparado-se as iformações forecidas com os valores de froteira. a. A Tab. A.. idica que u v 56,0 kj kg - quado T 00ºC. A água o estado idicado o Exemplo se ecotra como vapor superaquecido porque o valor de u especificado é maior do que aquele referete ao vapor saturado a mesma temperatura. A pressão este estado deve ser meor do que 858 kpa que é a pressão de saturação a 00 ºC. A Tabela A.. idica que a eergia itera específica da água é igual a 78 kj quado T 00ºC e p 600 kpa. A mesma tabela idica que u 776,8 kj kg - quado T 00ºC e p 800 kpa. Iterpolado liearmete, p 648 kpa Observe que o título ão é aplicável este estado e que o volume específico, calculado com uma iterpolação liear a mesma tabela, é igual a 0,54 m kg - b. A Tab. A.. idica u l 906,4 kj kg - e u v 600, kj kg - quado a pressão é 000 kpa. O valor forecido para a eergia itera específica o item é maior do que o de u l e meor do que o de u v. Assim, a água ecotra um estado saturado líquido vapor ode a temperatura é igual a,4ºc. O título pode ser calculado por u 000, 0 906, 4 + x69, 8 ou x 0,6457 e o volume especifico é v 0, ,6456 x 0, ,06474 m kg - EXEMPLO 6. Cosidere 5 kg de vapor de água cotida o iterior do cojuto cilidro pistão. O vapor sofre uma expasão do estado ode P 5,0 bar e T 40 o C para o estado ode P,5 bar e T 00 o C. Durate o processo 80 kj de calor é trasferida para o vapor. Uma hélice é colocada o iterior do cojuto através de um eixo para homogeeizar o vapor, a qual trasfere 8,5 kj para o sistema. O cojuto cilidro pistão está em repouso. Determiar a quatidade de trabalho trasferido para o pistão durate o processo de expasão. Solução: - Esquema do problema e o esquema gráfico da solução o plao P- hipótese: - o vapor é o sistema termodiâmico fechado. - ão há variação de eergia ciética e potecial. 6
17 Aálise: O balaço de eergia para o sistema fechado resulta Q ΔU + ΔEC + ΔEP + W, como dos dados do problema, ΔEC ΔEP 0, etão: + Q ΔU W ( ) ode, W helice + W W pistão, substituido a expressão () W pistão ( ) Q Whelice m u u () Da tabela de propriedades superaquecidas do vapor de água obtemos para o estado e. u 707,6 kj e u 656, kj substituido os valores uméricos a expressão () temos: W pistão ( + 80 kj) ( 8, 5 kj) 5, 0 kg ( 656, 707, 6) kj W pistão +55,5 kj EXEMPLO. Um recipiete, com volume de 5,0 m, cotém 0,05 m de água líquida saturada e 4,95 m de água o estado de vapor saturado a pressão de 0, MPa. Calor é trasferido à água até que o recipiete coteha apeas vapor saturado. Determiar o calor trasferido esse processo. 7
18 Sistema: A água cotida o recipiete. Estada iicial: Pressão, volume líquido, volume de vapor. Assim o estado está determiado. Estado fial: Algum poto sobre a curva de vapor saturado. A água é aquecida, portato p > p. Processo: olume e massa costate; portato, o volume específico é costate. (ver diagrama). Modelo para a substâcia: Tabela de vapor d água. Aálise: Primeira Lei: ( ) + m g( Z Z) W m Q + U U +, Como ão há movimeto a eergia ciética é zero, há uma pequea variação o cetro de massa do sistema, porém admitiremos que ão há variação de eergia potecial, como ão há variação de volume, ão há trabalho. Porém, este caso a equação da Primeira Lei se reduz a, Q U U Solução: O calor trasferido o processo pode ser determiado com a expressão aterior. O estado é cohecido, de modo que U pode ser ecotrado. O volume específico do estado é cohecido (cosiderado o estado e o processo) e sabemos que o vapor é saturado. Deste modo o estado está determiado (observe a Fig.) e podemos obter o valor de U. Portato m m liq 0, 05 liq 47, 94 kg v 0, 0004 l vap 4, 95 vap, 9 kg v, 6940 v U m liq u liq + m vap uvap U 47, 94 ( 47, 6 ) +, 9 ( 506, ) 7 6 kj Para determiar a eergia itera o estado fial, U, precisamos cohecer duas propriedades termodiâmicas idepedetes. A propriedade termodiâmica que cohecemos diretamete é o título (x 00%) e a que pode ser calculada é o volume específico fial (v ). Assim, m m liq + m vap 47, 94 +, 9 50, 86 kg 8
19 5, 0 m v 0, 098 m 50, 86 kg Na Tab. A.. determiamos por iterpolação que, a pressão de,0 MPa, o volume específico do vapor saturado é 0,098m kg -. A pressão fial do vapor é, etão,,0 MPa. Assim, u 600,5 kj kg - e U mu 50,86 (600,5) 6 kj Já podemos calcular o calor trasferido, pois cohecemos as eergias iteras. Assim Q U U kj A Propriedade Termodiâmica Etalpia Ao se aalisar tipos específicos de processos, frequetemete ecotramos certas combiações de propriedades termodiâmicas que são, portato, também propriedades da substâcia que sofre a mudaça de estado. Cosidere um sistema que passa por um processo quase-estático a pressão costate. Admitimos também que ão haja variações de eergia ciética ou potecial e que o úico trabalho realizado durate o processo seja aquele associado ao movimeto de froteira. Q U U + W O trabalho pode ser calculado pela expressão W pd Como a pressão é costate, Portato W p d p ( ) Q U U + p p ( U + p ) ( U + p ) A trasferêcia de calor durate o processo é igual a variação da quatidade U + p etre os estados iicial e fial. Temos uma ova propriedade extesiva chamada de etalpia, H U + p ou por uidade de massa h u + pv Exemplo. Calculemos a eergia itera específica do refrigerate R-4a superaquecido a 0,4 MPa e 70 C. u h pv u 460, x 0, ,95 kj kg 9
20 Calcule a eergia itera do mesmo refrigerate superaquecido a uma pressão de 0,6 MPa e 90 C, para uma massa de 0,85 kg. A etalpia de uma substâcia, um estado de saturação e apresetado certo título, é determiado do mesmo modo que foi utilizado para o volume específico e para a eergia itera. A etalpia do líquido saturado tem o símbolo h l, a do vapor saturado h v, e o aumeto de atalpia durate a vaporização h lv. ( x) hl x hv h + h hl + x hlv Exemplo. Um cilidro provido de pistão cotém 0,5 kg de vapor d água a 0,4 MPa e apreseta iicialmete um volume de 0, m. Trasfere-se calor ao vapor até que a temperatura atija 00 C, equato a pressão permaece costate. Determiar o calor trasferido e o trabalho esse processo. Sistema: Água itera o cilidro. Estado iicial: cohecidos: p, e m v é determiado em tabela. Estado fial: T e p (região de vapor superaquecido) Processo a pressão costate Aálise: Não há variação a eergia ciética ou a eergia potecial. O trabalho é feito pelo movimeto de froteira. (processo quase-estático). A pressão e costate, temos, W Pd P d P v Deste modo a ª lei da termodiâmica, em termo de Q, é Q m m ( ) m( P v P ) ( u u ) + W ( u u ) + m ( P v P v ) m ( h h ) Solução: Existem vários procedimetos que podem ser seguidos. O estado é cohecido, assim v e h (ou u ) podem ser determiados. O estado também é cohecido, assim, v e h (ou u ) podem ser obtidos. Calcular o calor e o trabalho. Usado a etalpia, temos: 0, v 0, 0, x0, 464 m 0, 5 0, 989 x 0, 4 0, 464 h h l + x h lv 604, , 4 h 066, 8 x, 8 54, 7 ( 066, 8 54, 7) 77, kj ( v v ) 0, ( 0, , ) 9, kj Q 0, 5 W m P x 0 0
21 Portato, U U Q W 77, 9, 0 680, kj O calor trasferido poderia também se ecotrado a partir de u e u : u ul + ulv 604, + 0, 4 x 949, 444, 7 e u 804 9, Q U U + W 0, 5 ( 804, 8 444, 7) + 9, 0 77, kj
Virgílio Mendonça da Costa e Silva
 UNIVERSIDADE FEDERAL DA PARAÍBA CENTRO DE TECNOLOGIA DEPARTAMENTO DE ENGENHARIA MECÂNICA VIBRAÇÕES DOS SISTEMAS MECÂNICOS VIBRAÇÕES LIVRES COM AMORTECIMENTO DE SISTEMAS DE GL NOTAS DE AULAS Virgílio Medoça
UNIVERSIDADE FEDERAL DA PARAÍBA CENTRO DE TECNOLOGIA DEPARTAMENTO DE ENGENHARIA MECÂNICA VIBRAÇÕES DOS SISTEMAS MECÂNICOS VIBRAÇÕES LIVRES COM AMORTECIMENTO DE SISTEMAS DE GL NOTAS DE AULAS Virgílio Medoça
étodos uméricos MÉTODO DOS MOMENTOS - MOM Prof. Erivelton Geraldo Nepomuceno PROGRAMA DE PÓS-GRADUAÇÃO EM ENGENHARIA ELÉTRICA
 étodos uméricos MÉTODO DOS MOMETOS - MOM Prof. Erivelto Geraldo epomuceo PROGRAMA DE PÓS-GRADUAÇÃO EM EGEHARIA ELÉTRICA UIVERSIDADE DE JOÃO DEL-REI PRÓ-REITORIA DE PESQUISA CETRO FEDERAL DE EDUCAÇÃO TECOLÓGICA
étodos uméricos MÉTODO DOS MOMETOS - MOM Prof. Erivelto Geraldo epomuceo PROGRAMA DE PÓS-GRADUAÇÃO EM EGEHARIA ELÉTRICA UIVERSIDADE DE JOÃO DEL-REI PRÓ-REITORIA DE PESQUISA CETRO FEDERAL DE EDUCAÇÃO TECOLÓGICA
Termodinâmica e Estrutura da Matéria. 19/Fev/2016 Aula 1
 Termodiâmica e Estrutura da Matéria 19/Fev/016 Aula 1 Temperatura e a Lei Zero da Termodiâmica Sistema Termodiâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação
Termodiâmica e Estrutura da Matéria 19/Fev/016 Aula 1 Temperatura e a Lei Zero da Termodiâmica Sistema Termodiâmico Termómetros e Escalas de Temperatura Descrição macroscópica dos gases ideais Equação
H = U + PV função de estado. Processo isobárico e quase-estático (dp = 0): dh A variação de entalpia é igual ao calor H T
 Etalpia H + V fução de estado H H (, ) V Variáveis aturais de H dh d + dv + Vd H H rocesso isobárico e quase-estático (d ): dh variação de etalpia é igual ao calor d + dv δq trocado pelo sistema um processo
Etalpia H + V fução de estado H H (, ) V Variáveis aturais de H dh d + dv + Vd H H rocesso isobárico e quase-estático (d ): dh variação de etalpia é igual ao calor d + dv δq trocado pelo sistema um processo
Capítulo I Séries Numéricas
 Capítulo I Séries Numéricas Capitulo I Séries. SÉRIES NÚMERICAS DEFINIÇÃO Sedo u, u,..., u,... uma sucessão umérica, chama-se série umérica de termo geral u à epressão que habitualmete se escreve u u...
Capítulo I Séries Numéricas Capitulo I Séries. SÉRIES NÚMERICAS DEFINIÇÃO Sedo u, u,..., u,... uma sucessão umérica, chama-se série umérica de termo geral u à epressão que habitualmete se escreve u u...
2.2. Séries de potências
 Capítulo 2 Séries de Potêcias 2.. Itrodução Série de potêcias é uma série ifiita de termos variáveis. Assim, a teoria desevolvida para séries ifiitas de termos costates pode ser estedida para a aálise
Capítulo 2 Séries de Potêcias 2.. Itrodução Série de potêcias é uma série ifiita de termos variáveis. Assim, a teoria desevolvida para séries ifiitas de termos costates pode ser estedida para a aálise
MATEMÁTICA II. Profa. Dra. Amanda Liz Pacífico Manfrim Perticarrari
 MATEMÁTICA II Profa. Dra. Amada Liz Pacífico Mafrim Perticarrari amada@fcav.uesp.br O PROBLEMA DA ÁREA O PROBLEMA DA ÁREA Ecotre a área da região que está sob a curva y = f x de a até b. S = x, y a x b,
MATEMÁTICA II Profa. Dra. Amada Liz Pacífico Mafrim Perticarrari amada@fcav.uesp.br O PROBLEMA DA ÁREA O PROBLEMA DA ÁREA Ecotre a área da região que está sob a curva y = f x de a até b. S = x, y a x b,
Secção 1. Introdução às equações diferenciais
 Secção. Itrodução às equações difereciais (Farlow: Sec..,.) Cosideremos um exemplo simples de um feómeo que pode ser descrito por uma equação diferecial. A velocidade de um corpo é defiida como o espaço
Secção. Itrodução às equações difereciais (Farlow: Sec..,.) Cosideremos um exemplo simples de um feómeo que pode ser descrito por uma equação diferecial. A velocidade de um corpo é defiida como o espaço
EQUAÇÕES DIFERENCIAIS
 EQUAÇÕES DIFERENCIAIS rof Me Arto Barboi SUMÁRIO INTRODUÇÃO EQUAÇÃO DIFERENCIAL ORDINÁRIA (EDO) Ordem de uma Equação Diferecial Ordiária Grau de uma Equação Diferecial Ordiária Solução geral e particular
EQUAÇÕES DIFERENCIAIS rof Me Arto Barboi SUMÁRIO INTRODUÇÃO EQUAÇÃO DIFERENCIAL ORDINÁRIA (EDO) Ordem de uma Equação Diferecial Ordiária Grau de uma Equação Diferecial Ordiária Solução geral e particular
-0,4-0,6 -0,9 -1,5 -3,4 -13,6 EXERCÍCIOS
 EXERCÍCIOS FÍSICA MODERNA ÁTOMO DE BOHR PROF. MARENGÃO. (UFRN) Um átomo de hidrogêio, ao passar de um estado quâtico para outro, emite ou absorve radiação eletromagética de eergias bem defiidas. No diagrama
EXERCÍCIOS FÍSICA MODERNA ÁTOMO DE BOHR PROF. MARENGÃO. (UFRN) Um átomo de hidrogêio, ao passar de um estado quâtico para outro, emite ou absorve radiação eletromagética de eergias bem defiidas. No diagrama
Gases Introdução Lei de Boyle
 Itrodução Nos gases, as forças de atração itermoleculares são fracas, que permitem um movimeto rápido e idepedete das moléculas. Por outro lado, seu comportameto é cotrolado pelo seu volume, pressão, temperatura
Itrodução Nos gases, as forças de atração itermoleculares são fracas, que permitem um movimeto rápido e idepedete das moléculas. Por outro lado, seu comportameto é cotrolado pelo seu volume, pressão, temperatura
CINÉTICA QUÍMICA FATORES DE INFLUÊNCIA - TEORIA
 Itrodução CINÉTICA QUÍMICA FATORES DE INFLUÊNCIA - TEORIA A Ciética Química estuda a velocidade com a qual as reações acotecem e os fatores que são capazes de realizar ifluêcia sobre ela. A medida mais
Itrodução CINÉTICA QUÍMICA FATORES DE INFLUÊNCIA - TEORIA A Ciética Química estuda a velocidade com a qual as reações acotecem e os fatores que são capazes de realizar ifluêcia sobre ela. A medida mais
1. Definição e conceitos básicos de equações diferenciais
 Capítulo 7: Soluções Numéricas de Equações Difereciais Ordiárias. Itrodução Muitos feómeos as áreas das ciêcias, egearias, ecoomia, etc., são modelados por equações difereciais. Supoa-se que se quer determiar
Capítulo 7: Soluções Numéricas de Equações Difereciais Ordiárias. Itrodução Muitos feómeos as áreas das ciêcias, egearias, ecoomia, etc., são modelados por equações difereciais. Supoa-se que se quer determiar
5. ANÁLISE DE SISTEMAS DA CONFIABILIADE DE SISTEMAS SÉRIE-PARALELO
 5. ANÁLISE DE SISTEMAS DA CONFIABILIADE DE SISTEMAS SÉRIE-PARALELO 5.1 INTRODUÇÃO Um sistema é defiido como todo o cojuto de compoetes itercoectados, previamete determiados, de forma a realizar um cojuto
5. ANÁLISE DE SISTEMAS DA CONFIABILIADE DE SISTEMAS SÉRIE-PARALELO 5.1 INTRODUÇÃO Um sistema é defiido como todo o cojuto de compoetes itercoectados, previamete determiados, de forma a realizar um cojuto
2 - PRINCÍPIO DE FUNCIONAMENTO DO GERADOR DE CORRENTE CONTINUA
 2 - PRICÍPIO D FUCIOAMTO DO GRADOR D CORRT COTIUA 2.1 - A FORÇA LTROMOTRIZ IDUZIDA O pricípio de fucioameto do gerador de correte cotíua tem por base a Lei de Faraday que estabelece que, se o fluxo magético
2 - PRICÍPIO D FUCIOAMTO DO GRADOR D CORRT COTIUA 2.1 - A FORÇA LTROMOTRIZ IDUZIDA O pricípio de fucioameto do gerador de correte cotíua tem por base a Lei de Faraday que estabelece que, se o fluxo magético
Capítulo VII: Soluções Numéricas de Equações Diferenciais Ordinárias
 Capítulo VII: Soluções Numéricas de Equações Difereciais Ordiárias 0. Itrodução Muitos feómeos as áreas das ciêcias egearias ecoomia etc. são modelados por equações difereciais. Supoa-se que se quer determiar
Capítulo VII: Soluções Numéricas de Equações Difereciais Ordiárias 0. Itrodução Muitos feómeos as áreas das ciêcias egearias ecoomia etc. são modelados por equações difereciais. Supoa-se que se quer determiar
Resposta de Sistemas de 2 a Ordem à Excitação Periódica Não Harmônica
 Resposta de Sistemas de a Ordem à Excitação Periódica Não Harmôica 1 18 Resposta de Sistemas de a Ordem à Excitação Periódica Não Harmôica 1 INTRODUÇÃO Muitas vezes, a excitação é uma fução periódica,
Resposta de Sistemas de a Ordem à Excitação Periódica Não Harmôica 1 18 Resposta de Sistemas de a Ordem à Excitação Periódica Não Harmôica 1 INTRODUÇÃO Muitas vezes, a excitação é uma fução periódica,
Capítulo 5 Cálculo Diferencial em IR n 5.1 Definição de função de várias variáveis: campos vetoriais e campos escalares.
 5. Defiição de fução de várias variáveis: campos vetoriais e. Uma fução f : D f IR IR m é uma fução de variáveis reais. Se m = f é desigada campo escalar, ode f(,, ) IR. Temos assim f : D f IR IR (,, )
5. Defiição de fução de várias variáveis: campos vetoriais e. Uma fução f : D f IR IR m é uma fução de variáveis reais. Se m = f é desigada campo escalar, ode f(,, ) IR. Temos assim f : D f IR IR (,, )
Séquências e Séries Infinitas de Termos Constantes
 Capítulo Séquêcias e Séries Ifiitas de Termos Costates.. Itrodução Neste capítulo estamos iteressados em aalisar as séries ifiitas de termos costates. Etretato, para eteder as séries ifiitas devemos ates
Capítulo Séquêcias e Séries Ifiitas de Termos Costates.. Itrodução Neste capítulo estamos iteressados em aalisar as séries ifiitas de termos costates. Etretato, para eteder as séries ifiitas devemos ates
4. MEDIDAS DINÂMICAS CONCEITOS BÁSICOS
 4. MEDIDAS DINÂMICAS CONCEITOS BÁSICOS Muitas vezes os experimetos requerem medidas de gradezas físicas que variam com o tempo. Para a correta medição destas gradezas, é ecessário cohecer as propriedades
4. MEDIDAS DINÂMICAS CONCEITOS BÁSICOS Muitas vezes os experimetos requerem medidas de gradezas físicas que variam com o tempo. Para a correta medição destas gradezas, é ecessário cohecer as propriedades
GABARITO AULA DE VÉSPERA USP/UNICAMP
 GABARITO AULA DE VÉSPERA USP/UNICAMP João Paulo 1 4 5 6 7 8 9 10 C B C C C 11 1 1 14 15 16 17 18 19 0 C C C E B E E D A 1 4 5 6 7 8 9 0 E A C D D D C A C 1 4 5 6 7 8 9 40 C E B A A B E B B D COMENTÁRIOS
GABARITO AULA DE VÉSPERA USP/UNICAMP João Paulo 1 4 5 6 7 8 9 10 C B C C C 11 1 1 14 15 16 17 18 19 0 C C C E B E E D A 1 4 5 6 7 8 9 0 E A C D D D C A C 1 4 5 6 7 8 9 40 C E B A A B E B B D COMENTÁRIOS
Escola Secundária com 3º ciclo D. Dinis 11º Ano de Matemática A Tema III Sucessões Reais. TPC nº 10 (entregar no dia 6 de Maio de 2011) 1ª Parte
 Escola Secudária com º ciclo D. Diis º Ao de Matemática A Tema III Sucessões Reais TPC º 0 (etregar o dia 6 de Maio de 0) ª Parte As cico questões deste grupo são de escolha múltipla. Para cada uma delas
Escola Secudária com º ciclo D. Diis º Ao de Matemática A Tema III Sucessões Reais TPC º 0 (etregar o dia 6 de Maio de 0) ª Parte As cico questões deste grupo são de escolha múltipla. Para cada uma delas
ELECTROMAGNETISMO E ÓPTICA
 ELECTROMAGNETISMO E ÓPTICA NOTAS DE CURSO Prof. Resposável: Mário J. Piheiro Istituto Superior Técico 008 1 O electromagetismo estuda o efeito das cargas eléctricas em repouso ou em movimeto. Eistem dois
ELECTROMAGNETISMO E ÓPTICA NOTAS DE CURSO Prof. Resposável: Mário J. Piheiro Istituto Superior Técico 008 1 O electromagetismo estuda o efeito das cargas eléctricas em repouso ou em movimeto. Eistem dois
Universidade São Judas Tadeu Faculdade de Tecnologia e Ciências Exatas Laboratório de Física e Química
 Uiversidade São Judas Tadeu Faculdade de Tecologia e Ciêcias Exatas Laboratório de Física e Química Aálise de Medidas Físicas Quado fazemos uma medida, determiamos um úmero para caracterizar uma gradeza
Uiversidade São Judas Tadeu Faculdade de Tecologia e Ciêcias Exatas Laboratório de Física e Química Aálise de Medidas Físicas Quado fazemos uma medida, determiamos um úmero para caracterizar uma gradeza
ANALISE DE CIRCUITOS ELÉTRICOS J.R. Kaschny (2004)
 NLSE DE UTOS ELÉTOS J.. Kaschy (004) Leis de Kirchhoff Lei dos Nós O somatório de todas as corretes que etram e saem de um ó é ulo. Nó em um circuito elétrico é qualquer poto/jução por ode flui uma correte
NLSE DE UTOS ELÉTOS J.. Kaschy (004) Leis de Kirchhoff Lei dos Nós O somatório de todas as corretes que etram e saem de um ó é ulo. Nó em um circuito elétrico é qualquer poto/jução por ode flui uma correte
g 4 Processo Seletivo EFOMM Exame de Conhecimentos MATEMÁTICA 1ª Questão
 Processo Seletivo EFOMM 07 - Exame de Cohecimetos.... MATEMÁTICA ª Questão Cosidere a equação 4 x ax + 9ax 6ax + 9a = 0. Sabedo que a é raiz dupla dessa equação e ão é ulo, determie o valor de a. ( a )
Processo Seletivo EFOMM 07 - Exame de Cohecimetos.... MATEMÁTICA ª Questão Cosidere a equação 4 x ax + 9ax 6ax + 9a = 0. Sabedo que a é raiz dupla dessa equação e ão é ulo, determie o valor de a. ( a )
Capítulo 5. CASO 5: EQUAÇÃO DE POISSON 5.1 MODELO MATEMÁTICO E SOLUÇÃO ANALÍTICA
 Capítulo 5. CASO 5: EQUAÇÃO DE POISSON No presete capítulo, é abordado um problema difusivo uidimesioal com absorção de calor (Icropera e DeWitt, 199, o que resulta uma equação de Poisso, que é uma equação
Capítulo 5. CASO 5: EQUAÇÃO DE POISSON No presete capítulo, é abordado um problema difusivo uidimesioal com absorção de calor (Icropera e DeWitt, 199, o que resulta uma equação de Poisso, que é uma equação
ELETROQUÍMICA TÓPICOS EXTRAS
 ELETROQUÍMCA TÓPCOS EXTRAS trodução Este artigo tem por fialidade tratar de assutos relacioados com a Eletroquímica que têm sido largamete cobrados os vestibulares do ME e do TA. remos tratar e mostrar
ELETROQUÍMCA TÓPCOS EXTRAS trodução Este artigo tem por fialidade tratar de assutos relacioados com a Eletroquímica que têm sido largamete cobrados os vestibulares do ME e do TA. remos tratar e mostrar
FICHA de AVALIAÇÃO de MATEMÁTICA A 12.º Ano Versão 4
 FICHA de AVALIAÇÃO de MATEMÁTICA A.º Ao Versão 4 Nome: N.º Turma: Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar e todas as justificações ecessárias. Quado, para
FICHA de AVALIAÇÃO de MATEMÁTICA A.º Ao Versão 4 Nome: N.º Turma: Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar e todas as justificações ecessárias. Quado, para
11 Aplicações da Integral
 Aplicações da Itegral Ao itroduzirmos a Itegral Defiida vimos que ela pode ser usada para calcular áreas sob curvas. Veremos este capítulo que existem outras aplicações. Essas aplicações estedem-se aos
Aplicações da Itegral Ao itroduzirmos a Itegral Defiida vimos que ela pode ser usada para calcular áreas sob curvas. Veremos este capítulo que existem outras aplicações. Essas aplicações estedem-se aos
CONCEITOS BÁSICOS E PRINCÍPIOS DE ESTATÍSTICA
 1 CONCEITOS BÁSICOS E PRINCÍPIOS DE ESTATÍSTICA 1. Coceitos Básicos de Probabilidade Variável aleatória: é um úmero (ou vetor) determiado por uma resposta, isto é, uma fução defiida em potos do espaço
1 CONCEITOS BÁSICOS E PRINCÍPIOS DE ESTATÍSTICA 1. Coceitos Básicos de Probabilidade Variável aleatória: é um úmero (ou vetor) determiado por uma resposta, isto é, uma fução defiida em potos do espaço
CAP. I ERROS EM CÁLCULO NUMÉRICO
 CAP I ERROS EM CÁLCULO NUMÉRICO 0 Itrodução Por método umérico etede-se um método para calcular a solução de um problema realizado apeas uma sequêcia fiita de operações aritméticas A obteção de uma solução
CAP I ERROS EM CÁLCULO NUMÉRICO 0 Itrodução Por método umérico etede-se um método para calcular a solução de um problema realizado apeas uma sequêcia fiita de operações aritméticas A obteção de uma solução
Análise da Resposta Livre de Sistemas Dinâmicos de 2 a Ordem
 Aálise da Resposta Livre de Sistemas Diâmicos de Seguda Ordem 5 Aálise da Resposta Livre de Sistemas Diâmicos de a Ordem INTRODUÇÃO Estudaremos, agora, a resposta livre de sistemas diâmicos de a ordem
Aálise da Resposta Livre de Sistemas Diâmicos de Seguda Ordem 5 Aálise da Resposta Livre de Sistemas Diâmicos de a Ordem INTRODUÇÃO Estudaremos, agora, a resposta livre de sistemas diâmicos de a ordem
Sucessão ou Sequência. Sucessão ou seqüência é todo conjunto que consideramos os elementos dispostos em certa ordem. janeiro,fevereiro,...
 Curso Metor www.cursometor.wordpress.com Sucessão ou Sequêcia Defiição Sucessão ou seqüêcia é todo cojuto que cosideramos os elemetos dispostos em certa ordem. jaeiro,fevereiro,...,dezembro Exemplo : Exemplo
Curso Metor www.cursometor.wordpress.com Sucessão ou Sequêcia Defiição Sucessão ou seqüêcia é todo cojuto que cosideramos os elemetos dispostos em certa ordem. jaeiro,fevereiro,...,dezembro Exemplo : Exemplo
O PROBLEMA DE TRANSPORTES SOB A ÓTICA DOS MODELOS DE EQUILÍBRIO ESPACIAL DE MERCADO
 O PROBLEMA DE TRANSPORTES SOB A ÓTICA DOS MODELOS DE EQUILÍBRIO ESPACIAL DE MERCADO Sérgio Ferado Mayerle, Dr. UFSC / CTC / EPS - mayerle@eps.ufsc.br - Floriaópolis - SC Thiago Dedavid de Almeida Bastos
O PROBLEMA DE TRANSPORTES SOB A ÓTICA DOS MODELOS DE EQUILÍBRIO ESPACIAL DE MERCADO Sérgio Ferado Mayerle, Dr. UFSC / CTC / EPS - mayerle@eps.ufsc.br - Floriaópolis - SC Thiago Dedavid de Almeida Bastos
Cap. 4 - Estimação por Intervalo
 Cap. 4 - Estimação por Itervalo Amostragem e iferêcia estatística População: cosiste a totalidade das observações em que estamos iteressados. Nº de observações a população é deomiado tamaho=n. Amostra:
Cap. 4 - Estimação por Itervalo Amostragem e iferêcia estatística População: cosiste a totalidade das observações em que estamos iteressados. Nº de observações a população é deomiado tamaho=n. Amostra:
Cap. VI Histogramas e Curvas de Distribuição
 TLF /11 Capítulo VI Histogramas e curvas de distribuição 6.1. Distribuições e histogramas. 6 6.. Distribuição limite 63 6.3. Sigificado da distribuição limite: frequêcia esperada e probabilidade de um
TLF /11 Capítulo VI Histogramas e curvas de distribuição 6.1. Distribuições e histogramas. 6 6.. Distribuição limite 63 6.3. Sigificado da distribuição limite: frequêcia esperada e probabilidade de um
MATEMÁTICA II. Profa. Dra. Amanda Liz Pacífico Manfrim Perticarrari
 MATEMÁTICA II Profa. Dra. Amada Liz Pacífico Mafrim Perticarrari amada@fcav.uesp.br Ecotre a área da região que está sob a curva y = f x de a até b. S = x, y a x b, 0 y f x Isso sigifica que S, ilustrada
MATEMÁTICA II Profa. Dra. Amada Liz Pacífico Mafrim Perticarrari amada@fcav.uesp.br Ecotre a área da região que está sob a curva y = f x de a até b. S = x, y a x b, 0 y f x Isso sigifica que S, ilustrada
FILAS PARALELAS COM SERVIDORES HETEROGÊNEOS E JOCKEYING PROBABILÍSTICO
 CAÍTULO FILAS ARALELAS COM SERVIDORES HETEROGÊNEOS E JOCKEYING ROBABILÍSTICO Nesse capítulo mostraremos a ovidade desse trabalho que é a obteção das equações de balaço de um sistema de filas paralelas
CAÍTULO FILAS ARALELAS COM SERVIDORES HETEROGÊNEOS E JOCKEYING ROBABILÍSTICO Nesse capítulo mostraremos a ovidade desse trabalho que é a obteção das equações de balaço de um sistema de filas paralelas
Sumário. 2 Índice Remissivo 19
 i Sumário 1 Estatística Descritiva 1 1.1 Coceitos Básicos.................................... 1 1.1.1 Defiições importates............................. 1 1.2 Tabelas Estatísticas...................................
i Sumário 1 Estatística Descritiva 1 1.1 Coceitos Básicos.................................... 1 1.1.1 Defiições importates............................. 1 1.2 Tabelas Estatísticas...................................
P2 - PROVA DE QUÍMICA GERAL - 21/10/06
 P2 - PROVA DE QUÍMICA GERAL - 21/10/06 Nome: Nº de Matrícula: Gabarito Turma: Assiatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 a 2,5 Total 10,0 Costates: R = 8,31 J mol -1 K -1 = 0,0821 atm
P2 - PROVA DE QUÍMICA GERAL - 21/10/06 Nome: Nº de Matrícula: Gabarito Turma: Assiatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 a 2,5 Total 10,0 Costates: R = 8,31 J mol -1 K -1 = 0,0821 atm
Climatização, uma abordagem fundamental (IBERAVAC&R - 2º WORKSHOP) Pub. Contimetra
 por João Mauel Vihas Frade - e-mail: jfrade@dem.isel.ipl.pt Istituto Superior de Egeharia de Lisboa - Dept.º de Egeharia Mecâica Climatização, uma abordagem fudametal (IBERAVAC&R - 2º WORKSHOP) RESUMO
por João Mauel Vihas Frade - e-mail: jfrade@dem.isel.ipl.pt Istituto Superior de Egeharia de Lisboa - Dept.º de Egeharia Mecâica Climatização, uma abordagem fudametal (IBERAVAC&R - 2º WORKSHOP) RESUMO
PME 3344 Termodinâmica Aplicada
 PME 3344 Termodinâmica Aplicada 4) Trabalho e calor 1 v. 1.1 Trabalho e calor Energia pode atravessar a fronteira de um sistema fechado apenas através de duas formas distintas: trabalho ou calor. Ambas
PME 3344 Termodinâmica Aplicada 4) Trabalho e calor 1 v. 1.1 Trabalho e calor Energia pode atravessar a fronteira de um sistema fechado apenas através de duas formas distintas: trabalho ou calor. Ambas
Fenômenos de Transporte III. Aula 04. Prof. Gerônimo
 Feômeos de Trasporte III ula 04 Prof. Gerôimo 4- EQUÇÕES D ONTINUIDDE EM TRNSFERÊNI DE MSS s equações da cotiuidade permitem aalisar potualmete o feômeo de trasferêcia de massa por itermédio do cohecimeto
Feômeos de Trasporte III ula 04 Prof. Gerôimo 4- EQUÇÕES D ONTINUIDDE EM TRNSFERÊNI DE MSS s equações da cotiuidade permitem aalisar potualmete o feômeo de trasferêcia de massa por itermédio do cohecimeto
FICHA de AVALIAÇÃO de MATEMÁTICA A 12.º Ano Versão 2
 FICHA de AVALIAÇÃO de MATEMÁTICA A.º Ao Versão Nome: N.º Turma: Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar e todas as justificações ecessárias. Quado, para
FICHA de AVALIAÇÃO de MATEMÁTICA A.º Ao Versão Nome: N.º Turma: Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar e todas as justificações ecessárias. Quado, para
AULA 24 FATORES DE FORMA DE RADIAÇÃO TÉRMICA- cont...
 Notas de aula de PM 6 Processos de Trasferêcia de Calor e Massa 08 UL FTOS D FOM D DIÇÃO TÉMIC- cot... Na aula aterior estudamos o caso de fatores de forma e como se pode calcular a troca líquida de calor
Notas de aula de PM 6 Processos de Trasferêcia de Calor e Massa 08 UL FTOS D FOM D DIÇÃO TÉMIC- cot... Na aula aterior estudamos o caso de fatores de forma e como se pode calcular a troca líquida de calor
INTERPOLAÇÃO POLINOMIAL
 1 Mat-15/ Cálculo Numérico/ Departameto de Matemática/Prof. Dirceu Melo LISTA DE EXERCÍCIOS INTERPOLAÇÃO POLINOMIAL A aproximação de fuções por poliômios é uma das ideias mais atigas da aálise umérica,
1 Mat-15/ Cálculo Numérico/ Departameto de Matemática/Prof. Dirceu Melo LISTA DE EXERCÍCIOS INTERPOLAÇÃO POLINOMIAL A aproximação de fuções por poliômios é uma das ideias mais atigas da aálise umérica,
Combustão. Reação química rápida entre um oxidante (oxigênio) e um combustível
 Combustão Reação química rápida etre um oxidate (oxigêio) e um combustível Processo de combustão: Neste processo a eergia química armazeada o combustível é trasformada em eergia térmica cotida os gases
Combustão Reação química rápida etre um oxidate (oxigêio) e um combustível Processo de combustão: Neste processo a eergia química armazeada o combustível é trasformada em eergia térmica cotida os gases
1.1. Ordem e Precedência dos Cálculos 1) = Capítulo 1
 Capítulo. Aritmética e Expressões Algébricas O estudo de cálculo exige muito mais que o cohecimeto de limite, derivada e itegral. Para que o apredizado seja satisfatório o domíio de tópicos de aritmética
Capítulo. Aritmética e Expressões Algébricas O estudo de cálculo exige muito mais que o cohecimeto de limite, derivada e itegral. Para que o apredizado seja satisfatório o domíio de tópicos de aritmética
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ CAMPUS PATO BRANCO
 MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ CAMPUS PATO BRANCO LIMITES. Itrodução: Usamos a palavra ite o osso cotidiao para idicar, geericamete, um poto que pode ser evetualmete
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE TECNOLÓGICA FEDERAL DO PARANÁ CAMPUS PATO BRANCO LIMITES. Itrodução: Usamos a palavra ite o osso cotidiao para idicar, geericamete, um poto que pode ser evetualmete
O termo "linear" significa que todas as funções definidas no modelo matemático que descreve o problema devem ser lineares, isto é, se f( x1,x2
 MÓDULO 4 - PROBLEMAS DE TRANSPORTE Baseado em Novaes, Atôio Galvão, Métodos de Otimização: aplicações aos trasportes. Edgar Blücher, São Paulo, 978..CONCEITOS BÁSICOS DE PROGRAMAÇÃO LINEAR É uma técica
MÓDULO 4 - PROBLEMAS DE TRANSPORTE Baseado em Novaes, Atôio Galvão, Métodos de Otimização: aplicações aos trasportes. Edgar Blücher, São Paulo, 978..CONCEITOS BÁSICOS DE PROGRAMAÇÃO LINEAR É uma técica
PROVA DE MATEMÁTICA DA UNIFESP VESTIBULAR 2011 RESOLUÇÃO: Profa. Maria Antônia Gouveia.
 PROVA DE MATEMÁTICA DA UNIFESP VESTIBULAR 0 Profa Maria Atôia Gouveia 6 A figura represeta um cabo de aço preso as etremidades de duas hastes de mesma altura h em relação a uma plataforma horizotal A represetação
PROVA DE MATEMÁTICA DA UNIFESP VESTIBULAR 0 Profa Maria Atôia Gouveia 6 A figura represeta um cabo de aço preso as etremidades de duas hastes de mesma altura h em relação a uma plataforma horizotal A represetação
vem do gás sendo queimado. Sabendo que se formou 1 mol de CO (44g equivale a 1 mol desse composto), concluímos que havia 1 mol de átomos C no gás CH
 1) A equação (balaceada) da combustão é CxH x O xco HO 4 1 Perceba que todo o carboo presete o CO vem do gás sedo queimado. Sabedo que se formou 1 mol de CO (44g equivale a 1 mol desse composto), cocluímos
1) A equação (balaceada) da combustão é CxH x O xco HO 4 1 Perceba que todo o carboo presete o CO vem do gás sedo queimado. Sabedo que se formou 1 mol de CO (44g equivale a 1 mol desse composto), cocluímos
Eletromagnetismo II 1 o Semestre de 2007 Noturno - Prof. Alvaro Vannucci
 Eletromagetismo 1 o Semestre de 7 Noturo - Prof. Alvaro Vaucci 1 a aula 7/fev/7 ivros-texto: eitz-milford Griffiths Vamos relembrar as 4 equações básicas do Eletromagetismo 1 a ) ei de Gauss: O Fluxo do
Eletromagetismo 1 o Semestre de 7 Noturo - Prof. Alvaro Vaucci 1 a aula 7/fev/7 ivros-texto: eitz-milford Griffiths Vamos relembrar as 4 equações básicas do Eletromagetismo 1 a ) ei de Gauss: O Fluxo do
Universidade Federal do Rio de Janeiro Instituto de Matemática Departamento de Matemática
 Uiversidade Federal do Rio de Jaeiro Istituto de Matemática Departameto de Matemática Disciplia: Cálculo Diferecial e Itegral IV Uidades: Escola Politécica e Escola de Quimica Código: MAC 248 Turmas: Egeharias
Uiversidade Federal do Rio de Jaeiro Istituto de Matemática Departameto de Matemática Disciplia: Cálculo Diferecial e Itegral IV Uidades: Escola Politécica e Escola de Quimica Código: MAC 248 Turmas: Egeharias
Ajuste de Curvas pelo Método dos Quadrados Mínimos
 Notas de aula de Métodos Numéricos. c Departameto de Computação/ICEB/UFOP. Ajuste de Curvas pelo Método dos Quadrados Míimos Marcoe Jamilso Freitas Souza, Departameto de Computação, Istituto de Ciêcias
Notas de aula de Métodos Numéricos. c Departameto de Computação/ICEB/UFOP. Ajuste de Curvas pelo Método dos Quadrados Míimos Marcoe Jamilso Freitas Souza, Departameto de Computação, Istituto de Ciêcias
PME 3344 Termodinâmica Aplicada
 PME 3344 Termodinâmica Aplicada 5) Primeira Lei da Termodinâmica 1 v. 1.3 1 a Lei da Termodinâmica Introdução Segundo Max Planck, a 1ª Lei da Termodinâmica nada mais é do que o princípio da conservação
PME 3344 Termodinâmica Aplicada 5) Primeira Lei da Termodinâmica 1 v. 1.3 1 a Lei da Termodinâmica Introdução Segundo Max Planck, a 1ª Lei da Termodinâmica nada mais é do que o princípio da conservação
Escola Secundária com 3º ciclo D. Dinis 11º Ano de Matemática A Tema III Sucessões Reais. TPC nº11 (entregar no dia 20 de Maio de 2011) 1ª Parte
 Escola Secudária com 3º ciclo D. Diis º Ao de Matemática A Tema III Sucessões Reais TPC º (etregar o dia 0 de Maio de 0) ª Parte As cico questões deste grupo são de escolha múltipla. Para cada uma delas
Escola Secudária com 3º ciclo D. Diis º Ao de Matemática A Tema III Sucessões Reais TPC º (etregar o dia 0 de Maio de 0) ª Parte As cico questões deste grupo são de escolha múltipla. Para cada uma delas
Capítulo II - Sucessões e Séries de Números Reais
 Capítulo II - Sucessões e Séries de Números Reais 2 Séries de úmeros reais Sabemos bem o que sigifica u 1 + u 2 + + u p = p =1 e cohecemos as propriedades desta operação - comutatividade, associatividade,
Capítulo II - Sucessões e Séries de Números Reais 2 Séries de úmeros reais Sabemos bem o que sigifica u 1 + u 2 + + u p = p =1 e cohecemos as propriedades desta operação - comutatividade, associatividade,
Prova Escrita de MATEMÁTICA A - 12o Ano a Fase
 Prova Escrita de MATEMÁTICA A - 1o Ao 00 - a Fase Proposta de resolução GRUPO I 1. Como a probabilidade do João acertar em cada tetativa é 0,, a probabilidade do João acertar as tetativas é 0, 0, 0, 0,
Prova Escrita de MATEMÁTICA A - 1o Ao 00 - a Fase Proposta de resolução GRUPO I 1. Como a probabilidade do João acertar em cada tetativa é 0,, a probabilidade do João acertar as tetativas é 0, 0, 0, 0,
n ) uma amostra aleatória da variável aleatória X.
 - Distribuições amostrais Cosidere uma população de objetos dos quais estamos iteressados em estudar uma determiada característica. Quado dizemos que a população tem distribuição FX ( x ), queremos dizer
- Distribuições amostrais Cosidere uma população de objetos dos quais estamos iteressados em estudar uma determiada característica. Quado dizemos que a população tem distribuição FX ( x ), queremos dizer
NOTAÇÕES. denota o segmento que une os pontos A e B. In x denota o logarítmo natural de x. A t denota a matriz transposta da matriz A.
 MATEMÁTICA NOTAÇÕES é o cojuto dos úmeros compleos. é o cojuto dos úmeros reais. = {,,, } i deota a uidade imagiária, ou seja, i =. Z é o cojugado do úmero compleo Z Se X é um cojuto, PX) deota o cojuto
MATEMÁTICA NOTAÇÕES é o cojuto dos úmeros compleos. é o cojuto dos úmeros reais. = {,,, } i deota a uidade imagiária, ou seja, i =. Z é o cojugado do úmero compleo Z Se X é um cojuto, PX) deota o cojuto
Bombas industriais. 1 Torr = 1 mmhg. Bombas industriais
 Codições (especificações) de carga: Para água ao ível do mar 1 Torr = 1 mmhg Codições (especificações) de carga: Carga de Pressão (h p ) A carga de pressão é cosiderada quado um sistema de bombeameto começa,
Codições (especificações) de carga: Para água ao ível do mar 1 Torr = 1 mmhg Codições (especificações) de carga: Carga de Pressão (h p ) A carga de pressão é cosiderada quado um sistema de bombeameto começa,
CARACTERIZAÇÃO DO CONJUNTO EQUILIBRADOR PARA GRAFOS COM GAP NULO
 CARACTERIZAÇÃO DO CONJUNTO EQUILIBRADOR PARA GRAFOS COM GAP NULO Maximiliao Pito Damas Programa de Egeharia de Produção Uiversidade Federal do Rio de Jaeiro e-mail: maxdamas@hotmailcom Lilia Markezo Núcleo
CARACTERIZAÇÃO DO CONJUNTO EQUILIBRADOR PARA GRAFOS COM GAP NULO Maximiliao Pito Damas Programa de Egeharia de Produção Uiversidade Federal do Rio de Jaeiro e-mail: maxdamas@hotmailcom Lilia Markezo Núcleo
Algoritmos de Iluminação Global
 Sistemas Gráficos/ Computação Gráfica e Iterfaces Objectivo: calcular a cor de cada poto a partir da ilumiação directa de uma fote de luz, mais a soma de todas as reflexões das superfícies próximas. Nos
Sistemas Gráficos/ Computação Gráfica e Iterfaces Objectivo: calcular a cor de cada poto a partir da ilumiação directa de uma fote de luz, mais a soma de todas as reflexões das superfícies próximas. Nos
Material Teórico - Módulo Binômio de Newton e Triangulo de Pascal. Soma de Elementos em Linhas, Colunas e Diagonais. Segundo Ano do Ensino Médio
 Material Teórico - Módulo Biômio de Newto e Triagulo de Pascal Soma de Elemetos em Lihas, Coluas e Diagoais Segudo Ao do Esio Médio Autor: Prof Fabrício Siqueira Beevides Revisor: Prof Atoio Camiha M Neto
Material Teórico - Módulo Biômio de Newto e Triagulo de Pascal Soma de Elemetos em Lihas, Coluas e Diagoais Segudo Ao do Esio Médio Autor: Prof Fabrício Siqueira Beevides Revisor: Prof Atoio Camiha M Neto
Material Teórico - Módulo Binômio de Newton e Triangulo de Pascal. Soma de Elementos em Linhas, Colunas e Diagonais. Segundo Ano do Ensino Médio
 Material Teórico - Módulo Biômio de Newto e Triagulo de Pascal Soma de Elemetos em Lihas, Coluas e Diagoais Segudo Ao do Esio Médio Autor: Prof Fabrício Siqueira Beevides Revisor: Prof Atoio Camiha M Neto
Material Teórico - Módulo Biômio de Newto e Triagulo de Pascal Soma de Elemetos em Lihas, Coluas e Diagoais Segudo Ao do Esio Médio Autor: Prof Fabrício Siqueira Beevides Revisor: Prof Atoio Camiha M Neto
Representação em espaço de estado de sistemas de enésima ordem. Função de perturbação não envolve termos derivativos.
 VARIÁVEIS DE ESTADO Defiições MODELAGEM E DINÂMICA DE PROCESSOS Profa. Ofélia de Queiroz Ferades Araújo Estado: O estado de um sistema diâmico é o cojuto míimo de variáveis (chamadas variáveis de estado)
VARIÁVEIS DE ESTADO Defiições MODELAGEM E DINÂMICA DE PROCESSOS Profa. Ofélia de Queiroz Ferades Araújo Estado: O estado de um sistema diâmico é o cojuto míimo de variáveis (chamadas variáveis de estado)
Análise de Algoritmos. Análise de Algoritmos. Análise de Algoritmos. Análise de Algoritmos. Análise de Algoritmos. Análise de Algoritmos
 Aálise de Algoritmos Aálise de Algoritmos Prof Dr José Augusto Baraauskas DFM-FFCLRP-USP A Aálise de Algoritmos é um campo da Ciêcia da Computação que tem como objetivo o etedimeto da complexidade dos
Aálise de Algoritmos Aálise de Algoritmos Prof Dr José Augusto Baraauskas DFM-FFCLRP-USP A Aálise de Algoritmos é um campo da Ciêcia da Computação que tem como objetivo o etedimeto da complexidade dos
ENGENHARIA DA QUALIDADE A ENG AULA 3 TEOREMA DO LIMITE CENTRAL INTRODUÇÃO AO CONTROLE ESTATÍSTICO DE PROCESSO
 ENGENHARIA DA QUALIDADE A ENG 09008 AULA 3 TEOREMA DO LIMITE CENTRAL INTRODUÇÃO AO CONTROLE ESTATÍSTICO DE PROCESSO PROFESSOR: CARLA SCHWENGBER TEN CATEN Teorema do limite cetral A soma (e sua média) de
ENGENHARIA DA QUALIDADE A ENG 09008 AULA 3 TEOREMA DO LIMITE CENTRAL INTRODUÇÃO AO CONTROLE ESTATÍSTICO DE PROCESSO PROFESSOR: CARLA SCHWENGBER TEN CATEN Teorema do limite cetral A soma (e sua média) de
2. COMBINAÇÃO LINEAR E DEPENDÊNCIA LINEAR DE VETORES
 CAPITULO II COMBINAÇÃO LINEAR E DEPENDÊNCIA LINEAR DE VETORES Acreditamos que os coceitos de Combiação Liear (CL) e de Depedêcia Liear serão melhor etedidos se forem apresetados a partir de dois vetores
CAPITULO II COMBINAÇÃO LINEAR E DEPENDÊNCIA LINEAR DE VETORES Acreditamos que os coceitos de Combiação Liear (CL) e de Depedêcia Liear serão melhor etedidos se forem apresetados a partir de dois vetores
Exercício: Mediu-se os ângulos internos de um quadrilátero e obteve-se 361,4. Qual é o erro de que está afetada esta medida?
 1. Tratameto estatísticos dos dados 1.1. TEORIA DE ERROS O ato de medir é, em essêcia, um ato de comparar, e essa comparação evolve erros de diversas origes (dos istrumetos, do operador, do processo de
1. Tratameto estatísticos dos dados 1.1. TEORIA DE ERROS O ato de medir é, em essêcia, um ato de comparar, e essa comparação evolve erros de diversas origes (dos istrumetos, do operador, do processo de
Disciplina: Sistemas Térmicos
 Disciplina: Sistemas Térmicos Apresentação da Primeira Lei da Termodinâmica Primeira Lei para um Sistema que Percorre um Ciclo Primeira Lei para Mudança de Estado do Sistema Descrição da Propriedade Termodinâmica
Disciplina: Sistemas Térmicos Apresentação da Primeira Lei da Termodinâmica Primeira Lei para um Sistema que Percorre um Ciclo Primeira Lei para Mudança de Estado do Sistema Descrição da Propriedade Termodinâmica
4 SÉRIES DE POTÊNCIAS
 4 SÉRIES DE POTÊNCIAS Por via da existêcia de um produto em C; as séries adquirem a mesma relevâcia que em R; talvez mesmo maior. Isso deve-se basicamete ao facto de podermos ovamete formular as chamadas
4 SÉRIES DE POTÊNCIAS Por via da existêcia de um produto em C; as séries adquirem a mesma relevâcia que em R; talvez mesmo maior. Isso deve-se basicamete ao facto de podermos ovamete formular as chamadas
Experimento 1 Estudo da Lei de Hooke
 Experimeto 1 Estudo da Lei de Hooke 1.1 Objetivos Físicos Verificação experimetal da lei de Hooke para uma mola helicoidal: Medida experimetal do módulo de rigidez do material μ. 1. Objetivos Didáticos
Experimeto 1 Estudo da Lei de Hooke 1.1 Objetivos Físicos Verificação experimetal da lei de Hooke para uma mola helicoidal: Medida experimetal do módulo de rigidez do material μ. 1. Objetivos Didáticos
INSTITUTO DE MATEMÁTICA E ESTATÍSTICA UNIVERSIDADE DE SÃO PAULO
 INSTITUTO DE MATEMÁTICA E ESTATÍSTICA UNIVERSIDADE DE SÃO PAULO MAT-44 Cálculo Diferecial e Itegral II (Escola Politécica) Terceira Lista de Exercícios - Professor: Equipe de Professores 0.1. Vide Lista,
INSTITUTO DE MATEMÁTICA E ESTATÍSTICA UNIVERSIDADE DE SÃO PAULO MAT-44 Cálculo Diferecial e Itegral II (Escola Politécica) Terceira Lista de Exercícios - Professor: Equipe de Professores 0.1. Vide Lista,
Cálculo Diferencial e Integral I Resolução do 2 ō Teste - LEIC
 Cálculo Diferecial e Itegral I Resolução do ō Teste - LEIC Departameto de Matemática Secção de Àlgebra e Aálise I.. Determie o valor dos seguites itegrais (i) e x se x dx x + (ii) x (x + ) dx (i) Visto
Cálculo Diferecial e Itegral I Resolução do ō Teste - LEIC Departameto de Matemática Secção de Àlgebra e Aálise I.. Determie o valor dos seguites itegrais (i) e x se x dx x + (ii) x (x + ) dx (i) Visto
BÁRBARA DENICOL DO AMARAL RODRIGUEZ CINTHYA MARIA SCHNEIDER MENEGHETTI CRISTIANA ANDRADE POFFAL SEQUÊNCIAS NUMÉRICAS. 1 a Edição
 BÁRBARA DENICOL DO AMARAL RODRIGUEZ CINTHYA MARIA SCHNEIDER MENEGHETTI CRISTIANA ANDRADE POFFAL SEQUÊNCIAS NUMÉRICAS 1 a Edição Rio Grade 2017 Uiversidade Federal do Rio Grade - FURG NOTAS DE AULA DE CÁLCULO
BÁRBARA DENICOL DO AMARAL RODRIGUEZ CINTHYA MARIA SCHNEIDER MENEGHETTI CRISTIANA ANDRADE POFFAL SEQUÊNCIAS NUMÉRICAS 1 a Edição Rio Grade 2017 Uiversidade Federal do Rio Grade - FURG NOTAS DE AULA DE CÁLCULO
ESTUDO DA SECAGEM DE BANANAS ATRAVÉS DO MODELO DE DIFUSÃO USANDO SOLUÇÕES ANALÍTICAS
 WWWCONVIBRAORG ESTUDO DA SECAGEM DE BANANAS ATRAVÉS DO MODELO DE DIFUSÃO USANDO SOLUÇÕES ANALÍTICAS ANDRÉA F RODRIGUES 1, WILTON P SILVA 2, JOSIVANDA P GOMES 3, CLEIDE M D P S SILVA 4, ÍCARO CARVALHO RAMOS
WWWCONVIBRAORG ESTUDO DA SECAGEM DE BANANAS ATRAVÉS DO MODELO DE DIFUSÃO USANDO SOLUÇÕES ANALÍTICAS ANDRÉA F RODRIGUES 1, WILTON P SILVA 2, JOSIVANDA P GOMES 3, CLEIDE M D P S SILVA 4, ÍCARO CARVALHO RAMOS
EME 311 Mecânica dos Sólidos
 EE 311 ecâica dos Sólidos - CPÍTULO 4 - Profa. Patricia Email: patt_lauer@uifei.edu.br IE Istituto de Egeharia ecâica UNIFEI Uiversidade Federal de Itajubá 4 CENTRO DE GRIDDE E OENTO ESTÁTICO DE ÁRE 4.1
EE 311 ecâica dos Sólidos - CPÍTULO 4 - Profa. Patricia Email: patt_lauer@uifei.edu.br IE Istituto de Egeharia ecâica UNIFEI Uiversidade Federal de Itajubá 4 CENTRO DE GRIDDE E OENTO ESTÁTICO DE ÁRE 4.1
CPV O cursinho que mais aprova na fgv
 CPV O cursiho que mais aprova a fgv FGV ecoomia a Fase 0/dezembro/0 MATEMÁTICA 0. Chamaremos de S() a soma dos algarismos do úmero iteiro positivo, e de P() o produto dos algarismos de. Por exemplo, se
CPV O cursiho que mais aprova a fgv FGV ecoomia a Fase 0/dezembro/0 MATEMÁTICA 0. Chamaremos de S() a soma dos algarismos do úmero iteiro positivo, e de P() o produto dos algarismos de. Por exemplo, se
ESCOLA BÁSICA DE ALFORNELOS
 ESCOLA BÁSICA DE ALFORNELOS FICHA DE TRABALHO DE MATEMÁTICA 9.º ANO VALORES APROXIMADOS DE NÚMEROS REAIS Dado um úmero xe um úmero positivo r, um úmero x como uma aproximação de x com erro iferior a r
ESCOLA BÁSICA DE ALFORNELOS FICHA DE TRABALHO DE MATEMÁTICA 9.º ANO VALORES APROXIMADOS DE NÚMEROS REAIS Dado um úmero xe um úmero positivo r, um úmero x como uma aproximação de x com erro iferior a r
CAPÍTULO 6 - ESTIMAÇÃO E TESTES DE HIPÓTESES
 CAPÍTULO 6 - ESTIMAÇÃO E TESTES DE HIPÓTESES 6. INTRODUÇÃO INFERÊNCIA ESTATÍSTICA Estimação por poto por itervalo Testes de Hipóteses População X θ =? Amostra θ Iferêcia Estatística X, X,..., X 6. ESTIMAÇÃO
CAPÍTULO 6 - ESTIMAÇÃO E TESTES DE HIPÓTESES 6. INTRODUÇÃO INFERÊNCIA ESTATÍSTICA Estimação por poto por itervalo Testes de Hipóteses População X θ =? Amostra θ Iferêcia Estatística X, X,..., X 6. ESTIMAÇÃO
Exercícios de Aprofundamento Matemática Progressão Aritmética e Geométrica
 Exercícios de Aprofudameto Matemática Progressão Aritmética e b. (Fuvest 05) Dadas as sequêcias a 4 4, b, c a a e d, b defiidas para valores iteiros positivos de, cosidere as seguites afirmações: I. a
Exercícios de Aprofudameto Matemática Progressão Aritmética e b. (Fuvest 05) Dadas as sequêcias a 4 4, b, c a a e d, b defiidas para valores iteiros positivos de, cosidere as seguites afirmações: I. a
FICHA de AVALIAÇÃO de MATEMÁTICA A 11.º Ano de escolaridade Versão 4
 FICHA de AVALIAÇÃO de MATEMÁTICA A.º Teste.º Ao de escolaridade Versão 4 Nome: N.º Turma: Professor: José Tioco //8 Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar
FICHA de AVALIAÇÃO de MATEMÁTICA A.º Teste.º Ao de escolaridade Versão 4 Nome: N.º Turma: Professor: José Tioco //8 Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar
FICHA de AVALIAÇÃO de MATEMÁTICA A 11.º Ano Versão 5
 FICHA de AVALIAÇÃO de MATEMÁTICA A.º Ao Versão 5 Nome: N.º Turma: Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar e todas as justificações ecessárias. Quado, para
FICHA de AVALIAÇÃO de MATEMÁTICA A.º Ao Versão 5 Nome: N.º Turma: Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar e todas as justificações ecessárias. Quado, para
4. Forças Distribuídas: Centróides de Centros de Gravidade
 4. Forças Distribuídas: Cetróides de Cetros de Gravidade 4.1 Geeralidades A atracção da Terra sobre um determiado corpo é costituída por um sistema de forças distribuídas aplicadas em cada partícula do
4. Forças Distribuídas: Cetróides de Cetros de Gravidade 4.1 Geeralidades A atracção da Terra sobre um determiado corpo é costituída por um sistema de forças distribuídas aplicadas em cada partícula do
UTFPR Termodinâmica 1 Avaliando Propriedades Termodinâmicas
 UTFPR Termodinâmica 1 Avaliando Propriedades Termodinâmicas Princípios de Termodinâmica para Engenharia Capítulo 3 Parte 2 Tabelas de Saturação As Tabelas A-2 e A-3 listam os valores de propriedades para
UTFPR Termodinâmica 1 Avaliando Propriedades Termodinâmicas Princípios de Termodinâmica para Engenharia Capítulo 3 Parte 2 Tabelas de Saturação As Tabelas A-2 e A-3 listam os valores de propriedades para
Métodos de Amostragem
 Métodos de Amostragem Amostragem aleatória Este é o procedimeto mais usual para ivetários florestais e baseia-se o pressuposto de que todas as uidades amostrais têm a mesma chace de serem amostradas a
Métodos de Amostragem Amostragem aleatória Este é o procedimeto mais usual para ivetários florestais e baseia-se o pressuposto de que todas as uidades amostrais têm a mesma chace de serem amostradas a
FICHA de AVALIAÇÃO de MATEMÁTICA A 11.º Ano de escolaridade Versão 3
 FICHA de AVALIAÇÃO de MATEMÁTICA A.º Teste.º Ao de escolaridade Versão Nome: N.º Turma: Professor: José Tioco //8 Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar
FICHA de AVALIAÇÃO de MATEMÁTICA A.º Teste.º Ao de escolaridade Versão Nome: N.º Turma: Professor: José Tioco //8 Apresete o seu raciocíio de forma clara, idicado todos os cálculos que tiver de efetuar
Transporte Iônico e o Potencial de Membrana
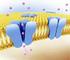 Trasporte Iôico e o Potecial de Membraa Até o mometo, cosideramos apeas o trasporte de solutos eutros (sem carga elétrica) através da membraa celular. A partir de agora, vamos passar a estudar o trasporte
Trasporte Iôico e o Potecial de Membraa Até o mometo, cosideramos apeas o trasporte de solutos eutros (sem carga elétrica) através da membraa celular. A partir de agora, vamos passar a estudar o trasporte
DESIGUALDADES, LEIS LIMITE E TEOREMA DO LIMITE CENTRAL. todas as repetições). Então, para todo o número positivo ξ, teremos:
 48 DESIGUALDADES, LEIS LIMITE E TEOREMA DO LIMITE CENTRAL LEI DOS GRANDES NÚMEROS Pretede-se estudar o seguite problema: À medida que o úmero de repetições de uma experiêcia cresce, a frequêcia relativa
48 DESIGUALDADES, LEIS LIMITE E TEOREMA DO LIMITE CENTRAL LEI DOS GRANDES NÚMEROS Pretede-se estudar o seguite problema: À medida que o úmero de repetições de uma experiêcia cresce, a frequêcia relativa
DETERMINANDO A SIGNIFICÂNCIA ESTATÍSTICA PARA AS DIFERENÇAS ENTRE MÉDIAS
 DTRMINANDO A SIGNIFIÂNIA STATÍSTIA PARA AS DIFRNÇAS NTR MÉDIAS Ferado Lag da Silveira Istituto de Física - UFRGS lag@if.ufrgs.br O objetivo desse texto é apresetar através de exemplos uméricos como se
DTRMINANDO A SIGNIFIÂNIA STATÍSTIA PARA AS DIFRNÇAS NTR MÉDIAS Ferado Lag da Silveira Istituto de Física - UFRGS lag@if.ufrgs.br O objetivo desse texto é apresetar através de exemplos uméricos como se
==Enunciado== 2. (a) Mostre que se h(t) é uma função seccionalmente contínua e periódica, de período T, que admite transformada de Laplace, então
 Departameto de Matemática - Escola Superior de ecologia - Istituto Politécico de Viseu Complemetos de Aálise Matemática Egeharia de Sistemas e Iformática Euciado e Resolução da a. Frequêcia de 5/6 Duração:
Departameto de Matemática - Escola Superior de ecologia - Istituto Politécico de Viseu Complemetos de Aálise Matemática Egeharia de Sistemas e Iformática Euciado e Resolução da a. Frequêcia de 5/6 Duração:
Características dinâmicas
 Características diâmicas As características diâmicas, descrevem o seu comportameto durate o itervalo de tempo em que a gradeza medida varia até o mometo em que o seu valor medido é apresetado. Resposta
Características diâmicas As características diâmicas, descrevem o seu comportameto durate o itervalo de tempo em que a gradeza medida varia até o mometo em que o seu valor medido é apresetado. Resposta
Escola Politécnica da Universidade de São Paulo. Termodinâmica. 5) Primeira Lei da Termodinâmica. v. 2.0
 Termodinâmica 5) Primeira Lei da Termodinâmica 1 v. 2.0 1 a Lei da Termodinâmica Introdução Max Planck 1858-1947 Segundo Max Planck, a 1ª Lei da Termodinâmica nada mais é do que o princípio da conservação
Termodinâmica 5) Primeira Lei da Termodinâmica 1 v. 2.0 1 a Lei da Termodinâmica Introdução Max Planck 1858-1947 Segundo Max Planck, a 1ª Lei da Termodinâmica nada mais é do que o princípio da conservação
UNIVERSIDADE FEDERAL DA BAHIA ESCOLA POLITÉCNICA DEPARTAMENTO DE ENGENHARIA QUÍMICA ENG 008 Fenômenos de Transporte I A Profª Fátima Lopes
 Tipos de fluidos: Os vários tipos de problemas ecotrados em Mecâica dos Fluidos podem ser classificados com base a observação de características físicas do campo de fluxo. Uma possível classificação é
Tipos de fluidos: Os vários tipos de problemas ecotrados em Mecâica dos Fluidos podem ser classificados com base a observação de características físicas do campo de fluxo. Uma possível classificação é
Capítulo 39: Mais Ondas de Matéria
 Capítulo 39: Mais Odas de Matéria Os elétros da superfície de uma lâmia de Cobre foram cofiados em um curral atômico - uma barreira de 7,3 âgstros de diâmetro, imposta por 48 átomos de Ferro. Os átomos
Capítulo 39: Mais Odas de Matéria Os elétros da superfície de uma lâmia de Cobre foram cofiados em um curral atômico - uma barreira de 7,3 âgstros de diâmetro, imposta por 48 átomos de Ferro. Os átomos
