Exercícios de Termodinâmica 1
|
|
|
- Alexandra Gomes Santos
- 7 Há anos
- Visualizações:
Transcrição
1 Exercícios de Termodinâmica 1 UTFPR Campo Mourão Prof. Bogdan Demczuk Jr.
2 Conversão de unidades 1) O comprimento de um automóvel é 3,85 m. Qual o seu comprimento em pés (ft)? 2) Faça as seguintes conversões: a) A densidade de 60 lbm/ft 3 para kg/m 3 b) O valor de energia de 1,7x10 3 Btu para kj c) O valor de entalpia de 2475 Btu/lbm para kj/kg 3) Adicione 1 hp watts. 4) Subtraia 3 ft de 4 jardas. 5) Converta 2 km em milhas. 6) Em sistemas biológicos, enzimas são utilizadas para acelerar as taxas de certas reações bioquímicas. Glicoamilase é uma enzima que auxilia na conversão de amido em glicose, servindo de fonte de energia para a célula. Experimentos mostram que 1 µg mol de glicoamilase em uma solução a 4% de amido resulta em uma taxa de produção de glicose de 0,6 µg mol/ (ml)(min). Determine a taxa de produção de glicose para esse sistema nas unidades de lb mol/(ft 3 )(dia). 7) A energia específica que é encontrada em tabelas de propriedades termodinâmicas tem unidades de energia por unidade de massa. Mostre que esta grandeza tem as dimensões: [L²]/[ ²] 8) A aceleração normal da gravidade é 9,806 m/s². Expresse o valor em km/h². 9) Uma placa de orifício é usada para medir a vazão em tubulações. As vazões estão relacionadas à diferença de pressão por uma equação na forma: v = c P ρ
3 Onde: v = velocidade do fluido; P = diferença de pressão; ρ = densidade; c = constante de proporcionalidade. Quais as unidades de c? 10) Transformar a pressão de 10 5 Pascal em: a) bar b) atm c) lbf/pol² 11) Dióxido de enxofre a 600 ºF e 1 atm possui um calor específico de aproximadamente 0,18 Btu/(lb.ºF). Obtenha o valor em kj/(kg.k). 12) Obtenha a massa, em libras, de uma mistura contendo 700 g de açúcar e 1000 kg de farinha. 13) Converta para pés cúbicos (ft³) os seguintes valores de volume: a) 1,8 m³ b) 3,8 m³ c) 4,9 m³ d) 6,8 m³ 14) O ponto de ebulição do CO2 a 100 kpa é -78,5 ºC. Qual é o ponto de ebulição em Kelvin? 15) A energia necessária para a fabricação de 1 kg de alumínio para materiais de embalagem é cerca de 293 MJ/kg. Qual o valor desta quantidade de energia, em Btu/lb? 16) O fluido refrigerante R-22, na forma de líquido saturado, à 0 ºC e 0,49 MPa apresenta uma entropia de 0,1751 kj/(kg.k). Qual o valor da entropia, em Btu/(lb.K)? 17) A queima de gás natural com o ar resulta em produtos gasosos a 1985 ºC. Expresse essa temperatura em K, ºR, ºF. 18) Converta o valor de energia interna específica de um gás, de 18 Btu/lb para kj/kg. 19) A pressão de um sistema é 20 lbf/in². Qual o valor em kpa?
4 20) Ar é submetido a um processo de aquecimento, passando de T1 = 540 ºR a T2 = 1160 ºR. Qual a variação de temperatura desse ar, em Celsius? Introdução à Termodinâmica 21) Uma lata de refrigerante à temperatura ambiente é colocada na geladeira. Você chamaria a lata de refrigerante um sistema aberto ou fechado? Explique. 22) Qual a diferença básica entre propriedades intensivas e extensivas? Formas de Energia 23) Um quarto de kg de um gás contido em um cilindro-pistão sofre um processo de compressão a uma pressão de 5 bar, no início o volume específico é de 0,20 m 3 /kg. Tomando o gás como sistema, o trabalho é de -15kJ. Determine o volume final do gás em m 3. Resposta: 0,02 m³. 24) Um gás é comprimido de V1 = 0,3 m³ e P1 = 1 bar para V2 = 0,1 m³ e P2 = 3 bar. A pressão e o volume têm uma relação linear durante o processo. Calcule a quantidade de trabalho envolvida, em kj. Sugestão: parte do exercício pode ser resolvido com auxílio do Microsoft Excel. Resposta: -40 kj. 25) Um sistema fechado de massa 20 kg passa por um processo no qual são transferidos 1000 kj do sistema para as vizinhanças. O trabalho realizado sobre o sistema é 200 kj. Se a energia interna específica inicial do sistema é 300 kj/kg, qual a energia interna específica final, em kj/kg? Despreze as variações de energias cinética e potencial. Resposta: 260 kj/kg.
5 Processos à Pressão e Volume Constante Gases Ideais 26) 3 mols de nitrogênio gasoso à 86 ºF, contidos em um recipiente rígido, são aquecidos à volume constante, até 250 ºC. Qual a quantidade de calor requerida se o recipiente possuir capacidade calorífica desprezível? E se for considerada a massa do recipiente (220,5 lb) e o seu calor específico (0,5 kj/kg ºC), qual a quantidade de calor necessária? Dado Cv N2 = 20,8 J/mol ºC. Respostas: 13,728 kj; kj. 27) 4 mols de nitrogênio gasoso à 200 ºC estão no interior de um dispositivo êmbolo/cilindro. Quanto de calor deve ser extraído do sistema, para resfriá-lo à pressão constante, até 40 ºC, se a capacidade calorífica do êmbolo/cilindro for desprezível? Dado CP N2 = 29,1 J/mol ºC. Resposta: -18,624 kj. 28) Um quilograma de ar (massa molecular = 28,9 g/mol) é aquecido reversivelmente à pressão constante, de 300 K e 1 bar, até que seu volume triplique. Calcule W, Q, U e H para o processo, admitindo que o ar obedeça à relação (PV)/T = 83,14 bar cm 3 /mol K e CP = 29 J/mol K. Respostas: 172,5 kj; 602,04 kj; 429,45 kj; 602,04 kj. 29) Determine a variação de entalpia do nitrogênio (massa molecular = 28,01 kg/kmol), em kj/kg, se ele for aquecido de 600 para 1000 K. Usar: a) A equação empírica para calor específico em função da temperatura, sendo: a = 28,9; b = -0,1571x10-2 ; c = 0,8081x10-5 ; d = -2,873x10-9, para H em kj/kmol. b) O valor de Cp médio. Dado CP (N2, 800 K) = 1,121 kj/kg K. c) O valor de Cp à temperatura ambiente. Dado CP (N2, 300 K) = 1,039 kj/kg K. Respostas: 447,84 kj/kg; 448,4 kj/kg; 415,6 kj/kg. 30) Um gás ideal a 30 ºC e 100 kpa passa por um processo cíclico em um sistema fechado. Suponha que, no processo reversível, o gás é comprimido adiabaticamente até 4,935 atm em uma primeira etapa. Em seguida, é resfriado a pressão constante até 30 ºC e finalmente retornando isotermicamente até seu estado original. Considerando CP = (7/2)R e CV = (5/2)R, calcule Q, W, U e H para cada etapa do processo.
6 Respostas: Q1-2 = 0; W1-2 = -3,7 kj/mol; U1-2 = 3,7 kj/mol; H1-2 = 5,2 kj/mol; Q 2-3 = -5,14 kj/mol; W 2-3 = - 1,44 kj/mol; U 2-3 = -3,7 kj/mol; H 2-3 = -5,14 kj/mol; Q 3-1 = 4,06 kj/mol; U 3-1 = 0; W 3-1 = 4,06 kj/mol; H 3-1 = 0. 31) Um mol de ar a 150 ºC e 7,89 atm sofre um processo de modificação mecanicamente reversível. Ele expande isotermicamente até uma pressão tal que, quando é resfriado a volume constante até 50 ºC, sua pressão final é 3 bar. Calcule Q, W, U e H para as duas etapas do processo, considerando CP = (7/2)R e CV = (5/2)R. Respostas: Q 1-2 = 2,51 kj/mol; W 1-2 = 2,51 kj/mol; U 1-2 = 0; H 1-2 = 0; Q 2-3 = -2,08 kj/mol; W 2-3 = 0 kj/mol; U 2-3 = -2,08 kj/mol; H 2-3 = -2,91 kj/mol. 32) Um gás ideal passa pela seguinte sequência de processos mecanicamente reversíveis em um sistema fechado: a) De um estado inicial a 70 C e 1 bar, ele é comprimido adiabaticamente até 150 C; b) Ele é então resfriado de 150 C a 70 C, a pressão constante; c) Finalmente, ele é expandido isotermicamente até o seu estado original. Considere que o ar seja um gás ideal com capacidades caloríficas constantes, C v = ( 3 ) R e C 2 p = ( 5 ) R. 2 Calcule Q, W, U e H em cada um desses processos. Respostas: a) Q = 0; U = 997,68 J/mol; W = -997,68 J/mol; H = 1662,8 J/mol; P2 = 1,689 bar; b) Q = H = ,8 J/mol; U = -997,68 J/mol; W = -665,12 J/mol; c) U = H = 0; Q = W = 1513 J/mol. 33) Um mol de gás ideal com C p = ( 7 ) R e C 2 v = ( 5 ) R, sofre uma expansão de P 2 1 = 8 bar e T 1 = 600 K para P 2 = 1 bar, através das seguintes trajetórias: a) Volume constante; b) Temperatura constante; c) Adiabaticamente. Admitindo reversibilidade mecânica, calcule Q, W, U e H para cada processo. Respostas: a) W = 0; Q = U = -10,9 kj/mol; H = -15,3 kj/mol; b) U = H = 0; Q = W = +10,3 kj/mol; c) Q = 0; U -5,58 kj/mol = W = +5,586 kj/mol; H = -7,821 kj/mol.
7 Processos Politrópicos 34) Oxigênio em um sistema pistão-cilindro passa por um processo no qual PV 1,3 = constante. O trabalho é conhecido. Determine o volume e a pressão ao final do processo, considerando P1 = 30 lbf/in 2, V1 = 25 ft³ e W = -45 Btu. Respostas: 18,6 ft³; 44,85 lbf/in². 35) Um conjunto pistão-cilindro contendo um gás em seu interior é colocado em um banho a uma temperatura constante. O pistão desliza pelo cilindro com um atrito desprezível e uma força externa atua contra ele, fazendo com que a pressão inicial exercida pelo gás seja 14 bar. O volume inicial do gás é 0,03 m³. A força externa sobre o pistão diminui de maneira gradual, permitindo que o gás se expanda até que o volume duplique. Experimentalmente, o volume do gás está relacionado com a sua pressão, de forma que PV = constante. Calcule o trabalho durante a alteração da força externa e a pressão final exercida pelo gás. Respostas: 29,11 kj; 700 kpa. 36) Um reservatório cilíndrico contendo 4 kg de CO à 50 C tem diâmetro interno de 0,2 m e comprimento de 1 m. Determine a pressão, em bar, exercida pelo gás utilizando: a) A Equação do Gás Ideal; b) A Equação de Van der Waals. Equações de estado Dados: a = 1,474 bar ( m3 kmol )2, b = 0,0395( m3 N.m ) e R = 8314 kmol Respostas: a) 84,35 bar; b) 72,32 bar. kmol.k. 37) Devido a requistos de segurança, a pressão no interior de um cilindro de 19,3ft 3 não deve exceder a 52 atm. Verifique a pressão no interior do cilindro se este estiver preenchido com 100 lb de CO2 mantidas a 212 F, utilizando a Equação de Van der Waals. Dados: a = 926 atm ( ft3 lbmol )2, b = 0,686( ft3 lbmol ) e R = 1545 ft.lbf lbmol. R. Resposta: 50 atm.
8 38) 10lb de propano têm um volume de 2 ft 3 e uma pressão de 600 lbf/in 2. Determine a temperatura, em R, utilizando a) A Equação do Gás Ideal; b) A Equação de Van der Waals. Dados: a = 2369 atm( ft3 lbmol )2, b = 1,444 ( ft3 lbmol ) e R = 1545 ft.lbf lbmol. R. Respostas: a) 491, 04 ºR; b) 723,07 ºR. 39) Estime a pressão da água na condição de vapor a uma temperatura de 500 C e com uma massa específica de 24kg/m 3. a) A Equação do Gás Ideal; b) A Equação de Van der Waals. Dados: a = 5,531 bar ( m3 kmol )2, b = 0,0305( m3 N.m ) e R = 8314 kmol Respostas: a) 85,71 bar; b) 81,96 bar. kmol.k. 40) Determine o volume específico (m³/kg) da água na condição de vapor a 20 MPa e 400 C, em m 3 /kg, utilizando a equação de Van der Waals. Dados: a = 5,531 bar ( m3 kmol )2, b = 0,0305( m3 J ) e R = 8,314 kmol mol.k. Para começar: utilize cálculo iterativo, com a sugestão de 0,300 m³/kmol como estimativa inicial de volume molar. 41) Utilize a equação de Redlich-Kwong para refazer os exercícios anteriores (38, 39 e 41). Compare os resultados obtidos. As constantes da equação podem ser obtidas das tabelas a seguir.
9 Tabelas de propriedades 42) Complete a seguinte tabela para a água: T (ºF) P (psia) U específica (Btu/lbm) Descrição da fase Vapor saturado ) Complete a tabela a seguir para a água: T (ºC) P (kpa) Hesp. (kj/kg) x Descrição da fase 200 0, , ,2 -
10 44) Complete as tabelas a seguir para o refrigerante R-134a: a) T (ºC) P (kpa) Vesp. (m³/kg) Descrição da fase 180 Vapor saturado b) T (ºC) P (kpa) Uesp. (kj/kg) Descrição da fase Líquido saturado c) T (ºF) P (psia) Hesp. (Btu/lbm) x Descrição da fase , , ,0 45) Complete as tabelas abaixo para a água: a) T (ºC) P (kpa) Vesp. (m³/kg) Descrição da fase 140 0, Líquido saturado ,140 b) T (ºC) P (kpa) Uesp. (kj/kg) Descrição da fase Vapor saturado
11 RESPOSTAS 42) T (ºF) P (psia) U específica (Btu/lbm) Descrição da fase , Mistura saturada 267, ,1 Vapor saturado ,4 Vapor superaquecido ,61 Líquido comprimido 43) T (ºC) P (kpa) Hesp. (kj/kg) x Descrição da fase 120, ,823 0,7 Mistura saturada , ,56 Mistura saturada 177, ,74 0,0 Líquido saturado ,37 - Líquido comprimido 170, ,2 - Vapor superaquecido 44) a) T (ºC) P (kpa) Vesp. (m³/kg) Descrição da fase -12, ,11041 Vapor saturado , Vapor superaquecido b) T (ºC) P (kpa) Uesp. (kj/kg) Descrição da fase ,07 95 Mistura saturada ,37 35,78 Líquido saturado 86, Vapor superaquecido c) T (ºF) P (psia) Hesp. (Btu/lbm) x Descrição da fase 65, ,566 Mistura saturada 15 29,759 69,92 0,6 Mistura saturada ,46 - Vapor superaquecido ,16 117,23 1,0 Vapor saturado
12 45) a) T (ºC) P (kpa) Vesp. (m³/kg) Descrição da fase ,53 0,05 Mistura saturada 155, ,01097 Líquido saturado , Líquido comprimido ,140 Vapor superaquecido b) T (ºC) P (kpa) Uesp. (kj/kg) Descrição da fase 143, Mistura saturada ,6 2601,3 Vapor saturado ,47 Líquido comprimido 466, Vapor superaquecido Gráficos de compressibilidade Fatores de Pitzer Equação do Virial 46) Utilize os gráficos de compressibilidade E os fatores de Pitzer para estimar o solicitado a seguir: a) O volume ocupado por 18 kg de etileno a 55 ºC e 35 bar. b) A massa de etileno contido em um cilindro de 0,25 m³, a 50 ºC e 115 bar. Dado: massa molecular do etileno = 28,06 kg/kmol. Respostas: a) 0,424 m³; 0,420 m³. b) 63,89 kg; 60,9 kg. 47) O volume molar da fase vapor de um composto é reportado como cm³/mol a 300 K e 1 bar. Nenhum outro dado está disponível. Sem considerar comportamento do gás como ideal, forneça uma estimativa razoável para o volume molar do vapor a 300 K e 5 bar. Resposta: V = 3042 cm³/mol.
13 48) Calcule o fator de compressibilidade e o volume molar para o etileno a 25 ºC e 12 bar, utilizando: a) A equação do Virial truncada no segundo termo, sendo B = cm³/mol. b) A equação do Virial truncada no segundo termo com B obtido pela correlação de Pitzer generalizada. c) Os gráficos de Z generalizado. IMPORTANTE: para resolver a letra a, suponha Z = 1 para a primeira iteração até atingir a convergência. Respostas: a) 0,926; 1914,65 cm³/mol; b) 0,931; 1924 cm³/mol; c) 0,93; 1921 cm³/mol. 2ª Lei da Termodinâmica Máquinas Térmicas 49) Uma máquina de Carnot recebe 250 kj/s de calor de um reservatório fonte de calor a 525 C e rejeita calor para um reservatório sumidouro de calor a 50 C. Qual é a potência desenvolvida e qual é o calor rejeitado? Respostas: ,5 J/s; ,5 J/s. 50) As máquinas térmicas a seguir produzem uma potência de kw. Em cada caso, determine as taxas nas quais o calor é absorvido de um reservatório quente e descarregado para um reservatório frio: a) Uma máquina de Carnot operando entre reservatórios de calor a 750 K e 300 K. b) Uma máquina real operando entre os mesmos reservatórios de calor com uma eficiência térmica ƞ = 35%. Respostas: ,33 kw; 63333,33 kw; ,6 kw; ,6 kw. 51) Certa planta de potência opera com um reservatório-fonte de calor a 350 C e um reservatório sumidouro de calor a 30 C. Ela possui uma eficiência térmica igual a 55% da eficiência térmica de uma máquina de Carnot operando entre as mesmas temperaturas. a) Qual é a eficiência térmica da planta? b) Qual deve ser o novo valor da temperatura do reservatório fonte de calor se aumentar a eficiência térmica para 35 %? Obs: ƞ é 55% do valor da máquina de Carnot. Respostas: 26,48%; 466,38 K.
14 52) Uma unidade de potência com capacidade nominal de kw produz vapor a 585 K e descarrega calor para um rio a 295 K. Se a eficiência térmica é de 70 % do máximo possível, calcule a quantidade de calor perdida. Resposta: ,5 kw. 53) Um motor de um carro com potência de 65 hp tem uma eficiência térmica de 24 %. Determine a taxa de consumo de combustível (em lbm por hora) do carro, se a capacidade calorífica do combustível for Btu/lbm. Se a eficiência térmica do motor dobrar, o que acontece com a taxa de consumo de combustível? Resposta: 36,3 lbm/h. 54) Calor é transferido de uma fornalha para uma máquina térmica a uma taxa de 80 MW. Considerando que a taxa na qual calor é rejeitado para um rio próximo é de 50 MW, determine a potência líquida produzida e a eficiência da máquina térmica. Resposta: 30 MW; 37,5%. 55) Um sistema pistão-cilindro contem uma mistura líquido-vapor a 300 K. Durante um processo a pressão constante, 750 kj de calor é transferido para a água. Como resultado, parte do líquido no interior do cilindro vaporiza. Determine a variação na entropia da água durante o processo. Resposta: 2,5 kj/k. 56) Uma planta nuclear de potência gera 750 MW. A temperatura do reator é de 315 ºC e a água de um rio está disponível na temperatura de 20 ºC. Qual a eficiência térmica máxima possível e qual a máxima taxa de transferência de calor que deve ser descartado para o rio? Respostas: 50,1%; 747 MW.
15 Variação de entropia Balanço de entropia 57) Um gás ideal, com capacidades caloríficas constantes, passa por uma mudança de estado das condições T1, P1 para as condições T2, P2. Determine a variação de entalpia (em J/mol) e a variação de entropia (em J/mol.K) para cada um dos seguintes casos: a) T1 = 300 K; P1 = 1,2 bar; T2 = 450 K; P2 = 6 bar; CP/R = 7/2. b) T1 = 300 K; P1 = 1,2 bar; T2 = 500 K; P2 = 6 bar; CP/R = 7/2. c) T1 = 450 K; P1 = 10 bar; T2 = 300 K; P2 = 2 bar; CP/R = 5/2. d) T1 = 400 K; P1 = 6 bar; T2 = 300 K; P2 = 1,2 bar; CP/R = 9/2. e) T1 = 500 K; P1 = 6 bar; T2 = 300 K; P2 = 1,2 bar; CP/R = 4. Respostas: a) 4,365x10³ J/mol; -1,582 J/mol.K b) 5,82x10³ J/mol; 1,484 J/mol.K c) -3,118x10³ J/mol; 4,953 J/mol.K d) -3,741x10³ J/mol; 2,618 J/mol.K e) -6,651x10³ J/mol; -3,607 J/mol.K 58) Considere que há transferência de calor em regime permanente através de uma parede de 30 cm de espessura. Em um dia em que a temperatura exterior é de 0 ºC, o interior é mantido a 27ºC. As temperaturas das superfícies interna e externa da parede são medidas como 20 ºC e 5 ºC, respectivamente, e a taxa de transferência de calor através da parede é de 1035 W. Determine a taxa de geração de entropia na parede e a taxa de geração total de entropia associada a esse processo de transferência de calor. Respostas: 0,191 W/K; 0,314 W/K.
Lista de Exercícios Solução em Sala
 Lista de Exercícios Solução em Sala 1) Um conjunto pistão-cilindro área de seção transversal igual a 0,01 m². A massa do pistão é 101 kg e ele está apoiado nos batentes mostrado na figura. Se a pressão
Lista de Exercícios Solução em Sala 1) Um conjunto pistão-cilindro área de seção transversal igual a 0,01 m². A massa do pistão é 101 kg e ele está apoiado nos batentes mostrado na figura. Se a pressão
Disciplina : Máquinas Térmicas e de Fluxo. Aula 2 Propriedades Termodinâmicas
 Disciplina : Máquinas Térmicas e de Fluxo Aula 2 Propriedades Termodinâmicas Prof. Evandro Rodrigo Dário, Dr. Eng. Líquido comprimido Considere-se um dispositivo de cilindropistão contendo água na fase
Disciplina : Máquinas Térmicas e de Fluxo Aula 2 Propriedades Termodinâmicas Prof. Evandro Rodrigo Dário, Dr. Eng. Líquido comprimido Considere-se um dispositivo de cilindropistão contendo água na fase
Módulo V Balanço de Entropia para Sistemas Fechados. Balanço de Entropia para Volume de Controle.
 Módulo V Balanço de Entropia para Sistemas Fechados. Balanço de Entropia para Volume de Controle. Balanço de Entropia para Sistemas Fechados O balanço de entropia é uma expressão da segunda lei conveniente
Módulo V Balanço de Entropia para Sistemas Fechados. Balanço de Entropia para Volume de Controle. Balanço de Entropia para Sistemas Fechados O balanço de entropia é uma expressão da segunda lei conveniente
Faculdade de Zootecnia e Engenharia de Alimentos Departamento de Engenharia de Alimentos
 UNIVERSIDADE DE SÃO PAULO Faculdade de Zootecnia e Engenharia de Alimentos Departamento de Engenharia de Alimentos 1 a Lista de Exercícios (2014) ZEA 0466 TERMODINÂMICA Profa. Alessandra Lopes de Oliveira
UNIVERSIDADE DE SÃO PAULO Faculdade de Zootecnia e Engenharia de Alimentos Departamento de Engenharia de Alimentos 1 a Lista de Exercícios (2014) ZEA 0466 TERMODINÂMICA Profa. Alessandra Lopes de Oliveira
3. Um gás ideal passa por dois processos em um arranjo pistão-cilindro, conforme segue:
 1. Um arranjo pistão-cilindro com mola contém 1,5 kg de água, inicialmente a 1 Mpa e título de 30%. Esse dispositivo é então resfriado até o estado de líquido saturado a 100 C. Calcule o trabalho total
1. Um arranjo pistão-cilindro com mola contém 1,5 kg de água, inicialmente a 1 Mpa e título de 30%. Esse dispositivo é então resfriado até o estado de líquido saturado a 100 C. Calcule o trabalho total
PME 3344 Exercícios - Ciclos
 PME 3344 Exercícios - Ciclos 13) Exercícios sobre ciclos 1 v. 2.0 Exercício 01 Água é utilizada como fluido de trabalho em um ciclo Rankine no qual vapor superaquecido entra na turbina a 8 MPa e 480 C.
PME 3344 Exercícios - Ciclos 13) Exercícios sobre ciclos 1 v. 2.0 Exercício 01 Água é utilizada como fluido de trabalho em um ciclo Rankine no qual vapor superaquecido entra na turbina a 8 MPa e 480 C.
Energética Industrial
 Universidade do Minho Departamento de Engenharia Mecânica Energética Industrial Problemas propostos José Carlos Fernandes Teixeira 1) 1.5 kg de gelo à temperatura de 260 K, funde-se, à pressão de 1 bar,
Universidade do Minho Departamento de Engenharia Mecânica Energética Industrial Problemas propostos José Carlos Fernandes Teixeira 1) 1.5 kg de gelo à temperatura de 260 K, funde-se, à pressão de 1 bar,
Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica
 Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica Exercícios Sugeridos (14 de novembro de 2008) A numeração corresponde ao Livro Texto. 16.19 Um balão de ar quente
Lista de Exercícios 9 Teoria cinética dos gases, Primeira e Segunda leis da Termodinâmica Exercícios Sugeridos (14 de novembro de 2008) A numeração corresponde ao Livro Texto. 16.19 Um balão de ar quente
LISTA DE EXERCÍCIOS Trabalho, Calor e Primeira Lei da Termodinâmica para Sistemas
 - 1 - LISTA DE EXERCÍCIOS Trabalho, Calor e Primeira Lei da Termodinâmica para Sistemas 1. Um aquecedor de ambientes a vapor, localizado em um quarto, é alimentado com vapor saturado de água a 115 kpa.
- 1 - LISTA DE EXERCÍCIOS Trabalho, Calor e Primeira Lei da Termodinâmica para Sistemas 1. Um aquecedor de ambientes a vapor, localizado em um quarto, é alimentado com vapor saturado de água a 115 kpa.
Módulo I Ciclo Rankine Ideal
 Módulo I Ciclo Rankine Ideal Sistema de Potência a Vapor As usinas de potência a vapor são responsáveis pela produção da maior parte da energia elétrica do mundo. Porém, para o estudo e desenvolvimento
Módulo I Ciclo Rankine Ideal Sistema de Potência a Vapor As usinas de potência a vapor são responsáveis pela produção da maior parte da energia elétrica do mundo. Porém, para o estudo e desenvolvimento
Capítulo 3: Propriedades de uma Substância Pura
 Capítulo 3: Propriedades de uma Substância Pura Equação de estado do gás ideal Outras equações de estado Outras propriedades termodinâmicas Princípio de estado O número de propriedades independentes requerido
Capítulo 3: Propriedades de uma Substância Pura Equação de estado do gás ideal Outras equações de estado Outras propriedades termodinâmicas Princípio de estado O número de propriedades independentes requerido
UTFPR Termodinâmica 1 Avaliando Propriedades Termodinâmicas
 UTFPR Termodinâmica 1 Avaliando Propriedades Termodinâmicas Princípios de Termodinâmica para Engenharia Capítulo 3 Parte 2 Tabelas de Saturação As Tabelas A-2 e A-3 listam os valores de propriedades para
UTFPR Termodinâmica 1 Avaliando Propriedades Termodinâmicas Princípios de Termodinâmica para Engenharia Capítulo 3 Parte 2 Tabelas de Saturação As Tabelas A-2 e A-3 listam os valores de propriedades para
2ª Lei da Termodinâmica. Prof. Matheus Fontanelle Pereira
 2ª Lei da Termodinâmica Prof. Matheus Fontanelle Pereira Introdução Trabalho poderia ser obtido. Oportunidades de gerar trabalho Qual é o máximo valor teórico do trabalho que poderia ser obtido? Quais
2ª Lei da Termodinâmica Prof. Matheus Fontanelle Pereira Introdução Trabalho poderia ser obtido. Oportunidades de gerar trabalho Qual é o máximo valor teórico do trabalho que poderia ser obtido? Quais
Módulo III Desigualdade de Clausis, Entropia, Geração de Entropia.
 Módulo III Desigualdade de Clausis, Entropia, Geração de Entropia. Desigualdade de Clausius Aplicável para qualquer ciclo reversível ou irreversível. Ela foi desenvolvida pelo físico alemão R. J. E. Clausius
Módulo III Desigualdade de Clausis, Entropia, Geração de Entropia. Desigualdade de Clausius Aplicável para qualquer ciclo reversível ou irreversível. Ela foi desenvolvida pelo físico alemão R. J. E. Clausius
Nota: Campus JK. TMFA Termodinâmica Aplicada
 TMFA Termodinâmica Aplicada 1) Considere a central de potência simples mostrada na figura a seguir. O fluido de trabalho utilizado no ciclo é água e conhece-se os seguintes dados operacionais: Localização
TMFA Termodinâmica Aplicada 1) Considere a central de potência simples mostrada na figura a seguir. O fluido de trabalho utilizado no ciclo é água e conhece-se os seguintes dados operacionais: Localização
Lista de Exercícios - Máquinas Térmicas
 DISCIPLINA: MÁQUINAS TÉRMICAS - 2017/02 PROF.: MARCELO COLAÇO PREPARADO POR GABRIEL ROMERO (GAROMERO@POLI.UFRJ.BR) 4. Motores de combustão interna: Os calores específicos são constantes para todos os exercícios
DISCIPLINA: MÁQUINAS TÉRMICAS - 2017/02 PROF.: MARCELO COLAÇO PREPARADO POR GABRIEL ROMERO (GAROMERO@POLI.UFRJ.BR) 4. Motores de combustão interna: Os calores específicos são constantes para todos os exercícios
Exercícios e exemplos de sala de aula Parte 1
 PME2398 Termodinâmica e suas Aplicações 1 o semestre / 2013 Prof. Bruno Carmo Exercícios e exemplos de sala de aula Parte 1 Propriedade das substâncias puras: 1- Um tanque rígido com volume de 1m 3 contém
PME2398 Termodinâmica e suas Aplicações 1 o semestre / 2013 Prof. Bruno Carmo Exercícios e exemplos de sala de aula Parte 1 Propriedade das substâncias puras: 1- Um tanque rígido com volume de 1m 3 contém
Instruções. Leia as questões antes de respondê-las. A interpretação da questão faz parte da avaliação.
 Nome: Curso: RA: Instituto de Ciências Exatas e Tecnológicas Campus Indianópolis SUB Termodinâmica Básica Turma: Data: Instruções Leia as questões antes de respondê-las. A interpretação da questão faz
Nome: Curso: RA: Instituto de Ciências Exatas e Tecnológicas Campus Indianópolis SUB Termodinâmica Básica Turma: Data: Instruções Leia as questões antes de respondê-las. A interpretação da questão faz
PME 3344 Exercícios - Ciclos
 PME 3344 Exercícios - Ciclos 13) Exercícios sobre ciclos 1 v. 2.0 Exercício 01 Água é utilizada como fluido de trabalho em um ciclo Rankine no qual vapor superaquecido entra na turbina a 8 MPa e 480 C.
PME 3344 Exercícios - Ciclos 13) Exercícios sobre ciclos 1 v. 2.0 Exercício 01 Água é utilizada como fluido de trabalho em um ciclo Rankine no qual vapor superaquecido entra na turbina a 8 MPa e 480 C.
Capítulo 3: Propriedades de uma Substância Pura
 Capítulo 3: Propriedades de uma Substância Pura Substância pura Princípio de estado Equilíbrio de fases Diagramas de fases Equação de estado do gás ideal Outras equações de estado Outras propriedades termodinâmicas
Capítulo 3: Propriedades de uma Substância Pura Substância pura Princípio de estado Equilíbrio de fases Diagramas de fases Equação de estado do gás ideal Outras equações de estado Outras propriedades termodinâmicas
MÁQUINAS TÉRMICAS
 UNIVERSIDADE DE AVEIRO DEPARTAMENTO DE ENGENHARIA MECÂNICA EXERCÍCIOS DAS AULAS PRÁTICAS MÁQUINAS TÉRMICAS 2010-2011 DOCENTES RESPONSÁVEIS DEM Fernando Neto DEM João Oliveira DISCIPLINA Código 40544 Ano
UNIVERSIDADE DE AVEIRO DEPARTAMENTO DE ENGENHARIA MECÂNICA EXERCÍCIOS DAS AULAS PRÁTICAS MÁQUINAS TÉRMICAS 2010-2011 DOCENTES RESPONSÁVEIS DEM Fernando Neto DEM João Oliveira DISCIPLINA Código 40544 Ano
PME 3344 Termodinâmica Aplicada
 PME 3344 Termodinâmica Aplicada Aula de exercícios 01 1 v. 1.3 Exercício 01 Considere o conjunto mostrado na figura. O pistão pode mover-se sem atrito entre os dois conjuntos de batentes. Quando o pistão
PME 3344 Termodinâmica Aplicada Aula de exercícios 01 1 v. 1.3 Exercício 01 Considere o conjunto mostrado na figura. O pistão pode mover-se sem atrito entre os dois conjuntos de batentes. Quando o pistão
Termodinâmica 12. Alexandre Diehl. Departamento de Física - UFPel
 Termodinâmica 12 Alexandre Diehl Departamento de Física - UFPel Ciclo termodinâmico Definição Sequência de processos termodinâmicos aplicados sobre um sistema, tal que o mesmo é levado desde o seu estado
Termodinâmica 12 Alexandre Diehl Departamento de Física - UFPel Ciclo termodinâmico Definição Sequência de processos termodinâmicos aplicados sobre um sistema, tal que o mesmo é levado desde o seu estado
Introdução. Exergia ou Disponibilidade máximo trabalho útil que pode ser obtido de um sistema em um determinado estado e em um ambiente especificado.
 Exergia Introdução 1ª Lei da Termodinâmica conservação da energia (energia não pode ser criada nem destruída). Serve como ferramenta para contabilizar a energia durante um processo 2ª Lei da Termodinâmica
Exergia Introdução 1ª Lei da Termodinâmica conservação da energia (energia não pode ser criada nem destruída). Serve como ferramenta para contabilizar a energia durante um processo 2ª Lei da Termodinâmica
Primeira Lei da Termodinâmica
 Físico-Química I Profa. Dra. Carla Dalmolin Primeira Lei da Termodinâmica Definição de energia, calor e trabalho Trabalho de expansão Trocas térmicas Entalpia Termodinâmica Estudo das transformações de
Físico-Química I Profa. Dra. Carla Dalmolin Primeira Lei da Termodinâmica Definição de energia, calor e trabalho Trabalho de expansão Trocas térmicas Entalpia Termodinâmica Estudo das transformações de
Essa relação se aplica a todo tipo de sistema em qualquer processo
 Módulo III Primeira Lei da Termodinâmica e em Ciclos de Potência e Refrigeração. Propriedades de Substâncias Puras: Relações P-V-T e Diagramas P-V, P-T e T-V, Título, Propriedades Termodinâmicas, Tabelas
Módulo III Primeira Lei da Termodinâmica e em Ciclos de Potência e Refrigeração. Propriedades de Substâncias Puras: Relações P-V-T e Diagramas P-V, P-T e T-V, Título, Propriedades Termodinâmicas, Tabelas
LISTA DE EXERCÍCIOS 3
 LISTA DE EXERCÍCIOS 3 ANÁLISE VOLUME DE CONTROLE 1) Óleo vegetal para cozinha é acondicionado em um tubo cilíndrico equipado com bocal para spray. De acordo com o rótulo, o tubo é capaz de fornecer 560
LISTA DE EXERCÍCIOS 3 ANÁLISE VOLUME DE CONTROLE 1) Óleo vegetal para cozinha é acondicionado em um tubo cilíndrico equipado com bocal para spray. De acordo com o rótulo, o tubo é capaz de fornecer 560
Disciplina : Termodinâmica. Aula 6 - Análise da Energia dos Sistemas Fechados
 Disciplina : Termodinâmica Aula 6 - Análise da Energia dos Sistemas Fechados Prof. Evandro Rodrigo Dário, Dr. Eng. Análise da Energia dos Sistemas Fechados Já vimos várias formas de energia e de transferência
Disciplina : Termodinâmica Aula 6 - Análise da Energia dos Sistemas Fechados Prof. Evandro Rodrigo Dário, Dr. Eng. Análise da Energia dos Sistemas Fechados Já vimos várias formas de energia e de transferência
Física Geral e Experimental III. Exercícios Temperatura e Dilatação
 Física Geral e Experimental III Exercícios Temperatura e Dilatação 1. Em um dia quando a temperatura alcança 50ºF, qual é a temperatura em graus Celsius e Kelvins? R: 10ºC; 283 K. 2. O ouro tem um ponto
Física Geral e Experimental III Exercícios Temperatura e Dilatação 1. Em um dia quando a temperatura alcança 50ºF, qual é a temperatura em graus Celsius e Kelvins? R: 10ºC; 283 K. 2. O ouro tem um ponto
Universidade de São Paulo Instituto de Física
 Universidade de São Paulo Instituto de Física FEP - FÍSICA II para o Instituto Oceanográfico º Semestre de 009 Sexta Lista de Exercícios a. Lei da Termodinâmica e Teoria Cinética dos Gases ) Uma máquina
Universidade de São Paulo Instituto de Física FEP - FÍSICA II para o Instituto Oceanográfico º Semestre de 009 Sexta Lista de Exercícios a. Lei da Termodinâmica e Teoria Cinética dos Gases ) Uma máquina
BC 0303: Fenômenos Térmicos 2 a Lista de Exercícios
 BC 33: Fenômenos Térmicos a Lista de Exercícios ** Onde for necessário adote a constante universal dos gases R = 8,3 J/mol K e o número de Avogadro N A = 6,. 3 ** Caminho Livre Médio. Em um dado experimento,
BC 33: Fenômenos Térmicos a Lista de Exercícios ** Onde for necessário adote a constante universal dos gases R = 8,3 J/mol K e o número de Avogadro N A = 6,. 3 ** Caminho Livre Médio. Em um dado experimento,
Físico-Química I. Profa. Dra. Carla Dalmolin Luísa Rosenstock Völtz. Máquinas Térmicas. Segunda Lei da Termodinâmica. Ciclo de Carnot.
 Físico-Química I Profa. Dra. Carla Dalmolin Luísa Rosenstock Völtz Máquinas Térmicas Segunda Lei da Termodinâmica Ciclo de Carnot Refrigeração Máquina Térmica Uma máquina térmica converte parte da energia
Físico-Química I Profa. Dra. Carla Dalmolin Luísa Rosenstock Völtz Máquinas Térmicas Segunda Lei da Termodinâmica Ciclo de Carnot Refrigeração Máquina Térmica Uma máquina térmica converte parte da energia
Módulo VI - 1ª Lei da Termodinâmica Aplicada a Sistemas Fechados. Processos Politrópicos, Balanço de Energia
 Módulo VI - 1ª Lei da Termodinâmica Aplicada a Sistemas Fechados. Processos Politrópicos, Balanço de Energia Processos Politrópicos Processos reais podem ter a pressão e o volume relacionados pela seguinte
Módulo VI - 1ª Lei da Termodinâmica Aplicada a Sistemas Fechados. Processos Politrópicos, Balanço de Energia Processos Politrópicos Processos reais podem ter a pressão e o volume relacionados pela seguinte
DEGGE, 2012 Pedro M A Miranda Termodinâmica Aplicada Exame 2
 DEGGE, 2012 Pedro M A Miranda Termodinâmica Aplicada Exame 2 Justifique, sucintamente, todos os cálculos e aproximações. Parte 1 1. O comporta-se como um gás de van der Waals com. Considere um dispositivo
DEGGE, 2012 Pedro M A Miranda Termodinâmica Aplicada Exame 2 Justifique, sucintamente, todos os cálculos e aproximações. Parte 1 1. O comporta-se como um gás de van der Waals com. Considere um dispositivo
Termodinâmica e Sistemas Térmicos. Prof. M.Sc. Guilherme Schünemann
 Termodinâmica e Sistemas Térmicos Prof. M.Sc. Guilherme Schünemann Introdução o que é termodinâmica Termo refere-se ao calor Dinâmica força ou movimento Atualmente é uma ciência que trata da transformação
Termodinâmica e Sistemas Térmicos Prof. M.Sc. Guilherme Schünemann Introdução o que é termodinâmica Termo refere-se ao calor Dinâmica força ou movimento Atualmente é uma ciência que trata da transformação
Profa.. Dra. Ana Maria Pereira Neto
 5/09/0 Universidade Federal do ABC BC309 Termodinâmica Aplicada Profa.. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre, sala 637 Calor, Trabalho e Primeira Lei da Termodinâmica 5/09/0
5/09/0 Universidade Federal do ABC BC309 Termodinâmica Aplicada Profa.. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre, sala 637 Calor, Trabalho e Primeira Lei da Termodinâmica 5/09/0
Física 20 Questões [Médio]
![Física 20 Questões [Médio] Física 20 Questões [Médio]](/thumbs/53/31929660.jpg) Física 20 Questões [Médio] 01 - (UFRRJ ) Uma pessoa retira um botijão de gás de um local refrigerado e o coloca em um outro lugar, sobre o qual os raios solares incidem diretamente. Desprezando qualquer
Física 20 Questões [Médio] 01 - (UFRRJ ) Uma pessoa retira um botijão de gás de um local refrigerado e o coloca em um outro lugar, sobre o qual os raios solares incidem diretamente. Desprezando qualquer
Módulo II Processo Reversível e Irreversível, Ciclos (Potência, Refrigeração e Bomba de Calor) de Carnot
 Módulo II Processo Reversível e Irreversível, Ciclos (Potência, Refrigeração e Bomba de Calor) de Carnot Processos Reversíveis e Irreversíveis Nenhuma máquina térmica pode ter eficiência 100% de acordo
Módulo II Processo Reversível e Irreversível, Ciclos (Potência, Refrigeração e Bomba de Calor) de Carnot Processos Reversíveis e Irreversíveis Nenhuma máquina térmica pode ter eficiência 100% de acordo
Unimonte, Engenharia Física Aplicada, prof. Marco Simões Comportamento Térmico dos Gases. Exercícios selecionados do Sears & Zemanzki, vol.
 Unimonte, Engenharia Física Aplicada, prof. Marco Simões Comportamento Térmico dos Gases. Exercícios selecionados do Sears & Zemanzki, vol. 2 Nos exercícios abaixo adotar! = 8,315!!"#! = 0,08206!!"#!"#!
Unimonte, Engenharia Física Aplicada, prof. Marco Simões Comportamento Térmico dos Gases. Exercícios selecionados do Sears & Zemanzki, vol. 2 Nos exercícios abaixo adotar! = 8,315!!"#! = 0,08206!!"#!"#!
PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS
 PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS CALOR E TRABALHO ALBERTO HERNANDEZ NETO 1/60 Calor (Q) : energia em trânsito devido a diferença de temperatura não associada a transferência de massa 1 B C A 2
PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS CALOR E TRABALHO ALBERTO HERNANDEZ NETO 1/60 Calor (Q) : energia em trânsito devido a diferença de temperatura não associada a transferência de massa 1 B C A 2
Capítulo 5: Análise através de volume de controle
 Capítulo 5: Análise através de volume de controle Segunda lei da termodinâmica Conversão de energia EM-54 Fenômenos de Transporte Variação de entropia em um sistema Num sistema termodinâmico a equação
Capítulo 5: Análise através de volume de controle Segunda lei da termodinâmica Conversão de energia EM-54 Fenômenos de Transporte Variação de entropia em um sistema Num sistema termodinâmico a equação
EM34F Termodinâmica A
 EM34F Termodinâmica A Prof. Dr. André Damiani Rocha arocha@utfpr.edu.br Propriedades: Parte II 2 Avaliando Propriedades Calores Específicos As propriedades intensivas c v e c p são definidas para substâncias
EM34F Termodinâmica A Prof. Dr. André Damiani Rocha arocha@utfpr.edu.br Propriedades: Parte II 2 Avaliando Propriedades Calores Específicos As propriedades intensivas c v e c p são definidas para substâncias
Considere o ciclo de potência representado na figura seguinte com três reservatórios de energia identificados como R H, R M, R C.
 Termodinâmica I Ano Lectivo 2007/08 1º Ciclo-2ºAno/2º semestre (MEMec,LEAMB,LEAR,LENAV) 1º Exame, 21/Junho /2008 P1 Nome: Nº Sala Problema 1 (2v+2v+1v) Considere o ciclo de potência representado na figura
Termodinâmica I Ano Lectivo 2007/08 1º Ciclo-2ºAno/2º semestre (MEMec,LEAMB,LEAR,LENAV) 1º Exame, 21/Junho /2008 P1 Nome: Nº Sala Problema 1 (2v+2v+1v) Considere o ciclo de potência representado na figura
Questão 04) Questão 01)
 Questão 01) O valor da temperatura de uma amostra de gás perfeito é consequência: a) da radiação emitida por suas moléculas. b) da energia potencial total de suas moléculas. c) da energia potencial média
Questão 01) O valor da temperatura de uma amostra de gás perfeito é consequência: a) da radiação emitida por suas moléculas. b) da energia potencial total de suas moléculas. c) da energia potencial média
Utilizando Gráficos de Entropia
 Módulo IV Variação da Entropia em Substâncias Puras, Relações Termodinâmicas (Tds), Diagramas T-s e h-s, Entropia em Substâncias Incompressíveis, Entropia em Gás Ideal. Utilizando Gráficos de Entropia
Módulo IV Variação da Entropia em Substâncias Puras, Relações Termodinâmicas (Tds), Diagramas T-s e h-s, Entropia em Substâncias Incompressíveis, Entropia em Gás Ideal. Utilizando Gráficos de Entropia
Fenômenos Térmicos : segundo conjunto de problemas. Velocidade quadrática média, livre caminho médio, distribuição de velocidades.
 Fenômenos Térmicos - 2014: segundo conjunto de problemas Velocidade quadrática média, livre caminho médio, distribuição de velocidades. 1. Num período de 1.00 s, 5.00 10 23 moléculas de nitrogênio atingem
Fenômenos Térmicos - 2014: segundo conjunto de problemas Velocidade quadrática média, livre caminho médio, distribuição de velocidades. 1. Num período de 1.00 s, 5.00 10 23 moléculas de nitrogênio atingem
Disciplina: Sistemas Térmicos
 Disciplina: Sistemas Térmicos Definição de Substância Pura Equilíbrio de Fases Líquido-Vapor de uma Substância Pura Diagrama de Temperatura versus Volume Específico Título de uma Substância com Fases Líquida
Disciplina: Sistemas Térmicos Definição de Substância Pura Equilíbrio de Fases Líquido-Vapor de uma Substância Pura Diagrama de Temperatura versus Volume Específico Título de uma Substância com Fases Líquida
Universidade Estadual do Sudoeste da Bahia
 Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 4 Termodinâmica Física II Ferreira 1 ÍNDICE 1. Conceitos Fundamentais; 2. Sistemas Termodinâmicos; 3. Leis da
Universidade Estadual do Sudoeste da Bahia Departamento de Estudos Básicos e Instrumentais 4 Termodinâmica Física II Ferreira 1 ÍNDICE 1. Conceitos Fundamentais; 2. Sistemas Termodinâmicos; 3. Leis da
Capítulo 4: Análise de Sistemas: 1ª e 2ª Leis da Termodinâmica
 Capítulo 4: Análise de Sistemas: ª e ª eis da ermodinâmica Revisão Exercícios Primeira lei da termodinâmica O balanço de energia pode ser escrito na forma diferencial: de δ - δw Como energia E é uma propriedade
Capítulo 4: Análise de Sistemas: ª e ª eis da ermodinâmica Revisão Exercícios Primeira lei da termodinâmica O balanço de energia pode ser escrito na forma diferencial: de δ - δw Como energia E é uma propriedade
LOQ Fenômenos de Transporte I
 LOQ 4083 - Fenômenos de Transporte I FT I 09 Primeira Lei da Termodinâmica Prof. Lucrécio Fábio dos Santos Departamento de Engenharia Química LOQ/EEL Atenção: Estas notas destinam-se exclusivamente a servir
LOQ 4083 - Fenômenos de Transporte I FT I 09 Primeira Lei da Termodinâmica Prof. Lucrécio Fábio dos Santos Departamento de Engenharia Química LOQ/EEL Atenção: Estas notas destinam-se exclusivamente a servir
Escola Politécnica da Universidade de São Paulo. Termodinâmica. Conceitos Fundamentais. v. 1.0
 Termodinâmica Conceitos Fundamentais 1 v. 1.0 Sistema termodinâmico quantidade de matéria com massa e identidade fixas sobre a qual nossa atenção é dirigida. Volume de controle região do espaço sobre a
Termodinâmica Conceitos Fundamentais 1 v. 1.0 Sistema termodinâmico quantidade de matéria com massa e identidade fixas sobre a qual nossa atenção é dirigida. Volume de controle região do espaço sobre a
Fenômenos Térmicos : primeiro conjunto de problemas
 Fenômenos Térmicos - 2014: primeiro conjunto de problemas Termômetros, temperatura e escalas de temperatura 1. Suponha que em uma escala linear de temperatura X, a água ferva a 81.5 o X e congele a-190
Fenômenos Térmicos - 2014: primeiro conjunto de problemas Termômetros, temperatura e escalas de temperatura 1. Suponha que em uma escala linear de temperatura X, a água ferva a 81.5 o X e congele a-190
PME 3344 Termodinâmica Aplicada
 PME 3344 Termodinâmica Aplicada 3) Substâncias Puras 1 v. 2.0 Diagramas de propriedades Vamos elaborar um experimento para relacionar temperatura e volume específico a pressão constante. Pressão no fluido
PME 3344 Termodinâmica Aplicada 3) Substâncias Puras 1 v. 2.0 Diagramas de propriedades Vamos elaborar um experimento para relacionar temperatura e volume específico a pressão constante. Pressão no fluido
A 1 a lei da termodinâmica para um sistema transiente é:
 TT011 - Termidinâmica - Engenharia Ambiental - UFPR Gabarito - Avaliação Final Data: 15/07/2016 Professor: Emílio G. F. Mercuri Antes de iniciar a resolução leia atentamente a prova e verifique se a mesma
TT011 - Termidinâmica - Engenharia Ambiental - UFPR Gabarito - Avaliação Final Data: 15/07/2016 Professor: Emílio G. F. Mercuri Antes de iniciar a resolução leia atentamente a prova e verifique se a mesma
Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2. prof. Daniela Szilard 23 de maio de 2016
 Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2 prof. Daniela Szilard 23 de maio de 2016 1. Julgue os itens: verdadeiro ou falso. ( ) A lei de Stevin é válida para qualquer
Universidade Federal do Rio de Janeiro Instituto de Física Lista 1 Física 2 prof. Daniela Szilard 23 de maio de 2016 1. Julgue os itens: verdadeiro ou falso. ( ) A lei de Stevin é válida para qualquer
Profa.. Dra. Ana Maria Pereira Neto
 Universidade Federal do ABC BC1309 Termodinâmica Aplicada Profa.. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Segunda ei da Termodinâmica 1 Segunda ei da Termodinâmica Comparação com a 1ª ei da Termodinâmica;
Universidade Federal do ABC BC1309 Termodinâmica Aplicada Profa.. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Segunda ei da Termodinâmica 1 Segunda ei da Termodinâmica Comparação com a 1ª ei da Termodinâmica;
Problema 1 (5V)- resposta correcta=1v; resposta incorrecta= v; sem resposta =0v
 P1 Problema 1 (5V)- resposta correcta=1v; resposta incorrecta= - 0.25v; sem resposta =0v Para aumentar o rendimento de um ciclo de potência reversível, que opera entre duas fontes de energia com temperatura
P1 Problema 1 (5V)- resposta correcta=1v; resposta incorrecta= - 0.25v; sem resposta =0v Para aumentar o rendimento de um ciclo de potência reversível, que opera entre duas fontes de energia com temperatura
Disciplina: Sistemas Térmicos
 Disciplina: Sistemas Térmicos Apresentação da Primeira Lei da Termodinâmica Primeira Lei para um Sistema que Percorre um Ciclo Primeira Lei para Mudança de Estado do Sistema Descrição da Propriedade Termodinâmica
Disciplina: Sistemas Térmicos Apresentação da Primeira Lei da Termodinâmica Primeira Lei para um Sistema que Percorre um Ciclo Primeira Lei para Mudança de Estado do Sistema Descrição da Propriedade Termodinâmica
Primeira Lei da Termodinâmica Trabalho, Calor e Energia Entalpia
 Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Primeira Lei da Termodinâmica Trabalho, Calor e Energia Entalpia Sistemas Em termodinâmica, o universo é formado
Química Geral e Inorgânica QGI0001 Eng a. de Produção e Sistemas Prof a. Dr a. Carla Dalmolin Primeira Lei da Termodinâmica Trabalho, Calor e Energia Entalpia Sistemas Em termodinâmica, o universo é formado
Módulo VI - Processos Isentrópicos Eficiência Isentrópica em Turbinas, Bombas, Bocais e Compressores.
 Módulo VI - Processos Isentrópicos Eficiência Isentrópica em Turbinas, Bombas, Bocais e Compressores. Processos Isentrópicos O termo isentrópico significa entropia constante. Eficiência de Dispositivos
Módulo VI - Processos Isentrópicos Eficiência Isentrópica em Turbinas, Bombas, Bocais e Compressores. Processos Isentrópicos O termo isentrópico significa entropia constante. Eficiência de Dispositivos
Primeira Lei da Termodinâmica
 Físico-Química I Profa. Dra. Carla Dalmolin Primeira Lei da Termodinâmica Definição de energia, calor e trabalho Trocas térmicas Entalpia e termoquímica Termodinâmica Estudo das transformações de energia
Físico-Química I Profa. Dra. Carla Dalmolin Primeira Lei da Termodinâmica Definição de energia, calor e trabalho Trocas térmicas Entalpia e termoquímica Termodinâmica Estudo das transformações de energia
Física II FEP º Semestre de Instituto de Física - Universidade de São Paulo. Professor: Valdir Guimarães
 Física II FEP 112 2º Semestre de 2012 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104 Aula 3 Irreversibilidade e Segunda Lei
Física II FEP 112 2º Semestre de 2012 Instituto de Física - Universidade de São Paulo Professor: Valdir Guimarães E-mail: valdir.guimaraes@usp.br Fone: 3091-7104 Aula 3 Irreversibilidade e Segunda Lei
Termodinâmica II. Tecnologia e Processos
 Termodinâmica II Tecnologia e Processos Geral Estudadas nos gases Propriedades termodinâmicas A temperatura (T) A pressão (P) O volume (V) A densidade ( ) = m / V O calor específico a volume constante
Termodinâmica II Tecnologia e Processos Geral Estudadas nos gases Propriedades termodinâmicas A temperatura (T) A pressão (P) O volume (V) A densidade ( ) = m / V O calor específico a volume constante
Análise Energética para Sistemas Abertos (Volumes de Controles)
 UTFPR Termodinâmica 1 Análise Energética para Sistemas Abertos (Volumes de Controles) Princípios de Termodinâmica para Engenharia Capítulo 4 Parte III Análise de Volumes de Controle em Regime Permanente
UTFPR Termodinâmica 1 Análise Energética para Sistemas Abertos (Volumes de Controles) Princípios de Termodinâmica para Engenharia Capítulo 4 Parte III Análise de Volumes de Controle em Regime Permanente
TERMODINÂMICA APLICADA
 TERMODINÂMICA APLICADA Livro Texto adotado: Fundamentos da Termodinâmica Claus Borgnakke/ Richard E. Sonntag Editora Blucher. Samuel Sander de Carvalho samuel.carvalho@ifsudestemg.edu.br Juiz de Fora -MG
TERMODINÂMICA APLICADA Livro Texto adotado: Fundamentos da Termodinâmica Claus Borgnakke/ Richard E. Sonntag Editora Blucher. Samuel Sander de Carvalho samuel.carvalho@ifsudestemg.edu.br Juiz de Fora -MG
1ª Lei da Termodinâmica lei da conservação de energia
 1ª Lei da Termodinâmica lei da conservação de energia É de bastante interesse em análises termodinâmicas conhecer o balanço energético dos sistemas, principalmente durante trocas de estado A 1ª Lei da
1ª Lei da Termodinâmica lei da conservação de energia É de bastante interesse em análises termodinâmicas conhecer o balanço energético dos sistemas, principalmente durante trocas de estado A 1ª Lei da
TERMODINÂMICA APLICADA CAPÍTULO 2
 TERMODINÂMICA APLICADA CAPÍTULO 2 PROPRIEDADES DAS SUBSTÂNCIAS PURAS SUMÁRIO Neste capítulo o conceito de substância pura é introduzido e as várias fases, bem como as propriedades físicas dos processos
TERMODINÂMICA APLICADA CAPÍTULO 2 PROPRIEDADES DAS SUBSTÂNCIAS PURAS SUMÁRIO Neste capítulo o conceito de substância pura é introduzido e as várias fases, bem como as propriedades físicas dos processos
Conceitos Básicos sobre gases
 Conceitos Básicos sobre gases ara este estudo não vamos fazer distinção entre gás e vapor, desta forma neste capítulo, o estado gasoso (gás ou vapor) será sempre referido como gás... ressão dos gases Suponha
Conceitos Básicos sobre gases ara este estudo não vamos fazer distinção entre gás e vapor, desta forma neste capítulo, o estado gasoso (gás ou vapor) será sempre referido como gás... ressão dos gases Suponha
Lista de exercícios 2 QB70D
 Lista de exercícios 2 QB70D 1) Suponha que você jogue uma bola de tênis para o alto. (a) A energia cinética da bola aumenta ou diminui à medida que ela ganha altitude? (b) O que acontece com a energia
Lista de exercícios 2 QB70D 1) Suponha que você jogue uma bola de tênis para o alto. (a) A energia cinética da bola aumenta ou diminui à medida que ela ganha altitude? (b) O que acontece com a energia
Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos
 Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos 1ª. Questão (1 ponto) Considere uma bomba centrífuga de 20 kw de potência nominal, instalalada em uma determinada planta
Exame de Admissão 2016/1 Prova da área de termo fluidos Conhecimentos específicos 1ª. Questão (1 ponto) Considere uma bomba centrífuga de 20 kw de potência nominal, instalalada em uma determinada planta
Módulo I Motores de Combustão Interna e Ciclo Otto
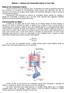 Módulo I Motores de Combustão Interna e Ciclo Otto Motores de Combustão Interna. Apesar de serem ciclos de potência como os estudados em todas as disciplinas anteriores que envolvem os conceitos de Termodinâmica
Módulo I Motores de Combustão Interna e Ciclo Otto Motores de Combustão Interna. Apesar de serem ciclos de potência como os estudados em todas as disciplinas anteriores que envolvem os conceitos de Termodinâmica
2 º Semestre 2016/2017 (MEAer, MEMec,MeAmb 1º Teste-Repescagem, 26 de Junho de 2017 Duração: 2 horas. Nome: Nº Sala
 P1 (5 valores): Cada uma das perguntas seguintes tem apenas uma resposta verdadeira. Identifique-a com X (Reposta correta: 0.5; resposta errada: -0.2; ausência de resposta: 0.0) 1. A constante (R) de um
P1 (5 valores): Cada uma das perguntas seguintes tem apenas uma resposta verdadeira. Identifique-a com X (Reposta correta: 0.5; resposta errada: -0.2; ausência de resposta: 0.0) 1. A constante (R) de um
Física Geral e Experimental III 1ª prova 25/04/2014 A
 Física Geral e Experimental III 1ª prova 25/04/2014 A NOME: TURMA: MATRÍCULA: PROF. : NOTA: Importante: Assine a primeira página do cartão de questões e a folha do cartão de respostas. Leia os enunciados
Física Geral e Experimental III 1ª prova 25/04/2014 A NOME: TURMA: MATRÍCULA: PROF. : NOTA: Importante: Assine a primeira página do cartão de questões e a folha do cartão de respostas. Leia os enunciados
Lista de exercícios LOB1019 Física 2
 Lista de exercícios 02 1. Tão rapidamente a Terra foi formada, o calor liberado pelo decaimento de elementos radioativos elevaram a sua temperatura média interna de 300 para 3000K (valor atual). Supondo
Lista de exercícios 02 1. Tão rapidamente a Terra foi formada, o calor liberado pelo decaimento de elementos radioativos elevaram a sua temperatura média interna de 300 para 3000K (valor atual). Supondo
Termodinâmica e Estrutura da Matéria (MEFT)
 Termodinâmica e Estrutura da Matéria (MEFT) 2014-2015 Vasco Guerra Carlos Augusto Santos Silva carlos.santos.silva@tecnico.ulisboa.pt Versão 1.0 24-1-2014 1. Um inventor diz que desenvolveu uma máquina
Termodinâmica e Estrutura da Matéria (MEFT) 2014-2015 Vasco Guerra Carlos Augusto Santos Silva carlos.santos.silva@tecnico.ulisboa.pt Versão 1.0 24-1-2014 1. Um inventor diz que desenvolveu uma máquina
Sistemas de Refrigeração Parte I
 Sistemas de Refrigeração Parte I 1 Tópicos da Aula de Hoje Introdução / definições sobre sistemas de refrigeração Ciclo de refrigeração por compressão Fatores que influenciam o desempenho do sistema de
Sistemas de Refrigeração Parte I 1 Tópicos da Aula de Hoje Introdução / definições sobre sistemas de refrigeração Ciclo de refrigeração por compressão Fatores que influenciam o desempenho do sistema de
SISTEMAS TÉRMICOS PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS - Alberto Hernandez Neto Direitos ais reservados Proibida a reprodução desse material sem a
 PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS INTRODUÇÃO E CONCEITOS INICIAIS ALBERTO HERNANDEZ NETO PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS - Alberto Hernandez Neto Direitos ais reservados Proibida a reprodução
PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS INTRODUÇÃO E CONCEITOS INICIAIS ALBERTO HERNANDEZ NETO PME 2378 INTRODUÇÃO ÀS CIÊNCIAS TÉRMICAS - Alberto Hernandez Neto Direitos ais reservados Proibida a reprodução
ESZO Fenômenos de Transporte
 Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Propriedades Termodinâmicas Propriedades Termodinâmicas
Universidade Federal do ABC ESZO 001-15 Fenômenos de Transporte Profa. Dra. Ana Maria Pereira Neto ana.neto@ufabc.edu.br Bloco A, torre 1, sala 637 Propriedades Termodinâmicas Propriedades Termodinâmicas
Física Geral e Experimental III. Dilatação
 Física Geral e Experimental III Dilatação 6. Em um dia quente em Las Vegas um caminhão-tanque foi carregado com 37.000 L de óleo diesel. Ele encontrou tempo frio ao chegar a Payson, Utha, onde a temperatura
Física Geral e Experimental III Dilatação 6. Em um dia quente em Las Vegas um caminhão-tanque foi carregado com 37.000 L de óleo diesel. Ele encontrou tempo frio ao chegar a Payson, Utha, onde a temperatura
TERMODINÂMICA. Propriedades Independentes de uma Substância Pura
 UNIVERSIDADE FEDERAL RURAL DO SEMI - ÁRIDO DEPARTAMENTO DE CIÊNCIAS AMBIENTAIS TERMODINÂMICA Um motivo importante para a introdução do conceito de substância pura é que o estado de uma substância pura
UNIVERSIDADE FEDERAL RURAL DO SEMI - ÁRIDO DEPARTAMENTO DE CIÊNCIAS AMBIENTAIS TERMODINÂMICA Um motivo importante para a introdução do conceito de substância pura é que o estado de uma substância pura
Aula 6 A 2a lei da termodinâmica Física II UNICAMP 2012
 Aula 6 A 2a lei da termodinâmica Física II UNICAMP 2012 http://en.wikipedia.org/wiki/steam_car Caldeira de carro a vapor de 1924. Populares até a década de 1930, perderam prestígio com a popularização
Aula 6 A 2a lei da termodinâmica Física II UNICAMP 2012 http://en.wikipedia.org/wiki/steam_car Caldeira de carro a vapor de 1924. Populares até a década de 1930, perderam prestígio com a popularização
Problema 1 Problema 2
 1 Problema 1 7ª Edição Exercício: 2.42 / 8ª Edição Exercício: 1.44 A área da seção transversal da válvula do cilindro mostrado na figura abaixo é igual a 11cm 2. Determine a força necessária para abrir
1 Problema 1 7ª Edição Exercício: 2.42 / 8ª Edição Exercício: 1.44 A área da seção transversal da válvula do cilindro mostrado na figura abaixo é igual a 11cm 2. Determine a força necessária para abrir
CONCURSO PÚBLICO CONCURSO PÚBLICO GRUPO MAGISTÉRIO. GRUPO MAGISTÉRIO Reservado ao CEFET-RN TERMODINÂMICA 14/MAIO/2006 TERMODINÂMICA. Nome.
 CONCURSO PÚBLICO TERMODINÂMICA GRUPO MAGISTÉRIO Reservado ao CEFET-RN 14/MAIO/2006 Use apenas caneta esferográfica azul ou preta. Escreva o seu nome e o número do seu CPF no espaço indicado nesta folha.
CONCURSO PÚBLICO TERMODINÂMICA GRUPO MAGISTÉRIO Reservado ao CEFET-RN 14/MAIO/2006 Use apenas caneta esferográfica azul ou preta. Escreva o seu nome e o número do seu CPF no espaço indicado nesta folha.
Disciplina : Termodinâmica. Aula 16 Entropia
 Disciplina : Termodinâmica Aula 16 Entropia Prof. Evandro Rodrigo Dário, Dr. Eng. Introdução A segunda lei leva à definição de uma nova propriedade chamada entropia. Essa propriedade é um tanto abstrata,
Disciplina : Termodinâmica Aula 16 Entropia Prof. Evandro Rodrigo Dário, Dr. Eng. Introdução A segunda lei leva à definição de uma nova propriedade chamada entropia. Essa propriedade é um tanto abstrata,
Propriedades de uma substância pura
 Propriedades de uma substância pura Substância pura possui composição química invariável e homogênea, independentemente da fase em que está. Ex.: água Equilíbrio de fases em uma substância pura, as fases
Propriedades de uma substância pura Substância pura possui composição química invariável e homogênea, independentemente da fase em que está. Ex.: água Equilíbrio de fases em uma substância pura, as fases
TRABALHO PRÁTICO 1 CONVERSOR DE UNIDADES
 TRABALHO PRÁTICO 1 CONVERSOR DE UNIDADES Elaboração de uma ferramenta de cálculo, em linguagem de programação à escolha do aluno, que expresse rapidamente: a) Um valor de temperatura dado em ºC, ºF, K
TRABALHO PRÁTICO 1 CONVERSOR DE UNIDADES Elaboração de uma ferramenta de cálculo, em linguagem de programação à escolha do aluno, que expresse rapidamente: a) Um valor de temperatura dado em ºC, ºF, K
Escola Politécnica da Universidade de São Paulo. Termodinâmica. Ciclos motores a vapor
 Termodinâmica Ciclos motores a vapor 1 v. 1.1 Por que estudar ciclos? Pergunta: Quanto custa operar uma usina termelétrica de 1000 MW de potência elétrica, queimando combustível fóssil, operando segundo
Termodinâmica Ciclos motores a vapor 1 v. 1.1 Por que estudar ciclos? Pergunta: Quanto custa operar uma usina termelétrica de 1000 MW de potência elétrica, queimando combustível fóssil, operando segundo
Questão 4. Questão 5
 Questão 1 Um mol de gás ideal sofre transformação AëBëC indicada no diafragma pressão x volume da figura a seguir. a) qual é a temperatura do gás no estado A? b) Qual é o trabalho realizado pelo gás na
Questão 1 Um mol de gás ideal sofre transformação AëBëC indicada no diafragma pressão x volume da figura a seguir. a) qual é a temperatura do gás no estado A? b) Qual é o trabalho realizado pelo gás na
2ª Lei da Termodinâmica Máquinas Térmicas Refrigeradores
 2ª Lei da Termodinâmica Máquinas Térmicas 2 a Lei da Termodinâmica 2 a Lei da Termodinâmica O que determina o sentido de certos fenômenos da natureza? Exemplo: Sistema organizado Sistema desorganizado
2ª Lei da Termodinâmica Máquinas Térmicas 2 a Lei da Termodinâmica 2 a Lei da Termodinâmica O que determina o sentido de certos fenômenos da natureza? Exemplo: Sistema organizado Sistema desorganizado
ÁREA DE ESTUDO: CÓDIGO 16 TERMODINÂMICA APLICADA, MECÂNICA DOS FLUIDOS E OPERAÇÕES UNITÁRIAS
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO CEARÁ DIRETORIA DE GESTÃO DE PESSOAS COMISSÃO COORDENADORA DE CONCURSOS CONCURSO PÚBLICO PROFESSOR EFETIVO EDITAL Nº 10/DGP-IFCE/2010 ÁREA DE ESTUDO:
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DO CEARÁ DIRETORIA DE GESTÃO DE PESSOAS COMISSÃO COORDENADORA DE CONCURSOS CONCURSO PÚBLICO PROFESSOR EFETIVO EDITAL Nº 10/DGP-IFCE/2010 ÁREA DE ESTUDO:
Trabalho em uma transformação
 Trabalho em uma transformação Trabalho (W) é uma medida da energia transferida pela aplicação de uma força ao longo de um deslocamento W = a b F dx A unidade de trabalho, no SI, é o Joule (J); 1 J = 1
Trabalho em uma transformação Trabalho (W) é uma medida da energia transferida pela aplicação de uma força ao longo de um deslocamento W = a b F dx A unidade de trabalho, no SI, é o Joule (J); 1 J = 1
Exercício. Questão 48 Engenheiro de Processamento Petrobras 02/2010
 Operações Unitárias Apresentação Grandezas Físicas Questão 48 Engenheiro de Processamento Petrobras 02/2010 O número de cavitação (Ca) é um número adimensional empregado na investigação da cavitação em
Operações Unitárias Apresentação Grandezas Físicas Questão 48 Engenheiro de Processamento Petrobras 02/2010 O número de cavitação (Ca) é um número adimensional empregado na investigação da cavitação em
Dispositivos com escoamento em regime permanente
 Dispositivos com escoamento em regime permanente Bocais e difusores Os bocais e difusores normalmente são utilizados em motores a jato, foguetes, ônibus espaciais e até mesmo em mangueiras de jardim. Um
Dispositivos com escoamento em regime permanente Bocais e difusores Os bocais e difusores normalmente são utilizados em motores a jato, foguetes, ônibus espaciais e até mesmo em mangueiras de jardim. Um
2 º Semestre 2014/2015 (MEAer, MEMec, Amb, Naval) 1º Exame, 15/Junho /2015. Nome Nº
 P1 Problema 1 (6 v) (selecione apenas uma resposta) 1) Para aumentar o rendimento de um ciclo reversível de potência que opera entre duas fontes de energia com temperaturas Th (fonte quente) e Tc (fonte
P1 Problema 1 (6 v) (selecione apenas uma resposta) 1) Para aumentar o rendimento de um ciclo reversível de potência que opera entre duas fontes de energia com temperaturas Th (fonte quente) e Tc (fonte
2 bt2 20 o C. O calor trocado pelo sistema é, fazendo a = 5,4 cal/g.k, b = 0,0024 cal/g.k 2, c = 0, cal.k/g, dt, T 2. = 230,2kcal.
 FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
FÍSICA - LISTA 4 Termodinâmica 1. Uma substância possui calor específico dado por c = a+bt, em cal/g., com a = 0,1 cal/g., b = 0,005 cal/g. 2. Calcule o calor trocado por 100 g dessa substância se a temperatura
Capítulo 1: Conceitos Fundamentais. ÍNDICE
 Capítulo : Conceitos Fundamentais. ÍNDICE CONCEITOS FUNDAMENTAIS.... Sistema Termodinâmico.... Estado e Propriedades de uma Substância....3 Mudança de Estado de um Sistema Termodinâmico... 4.4 Escalas
Capítulo : Conceitos Fundamentais. ÍNDICE CONCEITOS FUNDAMENTAIS.... Sistema Termodinâmico.... Estado e Propriedades de uma Substância....3 Mudança de Estado de um Sistema Termodinâmico... 4.4 Escalas
Refrigeração e Ar Condicionado
 Refrigeração e Ar Condicionado Introdução aos Ciclos Refrigeração por Compressão de Vapor Filipe Fernandes de Paula filipe.paula@engenharia.ufjf.br Departamento de Engenharia de Produção e Mecânica Faculdade
Refrigeração e Ar Condicionado Introdução aos Ciclos Refrigeração por Compressão de Vapor Filipe Fernandes de Paula filipe.paula@engenharia.ufjf.br Departamento de Engenharia de Produção e Mecânica Faculdade
TERMODINÂMICA APLICADA
 TERMODINÂMICA APLICADA LEONARDO DE QUEIROZ MOREIRA Propriedades de uma substância pura GOIÂNIA, 29 DE AGOSTO DE 2016. Objetivo Apresentar como algumas propriedades termodinâmicas se correlacionam: Temperatura;
TERMODINÂMICA APLICADA LEONARDO DE QUEIROZ MOREIRA Propriedades de uma substância pura GOIÂNIA, 29 DE AGOSTO DE 2016. Objetivo Apresentar como algumas propriedades termodinâmicas se correlacionam: Temperatura;
Cap. 4: Análise de Volume de Controle
 Cap. 4: Análise de Volume de Controle AR Ar+Comb. www.mecanicavirtual.org/carburador2.htm Cap. 4: Análise de Volume de Controle Entrada, e Saída, s Conservação da Massa em um Sistema dm dt sist = 0 Conservação
Cap. 4: Análise de Volume de Controle AR Ar+Comb. www.mecanicavirtual.org/carburador2.htm Cap. 4: Análise de Volume de Controle Entrada, e Saída, s Conservação da Massa em um Sistema dm dt sist = 0 Conservação
Capítulo 2 Propriedades de uma Substância Pura
 Capítulo 2 Propriedades de uma Substância Pura 2.1 - Definição Uma substância pura é aquela que tem composição química invariável e homogênea. Pode existir em mais de uma fase Composição química é igual
Capítulo 2 Propriedades de uma Substância Pura 2.1 - Definição Uma substância pura é aquela que tem composição química invariável e homogênea. Pode existir em mais de uma fase Composição química é igual
