É proibido portar celular.
|
|
|
- Teresa Abreu Peres
- 7 Há anos
- Visualizações:
Transcrição
1 Química Avaliação Mensal 1 os anos Décio mar/12 Nome: Nº: Turma: INSTRUÇÕES GERAIS 1. Nenhum material deve estar embaixo das carteiras. Livros e mochilas devem ficar guardados no armário. É proibido portar celular. 2. Sobre a mesa, deixe apenas o material indispensável e aceito para a prova. 3. Verifique se o tampo da sua carteira está limpo. Se não estiver, apague as anotações ou chame o professor. As anotações serão consideradas cola e sua prova será anulada. 4. Em nenhuma hipótese faça cálculos na carteira. 5. Régua, compassos, borracha etc. não podem ser emprestados após o início das provas. 6. Esta prova terá a duração de 60 min. Administre seu tempo. 7. Você só poderá sair da sala depois de transcorridos pelo menos 45 minutos, contados a partir do início da prova. 8. Leia o enunciado das questões de modo atento e cuidadoso. Nenhuma pergunta referente aos enunciados será respondida durante a prova. 9. Atenção para realizar exatamente o que estiver sendo pedido no enunciado de cada questão. Organize suas ideias antes de começar a escrever. Procure ser claro e objetivo em suas respostas. 10. As respostas devem ser feitas com tinta azul ou preta. Não use corretivos. Se extremamente necessário, passe um risco e coloque entre parênteses o trecho a ser anulado. Instruções Específicas 1. Verifique se sua prova contém 5 questões, distribuídas em 7 páginas. 2. Os problemas devem ser feitos a lápis. Resposta final a tinta. 3. Não é permitido o uso de calculadoras. 4. Letra legível é imprescindível. 5. Deixe os processos claramente expostos. Não serão aceitos apenas os resultados. 6. Use do máximo de seu capricho. O que não for entendido não poderá ser corrigido. A sua resposta deve ser clara, completa e precisa. A clareza e precisão da linguagem fazem parte do critério de avaliação. Bom trabalho! É proibido portar celular. 1
2 01. A embalagem de um produto comestível natural traz impresso os seguintes dizeres: isento de elementos químicos. a) Explique por que essa afirmação é incorreta. b) Como ela poderia ser enunciada corretamente? 02. Evidências experimentais mostram que somos capazes, em média, de segurar por um certo tempo um frasco que esteja a uma temperatura de 60 C, sem nos queimarmos. Suponha uma situação em que dois béqueres contendo cada um deles um líquido diferente (X e Y) tenham sido colocados sobre uma chapa elétrica de aquecimento, que está à temperatura de 100 C. A temperatura normal de ebulição do líquido X é 50 C e a do líquido Y é 120 C. a) Após certo tempo de contato com esta chapa, qual dos frascos poderá ser tocado com a mão sem que se corra o risco de sofrer queimaduras? Justifique a sua resposta. b) Se a cada um desses frascos for adicionada quantidade igual de um soluto não volátil, mantendo-se a chapa de aquecimento a 100 C, o que acontecerá com a temperatura de cada um dos líquidos? Explique. 03. Em determinada festa marcada para começar tarde da noite, os convidados começaram a chegar e a conversar. Dina os recepcionava no bar, onde havia dois baldes: um deles com gelo e o outro com gelo seco. Dina bradava aos quatro cantos: "Isso faz a festa tornar-se mais química, já que esses sólidos serão usados para resfriar as bebidas!" Para cada bebida, Clara escolhia o sólido mais apropriado. Curiosamente, alguém pediu duas doses iguais de uísque, uma com gelo e outra com gelo seco, mas colocou os copos em uma mesa e não consumiu as bebidas. Passado um certo tempo, um colega de faculdade resolveu verificar se Dina ainda era a "sabichona" de antigamente e foi logo perguntando: a) "Esses sólidos, quando colocados nas bebidas, sofrem transformações. Que nomes são dados para essas duas transformações? E por que essas transformações fazem com que as bebidas se resfriem?" b) "Dina, veja essas figuras e pense naqueles dois copos de uísque que nosso amigo não bebeu. Qual copo, da situação inicial (x ou y), corresponde ao copo d da situação final? Justifique. 2
3 c) Em algum dos copos, a concentração final de álcool ficou diferente da concentração inicial? Por quê?" Observações: Gelo seco = substância dióxido de carbono (CO 2 ) no estado sólido. Gelo comum = substância água (H 2 O) no estado sólido. Considerar a figura para responder ao item b. 04. A solubilidade do NaCl (sal de cozinha) aumenta com o aumento da temperatura. Sabe-se que, a 0 C, 60 g do sal formam, com água, 260 g de solução saturada. Aquecendo-se a solução a 80 C, a saturação só será mantida se forem acrescentados 20 g do sal. Pede-se: a) Construa (no gráfico representado na folha de respostas) a curva de solubilidade do sal. Deixe todos os cálculos registrados. b) Por meio do gráfico, determine aproximadamente a solubilidade do sal na temperatura de 60º C. c) Que massa de água a 20º C deve ser utilizada para dissolver 1 kg do sal de cozinha? Deixe todos os cálculos registrados. 3
4 05. Uma receita de biscoitinhos Petit Four de laranja leva os seguintes ingredientes: A densidade aparente da "massa" recém-preparada e antes de ser assada é de 1,10 g/cm 3. Entende-se por densidade aparente a relação entre a massa da "massa" ou do ingrediente, na "forma" em que se encontra, e o respectivo volume ocupado. a) Qual o volume ocupado pela "massa" recém-preparada, correspondente a uma receita? b) Como se justifica o fato de a densidade aparente da "massa" ser diferente da média ponderada das densidades aparentes dos constituintes? 4
5 Química Gabarito Avaliação Mensal 1 os anos Décio mar/12 Nome: Nº: Turma: 1. a) (0,5) Todas as substâncias são constituídas de elementos químicos, portanto não existe nenhum produto isento de substâncias químicas. b) (0,5) Isento de adição de aditivos ou conservantes. 2. a) (0,5) A chapa está a 100 o C; portanto, quando o líquido X atingir sua TE (50 o C), ele começa a mudar de estado físico, líquido para gasoso, e durante a mudança de estado a temperatura permanece constante, e assim podemos segurar o frasco sem nos queimarmos. Já com o líquido Y (TE = 120 o C) não é possível segurar o frasco, pois ele atinge uma temperatura maior do que podemos suportar. b) (0,5) A TE do líquido X sofre um aumento e a do líquido Y não sofre alteração. As partículas do soluto dificultam a passagem do estado líquido para o gasoso, aumentando, assim, a TE do líquido X. Como a chapa permanece em 100 o C, a TE do líquido Y não é atingida, mantendose o líquido a 100 o C, e a adição do soluto não altera essa temperatura. 3. a) (1,0) A transformação H 2 O (s) H 2 O (l) é chamada de fusão, já CO 2(s) CO 2(g) é chamada de sublimação. As bebidas se resfriam porque essas transformações são endotérmicas, ou seja, absorvem energia do sistema, resfriando as bebidas. 5
6 b) (1,0) A situação X corresponde à situação D. Na situação X, o CO 2 é mais denso que a bebida, permanecendo no fundo do copo. Quando o gelo seco começa a mudar de estado, ele passa diretamente para o estado gasoso, diminuindo, portanto, o nível do líquido no copo. c) (1,0) No copo que contém gelo, quando este muda de estado (S L), modifica a concentração de álcool, pois ocorre uma diluição. No copo que contém gelo seco, este vai para o estado gasoso, não alterando a concentração de álcool. 4. a) (1,0) b) (1,0) Por meio do gráfico, percebemos que a 60 o C dissolvem-se aproximadamente 37 g do soluto em 100 g de água. c) (1,0) A 20 0 C, temos: 32 g de sal 100 g de água 1000 g de sal X X = 3125 g de água 6
7 5. a) (1,0) Massa total = = 660 g. D = m/v, portanto: v = m/d, v = 660 g/1, 1 gcm -3, v = 600 cm 3 b) (1,0) De acordo com a definição de densidade aparente dada no texto, vemos que a massa ocupa certo volume na forma em que se encontra. Os ingredientes, depois de misturados, formam uma nova substância que pode ter o volume modificado, isso porque se estabelecem novas interações entre as partículas, aumentando ou diminuindo o volume, explicando, assim, essa aparente contradição. 7
É PROIBIDO PORTAR CELULAR.
 Química Avaliação Mensal 1 os anos Décio maio/12 Nome: Nº: Turma: INSTRUÇÕES GERAIS 1. Nenhum material deve estar embaixo das carteiras. Livros e mochilas devem ficar guardados no armário. 2. Sobre a mesa,
Química Avaliação Mensal 1 os anos Décio maio/12 Nome: Nº: Turma: INSTRUÇÕES GERAIS 1. Nenhum material deve estar embaixo das carteiras. Livros e mochilas devem ficar guardados no armário. 2. Sobre a mesa,
Nome: Nº: Turma: INSTRUÇÕES GERAIS. Instruções Específicas
 Química Avaliação os anos Rodrigo mar/1 Nome: Nº: Turma: INSTRUÇÕES GERAIS 1. Nenhum material deve estar embaixo das carteiras. Livros e mochilas devem ficar guardados no armário. É proibido portar celular..
Química Avaliação os anos Rodrigo mar/1 Nome: Nº: Turma: INSTRUÇÕES GERAIS 1. Nenhum material deve estar embaixo das carteiras. Livros e mochilas devem ficar guardados no armário. É proibido portar celular..
Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g)
 Aula 04 1/abr Marcelo Conteúdo EXTRA-classe: Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g) Fenômeno físico: não altera a natureza
Aula 04 1/abr Marcelo Conteúdo EXTRA-classe: Transformações da matéria: qualquer modificação que ocorra com a matéria é considerada uma fenômeno. Ex: H 2 O (l) H 2 O (g) Fenômeno físico: não altera a natureza
1) As substâncias puras benzeno, clorofórmio, hexano e álcool etílico encontram-se em frascos identificados apenas pelas letras A, B, C e D.
 Química Gabarito Avaliação de Sala 1B 1 os anos Décio mar/12 Nome: Nº: Turma: 1) As substâncias puras benzeno, clorofórmio, hexano e álcool etílico encontram-se em frascos identificados apenas pelas letras
Química Gabarito Avaliação de Sala 1B 1 os anos Décio mar/12 Nome: Nº: Turma: 1) As substâncias puras benzeno, clorofórmio, hexano e álcool etílico encontram-se em frascos identificados apenas pelas letras
Aluno(a): Código: 2 Rua T-53 Qd. 92 Lt. 10/11 nº 1356 Setor Bueno
 Aluno(a): Código: Série: 1ª Turma: Data: / / 01. Em 1911, Rutherford e colaboradores realizaram o experimento mostrado na figura abaixo: 02. Os fogos de artifício propiciam espetáculos em diferentes eventos.
Aluno(a): Código: Série: 1ª Turma: Data: / / 01. Em 1911, Rutherford e colaboradores realizaram o experimento mostrado na figura abaixo: 02. Os fogos de artifício propiciam espetáculos em diferentes eventos.
FORMULÁRIO DE DIVULGAÇÃO DO CONTEÚDO DA PROVA FINAL E RECUPERAÇÃO FINAL
 FORMULÁRIO DE DIVULGAÇÃO DO CONTEÚDO DA PROVA FINAL E RECUPERAÇÃO FINAL A) SÉRIE/ANO: 2º Ano Médio B) DISCIPLINA: Química - Enio C) CONTEÚDO A SER EXIGIDO/ORIENTAÇÃO PARA O ESTUDO: SOLUÇÕES: Coeficiente
FORMULÁRIO DE DIVULGAÇÃO DO CONTEÚDO DA PROVA FINAL E RECUPERAÇÃO FINAL A) SÉRIE/ANO: 2º Ano Médio B) DISCIPLINA: Química - Enio C) CONTEÚDO A SER EXIGIDO/ORIENTAÇÃO PARA O ESTUDO: SOLUÇÕES: Coeficiente
3.1. Estados físicos e mudanças de estado
 3.1. Estados físicos e mudanças de estado Os estados físicos da matéria Os materiais, à temperatura ambiente, podem encontrar-se, fundamentalmente, em três estados físicos: estado sólido, estado líquido
3.1. Estados físicos e mudanças de estado Os estados físicos da matéria Os materiais, à temperatura ambiente, podem encontrar-se, fundamentalmente, em três estados físicos: estado sólido, estado líquido
INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO
 2º EM Química A Priscila Av. Dissertativa 30/03/16 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta
2º EM Química A Priscila Av. Dissertativa 30/03/16 INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA LEIA COM MUITA ATENÇÃO 1. Verifique, no cabeçalho desta prova, se seu nome, número e turma estão corretos. 2. Esta
É proibido portar celular
 Química Teste/Prova os anos Rodrigo abr/ Nome: Nº: Turma: INSTRUÇÕES GERAIS. Nenhum material deve estar embaixo das carteiras. Livros e mochilas devem ficar guardados no armário.. Sobre a mesa, deixe apenas
Química Teste/Prova os anos Rodrigo abr/ Nome: Nº: Turma: INSTRUÇÕES GERAIS. Nenhum material deve estar embaixo das carteiras. Livros e mochilas devem ficar guardados no armário.. Sobre a mesa, deixe apenas
PROVA DE QUÍMICA 1 o TRIMESTRE DE 2015
 PROVA DE QUÍMICA 1 o TRIMESTRE DE 2015 PROF. MARCOS NOME Nº 9º ANO A prova deve ser feita com caneta azul ou preta. É terminantemente proibido o uso de corretor. Respostas com corretor serão anuladas.
PROVA DE QUÍMICA 1 o TRIMESTRE DE 2015 PROF. MARCOS NOME Nº 9º ANO A prova deve ser feita com caneta azul ou preta. É terminantemente proibido o uso de corretor. Respostas com corretor serão anuladas.
AVALIAÇÃO OBJETIVA DE FÍSICA E GEOGRAFIA
 CENTRO EDUCACIONAL CHARLES DARWIN AVALIAÇÃO OBJETIVA DE FÍSICA E GEOGRAFIA Segunda Avaliação 2ª Série Ensino Médio Primeiro Período 2016 Assinale com um X se estiver fazendo Progressão Parcial: Aluno(a):
CENTRO EDUCACIONAL CHARLES DARWIN AVALIAÇÃO OBJETIVA DE FÍSICA E GEOGRAFIA Segunda Avaliação 2ª Série Ensino Médio Primeiro Período 2016 Assinale com um X se estiver fazendo Progressão Parcial: Aluno(a):
Colégio Santa Dorotéia
 Colégio Santa Dorotéia Área de Ciências da Natureza Disciplina: Ciências Ano: 9º - Ensino Fundamental Professoras: Flávia Lage e Isabela Monteiro Ciências Atividades para Estudos Autônomos Data: 3 / 4
Colégio Santa Dorotéia Área de Ciências da Natureza Disciplina: Ciências Ano: 9º - Ensino Fundamental Professoras: Flávia Lage e Isabela Monteiro Ciências Atividades para Estudos Autônomos Data: 3 / 4
Aluno(a): Código: 2 Rua T-53 Qd. 92 Lt. 10/11 nº 1356 Setor Bueno
 Aluno(a):_ Código: Série: 1ª Turma: Data: / / 03. Em 1911, Rutherford e colaboradores realizaram o experimento mostrado na figura abaixo: 01. Analise a descrição dos modelos atômicos apresentada a seguir.
Aluno(a):_ Código: Série: 1ª Turma: Data: / / 03. Em 1911, Rutherford e colaboradores realizaram o experimento mostrado na figura abaixo: 01. Analise a descrição dos modelos atômicos apresentada a seguir.
Gabarito Resolvido de Química (12/03/2008) A tabela abaixo apresenta dados referentes a todas as questões da prova (pressão igual a 1 atm).
 Química 1 ano Teste/Prova Rodrigo mar/08 Gabarito Resolvido de Química (12/03/2008) A tabela abaixo apresenta dados referentes a todas as questões da prova (pressão igual a 1 atm). substância densidade
Química 1 ano Teste/Prova Rodrigo mar/08 Gabarito Resolvido de Química (12/03/2008) A tabela abaixo apresenta dados referentes a todas as questões da prova (pressão igual a 1 atm). substância densidade
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO
 UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
UNIVERSIDADE DO ESTADO DO RIO DE JANEIRO INSTITUTO DE QUÍMICA PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA PROVA DE SELEÇÃO/2011 DO CURSO DE MESTRADO 08/11/2010 PROVA ESCRITA Assinatura do candidato: Área de concentração:
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. DISCIPLINA:Química SÉRIE: 1º. ALUNO(a):
 GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 1º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 1º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
Química. Atividade 1 Recuperação 1 os anos Décio ago/09. Nome: Nº: Turma:
 Química Atividade 1 Recuperação 1 os anos Décio ago/09 Nome: Nº: Turma: Objetivo O objetivo dessa ficha é revisar alguns dos conceitos importantes para a prova de recuperação do 1º semestre. As dúvidas
Química Atividade 1 Recuperação 1 os anos Décio ago/09 Nome: Nº: Turma: Objetivo O objetivo dessa ficha é revisar alguns dos conceitos importantes para a prova de recuperação do 1º semestre. As dúvidas
Figura 1: Potencial químico de um solvente na presença de um soluto.
 Propriedades Coligativas 1. Introdução Algumas propriedades do solvente mudam quando um soluto é dissolvido nele para formar uma solução. O ponto de congelamento da água salgada, por exemplo, é menor que
Propriedades Coligativas 1. Introdução Algumas propriedades do solvente mudam quando um soluto é dissolvido nele para formar uma solução. O ponto de congelamento da água salgada, por exemplo, é menor que
Colégio São Paulo-Teresópolis/RJ. Disciplina: Ciências Data: /09/2014 Prof: Carolina série/ano: 6 o Ensino: Fundamental II. Exercícios ( ) Prova:( )
 Colégio São Paulo-Teresópolis/RJ Disciplina: Ciências Data: /09/2014 Prof: Carolina série/ano: 6 o Ensino: Fundamental II Nota Exercícios ( ) Prova:( ) GABARITO 1 Leia a definição e responda: ESTUDO DIRIGIDO
Colégio São Paulo-Teresópolis/RJ Disciplina: Ciências Data: /09/2014 Prof: Carolina série/ano: 6 o Ensino: Fundamental II Nota Exercícios ( ) Prova:( ) GABARITO 1 Leia a definição e responda: ESTUDO DIRIGIDO
EXPERIÊNCIA Nº 2: DETERMINAÇÃO DA TEMPERATURA DE FUSÃO DE SUBSTÂNCIAS
 UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química EXPERIÊNCIA Nº 2: DETERMINAÇÃO DA TEMPERATURA DE FUSÃO DE SUBSTÂNCIAS 1. Introdução: O processo de mudança de estado físico, do
UFSC Departamento de Química QMC 5119 Introdução ao Laboratório de Química EXPERIÊNCIA Nº 2: DETERMINAÇÃO DA TEMPERATURA DE FUSÃO DE SUBSTÂNCIAS 1. Introdução: O processo de mudança de estado físico, do
Colégio Santa Dorotéia Área de Ciências da Natureza Disciplina: Química Ano: 1 o Ensino Médio Professora: Karine R. de Almeida
 Área de Ciências da Natureza Disciplina: Ano: 1 o Ensino Médio Professora: Karine R. de Almeida Atividades para Estudos Autônomos Data: 3 / 4 / 2019 QUESTÃO 1 (KRA-2019) Aluno(a): N o : Turma: ATIVIDADES
Área de Ciências da Natureza Disciplina: Ano: 1 o Ensino Médio Professora: Karine R. de Almeida Atividades para Estudos Autônomos Data: 3 / 4 / 2019 QUESTÃO 1 (KRA-2019) Aluno(a): N o : Turma: ATIVIDADES
Experiência 2: Temperatura de fusão de uma substância
 Experiência 2: de fusão de uma substância 1. Objetivos Ao final desta atividade experimental espera-se que os alunos sejam capazes de: - Identificar compostos e determinar suas purezas usando pontos de
Experiência 2: de fusão de uma substância 1. Objetivos Ao final desta atividade experimental espera-se que os alunos sejam capazes de: - Identificar compostos e determinar suas purezas usando pontos de
PROCESSOS DE SEPARAÇÃO. Prof. Ms. George Verçoza
 PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
PROCESSOS DE SEPARAÇÃO Prof. Ms. George Verçoza Separação magnética: Separa misturas do tipo sólido-sólido nas quais um dos componentes tem propriedades magnéticas e é atraído por um ímã. Ex: Ferro e areia.
SOLUÇÕES Folha 01 João Roberto Mazzei
 01. (PUC SP 2009) O gráfico a seguir representa a curva de solubilidade do nitrato de potássio (KNO 3) em água. A 70 C, foram preparadas duas soluções, cada uma contendo 70 g de nitrato de potássio (KNO
01. (PUC SP 2009) O gráfico a seguir representa a curva de solubilidade do nitrato de potássio (KNO 3) em água. A 70 C, foram preparadas duas soluções, cada uma contendo 70 g de nitrato de potássio (KNO
Segundo o gráfico, o líquido mais volátil será a substância a) A b) B c) C d) D
 Professor: Alfênio Coligativas / Tonoscopia 01 (UEG GO) As propriedades físicas dos líquidos podem ser comparadas a partir de um gráfico de pressão de vapor em função da temperatura, como mostrado no gráfico
Professor: Alfênio Coligativas / Tonoscopia 01 (UEG GO) As propriedades físicas dos líquidos podem ser comparadas a partir de um gráfico de pressão de vapor em função da temperatura, como mostrado no gráfico
AVALIAÇÃO DE QUÍMICA
 Nome: nº: Ensino: ano/série: Componente Curricular: Professor(a): Data: / / Nota: AVALIAÇÃO DE QUÍMICA Instruções: (1) Preencha por completo o cabeçalho da avaliação. (2) Responda às questões dissertativas
Nome: nº: Ensino: ano/série: Componente Curricular: Professor(a): Data: / / Nota: AVALIAÇÃO DE QUÍMICA Instruções: (1) Preencha por completo o cabeçalho da avaliação. (2) Responda às questões dissertativas
QiD 1 1ª SÉRIE PARTE 3 FÍSICA
 QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. (1,0) Estime a ordem de grandeza do numero de passos que um atleta dá durante uma prova de maratona, sabendo que seu deslocamento é cerca de 42km e que um passo de um atleta
QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. (1,0) Estime a ordem de grandeza do numero de passos que um atleta dá durante uma prova de maratona, sabendo que seu deslocamento é cerca de 42km e que um passo de um atleta
Experiência 2 : TEMPERATURA DE FUSÃO DE UMA SUBSTÂNCIA
 Experiência 2 : TEMPERATURA DE FUSÃO DE UMA SUBSTÂNCIA 1. Objetivos Ao final desta atividade experimental espera-se que os alunos sejam capazes de: - Identificar compostos e determinar suas purezas usando
Experiência 2 : TEMPERATURA DE FUSÃO DE UMA SUBSTÂNCIA 1. Objetivos Ao final desta atividade experimental espera-se que os alunos sejam capazes de: - Identificar compostos e determinar suas purezas usando
Colégio XIX de Março Educação do jeito que deve ser
 Colégio XIX de Março Educação do jeito que deve ser 2017 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 16/05/2017 Nota: Professor(a): Paulo Fernando Valor da Prova: 40 pontos Orientações
Colégio XIX de Março Educação do jeito que deve ser 2017 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 16/05/2017 Nota: Professor(a): Paulo Fernando Valor da Prova: 40 pontos Orientações
Escola Básica de Valadares. Provas de aferição 5.º Ano 2017/2018
 Escola Básica de Valadares Provas de aferição 5.º Ano 2017/2018 Calendário Práticas Entre 21 e 30 de maio (calendário a divulgar) Escrita Educação Visual e Educação Tecnológica Educação Musical 8 de junho
Escola Básica de Valadares Provas de aferição 5.º Ano 2017/2018 Calendário Práticas Entre 21 e 30 de maio (calendário a divulgar) Escrita Educação Visual e Educação Tecnológica Educação Musical 8 de junho
O QUE É QUÍMICA? Química é uma ciência experimental que estuda a estrutura, composição e a transformação da matéria.
 POR QUE ESTUDAR QUÍMICA? A Química contribui para a melhora da qualidade de vida das pessoas, se souber usá-la corretamente. Nosso futuro depende de como vamos usar o conhecimento Químico. A química se
POR QUE ESTUDAR QUÍMICA? A Química contribui para a melhora da qualidade de vida das pessoas, se souber usá-la corretamente. Nosso futuro depende de como vamos usar o conhecimento Químico. A química se
Introdução. Uma mistura éconstituída por duas ou mais substâncias puras, sejam simples ou compostas MISTURA
 SOLUÇÕES Introdução MISTURA MISTURA HETEROGÊNEA Uma mistura éconstituída por duas ou mais substâncias puras, sejam simples ou compostas A mistura seráheterogênea quando apresentar duas ou mais fases perceptíveis.
SOLUÇÕES Introdução MISTURA MISTURA HETEROGÊNEA Uma mistura éconstituída por duas ou mais substâncias puras, sejam simples ou compostas A mistura seráheterogênea quando apresentar duas ou mais fases perceptíveis.
COLÉGIO XIX DE MARÇO excelência em educação
 COLÉGIO XIX DE MARÇO excelência em educação 1ª PROVA DE RECUPERAÇÃO DE CIÊNCIAS Aluno: Nº Série: 9º Turma: Data: Nota: Professora: Egberto Valor da Prova: 50 pontos Assinatura do responsável: Orientações
COLÉGIO XIX DE MARÇO excelência em educação 1ª PROVA DE RECUPERAÇÃO DE CIÊNCIAS Aluno: Nº Série: 9º Turma: Data: Nota: Professora: Egberto Valor da Prova: 50 pontos Assinatura do responsável: Orientações
JURANDIR SOARES Química Introdução ao Estudo das Soluções PAZ NA ESCOLA
 JURANDIR SOARES Química Introdução ao Estudo das Soluções PAZ NA ESCOLA DATA: 28/02 Conteúdos: - SOLUÇÕES OBJETIVO da aula: - Apresentar a importância e aplicações das Soluções e correlaciona-los com o
JURANDIR SOARES Química Introdução ao Estudo das Soluções PAZ NA ESCOLA DATA: 28/02 Conteúdos: - SOLUÇÕES OBJETIVO da aula: - Apresentar a importância e aplicações das Soluções e correlaciona-los com o
EXPERIÊNCIA 2 TEMPERATURA DE FUSÃO DE UMA SUBSTÂNCIA
 EXPERIÊNCIA 2 TEMPERATURA DE FUSÃO DE UMA SUBSTÂNCIA 1. OBJETIVOS No final desta experiência espera-se que o aluno seja capaz de: Determinar pontos de fusões usando o método gráfico da curva de resfriamento.
EXPERIÊNCIA 2 TEMPERATURA DE FUSÃO DE UMA SUBSTÂNCIA 1. OBJETIVOS No final desta experiência espera-se que o aluno seja capaz de: Determinar pontos de fusões usando o método gráfico da curva de resfriamento.
PROCESSO SELETIVO 2011
 PROCESSO SELETIVO 2011 Data da Prova: 05/12/2010 Início: 14h00 Duração: 5 horas Caderno de Questões Nome do candidato: Nº de inscrição: Antes de iniciar a prova, leia atentamente as seguintes instruções:
PROCESSO SELETIVO 2011 Data da Prova: 05/12/2010 Início: 14h00 Duração: 5 horas Caderno de Questões Nome do candidato: Nº de inscrição: Antes de iniciar a prova, leia atentamente as seguintes instruções:
Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente.
 SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
SOLUÇÕES Mistura: material formado por duas ou mais substâncias, sendo cada uma destas denominada componente. Fase: numa mistura, é cada uma das porções que apresenta aspecto homogéneo ou uniforme. CLASSIFICAÇÃO
EXPERIÊNCIA 3 TEMPERATURA DE FUSÃO DE UMA SUBSTÂNCIA
 EXPERIÊNCIA 3 TEMPERATURA DE FUSÃO DE UMA SUBSTÂNCIA 1. OBJETIVOS No final desta experiência espera-se que o aluno seja capaz de: Determinar pontos de fusões usando o método gráfico da curva de resfriamento.
EXPERIÊNCIA 3 TEMPERATURA DE FUSÃO DE UMA SUBSTÂNCIA 1. OBJETIVOS No final desta experiência espera-se que o aluno seja capaz de: Determinar pontos de fusões usando o método gráfico da curva de resfriamento.
QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO
 Química Avaliação Bimestral 1 o ano Vivian março/ 2011 Nome: Turma: QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO Substância T. F. (ºC) T.E. (ºC) Densidade a 20ºC (g/cm 3 ) Solubilidade (g/100 g de água)
Química Avaliação Bimestral 1 o ano Vivian março/ 2011 Nome: Turma: QUESTÕES DISSERTATIVAS - GABARITO RESOLVIDO Substância T. F. (ºC) T.E. (ºC) Densidade a 20ºC (g/cm 3 ) Solubilidade (g/100 g de água)
Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância.
 Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância. Vejamos alguns exemplos: Ao agitar a mistura, a sacarose (disperso)
Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância. Vejamos alguns exemplos: Ao agitar a mistura, a sacarose (disperso)
Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015
 Química Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015 1. (Ufv 1999 - adaptada) Dadas as afirmativas: I. A molécula de N 2 é diatômica. II. Substância composta é aquela formada por dois ou mais
Química Lista de Exercicios 1 o ano Patrícia Cecilia abril/2015 1. (Ufv 1999 - adaptada) Dadas as afirmativas: I. A molécula de N 2 é diatômica. II. Substância composta é aquela formada por dois ou mais
1) O que aconteceu com o cubo de gelo no béquer 1? Que conclusão você tira desse resultado?...
 Nº da Prática: 01 Data: / / Título da Prática: Qual o líquido é mais denso: a água líquida ou o álcool? S Comparar as densidades da água líquida, do gelo e do álcool. 2 cubos de gelo; álcool; água. Coloque
Nº da Prática: 01 Data: / / Título da Prática: Qual o líquido é mais denso: a água líquida ou o álcool? S Comparar as densidades da água líquida, do gelo e do álcool. 2 cubos de gelo; álcool; água. Coloque
Experiência 04 - Solubilidade
 Experiência 04 - Solubilidade 01. OBJETIVOS: No final desta experiência o aluno deverá ser capaz de: Identificar algumas variáveis que afetam a solubilidade. Utilizar técnicas simples de extração, recristalização
Experiência 04 - Solubilidade 01. OBJETIVOS: No final desta experiência o aluno deverá ser capaz de: Identificar algumas variáveis que afetam a solubilidade. Utilizar técnicas simples de extração, recristalização
SOLUBILIDADE DE SÓLIDOS EM LÍQUIDOS
 EXPERIMENTO 4 SOLUBILIDADE DE SÓLIDOS EM LÍQUIDOS OBJETIVOS Observar soluções insaturadas, saturadas e supersaturadas; Construir a curva de solubilidade de um sal inorgânico. INTRODUÇÃO Os depósitos naturais
EXPERIMENTO 4 SOLUBILIDADE DE SÓLIDOS EM LÍQUIDOS OBJETIVOS Observar soluções insaturadas, saturadas e supersaturadas; Construir a curva de solubilidade de um sal inorgânico. INTRODUÇÃO Os depósitos naturais
1º trimestre Sala de estudos Ciências Data: março/2017 Ensino Fundamental 9º ano Classe: Profª. Elisete Nome: nº
 . 1º trimestre Sala de estudos Ciências Data: março/2017 Ensino Fundamental 9º ano Classe: Profª. Elisete Nome: nº Conteúdo: Propriedades da matéria; mudanças de estado físico; transformações de unidades..
. 1º trimestre Sala de estudos Ciências Data: março/2017 Ensino Fundamental 9º ano Classe: Profª. Elisete Nome: nº Conteúdo: Propriedades da matéria; mudanças de estado físico; transformações de unidades..
EXPERIÊNCIA 5 SOLUBILIDADE
 EXPERIÊNCIA 5 SOLUBILIDADE 1. OBJETIVOS No final desta experiência, espera-se que o aluno seja capaz de: Identificar algumas variáveis que afetam a solubilidade. Utilizar técnicas simples de extração,
EXPERIÊNCIA 5 SOLUBILIDADE 1. OBJETIVOS No final desta experiência, espera-se que o aluno seja capaz de: Identificar algumas variáveis que afetam a solubilidade. Utilizar técnicas simples de extração,
Colégio XIX de Março Educação do jeito que deve ser
 Colégio XIX de Março Educação do jeito que deve ser 2017 1ª PROVA PARCIAL DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 25/03/2017 Nota: Professor(a): Paulo Fernando Valor da Prova: 40 pontos Orientações
Colégio XIX de Março Educação do jeito que deve ser 2017 1ª PROVA PARCIAL DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 25/03/2017 Nota: Professor(a): Paulo Fernando Valor da Prova: 40 pontos Orientações
4.1. Propriedades físicas e propriedades químicas dos materiais
 Ciências Físico-químicas - 7º ano de escolaridade Unidade 4 O MUNDO MATERIAL 4.1. Propriedades físicas e propriedades químicas dos materiais - Propriedades físicas e químicas dos materiais - Densidade
Ciências Físico-químicas - 7º ano de escolaridade Unidade 4 O MUNDO MATERIAL 4.1. Propriedades físicas e propriedades químicas dos materiais - Propriedades físicas e químicas dos materiais - Densidade
Escola Secundária Jerónimo Emiliano de Andrade. Ciências Físico-Químicas 8.º Ano
 Escola Secundária Jerónimo Emiliano de Andrade 8.º Ano FICHA INFORMATIVA 1 Classificação dos materiais NOME: N.º TURMA DATA: / / CLASSIFICAÇÃO DOS MATERIAIS DE ACORDO COM ALGUNS CRITÉRIOS Podem distinguir-se
Escola Secundária Jerónimo Emiliano de Andrade 8.º Ano FICHA INFORMATIVA 1 Classificação dos materiais NOME: N.º TURMA DATA: / / CLASSIFICAÇÃO DOS MATERIAIS DE ACORDO COM ALGUNS CRITÉRIOS Podem distinguir-se
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma:
 TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
TRABALHO DE RECUPERAÇÃO 1º TRIMESTRE - QUÍMICA 9º ANO Nome: Turma: ROTEIRO E INSTRUÇÕES: Estados físicos da matéria. Mudanças de estado físico. Substâncias e misturas. O trabalho deve ser respondido à
QUÍMICA FRENTE II FICHA 11 PROPRIEDADES COLIGATIVAS
 Propriedades Coligativas São aquelas propriedades das substâncias puras que são modificadas quando se adiciona um soluto não volátil a elas. Essas propriedades, portanto, não são explicadas pela natureza
Propriedades Coligativas São aquelas propriedades das substâncias puras que são modificadas quando se adiciona um soluto não volátil a elas. Essas propriedades, portanto, não são explicadas pela natureza
Conteúdo: ESTUDO DAS DISPERSÕES E SOLUÇÕES
 Atividade/Exercício: FIXAÇÃO DE ESTUDO DAS SOLUÇÕES Disciplina: QUÍMICA Educador: ENDERSON BASTANI 1ª Etapa 23/ 04 /2019 Ano/Série: 2º Educando(a): Turma: Conteúdo: ESTUDO DAS DISPERSÕES E SOLUÇÕES QUESTÃO
Atividade/Exercício: FIXAÇÃO DE ESTUDO DAS SOLUÇÕES Disciplina: QUÍMICA Educador: ENDERSON BASTANI 1ª Etapa 23/ 04 /2019 Ano/Série: 2º Educando(a): Turma: Conteúdo: ESTUDO DAS DISPERSÕES E SOLUÇÕES QUESTÃO
Atividade extra. Questão 1 Cecierj Questão 2 Cecierj Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Mistura de Soluções, Solubilidade e Propriedades Coligativas. Química 2/set
 Mistura de Soluções, Solubilidade e Propriedades Coligativas Química 2/set Mistura de Soluções 1 L 20 g/l 1 L 50 g/l 2L 70 g ou 35 g/l m a.v a + m b.v b = m f.v f m f = m a + m b Curvas de Solubilidade
Mistura de Soluções, Solubilidade e Propriedades Coligativas Química 2/set Mistura de Soluções 1 L 20 g/l 1 L 50 g/l 2L 70 g ou 35 g/l m a.v a + m b.v b = m f.v f m f = m a + m b Curvas de Solubilidade
AULA PRÁTICA DE QUÍMICA GERAL Estudando a água parte 40 Comportamento da água com sal - 3 9º NO DO ENSINO FUNDAMENTAL - 1º e 2º ANO DO ENSINO MÉDIO
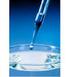 AULA PRÁTICA DE QUÍMICA GERAL Estudando a água parte 40 Comportamento da água com sal - 3 9º NO DO ENSINO FUNDAMENTAL - 1º e 2º ANO DO ENSINO MÉDIO INTRODUÇÃO Um dos problemas mais comuns para que os estudantes
AULA PRÁTICA DE QUÍMICA GERAL Estudando a água parte 40 Comportamento da água com sal - 3 9º NO DO ENSINO FUNDAMENTAL - 1º e 2º ANO DO ENSINO MÉDIO INTRODUÇÃO Um dos problemas mais comuns para que os estudantes
PROVA MODELO DE FÍSICA E QUÍMICA 2018
 Página 1 de 9 Prova de ingresso escrita específica para avaliar a capacidade para a frequência do ciclo de estudos de licenciatura, para alunos internacionais, Decreto-Lei n.º 36/2014, de 10 de março AVALIAÇÃO
Página 1 de 9 Prova de ingresso escrita específica para avaliar a capacidade para a frequência do ciclo de estudos de licenciatura, para alunos internacionais, Decreto-Lei n.º 36/2014, de 10 de março AVALIAÇÃO
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011
 ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Leia atentamente o texto que
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Leia atentamente o texto que
JAMILE ROSA RAMPINELLI
 Química Geral JAMILE ROSA RAMPINELLI Bacharel em Química Ind. UNIVILLE Mestre em Engenharia de Alimentos UFSC Doutora em Engenharia Química UFSC QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução:
Química Geral JAMILE ROSA RAMPINELLI Bacharel em Química Ind. UNIVILLE Mestre em Engenharia de Alimentos UFSC Doutora em Engenharia Química UFSC QUÍMICA A Ciência Central 9ª Edição Capítulo 1 Introdução:
Lista de exercícios de recuperação em Física
 Ciências da Natureza e suas Tecnologias Física Petrônio L. Freitas Lista de exercícios de recuperação final Recup.Final 35 pontos 22,8 pontos 10 12 2017 2 º ano A, B e C Lista de exercícios de recuperação
Ciências da Natureza e suas Tecnologias Física Petrônio L. Freitas Lista de exercícios de recuperação final Recup.Final 35 pontos 22,8 pontos 10 12 2017 2 º ano A, B e C Lista de exercícios de recuperação
Concentração de soluções e diluição
 Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
Concentração de soluções e diluição 1. Introdução Uma solução é uma dispersão homogênea de duas ou mais espécies de substâncias moleculares ou iônicas. É um tipo especial de mistura, em que as partículas
OS ESTADOS FÍSICOS DA MATÉRIA Observe a história: Responda: 1) Quais foram as transformações que ocorreram na água no decorrer da história?
 2 - AS TRANSFORMAÇÕES DA MATÉRIA A matéria pode passar por diversas transformações. Essas transformações podem ser físicas ou químicas. > Alterações físicas caracterizam-se por não ocorrer mudanças na
2 - AS TRANSFORMAÇÕES DA MATÉRIA A matéria pode passar por diversas transformações. Essas transformações podem ser físicas ou químicas. > Alterações físicas caracterizam-se por não ocorrer mudanças na
a) 20 d) 100 b) 40 e) 160 c) 80
 01) (Unifesp-SP) Uma solução contendo 14 g de cloreto de sódio dissolvidos em 200 ml de água foi deixada em um frasco aberto, a 30 C. Após algum tempo, começou a cristalizar o soluto. Qual volume mínimo
01) (Unifesp-SP) Uma solução contendo 14 g de cloreto de sódio dissolvidos em 200 ml de água foi deixada em um frasco aberto, a 30 C. Após algum tempo, começou a cristalizar o soluto. Qual volume mínimo
HORÁRIO DAS AVALIAÇÕES 2016
 OBSERVAÇÕES E PROCEDIMENTOS EM DIAS DE AVALIAÇÃO 1) Solicitamos aos alunos que estejam na sala 10 minutos antes do horário marcado para o início das avaliações e que não a deixem sem assinar a lista, que
OBSERVAÇÕES E PROCEDIMENTOS EM DIAS DE AVALIAÇÃO 1) Solicitamos aos alunos que estejam na sala 10 minutos antes do horário marcado para o início das avaliações e que não a deixem sem assinar a lista, que
Experiência 2. DETERMINAÇÃO DO PONTO DE FUSÃO DE SUBSTÂNCIAS
 Experiência 2. DETERMINAÇÃO DO PONTO DE FUSÃO DE SUBSTÂNCIAS 1. Objetivos Ao final desta atividade experimental espera-se que o aluno seja capaz de: - Identificar compostos e determinar suas purezas usando
Experiência 2. DETERMINAÇÃO DO PONTO DE FUSÃO DE SUBSTÂNCIAS 1. Objetivos Ao final desta atividade experimental espera-se que o aluno seja capaz de: - Identificar compostos e determinar suas purezas usando
Dependendo do diâmetro (Ø) das partículas que constituem o disperso, as dispersões podem ser:
 Soluções Químicas A mistura de dois ou mais materiais podem ser uma perfeita dissolução denominada mistura homogênea ou uma separação total das partes constituintes do sistema a qual chamamos mistura heterogênea.
Soluções Químicas A mistura de dois ou mais materiais podem ser uma perfeita dissolução denominada mistura homogênea ou uma separação total das partes constituintes do sistema a qual chamamos mistura heterogênea.
QUÍMICA. Soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais. Parte 2. Prof a.
 QUÍMICA Parte 2 Prof a. Giselle Blois EXERCÍCIOS 1. (FMU-FIAM-FAAM-SP) Os frascos contêm soluções saturadas de cloreto de sódio (sal de cozinha). Podemos afirmar que: a) a solução do frasco II é a mais
QUÍMICA Parte 2 Prof a. Giselle Blois EXERCÍCIOS 1. (FMU-FIAM-FAAM-SP) Os frascos contêm soluções saturadas de cloreto de sódio (sal de cozinha). Podemos afirmar que: a) a solução do frasco II é a mais
Lista de Exercícios - CALORIMETRIA, MUDANÇA DE FASE E TROCA DE CALOR
 9º EF EXERCÍCIOS Lista de Exercícios - CALORIMETRIA, MUDANÇA DE FASE E TROCA DE CALOR 1 Quantas calorias são necessárias para vaporizar 1,00 litro de água, se a sua temperatura é, inicialmente, igual a
9º EF EXERCÍCIOS Lista de Exercícios - CALORIMETRIA, MUDANÇA DE FASE E TROCA DE CALOR 1 Quantas calorias são necessárias para vaporizar 1,00 litro de água, se a sua temperatura é, inicialmente, igual a
QUÍMICA Tipos de soluções Edson Mesquita
 QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
I SIMULADO DE QUÍMICA
 PROVA DISCURSIVA I SIMULADO DE QUÍMICA INSTRUÇÕES Verifique se esse Caderno contém 4 questões discursivas de: QUÍMICA Se o Caderno estiver incompleto ou contiver imperfeição gráfica que prejudique a leitura,
PROVA DISCURSIVA I SIMULADO DE QUÍMICA INSTRUÇÕES Verifique se esse Caderno contém 4 questões discursivas de: QUÍMICA Se o Caderno estiver incompleto ou contiver imperfeição gráfica que prejudique a leitura,
QUÍMICA RECUPERAÇÃO PARALELA. Prof. ALEXANDRE D. MARQUIORETO
 QUÍMICA RECUPERAÇÃO PARALELA Prof. ALEXANDRE D. MARQUIORETO SOLUÇÕES são misturas homogêneas de duas ou mais substâncias. SOLUÇÃO = SOLUTO + SOLVENTE Que se dissolve Que dissolverá Como se forma uma solução?
QUÍMICA RECUPERAÇÃO PARALELA Prof. ALEXANDRE D. MARQUIORETO SOLUÇÕES são misturas homogêneas de duas ou mais substâncias. SOLUÇÃO = SOLUTO + SOLVENTE Que se dissolve Que dissolverá Como se forma uma solução?
Profº André Montillo
 Profº André Montillo www.montillo.com.br Definição: É uma Mistura Homogênia de 2 ou mais substâncias. Na Solução não ocorre uma reação química, porque não há formação de novas substâncias e não há alterações
Profº André Montillo www.montillo.com.br Definição: É uma Mistura Homogênia de 2 ou mais substâncias. Na Solução não ocorre uma reação química, porque não há formação de novas substâncias e não há alterações
Escola Básica de Valadares. Provas de aferição 8.º Ano 2017/2018
 Escola Básica de Valadares Provas de aferição 8.º Ano 2017/2018 Calendário Práticas Entre 21 de maio e 5 de junho (calendário a divulgar) Escrita Educação Visual Educação Física 12 de junho terça-feira
Escola Básica de Valadares Provas de aferição 8.º Ano 2017/2018 Calendário Práticas Entre 21 de maio e 5 de junho (calendário a divulgar) Escrita Educação Visual Educação Física 12 de junho terça-feira
Quí. Quí. Allan Rodrigues Monitor: João Castro
 Quí. Professor: Abner Camargo Allan Rodrigues Monitor: João Castro Solubilidade 05 jun RESUMO Classificação das soluções Existe uma regra para solubilidade dos compostos, não é possível ter uma solução
Quí. Professor: Abner Camargo Allan Rodrigues Monitor: João Castro Solubilidade 05 jun RESUMO Classificação das soluções Existe uma regra para solubilidade dos compostos, não é possível ter uma solução
Colégio São Paulo-Teresópolis/RJ
 Colégio São Paulo-Teresópolis/RJ Disciplina: Ciências Data: /10/2017 Professor(a): Carolina Maria 6 º ano Ensino Fundamental Nota: Etapa: 3 a Exercícios (X) A1( ) A2 ( ) A3 ( ) 2ª ch. () Turma: Aluno (a):
Colégio São Paulo-Teresópolis/RJ Disciplina: Ciências Data: /10/2017 Professor(a): Carolina Maria 6 º ano Ensino Fundamental Nota: Etapa: 3 a Exercícios (X) A1( ) A2 ( ) A3 ( ) 2ª ch. () Turma: Aluno (a):
Roteiro de estudos 1º trimestre. Matemática-Física-Química. Orientação de estudos
 Roteiro de estudos 1º trimestre. Matemática-Física-Química O roteiro foi montado especialmente para reforçar os conceitos dados em aula. Com os exercícios você deve fixar os seus conhecimentos e encontrar
Roteiro de estudos 1º trimestre. Matemática-Física-Química O roteiro foi montado especialmente para reforçar os conceitos dados em aula. Com os exercícios você deve fixar os seus conhecimentos e encontrar
2-) Observe os sistemas
 SOLUBILIDADE Boa atividade!!! Professora Luciane 1-) Um determinado sal tem coeficiente de solubilidade igual a 34g/100g de água, a 20ºC. Tendo-se 450g de água a 20 ºC, qual a quantidade, em gramas, desse
SOLUBILIDADE Boa atividade!!! Professora Luciane 1-) Um determinado sal tem coeficiente de solubilidade igual a 34g/100g de água, a 20ºC. Tendo-se 450g de água a 20 ºC, qual a quantidade, em gramas, desse
EXERCÍCIOS SUBSTÂNCIAS E MISTURAS
 EXERCÍCIOS SUBSTÂNCIAS E MISTURAS 1- Considere o sistema e responda as questões: A) Quantos átomos estão representados? B) Quantos elementos químicos há no sistema? C) Quantas moléculas estão representadas
EXERCÍCIOS SUBSTÂNCIAS E MISTURAS 1- Considere o sistema e responda as questões: A) Quantos átomos estão representados? B) Quantos elementos químicos há no sistema? C) Quantas moléculas estão representadas
FICHA DE PREPARAÇÃO PARA O TESTE Nº5 FQ -7ºANO
 FICHA DE PREPARAÇÃO PARA O TESTE Nº5 FQ -7ºANO -CLASSIFICAÇÃO DOS MATERIAIS - SUBSTÃNCIAS E MISTURAS - SOLUÇÕES -TRANSFORMAÇÕES QUÍMICAS E FÍSICAS 1. A Química é a ciência que estuda as propriedades e
FICHA DE PREPARAÇÃO PARA O TESTE Nº5 FQ -7ºANO -CLASSIFICAÇÃO DOS MATERIAIS - SUBSTÃNCIAS E MISTURAS - SOLUÇÕES -TRANSFORMAÇÕES QUÍMICAS E FÍSICAS 1. A Química é a ciência que estuda as propriedades e
Química. Exercícios sobre soluções I. Resumo. 2. Observe a tabela de solubilidade abaixo para várias substâncias:
 Exercícios sobre soluções I Resumo 2. Observe a tabela de solubilidade abaixo para várias substâncias: Classifique o tipo de solução (saturada, insaturada ou supersaturada) que obteremos se adicionarmos
Exercícios sobre soluções I Resumo 2. Observe a tabela de solubilidade abaixo para várias substâncias: Classifique o tipo de solução (saturada, insaturada ou supersaturada) que obteremos se adicionarmos
FÍSICA, 2º Ano do Ensino Médio Diagrama de Fase
 Estuda as fases em que uma substância pura pode se apresentar, de acordo com as condições de pressão e de temperatura a que está submetida. A neblina que se observa na foto resulta da transformação do
Estuda as fases em que uma substância pura pode se apresentar, de acordo com as condições de pressão e de temperatura a que está submetida. A neblina que se observa na foto resulta da transformação do
Colégio XIX de Março Educação do jeito que deve ser
 Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
Colégio XIX de Março Educação do jeito que deve ser 2018 1ª PROVA SUBSTITUTIVA DE QUÍMICA Aluno(a): Nº Ano: 1º Turma: Data: 07/05/2018 Nota: Professor(a): Taynara e Paulo Fernando Valor da Prova: 40 pontos
QUÍMICA TAISSA LUKJANENKO
 QUÍMICA TAISSA LUKJANENKO SUBSTÂNCIA PURA MISTURA ESTUDO DAS SUBSTÂNCIAS E MISTURAS SUBSTÂNCIA: material formado por moléculas quimicamente iguais. Substância simples: é constituída de uma molécula formada
QUÍMICA TAISSA LUKJANENKO SUBSTÂNCIA PURA MISTURA ESTUDO DAS SUBSTÂNCIAS E MISTURAS SUBSTÂNCIA: material formado por moléculas quimicamente iguais. Substância simples: é constituída de uma molécula formada
Qui. Allan Rodrigues Xandão (Victor Pontes)
 Semana 16 Allan Rodrigues Xandão (Victor Pontes) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. Solubilidade
Semana 16 Allan Rodrigues Xandão (Victor Pontes) Este conteúdo pertence ao Descomplica. Está vedada a cópia ou a reprodução não autorizada previamente e por escrito. Todos os direitos reservados. Solubilidade
FÍSICA QUESTÕES DISCURSIVAS INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA
 FÍSICA QUESTÕES DISCURSIVAS N ọ DE ORDEM: N ọ DE INSCRIÇÃO: NOME: INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA 1. Verifique se este caderno contém 5 questões discursivas e/ou qualquer tipo de defeito. Qualquer
FÍSICA QUESTÕES DISCURSIVAS N ọ DE ORDEM: N ọ DE INSCRIÇÃO: NOME: INSTRUÇÕES PARA A REALIZAÇÃO DA PROVA 1. Verifique se este caderno contém 5 questões discursivas e/ou qualquer tipo de defeito. Qualquer
MODO COMPLETO, AS ETAPAS E OS CÁLCULOS
 Física QUESTÕES de 01 a 06 LEIA CUIDADOSAMENTE O ENUNCIADO DE CADA QUESTÃO, FORMULE SUAS RESPOSTAS COM OBJETIVIDADE E CORREÇÃO DE LINGUAGEM E, EM SEGUIDA, TRANSCREVA COMPLETAMENTE CADA UMA NA FOLHA DE
Física QUESTÕES de 01 a 06 LEIA CUIDADOSAMENTE O ENUNCIADO DE CADA QUESTÃO, FORMULE SUAS RESPOSTAS COM OBJETIVIDADE E CORREÇÃO DE LINGUAGEM E, EM SEGUIDA, TRANSCREVA COMPLETAMENTE CADA UMA NA FOLHA DE
EXPERIÊNCIA 2 DETERMINAÇÃO DA MASSA MOLECULAR DE UM GÁS EFEITO DA PRESSÃO NO PONTO DE EBULIÇÃO
 1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: Interpretar as leis que regem o comportamento dos gases ideais. Utilizar a equação da lei do gás ideal, PV = nrt Medir o volume e a
1. OBJETIVOS No final desta experiência o aluno deverá ser capaz de: Interpretar as leis que regem o comportamento dos gases ideais. Utilizar a equação da lei do gás ideal, PV = nrt Medir o volume e a
Exercícios sobre Solubilidade - conceitos e curvas
 Exercícios sobre Solubilidade - conceitos e curvas 01. (Ufrrj) Ao analisar o gráfico acima, percebe-se que a) a solubilidade do KCl é maior que a do KBr. b) à medida que a temperatura aumenta a solubilidade
Exercícios sobre Solubilidade - conceitos e curvas 01. (Ufrrj) Ao analisar o gráfico acima, percebe-se que a) a solubilidade do KCl é maior que a do KBr. b) à medida que a temperatura aumenta a solubilidade
PROPRIEDADES DA MATÉRIA. Em relação aos três estados físicos de agregação da matéria: sólido, líquido e gasoso, é correto afirmar que
 LISTA: 02 1ª série Ensino Médio Professor(a): Leonardo Gomes Turma: A ( ) / B ( ) Aluno(a): Segmento temático: PROPRIEDADES DA MATÉRIA DIA: MÊS: 02 2017 Questão 01 - (IFGO/2015) Em relação aos três estados
LISTA: 02 1ª série Ensino Médio Professor(a): Leonardo Gomes Turma: A ( ) / B ( ) Aluno(a): Segmento temático: PROPRIEDADES DA MATÉRIA DIA: MÊS: 02 2017 Questão 01 - (IFGO/2015) Em relação aos três estados
Sua prova deve ser feita à caneta azul ou preta. Não rasure e não use corretivo. Entregue no dia da prova.
 Aluno(a): nº: Turma: Nota Ano: 2º Ano E.M. Data: /08/2019 Série Professor(a): Everton Trabalho Recuperação Matéria: Física Valor: 5,0 Sua prova deve ser feita à caneta azul ou preta. Não rasure e não use
Aluno(a): nº: Turma: Nota Ano: 2º Ano E.M. Data: /08/2019 Série Professor(a): Everton Trabalho Recuperação Matéria: Física Valor: 5,0 Sua prova deve ser feita à caneta azul ou preta. Não rasure e não use
Resoluções dos exercícios propostos
 1 P.109 p a) AB corresponde a uma fusão (passagem da Sólido F fase sólida para a fase líquida). A B Líquido G b) B corresponde a uma vaporização E (passagem da fase líquida para a fase de D Vapor vapor).
1 P.109 p a) AB corresponde a uma fusão (passagem da Sólido F fase sólida para a fase líquida). A B Líquido G b) B corresponde a uma vaporização E (passagem da fase líquida para a fase de D Vapor vapor).
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. DISCIPLINA:Química SÉRIE: 3º. ALUNO(a): Lista de Exercícios P1 I Bimestre
 GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 3º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 3º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
2. Considere um bloco de gelo de massa 300g á temperatura de 20 C, sob pressão normal. Sendo L F
 1. Considere um bloco de gelo de massa 300g encontra-se a 0 C. Para que todo gelo se derreta, obtendo água a 0 C são necessárias 24.000 cal. Determine o calor latente de fusão do gelo. 2. Considere um
1. Considere um bloco de gelo de massa 300g encontra-se a 0 C. Para que todo gelo se derreta, obtendo água a 0 C são necessárias 24.000 cal. Determine o calor latente de fusão do gelo. 2. Considere um
HORÁRIO DAS AVALIAÇÕES 2017
 OBSERVAÇÕES E PROCEDIMENTOS EM DIAS DE AVALIAÇÃO 1) Solicitamos aos alunos que estejam na sala 10 minutos antes do horário marcado para o início das avaliações e que não a deixem sem assinar a lista, que
OBSERVAÇÕES E PROCEDIMENTOS EM DIAS DE AVALIAÇÃO 1) Solicitamos aos alunos que estejam na sala 10 minutos antes do horário marcado para o início das avaliações e que não a deixem sem assinar a lista, que
MASSA ATÔMICA. 1u corresponde a 1, g, que equivale aproximadamente à massa de um próton ou de um nêutron.
 Cálculos Químicos MASSA ATÔMICA Na convenção da IUPAC (União Internacional de Química Pura e Aplicada) realizada em 1961, adotou-se como unidade padrão para massa atômica o equivalente a 1/12 da massa
Cálculos Químicos MASSA ATÔMICA Na convenção da IUPAC (União Internacional de Química Pura e Aplicada) realizada em 1961, adotou-se como unidade padrão para massa atômica o equivalente a 1/12 da massa
Ensino Fundamental - II
 Ensino Fundamental - II OBSERVAÇÕES E PROCEDIMENTOS EM DIAS DE AVALIAÇÃO 1) Solicitamos aos alunos que estejam na sala 10 minutos antes do horário marcado para o início das avaliações e que não a deixem
Ensino Fundamental - II OBSERVAÇÕES E PROCEDIMENTOS EM DIAS DE AVALIAÇÃO 1) Solicitamos aos alunos que estejam na sala 10 minutos antes do horário marcado para o início das avaliações e que não a deixem
Ensino Fundamental - II
 Ensino Fundamental - II OBSERVAÇÕES E PROCEDIMENTOS EM DIAS DE AVALIAÇÃO 1) Solicitamos aos alunos que estejam na sala 10 minutos antes do horário marcado para o início das avaliações e que não a deixem
Ensino Fundamental - II OBSERVAÇÕES E PROCEDIMENTOS EM DIAS DE AVALIAÇÃO 1) Solicitamos aos alunos que estejam na sala 10 minutos antes do horário marcado para o início das avaliações e que não a deixem
Atividade complementar de Química. Transformações físicas - Mudanças de estados físicos
 Atividade complementar de Química Transformações físicas - Mudanças de estados físicos Educação de Jovens e Adultos Neste material serão revisadas as mudanças de estados físicos da matéria, relacionando-as
Atividade complementar de Química Transformações físicas - Mudanças de estados físicos Educação de Jovens e Adultos Neste material serão revisadas as mudanças de estados físicos da matéria, relacionando-as
CAPA DO CADERNO DE TEXTO PROVA DE CONHECIMENTOS GERAIS EM QUÍMICA. (Esta capa será destacada para impedir identificação do caderno de texto)
 CAPA DO CADERNO DE TEXTO PROVA DE CONHECIMENTOS GERAIS EM QUÍMICA Nome do candidato Ass. do candidato (Esta capa será destacada para impedir identificação do caderno de texto) INSTRUÇÕES: Preencha atentamente
CAPA DO CADERNO DE TEXTO PROVA DE CONHECIMENTOS GERAIS EM QUÍMICA Nome do candidato Ass. do candidato (Esta capa será destacada para impedir identificação do caderno de texto) INSTRUÇÕES: Preencha atentamente
