ROTEIRO DE ESTUDOS PARA A RECUPERAÇÃO 1º. SEMESTRE 2016 DISCIPLINA: CIÊNCIAS ANO: 9º PROFESSORA: SILVIA
|
|
|
- Irene Maranhão Tavares
- 7 Há anos
- Visualizações:
Transcrição
1 ROTEIRO DE ESTUDOS PARA A RECUPERAÇÃO 1º. SEMESTRE 2016 DISCIPLINA: CIÊNCIAS ANO: 9º PROFESSORA: SILVIA Orientações de estudo: Estude as aulas nas apostilas 1 e 2, refazendo todos os exercícios propostos. Prepare um banco de fórmulas conforme as mesmas forem surgindo nas aulas estudadas. ATENÇÃO às unidades que devem ser adotadas em cada fórmula Anote-as. Refaça as avaliações mensais e bimestrais propostas para o 1º. Semestre. O roteiro deverá ser respondido pelo próprio aluno antes das aulas de recuperação. As dúvidas deverão ser anotadas para serem esclarecidas nas aulas de recuperação. Química Módulo I: Fenômenos Físicos e Químicos 1- Qual é o objeto da Química? 2- O que é matéria? O que vem a ser estado de agregação da matéria? 3- As propriedades da matéria são agrupadas em: propriedades gerais e propriedades específicas. Diferencie-as 4- Quanto às propriedades gerais da matéria, descreva as seguintes: a) Extensão b) Impenetrabilidade c) Divisibilidade d) Compressibilidade e) Inércia f) Massa g) Volume h) Indestrutibilidade i) Elasticidade 5- Quanto às propriedades Específicas da matéria, descreva as seguintes: a) Densidade b) Ponto de fusão c) Ponto de ebulição d) Propriedades organolépticas: 6- Associe ponto de ebulição e altitude: 7- Quanto às propriedades organolépticas, descreva duas delas para cada uma das substâncias abaixo: a) Sal b) Açúcar c) Azeite 8- O que são fenômenos? Diferencie fenômenos físicos de fenômenos químicos: 9- Classifique os fenômenos abaixo em químicos(q) ou Físicos(F): a) Papel rasgado b) Gelo derretendo c) Vidro sendo moldado para formar uma peça d) Fogueira acesa: e) Prego enferrujado: f) Lata de refrigerante amassada g) Produção do vinagre a partir do vinho h) Cozimento de um ovo i) Vento agitando as roupas do varal j) Produção da coalhada a partir do leite
2 Módulos II e III: Substâncias e Sistemas/ Métodos de Separação de Mistura 10- Diferencie substância pura simples de substância pura composta: 11- Defina: a) Mistura: b) Fases: c) Mistura homogênea: d) Mistura heterogênea: 12- Classifique os sistemas abaixo em substância pura simples ou substância pura composta: 13- Classifique os sistemas abaixo em homogêneos ou heterogêneos, colocando também o número de elementos e a quantidade de fases que apresentam: a) Água + ar dissolvido b) Água + água não dissolvido (bolhas) c) Leite longa vida d) Vinho e) Gasolina + querosene f) Água + éter + gasolina g) Ar atmosférico: h) Gás oxigênio+ gás hélio + gás nitrogênio i) Água + pouco sal + pedra + areia j) Água e gelo: 14- Sobre as técnicas de separação de misturas homogêneas e heterogêneas, complete os quadros abaixo: a) Técnica: Catação b) Técnica: Flotação c) Técnica: Levigação d) Técnica: Tamisação e) Técnica: Separação magnética: f) Técnica: Ventilação g) Técnica: Filtração Simples Lembre-se que: São miscíveis entre si: água, álcool, éter gasolina, querosene h) Técnica: Decantação simples e Decantação com funil de bromo i) Técnica: Centrifugação j) Técnica: Destilação Simples k) Técnica: Dissolução fracionada l) Técnica: Fusão fracionada m) Técnica: Destilação fracionada
3 Módulo IV: Os Átomos 15- Quanto ao átomo, responda: a) Como é formado? b) Quanto às cargas elétricas, como podem ser suas partículas? c) como sua massa é calculada? d) como seu tamanho é calculado? e) Qual é a relação existente entre o número de prótons e de elétrons? f) O que vem e ser número atômico? Como é representado? g) O que vem e ser número de massa? Como é representada? 16- Dê o número de prótons, elétrons e nêutrons dos seguintes átomos: a) 11 Na 23 b) 76 Os 130 c) 33 As 75 d) 10 Ne 20 e) 82 Pb Um átomo possui número de massa igual a 32 e apresenta número atômico igual a 16. Qual é o seu número de nêutrons? 18- O átomo X, com número de massa igual a 52, apresenta número atômico igual a 12. Qual é o seu número de nêutrons? 19- Dê a definição de: a) isótopos: b) isóbaros: c) isótonos: 20- Sobre os átomos A e B são conhecidos os seguintes dados: a) o átomo A tem 28 elétrons e número de massa igual a 59; b) os átomos A e B são isótonos entre si; c) o átomo B tem número atômico 32 Calcule o número de massa do átomo B: 21- Sobre os átomos A e B são conhecidos os seguintes dados: a) o átomo A tem 35 elétrons e número de massa igual a 89; b) os átomos A e B são isótonos entre si; c) o átomo B tem número atômico 38. Calcule o número de massa do átomo B: 22-Sabendo-se que dois átomos hipotéticos A (Z= 55) e B(Z = 48) são isóbaros entre si e que o átomo A possui 45 nêutrons, determine o número de nêutrons do átomo B: 23- São dados os átomos hipotéticos: 55 A 133, 35B 62, 59 C 137, 36D 81, 35E 81. a) Identifique os isótonos: b) Identifique os isóbaros: 24- Os números atômicos, de massa e de nêutrons de um átomo são expressos, respectivamente por: (3x +3), (6x) e (x +1). Determine os números de prótons e nêutrons desse átomo Módulo V: Tabela Periódica e Ciclos Biogeoquímicos: Carbono e Nitrogênio 25- Esquematize o ciclo do carbono e identifique: a) Os fenômenos que ocorrem: b) Os seres vivos que dele participam. c) A interferência humana e suas consequências: 26- Sobre o ciclo do nitrogênio, responda; a) Qual é a importância das bactérias nitrificantes? b) Associe plantas leguminosas com a prática da adubação verde na agricultura: c) Qual á a importância desse elemento químico para os seres vivos? d) De que maneira o nitrogênio volta à atmosfera, na forma de CO 2? 27- Sobre a tabela periódica, responda: a) Qual é o critério de classificação adotado? b) Descreva as características de uma família: c) O que são períodos? O que descrevem? d) Quem são os representantes da família O? Que outros nomes são utilizados para essa família? Justifique : 28- Dê os símbolos químicos dos seguintes elementos: Hidrogênio; sódio; magnésio; cálcio; cromo; cobre; prata; ouro; mercúrio; alumínio; fósforo; oxigênio; potássio; nitrogênio; carbono; cloro; bromo; enxofre, ferro, flúor.
4 Física Módulo I: Grandezas e Unidades Físicas 29- O que é Grandeza? 30- As grandezas podem ser classificadas em Vetoriais e Escalares. Diferencie-as, citando cinco exemplos de cada tipo: 31- Cite três unidades utilizadas em cada uma das grandezas abaixo: a) Comprimento: b) Tempo: c) Massa: d) Volume: 32- Faça as conversões de unidades pedidas seguir: a) 120m em km: b) 2,53km em m; c) 2h em min; d) 3,5kg em g; e) 3horas e 20 min em s; f) 540g em kg Módulo II: As 3 Leis do Movimento 33-Quais são as 3(três) Leis de Newton? 34-Enuncie a 1ª. Lei de Newton e dê um exemplo: 35-O que é movimento retilíneo uniforme(mru)? 36-Enuncie a 2ª Lei de Newton 37-Enuncie a 3ª Lei de Newton e cite um exemplo: 38-O que é força de atrito? 39-Diferencie força de atrito estático de força de atrito cinético: 40-Um corpo com massa de 0,9kg foi empurrado por uma força que lhe comunicou uma aceleração de 5,0m/s 2. Calcule a intensidade da força: 41- Sobre um corpo de 2000g atua uma força horizontal de intensidade 14N. a) Esquematize o conjunto descrito acima: b) Calcule a aceleração que ele adquire: 42-Na Terra, a aceleração da gravidade é de 9,8m/s 2 e, na Lua, 1,6m/s 2. Para um corpo de massa 12kg, determine: a) O peso desse corpo na Terra. b) A massa e o peso desse corpo na Lua: 43-Imagine que duas forças atuam sobre um bloco de massa 8kg. Ambas possuem a mesma direção(horizontal) e seus valores são de 14N e 25N, respectivamente F 1 e F 2.Calcule o valor e o sentido da Força Resultante quando: a) As forças F 1 e F 2 atuam no mesmo sentido( faça esquema do conjunto): b) As forças F 1 e F 2 atuam em sentidos contrários ( faça esquema do conjunto): Módulo III: Pressão e Empuxo quando necessário, adote: g= 10m/s 2 ou g = 10 N/kg verifique se as unidades são compatíveis 44- O que nos informa a pressão exercida pelas forças num material sólido? 45- Quais são as unidades de pressão? 46- Um corpo de massa igual a 10kg assumiu, após a ação de uma força, uma aceleração de 3m/s s.a força aplicada sobre ele foi de: 47- Se um material possui densidade igual a 7,0g/cm 3, 200m 3 deste material deve possuir massa igual a: 48- Três objetos A, B e C estão apoiados sobre um solo arenoso. A tabela indica os dados de cada objeto: Objeto Massa Área de contato com o solo A 0,2kg 125cm 2 B 1,2kg 2cm 2 C 2,3kg 320cm 2 Calcule: a) A pressão que cada um deles exerce contra o solo: b) Qual deles afunda mais no solo arenoso? Por quê? c) Coloque o objeto A sobre o abjeto C e calcule agora a nova pressão exercida sobre o solo: 49- Se a situação proposta no exercício anterior estivesse acontecendo num planeta onde a força exercida pela gravidade fosse de 0,6N/kg: a) Quais seriam as pressões exercidas pelos objetos A, B e C? b) Quais seriam as massas dos objetos A, B e C? RESPOSTAS: 46) F = 30N; 47) m = 1,4kg; 48) a) p A = 0,016kg/ cm 2 ; p B = 12 / 2 p B = 6kg/ cm 2; p C = 0,009kg/ cm 2 ; b) O objeto B, pois exerce maior pressão contra o solo; c) p = 0,078 kg/ cm 2 ; 49) a) p A = 0,0009 kg/ cm 2 ;p B = 0,36kg/ cm 2 ;p C =0,004kg/ cm 2 ; b) m A = 0,2Kg ; m B = 1,2kg ;m C = 2,3kg 50- Uma caixa de 0,5m 2 de área de base tem massa igual a 35kg. A pressão que ela exerce sobre o piso onde está apoiada é de: (adote g = 10N/kg) 51- A pressão exercida por um livro de massa igual a 1,2Kg que está apoiado, por sua face menor que tem 20cm x 5cm, sobre uma mesa, é de: 22) p = 0,12Kg/ cm Enumere as características mais importantes sobre a pressão que os líquidos exercem: 53-Qual é pressão que a água doce exerce a 10 metros de profundidade?( adote d águ doce = 1000N/m 3 ) 54-Com os dados do exercício anterior, calcule como sendo água salgada:?( adote d águ salgada = 1300N/m 3 ) 55-Submerso num lago, um mergulhador constata que a pressão marcada no seu medidor que se encontra no seu pulso corresponde a 1,6x10 5 N/m 2. A que profundidade se encontra o mergulhador?
5 56-Em uma instalação hidráulica, Jairo deseja que sua torneira do jardim jorre com pressão de Pa. A que altura da torneira ele deve instalar a caixa d água? Módulo IV: Energia, Trabalho e Potência 57- Enumere as condições necessárias para que haja trabalho: 58-Um carrinho é deslocado num plano horizontal sob a ação de uma força horizontal de 50N. Sendo o deslocamento igual a 5cm, calcule o trabalho realizado: 59-Uma força de 20 N, desloca na mesma direção e sentido da força um corpo de 4 kg, realizando assim um trabalho de 200 J a uma distância x. Qual o valor de x? 60-A massa de um esquiador é de 70kg. Ele gasta 35 segundos para chegar ao topo de uma rampa. A altura do topo da rampa é de 200m. Calcule: a) O peso do esquiador: b) O trabalho realizado pelo seu peso ao escalar essa rampa: 61- Cite diversos tipos de energia, incluindo exemplos para cada caso: 62-Um corpo de massa 5kg á abandonado de uma altura de 8m.Calcule a energia cinética que ele apresentará ao chegar ao solo. 63-Um corpo com massa de 400g se move a uma velocidade constante de 5m/s. Qual será a sua energia cinética? 64-Um corpo com massa de 2kg está a 400cm de altura em relação ao solo. Calcule sua energia potencial gravitacional: 65-Em uma construção, um saco de cimento 55kg está a uma altura de 120cm. Responda: a) Esse saco de cimento tem energia? Por quê? b) Que nome recebe essa energia? c) Qual é o valor dessa energia? d) Que energia esse saco de cimento adquire durante a queda? 66-Uma máquina realiza um trabalho de J em 5 segundos.calcule a potência da máquina: 67-Se um corpo executa um trabalho de 500J em 2 minutos, qual será a sua potência? 68-A potência consumida por uma máquina é de 350W. Sabendo-se que ela trabalha durante 5 minutos, determine: a) o trabalho do motor: b) o trabalho útil que ela fornece, se seu rendimento é de 60% Módulo III: Temperatura e Calor 69- Diferencie calor de temperatura. 70- O que são escalas termométricas? Cite exemplos: 71- Descreva como foi elaborada a escala : a) Celsius; b) Kelvin; c) Fahrenheit. 72- O que é o zero absoluto? Qual é o seu valor em K,F e C? 73- Efetue as conversões de escalas: a) 10ºC em ºF b) -40ºc em ºF c) 150K em ºC d) 112ºF em ºC e) 315K em ºF BOM TRABALHO!
BIMESTRAL QUÍMICA - 1ºBIMESTRE
 BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
BIMESTRAL QUÍMICA - 1ºBIMESTRE Série: 3ªEM Gabarito Questão 01) O vapor obtido pela ebulição das seguintes soluções: I. água e sal II. água e açúcar III. água e álcool é constituído de água pura apenas:
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2014 Disciplina: QUÍMICA Ano: 1º Professora: Maria Luiza ENSINO MÉDIO Caro aluno, você está recebendo o conteúdo de recuperação.
SOLUÇÃO PRATIQUE EM CASA
 SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
SOLUÇÃO PC1. Incorreta. Seria pura se apresentasse apenas moléculas de água em sua composição, porém, a água potável apresenta diversos tipos de sais dissolvidos. Correta. A água do mar pode se tornar
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA
 ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA Nome: Nº Série: 9º EFII Data: / /2015 Professor: Gustavo/Priscila Anual I. Introdução Caro aluno, Neste ano de 2015 você não obteve o mínimo de pontos e, por isso
ROTEIRO DE RECUPERAÇÃO FINAL DE QUÍMICA Nome: Nº Série: 9º EFII Data: / /2015 Professor: Gustavo/Priscila Anual I. Introdução Caro aluno, Neste ano de 2015 você não obteve o mínimo de pontos e, por isso
COLÉGIO SHALOM. Atividades de Recuperação semestral - Química 9º Ano Valor: 12,0
 COLÉGIO SHALOM Atividades de Recuperação semestral - Química 9º Ano Valor: 12,0 Profª: Nize G. Chagas Pavinato Aluno(a): Data: / / 1. Ligas metálicas importantes na indústria tais como o aço-carbono que
COLÉGIO SHALOM Atividades de Recuperação semestral - Química 9º Ano Valor: 12,0 Profª: Nize G. Chagas Pavinato Aluno(a): Data: / / 1. Ligas metálicas importantes na indústria tais como o aço-carbono que
COLÉGIO NOSSA SENHORA DO MONTE CALVÁRIO CIÊNCIAS
 COLÉGIO NOSSA SENHORA DO MONTE CALVÁRIO CIÊNCIAS SEGMENTO: ENSINO FUNDAMENTAL II ANO: 9º TÍTULO: ATIVIDADE DE REVISÃO PARA AVALIAÇÃO MENSAL II PROFESSORA: ALESSANDRA ARCA DATA: 20/ 04/ 2016 1. Classifique
COLÉGIO NOSSA SENHORA DO MONTE CALVÁRIO CIÊNCIAS SEGMENTO: ENSINO FUNDAMENTAL II ANO: 9º TÍTULO: ATIVIDADE DE REVISÃO PARA AVALIAÇÃO MENSAL II PROFESSORA: ALESSANDRA ARCA DATA: 20/ 04/ 2016 1. Classifique
Dificuldades no Ensino e Aprendizagem em Química
 Dificuldades no Ensino e Aprendizagem em Química Metodologia do Ensino II Profª Tathiane Milaré 1 2 3 Exemplo: Química da última série do Ensino Fundamental 4 Junho Agosto Setembro Outubro Novembro Fev.
Dificuldades no Ensino e Aprendizagem em Química Metodologia do Ensino II Profª Tathiane Milaré 1 2 3 Exemplo: Química da última série do Ensino Fundamental 4 Junho Agosto Setembro Outubro Novembro Fev.
Recursos para Estudo / Atividades
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2013 Disciplina: Química Série: 1ª Professora: Maria Luiza Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2013 Disciplina: Química Série: 1ª Professora: Maria Luiza Turma: FG Caro aluno, você está recebendo o conteúdo de recuperação.
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
QiD 1 1ª SÉRIE PARTE 3 FÍSICA
 QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. (1,0) Estime a ordem de grandeza do numero de passos que um atleta dá durante uma prova de maratona, sabendo que seu deslocamento é cerca de 42km e que um passo de um atleta
QiD 1 1ª SÉRIE PARTE 3 FÍSICA 1. (1,0) Estime a ordem de grandeza do numero de passos que um atleta dá durante uma prova de maratona, sabendo que seu deslocamento é cerca de 42km e que um passo de um atleta
2ª PROVA PARCIAL DE CIÊNCIAS
 COLÉGIO XIX DE MARÇO Educação do jeito que deve ser 2016 2ª PROVA PARCIAL DE CIÊNCIAS Aluno(a): Nº Ano: 9ª Turma: Data: 06/08/2016 Nota: Professor(a): Pâmella Duarte e Paulo Fernando Valor da Prova: 40
COLÉGIO XIX DE MARÇO Educação do jeito que deve ser 2016 2ª PROVA PARCIAL DE CIÊNCIAS Aluno(a): Nº Ano: 9ª Turma: Data: 06/08/2016 Nota: Professor(a): Pâmella Duarte e Paulo Fernando Valor da Prova: 40
O Que é Química? Pra que serve a Química?²
 O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
O Que é Química? Ciência que estuda as propriedades das substâncias e as leis que regem as suas combinações e decomposições ¹ Pra que serve a Química?² 1 Dicionário Michaelis 2 Figuras retiradas da Web
Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria.
 O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
O Que é Química? Química é uma Ciência Experimental que estuda a estrutura, composição e a transformação da matéria. O Método Científico OBSERVAÇÕES PROBLEMA HIPÓTESE(S) EXPERIMENTOS CONCLUSÕES CIÊNCIA:
2-Nos sistemas abaixo, diga quantos átomos, elementos, moléculas e substâncias estão representados:
 LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
LISTA DE EXERCÍCIOS- 1 1-Classifique os processos em físicos ou químicos: a) Sublimação do gelo seco b) Solidificação da água c) Queima da gasolina d) Roupa secando no varal e) Amassar papel - f) Combustão
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano
 EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
EXERCÍCIOS DE CIÊNCIAS PARA O 9 ano 1- Um sistema formado por três cubos de gelo, solução aquosa de sal de cozinha e areia apresenta quantas fases e quantos componentes? 3 componentes (água, areia e sal)
9º Ano/Turma: Data / / ) Observe os sistemas onde as esferas representam átomos. Sobre esses sistemas, a afirmação incorreta é:
 Estudante: Educadora: Daiana Araújo 9º Ano/Turma: Data / /2015 C.Curricular: Ciências/ Química 1) Observe os sistemas onde as esferas representam átomos. Sobre esses sistemas, a afirmação incorreta é:
Estudante: Educadora: Daiana Araújo 9º Ano/Turma: Data / /2015 C.Curricular: Ciências/ Química 1) Observe os sistemas onde as esferas representam átomos. Sobre esses sistemas, a afirmação incorreta é:
Exercícios Métodos de Separação. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017
 Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
Exercícios Métodos de Separação Nome: nº: Ano: 1º E.M. Professor (a): Cassio Pacheco Disciplina: Química Data da entrega: 01/06/2017 Questões Objetivas 1- Para a separação das misturas: gasolina-água e
SIMPLES SUBSTÂNCIA PURA COMPOSTA HOMOGÊNEO MISTURA HOMOGÊNEA SISTEMA SUBSTÂNCIA PURA HETEROGÊNEO MISTURA HETEROGÊNEA
 Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
Sistemas materiais HOMOGÊNEO SUBSTÂNCIA PURA? SIMPLES MISTURA HOMOGÊNEA? COMPOSTA SISTEMA? HETEROGÊNEO SUBSTÂNCIA PURA MISTURA HETEROGÊNEA Sistema É parte do universo físico que contenha ou não matéria,
26/08/15 SUBSTÂNCIAS E MISTURAS. Prof. Ms. Mayanderson (Xuxu)
 SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
SUBSTÂNCIAS E MISTURAS FENÔMENO FÍSICO: Não altera estrutura íntima da matéria. Exemplos: rasgar papel; derreter gelo (qualquer mudança de estado Físico); passagem de corrente elétrica por um Fio de cobre;
https://edsonnossol.wordpress.com
 https://edsonnossol.wordpress.com enossol@ufu.br Classificação da matéria Química Fundamental I Prof. Edson Nossol Uberlândia, 12/04/2017 Matéria: é tudo aquilo que ocupa espaço e tem massa Química: estudo
https://edsonnossol.wordpress.com enossol@ufu.br Classificação da matéria Química Fundamental I Prof. Edson Nossol Uberlândia, 12/04/2017 Matéria: é tudo aquilo que ocupa espaço e tem massa Química: estudo
Sistemas, Substâncias puras e Misturas Separação de Misturas
 INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA BAIANO Campus Valença Sistemas, Substâncias puras e Misturas Separação de Misturas Professor: José Tiago Pereira Barbosa 1 Sistemas Para facilitar a
Disciplina: Química Segmento: EM Ano/Série: 1º Turma: TA Assunto: Roteiro de Estudos Para Recuperação da I Etapa /2019 Aluno (a): Nº: Nota:
 Disciplina: Química Segmento: EM Ano/Série: 1º Turma: TA Assunto: Roteiro de Estudos Para Recuperação da I Etapa /2019 Aluno (a): Nº: Nota: Valor: 5,0 Pontos Professor (a): Rodrigo Xavier Querido (a) aluno
Disciplina: Química Segmento: EM Ano/Série: 1º Turma: TA Assunto: Roteiro de Estudos Para Recuperação da I Etapa /2019 Aluno (a): Nº: Nota: Valor: 5,0 Pontos Professor (a): Rodrigo Xavier Querido (a) aluno
PROMILITARES 16/08/2018 QUÍMICA. Professora Caroline Azevedo SEPARAÇÃO DE MISTURAS
 QUÍMICA Professora Caroline Azevedo SEPARAÇÃO DE MISTURAS Misturas Mistura Homogênea: duas ou mais substâncias com 1 fase. Mistura Heterogênea: duas ou mais substâncias com mais de 1 fase. Processos de
QUÍMICA Professora Caroline Azevedo SEPARAÇÃO DE MISTURAS Misturas Mistura Homogênea: duas ou mais substâncias com 1 fase. Mistura Heterogênea: duas ou mais substâncias com mais de 1 fase. Processos de
RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO
 6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
6 anos ETAPA Rec Final 2017 RECUPERAÇÃO SEMESTRAL (RS) PROJETO DE RECUPERAÇÃO DISCIPLINA PROFESSOR CONTEÚDOS QUÍMICA Claudia Figueiredo Apostila 5 Substâncias puras e misturas. Apostila 6,7 e 8 Separação
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017
 ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 1º ano Nome Nº Turma Data 15/12 Nota 08 Disciplina QUÍMICA TRABALHO Prof. ORLANDO Valor 30 ESTUDOS INDEPENDENTES DE RECUPERAÇÃO 01) Na química temos
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 1º ano Nome Nº Turma Data 15/12 Nota 08 Disciplina QUÍMICA TRABALHO Prof. ORLANDO Valor 30 ESTUDOS INDEPENDENTES DE RECUPERAÇÃO 01) Na química temos
Exercícios de Recuperação
 Ensino Fundamental Nível II Comp. Curricular: Ciências Data: 1º e 2º Período Aluno(a): Nº Turma: 1-9 Professor: Ana Cristina D Azevedo Visto: Nota: Exercícios de Recuperação Fenômenos 1. As transformações
Ensino Fundamental Nível II Comp. Curricular: Ciências Data: 1º e 2º Período Aluno(a): Nº Turma: 1-9 Professor: Ana Cristina D Azevedo Visto: Nota: Exercícios de Recuperação Fenômenos 1. As transformações
1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente:
 2 1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente: a) decantação e liquefação. b) sedimentação e destilação. c) filtração e sublimação.
2 1. Para a separação das misturas: gasolina-água e nitrogênio-oxigênio, os processos mais adequados são respectivamente: a) decantação e liquefação. b) sedimentação e destilação. c) filtração e sublimação.
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017
 III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
III OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 03/06/2017 ENSINO FUNDAMENTAL 9. o ano - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada),
TESTE GLOBAL AGRUPAMENTO / ESCOLA: NOME: N.º: TURMA: ANO LETIVO: / AVALIAÇÃO: PROFESSOR: ENC. EDUCAÇÃO: GRUPO I
 TESTE GLOBAL AGRUPAMENTO / ESCOLA: NOME: N.º: TURMA: ANO LETIVO: / AVALIAÇÃO: PROFESSOR: ENC. EDUCAÇÃO: GRUPO I 1. O gráfico da figura 1 representa os valores da velocidade em função do tempo, de uma partícula
TESTE GLOBAL AGRUPAMENTO / ESCOLA: NOME: N.º: TURMA: ANO LETIVO: / AVALIAÇÃO: PROFESSOR: ENC. EDUCAÇÃO: GRUPO I 1. O gráfico da figura 1 representa os valores da velocidade em função do tempo, de uma partícula
Plano de Recuperação 1º Semestre EF2-2013
 Professor: Cybelle e Ângela Ano: 9º Objetivos: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados em Ciências nos quais apresentou defasagens e os quais lhe servirão como pré-requisitos
Professor: Cybelle e Ângela Ano: 9º Objetivos: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados em Ciências nos quais apresentou defasagens e os quais lhe servirão como pré-requisitos
9 o EF. Jeosafá de P. Lima
 9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
9 o EF QUÍMICA Estudo dirigido Jeosafá de P. Lima Todas 1- A combustão do gás de cozinha (gás butano) é representada pela equação química abaixo: C4H10 + 13 / 2 O2 4 CO2 + 5 H2O O número de substâncias
Conceitos importantes: a) Matéria : Tudo o que possui massa e ocupa lugar no espaço.
 SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
SISTEMAS QUÍMICOS E SUAS TRANSFORMAÇÕES Prof. Ms. Mayanderson (Xuxu) QUÍMICA: A química estuda a natureza, as propriedades, a composição e as transformações da matéria. Ela está em nosso cotidiano e, ao
Como o átomo é um sistema eletricamente neutro, o número de prótons é sempre igual ao número de elétrons.
 Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 9º ano Ensino Fundamental A estrutura da matéria A concepção moderna do átomo Como o átomo é um sistema eletricamente neutro, o número
Apostila de Química (3º bimestre-2009) Professor: Eduardo Mesquita 9º ano Ensino Fundamental A estrutura da matéria A concepção moderna do átomo Como o átomo é um sistema eletricamente neutro, o número
2007 3ª. fase Prova para alunos da 9º. Ano LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 01) Essa prova destina-se exclusivamente a alunos da 9º. ano.
 2007 3ª. fase Prova para alunos da 9º. Ano LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 01) Essa prova destina-se exclusivamente a alunos da 9º. ano. 02) A prova contém oito (8) questões e TODAS DEVEM SER RESOLVIDAS.
2007 3ª. fase Prova para alunos da 9º. Ano LEIA ATENTAMENTE AS INSTRUÇÕES ABAIXO: 01) Essa prova destina-se exclusivamente a alunos da 9º. ano. 02) A prova contém oito (8) questões e TODAS DEVEM SER RESOLVIDAS.
02- Quais das propriedades a seguir são as mais indicadas para verificar se é pura uma certa amostra sólida de uma substância conhecida?
 PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
PROFESSOR: EQUIPE DE QUÍMICA BANCO DE QUESTÕES - QUÍMICA - 9º ANO - ENSINO FUNDAMENTAL ============================================================================================= 01- Massa, extensão
4) O íon de 11²³Na + contém: (Assinale a alternativa verdadeira)
 Componente Curricular: Química Professora: Adriana Aluno(a) Nº: Atividade: Lista de exercícios conceitos fundamentais da química, atomística, tabela periódica, ligações químicas e radioatividade. Menção:
Componente Curricular: Química Professora: Adriana Aluno(a) Nº: Atividade: Lista de exercícios conceitos fundamentais da química, atomística, tabela periódica, ligações químicas e radioatividade. Menção:
Estados de agregação da matéria. Mudanças de estado. Fenômenos
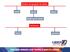 Estados de agregação da matéria sólido líquido gasoso Mudanças de estado Fenômenos físicos químicos Sistemas Interação Aspecto Composição aberto isolado substância mistura fechado homogêneo heterogêneo
Estados de agregação da matéria sólido líquido gasoso Mudanças de estado Fenômenos físicos químicos Sistemas Interação Aspecto Composição aberto isolado substância mistura fechado homogêneo heterogêneo
Roteiro para recuperação paralela
 Roteiro para recuperação paralela 9º Ano A/B - 1º trimestre de 2017 Disciplina Física 1. Objetivo: Retomar os conteúdos e atividades que não foram totalmente compreendidos e assimilados durante o 1º Trimestre.
Roteiro para recuperação paralela 9º Ano A/B - 1º trimestre de 2017 Disciplina Física 1. Objetivo: Retomar os conteúdos e atividades que não foram totalmente compreendidos e assimilados durante o 1º Trimestre.
IX OSEQUIM - Olimpíada Sergipana de Química 2ª Etapa - Modalidade A
 Bom dia aluno! Está é a prova da segunda etapa da IX OSEQUIM, Olimpíada Sergipana de Química, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2015. Confira se a sua prova
Bom dia aluno! Está é a prova da segunda etapa da IX OSEQUIM, Olimpíada Sergipana de Química, modalidade A, para alunos que se encontram cursando o 1º. Ano do ensino médio em 2015. Confira se a sua prova
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS.
 SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
SUBSTÂNCIAS PURAS, MISTURAS E SEPARAÇÃO DE MISTURAS. CAPÍTULOS 6 E 7 Prof.ª Tatiana Lima Substâncias Puras * Conceito Toda matéria cuja fusão e ebulição ocorrem a uma temperatura constante. SIMPLES * Tipos
QUÍMICA INORGÂNICA ESTRUTURA ATÔMICA PROF. NEIF NAGIB
 QUÍMICA INORGÂNICA ESTRUTURA ATÔMICA PROF. NEIF NAGIB JONH DALTON: Postulados de Dalton: 1- Toda matéria é formada por entidades extremamente pequenas, os átomos. 2- Os átomos são indivisíveis. 3- O número
QUÍMICA INORGÂNICA ESTRUTURA ATÔMICA PROF. NEIF NAGIB JONH DALTON: Postulados de Dalton: 1- Toda matéria é formada por entidades extremamente pequenas, os átomos. 2- Os átomos são indivisíveis. 3- O número
Exercícios de Revisão Ensino Médio 2º Bimestre Química: Setor A 1ª Série Professor Diego
 Exercícios de Revisão Ensino Médio 2º Bimestre Química: Setor A 1ª Série Professor Diego 1. (UFES) Na perfuração de uma jazida petrolífera, a pressão dos gases faz com que o petróleo jorre para fora. Ao
Exercícios de Revisão Ensino Médio 2º Bimestre Química: Setor A 1ª Série Professor Diego 1. (UFES) Na perfuração de uma jazida petrolífera, a pressão dos gases faz com que o petróleo jorre para fora. Ao
Atividade extra. Questão 1 Cecierj Questão 2 Cecierj Ciências da Natureza e suas Tecnologias Química
 Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
Atividade extra Questão 1 Cecierj - 2013 Desenhe uma esfera de ferro e outra de chumbo que tenham massas iguais. Para isso, considere as seguintes densidades: densidade do ferro = 7,9 g/cm3 densidade do
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 TRABALHO DE ESTUDOS INDEPENDENTES
 ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 TRABALHO DE ESTUDOS INDEPENDENTES Nome Nº Turma 9º 15 / 16 Data Nota Disciplina CIENCIAS Prof.ª JACIARA MACIEL Valor 1. As partículas que constituem
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2017 TRABALHO DE ESTUDOS INDEPENDENTES Nome Nº Turma 9º 15 / 16 Data Nota Disciplina CIENCIAS Prof.ª JACIARA MACIEL Valor 1. As partículas que constituem
ORIENTAÇÃO DE ESTUDOS
 ORIENTÇÃO DE ESTUDOS RECUPERÇÃO SEMESTRL 2º no do Ensino Médio Disciplina: Física 1. figura representa dois corpos suspensos por uma haste de peso desprezível, em equilíbrio. Sendo a massa do corpo igual
ORIENTÇÃO DE ESTUDOS RECUPERÇÃO SEMESTRL 2º no do Ensino Médio Disciplina: Física 1. figura representa dois corpos suspensos por uma haste de peso desprezível, em equilíbrio. Sendo a massa do corpo igual
SEPARAÇÃO DE MISTURAS
 SEPARAÇÃO DE MISTURAS Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias. Água do mar Não apresenta muita utilidade H 2 O NaCl Apresentam inúmeras aplicações
SEPARAÇÃO DE MISTURAS Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias. Água do mar Não apresenta muita utilidade H 2 O NaCl Apresentam inúmeras aplicações
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK
 PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: BISMARCK Substância Pura: Um único tipo de substância Simples: formada por átomos de um único elemento. Composta: formada por átomos de mais de um elemento.
MÉTODOS DE SEPARAÇÃO DE MISTURAS. 9º ano
 MÉTODOS DE SEPARAÇÃO DE MISTURAS 9º ano Separações de Misturas são utilizadas para decompor misturas de substâncias em um sistema qualquer nos dois ou mais componentes originais. Podem ser para separar
MÉTODOS DE SEPARAÇÃO DE MISTURAS 9º ano Separações de Misturas são utilizadas para decompor misturas de substâncias em um sistema qualquer nos dois ou mais componentes originais. Podem ser para separar
4. (1,0) O gráfico representa a velocidade escalar de um atleta em função do tempo em uma competição olímpica.
 PARA A VALIDADE DO QiD, AS RESPOSTAS DEVEM SER APRESENTADAS EM FOLHA PRÓPRIA, FORNECIDA PELO COLÉGIO, COM DESENVOLVIMENTO E SEMPRE A TINTA. TODAS AS QUESTÕES DE MÚLTIPLA ESCOLHA DEVEM SER JUSTIFICADAS.
PARA A VALIDADE DO QiD, AS RESPOSTAS DEVEM SER APRESENTADAS EM FOLHA PRÓPRIA, FORNECIDA PELO COLÉGIO, COM DESENVOLVIMENTO E SEMPRE A TINTA. TODAS AS QUESTÕES DE MÚLTIPLA ESCOLHA DEVEM SER JUSTIFICADAS.
Apostila de Química 12 A Matéria
 Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
Apostila de Química 12 A Matéria 1.0 Átomo x Elemento Átomo é uma partícula fundamental que compõe toda a matéria. Elemento químico é um conjunto de átomos quimicamente iguais (com o mesmo número atômico).
Metodologia do Ensino de Química II
 Metodologia do Ensino de Química II Profª Tathiane Milaré A disciplina 1. A natureza da Química e suas implicações no ensino 2. Dificuldades no ensino e aprendizagem em Química 3. Programas curriculares
Metodologia do Ensino de Química II Profª Tathiane Milaré A disciplina 1. A natureza da Química e suas implicações no ensino 2. Dificuldades no ensino e aprendizagem em Química 3. Programas curriculares
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
QUÍMICA Profº JAISON
 QUÍMICA Profº JAISON Determine o número atômico e o número de massa dos átomos A e B, que são isóbaros e apresentam a seguinte representação: 10+x 5x A 11+x 4x+8 B Afinal, o que é matéria? Chamamos de
QUÍMICA Profº JAISON Determine o número atômico e o número de massa dos átomos A e B, que são isóbaros e apresentam a seguinte representação: 10+x 5x A 11+x 4x+8 B Afinal, o que é matéria? Chamamos de
Professores: Murilo. Física. 3ª Série. 300 kg, que num determinado ponto está a 3 m de altura e tem energia cinética de 6000 J?
 Física Professores: Murilo 3ª Série EXERCÍCIOS DE Trabalho, Potência e Energia 1. Um corpo de massa 150 kg, está posicionado 17 m acima do solo. Sabendo que a aceleração da gravidade vale 10 m/s², qual
Física Professores: Murilo 3ª Série EXERCÍCIOS DE Trabalho, Potência e Energia 1. Um corpo de massa 150 kg, está posicionado 17 m acima do solo. Sabendo que a aceleração da gravidade vale 10 m/s², qual
PROMILITARES 09/08/2018 QUÍMICA. Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS
 QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
QUÍMICA Professora Caroline Azevedo ASPECTOS MACROSCÓPICOS Conteúdos abordados na aula de hoje: 1. Matéria, corpo e objeto; 2. Energias; 3. Fenômenos; 4. Classificação da matéria. Matéria e suas transformações
SUBSTÂNCIAS E MISTURAS
 SUBSTÂNCIAS E MISTURAS SUBSTÂNCIAS Uma substância química (ou apenas substância) é um material que apresenta um conjunto de propriedades bem definido e constante e tem composição fixa, independente da
SUBSTÂNCIAS E MISTURAS SUBSTÂNCIAS Uma substância química (ou apenas substância) é um material que apresenta um conjunto de propriedades bem definido e constante e tem composição fixa, independente da
Tarefa 22 Professor Gustavo
 6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
6º ano Química Tarefa 22 Professor Gustavo 01. Uma amostra de água do mar contaminada com óleo foi coletada em alto mar. Sobre os procedimentos aplicados para a separação eficiente dos componentes dessa
INSTITUTO GEREMARIO DANTAS COMPONENTE CURRICULAR: QUÍMICA EXERCÍCIOS DE RECUPERAÇÃO PARCIAL 2016
 INSTITUTO GEREMARIO DANTAS Educação Infantil, Ensino Fundamental e Médio Fone: (21) 21087900 Rio de Janeiro RJ www.igd.com.br Aluno(a): 9º Ano: Nº Professora: Lúcia Nascimento COMPONENTE CURRICULAR: QUÍMICA
INSTITUTO GEREMARIO DANTAS Educação Infantil, Ensino Fundamental e Médio Fone: (21) 21087900 Rio de Janeiro RJ www.igd.com.br Aluno(a): 9º Ano: Nº Professora: Lúcia Nascimento COMPONENTE CURRICULAR: QUÍMICA
Dificuldades no Ensino e Aprendizagem em Química
 Dificuldades no Ensino e Aprendizagem em Química Metodologia do Ensino II Profª Tathiane Milaré Exercício As variações de entalpia envolvidas nas etapas de formação de NaCl (s) a partir de átomos gasosos
Dificuldades no Ensino e Aprendizagem em Química Metodologia do Ensino II Profª Tathiane Milaré Exercício As variações de entalpia envolvidas nas etapas de formação de NaCl (s) a partir de átomos gasosos
Química Fascículo 01 Elisabeth Pontes Araújo Elizabeth Loureiro Zink José Ricardo Lemes de Almeida
 Química Fascículo 01 Elisabeth Pontes Araújo Elizabeth Loureiro Zink José Ricardo Lemes de Almeida Índice Substâncias e Misturas...1 Evolução do Modelo Atômico...3 Tabela Periódica...4 Exercícios...5 Gabarito...7
Química Fascículo 01 Elisabeth Pontes Araújo Elizabeth Loureiro Zink José Ricardo Lemes de Almeida Índice Substâncias e Misturas...1 Evolução do Modelo Atômico...3 Tabela Periódica...4 Exercícios...5 Gabarito...7
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2015
 ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2015 1º ano Nome Nº Turma Data Nota Disciplina QUÍMICA Prof. ORLANDO Valor TRABALHO DE ESTUDOS INDEPENDENTES DE RECUPERAÇÃO QUÍMICA 1ºANO 1)Fazer a distribuição
ESCOLA ESTADUAL DR. JOSÉ MARQUES DE OLIVEIRA - ANO 2015 1º ano Nome Nº Turma Data Nota Disciplina QUÍMICA Prof. ORLANDO Valor TRABALHO DE ESTUDOS INDEPENDENTES DE RECUPERAÇÃO QUÍMICA 1ºANO 1)Fazer a distribuição
Plano de Recuperação 1º Semestre EF2-2011
 Professor: Ângela Ano: 9º Objetivos: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados em Ciências nos quais apresentou defasagens e os quais lhe servirão como pré-requisitos para
Professor: Ângela Ano: 9º Objetivos: Proporcionar ao aluno a oportunidade de resgatar os conteúdos trabalhados em Ciências nos quais apresentou defasagens e os quais lhe servirão como pré-requisitos para
2. Ao afirmarmos que o gelo seco sublima, estamos nos referindo à:
 1. Observe as figuras a seguir, onde os átomos são representados por esferas e cada tamanho representa um átomo diferente. Depois, assinale a alternativa VERDADEIRA: ( A ) Nas figuras 1 e 2 encontramos
1. Observe as figuras a seguir, onde os átomos são representados por esferas e cada tamanho representa um átomo diferente. Depois, assinale a alternativa VERDADEIRA: ( A ) Nas figuras 1 e 2 encontramos
COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROFESSOR: JOÃO MEDEIROS
 COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: JOÃO MEDEIROS 2012 Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias.
COLÉGIO NOVO ANGLO DE JABOTICABAL (QUÍMICA) PROCESSOS DE SEPARAÇÃO DE MISTURAS PROFESSOR: JOÃO MEDEIROS 2012 Natureza É raro encontrarmos substâncias puras, normalmente encontramos misturas de substâncias.
1ª QUESTÃO Valor 1,0 = 1. Dados: índice de refração do ar: n 2. massa específica da cortiça: 200 kg/m 3. 1 of :36
 1ª QUESTÃO Valor 1,0 Uma lâmpada é colocada no fundo de um recipiente com líquido, diretamente abaixo do centro de um cubo de cortiça de 10 cm de lado que flutua no líquido. Sabendo que o índice de refração
1ª QUESTÃO Valor 1,0 Uma lâmpada é colocada no fundo de um recipiente com líquido, diretamente abaixo do centro de um cubo de cortiça de 10 cm de lado que flutua no líquido. Sabendo que o índice de refração
Ano: 9º Turma: 91 / 92
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2013 Disciplina: Ciências Professor (a): SUELI COSTA Ano: 9º Turma: 91 / 92 Caro aluno, você está recebendo o conteúdo de recuperação.
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Paralela 1ª Etapa 2013 Disciplina: Ciências Professor (a): SUELI COSTA Ano: 9º Turma: 91 / 92 Caro aluno, você está recebendo o conteúdo de recuperação.
Matemática. ProfªRegiane Cruz.
 Matemática ProfªRegiane Cruz regianeapcruz@yahoo.com.br Tópicos importantes: Interpretação Regra de Três Simples Porcentagem Perímetro Área Teorema de Pitágoras Trigonometria https://agrcanelas.edu.pt/blogs/expressojovem/2018/02/05/piadas-de-mat/
Matemática ProfªRegiane Cruz regianeapcruz@yahoo.com.br Tópicos importantes: Interpretação Regra de Três Simples Porcentagem Perímetro Área Teorema de Pitágoras Trigonometria https://agrcanelas.edu.pt/blogs/expressojovem/2018/02/05/piadas-de-mat/
Versão 1. Utiliza apenas caneta ou esferográfica de tinta indelével, azul ou preta.
 Teste Intermédio de Físico-Química Versão 1 Teste Intermédio Físico-Química Versão 1 Duração do Teste: 90 minutos 18.04.2013 9.º Ano de Escolaridade Decreto-Lei n.º 6/2001, de 18 de janeiro????????????
Teste Intermédio de Físico-Química Versão 1 Teste Intermédio Físico-Química Versão 1 Duração do Teste: 90 minutos 18.04.2013 9.º Ano de Escolaridade Decreto-Lei n.º 6/2001, de 18 de janeiro????????????
Exercícios de Revisão
 Aluno: Ano: 9º Revisão: Avaliação Trimestral Disciplina: Física/Química Trimestre: 2º Nome do Professor: Marcos Benfica Exercícios de Revisão 1) Um garçom, desejoso por demonstrar suas habilidades, puxou
Aluno: Ano: 9º Revisão: Avaliação Trimestral Disciplina: Física/Química Trimestre: 2º Nome do Professor: Marcos Benfica Exercícios de Revisão 1) Um garçom, desejoso por demonstrar suas habilidades, puxou
LISTA DE EXERCÍCIO PARA A PROVA MENSAL
 Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
Professor: Cassio Pacheco Aluno (a) Disciplia Química 1 Ano LISTA DE EXERCÍCIO PARA A PROVA MENSAL 1-. Assinale a alternativa onde você encontra somente substâncias compostas: a) H 2, P 4, H 2 O, O 2 b)
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES. Prof a. Giselle Blois. Estudo da matéria: substâncias, misturas, processos de separação Parte 2
 QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
QUÍMICA SUBSTÂNCIAS E SUAS PROPRIEDADES Estudo da matéria: substâncias, misturas, Parte 2 Prof a. Giselle Blois Métodos de separação de misturas: O método empregado vai depender da mistura, já que esta
Lista de Exercício. 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada sistema?
 Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
Professor: Cassio Pacheco Disciplina: Química 1 Ano Data de entrega: 07/04/2016 Lista de Exercício 1- Observe a representação dos sistemas I, II e III e seus componentes. Qual o número de fases em cada
Lista de exercícios 1 Química 1 Professor Sávio
 Lista de exercícios 1 Química 1 Professor Sávio 01 - (UEL PR/Janeiro) Quando Fahrenheit definiu a escala termométrica que hoje leva o seu nome, o primeiro ponto fixo definido por ele, o 0F, corresponde
Lista de exercícios 1 Química 1 Professor Sávio 01 - (UEL PR/Janeiro) Quando Fahrenheit definiu a escala termométrica que hoje leva o seu nome, o primeiro ponto fixo definido por ele, o 0F, corresponde
E.E. DR. JOSÉ MARQUES DE OLIVEIRA TRABALHO DE RECUPERAÇÃO FINAL NOME - Série- 9º ANO VALOR 30 pontos BIOLOGIA - Prof.
 E.E. DR. JOSÉ MARQUES DE OLIVEIRA TRABALHO DE RECUPERAÇÃO FINAL NOME - Série- 9º ANO VALOR 30 pontos BIOLOGIA - Prof. Hallan Beraldo 1) Os átomos da maioria dos elementos químicos não existem isoladamente,
E.E. DR. JOSÉ MARQUES DE OLIVEIRA TRABALHO DE RECUPERAÇÃO FINAL NOME - Série- 9º ANO VALOR 30 pontos BIOLOGIA - Prof. Hallan Beraldo 1) Os átomos da maioria dos elementos químicos não existem isoladamente,
Atividades de Recuperação Paralela de Química Setor A
 Atividades de Recuperação Paralela de Química Setor A 1ª série Ensino Médio. Conteúdos para estudos: Livro-texto Capítulo 1 SUBSTÂNCIAS QUÍMICAS: Diferenciar fenômenos químicos e físicos, diferenciar substâncias
Atividades de Recuperação Paralela de Química Setor A 1ª série Ensino Médio. Conteúdos para estudos: Livro-texto Capítulo 1 SUBSTÂNCIAS QUÍMICAS: Diferenciar fenômenos químicos e físicos, diferenciar substâncias
Atividades de Recuperação Paralela de Química
 Atividades de Recuperação Paralela de Química 1ª série Ensino Médio. Conteúdos para estudos: Química A Livro-texto Capítulo 1 SUBSTÂNCIAS QUÍMICAS: Diferenciar fenômenos químicos e físicos, diferenciar
Atividades de Recuperação Paralela de Química 1ª série Ensino Médio. Conteúdos para estudos: Química A Livro-texto Capítulo 1 SUBSTÂNCIAS QUÍMICAS: Diferenciar fenômenos químicos e físicos, diferenciar
GOIÂNIA, / / PROFESSORA: Núbia de Andrade. Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações:
 GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
GOIÂNIA, / / 2017 PROFESSORA: Núbia de Andrade DISCIPLINA: SÉRIE:1º ALUNO(a): No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente as seguintes orientações: - É fundamental
CONTEÚDO FISICANDO AULA 01 CHARLES THIBES
 CONTEÚDO Áreas das figuras planas: Notação científica Sistema Internacional de Unidades Termologia Escalas de temperatura Relação entre energia elétrica, potência e tempo Calorimetria Calor sensível e
CONTEÚDO Áreas das figuras planas: Notação científica Sistema Internacional de Unidades Termologia Escalas de temperatura Relação entre energia elétrica, potência e tempo Calorimetria Calor sensível e
INTRODUÇÃO À QUÍMICA
 INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
INTRODUÇÃO À QUÍMICA O QUE É QUÍMICA? É a ciência que estuda a matéria, suas propriedades, transformações e interações, bem como a energia envolvida nestes processos. QUAL A IMPORTÂNCIA DA QUÍMICA? Entender
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011
 ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Classifique as transformações
ESCOLA SALESIANA DE MANIQUE TESTE DE AVALIAÇÃO DE CIÊNCIAS FÍSICO-QUÍMICAS ANO LECTIVO 2010/2011 Nome: 7.º Ano Turma Nº: Encarregado de Educação: Classificação: Professor: 1. Classifique as transformações
Fundamentos de Química. PROFª LORAINE JACOBS
 Fundamentos de Química PROFª LORAINE JACOBS lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Matéria e Energia Matéria e Energia Matéria Essência Tem existência física real Tem
Fundamentos de Química PROFª LORAINE JACOBS lorainejacobs@utfpr.edu.br http://paginapessoal.utfpr.edu.br/lorainejacobs Matéria e Energia Matéria e Energia Matéria Essência Tem existência física real Tem
La Salle Águas Claras 9º ano. Propriedades da Matéria
 La Salle Águas Claras 9º ano Propriedades da Matéria Matéria Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Uma porção delimitada de matéria recebe
La Salle Águas Claras 9º ano Propriedades da Matéria Matéria Matéria é tudo que tem massa e ocupa lugar no espaço. Não existe vida nem manutenção da vida sem matéria. Uma porção delimitada de matéria recebe
Processos de Separação Misturas Para misturas Heterogêneas
 Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Ventilação: Sólido + Sólido O sólido menos denso é separado por uma corrente de ar. Catação: Sólido + Sólido Sólidos de aspectos diferentes são separados com as mãos ou uma pinça Levigação: Sólido + Sólido
Entrelinha 1,5. Utiliza apenas caneta ou esferográfica de tinta indelével, azul ou preta.
 Teste Intermédio de Físico-Química Entrelinha 1,5 Teste Intermédio Físico-Química Entrelinha 1,5 (Versão única igual à Versão 1) Duração do Teste: 90 minutos 18.04.2013 9.º Ano de Escolaridade Decreto-Lei
Teste Intermédio de Físico-Química Entrelinha 1,5 Teste Intermédio Físico-Química Entrelinha 1,5 (Versão única igual à Versão 1) Duração do Teste: 90 minutos 18.04.2013 9.º Ano de Escolaridade Decreto-Lei
FÍSICA - 1 o ANO MÓDULO 26 ENERGIA
 FÍSICA - 1 o ANO MÓDULO 26 ENERGIA m g h E pg = t P = m g h 16 F (N) 8 0 2 4 S (m) Como pode cair no enem? (ENEM) Com o objetivo de se testar a eficiência de fornos de micro-ondas, planejou-se o aquecimento
FÍSICA - 1 o ANO MÓDULO 26 ENERGIA m g h E pg = t P = m g h 16 F (N) 8 0 2 4 S (m) Como pode cair no enem? (ENEM) Com o objetivo de se testar a eficiência de fornos de micro-ondas, planejou-se o aquecimento
T.C de Química 1 o ano Prof. Alan Ibiapina
 T.C de Química 1 o ano Prof. Alan Ibiapina 01. Na natureza nada se cria nada se perde; tudo se transforma. Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em
T.C de Química 1 o ano Prof. Alan Ibiapina 01. Na natureza nada se cria nada se perde; tudo se transforma. Esse enunciado é conhecido como Lei da Conservação das Massas ou Lei de Lavoisier. Na época em
Universidade Estácio de Sá Prof. Robson Lourenço Cavalcante DISCIPLINA: FÍSICA TEÓRICA II Lista 1 Fluidos parte A ESTÁTICA DOS FLUIDOS
 1)Uma janela de escritório tem dimensões de 3,4 m de largura por 2,1 m de altura. A passagem de uma tempestade a pressão atmosférica no exterior baixa para 0,96 atm. No escritório a pressão mantém-se a
1)Uma janela de escritório tem dimensões de 3,4 m de largura por 2,1 m de altura. A passagem de uma tempestade a pressão atmosférica no exterior baixa para 0,96 atm. No escritório a pressão mantém-se a
GERAL. Unidade 1. Princípios. Elementares
 QUÍMICA GERAL Unidade 1 Princípios Elementares em Química O estudo da química A perspectiva molecular da química A matéria é constituída de relativamente poucos elementos. No nível microscópico, a matéria
QUÍMICA GERAL Unidade 1 Princípios Elementares em Química O estudo da química A perspectiva molecular da química A matéria é constituída de relativamente poucos elementos. No nível microscópico, a matéria
Hidrostática e Calorimetria PROF. BENFICA
 Hidrostática e Calorimetria PROF. BENFICA benfica@anhanguera.com www.marcosbenfica.com LISTA 1 Conceitos Iniciais/Hidrostática 1) Calcular o peso específico, o volume específico e a massa específica de
Hidrostática e Calorimetria PROF. BENFICA benfica@anhanguera.com www.marcosbenfica.com LISTA 1 Conceitos Iniciais/Hidrostática 1) Calcular o peso específico, o volume específico e a massa específica de
O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS.
 Lista de exercícios para a prova de recuperação final 1º ano EM Conteúdo. O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS. - Misturas e substâncias - Tabela e propriedades
Lista de exercícios para a prova de recuperação final 1º ano EM Conteúdo. O ALUNO DEVERÁ VIR PARA A AULA DE RECUPERAÇÃO COM A LISTA PRONTA PARA TIRAR DÚVIDAS. - Misturas e substâncias - Tabela e propriedades
GOIÂNIA, _16 / 11 / PROFESSOR: Jonas Tavares. ALUNO(a): L2 4º Bim Data da Prova: 16/11/2016
 GOIÂNIA, _16 / 11 / 2016 PROFESSOR: Jonas Tavares DISCIPLINA: Física SÉRIE: 3º ALUNO(a): L2 4º Bim Data da Prova: 16/11/2016 No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, _16 / 11 / 2016 PROFESSOR: Jonas Tavares DISCIPLINA: Física SÉRIE: 3º ALUNO(a): L2 4º Bim Data da Prova: 16/11/2016 No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica
 Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
Classificação da Matéria (Substância e Alotropia), Introdução à Atomística, Modelo de Rutherford-Böhr e Distribuição Eletrônica Classificação da Matéria (Substância e Alotropia), Introdução à Atomística,
FÍSICA - 2 o ANO MÓDULO 02 HIDROSTÁTICA EXERCÍCIOS PARTE 1
 FÍSICA - 2 o ANO MÓDULO 02 HIDROSTÁTICA EXERCÍCIOS PARTE 1 Como pode cair no enem (ENEM) Com a frequente adultertação de combustíveis, além de fiscalização, há necessidade de prover meios para que o consumidor
FÍSICA - 2 o ANO MÓDULO 02 HIDROSTÁTICA EXERCÍCIOS PARTE 1 Como pode cair no enem (ENEM) Com a frequente adultertação de combustíveis, além de fiscalização, há necessidade de prover meios para que o consumidor
COLÉGIO XIX DE MARÇO Educação do jeito que deve ser 1ª PROVA PARCIAL DE CIÊNCIAS
 COLÉGIO XIX DE MARÇO Educação do jeito que deve ser 2016 1ª PROVA PARCIAL DE CIÊNCIAS Aluno(a): Nº Ano: 9ª Turma: Data: 02/04/2016 Nota: Professor(a): Pâmella Duarte/Paulo Fernando Valor da Prova: 40 pontos
COLÉGIO XIX DE MARÇO Educação do jeito que deve ser 2016 1ª PROVA PARCIAL DE CIÊNCIAS Aluno(a): Nº Ano: 9ª Turma: Data: 02/04/2016 Nota: Professor(a): Pâmella Duarte/Paulo Fernando Valor da Prova: 40 pontos
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão:
 1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
1. Considere a tabela de pontos de fusão e ebulição das substâncias a seguir, a 1 atm de pressão: Substância PF ( C) PE ( C) Cloro -101,0-34,6 Flúor -219,6-188,1 Bromo -7,2 58,8 Mercúrio -38,8 356,6 Iodo
LOGO. Classificação da matéria. Profa. Samara Garcia
 LOGO Classificação da matéria Profa. Samara Garcia Classificação da matéria Substância pura: matéria formada por unidades químicas iguais, sejam átomos ou moléculas, e assim apresentam propriedades químicas
LOGO Classificação da matéria Profa. Samara Garcia Classificação da matéria Substância pura: matéria formada por unidades químicas iguais, sejam átomos ou moléculas, e assim apresentam propriedades químicas
