Determinação da concentração das proteínas plasmáticas (proteinémia)
|
|
|
- Agustina Paiva Galindo
- 7 Há anos
- Visualizações:
Transcrição
1 Determinação da concentração das proteínas plasmáticas (proteinémia) Faculdade de Medicina da Universidade de Coimbra Bioquímica I 1.º Ano do Mestrado Integrado de Medicina Turma 6 Ano lectivo 2010/2011
2 Sumário Nesta actividade experimental pretende-se determinar a quantidade de proteína no soro plasmático. Para o efeito procedeu-se à espectrofotometria de uma amostra de soro, tendo-se traçado primeiramente uma curva padrão.
3 Objectivos Aprofundar os conhecimentos sobre compostos proteicos; Determinar a proteinémia de uma amostra; Compreender de que forma a proteinémia nos permite identificar diversas patologias.
4 Introdução As proteínas são polímeros de L-aminoácidos, unidos entre si por ligações peptídicas (planar e rígida). Todos os peptídeos possuem um grupo NH 2 e um grupo COOH terminais; são estes dois grupos moleculares, consoante estejam ou não livres, os responsáveis pelo comportamento ácido-base das proteínas. Cadeia lateral - define as características de cada aminoácido (de acordo com ph)
5 Introdução Com base na interacção dos grupos R com a água(ph=7) existem aminoácidos: Apolares; Polares Com carga Positiva Negativa Sem carga
6 Introdução A forma iónica dos aminoácidos pode ser influenciada pelo ph; PI: ph exacto ao qual determinado aminoácido tem carga nula e existe na sua forma de zwitterião (ião híbrido, com duas cargas opostas); A carga eléctrica a um determinado ph permite a separação de aminoácidos por electroforese ou por cromatografia de troca iónica; A cadeia polipeptídica tem uma determinada direcção: o grupo amina terminal localiza-se à esquerda e grupo carboxilo terminal à direita.
7 Introdução Estrutura das proteínas - primária - secundária (hélice alfa ou folhas beta) - terciária - quaternária Classificação das proteínas - Holoproteínas - Heteroproteínas
8 Introdução Funções das proteínas - Catálise enzimática - Transporte e armazenamento - Movimento - Suporte mecânico - Respostas imunológicas - Geração e transmissão do impulso nervoso - Controlo do crescimento e diferenciação - Manutenção da pressão osmótica - Tampões
9 Introdução PROTEÍNAS PLASMÁTICAS Proteínas simples : Albumina É a proteína plasmática mais abundante. Tem como principais funções: 1. Manutenção da pressão osmótica 2. Transporte de substâncias (ex. hormonas, cálcio, drogas) Glicoproteínas: maior parte (ex. imunoglobulinas) Lipoproteínas: intervêm no transporte de lípidos.
10 Introdução PROTEÍNAS PLASMÁTICAS Concentração de proteínas plasmáticas (g/100ml) Albumina 4,0-5,2 Globulinas 1,9-2,7 Globulina α1 0,2 0,4 Globulina α2 0,4 0,7 Globulina β 0,7 0,9 Globulina γ 0,7 1,4 Relação 2:1 entre albumina e globulinas Proteinémia normal: g/l
11 Introdução CORRELAÇÕES CLÍNICAS Hiperproteinémia 1. A relação albumina/ globulina é normal: hemoconcentração A relação albumina/ globulina é anormal: a) aumento de albumina erro técnico b) aumento das globulinas: - Síndromes infecciosos - Mieloma múltiplo - Macroglobulinémia de Waldenström
12 Introdução CORRELAÇÕES CLÍNICAS Hipoproteinémia - Perdas renais: síndrome nefrótico - Processos neoplásicos - Processos de absorção deficiente - Defeito de síntese: insuficiência hepatocelular das doenças crónicas - Gastroenteropatias exsudativas
13 Introdução CORRELAÇÕES CLÍNICAS Hipoalbuminémia 1. Diminuição de síntese (Nutrição deficiente, Absorção deficiente, Doenças hepáticas) 2. Aumento do volume de distribuição (Hiperhidratação, Aumento da permeabilidade capilar, Hipoxémia, Septicémia) 3. Aumento da excreção ou degradação (Síndrome nefrótico, Enteropatias com perda de proteínas, Queimaduras, Hemorragias, Estados de aumento do catabolismo (sepsis, febre, doenças malignas).
14 Introdução Determinação das concentração de proteínas plasmáticas A concentração de proteínas é determinada a partir da densidade óptica (DO) da solução a um determinado comprimento de onda(λ) ao qual apresentam o máximo de absorção. A banda de absorção das proteínas encontra-se nos 280nm (ultravioleta) devido à presença de aminoácidos aromáticos (Tyr, Trp, Phe). Utiliza-se o espectrofotómetro de luz visível, logo é necessário corar as proteínas. Para tal, o reagente mais utilizado é o Biureto. O cobre do Biureto reage com a cadeia peptídica (no mínimo 2 ligações peptidicas), e ocorre a formação de um complexo de cor violeta, que permite identificar a presença do Biureto numa amostra, por espectrofotometria a λ max 540 nm.
15 Introdução Determinação das concentração de proteínas membranares Para libertar as proteínas dos lípidos que constituem as membranas DETERGENTE desnatura as proteínas separa os constituintes das membranas Interacção mais eficaz com o reagente de detecção, e consequente obtenção de resultados mais reprodutíveis
16 Material Tubos de Ensaio; Pipetas graduadas; Macrocontrolador de Pipetas; Espectrofotómetro; Cuvetes; Albumina a 0,4%; Água desionizada; Amostra; Reagente (biureto).
17 Procedimentos Procedimentos dos grupos I e III 1. Fazer uma curva padrão segundo o esquema: TUBOS ALBUMINA 0,4% H 2 O REAGENTE DO (540 nm) 1 0 ml 2,00 ml 2 ml 2 0,25 ml 1,75 ml 2 ml 3 0,45 ml 1,55 ml 2 ml 4 0,65 ml 1,35 ml 2 ml 5 0,85 ml 1,15 ml 2 ml 2. Ler a DO a 540 nm. O tubo 1 deve ser ajustado a zero de absorvância, passando a funcionar como branco, para que a curva padrão passe na origem do gráfico.
18 Procedimentos Procedimentos dos grupos II e IV 1. Preparar as amostras fazendo uma diluição do soro sanguíneo de 20 vezes com o soro fisiológico. As amostras devem ser preparadas em duplicado e determinada a média, conforme o seguinte esquema. DO (540 nm) 0,5 ml AMOSTRA 1,5 ml H 2 O 2 ml de reagente 0,5 ml AMOSTRA 1,5 ml H 2 O 2 ml de reagente MÉDIA Esperar 10 minutos. 2. Ler a DO a 540 nm. 3. Fazer os cálculos para a determinação da quantidade de proteína no soro sanguíneo (mg/ml; g/l), tendo em conta o factor de diluição (20x).
19 Resultados
20 Resultados do grupo I Exemplificação do cálculo da massa de Albumina 0,4% TUBO 2 0,4g 100ml x 0,25ml x = 1 mg TUBO Albumina (mg) DO (540 nm) , ,8 0, ,6 0, ,4 0,148 DO (540 nm) 0,16 0,14 0,12 0,1 0,08 0,06 0,04 0, Massa de Albumina (mg) Tabela 1 Valores de absorvância obtidos para 540 nm, e a quantidade de albumina, em mg, presente no respectivo um. Gráfico 1 - Relação entre massa de albumina na amostra, em miligramas, e absorvância para 540 nm.
21 Resultados do grupo III TUBO Albumina (mg) DO (540 nm) , ,8 0, ,6 0, ,4 0,237 DO (540 nm) 0,16 0,26 0,24 0,14 0,22 0,12 0,2 0,18 0,16 0,14 0,08 0,12 0,06 0,1 0,08 0,04 0,06 0,02 0,04 0, Massa de Albumina (mg) Tabela 2 Valores de absorvância obtidos para 540 nm, e a quantidade de albumina, em mg, presente no respectivo um. Gráfico 2 - Relação entre massa de albumina na amostra, em miligramas, e absorvância para 540 nm.
22 Resultados e Cálculos do grupo II Tubo 1 0,272 Tubo 2 0,279 Absorvância=0,276 Nota: Devido aos erros do gráfico do Grupo I, o Grupo II guiou-se pelo gráfico do Grupo III. Média da DO para os dois tubos: 0,276 3,96 mg de albumina Se 3,96 mg proteína Logo 7,91 mg proteína 0,5 ml de amostra 1 ml de amostra Concentração no soro, tendo em conta o factor de diluição (20 x), é de 7,91 x 20 = 158 mg/ml
23 Resultados e Cálculos do grupo IV Tubo 1 0,234 Tubo 2 0,226 Absorvância=0,230 Média da DO para os dois tubos: 0,230 3,25 mg de albumina Se 3,25 mg proteína Logo 6,50 mg proteína 0,5 ml de amostra 1 ml de amostra Concentração no soro, tendo em conta o factor de diluição (20 x), é de 6,50 x 20 = 130 mg/ml
24 Discussão Verificamos que quanto maior é o volume de albumina, mais azul fica a solução após a adição de reagente biureto; e que quanto maior a concentração de albumina, maior é a absorvância (D.O.). A partir da média das absorvâncias das duas amostras (D.O. = 0,23), encontrámos o valor da quantidade da proteína albumina no soro sanguíneo (através do gráfico da curva-padrão) e, tendo em conta o factor de diluição de 20x, multiplicámos por 20. O valor obtido de 130 mg/ml é bastante acima dos valores normais [N g/l], o que pode indicar que estamos perante um indivíduo com hiperproteinémia ou que ocorreram erros experimentais significativos.
25 Discussão Apesar de o gráfico obtido se aproximar de uma recta, não o é. Este facto contraria a Lei de Lambert-Beer, o que pode ser explicado pelo facto de existirem erros experimentais: erros de medições, erros de calibração, erros associados aos aparelhos, entre outros. O espectrofotómetro apenas teve em conta o valor da absorvância da proteína albumina, havendo outras proteínas no soro cuja absorvância é desprezada.
26 Conclusão Através da leitura da densidade óptica de uma amostra de sangue por espectrofotometria, é possível determinar a quantidade de proteína existente no sangue e a sua concentração, ou proteinémia. A determinação da proteinémia é importante no diagnóstico de variadas patologias (tais como síndromes infecciosos, perdas renais, processos neoplásicos, processos de absorção deficiente, entre outros) já que as proteínas plasmáticas desempenham variadas funções no organismo e as alterações da sua concentração podem ter causas patológicas.
27 Bibliografia BERG, Jeremy M.; TYMOCZKO, John L.; STRYER, Lubert; Biochemistry; Freeman, 6th Edition, Protocolos experimentais de Bioquímica I.
BIOQUÍMICA I 1º ANO MESTRADO INTEGRADO MEDICINA
 BIOQUÍMICA I 1º ANO MESTRADO INTEGRADO MEDICINA 2009 2010 Seminário Orientado 2 Métodos de identificação de biomoléculas e análise de proteínas Autoria Amélia Fernandes Ana Caetano Ana Padilha Ana Martins
BIOQUÍMICA I 1º ANO MESTRADO INTEGRADO MEDICINA 2009 2010 Seminário Orientado 2 Métodos de identificação de biomoléculas e análise de proteínas Autoria Amélia Fernandes Ana Caetano Ana Padilha Ana Martins
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
Electroforese de proteínas plasmáticas
 6ª aula prática Electroforese de proteínas plasmáticas 1º Ano, Turma 6 Bioquímica I FMUC Objectivos Análise qualitativa de proteínas plasmáticas (separação por electroforese) Compreender a utilidade deste
6ª aula prática Electroforese de proteínas plasmáticas 1º Ano, Turma 6 Bioquímica I FMUC Objectivos Análise qualitativa de proteínas plasmáticas (separação por electroforese) Compreender a utilidade deste
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010. Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA PRÁTICA Determinação
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2009/2010 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 7ª AULA PRÁTICA Determinação
PURIFICAÇÃO PARCIAL DOS ANTICORPOS PRESENTES NO SORO NORMAL ATRAVÉS DA PRECIPITAÇÃO DA FRAÇÃO GAMA- GLOBULINA COM SULFATO AMÔNIO
 PURIFICAÇÃO PARCIAL DOS ANTICORPOS PRESENTES NO SORO NORMAL ATRAVÉS DA PRECIPITAÇÃO DA FRAÇÃO GAMA- GLOBULINA COM SULFATO AMÔNIO Priscila Diniz Lopes Doutoranda em MV, área de concentração Patologia Animal
PURIFICAÇÃO PARCIAL DOS ANTICORPOS PRESENTES NO SORO NORMAL ATRAVÉS DA PRECIPITAÇÃO DA FRAÇÃO GAMA- GLOBULINA COM SULFATO AMÔNIO Priscila Diniz Lopes Doutoranda em MV, área de concentração Patologia Animal
Detecção de proteínas. Proteínas são heteropolímeros de aminoácidos unidos por ligações peptídicas
 Detecção de proteínas Proteínas são heteropolímeros de aminoácidos unidos por ligações peptídicas A detecção e quantificação de uma proteína através de espectrofotometria se baseia nas propriedades de
Detecção de proteínas Proteínas são heteropolímeros de aminoácidos unidos por ligações peptídicas A detecção e quantificação de uma proteína através de espectrofotometria se baseia nas propriedades de
Constituintes básicos de uma célula - Biomoléculas. Biomoléculas
 Biomoléculas Todas as moléculas que fazem parte da constituição dos seres vivos são designadas biomoléculas. Formam-se a partir da união de bioelementos. Biomoléculas Os bioelementos combinam-se entre
Biomoléculas Todas as moléculas que fazem parte da constituição dos seres vivos são designadas biomoléculas. Formam-se a partir da união de bioelementos. Biomoléculas Os bioelementos combinam-se entre
Aminoácidos e peptídeos. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012. Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 5ª AULA PRÁTICA Determinação
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 5ª AULA PRÁTICA Determinação
Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N Professores. Carlos T. Hotta Ronaldo B.
 Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2016 Professores Carlos T. Hotta Ronaldo B. Quaggio 1 1. Um extrato de proteínas foi obtido a partir da
Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2016 Professores Carlos T. Hotta Ronaldo B. Quaggio 1 1. Um extrato de proteínas foi obtido a partir da
Origem grego (protos) primeira, mais importante
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
Macromolécula mais abundante nas células
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008. Disciplina de BIOQUÍMICA I Curso de MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2007/2008 Disciplina de BIOQUÍMICA I Curso de MEDICINA º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação da actividade enzimática
AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES
 Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Biologia e Geologia 10º ano. Natércia Charruadas 2011
 Biologia e Geologia 10º ano Natércia Charruadas 2011 Todos os seres vivos, logo todas as células, são constituídos por moléculas orgânicas de grandes dimensões macromoléculas. Estas são formadas por um
Biologia e Geologia 10º ano Natércia Charruadas 2011 Todos os seres vivos, logo todas as células, são constituídos por moléculas orgânicas de grandes dimensões macromoléculas. Estas são formadas por um
Proteínas. Proteínas são polímeros de aminoácidos
 Proteínas Estrutura & Propriedades Proteínas são polímeros de aminoácidos Existem 20 tipos diferentes de aminoácidos Aminoácidos são ácidos fracos A carga elétrica do aminoácido varia de acordo com o ph
Proteínas Estrutura & Propriedades Proteínas são polímeros de aminoácidos Existem 20 tipos diferentes de aminoácidos Aminoácidos são ácidos fracos A carga elétrica do aminoácido varia de acordo com o ph
São macromoléculas com alto peso molecular, formadas por unidades denominadas aminoácidos (aa), ligados entre si através de ligações peptídicas.
 AS PROTEÍNAS São macromoléculas com alto peso molecular, formadas por unidades denominadas aminoácidos (aa), ligados entre si através de ligações peptídicas. Mais de 100 aa Menos de 100 aa polipeptídeo
AS PROTEÍNAS São macromoléculas com alto peso molecular, formadas por unidades denominadas aminoácidos (aa), ligados entre si através de ligações peptídicas. Mais de 100 aa Menos de 100 aa polipeptídeo
29/08/2015 QUÍMICA DE PROTEÍNAS. Medicina Veterinária IBGM - IBS. Medicina Veterinária IBGM - IBS
 QUÍMICA DE PROTEÍNAS D i s c i p l i n a : b i o q u í m i c a, p r o f. D r. Va g n e O l i v e i ra E-mail: vagne_melo_oliveira@outlook.com Medicina Veterinária IBGM - IBS Medicina Veterinária IBGM -
QUÍMICA DE PROTEÍNAS D i s c i p l i n a : b i o q u í m i c a, p r o f. D r. Va g n e O l i v e i ra E-mail: vagne_melo_oliveira@outlook.com Medicina Veterinária IBGM - IBS Medicina Veterinária IBGM -
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III
 Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
Aula: 18 Temática: Estrutura dos aminoácidos e proteínas parte III A maioria das cadeias polipeptídicas naturais contém entre 50 e 2.000 aminoácidos e são comumente referidas como proteínas. Peptídeos
Solubilidade das Proteínas
 TÉCNICAS LABORATORIAIS EM QUÍMICA E BIOQUÍMICA Solubilidade das Proteínas Miguel Mourato (Coordenador) Joana Sales Mestrado em Engenharia Zootécnica ISA, 2018/2019 1 Proteínas macromoléculas constituídas
TÉCNICAS LABORATORIAIS EM QUÍMICA E BIOQUÍMICA Solubilidade das Proteínas Miguel Mourato (Coordenador) Joana Sales Mestrado em Engenharia Zootécnica ISA, 2018/2019 1 Proteínas macromoléculas constituídas
Aminoácidos, Péptidos e Proteínas
 Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas
 Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Composição e Estrutura Molecular dos Sistemas Biológicos
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica Composição e Estrutura Molecular dos Sistemas Biológicos Átomos e Moléculas Hierarquia
Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica Composição e Estrutura Molecular dos Sistemas Biológicos Átomos e Moléculas Hierarquia
Biomoléculas. * Este esquema não está a incluir as Vitaminas que são classificadas no grupo de moléculas orgânicas. Biomoléculas
 Biomoléculas Biomoléculas Inorgânicas Orgânicas Água Sais Minerais Glícidos Lípidos Prótidos Ácidos Nucléicos * Este esquema não está a incluir as Vitaminas que são classificadas no grupo de moléculas
Biomoléculas Biomoléculas Inorgânicas Orgânicas Água Sais Minerais Glícidos Lípidos Prótidos Ácidos Nucléicos * Este esquema não está a incluir as Vitaminas que são classificadas no grupo de moléculas
Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Funcionamento do Espectrofotômetro. Glicemia. Professor: Dr.
 Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Funcionamento do Espectrofotômetro. Glicemia. Professor: Dr. Fernando Ananias NOME: RA: ATIVIDADE PRÁTICA 1 A- ESPECTROFOTOMETRIA Espectroscopia
Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Funcionamento do Espectrofotômetro. Glicemia. Professor: Dr. Fernando Ananias NOME: RA: ATIVIDADE PRÁTICA 1 A- ESPECTROFOTOMETRIA Espectroscopia
DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DE TRIGLICÉRIDOS E COLESTEROL
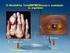 DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DE TRIGLICÉRIDOS E COLESTEROL Determinação da concentração plasmática de triglicéridos por um método enzimático O conteúdo em triglicéridos pode ser determinado
DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DE TRIGLICÉRIDOS E COLESTEROL Determinação da concentração plasmática de triglicéridos por um método enzimático O conteúdo em triglicéridos pode ser determinado
Rafael Mesquita. Aminoácidos
 Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
INTRODUÇÃO À BIOQUÍMICA DA CÉLULA. Bioquímica Celular Prof. Júnior
 INTRODUÇÃO À BIOQUÍMICA DA CÉLULA Histórico INTRODUÇÃO 1665: Robert Hooke Compartimentos (Células) 1840: Theodor Schwann Teoria Celular 1. Todos os organismos são constituídos de uma ou mais células 2.
INTRODUÇÃO À BIOQUÍMICA DA CÉLULA Histórico INTRODUÇÃO 1665: Robert Hooke Compartimentos (Células) 1840: Theodor Schwann Teoria Celular 1. Todos os organismos são constituídos de uma ou mais células 2.
Turma Fisioterapia - 2º Termo. Profa. Dra. Milena Araújo Tonon Corrêa
 Turma Fisioterapia - 2º Termo Profa. Dra. Milena Araújo Tonon Corrêa Administração Absorção Fármaco na circulação sistêmica Distribuído Biotransformado Excretado Farmacocinética : O que o organismo faz
Turma Fisioterapia - 2º Termo Profa. Dra. Milena Araújo Tonon Corrêa Administração Absorção Fármaco na circulação sistêmica Distribuído Biotransformado Excretado Farmacocinética : O que o organismo faz
PROTEÍNAS. A palavra proteína derivada de proteos, (grego = primeira ou a mais importante)
 PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
PROTEÍNAS A palavra proteína derivada de proteos, (grego = primeira ou a mais importante) Macromolécula mais abundante nas células Produto final da informação genética (DNA-RNA-Proteína) Diversidade funcional
Proteínas. - Revisão - Prof a. Dr a. Elisa d Avila Costa Cavalcanti. Bromatologia EN/UNIRIO
 Proteínas - Revisão - Prof a. Dr a. Elisa d Avila Costa Cavalcanti Bromatologia EN/UNIRIO 2018.2 O que são proteínas? Aminoácidos α 21 tipos Grupos R Tendência de interagir com a água em ph intracelular
Proteínas - Revisão - Prof a. Dr a. Elisa d Avila Costa Cavalcanti Bromatologia EN/UNIRIO 2018.2 O que são proteínas? Aminoácidos α 21 tipos Grupos R Tendência de interagir com a água em ph intracelular
Lista de Exercícios de Bioquímica
 Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Universidade Federal de Santa Catarina - UFSC Departamento de Bioquímica - CCB Disciplina: BQA5125 - Bioquímica para Engenharia Sanitária e Ambiental Bolsistas REUNI: Priscila G. A. Martins e Tiago Bortolotto
Engenharia Biomédica. Relatório Cinética da Enzima Invertase
 Engenharia Biomédica Bioquímica e Biologia Molecular Relatório Cinética da Enzima Invertase Relatório realizado por: Ana Calhau nº54605 Dárcio Silva nº54214 José Frazão nº54198 1º Semestre, Ano Lectivo
Engenharia Biomédica Bioquímica e Biologia Molecular Relatório Cinética da Enzima Invertase Relatório realizado por: Ana Calhau nº54605 Dárcio Silva nº54214 José Frazão nº54198 1º Semestre, Ano Lectivo
BIOQUÍMICA. Profº André Montillo
 BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
BIOQUÍMICA Profº André Montillo www.montillo.com.br Definição: É uma Molécula Orgânica que contém simultaneamente grupo funcionais amina (NH2) e carboxílico (COOH) É formado pelos seguintes Átomos: o Carbono
- Apresentam uma fórmula básica: um átomo central de carbono onde se ligam:
 1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
Aula 5 Estrutura e função de proteínas
 Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
Aula 5 Estrutura e função de proteínas parte 1: aminoácidos Parte 2: estrutura Proteínas As proteínas são os principais constituinte da célula Importantes na manutenção da vida Desempenham diversas funções
Proteinas. Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini
 Proteinas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Proteinas Moléculas orgânicas; Alto peso molecular; Fundamentais estrutural e funcionalmente;
Proteinas Disciplina: Bioquímica Curso: Análises Clínicas 3º. Módulo Docente: Profa. Dra. Marilanda Ferreira Bellini Proteinas Moléculas orgânicas; Alto peso molecular; Fundamentais estrutural e funcionalmente;
Proteínas funcionais: hemoglobina e mioglobina
 BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011 9ª aula teórica 18 Outubro 2010 Proteínas funcionais: hemoglobina e mioglobina - Biochemistry (J. M. Berg, J. L. Tymozko, L. Stryer) 6ª Ed., W. H.
BIOQUÍMICA 1º ano de Medicina Ensino teórico 2010/2011 9ª aula teórica 18 Outubro 2010 Proteínas funcionais: hemoglobina e mioglobina - Biochemistry (J. M. Berg, J. L. Tymozko, L. Stryer) 6ª Ed., W. H.
LIGAÇÃO PEPTÍDICA. ligação peptídica DIPEPTÍDEO AMINOÁCIDOS
 PROTEÍNAS PROTEÍNAS LIGAÇÃO PEPTÍDICA DIPEPTÍDEO AMINOÁCIDOS ligação peptídica PEPTÍDEO Resíduo N-terminal Resíduo C-terminal OLIGOPEPTÍDEOS: 2 a 10 resíduos de aminoácidos. Exemplos: dipeptídio (2 aminoácidos),
PROTEÍNAS PROTEÍNAS LIGAÇÃO PEPTÍDICA DIPEPTÍDEO AMINOÁCIDOS ligação peptídica PEPTÍDEO Resíduo N-terminal Resíduo C-terminal OLIGOPEPTÍDEOS: 2 a 10 resíduos de aminoácidos. Exemplos: dipeptídio (2 aminoácidos),
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas.
 São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
São macromoléculas formadas pela união de muitos aminoácidos. Esses aminoácidos estão ligados um ao outro por meio de ligações peptídicas. Proteínas possuem muitas funções dentro do organismo. Aminoácidos
Estrutura Secundária
 Bioinformática I Estrutura Secundária Profa. Dra. Ignez Caracelli bit.603@gmail.com Julio Zukerman Schpector 1 Ignez Caracelli aminoácido em sua forma ionizada forma zwitteriônica cadeia lateral amino-terminal
Bioinformática I Estrutura Secundária Profa. Dra. Ignez Caracelli bit.603@gmail.com Julio Zukerman Schpector 1 Ignez Caracelli aminoácido em sua forma ionizada forma zwitteriônica cadeia lateral amino-terminal
Proteínas: Estrutura terciária
 Proteínas Proteínas Proteínas Estrutura Primária Ligação covalente Secundária Ligação de Hs Terciária Ligações S-S e H Interacções hidrofóbicas e electrostáticas Forças de Van der Walls Quaternária Ligações
Proteínas Proteínas Proteínas Estrutura Primária Ligação covalente Secundária Ligação de Hs Terciária Ligações S-S e H Interacções hidrofóbicas e electrostáticas Forças de Van der Walls Quaternária Ligações
Aminoácidos e Peptídeos
 Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
MONITORIZAÇÃO DA DEGRADAÇÃO DO GLICOGÉNIO
 MONITORIZAÇÃO DA DEGRADAÇÃO DO GLICOGÉNIO 1. Objectivo Neste trabalho, ir-se-á observar a degradação do glicogénio ao longo tempo: i) em meio ácido e à temperatura de 100ºC (degradação química); ii) em
MONITORIZAÇÃO DA DEGRADAÇÃO DO GLICOGÉNIO 1. Objectivo Neste trabalho, ir-se-á observar a degradação do glicogénio ao longo tempo: i) em meio ácido e à temperatura de 100ºC (degradação química); ii) em
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011. Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 8ª AULA PRÁTICA Determinação
Introdução. Estrutura dos Aminoácidos e Proteínas. Aminoácidos componentes de proteínas. Aminoácidos componentes de proteínas 10/02/2012.
 Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Ligação peptídica Aminoácido 1 Aminoácido 2 um dipeptídeo A ligação peptídica é uma amida. O -C NH 2 Não são reações espontâneas
Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Ligação peptídica Aminoácido 1 Aminoácido 2 um dipeptídeo A ligação peptídica é uma amida. O -C NH 2 Não são reações espontâneas
Bioquímica: Componentes orgânicos e inorgânicos necessários à vida. Leandro Pereira Canuto
 Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
3. Metais Ambiente e Vida. A Cor nos Complexos Dulce Campos
 A Cor nos Complexos 1 A Cor nos Complexos Porquê uma solução apresenta cor? 2 A Cor nos Complexos 3 A Cor nos Complexos Porquê os complexos apresentam cor? [Ar] 3d 1 4 A Cor nos Complexos Espectro de Absorção
A Cor nos Complexos 1 A Cor nos Complexos Porquê uma solução apresenta cor? 2 A Cor nos Complexos 3 A Cor nos Complexos Porquê os complexos apresentam cor? [Ar] 3d 1 4 A Cor nos Complexos Espectro de Absorção
Faculdade de Medicina. Bioquímica I
 Faculdade de Medicina Bioquímica I Aprofundar conhecimentos acerca da composição química do sangue Determinar o Hematócrito INTRODUÇÃO O sangue é constituído por plasma e células sanguíneas, de entre as
Faculdade de Medicina Bioquímica I Aprofundar conhecimentos acerca da composição química do sangue Determinar o Hematócrito INTRODUÇÃO O sangue é constituído por plasma e células sanguíneas, de entre as
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO CENTRO DE CIÊNCIAS MATEMÁTICAS E DA NATUREZA INSTITUTO DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA
 UNIVERSIDADE FEDERAL DO RIO DE JANEIRO CENTRO DE CIÊNCIAS MATEMÁTICAS E DA NATUREZA INSTITUTO DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA DISCIPLINA: IQB-248 - BIOQUÍMICA EQ PRÉ-REQUISITOS: QUÍMICA ORGÂNICA
UNIVERSIDADE FEDERAL DO RIO DE JANEIRO CENTRO DE CIÊNCIAS MATEMÁTICAS E DA NATUREZA INSTITUTO DE QUÍMICA DEPARTAMENTO DE BIOQUÍMICA DISCIPLINA: IQB-248 - BIOQUÍMICA EQ PRÉ-REQUISITOS: QUÍMICA ORGÂNICA
Faculdade de Imperatriz FACIMP
 Faculdade de Imperatriz FACIMP Disciplina: Farmacologia Prof. Dr. Paulo Roberto da Silva Ribeiro 5 o Período de Farmácia e Bioquímica 1 o Semestre de 2007 Prof. Dr. Paulo Roberto 1 FARMACOCINÉTICA PROCESSOS
Faculdade de Imperatriz FACIMP Disciplina: Farmacologia Prof. Dr. Paulo Roberto da Silva Ribeiro 5 o Período de Farmácia e Bioquímica 1 o Semestre de 2007 Prof. Dr. Paulo Roberto 1 FARMACOCINÉTICA PROCESSOS
PRÁTICA: CARACTERIZAÇÃO DE PROTEÍNAS
 CENTRO DE CIÊNCIAS E TECNOLOGIA DISCIPLINA BIOQUÍMICA Profas. Roziana Jordão e Alexandra Salgueiro PRÁTICA: CARACTERIZAÇÃO DE PROTEÍNAS I Objetivos Caracterizar a presença de proteínas; Verificar experimentalmente
CENTRO DE CIÊNCIAS E TECNOLOGIA DISCIPLINA BIOQUÍMICA Profas. Roziana Jordão e Alexandra Salgueiro PRÁTICA: CARACTERIZAÇÃO DE PROTEÍNAS I Objetivos Caracterizar a presença de proteínas; Verificar experimentalmente
Espectros de Absorção
 Espectros de Absorção Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 21 /4/99 Introdução Este trabalho prático trabalhos consistiu no estudo, análise e interpretação do espectro de absorção de espécies
Espectros de Absorção Rui Pedro Lousa das Neves Bioquímica Grupo 3 Coimbra 21 /4/99 Introdução Este trabalho prático trabalhos consistiu no estudo, análise e interpretação do espectro de absorção de espécies
Universidade de São Paulo QFL0343: Reações de Compostos Orgânicos II e Biomoléculas Grupo 2: Peptídeos e Proteínas - Estrutura de Proteínas
 Universidade de São Paulo QFL0343: Reações de Compostos Orgânicos II e Biomoléculas - 2016 Grupo 2: Peptídeos e Proteínas - Estrutura de Proteínas Alex Monteiro Magalhães (8020779) Karina Brandt (8566483)
Universidade de São Paulo QFL0343: Reações de Compostos Orgânicos II e Biomoléculas - 2016 Grupo 2: Peptídeos e Proteínas - Estrutura de Proteínas Alex Monteiro Magalhães (8020779) Karina Brandt (8566483)
Departamento de Zoologia da Universidade de Coimbra
 Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Departamento de Zoologia da Universidade de Coimbra Armando Cristóvão Adaptado de "The Tools of Biochemistry" de Terrance G. Cooper Espectrofotometria de Absorção Uma das primeiras características químicas
Objectivo: Separar uma proteína das restantes no extracto celular. Estratégia: Existem inúmeras técnicas de purificação disponíveis.
 Objectivo: Separar uma proteína das restantes no extracto celular Estratégia: Existem inúmeras técnicas de purificação disponíveis. O procedimento exacto e a ordem dos métodos a aplicar dependem do tipo
Objectivo: Separar uma proteína das restantes no extracto celular Estratégia: Existem inúmeras técnicas de purificação disponíveis. O procedimento exacto e a ordem dos métodos a aplicar dependem do tipo
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos
 Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Graduação em Biotecnologia Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Metodologias para quantificar proteínas Qualquer trabalho com proteína deve envolver a quantificação
Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Metodologias para quantificar proteínas Qualquer trabalho com proteína deve envolver a quantificação
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA EQUILÍBRIO ÁCIDO-BASE NO ORGANISMO HUMANO REGULAÇÃO DA CONCENTRAÇÃO HIDROGENIÓNICA - IMPORTÂNCIA
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 5ª AULA PRÁTICA EQUILÍBRIO ÁCIDO-BASE NO ORGANISMO HUMANO REGULAÇÃO DA CONCENTRAÇÃO HIDROGENIÓNICA - IMPORTÂNCIA
QBQ 0316 Bioquímica Experimental. Carlos Hotta. Análise de dados (P1 e P2)
 QBQ 0316 Bioquímica Experimental Carlos Hotta Análise de dados (P1 e P2) 26/08/2016 Análise de resultados P2 Passo 1: calcular massa de glicose em cada pocinho 5 µmol glicose 1000 µl 5000 nmol glicose
QBQ 0316 Bioquímica Experimental Carlos Hotta Análise de dados (P1 e P2) 26/08/2016 Análise de resultados P2 Passo 1: calcular massa de glicose em cada pocinho 5 µmol glicose 1000 µl 5000 nmol glicose
AMINOÁCIDOS. - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos;
 1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos. Referência: Stryer ou Lehninger
 Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos Referência: Stryer ou Lehninger Deoxi-hemoglobina Slide - Lehninger 5a edição Estrutura de proteínas
Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos Referência: Stryer ou Lehninger Deoxi-hemoglobina Slide - Lehninger 5a edição Estrutura de proteínas
Doseamento do Fe 2+ por espectroscopia de absorção
 Práticas Laboratoriais de Diagnóstico e Teoria do Restauro I (Ciências da Arte e do Património) Doseamento do Fe 2+ por espectroscopia de absorção Objectivo Determinar a concentração do ferro(ii) numa
Práticas Laboratoriais de Diagnóstico e Teoria do Restauro I (Ciências da Arte e do Património) Doseamento do Fe 2+ por espectroscopia de absorção Objectivo Determinar a concentração do ferro(ii) numa
Lista de Exercícios Aminoácidos e Proteínas
 Universidade do Estado de Santa Catarina Centro de Ciências Tecnológicas CCT Departamento de Química BIO0001 - Bioquímica Lista de Exercícios Aminoácidos e Proteínas 1) Uma solução de 100 ml de glicina
Universidade do Estado de Santa Catarina Centro de Ciências Tecnológicas CCT Departamento de Química BIO0001 - Bioquímica Lista de Exercícios Aminoácidos e Proteínas 1) Uma solução de 100 ml de glicina
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012. Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICOPRÁTICO 5ª AULA TEÓRICOPRÁTICA RESOLUÇÃO
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2011/2012 Unidade Curricular de BIOQUÍMICA I Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICOPRÁTICO 5ª AULA TEÓRICOPRÁTICA RESOLUÇÃO
DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE
 ATIVIDADE EXPERIMENTAL N o 1 DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE Materiais: 01 balão volumétrico
ATIVIDADE EXPERIMENTAL N o 1 DETERMINAÇÃO DO ESPECTRO DE ABSORÇÃO DE SOLUÇÕES AQUOSAS DE PERMANGANATO DE POTÁSSIO, CROMATO DE POTÁSSIO, DICROMATO DE POTÁSSIO E SULFATO DE COBRE Materiais: 01 balão volumétrico
UNIVERSIDADE PRESBITERIANA MACKENZIE
 Unidade Universitária: Centro de Ciências Biológicas e da Saúde Curso: Nutrição Disciplina: Bioquímica DRT: Professor(es): José Alves Rocha Filho 1131860 Carga horária: 4 horas aula (2 teóricas 2 práticas)/semana
Unidade Universitária: Centro de Ciências Biológicas e da Saúde Curso: Nutrição Disciplina: Bioquímica DRT: Professor(es): José Alves Rocha Filho 1131860 Carga horária: 4 horas aula (2 teóricas 2 práticas)/semana
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
ESTRUTURA DAS PROTEÍNAS Como é a estrutura tridimensional das proteínas??? 4 níveis estruturais Estrutura primária, secundária, terciária e quaternária Mantidas por: ligações covalentes (ligação peptídica
PROTEÍNA Deriva do grego proteios (da primeira classe) Berzellius (1838).
 PROTEÍNAS PROTEÍNA Deriva do grego proteios (da primeira classe) Berzellius (1838). As proteínas desempenham um papel fundamental em todos os processos biológicos. São as macromoléculas mais comuns do
PROTEÍNAS PROTEÍNA Deriva do grego proteios (da primeira classe) Berzellius (1838). As proteínas desempenham um papel fundamental em todos os processos biológicos. São as macromoléculas mais comuns do
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA
 Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
Disciplina de BIOQUÍMICA do Ciclo Básico de MEDICINA Universidade dos Açores 1º Ano ENSINO PRÁTICO 4ª AULA PRÁTICA CONCEITO DE SOLUÇÕES TAMPÃO, ph E pk 1. Conceito de soluções tampão (ph e pk) 2. Principais
CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de , DOU de PLANO DE CURSO
 CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de 01.11.12, DOU de 06.11.12 Componente Curricular: Bioquímica II Código: FAR 309 Pré-requisito: BIOQUÍMICA I Período Letivo: 2016.1 Professor: Nádia
CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de 01.11.12, DOU de 06.11.12 Componente Curricular: Bioquímica II Código: FAR 309 Pré-requisito: BIOQUÍMICA I Período Letivo: 2016.1 Professor: Nádia
CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de , DOU de PLANO DE CURSO. Componente Curricular: Bioquímica I
 CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de 01.11.12, DOU de 06.11.12 Componente Curricular: Bioquímica I Código: FAR 305 Pré-requisito: ----- Período Letivo: 2016.1 Professor: Nádia Chiachio
CURSO DE FARMÁCIA Reconhecido pela Portaria MEC nº 220 de 01.11.12, DOU de 06.11.12 Componente Curricular: Bioquímica I Código: FAR 305 Pré-requisito: ----- Período Letivo: 2016.1 Professor: Nádia Chiachio
Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP. Prof. Marcos Túlio Oliveira Depto. Tecnologia
 Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP Prof. Marcos Túlio Oliveira Depto. Tecnologia Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP Green Fluorescent Protein (GFP) Engenharia
Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP Prof. Marcos Túlio Oliveira Depto. Tecnologia Engenharia de Proteínas 2017 Ciências Biológicas FCAV/UNESP Green Fluorescent Protein (GFP) Engenharia
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Todas essas forças são usadas para a manutenção da estrutura tridimensional das proteínas - conformação A conformação de uma proteína é fundamental para a função que ela exerce
ESTRUTURA DAS PROTEÍNAS Todas essas forças são usadas para a manutenção da estrutura tridimensional das proteínas - conformação A conformação de uma proteína é fundamental para a função que ela exerce
DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DAS BILIRRUBINAS (BILIRRUBINÉMIA) BILIRRUBINA. * Catabolismo do Heme e produção de Bilirrubina
 DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DAS BILIRRUBINAS (BILIRRUBINÉMIA) BILIRRUBINA A bilirrubina refere-se à concentração de bilirrubina (Brb) no sangue. A bilirrubina é um produto do catabolismo do
DETERMINAÇÃO DA CONCENTRAÇÃO PLASMÁTICA DAS BILIRRUBINAS (BILIRRUBINÉMIA) BILIRRUBINA A bilirrubina refere-se à concentração de bilirrubina (Brb) no sangue. A bilirrubina é um produto do catabolismo do
Biologia Molecular (Parte I)
 Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
Laboratório de Análise Instrumental
 Laboratório de Análise Instrumental Prof. Renato Camargo Matos Profa. Maria Auxiliadora Costa Matos http://www.ufjf.br/nupis DIA/MÊS ASSUNTO 06/03 Apresentação do curso 13/03 PRÁTICA 1: Determinação de
Laboratório de Análise Instrumental Prof. Renato Camargo Matos Profa. Maria Auxiliadora Costa Matos http://www.ufjf.br/nupis DIA/MÊS ASSUNTO 06/03 Apresentação do curso 13/03 PRÁTICA 1: Determinação de
Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Doseamento de Uréia, Creatinina, AST e ALT. Professor: Dr.
 Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Doseamento de Uréia, Creatinina, AST e ALT. Professor: Dr. Fernando Ananias NOME: RGM: ATIVIDADE PRÁTICA 2 1) DETERMINAÇÃO DE URÉIA E CREATININA
Curso: FARMÁCIA Disciplina: Bioquímica Clínica Título da Aula: Doseamento de Uréia, Creatinina, AST e ALT. Professor: Dr. Fernando Ananias NOME: RGM: ATIVIDADE PRÁTICA 2 1) DETERMINAÇÃO DE URÉIA E CREATININA
Farmacodinamia. Estudo dos mecanismos de acção e efeitos dos fármacos
 Sumário Farmacodinamia. Conceito de receptor. Afinidade e eficácia; constantes de afinidade. Tipos e subtipos de receptores. Mecanismos transductores / efectores; família da proteína G, receptores ligados
Sumário Farmacodinamia. Conceito de receptor. Afinidade e eficácia; constantes de afinidade. Tipos e subtipos de receptores. Mecanismos transductores / efectores; família da proteína G, receptores ligados
Profº Lásaro Henrique
 Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
Profº Lásaro Henrique Proteínas são macromoléculas complexas, compostas de aminoácidos. São os constituintes básicos da vida e necessárias para os processos químicos que ocorrem nos organismos vivos. Nos
REVISÃO: ENADE BIOQUÍMICA - 1
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
MACRONUTRIENTES III PROTEÍNAS
 MACRONUTRIENTES III PROTEÍNAS 1 PROTEÍNAS As proteínas são compostos orgânicos de estrutura complexa e massa molecular elevada, elas são sintetizadas pelos organismos vivos através da condensação de um
MACRONUTRIENTES III PROTEÍNAS 1 PROTEÍNAS As proteínas são compostos orgânicos de estrutura complexa e massa molecular elevada, elas são sintetizadas pelos organismos vivos através da condensação de um
PROTEÍNAS Professores: Manoela e Marco Aurélio 2017
 PROTEÍNAS Professores: Manoela e Marco Aurélio 2017 Bioquímica Celular Elementos químicos da matéria viva Principais substâncias presentes na matéria viva Proteínas - Nutriente construtor (função plástica)
PROTEÍNAS Professores: Manoela e Marco Aurélio 2017 Bioquímica Celular Elementos químicos da matéria viva Principais substâncias presentes na matéria viva Proteínas - Nutriente construtor (função plástica)
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA. Aminoácidos. Prof. Willame Bezerra
 CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
UNIVERSIDADE FEDERAL DO VALE DO SÃO FRANCISCO PROGRAMA DE DISCIPLINA
 PROGRAMA DE DISCIPLINA NOME COLEGIADO CÓDIGO SEMESTRE ENGENHARIA AGRO0010 DRAULIO COSTA DA SILVA AGRONÔMICA 2016.1 CARGA HORÁRIA TEÓR: 30h PRÁT: 30h HORÁRIOS: Seg 08-10h / Ter 14-16 -18h CURSOS ATENDIDOS
PROGRAMA DE DISCIPLINA NOME COLEGIADO CÓDIGO SEMESTRE ENGENHARIA AGRO0010 DRAULIO COSTA DA SILVA AGRONÔMICA 2016.1 CARGA HORÁRIA TEÓR: 30h PRÁT: 30h HORÁRIOS: Seg 08-10h / Ter 14-16 -18h CURSOS ATENDIDOS
ESTUDO DA ESTABILIDADE E PROPRIEDADES DE COMPOSTOS DE COORDENAÇÃO
 versão Fev 2007 TRABALHO 2 ESTUDO DA ESTABILIDADE E PROPRIEDADES DE COMPOSTOS DE COORDENAÇÃO 1. OBJECTIVOS 1) Determinação da estequiometria e do coeficiente de extinção molar do complexo [Ni- EDTA] 2-
versão Fev 2007 TRABALHO 2 ESTUDO DA ESTABILIDADE E PROPRIEDADES DE COMPOSTOS DE COORDENAÇÃO 1. OBJECTIVOS 1) Determinação da estequiometria e do coeficiente de extinção molar do complexo [Ni- EDTA] 2-
Introdução. radiação ultravioleta SUBSTÂNCIA radiação fluorescente e visível excitação após a desativação λ i
 Introdução Substância fluorescente: radiação ultravioleta SUBSTÂNCIA radiação fluorescente e visível excitação após a desativação λ i λ f UV Violeta Azul Verde Amarelo Alaranjado Vermelho IV < 380 400
Introdução Substância fluorescente: radiação ultravioleta SUBSTÂNCIA radiação fluorescente e visível excitação após a desativação λ i λ f UV Violeta Azul Verde Amarelo Alaranjado Vermelho IV < 380 400
b
 a 1 2 3 4 5 8 6 7 b c d e 1 2 C B A Todos os seres vivos e as suas células são constituídos por moléculas orgânicas de grandes dimensões, as MACROMOLÉCULAS. O H As biomoléculas desempenham várias funções:
a 1 2 3 4 5 8 6 7 b c d e 1 2 C B A Todos os seres vivos e as suas células são constituídos por moléculas orgânicas de grandes dimensões, as MACROMOLÉCULAS. O H As biomoléculas desempenham várias funções:
Manutenção do ph do sangue
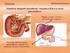 Manutenção do ph do sangue Muitos dos fluidos biológicos, quer no interior, quer no exterior das células, apresentam intervalos de ph muito apertados, ou seja um valor de ph praticamente constante, uma
Manutenção do ph do sangue Muitos dos fluidos biológicos, quer no interior, quer no exterior das células, apresentam intervalos de ph muito apertados, ou seja um valor de ph praticamente constante, uma
Colheita e manuseamento de fluidos biológicos
 Colheita e manuseamento de fluidos biológicos Na aula de hoje, vamos falar de: 1. Importância da análise de amostras biológicas como ferramentas de diagnóstico 2. Composição dos dois fluidos mais analisados:
Colheita e manuseamento de fluidos biológicos Na aula de hoje, vamos falar de: 1. Importância da análise de amostras biológicas como ferramentas de diagnóstico 2. Composição dos dois fluidos mais analisados:
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011. Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano
 Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 4ª AULA PRÁTICA Determinação
Faculdade de Medicina da Universidade de Coimbra Ano Lectivo 2010/2011 Unidade Curricular de BIOQUÍMICA II Mestrado Integrado em MEDICINA 1º Ano ENSINO PRÁTICO E TEORICO-PRÁTICO 4ª AULA PRÁTICA Determinação
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs
 Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
13/08/2018. Escala de ph. Escala de ph. Crescimento básico. Crescimento ácido. Neutro. básico
 Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Problemas sobre o doseamento da actividade de enzimas
 Problemas sobre o doseamento da actividade de enzimas Perg. 1: Uma enzima E catalisa a transformação A P. Num tubo de ensaio colocou-se A, tampão e ao minuto zero adicionou-se uma determinada quantidade
Problemas sobre o doseamento da actividade de enzimas Perg. 1: Uma enzima E catalisa a transformação A P. Num tubo de ensaio colocou-se A, tampão e ao minuto zero adicionou-se uma determinada quantidade
UFSC. Química (Amarela) Resposta: = 05
 Resposta: 01 + 04 = 05 01. Correto. Apresenta carboxila e grupamento amino no carbono alfa. 02. Incorreto. Com a elevação do ph ocorre a desprotonação da carboxila formando carga negativa. 04. Correto.
Resposta: 01 + 04 = 05 01. Correto. Apresenta carboxila e grupamento amino no carbono alfa. 02. Incorreto. Com a elevação do ph ocorre a desprotonação da carboxila formando carga negativa. 04. Correto.
Departamento de Bioquímica. Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N. Professores. Carlos Takeshi Hotta
 Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2013 Professores Carlos Takeshi Hotta Guilherme Menegon Arantes 1 1. O ácido dinitrosalicílico (DNS) pode
Departamento de Bioquímica Instituto de Química USP EXERCÍCIOS BIOQUÍMICA EXPERIMENTAL QBQ 0316N 2013 Professores Carlos Takeshi Hotta Guilherme Menegon Arantes 1 1. O ácido dinitrosalicílico (DNS) pode
Trabalho realizado por: Ariana Gonçalves nº Ricardo Figueiredo nº
 Trabalho realizado por: Ariana Gonçalves nº. 57301 Ricardo Figueiredo nº. 57284 Composição: Lípidos (anfipáticos); Proteínas; Glícidos: Sob a forma de glicolípidos e glicoproteínas. (em proporções variáveis)
Trabalho realizado por: Ariana Gonçalves nº. 57301 Ricardo Figueiredo nº. 57284 Composição: Lípidos (anfipáticos); Proteínas; Glícidos: Sob a forma de glicolípidos e glicoproteínas. (em proporções variáveis)
