Profª Eleonora Slide de aula
|
|
|
- Adriana Nathalia Gil Fontes
- 7 Há anos
- Visualizações:
Transcrição
1 Aminoácidos e Peptídeos Profª Eleonora Slide de aula
2 Aminoácidos Estrutura Geral Ácido carboxílico com amina primária (N 2 ) no carbono α. Isomeria Ao carbono α estão ligados 4 grupos substituintes diferentes: grupo carboxila, grupo amino, grupo R (ou cadeia lateral) e um átomo de hidrogênio. carbono α é um carbono assimétrico om exceção da glicina (R=) todos os demais aminoácidos são oticamente ativos. s estereoisômeros são designados por D e L. Na natureza os aminoácidos são encontrados na forma L. lassificação dos aminoácidos Polaridade do grupo R Grupamento funcional do grupo R Essencial + Exceção: 3 N α Prolina: amina secundária (N) R
3 Quanto à polaridade do grupo R Grupo R não polar: aqueles onde R é um hidrocarboneto alifático ou aromático. glicina (Gly ou G) metionina (Met ou M) alanina (Ala ou A) fenilalanina (Phe ou F) valina (Val ou V) prolina (Pro ou P) leucina (Leu ou L) triptofano (Trp ou W) isoleucina (Ile ou I) Grupo R polar não carregado: aqueles onde R apresenta grupamento polar não dissociado em p fisiológico (p = 7,0). serina (Ser ou S) asparagina (Asn ou N) treonina (Thr ou T) glutamina (Gln ou Q) cisteína (ys ou ) tirosina (Tyr ou Y) Grupo R carregado positivamente: aqueles onde R apresenta carga positiva em p fisiológico (p = 7,0). histidina (is ou ) lisina (Lys ou K) arginina (Arg ou R) Grupo R carregado negativamente: aqueles onde R apresenta carga negativa em p fisiológico (p = 7,0). ácido aspártico (Asp ou D) ácido glutâmico (Glu ou E)
4 Quanto à natureza do grupamento R Alifático: Gly, Ala, Val, Leu, Ile Aromático: Phe, Trp, Tyr Sulfonado: ys, Met Básico: Lys, Arg, is idroxilado: Ser, Thr Dicarboxílico: Asp, Glu Amida de ácido dicarboxílico: Asn, Glu Amina secundária: Pro Essenciais São aqueles que não podem ser sintetizados pelo organismo, devendo ser administrados préformados na dieta. ada espécie tem seus aminoácidos essenciais. Espécie humana: Arg, Phe, is, Ile, Leu, Lys, Met, Trp, Val
5 Estrutura dos Aminoácidos Grupo R não polar, alifático ou aromático 3 N N 3 3 N N N Glicina Alanina Valina 3 3 Leucina 3 Isoleucina 3 N S 3 N N N + 2 N 3 Metionina Fenilalanina Prolina Triptofano
6 Aminoácidos com cadeias laterais apolares Estes aminoácidos possuem cadeia lateral que não apresenta a capacidade de receber ou doar elétrons, de participar de ligações iônicas ou de formar pontes de hidrogênio. Entretanto, podem promover interações hidrofóbicas (*). (*) Associação de grupos não polares, tais como cadeias de hidrocarbonetos, em meio aquoso. Em sistemas vivos, estas interações contribuem para a estabilidade das moléculas de proteínas, das membranas e de várias outras estruturas subcelulares. s valores de pk dos grupos αcarboxila (pk 1 2,3) e αamino (pk 2 9,6) são semelhantes para todos os aminoácidos deste grupo. A cadeia lateral da prolina e o seu grupo αamino formam um anel, de forma que, este aminoácido difere dos demais pelo fato de conter um grupo imino ao invés de um grupo amino. A glicina (cadeia lateral = ) é o único aminoácido que não possui carbono assimétrico.
7 Grupo R polar, não carregado 3 N + 3 N + 3 N S Serina Treonina isteína 3 N N N N 2 N 2 Asparagina Glutamina Tirosina
8 Aminoácidos com cadeias laterais polares (desprovidos de carga elétrica) Estes aminoácidos apresentam carga líquida igual à zero em p neutro, embora as cadeias laterais de cisteína e tirosina possam perder um próton em p alcalino. s aminoácidos serina, treonina e tirosina contêm grupos hidroxila que podem participar da formação de pontes de hidrogênio (*). (*) Resultam da atração eletrostática entre um átomo eletronegativo (normalmente ou N) e um átomo de hidrogênio ligado covalentemente a um segundo átomo eletronegativo. átomo de hidrogênio, desta forma, é compartilhado entre dois átomos eletronegativo. As cadeias laterais da asparagina e da glutamina contem, cada uma, um grupo carbonila e um grupo amida que podem participar também de pontes de hidrogênio. A cadeia lateral da cisteína contém um grupamento sulfidrila (S). Nas proteínas os grupos sulfidrilas de duas cisteínas podem se tornar oxidados e formar um dímero cistina que contém uma ligação denominada ponte dissulfeto (*). (*) A ponte dissulfeto (SS) é uma ligação covalente formada pelos grupos sulfidrila (S) de dois resíduos de cisteína para produzir um resíduo de cistina.
9 3 N + 3 N + 3 N + Grupo R carregado positivamente N 3 Lisina N N 2 + N 2 Arginina 2 N N + istidina + 3 N 3 N + Grupo R carregado negativamente 2 Ácido Aspártico 2 2 Ácido Glutâmico
10 Aminoácidos com cadeias laterais básicas As cadeias laterais dos aminoácidos básicos são aceptoras de prótons. Em p fisiológico, as cadeias laterais da lisina e da arginina se encontram completamente ionizadas, com carga positiva. Já a histidina é fracamente básica e o aminoácido livre, em geral, não apresenta carga elétrica em p fisiológico. Entretanto quando a histidina se encontra incorporada em uma proteína, a sua cadeia lateral pode se apresentar com carga positiva ou neutra, dependendo do ambiente iônico fornecido pela cadeia polipeptídica da proteína. Aminoácidos com cadeias laterais ácidas s aminoácidos ácido aspártico e ácido glutâmico são doadores de prótons. Em p neutro, as cadeias laterais desses aminoácidos se encontram completamente ionizadas, contendo um grupo carboxilato carregado negativamente ( ). Esses aminoácidos são, portanto, denominados aspartato e glutamato, para enfatizar o fato de estarem carregados negativamente em p fisiológico.
11 Estrutura e classificação dos aminoácidos Profª Eleonora Slide de aula
12 Grupos ionizáveis arga elétrica dos aminoácidos varia com o p forma protonada: e N 3 + forma desprotonada: e N 2 Profª Eleonora Slide de aula 3 + N 3 + N 2 N R R R (a) (c) (b) (a) em soluções muito ácidas os dois grupos se apresentam protonados (b) em soluções muito alcalinas os dois grupos se apresentam desprotonados (c) em soluções neutras os aminoácidos se apresentam como um íon dipolar A conversão entre as formas a, b e c em função do p do meio pode ser evidenciada através da curva de titulação do aminoácido.
13 urva de Titulação da Alanina urva de titulação de aminoácido p 14 Etapa 1: titulação do grupo Etapa 2: titulação do grupo N 3 + (a) + N 3 R 3+ N pk 2 = 9,69 e (b) + N 3 R + N R 3 Alanina (em meio ácido) 8 d (c) + N 3 R 6 4 pk 1 = 2,34 c pi = 6,02 (forma dipolar isoelétrica) (d) + N 3 R N 2 R álculo do ponto isoelétrico 2 a b (e) N 2 R pi = p = pk 1 + pk 2 2 0,5 1,0 1,5 2,0 Equivalentes de Na adicionados pi = p = 2,34 + 9,69 = 6,02 2 Ponto isoelétrico é o p da solução para o qual a carga absoluta do aminoácido é nula. No ponto isoelétrico não há migração, em meio elétrico, nem para o eletrodo positivo (ânodo), nem para o eletrodo negativo (cátodo).
14 Aminoácido Abreviação pk 1 () pk 2 (N 3+ ) pk 3 (Grupo R) pi Valores de pk dos grupos ionizáveis de aminoácidos Grupo R não polar, alifático Glicina Alanina Valina Leucina Isoleucina Prolina Gly Ala Val Leu Ile Pro 2,34 2,34 2,32 2,36 2,36 1,99 9,60 9,69 9,62 9,60 9,68 10,96 5,97 6,01 5,97 5,98 6,02 6,48 Grupo R aromático Fenilalanina Tirosina Triptofano Phe Tyr Trp 1,83 2,20 2,38 9,13 9,11 9,39 10,07 5,48 5,66 5,89 Grupo R polar, não carregado Serina Treonina isteína Metionina Ser Thr ys Met 2,21 2,11 1,96 2,28 9,15 9,62 8,18 9,21 13,60 13,60 10,28 5,68 5,87 5,07 5,74 Asparagina Asn 2,02 8,80 5,41 Glutamina Grupo R carregado negativamente Ácido aspártico Gln Asp 2,17 1,88 9,13 9,60 3,65 5,65 2,77 Ácido glutâmico Grupo R carregado positivamente Lisina Arginina istidina Glu Lys Arg is 2,19 2,18 2,17 1,82 9,67 8,95 9,04 9,17 4,25 10,53 12,48 6,0 3,22 9,74 10,76 7,59
15 Reações químicas dos aminoácidos Reações comuns da química orgânica relativa aos grupos e N 2 Grupamento carboxila Esterificação por álcoois R + R' R R' + 2 N 2 N 2 Utilizada no isolamento de aminoácidos Formação de amidas R + R' N 2 R N R' + 2 N 2 N 2 Ligação peptídica
16 Grupamento amino Resistente à hidrólise Pode ser removido por oxidação. Agentes oxidantes: 2 2, KMn 4, etc. Grupo R Reações decorrentes da reatividade do grupo R. Assim, a cisteína apresenta reações característica do grupamento sulfidrila (S), a tirosina as do grupamento fenólico, etc. As reações químicas dos aminoácidos são utilizadas para: Identificação e análise de aminoácidos Identificação e sequenciamento de aminoácidos em proteínas Identificação de resíduos específicos necessários para a atividade biológica de proteínas nativas Modificações químicas de resíduos de aminoácidos capazes de alterar a atividade biológica da proteína Síntese química de peptídeos
17 Reações químicas características de aminoácidos Duas reações são amplamente utilizadas para a detecção, medida e identificação de aminoácidos Reação da ninidrina Resulta na desaminação oxidativa de αaminoácidos produzindo 2 ; N 3 ; um aldeído com um carbono a menos e a ninidrina reduzida. A ninidrina reduzida ou hidridantina reage com o N 3 e com outra molécula de ninidrina formando um complexo arroxeado (λ = 570 nm) ninidrina + R N 2 aminoácido 2 + R N 3 = N _ hidridantina ninidrina bservação Nos aminoácidos com grupo amina secundária, como é o caso da prolina, o produto da reação é diferente e origina uma cor amarela (λ = 440 nm). Neste caso não há a liberação de N 3, porém, há a produção de teores quantitativos de 2. complexo arroxeado
18 Reação com 1flúor2,4dinitrobenzeno (FDNB) Em solução levemente alcalina, o FDNB reage com os αaminoácidos para produzir derivado do 2,4dinitrofenil de cor amarela. N 2 + N 2 F FDNB R N 2 α aminoácido F N 2 N 2 N R 2,4dinitrofenilaminoácido
19 Ligação peptídica (ou ligação amida) Profª Eleonora Slide de aula R 1 R 2 2 R 1 R 2 2 N α + N α 2 N α N α ligação p ep tídica α N α s carbonos α de dois aminoácidos adjacentes e os átomos dos grupamentos que participam da ligação peptídica a unidade peptídica estão todos em um mesmo plano. polímero formado pelo encadeamento de aminoácidos é constituído por unidades planares unidades peptídicas unidas entre si por uma articulação flexível o carbono α. s oligômeros de aminoácidos são denominados peptídeos 2 resíduos de aminoácidos: dipeptídeo 3 resíduos de aminoácidos: tripeptídeo 4 resíduos de aminoácidos: tetrapeptídeo, etc. adeia polipeptídica ou cadeia peptídica é uma seqüência de mais de dois resíduos de aminoácidos. A seqüência dos aminoácidos na cadeia peptídica é denominada de estrutura primária.
20 Peptídeo a) s quatro átomos dos grupamentos envolvidos na ligação peptídica (em vermelho) se dispõem em um plano. A unidade peptídica está representada por um retângulo. b) As unidades peptídicas podem se movimentar umas em relação às outras. É possível uma rotação (indicada pelas setas) em torno das ligações com o carbono α. c) A cadeia polipeptídica consiste em um arranjo flexível de unidades planas, as unidades peptídicas, conectadas por uma articulação, o carbono α. As cadeias laterais dos aminoácidos estão representadas.
21 Ligação peptídica (ou ligação amida) 4 resíduos de aminoácidos: tetrapeptídeo
22 que diferencia um peptídeo de uma proteína? Muitos autores se baseiam na dimensão da estrutura, em termos do número de resíduos de aminoácidos. Por exemplo: n < 80 a 100 aminoácidos cadeia peptídica n > 80 a 100 aminoácidos cadeia protéica Entretanto a distinção entre peptídeo e proteína deve se basear nas respectivas funções biológicas. Nomenclatura de peptídeos As cadeias peptídicas são nomeadas da extremidade amino terminal (ou Nterminal) para a extremidade carboxila terminal (ou terminal). Não há possibilidade de ionização do grupamento que terminal faz parte da ligação peptídica N terminal 3 + N N N N N N GLU LYS GLISERTR (Glutamil lisil glicil seril treonina) s grupos amina e carboxila terminais e os grupos ionizáveis das cadeias laterais (grupos R) são os responsáveis pelas propriedades ácidobásicas dos peptídeos.
23 idrólise das ligações peptídicas idrólise total: por fervura com ácido ou base forte ocorre a hidrólise de todas as ligações peptídicas. idrólise seletiva: por certas enzimas proteolíticas. A hidrólise ocorre nas ligações peptídicas de aminoácidos específicos. Enzimas proteolíticas Tripsina hidrolisa apenas as ligações peptídicas cujo grupo carboxila pertence a um resíduo de lisina ou arginina. Quimotripsina hidrolisa apenas ligações peptídicas cujo grupo carboxila pertence a um resíduo de fenilalanina, triptofano ou tirosina. Pepsina hidrolisa apenas as ligações peptídicas cujo grupo amino pertence a um resíduo de fenilalanina, triptofano, tirosina. Termolisina hidrolisa apenas as ligações peptídicas cujo grupo amino pertence a um resíduo de leucina, isoleucina ou valina.
24 Método químico seletivo Brometo de cianogênio hidrolisa apenas ligações peptídicas cujo grupo carboxila pertence a um resíduo de metionina. Exemplo de peptídeo hidrolisado por diferentes proteases Tyr Lys Glu Met Leu Gly Arg Ala Gly Tripsina (3 fragmentos) Tyr Lys // Glu Met Leu Gly Arg // Ala Gly Quimotripsina (2 fragmentos) Tyr // Lys Glu Met Leu Gly Arg Ala Gly Termolisina (2 fragmentos) Tyr Lys Glu Met // Leu Gly Arg Ala Gly
25 Determinação da seqüência de aminoácidos nos fragmentos de peptídeos Reação com fenilisotiocianato (Reagente de Edman) Método de degradação de Edman, conduzido em meio levemente alcalino, marca e remova o resíduo Nterminal de peptídeos, deixando intactas as outras ligações peptídicas. Após a remoção e identificação, por cromatografia, do resíduo Nterminal, o novo resíduo Nterminal exposto pode ser marcado e removido pela repetição da mesma reação.
26 onfiguração Arranjo tridimensional das cadeias polipeptídicas Profª Eleonora Slide de aula Arranjo espacial de uma molécula orgânica que é conferido pela presença de: Dupla ligação: ao redor das quais não há liberdade de rotação, o que determina as configurações cistrans. = Ácido fumárico (trans) = Ácido maléico (cis) entro quiral: ao redor do qual os grupos substituídos estão arranjados em uma seqüência determinada (configuração L ou D) 2 N N 2 3 L alanina 3 D alanina Para passar de uma configuração para a outra é necessário que ocorra um rompimento de ligação.
27 onformação Arranjo espacial de grupos substituídos em moléculas orgânicas que podem assumir várias posições espaciais, sem o rompimento de ligações devido à liberdade de rotação ao redor de ligações simples carbonocarbono. Exemplo: etano Forma escalonada Forma eclipsada
AMINOÁCIDOS E PROTEÍNAS
 AMINOÁCIDOS E PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição
AMINOÁCIDOS E PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição
STRYER, L.; TYMOCZKO, J.L.; BERG, J.M.
 2 Proteínas: STRYER, L.; TYMOCZKO, J.L.; BERG, J.M. Bioquímica. 6 ed. Rio de Janeiro: Guanabara Koogan, 2008. Capítulo 2 e 3; as edições 4 e 5 também podem ser utilizadas (Cap. 3 e 4). 2.1 Aminoácidos
2 Proteínas: STRYER, L.; TYMOCZKO, J.L.; BERG, J.M. Bioquímica. 6 ed. Rio de Janeiro: Guanabara Koogan, 2008. Capítulo 2 e 3; as edições 4 e 5 também podem ser utilizadas (Cap. 3 e 4). 2.1 Aminoácidos
13/08/2018. Escala de ph. Escala de ph. Crescimento básico. Crescimento ácido. Neutro. básico
 Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Aminoácidos peptídeos e proteínas
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Aminoácidos não-essenciais: alanina, ácido aspártico, ácido glutâmico, cisteína, glicina, glutamina, hidroxiprolina, prolina, serina e tirosina.
 AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA. Aminoácidos. Prof. Willame Bezerra
 CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
Aminoácidos. Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP.
 Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aula 1. Referência. Bancos de Dados. Linguagem x Informação. Introdução a Bioquímica: Biomoléculas. Introdução ao Curso: Aminoácidos.
 Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
Aula 3: Estrutura de Proteínas. Bioquímica para Odonto - Bloco I Profa. Lucia Bianconi. Funções das Proteínas. Catalisadores (enzimas)
 Aula 3: Estrutura de Proteínas Bioquímica para Odonto - Bloco I Profa. Lucia Bianconi Funções das Proteínas Catalisadores (enzimas) Transportadoras (Oxigênio, Ferro, Vitaminas, fármacos) Armazenamento
Aula 3: Estrutura de Proteínas Bioquímica para Odonto - Bloco I Profa. Lucia Bianconi Funções das Proteínas Catalisadores (enzimas) Transportadoras (Oxigênio, Ferro, Vitaminas, fármacos) Armazenamento
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
Aminoácidos e Peptídeos. Profa. Alana Cecília
 Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
Aminoácidos FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
AMINOÁCIDOS. Dra. Flávia Cristina Goulart. Bioquímica
 AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
RMN em proteínas pequenas
 COSY COrrelated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) mais simples Primeiro experimento 2D proposto (Jeener, 1971) Período de mistura: 1 único pulso de 90 Transferência da coerência entre
COSY COrrelated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) mais simples Primeiro experimento 2D proposto (Jeener, 1971) Período de mistura: 1 único pulso de 90 Transferência da coerência entre
Estas aminas são bases de Lewis já que sobram elétrons no átomo de nitrogênio e como tal podem reagir com ácidos.
 01. Os compostos mostrados são respectivamente amina primária, amina secundária e amina terciária. O composto III, por não apresentar ligações (pontes) de hidrogênio, é o menos solúvel em água, tornando
01. Os compostos mostrados são respectivamente amina primária, amina secundária e amina terciária. O composto III, por não apresentar ligações (pontes) de hidrogênio, é o menos solúvel em água, tornando
Rafael Mesquita. Aminoácidos
 Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
BÁSICA EM IMAGENS. Aminoácidos, peptídeos e proteínas
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila
 Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
Proteínas. Dra. Flávia Cristina Goulart. Bioquímica
 Proteínas Dra. Flávia Cristina Goulart Bioquímica Os aa. e as proteínas Nos animais, as proteínas correspondem à cerca de 80% do peso dos músculos desidratados, cerca de 70% da pele e 90% do sangue seco.
Proteínas Dra. Flávia Cristina Goulart Bioquímica Os aa. e as proteínas Nos animais, as proteínas correspondem à cerca de 80% do peso dos músculos desidratados, cerca de 70% da pele e 90% do sangue seco.
Aminoácidos. Bioquímica Prof. Dr. Marcelo Soares
 Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
 Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
REVISÃO: ENADE BIOQUÍMICA - 1
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs
 Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
13/03/2016. Profª. Drª. Andréa Fontes Garcia E -mail:
 Profª. Drª. Andréa Fontes Garcia E -mail: andrea@salesiano-ata.br 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
Profª. Drª. Andréa Fontes Garcia E -mail: andrea@salesiano-ata.br 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
- Apresentam uma fórmula básica: um átomo central de carbono onde se ligam:
 1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
Aula 8 Síntese de proteínas
 Aula 8 Síntese de proteínas As proteínas que podem ser enzimas, hormônios, pigmentos, anticorpos, realizam atividades específicas no metabolismo dos seres vivos. São produzidas sob o comando do DNA. Observe
Aula 8 Síntese de proteínas As proteínas que podem ser enzimas, hormônios, pigmentos, anticorpos, realizam atividades específicas no metabolismo dos seres vivos. São produzidas sob o comando do DNA. Observe
14/02/2017. Genética. Professora Catarina
 14/02/2017 Genética Professora Catarina 1 A espécie humana Ácidos nucleicos Tipos DNA ácido desoxirribonucleico RNA ácido ribonucleico São formados pela união de nucleotídeos. 2 Composição dos nucleotídeos
14/02/2017 Genética Professora Catarina 1 A espécie humana Ácidos nucleicos Tipos DNA ácido desoxirribonucleico RNA ácido ribonucleico São formados pela união de nucleotídeos. 2 Composição dos nucleotídeos
1164 BIOLOGIA ESTRUTURAL Aula 1 Prof. Dr. Valmir Fadel
 H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
Programa de Pós-Graduação em Química
 1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
Graduação em Biotecnologia Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia Aminoácidos Grupos funcionais em bioquímica Propriedades químicas da água Estrutura e
Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia Aminoácidos Grupos funcionais em bioquímica Propriedades químicas da água Estrutura e
LIGAÇÕES QUÍMICAS REVIS I ÃO
 LIGAÇÕES QUÍMICAS REVISÃO Ligações químicas e forças atrativas 1-Ligações covalentes Ligação química entre dois átomos na qual elétrons são compartilhados Ligação Forte Energia de ligação é a energia necessária
LIGAÇÕES QUÍMICAS REVISÃO Ligações químicas e forças atrativas 1-Ligações covalentes Ligação química entre dois átomos na qual elétrons são compartilhados Ligação Forte Energia de ligação é a energia necessária
SÍNTESE DOS AMINOÁCIDOS. Prof. Henning Ulrich
 SÍNTESE DOS AMINOÁCIDOS Prof. Henning Ulrich CATABOLISMO DOS AMINOÁCIDOS EM MAMÍFEROS TRANSAMINAÇÕES CATALISADAS POR ENZIMAS Em muitas reações das aminotransferases, o -cetoglutarato é o receptor do grupo
SÍNTESE DOS AMINOÁCIDOS Prof. Henning Ulrich CATABOLISMO DOS AMINOÁCIDOS EM MAMÍFEROS TRANSAMINAÇÕES CATALISADAS POR ENZIMAS Em muitas reações das aminotransferases, o -cetoglutarato é o receptor do grupo
1. INTRODUÇÃO. Polímeros biológicos. Polissacarídeos Proteínas Ácidos Nucléicos. Reservas de energia. Armazenamento e Transmissão de informações
 AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
Estrutura e Função de Proteínas
 Estrutura e Função de Proteínas As Proteínas As proteínas observadas na natureza evoluíram pela pressão selectiva para efetuar funções específicas. As propriedades funcionais das proteínas dependem da
Estrutura e Função de Proteínas As Proteínas As proteínas observadas na natureza evoluíram pela pressão selectiva para efetuar funções específicas. As propriedades funcionais das proteínas dependem da
Química Orgânica. Química Orgânica. Química Orgânica. Aula 2 Acidez e Basicidade. Prof. Davyson Moreira
 Aula 2 Acidez e Basicidade Prof. Davyson Moreira (davysonmoreira@hotmail.com) 1 Primeira definição de importância. Define ácido como substâncias doadoras de prótons e bases substâncias doadoras de -OH
Aula 2 Acidez e Basicidade Prof. Davyson Moreira (davysonmoreira@hotmail.com) 1 Primeira definição de importância. Define ácido como substâncias doadoras de prótons e bases substâncias doadoras de -OH
CONCEITOS DE BRÖNSTED-LOWRY CONCEITOS DE ÁCIDOS E BASES CONCEITOS DE ARRHENIUS. Ácido: Ácido: HCN + H O H O + - Base ou hidróxido: Base: + +
 Ácido: CONCEITOS DE ÁCIDOS E BASES CONCEITOS DE ARRENIUS Toda substância que em solução aquosa, sofre ionização, produzindo como cátion, apenas o íon CN O ( aq ) CN ( aq ) Na realidade, o íon, quando em
Ácido: CONCEITOS DE ÁCIDOS E BASES CONCEITOS DE ARRENIUS Toda substância que em solução aquosa, sofre ionização, produzindo como cátion, apenas o íon CN O ( aq ) CN ( aq ) Na realidade, o íon, quando em
Proteínas e aminoácidos
 Proteínas e aminoácidos Digestão Absorção Metabolismo Disciplina de Bioquímica Profa. Dra. Celene Fernandes Bernardes Proteínas da dieta Proteínas endógenas Proteínas endógenas Síntese de aminoácidos não
Proteínas e aminoácidos Digestão Absorção Metabolismo Disciplina de Bioquímica Profa. Dra. Celene Fernandes Bernardes Proteínas da dieta Proteínas endógenas Proteínas endógenas Síntese de aminoácidos não
Proteínas. As proteínas são o centro da acção em todos os processos biológicos. Voet & Voet Biochemistry
 Proteínas As proteínas são o centro da acção em todos os processos biológicos. Voet & Voet Biochemistry As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (~50% do peso sêco)
Proteínas As proteínas são o centro da acção em todos os processos biológicos. Voet & Voet Biochemistry As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (~50% do peso sêco)
Aminoácidos. subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes
 . Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
. Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
Dra. Kátia R. P. de Araújo Sgrillo. sgrillo.ita@ftc.br
 Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br como os demais compostos constituintes de um organismo não são permanentes, estando em contínua DEGRADAÇÃO e SÍNTESE. Proteína Meia-vida Estima-se
Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br como os demais compostos constituintes de um organismo não são permanentes, estando em contínua DEGRADAÇÃO e SÍNTESE. Proteína Meia-vida Estima-se
Introdução. Estrutura dos Aminoácidos e Proteínas. Aminoácidos componentes de proteínas. Aminoácidos componentes de proteínas 10/02/2012.
 Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Profª Eleonora Slide de aula. Metabolismo dos Aminoácidos
 Metabolismo dos Aminoácidos Metabolismo dos Aminoácidos Além de constituintes das proteínas, os aminoácidos são também os precursores de outros compostos nitrogenados, aos quais podem fornecer não só o
Metabolismo dos Aminoácidos Metabolismo dos Aminoácidos Além de constituintes das proteínas, os aminoácidos são também os precursores de outros compostos nitrogenados, aos quais podem fornecer não só o
Aminoácidos. Estrutura e Função das Proteínas UNIDADE I I. VISÃO GERAL II. ESTRUTURA DOS AMINOÁCIDOS COOH C H R
 UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
Proteína INTRODUÇÃO 1
 Proteína INTRODUÇÃO 1 DEFINIÇÃO Compostos Orgânicos (amina e carboxila) Massa (peso) molecular entre 5.000 e 1.000.000 Compostos por cadeias peptídicas Aminoácidos. 2 IMPORTÂNCIA Componentes fundamentais
Proteína INTRODUÇÃO 1 DEFINIÇÃO Compostos Orgânicos (amina e carboxila) Massa (peso) molecular entre 5.000 e 1.000.000 Compostos por cadeias peptídicas Aminoácidos. 2 IMPORTÂNCIA Componentes fundamentais
Aminoácidos e peptídeos. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
www.professormazzei.com - FUNÇÕES NITROGENADAS Folha 01 João Roberto Mazzei
 01. (UEL 2009) O chocolate estimula a produção do hormônio 2-feniletilamina, percursor da serotonina, um neurotransmissor que causa a sensação de bem-estar. Considere as afirmativas. I. A substância 2-feniletilamina
01. (UEL 2009) O chocolate estimula a produção do hormônio 2-feniletilamina, percursor da serotonina, um neurotransmissor que causa a sensação de bem-estar. Considere as afirmativas. I. A substância 2-feniletilamina
AMINOÁCIDOS.! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico NH2 I R - C - C = 0O I I H OH
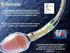 Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
Profª Eleonora Slide de aula. aminoácidos de cadeias polipeptídicas
 Determinação da seqüência de aminoácidos de cadeias polipeptídicas Determinação da seqüência de aminoácidos de cadeias polipeptídicas 1ª Etapa: Determinação da composição em aminoácidos Hidrólise de todas
Determinação da seqüência de aminoácidos de cadeias polipeptídicas Determinação da seqüência de aminoácidos de cadeias polipeptídicas 1ª Etapa: Determinação da composição em aminoácidos Hidrólise de todas
Proteínas: aspectos gerais
 Proteínas: aspectos gerais As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (mais de 50% do seu peso seco) As proteínas são omnipresentes na célula, pois estão ligadas a todos
Proteínas: aspectos gerais As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (mais de 50% do seu peso seco) As proteínas são omnipresentes na célula, pois estão ligadas a todos
4/14/2015. Proteínas. Fundamentos da Estrutura de Proteínas Parte 1. Funções biológicas das Proteínas
 1 Todo o material disponibilizado é preparado para as disciplinas que ministramos e colocado para ser acessado livremente pelos alunos ou interessados. Solicitamos que não seja colocado em sites nãolivres.
1 Todo o material disponibilizado é preparado para as disciplinas que ministramos e colocado para ser acessado livremente pelos alunos ou interessados. Solicitamos que não seja colocado em sites nãolivres.
Química Orgânica I. Ácidos e Bases, tipos de reações, intermediários de reações, termodinâmica e cinética de reações orgânicas.
 Química Orgânica I Ácidos e Bases, tipos de reações, intermediários de reações, termodinâmica e cinética de reações orgânicas Aula 4 (Parte I) Profa. Alceni Augusta Werle Profa Tânia Márcia Sacramento
Química Orgânica I Ácidos e Bases, tipos de reações, intermediários de reações, termodinâmica e cinética de reações orgânicas Aula 4 (Parte I) Profa. Alceni Augusta Werle Profa Tânia Márcia Sacramento
Proteínas V: proteínas fibrosas
 MÓDULO 3 - AULA 15 Objetivo Conhecer as características estruturais das proteínas fibrosas. As proteínas podem ser subdivididas em dois grandes grupos: proteínas fibrosas e proteínas globulares. Esta classificação
MÓDULO 3 - AULA 15 Objetivo Conhecer as características estruturais das proteínas fibrosas. As proteínas podem ser subdivididas em dois grandes grupos: proteínas fibrosas e proteínas globulares. Esta classificação
(500 U/1 mg) (100 U/0.02 mg) (100 U/0.05mg) (80 U/0.02mg)
 log PM 9//202 Ex 7. Purificação de uma celulase por cromatografia de troca iônica e filtração em gel sendo dados a quantidade de material aplicado e a correspondente atividade enzimática a) Recuperação?
log PM 9//202 Ex 7. Purificação de uma celulase por cromatografia de troca iônica e filtração em gel sendo dados a quantidade de material aplicado e a correspondente atividade enzimática a) Recuperação?
ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial. Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica
 ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica Prof. Diogo Schott diogo.schott@yahoo.com Substâncias orgânicas
ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica Prof. Diogo Schott diogo.schott@yahoo.com Substâncias orgânicas
Soluções de Conjunto de Problemas 1
 Soluções de 7.012 Conjunto de Problemas 1 Questão 1 a) Quais são os quatro tipos principais de moléculas biológicas discutidos na aula? Cite uma função importante de cada tipo de molécula biológica na
Soluções de 7.012 Conjunto de Problemas 1 Questão 1 a) Quais são os quatro tipos principais de moléculas biológicas discutidos na aula? Cite uma função importante de cada tipo de molécula biológica na
AMINOÁCIDOS. - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos;
 1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
BIOLOGIA EXERCÍCIOS. Anabolismo Nuclear
 Anabolismo Nuclear EXERCÍCIOS 1. mesmo responsável pela decodificação do genoma humano em 2001, o presidente dos EUA, Barack Obama, pediu a seus conselheiros especializados em biotecnologia para analisarem
Anabolismo Nuclear EXERCÍCIOS 1. mesmo responsável pela decodificação do genoma humano em 2001, o presidente dos EUA, Barack Obama, pediu a seus conselheiros especializados em biotecnologia para analisarem
Revisão de Química Orgânica
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Revisão de Química Orgânica Prof. Dra. Narlize Silva Lira Cavalcante A Química Orgânica e a Vida A uímica
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Revisão de Química Orgânica Prof. Dra. Narlize Silva Lira Cavalcante A Química Orgânica e a Vida A uímica
Aminoácidos. UNIDADE I Estrutura e Função das Proteínas COOH I. VISÃO GERAL II. ESTRUTURA DOS AMINOÁCIDOS. Aminoácido livre
 UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
Influência da Genética desempenho
 UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI luizcarnevalijr@usp.br
UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI luizcarnevalijr@usp.br
Metabolismo das Proteínas e aminoácidos
 Metabolismo das Proteínas e aminoácidos Compostos à base de C, H, O e N com funções importantes no organismo animal e vegetal. São grandes moléculas, polímeros de aminoácidos ligadas por ligações peptídicas
Metabolismo das Proteínas e aminoácidos Compostos à base de C, H, O e N com funções importantes no organismo animal e vegetal. São grandes moléculas, polímeros de aminoácidos ligadas por ligações peptídicas
AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES
 UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
Fisiologia do Exercício. cio. Aula 1
 Aula 1 Conceito É a capacidade de realizar trabalho. É tudo que pode modificar a matéria TRABALHO É o produto da força ou componente da força na direção do deslocamento, pelo deslocamento. Portanto, para
Aula 1 Conceito É a capacidade de realizar trabalho. É tudo que pode modificar a matéria TRABALHO É o produto da força ou componente da força na direção do deslocamento, pelo deslocamento. Portanto, para
FRENTE III QUÍMICA ORGÂNICA BIOQUÍMICA: AMINOACIDOS, PEPTIDEOS E PROTEINAS
 INTRODUÇÃO Os organismos vivos são constituídos por moléculas, átomos e íons, que por si só, não possuem vida. Mas o que distingue organismos vivos objetos? - Capacida se reproduzir; - Capacida extrair,
INTRODUÇÃO Os organismos vivos são constituídos por moléculas, átomos e íons, que por si só, não possuem vida. Mas o que distingue organismos vivos objetos? - Capacida se reproduzir; - Capacida extrair,
Átomos Moléculas Íons Biomoléculas. Matéria é formada por Átomos. Obs.: teoria confirmada apenas no início do século XX.
 Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
II Correto. Quanto maior a distância entre as cargas, mais fraca é a ligação e menos energia é empregada na sua quebra.
 01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando menos o ácido que passa a ser o mais fraco entre os listados.
01. Item B I Correto. A energia para quebrar a ligação H (568 kj/mol) é a maior da tabela. Isto torna mais difícil a sua quebra, portanto ionizando menos o ácido que passa a ser o mais fraco entre os listados.
METABOLISMO DE AMI OÁCIDOS
 METABOLISMO DE AMI OÁCIDOS As proteínas constituintes dos organismos estão continuamente sendo renovadas (turnover das proteínas). * Os aminoácidos presentes nas células animais originam-se das proteínas
METABOLISMO DE AMI OÁCIDOS As proteínas constituintes dos organismos estão continuamente sendo renovadas (turnover das proteínas). * Os aminoácidos presentes nas células animais originam-se das proteínas
Membranas Biológicas. Profª Eleonora Slide de aula
 Membranas Biológicas Profª Eleonora Slide de aula Membranas Biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Membranas Biológicas Profª Eleonora Slide de aula Membranas Biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Organic Chemistry. 4 th Edition Paula Yurkanis Bruice. Irene Lee Case Western Reserve University Cleveland, OH 2004, Prentice Hall.
 Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 5 Estereoquímica Arranjo de Átomos no Espaço Estereoquímica de Reações de Adição Irene Lee Case Western Reserve University eveland, O 2004, Prentice
Organic Chemistry 4 th Edition Paula Yurkanis Bruice Aula 5 Estereoquímica Arranjo de Átomos no Espaço Estereoquímica de Reações de Adição Irene Lee Case Western Reserve University eveland, O 2004, Prentice
Aminoácidos e Peptídeos
 Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Metabolismo dos aminoácidos: - Síntese e degradação dos aminoácidos. Objectivos: Analisar o metabolismo dos aminoácidos:
 BIOQUÍMICA Ensino teórico - 1º ano Mestrado Integrado em Medicina 2010/2011 22 ª aula teórica Metabolismo dos aminoácidos: - Síntese e degradação dos aminoácidos 13-dez-10 Objectivos: Analisar o metabolismo
BIOQUÍMICA Ensino teórico - 1º ano Mestrado Integrado em Medicina 2010/2011 22 ª aula teórica Metabolismo dos aminoácidos: - Síntese e degradação dos aminoácidos 13-dez-10 Objectivos: Analisar o metabolismo
Reação de neutralização:
 01 Reação de neutralização: Ácido entanodioico Hidróxido de sódio Etanoato de sódio Água (oxálico) 1 02 Deslocamento do hidrogênio: Propanoato de sódio (A) Neutralização: Propanoato de sódio (B) Liberação
01 Reação de neutralização: Ácido entanodioico Hidróxido de sódio Etanoato de sódio Água (oxálico) 1 02 Deslocamento do hidrogênio: Propanoato de sódio (A) Neutralização: Propanoato de sódio (B) Liberação
FRENTE III QUÍMICA ORGÂNICA BIOQUÍMICA: CARBOIDRATOS E LIPIDEOS
 CARBOIDRATOS Os carboidratos são as biomoléculas mais abundantes na natureza. Estima-se que, por meio da fotossíntese, as plantas produzem 6.000.000 de toneladas do carboidrato celulose por hora no mundo.
CARBOIDRATOS Os carboidratos são as biomoléculas mais abundantes na natureza. Estima-se que, por meio da fotossíntese, as plantas produzem 6.000.000 de toneladas do carboidrato celulose por hora no mundo.
LIPÍDIOS. 1º ano Pró Madá
 LIPÍDIOS 1º ano Pró Madá O QUE SÃO? Também chamados de gorduras Compostos com estrutura molecular variada principalmente, por moléculas de hidrogênio, oxigênio, carbono Característica principal insolubilidade
LIPÍDIOS 1º ano Pró Madá O QUE SÃO? Também chamados de gorduras Compostos com estrutura molecular variada principalmente, por moléculas de hidrogênio, oxigênio, carbono Característica principal insolubilidade
Aminoácidos e Peptideos
 Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
Você deve desenhar o aminoácido com o grupo amino protonado (pka > 7) e o grupo carboxílico desprotonado (pka <7).
 QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
Entendem-se por compostos heterocíclicos, aqueles compostos orgânicos cíclicos estáveis, que contem no seu anel um ou mais átomos diferentes do
 1 2 3 Entendem-se por compostos heterocíclicos, aqueles compostos orgânicos cíclicos estáveis, que contem no seu anel um ou mais átomos diferentes do carbono. 4 5 O prefixo ribo também é aceitável para
1 2 3 Entendem-se por compostos heterocíclicos, aqueles compostos orgânicos cíclicos estáveis, que contem no seu anel um ou mais átomos diferentes do carbono. 4 5 O prefixo ribo também é aceitável para
Ligações Iônicas. Tipos de Ligações
 Ligações Iônicas Tipos de Ligações Existem diversos tipos de ligações para se considerar quando analisar a composição química de um composto. Uma ligação pode ser definida como uma força que prende grupos
Ligações Iônicas Tipos de Ligações Existem diversos tipos de ligações para se considerar quando analisar a composição química de um composto. Uma ligação pode ser definida como uma força que prende grupos
LISTA DE EXERCÍCIOS REAÇÕES ORGÂNICAS
 Nome: nº: Ensino: Curso Pré-Vestibular ano/série: Componente Curricular: Química Professor: Ricardo Honda Data: / / 2011 LISTA DE EXERCÍCIOS REAÇÕES ORGÂNICAS 1) (FUVEST 2010 1ª Fase) Em um experimento,
Nome: nº: Ensino: Curso Pré-Vestibular ano/série: Componente Curricular: Química Professor: Ricardo Honda Data: / / 2011 LISTA DE EXERCÍCIOS REAÇÕES ORGÂNICAS 1) (FUVEST 2010 1ª Fase) Em um experimento,
CÓDIGO GENÉTICO E SÍNTESE PROTEICA
 Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA 1. Síntese de proteínas pelos ribossomos a partir do RNAm. a) RNAm: molécula de RNA que contem a informação genética necessária para
Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA 1. Síntese de proteínas pelos ribossomos a partir do RNAm. a) RNAm: molécula de RNA que contem a informação genética necessária para
Membranas Biológicas. Profª Eleonora Slide de aula
 Membranas Biológicas Profª Eleonora Slide de aula Membranas biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Membranas Biológicas Profª Eleonora Slide de aula Membranas biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Aula 1 Enzimas são Proteínas Globulares
 Aula 1 Enzimas são Proteínas Globulares Já existem 4.725 enzimas conhecidas, distribuídas em grupos de acordo com suas características catalíticas, como veremos na aula 2. Apesar de bem conhecidas atualmente,
Aula 1 Enzimas são Proteínas Globulares Já existem 4.725 enzimas conhecidas, distribuídas em grupos de acordo com suas características catalíticas, como veremos na aula 2. Apesar de bem conhecidas atualmente,
Exercícios sobre Bioquímica
 Exercícios sobre Bioquímica 01. (Uerj) Na presença de certos solventes, as proteínas sofrem alterações tanto em sua estrutura espacial quanto em suas propriedades biológicas. No entanto, com a remoção
Exercícios sobre Bioquímica 01. (Uerj) Na presença de certos solventes, as proteínas sofrem alterações tanto em sua estrutura espacial quanto em suas propriedades biológicas. No entanto, com a remoção
Estrutura das Proteínas pode ser descrita em 4 níveis de organização
 PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
BIOQUÍMICA I AULAS PRÁTICAS. 2º ano, 1º semestre
 BIOQUÍMICA I AULAS PRÁTICAS 2º ano, 1º semestre 2013-2014 Objectivo Bases teórico/práticas das metodologias experimentais necessárias ao estudo qualitativo e quantitativo de macromoléculas - péptidos e
BIOQUÍMICA I AULAS PRÁTICAS 2º ano, 1º semestre 2013-2014 Objectivo Bases teórico/práticas das metodologias experimentais necessárias ao estudo qualitativo e quantitativo de macromoléculas - péptidos e
Componentes Químicos das Células
 Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
COLÉGIO PEDRO II CAMPUS TIJUCA II. DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI
 COLÉGIO PEDRO II CAMPUS TIJUCA II DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI 1º & 2º TURNOS 3ª SÉRIE / ENSINO MÉDIO REGULAR & INTEGRADO ANO LETIVO 2015 PROFESSORES: FRED & PEDRO
COLÉGIO PEDRO II CAMPUS TIJUCA II DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI 1º & 2º TURNOS 3ª SÉRIE / ENSINO MÉDIO REGULAR & INTEGRADO ANO LETIVO 2015 PROFESSORES: FRED & PEDRO
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas
 Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Profª Eleonora Slide de aula. Cadeia de Transporte de Elétrons e Fosforilação Oxidativa
 Cadeia de Transporte de Elétrons e Fosforilação Oxidativa Cadeia de Transporte de Elétrons ou Cadeia Respiratória Os transportadores de elétrons sempre funcionam em uma seqüência determinada Os potenciais
Cadeia de Transporte de Elétrons e Fosforilação Oxidativa Cadeia de Transporte de Elétrons ou Cadeia Respiratória Os transportadores de elétrons sempre funcionam em uma seqüência determinada Os potenciais
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos
 Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES
 UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI luizcarnevalijr@usp.br
UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI luizcarnevalijr@usp.br
www.professormazzei.com POLÍMEROS Folha 01 João Roberto Mazzei
 01. (UFMG 2008) As proteínas são polímeros naturais formados através de ligações peptídicas que se estabelecem quando o grupo amino de um aminoácido reage com o grupo carboxila de outro. Considere a estrutura
01. (UFMG 2008) As proteínas são polímeros naturais formados através de ligações peptídicas que se estabelecem quando o grupo amino de um aminoácido reage com o grupo carboxila de outro. Considere a estrutura
Aminoácidos, Péptidos e Proteínas
 Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Composição química celular
 Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
Ácidos Nucléicos Duplicação do DNA e Síntese de PROTEÍNAS. Paulo Dutra
 Ácidos Nucléicos Duplicação do DNA e Síntese de PROTEÍNAS Paulo Dutra ÁCIDOS NUCLEICOS Nucleotídeos É a unidade formadora dos ácidos nucléicos: DNA e RNA. É composto por um radical fosfato, uma pentose
Ácidos Nucléicos Duplicação do DNA e Síntese de PROTEÍNAS Paulo Dutra ÁCIDOS NUCLEICOS Nucleotídeos É a unidade formadora dos ácidos nucléicos: DNA e RNA. É composto por um radical fosfato, uma pentose
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I. Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas.
 Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
Bioinformática Estrutural Aula 1
 Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária Paula.kuser-falcao@embrapa.br Pratique Atividade Física Paula
Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária Paula.kuser-falcao@embrapa.br Pratique Atividade Física Paula
