Introdução à Análise Química
|
|
|
- Bernardo Coradelli Carneiro
- 7 Há anos
- Visualizações:
Transcrição
1 Introdução à Análise Química 2 semestre 2011 Profa. Maria Auxiliadora Costa Matos
2 Data/mês ASSUNTO 08/ago Erros e Tratamento de Dados 15/ago Introdução à Volumetria/Volumetria de Neutralização 22/ago Volumetria de Neutralização 29/ago Volumetria de Neutralização 05/set Volumetria de Neutralização 12/ set Volumetria de Neutralização 19/ set 1º TVC 26/ set Volumetria de Precipitação 03/out Volumetria de Precipitação/ Volumetria de Complexação 10/ out Volumetria de Complexação 17/ out Semana do ICE (não haverá aula) 24/ out ENQA 31/out 2º TVC 07/nov Volumetria de Oxidação-redução 14/nov Recesso 21/nov Volumetria de Oxidação-redução 28/nov Gravimetria 05/dez 3º TVC 12/dez 2 a chamada Nota final = (1ºTVC + 2ºTVC + 3ºTVC)/3
3 REFERÊNCIAS BIBLIOGRÁFICAS 1. Harris, D. C. Análise Química Quantitativa, Editora LTC, 5 a edição, Skoog, D. A, West, D. M., Holler, F. J., Crouch, S. R. Fundamentos de Química Analítica, Editora Thomson, tradução da 8ª edição, Skoog, D.A.; West, D.M.; Holler, F.J. Fundamentals of Analytical Chemistry, 6 a ed., Saunders, Philadelphia, 1992, ou versão condensada, mesmos autores, Analytical Chemistry, An Introduction, 6 a ed., Saunders, Philadelphia, Jeffery, G. H.; Bassett, J.; Mendham, J.; Denney, R. C. Tradução Macêdo H. Vogel Análise Química Quantitativa, Editora Guanabara Koogan S.A, 5 a. edição, 1992.
4 INTRODUÇÃO À QUÍMICA ANALÍTICA Química Analítica é o ramo da química que envolve a separação, identificação e determinação das quantidades relativas dos componentes de uma amostra. QUÍMICA ANALÍTICA ANÁLISE QUALITATIVA ANÁLISE QUANTITATIVA Revela a identidade química das espécies em uma amostra Estabelece a quantidade relativa de uma ou mais espécies (analitos) em termos numéricos em uma amostra
5 Química Bioquímica Química Inorgânica Química Orgânica Físico-Química Geologia Geofísica Geoquímica Paleontologia Paleobiologia Ciências do meio Ambiente Ecologia Meteorologia Oceanografia Biologia Botânica Genética Microbiologia Biologia Molecular Zoologia Agricultura Agronomia Ciências dos animais Ciências da Produção Ciência dos Alimentos Horticultura Ciências Sociais Química Analítica Ciências Sociais Arqueologia Antropologia Forense Física Astrofísica Astronomia Biofísica Engenharia Civil Química Elétrica Mecânica Medicina Análises Clinicas Química Medicinal Farmácia Toxicologia Ciências dos materiais Metalurgia Polimentos Estado Sólido
6 De um modo geral, a análise química quantitativa pode ser estabelecida em etapas, com grau de importância e influência no resultado final da análise: I - Definição do problema analítico II - Escolha do método analítico adequado III - Obtenção de uma amostra representativa - Amostragem IV - Preparo da amostra V - Análise Química Calibração Medida VI - Avaliação - Tratamento & interpretação dos dados Controle de Qualidade Analítica Apresentação dos Resultados
7 DEFINIÇÃO DO PROBLEMA ANALÍTICO Traduzir questões gerais, em questões especificas acessíveis que possam ser reproduzidas através de medidas químicas. Problema analítico? Objetivo da análise? Determinação de cálcio e magnésio na água para avaliação da sua dureza e classificação quanto ao uso ou destinação. Avaliação dos níveis de concentração de herbicidas em um lote de morangos. Problemas Analítico: Controle de qualidade (matéria prima e/ou produto final) Controle de produção (adição de C, Ni, Cr na fabricação de aço) Avaliação ambiental (poluentes) Exposição ocupacional (análise do ambiente ou fluídos biológicos)
8 FATORES QUE INFLUENCIAM NA ESCOLHA 1) Faixa de concentração da espécie a ser analisada: O analito é um componente majoritário (Métodos clássicos) ou um componente traço (Métodos mais sensíveis - instrumentais)? Quanto menor o nível de concentração analisada, mais critico será o risco de contaminação a partir de reagente e aparatos. Componente Nível de concentração traço menor que 0,01% micro 0,01 a 1% macro 1 a 100% 2) Nível de exatidão desejado: O tempo requerido para a uma análise aumenta de forma exponencial com nível de exatidão desejado. 3) Componentes presentes na amostra Interferentes: É necessário conhecer a composição química aproximada da amostra antes de selecionar um método para a determinação quantitativa de um ou mais componentes. Uma análise qualitativa pode ser realizada para uma triagem da amostra identificando componente que possam interferir no método a ser escolhido. Homogeneização; 4) Propriedade física e química da amostra bruta Perdas por volatilidade; Alteração da composição, durante armazenamento ou sob condições de análise; 5) Número de amostras & tempo de análise Métodos para decomposição ou dissolução da amostra sem perda de analito.
9 MÉTODO MÉTODOS CLÁSSICOS MÉTODOS INSTRUMENTAIS - Ideal para análises esporádicas - Baixo custo - Aparelhagem de fácil aquisição - Macro constituinte - Ideal para rotina - Custo mais elevado - Pessoal treinado - Análise de traços -Necessita calibração do aparelho -Grande aplicação em industria -Maior sensibilidade Quais os fatores desejável no método escolhido? a) Método deve ser eficiente e, sempre que possível, simples e rápido; b) Não deve causar danos ao recipiente no qual a amostra será tratada; c) Não deve causar qualquer perda do constituinte de interesse; d) Não deve permitir ou promover contaminação dos constituintes a serem determinados, inserções de interferentes, amenos que possam ser facilmente removidos. e) Máxima segurança operacional
10 AMOSTRAGEM Amostragem é o processo de selecionar uma amostra bruta representativa de um lote ou população a ser investigada, refletindo adequadamente as propriedades de interesse. Preparo da amostra é o processo que converte uma amostra bruta em uma amostra de laboratório homogênea. Também, referem-se, as etapas que eliminam as espécies interferentes ou que concentram os constituintes em análise. Lote Amostragem Amostra bruta representativa Preparo da amostra Amostra homogênea de laboratório 1 Alíquota 2 Alíquota 3 Alíquota
11 PREPARO DA AMOSTRA A primeira etapa de uma análise consiste em submeter a amostra a um tratamento adequado visando sua preparação para os passos subseqüentes da análise. Pré-tratamento Tratamento Preliminares Preparo da amostra Dissolução, decomposição da amostra, separação dos constituintes, concentração do analito Separação granulométrica Secagem Moagem de sólidos Filtração Extração líquida Extração em fase sólida (SPE) Cromatografia em colunas abertas Destilação, vaporização, etc Etapas precedentes a análise: preparação da amostra Amostras reais geralmente são amostras complexas Amostras analíticas que apresentam uma mistura complexa de espécies e geralmente comportamento longe do ideal quanto a solubilidade, volatilidade, estabilidade e homogeneidade. Ex: Amostras de solo, sedimento, rochas, tecido animal, tecido vegetal, fluidos biológicos, etc
12 ANÁLISE QUÍMICA Medir a concentração do analito em várias alíquotas idênticas (replicatas) para avaliar a incerteza da análise. Para cada método devem ser verificadas todas as variáveis que afetam a análise propriamente dita, além dos interferentes químicos ou não, para que não haja comprometimento do resultado. TRATAMENTO DE DADOS Métodos de calibração (instrumentais) Comparação com padrões analíticos certificados Tratamento estatístico sempre que necessário, para validar os resultados. APRESENTAÇÃO DOS RESULTADOS OBTIDOS O cuidado com todo processo de análise é muito importante, porque o resultado obtido é um número. Este número muitas vezes pode gerar ações imediatas de órgãos oficiais de saneamento básico, saúde pública ou ainda controle ambiental. Retirada de produtos do mercado Fechamento de indústrias Afastamento do trabalho Rodízio de automóveis Indicação para uma cirurgia
13 Soluções e Unidades de concentração
14 CONCENTRAÇÃO QUÍMICA Solução é uma mistura homogênea de duas ou mais substâncias. A espécie em menor quantidade em uma solução é chamada de soluto, e a espécie em maior quantidade é chamada de solvente. Concentração química de uma substância refere-se à quantidade de soluto contida em um dado volume ou massa de solução ou de solvente. 1. Concentração em g/l: Representa a massa de soluto expressa em gramas por volume da solução expresso em litro. A concentração (em qualquer unidade) é válida para qualquer quantidade da solução, independente da massa e do volume. Solução 1 mol/l de HCl (n mol = 1 mol em 1000 ml de solução). Solução HCl 1 mol/l Pedro 11/03/ Uma alíquota de 10 ml da solução do frasco é transferida para um erlenmeyer (n mol = 0,01 mols em 10 ml de solução).
15 CONCENTRAÇÃO QUÍMICA Solução é uma mistura homogênea de duas ou mais substâncias. A espécie em menor quantidade em uma solução é chamada de soluto, e a espécie em maior quantidade é chamada de solvente. Concentração química de uma substância refere-se à quantidade de soluto contida em um dado volume ou massa de solução ou de solvente. 1. Concentração em g/l: Representa a massa de soluto expressa em gramas por volume da solução expresso em litro. A concentração (em qualquer unidade) é válida para qualquer quantidade da solução, independente da massa e do volume. 2. Concentração em mol/l: É o número de moles de uma substância por litro de solução. Concentração entre [ ] é expressa em mol/l concentração no equilíbrio Exemplo 1: Uma porção de 100 ml água do mar contém 2,70 g de cloreto de sódio. Qual a concentração em mol/l de NaCl no oceano?
16 3. Partes por milhão (ppm) e partes por bilhão (ppb): ppm gramas de substâncias por 1 milhão de gramas da solução ou mistura total. ppb gramas de substâncias por 1 bilhão de gramas de solução ou mistura total. 1 ppm = 1 µg/g 1 ppb = 1 ng/g Soluções aquosas e bem diluídas 1 mg/l ou 1 µg/ml Soluções aquosas e bem diluídas 1 µg/l ou 1 ng/ml Exemplo 2: A concentração de C 29 H 60 na água de chuva no verão é de 34 ppb. Encontre a molaridade do C 29 H Composição Percentual: A porcentagem de um componente em uma mistura ou solução é usualmente expressa como percentual massa/massa (% m/m) ou peso/peso (% p/p). As unidades de massa ou volume devem sempre ser expressas para evitar ambigüidade. Exemplo: 3. Qual a massa de etanol em 250 g de uma solução 95 % (m/m)? 4. Qual a massa de ácido acético em 250mL de vinagre com teor de 4,0% (m/v)? 5. Qual a concentração em mol/l de uma solução de H 2 SO 4 a 95,0% (m/m) e densidade 1,84 g/cm 3?
17 5. Normalidade: Razão entre o n de equivalente-grama do soluto e o volume da solução em litros. N = n equiv-g V (L) Sendo: n equiv-g = massa (g) E equiv-g E equiv-g = = Massa molar y N = massa (g) E equiv-g x V (L) ÁCIDOS: y = n o de H + ionizáveis BASES: y = n o de OH - SAIS: y = carga positiva (ou negativa) total ELEMENTOS QUÍMICOS: y = valência
18 PREPARO DE SOLUÇÕES Para se preparar uma solução com uma concentração em mol/l desejada de um sólido ou líquido puro, pesamos uma massa exata do reagente e a dissolvemos no volume desejado em um balão volumétrico. Exemplo 6: Quantos gramas de CuSO 4.5H 2 O devem ser dissolvidos em um balão volumétrico de 500,00 ml para o preparo de uma solução que contém 8,00 mmol/l de Cu 2+? Dado MM CuSO 4.5H 2 O = 249,69 g/mol.
19 DILUIÇÃO Soluções diluídas devem ser preparadas a partir de soluções concentradas. Um volume ou massa desejados de uma solução concentrada é transferido para um balão volumétrico e diluído para um volume ou massa final pretendidos. O princípio básico da diluição é que o número de mol do soluto é o mesmo na alíquota da solução concentrada e solução diluída. C sol. conc. x V sol. conc. = C sol. diluída x V sol. dil Solução 1 mol/l de HCl (n mol = 1 mol em 1000 ml de solução). Solução HCl 1 mol/l Pedro 11/03/ Adição de 40 ml de água. 1 - Uma alíquota de 10 ml da solução do frasco é transferida para um balão volumétrico (n mol = 0,01 mols em 10 ml de solução) Volume final 50 ml (n mol = 0,01 mols em 50 ml de solução). Exemplo 7: A concentração molar do H 2 S0 4 concentrado para uso em laboratório é 17,8 mol/l. Quantos mililitros desse reagente devem ser diluídos para preparar 250 ml de H 2 S0 4 0,150 mol/l?
Química Analítica IV
 Química Analítica IV 1 semestre 2012 Profa. Maria Auxiliadora Costa Matos Data/mês 08/mar 15/mar 22/mar 29/mar 05/abr 12/abr 19/abr 26/abr 03/mai 10/mai 17/mai 24/mai 31/mai 07/jun 14/jun 21/jun 28/jun
Química Analítica IV 1 semestre 2012 Profa. Maria Auxiliadora Costa Matos Data/mês 08/mar 15/mar 22/mar 29/mar 05/abr 12/abr 19/abr 26/abr 03/mai 10/mai 17/mai 24/mai 31/mai 07/jun 14/jun 21/jun 28/jun
Química. Disciplina QUIO94 - Introdução à Análise. 1 semestre Profa. Maria Auxiliadora Costa Matos. Download aulas:
 Introdução a Analise Química - I sem/2013 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO94 - Introdução à Análise Química
Introdução a Analise Química - I sem/2013 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO94 - Introdução à Análise Química
Introdução à Análise Química
 Introdução a Analise Química - II sem/2012 Profa Ma Auxiliadora - 1 Introdução à Análise Química 1 semestre 2012 Profa. Maria Auxiliadora Costa Matos Introdução a Analise Química - II sem/2012 Profa Ma
Introdução a Analise Química - II sem/2012 Profa Ma Auxiliadora - 1 Introdução à Análise Química 1 semestre 2012 Profa. Maria Auxiliadora Costa Matos Introdução a Analise Química - II sem/2012 Profa Ma
Química. Disciplina QUIO94 - Introdução à Análise. 2 semestre Profa. Maria Auxiliadora Costa Matos. Download aulas:
 Introdução a Analise Química - II sem/2013 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO94 - Introdução à Análise Química
Introdução a Analise Química - II sem/2013 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO94 - Introdução à Análise Química
Química. Disciplina QUIO94 - Introdução à Análise. 2 semestre Profa. Maria Auxiliadora Costa Matos. Downloads aulas:
 Introdução a Analise Química 2a sem/2014 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO94 - Introdução à Análise Química
Introdução a Analise Química 2a sem/2014 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina QUIO94 - Introdução à Análise Química
INTRODUÇÃO À ANÁLISE QUÍMICA
 INTRODUÇÃO À ANÁLISE QUÍMICA 2º SEMESTRE DE 2016 Profa. Dra. Denise Lowinsohn denise.lowinsohn@ufjf.edu.br Downloads aulas: http://www.ufjf.br/nupis/ CRONOGRAMA DIA/MÊS ASSUNTO 22/08 Soluções e cálculos
INTRODUÇÃO À ANÁLISE QUÍMICA 2º SEMESTRE DE 2016 Profa. Dra. Denise Lowinsohn denise.lowinsohn@ufjf.edu.br Downloads aulas: http://www.ufjf.br/nupis/ CRONOGRAMA DIA/MÊS ASSUNTO 22/08 Soluções e cálculos
INTRODUÇÃO À ANÁLISE QUÍMICA
 INTRODUÇÃO À ANÁLISE QUÍMICA 1º SEMESTRE DE 2017 Profa. Dra. Denise Lowinsohn denise.lowinsohn@ufjf.edu.br Downloads aulas: http://www.ufjf.br/nupis/ CRONOGRAMA DIA/MÊS ASSUNTO 06/03 Soluções e cálculos
INTRODUÇÃO À ANÁLISE QUÍMICA 1º SEMESTRE DE 2017 Profa. Dra. Denise Lowinsohn denise.lowinsohn@ufjf.edu.br Downloads aulas: http://www.ufjf.br/nupis/ CRONOGRAMA DIA/MÊS ASSUNTO 06/03 Soluções e cálculos
I semestre Profa. Maria Auxiliadora Costa Matos
 Introdução a Analise Química 1a sem/2018 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplinas QUIO94 - Introdução à Análise Química
Introdução a Analise Química 1a sem/2018 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplinas QUIO94 - Introdução à Análise Química
Soluções e Unidades de concentrações
 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Química das Soluções QUI084 I semestre 2017 AULA REVISÃO Soluções e Unidades de concentrações Profa.
Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Química das Soluções QUI084 I semestre 2017 AULA REVISÃO Soluções e Unidades de concentrações Profa.
QUI 072/150 Química Analítica V Análise Instrumental. Aula 1 Introdução Química Analítica
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 072/150 Química Analítica V Análise Instrumental Aula 1 Introdução Química Analítica Prof. Julio C. J. Silva
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 072/150 Química Analítica V Análise Instrumental Aula 1 Introdução Química Analítica Prof. Julio C. J. Silva
Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada
 1 Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada 1. Questões de estudo - Como preparar uma solução aquosa de NaOH 0,1 M? - Como preparar uma solução
1 Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada 1. Questões de estudo - Como preparar uma solução aquosa de NaOH 0,1 M? - Como preparar uma solução
É o cálculo das quantidades de reagentes e/ou produtos das reações químicas.
 Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
Boas Práticas Laboratoriais Preparo de soluções
 Boas Práticas Laboratoriais Preparo de soluções Disciplina de Reumatologia 2011 http://www.ruf.rice.edu/~bioslabs/schedules/talks/solutions_dilutions/bioedmixtures.htm O que fazer antes do preparo Vc sabe
Boas Práticas Laboratoriais Preparo de soluções Disciplina de Reumatologia 2011 http://www.ruf.rice.edu/~bioslabs/schedules/talks/solutions_dilutions/bioedmixtures.htm O que fazer antes do preparo Vc sabe
PRÁTICA 03 - DETERMINAÇÃO DE CLORETO PELO MÉTODO DE MOHR E FAJANS
 PRÁTICA 03 - DETERMINAÇÃO DE CLORETO PELO MÉTODO DE MOHR E FAJANS Aula 13 METAS Familiarizar com as técnicas de preparo e padronização de uma solução de AgNO3; determinar a concentração de cloreto em soro
PRÁTICA 03 - DETERMINAÇÃO DE CLORETO PELO MÉTODO DE MOHR E FAJANS Aula 13 METAS Familiarizar com as técnicas de preparo e padronização de uma solução de AgNO3; determinar a concentração de cloreto em soro
Introdução à Volumetria. Profa. Lilian Lúcia Rocha e Silva
 Introdução à Volumetria Profa. Lilian Lúcia Rocha e Silva INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução que contém um soluto
Introdução à Volumetria Profa. Lilian Lúcia Rocha e Silva INTRODUÇÃO À VOLUMETRIA TITULAÇÃO Processo no qual uma solução padrão ou solução de referência é adicionada a uma solução que contém um soluto
A ÁLISE TITRIMÉTRICA
 A ÁLISE TITRIMÉTRICA Análise titrimétrica - O termo análise titrimétrica refere-se à análise química quantitativa feita pela determinação do volume de uma solução, cuja concentração é conhecida com exatidão,
A ÁLISE TITRIMÉTRICA Análise titrimétrica - O termo análise titrimétrica refere-se à análise química quantitativa feita pela determinação do volume de uma solução, cuja concentração é conhecida com exatidão,
Após agitação, mantendo-se a temperatura a 20ºC, coexistirão solução saturada e fase sólida no(s) tubo(s)
 01) (Covest-2006) Uma solução composta por duas colheres de sopa de açúcar (34,2g) e uma colher de sopa de água (18,0 g) foi preparada. Sabendo que: MMsacarose = 342,0g mol -1, MMágua = 18,0 g mol -1,
01) (Covest-2006) Uma solução composta por duas colheres de sopa de açúcar (34,2g) e uma colher de sopa de água (18,0 g) foi preparada. Sabendo que: MMsacarose = 342,0g mol -1, MMágua = 18,0 g mol -1,
Título: Iodometria. Aula Experimental n 16
 Aula Experimental n 16 Objetivos: - Padronização de solução de Na 2 S 2 O 3. - Determinação do teor de cobre (Cu 2 ) de uma amostra. - Determinação do teor de Cloro ativo em uma amostra de água sanitária.
Aula Experimental n 16 Objetivos: - Padronização de solução de Na 2 S 2 O 3. - Determinação do teor de cobre (Cu 2 ) de uma amostra. - Determinação do teor de Cloro ativo em uma amostra de água sanitária.
Disciplina Metodologia Analítica QUI102. I semestre AULA 01 Profa. Maria Auxiliadora Costa Matos
 Metodologia Analítica I sem/2017 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Metodologia Analítica QUI102 I semestre 2017
Metodologia Analítica I sem/2017 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Metodologia Analítica QUI102 I semestre 2017
tem-se no equilíbrio que 1 mol de HCl reagiu com 1 mol de NaOH, ou seja: n(hcl) = n(naoh)
 Experiência 8: TITULAÇÕES ÁCIDO-BASE 1. Objetivos Após a realização desta atividade experimental, espera-se que o aluno seja capaz de: - Determinar a concentração de um ácido e uma base por titulação.
Experiência 8: TITULAÇÕES ÁCIDO-BASE 1. Objetivos Após a realização desta atividade experimental, espera-se que o aluno seja capaz de: - Determinar a concentração de um ácido e uma base por titulação.
Disciplina Metodologia Analítica QUI102 1 semestre AULA 01 Profa. Maria Auxiliadora Costa Matos
 Metodologia Analítica I sem/2013 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Metodologia Analítica QUI102 1 semestre 2013
Metodologia Analítica I sem/2013 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Metodologia Analítica QUI102 1 semestre 2013
www.professormazzei.com SOLUÇÕES Folha 03 João Roberto Mazzei
 01. (UERJ 2008) Certos medicamentos são preparados por meio de uma série de diluições. Assim, utilizando-se uma quantidade de água muito grande, os medicamentos obtidos apresentam concentrações muito pequenas.
01. (UERJ 2008) Certos medicamentos são preparados por meio de uma série de diluições. Assim, utilizando-se uma quantidade de água muito grande, os medicamentos obtidos apresentam concentrações muito pequenas.
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA
 UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA PROPOSTA DE ATIVIDADES DIDÁTICAS DISCIPLINA DE QUÍMICA GERAL EXPERIMENTAL ORIENTADORA: Profa. Dra. Liane M. Rossi MONITORES: Bernardo A. Iglesias/Lucas L.
UNIVERSIDADE DE SÃO PAULO INSTITUTO DE QUÍMICA PROPOSTA DE ATIVIDADES DIDÁTICAS DISCIPLINA DE QUÍMICA GERAL EXPERIMENTAL ORIENTADORA: Profa. Dra. Liane M. Rossi MONITORES: Bernardo A. Iglesias/Lucas L.
GRAVIMETRIA. Profa. Lilian Silva
 GRAVIMETRIA Profa. Lilian Silva Agente precipitante Gravimetria separação filtração secagem/ calcinação amostra pesagem precipitado cálculos Gravimetria É o processo de isolar e de pesar um elemento, ou
GRAVIMETRIA Profa. Lilian Silva Agente precipitante Gravimetria separação filtração secagem/ calcinação amostra pesagem precipitado cálculos Gravimetria É o processo de isolar e de pesar um elemento, ou
GRAVIMETRIA. Qui-094 Introdução a Análise Química Profa Maria Auxiliadora Costa Matos 2011-1
 GRAVIMETRIA Qui-094 Introdução a Análise Química Profa Maria Auxiliadora Costa Matos 2011-1 1 GRAVIMETRIA OU ANÁLISE GRAVIMETRICA Processo de isolar ou de pesar um composto definido de um elemento na forma
GRAVIMETRIA Qui-094 Introdução a Análise Química Profa Maria Auxiliadora Costa Matos 2011-1 1 GRAVIMETRIA OU ANÁLISE GRAVIMETRICA Processo de isolar ou de pesar um composto definido de um elemento na forma
GOIÂNIA, / / 2016. PROFESSORA: Núbia de Andrade. DISCIPLINA:Química SÉRIE: 2º. ALUNO(a):
 GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 2º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 2º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
Critérios Específicos de Classificação da Questão Aula
 Critérios Específicos de da Questão Aula Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos DISCIPLINA: Física e Química Módulo: Q 05/06 0 ºAno de escolaridade Data: 3 de novembro
Critérios Específicos de da Questão Aula Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos DISCIPLINA: Física e Química Módulo: Q 05/06 0 ºAno de escolaridade Data: 3 de novembro
Resolução: Resposta: D. Resolução: Resposta: B.
 45 Em química, uma solução apresenta, como característica importante, a: A presença de soluto e de solvente na mesma concentração em quantidade de matéria. B propriedade de dispersar a luz. C ocorrência
45 Em química, uma solução apresenta, como característica importante, a: A presença de soluto e de solvente na mesma concentração em quantidade de matéria. B propriedade de dispersar a luz. C ocorrência
REMOÇÃO DE METAIS PESADOS DE SOLUÇÃO RESIDUAL DA DETERMINAÇÃO DA DEMANDA QUÍMICA DE OXIGÊNIO
 REMOÇÃO DE METAIS PESADOS DE SOLUÇÃO RESIDUAL DA DETERMINAÇÃO DA DEMANDA QUÍMICA DE OXIGÊNIO Géssica Aparecida SILVEIRA Ruth Helena GIANSANTE Luciana Maria SARAN* Faculdade de Ciências Agrárias e Veterinárias,
REMOÇÃO DE METAIS PESADOS DE SOLUÇÃO RESIDUAL DA DETERMINAÇÃO DA DEMANDA QUÍMICA DE OXIGÊNIO Géssica Aparecida SILVEIRA Ruth Helena GIANSANTE Luciana Maria SARAN* Faculdade de Ciências Agrárias e Veterinárias,
Reconhecer as vidrarias volumétricas utilizadas no preparo de soluções;
 AULA 5 Preparo e diluição de soluções OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
AULA 5 Preparo e diluição de soluções OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
Volumetria de Neutralização Ácido-Base
 Volumetria de Neutralização Ácido-Base 1 O que é um Processo de Titulação? A Titulação é uma operação analítica utilizada em análises volumétricas com o objetivo de determinar a Concentração de soluções.
Volumetria de Neutralização Ácido-Base 1 O que é um Processo de Titulação? A Titulação é uma operação analítica utilizada em análises volumétricas com o objetivo de determinar a Concentração de soluções.
P2 - PROVA DE QUÍMICA GERAL - 08/10/07
 P2 - PRVA DE QUÍMICA GERAL - 08/10/07 Nome: Nº de Matrícula: GABARIT Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 R = 8,314 J mol -1 K -1 = 0,0821 atm L mol
P2 - PRVA DE QUÍMICA GERAL - 08/10/07 Nome: Nº de Matrícula: GABARIT Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 R = 8,314 J mol -1 K -1 = 0,0821 atm L mol
Química Analítica IV ERRO E TRATAMENTO DE DADOS ANALÍTICOS
 Química Analítica IV 1 semestre 2012 Profa. Maria Auxiliadora Costa Matos ERRO E TRATAMENTO DE DADOS ANALÍTICOS Todas as medidas físicas possuem um certo grau de incerteza. Quando se faz uma medida, procura-se
Química Analítica IV 1 semestre 2012 Profa. Maria Auxiliadora Costa Matos ERRO E TRATAMENTO DE DADOS ANALÍTICOS Todas as medidas físicas possuem um certo grau de incerteza. Quando se faz uma medida, procura-se
QUI 070 Química Analítica V Análise Instrumental. Aula 8 Potenciometria
 Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 8 Potenciometria Julio C. J. Silva Juiz de Fora, 2014 Potenciometria
Universidade Federal de Juiz de Fora (UFJF) Instituto de Ciências Exatas Depto. de Química QUI 070 Química Analítica V Análise Instrumental Aula 8 Potenciometria Julio C. J. Silva Juiz de Fora, 2014 Potenciometria
Propriedades dos Precipitados
 ANÁLISE GRAVIMÉTRICA ANÁLISE GRAVIMÉTRICA A análise gravimétrica ou gravimetria, é um método analítico quantitativo cujo processo envolve a separação e pesagem de um elemento ou um composto do elemento
ANÁLISE GRAVIMÉTRICA ANÁLISE GRAVIMÉTRICA A análise gravimétrica ou gravimetria, é um método analítico quantitativo cujo processo envolve a separação e pesagem de um elemento ou um composto do elemento
Titulações Ácido-Base Titulações de Neutralização
 Titulações Ácido-Base Titulações de Neutralização Reacções de neutralização Métodos quantitativos Doseamentos Medição de ph e uso de indicadores Soluções tampão No ponto de meia titulação ph = pk a e consoante
Titulações Ácido-Base Titulações de Neutralização Reacções de neutralização Métodos quantitativos Doseamentos Medição de ph e uso de indicadores Soluções tampão No ponto de meia titulação ph = pk a e consoante
Reacções de precipitação
 Reacções de precipitação Ocorre uma reacção de precipitação quando se forma uma precipitado, ou seja, um sólido insolúvel que se separa da solução. Na precipitação a partir de soluções aquosas normalmente
Reacções de precipitação Ocorre uma reacção de precipitação quando se forma uma precipitado, ou seja, um sólido insolúvel que se separa da solução. Na precipitação a partir de soluções aquosas normalmente
Escola Secundária de Lagoa. Ficha de Trabalho 4. Física e Química A 11º Ano Turma A Paula Melo Silva. Revisão 10º Ano: As três miudinhas
 Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 4 Cálculos estequiométricos Parte Um Revisão 10º Ano: As três miudinhas Quantidade em química corresponde
Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 4 Cálculos estequiométricos Parte Um Revisão 10º Ano: As três miudinhas Quantidade em química corresponde
VOLUMETRIA DE NEUTRALIZAÇÃO
 VOLUMETRIA DE NEUTRALIZAÇÃO 1 semestre 2011 Profa. Maria Auxiliadora Costa Matos Volumetria de neutralização envolve a titulação de espécies químicas ácidas com uma solução padrão alcalina (ALCALIMETRIA)
VOLUMETRIA DE NEUTRALIZAÇÃO 1 semestre 2011 Profa. Maria Auxiliadora Costa Matos Volumetria de neutralização envolve a titulação de espécies químicas ácidas com uma solução padrão alcalina (ALCALIMETRIA)
De acordo com o estado de agregação da solução. De acordo com o estado físico do soluto e do estado físico do solvente
 1. INTRODUÇÃO Quando a mistura apresenta as mesmas características em toda a extensão do recipiente temos uma mistura homogênea e, se tiver mais de um aspecto a mistura será heterogênea. Deste modo: I.P.C.:
1. INTRODUÇÃO Quando a mistura apresenta as mesmas características em toda a extensão do recipiente temos uma mistura homogênea e, se tiver mais de um aspecto a mistura será heterogênea. Deste modo: I.P.C.:
Currículo do Curso de Química
 Currículo do Curso de Química Bacharelado ATUAÇÃO O Curso de Bacharelado em Química com Ênfase em Química Ambiental visa a formação de recursos humanos capazes de atuar profissionalmente em indústrias
Currículo do Curso de Química Bacharelado ATUAÇÃO O Curso de Bacharelado em Química com Ênfase em Química Ambiental visa a formação de recursos humanos capazes de atuar profissionalmente em indústrias
Química 1 Cecília e Regina 2ºEM/TI 2º. Química 1-2ºTI
 2º anos - 2012 Matéria Professor(a) Ano/Série Turma Data Trimestre Química 1 Cecília e Regina 2ºEM/TI 2º Aluno(a) Número Observação Química 1-2ºTI Projeto de Recuperação Paralela Atividades podem ser feitas
2º anos - 2012 Matéria Professor(a) Ano/Série Turma Data Trimestre Química 1 Cecília e Regina 2ºEM/TI 2º Aluno(a) Número Observação Química 1-2ºTI Projeto de Recuperação Paralela Atividades podem ser feitas
CURSO APOIO QUÍMICA RESOLUÇÃO
 QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
t 1 t 2 Tempo t 1 t 2 Tempo
 Concentração 01)Uma reação química atinge o equilíbrio químico quando: a) ocorre simultaneamente nos sentidos direto e inverso. b) as velocidades das reações direta e inversa são iguais. c) os reatantes
Concentração 01)Uma reação química atinge o equilíbrio químico quando: a) ocorre simultaneamente nos sentidos direto e inverso. b) as velocidades das reações direta e inversa são iguais. c) os reatantes
ENGENHARIA QUÍMICA. COORDENADOR Cláudio Ferreira Lima cflima@ufv.br
 ENGENHARIA QUÍMICA COORDENADOR Cláudio Ferreira Lima cflima@ufv.br 228 Currículos dos Cursos do CCE UFV Engenheiro Químico ATUAÇÃO O Engenheiro Químico tem uma atuação bastante ampla, com enfoque principal
ENGENHARIA QUÍMICA COORDENADOR Cláudio Ferreira Lima cflima@ufv.br 228 Currículos dos Cursos do CCE UFV Engenheiro Químico ATUAÇÃO O Engenheiro Químico tem uma atuação bastante ampla, com enfoque principal
Soluções, concentrações e diluições
 Soluções, concentrações e diluições Mistura homogênea constituída: soluto (presente em menor quantidade) solvente (presente em maior quantidade). MASSA MOLECULAR: soma das massas atômicas de cada átomo
Soluções, concentrações e diluições Mistura homogênea constituída: soluto (presente em menor quantidade) solvente (presente em maior quantidade). MASSA MOLECULAR: soma das massas atômicas de cada átomo
Aula S16: Monitoração Ambiental e Análise Química
 QUÍMICA ANALÍTICA AMBIENTAL 1º período de 2014 Aula S16: Monitoração Ambiental e Análise Química Prof. Rafael Arromba de Sousa Departamento de Química UFJF www.ufjf.br/baccan - rafael.arromba@ufjf.edu.br
QUÍMICA ANALÍTICA AMBIENTAL 1º período de 2014 Aula S16: Monitoração Ambiental e Análise Química Prof. Rafael Arromba de Sousa Departamento de Química UFJF www.ufjf.br/baccan - rafael.arromba@ufjf.edu.br
Curvas de Solubilidade
 Curvas de Solubilidade Solução é uma mistura homogênea de duas ou mais substâncias. Para se obter uma solução, devemos ter dois componentes importantes: o soluto e o solvente. O soluto é a substância que
Curvas de Solubilidade Solução é uma mistura homogênea de duas ou mais substâncias. Para se obter uma solução, devemos ter dois componentes importantes: o soluto e o solvente. O soluto é a substância que
TÍTULO DA PRÁTICA: OPERAÇÃO DE MEDIDAS E NOTAÇÃO CIENTÍFICA
 ROTEIRO DA AULA PRÁTICA DE QUÍMICA GERAL TÍTULO DA PRÁTICA: OPERAÇÃO DE MEDIDAS E NOTAÇÃO CIENTÍFICA 1 - A incerteza na ciência A natureza intrínseca da observação científica traz consigo o fato de que
ROTEIRO DA AULA PRÁTICA DE QUÍMICA GERAL TÍTULO DA PRÁTICA: OPERAÇÃO DE MEDIDAS E NOTAÇÃO CIENTÍFICA 1 - A incerteza na ciência A natureza intrínseca da observação científica traz consigo o fato de que
Química Analítica I Tratamento dos dados analíticos Soluções analíticas
 Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
Química Analítica I Tratamento dos dados analíticos Soluções analíticas Profª Simone Noremberg Kunz 2 Mol Medidas em química analítica É a quantidade de uma espécie química que contém 6,02x10 23 partículas
DETERMINAÇÃO DA MASSA VOLÚMICA DE UM SÓLIDO
 Escola Básica dos 2º e 3º Ciclos de Santo António Ciências Físico-Químicas 2009/2010 DETERMINAÇÃO DA MASSA VOLÚMICA DE UM SÓLIDO Trabalho realizado por: Ano: Nº T: Índice Introdução 3 Objectivos.4 Material/
Escola Básica dos 2º e 3º Ciclos de Santo António Ciências Físico-Químicas 2009/2010 DETERMINAÇÃO DA MASSA VOLÚMICA DE UM SÓLIDO Trabalho realizado por: Ano: Nº T: Índice Introdução 3 Objectivos.4 Material/
Manual de Métodos de Análises de Bebidas e Vinagres
 1 MÉTODO Densimétrico 2 PRINCÍPIO Baseia-se na separação do álcool por destilação da amostra e sua posterior quantificação de acordo com a densidade relativa do destilado a 20 ºC. 3 - MATERIAL 3.1 EQUIPAMENTO
1 MÉTODO Densimétrico 2 PRINCÍPIO Baseia-se na separação do álcool por destilação da amostra e sua posterior quantificação de acordo com a densidade relativa do destilado a 20 ºC. 3 - MATERIAL 3.1 EQUIPAMENTO
Objetivos da disciplina:
 Aplicar e utilizar princípios de metrologia em calibração de instrumentos e malhas de controle. Objetivos da disciplina: Aplicar e utilizar princípios de metrologia calibração de instrumentos e malhas
Aplicar e utilizar princípios de metrologia em calibração de instrumentos e malhas de controle. Objetivos da disciplina: Aplicar e utilizar princípios de metrologia calibração de instrumentos e malhas
Escola Básica e Secundária da Calheta. Físico-Química 7.º Ano de escolaridade
 Escola Básica e Secundária da Calheta Físico-Química 7.º Ano de escolaridade Ano letivo 2015/2016 FICHA INFORMATIVA 1 Classificação dos materiais NOME: N.º TURMA DATA DA REALIZAÇÃO: / / CLASSIFICAÇÃO DOS
Escola Básica e Secundária da Calheta Físico-Química 7.º Ano de escolaridade Ano letivo 2015/2016 FICHA INFORMATIVA 1 Classificação dos materiais NOME: N.º TURMA DATA DA REALIZAÇÃO: / / CLASSIFICAÇÃO DOS
Disciplina Metodologia Analítica QUI102 1 semestre AULA 01 Profa. Maria Auxiliadora Costa Matos
 Metodologia Analítica I sem/2014 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Metodologia Analítica QUI102 1 semestre 2014
Metodologia Analítica I sem/2014 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Metodologia Analítica QUI102 1 semestre 2014
ANÁLISE QUÍMICA QUALITATIVA
 Escola Secundária do Padre António Martins Oliveira de Lagoa Técnicas Laboratoriais de Química ANÁLISE QUÍMICA QUALITATIVA Pedro Pinto Nº 14 11ºA 22/04/2004 Índice Objectivo do Trabalho... 2 Fundamentos
Escola Secundária do Padre António Martins Oliveira de Lagoa Técnicas Laboratoriais de Química ANÁLISE QUÍMICA QUALITATIVA Pedro Pinto Nº 14 11ºA 22/04/2004 Índice Objectivo do Trabalho... 2 Fundamentos
Disciplina Metodologia Analítica QUI102. I semestre AULA 01 Profa. Maria Auxiliadora Costa Matos
 Metodologia Analítica I sem/2016 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Metodologia Analítica QUI102 I semestre 2016
Metodologia Analítica I sem/2016 Profa Ma Auxiliadora - 1 Universidade Federal de Juiz de Fora Instituto de Ciências Exatas Departamento de Química Disciplina Metodologia Analítica QUI102 I semestre 2016
A.L.2.3 NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO-BASE
 A.L.2.3 NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO-BASE QUÍMICA 11.ºANO QUESTÃO-PROBLEMA Como neutralizar resíduos de ácidos/bases do laboratório de Química da escola? Como identificar se os resíduos são de uma
A.L.2.3 NEUTRALIZAÇÃO: UMA REACÇÃO DE ÁCIDO-BASE QUÍMICA 11.ºANO QUESTÃO-PROBLEMA Como neutralizar resíduos de ácidos/bases do laboratório de Química da escola? Como identificar se os resíduos são de uma
Volumetria de Neutralização Ácido-Base
 Volumetria de Neutralização Ácido-Base Preparação & Padronização de Soluções ETEC Tiquatira (SP) Professor Daniel e Professor Juarez Abril de 2012 Página 1 de 9 Volumetria de Neutralização Ácido-Base 1
Volumetria de Neutralização Ácido-Base Preparação & Padronização de Soluções ETEC Tiquatira (SP) Professor Daniel e Professor Juarez Abril de 2012 Página 1 de 9 Volumetria de Neutralização Ácido-Base 1
Currículos dos Cursos do CCE UFV ENGENHARIA QUÍMICA. COORDENADOR Antônio Marcos de Oliveira Siqueira antonio.siqueira@ufv.br
 278 Currículos dos Cursos do CCE UFV ENGENHARIA QUÍMICA COORDENADOR Antônio Marcos de Oliveira Siqueira antonio.siqueira@ufv.br UFV Catálogo de Graduação 2014 279 Engenheiro Químico ATUAÇÃO O Engenheiro
278 Currículos dos Cursos do CCE UFV ENGENHARIA QUÍMICA COORDENADOR Antônio Marcos de Oliveira Siqueira antonio.siqueira@ufv.br UFV Catálogo de Graduação 2014 279 Engenheiro Químico ATUAÇÃO O Engenheiro
www.professormazzei.com PROPREDADES COLIGATIVAS Folha 03 João Roberto Mazzei
 01. (UNESP 1989) Considerar duas soluções de ácido clorídrico e outra de ácido acético (ácido etanóico), ambas 10 2 M. Pergunta-se: a) Qual das duas soluções apresenta menor temperatura de congelação?
01. (UNESP 1989) Considerar duas soluções de ácido clorídrico e outra de ácido acético (ácido etanóico), ambas 10 2 M. Pergunta-se: a) Qual das duas soluções apresenta menor temperatura de congelação?
b) Qual é a confusão cometida pelo estudante em sua reflexão?
 1º B EM Química A Lailson Aval. Trimestral 28/03/11 1. Qual o estado físico (sólido, líquido ou gasoso) das substâncias da tabela a seguir, quando as mesmas se encontram no Deserto da Arábia, à temperatura
1º B EM Química A Lailson Aval. Trimestral 28/03/11 1. Qual o estado físico (sólido, líquido ou gasoso) das substâncias da tabela a seguir, quando as mesmas se encontram no Deserto da Arábia, à temperatura
ANEXO II DILUIÇÕES E SOLUÇÕES
 ANEXO II DILUIÇÕES E SOLUÇÕES 1. DILUIÇÕES Diluição é o procedimento de adição de uma substância a outra para reduzir a concentração de uma das substâncias. O uso mais comum da palavra diluição ocorre
ANEXO II DILUIÇÕES E SOLUÇÕES 1. DILUIÇÕES Diluição é o procedimento de adição de uma substância a outra para reduzir a concentração de uma das substâncias. O uso mais comum da palavra diluição ocorre
Átomos & Moléculas. Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica.
 Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica. SUBSTÂNCIA (Material Puro): material formado
Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica. SUBSTÂNCIA (Material Puro): material formado
C o l é g i o R i c a r d o R o d r i g u e s A l v e s
 C o l é g i o R i c a r d o R o d r i g u e s A l v e s Educação Infantil - Ensino Fundamental I - Ensino Médio 1 TRIMESTRE Química 1ª Série do Ensino Médio Conteúdo Introdução a Química Átomo Molécula
C o l é g i o R i c a r d o R o d r i g u e s A l v e s Educação Infantil - Ensino Fundamental I - Ensino Médio 1 TRIMESTRE Química 1ª Série do Ensino Médio Conteúdo Introdução a Química Átomo Molécula
Práticas de. Química Geral e Orgânica. para Engenharia Ambiental
 Apostila de Aulas Práticas de Prof. Alonso Goes Guimarães Práticas de Química Geral e Orgânica para Engenharia Ambiental Apostila de Aulas Práticas de INTRODUÇÂO A química é uma ciência experimental e
Apostila de Aulas Práticas de Prof. Alonso Goes Guimarães Práticas de Química Geral e Orgânica para Engenharia Ambiental Apostila de Aulas Práticas de INTRODUÇÂO A química é uma ciência experimental e
CENTRO PAULA SOUZA ETEC TIQUATIRA
 CENTRO PAULA SOUZA ETEC TIQUATIRA ALINE CRISTINE FERREIRA GABRIEL NOGUEIRA ALVES LUCAS EDUARDO GOMES FUNICO NAOMÍ MATSURA BRAZ ATIVIDADE DE BROMATOLOGIA (PESQUISA LISTA DE EXERCÍCIOS) SÃO PAULO 2014 LISTA
CENTRO PAULA SOUZA ETEC TIQUATIRA ALINE CRISTINE FERREIRA GABRIEL NOGUEIRA ALVES LUCAS EDUARDO GOMES FUNICO NAOMÍ MATSURA BRAZ ATIVIDADE DE BROMATOLOGIA (PESQUISA LISTA DE EXERCÍCIOS) SÃO PAULO 2014 LISTA
Aula 8 NOÇÕES DE SEGURANÇA EM LABORATÓRIO. Maria de Lara Palmeira de Macedo Arguelho Beatriz
 Aula 8 NOÇÕES DE SEGURANÇA EM LABORATÓRIO META Proporcionar ao aluno a aprendizagem das técnicas de calibração de material volumétrico através da calibração de pipetas. OBJETIVOS Ao fi nal desta aula,
Aula 8 NOÇÕES DE SEGURANÇA EM LABORATÓRIO META Proporcionar ao aluno a aprendizagem das técnicas de calibração de material volumétrico através da calibração de pipetas. OBJETIVOS Ao fi nal desta aula,
A) 11,7 gramas B) 23,4 gramas C) 58,5 gramas D) 68,4 gramas E) 136,8 gramas
 Questão 1 Sejam dadas as seguintes soluções aquosas: I) 0,2 mol/l de cloreto de potássio (KCl) II) 0,3 mol/l de glicose (C 6 H 12 O 6 ) III) 0,1 mol/l de sacarose (C 12 H 22 O 11 ) IV) 0,2 mol/l de sulfato
Questão 1 Sejam dadas as seguintes soluções aquosas: I) 0,2 mol/l de cloreto de potássio (KCl) II) 0,3 mol/l de glicose (C 6 H 12 O 6 ) III) 0,1 mol/l de sacarose (C 12 H 22 O 11 ) IV) 0,2 mol/l de sulfato
Actualmente existe uma preocupação com alguns poluentes atmosféricos, devido à sua toxicidade.
 Actualmente existe uma preocupação com alguns poluentes atmosféricos, devido à sua toxicidade. Então quando é que dizemos que um poluente tem efeito tóxico? Quando é prejudicial para os seres vivos, afectando
Actualmente existe uma preocupação com alguns poluentes atmosféricos, devido à sua toxicidade. Então quando é que dizemos que um poluente tem efeito tóxico? Quando é prejudicial para os seres vivos, afectando
http://www.oc-praktikum.de SO 4 O 2 (120.1) (138.1) (98.1) (180.2) (60.1)
 NP 5012 Síntese do ácido acetilsalicílico (aspirina) a partir do ácido salicílico e anidrido acético CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1)
NP 5012 Síntese do ácido acetilsalicílico (aspirina) a partir do ácido salicílico e anidrido acético CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1)
Sistema de Controle Acadêmico. Grade Curricular. Curso : QUÍMICA. CRÉDITOS Obrigatórios: 201 Optativos: 6. 1º Semestre
 Universidade Federal Rural do Rio de Janeiro Pró-reitoria de Graduação - DAARG DRA - Divisão de Registros Acadêmicos Sistema de Controle Acadêmico Grade Curricular 30/01/2014-13:17:07 Curso : QUÍMICA VAGAS
Universidade Federal Rural do Rio de Janeiro Pró-reitoria de Graduação - DAARG DRA - Divisão de Registros Acadêmicos Sistema de Controle Acadêmico Grade Curricular 30/01/2014-13:17:07 Curso : QUÍMICA VAGAS
INSTITUTO SUPERIOR TÉCNICO
 INSTITUTO SUPERIOR TÉCNICO Mestrado Integrado em Engenharia Biológica Laboratório de Análise Química Determinação do Ácido Acetilsalicílico num comprimido por Espectroscopia de Absorção Molecular Sílvia
INSTITUTO SUPERIOR TÉCNICO Mestrado Integrado em Engenharia Biológica Laboratório de Análise Química Determinação do Ácido Acetilsalicílico num comprimido por Espectroscopia de Absorção Molecular Sílvia
Substâncias Puras e Misturas
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES Substâncias Puras e Misturas Elementos Químicos
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES Substâncias Puras e Misturas Elementos Químicos
CURSO DE CIÊNCIAS E TECNOLOGIAS CURSO TECNOLÓGICO DE INFORMÁTICA. ENSINO SECUNDÁRIO Componente de Formação Específica
 CURSO DE CIÊNCIAS E TECNOLOGIAS CURSO TECNOLÓGICO DE INFORMÁTICA ENSINO SECUNDÁRIO Componente de Formação Específica Disciplinas de Física e Química A e Física e Química B Endereços da Internet http://www.windows.umich.edu/
CURSO DE CIÊNCIAS E TECNOLOGIAS CURSO TECNOLÓGICO DE INFORMÁTICA ENSINO SECUNDÁRIO Componente de Formação Específica Disciplinas de Física e Química A e Física e Química B Endereços da Internet http://www.windows.umich.edu/
Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos
 Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos NOME Nº Turma Informação Professor Enc. de Educação 1. Os átomos dos isótopos e do carbono têm (A) números atómicos
Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos NOME Nº Turma Informação Professor Enc. de Educação 1. Os átomos dos isótopos e do carbono têm (A) números atómicos
Química Prof. Rogério 2016. Química. Professor Rogério. Imagens meramente ilustrativas, domínio público sites diversos/internet
 Química Prof. Rogério 2016 Química Professor Rogério Imagens meramente ilustrativas, domínio público sites diversos/internet 1º MOMENTO - Propriedades básicas da matéria - Tabela periódica - Estrutura
Química Prof. Rogério 2016 Química Professor Rogério Imagens meramente ilustrativas, domínio público sites diversos/internet 1º MOMENTO - Propriedades básicas da matéria - Tabela periódica - Estrutura
Para compreender o conceito de reacção de precipitação é necessário considerar as noções básicas de dissolução e de solubilidade de sais em água.
 ESTUDO DA SOLUBILIDADE DE ALGUNS SAIS EM ÁGUA INTRODUÇÃO Para compreender o conceito de reacção de precipitação é necessário considerar as noções básicas de dissolução e de solubilidade de sais em água.
ESTUDO DA SOLUBILIDADE DE ALGUNS SAIS EM ÁGUA INTRODUÇÃO Para compreender o conceito de reacção de precipitação é necessário considerar as noções básicas de dissolução e de solubilidade de sais em água.
QUÍMICA PISM II (MÓDULO I)
 QUÍMICA PISM II (MÓDULO I) 1 - SOLUÇÕES Solução é qualquer mistura homogênea de duas ou mais substâncias. Os componentes de uma solução são chamados de soluto e de solvente: - soluto: substância dissolvida
QUÍMICA PISM II (MÓDULO I) 1 - SOLUÇÕES Solução é qualquer mistura homogênea de duas ou mais substâncias. Os componentes de uma solução são chamados de soluto e de solvente: - soluto: substância dissolvida
UNIVERSIDADE DE CUIABÁ QUIMICA GERAL DOCENTE: ADRIANO LUIZ SANTANA AULAS PRÁTICAS DE QUÍMICA GERAL. Discente:
 UNIVERSIDADE DE CUIABÁ QUIMICA GERAL DOCENTE: ADRIANO LUIZ SANTANA AULAS PRÁTICAS DE QUÍMICA GERAL Discente: AULA PRÁTICA N º VI ASSUNTO: REAÇÕES QUIMICAS OBJETIVOS: Observar as reações químicas em soluções
UNIVERSIDADE DE CUIABÁ QUIMICA GERAL DOCENTE: ADRIANO LUIZ SANTANA AULAS PRÁTICAS DE QUÍMICA GERAL Discente: AULA PRÁTICA N º VI ASSUNTO: REAÇÕES QUIMICAS OBJETIVOS: Observar as reações químicas em soluções
VI Olimpíada Norte - Nordeste de Química e
 VI Olimpíada Norte - Nordeste de Química e Seletiva para a Olimpíada Ibero-americana de Química - 2000 Exame aplicado em 27.05.2000 Somente as questões de números 1 a 6 serão consideradas na composição
VI Olimpíada Norte - Nordeste de Química e Seletiva para a Olimpíada Ibero-americana de Química - 2000 Exame aplicado em 27.05.2000 Somente as questões de números 1 a 6 serão consideradas na composição
www.professormazzei.com Estequiometria Folha 03 Prof.: João Roberto Mazzei
 01. (CFTCE 2007) Dada a reação de neutralização: HCl + NaOH NaCl + H 2O, a massa de NaCl, produzida a partir de 80 g de hidróxido de sódio (NaOH), é: a) 58,5 g b) 40 g c) 117 g d) 80 g e) 120 g 02. (CFTCE
01. (CFTCE 2007) Dada a reação de neutralização: HCl + NaOH NaCl + H 2O, a massa de NaCl, produzida a partir de 80 g de hidróxido de sódio (NaOH), é: a) 58,5 g b) 40 g c) 117 g d) 80 g e) 120 g 02. (CFTCE
ESTRUTURAS DE MADEIRA
 ESTRUTURAS DE MADEIRA PROPRIEDADES FÍSICAS DA MADEIRA AULAS 2 e 3 EDER BRITO GENERALIDADES A madeira é um material não homogêneo com muitas variações. Além disto, existem diversas espécies com diferentes
ESTRUTURAS DE MADEIRA PROPRIEDADES FÍSICAS DA MADEIRA AULAS 2 e 3 EDER BRITO GENERALIDADES A madeira é um material não homogêneo com muitas variações. Além disto, existem diversas espécies com diferentes
Universidade de São Paulo Escola Superior de Agricultura Luiz de Queiroz Departamento de Produção Vegetal
 Universidade de São Paulo Escola Superior de Agricultura Luiz de Queiroz Departamento de Produção Vegetal AVALIAÇÃO DA QUALIDADE DAS SEMENTES DE GRAMÍNEAS FORRAGEIRAS ANA D. L. C. NOVEMBRE adlcnove@usp.br
Universidade de São Paulo Escola Superior de Agricultura Luiz de Queiroz Departamento de Produção Vegetal AVALIAÇÃO DA QUALIDADE DAS SEMENTES DE GRAMÍNEAS FORRAGEIRAS ANA D. L. C. NOVEMBRE adlcnove@usp.br
Série: 2º ano. Assunto: Estequiometria
 Aluno: Série: 2º ano Assunto: Estequiometria 1) A massa de dióxido de carbono liberada na queima de 80 g de metano, quando utilizado como combustível, é: (Dados: massas molares, em g/mol: H = 1, C =12,
Aluno: Série: 2º ano Assunto: Estequiometria 1) A massa de dióxido de carbono liberada na queima de 80 g de metano, quando utilizado como combustível, é: (Dados: massas molares, em g/mol: H = 1, C =12,
PRÁTICA 03 CALIBRAÇÃO DE APARELHOS VOLUMÉTRIOS.
 PRÁTICA 03 CALIBRAÇÃO DE APARELHOS VOLUMÉTRIOS. MATERIAIS Termômetro Erlenmeyer Pipetas volumétricas de 10 e 25 ml Bureta de 25 ml Balão volumétrico de 100 ml Suporte universal e garra para bureta Balanças
PRÁTICA 03 CALIBRAÇÃO DE APARELHOS VOLUMÉTRIOS. MATERIAIS Termômetro Erlenmeyer Pipetas volumétricas de 10 e 25 ml Bureta de 25 ml Balão volumétrico de 100 ml Suporte universal e garra para bureta Balanças
Aula 9 2S 2011. Cromatografia Gasosa. Prof. Rafael Sousa
 Analítica V: Aula 9 2S 2011 Cromatografia Gasosa ATENÇÃO À SEQUENCIA DAS PRÁTICAS: Relatórios da 8ª Prática deverão ser entregues normalmente (escaninhos) Prof. Rafael Sousa Departamento de Química - ICE
Analítica V: Aula 9 2S 2011 Cromatografia Gasosa ATENÇÃO À SEQUENCIA DAS PRÁTICAS: Relatórios da 8ª Prática deverão ser entregues normalmente (escaninhos) Prof. Rafael Sousa Departamento de Química - ICE
AULA 3. Soluções: preparo e diluição. Laboratório de Química QUI OBJETIVOS
 AULA 3 Soluções: preparo e diluição OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
AULA 3 Soluções: preparo e diluição OBJETIVOS Preparar soluções a partir de reagentes sólidos e líquidos; Fazer cálculos prévios da quantidade de reagentes sólidos ou líquidos necessários para o preparo
PROPRIEDADES: Hidróxido de Sódio NaOH.
 Densidade: 2,3 g cm 3 Massa Molar: 40,01 g mol -1. Ponto de Fusão: 318ºC Ponto de Ebulição: 1390ºC PROPRIEDADES: Hidróxido de Sódio NaOH. Toxicidade: Pode causar graves queimaduras na boca, garganta e
Densidade: 2,3 g cm 3 Massa Molar: 40,01 g mol -1. Ponto de Fusão: 318ºC Ponto de Ebulição: 1390ºC PROPRIEDADES: Hidróxido de Sódio NaOH. Toxicidade: Pode causar graves queimaduras na boca, garganta e
CURSO: Farmácia DISCIPLINA: Controle de Qualidade de Medicamentos CRÉDITOS: 02 CARGA HORÁRIA: 40 horas TURNO: Diurno (Terça - feira (C/D 9h30min as
 CURSO: Farmácia DISCIPLINA: Controle de Qualidade de Medicamentos CRÉDITOS: 02 CARGA HORÁRIA: 40 horas TURNO: Diurno (Terça - feira (C/D 9h30min as 11h10min)) SEMESTRE/ANO: 2011.1 PROFESSORA: Erika Liz
CURSO: Farmácia DISCIPLINA: Controle de Qualidade de Medicamentos CRÉDITOS: 02 CARGA HORÁRIA: 40 horas TURNO: Diurno (Terça - feira (C/D 9h30min as 11h10min)) SEMESTRE/ANO: 2011.1 PROFESSORA: Erika Liz
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2
 I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
CURSINHO TRIU QUÍMICA FRENTE B
 CURSINHO TRIU QUÍMICA FRENTE B AULA 3 EXPRESSÕES DE CONCENTRAÇÃO (CONT.) E PROPRIEDADES COLIGATIVAS DATA: 01/09/2014 1) EXPRESSÕES DE CONCENTRAÇÃO (CONTINUAÇÃO) a. FRAÇÃO EM MOL Fração em mols ou fração
CURSINHO TRIU QUÍMICA FRENTE B AULA 3 EXPRESSÕES DE CONCENTRAÇÃO (CONT.) E PROPRIEDADES COLIGATIVAS DATA: 01/09/2014 1) EXPRESSÕES DE CONCENTRAÇÃO (CONTINUAÇÃO) a. FRAÇÃO EM MOL Fração em mols ou fração
ORIENTAÇÃO DE ESTUDOS
 ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 1º Ano do Ensino Médio Disciplina: Química 1. Considere a tabela a seguir, onde estão relacionados os pontos de fusão e de ebulição de algumas substâncias sob
ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 1º Ano do Ensino Médio Disciplina: Química 1. Considere a tabela a seguir, onde estão relacionados os pontos de fusão e de ebulição de algumas substâncias sob
Tratamento de Águas I
 Tratamento de Águas I Tecnologia em Gerenciamento Ambiental Prof. Dr. Eduardo Eyng QUALIDADE DAS ÁGUAS E PARÂMETROS IMPORTANTES Disponibilidade e usos da água Embora a maior parte do nosso planeta esteja
Tratamento de Águas I Tecnologia em Gerenciamento Ambiental Prof. Dr. Eduardo Eyng QUALIDADE DAS ÁGUAS E PARÂMETROS IMPORTANTES Disponibilidade e usos da água Embora a maior parte do nosso planeta esteja
Aos materiais que a Química usa como matéria-prima podemos classificá-los como:
 Sumário Módulo inicial Unidade temática 0 A sua origem, a sua constituição e a sua composição. Classificação de misturas e classificação de substâncias. Processos físicos de separação de misturas. Unidades
Sumário Módulo inicial Unidade temática 0 A sua origem, a sua constituição e a sua composição. Classificação de misturas e classificação de substâncias. Processos físicos de separação de misturas. Unidades
7. EQUILÍBRIO QUÍMICO
 Departamento de Química Inorgânica IQ / UFRJ IQG 18 / IQG 1 7. EQUILÍBRIO QUÍMICO I. INTRODUÇÃO Quando a concentração de todos os reagentes e produtos, em um sistema fechado, não variam mais com o tempo
Departamento de Química Inorgânica IQ / UFRJ IQG 18 / IQG 1 7. EQUILÍBRIO QUÍMICO I. INTRODUÇÃO Quando a concentração de todos os reagentes e produtos, em um sistema fechado, não variam mais com o tempo
Álcool Desinfetante 77ºGL (70% p/p ou 77% v/v a 15ºC)
 Álcool Desinfetante 77ºGL (70% p/p ou 77% v/v a 15ºC) O Álcool para Desinfecção deverá conter não menos que 76,9ºGL correspondente a 76,9%v/v ou 70%p/p e não mais que 81,4ºGL correspondente a 81,4%v/v
Álcool Desinfetante 77ºGL (70% p/p ou 77% v/v a 15ºC) O Álcool para Desinfecção deverá conter não menos que 76,9ºGL correspondente a 76,9%v/v ou 70%p/p e não mais que 81,4ºGL correspondente a 81,4%v/v
H 9. O Em relação à equação acima, que representa a obtenção ), é INCORRETO afirmar que: Cl 5 O C 14 + H 2
 QUÍMICA As questões 31 e 32, referem-se ao texto abaixo. RGANCLRADS Defensivos agrícolas para as indústrias. Agrotóxicos para os defensores da natureza. Pontos de vista diferentes sobre substâncias usadas
QUÍMICA As questões 31 e 32, referem-se ao texto abaixo. RGANCLRADS Defensivos agrícolas para as indústrias. Agrotóxicos para os defensores da natureza. Pontos de vista diferentes sobre substâncias usadas
c B = 25 g/l m soluto = 200 g V solução = 2,5 L ; V esfera = πr 3 F I C H A N. o 2 T E R R A E M T R A N S F O R M A Ç Ã O
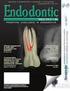 F I C H A N. o 2 T E R R A E M T R A N S F O R M A Ç Ã O Nome N. o Turma Data / / Prof. Enc. de educação 01. Considera duas soluções aquosas de sulfato de cobre, ambas de cor azul. Solução A m soluto =
F I C H A N. o 2 T E R R A E M T R A N S F O R M A Ç Ã O Nome N. o Turma Data / / Prof. Enc. de educação 01. Considera duas soluções aquosas de sulfato de cobre, ambas de cor azul. Solução A m soluto =
REVISÃO SOBRE PREPARO DE SOLUÇÕES
 Ministério da Educação UNIVERSIDADE FEDERAL DO PARANÁ Setor de Ciências da Saúde Departamento de Farmácia Disciplina de Química Medicinal Farmacêutica REVISÃO SOBRE PREPARO DE SOLUÇÕES CONCENTRAÇÃO COMUM
Ministério da Educação UNIVERSIDADE FEDERAL DO PARANÁ Setor de Ciências da Saúde Departamento de Farmácia Disciplina de Química Medicinal Farmacêutica REVISÃO SOBRE PREPARO DE SOLUÇÕES CONCENTRAÇÃO COMUM
