Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica.
|
|
|
- Vitória Back Malheiro
- 7 Há anos
- Visualizações:
Transcrição
1 Pontifícia Universidade Católica de Goiás Departamento de Biologia Prof. Hugo Henrique Pádua M.Sc. Fundamentos de Biofísica Água e Soluções
2 Água Introdução a biofísica
3 Água Introdução a biofísica
4 Água Propriedades Macroscópicas da Água 1. Densidade 2. Calor específico 3. Calor de Vaporização 4. Tensão Superficial 5. Viscosidade
5 Água Propriedades Macroscópicas da Água 1. Densidade A densidade do gelo é menor que a da água líquida
6 Água Propriedades Macroscópicas da Água 2. Calor específico Quantidade de energia térmica que deve ser fornecido a uma substância para elevar sua temperatura. A água possui calor específico muito alto 1Kcal (4,2 KJ) 1,0ºC 1 L H 2 O A água age como moderador térmico. Impedi variações bruscas que afetam o metabolismo celular.
7 Água Propriedades Macroscópicas da Água 3. Calor de vaporização Alto calor de vaporização. Desidratação de um sistema biológico Regulação da temperatura corpórea - Homeotermia Sudorese Perspiração imperceptível
8 Água Propriedades Macroscópicas da Água 4. Tensão superficial Alta coesão entre as moléculas de água
9 Água Propriedades Macroscópicas da Água 5. Viscosidade medida de resistência ao escoamento A água deveria ter alta viscosidade Dificultaria as trocas hídricas Afetaria a circulação sanguínea Mas a viscosidade da água é muito baixa
10 Água Propriedades Microscópicas da Água ( água como solvente) 1. Substâncias iônicas 2. Substâncias Covalente 3. Substâncias Anfipáticas
11 Água Natureza Polar da Molécula da Água Características Físico-químicas da água
12 Água Natureza Polar da Molécula da Água Características Físico-químicas da água Eletronegatividade
13 Água Natureza Polar da Molécula da Água Características Físico-químicas da água
14 Água Natureza Polar da Molécula da Água Características Físico-químicas da água A água é um dipolo A natureza polar da água que determina em grande parte, suas propriedades como solvente
15 Água Natureza Polar da Molécula da Água Características Físico-químicas da água
16 Água Propriedades Microscópicas da Água ( água como solvente) Eletronegatividade similar Conformação linear
17 Água Propriedades Microscópicas da Água ( água como solvente) 1. Substâncias iônicas / 2.covalente com carga Atração eletrostática Substâncias hidrofílicas
18 Água Propriedades Microscópicas da Água ( água como solvente) 2.Covalente sem carga Substâncias hidrofóbicas
19 Água Propriedades Microscópicas da Água ( água como solvente) 3. Substâncias anfipáticas
20
21
22 Soluções CONCEITO É uma mistura unifásica de mais de um componente É expressa em termos de concentração Quantidade de soluto em solução gasoso sólido líquido
23 Soluções Na solução aquosa o solvente é a água Componente dispersor SOLVENTE C = CONCENTRAÇÃO Quantidade de soluto (mol) Quantidade de solvente (L) Componente disperso SOLUTO
24 Soluções MODOS DE EXPRESSAR CONCENTRAÇÃO Porcentual. g% ou % gramas de soluto por 100mL de solução Molar. mol/l ou M mols de soluto por litro de solução Molal. W mols de soluto por kilograma de solvente
25 Soluções Percentual 200 ml de solução aquosa de NaCl a 5% g - ml 5 g - x g ml 200 ml x = 10 g de NaCl completar até 200 ml com água Q = conc. (g%) x V (ml) 100 Q = quantidade de soluto (g)
26 Soluções Molar 100 ml de solução aquosa de Glicose 0,5 mol/l MM = 180 g/mol 0,5 mol x mol x = 0,05 mol ml (1 L) 100 ml 1 mol g 0,05 mol - y g y = 9 g de Glicose completar até 100 ml com água Q = MM x M x V (L)
27 Soluções Molal 100 ml de solução aquosa de Glicose 0,5 m MM = 180 g/mol 0,5 mol x mol x = 0,05 mol ml (1 L) 100 ml 100 g 1 mol g 0,05 mol - y g y = 9 g de Glicose dissolvidos em 100 g de água 100 ml = 100 g Q = MM x M x V (g)
28 Soluções SOLUÇÕES SATURADAS E NÃO-SATURADAS O que limita a concentração é a solubilidade do soluto Não é possível fazer uma solução a 20% com um soluto que possui solubilidade de 18% Solução não-saturada Soluto presente em quantidade abaixo do limite de solubilidade Solução saturada Soluto presente em quantidade igual ao limite de solubilidade Soluções se saturam porque todas as moléculas de solvente envolvem o soluto, quando não há mais solvente para envolver o soluto forma-se corpo de fundo
29 Soluções CONCENTRAÇÃO E DILUIÇÃO Diluir é diminuir a concentração de soluto Concentrar é aumentar a concentração de soluto C 1. V 1 = C 2. V 2 C 1 = concentração inicial C 2 = concentração final V 1 = volume inicial V 2 = volume final Para obter soluções diluídas basta utilizar a relação entre as concentrações e os volumes iniciais e finais para saber quanto utilizar da solução estoque
30 Soluções CONCENTRAÇÃO E DILUIÇÃO C 1. V 1 = C 2. V 2 20 ml de uma solução de 1 mg/ml a partir de uma solução de concentração 5 mg/l (solução estoque) C 1 = 5 mg/ml C 2 = 1 mg/ml V 1 =? V 2 = 20 ml C 1. V 1 = C 2. V 2 5 mg/ml. V 1 = 1 mg/ml. 20 ml V 1 = V 1 = 4 ml 1 mg/ml. 20 ml 5 mg/ml 4 ml da solução estoque (5mg/mL) adicionados de água até completar 20 ml de volume final 4 ml da solução estoque + 16 ml de água para obter 20 ml da solução na concentração de 1 mg/ml
31 Soluções CONCENTRAÇÃO E DILUIÇÃO DIFERENÇA ENTRE DILUIÇÃO A:B E MISTURA NA PROPORÇÃO A:B Para descrever o procedimento de obtenção de uma solução de uma determinada concentração a partir da diluição de uma solução de concentração maior, duas expressões comumente usadas são diluição A:B e mistura na proporção ou razão A:B Ambas têm a mesma representação gráfica (A:B), o que causa uma certa confusão, mas têm significado químico diferente Por isso, deve-se prestar bastante atenção na palavra que antecede a notação A:B
32 Soluções CONCENTRAÇÃO E DILUIÇÃO DIFERENÇA ENTRE DILUIÇÃO A:B E MISTURA NA PROPORÇÃO A:B Diluição A:B Pegar um volume A e adicionar o solvente para obter o volume final B Volume final = B Mistura A:B Pegar um volume A e adicionar um volume B Volume final = A + B
33 Soluções CONCENTRAÇÃO E DILUIÇÃO DIFERENÇA ENTRE DILUIÇÃO A:B E MISTURA NA PROPORÇÃO A:B
34 Soluções Uma aluna está no laboratório preparando soluções para avaliar a atividade de enzimas salivares. Ela precisa de solução aquosa de NaCl na concentração de 0,9%. Entretanto, ela não dispõe do sal na forma sólida, apenas de soluções de NaCl mais concentradas. Os rótulos dos frascos contêm informações para diluição. Qual o procedimento de obtenção da solução a 0,9%? Rótulo da solução A Concentração: NaCl 3,6 %(m/v) Instrução do rótulo: diluir 1:4 com água para obter NaCl 0,9% Rótulo da solução B Concentração: NaCl 4,5 %(m/v) Instrução do rótulo: misturar com água na proporção 1:4 para obter NaCl 0,9%
35 SOLUTO LÍQUIDO Soluções Quando se fazem soluções líquido-líquido é comum indicar o volume do soluto ao invés da massa Solução de etanol a 20% (v/v)
36 Soluções MEDIDA DO VOLUME DE SOLUÇÕES Quando adicionamos soluções aquosas em provetas, buretas e pipetas, observamos que a superfície de separação entre o líquido e o ar não é plana, mas geralmente tem formato côncavo. Essa superfície é denominada menisco. A leitura do volume em tais vidrarias deve ser realizada na parte inferior do menisco.
37 Soluções Exercícios de Fixação 1.Um frasco de laboratório contém 2,0 litros de uma solução aquosa de NaCl. A massa do sal dissolvida na solução é de 120g. Que volume deve ser retirado da solução inicial para que se obtenham 30g de sal dissolvido? a) 1,0 litro b) 0,5 litro c) 0,25 litro d) 1,5 litros e) 0,75 litro 2. Um aluno dissolveu 8,70 g de NaCl (M.M. = 58 g/mol; pureza de 100%) em água destilada suficiente para preparar 100 ml de solução. Qual é a molaridade da solução? 3. Qual o volume de H 2 SO 4 18 mol/l necessário para preparar 500 ml de uma solução a 0,15 mol/l?
38 Soluções Propriedades Especiais das Soluções 1. Densidade 2. Tensão Superficial 3. Viscosidade 4. Efeito do soluto no ponto de Fusão e Ebulição 5. Difusão e Osmose
39 Soluções Propriedades Especiais das Soluções Efeito do soluto no ponto de Fusão e Ebulição Ponto de Fusão Ponto de ebulição 0ºC 100ºC <0ºC >100ºC
40 Soluções Propriedades Especiais das Soluções Difusão - Movimento espontâneo de partículas individuais, causado pela energia cinética das próprias moléculas ou íons (transporte passivo). Características da Difusão Movimento de componentes de uma mistura qualquer, de acordo com a 2º lei da termodinâmica O movimento ocorre de uma região para outra obedecendo um gradiente de concentração ( de onde tem mais para onde tem menos) Ocorrem em meios gasosos ( aroma de um perfume), Líquidos e sólidos ( pode durar até séculos ate que se note a migração de partículas)
41 Soluções Propriedades Especiais das Soluções Difusão
42 Soluções Propriedades Especiais das Soluções Difusão Fatores que influenciam a difusão Gradiente de Concentração Gradiente de pressão Tamanho da partícula Temperatura Distância Tempo Permeabilidade da membrana à substância
43 Soluções Propriedades Especiais das Soluções Difusão CONCENTRAÇÃO E PRESSÃO Quanto maior é o gradiente de concentração e pressão, mais rápida é a difusão
44 Soluções Propriedades Especiais das Soluções Difusão Tamanho da Partícula Partículas menores difundem-se mais rapidamente
45 Soluções Propriedades Especiais das Soluções Difusão Temperatura O aumento da temperatura favorece a difusão em função do aumento da energia cinética das moléculas
46 Soluções Propriedades Especiais das Soluções Difusão Distância x Tempo A difusão de solutos a longas distâncias é muito lenta período de 8 anos para uma pequena molécula com coeficiente de difusão de 10-5 cm 2 /s difundir 1 m na água apenas 0,6 s para difundir 5 μm Difusão é importante para pequenas distâncias (células)
47 Soluções Propriedades Especiais das Soluções Osmose - um caso especial de difusão Movimento espontâneo das moléculas de água A água vai para onde há maior concentração de soluto Portanto a água se move para a região onde tem menos água
48 Soluções Propriedades Especiais das Soluções Osmose - um caso especial de difusão
49 Soluções Propriedades Especiais das Soluções Osmose - um caso especial de difusão
50 Soluções Osmose das moléculas de água e difusão da glicose G H 2 O INÍCIO DURANTE EQUILÍBRIO G H 2 O X H 2 O Início: concentração de glicose A > B. Durante: ocorre osmose mais rápido que difusão das moléculas de glicose, por isso o nível de água varia. Equilíbrio: níveis e concentrações iguais. X H 2 O G H 2 O G H 2 O
51 Soluções Osmose das moléculas de água, sem difusão da macromolécula INÍCIO DURANTE EQUILÍBRIO Início: concentração diferente; pressão de solvente é menor em A. Durante: ocorre apenas osmose pois a macromolécula não permeia a membrana, por isso o nível de água varia. Equilíbrio: níveis diferentes, pressões hidrostática e osmótica iguais.
52 Soluções Osmose, sem difusão da macromolécula e difusão do sal INÍCIO DURANTE EQUILÍBRIO Início: pressão de solvente é menor em A. Durante: ocorre osmose e difusão do sal pois a macromolécula não permeia a membrana, por isso o nível de água varia. Equilíbrio: níveis diferentes, concentrações iguais em volumes diferentes (quantidades em A são maiores).
53 Soluções PRESSÃO OSMÓTICA A quantidade exata de pressão necessária para interromper a osmose é chamada de pressão osmótica da solução de soluto
54 Soluções PRESSÃO OSMÓTICA Quanto maior é a pressão osmótica de uma solução, menor é a sua concentração de água e maior a sua concentração de solutos
55 Soluções Osmolaridade Mede a quantidade de partículas existentes num determinado solvente. Nº de partículas osmoticamente ativas por litro de solução (Osmol/L), partículas estas capazes de criar gradientes osmóticos. Quanto maior a osmolaridade de uma solução, maior será a quantidade de partículas que possui, menor será a concentração de água (as partículas ocupam o espaço que seria ocupado pela água) e por isso cria maior resistência à perda de água.
56 Soluções Osmolaridade Muitas moléculas ao se dissolverem, são separadas em suas partículas constituintes, pela ação do solvente: Geralmente, as partículas separadas possuem carga elétrica, e por isso se denominam eletrólitos; Uma conseqüência direta da hidrólise é que a concentração de partículas é maiordo que a concentração de moléculas; A unidade de concentração de partículas é a osmolaridade (Osmol, osm)
57 Soluções Osmolaridade A concentração osmolar é igual à concentração Molar (Molaridade) multiplicada pelo número de partículas: Cosm = M x n. 1 mol de NaCl 1 mol de Na mol de Cl -
58 Soluções Osmose reversa A osmose inversa ou osmose reversa é um processo de separação em que um solvente é separado de um soluto por uma membrana permeável ao solvente e impermeável ao soluto. Isso ocorre quando se aplica uma grande pressão sobre este meio aquoso, o que contraria o fluxo natural da osmose.
59 Suspensões e Colóides
60 Dispersões As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância Dispersões Suspensão ou mistura grosseira Colóide Solução
61 Dispersões Introdução a biofísica
62 Soluções SOLUÇÃO - As partículas da fase dispersa: Não se sedimentam sob ação da gravidade, nem de centrífugas; Não são retidos por filtros; Não são visíveis ao microscópio.
63 Suspensões Suspensão As suspensões ou misturas grosseiras são misturas heterogêneas onde o componente que aparece em menor quantidade é denominado disperso e o componente que aparece em maior quantidade é denominado dispersante. São misturas de grandes partículas. Grandes o suficiente para serem vistas a olho nú dispersante é o equivalente ao solvente disperso é o equivalente ao soluto.
64 Suspensões Suspensão Características Gerais Consistem numa substância insolúvel dispersa em um líquido; São heterogêneas; Nãos são límpidas (são opacas); Sedimentam; Não passam através de filtros; Não passam através de membranas.
65 Suspensões Leite de magnésia hidróxido de magnésio + água Água + areia
66 Coloide Colóide (do grego kólla, cola + eîdos, forma) ou dispersões coloidais - são misturas heterogêneas onde o componente que aparece em menor quantidade é denominado disperso e o componente que aparece em maior quantidade é denominado dispergente. Em uma dispersão coloidal, as partículas do disperso possuem as seguintes características:
67 Coloide gelatina sangue leite sorvete
68 Coloide Colóides Características Gerais Consistem numa substância insolúvel dispersa em um líquido; São heterogêneas; Não se sedimentam; Passam através de filtros; Não passam através de membranas.
69 Coloide Tipos de dispersões coloidais Sol: é uma dispersão coloidal na qual o dispersante é o líquido e o disperso é o sólido, por exemplo um pouco de maizena com água. Gel: é uma dispersão coloidal na qual o dispersante é o sólido e o disperso é o líquido, por exemplo gelatina pronta e geléia.
70 Coloide Efeito Tyndall As partículas que compõem os sistemas coloidais são muito pequenas para serem identificadas a olho nu, mas o seu tamanho é maior do que o do comprimento de onda da luz visível. Por isso, uma luz que atravesse um sistema coloidal será refratada pelas partículas.
71 Coloide Efeito Tyndall Baseado nessa observação, basta apontar um feixe de luz para um sistema (geralmente líquido ou sólido) para classificá-lo. Um colóide irá dar origem a difusão pela refração do feixe nas partículas. Uma solução não altera o feixe de luz. Em uma solução coloidal autêntica, a energia interna das partículas aumenta de acordo com a intensidade da luz aplicada
72 Coloide Efeito Tyndall
73
74 Coloide Diálise - A diálise é um processo onde as substâncias em solução são separados por suas diferenças de peso molecular. Desde que a membrana porosa seletivamente permite a passagem de solutos menor, mantendo espécies de maior porte, a diálise pode ser efetivamente usada como um processo de separação com base na rejeição de tamanho. Separação de um soluto de um coloide através de uma membrana Hemodiálise
75 Coloide Hemodiálise
76
77
CURSINHO TRIU QUÍMICA FRENTE B
 CURSINHO TRIU QUÍMICA FRENTE B AULA 3 EXPRESSÕES DE CONCENTRAÇÃO (CONT.) E PROPRIEDADES COLIGATIVAS DATA: 01/09/2014 1) EXPRESSÕES DE CONCENTRAÇÃO (CONTINUAÇÃO) a. FRAÇÃO EM MOL Fração em mols ou fração
CURSINHO TRIU QUÍMICA FRENTE B AULA 3 EXPRESSÕES DE CONCENTRAÇÃO (CONT.) E PROPRIEDADES COLIGATIVAS DATA: 01/09/2014 1) EXPRESSÕES DE CONCENTRAÇÃO (CONTINUAÇÃO) a. FRAÇÃO EM MOL Fração em mols ou fração
Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada
 1 Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada 1. Questões de estudo - Como preparar uma solução aquosa de NaOH 0,1 M? - Como preparar uma solução
1 Experiência 07: Preparo de Solução a partir de Substâncias sólidas, Liquidas e de Solução Concentrada 1. Questões de estudo - Como preparar uma solução aquosa de NaOH 0,1 M? - Como preparar uma solução
É o cálculo das quantidades de reagentes e/ou produtos das reações químicas.
 Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
Estequiometria Introdução Estequiometria É derivada da palavra grega STOICHEON (elemento) e METRON (medida) significa medida dos elementos químicos", ou ainda medir algo que não pode ser dividido. É o
A) 11,7 gramas B) 23,4 gramas C) 58,5 gramas D) 68,4 gramas E) 136,8 gramas
 Questão 1 Sejam dadas as seguintes soluções aquosas: I) 0,2 mol/l de cloreto de potássio (KCl) II) 0,3 mol/l de glicose (C 6 H 12 O 6 ) III) 0,1 mol/l de sacarose (C 12 H 22 O 11 ) IV) 0,2 mol/l de sulfato
Questão 1 Sejam dadas as seguintes soluções aquosas: I) 0,2 mol/l de cloreto de potássio (KCl) II) 0,3 mol/l de glicose (C 6 H 12 O 6 ) III) 0,1 mol/l de sacarose (C 12 H 22 O 11 ) IV) 0,2 mol/l de sulfato
www.professormazzei.com PROPREDADES COLIGATIVAS Folha 03 João Roberto Mazzei
 01. (UNESP 1989) Considerar duas soluções de ácido clorídrico e outra de ácido acético (ácido etanóico), ambas 10 2 M. Pergunta-se: a) Qual das duas soluções apresenta menor temperatura de congelação?
01. (UNESP 1989) Considerar duas soluções de ácido clorídrico e outra de ácido acético (ácido etanóico), ambas 10 2 M. Pergunta-se: a) Qual das duas soluções apresenta menor temperatura de congelação?
Maria do Anjo Albuquerque
 ispersões na atmosfera Maria do Anjo Albuquerque Atmosfera A atmosfera é uma solução gasosa de vários gases (sobretudo oxigénio, dióxido de carbono e vapor de água) dispersos em azoto (componente maioritário);
ispersões na atmosfera Maria do Anjo Albuquerque Atmosfera A atmosfera é uma solução gasosa de vários gases (sobretudo oxigénio, dióxido de carbono e vapor de água) dispersos em azoto (componente maioritário);
As dispersões coloidais são compostas por dispersante e disperso. O dispersante é o equivalente ao solvente e o disperso é o equivalente ao soluto.
 Conceito Um coloide, ou dispersão coloidal, consiste numa mistura na qual uma ou mais substâncias se encontram uniformemente disseminadas (dispersas) numa outra substância, sob a forma de pequenas partículas,
Conceito Um coloide, ou dispersão coloidal, consiste numa mistura na qual uma ou mais substâncias se encontram uniformemente disseminadas (dispersas) numa outra substância, sob a forma de pequenas partículas,
Após agitação, mantendo-se a temperatura a 20ºC, coexistirão solução saturada e fase sólida no(s) tubo(s)
 01) (Covest-2006) Uma solução composta por duas colheres de sopa de açúcar (34,2g) e uma colher de sopa de água (18,0 g) foi preparada. Sabendo que: MMsacarose = 342,0g mol -1, MMágua = 18,0 g mol -1,
01) (Covest-2006) Uma solução composta por duas colheres de sopa de açúcar (34,2g) e uma colher de sopa de água (18,0 g) foi preparada. Sabendo que: MMsacarose = 342,0g mol -1, MMágua = 18,0 g mol -1,
Prof.: Eduardo Campos
 Prof.: Eduardo Campos Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância. Vejamos alguns exemplos: Ao agitar a mistura,
Prof.: Eduardo Campos Definição: As dispersões são misturas nas quais uma substância está disseminada na forma de partículas no interior de uma outra substância. Vejamos alguns exemplos: Ao agitar a mistura,
Critérios Específicos de Classificação da Questão Aula
 Critérios Específicos de da Questão Aula Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos DISCIPLINA: Física e Química Módulo: Q 05/06 0 ºAno de escolaridade Data: 3 de novembro
Critérios Específicos de da Questão Aula Curso Profissional de Técnico de Gestão e Programação de Sistemas Informáticos DISCIPLINA: Física e Química Módulo: Q 05/06 0 ºAno de escolaridade Data: 3 de novembro
GOIÂNIA, / / 2016. PROFESSORA: Núbia de Andrade. DISCIPLINA:Química SÉRIE: 2º. ALUNO(a):
 GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 2º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
GOIÂNIA, / / 2016 PROFESSORA: Núbia de Andrade DISCIPLINA:Química SÉRIE: 2º ALUNO(a): Lista de Exercícios P1 I Bimestre No Anhanguera você é + Enem Antes de iniciar a lista de exercícios leia atentamente
Transportes através da membrana plasmática. Profa Cristina Lacerda Soares Petrarolha Silva FISMA/FCAA - FEA
 Transportes através da membrana plasmática Profa Cristina Lacerda Soares Petrarolha Silva FISMA/FCAA - FEA INTRODUÇÃO A capacidade de uma membrana de ser atravessada por algumas substâncias e não por outras
Transportes através da membrana plasmática Profa Cristina Lacerda Soares Petrarolha Silva FISMA/FCAA - FEA INTRODUÇÃO A capacidade de uma membrana de ser atravessada por algumas substâncias e não por outras
Escola Básica e Secundária da Calheta. Físico-Química 7.º Ano de escolaridade
 Escola Básica e Secundária da Calheta Físico-Química 7.º Ano de escolaridade Ano letivo 2015/2016 FICHA INFORMATIVA 1 Classificação dos materiais NOME: N.º TURMA DATA DA REALIZAÇÃO: / / CLASSIFICAÇÃO DOS
Escola Básica e Secundária da Calheta Físico-Química 7.º Ano de escolaridade Ano letivo 2015/2016 FICHA INFORMATIVA 1 Classificação dos materiais NOME: N.º TURMA DATA DA REALIZAÇÃO: / / CLASSIFICAÇÃO DOS
CURSOS DE ENFERMAGEM E FARMÁCIA
 CURSOS DE ENFERMAGEM E FARMÁCIA DISCIPLINA: BIOFÍSICA Prof.a: Msd. Érica Muniz ESTRUTURAS MOLECULARES ÁGUA E SUA IMPORTANCIA BIOLÓGICA DIFUSÃO,OSMOSE E TÔNUS ÁTOMOS E MOLÉCULAS Átomo: menor estrutura neutra
CURSOS DE ENFERMAGEM E FARMÁCIA DISCIPLINA: BIOFÍSICA Prof.a: Msd. Érica Muniz ESTRUTURAS MOLECULARES ÁGUA E SUA IMPORTANCIA BIOLÓGICA DIFUSÃO,OSMOSE E TÔNUS ÁTOMOS E MOLÉCULAS Átomo: menor estrutura neutra
Colóides. 2) Indique em que fase de agregação se encontram respectivamente o disperso e o dispergente nas dispersões coloidais abaixo:
 Colóides Questionário 1) Dê a definição de dispersão coloidal e discorra sobre suas características principais em relação às partículas do disperso R= As dispersões coloidais são misturas heterogêneas
Colóides Questionário 1) Dê a definição de dispersão coloidal e discorra sobre suas características principais em relação às partículas do disperso R= As dispersões coloidais são misturas heterogêneas
Boas Práticas Laboratoriais Preparo de soluções
 Boas Práticas Laboratoriais Preparo de soluções Disciplina de Reumatologia 2011 http://www.ruf.rice.edu/~bioslabs/schedules/talks/solutions_dilutions/bioedmixtures.htm O que fazer antes do preparo Vc sabe
Boas Práticas Laboratoriais Preparo de soluções Disciplina de Reumatologia 2011 http://www.ruf.rice.edu/~bioslabs/schedules/talks/solutions_dilutions/bioedmixtures.htm O que fazer antes do preparo Vc sabe
Francisco Hevilásio F. Pereira Fisiologia Vegetal
 FISIOLOGIA VEGETAL Nutrição Mineral de plantas Parte II Pombal PB Transporte de íons na planta Transporte passivo e ativo Transporte passivo É aquele que ocorre a favor do gradiente de potencial químico
FISIOLOGIA VEGETAL Nutrição Mineral de plantas Parte II Pombal PB Transporte de íons na planta Transporte passivo e ativo Transporte passivo É aquele que ocorre a favor do gradiente de potencial químico
Curvas de Solubilidade
 Curvas de Solubilidade Solução é uma mistura homogênea de duas ou mais substâncias. Para se obter uma solução, devemos ter dois componentes importantes: o soluto e o solvente. O soluto é a substância que
Curvas de Solubilidade Solução é uma mistura homogênea de duas ou mais substâncias. Para se obter uma solução, devemos ter dois componentes importantes: o soluto e o solvente. O soluto é a substância que
Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos
 Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos NOME Nº Turma Informação Professor Enc. de Educação 1. Os átomos dos isótopos e do carbono têm (A) números atómicos
Escola Secundária de Casquilhos Teste 1 de Física e Química A 10º ANO 22/10/2013 90 minutos NOME Nº Turma Informação Professor Enc. de Educação 1. Os átomos dos isótopos e do carbono têm (A) números atómicos
Átomos & Moléculas. Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica.
 Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica. SUBSTÂNCIA (Material Puro): material formado
Átomos & Moléculas H + H H H H + H + O O H H Átomos Moléculas Definição: é uma porção de matéria que tem propriedades bem definidas e que lhe são característica. SUBSTÂNCIA (Material Puro): material formado
Concentrações. Flavia de Almeida Vieira Tatiana Dillenburg Saint Pierre
 Flavia de Almeida Vieira Tatiana Dillenburg Saint Pierre Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
Flavia de Almeida Vieira Tatiana Dillenburg Saint Pierre Este documento tem nível de compartilhamento de acordo com a licença 3.0 do Creative Commons. http://creativecommons.org.br http://creativecommons.org/licenses/by-sa/3.0/br/legalcode
CURSO APOIO QUÍMICA RESOLUÇÃO
 QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
QUÍMICA CURSO APOIO 15. O sulfato de sódio é um composto utilizado na indústria de celulose e na fabricação de detergentes. Por apresentar grande afinidade por água, pode ser encontrado na forma de um
Fisiologia Vegetal. Água Introdução. Informações gerais. 1. Constituinte mais abundante nos vegetais ex.:
 Água Introdução Fisiologia Vegetal Informações gerais 1. Constituinte mais abundante nos vegetais ex.: Planta parte % água MF Alface folha nova 94.3 Cenoura raiz madura 90.3 Batata tubérculo 79.8 Coco
Água Introdução Fisiologia Vegetal Informações gerais 1. Constituinte mais abundante nos vegetais ex.: Planta parte % água MF Alface folha nova 94.3 Cenoura raiz madura 90.3 Batata tubérculo 79.8 Coco
Lista de Exercícios. Estudo da Matéria
 FACULDADE PITÁGORAS DE BETIM Credenciada pela portaria 792, de 27 de março de 2006. Curso: Engenharia Química Lista de Exercícios Disciplina: Química Geral Semestre: 2º / 2013 Docente: Carla Soares Souza
FACULDADE PITÁGORAS DE BETIM Credenciada pela portaria 792, de 27 de março de 2006. Curso: Engenharia Química Lista de Exercícios Disciplina: Química Geral Semestre: 2º / 2013 Docente: Carla Soares Souza
I Curso de Férias em Fisiologia - UECE
 I Curso de Férias em Fisiologia - UECE Realização: Instituto Superior de Ciências Biomédicas Mestrado Acadêmico em Ciências Biológicas Apoio: 1 FISIOLOGIA CELULAR Laboratório de Eletrofisiologia 1. POTENCIAL
I Curso de Férias em Fisiologia - UECE Realização: Instituto Superior de Ciências Biomédicas Mestrado Acadêmico em Ciências Biológicas Apoio: 1 FISIOLOGIA CELULAR Laboratório de Eletrofisiologia 1. POTENCIAL
Aos materiais que a Química usa como matéria-prima podemos classificá-los como:
 Sumário Módulo inicial Unidade temática 0 A sua origem, a sua constituição e a sua composição. Classificação de misturas e classificação de substâncias. Processos físicos de separação de misturas. Unidades
Sumário Módulo inicial Unidade temática 0 A sua origem, a sua constituição e a sua composição. Classificação de misturas e classificação de substâncias. Processos físicos de separação de misturas. Unidades
Lista de Exercícios Química Geral Entropia e energia livre
 Lista de Exercícios Química Geral Entropia e energia livre 1. Se a reação A + B C tiver uma constante de equilíbrio maior do que 1, qual das seguintes indicações está correta? a) A reação não é espontânea.
Lista de Exercícios Química Geral Entropia e energia livre 1. Se a reação A + B C tiver uma constante de equilíbrio maior do que 1, qual das seguintes indicações está correta? a) A reação não é espontânea.
Propriedades coligativas: são propriedades que dependem da concentração de partículas (solutos) dissolvidas, mas não da natureza dessas partículas.
 Química Geral Aula 2 Marcelo Propriedades coligativas: são propriedades que dependem da concentração de partículas (solutos) dissolvidas, mas não da natureza dessas partículas. Em 50 C a água pura estará
Química Geral Aula 2 Marcelo Propriedades coligativas: são propriedades que dependem da concentração de partículas (solutos) dissolvidas, mas não da natureza dessas partículas. Em 50 C a água pura estará
4. SISTEMAS COLOIDAIS
 4. SISTEMAS COLOIDAIS I. INTRODUÇÃO Nas aulas práticas anteriores discutimos soluções que representam um tipo de mistura de substâncias, os quais, por não diferenciarmos mais soluto e solvente são chamados
4. SISTEMAS COLOIDAIS I. INTRODUÇÃO Nas aulas práticas anteriores discutimos soluções que representam um tipo de mistura de substâncias, os quais, por não diferenciarmos mais soluto e solvente são chamados
Aula 01 QUÍMICA GERAL
 Aula 01 QUÍMICA GERAL 1 Natureza da matéria Tales de Mileto (624-548 a. C.) Tudo é água Anaxímenes de Mileto (585-528 a. C.) Tudo provém do ar e retorna ao ar Empédocle (484-424 a. C.) As quatro raízes,
Aula 01 QUÍMICA GERAL 1 Natureza da matéria Tales de Mileto (624-548 a. C.) Tudo é água Anaxímenes de Mileto (585-528 a. C.) Tudo provém do ar e retorna ao ar Empédocle (484-424 a. C.) As quatro raízes,
PROPRIEDADES COLIGATIVAS PARTE 2
 PROPRIEDADES COLIGATIVAS PARTE 2 1. (Adaptado) Tendo em vista o momento em que um líquido se encontra em equilíbrio com seu vapor, leia atentamente as afirmativas abaixo: I. A evaporação e a condensação
PROPRIEDADES COLIGATIVAS PARTE 2 1. (Adaptado) Tendo em vista o momento em que um líquido se encontra em equilíbrio com seu vapor, leia atentamente as afirmativas abaixo: I. A evaporação e a condensação
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2
 I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
I OLIMPÍADA DE QUÍMICA DO GRANDE ABC - 13/06/2015 ENSINO MÉDIO - FASE 2 INSTRUÇÕES: 1. A prova consta de 3 questões discursivas (5 pontos cada) e de 17 questões objetivas (1 ponto cada), cada uma com 4
www.professormazzei.com SOLUÇÕES Folha 03 João Roberto Mazzei
 01. (UERJ 2008) Certos medicamentos são preparados por meio de uma série de diluições. Assim, utilizando-se uma quantidade de água muito grande, os medicamentos obtidos apresentam concentrações muito pequenas.
01. (UERJ 2008) Certos medicamentos são preparados por meio de uma série de diluições. Assim, utilizando-se uma quantidade de água muito grande, os medicamentos obtidos apresentam concentrações muito pequenas.
Soluções, concentrações e diluições
 Soluções, concentrações e diluições Mistura homogênea constituída: soluto (presente em menor quantidade) solvente (presente em maior quantidade). MASSA MOLECULAR: soma das massas atômicas de cada átomo
Soluções, concentrações e diluições Mistura homogênea constituída: soluto (presente em menor quantidade) solvente (presente em maior quantidade). MASSA MOLECULAR: soma das massas atômicas de cada átomo
Modelos atômicos. Modelo de Bohr
 Modelos atômicos Modelo de Bohr O modelo de Bohr apresenta limitações significativas, não servindo para explicar vários dos fenômenos nos quais estão envolvidos elétrons. As deficiências do modelo de Bohr
Modelos atômicos Modelo de Bohr O modelo de Bohr apresenta limitações significativas, não servindo para explicar vários dos fenômenos nos quais estão envolvidos elétrons. As deficiências do modelo de Bohr
Classificação Solução Colóide Suspensão Exemplo: açúcar na água, sal de cozinha na água, álcool hidratado.
 Química - Unidade 5 de 12: GOVERNO DO ESTADO DE MATO GROSSO DO SUL Conteúdo 10: Dispersões (definição,classificação, e características) Habilidade e competência: Identificar a diferença entre dispersões,
Química - Unidade 5 de 12: GOVERNO DO ESTADO DE MATO GROSSO DO SUL Conteúdo 10: Dispersões (definição,classificação, e características) Habilidade e competência: Identificar a diferença entre dispersões,
Água e óleo. Solução de CuSO 4. Qual dos sistemas é uma dispersão? Por que?
 Solução de CuSO 4 Água e óleo Por que? Qual dos sistemas é uma dispersão? Solução de CuSO 4 Disperso Dispersante Sistema Distribuição uniforme de partículas Dispersão Os constituintes de uma substância
Solução de CuSO 4 Água e óleo Por que? Qual dos sistemas é uma dispersão? Solução de CuSO 4 Disperso Dispersante Sistema Distribuição uniforme de partículas Dispersão Os constituintes de uma substância
Aula 11 Mudança de Estado Físico Questões Atuais Vestibulares de SP
 1. (Fuvest 011) Um forno solar simples foi construído com uma caixa de isopor, forrada internamente com papel alumínio e fechada com uma tampa de vidro de 40 cm x 50 cm. Dentro desse forno, foi colocada
1. (Fuvest 011) Um forno solar simples foi construído com uma caixa de isopor, forrada internamente com papel alumínio e fechada com uma tampa de vidro de 40 cm x 50 cm. Dentro desse forno, foi colocada
A forma geral de uma equação de estado é: p = f ( T,
 Aula: 01 Temática: O Gás Ideal Em nossa primeira aula, estudaremos o estado mais simples da matéria, o gás, que é capaz de encher qualquer recipiente que o contenha. Iniciaremos por uma descrição idealizada
Aula: 01 Temática: O Gás Ideal Em nossa primeira aula, estudaremos o estado mais simples da matéria, o gás, que é capaz de encher qualquer recipiente que o contenha. Iniciaremos por uma descrição idealizada
1 Seleccionar material adequado à separação dos componentes de uma mistura heterogénea.
 ACTIVIDADE LABORATORIAL Ciências Físico-Químicas 7ºANO VOU SEPARAR OS COMPONENTES DE UMA MISTURA O que se pretende 1 Seleccionar material adequado à separação dos componentes de uma mistura heterogénea.
ACTIVIDADE LABORATORIAL Ciências Físico-Químicas 7ºANO VOU SEPARAR OS COMPONENTES DE UMA MISTURA O que se pretende 1 Seleccionar material adequado à separação dos componentes de uma mistura heterogénea.
b) Qual é a confusão cometida pelo estudante em sua reflexão?
 1º B EM Química A Lailson Aval. Trimestral 28/03/11 1. Qual o estado físico (sólido, líquido ou gasoso) das substâncias da tabela a seguir, quando as mesmas se encontram no Deserto da Arábia, à temperatura
1º B EM Química A Lailson Aval. Trimestral 28/03/11 1. Qual o estado físico (sólido, líquido ou gasoso) das substâncias da tabela a seguir, quando as mesmas se encontram no Deserto da Arábia, à temperatura
PROBLEMAS DE TERMOLOGIA
 PROBLEMAS DE TERMOLOGIA 1 - Numa estação meteorológica, foi registrada uma temperatura máxima de 25ºC. Qual é a indicação da máxima na escala Fahrenheit? 2 - Numa escala termométrica X, marca-se -10ºX
PROBLEMAS DE TERMOLOGIA 1 - Numa estação meteorológica, foi registrada uma temperatura máxima de 25ºC. Qual é a indicação da máxima na escala Fahrenheit? 2 - Numa escala termométrica X, marca-se -10ºX
DISPERSÕES. Profa. Kátia Aquino
 DISPERSÕES Profa. Kátia Aquino O que é uma dispersão do ponto de vista químico? Mistura de duas ou mais substâncias, em que as partículas de uma fase a fase dispersa se encontram distribuidas em outra
DISPERSÕES Profa. Kátia Aquino O que é uma dispersão do ponto de vista químico? Mistura de duas ou mais substâncias, em que as partículas de uma fase a fase dispersa se encontram distribuidas em outra
Aulas: 1, 2 e 3. 4. Qual será a massa de uma amostra de 150 ml de urina, sabendo-se que sua densidade é 1,085 g.ml -1?
 Lista de Exercícios Professor: Igor Saburo Suga Serie: Nome: Aulas: 1, 2 e 3 Ano: n⁰ 1. Transforme as massas em gramas: a) 0,20 kg; b) 200 mg; c) 1x10-3 kg; d)5,0 x 10 2 mg 2. Transforme os volumes em
Lista de Exercícios Professor: Igor Saburo Suga Serie: Nome: Aulas: 1, 2 e 3 Ano: n⁰ 1. Transforme as massas em gramas: a) 0,20 kg; b) 200 mg; c) 1x10-3 kg; d)5,0 x 10 2 mg 2. Transforme os volumes em
Escola Secundária de Lagoa. Ficha de Trabalho 4. Física e Química A 11º Ano Turma A Paula Melo Silva. Revisão 10º Ano: As três miudinhas
 Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 4 Cálculos estequiométricos Parte Um Revisão 10º Ano: As três miudinhas Quantidade em química corresponde
Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 4 Cálculos estequiométricos Parte Um Revisão 10º Ano: As três miudinhas Quantidade em química corresponde
EQUILÍBRIO QUÍMICO: é o estado de um sistema reacional no qual não ocorrem variações na composição do mesmo ao longo do tempo.
 IV INTRODUÇÃO AO EQUILÍBRIO QUÍMICO IV.1 Definição EQUILÍBRIO QUÍMICO: é o estado de um sistema reacional no qual não ocorrem variações na composição do mesmo ao longo do tempo. Equilíbrio químico equilíbrio
IV INTRODUÇÃO AO EQUILÍBRIO QUÍMICO IV.1 Definição EQUILÍBRIO QUÍMICO: é o estado de um sistema reacional no qual não ocorrem variações na composição do mesmo ao longo do tempo. Equilíbrio químico equilíbrio
t 1 t 2 Tempo t 1 t 2 Tempo
 Concentração 01)Uma reação química atinge o equilíbrio químico quando: a) ocorre simultaneamente nos sentidos direto e inverso. b) as velocidades das reações direta e inversa são iguais. c) os reatantes
Concentração 01)Uma reação química atinge o equilíbrio químico quando: a) ocorre simultaneamente nos sentidos direto e inverso. b) as velocidades das reações direta e inversa são iguais. c) os reatantes
Reacções de precipitação
 Reacções de precipitação Ocorre uma reacção de precipitação quando se forma uma precipitado, ou seja, um sólido insolúvel que se separa da solução. Na precipitação a partir de soluções aquosas normalmente
Reacções de precipitação Ocorre uma reacção de precipitação quando se forma uma precipitado, ou seja, um sólido insolúvel que se separa da solução. Na precipitação a partir de soluções aquosas normalmente
7. EQUILÍBRIO QUÍMICO
 Departamento de Química Inorgânica IQ / UFRJ IQG 18 / IQG 1 7. EQUILÍBRIO QUÍMICO I. INTRODUÇÃO Quando a concentração de todos os reagentes e produtos, em um sistema fechado, não variam mais com o tempo
Departamento de Química Inorgânica IQ / UFRJ IQG 18 / IQG 1 7. EQUILÍBRIO QUÍMICO I. INTRODUÇÃO Quando a concentração de todos os reagentes e produtos, em um sistema fechado, não variam mais com o tempo
Propriedades térmicas em Materiais
 FACULDADE SUDOESTE PAULISTA Ciência e Tecnologia de Materiais Prof. Msc. Patrícia Correa Propriedades térmicas em Materiais Noções importantes para entendermos os mecanismos de transporte através dos materiais
FACULDADE SUDOESTE PAULISTA Ciência e Tecnologia de Materiais Prof. Msc. Patrícia Correa Propriedades térmicas em Materiais Noções importantes para entendermos os mecanismos de transporte através dos materiais
Átomos Moléculas Íons Biomoléculas. Matéria é formada por Átomos. Obs.: teoria confirmada apenas no início do século XX.
 Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
Átomos Moléculas Íons Biomoléculas Estrutura da Matéria Matéria é formada por Átomos Obs.: teoria confirmada apenas no início do século XX. Os átomos dificilmente existem livres e possuem grande tendência
ATIVIDADE DE ÁGUA (Aw) E REAÇÕES DE DETERIORAÇÃO
 ATIVIDADE DE ÁGUA (Aw) E REAÇÕES DE DETERIORAÇÃO Água A molécula de água é triatômica e possui estrutura tetraédrica. Tem baixo peso molecular, pequeno volume e é diamagnética. Apresentaria um ângulo de
ATIVIDADE DE ÁGUA (Aw) E REAÇÕES DE DETERIORAÇÃO Água A molécula de água é triatômica e possui estrutura tetraédrica. Tem baixo peso molecular, pequeno volume e é diamagnética. Apresentaria um ângulo de
Membranas Biológicas. Profª Eleonora Slide de aula
 Membranas Biológicas Profª Eleonora Slide de aula Membranas Biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
Membranas Biológicas Profª Eleonora Slide de aula Membranas Biológicas Todas as células possuem na sua periferia uma membrana, a qual fornece a barreira necessária que separa o lado interno do lado externo.
tem-se no equilíbrio que 1 mol de HCl reagiu com 1 mol de NaOH, ou seja: n(hcl) = n(naoh)
 Experiência 8: TITULAÇÕES ÁCIDO-BASE 1. Objetivos Após a realização desta atividade experimental, espera-se que o aluno seja capaz de: - Determinar a concentração de um ácido e uma base por titulação.
Experiência 8: TITULAÇÕES ÁCIDO-BASE 1. Objetivos Após a realização desta atividade experimental, espera-se que o aluno seja capaz de: - Determinar a concentração de um ácido e uma base por titulação.
Aula 16 A Regra das Fases
 Aula 16 A Regra das Fases 1. Introdução Poderíamos especular se quatro fases de uma única substância poderiam estar em equilíbrio (como, por exemplo, as duas formas sólidas do estanho, o estanho líquido
Aula 16 A Regra das Fases 1. Introdução Poderíamos especular se quatro fases de uma única substância poderiam estar em equilíbrio (como, por exemplo, as duas formas sólidas do estanho, o estanho líquido
Unidade 2 Substâncias e átomos
 Unidade 2 Substâncias e átomos Substâncias Puras pág. 51 A matéria é composta por uma ou mais substâncias químicas. Porém, é difícil saber se um corpo é composto por uma única substância ou por uma mistura
Unidade 2 Substâncias e átomos Substâncias Puras pág. 51 A matéria é composta por uma ou mais substâncias químicas. Porém, é difícil saber se um corpo é composto por uma única substância ou por uma mistura
PROPRIEDADES: Hidróxido de Sódio NaOH.
 Densidade: 2,3 g cm 3 Massa Molar: 40,01 g mol -1. Ponto de Fusão: 318ºC Ponto de Ebulição: 1390ºC PROPRIEDADES: Hidróxido de Sódio NaOH. Toxicidade: Pode causar graves queimaduras na boca, garganta e
Densidade: 2,3 g cm 3 Massa Molar: 40,01 g mol -1. Ponto de Fusão: 318ºC Ponto de Ebulição: 1390ºC PROPRIEDADES: Hidróxido de Sódio NaOH. Toxicidade: Pode causar graves queimaduras na boca, garganta e
Aluno(a): Nº. Professor: Série: 1 Disciplina: Data da prova:
 Lista de Exercícios Aluno(a): Nº. Professor: Série: 1 Disciplina: Data da prova: 1. (UFAC) O gráfico abaixo mostra a curva de aquecimento para o clorofórmio, usualmente utilizado como solvente para lipídeos.
Lista de Exercícios Aluno(a): Nº. Professor: Série: 1 Disciplina: Data da prova: 1. (UFAC) O gráfico abaixo mostra a curva de aquecimento para o clorofórmio, usualmente utilizado como solvente para lipídeos.
Série: 2º ano. Assunto: Estequiometria
 Aluno: Série: 2º ano Assunto: Estequiometria 1) A massa de dióxido de carbono liberada na queima de 80 g de metano, quando utilizado como combustível, é: (Dados: massas molares, em g/mol: H = 1, C =12,
Aluno: Série: 2º ano Assunto: Estequiometria 1) A massa de dióxido de carbono liberada na queima de 80 g de metano, quando utilizado como combustível, é: (Dados: massas molares, em g/mol: H = 1, C =12,
VI Olimpíada Norte - Nordeste de Química e
 VI Olimpíada Norte - Nordeste de Química e Seletiva para a Olimpíada Ibero-americana de Química - 2000 Exame aplicado em 27.05.2000 Somente as questões de números 1 a 6 serão consideradas na composição
VI Olimpíada Norte - Nordeste de Química e Seletiva para a Olimpíada Ibero-americana de Química - 2000 Exame aplicado em 27.05.2000 Somente as questões de números 1 a 6 serão consideradas na composição
Volumetria de Neutralização Ácido-Base
 Volumetria de Neutralização Ácido-Base 1 O que é um Processo de Titulação? A Titulação é uma operação analítica utilizada em análises volumétricas com o objetivo de determinar a Concentração de soluções.
Volumetria de Neutralização Ácido-Base 1 O que é um Processo de Titulação? A Titulação é uma operação analítica utilizada em análises volumétricas com o objetivo de determinar a Concentração de soluções.
Substâncias Puras e Misturas
 MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES Substâncias Puras e Misturas Elementos Químicos
MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES Substâncias Puras e Misturas Elementos Químicos
Termologia. Ramo da física que estuda o. relacionados.
 Termologia Termologia Ramo da física que estuda o calor e os fenômenos relacionados. TEMPERATURA ATemperatura é uma grandeza física que mede o nível de agitaçãodas partículas (átomos ou moléculas) que
Termologia Termologia Ramo da física que estuda o calor e os fenômenos relacionados. TEMPERATURA ATemperatura é uma grandeza física que mede o nível de agitaçãodas partículas (átomos ou moléculas) que
Obtenção de matéria pelos seres heterotróficos transportes transmembranares
 Obtenção de matéria pelos seres heterotróficos transportes transmembranares 1 Processos de transporte A membrana plasmática pode facilitar, dificultar ou impedir a passagem de substâncias, uma propriedade
Obtenção de matéria pelos seres heterotróficos transportes transmembranares 1 Processos de transporte A membrana plasmática pode facilitar, dificultar ou impedir a passagem de substâncias, uma propriedade
QUÍMICA Tipos de soluções Edson Mesquita
 QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
QUÍMICA Tipos de soluções Edson Mesquita 1 Soluções Uma solução é uma mistura homogênea de substâncias puras (átomos, moléculas ou íons) na qual não há precipitação. Substância pura: substância com composição
Água na atmosfera. Capítulo 5 - Ahrens
 Água na atmosfera Capítulo 5 - Ahrens Propriedades da água Estados Físicos Única substântica natural que ocorre naturalmente nos três estados sobre a superfície da terra Capacidade Térmica Mais alta se
Água na atmosfera Capítulo 5 - Ahrens Propriedades da água Estados Físicos Única substântica natural que ocorre naturalmente nos três estados sobre a superfície da terra Capacidade Térmica Mais alta se
Água, Soluções e Suspensões.
 Água, Soluções e Suspensões. A água é a molécula mais abundante nos seres vivos. Cerca de 75% de um adulto. No planeta não existem seres vivos sem água. Fases da água: Sólida Líquida Gasosa Na dependência
Água, Soluções e Suspensões. A água é a molécula mais abundante nos seres vivos. Cerca de 75% de um adulto. No planeta não existem seres vivos sem água. Fases da água: Sólida Líquida Gasosa Na dependência
Água e Soluções Biológicas
 Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Biofísica Água e Soluções Biológicas 1. Introdução 2. A estrutura da molécula de água 2.1.
Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Biofísica Água e Soluções Biológicas 1. Introdução 2. A estrutura da molécula de água 2.1.
GERAL I. Fonte de consultas: http://dequi.eel.usp.br/domingos. Email: giordani@dequi.eel.usp.br. Telefone: 3159-5142
 QUÍMICA GERAL I Fonte de consultas: http://dequi.eel.usp.br/domingos Email: giordani@dequi.eel.usp.br Telefone: 3159-5142 QUÍMICA GERAL I Unidade 1 Princípios Elementares em Química O estudo da química
QUÍMICA GERAL I Fonte de consultas: http://dequi.eel.usp.br/domingos Email: giordani@dequi.eel.usp.br Telefone: 3159-5142 QUÍMICA GERAL I Unidade 1 Princípios Elementares em Química O estudo da química
c B = 25 g/l m soluto = 200 g V solução = 2,5 L ; V esfera = πr 3 F I C H A N. o 2 T E R R A E M T R A N S F O R M A Ç Ã O
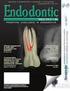 F I C H A N. o 2 T E R R A E M T R A N S F O R M A Ç Ã O Nome N. o Turma Data / / Prof. Enc. de educação 01. Considera duas soluções aquosas de sulfato de cobre, ambas de cor azul. Solução A m soluto =
F I C H A N. o 2 T E R R A E M T R A N S F O R M A Ç Ã O Nome N. o Turma Data / / Prof. Enc. de educação 01. Considera duas soluções aquosas de sulfato de cobre, ambas de cor azul. Solução A m soluto =
Colégio Saint Exupéry
 Colégio Saint Exupéry Apostila QUÍMICA No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas
Colégio Saint Exupéry Apostila QUÍMICA No nosso dia-a-dia o ato de classificar as coisas é algo corriqueiro. Em um faqueiro colocamos em um mesmo espaço as facas, em outro os garfos, etc. Agrupar coisas
Biologia Professor Leandro Gurgel de Medeiros
 Biologia Professor Leandro Gurgel de Medeiros Aula 02: Biologia Celular (Membrana Plásmática) Biologia celular é o ramo da biologia que estuda as células no que diz respeito à sua estrutura, suas funções
Biologia Professor Leandro Gurgel de Medeiros Aula 02: Biologia Celular (Membrana Plásmática) Biologia celular é o ramo da biologia que estuda as células no que diz respeito à sua estrutura, suas funções
Resolução: Resposta: D. Resolução: Resposta: B.
 45 Em química, uma solução apresenta, como característica importante, a: A presença de soluto e de solvente na mesma concentração em quantidade de matéria. B propriedade de dispersar a luz. C ocorrência
45 Em química, uma solução apresenta, como característica importante, a: A presença de soluto e de solvente na mesma concentração em quantidade de matéria. B propriedade de dispersar a luz. C ocorrência
A ÁLISE TITRIMÉTRICA
 A ÁLISE TITRIMÉTRICA Análise titrimétrica - O termo análise titrimétrica refere-se à análise química quantitativa feita pela determinação do volume de uma solução, cuja concentração é conhecida com exatidão,
A ÁLISE TITRIMÉTRICA Análise titrimétrica - O termo análise titrimétrica refere-se à análise química quantitativa feita pela determinação do volume de uma solução, cuja concentração é conhecida com exatidão,
Resolução do Exame de Física e Química A 11.º ano, 2009, 2.ª fase, 14 de Julho de 2009.
 Resolução do Exame de Física e Química A.º ano, 009,.ª fase, 4 de Julho de 009. ivisão de Educação da Sociedade Portuguesa de Física....... [Por exemplo...] A destilação da água do mar é um processo de
Resolução do Exame de Física e Química A.º ano, 009,.ª fase, 4 de Julho de 009. ivisão de Educação da Sociedade Portuguesa de Física....... [Por exemplo...] A destilação da água do mar é um processo de
ORIENTAÇÃO DE ESTUDOS
 ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 1º Ano do Ensino Médio Disciplina: Química 1. Considere a tabela a seguir, onde estão relacionados os pontos de fusão e de ebulição de algumas substâncias sob
ORIENTAÇÃO DE ESTUDOS RECUPERAÇÃO SEMESTRAL 1º Ano do Ensino Médio Disciplina: Química 1. Considere a tabela a seguir, onde estão relacionados os pontos de fusão e de ebulição de algumas substâncias sob
P2 - PROVA DE QUÍMICA GERAL - 08/10/07
 P2 - PRVA DE QUÍMICA GERAL - 08/10/07 Nome: Nº de Matrícula: GABARIT Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 R = 8,314 J mol -1 K -1 = 0,0821 atm L mol
P2 - PRVA DE QUÍMICA GERAL - 08/10/07 Nome: Nº de Matrícula: GABARIT Turma: Assinatura: Questão Valor Grau Revisão 1 a 2,5 2 a 2,5 3 a 2,5 4 a 2,5 Total 10,0 R = 8,314 J mol -1 K -1 = 0,0821 atm L mol
SUBSTÂNCIAS, MISTURAS E SEPARAÇÃO DE MISTURAS
 NOTAS DE AULA (QUÍMICA) SUBSTÂNCIAS, MISTURAS E SEPARAÇÃO DE MISTURAS PROFESSOR: ITALLO CEZAR 1 INTRODUÇÃO A química é a ciência da matéria e suas transformações, isto é, estuda a matéria. O conceito da
NOTAS DE AULA (QUÍMICA) SUBSTÂNCIAS, MISTURAS E SEPARAÇÃO DE MISTURAS PROFESSOR: ITALLO CEZAR 1 INTRODUÇÃO A química é a ciência da matéria e suas transformações, isto é, estuda a matéria. O conceito da
Solução. Tipos de Soluções
 Solução Uma solução é uma mistura homogênea de um soluto (substância a ser dissolvida) distribuída através de um solvente (substância que efetua a dissolução). Quando temos uma mistura heterogênea, suas
Solução Uma solução é uma mistura homogênea de um soluto (substância a ser dissolvida) distribuída através de um solvente (substância que efetua a dissolução). Quando temos uma mistura heterogênea, suas
1.2. Os alunos colocaram sobrecargas sobre o paralelepípedo, para averiguar se a intensidade da força de atrito depende:
 Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 24 Global 1. Numa segunda série de ensaios, os alunos colocaram sobrecargas sobre o paralelepípedo e abandonaram
Escola Secundária de Lagoa Física e Química A 11º Ano Turma A Paula Melo Silva Ficha de Trabalho 24 Global 1. Numa segunda série de ensaios, os alunos colocaram sobrecargas sobre o paralelepípedo e abandonaram
Massa é a grandeza física que mede quanto de matéria possui um corpo ou objeto. Ocupar lugar no espaço significa ter volume.
 Matéria é tudo que tem massa e ocupa lugar no espaço Massa é a grandeza física que mede quanto de matéria possui um corpo ou objeto. Ocupar lugar no espaço significa ter volume. Como exemplos de matéria
Matéria é tudo que tem massa e ocupa lugar no espaço Massa é a grandeza física que mede quanto de matéria possui um corpo ou objeto. Ocupar lugar no espaço significa ter volume. Como exemplos de matéria
ELETROQUÍMICA: PILHAS ELETRÓLISE
 ELETROQUÍMICA: PILHAS ELETRÓLISE Profa. Adélia Química Aplicada HISTÓRICO 1800 ALESSANDRO VOLTA Ele empilhou pequenos discos de zinco e cobre, separando-os com pedaços de um material poroso (feltro) embebidos
ELETROQUÍMICA: PILHAS ELETRÓLISE Profa. Adélia Química Aplicada HISTÓRICO 1800 ALESSANDRO VOLTA Ele empilhou pequenos discos de zinco e cobre, separando-os com pedaços de um material poroso (feltro) embebidos
Física 2 - Termodinâmica
 Física 2 - Termodinâmica Calor e Temperatura Criostatos de He 3-272.85 C Termodinâmica Energia Térmica Temperatura, Calor, Entropia... Máquinas Térmicas : Refrigeradores, ar-condicionados,... Física Térmica
Física 2 - Termodinâmica Calor e Temperatura Criostatos de He 3-272.85 C Termodinâmica Energia Térmica Temperatura, Calor, Entropia... Máquinas Térmicas : Refrigeradores, ar-condicionados,... Física Térmica
4ª AULA PRÁTICA DE FÍSICA MÉDICA
 4ª AULA PRÁTICA DE FÍSICA MÉDICA Porque será que não respiramos simplesmente pela pele? I. Resolva as seguintes questões: a) A partir da Lei de Fick para um fluxo de partículas por unidade de área e de
4ª AULA PRÁTICA DE FÍSICA MÉDICA Porque será que não respiramos simplesmente pela pele? I. Resolva as seguintes questões: a) A partir da Lei de Fick para um fluxo de partículas por unidade de área e de
Membrana celular: Transporte
 Membrana celular: Transporte Processos de Transporte Transporte em grande quantidade Transporte de íons e moléculas 1 Processos de Transporte: Transporte de íons e moléculas Qual a importância da manutenção
Membrana celular: Transporte Processos de Transporte Transporte em grande quantidade Transporte de íons e moléculas 1 Processos de Transporte: Transporte de íons e moléculas Qual a importância da manutenção
Lista de Exercícios Estequiometria
 Lista de Exercícios Estequiometria Átomos e Mols de Átomos Fonte: Química Geral, Vol. 1 John B. Russel 1. Calcule a massa atômica do elemento X, dado que 2,02 x l0 6 átomos de X têm uma massa de 1,70 x
Lista de Exercícios Estequiometria Átomos e Mols de Átomos Fonte: Química Geral, Vol. 1 John B. Russel 1. Calcule a massa atômica do elemento X, dado que 2,02 x l0 6 átomos de X têm uma massa de 1,70 x
Capítulo 12. Tipos de Soluções. Unidades de Concentração Efeito da Temperatura na Solubilidade Efeito da Pressão na Solubilidade de Gases
 Capítulo 12 Propriedades Físicas das Soluções Tipos de Soluções Perspectiva Molecular do Processo de Dissolução Unidades de Concentração Efeito da Temperatura na Solubilidade Efeito da Pressão na Solubilidade
Capítulo 12 Propriedades Físicas das Soluções Tipos de Soluções Perspectiva Molecular do Processo de Dissolução Unidades de Concentração Efeito da Temperatura na Solubilidade Efeito da Pressão na Solubilidade
Química Inorgânica Aula 3
 Química Inorgânica Aula 3 Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira LIGAÇÕES QUÍMICAS O que são Ligações Químicas? São as ligações que se estabelecem entre a união de dois átomos.
Química Inorgânica Aula 3 Orientadora: Drª Karla Vieira Professor Monitor: Gabriel Silveira LIGAÇÕES QUÍMICAS O que são Ligações Químicas? São as ligações que se estabelecem entre a união de dois átomos.
Eletroquímica. Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química
 Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Eletroquímica Professora: Melissa Soares Caetano Disciplina QUI 702 Eletroquímica estuda as relações
Universidade Federal de Ouro Preto Instituto de Ciências Exatas e Biológicas Departamento de Química Eletroquímica Professora: Melissa Soares Caetano Disciplina QUI 702 Eletroquímica estuda as relações
C o l é g i o R i c a r d o R o d r i g u e s A l v e s
 C o l é g i o R i c a r d o R o d r i g u e s A l v e s Educação Infantil - Ensino Fundamental I - Ensino Médio 1 TRIMESTRE Química 1ª Série do Ensino Médio Conteúdo Introdução a Química Átomo Molécula
C o l é g i o R i c a r d o R o d r i g u e s A l v e s Educação Infantil - Ensino Fundamental I - Ensino Médio 1 TRIMESTRE Química 1ª Série do Ensino Médio Conteúdo Introdução a Química Átomo Molécula
FÍSICO-QUÍMICA TERMOQUÍMICA Aula 1
 FÍSICO-QUÍMICA TERMOQUÍMICA Aula 1 A termoquímica é parte da termodinâmica e corresponde ao segmento da química que compreende as trocas de calor e seus efeitos nas substâncias e reações químicas. Os primeiros
FÍSICO-QUÍMICA TERMOQUÍMICA Aula 1 A termoquímica é parte da termodinâmica e corresponde ao segmento da química que compreende as trocas de calor e seus efeitos nas substâncias e reações químicas. Os primeiros
AS SOLUÇÕES. Soluções, colóides e suspensões. disperso), se distribui de maneira uniforme ao longo
 AS SOLUÇÕES Solução é um tipo mistura chamada de dispersão na qual uma substância, sob forma de pequenas partículas ( disperso), se distribui de maneira uniforme ao longo de toda a extensão de uma outra
AS SOLUÇÕES Solução é um tipo mistura chamada de dispersão na qual uma substância, sob forma de pequenas partículas ( disperso), se distribui de maneira uniforme ao longo de toda a extensão de uma outra
Potencial hidrogeniônico e hidroxiliônico - ph e poh
 Potencial hidrogeniônico e hidroxiliônico - ph e poh 01. (Fuvest) Coloca-se em um recipiente de vidro água destilada, gotas de solução de fenolftaleína e, em seguida, pedaços de sódio metálico: Observa-se,
Potencial hidrogeniônico e hidroxiliônico - ph e poh 01. (Fuvest) Coloca-se em um recipiente de vidro água destilada, gotas de solução de fenolftaleína e, em seguida, pedaços de sódio metálico: Observa-se,
Concurso de Seleção 2004 NÚMERO DE INSCRIÇÃO - QUÍMICA
 QUÍMICA QUESTÃO 21 Muitas pessoas já ouviram falar de gás hilariante. Mas será que ele é realmente capaz de provocar o riso? Na verdade, essa substância, o óxido nitroso (N 2 O), descoberta há quase 230
QUÍMICA QUESTÃO 21 Muitas pessoas já ouviram falar de gás hilariante. Mas será que ele é realmente capaz de provocar o riso? Na verdade, essa substância, o óxido nitroso (N 2 O), descoberta há quase 230
Polaridade e Geometria Molecular
 Polaridade e Geometria Molecular Prof. Leandro Zatta Prof. Leandro Zatta 1 Conceitos Prof. Leandro Zatta 2 Eletronegatividade Polaridade de ligação Momentos de dipolo Geometria molecular Modelo de ligação
Polaridade e Geometria Molecular Prof. Leandro Zatta Prof. Leandro Zatta 1 Conceitos Prof. Leandro Zatta 2 Eletronegatividade Polaridade de ligação Momentos de dipolo Geometria molecular Modelo de ligação
GRAVIMETRIA. Profa. Lilian Silva
 GRAVIMETRIA Profa. Lilian Silva Agente precipitante Gravimetria separação filtração secagem/ calcinação amostra pesagem precipitado cálculos Gravimetria É o processo de isolar e de pesar um elemento, ou
GRAVIMETRIA Profa. Lilian Silva Agente precipitante Gravimetria separação filtração secagem/ calcinação amostra pesagem precipitado cálculos Gravimetria É o processo de isolar e de pesar um elemento, ou
Laboratório de Física I. Experiência 3 Determinação do coeficiente de viscosidade de líquidos. 26 de janeiro de 2016
 4310256 Laboratório de Física I Experiência 3 Determinação do coeficiente de viscosidade de líquidos 1 o semestre de 2016 26 de janeiro de 2016 3. Determinação do coeficiente de viscosidade de líquidos
4310256 Laboratório de Física I Experiência 3 Determinação do coeficiente de viscosidade de líquidos 1 o semestre de 2016 26 de janeiro de 2016 3. Determinação do coeficiente de viscosidade de líquidos
FICHA (IN)FORMATIVA Nº 3 Biologia e Geologia Módulo 2. Célula
 FICHA (IN)FORMATIVA Nº 3 Biologia e Geologia Módulo 2 A célula e o transporte transmembranar Célula Teoria celular a célula é a unidade estrutural e funcional de todos os organismos; as novas células formam-se
FICHA (IN)FORMATIVA Nº 3 Biologia e Geologia Módulo 2 A célula e o transporte transmembranar Célula Teoria celular a célula é a unidade estrutural e funcional de todos os organismos; as novas células formam-se
Capítulo 4: Análise de Sistemas - 1ª e 2ª Leis da Termodinâmica
 Capítulo 4: Análise de Sistemas - 1ª e ª Leis da Termodinâmica A primeira lei da termodinâmica Alguns casos particulares Primeira lei em um ciclo termodinâmico Exercícios Primeira lei da termodinâmica
Capítulo 4: Análise de Sistemas - 1ª e ª Leis da Termodinâmica A primeira lei da termodinâmica Alguns casos particulares Primeira lei em um ciclo termodinâmico Exercícios Primeira lei da termodinâmica
COMPORTAMENTO DOS GASES - EXERCÍCIOS DE FIXAÇÃO E TESTES DE VESTIBULARES
 www.agraçadaquímica.com.br COMPORTAMENTO DOS GASES - EXERCÍCIOS DE FIXAÇÃO E TESTES DE VESTIBULARES 1. (UNIPAC-96) Um mol de gás Ideal, sob pressão de 2 atm, e temperatura de 27ºC, é aquecido até que a
www.agraçadaquímica.com.br COMPORTAMENTO DOS GASES - EXERCÍCIOS DE FIXAÇÃO E TESTES DE VESTIBULARES 1. (UNIPAC-96) Um mol de gás Ideal, sob pressão de 2 atm, e temperatura de 27ºC, é aquecido até que a
