H C. A substituição de um átomo de H no etano com outro átomo de C e mais três átomos de H produz o propano, C3H8: H C
|
|
|
- Micaela de Carvalho Rios
- 8 Há anos
- Visualizações:
Transcrição
1 Estruturas orgânicas APÊDIE epresentamos as moléculas orgânicas da natureza como as estruturas da Figura 2.2. Este apêndice apresenta uma breve revisão dos princípios da estrutura molecular dos compostos orgânicos, para auxiliar o leitor a interpretar os diagramas estruturais encontrados neste livro. idrocarbonetos; alcanos s hidrocarbonetos são compostos orgânicos que contêm somente carbono e hidrogênio. carbono possui quatro elétrons de valência (os elétrons de valência estão na parte externa da camada de eletrônica e estão disponíveis para o compartilhamento com outros átomos), que podem ser compartilhados com até quatro outros átomos. Esses elétrons compartilhados constituem as ligações químicas. Eles são a cola que mantém a molécula unida. hidrocarboneto mais simples é o 4, metano, o principal componente do gás natural. carbono também pode compartilhar elétrons com outros átomos de carbono. Se substituirmos um dos átomos de no metano por um átomo de e adicionarmos mais três átomos de, o resultado é o etano, 26, cuja estrutura pode ser representada traçando-se linhas entre os átomos que compartilham elétrons: A substituição de um átomo de no etano com outro átomo de e mais três átomos de produz o propano, 38: s próximos membros dessa série de moléculas são butano, 410, pentano, 512, hexano, 614 e assim por diante. ada vez que um átomo de é adicionado, o mesmo acontece com dois átomos de ; a fórmula geral para essa série, denominada alcanos, é n2n+2. adeias ramificadas; isômeros Entretanto, quando chegamos ao butano, há duas formas de arranjarmos as ligações: ou quarto átomo de pode ser adicionado ao final da cadeia de três átomos de ou no meio. As duas moléculas possuem a mesma fórmula química, mas, como o arranjo da ligação difere, elas apresentam diferentes propriedades físicas (por exemplo, diferentes pontos de fusão e ebulição) e químicas (diferente reatividade). São chamadas de isômeros. primeiro isômero é denominado de n-butano (n- para normal ; todos os alcanos de cadeia linear carregam esse prefixo) e o segundo, de isobutano.
2 À medida que o número de átomos de aumenta, o número de isômeros possíveis cresce rapidamente. Para fazer a distinção entre esses isômeros, foi desenvolvido um esquema sistemático de nomenclatura. nome se baseia na cadeia mais longa de átomos de na molécula, e a posição da substituição de uma cadeia mais curta é numerada com origem no final da cadeia mais longa. Por exemplo, o nome sistemático para o isobutano é 2-metilpropano, porque a cadeia mais longa possui três átomos de, e o segundo átomo de dessa cadeia carrega um grupo metila. sufixo il indica um fragmento em que uma ligação a um átomo de é substituída por uma ligação com o restante da molécula, ou seja: 3 metano 3 metila É conveniente juntar os átomos de com os átomos de, aos quais eles estão ligados, tornando implícitas as ligações. utro exemplo de um hidrocarboneto de cadeia ramificada é o 2,2,4-trimetilpentano: Essa molécula, também chamada de iso-octano, é um isômero de n-octano. As propriedades de combustão do iso-octano definem a escala de octanagem da qualidade da gasolina. s n-alcanos são moléculas de cadeia linear, e os seus isômeros são moléculas de cadeia ramificada. s organismos produzem hidrocarbonetos de cadeia linear como os principais componentes de gorduras e lipídios. As gorduras são moléculas de armazenamento de energia, e os lipídios são os blocos de construção das membranas biológicas. onseqüentemente, o petróleo contém uma proporção considerável de hidrocarbonetos de cadeia linear. Mas ele também contém muitos hidrocarbonetos de cadeia ramificada, porque as condições de altas pressão e temperatura dos depósitos geológicos induzem ao rearranjo das ligações. Esse processo é deliberadamente contínuo nos reatores químicos das refinarias de petróleo, visto que os hidrocarbonetos com cadeias ramificadas possuem classificação de octanagem mais elevada do que os de cadeias lineares. 3 Anéis o processo de ligar os átomos de entre si, é possível formar anéis, além de cadeias. Podemos ter: ciclopropano ciclobutano ciclopentano e assim por diante. s anéis também podem ser unidos para formar as moléculas policíclicas. Um exemplo disso é o marcador molecular biológico, bacterio-hopanotetrol (veja a Figura 2.2), que possui quatro anéis de seis membros e um anel de cinco membros, além de uma cadeia de sete carbonos. Essa molécula complexa é produzida pelas bactérias, mas os animais também produzem moléculas policíclicas, tal como o colesterol ( ): s números indicam as posições dos 27 carbonos; nem todas as ligações são mostradas: os carbonos 3, 6, 8, 9, 14, 17, 20 e 25 são, cada qual, ligados a um único hidrogênio; os carbonos 1, 2, 4, 7, 11, 12, 15, 16, 22, 23 e 24 são ligados a dois hidrogênios; os carbonos 18, 19, 21, 26 e 27 são ligados a três hidrogênios; os carbonos 5, 10 e 13 não possuem ligação. 2 Química ambiental
3 esolução de problema A.1 Isômeros de pentano Quantos isômeros de pentano existem? Desenhe e nomeie-os. Um isômero é obviamente o n-pentano de cadeia linear: utro isômero é obtido inserindo-se um grupo metila no meio de uma cadeia de quatro átomos de : Esse é o 2-metilbutano (note que não importa qual dos dois átomos de no meio está ligado aos grupos metila, porque se obtém a mesma molécula girando-se a estrutura). Finalmente, os dois grupos metila podem estar ligados ao do meio de uma cadeia de três : Esse é o 2,2-dimetilpropano. utro nome, igualmente descritivo, seria tetrametilmetano, o qual identifica que essa molécula pode se derivar do 4 substituindo-se todos os quatro átomos de por grupos metila. ão há outra maneira de combinar as moléculas com a fórmula pentano possui três isômeros. idrocarbonetos insaturados carbono pode compartilhar dois ou três de seus quatro elétrons de valência por vez, formando ligações duplas ou triplas (simbolizadas por linhas duplas ou triplas, e ). hidrocarboneto mais simples com uma ligação dupla é o eteno (comumente chamado de etileno), 2 2, e o mais simples com uma ligação tripla é o etino (chamado de acetileno),. s átomos de nesses alcenos e alcinos mais simples podem ser substituídos por átomos de para formar moléculas mais complexas. Por exemplo, substituir um átomo de em etileno e acetileno por um grupo metila produz o propeno (geralmente chamado de propileno), 2 3, e propino, 3, respectivamente. Se há duas ou mais ligações duplas ou triplas, temos um poli-eno ou poli-ino. As moléculas com ligações ou são considerados insaturados, porque os átomos de não possuem o complemento integral dos quatro possíveis parceiros de ligação. Estamos todos familiarizados com os óleos de cozinha insaturados e poliinsaturados, porque podem contribuir menos do que os óleos saturados para as doenças cardíacas. s óleos insaturados contêm moléculas de gordura com uma ligação dupla em suas cadeias de hidrocarboneto, e os óleos poliinsaturados possuem duas ou mais ligações duplas em uma cadeia. Forma molecular As moléculas insaturadas diferem das moléculas saturadas na forma, porque os ângulos da ligação diferem. s pares de elétrons na camada de valência tentam se manter o mais distante possível um do outro. Desse modo, se um átomo de possui quatro parceiros de ligação, as ligações se estendem para os quatro cantos de um tetraedro (ângulos de ligação de 109,5º). Mas, se há uma ligação dupla, os dois pares de elétron na ligação são forçados a ocupar a mesma região no espaço e juntos permanecem o mais distante possível dos outros dois pares de elétrons nas ligações simples. As três ligações, uma dupla e duas simples, apontam para os cantos de um triângulo eqüilátero (ângulos de ligação de aproximadamente 120º). resultado é que a unidade com dois carbonos, com suas ligações simples associadas, é planar. Portanto, o etileno pode ser representado como: Apêndice Estruturas orgânicas 3
4 Analogamente, os elétrons em uma ligação tripla ficam o mais distante possível do par nas ligações simples restantes, produzindo um ângulo de ligação de 180º. Uma ligação tripla é colinear com as ligações simples associadas; o acetileno pode ser representado como: utro importante aspecto geométrico é a facilidade de rotação em torno de uma ligação. A rotação é fácil em torno das ligações simples; as partes da molécula conectadas por uma ligação única podem adotar várias orientações intercambiáveis. ontudo, a rotação em torno de uma ligação dupla é difícil; isso só ocorre sob temperaturas muito elevadas. onseqüentemente, há duas orientações separadas para as partes da molécula conectadas por uma ligação dupla, tais como: 3 3 cis-2-buteno ou 3 3 trans-2-buteno Essas duas orientações são chamadas de cis e trans (grupos metila do mesmo lado ou em lados opostos da ligação dupla). omo a ligação dupla não gira, trata-se de isômeros geométricos, que possuem propriedades físicas e químicas diferentes porque suas formas são diferentes. epresentações da estrutura do carbono Para reduzir a desordem nos diagramas estruturais orgânicos, pode-se simplesmente representar a estrutura do carbono como uma série de linhas interconectadas. Por exemplo, o n-octano e o iso-octano podem se representados como: n-octano e iso-octano s átomos de e estão implícitos nessas representações. Subentende-se que as linhas conectam os átomos de, que possuem tantas ligações quantas forem necessárias para completar seu complemento de quatro ligações. A dobra entre as linhas representa o fato de que os átomos saturados de possuem ângulos de ligação tetraédricos. Quando a estrutura de carbono contém ligações duplas ou triplas, isso é indicado por linhas duplas ou triplas traçadas no ponto apropriado. cis-2-buteno 2-butino ote que as linhas são colineares para o 2-butino, por causa dos ângulos de ligação de 180º. Às vezes, a representação da estrutura é utilizada com parte dos átomos de mantidos para fins de clareza, assim como na estrutura de colesterol. esolução de Problema A.2 Estruturas de nome Denomine os seguintes compostos com base nas representações das estruturas: cis-3-hexeno 2-metil-trans-3-penteno ote que essas duas moléculas têm o mesmo número de átomos e ; elas são isômeros. icloexeno 1,3-cicloexadieno As ligações são sempre cis em uma estrutura anelar, por isso essa designação é dispensável. 4 Química ambiental
5 ompostos aromáticos Quando o anel com seis membros possui três ligações duplas, um tipo diferente de molécula, o benzeno, é formado. As ligações duplas podem ser representadas de duas formas alternativas, porém equivalentes: benzeno ormalmente, as ligações duplas são mais curtas do que as ligações simples, mas no benzeno todas as seis ligações de carbono-carbono apresentam o mesmo comprimento. s elétrons acabam adotando ambas as combinações de ligações ao mesmo tempo, um fenômeno denominado ressonância (e indicado pela seta de duas pontas acima desenhada). Em geral, representamos essa situação inscrevendo um círculo no anel. Em virtude da ressonância, a molécula de benzeno é mais estável e menos reativa do que se poderia esperar de uma molécula com três ligações duplas. s átomos de hidrogênio no benzeno podem ser substituídos por átomos de carbono, fazendo surgir uma grande classe de moléculas chamada (por razões históricas) de moléculas aromáticas. Por exemplo, o metilbenzeno, também chamado de tolueno, é um solvente comum: 3 tolueno A molécula de lignina na Figura 2.4 é uma molécula aromática muito complexa. Quando dois ou mais átomos de no benzeno são substituídos, a possibilidade de isômeros aumenta novamente. Por exemplo, há três isômeros de xileno, a molécula obtida pela substituição de dois grupos metila no benzeno: o- m- p- Eles são designados como orto-, meta- e para-, abreviados como o-, m- e p- (os nomes sistemáticos, contudo, são 1,2-, 1,3- e 1,4-dimetilbenzeno). Quando uma molécula de benzeno se liga a uma molécula orgânica maior, ela é chamada de grupo fenila. Por exemplo, o inseticida DDT é o diclorodifeniltricloroetano. Assim como no caso dos anéis saturados nos alcanos policíclicos, é possível unir os anéis de benzeno para formar os hidrocarbonetos aromáticos policíclicos [PA], por exemplo: naftaleno antraceno Esses PAs constituem subprodutos de combustão incompleta. São motivos de preocupação como potentes carcinógenos. PA mais comum é a grafite, cuja estrutura é uma lâmina contínua de anéis de benzeno (veja a Figura 2.4). eteroátomos; grupos funcionais s compostos orgânicos se baseiam no carbono e no hidrogênio, mas geralmente contêm átomos de outros elementos, coletivamente conhecidos como heteroátomos. s elementos mais comumente encontrados são halogêneos, oxigênio, nitrogênio, enxofre e fósforo. Freqüentemente, esses heteroátomos são locais de reatividade química, e os grupos químicos que os Apêndice Estruturas orgânicas 5
6 contêm são chamados de grupos funcionais (veja a Tabela A.1). As ligações duplas e triplas também constituem grupos funcionais; seus elétrons são ligados mais frouxamente do que os das ligações simples, tornando-os mais reativos. s átomos de halogêneo formam somente uma ligação e podem, em princípio, ser substituídos por qualquer dos átomos de em um hidrocarboneto. símbolo geral para os organo-halogenados é X, onde X representa F, l, Br ou I; e representa o restante da molécula orgânica. s organo-halogenados são geralmente menos reativos do que o hidrocarboneto original. Essa é uma das razões de os pesticidas à base de organoclorados, tal como o DDT, representarem uma preocupação ambiental. Em razão de sua baixa reatividade, duram muito e podem se acumular nos tecidos do organismo animal, até mesmo do humano. s átomos de oxigênio formam duas ligações covalentes, como ocorre na 2. Se um átomo de forma uma ligação com um átomo de, bem como com um átomo de, obtemos um álcool, simbolizado por. s álcoois são nomeados acrescentando-se ol ao final do nome da molécula orgânica. álcool ingerível é o álcool etílico, ou etanol, 3 2. A molécula complexa na Figura 2.2 é designada como bacterio-hopanotetrol por causa dos quatro grupos de álcool que contém. TABELA A.1 Grupos funcionais orgânicos selecionados. ome da classe Grupo funcional Estrutura geral de classe* Alcano enhum Alceno Alcino aleto X (X = F, l, Br, I) X Álcool Éter Aldeído etona Amina Imina itrilo Ácido carboxílico Éster Amida *Em algumas classes,, e podem ser. 6 Química ambiental
7 Se o átomo de é ligado a dois átomos de, temos um éter,. Fazemos a distinção entre e porque os dois fragmentos orgânicos que estão conectados ao átomo de não precisam ser iguais. Um exemplo é: metil-terc-butil éter abreviado como MTBE (o -terc representa terciário e o terc-butil é uma forma de designar um grupo de quatro carbonos, em que todas as ligações que partem do átomo conector de seguem para outros átomos de ). Atualmente, o MTBE é utilizado como aditivo da gasolina com o propósito de reduzir a poluição, mas ganhou notoriedade por causa da contaminação de lençóis freáticos por vazamentos de gasolina. ote que a estrutura de lignina (veja a Figura 2.4) possui muitos grupos de álcool e éter. átomo de também pode formar uma ligação dupla com um átomo de, e o grupo resultante é chamado de carbonila. s compostos de carbonila se distinguem pelo que está ligado ao átomo de. As cetonas possuem dois outros átomos de, e os aldeídos possuem um átomo de e um átomo de. s exemplos comuns são: 3 3 acetona utros grupos funcionais são os ácidos carboxílicos e os ésteres: e 3 acetaldeído ácido orgânico éster A química do grupo carbonila é consideravelmente alterada quando se tem um grupo ou ligado ao átomo de. s poliésteres constituem uma importante classe de moléculas de polímero em que os hidrocarbonetos são ligados repetindo-se os grupos éster em longas cadeias. São amplamente utilizados em tecidos e recipientes de plástico. Finalmente, dois átomos de oxigênio podem compartilhar uma ligação simples, enquanto cada um deles possui outra ligação simples com ou com. São os peróxidos, com a fórmula geral. Se um dos grupos for o, temos um hidroxiperóxido; o membro mais simples da família,, é o peróxido de hidrogênio. A ligação é fraca, e os peróxidos são uma classe reativa de moléculas. Eles desempenham um papel importante na química da poluição. omo o enxofre está no mesmo grupo da tabela periódica que o oxigênio, as mesmas regras de valência se aplicam e grupos funcionais similares são encontrados tanto no enxofre orgânico quanto nos compostos orgânicos de oxigênio. Entretanto, por ser um átomo maior, ele é capaz de ter mais do que oito elétrons em sua camada de valência quando se combina com elementos altamente necessitados de elétrons (eletronegativos), tais como oxigênio e flúor. s átomos de oxigênio podem prontamente se somar aos compostos orgânicos de enxofre, produzindo sulfonas, 2 S, sulfóxidos, 2 S 2 ou ácidos sulfônicos, S 3. Embora muito menos abundantes do que o oxigênio nos tecidos biológicos, o enxofre é um componente significativo do carvão e do petróleo, além de ser um importante fator de contribuição para a poluição atmosférica, quando esses combustíveis fósseis são queimados. s compostos com três ligações a um átomo de são as aminas. Além da amônia, 3, incluem as aminas primárias, 2, aminas secundárias,, e aminas terciárias,,,. s compostos com de dupla ligação são as iminas,, (os s também podem ser ), e os compostos com de tripla ligação são os nitrilos,. Uma classe importante de compostos é o das amidas, na qual um átomo de é conectado ao átomo de de um grupo carbonila: s polímeros de poliamida (por exemplo, náilon) são importantes como fibras e plásticos, e as moléculas de proteína, que possuem aminoácidos ligados de uma ponta a outra por conexões de amida são as próprias poliamidas da natureza. Apêndice Estruturas orgânicas 7
8 2 fósforo está no mesmo grupo que o nitrogênio na tabela periódica e os análogos de fósforo das aminas são as fosfinas. Entretanto, o fósforo forma ligações muito mais fortes com o oxigênio do que com o carbono ou o hidrogênio. a natureza, os átomos de P estão sempre cercados por átomos de. A forma mais comum é o íon fosfato, P, que pode se condensar em íons fosfato, tal como o tripolifosfato, ao formar ligações P P. Muitas moléculas biológicas importantes são os ésteres de fosfato, P ; os ácidos nucléicos são polímeros mantidos unidos por ligações de fosfodiéster, P 2. 8 Química ambiental
Ensino Médio Química QUÍMICA 30 ano
 QUÍMICA 3 0 ano CADEIAS CARBÔNICAS QUÍMICA ORGÂNICA orgânica é o ramo da química que estuda os compostos de carbono. O carbono pertence ao segundo período, grupo IVA da tabela periódica. 6C 12 1s 2 2s
QUÍMICA 3 0 ano CADEIAS CARBÔNICAS QUÍMICA ORGÂNICA orgânica é o ramo da química que estuda os compostos de carbono. O carbono pertence ao segundo período, grupo IVA da tabela periódica. 6C 12 1s 2 2s
Hidrocarbonetos. Alcenos (C n H 2n ) ligações duplas geometria triângular plana em cada C
 Hidrocarbonetos Saturados Insaturados Alcanos (C n H 2n+2 ) ligações simples geometria tetraédrica em cada C Alcenos (C n H 2n ) ligações duplas geometria triângular plana em cada C Alcinos (C n H 2n 2
Hidrocarbonetos Saturados Insaturados Alcanos (C n H 2n+2 ) ligações simples geometria tetraédrica em cada C Alcenos (C n H 2n ) ligações duplas geometria triângular plana em cada C Alcinos (C n H 2n 2
Estrutura Eletrônica e Ligação Aula 2. QO-427 Prof. J. Augusto
 Estrutura Eletrônica e Ligação Aula 2 QO-427 Prof. J. Augusto Química Orgânica Orgânica até meados de 1800 referia-se a compostos de fontes com vida ( fontes minerais eram inorgânicos ) Wöhler em 1828
Estrutura Eletrônica e Ligação Aula 2 QO-427 Prof. J. Augusto Química Orgânica Orgânica até meados de 1800 referia-se a compostos de fontes com vida ( fontes minerais eram inorgânicos ) Wöhler em 1828
Reações orgânicas. Mestranda: Daniele Potulski Disciplina: Química da Madeira I
 Reações orgânicas Mestranda: Daniele Potulski Disciplina: Química da Madeira I Introdução Quase todos os compostos orgânicos tem moléculas apolares ou com baixa polaridade; Essa característica é um fator
Reações orgânicas Mestranda: Daniele Potulski Disciplina: Química da Madeira I Introdução Quase todos os compostos orgânicos tem moléculas apolares ou com baixa polaridade; Essa característica é um fator
FCAV/UNESP. DISCIPLINA: Química Orgânica. ASSUNTO: Hidrocarbonetos
 FCAV/UNESP DISCIPLINA: Química Orgânica ASSUNTO: Hidrocarbonetos HIDROCARBONETOS São compostos orgânicos formados exclusivamente por átomos de carbono e de hidrogênio. Subdivisões: HIDROCARBONETOS Podem
FCAV/UNESP DISCIPLINA: Química Orgânica ASSUNTO: Hidrocarbonetos HIDROCARBONETOS São compostos orgânicos formados exclusivamente por átomos de carbono e de hidrogênio. Subdivisões: HIDROCARBONETOS Podem
01) Considere as seguintes substâncias: e as seguintes funções químicas: a ácido carboxílico.
 01) onsidere as seguintes substâncias: I) 3 e as seguintes funções químicas: a ácido carboxílico. B álcool. aldeído. II) III) IV) 3 3 3 D cetona. E éster. F éter. A opção que associa corretamente as substâncias
01) onsidere as seguintes substâncias: I) 3 e as seguintes funções químicas: a ácido carboxílico. B álcool. aldeído. II) III) IV) 3 3 3 D cetona. E éster. F éter. A opção que associa corretamente as substâncias
E.E. Nossa Senhora da Penha. 3º ano do Ensino Médio Química Orgânica Prof. Willian
 E.E. ossa Senhora da Penha 3º ano do Ensino Médio Química rgânica Prof. Willian Química rgânica: é o ramo da Química que estuda os compostos que contém carbono, chamados compostos orgânicos. Tem carbono
E.E. ossa Senhora da Penha 3º ano do Ensino Médio Química rgânica Prof. Willian Química rgânica: é o ramo da Química que estuda os compostos que contém carbono, chamados compostos orgânicos. Tem carbono
AULA PRÁTICA DE SALA DE AULA FQA - Espécies maioritárias e vestigiais 10º ANO 8 fev. 2013
 AULA PRÁTICA DE SALA DE AULA FQA - Espécies maioritárias e vestigiais 10º ANO 8 fev. 2013 / Nome: nº 1. Atualmente, a troposfera é constituída por espécies maioritárias, como o azoto, N 2, o oxigénio,
AULA PRÁTICA DE SALA DE AULA FQA - Espécies maioritárias e vestigiais 10º ANO 8 fev. 2013 / Nome: nº 1. Atualmente, a troposfera é constituída por espécies maioritárias, como o azoto, N 2, o oxigénio,
LIGAÇÕES INTERATÔMICAS
 UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
UNIDADE 2 - LIGAÇÕES INTERATÔMICAS 2.1. FORÇAS DE LIGAÇÃO FORTES Importante conhecer-se as atrações que mantêm os átomos unidos formando os materiais sólidos. Por exemplo, uma peça de cobre contém 8,4x10
Ligações Químicas. Profª. Drª Narlize Silva Lira. Agosto /2014
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Ligações Químicas Profª. Drª Narlize Silva Lira Agosto /2014 A Química Orgânica e a Vida A química orgânica
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Ligações Químicas Profª. Drª Narlize Silva Lira Agosto /2014 A Química Orgânica e a Vida A química orgânica
Prof. César Lourenço
 Prof. ésar Lourenço Prof. ésar Lourenço + l l ouve a troca do IDROGÊNIO pelo LORO REAÇÃO DE SUBSTITUIÇÃO É quando um átomo ou grupo de átomos é substituído por um radical do outro reagente. l + l l + LUZ
Prof. ésar Lourenço Prof. ésar Lourenço + l l ouve a troca do IDROGÊNIO pelo LORO REAÇÃO DE SUBSTITUIÇÃO É quando um átomo ou grupo de átomos é substituído por um radical do outro reagente. l + l l + LUZ
Reações Orgânicas parte II: Adição, oxidação e redução. Profa. Kátia Aquino
 Reações Orgânicas parte II: Adição, oxidação e redução Profa. Kátia Aquino 1. Reação de adição A reação de adição ocorre em compostos insaturados como alcenos e alcinos. Importante salientar que a dupla
Reações Orgânicas parte II: Adição, oxidação e redução Profa. Kátia Aquino 1. Reação de adição A reação de adição ocorre em compostos insaturados como alcenos e alcinos. Importante salientar que a dupla
= 0 molécula. cada momento dipolar existente na molécula. Lembrando que u R
 Lista de Exercícios de Geometria e Ligações 1) Numere a segunda coluna (estruturas geométricas) de acordo com a primeira coluna (compostos químicos). 1. NH 3 ( ) linear 2. CO 2 ( ) angular 3. H 2 O ( )
Lista de Exercícios de Geometria e Ligações 1) Numere a segunda coluna (estruturas geométricas) de acordo com a primeira coluna (compostos químicos). 1. NH 3 ( ) linear 2. CO 2 ( ) angular 3. H 2 O ( )
Exercícios de Aprendizagem
 UFMS/CPCS AGRONOMIA Disciplina: Química Orgânica Professora Matildes Blanco LISTA -EXERCÍCIOS REFERENTE À AVALIAÇÃO 01 (P1) Exercícios de Aprendizagem 01) Escreva as fórmulas estruturais e moleculares
UFMS/CPCS AGRONOMIA Disciplina: Química Orgânica Professora Matildes Blanco LISTA -EXERCÍCIOS REFERENTE À AVALIAÇÃO 01 (P1) Exercícios de Aprendizagem 01) Escreva as fórmulas estruturais e moleculares
TD de química orgânica. Assunto: isomeria ( 2º ano) Professor: Jorge Luiz. 1) Os compostos etanol e éter dimetílico demonstram que caso de isomeria?
 TD de química orgânica Assunto: isomeria ( 2º ano) Professor: Jorge Luiz Assunto: Isomeria Plana 1) Os compostos etanol e éter dimetílico demonstram que caso de isomeria? a) Cadeia. b) Posição. c) Compensação.
TD de química orgânica Assunto: isomeria ( 2º ano) Professor: Jorge Luiz Assunto: Isomeria Plana 1) Os compostos etanol e éter dimetílico demonstram que caso de isomeria? a) Cadeia. b) Posição. c) Compensação.
COLÉGIO NOSSA SENHORA DE LOURDES PROFESSOR WLADIMIR CAMILLO
 Química orgânica I) BREVE HISTÓRICO: COLÉGIO NOSSA SENHORA DE LOURDES PROFESSOR WLADIMIR CAMILLO 1777 Bergman Primeira separação da Química Orgânica e Inorgânica. Química Inorgânica: estuda os compostos
Química orgânica I) BREVE HISTÓRICO: COLÉGIO NOSSA SENHORA DE LOURDES PROFESSOR WLADIMIR CAMILLO 1777 Bergman Primeira separação da Química Orgânica e Inorgânica. Química Inorgânica: estuda os compostos
QUIMICA ORGÂNICA BÁSICA
 QUIMICA ORGÂNICA BÁSICA Hibridização Revisão - Química Orgânica Básica 1 Tabela Periódica 2 Moléculas Diatômicas 3 Moléculas Poliatômicas 4 Eletronegatividade 5 A interação da luz e a matéria 6 Hibridização
QUIMICA ORGÂNICA BÁSICA Hibridização Revisão - Química Orgânica Básica 1 Tabela Periódica 2 Moléculas Diatômicas 3 Moléculas Poliatômicas 4 Eletronegatividade 5 A interação da luz e a matéria 6 Hibridização
QUÍMICA 2C2H2 5O2 4CO2 2H2O. Prof. Rodolfo
 QUÍMICA Prof. Rodolfo 1. Considere a tabela abaixo, em que H c representa a entalpia de combustão para os compostos listados, a 25 C: Nome IUPAC Nome usual Estado físico (25 C) ΔHc kj/mol Etanol Álcool
QUÍMICA Prof. Rodolfo 1. Considere a tabela abaixo, em que H c representa a entalpia de combustão para os compostos listados, a 25 C: Nome IUPAC Nome usual Estado físico (25 C) ΔHc kj/mol Etanol Álcool
Resolução da Prova de Química Vestibular Verão UERGS/2003 Prof. Emiliano Chemello
 Fácil Resolução da Prova de Química Vestibular Verão UERGS/2003 Prof. Emiliano Chemello Médio www.quimica.net/emiliano emiliano@quimica.net Difícil Níveis de dificuldade das Questões 01. Em um frasco,
Fácil Resolução da Prova de Química Vestibular Verão UERGS/2003 Prof. Emiliano Chemello Médio www.quimica.net/emiliano emiliano@quimica.net Difícil Níveis de dificuldade das Questões 01. Em um frasco,
Hidrogênio x Hidrogênio Hidrogênio x Não metal Não metal x Não metal
 LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
RESPOSTAS DOS EXERCÍCIOS
 Respostas dos Exercícios 1 RESPOSTAS DOS EXERCÍCIOS CAPÍTULO 1 1. a) 1s 2 2s 2 2p 6 3s 1 b) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 c) 1s 2 2s 2 2p 6 3s 2 3p 1 d) 1s 2 2s 2 2p 6 3s 2 3p 2 e) 1s 2 2s 2 2p 6 3s 2
Respostas dos Exercícios 1 RESPOSTAS DOS EXERCÍCIOS CAPÍTULO 1 1. a) 1s 2 2s 2 2p 6 3s 1 b) 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 c) 1s 2 2s 2 2p 6 3s 2 3p 1 d) 1s 2 2s 2 2p 6 3s 2 3p 2 e) 1s 2 2s 2 2p 6 3s 2
PRE-VEST AMANDA 14-05-2015 QUÍMICA. Rua Lúcio José Filho, 27 Parque Anchieta Tel: 3012-8339. f) 3-etil-2-metil-2-hexeno;
 PRE-VEST AMANDA 14-05-2015 QUÍMICA Lista de Exercícios Hidrocarbonetos Classificação e Nomenclatura de alcanos e alcenos. 01) Escreva as fórmulas estruturais e moleculares dos seguintes alcanos: a) propano;
PRE-VEST AMANDA 14-05-2015 QUÍMICA Lista de Exercícios Hidrocarbonetos Classificação e Nomenclatura de alcanos e alcenos. 01) Escreva as fórmulas estruturais e moleculares dos seguintes alcanos: a) propano;
A B σ σ + A B C A + A B C C
 REAÇÕES DE ADIÇÃO As reações de adição ocorrem com a entrada de novos átomos na molécula, sem que esta perca nenhum dos átomos constituintes de sua estrutura. Tais reações podem ocorrer com a quebra de
REAÇÕES DE ADIÇÃO As reações de adição ocorrem com a entrada de novos átomos na molécula, sem que esta perca nenhum dos átomos constituintes de sua estrutura. Tais reações podem ocorrer com a quebra de
Departamento de Química ICEx UFMG Exercícios de Fixação LIGAÇÃO COVALENTE
 Departamento de Química ICEx UFMG Exercícios de Fixação LIGAÇÃO COVALENTE Questão 1 Considerando os íons NO 2+ e NO 2-, faça o que se pede: a. Represente cada um dos íons através de um número adequado
Departamento de Química ICEx UFMG Exercícios de Fixação LIGAÇÃO COVALENTE Questão 1 Considerando os íons NO 2+ e NO 2-, faça o que se pede: a. Represente cada um dos íons através de um número adequado
Cadeias Carbônicas hidrocarbonetos
 Resoluções Segmento: Pré-vestibular Coleção: Alfa, Beta e Gama. Disciplina: Química Caderno de Exercícios 1 Série: 12 Cadeias Carbônicas hidrocarbonetos 1. Pode-se distinguir uma amostra sólida de um composto
Resoluções Segmento: Pré-vestibular Coleção: Alfa, Beta e Gama. Disciplina: Química Caderno de Exercícios 1 Série: 12 Cadeias Carbônicas hidrocarbonetos 1. Pode-se distinguir uma amostra sólida de um composto
Orbitais híbridos sp 2
 Hibridização Para entendermos o que é hibridização (também chamada de hibridação) ou um orbital híbrido nós estudaremos a molécula do metano (CH 4). A estrutura do metano experimentalmente é tetraédrica.
Hibridização Para entendermos o que é hibridização (também chamada de hibridação) ou um orbital híbrido nós estudaremos a molécula do metano (CH 4). A estrutura do metano experimentalmente é tetraédrica.
TERMOQUÍMICA. Desta forma podemos dizer que qualquer mudança química geralmente envolve energia.
 TERMOQUÍMICA 1 Introdução A sociedade moderna depende das mais diversas formas de energia para sua existência. Quase toda a energia de que dependemos é obtida a partir de reações químicas, como a queima
TERMOQUÍMICA 1 Introdução A sociedade moderna depende das mais diversas formas de energia para sua existência. Quase toda a energia de que dependemos é obtida a partir de reações químicas, como a queima
3. Ligações Químicas Deslocalizadas
 3. Ligações Químicas Deslocalizadas 3.1. Ressonância 3.2. Ligações Duplas em Conjugação 3.3. Ligação dupla em conjugação com um orbital p em um átomo adjacente 3.4. Hiperconjugação 3.5. Aromaticidade 3.6.
3. Ligações Químicas Deslocalizadas 3.1. Ressonância 3.2. Ligações Duplas em Conjugação 3.3. Ligação dupla em conjugação com um orbital p em um átomo adjacente 3.4. Hiperconjugação 3.5. Aromaticidade 3.6.
3. Elemento Químico Elemento Químico é um conjunto de átomos iguais (do mesmo tipo). E na linguagem dos químicos eles são representados por Símbolos.
 Química Profª SIMONE MORGADO Aula 1 Elemento, substância e mistura 1. Conceito de Química A Química é uma ciência que busca compreender os mistérios da matéria, sua organização e transformações, bem como
Química Profª SIMONE MORGADO Aula 1 Elemento, substância e mistura 1. Conceito de Química A Química é uma ciência que busca compreender os mistérios da matéria, sua organização e transformações, bem como
Os lipídeos se encontram distribuídos em todos os tecidos, principalmente nas membranas celulares.
 LIPÍDEOS Os lipídeos se encontram distribuídos em todos os tecidos, principalmente nas membranas celulares. Por convenção (Congresso Internacional de Bioquímica em 1922) ésteres de ácidos graxos, ou seja,
LIPÍDEOS Os lipídeos se encontram distribuídos em todos os tecidos, principalmente nas membranas celulares. Por convenção (Congresso Internacional de Bioquímica em 1922) ésteres de ácidos graxos, ou seja,
Bombas de Vácuo e Compressores de Anel Líquido Nash para Indústrias Químicas
 Bombas de Vácuo e Compressores de Anel Líquido Nash para Indústrias Químicas Bombas de Vácuo e Compressores de Anel Líquido NASH Tecnologia e Experiência Gardner Denver Nash atende indústrias petroquímicas,
Bombas de Vácuo e Compressores de Anel Líquido Nash para Indústrias Químicas Bombas de Vácuo e Compressores de Anel Líquido NASH Tecnologia e Experiência Gardner Denver Nash atende indústrias petroquímicas,
BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR
 BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR As moléculas que constituem as células são formadas pelos mesmos átomos encontrados nos seres inanimados. Todavia, na origem e evolução das células, alguns
BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR As moléculas que constituem as células são formadas pelos mesmos átomos encontrados nos seres inanimados. Todavia, na origem e evolução das células, alguns
Como se obtém gasolina de petróleo?
 CEEJA QUÍMICA CONTEÚDO PARA U. E. 14 Como se obtém gasolina de petróleo? O que vamos aprender? Formação do petróleo Produtos derivados do petróleo Separação dos produtos do petróleo: destilação fracionada
CEEJA QUÍMICA CONTEÚDO PARA U. E. 14 Como se obtém gasolina de petróleo? O que vamos aprender? Formação do petróleo Produtos derivados do petróleo Separação dos produtos do petróleo: destilação fracionada
3ª Série Nomenclatura IUPAC
 3ª Série Nomenclatura IUPAC COLÉGIO TIA IVONE - CTI DISCIPLINA: QUÍMICA Data: / /2012 PROFESSOR: NEW CRISTIAN Apostila SÉRIE: 3ª SÉRIE DO ENSINO MÉDIO Aluno(a): Nomenclatura IUPAC Assim como acontece na
3ª Série Nomenclatura IUPAC COLÉGIO TIA IVONE - CTI DISCIPLINA: QUÍMICA Data: / /2012 PROFESSOR: NEW CRISTIAN Apostila SÉRIE: 3ª SÉRIE DO ENSINO MÉDIO Aluno(a): Nomenclatura IUPAC Assim como acontece na
UFU 2014 VESTIBULAR DE MAIO 1ª FASE
 UFU 2014 VESTIBULAR DE MAIO 1ª FASE 1-O iodo-132, devido à sua emissão de partículas beta e radiação gama, tem sido muito empregado no tratamento de problemas na tireoide. A curva abaixo ilustra o decaimento
UFU 2014 VESTIBULAR DE MAIO 1ª FASE 1-O iodo-132, devido à sua emissão de partículas beta e radiação gama, tem sido muito empregado no tratamento de problemas na tireoide. A curva abaixo ilustra o decaimento
As Propriedades das Misturas (Aulas 18 a 21)
 As Propriedades das Misturas (Aulas 18 a 21) I Introdução Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanometro (10 Angstrons). A solução ainda pode
As Propriedades das Misturas (Aulas 18 a 21) I Introdução Em Química, solução é o nome dado a dispersões cujo tamanho das moléculas dispersas é menor que 1 nanometro (10 Angstrons). A solução ainda pode
Química. Resolução das atividades complementares. Q9 Classificação de substâncias
 Resolução das atividades complementares Química Q9 Classificação de substâncias p. 54 O sulfato de magnésio é um sal inorgânico de caráter neutro. A solução aquosa de sulfato de magnésio é um medicamento
Resolução das atividades complementares Química Q9 Classificação de substâncias p. 54 O sulfato de magnésio é um sal inorgânico de caráter neutro. A solução aquosa de sulfato de magnésio é um medicamento
PARECER DOS RECURSOS
 Associação Catarinense das Fundações Educacionais ACAFE PROCESSO SELETIVO ADMISSÃO DE PROFESSORES EM CARÁTER TEMPORÁRIO EDITAL Nº 15/ 2012/ SED PARECER DOS RECURSOS CARGO: Professor de Química 11) Com
Associação Catarinense das Fundações Educacionais ACAFE PROCESSO SELETIVO ADMISSÃO DE PROFESSORES EM CARÁTER TEMPORÁRIO EDITAL Nº 15/ 2012/ SED PARECER DOS RECURSOS CARGO: Professor de Química 11) Com
Respostas da terceira lista de exercícios de química. Prof a. Marcia M. Meier
 Respostas da terceira lista de exercícios de química Prof a. Marcia M. Meier 1) O íon brometo não aceita mais de um elétron, pois este segundo elétron ocupará numeros quânticos maiores quando comparado
Respostas da terceira lista de exercícios de química Prof a. Marcia M. Meier 1) O íon brometo não aceita mais de um elétron, pois este segundo elétron ocupará numeros quânticos maiores quando comparado
INSTRUMENTAÇÃO E CONTROLE DE PROCESSOS MEDIÇÃO DE TEMPERATURA TERMÔMETROS DE RESISTÊNCIA
 INSTRUMENTAÇÃO E CONTROLE DE PROCESSOS MEDIÇÃO DE TEMPERATURA TERMÔMETROS DE RESISTÊNCIA Introdução O uso de termômetros de resistência esta se difundindo rapidamente devido a sua precisão e simplicidade
INSTRUMENTAÇÃO E CONTROLE DE PROCESSOS MEDIÇÃO DE TEMPERATURA TERMÔMETROS DE RESISTÊNCIA Introdução O uso de termômetros de resistência esta se difundindo rapidamente devido a sua precisão e simplicidade
QUÍMICA. Lista de Exercícios Isomeria Geométrica e Óptica
 QUÍMIA Prof. Rodrigo Rocha Lista de Exercícios Isomeria Geométrica e Óptica 1. A reação do tetracloroetano ( 2 2 l 4 ) com zinco metálico produz cloreto de zinco e duas substâncias orgânicas isoméricas,
QUÍMIA Prof. Rodrigo Rocha Lista de Exercícios Isomeria Geométrica e Óptica 1. A reação do tetracloroetano ( 2 2 l 4 ) com zinco metálico produz cloreto de zinco e duas substâncias orgânicas isoméricas,
LIGAÇÃO QUÍMICA NO CARBONO GEOMETRIA MOLECULAR HIBRIDAÇÃO. 06-11-2006 Maria da Conceição Paiva 1
 LIGAÇÃO QUÍMICA NO CARBONO GEOMETRIA MOLECULAR IBRIDAÇÃO 06-11-2006 Maria da Conceição Paiva 1 Geometria molecular O arranjo tri-dimensional dos átomos numa molécula geometria molecular A teoria da repulsão
LIGAÇÃO QUÍMICA NO CARBONO GEOMETRIA MOLECULAR IBRIDAÇÃO 06-11-2006 Maria da Conceição Paiva 1 Geometria molecular O arranjo tri-dimensional dos átomos numa molécula geometria molecular A teoria da repulsão
UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR
 UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Carbono é um elemento cujos átomos podem se organizar sob a forma de diferentes alótropos. Alótropos H de combustão a 25
UFMG - 2005 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR Química Questão 01 Carbono é um elemento cujos átomos podem se organizar sob a forma de diferentes alótropos. Alótropos H de combustão a 25
Desidratação de Álcoois
 Desidratação de Álcoois Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 EXERCÍCIOS DE APLICAÇÃO 01 (Unifenas-MG) A busca de fontes alternativas, devido à possível escassez do petróleo, fez
Desidratação de Álcoois Portal de Estudos em Química (PEQ) www.profpc.com.br Página 1 EXERCÍCIOS DE APLICAÇÃO 01 (Unifenas-MG) A busca de fontes alternativas, devido à possível escassez do petróleo, fez
Exercício de revisão do 3º Ano Ensino Médio 3ª UNIDADE
 Rua Siqueira de Menezes, 406 Centro, Capela SE, 49700000, Brasil Exercício de revisão do 3º Ano Ensino Médio 3ª UNIDADE 1. O propeno e o ciclopropano são representados, respectivamente, pelas fórmulas.
Rua Siqueira de Menezes, 406 Centro, Capela SE, 49700000, Brasil Exercício de revisão do 3º Ano Ensino Médio 3ª UNIDADE 1. O propeno e o ciclopropano são representados, respectivamente, pelas fórmulas.
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo
 Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Prática sobre ponto de fulgor de combustíveis líquidos
 Química e Energia - Prof. Barbieri ICET Instituto de Ciências Exatas e Tecnologia Quando um corpo combustível é aquecido, atinge diferentes estágios da temperatura, os quais são conhecidos por: Ponto de
Química e Energia - Prof. Barbieri ICET Instituto de Ciências Exatas e Tecnologia Quando um corpo combustível é aquecido, atinge diferentes estágios da temperatura, os quais são conhecidos por: Ponto de
Fração. Página 2 de 6
 1. (Fgv 2014) De acordo com dados da Agência Internacional de Energia (AIE), aproximadamente 87% de todo o combustível consumido no mundo são de origem fóssil. Essas substâncias são encontradas em diversas
1. (Fgv 2014) De acordo com dados da Agência Internacional de Energia (AIE), aproximadamente 87% de todo o combustível consumido no mundo são de origem fóssil. Essas substâncias são encontradas em diversas
APOSTILA DE QUÍMICA ORGÂNICA 4º BIMESTRE
 Nome: nº: Bimestre: 4º Ano/série: 2ª série Ensino: Médio Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA ORGÂNICA 4º BIMESTRE TEORIA 15 ISOMERIA PLANA Isomeria: fenômeno
Nome: nº: Bimestre: 4º Ano/série: 2ª série Ensino: Médio Componente Curricular: Química Professor: Ricardo Honda Data: / / APOSTILA DE QUÍMICA ORGÂNICA 4º BIMESTRE TEORIA 15 ISOMERIA PLANA Isomeria: fenômeno
UFMG - 2003 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR
 UFMG - 2003 3º DIA QUÍMICA BERNULLI CLÉGI E PRÉ-VESTIBULAR Química Questão 01 A glicose, C 6 6, é uma das fontes de energia mais importantes para os organismos vivos. A levedura, por exemplo, responsável
UFMG - 2003 3º DIA QUÍMICA BERNULLI CLÉGI E PRÉ-VESTIBULAR Química Questão 01 A glicose, C 6 6, é uma das fontes de energia mais importantes para os organismos vivos. A levedura, por exemplo, responsável
Cadex Pré-vestibular Química Volume I Série 4 Geometria molecular; polaridade; forças intermoleculares
 01 I. H 2, linear (a) II. O 2, linear (a) III. H 2 O, angular (b) IV. NH 3, piramidal (c) V. CH 4, tetraédrica (e) VI. CO 2, linear (a) VII. BF 3, trigonal (d) VIII. H 2 S, angular (b) IX. CCl 4, tetraédrica
01 I. H 2, linear (a) II. O 2, linear (a) III. H 2 O, angular (b) IV. NH 3, piramidal (c) V. CH 4, tetraédrica (e) VI. CO 2, linear (a) VII. BF 3, trigonal (d) VIII. H 2 S, angular (b) IX. CCl 4, tetraédrica
MOLÉCULAS NA TROPOSFERA. Espécies Maioritárias e Espécies Vestigiais
 MOLÉCULAS NA TROPOSFERA Espécies Maioritárias e Espécies Vestigiais 18-01-2013 Dulce Campos 2 Estudo da molécula de oxigénio A atmosfera é constituída maioritariamente por moléculas. Os átomos ligam-se,
MOLÉCULAS NA TROPOSFERA Espécies Maioritárias e Espécies Vestigiais 18-01-2013 Dulce Campos 2 Estudo da molécula de oxigénio A atmosfera é constituída maioritariamente por moléculas. Os átomos ligam-se,
Liquido saturado é aquele que está numa determinada temperatura e pressão eminente de iniciar a transformação para o estado vapor.
 Módulo IV Propriedades de Substâncias Puras: Relações P-V-T e Diagramas P-V, P-T e T-V, Título, Propriedades Termodinâmicas, Tabelas Termodinâmicas, Energia Interna, Entalpia, Calores Espercíficos c v
Módulo IV Propriedades de Substâncias Puras: Relações P-V-T e Diagramas P-V, P-T e T-V, Título, Propriedades Termodinâmicas, Tabelas Termodinâmicas, Energia Interna, Entalpia, Calores Espercíficos c v
QUÍMICA ORGÂNICA Teoria Geral
 QUÍMICA RGÂNICA Teoria Geral Tipos de Carbono Dependendo do número de ligações que o átomo de carbono faz com outros carbonos, podemos classificá-los como:! rimário: ligado diretamente a, no máximo, um
QUÍMICA RGÂNICA Teoria Geral Tipos de Carbono Dependendo do número de ligações que o átomo de carbono faz com outros carbonos, podemos classificá-los como:! rimário: ligado diretamente a, no máximo, um
AULA 6 Esquemas Elétricos Básicos das Subestações Elétricas
 CONSIDERAÇÕES INICIAIS AULA 6 Esquemas Elétricos Básicos das Subestações Elétricas Quando planejamos construir uma subestação, o aspecto de maior importância está na escolha (e, conseqüentemente, da definição)
CONSIDERAÇÕES INICIAIS AULA 6 Esquemas Elétricos Básicos das Subestações Elétricas Quando planejamos construir uma subestação, o aspecto de maior importância está na escolha (e, conseqüentemente, da definição)
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I. Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas.
 Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
Aula: 16 Temática: Estrutura dos aminoácidos e proteínas parte I Acompanhe! Iremos iniciar o estudo da estrutura dos aminoácidos e proteínas. Introdução: A proteína é o composto orgânico mais abundante
EXERCÍCIOS DE APLICAÇÃO
 Energia de Ligação 01 (Fuvest-SP) om base nos dados da tabela, EXERÍIOS DE APLIAÇÃO pode-se estimar que o da reação representada por 2(g) + l 2(g) 2 l(g), dado em kj por mol de l(g), é igual a: a) - 92,5
Energia de Ligação 01 (Fuvest-SP) om base nos dados da tabela, EXERÍIOS DE APLIAÇÃO pode-se estimar que o da reação representada por 2(g) + l 2(g) 2 l(g), dado em kj por mol de l(g), é igual a: a) - 92,5
O Petróleo é um fonte de energia não renovável, e no momento uma das maiores fontes de energia para a humanidade.
 PETRÓLEO Atualmente o Petróleo é um dos recursos naturais de que a nossa sociedade mais depende, pois diversos produtos que conhecemos e utilizamos são derivados desse combustível que move o mundo. O Petróleo
PETRÓLEO Atualmente o Petróleo é um dos recursos naturais de que a nossa sociedade mais depende, pois diversos produtos que conhecemos e utilizamos são derivados desse combustível que move o mundo. O Petróleo
Espectroscopia no Infravermelho
 Espectroscopia no Infravermelho Análogo ao UV: irradiação da amostra com luz I.V. Parte absorvida (A) Parte transmitida (T) Espectro I.V : %A (ou %T) versus freqüência ou comprimento de onda ou número
Espectroscopia no Infravermelho Análogo ao UV: irradiação da amostra com luz I.V. Parte absorvida (A) Parte transmitida (T) Espectro I.V : %A (ou %T) versus freqüência ou comprimento de onda ou número
Claudi Cândia /Sara Regina. Aluno(a): PROVA COMENTADA
 QUÍMICA AVALIAÇÃO Claudi Cândia /Sara Regina Aluno(a): PROVA COMENTADA III UNIDADE Nota: Série: 2 a Ensino Médio Turma: A / B / C / D Data: 14/08/2015 1. A prova é composta de 07 questões abertas e 03
QUÍMICA AVALIAÇÃO Claudi Cândia /Sara Regina Aluno(a): PROVA COMENTADA III UNIDADE Nota: Série: 2 a Ensino Médio Turma: A / B / C / D Data: 14/08/2015 1. A prova é composta de 07 questões abertas e 03
QUÍMICA POR QUE ESTUDAR QUÍMICA?
 QUÍMICA POR QUE ESTUDAR QUÍMICA? A Química contribui para a melhora da qualidade de vida das pessoas, se souber usá-la corretamente. Nosso futuro depende de como vamos usar o conhecimento Químico. A química
QUÍMICA POR QUE ESTUDAR QUÍMICA? A Química contribui para a melhora da qualidade de vida das pessoas, se souber usá-la corretamente. Nosso futuro depende de como vamos usar o conhecimento Químico. A química
38 C 37 B 39 D. Sabendo-se que a amônia (NH 3. ) é constituída por moléculas polares e apresenta boa solubilidade em água. o diclorometano (CH 2.
 QUÍMICA 37 B Sabendo-se que a amônia (N 3 ) é constituída por moléculas polares e apresenta boa solubilidade em água o diclorometano (C Cl ) não possui isômeros Sua molécula apresenta polaridade, devido
QUÍMICA 37 B Sabendo-se que a amônia (N 3 ) é constituída por moléculas polares e apresenta boa solubilidade em água o diclorometano (C Cl ) não possui isômeros Sua molécula apresenta polaridade, devido
ESTRUTURA E REATIVIDADE DE ALCENOS E ALCINOS
 ESTRUTURA E REATIVIDADE DE ALCENOS E ALCINOS INTRODUÇÃO NOMENCLATURA DE ALCENOS NOMEIE O HIDROCARBONETO PRINCIPAL SUFIXO ENO NUMERE OS ÁTOMOS DE CARBONO DA CADEIA NOMENCLATURA DE ALCENOS ESCREVA O NOME
ESTRUTURA E REATIVIDADE DE ALCENOS E ALCINOS INTRODUÇÃO NOMENCLATURA DE ALCENOS NOMEIE O HIDROCARBONETO PRINCIPAL SUFIXO ENO NUMERE OS ÁTOMOS DE CARBONO DA CADEIA NOMENCLATURA DE ALCENOS ESCREVA O NOME
FUNÇÕES ORGÂNICAS: HIDROCARBONETOS. Giseli Menegat e Maira Gazzi Manfro
 FUNÇÕES ORGÂNICAS: HIDROCARBONETOS Giseli Menegat e Maira Gazzi Manfro giseli.menegat@caxias.ifrs.edu.br maira.manfro@caxias.ifrs.edu.br O QUE SÃO HIDROCARBONETOS? São compostos formados exclusivamente
FUNÇÕES ORGÂNICAS: HIDROCARBONETOS Giseli Menegat e Maira Gazzi Manfro giseli.menegat@caxias.ifrs.edu.br maira.manfro@caxias.ifrs.edu.br O QUE SÃO HIDROCARBONETOS? São compostos formados exclusivamente
3.1 Definições Uma classe é a descrição de um tipo de objeto.
 Unified Modeling Language (UML) Universidade Federal do Maranhão UFMA Pós Graduação de Engenharia de Eletricidade Grupo de Computação Assunto: Diagrama de Classes Autoria:Aristófanes Corrêa Silva Adaptação:
Unified Modeling Language (UML) Universidade Federal do Maranhão UFMA Pós Graduação de Engenharia de Eletricidade Grupo de Computação Assunto: Diagrama de Classes Autoria:Aristófanes Corrêa Silva Adaptação:
Associação Catarinense das Fundações Educacionais ACAFE PARECER RECURSO DISCIPLINA QUÍMICA
 33) Assinale a alternativa correta, na qual todas as substâncias são compostas e líquidas à temperatura ambiente. A O 3, O 2 ; CH 3 CH 2 OH B H 2 ; CO 2 ; CH 3 OH C H 2 O; NH 3 ; CO D H 2 O; CH 3 CH 2
33) Assinale a alternativa correta, na qual todas as substâncias são compostas e líquidas à temperatura ambiente. A O 3, O 2 ; CH 3 CH 2 OH B H 2 ; CO 2 ; CH 3 OH C H 2 O; NH 3 ; CO D H 2 O; CH 3 CH 2
Isomeria plana. www.sotaodaquimica.com.br Contato: sotaodaquimica@gmail.com
 Isomeria plana 01. (Uerj) A gasolina é uma mistura de hidrocarbonetos diversos que apresenta, dentre outros, os seguintes componentes: Os pares de componentes I - II e I - III apresentam isomeria plana,
Isomeria plana 01. (Uerj) A gasolina é uma mistura de hidrocarbonetos diversos que apresenta, dentre outros, os seguintes componentes: Os pares de componentes I - II e I - III apresentam isomeria plana,
Química E Extensivo V. 2
 Química E Extensivo V Exercícios 01) E Propano e butano são hidrocarbonetos pertencentes à subfunção alcano Para a diferenciação dos nomes de cada substância, deve-se observar o sufixo (ano) de alcano,
Química E Extensivo V Exercícios 01) E Propano e butano são hidrocarbonetos pertencentes à subfunção alcano Para a diferenciação dos nomes de cada substância, deve-se observar o sufixo (ano) de alcano,
CARBOIDRATOS. INTRODUÇÃO -Biomoléculas mais abundantes -Base da nutrição animal
 INTRODUÇÃO -Biomoléculas mais abundantes -Base da nutrição animal CARBOIDRATOS *Os animais não são capazes de sintetizar carboidratos a partir de substratos simples não energéticos, precisando obtê-los
INTRODUÇÃO -Biomoléculas mais abundantes -Base da nutrição animal CARBOIDRATOS *Os animais não são capazes de sintetizar carboidratos a partir de substratos simples não energéticos, precisando obtê-los
O Princípio da Complementaridade e o papel do observador na Mecânica Quântica
 O Princípio da Complementaridade e o papel do observador na Mecânica Quântica A U L A 3 Metas da aula Descrever a experiência de interferência por uma fenda dupla com elétrons, na qual a trajetória destes
O Princípio da Complementaridade e o papel do observador na Mecânica Quântica A U L A 3 Metas da aula Descrever a experiência de interferência por uma fenda dupla com elétrons, na qual a trajetória destes
Gabarito -Funções Orgânicas 2015
 Gabarito: Resposta da questão 1: [Resposta do ponto de vista da disciplina de Química] As cenouras de coloração laranja podem ter sido trazidas a Pernambuco durante a invasão holandesa e contêm um pigmento
Gabarito: Resposta da questão 1: [Resposta do ponto de vista da disciplina de Química] As cenouras de coloração laranja podem ter sido trazidas a Pernambuco durante a invasão holandesa e contêm um pigmento
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL
 RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
RESUMOS TEÓRICOS de QUÍMICA GERAL e EXPERIMENTAL 5 ESTUDO DA MATÉRIA 1 DEFINIÇÕES Matéria é tudo que ocupa lugar no espaço e tem massa. Nem tudo que existe no universo e matéria. Por exemplo, o calor e
QUÍMICA SEGUNDA ETAPA - 1997
 QUÍMICA SEGUNDA ETAPA - 1997 QUESTÃO 01 Os valores das sucessivas energias de ionização de um átomo constituem uma evidência empírica da existência de níveis de energia. Os diagramas abaixo pretendem representar,
QUÍMICA SEGUNDA ETAPA - 1997 QUESTÃO 01 Os valores das sucessivas energias de ionização de um átomo constituem uma evidência empírica da existência de níveis de energia. Os diagramas abaixo pretendem representar,
Exercícios Sobre LigaÇões iônicas
 Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
www.enemdescomplicado.com.br
 Exercícios de Física Gravitação Universal 1-A lei da gravitação universal de Newton diz que: a) os corpos se atraem na razão inversa de suas massas e na razão direta do quadrado de suas distâncias. b)
Exercícios de Física Gravitação Universal 1-A lei da gravitação universal de Newton diz que: a) os corpos se atraem na razão inversa de suas massas e na razão direta do quadrado de suas distâncias. b)
7 - Análise de redes Pesquisa Operacional CAPÍTULO 7 ANÁLISE DE REDES. 4 c. Figura 7.1 - Exemplo de um grafo linear.
 CAPÍTULO 7 7 ANÁLISE DE REDES 7.1 Conceitos Básicos em Teoria dos Grafos Diversos problemas de programação linear, inclusive os problemas de transporte, podem ser modelados como problemas de fluxo de redes.
CAPÍTULO 7 7 ANÁLISE DE REDES 7.1 Conceitos Básicos em Teoria dos Grafos Diversos problemas de programação linear, inclusive os problemas de transporte, podem ser modelados como problemas de fluxo de redes.
Calculando RPM. O s conjuntos formados por polias e correias
 A U L A Calculando RPM O problema O s conjuntos formados por polias e correias e os formados por engrenagens são responsáveis pela transmissão da velocidade do motor para a máquina. Geralmente, os motores
A U L A Calculando RPM O problema O s conjuntos formados por polias e correias e os formados por engrenagens são responsáveis pela transmissão da velocidade do motor para a máquina. Geralmente, os motores
CORPO DE BOMBEIRO MILITAR DO DISTRITO FEDERAL DIRETORIA DE ENSINO E INSTRUÇÃO CENTRO DE ASSISTÊNCIA AO ENSINO COLÉGIO MILITAR DOM PEDRO II
 CORPO DE BOMBEIRO MILITAR DO DISTRITO FEDERAL DIRETORIA DE ENSINO E INSTRUÇÃO CENTRO DE ASSISTÊNCIA AO ENSINO COLÉGIO MILITAR DOM PEDRO II Questão 01 - O esquema a seguir representa, de forma simplificada,
CORPO DE BOMBEIRO MILITAR DO DISTRITO FEDERAL DIRETORIA DE ENSINO E INSTRUÇÃO CENTRO DE ASSISTÊNCIA AO ENSINO COLÉGIO MILITAR DOM PEDRO II Questão 01 - O esquema a seguir representa, de forma simplificada,
ipea políticas sociais acompanhamento e análise 7 ago. 2003 117 GASTOS SOCIAIS: FOCALIZAR VERSUS UNIVERSALIZAR José Márcio Camargo*
 GASTOS SOCIAIS: FOCALIZAR VERSUS UNIVERSALIZAR José Márcio Camargo* Como deve ser estruturada a política social de um país? A resposta a essa pergunta independe do grau de desenvolvimento do país, da porcentagem
GASTOS SOCIAIS: FOCALIZAR VERSUS UNIVERSALIZAR José Márcio Camargo* Como deve ser estruturada a política social de um país? A resposta a essa pergunta independe do grau de desenvolvimento do país, da porcentagem
Exercícios sobre Termoquímica- variação de entalpia
 Exercícios sobre Termoquímica- variação de entalpia 01. (Cesgranrio) Quando se adiciona cal viva (CaO) à água, há uma liberação de calor devida à seguinte reação química: CaO + H 2O Ca(OH) 2 + X kcal/mol
Exercícios sobre Termoquímica- variação de entalpia 01. (Cesgranrio) Quando se adiciona cal viva (CaO) à água, há uma liberação de calor devida à seguinte reação química: CaO + H 2O Ca(OH) 2 + X kcal/mol
Exemplos: petróleo, metano, gás de cozinha, gasolina, querosene, etc.
 QUÍMICA 5 AULA 3 4 HIDROCARBONETOS Constituem uma classe de compostos orgânicos muito grande, variada e importante, pois englobam o petróleo e seus derivados, o gás natural etc. Em função do tipo de ligação
QUÍMICA 5 AULA 3 4 HIDROCARBONETOS Constituem uma classe de compostos orgânicos muito grande, variada e importante, pois englobam o petróleo e seus derivados, o gás natural etc. Em função do tipo de ligação
TONALIDADE X FREQUÊNICA
 Som, notas e tons TONALIDADE X FREQUÊNICA O violão é um instrumento musical e o seu objetivo é fazer música. Música é a organização de sons em padrões que o cérebro humano acha agradável (ou pelo menos
Som, notas e tons TONALIDADE X FREQUÊNICA O violão é um instrumento musical e o seu objetivo é fazer música. Música é a organização de sons em padrões que o cérebro humano acha agradável (ou pelo menos
CICLOPENTANO ETENO BUTANO PROPINO ETANO. - Eu sou um Alceno! - Eu sou um Alcano!
 ETENO possui apenas 2 carbonos 2. Tenho apenas 1 ligação dupla 4. Não tenho ramificações 5. Possuo 4 hidrogênios CICLOPENTANO possui 5 carbonos 2. Possuo apenas ligações 5. Possuo 10 hidrogênios BUTANO
ETENO possui apenas 2 carbonos 2. Tenho apenas 1 ligação dupla 4. Não tenho ramificações 5. Possuo 4 hidrogênios CICLOPENTANO possui 5 carbonos 2. Possuo apenas ligações 5. Possuo 10 hidrogênios BUTANO
Química Orgânica. Prof. ALEXANDRE D. MARQUIORETO
 Química Orgânica Prof. ALEXANDRE D. MARQUIORETO Aspirina (AAS) Sacarina sódica Ácido cítrico Ciclamato de sódio Introdução Função química é uma série de compostos que possuem propriedades químicas semelhantes.
Química Orgânica Prof. ALEXANDRE D. MARQUIORETO Aspirina (AAS) Sacarina sódica Ácido cítrico Ciclamato de sódio Introdução Função química é uma série de compostos que possuem propriedades químicas semelhantes.
TURMA DOS 30 01. Considere a cadeia carbônica representada a seguir:
 01. Considere a cadeia carbônica representada a seguir: 06. Considere as seguintes substâncias e suas fórmulas estruturais: I. Antídoto efetivo no envenenamento por arsênio: Os carbonos numerados classificam-se
01. Considere a cadeia carbônica representada a seguir: 06. Considere as seguintes substâncias e suas fórmulas estruturais: I. Antídoto efetivo no envenenamento por arsênio: Os carbonos numerados classificam-se
Escalas. Antes de representar objetos, modelos, peças, A U L A. Nossa aula. O que é escala
 Escalas Introdução Antes de representar objetos, modelos, peças, etc. deve-se estudar o seu tamanho real. Tamanho real é a grandeza que as coisas têm na realidade. Existem coisas que podem ser representadas
Escalas Introdução Antes de representar objetos, modelos, peças, etc. deve-se estudar o seu tamanho real. Tamanho real é a grandeza que as coisas têm na realidade. Existem coisas que podem ser representadas
CAPÍTULO 6 Termologia
 CAPÍTULO 6 Termologia Introdução Calor e Temperatura, duas grandezas Físicas bastante difundidas no nosso dia-a-dia, e que estamos quase sempre relacionando uma com a outra. Durante a explanação do nosso
CAPÍTULO 6 Termologia Introdução Calor e Temperatura, duas grandezas Físicas bastante difundidas no nosso dia-a-dia, e que estamos quase sempre relacionando uma com a outra. Durante a explanação do nosso
INFORMATIVO DE PRODUTO
 Sensor / Detector de Gás Natural e Derivados de Metano Com Saída Relé NA / NF Código: ALM1224BR O Detector de Gás, código ALM1224BR é um equipamento que deve ser instalado na parede de cozinhas, salas
Sensor / Detector de Gás Natural e Derivados de Metano Com Saída Relé NA / NF Código: ALM1224BR O Detector de Gás, código ALM1224BR é um equipamento que deve ser instalado na parede de cozinhas, salas
Os motores de CA podem ser monofásicos ou polifásicos. Nesta unidade, estudaremos os motores monofásicos alimentados por uma única fase de CA.
 Motores elétricos Os motores de CA podem ser monofásicos ou polifásicos. Nesta unidade, estudaremos os motores monofásicos alimentados por uma única fase de CA. Para melhor entender o funcionamento desse
Motores elétricos Os motores de CA podem ser monofásicos ou polifásicos. Nesta unidade, estudaremos os motores monofásicos alimentados por uma única fase de CA. Para melhor entender o funcionamento desse
Probabilidade - aula I
 e 27 de Fevereiro de 2015 e e Experimentos Aleatórios e Objetivos Ao final deste capítulo você deve ser capaz de: Entender e descrever espaços amostrais e eventos para experimentos aleatórios. Interpretar
e 27 de Fevereiro de 2015 e e Experimentos Aleatórios e Objetivos Ao final deste capítulo você deve ser capaz de: Entender e descrever espaços amostrais e eventos para experimentos aleatórios. Interpretar
3.4 O Princípio da Equipartição de Energia e a Capacidade Calorífica Molar
 3.4 O Princípio da Equipartição de Energia e a Capacidade Calorífica Molar Vimos que as previsões sobre as capacidades caloríficas molares baseadas na teoria cinética estão de acordo com o comportamento
3.4 O Princípio da Equipartição de Energia e a Capacidade Calorífica Molar Vimos que as previsões sobre as capacidades caloríficas molares baseadas na teoria cinética estão de acordo com o comportamento
www.elesapiens.com GLOSSÁRIO DE QUÍMICA ADUBO: É qualquer substância orgânica ou inorgânica que melhora a qualidade da terra.
 GLOSSÁRIO DE QUÍMICA ADUBO: É qualquer substância orgânica ou inorgânica que melhora a qualidade da terra. ALQUIMIA: A alquimia foi uma antiga prática que buscava encontrar o que chamavam de Pedra Filosofal,
GLOSSÁRIO DE QUÍMICA ADUBO: É qualquer substância orgânica ou inorgânica que melhora a qualidade da terra. ALQUIMIA: A alquimia foi uma antiga prática que buscava encontrar o que chamavam de Pedra Filosofal,
se complete no sentido indicado, assinale a alternativa correta. a) Há menos energia armazenada nos produtos do que nos reagentes.
 Questão 01) Sejam dados os processos abaixo:. Fe(s) Fe(l).. H 2 O(l) H 2 (g) + 1/2 O 2 (g) C(s) + O 2 (g) CO 2 (g) V. H 2 O(v) H 2 O(s) V. NH 3 (g) 1/2 N 2 (g) + 3/2 N 2 (g) A opção que representa somente
Questão 01) Sejam dados os processos abaixo:. Fe(s) Fe(l).. H 2 O(l) H 2 (g) + 1/2 O 2 (g) C(s) + O 2 (g) CO 2 (g) V. H 2 O(v) H 2 O(s) V. NH 3 (g) 1/2 N 2 (g) + 3/2 N 2 (g) A opção que representa somente
SISTEMA EXCRETOR P R O F E S S O R A N A I A N E
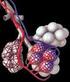 SISTEMA EXCRETOR P R O F E S S O R A N A I A N E O que não é assimilado pelo organismo O que o organismo não assimila, isto é, os materiais inúteis ou prejudiciais ao seu funcionamento, deve ser eliminado.
SISTEMA EXCRETOR P R O F E S S O R A N A I A N E O que não é assimilado pelo organismo O que o organismo não assimila, isto é, os materiais inúteis ou prejudiciais ao seu funcionamento, deve ser eliminado.
Centro Universitário Anchieta Engenharia Química Química Orgânica I Prof. Vanderlei I Paula Lista de exercícios 4 / Data: 02/05/2015
 01 - A adição de Br a um alceno pode conduzir a produtos diferentes caso, nessa reação, seja empregado o alceno puro ou o alceno misturado a uma pequena quantidade de peróxido. 2 + Br 2 Br 2 + Br peróxido
01 - A adição de Br a um alceno pode conduzir a produtos diferentes caso, nessa reação, seja empregado o alceno puro ou o alceno misturado a uma pequena quantidade de peróxido. 2 + Br 2 Br 2 + Br peróxido
CONTEÚDO E HABILIDADES DINÂMICA LOCAL INTERATIVA INTERATIVIDADE FINAL AULA QUÍMICA. Unidade III. Ligações químicas e funções inorgânicas.
 Unidade III Ligações químicas e funções inorgânicas. 2 Aula 12.1 Conteúdo: Geometria molecular Polaridade das moléculas 3 Habilidades: Relacionar informações apresentadas em diferentes formas de linguagem
Unidade III Ligações químicas e funções inorgânicas. 2 Aula 12.1 Conteúdo: Geometria molecular Polaridade das moléculas 3 Habilidades: Relacionar informações apresentadas em diferentes formas de linguagem
Tecnologia Mecânica MATERIAIS. Roda de aço. Mapa do Brasil em cobre. Prof. Marcio Gomes
 Alumínio Tecnologia Mecânica Ferro fundido MATERIAIS Roda de aço Mapa do Brasil em cobre Introdução Átomo: modelo de Bohr Tecnologia Mecânica O átomo, que não dá para a gente ver nem com um microscópio,
Alumínio Tecnologia Mecânica Ferro fundido MATERIAIS Roda de aço Mapa do Brasil em cobre Introdução Átomo: modelo de Bohr Tecnologia Mecânica O átomo, que não dá para a gente ver nem com um microscópio,
Base Nacional Comum Curricular 2016. Lemann Center at Stanford University
 Base Nacional Comum Curricular 2016 Lemann Center at Stanford University Parte II: Base Nacional Comum: Análise e Recomendações da Seção de Matemática Phil Daro Dezembro, 2015 BASE NACIONAL COMUM: ANÁLISE
Base Nacional Comum Curricular 2016 Lemann Center at Stanford University Parte II: Base Nacional Comum: Análise e Recomendações da Seção de Matemática Phil Daro Dezembro, 2015 BASE NACIONAL COMUM: ANÁLISE
Propriedades químicas para o benzeno
 Programa RISC EXEMPLO 2: Irrigação e volatilização utilizando água subterrânea. Passo 1: Escolha dos contaminantes Tendo em vista que a contaminação de águas subterrâneas de poços residenciais é geralmente
Programa RISC EXEMPLO 2: Irrigação e volatilização utilizando água subterrânea. Passo 1: Escolha dos contaminantes Tendo em vista que a contaminação de águas subterrâneas de poços residenciais é geralmente
Manual de Segurança do Laboratório de Química
 Manual de Segurança do Laboratório de Química Universidade Federal do Pampa Campus Caçapava do Sul 1 INTRODUÇÃO O Manual de Segurança do Laboratório de Química foi elaborado com o objetivo de fornecer
Manual de Segurança do Laboratório de Química Universidade Federal do Pampa Campus Caçapava do Sul 1 INTRODUÇÃO O Manual de Segurança do Laboratório de Química foi elaborado com o objetivo de fornecer
