PROVA 1. Universidade Federal de Lavras. Comissão Permanente de Processo Seletivo TRIÊNIO DEZEMBRO
|
|
|
- Eduardo Capistrano Benevides
- 8 Há anos
- Visualizações:
Transcrição
1 PS TRIÊNIO 8- - DEZEMRO - 7 Universidade Federal de Lavras Comissão Permanente de Processo Seletivo PROV iologia, Física, Matemática e Química INSTRUÇÕES pós a autorização do aplicador, abra o caderno e faça a conferência, conforme instruções abaixo. Confira se sua prova tem (uma) tabela periódica (verso da capa) e 4 questões de múltipla escolha ( de iologia, de Física, de Matemática e de Química). Cada questão apresenta 4 (quatro) alternativas de resposta. penas (uma) alternativa responde à questão. O formulário-resposta deverá ser preenchido seguindo as instruções contidas no próprio formulário. TENÇÃO! O não-cumprimento das instruções acarretará a anulação da(s) questão(ões). O tempo de duração das provas INCLUI o preenchimento do formulário-resposta. interpretação das questões faz parte da prova. Qualquer irregularidade observada quanto a esses itens deverá ser comunicada ao aplicador. Este caderno será obrigatoriamente devolvido ao aplicador ao final da prova. O candidato deverá apenas destacar a contracapa na qual se encontra o rascunho do gabarito. devolução do formulário-resposta e do caderno de provas é de inteira responsabilidade do candidato. oa Prova!
2 Classificação Periódica dos Elementos I II 3 III 4 IV 5 V 6 VI 7 VII 8 9 VIII I II 3 III 4 IV 5 V 6 VI 7 VII 8 Número atômico H, Li 7, Na 3, 9 K 39, 37 Rb 85,5 55 Cs 33, 87 Fr 3* 4 e 9, Mg 4, Ca 4, 38 Sr 88, 56 a 37, 88 Ra 6* Sc 45, 39 Y 89, 57 a 7 La Lu Série dos Lantanídeos 89 a 3 c Lr Série dos ctinídeos Ti 48, 4 Zr 9, 7 Hf 78,5 4 Rf 6* 57 La 39, 89 c 7* SÍMOLO Massa atômica * Nº de massa do isótopo mais estável 3 V 5, 4 Nb 93, 73 Ta 8, 5 Db 6* 58 Ce 4, 9 Th 3, 4 Cr 5, 4 Mo 96, 74 W 84, 6 Sg Pr 4, 9 Pa 3, 5 Mn 55, 43 Tc 98* 75 Re 86, 7 h Nd 44, 9 U 38, 6 Fe 56, 44 Ru, 76 Os 9, 8 Hs Pm 45* 93 Np 37* 7 Co 59, 45 Rh 3, 77 Ir 9, 9 Mt Sm 5, 94 Pu 44* 8 Ni 59, 46 Pd 6, 78 Pt 95, Uun 9 Cu 63,5 47 g 8, 79 u 97, Uun 3 Zn 65, 48 Cd, 8 Hg, Uub Série dos Lantanídeos 63 Eu 5, 64 Gd 57, 65 Tb 59, Série dos ctinídeos 95 m 43* 96 Cm 47* 97 k 47* 5, 3 l 7, 3 Ga 7, 49 In 5, 8 Tl 4, 66 Dy 6,5 98 Cf 5* 6 C, 4 Si 8, 3 Ge 7,5 5 Sn 9, 8 Pb 7, 67 Ho 65, 99 Es 5* 7 N 4, 5 P 3, 33 s 75, 5 Sb, 83 i 9, 68 Er 67, Fm 57* 8 O 6, 6 S 3, 34 Se 79, 5 Te 8, 84 Po 9* 69 Tm 69, Md 58* 9 F 9, 7 Cl 35,5 35 r 8, 53 I 7, 85 t * 7 Yb 73, No 59* He 4, Ne, 8 r 4, 36 Kr 84, 54 Xe 3, 86 Rn * 7 Lu 75, 3 Lr 6* Reatividade dos metais: Li>K>Ca>Na>Mg>l>Zn>Cr>Fe>Ni>Sn>Pb>H>Cu>Hg>g>Pt>u Número de vogadro: 6, x 3 Constante de Faraday: 965 C - Constante dos gases perfeitos:,8. atm L K - mol -
3 Processo Seletivo de valiação Seriada ª etapa (Grupo IX - Triênio 8-) _ QUESTÕES DE IOLOGI: a. O conhecimento e o uso adequado de métodos contraceptivos podem reduzir a ocorrência de uma gravidez indesejada, principalmente na adolescência. Vários métodos utilizam uma associação de estrogênio e progesterona sintéticos que inibem parcialmente a hipófise e impedem que essa glândula libere o FSH e o LH; por isso, não ocorre a ovulação. Qual dos métodos contraceptivos não atua desse modo? () Pílula anticoncepcional () nticoncepcionais hormonais injetáveis (C) Pílula do dia seguinte (D) Implante subcutâneo de progesterona. Quantos gametas serão formados a partir da célula de número do desenho?. 3. () 3 () 64 (C) 6 (D) I II III figura mostra os três tipos de tecido muscular de um mamífero. É correto afirmar que () o tecido muscular em I é do tipo estriado esquelético, cuja contração é involuntária e rápida. () o tecido muscular em II é do tipo liso, cuja principal característica é ter núcleo central e contração voluntária e principalmente neurogênica. (C) o tecido muscular em I é do tipo estriado cardíaco e tem como características a contração miogênica e muitos núcleos periféricos. (D) o tecido muscular em III é do tipo estriado cardíaco e a seta indica o disco intercalar. 4. O desenho representa as etapas da transcrição e tradução em uma célula eucariótica. Os números, e 3 representam, respectivamente: () DN, RNt, ribossomo () DN, RNm, ribossomo (C) RNt, DN, ribossomo (D) Ribossomo, DN, RNm 5. Em relação à evolução dos primeiros seres vivos, assinale a alternativa que indica a ordem temporal correta em que esses organismos surgiram. I - II - III - IV - Organismos autotróficos. Organismos heterotróficos anaeróbicos. Organismos heterotróficos aeróbicos. Organismos multicelulares. () II, I, IV e III () II, I, III e IV (C) I, II, III e IV (D) I, III, II e IV 6. Plantas transgênicas são produzidas pela engenharia genética, mediante um conjunto de técnicas que permite a manipulação do DN, conhecida também como tecnologia do DN recombinante. Marque a alternativa que mostra os passos corretos na obtenção de uma planta transgênica. () DN modificado, clonagem em um plasmídeo, transferência para célula vegetal, seleção de transformantes, vegetal transgênico adulto. () DN modificado, retirada do óvulo, transferência do embrião, seleção de transformantes, vegetal transgênico adulto. (C) Retirada das células da planta doadora, retirada do núcleo, fusão das células, transferência para célula receptora, seleção de transformantes, vegetal transgênico adulto. (D) Retirada das células da planta doadora, clonagem em um plasmídeo, retirada do núcleo, fusão das células, transferência para célula vegetal receptora, vegetal transgênico adulto. 3
4 Processo Seletivo de valiação Seriada ª etapa (Grupo IX - Triênio 8-) 7. figura representa um processo de digestão intracelular. Com base na figura, assinale a alternativa correta. () O processo de digestão representado na figura é chamado de autofagia. () s enzimas lisossômicas são produzidas na organela, empacotadas na organela, formando os lisossomas secundários. (C) Durante a fagocitose, desenvolve-se no interior da célula um vacúolo chamado fagossoma, que se funde com o lisossoma, formando um vacúolo digestivo, indicado em 3. (D) O 4 representa um corpo residual, que é eliminado por endocitose na superfície da célula. 8. Para o crescimento e desenvolvimento do corpo que se desgasta continuamente, os organismos precisam, para sua reconstrução, retirar matéria e energia do meio. Tais funções (desenvolver/ crescer/ reconstruir) realizam-se mediante diferentes processos do metabolismo. I - II - III - nalise as proposições abaixo sobre esses processos orgânicos e, a seguir, assinale a alternativa correta. O processo de formação da matéria viva no interior das células é denominado nabolismo. O processo de degradação de moléculas para obtenção de energia é chamado de Catabolismo. O conjunto dos processos citados anteriormente é denominado Metabolismo () penas a proposição II está correta. () penas a proposição I está correta. (C) Todas as proposições estão corretas. (D) s proposições I e II estão corretas. 9. fotossíntese é um processo que ocorre predominantemente nas folhas. Em muitas plantas, principalmente nas dicotiledôneas, o tecido fotossintético pode ser subdividido em () parênquima paliçádico e aerífero. () parênquima lacunoso e aerífero. (C) parênquima lacunoso e aqüífero. (D) parênquima paliçádico e lacunoso.. Com relação à permeabilidade da membrana celular, sabe-se que a fluidez e a disposição das moléculas de lipídeos interferem no processo de transporte celular. Dessa forma, considere as seguintes proposições e marque, a seguir, a alternativa CORRET. I - II - III - Quanto menos fluida é a camada lipídica, mais rapidamente a água passa por ela. O transporte ativo é possível devido à energia fornecida pela quebra do TP. Vários açúcares, como a glicose, têm seu transporte facilitado por enzimas contidas na membrana. () Estão corretas as proposições II e III. () Estão corretas as proposições I e II (C) Estão corretas as proposições I e III (D) Todas as proposições estão corretas. QUESTÕES DE FÍSIC: a. Um carro de corridas deve possuir formas aerodinâmicas (geometria) privilegiadas para produzir o menor arraste do ar, minimizando, assim, as forças resistivas que nele atuam. força de arraste pode ser dada por: f = Dv, sendo v a velocidade do carro e D uma constante que depende da forma e do tamanho do carro e da densidade do ar. Considerando o MKS, sistema internacional (SI), a constante D tem a seguinte unidade: () kg/m () kg/m 3 (C) kg.m.s - (D) D é uma constante adimensional.. Hoje, as televisões modernas apresentam telas em cristal líquido (LCD) ou plasma. s TVs antigas possuem um tubo de raios catódicos (CRT) onde os elétrons são acelerados, a partir do repouso, até colidirem com a tela frontal, formando a imagem. Desprezando uma rápida desaceleração final, o gráfico abaixo v x t mostra uma típica variação da velocidade de um elétron nesses tubos. o analisar esse gráfico, pode-se afirmar que a distância percorrida pelo elétron até atingir a tela é () 4 cm () cm (C) 3 cm (D) 5 cm v( 6 m/s) t( -7 s)
5 Processo Seletivo de valiação Seriada ª etapa (Grupo IX - Triênio 8-) _ 3 3. Num parque de diversões, uma criança está sentada na periferia de uma roda, de raio m, que gira com movimento circular uniforme, completando uma volta a cada 4 s. Pode-se afirmar que essa criança está submetida a uma aceleração radial de () zero, pois o movimento é circular uniforme. π () m/s (C) 9,8 m/s (D) 3,4 m/s II - força normal N r e o peso P r formam um par ação-reação, pois tem o mesmo módulo, direção e sentido. Pode-se afirmar que () as duas afirmações estão incorretas. () as duas afirmações estão corretas. (C) somente a afirmativa I está correta. (D) somente a afirmativa II está correta. 4. Uma prancha uniforme e indeformável de peso 4 N e comprimento m repousa horizontalmente sobre os apoios e C, cuja distância é de 6 m (Figura abaixo). Uma pessoa de peso 8 N caminha sobre essa prancha a partir do apoio, no sentido da extremidade. Pode-se afirmar que essa pessoa pode caminhar, além do apoio C, sem que a prancha gire, a distância de 6. Dois corpos de massas M e M estão ligados por um fio ideal (inextensível e sem massa) que passa por uma roldana isenta de atrito, conforme mostra a figura abaixo. O coeficiente de atrito estático µ e entre a massa M e a superfície horizontal é,6. Considerando a massa de M = 3 kg e g = m/s, pode-se afirmar que o valor máximo de M, para que o sistema permaneça em equilíbrio estático, é M (), m () 4, m (C) 3, m (D),5 m 5. Um bloco é colocado sobre uma superfície horizontal áspera. Uma força horizontal F r é aplicada no bloco, mas esse não se move devido à força de atrito estático F r at e. baixo é apresentado o diagrama de forças que atuam no bloco. N r F r at e C F r (),6 kg (), kg (C),8 kg (D), kg 7. Um bloco de massa,6 kg comprime uma mola de constante elástica K = N/m. O bloco, ao ser liberado pela mola, percorre o caminho mostrado na figura abaixo. o passar pelo ponto P (h =,6 m), 75% de sua energia é cinética. Considere que a energia potencial gravitacional é zero na linha pontilhada, g = m/s e o sistema isento de atrito. Pode-se afirmar que a mola foi contraída de P M h =,6 m I - P r nalisando-se esse diagrama, duas afirmativas são feitas: força de atrito estático F r at e e a força F r formam um par ação-reação, pois tem o mesmo módulo, direção e sentido. () cm () 8 cm (C) 9 cm (D) cm
6 4 Processo Seletivo de valiação Seriada ª etapa (Grupo IX - Triênio 8-) 8. figura abaixo mostra um plano inclinado de massa M sobre um plano horizontal sem atrito. bandona-se nesse plano inclinado um bloco de massa m, que desliza sem atrito ao longo desse, colidindo com um anteparo e parando. m QUESTÕES DE MTEMÁTIC: a 3. O valor da expressão 9 ( 6 ) + 3 ( 6 + ) é M anteparo () 3 3 () 5 (C) 3 nalisando-se o movimento do plano inclinado M, pode-se afirmar que esse () move-se, inicialmente, para a esquerda e depois retorna à sua posição inicial. () move-se, inicialmente, para a direita e depois retorna à sua posição inicial. (C) move-se para a esquerda e pára. (D) permanece parado o tempo todo. (D) 3. Uma revista sobre curiosidades possui uma seção intitulada CONHECIMENTOS MIS OU MENOS INÚTEIS DO COTIDINO. Nessa seção apareceu o seguinte: Uma escova de dentes possui meia centena de furos com cinco dúzias de cerdas em cada um deles e cada cerda mede, decímetro. 9. Foram observados no sistema α-centauro dois planetas: um com massa M e outro com massa 4 M. Na linha que une os dois planetas, há um ponto P onde os campos gravitacionais gerados por M e 4 M se anulam. Considerando d a distância do planeta M ao ponto P e d a distância de 4 M ao ponto P, pode-se d afirmar que a razão vale d () 4 () (C) 4 (D). Um jato comercial pressurizado voa a 3. pés de altitude. pressão interna na aeronave é P i =,9 atm e a pressão externa P e =,3 atm. Considerando atm = 5 N/m, pode-se afirmar que a força devido a diferença de pressão sobre uma janela de dimensões,5 m x,4 m é de (). N () 4. N (C) 6. N (D) 4. N O comprimento total de fio necessário para confeccionar essa escova de dentes é () 38 m (),3 km (C),3 km (D) 3 cm 3. s experiências mostram que uma pessoa não é capaz de distinguir entre,5 g e g, mas, na maioria das vezes, ela acha g mais pesado que g. Com um peso inicial de 4 g, o resultado é bem diferente. Uma pessoa não pode realmente distinguir entre 4 g e 4 g. O aumento deveria ser de g em vez de g. Da mesma forma, a experiência mostra que 63 g pode ser distinguido de 6 g, 84 g de 8 g, mas que os intervalos não podem ser reduzidos. Quatro pesos são apresentados a uma pessoa que os identifica como sendo g, 4 g, g e 6 g, dando um peso total de 4 g. Tendo como base as informações acima, o erro máximo que essa pessoa poderia cometer é () de 3 g () inferior a 7 g (C) inferior a 5 g (D) de 5 g
7 Processo Seletivo de valiação Seriada ª etapa (Grupo IX - Triênio 8-) _ 5 4. Três conjuntos, e C possuem, respectivamente, três, quatro e cinco elementos e satisfazem às propriedades: I) Eles têm um único elemento em comum. II) intersecção de dois quaisquer deles tem exatamente dois elementos. 7. Considere três estranhas máquinas de calcular, e C. Essas máquinas só admitem como entradas e saídas os números zero e um. máquina opera da seguinte forma: zero operado com zero resulta zero; um operado com um resulta um, e zero operado com um resulta zero, que pode ser esquematizado como O número de elementos da união desses três conjuntos é () 6 () (C) (D) 7 5. Considere as funções f(x) = x x e g(x) = x. f ο g (x) são s raízes da função composta ( ) () e () (C) e (D) e 3 Para a máquina, a saída é zero somente quando ambas as entradas são zero. máquina C admite apenas uma entrada e a saída é sempre diferente da entrada. Interligando essas máquinas, como no diagrama, a saída é x C? 6. relação de amizade entre as pessoas pode ser modelada da seguinte forma: as pessoas são representadas por pontos e se é amigo de, o ponto é ligado ao ponto por uma reta. Estamos considerando a situação de reciprocidade: se é amigo de, então é amigo de. Em uma festa com sete pessoas, as relações de amizade são dadas por F G C () () (C) mesmo com valor de x conhecido, as informações não são suficientes para determinar a saída. (D) o resultado depende se x = ou se x =. 8. Na figura, CD é um quadrado de cm de lado, FD e EC são triângulos equiláteros. medida do segmento EF é E D F C ssinale a alternativa INCORRET. () É possível todos se darem as mãos formando um círculo, de forma que todos estejam de mãos dadas a amigos. () Duas pessoas quaisquer podem retirar-se da festa e, mesmo assim, cada um dos que permanecerem continuam a ter amigos na festa. () 3 () 3 E D (C) migo de meu amigo é meu amigo. (D) Existe uma pessoa que é amiga de todos na festa. (C) (D) 3
8 6 Processo Seletivo de valiação Seriada ª etapa (Grupo IX - Triênio 8-) 9. Uma casa de 3 m tem dois quartos de mesmo tamanho e uma sala 5% maior que a área de um quarto. Qual o tamanho de um quarto, se a área restante, correspondente aos outros cômodos da casa, ocupa 6% da área total da casa? () 6 m () 5 m (C) 8 m (D) m 3. Um dos problemas mais famosos não resolvidos na matemática é a afirmação feita por Christian Goldbach, em 74, conhecida hoje como conjectura de Goldbach: todo número natural par maior que é soma de dois primos ; por exemplo: 4 = +, 6 = 3 + 3, 8 = 5 + 3, = 3 + 7, relembrando que um número primo é um número diferente de que só é divisível por ele mesmo e por. Verificações por computador já comprovaram a conjectura para números muito grandes, por exemplo: = Caso a conjectura seja verdadeira, assinale a alternativa INCORRET. () Todo número par maior que é soma de dois primos, sendo que um deles é maior ou igual à sua metade. () Para cada número par maior que, existem apenas dois números primos cuja soma é esse número. (C) Todo número ímpar maior que 5 é soma de três números primos. (D) Todo número maior que 4 e divisível por 4 é soma de quatro números primos. QUESTÕES DE QUÍMIC: 3 a 4 3. baixo são apresentadas as fórmulas eletrônicas I, II e III de três substâncias que apresentam o elemento cloro em suas composições. H Cl Cl Cl Na + Cl I II III Sobre essas substâncias, é correto afirmar que () II é uma Molécula Polar. () III apresenta Ligação Covalente Polar. (C) I e III são substâncias iônicas. (D) I é uma Molécula Polar e apresenta ligação s-p Marque a alternativa que apresenta corretamente a função química a que pertencem as moléculas abaixo. KMnO 4 / HNO 3 / NH 4 OH/ NaCl/ SO 3 () Óxido iônico/ ácido/ óxido básico/ sal/ óxido ácido. () Sal oxigenado/ hidrácido/ base/ sal não oxigenado/ óxido iônico. (C) Óxido básico/ monoácido/ óxido básico/ sal binário/ óxido anfótero (D) Sal oxigenado/ oxácido/ base/ sal não oxigenado/ óxido molecular 33. Em uma reação de redução com hidrogênio, 5 g de um óxido metálico do tipo MO produz 8 g do metal puro, conforme esquema. Qual é o óxido metálico? H + MO M + H O () FeO () NiO (C) MnO (D) CuO 34. O leite de magnésia é um medicamento que pode ser utilizado como antiácido ou como laxante, dependendo da dose administrada. Uma colher de sopa (5 ml) contém aproximadamente mg de hidróxido de magnésio [Mg(OH) ]. o analisar a reação química abaixo (balanceada), calcule a massa aproximada de HCl que pode ser neutralizada ao ingerirmos ml de leite de magnésia. HCl + Mg(OH) MgCl + H O () g (), g (C),6 g (D) 6 g 35. O íon nitrônio, NO +, é produzido pela reação entre ácido sulfúrico e ácido nítrico, e é comumente utilizado como eletrófilo em reações de nitração via substituição eletrofílica aromática. Os números de oxidação dos átomos de O e N no íon nitrônio são, respectivamente: () - e +5 () e + (C) + e - (D) + e -3
9 Processo Seletivo de valiação Seriada ª etapa (Grupo IX - Triênio 8-) _ s propriedades das substâncias podem ser explicadas com base nas ligações estabelecidas entre seus átomos e também nas interações que ocorrem entre suas moléculas. Com relação às propriedades físicas, destaca-se que essas forças ou ligações intermoleculares são responsáveis pela explicação de propriedades importantes, tais como temperatura (ponto) de fusão, solubilidade, condutividade, entre outras. Considere a informação acima e analise a tabela a seguir, na qual são apresentadas algumas propriedades das substâncias P e Q, ambas em estado sólido. Propriedades Substâncias P Q Solubilidade em água Solúvel Não solúvel Solubilidade em CCl 4 Não solúvel Solúvel Condutividade elétrica no Não conduz Não conduz estado sólido Condutividade em solução Conduz Não conduz saturada Ponto de fusão (ºC) 9 73 É possível afirmar que () P corresponde a uma substância molecular e Q, a uma substância iônica. () P e Q são substâncias moleculares. (C) Q corresponde a uma substância molecular e P, a uma substância iônica. (D) Q e P são substâncias iônicas. 38. O quadro abaixo apresenta duas colunas da tabela periódica. Complete os espaços vazios com elementos do conjunto Q = {, D, M, X, Z}, dispostos aleatoriamente. l Ga In Tl Considere que: O elemento é o mais eletronegativo e o elemento D é o menos eletronegativo do conjunto Q. O íon l 3+ é isoletrônico com o íon M 4+ e o íon In + é isoletrônico com o X +. Marque a alternativa que apresenta corretamente os elementos do conjunto Q que compõem a coluna a ser preenchida. (), Z, M, X, D (), M, Z, X, D (C) D, X, Z, M, (D) D, X, M, Z, 39. aseando-se na análise da ilustração de Maurício de Sousa, a seguir, e nas propriedades da matéria, assinale a opção CORRET. 37. Todo material possui um conjunto único de propriedades que nos permitem reconhecê-lo dentre outras matérias. baixo apresentam-se duas colunas: a ª contém vários materiais e a ª contém algumas propriedades. ssocie a cada conjunto de propriedades um único material e assinale a alternativa que satisfaz, corretamente, essa correlação. ª COLUN alumínio gás de cozinha 3 madeira 4 vidro ª COLUN Ponto de fusão alto. Densidade menor que a da água, inflamável. Ponto de fusão baixo, inflamável. Densidade maior que a da água. () 3 4 () 4 3 (C) 3 4 (D) 4 3 Maurício de Sousa. Turma da Mônica. O Estado de São Paulo. () passagem do estado sólido para o estado gasoso é denominado de condensação. () Fusão é o fenômeno em que o líquido e o gás estão em equilíbrio. (C) s transformações ocorridas pela água na ilustração podem ser consideradas um fenômeno químico. (D) uma temperatura de ºC e uma pressão de atm, a água passa do estado líquido para o estado gasoso.
10 8 Processo Seletivo de valiação Seriada ª etapa (Grupo IX - Triênio 8-) 4. s equações químicas constituem um importante recurso para os químicos na representação de diversos fenômenos da natureza. Considere as três equações químicas representadas abaixo e assinale a alternativa correta. I) Ca (OH) + H SO 4 CaSO 4 + H O II) Ca + ZnCl CaCl + Zn III) KClO 3 KCl + 3O () III representa uma reação de síntese do clorato de potássio. () II representa uma reação de deslocamento e de oxirredução. (C) I representa uma reação de oxirredução. (D) III representa uma reação de decomposição do cloreto de potássio.
11 RSCUNHO TENÇÃO: Esta contracapa não poderá ser utilizada para nenhuma anotação, a não ser as marcações do gabarito-rascunho
Classificação Periódica dos Elementos
 Classificação Periódica dos Elementos 1 2 3 1 Massa atômica relativa. A incerteza no último dígito é 1, exceto quando indicado entre parênteses. Os valores com * referemse Número Atômico 18 ao isótopo
Classificação Periódica dos Elementos 1 2 3 1 Massa atômica relativa. A incerteza no último dígito é 1, exceto quando indicado entre parênteses. Os valores com * referemse Número Atômico 18 ao isótopo
Somente identifique sua prova com o código de inscrição (não coloque seu nome);
 Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas as páginas; Não é permitida
Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas as páginas; Não é permitida
Decreto-Lei n.º 74/2004, de 26 de março. Decreto-Lei n.º 74/2004, de 26 de março
 EXAME NACIONAL DO ENSINO SECUNDÁRIO EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 74/2004, de 26 de março Decreto-Lei n.º 74/2004, de 26 de março Prova Escrita de Física e Química A Prova Escrita
EXAME NACIONAL DO ENSINO SECUNDÁRIO EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 74/2004, de 26 de março Decreto-Lei n.º 74/2004, de 26 de março Prova Escrita de Física e Química A Prova Escrita
121,8 127,6 126,9 131,3. Sb Te I Xe 27,0 28,1 31,0 32,1 35,5 39,9 69,7 72,6 74,9 79,0 79,9 83, Ga Ge As Se Br Kr. In Sn 114,8 118,7.
 PRVA DE QUÍMICA º 2º 3º 4º 5º 6º 7º TABELA PERIÓDICA DS ELEMENTS (IA),0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr Mn Fe
PRVA DE QUÍMICA º 2º 3º 4º 5º 6º 7º TABELA PERIÓDICA DS ELEMENTS (IA),0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr Mn Fe
Somente identifique sua prova com o código de inscrição (não coloque seu nome);
 Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas as páginas; Não é permitida
Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas as páginas; Não é permitida
Versão 2. Utilize apenas caneta ou esferográfica de tinta indelével, azul ou preta.
 Teste Intermédio de Física e Química A Versão Teste Intermédio Física e Química A Versão Duração do Teste: 90 minutos 30.05.01 10.º Ano de Escolaridade Decreto-Lei n.º 74/004, de 6 de março Na folha de
Teste Intermédio de Física e Química A Versão Teste Intermédio Física e Química A Versão Duração do Teste: 90 minutos 30.05.01 10.º Ano de Escolaridade Decreto-Lei n.º 74/004, de 6 de março Na folha de
Exame de Seleção Mestrado em Química Turma 2014 I. Candidato: RG:
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2014
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2014
MODALIDADE EM2. 3 a Olimpíada de Química do Rio de Janeiro 2008 EM2 1 a Fase
 MODALIDADE EM2 Leia atentamente as instruções abaixo: Esta prova destina-se exclusivamente aos alunos das 2 a séries do ensino médio. A prova contém dez questões objetivas, cada uma com cinco alternativas,
MODALIDADE EM2 Leia atentamente as instruções abaixo: Esta prova destina-se exclusivamente aos alunos das 2 a séries do ensino médio. A prova contém dez questões objetivas, cada uma com cinco alternativas,
Identificação do candidato UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2018.
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2018.
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA QUÍMICA (12º ANO) MÓDULO 3 MATRIZ DA PROVA
 Cursos Científico - Humanísticos de Ciências e Tecnologias ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA Ensino Recorrente de Nível Secundário QUÍMICA (12º ANO) MÓDULO 3 TIPO DE PROVA: ESCRITA DURAÇÃO:
Cursos Científico - Humanísticos de Ciências e Tecnologias ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA Ensino Recorrente de Nível Secundário QUÍMICA (12º ANO) MÓDULO 3 TIPO DE PROVA: ESCRITA DURAÇÃO:
EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2009/01
 Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2009/01 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES: - identifique
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2009/01 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES: - identifique
Gabarito - Química - Grupo A
 1 a QUESTÃO: (1,5 ponto) Avaliador Revisor A estrutura dos compostos orgânicos começou a ser desvendada nos meados do séc. XIX, com os estudos de ouper e Kekulé, referentes ao comportamento químico do
1 a QUESTÃO: (1,5 ponto) Avaliador Revisor A estrutura dos compostos orgânicos começou a ser desvendada nos meados do séc. XIX, com os estudos de ouper e Kekulé, referentes ao comportamento químico do
Anexo 1. Tabela de constantes. g = 10 m s -2. Velocidade de propagação da luz no vácuo c = 3, m s -1
 Anexo 1 Tabela de constantes Velocidade de propagação da luz no vácuo c = 3,00 10 8 m s -1 Módulo da aceleração gravítica de um corpo junto à superfície da Terra g = 10 m s - Constante de gravitação universal
Anexo 1 Tabela de constantes Velocidade de propagação da luz no vácuo c = 3,00 10 8 m s -1 Módulo da aceleração gravítica de um corpo junto à superfície da Terra g = 10 m s - Constante de gravitação universal
Química. A) Considerando-se que o pk a1 é aproximadamente 2, quais os valores de pk a2 e pk a3?
 Química 01. O gráfico a seguir representa a variação do ph de 50 ml de uma solução aquosa de um ácido H 3 X em função do volume de NaOH 0,30 moll -1 adicionado. A) Considerando-se que o pk a1 é aproximadamente
Química 01. O gráfico a seguir representa a variação do ph de 50 ml de uma solução aquosa de um ácido H 3 X em função do volume de NaOH 0,30 moll -1 adicionado. A) Considerando-se que o pk a1 é aproximadamente
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA QUÍMICA (12º ANO) MÓDULO 2 MATRIZ DA PROVA
 Cursos Científico - Humanísticos de Ciências e Tecnologias ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA Ensino Recorrente de Nível Secundário QUÍMICA (12º ANO) MÓDULO 2 TIPO DE PROVA: ESCRITA DURAÇÃO:
Cursos Científico - Humanísticos de Ciências e Tecnologias ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA Ensino Recorrente de Nível Secundário QUÍMICA (12º ANO) MÓDULO 2 TIPO DE PROVA: ESCRITA DURAÇÃO:
Somente identifique sua prova com o código de inscrição (não coloque seu nome);
 Minas Gerais PPGMQMG 2/2018 Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas
Minas Gerais PPGMQMG 2/2018 Orientações gerais Somente identifique sua prova com o (não coloque seu nome); Assim que assinar a lista de presença verifique seu e preencha todos os campos referentes em todas
QUÍMICA VESTIBULAR 2005 2ª ETAPA
 QUÍMICA VESTIBULAR 2005 2ª ETAPA 1 2 3 4 5 6 7 1 1 1, 00 2 3 4 Li Be 6, 94 9, 01 11 12 Na Mg 22, 99 24, 31 19 20 K Ca 39, 10 40, 08 37 38 Rb Sr 85, 47 87, 62 55 56 Cs Ba 132, 91 137, 33 87 88 Fr Ra 223,
QUÍMICA VESTIBULAR 2005 2ª ETAPA 1 2 3 4 5 6 7 1 1 1, 00 2 3 4 Li Be 6, 94 9, 01 11 12 Na Mg 22, 99 24, 31 19 20 K Ca 39, 10 40, 08 37 38 Rb Sr 85, 47 87, 62 55 56 Cs Ba 132, 91 137, 33 87 88 Fr Ra 223,
Identificação do candidato UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2018.
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2018.
MÓDULO 6 MATRIZ DA PROVA
 ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (11º ANO) Programa iniciado 2016/2017 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (11º ANO) Programa iniciado 2016/2017 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe
 A H,0 Li 7,0 Na 2,0 9 K 9,0 7 Rb 85,5 55 Cs,0 87 Fr (22) 2 2A Be 9,0 2 Mg 2,0 20 Ca 0,0 8 Sr 88,0 56 Ba 7,0 88 Ra (226) Elementos de Transição B B 5B 6B 7B 8B B 2B 5 6 7 A A 5A 6A 7A 78,5 8,0 8,0 86,0
A H,0 Li 7,0 Na 2,0 9 K 9,0 7 Rb 85,5 55 Cs,0 87 Fr (22) 2 2A Be 9,0 2 Mg 2,0 20 Ca 0,0 8 Sr 88,0 56 Ba 7,0 88 Ra (226) Elementos de Transição B B 5B 6B 7B 8B B 2B 5 6 7 A A 5A 6A 7A 78,5 8,0 8,0 86,0
Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular
 Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Data: 08..2009 Duração: 05 horas Conhecimentos Específicos: Matemática: 01 a 05 Redação Química: 06 a Coloque, de imediato,
Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Data: 08..2009 Duração: 05 horas Conhecimentos Específicos: Matemática: 01 a 05 Redação Química: 06 a Coloque, de imediato,
Exame de Seleção Mestrado em Química Turma 2013 II CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS 11 1B. 26 Fe 55,8 44 Ru 101,1 76 Os 190,2
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2013
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2013
MÓDULO 1 MATRIZ DA PROVA
 ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
= 0 molécula. cada momento dipolar existente na molécula. Lembrando que u R
 Lista de Exercícios de Geometria e Ligações 1) Numere a segunda coluna (estruturas geométricas) de acordo com a primeira coluna (compostos químicos). 1. NH 3 ( ) linear 2. CO 2 ( ) angular 3. H 2 O ( )
Lista de Exercícios de Geometria e Ligações 1) Numere a segunda coluna (estruturas geométricas) de acordo com a primeira coluna (compostos químicos). 1. NH 3 ( ) linear 2. CO 2 ( ) angular 3. H 2 O ( )
Universidade Federal de Goiás. Instituto de Química. Coordenadoria de Pós-Graduação em Química
 Nº. de Inscrição Universidade Federal de Goiás Instituto de Química Coordenadoria de Pós-Graduação em Química EXAME DE SELEÇÃO DO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA 2018/2 IDENTIFICAÇÃO DO CANDIDATO
Nº. de Inscrição Universidade Federal de Goiás Instituto de Química Coordenadoria de Pós-Graduação em Química EXAME DE SELEÇÃO DO PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA 2018/2 IDENTIFICAÇÃO DO CANDIDATO
Física. Pré Vestibular / / Aluno: Nº: Turma: ENSINO MÉDIO
 Pré Vestibular ísica / / luno: Nº: Turma: LEIS DE NEWTON 01. (TEC daptada) Dois blocos e de massas 10 kg e 20 kg, respectivamente, unidos por um fio de massa desprezível, estão em repouso sobre um plano
Pré Vestibular ísica / / luno: Nº: Turma: LEIS DE NEWTON 01. (TEC daptada) Dois blocos e de massas 10 kg e 20 kg, respectivamente, unidos por um fio de massa desprezível, estão em repouso sobre um plano
Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular
 Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Data: 24.10.2010 Duração das 13 às 18 horas. Conhecimentos Específicos: Matemática: 01 a 05 Redação Química: 06 a 10
Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Data: 24.10.2010 Duração das 13 às 18 horas. Conhecimentos Específicos: Matemática: 01 a 05 Redação Química: 06 a 10
Universidade Federal do Ceará 2ª ETAPA PROVA ESPECÍFICA DE QUÍMICA PROVA ESPECÍFICA DE QUÍMICA. Data: Duração: 04 horas CORRETOR 1
 1ª AVALIAÇÃO AVALIAÇÃO FINAL CORRETOR 1 01 02 03 04 05 06 07 08 Reservado à CCV Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Reservado à CCV 2ª ETAPA PROVA ESPECÍFICA
1ª AVALIAÇÃO AVALIAÇÃO FINAL CORRETOR 1 01 02 03 04 05 06 07 08 Reservado à CCV Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Reservado à CCV 2ª ETAPA PROVA ESPECÍFICA
Exame de Seleção Mestrado em Química Turma Candidato: CPF:
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2014.2
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2014.2
Lista de Exercícios Física 2 - Prof. Mãozinha Tarefa 15 Eletromagnetismo. Resumo de fórmulas. Fórmulas para cargas elétricas
 Resumo de fórmulas Força magnética em uma carga elétrica em movimento F = q. v. B. senθ Fórmulas para cargas elétricas Raio de uma trajetória circular gerada por uma partícula em um campo magnético R =
Resumo de fórmulas Força magnética em uma carga elétrica em movimento F = q. v. B. senθ Fórmulas para cargas elétricas Raio de uma trajetória circular gerada por uma partícula em um campo magnético R =
www.enemdescomplicado.com.br
 Exercícios de Física Gravitação Universal 1-A lei da gravitação universal de Newton diz que: a) os corpos se atraem na razão inversa de suas massas e na razão direta do quadrado de suas distâncias. b)
Exercícios de Física Gravitação Universal 1-A lei da gravitação universal de Newton diz que: a) os corpos se atraem na razão inversa de suas massas e na razão direta do quadrado de suas distâncias. b)
121,8 127,6 126,9 131,3. Sb Te I Xe. Pb Bi Po At Rn 69,7 72,6 74,9 79,0 79,9 83, Ga Ge As Se Br Kr. In Sn 114,8 118,7.
 PROVA DE QUÍMICA TABELA PERIÓDICA DOS ELEMENTOS º 2º 3º 4º 5º 6º 7º (IA) H,0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr
PROVA DE QUÍMICA TABELA PERIÓDICA DOS ELEMENTOS º 2º 3º 4º 5º 6º 7º (IA) H,0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr
Verifique se este Caderno contém 12 questões discursivas, distribuídas de acordo com o quadro a seguir:
 1 Confira se os dados contidos na parte inferior desta capa estão corretos e, em seguida, assine no espaço reservado para isso. Se, em qualquer outro local deste Caderno, você assinar, rubricar, escrever
1 Confira se os dados contidos na parte inferior desta capa estão corretos e, em seguida, assine no espaço reservado para isso. Se, em qualquer outro local deste Caderno, você assinar, rubricar, escrever
VERSÃO 1. Prova Escrita de Física e Química A. 10.º e 11.º Anos de Escolaridade. Prova 715/2.ª Fase
 EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 74/2004, de 26 de Março Prova Escrita de Física e Química A 10.º e 11.º Anos de Escolaridade Prova 715/2.ª Fase 15 Páginas Duração da Prova: 120 minutos.
EXAME NACIONAL DO ENSINO SECUNDÁRIO Decreto-Lei n.º 74/2004, de 26 de Março Prova Escrita de Física e Química A 10.º e 11.º Anos de Escolaridade Prova 715/2.ª Fase 15 Páginas Duração da Prova: 120 minutos.
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DOS VALES DO JEQUITINHONHA E MUCURI DIAMANTINA MINAS GERAIS PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO
 MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DOS VALES DO JEQUITINHONHA E MUCURI DIAMANTINA MINAS GERAIS PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO EDITAL Nº 009/2017, DE 21 DE DEZEMBRO DE 2016 SELEÇÃO DO
MINISTÉRIO DA EDUCAÇÃO UNIVERSIDADE FEDERAL DOS VALES DO JEQUITINHONHA E MUCURI DIAMANTINA MINAS GERAIS PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO EDITAL Nº 009/2017, DE 21 DE DEZEMBRO DE 2016 SELEÇÃO DO
Universidade Federal do Ceará Coordenadoria de Concursos - CCV 2ª ETAPA PROVA ESPECÍFICA DE QUÍMICA PROVA ESPECÍFICA DE QUÍMICA
 1ª AVALIAÇÃO CORRETOR 1 01 02 03 04 05 06 07 08 Reservado à CCV AVALIAÇÃO FINAL Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Reservado à CCV 2ª ETAPA PROVA ESPECÍFICA
1ª AVALIAÇÃO CORRETOR 1 01 02 03 04 05 06 07 08 Reservado à CCV AVALIAÇÃO FINAL Universidade Federal do Ceará Coordenadoria de Concursos - CCV Comissão do Vestibular Reservado à CCV 2ª ETAPA PROVA ESPECÍFICA
Identificação do candidato. Exame de Seleção Mestrado em Química Turma I CANDIDATO: RG:
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2017.
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2017.
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação
 Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2012/1 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES IMPROTANTES: -
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2012/1 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES IMPROTANTES: -
Si, Ge, SiO 2, ZnS, etc. PF s e dureza elevados Insolúveis Isolantes (ou semicondutores)
 Sólidos covalentes C, diamante C, grafite Si, Ge, SiO 2, ZnS, etc. PF s e dureza elevados Insolúveis Isolantes (ou semicondutores) Sólidos covalentes TEV: rede 3D de ligações covalentes C, diamante (sp
Sólidos covalentes C, diamante C, grafite Si, Ge, SiO 2, ZnS, etc. PF s e dureza elevados Insolúveis Isolantes (ou semicondutores) Sólidos covalentes TEV: rede 3D de ligações covalentes C, diamante (sp
ESCOLA SECUNDÁRIA DE CASQUILHOS
 ESCOLA SECUNDÁRIA DE CASQUILHOS FQA Ficha 3 - Forças fundamentais, leis de Newton e Lei da gravitação universal 11.º Ano Turma A e B 1 outubro 2014 NOME Nº Turma 1. Associe um número da coluna 1 a uma
ESCOLA SECUNDÁRIA DE CASQUILHOS FQA Ficha 3 - Forças fundamentais, leis de Newton e Lei da gravitação universal 11.º Ano Turma A e B 1 outubro 2014 NOME Nº Turma 1. Associe um número da coluna 1 a uma
FÍSICA CADERNO DE QUESTÕES
 CONCURSO DE ADMISSÃO AO CURSO DE FORMAÇÃO E GRADUAÇÃO FÍSICA CADERNO DE QUESTÕES 2015 1 a QUESTÃO Valor: 1,00 Uma mola comprimida por uma deformação x está em contato com um corpo de massa m, que se encontra
CONCURSO DE ADMISSÃO AO CURSO DE FORMAÇÃO E GRADUAÇÃO FÍSICA CADERNO DE QUESTÕES 2015 1 a QUESTÃO Valor: 1,00 Uma mola comprimida por uma deformação x está em contato com um corpo de massa m, que se encontra
COMISSÃO PERMANENTE DE SELEÇÃO COPESE PRÓ-REITORIA DE GRADUAÇÃO PROGRAD CONCURSO VESTIBULAR 2010 PROVA DE QUÍMICA
 Questão 1: A pirita (FeS 2 ), mineral conhecido como ouro de tolo, é utilizada na fabricação de ácido sulfúrico. Uma das formas de produção desse ácido, a partir da pirita, é o aquecimento em etapas sequenciais
Questão 1: A pirita (FeS 2 ), mineral conhecido como ouro de tolo, é utilizada na fabricação de ácido sulfúrico. Uma das formas de produção desse ácido, a partir da pirita, é o aquecimento em etapas sequenciais
121,8 127,6 126,9 131,3. Sb Te I Xe. In Sn 69,7 72,6 74,9 79,0 79,9 83,8 112,4 107,9 85,5 87,6 88,9 91,2 92,9 95,9 (98) 101,1 102,9 106,4 140,1
 PROVA DE QUÍMICA º 2º 3º 4º 5º 6º 7º TABELA PERIÓDICA DOS ELEMENTOS (IA) H,0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr
PROVA DE QUÍMICA º 2º 3º 4º 5º 6º 7º TABELA PERIÓDICA DOS ELEMENTOS (IA) H,0 3 Li 6,9 Na 23,0 9 K 39, 2 (IIA) 4 Be 9,0 2 Mg 24,3 3 (III B) 4 5 6 7 8 9 0 2 20 2 22 23 24 25 26 27 28 29 30 Ca Sc Ti V Cr
MÓDULO 2 MATRIZ DA PROVA
 ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (10º ANO) Programa iniciado 2015/2016 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
DATA: 17/12/2015 VALOR: 20,0 NOTA: NOME COMPLETO:
 DISCIPLINA: FÍSICA PROFESSORES: Erich/ André NOME COMPLETO: I N S T R U Ç Õ E S DATA: 17/12/2015 VALOR: 20,0 NOTA: ASSUNTO: TRABALHO DE RECUPERAÇÃO FINAL SÉRIE: 1 a EM Circule a sua turma: Funcionários:
DISCIPLINA: FÍSICA PROFESSORES: Erich/ André NOME COMPLETO: I N S T R U Ç Õ E S DATA: 17/12/2015 VALOR: 20,0 NOTA: ASSUNTO: TRABALHO DE RECUPERAÇÃO FINAL SÉRIE: 1 a EM Circule a sua turma: Funcionários:
TABELA PERIÓDICA DOS ELEMENTOS. N atômico 1 H Massa atômica 1, Ru 101,1 76 Os 190,2 108 Hs (265) 45 Rh 102,9 77
 Ministério da Educação Secretaria de Educação Profissional e Tecnológica Instituto Federal de Educação, Ciência e Tecnologia de Minas Gerais Campus São João Evangelista Disciplina: Química II Professor:
Ministério da Educação Secretaria de Educação Profissional e Tecnológica Instituto Federal de Educação, Ciência e Tecnologia de Minas Gerais Campus São João Evangelista Disciplina: Química II Professor:
Cadex Pré-vestibular Química Volume I Série 4 Geometria molecular; polaridade; forças intermoleculares
 01 I. H 2, linear (a) II. O 2, linear (a) III. H 2 O, angular (b) IV. NH 3, piramidal (c) V. CH 4, tetraédrica (e) VI. CO 2, linear (a) VII. BF 3, trigonal (d) VIII. H 2 S, angular (b) IX. CCl 4, tetraédrica
01 I. H 2, linear (a) II. O 2, linear (a) III. H 2 O, angular (b) IV. NH 3, piramidal (c) V. CH 4, tetraédrica (e) VI. CO 2, linear (a) VII. BF 3, trigonal (d) VIII. H 2 S, angular (b) IX. CCl 4, tetraédrica
Universidade Federal de Uberlândia PROGRAD Pró-Reitoria de Graduação. - Comissão Permanente de Vestibular PROCESSO SELETIVO
 Universidade Federal de Uberlândia PROGRAD Pró-Reitoria de Graduação - Comissão Permanente de Vestibular PROCESSO SELETIVO 2009/2 2 SEGUNDO DIA 13 de julho de 2009 Início às 14h, com duração de 4h e 30
Universidade Federal de Uberlândia PROGRAD Pró-Reitoria de Graduação - Comissão Permanente de Vestibular PROCESSO SELETIVO 2009/2 2 SEGUNDO DIA 13 de julho de 2009 Início às 14h, com duração de 4h e 30
Hidrogênio x Hidrogênio Hidrogênio x Não metal Não metal x Não metal
 LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
LIGAÇÃ QUÍMICA Introdução: s átomos, ao se unirem, procuram perder ou ganhar elétrons na última camada até atingirem a configuração eletrônica de um gás nobre. Teoria do octeto: s átomos dos elementos
1 a QUESTÃO Valor 1,0
 1 a QUESTÃO Valor 1,0 Um esquimó aguarda a passagem de um peixe sob um platô de gelo, como mostra a figura abaixo. Ao avistá-lo, ele dispara sua lança, que viaja com uma velocidade constante de 50 m/s,
1 a QUESTÃO Valor 1,0 Um esquimó aguarda a passagem de um peixe sob um platô de gelo, como mostra a figura abaixo. Ao avistá-lo, ele dispara sua lança, que viaja com uma velocidade constante de 50 m/s,
Fluorescênciaderaios-X
 4 Fluorescênciaderaios-X XRF, TXRF http://en.wikipedia.org/wiki/x-ray_fluorescence Possível analisar materiais sólidos directamente sem preparação Existe equipamento portátil Permite analisar componentes
4 Fluorescênciaderaios-X XRF, TXRF http://en.wikipedia.org/wiki/x-ray_fluorescence Possível analisar materiais sólidos directamente sem preparação Existe equipamento portátil Permite analisar componentes
IX Olimpíada Catarinense de Química 2013. Etapa I - Colégios
 I Olimpíada Catarinense de Química - 2013 I Olimpíada Catarinense de Química 2013 Etapa I - Colégios Imagem: Oxidação Fonte:Gilson Rocha Reynaldo, 2013 Primeiro Ano Conselho Regional de Química CRQ III
I Olimpíada Catarinense de Química - 2013 I Olimpíada Catarinense de Química 2013 Etapa I - Colégios Imagem: Oxidação Fonte:Gilson Rocha Reynaldo, 2013 Primeiro Ano Conselho Regional de Química CRQ III
Bacharelado Engenharia Civil
 Bacharelado Engenharia Civil Disciplina: Física Geral e Experimental I Força e Movimento- Leis de Newton Prof.a: Msd. Érica Muniz Forças são as causas das modificações no movimento. Seu conhecimento permite
Bacharelado Engenharia Civil Disciplina: Física Geral e Experimental I Força e Movimento- Leis de Newton Prof.a: Msd. Érica Muniz Forças são as causas das modificações no movimento. Seu conhecimento permite
MÓDULO 5 MATRIZ DA PROVA
 ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (11º ANO) Programa iniciado 2016/2017 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
ESCOLA SECUNDÁRIA FERREIRA DIAS AGUALVA - SINTRA FÍSICA E QUÍMICA A (11º ANO) Programa iniciado 2016/2017 TIPO DE PROVA: ESCRITA DURAÇÃO: 90 minutos Cursos Científico - Humanísticos de Ciências e Tecnologias
Resolução da Prova de Química Vestibular Verão UERGS/2003 Prof. Emiliano Chemello
 Fácil Resolução da Prova de Química Vestibular Verão UERGS/2003 Prof. Emiliano Chemello Médio www.quimica.net/emiliano emiliano@quimica.net Difícil Níveis de dificuldade das Questões 01. Em um frasco,
Fácil Resolução da Prova de Química Vestibular Verão UERGS/2003 Prof. Emiliano Chemello Médio www.quimica.net/emiliano emiliano@quimica.net Difícil Níveis de dificuldade das Questões 01. Em um frasco,
Exercícios Sobre LigaÇões iônicas
 Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
Exercícios Sobre LigaÇões iônicas Dados: 01. (Ufrj - adaptado) A caiação é um processo tradicionalmente utilizado na pintura de casas. Uma das maneiras de se preparar o pigmento consiste em misturar cal
Tabela Periódica* 1 H 1,0. Massa atômica. 20,2 18 Ar 39,9 2º VESTIBULAR UFOP Fe. 29 Cu. 28 Ni. 27 Co. 58,9 45 Rh 102,9 77 Ir 192,2 109 Mt
 Tabela Periódica* 1 1 18 1 1,0 2 Número atômico 1 1,0 13 14 15 16 17 2 e 4,0 2 3 3 Li 6,9 11 Na 23,0 4 Be 9,0 Massa atômica 12 Mg 24,3 3 4 5 6 7 8 9 10 11 12 5 B 10,8 13 Al 27,0 6 C 12,0 14 Si 28,1 7 N
Tabela Periódica* 1 1 18 1 1,0 2 Número atômico 1 1,0 13 14 15 16 17 2 e 4,0 2 3 3 Li 6,9 11 Na 23,0 4 Be 9,0 Massa atômica 12 Mg 24,3 3 4 5 6 7 8 9 10 11 12 5 B 10,8 13 Al 27,0 6 C 12,0 14 Si 28,1 7 N
Prova de Química Resolvida Segunda Etapa Vestibular UFMG 2011 Professor Rondinelle Gomes Pereira
 QUESTÃO 01 Neste quadro, apresentam-se as concentrações aproximadas dos íons mais abundantes em uma amostra de água típica dos oceanos e em uma amostra de água do Mar Morto: 1. Assinalando com um X a quadrícula
QUESTÃO 01 Neste quadro, apresentam-se as concentrações aproximadas dos íons mais abundantes em uma amostra de água típica dos oceanos e em uma amostra de água do Mar Morto: 1. Assinalando com um X a quadrícula
QUÍMICA. Questões de 09 a 12
 GRUP 1 TIP A QUÍ. 11 QUÍMICA Questões de 09 a 12 09. ácido sulfúrico, um dos insumos mais importantes da indústria química, é produzido pelo chamado Processo de Contato. Esse processo envolve as seguintes
GRUP 1 TIP A QUÍ. 11 QUÍMICA Questões de 09 a 12 09. ácido sulfúrico, um dos insumos mais importantes da indústria química, é produzido pelo chamado Processo de Contato. Esse processo envolve as seguintes
Não arredonde nenhum valor de massa consultado na tabela periódica.
 Ministério da Educação Secretaria de Educação Profissional e Tecnológica Instituto Federal de Educação, Ciência e Tecnologia de Minas Gerais Campus São João Evangelista Disciplina: Química II Professor:
Ministério da Educação Secretaria de Educação Profissional e Tecnológica Instituto Federal de Educação, Ciência e Tecnologia de Minas Gerais Campus São João Evangelista Disciplina: Química II Professor:
Física e Química A Tabela de Constantes Formulário Tabela Periódica
 Física e Quíica A Tabela de Constantes Forulário Tabela Periódica http://fisicanalixa.blogspot.pt/ CONSTANTES Velocidade de propagação da luz no vácuo c = 3,00 10 8 s 1 Módulo da aceleração gravítica de
Física e Quíica A Tabela de Constantes Forulário Tabela Periódica http://fisicanalixa.blogspot.pt/ CONSTANTES Velocidade de propagação da luz no vácuo c = 3,00 10 8 s 1 Módulo da aceleração gravítica de
Questão 46. Questão 48. Questão 47. alternativa D. alternativa E
 Questão 46 Correndo com uma bicicleta, ao longo de um trecho retilíneo de uma ciclovia, uma criança mantém a velocidade constante de módulo igual a,50 m/s. O diagrama horário da posição para esse movimento
Questão 46 Correndo com uma bicicleta, ao longo de um trecho retilíneo de uma ciclovia, uma criança mantém a velocidade constante de módulo igual a,50 m/s. O diagrama horário da posição para esse movimento
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação
 Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2011/1 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES IMPROTANTES: -
Universidade Federal de Goiás Instituto de Química Coordenação de Pós-graduação EXAME DE SELEÇÃO DO MESTRADO EM QUÍMICA 2011/1 IDENTIFICAÇÃO DO CANDIDATO Número de Inscrição: INSTRUÇÕES IMPROTANTES: -
QUÍMICA. Questões de 01 a 04
 GRUPO 1 QUÍ. 1 QUÍMICA Questões de 01 a 04 01. Os íons cálcio dissolvidos em água são responsáveis pela dureza desta. Em determinadas regiões do Estado de Minas Gerais, nas estações de tratamento de água,
GRUPO 1 QUÍ. 1 QUÍMICA Questões de 01 a 04 01. Os íons cálcio dissolvidos em água são responsáveis pela dureza desta. Em determinadas regiões do Estado de Minas Gerais, nas estações de tratamento de água,
BANCO DE QUESTÕES - BIOLOGIA - 1ª SÉRIE - ENSINO MÉDIO ==============================================================================================
 PROFESSOR: Leonardo Mariscal BANCO DE QUESTÕES - BIOLOGIA - 1ª SÉRIE - ENSINO MÉDIO ============================================================================================== Assunto: Organelas citoplasmáticas
PROFESSOR: Leonardo Mariscal BANCO DE QUESTÕES - BIOLOGIA - 1ª SÉRIE - ENSINO MÉDIO ============================================================================================== Assunto: Organelas citoplasmáticas
Somente identifique sua prova com o código de inscrição (não coloque seu nome);
 Minas Gerais PPGMQMG 1/019 Orientações gerais Somente identifique sua prova com o código de inscrição (não coloque seu nome); Assim que assinar a lista de presença verifique seu código de inscrição e preencha
Minas Gerais PPGMQMG 1/019 Orientações gerais Somente identifique sua prova com o código de inscrição (não coloque seu nome); Assim que assinar a lista de presença verifique seu código de inscrição e preencha
UNIVERSIDADE FEDERAL DE ALAGOAS POLÍCIA MILITAR DE ALAGOAS CORPO DE BOMBEIROS MILITAR DE ALAGOAS. Coordenadoria Permanente do Vestibular (COPEVE)
 UNIVERSIDADE FEDERAL DE ALAGOAS POLÍCIA MILITAR DE ALAGOAS CORPO DE BOMBEIROS MILITAR DE ALAGOAS Coordenadoria Permanente do Vestibular (COPEVE) PSS - 2002 QUÍMICA INSTRUÇÕES - Ao receber este caderno
UNIVERSIDADE FEDERAL DE ALAGOAS POLÍCIA MILITAR DE ALAGOAS CORPO DE BOMBEIROS MILITAR DE ALAGOAS Coordenadoria Permanente do Vestibular (COPEVE) PSS - 2002 QUÍMICA INSTRUÇÕES - Ao receber este caderno
Escolha sua melhor opção e estude para concursos sem gastar nada
 Escolha sua melhor opção e estude para concursos sem gastar nada VALORES DE CONSTANTES E GRANDEZAS FÍSICAS - aceleração da gravidade g = 10 m/s 2 - calor específico da água c = 1,0 cal/(g o C) = 4,2 x
Escolha sua melhor opção e estude para concursos sem gastar nada VALORES DE CONSTANTES E GRANDEZAS FÍSICAS - aceleração da gravidade g = 10 m/s 2 - calor específico da água c = 1,0 cal/(g o C) = 4,2 x
Respostas da terceira lista de exercícios de química. Prof a. Marcia M. Meier
 Respostas da terceira lista de exercícios de química Prof a. Marcia M. Meier 1) O íon brometo não aceita mais de um elétron, pois este segundo elétron ocupará numeros quânticos maiores quando comparado
Respostas da terceira lista de exercícios de química Prof a. Marcia M. Meier 1) O íon brometo não aceita mais de um elétron, pois este segundo elétron ocupará numeros quânticos maiores quando comparado
Mecânica 2007/2008. 3ª Série
 Mecânica 2007/2008 3ª Série Questões: 1. Se o ouro fosse vendido a peso, preferia comprá-lo na serra da Estrela ou em Lisboa? Se fosse vendido pela massa em qual das duas localidades preferia comprá-lo?
Mecânica 2007/2008 3ª Série Questões: 1. Se o ouro fosse vendido a peso, preferia comprá-lo na serra da Estrela ou em Lisboa? Se fosse vendido pela massa em qual das duas localidades preferia comprá-lo?
Exercícios para a Prova 1 de Química - 1 Trimestre
 Exercícios para a Prova 1 de Química - 1 Trimestre 1. Seja o esquema: Entre as alternativas abaixo, indique as corretas sobre o esquema: a) Temos 5 componentes. b) É formado por 2 substâncias simples.
Exercícios para a Prova 1 de Química - 1 Trimestre 1. Seja o esquema: Entre as alternativas abaixo, indique as corretas sobre o esquema: a) Temos 5 componentes. b) É formado por 2 substâncias simples.
(a) a aceleração do sistema. (b) as tensões T 1 e T 2 nos fios ligados a m 1 e m 2. Dado: momento de inércia da polia I = MR / 2
 F128-Lista 11 1) Como parte de uma inspeção de manutenção, a turbina de um motor a jato é posta a girar de acordo com o gráfico mostrado na Fig. 15. Quantas revoluções esta turbina realizou durante o teste?
F128-Lista 11 1) Como parte de uma inspeção de manutenção, a turbina de um motor a jato é posta a girar de acordo com o gráfico mostrado na Fig. 15. Quantas revoluções esta turbina realizou durante o teste?
3) Uma mola de constante elástica k = 400 N/m é comprimida de 5 cm. Determinar a sua energia potencial elástica.
 Lista para a Terceira U.L. Trabalho e Energia 1) Um corpo de massa 4 kg encontra-se a uma altura de 16 m do solo. Admitindo o solo como nível de referência e supondo g = 10 m/s 2, calcular sua energia
Lista para a Terceira U.L. Trabalho e Energia 1) Um corpo de massa 4 kg encontra-se a uma altura de 16 m do solo. Admitindo o solo como nível de referência e supondo g = 10 m/s 2, calcular sua energia
LEIA ATENTAMENTE AS INSTRUÇÕES
 CADERNO DE QUESTÕES UNIVERSIDADE FEDERAL DE GOIÁS PRÓ-REITORIA DE GRADUAÇÃO CENTRO DE SELEÇÃO PROCESSO SELETIVO/2010-2 GRUPO 1 Química 1º DIA 06/06/2010 SÓ ABRA ESTE CADERNO QUANDO AUTORIZADO LEIA ATENTAMENTE
CADERNO DE QUESTÕES UNIVERSIDADE FEDERAL DE GOIÁS PRÓ-REITORIA DE GRADUAÇÃO CENTRO DE SELEÇÃO PROCESSO SELETIVO/2010-2 GRUPO 1 Química 1º DIA 06/06/2010 SÓ ABRA ESTE CADERNO QUANDO AUTORIZADO LEIA ATENTAMENTE
AULA 03 Tabela Periódica
 Faculdade de Tecnologia e Ciências FTC Colegiado de Engenharia Civil Química Geral AULA 03 Tabela Periódica PROFESSORA: Shaiala Aquino shaiaquino@hotmail.com Henry Moseley A.B.Chancourtois ( 1820-1886)
Faculdade de Tecnologia e Ciências FTC Colegiado de Engenharia Civil Química Geral AULA 03 Tabela Periódica PROFESSORA: Shaiala Aquino shaiaquino@hotmail.com Henry Moseley A.B.Chancourtois ( 1820-1886)
1. Qual a fórmula do composto formado entre o cálcio, Ca (Z = 20) e o flúor F (Z = 9)?
 EXERCÍCIOS REVISÃO 1ª série 1. Qual a fórmula do composto formado entre o cálcio, Ca (Z = 20) e o flúor F (Z = 9)? 2. Qual a fórmula do composto formado entre o potássio, K (Z = 19) e o enxofre, S (Z =
EXERCÍCIOS REVISÃO 1ª série 1. Qual a fórmula do composto formado entre o cálcio, Ca (Z = 20) e o flúor F (Z = 9)? 2. Qual a fórmula do composto formado entre o potássio, K (Z = 19) e o enxofre, S (Z =
COMENTÁRIO DA PROVA DE FÍSICA
 COMENTÁRIO DA PROVA DE FÍSICA A prova de Física da UFPR 2013/2014 apresentou algumas questões fáceis, algumas difíceis e maioria de questões médias. Dessa forma, é possível afirmar que, quanto ao nível,
COMENTÁRIO DA PROVA DE FÍSICA A prova de Física da UFPR 2013/2014 apresentou algumas questões fáceis, algumas difíceis e maioria de questões médias. Dessa forma, é possível afirmar que, quanto ao nível,
a) Incorreta. O aumento da temperatura desloca o equilíbrio para o lado direito, no sentido da formação do vapor (transformação endotérmica).
 01 a) Incorreta. O aumento da temperatura desloca o equilíbrio para o lado direito, no sentido da formação do vapor (transformação endotérmica). b) Incorreta. Quanto mais volátil o líquido, menor será
01 a) Incorreta. O aumento da temperatura desloca o equilíbrio para o lado direito, no sentido da formação do vapor (transformação endotérmica). b) Incorreta. Quanto mais volátil o líquido, menor será
Fortaleza Ceará TD DE FÍSICA ENEM PROF. ADRIANO OLIVEIRA/DATA: 30/08/2014
 TD DE FÍSICA ENEM PROF. ADRIANO OLIVEIRA/DATA: 30/08/2014 1. Uma ave marinha costuma mergulhar de uma altura de 20 m para buscar alimento no mar. Suponha que um desses mergulhos tenha sido feito em sentido
TD DE FÍSICA ENEM PROF. ADRIANO OLIVEIRA/DATA: 30/08/2014 1. Uma ave marinha costuma mergulhar de uma altura de 20 m para buscar alimento no mar. Suponha que um desses mergulhos tenha sido feito em sentido
Soluções das Questões de Física da Universidade do Estado do Rio de Janeiro UERJ
 Soluções das Questões de Física da Universidade do Estado do Rio de Janeiro UERJ º Exame de Qualificação 011 Questão 6 Vestibular 011 No interior de um avião que se desloca horizontalmente em relação ao
Soluções das Questões de Física da Universidade do Estado do Rio de Janeiro UERJ º Exame de Qualificação 011 Questão 6 Vestibular 011 No interior de um avião que se desloca horizontalmente em relação ao
AVALIAÇÃO 05 QUÍMICA III UNIDADE Valor = 10,0 (Dez)
 Aluno(a) Turma N o Série 2 a Ensino Médio Data 16 / 08 / 11 INSTRUÇÕES: AVALIAÇÃO 05 QUÍMICA III UNIDADE Valor = 10,0 (Dez) I. Leia cuidadosamente o enunciado de cada questão, formule suas respostas com
Aluno(a) Turma N o Série 2 a Ensino Médio Data 16 / 08 / 11 INSTRUÇÕES: AVALIAÇÃO 05 QUÍMICA III UNIDADE Valor = 10,0 (Dez) I. Leia cuidadosamente o enunciado de cada questão, formule suas respostas com
COLÉGIO NOSSA SENHORA DA PIEDADE. Programa de Recuperação Final. 1ª Etapa 2013. Ano: 1
 COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final 1ª Etapa 2013 Disciplina: Química Professora: Maria Luiza Ano: 1 Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista de
COLÉGIO NOSSA SENHORA DA PIEDADE Programa de Recuperação Final 1ª Etapa 2013 Disciplina: Química Professora: Maria Luiza Ano: 1 Caro aluno, você está recebendo o conteúdo de recuperação. Faça a lista de
Lista de Exercícios para Recuperação Final. Nome: Nº 1 º ano / Ensino Médio Turma: A e B Disciplina(s): Física LISTA DE EXERCÍCIOS RECUPERAÇÃO - I
 Lista de Exercícios para Recuperação Final Nome: Nº 1 º ano / Ensino Médio Turma: A e B Disciplina(s): Física Data: 04/12/2014 Professor(a): SANDRA HELENA LISTA DE EXERCÍCIOS RECUPERAÇÃO - I 1. Dois móveis
Lista de Exercícios para Recuperação Final Nome: Nº 1 º ano / Ensino Médio Turma: A e B Disciplina(s): Física Data: 04/12/2014 Professor(a): SANDRA HELENA LISTA DE EXERCÍCIOS RECUPERAÇÃO - I 1. Dois móveis
Equipe de Química QUÍMICA
 Aluno (a): Série: 3ª Turma: TUTORIAL 11R Ensino Médio Equipe de Química Data: QUÍMICA SOLUÇÕES As misturas podem ser homogêneas ou heterogêneas. As misturas homogêneas possuem uma fase distinta. As misturas
Aluno (a): Série: 3ª Turma: TUTORIAL 11R Ensino Médio Equipe de Química Data: QUÍMICA SOLUÇÕES As misturas podem ser homogêneas ou heterogêneas. As misturas homogêneas possuem uma fase distinta. As misturas
Medicina. Prova Discursiva. Caderno de Prova. Instruções. Informações Gerais. Boa prova! 16/12/2012
 Prova Discursiva Medicina 16/12/2012 Caderno de Prova Este caderno, com 16 páginas numeradas sequencialmente, contém 5 questões de Biologia e 5 questões de Química. A Classificação Periódica dos Elementos
Prova Discursiva Medicina 16/12/2012 Caderno de Prova Este caderno, com 16 páginas numeradas sequencialmente, contém 5 questões de Biologia e 5 questões de Química. A Classificação Periódica dos Elementos
APOSTILA TECNOLOGIA MECANICA
 FACULDADE DE TECNOLOGIA DE POMPEIA CURSO TECNOLOGIA EM MECANIZAÇÃO EM AGRICULTURA DE PRECISÃO APOSTILA TECNOLOGIA MECANICA Autor: Carlos Safreire Daniel Ramos Leandro Ferneta Lorival Panuto Patrícia de
FACULDADE DE TECNOLOGIA DE POMPEIA CURSO TECNOLOGIA EM MECANIZAÇÃO EM AGRICULTURA DE PRECISÃO APOSTILA TECNOLOGIA MECANICA Autor: Carlos Safreire Daniel Ramos Leandro Ferneta Lorival Panuto Patrícia de
QUÍMICA SEGUNDA ETAPA - 1997
 QUÍMICA SEGUNDA ETAPA - 1997 QUESTÃO 01 Os valores das sucessivas energias de ionização de um átomo constituem uma evidência empírica da existência de níveis de energia. Os diagramas abaixo pretendem representar,
QUÍMICA SEGUNDA ETAPA - 1997 QUESTÃO 01 Os valores das sucessivas energias de ionização de um átomo constituem uma evidência empírica da existência de níveis de energia. Os diagramas abaixo pretendem representar,
PROVA DE QUÍMICA MÓDULO I DO PISM (triênio )
 PRVA DE QUÍMICA MÓDUL I D PISM (triênio 006-008) CLASSIFICAÇÃ PERIÓDICA DS ELEMENTS 1 18 1 3 4 6 7 1 1,0 3 Li 6,9 11 Na 3,0 19 K 39,1 37 Rb 8, Cs 13,9 67 Fr 3,0 4 Be 9,0 1 Mg 4,3 0 Ca 40,1 38 Sr 87,6 6
PRVA DE QUÍMICA MÓDUL I D PISM (triênio 006-008) CLASSIFICAÇÃ PERIÓDICA DS ELEMENTS 1 18 1 3 4 6 7 1 1,0 3 Li 6,9 11 Na 3,0 19 K 39,1 37 Rb 8, Cs 13,9 67 Fr 3,0 4 Be 9,0 1 Mg 4,3 0 Ca 40,1 38 Sr 87,6 6
Aulas 13 e 14. Soluções
 Aulas 13 e 14 Soluções Definição Solução é a denominação ao sistema em que uma substância está distribuída, ou disseminada, numa segunda substância sob forma de pequenas partículas. Exemplos Dissolvendo-se
Aulas 13 e 14 Soluções Definição Solução é a denominação ao sistema em que uma substância está distribuída, ou disseminada, numa segunda substância sob forma de pequenas partículas. Exemplos Dissolvendo-se
Intensivo 2015.2. Trabalho, potência e Energia mecânica. Obs: cada andar do edifício tem aproximadamente 2,5m.
 Intensivo 2015.2 Trabalho, potência e Energia mecânica 01 - (PUC PR) Uma motocicleta de massa 100kg se desloca a uma velocidade constante de 10m/s. A energia cinética desse veículo é equivalente ao trabalho
Intensivo 2015.2 Trabalho, potência e Energia mecânica 01 - (PUC PR) Uma motocicleta de massa 100kg se desloca a uma velocidade constante de 10m/s. A energia cinética desse veículo é equivalente ao trabalho
Trabalho e potência. 1º caso: a força F não é paralela a d. 2º caso: a força F é paralela a d. 3º caso: a força F é perpendicular a d
 Trabalho e potência Trabalho mecânico Realizar trabalho, em Física, implica a transferência de energia de um sistema para outro e, para que isso ocorra, são necessários uma força e um deslocamento adequados.
Trabalho e potência Trabalho mecânico Realizar trabalho, em Física, implica a transferência de energia de um sistema para outro e, para que isso ocorra, são necessários uma força e um deslocamento adequados.
Biologia. Sistema circulatório
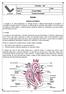 Aluno (a): Série: 3ª Turma: TUTORIAL 10R Ensino Médio Equipe de Biologia Data: Biologia Sistema circulatório O coração e os vasos sanguíneos e o sangue formam o sistema cardiovascular ou circulatório.
Aluno (a): Série: 3ª Turma: TUTORIAL 10R Ensino Médio Equipe de Biologia Data: Biologia Sistema circulatório O coração e os vasos sanguíneos e o sangue formam o sistema cardiovascular ou circulatório.
a) h0/16 b) h0/8 c) h0/4 d) h0/3 e) h0/2 Gabarito: A
 FÍSICA. Para um corpo em MHS de amplitude A, que se encontra incialmente na posição A/, com velocidade positiva, a fase inicial é, em radianos, a) b) c) d) e). O planeta Terra possui raio R e gira com
FÍSICA. Para um corpo em MHS de amplitude A, que se encontra incialmente na posição A/, com velocidade positiva, a fase inicial é, em radianos, a) b) c) d) e). O planeta Terra possui raio R e gira com
ELETRÓLISE - TEORIA. Eletrólitos são condutores iônicos de corrente elétrica. Para que ocorra essa condução, é necessário:
 ELETRÓLISE - TEORIA Introdução Dentro do estudo de eletroquímica temos a eletrólise, que consiste num processo não-espontâneo, baseado na decomposição de uma espécie química (eletrólito) por uma corrente
ELETRÓLISE - TEORIA Introdução Dentro do estudo de eletroquímica temos a eletrólise, que consiste num processo não-espontâneo, baseado na decomposição de uma espécie química (eletrólito) por uma corrente
Projeto rumo ao ita. Química. Exercícios de Fixação. Exercícios Propostos. Termodinâmica. ITA/IME Pré-Universitário 1. 06. Um gás ideal, com C p
 Química Termodinâmica Exercícios de Fixação 06. Um gás ideal, com C p = (5/2)R e C v = (3/2)R, é levado de P 1 = 1 bar e V 1 t = 12 m³ para P 2 = 12 bar e V 2 t = 1m³ através dos seguintes processos mecanicamente
Química Termodinâmica Exercícios de Fixação 06. Um gás ideal, com C p = (5/2)R e C v = (3/2)R, é levado de P 1 = 1 bar e V 1 t = 12 m³ para P 2 = 12 bar e V 2 t = 1m³ através dos seguintes processos mecanicamente
Lista de Exercícios - Unidade 8 Eu tenho a força!
 Lista de Exercícios - Unidade 8 Eu tenho a força! Forças 1. (UFSM 2013) O uso de hélices para propulsão de aviões ainda é muito frequente. Quando em movimento, essas hélices empurram o ar para trás; por
Lista de Exercícios - Unidade 8 Eu tenho a força! Forças 1. (UFSM 2013) O uso de hélices para propulsão de aviões ainda é muito frequente. Quando em movimento, essas hélices empurram o ar para trás; por
Olimpíada Brasileira de Física 2001 2ª Fase
 Olimpíada Brasileira de Física 2001 2ª Fase Gabarito dos Exames para o 1º e 2º Anos 1ª QUESTÃO Movimento Retilíneo Uniforme Em um MRU a posição s(t) do móvel é dada por s(t) = s 0 + vt, onde s 0 é a posição
Olimpíada Brasileira de Física 2001 2ª Fase Gabarito dos Exames para o 1º e 2º Anos 1ª QUESTÃO Movimento Retilíneo Uniforme Em um MRU a posição s(t) do móvel é dada por s(t) = s 0 + vt, onde s 0 é a posição
Vazamento cria dúvidas sobre futuro da energia nuclear
 Educadora: Daiana de Oliveira Componente Curricular: Ciências Data: / /2012 Estudante: 9º ano Vazamento cria dúvidas sobre futuro da energia nuclear Tragédia na usina de Fukushima, no Japão, faz com que
Educadora: Daiana de Oliveira Componente Curricular: Ciências Data: / /2012 Estudante: 9º ano Vazamento cria dúvidas sobre futuro da energia nuclear Tragédia na usina de Fukushima, no Japão, faz com que
Exame de Seleção Mestrado em Química Turma 2015 I
 UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2015
UNIVERSIDADE ESTADUAL DE SANTA CRUZ PRÓ-REITORIA DE PESQUISA E PÓS-GRADUAÇÃO DPTO DE CIÊNCIAS EXATAS E TECNOLÓGICAS PROGRAMA DE PÓS-GRADUAÇÃO EM QUÍMICA Exame de Seleção Mestrado em Química Turma 2015
UFMG - 2003 3º DIA QUÍMICA BERNOULLI COLÉGIO E PRÉ-VESTIBULAR
 UFMG - 2003 3º DIA QUÍMICA BERNULLI CLÉGI E PRÉ-VESTIBULAR Química Questão 01 A glicose, C 6 6, é uma das fontes de energia mais importantes para os organismos vivos. A levedura, por exemplo, responsável
UFMG - 2003 3º DIA QUÍMICA BERNULLI CLÉGI E PRÉ-VESTIBULAR Química Questão 01 A glicose, C 6 6, é uma das fontes de energia mais importantes para os organismos vivos. A levedura, por exemplo, responsável
