RMN em proteínas pequenas
|
|
|
- Sebastião Cesário
- 5 Há anos
- Visualizações:
Transcrição
1 COSY COrrelated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) mais simples Primeiro experimento 2D proposto (Jeener, 1971) Período de mistura: 1 único pulso de 90 Transferência da coerência entre spins acoplados escalarmente (max. 3 ligações) Permite obter as constantes de acoplamento J entre spins acoplados
2 TOCSY TOtal Correlated SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) Período de mistura: sequência spin-lock entre dois pulsos de 90 Transferências sucessivas da coerência entre spins acoplados escalarmente (max. 3 ligações em cada transferência)
3 NOESY Nuclear Overhauser Enhancement SpectroscopY Experimento 2D homonuclear ( 1 H- 1 H) Período de mistura: tempo de espera entre dois pulsos de 90 Transferência da coerência entre spins acoplados dipolarmente (max. 5 Å de distância) via efeito Overhauser nuclear (NOE)
4 RMN em proteínas pequenas 1D 1 H: grande sobreposição de picos 2D COSY: sistemas de spin; acoplamento J TOCSY: sistemas de spin NOESY: assinalamento seqüencial; NOEs
5 1D 1 H a proteína está estruturada? a amostra possui impurezas? a proteína está agregada? pode ser utilizado para determinar a concentração da amostra
6 2D COSY picos cruzados entre prótons com até 3 ligações químicas entre si (sistema de spin) Não conecta um aminoácido com outro Aminoácidos serão sistemas de spin independentes: assinalamento mostra padrão em fase-antifase, que pode ser utilizado para calcular J A equação de Kaplus relaciona o valor de 3 J NHA ao angulo O gráfico de Ramachandran limita o valor do ângulo Restrição experimental estrutural
7 2D TOCSY picos cruzados entre todos os prótons de um sistema de spin Conecta (quase!) todos os prótons de um aminoácido: assinalamento COSY TOCSY
8 Glicina (Gly, G) Sistema: AX menor aminoácido oticamente inativo alifático hidrofóbico (0.67) neutro peso molecular = 57 ocorrência % = 7.5 pka's : N = 9.60 C = 2.35 pi = 5.97 único aminoácido com dois prótons A (HA1 e HA2) em geral ocorre quebra de degenerescência dos prótons HA1 e HA2 acoplamento HA1-HA2 é usualmente forte e pode ser visto nos espectros COSY ou TOCSY
9 Alanina (Ala, A) Sistema: A3X alifático hidrofóbico (1.0) neutro peso molecular = 71 ocorrência % = 9.0 pka's : N = 9.69 C = 2.34 pi = 6.01 pico intenso HN-HB 3 no espectro TOCSY pico intenso HA-HB 3 nos espectros TOCSY e COSY
10 Treonina (Thr, T) Sistema: A3MX faz pontes de hidrogênio polar hidrofílico (-0.75) neutro peso molecular = 101 ocorrência % = 6.0 pka's : N = 9.62 C = 2.11 pi = 5.87 o próton HG1 pode aparecer nos espectros (~5 ppm) caso realizar uma ponte de hidrogênio as vezes os deslocamentos químicos dos prótons HB são maiores do que do próton HA pico intenso HA-HG2 3 no espectro TOCSY picos intensos HB1,2-HG2 3 nos espectros TOCSY e COSY pico HA-HG2 3 semelhante ao pico HA-HB 3 da Alanina, porém mais fraco
11 Serina (Ser, S) Sistema: AMX faz pontes de hidrogênio polar hidrofílico (-1.1) neutro peso molecular = 87 ocorrência % = 7.1 pka's : N = 9.15 C = 2.21 pi = 5.68 em geral ocorre quebra de degenerescência dos prótons HB1 e HB2 o próton HG1 pode aparecer nos espectros (~5 ppm) caso realizar uma ponte de hidrogênio assinalar, inicialmente, apenas como resíduo AMX
12 Cisteína (Cys, C) Sistema: AMX grupo sulfidril (-SH) altamente reativo forma ligações de dissulfeto hidrofóbico (0.17) levemente carregado peso molecular = 103 ocorrência % = 2.8 pka's : N = 8.18 C = 1.96 R = pi = 5.07 as formas reduzida e oxidada costumam apresentar deslocamentos químicos distintos assinalar, inicialmente, apenas como resíduo AMX
13 Aspartato (Asp, D) Sistema: AMX polar hidrofílico (-3.0) carga negativa (ácido) peso molecular = 115 ocorrência % = 5.5 pka's : N = 9.60 C = 2.19 R = 3.65 pi = 2.77 assinalar, inicialmente, apenas como resíduo AMX
14 Asparagina (Asn, N) Sistema: AMX + AX amina na cadeia lateral faz pontes de hidrogênio polar hidrofílico (-2.7) neutro peso molecular = 114 ocorrência % = 4.4 pka's : N = 8.08 C = 2.02 pi = 5.41 assinalar, inicialmente, apenas como resíduo AMX os prótons HD21 e HD22 estão desconectados (via COSY e TOCSY) do resto do sistema pico TOCSY entre os dois prótons HD21 e HD22 picos NOE conectando os dois prótons HD21 e HD22 com HB1 e HB2
15 Metionina (Met, M) Sistema: AM(PT)X + A inicializador de proteínas átomo de S em ligação tio-éter (-S-CH3) hidrofóbico (1.1) neutro peso molecular = 131 ocorrência % = 1.7 pka's : N = 9.21 C = 2.28 pi = 5.74 assinalar, inicialmente, apenas como resíduo AM(PT)X deslocamentos químicos HB1 e HB2 são menores doque de HG1 e HG2 o grupo metil HE 3 está desconectado (via COSY e TOCSY) do resto do sistema, e só aparece como um pico forte na diagonal pico NOE conectando o grupo metil HE 3 com HG1 e HG2
16 Glutamato (Glu, E) Sistema: AM(PT)X polar hidrofílico (-2.6) carga negativa (ácido) peso molecular = 129 ocorrência % = 62 pka's : N = 9.67 C = 2.19 R = 4.25 pi = 3.2 assinalar, inicialmente, apenas como resíduo AM(PT)X deslocamentos químicos HB1 e HB2 são menores doque de HG1 e HG2
17 Glutamina (Gln, Q) Sistema: AM(PT)X + AX amina na cadeia lateral faz pontes de hidrogênio polar hidrofílico (-2.9) neutro peso molecular = 128 ocorrência % = 3.9 pka's : N = 9.13 C = 2.17 pi = 5.65 assinalar, inicialmente, apenas como resíduo AM(PT)X deslocamentos químicos HB1 e HB2 são menores doque de HG1 e HG2 os prótons HE21 e HE22 estão desconectados (via COSY e TOCSY) do resto do sistema pico TOCSY entre os dois prótons HE21 e HE22 picos NOE conectando os dois prótons HE21 e HE22 com HG1 e HG2
18 Histidina (His, H) Sistema: AMX + AX anel imidazol na cadeia lateral reativo polar hidrofílico (-1.7) carga positiva fraca (básico) peso molecular = 137 ocorrência % = 2.1 pka's : N = 9.17 C = 1.82 R = 6.00 pi = 7.5 assinalar, inicialmente, apenas como resíduo AMX os prótons do anel estão desconectados (via COSY e TOCSY) do resto do sistema deslocamentos químicos dos prótons do anel são, em geral, dependentes do ph prótons H-N (HD1 e HE2) do anel não são, em geral, observados pico TOCSY fraco entre os prótons H-C (HD2 e HE1) do anel picos NOE conectando os dois prótons HB1 e HB2 com o próton HD2 do anel
19 Tirosina (Tyr, Y) Sistema: AMX+AA'XX' faz ponte de hidrogênio absorve UV aromático polar hidrofóbico (0.08) fracamente carregado peso molecular = 163 ocorrência % = 3.5 pka's : N = 9.11 C = 2.20 R = pi = 5.66 assinalar, inicialmente, apenas como resíduo AMX os prótons do anel estão desconectados (via COSY e TOCSY) do resto do sistema prótons HD1,2 são, em geral, degenerados prótons HE1,2 são, em geral, degenerados pico TOCSY e COSY fortes entre os prótons do anel picos NOE conectando os dois prótons HB1 e HB2 com os prótons HD1,2 do anel
20 Fenilalanina (Phe, F) Sistema: AMX+AA'XX'M absorve UV aromático fortemente hidrofóbico (2.5) neutro peso molecular = 147 ocorrência % = 3.5 pka's : N = 9.13 C = 1.83 pi = 5.48 assinalar, inicialmente, apenas como resíduo AMX os prótons do anel estão desconectados (via COSY e TOCSY) do resto do sistema prótons HD1,2 são, em geral, degenerados prótons HE1,2 são, em geral, degenerados pico TOCSY e COSY fortes entre os prótons do anel picos NOE conectando os dois prótons HB1 e HB2 com os prótons HD1,2 do anel
21 Triptofano (Trp, W) Sistema: AMX+A(X)MP+A maior aminoácido aminoácido mais raro faz pontes de hidrogênio absorve UV aromático polar fortemente hidrofóbico (1.5) neutro peso molecular = 186 ocorrência % = 1.1 pka's : N = 9.39 C = 2.38 pi = 5.89 assinalar, inicialmente, apenas como resíduo AMX próton HE1 do anel tem deslocamento químico próximo a 10 ppm os prótons dos dois anéis estão desconectados (via COSY e TOCSY) entre si e do resto do sistema pico TOCSY e COSY fortes entre os prótons de cada anel pico NOE intenso conectando os dois anéis (HE1 e HZ2) picos NOE conectando os dois prótons HB1 e HB2 com o próton HZ2 do anel
22 Valina (Val, V) Sistema: A3B3MX alifático hidrofóbico (2.3) neutro peso molecular = 99 ocorrência % = 6.9 pka's : N = 9.62 C = 2.32 pi = 5.97 picos intensos HA-HG1 3 e HA-HG2 3 no espectro TOCSY picos médios HN-HG1 3 e HN-HG2 3 no espectro TOCSY procurar pelo padrão característico nas linhas de HG1 3 e HG2 3 pode ocorrer degenerescência dos picos HG1 3 e HG2 3
23 Leucina (Leu, L) Sistema: A3B3MPTX isômero da Isoleucina alifático hidrofóbico (2.2) neutro peso molecular = 113 ocorrência % = 7.5 pka's : N = 9.60 C = 2.36 pi = 5.9 picos médios HA-HD1 3 e HA-HD2 3 no espectro TOCSY picos fracos HN-HD1 3 e HN-HD2 3 no espectro TOCSY procurar pelo padrão característico nas linhas de HD1 3 e HD2 3 deslocamentos químicos dos prótons HB1, HB e HG são praticamente idênticos pode ocorrer degenerescência dos picos HD1 3 e HD2 3
24 Isoleucina (Ile, I) Sistema: A3MPT(B3)X isômero da Leucina alifático hidrofóbico (3.1) neutro peso molecular = 113 ocorrência % = 4.6 pka's : N = 9.68 C = 2.36 pi = 6.02 picos forte HA-HG2 3 e médio HA-HD1 3 no espectro TOCSY picos médio HN-HG2 3 no e fraco HN-HD1 3 espectro TOCSY procurar pelo padrão característico nas linhas de HG2 3 e HD1 3
25 Lisina (Lys, K) Sistema: A2(F2T2)MPX amina na cadeia lateral reativo hidrofílico (-4.6) carga positiva forte (básico) peso molecular = 128 ocorrência % = 7.0 pka's : N = 8.95 C = 2.18 R = pi = 9.74 picos fortes HD1,2-HE1.2 nos espectros TOCSY e COSY picos HN-HE1,2 muito fracos ou ausentes picos HN-HZ1,2 não costumam aparecer os picos de acoplamento com HZ1,2 são, em geral, largos, podendo estar ausentes sistema muito fácil de ser confundido com a Arginina
26 Arginina (Arg, R) Sistema: A2(T2)MPX cadeia lateral guanidínica reativo hidrofílico (-7.5) carga positiva forte (básico) peso molecular = 156 ocorrência % = 4.7 pka's : N = 9.04 C = 2.17 R = pi = picos fortes HG1,2-HD1.2 nos espectros TOCSY e COSY picos HN-HD1,2 muito fracos ou ausentes pico HN-HE não costuma aparecer os picos de acoplamento com HE são, em geral, largos, podendo estar ausentes sistema muito fácil de ser confundido com a Lisina
27 Prolina (Pro, P) Sistema: A2(T2)MPX iminoácido promove turns alifático hidrofílico (-0.29) neutro peso molecular = 97 ocorrência % = 4.6 pka's : N = C = 1.99 pi = 6.48 não possui correlacões à esquerda da água pois não possui próton amídico HN os picos de acoplamento com HD1 e HD2 costumam aparecer em uma região relativamente descongestionada nos espectros TOCSY, COSY e NOESY sempre irá aparecer um pico de correlação NOESY de um dos prótons HD1, HD2 da prolina para o pico HA do resíduo anterior isomeria cis-trans pode provocar o aparecimento de um segundo sistema de spins semelhante
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA. Aminoácidos. Prof. Willame Bezerra
 CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
CURSO: ENFERMAGEM DISCIPLINA: BIOQUÍMICA HUMANA PROF. WILLAME BEZERRA Aminoácidos Prof. Willame Bezerra As proteínas são as biomoléculas mais abundantes nos seres vivos e exercem funções fundamentais em
13/08/2018. Escala de ph. Escala de ph. Crescimento básico. Crescimento ácido. Neutro. básico
 Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Escala de ph Crescimento básico Neutro Crescimento ácido Escala de ph básico 1 Sistema tampão Um par conjugado ácido-base tende a resistir a alteração de ph, quando pequenas quantidades de ácido ou base
Aminoácidos. Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP.
 Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aminoácidos Prof. Dr. Walter F. de Azevedo Jr. Laboratório de Sistemas BioMoleculares. Departamento de Física. UNESP São José do Rio Preto. SP. Resumo Introdução Quiralidade Ligação peptídica Cadeia peptídica
Aminoácidos peptídeos e proteínas
 Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Pontifícia Universidade Católica de Goiás Departamento de Biologia Aminoácidos peptídeos e proteínas Prof. Macks Wendhell Gonçalves, Msc mackswendhell@gmail.com Algumas funções de proteínas A luz produzida
Aminoácidos não-essenciais: alanina, ácido aspártico, ácido glutâmico, cisteína, glicina, glutamina, hidroxiprolina, prolina, serina e tirosina.
 AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
AMINOÁCIDOS Os aminoácidos são as unidades fundamentais das PROTEÍNAS. Existem cerca de 300 aminoácidos na natureza, mas nas proteínas podemos encontrar 20 aminoácidos principais Estruturalmente são formados
Experimento 1D. Consiste de dois períodos, nos quais sequências complexas de pulsos intercalados com tempos de espera podem ocorrer.
 Experimento 1D Consiste de dois períodos, nos quais sequências complexas de pulsos intercalados com tempos de espera podem ocorrer. preparação dos spins através de pulsos e de tempos de espera detecção
Experimento 1D Consiste de dois períodos, nos quais sequências complexas de pulsos intercalados com tempos de espera podem ocorrer. preparação dos spins através de pulsos e de tempos de espera detecção
Aminoácidos FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS Aminoácidos Disciplina: Bioquímica I Prof. Me. Cássio Resende de Morais Introdução Proteínas são as macromoléculas
Programa de Pós-Graduação em Química
 1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
1/12 Programa de Pós-Graduação em Química PROVA DE CONHECIMENTOS ESPECÍFICOS Duração da Prova: 4 horas São José do Rio Preto, 24 de Janeiro de 2013. Departamento 1 2/12 Questão 1. Os haloalcanos, também
1164 BIOLOGIA ESTRUTURAL Aula 1 Prof. Dr. Valmir Fadel
 H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
H C N O S Água Pontes de Hidrogênio -Interação fraca com grupos polares e carregados - orientada (Lehninger, cap. 4) AMINO-ÁCIDOS ISÔMERO L ISÔMERO D 20 amino-ácidos mais comuns Alanina CH3-CH(NH2)-COOH
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Propriedades, funções e transformações de aminoácidos e proteínas
14/02/2017. Genética. Professora Catarina
 14/02/2017 Genética Professora Catarina 1 A espécie humana Ácidos nucleicos Tipos DNA ácido desoxirribonucleico RNA ácido ribonucleico São formados pela união de nucleotídeos. 2 Composição dos nucleotídeos
14/02/2017 Genética Professora Catarina 1 A espécie humana Ácidos nucleicos Tipos DNA ácido desoxirribonucleico RNA ácido ribonucleico São formados pela união de nucleotídeos. 2 Composição dos nucleotídeos
Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila
 Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
Aminoácidos e Peptídios 1 Aminoácidos Aminoácido: um composto que contém tanto um grupo amino como um grupo carboxila aaminoácido: têm um grupo carboxila e um grupo amino ligados ao mesmo átomo de carbono
BÁSICA EM IMAGENS. Aminoácidos, peptídeos e proteínas
 Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Universidade Federal de Pelotas Instituto de Química e Geociências Departamento de Bioquímica 04 BÁSICA EM IMAGENS - um guia para a sala de aula Aminoácidos, peptídeos e proteínas Generalidades AAs x Proteínas
Rafael Mesquita. Aminoácidos
 Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Aminoácidos As Proteínas são polímeros de Aminoácidos Os Aminoácidos apresentam pelo menos um grupo carboxílico e um grupo amino Aminoácidos têm como fórmula geral COOH + H 3 N - C - H R Aminoácidos constituintes
Aula 1. Referência. Bancos de Dados. Linguagem x Informação. Introdução a Bioquímica: Biomoléculas. Introdução ao Curso: Aminoácidos.
 Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao urso: Aminoácidos eferência Autores: Ignez aracelli e Julio Zukerman-Schpector Editora: EdUFSar Ignez aracelli BioMat DF UNESP/Bauru Julio Zukerman
- Apresentam uma fórmula básica: um átomo central de carbono onde se ligam:
 1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
1 4 Aminoácidos e proteínas a) Aminoácidos - São encontrados polimerizados formando proteínas ou livres - São degradados, originando moléculas intermediárias da síntese de glicose e lipídeos - Alguns são
Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia REVISÃO QUÍMICA Principais grupos funcionais em proteômica O que é uma ligação de hidrogênio? átomo eletronegativo
Aminoácidos e Peptídeos. Profa. Alana Cecília
 Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
Aminoácidos e Peptídeos Profa. Alana Cecília O que são aminoácidos? A estrutura geral dos aminoácidos inclui um grupo amina e um grupo carboxila, ambos ligados ao carbono α (aquele próximo ao grupo carboxila);
AMINOÁCIDOS. Dra. Flávia Cristina Goulart. Bioquímica
 AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
AMINOÁCIDOS Dra. Flávia Cristina Goulart Bioquímica Os aminoácidos (aa). O que são? AMINOÁCIDOS São as unidades fundamentais das PROTEÍNAS. São ácidos orgânicos formados por átomos de carbono, hidrogênio,
REVISÃO: ENADE BIOQUÍMICA - 1
 FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
FUNDAÇÃO CARMELITANA MÁRIO PALMÉRIO FACIHUS - FACULDADE DE CIÊNCIAS HUMANAS E SOCIAIS REVISÃO: ENADE BIOQUÍMICA - 1 Prof. Me. Cássio Resende de Morais Propriedades da Água Introdução Substância líquida,
Soluções de Conjunto de Problemas 1
 Soluções de 7.012 Conjunto de Problemas 1 Questão 1 a) Quais são os quatro tipos principais de moléculas biológicas discutidos na aula? Cite uma função importante de cada tipo de molécula biológica na
Soluções de 7.012 Conjunto de Problemas 1 Questão 1 a) Quais são os quatro tipos principais de moléculas biológicas discutidos na aula? Cite uma função importante de cada tipo de molécula biológica na
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs
 Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
Aminoácidos (aas) Prof.ª: Suziane Antes Jacobs Introdução Pequenas moléculas propriedades únicas Unidades estruturais (UB) das proteínas N- essencial para a manutenção da vida; 20 aminoácidos-padrão -
Aminoácidos. subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes
 . Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
. Aminoácidos subunidades monoméricas que compõe a estrutura de milhares de proteínas diferentes aminoácido Para entender a estrutura 3D das proteínas, vamos dissecá-la em níveis organizacionais para facilitar
Bioinformática Estrutural Aula 1
 Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária Paula.kuser-falcao@embrapa.br Pratique Atividade Física Paula
Bioinformática Estrutural Aula 1 03 de Junho de 2013 Paula Kuser-Falcão Laboratório de Bioinformática Aplicada Embrapa Informática Agropecuária Paula.kuser-falcao@embrapa.br Pratique Atividade Física Paula
Aminoácidos. Bioquímica Prof. Dr. Marcelo Soares
 Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
Aminoácidos Aminoácidos Nutrição Século XIX: produtos contendo Nitrogênio eram essenciais para a sobrevivência dos animais G. J. Mulder (1839): termo Proteínas Gr Proteios (Primário) Teoria: Proteínas
COLÉGIO PEDRO II CAMPUS TIJUCA II. DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI
 COLÉGIO PEDRO II CAMPUS TIJUCA II DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI 1º & 2º TURNOS 3ª SÉRIE / ENSINO MÉDIO REGULAR & INTEGRADO ANO LETIVO 2015 PROFESSORES: FRED & PEDRO
COLÉGIO PEDRO II CAMPUS TIJUCA II DEPARTAMENTO DE BIOLOGIA E CIÊNCIAS COORD.: PROFa. CRISTIANA LIMONGI 1º & 2º TURNOS 3ª SÉRIE / ENSINO MÉDIO REGULAR & INTEGRADO ANO LETIVO 2015 PROFESSORES: FRED & PEDRO
CÓDIGO GENÉTICO E SÍNTESE PROTEICA
 Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA 1. Síntese de proteínas pelos ribossomos a partir do RNAm. a) RNAm: molécula de RNA que contem a informação genética necessária para
Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA 1. Síntese de proteínas pelos ribossomos a partir do RNAm. a) RNAm: molécula de RNA que contem a informação genética necessária para
Aminoácidos e Peptideos
 Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
Aminoácidos e Peptideos O que são aminoácidos? Precursores de vários tipos de biomoléculas Compostos formados por : um grupo amina primário [ ] um grupo ácido carboxílico [ ] ambos ligados a um carbono
13/03/2016. Profª. Drª. Andréa Fontes Garcia E -mail:
 Profª. Drª. Andréa Fontes Garcia E -mail: andrea@salesiano-ata.br 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
Profª. Drª. Andréa Fontes Garcia E -mail: andrea@salesiano-ata.br 1 Estrutura geral dos amionoácidos de ocorrência biológica Grupamento amino Grupamento carboxilato (ácido carboxílico) Hidrogênio Grupamento
BIOLOGIA EXERCÍCIOS. Anabolismo Nuclear
 Anabolismo Nuclear EXERCÍCIOS 1. mesmo responsável pela decodificação do genoma humano em 2001, o presidente dos EUA, Barack Obama, pediu a seus conselheiros especializados em biotecnologia para analisarem
Anabolismo Nuclear EXERCÍCIOS 1. mesmo responsável pela decodificação do genoma humano em 2001, o presidente dos EUA, Barack Obama, pediu a seus conselheiros especializados em biotecnologia para analisarem
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011
 BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
BIOQUÍMICA I 1º ano de Medicina Ensino teórico 2010/2011 7ª aula teórica 11 Outubro 2010 Proteínas estruturais e funcionais Organização estrutural das proteínas Estrutura e diferentes funções de proteínas
ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial. Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica
 ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica Prof. Diogo Schott diogo.schott@yahoo.com Substâncias orgânicas
ESCOLA TÉCNICA ESTADUAL FREDERICO GUILHERME SCHMIDT Escola Técnica Industrial Disciplina de Biologia Primeiro Ano Curso Técnico de Eletromecânica Prof. Diogo Schott diogo.schott@yahoo.com Substâncias orgânicas
Graduação em Biotecnologia Disciplina de Proteômica. Caroline Rizzi Doutoranda em Biotecnologia -UFPel
 Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia Aminoácidos Grupos funcionais em bioquímica Propriedades químicas da água Estrutura e
Graduação em Biotecnologia Disciplina de Proteômica Caroline Rizzi Doutoranda em Biotecnologia -UFPel Bibliografia Aminoácidos Grupos funcionais em bioquímica Propriedades químicas da água Estrutura e
Proteínas: aspectos gerais
 Proteínas: aspectos gerais As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (mais de 50% do seu peso seco) As proteínas são omnipresentes na célula, pois estão ligadas a todos
Proteínas: aspectos gerais As proteínas são os compostos orgânicos mais abundantes dos organismos vivos (mais de 50% do seu peso seco) As proteínas são omnipresentes na célula, pois estão ligadas a todos
 Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem do grego protos
1. INTRODUÇÃO. Polímeros biológicos. Polissacarídeos Proteínas Ácidos Nucléicos. Reservas de energia. Armazenamento e Transmissão de informações
 AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
AMINOÁIDOS 1. INTRODUÇÃO Polímeros biológicos Polissacarídeos Proteínas Ácidos Nucléicos Reservas de energia Materiais estruturais Marcadores bioquímicos Armazenamento e Transmissão de informações PROTEÍNAS
Aminoácidos e peptídeos. Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I
 Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e peptídeos Prof.: Matheus de Souza Gomes Disciplina: Bioquímica I Patos de Minas 2017 Conteúdo Aminoácidos e peptídeos Constituição das proteínas Aminoácidos Estrutura Classificação Ácido
Aminoácidos e Peptídeos
 Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
Aminoácidos e Peptídeos 1 Qual a importância em conhecer os aminoácidos? 2 Aminoácidos Peptídeos Proteínas (polipeptídeos) Mas... O que são essas biomoléculas e onde estão localizadas? 3 Proteínas e peptídeos:
a. RE: b. RE: c. RE:
 1. O veneno de diversas serpentes contém a enzima fosfolipase A2, que catalisa a hidrólise de ácidos graxos na posição C-2 dos glicerolfosfolipídeos. O produto fosfolipídico resultante dessa hidrólise
1. O veneno de diversas serpentes contém a enzima fosfolipase A2, que catalisa a hidrólise de ácidos graxos na posição C-2 dos glicerolfosfolipídeos. O produto fosfolipídico resultante dessa hidrólise
AMINOÁCIDOS.! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico NH2 I R - C - C = 0O I I H OH
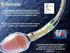 Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
Aminoácidos AMNOÁCDOS! São biomoléculas que apresentam na sua constituição as funções amina primária e ácido carboxílico radical R C-alfa N2 R - C - C = 0O O amina primária ácido carboxílico Aminoácidos
Entendem-se por compostos heterocíclicos, aqueles compostos orgânicos cíclicos estáveis, que contem no seu anel um ou mais átomos diferentes do
 1 2 3 Entendem-se por compostos heterocíclicos, aqueles compostos orgânicos cíclicos estáveis, que contem no seu anel um ou mais átomos diferentes do carbono. 4 5 O prefixo ribo também é aceitável para
1 2 3 Entendem-se por compostos heterocíclicos, aqueles compostos orgânicos cíclicos estáveis, que contem no seu anel um ou mais átomos diferentes do carbono. 4 5 O prefixo ribo também é aceitável para
Aminoácidos, Péptidos e Proteínas
 Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Aminoácidos, Péptidos e Proteínas Proteínas: -São as macromoléculas biológicas mais abundantes, presentes em todas as células. - Ocorrem numa variedade enorme numa mesma célula. - Exibem uma enorme diversidade
Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos. Referência: Stryer ou Lehninger
 Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos Referência: Stryer ou Lehninger Deoxi-hemoglobina Slide - Lehninger 5a edição Estrutura de proteínas
Estrutura e propriedade de aminoácidos Definição de ácidos fracos, fortes Ligação peptídica Peptídeos Referência: Stryer ou Lehninger Deoxi-hemoglobina Slide - Lehninger 5a edição Estrutura de proteínas
Bioinformática RESSONÂNCIA MAGNÉTICA NUCLEAR - RMN. Disciplina de Bioinformática Alunas: Rayssa H Arruda Pereira Taciane Barbosa Henriques
 Bioinformática RESSONÂNCIA MAGNÉTICA NUCLEAR - RMN Disciplina de Bioinformática Alunas: Rayssa H Arruda Pereira Taciane Barbosa Henriques Introdução A espectroscopia por Ressonância Magnética Nuclear (RMN)
Bioinformática RESSONÂNCIA MAGNÉTICA NUCLEAR - RMN Disciplina de Bioinformática Alunas: Rayssa H Arruda Pereira Taciane Barbosa Henriques Introdução A espectroscopia por Ressonância Magnética Nuclear (RMN)
4/14/2015. Proteínas. Fundamentos da Estrutura de Proteínas Parte 1. Funções biológicas das Proteínas
 1 Todo o material disponibilizado é preparado para as disciplinas que ministramos e colocado para ser acessado livremente pelos alunos ou interessados. Solicitamos que não seja colocado em sites nãolivres.
1 Todo o material disponibilizado é preparado para as disciplinas que ministramos e colocado para ser acessado livremente pelos alunos ou interessados. Solicitamos que não seja colocado em sites nãolivres.
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos
 Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
Proteínas São macromoléculas complexas, compostas de aminoácidos, e necessárias para os processos químicos que ocorrem nos organismos vivos São os constituintes básicos da vida: tanto que seu nome deriva
CÓDIGO GENÉTICO E SÍNTESE PROTEICA
 Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA Dogma central da Biologia Descreve o fluxo unidirecional de informações, do DNA à síntese de proteínas. Duplicação/Replicação Síntese
Terceirão Biologia 1 Professor João CÓDIGO GENÉTICO E SÍNTESE PROTEICA Dogma central da Biologia Descreve o fluxo unidirecional de informações, do DNA à síntese de proteínas. Duplicação/Replicação Síntese
Influência da Genética desempenho
 UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI luizcarnevalijr@usp.br
UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI luizcarnevalijr@usp.br
AMINOÁCIDOS. - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos;
 1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
1 AMINOÁCIDOS - Os aminoácidos são os elementos constituintes de peptídeos, proteínas; - Precursores de hormônios, neurotransmissores, nucleotídeos; - Ocorrem em grande variedade, sendo descritos cerca
Introdução. Estrutura dos Aminoácidos e Proteínas. Aminoácidos componentes de proteínas. Aminoácidos componentes de proteínas 10/02/2012.
 Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
Introdução Estrutura dos Aminoácidos e Prof. Dr. Bruno Lazzari de Lima : Componentes celulares mais importantes. Diversidade de forma e função. Estruturais. Enzimáticas. Transportadoras. Ex.: Insulina,
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
Você deve desenhar o aminoácido com o grupo amino protonado (pka > 7) e o grupo carboxílico desprotonado (pka <7).
 QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
QBQ4010 Introdução à Bioquímica Exercícios sobre sistema tampão, aminoácidos e estrutura de proteínas 1. Você estagiário de um laboratório bioquímica, recebeu a função de preparar uma solução tamponada
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS. Bianca Zingales IQ-USP
 MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
MÓDULO 1 ESTRUTURA DE BIOMOLÉCULAS Bianca Zingales IQ-USP Biomoléculas As biomoléculas são compostos químicos presentes nas células de todos os seres vivos. São em geral moléculas orgânicas, compostas
Lista de Exercícios Bioquímica de Macromoléculas - Nanotecnologia
 Lista de Exercícios Bioquímica de Macromoléculas - Nanotecnologia 1 - Catecóis substituídos com longas cadeias acilas são os componentes encontrados na urtiga responsáveis pela sensação de queimadura e
Lista de Exercícios Bioquímica de Macromoléculas - Nanotecnologia 1 - Catecóis substituídos com longas cadeias acilas são os componentes encontrados na urtiga responsáveis pela sensação de queimadura e
Bauru, 11 de agosto de 2008.
 Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao Curso: Aminoácidos Ignez Caracelli BioMat DF UNESP/Bauru Julio Zukerman Schpector LaCrEMM DQ UFSCar Bauru, 11 de agosto de 2008. 1 Avaliação 1seminário
Introdução a Bioquímica: Biomoléculas Aula 1 Introdução ao Curso: Aminoácidos Ignez Caracelli BioMat DF UNESP/Bauru Julio Zukerman Schpector LaCrEMM DQ UFSCar Bauru, 11 de agosto de 2008. 1 Avaliação 1seminário
Palavras chave: peptídeo; estrutura 3D; SDS micelas
 Estudo estrutural por RMN de 1 H de peptídeos bioativos isolados da secreção cutânea de Hypsiobas albopunctatus e Leptodactylus labyrinthicus Eliane Santana FERNANDES *1, Luciano Morais LIÃO 1, Aline Lima
Estudo estrutural por RMN de 1 H de peptídeos bioativos isolados da secreção cutânea de Hypsiobas albopunctatus e Leptodactylus labyrinthicus Eliane Santana FERNANDES *1, Luciano Morais LIÃO 1, Aline Lima
Composição química celular
 Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
Natália Paludetto Composição química celular Proteínas Enzimas Ácidos nucléicos Proteínas Substâncias sólidas; Componente orgânico mais abundante da célula. Podem fornecer energia quando oxidadas, mas
Astrobiologia azevedolab.net. Prof. Dr. Walter F. de Azevedo Jr.
 Astrobiologia azevedolab.net Prof. Dr. Walter F. de Azevedo Jr. O que é Astrobiologia? O que é vida? Estamos sozinhos no Universo? Hidrogênio Hélio Próton Nêutron Elétron F = G g Mm r 2 r m Onde G = 6,6726.10-11
Astrobiologia azevedolab.net Prof. Dr. Walter F. de Azevedo Jr. O que é Astrobiologia? O que é vida? Estamos sozinhos no Universo? Hidrogênio Hélio Próton Nêutron Elétron F = G g Mm r 2 r m Onde G = 6,6726.10-11
Aminoácidos AMINOÁCIDOS, PEPTÍDEOS E PROTEÍNAS. Universidade Federal de Mato Grosso Disciplina de Bioquímica H2N C COOH
 1 2 Universidade Federal de Mato Grosso Disciplina de Bioquímica AMINOÁCIDOS, PEPTÍDEOS E PROTEÍNAS Vagalume (fireflies) Prof. Ms. Reginaldo Vicente Ribeiro Eritrócitos Luciferina Rinoceronte Queratina
1 2 Universidade Federal de Mato Grosso Disciplina de Bioquímica AMINOÁCIDOS, PEPTÍDEOS E PROTEÍNAS Vagalume (fireflies) Prof. Ms. Reginaldo Vicente Ribeiro Eritrócitos Luciferina Rinoceronte Queratina
Professor Antônio Ruas
 Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
BIOQUÍMICA PARA ODONTO
 BIOQUÍMICA PARA ODONTO Aula 3: Autoria: Ligação peptídica Proteínas globulares: estrutura primária, secundária e terciária Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade
BIOQUÍMICA PARA ODONTO Aula 3: Autoria: Ligação peptídica Proteínas globulares: estrutura primária, secundária e terciária Luiza Higa Programa de Biologia Estrutural Instituto de Bioquímica Médica Universidade
A glicina é o mais simples dos aminoácidos. resíduo é facil de acomodar em estruturas. em qualquer conformação. O carbono α da glicina não é.
 Aminoácidos: Glicina A glicina é o mais simples dos aminoácidos. Devido à simplicidade da sua cadeia lateral este resíduo é facil de acomodar em estruturas proteícas, podendo surgir em qualquer local e
Aminoácidos: Glicina A glicina é o mais simples dos aminoácidos. Devido à simplicidade da sua cadeia lateral este resíduo é facil de acomodar em estruturas proteícas, podendo surgir em qualquer local e
Aula 1 Enzimas são Proteínas Globulares
 Aula 1 Enzimas são Proteínas Globulares Já existem 4.725 enzimas conhecidas, distribuídas em grupos de acordo com suas características catalíticas, como veremos na aula 2. Apesar de bem conhecidas atualmente,
Aula 1 Enzimas são Proteínas Globulares Já existem 4.725 enzimas conhecidas, distribuídas em grupos de acordo com suas características catalíticas, como veremos na aula 2. Apesar de bem conhecidas atualmente,
Aminoácidos. Estrutura e Função das Proteínas UNIDADE I I. VISÃO GERAL II. ESTRUTURA DOS AMINOÁCIDOS COOH C H R
 UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
Introdução aos aminoácidos
 MÓDULO 2 - AULA 8 Aminoácidos não essenciais Aminoácidos essenciais Glicina 11355 mg Lisina 1958 mg Prolina 6808 mg Leucina 1569 mg Hidroxiprolina 5789 mg Valina 1223 mg Ácido Glutâmico 5065 mg Fenilalanina
MÓDULO 2 - AULA 8 Aminoácidos não essenciais Aminoácidos essenciais Glicina 11355 mg Lisina 1958 mg Prolina 6808 mg Leucina 1569 mg Hidroxiprolina 5789 mg Valina 1223 mg Ácido Glutâmico 5065 mg Fenilalanina
Componentes Químicos das Células
 Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Componentes Químicos das Células Os seres vivos são um sistema Fundamentam-se em: químico! compostos de carbono, ou seja, na química orgânica. Dependem de reações químicas que ocorrem em soluções aquosas,
Química da Vida Nutrição
 Química da Vida Nutrição Prof. João Ronaldo Tavares de Vasconcellos Neto FEV/2011 Propriedades Atômicas Elementos e Compostos químicos; Alguns símbolos são derivados do latim Por Exemplo: o símbolo do
Química da Vida Nutrição Prof. João Ronaldo Tavares de Vasconcellos Neto FEV/2011 Propriedades Atômicas Elementos e Compostos químicos; Alguns símbolos são derivados do latim Por Exemplo: o símbolo do
Caraterização molecular e funcional de variantes alfa de hemoglobina identificadas no Centro Hospitalar e Universitário de Coimbra
 IV. Resultados Caraterização molecular e funcional de variantes alfa de hemoglobina identificadas no Centro Hospitalar e Universitário de Coimbra 59 Resultados 1. VARIANTES DESCRITAS Indivíduo I 1.1. CASO
IV. Resultados Caraterização molecular e funcional de variantes alfa de hemoglobina identificadas no Centro Hospitalar e Universitário de Coimbra 59 Resultados 1. VARIANTES DESCRITAS Indivíduo I 1.1. CASO
Estrutura das Proteínas pode ser descrita em 4 níveis de organização
 PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
PROTEÍNAS DNA Proteínas As proteínas são as macromoléculas mais abundantes nas células vivas. Elas são os instrumentos moleculares através dos quais a informação genética é expressa. O nome proteína vem
STRYER, L.; TYMOCZKO, J.L.; BERG, J.M.
 2 Proteínas: STRYER, L.; TYMOCZKO, J.L.; BERG, J.M. Bioquímica. 6 ed. Rio de Janeiro: Guanabara Koogan, 2008. Capítulo 2 e 3; as edições 4 e 5 também podem ser utilizadas (Cap. 3 e 4). 2.1 Aminoácidos
2 Proteínas: STRYER, L.; TYMOCZKO, J.L.; BERG, J.M. Bioquímica. 6 ed. Rio de Janeiro: Guanabara Koogan, 2008. Capítulo 2 e 3; as edições 4 e 5 também podem ser utilizadas (Cap. 3 e 4). 2.1 Aminoácidos
Biofísica azevedolab.net. Molecular Astrobiologia. Prof. Dr. Walter F. de Azevedo Jr.
 Biofísica Molecular Astrobiologia Prof. Dr. Walter F. de Azevedo Jr. O que é Astrobiologia? O que é vida? Estamos sozinhos no Universo? Hidrogênio Hélio Próton Nêutron Elétron F = G g Mm r 2 r m Onde G
Biofísica Molecular Astrobiologia Prof. Dr. Walter F. de Azevedo Jr. O que é Astrobiologia? O que é vida? Estamos sozinhos no Universo? Hidrogênio Hélio Próton Nêutron Elétron F = G g Mm r 2 r m Onde G
AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES
 Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Universidade Estadual Paulista Júlio de Mesquita Filho Faculdade de Odontologia de Araçatuba Departamento de Ciências Básicas AMINOÁCIDOS E PROTEÍNAS: ESTRUTURA E FUNÇÕES Professora Marcelle Danelon Tópicos
Aminoácidos. UNIDADE I Estrutura e Função das Proteínas COOH I. VISÃO GERAL II. ESTRUTURA DOS AMINOÁCIDOS. Aminoácido livre
 UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
UNIDADE I Estrutura e Função das Proteínas Aminoácidos 1 I. VISÃO GERAL As proteínas são as moléculas mais abundantes e com maior diversidade de funções nos sistemas vivos. Praticamente todos os processos
Professor Antônio Ruas
 Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Universidade Estadual do Rio Grande do Sul Curso Superior de Tecnologia em Gestão Ambiental Componente curricular: BIOLOGIA GERAL Aula 4 Professor Antônio Ruas 1. Temas: Macromoléculas celulares Produção
Origem grego (protos) primeira, mais importante
 PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
PROTEÍNAS Origem grego (protos) primeira, mais importante A palavra proteína que eu proponho vem derivada de proteos, porque ela parece ser a substância primitiva ou principal da nutrição animal, as plantas
Fármacos 8/13/2010. Aula 2 Fundamentos da Estrutura de Proteínas Parte 1. vai onde? o que vai fazer? de onde veio? onde foi parar?
 Introdução a Bioquímica: Biomoléculas Fármacos 1 Aula 2 Fundamentos da Estrutura de Proteínas Parte 1 Ignez aracelli Julio Zukerman Schpector São arlos, 16 de agosto de 2010. 4 vai onde? de onde veio?
Introdução a Bioquímica: Biomoléculas Fármacos 1 Aula 2 Fundamentos da Estrutura de Proteínas Parte 1 Ignez aracelli Julio Zukerman Schpector São arlos, 16 de agosto de 2010. 4 vai onde? de onde veio?
A QUÍMICA DOS AMINOÁCIDOS E PEPTÍDEOS
 A QUÍMICA DOS AMINOÁCIDOS E PEPTÍDEOS META Introduzir o estudo do conhecimento das estruturas e das propriedades químicas dos aminoácidos e peptídeos. OBJETIVOS Ao final desta aula, o aluno deverá: reconhecer
A QUÍMICA DOS AMINOÁCIDOS E PEPTÍDEOS META Introduzir o estudo do conhecimento das estruturas e das propriedades químicas dos aminoácidos e peptídeos. OBJETIVOS Ao final desta aula, o aluno deverá: reconhecer
COO - NH 3+ C H 08/12/2017. Estrutura dos aminoácidos. Aminoácidos no solo. Absorção AMINOÁCIDOS COMO SINALIZADORES EM PLANTAS
 Estrutura dos aminoácidos AMINOÁCIDOS COMO SINALIZADORES EM PLANTAS D.Sc. WALQUÍRIA FERNANDA TEIXEIRA COO - NH 3+ C H R Figura 1. Estrutura geral dos aminoácidos Absorção Aminoácidos no solo Aminoácidos
Estrutura dos aminoácidos AMINOÁCIDOS COMO SINALIZADORES EM PLANTAS D.Sc. WALQUÍRIA FERNANDA TEIXEIRA COO - NH 3+ C H R Figura 1. Estrutura geral dos aminoácidos Absorção Aminoácidos no solo Aminoácidos
Biologia Molecular (Parte I)
 Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
Biologia Molecular (Parte I) Introdução 1. Substâncias Inorgânicas 1.1. Água A água faz pontes de hidrogênio Polaridade Propriedades da água Solvente Universal Participa de reações químicas vitais Adesão
BIOQUÍMICA I AULAS PRÁTICAS. 2º ano, 1º semestre
 BIOQUÍMICA I AULAS PRÁTICAS 2º ano, 1º semestre 2013-2014 Objectivo Bases teórico/práticas das metodologias experimentais necessárias ao estudo qualitativo e quantitativo de macromoléculas - péptidos e
BIOQUÍMICA I AULAS PRÁTICAS 2º ano, 1º semestre 2013-2014 Objectivo Bases teórico/práticas das metodologias experimentais necessárias ao estudo qualitativo e quantitativo de macromoléculas - péptidos e
UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES
 UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI luizcarnevalijr@usp.br
UNIVERSIDADE GAMA FILHO PÓS-GRADUAÇÃO Nível: LATO SENSU Curso: FISIOLOGIA E TREINAMENTO APL. ATIVIDADES DE ACADEMIAS E CLUBES Influência da Genética desempenho Prof. Drd. LUIZ CARLOS CARNEVALI luizcarnevalijr@usp.br
UNIVERSIDADE FEDERAL DE ALAGOAS ENGENHARIA DE PESCA DISCIPLINA: BIOQUÍMICA AMINOÁCIDOS II SÍNTESE
 UNIVERSIDADE FEDERAL DE ALAGOAS ENGENHARIA DE PESCA DISCIPLINA: BIOQUÍMICA AMINOÁCIDOS II SÍNTESE Dra. Talita Espósito BIOSSINTESE DE AA amônia + H 3 N COO - C H Esqueleto carbônico NH 4 + R COO - aminoácidos
UNIVERSIDADE FEDERAL DE ALAGOAS ENGENHARIA DE PESCA DISCIPLINA: BIOQUÍMICA AMINOÁCIDOS II SÍNTESE Dra. Talita Espósito BIOSSINTESE DE AA amônia + H 3 N COO - C H Esqueleto carbônico NH 4 + R COO - aminoácidos
Aminoácidos e proteínas
 Aminoácidos e proteínas Visão geral 2 https://www.youtube.com/watch?v=qbrfimcxznm Importância dessa aula Serina Fosfoserina Treonina Fosfotreonina Fosforilação de resíduos de aa modifica a atividade enzimática
Aminoácidos e proteínas Visão geral 2 https://www.youtube.com/watch?v=qbrfimcxznm Importância dessa aula Serina Fosfoserina Treonina Fosfotreonina Fosforilação de resíduos de aa modifica a atividade enzimática
Carla Bittar Bioquímica e Metabolismo Animal
 Carla Bittar Bioquímica e Metabolismo Animal Compostos orgânicos Unidades formadoras de PROTEÍNAS Ligações covalentes com perda de água Moléculas pequenas PM de aproximadamente 130 Estrutura da célula
Carla Bittar Bioquímica e Metabolismo Animal Compostos orgânicos Unidades formadoras de PROTEÍNAS Ligações covalentes com perda de água Moléculas pequenas PM de aproximadamente 130 Estrutura da célula
Bioquímica. Práticas de. Simulação Computacional. no Estudo de Aminoácidos e Proteínas. Renato Massaharu Hassunuma. Patrícia Carvalho Garcia
 1010001001110101010011110100010101010101010100101000101001001010101010101010101 0101010101010001010101010110011011010101011101010101000101011010101000101010101 1011101010101010101010101101000100111010101001111010001010101010101010010100010
1010001001110101010011110100010101010101010100101000101001001010101010101010101 0101010101010001010101010110011011010101011101010101000101011010101000101010101 1011101010101010101010101101000100111010101001111010001010101010101010010100010
Aula 3: Estrutura de Proteínas. Bioquímica para Odonto - Bloco I Profa. Lucia Bianconi. Funções das Proteínas. Catalisadores (enzimas)
 Aula 3: Estrutura de Proteínas Bioquímica para Odonto - Bloco I Profa. Lucia Bianconi Funções das Proteínas Catalisadores (enzimas) Transportadoras (Oxigênio, Ferro, Vitaminas, fármacos) Armazenamento
Aula 3: Estrutura de Proteínas Bioquímica para Odonto - Bloco I Profa. Lucia Bianconi Funções das Proteínas Catalisadores (enzimas) Transportadoras (Oxigênio, Ferro, Vitaminas, fármacos) Armazenamento
OBJETIVOS INTERAÇÕES INTERMOLECULARES INTERAÇÕES INTERMOLECULARES.
 OBJETIVOS aandrico@if.sc.usp.br Interações Intermoleculares Mecanismo de Ação Modo de Ligação Complexos Recetor-Ligante Exemplos e Exercícios INTERAÇÕES INTERMOLECULARES INTERAÇÕES INTERMOLECULARES O processo
OBJETIVOS aandrico@if.sc.usp.br Interações Intermoleculares Mecanismo de Ação Modo de Ligação Complexos Recetor-Ligante Exemplos e Exercícios INTERAÇÕES INTERMOLECULARES INTERAÇÕES INTERMOLECULARES O processo
AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES
 UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
UNIVERSIDADE DE SÃO PAULO FACULDADE DE CIÊNCIAS FARMACÊUTICAS REATIVIDADE DE COMPOSTOS ORGÂNICOS II E BIOMOLÉCULAS NOTURNO AMINOÁCIDOS: ESTRUTURA E PROPRIEDADES Cibele Rosalin Líria Domingues Luma Antonio
UNIDADES REPRESENTATIVAS DE AMINOÁCIDOS E KIT EDUCACIONAL
 1 / 28 Relatório Descritivo UNIDADES REPRESENTATIVAS DE AMINOÁCIDOS E KIT EDUCACIONAL COMPREENDENDO AS MESMAS. 1 2 Campo da Invenção A presente invenção compreende um conjunto de unidades representativas
1 / 28 Relatório Descritivo UNIDADES REPRESENTATIVAS DE AMINOÁCIDOS E KIT EDUCACIONAL COMPREENDENDO AS MESMAS. 1 2 Campo da Invenção A presente invenção compreende um conjunto de unidades representativas
BIOQUÍMICA GERAL. Prof. Dr. Franciscleudo B. Costa UATA/CCTA/UFCG. Aula 4 Aminoácidos. Origem dos aminoácidos. Estrutura Química Geral
 Universidade Federal de Campina Grande Centro de Ciências e Tecnologia Agroalimentar Unidade Acadêmica de Tecnologia de Alimentos BIOQUÍMICA GERAL FRANCISCLEUDO BEZERRA DA COSTA PROFESSOR Câmpus de Pombal
Universidade Federal de Campina Grande Centro de Ciências e Tecnologia Agroalimentar Unidade Acadêmica de Tecnologia de Alimentos BIOQUÍMICA GERAL FRANCISCLEUDO BEZERRA DA COSTA PROFESSOR Câmpus de Pombal
Simulador de eletroforese
 Simulador de eletroforese O roteiro para utilização do software está dividido em quatro partes. Parte I. Comportamento de ácidos fracos. Parte II. Comportamento de um aminoácido com cadeia lateral não
Simulador de eletroforese O roteiro para utilização do software está dividido em quatro partes. Parte I. Comportamento de ácidos fracos. Parte II. Comportamento de um aminoácido com cadeia lateral não
Aminoácidos e Proteínas
 Aminoácidos e Proteínas PROTEÍNAS As proteínas são as macromoléculas mais abundantes nas células vivas. Ocorrem em todas as células e em todas as partes das mesmas. FUNÇÕES DAS PROTEÍNAS Formam estruturas
Aminoácidos e Proteínas PROTEÍNAS As proteínas são as macromoléculas mais abundantes nas células vivas. Ocorrem em todas as células e em todas as partes das mesmas. FUNÇÕES DAS PROTEÍNAS Formam estruturas
Bioinformática. Conceitos Fundamentais de Biologia Molecular. Paulo Henrique Ribeiro Gabriel phrg@ufu.br
 Bioinformática Conceitos Fundamentais de Biologia Molecular Paulo Henrique Ribeiro Gabriel phrg@ufu.br Faculdade de Computação Universidade Federal de Uberlândia 24 de agosto de 2015 Paulo H. R. Gabriel
Bioinformática Conceitos Fundamentais de Biologia Molecular Paulo Henrique Ribeiro Gabriel phrg@ufu.br Faculdade de Computação Universidade Federal de Uberlândia 24 de agosto de 2015 Paulo H. R. Gabriel
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas
 Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Universidade Salgado de Oliveira Disciplina de Bioquímica Básica Proteínas Profª Larissa dos Santos Introdução As proteínas (ou também conhecidas como polipeptídeos) são as macromoléculas mais abundantes
Prof. Marcelo Langer. Curso de Biologia. Aula Genética
 Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
Prof. Marcelo Langer Curso de Biologia Aula Genética CÓDIGO GENÉTICO Uma linguagem de códons e anticódons, sempre constituídos por 3 NUCLEOTÍDEOS. 64 CODONS = 4 tipos diferentes de nucleotídeos, combinação
Estruturas β. Cadeias β anti-paralelas φ = -139, ψ= Cadeias β paralelas φ = -119, ψ= +113
 Estruturas β A estrutura em folhaβconstitui 20-28% da estrutura secundária das protéinas globulares conhecidas. A conformação extendida da cadeia polipeptídica foi proposta nos anos 30, mas só observada
Estruturas β A estrutura em folhaβconstitui 20-28% da estrutura secundária das protéinas globulares conhecidas. A conformação extendida da cadeia polipeptídica foi proposta nos anos 30, mas só observada
CÓDIGO GENÉTICO Lista I 20 Questões Professor Charles Reis Curso Expoente
 CÓDIGO GENÉTICO Lista I 20 Questões Professor Charles Reis Curso Expoente 01. (FUVEST) A seguir está representada a sequência dos 13 primeiros pares de nucleotídeos da região codificadora de um gene. A
CÓDIGO GENÉTICO Lista I 20 Questões Professor Charles Reis Curso Expoente 01. (FUVEST) A seguir está representada a sequência dos 13 primeiros pares de nucleotídeos da região codificadora de um gene. A
EXERCÍCIOS DE REVISÃO - BIOLOGIA - PROF. BELAN.
 EXERCÍCIOS DE REVISÃO - BIOLOGIA - PROF. BELAN. 1. (UECE 2017) Qualquer ser vivo precisa de energia para realizar suas funções metabólicas. Seres vivos aeróbios realizam o processo conhecido como respiração
EXERCÍCIOS DE REVISÃO - BIOLOGIA - PROF. BELAN. 1. (UECE 2017) Qualquer ser vivo precisa de energia para realizar suas funções metabólicas. Seres vivos aeróbios realizam o processo conhecido como respiração
AMINOÁCIDOS AMINOÁCIDOS AMINOÁCIDOS AMINOÁCIDOS. Estrutura Básica de um Aminoácido
 AMINOÁCIDOS AMINOÁCIDOS São ácidos orgânicos formados por átomos de carbono, hidrogênio, oxigênio e nitrogênio. Alguns tipos de aminoácidos contêm também átomos de enxofre e fósforo que aparecem, portanto
AMINOÁCIDOS AMINOÁCIDOS São ácidos orgânicos formados por átomos de carbono, hidrogênio, oxigênio e nitrogênio. Alguns tipos de aminoácidos contêm também átomos de enxofre e fósforo que aparecem, portanto
