I. Fracionando a vida: Os bioquímicos fracionam um organismo e analisam os componentes individuais.
|
|
|
- Flávio Brunelli Paranhos
- 8 Há anos
- Visualizações:
Transcrição
1 Bioquímica I: Macromoléculas I. Fracionando a vida: Os bioquímicos fracionam um organismo e analisam os componentes individuais. 1) Qual é a composição atômica das células vivas/organismos? H: 60% O: 25% C: 12% N: ~5% P, S, Mg, Mn, Se, também estão presentes em quantidades menores Em certos níveis de estudo, a maioria dos organismos parece igual especialmente a nível celular. 2) Qual é a composição molecular das células? Principalmente água: ~80% O restante: Lipídios, gordura: 10% Carboidratos: 15% Proteínas: 50% Ácidos Nucléicos: 15% ** As proteínas são as macromoléculas-chave, têm diversos papéis estruturais e funcionais nas células) ** Ácidos Nucléicos (DNA, RNA; DNA armazena as informações hereditárias na célula) Até certo nível, forças químicas determinam a forma das moléculas e a forma determina a função. Que forças fornecem às moléculas suas propriedades? II. Forças Covalentes Ligações e interações químicas mantêm as moléculas juntas: 1) Ligações Covalentes - tipo mais importante de ligações - tipo de ligações mais fortes força ~80 kcal/mol Uma ligação covalente é o compartilhamento de um par de elétrons:
2 2 A energia térmica (vibracional) média em temperatura ambiente é em média ~5 kcal/mol. Considerando-se que são necessários ~80 kcal/mol para quebrar uma ligação covalente, pode-se dizer que elas são relativamente estáveis à temperatura ambiente. Tipos de ligações covalentes: Simples C-C (um par de elétrons) Dupla C=C (dois pares de elétrons) Tripla C=C (três pares de elétrons) Força 80 kcal/mol 150 kcal/mol 200 kcal/mol Existe uma rotação livre ao redor de uma ligação covalente simples, porém isso não ocorre com as ligações duplas e triplas. As ligações covalentes também possuem um ângulo fixo. Algumas ligações covalentes envolvem o compartilhamento desigual de elétrons. Alguns átomos estão ligados aos elétrons de forma mais forte do que outros átomos. A tendência para atrair elétrons é a chamada medida de eletronegatividade de um átomo. Observe algumas ligações com compartilhamento desigual de elétrons: As ligações polares apresentam movimentos bipolares; possuem polaridade O oxigênio é um átomo mais eletronegativo quando comparado com o hidrogênio e, portanto, uma ligação O-H é considerada uma ligação polar. Carbono e hidrogênio possuem eletronegatividades semelhantes. Dessa forma, uma ligação C-H é considerada uma ligação apolar. 2) Ligações de Hidrogênio atração entre uma carga levemente positiva em um átomo de hidrogênio e uma carga levemente negativa em um átomo próximo força da ligação ~ 5 kcal/mol (relativamente fraca) mais forte quando o doador, o hidrogênio, e o receptor estão a uma distância de mais ou menos 0,25nm as ligações de hidrogênio fornecem ordem e estrutura às moléculas uma única ligação de hidrogênio é fraca, mas a maior parte das moléculas são compostas por diversas ligações de hidrogênio, fato esse que proporciona força geral à molécula As propriedades da água são determinadas por interações de ligações de hidrogênio. A água é muito bem estruturada, mesmo sendo um líquido. A formação do gelo deve-se ao conjunto de redes de ligações de hidrogênio.
3 3 Ligações de hidrogênio entre regiões diferentes de uma molécula de proteína: NA água, essas regiões irão formar ligações de hidrogênio com as moléculas da água. Essas moléculas adotam uma conformação mais favorável, quando elas interagem com água. 3) Ligações Iônicas interação eletrostática entre dois grupos de cargas opostas em uma molécula causa limitante do compartilhamento desigual de elétrons; um átomo fica com o elétron NaCl fi Na + + Cl - compartilhamento desigual de elétrons, Cl fica com ambos os elétrons. Em solução, esse grupo torna-se ionizado, perde um próton e fica com carga negativa:
4 4 Átomos carregados podem ser atraídos por átomos de carga oposta: a força da ligação iônica é de aproximadamente 3-7 kcal/mol, mais forte quando os dois átomos estão a uma distância de aproximadamente 0,28mm 4) Interação de Van Der Walls força de atração não específica que está presente quando qualquer um dos dois átomos chega a uma distância menor mais favorável quando os átomos estão a uma distância de aproximadamente 0,2-0,3 nm polaridade transitória induziu entre átomos uma ligação apolar que leva à atração dos átomos próximos interação muito fraca força é ~ 1 kcal/mol. No entanto, a soma de diversas interações de Van Der Walls leva a um aumento da força e estabilidade Exemplo: Um ligante interagindo com seu receptor é completado por diversas interações não-covalentes tais como as interações de Van Der Walls. 5) Interações Hidrofóbicas / Entropia De maneira geral, a estrutura de uma molécula é mantida por diversas interações. Uma molécula tem uma forma particular porque adota o estado de menor energia (minimiza entropia) Ao adotar essa forma, as conformações alternativas são selecionadas e os grupos que não podem formar pontes de hidrogênio com a água (hidrofóbicos) tendem a aglomerar-se dentro da molécula (longe da água). Hidrofóbico: ( odeia água ) moléculas sem carga, apolares, não interagem com a água Hidrofílico: ( ama água ): moléculas com carga ou polares, de ligações de hidrogênio com água A forma que as macromoléculas biológicas podem adotar depende de um grande número de interações moleculares. III. Principais Macromoléculas A. Lipídios, Fosfolipídios Estrutura de um carboidrato: CH 3 (CH 2 ) 3 CH 3
5 5 Se adicionarmos um grupo hidroxila (OH) a um carboidrato, teremos um álcool: CH 3 (CH 2 ) 4 OH Álcoois de cadeia curta são solúveis em água. Podemos criar um ácido graxo adicionando um grupo carboxila (COOH) ao grupo dos carboidratos: CH 3 (CH 2 ) 3 COOH Um ácido graxo é uma molécula anfipática contém tanto porções hidrofóbicas quanto porções hidrofílicas. Um ácido graxo também pode ser representado por:
6 6 Três ácidos graxos e uma molécula de glicerol podem ser combinados em uma síntese de desidratação para formar um lipídio (um triglicéride). Triglicérides são formas principais de armazenamento de ácidos graxos dentro das células. Fosfolipídeos: Um subgrupo de lipídios que desempenha um papel-chave na estrutura celular. Fosfolipídios são formados por dois ácidos graxos e um grupo fosfato:
7 7 Os fosfolipídeos também podem ser representados como: em solução, os fosfolipídios irão se reunir para formar micelas Uma micela Os fosfolipídeos formam uma bicamada em solução aquosa. Uma célula típica é englobada por uma membrana plasmática, que é composta de uma bicamada de fosfolipídeos (2 camadas de moléculas de fosfolipídeos dispostas em uma bicamada lipídica) O interior hidrofóbico da membrana plasmática é impermeável às moléculas carregadas ou polares.
8 8 B. Açúcares, Carboidratos 1) Fórmula geral de um açúcar: (CH 2 O) n ex.: Glicose C 6 H 12 O 6 Em todos os açúcares, n-1 dos carbonos possuem um grupo hidroxila (OH) e o Carbono C- 1 possui um grupo carbonil (C=O). A localização do grupo carbonil e a orientação dos grupos hidroxila determinam o tipo de açúcar. Se o grupo carbonil estiver no final (um grupo aldeído), então o açúcar é uma aldose (ex.: glicose) Se o grupo carbonil estiver no meio da cadeia (um grupo cetona), então o açúcar é uma cetose (ex.: frutose) Açúcares compostos por seis átomos de carbono são chamados de hexoses (ex.: glicose) Açúcares compostos por cinco átomos de carbono são chamados de pentoses (ex.: ribose)
9 9 Os açúcares compostos por três átomos de carbono são chamados de trioses (ex.: gliceraldeído) 2) Conformação dos açúcares a) Monossacarídeos A glicose é encontrada com mais freqüência em forma de anel em solução: A orientação do grupo OH no carbono C-1 pode ser tanto alfa (abaixo do plano do anel) ou beta (acima do plano do anel) b) Dissacarídeos Os dissacarídeos são formados por dois monossacarídeos unidos por uma ligação covalente: Lactose (forma) (Galactose (1 fi 4) Glicose) A enzima lactase quebra a lactose em glicose e galactose. Muitos indivíduos adultos param de sintetizar a enzima lactase. Como resultado, uma grande porcentagem de certas populações torna-se intolerante à lactose. c) Polissacarídeos Polissacarídeos são formados por diversas unidades de monossacarídeos (geralmente monômeros de glicose) ligados para formar cadeias longas. ex.: amido, glicogênio, celulose Polissacarídeos são usados como uma forma de armazenar energia e também para funções estruturais. Amido é um polímero de Glicose (1 fi 4) ligação
10 10 Celulose desempenha um papel importante nas plantas, uma das moléculas mais abundantes na terra. É um polímero não ramificado de glicose em ligação (1 fi 4). As unidades alternantes de glicose possibilitam que as moléculas adjacentes de celulose formem ligações de hidrogênio umas com as outras. A capacidade das ligações de hidrogênio da celulose leva à força das paredes celulares e de fibras tais como a madeira. Bioquímica II: Proteínas Proteínas possuem diversas funções nas células papéis estruturas e funcionais 10 5 tipos diferentes de proteínas são produzidas por células eucarióticas As proteínas são polímeros de blocos de construção conhecidos como aminoácidos 20 aminoácidos diferentes fi podem resultar em 20 n combinações de proteínas de extensão n Ácidos Nucléicos armazenam e transferem material genético quatro diferentes blocos de construção chamados de nucleotídeos fi podem resultar em 4 n combinações diferentes de ácidos nucléicos de extensão n 1. Amino ácidos e Ligações Peptídicas Fórmula Geral dos Aminoácidos: O grupo R (cadeia lateral) varia ao longo de 20 aminoácidos diferentes. Os 20 aminoácidos diferentes compõem todas as proteínas. Peptídeos são oligômeros de aminoácidos formados: através de uma reação de desidratação quando o grupo carboxila do peptídeo está ligado ao grupo amino de um segundo aminoácido.
11 11 A ligação peptídica é plana, tem caráter parcial de dupla ligação. Não há rotação ao redor da ligação amida. A estrutura real da ligação peptídica é um híbrido das duas formas apresentadas abaixo: No entanto, existe a rotação ao redor das ligações adjacentes à ligação peptídica. Uma unidade peptídica é uma disposição plana de quatro átomos. Um polipeptídeo longo composto por diversos aminoácidos é chamado de proteína. Cada proteína possui uma ordem específica de aminoácidos e adota uma forma particular determinada pela seqüência de aminoácidos. 2. Os Vinte Diferentes Aminoácidos a. Cadeias laterais polares porém sem carga As cadeias laterais desses grupos podem foram ligações de hidrogênio com outros grupos polares b. Cadeias laterais polares e carregadas
12 12 As cadeias laterais desses aminoácidos podem formar ligações de hidrogênio ou ligações iônicas 1. Com cargas positivas 2. Cargas negativas c. Cadeias laterais hidrofóbicas (apolares, sem carga) As cadeias laterais da maior parte dos aminoácidos não pode formar ligações de hidrogênio ou ligações iônicas e comportam-se melhor em ambientes apolares. Tais aminoácidos preferem ficar no interior das proteínas em uma solução aquosa.
13 13 Apesar do fato da Tirosina ser fortemente apolar, sua cadeia lateral possui um grupo hidroxila que é polar e pode formar ligações de hidrogênio. Algumas proteínas são chamadas de proteína transmembrana. Uma região de proteínas transmembrana atravessa a membrana da célula ou o compartimento celular no qual elas são encontradas
14 14 d. Casos especiais 3. Estrutura das Proteínas Para entendermos a estrutura das proteínas uma combinação de forças determina a estrutura: efeito hidrofóbico ligações iônicas ligações de hidrogênio ligações de dissulfeto
15 15 Década de 30: Linus Pauling propôs que o grupo NH em um aminoácido, e o grupo C=O em outro aminoácido(s) podem interagir para formar uma ligação de hidrogênio. Ele previu que esses grupos iriam interagir, resultando em uma estrutura polipeptídica (polipetídica) chamada de hélice a (hélice alfa). EM uma hélice a ( )o grupo CO do aminoácidos n liga-se ao hidrogênio (no do) grupo NH do aminoácido(s) (n+4). Estrutura da a -hélice: Pauling previu também outro tipo de estrutura polipeptídica (polipetídica) chamada de folha beta pregueada (folha ß pregueada). Na estrutura pregueada, existem atrações intermoleculares entre duas ou mais cadeias polipetídicas: (NR)* Cadeias antiparalelas são cadeias opostas, são paralelas mas em direção contrária. Não são não paralelas como se se apresentam na figura acima.
16 16 Níveis de Estrutura de Proteína: a) Estrutura primária: A seqüência linear de aminoácidos (ex.: NH3 +..met-cis-leu-lis-glu COO-) b) Estrutura secundária A disposição local dos aminoácidos próximos na cadeia linear para formar estruturas como hélices, - folhas pregueadas e alças e molas aleatórias. c) Estrutura terciária Disposição espacial de aminoácidos afastados na cadeia do polipeptídio (polipetídeo) linear para formar a estrutura tridimensional completa (dobrada) da proteína. Também inclui ligações de dissulfetos : d) Estrutura quaternária Interação de mais de uma cadeia polipeptídica (polipetídica); associação entre proteínas diferentes para formar complexos como dímeros, trímeros, tetrâmeros: 4. Estrutura e Função das Proteínas A estrutura determina a função das proteínas. Veja um exemplo de proteína que catalisa uma reação bioquímica. Triose fosfato isomerase (TFI) TFI é uma proteína dimérica composta (um dímero de proteína composto) de duas cadeias polipeptídicas (polipetídicas) de 247 aminoácidos cada uma. O polipeptídio (polipetídeo) dobra-se para formar uma enzima em forma de cesta com um poço no centro. APENAS O DÍMERO É ENZIMATICAMENTE ATIVO! A TFI catalisa a seguinte reação:
17 17 Apesar de essa proteína possuir 247 aminoácidos, apenas três deles (Glu165, His95 e Lis12) são importantes na função catalítica da TFI. O sítio catalítico (ativo) é formado quando a proteína dobra-se em sua forma 3-D final e os três aminoácidos ficam próximos. Observe o sítio ativo da TFI: Mecanismo: 1) G 3-P liga-se ao sítio ativo da TFI (N de His95) 2) Lys12 estabiliza G 3-P no sítio ativo 3) Glu165 age como um catalisador básico (B-) pega um H+ do grupo C2 (o carbono próximo ao carbonil) do G 3-P 4) His95 doa um a H+ para o grupo C1 (carbonil) de G 3-P para formar o grupo OH em C1. (e facilita a formação do enediol intermediário) 5) Glu165 pega o H+ do grupo C1 do intermediário. 6) His95 pega o próton do grupo OH no grupo C2 do intermediário TFI estabiliza (diminui a energia do intermediário) o intermediário fortemente desfavorável, que possui uma energia livre positiva bem maior do que o G 3-P ou o DHAP (uma energia livre bem mais positiva do que G 3-P ou DHAP). A TFI também acelera 10 vezes a reação. O aminoácido que estabiliza o estágio de transição é o Glu165. Se substituirmos Glu165 em TFI pelo Ácido aspártico (que é apenas um carbono mais curto do que a glu), reduzimos a atividade da enzima em 1000 vezes (TFI torna-se 1000 vezes menos eficaz) ARTIGOS DO WASHINGTON POST, 21/5/93 pág. A3 Influenza s Burglary Tools de Boyce Rensberger e NY TIMES, 21/5/93 Breakthrough on Flu Viruses Reported de Warren E. Leary
18 18 Bioquímica III: Energia Livre e Reações cinéticas (Reação Cinética) TFI catalisa a seguinte reação: Diagrama de Energia Livre para a Reação Acima: TFI diminui a energia de ativação (Ea) da reação. TFI faz isso ao estabilizar o estágio de transição (cis-enediol) TFI (como com todas as enzimas) não afeta os (dos) valores de G ' de uma reação química. 1.Equlíbrio da Reação, Keq e Energia Livre Em equilíbrio, as moléculas tendem a permanecer em seu estado energético mais baixo. Dois estágios, S1 e S2 com diferenças de energia entre os dois expressas como G ' = variação na energia livre sob as condições padronizadas (as condição normais). A equação que relaciona G às concentrações de S1 e S2: G = Diferença de Energia Livre na Reação G= Energia Livre em condições padronizadas específicas RT = constante de gás x T (em Kelvins) [S1]/[S2] = razão entre os produtos e os reagentes
19 19 Em equilíbrio para a reação,?g = 0 ( não há variação líquida de energia livre ) (não há reação líquida) RT = 0,59 kcal/mol a 25 C, RT = 0,61 kcal/mol a 37 C então RT ~0,6 Keq = razão das constantes K 1 [S 1 ] = K 2 [S 2 ] razão da reação dianteira = K 1 [S 1 ] razão da reação reversa = K 2 [S 2 ] Exemplo: G3P fi DHAP ( G 0 = -1,86 kcal/mol) Em equilíbrio Keq = 22 Em equilíbrio haverá 22x mais DHAP do que G3P Dado G3P puro: A reação prossegue fi DHAP (síntese líquida de DHAP) Dado DHAP puro: A reação prossegue para formar G3P (síntese líquida de G3P) Quando G3P = DHAP G Rxn = 0 (não há variação líquida) Is 22:1
20 20 ~ 7:1 A reação prossegue para a direita fi DHAP A direção de uma reação depende de: 1) diferença da energia intrínseca entre os produtos e os reagentes 2) as concentrações das reações e dos produtos Isso é descrito pela equação:
21 21 Se G de rxn < 0, rxn prosseguirá adiante fi (reação exergônica) Se G de rxn > 0, rxn prosseguira reversamente (reação endergônica) Se G = 0, rxn está em equilíbrio, não há variação líquida de energia livre Exemplo: SE a razão de DHAP: G3P fosse 7,4:1, qual seria o G do rxn e em qual direção prosseguiria? G = G 0 + RTIn [ PRODUTO ] [ REAGENTES] G = -1,86kcal/mol + 0,60kcal/mol In 7,4 G = -0,66 (G<0) Portanto, a reação prosseguirá adiante fi para produzir DHAP 2. Reações Acopladas Observe a reação A fi B A reação tenderá a prosseguir na direção da molécula que apresenta a menor energia livre. Como impulsionamos uma reação para frente que possui um G 0 > 0? É possível acoplar uma reação desfavorável ( G>0) com uma reação favorável ( G<0) Algumas vezes o acoplamento pode resultar em condições desfavoráveis, mas é geralmente mais favorável que a reação original não acoplada. Rxn 1: A fib G 0 > 0 Rxn 2: C fid G 0 < 0 A+C fib+d G 0 < 0 (poderia ser inferior a 0 ou próximo de 0) Exemplo: A + X fi B C fi D +X A + C fi B+ D (reação geral) As células usam esses mecanismos de acoplamento de reações desfavoráveis com reações favoráveis para que as reações possam prosseguir adiante. Exemplo: 1) Glicose + Pi fi Glicose 6-Fosfatase + H 2 O G 0 = 3,3 kcal/mol 2) ATP + H 2 O fi ADP + Pi H 2 O = -7,3 kcal/mol Glicose + ATP figlicose 6-P + ADP G 0 = -4,0 kcal/mol As células usam a energia da hidrólise do ATP para dirigir a reação 1 energeticamente desfavorável. Pi = PO fosfato inorgânico O ATP é uma fonte principal de energia. O ATP armazena energia aproximando cargas negativas em ligações altamente energéticas e libera essa energia quando a ligação é quebrada.
22 22 Todas as reações que ocorrem nas células (1000) possuem G < 0 * As enzimas aumentam a taxa de reações; no entanto, elas não alteram as concentrações de equilíbrio ou G para a reação. 3.1 Taxas de Reação e o Papel das Enzimas Para a reação G3P fi DHAP Observe o perfil energético da reação Energia de ativação (Ea) = barreira energética ou energia livre de ativação para a reação. Enzima (TFI) reduz a Ea estabilizando (reduzindo a energia livre de) estado de transição (intermediário). Na presença de TFI, a Ea para a reação é de 3 kcal/mol Em equilíbrio G = 0, a energia de ativação é de 26 kcal/mol Em equilíbrio, existem ~10 19 mais G3P do que cis-enediol (ou menos cis-enediol do que G3P). Portanto, a reação prossegue lentamente na ausência da enzima. Na presença da enzima, G = 13 kcal/mol. TFI estabiliza a cis-enediol intermediária, reduzindo assim sua energia livre de 26 kcal/mol para 13 kcal/mol. Em equilíbrio G=0; a energia de ativação é de 13 kcal/mol:
23 23 Em equilíbrio, existe ~10 10 mais G3P do que cis-enediol (ou menos cis-enediol do que G3P). A razão de [cis-enediol] para [G3P] é 10 9 vezes melhor na presença da enzima TFI. Mas como sabemos que as enzimas reduzem a Ea para a reação ligando-se ao estágio de transição? Porque os análogos do estágio de transição (moléculas estáveis) que se parecem com o estágio de transição ligam melhor as enzimas do que qualquer reagente ou produto. Papel das Enzimas nas Reações Químicas: Uma reação pode ser exergônica, mas ter muita Ea; portanto, precisamos de uma enzima para reduzir a Ea Uma reação pode ser endergônica e não prosseguir a não ser que esteja acoplada a uma reação exergônica. Uma enzima pode catalisar a reação acoplada, permitindo, portanto, que a reação prossiga Reações exergônicas ( G<0), reações endergônicas ( G>0) 4. Cinética das Enzimas (Cinética de Michaelis-Menten 1913) Podemos obter um modelo do mecanismo da reação enzimática da seguinte forma: K 1 = Constante de taxa de reação adiante K 2 = Constante de taxa de reação reversa K 3 = Taxa de reação adiante S = substrato E = enzima ES = complexo enzima substrato P = produto K1= ((# moles/l de ES formado.)/seg)/((# moles/l de E)(# moles de S)) = 1/ (mol/l x seg) unidades K2= ((# moles/l de S formado.)/seg)/((# moles/l de ES) K3= ((# moles/l de P formado.)/seg)/((# moles/l de ES) = 1/seg unidades = 1/seg unidades
24 24 1) Taxa Catalítica A taxa catalítica é igual ao produto das concentrações de ES e K 3 V = K3[ES] V = velocidade ou taxa de reação 2) A fração (f) da enzima ligada ao substrato é: [ ES ] [ ] f = [E T ] = Concentração total da enzima f E T [ S ] [ S ] + K m [E T ] = Concentração da enzima ligada = f = fração da enzima ligada ao substrato [ ] [ ] [ S] ES = ET [ S ] + K m Qual é a fração (f) da enzima ligada quando: 1) [S] = K m fração da enzima ligada = ½ k k k 2 3 m = = Constante de Michaelis K moles k = sec sec m = units 1 1 (moles) ( sec ) K m é uma medida da afinidade de uma enzima por seu substrato 2) [S] << K m fração de enzima ligada depende da afinidade da enzima por seu substrato 3) [S] >> K m fração ligada é 1 (enzima é limitada toda ligada com o substrato) A Taxa de Reação é V = K 3 [ES]; substituindo na equação:
25 25 A taxa máxima de reação (Vmax) é obtida quando a enzima é saturada com o substrato [ S] (quando [S]>> K m ) and aproxima-se de 1 (f =1) S + K V = K 3 [E T ] (1) V max = K 3 [E T ] Vmáx [ S ] [ S ] + K m [ ] m Então V = fi Equação de Michaelis-Menten Observe a representação gráfica da velocidade de reação como uma função da concentração do substrato [S], para um enzima que obedece à cinética de Michaelis- Menten 1) [S] é baixa ([S] no denominador não é mais importante) 2) [S] é alta (Valor de Km no denominador não é importante) então V= V max 3) [S] = Km (já que Km = [S]) então V = ½ V max Km é a [S] na qual metade da enzima está ligada ao substrato Qual é a velocidade da formação do produto: Per [E], per [S] Quando [S] é pequena, a maior parte da enzima está livre[e] = [E T ]
26 26 V = K 3 / K m = K cat K cat = # transferência; # do molécula transferida pela enzima por unidade de tempo para formar um produto Para a Triose Fosfato Isomerase: K 1 = 10 8 l/(moles x seg) K 2 = 430/seg K 3 = 430/seg K 3 / K m = K cat = ~ (10 8 produtos)/(reagentes x enzima x seg) A taxa da reação de TFI é limitada apenas pela difusão; sempre que a TFI encontra a G3P, a TFI converte a G3P em DHAP A taxa de difusão é de ~10 8 (portanto a enzima raramente encontra o substrato) TFI é, portanto, cineticamente perfeita sempre que encontra o substrato, converte o mesmo em seu produto Material Suplementar sobre Cinética das Enzimas (de 10/9/97). suplemento para o Capítulo 6 de Purves et al. Bioquímica IV: Metabolismo Energético Revisão de Cinética Estrutura do ATP em ph 7.0:
27 27 existe uma grande repulsão eletrostática entre os grupos fosfato com cargas negativas. A hidrólise do ATP para ADP + Pi libera energia livre e reduz a repulsão Como se produz ATP (energia para as células)? Através de um processo conhecido como Glicólise ( glico açúcar, lise quebra) Na glicólise, 1 molécula de glicose é convertida em 2 moléculas de piruvato Eficiência energética desse processo: Com Oxigênio: C 6 H 12 O 6 + 6H 2 O 6CO 2 + 6CO 2 + 6H 2 Oproduz 686 kcal/mol
28 28 Sem Oxigênio: C 6 H 12 O 6 2 lactatos 2 ATPs C 6 H 12 O 6 2 etanol + CO 2 2 ATPs A glicólise ocorre no citoplasma das células, não necessita de oxigênio e ocorre em todos os organismos ~ há 3,5 bilhões de anos: não havia oxigênio suficiente portanto os organismo possuíam um metabolismo anaeróbico ~ há 2,5 bilhões de anos: havia oxigênio suficiente para realizar metabolismo aeróbico A glicólise pode ser realizada nos extratos de leveduras (i.e. as leveduras vivas não são necessárias, apenas as enzimas. O termo enzima significa na levedura ) A glicólise possui duas fases: 1) Fase de investimento de energia (usa ATP) 2) Fase de geração de energia (produz ATP) Resumo das Reações da Glicólise: Composta por 10 etapas: 1 açúcar de 6-carbonos é convertido em moléculas de 2 3- carbonos. Uma observação importante: A reação G3P DHAP apresenta G = -1,86 kcal/mol No entanto, na glicólise DHAP é convertido em G3P. Dessa forma G dessa reação é + 1,86 kcal/mol! Como a reação prossegue nas células?? Uma vez que o G3P é usado em reações posteriores, a [G3P] diminui, o que direciona a reação para a direita, produzindo mais G3P. Mesmo que G > 0, o valor de G < 0 em virtude da razão de produtos/reagentes
29 29 G = G 0 + RTIn [ PRODUTO ] [ REAGENTES] Na célula, todas as reações prosseguirão adiante uma vez que G < 0 (obtido mantendo-se uma razão ótima de produtos / reagentes) TABELA DE valores de G e G das reações na glicólise. Observe que grande parte de G > 0, mas todos os valores de G são < 0 Portanto, a reação prossegue formando o piruvato! A Quinase é uma enzima que adiciona um grupo fosfato à molécula. Regulação das Vias O objetivo da glicólise é produzir ATP. O ATP produzido é usado em outras reações na célula (reações biossintéticas, transporte, etc.) A células sente a razão de ATP/ADP por exemplo: quando os músculos estão trabalhando intensamente, o ATP é convertido em ADP se a [ATP] for alta, a glicólise é baixa se a [ATP] for baixa, a glicólise é iniciada (aumento de ADP ativa a glicólise) É possível variar as velocidades de reação (v) das enzimas na glicólise trocando-se as variáveis na equação: Para Aumentar a Taxa de Glicólise: 1) Aumentar [E T ]; produzir mais enzimas por exemplo: após a ingestão de altos níveis de carboidratos os níveis de piruvatoquinase aumentam 2) Aumento da [S]; se aumentarmos a quantidade de substrato, aumentaremos a fração (f) da enzima que é ocupada pelo substrato: 3) Se K m for alterado poderá afetar a taxa da reação se K m for mais alto fi taxa mais lenta se K m mais baixo fi taxa mais rápida É possível alterar K m de uma enzima variando-se a forma do sítio ativo (sítio catalítico) da enzima
30 30 Exemplo: A ligação dos reguladores no sítio alostérico leva a uma variação da forma da enzima o que afeta o K m da enzima. Se diminuirmos K m fi a taxa (v) aumenta porque f será aumentado também Se aumentarmos K m fi a taxa (v) diminui porque diminuímos f A ligação dos reguladores no sítio ativo altera o sítio a posição de alguns aminoácidos muda em alguns angstroms suficiente para inativar a enzima. Regulação das Vias: Regulação de Feedback e Feed-Forward A maior parte das enzimas que catalisa reações nas vias bioquímicas é regulada. Exemplo de Via 1) F pode agir como um inibidor de feedback da enzima que catalisa a etapa C fi D (primeira etapa comprometida na síntese de F 2) I pode agir como um inibidor de feedback da enzima que catalisa a etapa C fi G para reduzir a velocidade daquela etapa 3) Tanto I quanto G juntos ou sozinhos podem agir como inibidores de feedback da etapa A fi B 4) A pode agir como um inibidor feed forward da etapa B fi C para aumentar a velocidade daquela reação Por exemplo: se tivermos muito A (A está construindo), é possível ir para a etapa de limitação de velocidade, diminuir K m da enzima e acelerar a reação
31 31 Normalmente, o produto final de uma via geralmente regula a primeira etapa comprometida da via (ou primeira etapa que necessita de enzimas) Na glicólise, certas enzimas são reguladas de forma que a velocidade da glicólise possa ser aumentada ou diminuída dependendo das exigências energéticas da célula. Regulação da enzima hexoquinase: G6-P inibe a hexoquinase se a glicólise for bloqueada ou freada. Regulação da enzima fosfofrutoquinase (enzima PFRK) ATP age como um regulador negativo da enzima PFK. Em alto [ATP], ATP liga-se ao sítio alostérico e altera a atividade catalítica da PFK (aumenta K m ) Em baixo, ATP liga-se ao sítio ativo da PFK e ativa PFK Alto [ADP] ativa a PFK
As membranas são os contornos das células, compostos por uma bicamada lipídica
 Células e Membranas As membranas são os contornos das células, compostos por uma bicamada lipídica Organelas são compartimentos celulares limitados por membranas A membrana plasmática é por si só uma organela.
Células e Membranas As membranas são os contornos das células, compostos por uma bicamada lipídica Organelas são compartimentos celulares limitados por membranas A membrana plasmática é por si só uma organela.
ENZIMAS. Células podem sintetizar enzimas conforme a sua necessidade.
 ENZIMAS As enzimas são proteínas, catalisadores (aumenta a velocidade de uma determinada reação química) biológicos (proteínas) de alta especificidade. Praticamente todas as reações que caracterizam o
ENZIMAS As enzimas são proteínas, catalisadores (aumenta a velocidade de uma determinada reação química) biológicos (proteínas) de alta especificidade. Praticamente todas as reações que caracterizam o
ESTRUTURA DAS PROTEÍNAS
 ESTRUTURA DAS PROTEÍNAS Aminoácidos ligam-se por ligações peptídicas = reação de condensação entre: OH do grupo carboxila de um aminoácido H do grupo amina do outro aminoácido ( liberação de uma molécula
ESTRUTURA DAS PROTEÍNAS Aminoácidos ligam-se por ligações peptídicas = reação de condensação entre: OH do grupo carboxila de um aminoácido H do grupo amina do outro aminoácido ( liberação de uma molécula
O QUE SÃO SUBSTÂNCIAS INORGÂNICAS? QUAL A FUNÇÃO BIOLÓGICA DE CADA UMA?
 O QUE SÃO SUBSTÂNCIAS ORGÂNICAS? O QUE SÃO SUBSTÂNCIAS INORGÂNICAS? QUAL A FUNÇÃO BIOLÓGICA DE CADA UMA? SUBSTÂNCIAS ORGÂNICAS: CARBONO, HIDROGÊNIO, OXIGÊNIO E NITROGÊNIO FORMAM CADEIAS LONGAS E COMPLEXAS
O QUE SÃO SUBSTÂNCIAS ORGÂNICAS? O QUE SÃO SUBSTÂNCIAS INORGÂNICAS? QUAL A FUNÇÃO BIOLÓGICA DE CADA UMA? SUBSTÂNCIAS ORGÂNICAS: CARBONO, HIDROGÊNIO, OXIGÊNIO E NITROGÊNIO FORMAM CADEIAS LONGAS E COMPLEXAS
Água e Solução Tampão
 União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
União de Ensino Superior de Campina Grande Faculdade de Campina Grande FAC-CG Curso de Fisioterapia Água e Solução Tampão Prof. Dra. Narlize Silva Lira Cavalcante Fevereiro /2015 Água A água é a substância
UFABC Bacharelado em Ciência & Tecnologia
 UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Energia de interação entre macromoléculas Interações em meio
UFABC Bacharelado em Ciência & Tecnologia Transformações Bioquímicas (BC0308) Prof Luciano Puzer http://professor.ufabc.edu.br/~luciano.puzer/ Energia de interação entre macromoléculas Interações em meio
Profa. Dra. Juliana Garcia de Oliveira Disciplina: Biologia celular e molecular Cursos: Ciências Biológicas, Enfermagem, Nutrição e TO.
 Profa. Dra. Juliana Garcia de Oliveira Disciplina: Biologia celular e molecular Cursos: Ciências Biológicas, Enfermagem, Nutrição e TO. Bases Macromoleculares das Células Composição química das células
Profa. Dra. Juliana Garcia de Oliveira Disciplina: Biologia celular e molecular Cursos: Ciências Biológicas, Enfermagem, Nutrição e TO. Bases Macromoleculares das Células Composição química das células
UNIVERSIDADE COMUNITÁRIA DA REGIÃO DE CHAPECÓ ÁREA DE CIÊNCIAS DA SAÚDE CURSO DE FISIOTERAPIA CIÊNCIAS MORFOLÓGICAS II
 UNIVERSIDADE COMUNITÁRIA DA REGIÃO DE CHAPECÓ ÁREA DE CIÊNCIAS DA SAÚDE CURSO DE FISIOTERAPIA CIÊNCIAS MORFOLÓGICAS II Respiração Celular 1º estágio: GLICÓLISE 2º estágio: CK Ciclo de Krebs 3º estágio:
UNIVERSIDADE COMUNITÁRIA DA REGIÃO DE CHAPECÓ ÁREA DE CIÊNCIAS DA SAÚDE CURSO DE FISIOTERAPIA CIÊNCIAS MORFOLÓGICAS II Respiração Celular 1º estágio: GLICÓLISE 2º estágio: CK Ciclo de Krebs 3º estágio:
Capacidade de organizar os produtos da digestão usando a energia extraída dos mesmos produtos da digestão (REGULAÇÃO)
 Capacidade de organizar os produtos da digestão usando a energia extraída dos mesmos produtos da digestão (REGULAÇÃO) As proteínas são digeridas até aminoácidos, as gorduras (triglicérides) até glicerol
Capacidade de organizar os produtos da digestão usando a energia extraída dos mesmos produtos da digestão (REGULAÇÃO) As proteínas são digeridas até aminoácidos, as gorduras (triglicérides) até glicerol
GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES. Professor Cristiano
 GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES Professor Cristiano GEOMETRIA MOLECULAR É o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Dependendo dos átomos que a
GEOMETRIA MOLECULAR E INTERAÇÕES QUÍMICAS MOLECULARES Professor Cristiano GEOMETRIA MOLECULAR É o estudo de como os átomos estão distribuídos espacialmente em uma molécula. Dependendo dos átomos que a
Professor Fernando Stuchi M ETABOLISMO DE C ONSTRUÇÃO
 M ETABOLISMO DE C ONSTRUÇÃO P ROTEÍNAS P ROPRIEDADE BÁSICA São grandes moléculas (macromoléculas) constituídas por aminoácidos, através de ligações peptídicas. É o composto orgânico mais abundante no corpo
M ETABOLISMO DE C ONSTRUÇÃO P ROTEÍNAS P ROPRIEDADE BÁSICA São grandes moléculas (macromoléculas) constituídas por aminoácidos, através de ligações peptídicas. É o composto orgânico mais abundante no corpo
Estrutura e função dos ácidos nucléicos. Profa. Melissa de Freitas Cordeiro-Silva
 Estrutura e função dos ácidos nucléicos Profa. Melissa de Freitas Cordeiro-Silva > Polímeros de nucleotídeos Funções: DNA (ácido desoxirribonucléico) : > Armazenar as informações necessárias para a construção
Estrutura e função dos ácidos nucléicos Profa. Melissa de Freitas Cordeiro-Silva > Polímeros de nucleotídeos Funções: DNA (ácido desoxirribonucléico) : > Armazenar as informações necessárias para a construção
23/03/2015. Moléculas orgânicas - Carboidratos
 Moléculas orgânicas - Carboidratos São formados por C, H, O. São Conhecidos como: Hidratos de Carbono Glucídios Glicídios Açúcares Sacarídeos Funções: Energética (glicose); Glicogênio : reserva energética
Moléculas orgânicas - Carboidratos São formados por C, H, O. São Conhecidos como: Hidratos de Carbono Glucídios Glicídios Açúcares Sacarídeos Funções: Energética (glicose); Glicogênio : reserva energética
Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe!
 Aula: 2 Temática: Ácidos Nucléicos Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe! Introdução: Os ácidos nucléicos são as moléculas com a função de armazenamento e expressão da informação
Aula: 2 Temática: Ácidos Nucléicos Hoje estudaremos a bioquímica dos ácidos nucléicos. Acompanhe! Introdução: Os ácidos nucléicos são as moléculas com a função de armazenamento e expressão da informação
Dra. Kátia R. P. de Araújo Sgrillo. Sgrillo.ita@ftc.br
 Dra. Kátia R. P. de Araújo Sgrillo Sgrillo.ita@ftc.br A conversão do fluxo de elétrons em trabalho biológico requer transdutores moleculares (circuito microscópico), análogos aos motores elétricos que
Dra. Kátia R. P. de Araújo Sgrillo Sgrillo.ita@ftc.br A conversão do fluxo de elétrons em trabalho biológico requer transdutores moleculares (circuito microscópico), análogos aos motores elétricos que
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2010_2011_1º Teste 25/10/2010
 BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2010_2011_1º Teste 25/10/2010 (Duração: 1,5 h) Nome do Aluno: Nº: Curso: Cada uma das questões de escolha múltipla (1 à 40) tem a cotação de 0,5 valores. Será descontado
BIOQUÍMICA E BIOLOGIA MOLECULAR 1º S_2010_2011_1º Teste 25/10/2010 (Duração: 1,5 h) Nome do Aluno: Nº: Curso: Cada uma das questões de escolha múltipla (1 à 40) tem a cotação de 0,5 valores. Será descontado
Bioenergética. Profa. Kalyne de Menezes Bezerra Cavalcanti
 Bioenergética Profa. Kalyne de Menezes Bezerra Cavalcanti Natal/RN Fevereiro de 2011 Substratos para o exercício O corpo utiliza nutrientes carboidratos, gorduras e proteínas consumidos diariamente para
Bioenergética Profa. Kalyne de Menezes Bezerra Cavalcanti Natal/RN Fevereiro de 2011 Substratos para o exercício O corpo utiliza nutrientes carboidratos, gorduras e proteínas consumidos diariamente para
COMPOSIÇÃO QUÍMICA CELULAR COMPOSTOS INORGÂNICOS: ÁGUA- SAIS MINERAIS COMPOSTOS ORGÂNICOS: CARBOIDRATOS
 COMPOSIÇÃO QUÍMICA CELULAR COMPOSTOS INORGÂNICOS: ÁGUA- SAIS MINERAIS COMPOSTOS ORGÂNICOS: CARBOIDRATOS COMPOSTOS INORGÂNICOS Não apresentam Carbono em sua estrutura DOIS TIPOS: Água e Sais Minerais ÁGUA:
COMPOSIÇÃO QUÍMICA CELULAR COMPOSTOS INORGÂNICOS: ÁGUA- SAIS MINERAIS COMPOSTOS ORGÂNICOS: CARBOIDRATOS COMPOSTOS INORGÂNICOS Não apresentam Carbono em sua estrutura DOIS TIPOS: Água e Sais Minerais ÁGUA:
Ácidos nucléicos. São polímeros compostos por nucleotídeos. Açúcar - pentose. Grupo fosfato. Nucleotídeo. Base nitrogenada
 ÁCIDOS NUCLÉICOS Ácidos nucléicos São polímeros compostos por nucleotídeos Açúcar - pentose Nucleotídeo Grupo fosfato Base nitrogenada Composição dos Ácidos nucléicos pentoses: numeração da pentose: pentose
ÁCIDOS NUCLÉICOS Ácidos nucléicos São polímeros compostos por nucleotídeos Açúcar - pentose Nucleotídeo Grupo fosfato Base nitrogenada Composição dos Ácidos nucléicos pentoses: numeração da pentose: pentose
M E T B O L I S M O CATABOLISMO ANABOLISMO
 METABOLISMO É o conjunto das reações químicas que ocorrem num organismo vivo com o fim de promover a satisfação de necessidades estruturais e energéticas. ...metabolismo Do ponto de vista físico-químico,
METABOLISMO É o conjunto das reações químicas que ocorrem num organismo vivo com o fim de promover a satisfação de necessidades estruturais e energéticas. ...metabolismo Do ponto de vista físico-químico,
ENZIMAS E METABOLISMO
 ENZIMAS E METABOLISMO Metabolismo Celular é o conjunto de todas as reacções químicas celulares acompanhadas de transferência de energia. ANABOLISMO conjunto de reacções químicas que conduzem à biossíntese
ENZIMAS E METABOLISMO Metabolismo Celular é o conjunto de todas as reacções químicas celulares acompanhadas de transferência de energia. ANABOLISMO conjunto de reacções químicas que conduzem à biossíntese
Princípios moleculares dos processos fisiológicos
 2012-04-30 UNIVERSIDADE AGOSTINHO NETO FACULDADE DE CIÊNCIAS DEI-BIOLOGIA ---------------------------------------------- Aula 5: Princípios moleculares dos processos fisiológicos (Fisiologia Vegetal, Ano
2012-04-30 UNIVERSIDADE AGOSTINHO NETO FACULDADE DE CIÊNCIAS DEI-BIOLOGIA ---------------------------------------------- Aula 5: Princípios moleculares dos processos fisiológicos (Fisiologia Vegetal, Ano
QUÍMICA CELULAR NUTRIÇÃO TIPOS DE NUTRIENTES NUTRIENTES ENERGÉTICOS 4/3/2011 FUNDAMENTOS QUÍMICOS DA VIDA
 NUTRIÇÃO QUÍMICA CELULAR PROFESSOR CLERSON CLERSONC@HOTMAIL.COM CIESC MADRE CLÉLIA CONCEITO CONJUNTO DE PROCESSOS INGESTÃO, DIGESTÃO E ABSORÇÃO SUBSTÂNCIAS ÚTEIS AO ORGANISMO ESPÉCIE HUMANA: DIGESTÃO ONÍVORA
NUTRIÇÃO QUÍMICA CELULAR PROFESSOR CLERSON CLERSONC@HOTMAIL.COM CIESC MADRE CLÉLIA CONCEITO CONJUNTO DE PROCESSOS INGESTÃO, DIGESTÃO E ABSORÇÃO SUBSTÂNCIAS ÚTEIS AO ORGANISMO ESPÉCIE HUMANA: DIGESTÃO ONÍVORA
METABOLISMO. Nesta 3 a parte da disciplina nosso principal objetivo é compreender os mecanismos pelos quais as células regulam o seu metabolismo
 METABOLISMO Nesta 3 a parte da disciplina nosso principal objetivo é compreender os mecanismos pelos quais as células regulam o seu metabolismo Mas o que é metabolismo? Metabolismo é o nome que damos ao
METABOLISMO Nesta 3 a parte da disciplina nosso principal objetivo é compreender os mecanismos pelos quais as células regulam o seu metabolismo Mas o que é metabolismo? Metabolismo é o nome que damos ao
ÁCIDOS NUCLEÍCOS RIBOSSOMO E SÍNTESE PROTEÍCA
 ÁCIDOS NUCLEÍCOS RIBOSSOMO E SÍNTESE PROTEÍCA ÁCIDOS NUCLÉICOS: Moléculas orgânicas complexas, formadas polimerização de nucleotídeos (DNA e RNA) pela Contêm a informação que determina a seqüência de aminoácidos
ÁCIDOS NUCLEÍCOS RIBOSSOMO E SÍNTESE PROTEÍCA ÁCIDOS NUCLÉICOS: Moléculas orgânicas complexas, formadas polimerização de nucleotídeos (DNA e RNA) pela Contêm a informação que determina a seqüência de aminoácidos
Equipe de Biologia. Biologia
 Aluno (a): Série: 3ª Turma: TUTORIAL 5B Ensino Médio Equipe de Biologia Data: Biologia Ácidos nucléicos Os ácidos nucléicos são moléculas gigantes (macromoléculas), formadas por unidades monoméricas menores
Aluno (a): Série: 3ª Turma: TUTORIAL 5B Ensino Médio Equipe de Biologia Data: Biologia Ácidos nucléicos Os ácidos nucléicos são moléculas gigantes (macromoléculas), formadas por unidades monoméricas menores
LIGAÇÕES QUÍMICAS TEORIA CORPUSCULAR
 LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
LIGAÇÕES QUÍMICAS 5 TEORIA CORPUSCULAR 1 INTRODUÇÃO O fato de os gases nobres existirem na natureza como átomos isolados, levou os cientistas KOSSEL e LEWIS a elaborar um modelo para as ligações químicas.
Membrana Celular: Bicamada Lipídica Nutrição
 Membrana Celular: Bicamada Lipídica Nutrição Prof. João Ronaldo Tavares de Vasconcellos Neto FEV/2011 BICAMADA LIPÍDICA Bicamada Formada por 50% de lipídeos (latu senso); As moléculas das membranas são
Membrana Celular: Bicamada Lipídica Nutrição Prof. João Ronaldo Tavares de Vasconcellos Neto FEV/2011 BICAMADA LIPÍDICA Bicamada Formada por 50% de lipídeos (latu senso); As moléculas das membranas são
Professor Carlos - Proteinas
 14085. (Fuvest 2001) Os três compostos abaixo têm uso farmacológico Considere as afirmações: I Nas moléculas dos três compostos, há ligações peptídicas. II A porcentagem em massa de oxigênio na dropropizina
14085. (Fuvest 2001) Os três compostos abaixo têm uso farmacológico Considere as afirmações: I Nas moléculas dos três compostos, há ligações peptídicas. II A porcentagem em massa de oxigênio na dropropizina
BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR
 BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR As moléculas que constituem as células são formadas pelos mesmos átomos encontrados nos seres inanimados. Todavia, na origem e evolução das células, alguns
BASES MACROMOLECULARES DA CONSTITUIÇÃO CELULAR As moléculas que constituem as células são formadas pelos mesmos átomos encontrados nos seres inanimados. Todavia, na origem e evolução das células, alguns
Criado e Desenvolvido por: RONNIELLE CABRAL ROLIM Todos os direitos são reservados 2015. www.tioronni.com
 Criado e Desenvolvido por: RONNIELLE CABRAL ROLIM Todos os direitos são reservados 2015. www.tioronni.com ÁCIDOS NUCLEICOS ÁCIDOS NUCLÉICOS: são substâncias formadoras de genes, constituídas por um grande
Criado e Desenvolvido por: RONNIELLE CABRAL ROLIM Todos os direitos são reservados 2015. www.tioronni.com ÁCIDOS NUCLEICOS ÁCIDOS NUCLÉICOS: são substâncias formadoras de genes, constituídas por um grande
DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X
 DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X Disciplina: Engenharia de Proteínas Ma. Flávia Campos Freitas Vieira NÍVEIS ESTRUTURAIS DAS PROTEÍNAS Fonte: Lehninger, 2010.
DETERMINAÇÃO DA ESTRUTURA TRIDIMENSIONAL DE PROTEÍNAS POR DIFRAÇÃO DE RAIOS-X Disciplina: Engenharia de Proteínas Ma. Flávia Campos Freitas Vieira NÍVEIS ESTRUTURAIS DAS PROTEÍNAS Fonte: Lehninger, 2010.
Introdução. Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo.
 Introdução Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo. Existem também sistemas, em que as reações direta e inversa
Introdução Muitas reações ocorrem completamente e de forma irreversível como por exemplo a reação da queima de um papel ou palito de fósforo. Existem também sistemas, em que as reações direta e inversa
CARBOIDRATOS. INTRODUÇÃO -Biomoléculas mais abundantes -Base da nutrição animal
 INTRODUÇÃO -Biomoléculas mais abundantes -Base da nutrição animal CARBOIDRATOS *Os animais não são capazes de sintetizar carboidratos a partir de substratos simples não energéticos, precisando obtê-los
INTRODUÇÃO -Biomoléculas mais abundantes -Base da nutrição animal CARBOIDRATOS *Os animais não são capazes de sintetizar carboidratos a partir de substratos simples não energéticos, precisando obtê-los
Apostila de Química Geral
 Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Cursinho Vitoriano UNESP - Universidade Estadual Paulista "Júlio de Mesquita Filho" Câmpus de São José do Rio Preto Apostila de Química Geral Período noturno Ligações químicas interatômicas Vanessa R.
Regulação do metabolismo do glicogênio
 Regulação do metabolismo do glicogênio A U L A 27 objetivos Ao final desta aula, você deverá ser capaz de: Aprender sobre as vias de regulação do metabolismo de glicogênio. Reforçar os conceitos adquiridos
Regulação do metabolismo do glicogênio A U L A 27 objetivos Ao final desta aula, você deverá ser capaz de: Aprender sobre as vias de regulação do metabolismo de glicogênio. Reforçar os conceitos adquiridos
3ªsérie B I O L O G I A
 3.1 QUESTÃO 1 Três consumidores, A, B e C, compraram, cada um deles, uma bebida em embalagem longa vida, adequada às suas respectivas dietas. As tabelas abaixo trazem informações nutricionais sobre cada
3.1 QUESTÃO 1 Três consumidores, A, B e C, compraram, cada um deles, uma bebida em embalagem longa vida, adequada às suas respectivas dietas. As tabelas abaixo trazem informações nutricionais sobre cada
TEXTO PARA A PRÓXIMA QUESTÃO (Ufc) Na(s) questão(ões) a seguir escreva no espaço apropriado a soma dos itens corretos.
 Respiração e Fermentação 1. (Fuvest) O fungo 'Saccharomyces cerevisiae' (fermento de padaria) é um anaeróbico facultativo. Quando cresce na ausência de oxigênio, consome muito mais glicose do que quando
Respiração e Fermentação 1. (Fuvest) O fungo 'Saccharomyces cerevisiae' (fermento de padaria) é um anaeróbico facultativo. Quando cresce na ausência de oxigênio, consome muito mais glicose do que quando
BIOFÍSICA MEMBRANAS BIOLÓGICAS
 BIOFÍSICA MEMBRANAS BIOLÓGICAS CÉLULA Unidade fundamental dos seres vivos Menor estrutura biológica capaz de ter vida autônoma Átomos Moléculas Estruturas supramoleculares Células tecidos órgãos Sistemas
BIOFÍSICA MEMBRANAS BIOLÓGICAS CÉLULA Unidade fundamental dos seres vivos Menor estrutura biológica capaz de ter vida autônoma Átomos Moléculas Estruturas supramoleculares Células tecidos órgãos Sistemas
Quando esses temas são compreendidos, o aprendizado da química orgânica se torna muito mais fácil, diminuindo a necessidade de memorização.
 REAÇÕES ORGÂNIAS A primeira vista, a química orgânica pode ser observada como uma coleção confusa de milhões de compostos, dezenas de grupos funcionais e um número infinito de reações químicas. Ao estudá-la,
REAÇÕES ORGÂNIAS A primeira vista, a química orgânica pode ser observada como uma coleção confusa de milhões de compostos, dezenas de grupos funcionais e um número infinito de reações químicas. Ao estudá-la,
Membranas Biológicas e Transporte
 Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Introdução a Bioquímica Membranas Biológicas e Transporte 1. Introdução 2. Os Constituintes
Universidade Federal do Ceará Centro de Ciências Departamento de Bioquímica e Biologia Molecular Disciplina de Introdução a Bioquímica Membranas Biológicas e Transporte 1. Introdução 2. Os Constituintes
A base molecular da vida Constituintes da matéria-viva
 A base molecular da vida Constituintes da matéria-viva Principais elementos químicos dos seres vivos Quando se analisa a matéria-viva que constitui os seres vivos, encontram-se principalmente os seguintes
A base molecular da vida Constituintes da matéria-viva Principais elementos químicos dos seres vivos Quando se analisa a matéria-viva que constitui os seres vivos, encontram-se principalmente os seguintes
COLÉGIO SANTA TERESINHA R. Madre Beatriz 135 centro Tel. (33) 3341-1244 www.colegiosantateresinha.com.br
 PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
PLANEJAMENTO DE AÇÕES DA 2 ª ETAPA 2015 PERÍODO DA ETAPA: 01/09/2015 á 04/12/2015 TURMA: 9º Ano EF II DISCIPLINA: CIÊNCIAS / QUÍMICA 1- S QUE SERÃO TRABALHADOS DURANTE A ETAPA : Interações elétricas e
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é:
 01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
01) (ACAFE) O grupo de átomos que é encontrado na forma monoatômica pelo fato de serem estáveis é: a) Halogênios b) Calcogênios c) Metais Alcalinos Terrosos d) Metais Alcalinos e) Gases Nobres 02) (UFF-RJ)
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS
 Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
Profa Fernanda Galante Fundamentos de Química e Biologia Molecular/ Nutrição Material 3 1 LIGAÇÕES QUIMICAS REGRA DO OCTETO Cada átomo tem um número de elétrons diferente e estes e - (elétrons) estão distribuídos
7.012 Conjunto de Problemas 5
 Nome Seção 7.012 Conjunto de Problemas 5 Pergunta 1 Enquanto estudava um problema de infertilidade, você tentou isolar um gene hipotético de coelho que seria responsável pela prolífica reprodução desses
Nome Seção 7.012 Conjunto de Problemas 5 Pergunta 1 Enquanto estudava um problema de infertilidade, você tentou isolar um gene hipotético de coelho que seria responsável pela prolífica reprodução desses
O processo da Expressão Gênica
 Coordenadoria de Educação e Difusão de Ciências Rua 9 de Julho, 1205 - São Carlos - São Paulo e-mail: cbme@if.sc.usp.br- Telefone: (16) 3373-9159 http://cbme.ifsc.usp.br http://cbme.usp.br O processo da
Coordenadoria de Educação e Difusão de Ciências Rua 9 de Julho, 1205 - São Carlos - São Paulo e-mail: cbme@if.sc.usp.br- Telefone: (16) 3373-9159 http://cbme.ifsc.usp.br http://cbme.usp.br O processo da
As proteínas transportadoras
 As proteínas transportadoras 10 A U L A objetivos Ao final desta aula, você deverá compreender o que são: Proteínas transportadoras: carreadores e canais. Aquaporinas. Biologia Celular As proteínas transportadoras
As proteínas transportadoras 10 A U L A objetivos Ao final desta aula, você deverá compreender o que são: Proteínas transportadoras: carreadores e canais. Aquaporinas. Biologia Celular As proteínas transportadoras
QUIMICA ORGÂNICA BÁSICA
 QUIMICA ORGÂNICA BÁSICA Hibridização Revisão - Química Orgânica Básica 1 Tabela Periódica 2 Moléculas Diatômicas 3 Moléculas Poliatômicas 4 Eletronegatividade 5 A interação da luz e a matéria 6 Hibridização
QUIMICA ORGÂNICA BÁSICA Hibridização Revisão - Química Orgânica Básica 1 Tabela Periódica 2 Moléculas Diatômicas 3 Moléculas Poliatômicas 4 Eletronegatividade 5 A interação da luz e a matéria 6 Hibridização
Elementos do bloco p
 Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Elementos do bloco p Características gerais principais Estados de oxidação e tipos de ligações Inicialmente, para efeitos didáticos, serão utilizados os elementos do grupo 13 (B, Al, Ga, In Tl), que apresentam
Enzimática. Representação termodinâmica da ação catalítica de uma enzima: reação não catalisada. reação enzimaticamente catalisada (+) (o)
 Cinética Enzimática Representação termodinâmica da ação catalítica de uma enzima: (+) reação não catalisada (o) reação enzimaticamente catalisada 1 Hipótese chave-fechadura Centro ativo complementar em
Cinética Enzimática Representação termodinâmica da ação catalítica de uma enzima: (+) reação não catalisada (o) reação enzimaticamente catalisada 1 Hipótese chave-fechadura Centro ativo complementar em
www.aliancaprevestibular.com
 Professor Juliana Villa-Verde Disciplina Bio I Lista nº Assuntos Texto I Intodução à Citologia CITOLOGIA É o ramo da biologia que estuda a célula, unidade básica dos seres vivos. Hans e Zacarias Jensen
Professor Juliana Villa-Verde Disciplina Bio I Lista nº Assuntos Texto I Intodução à Citologia CITOLOGIA É o ramo da biologia que estuda a célula, unidade básica dos seres vivos. Hans e Zacarias Jensen
INTERAÇÃO DOS RAIOS-X COM A MATÉRIA
 INTERAÇÃO DOS RAIOS-X COM A MATÉRIA RAIOS-X + MATÉRIA CONSEQUÊNCIAS BIOLÓGICAS EFEITOS DAZS RADIAÇÕES NA H2O A molécula da água é a mais abundante em um organismo biológico, a água participa praticamente
INTERAÇÃO DOS RAIOS-X COM A MATÉRIA RAIOS-X + MATÉRIA CONSEQUÊNCIAS BIOLÓGICAS EFEITOS DAZS RADIAÇÕES NA H2O A molécula da água é a mais abundante em um organismo biológico, a água participa praticamente
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE
 LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
LIGAÇÃO COVALENTE APOLAR ELEMENTOS COM MESMA ELETRONEGATIVIDADE LIGAÇÃO COVALENTE POLAR ELEMENTOS COM ELETRONEGATIVIDADES DIFERENTES MOLÉCULA APOLAR VETORES SE ANULAM ///// µ R = 0 MOLÉCULA APOLAR VETORES
Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2
 11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
11 Segundo a Portaria do Ministério da Saúde MS n.o 1.469, de 29 de dezembro de 2000, o valor máximo permitido (VMP) da concentração do íon sulfato (SO 2 4 ), para que a água esteja em conformidade com
RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011
 RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011 Questão 26 Como a questão pede a separação do sólido solúvel do líquido, o único processo recomendado é a destilação simples. Lembrando que filtração e decantação
RESOLUÇÃO DA PROVA DE QUÍMICA DA UFRGS 2011 Questão 26 Como a questão pede a separação do sólido solúvel do líquido, o único processo recomendado é a destilação simples. Lembrando que filtração e decantação
Dra. Kátia R. P. de Araújo Sgrillo. sgrillo.ita@ftc.br
 Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br O metabolismo de carboidratos em humanos pode ser dividido nas seguintes categorias: 1. Glicólise 2. Ciclo de Krebs 3. Glicogênese 4. Glicogenólise
Dra. Kátia R. P. de Araújo Sgrillo sgrillo.ita@ftc.br O metabolismo de carboidratos em humanos pode ser dividido nas seguintes categorias: 1. Glicólise 2. Ciclo de Krebs 3. Glicogênese 4. Glicogenólise
As bactérias operárias
 A U A UL LA As bactérias operárias Na Aula 47 você viu a importância da insulina no nosso corpo e, na Aula 48, aprendeu como as células de nosso organismo produzem insulina e outras proteínas. As pessoas
A U A UL LA As bactérias operárias Na Aula 47 você viu a importância da insulina no nosso corpo e, na Aula 48, aprendeu como as células de nosso organismo produzem insulina e outras proteínas. As pessoas
Soluções para Conjunto de Problemas 1
 Soluções para 7.012 Conjunto de Problemas 1 Pergunta 1 a) Quais são os quatro principais tipos de moléculas biológicas discutidas na palestra? Cite uma função importante para cada tipo de molécula biológica
Soluções para 7.012 Conjunto de Problemas 1 Pergunta 1 a) Quais são os quatro principais tipos de moléculas biológicas discutidas na palestra? Cite uma função importante para cada tipo de molécula biológica
 Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
Reações Químicas Reações Químicas DG O QUE É UMA REAÇÃO QUÍMICA? É processo de mudanças químicas, onde ocorre a conversão de uma substância, ou mais, em outras substâncias. A + B REAGENTES C +
Síntese Artificial de Peptídeos
 Síntese Artificial de Peptídeos Rebeca Bayeh Seminário apresentado para a disciplina Princípios Físicos Aplicados à Fisiologia (PGF530) Prof. Dr. Adriano Mesquita Alencar Segundo semestre de 2013 Motivação
Síntese Artificial de Peptídeos Rebeca Bayeh Seminário apresentado para a disciplina Princípios Físicos Aplicados à Fisiologia (PGF530) Prof. Dr. Adriano Mesquita Alencar Segundo semestre de 2013 Motivação
Enzimas. Profª Eleonora Slide de aula
 Enzimas Profª Eleonora Slide de aula Enzimas São proteínas capazes de promover catálise de reações biológicas. Possuem alta especificidade e grande poder catalítico. Especificidade: o substrato sofre ação
Enzimas Profª Eleonora Slide de aula Enzimas São proteínas capazes de promover catálise de reações biológicas. Possuem alta especificidade e grande poder catalítico. Especificidade: o substrato sofre ação
Mary Santiago Silva 05/05/2010
 Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
Espectrometria de Massas Interpretação do Espectro de Massas Prof. Marcelo da Rosa Alexandre Departamento de Química - UFS Introdução Fragmentação em espectro de massas por EI oferece importante informação
Membranas biológicas. Profa Estela Rossetto
 Membranas biológicas Profa Estela Rossetto Membranas Biológicas Delimitam e permitem trocas entre compartimentos http://www.accessexcellence.org/rc/vl/gg/pmembranes.html Composição e Estrutura Lipídios
Membranas biológicas Profa Estela Rossetto Membranas Biológicas Delimitam e permitem trocas entre compartimentos http://www.accessexcellence.org/rc/vl/gg/pmembranes.html Composição e Estrutura Lipídios
Função orgânica nossa de cada dia. Profa. Kátia Aquino
 Função orgânica nossa de cada dia Profa. Kátia Aquino Vamos analisar! Funções Carboidratros (ou Glicídios) Energética: eles são os maiores fornecedores de energia para os seres vivos, principalmente a
Função orgânica nossa de cada dia Profa. Kátia Aquino Vamos analisar! Funções Carboidratros (ou Glicídios) Energética: eles são os maiores fornecedores de energia para os seres vivos, principalmente a
Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe!
 Aula: 31 Temática: Vitaminas parte I Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe! Introdução O termo vitamina refere-se a um fator dietético essencial requerido por um organismo em
Aula: 31 Temática: Vitaminas parte I Nestas últimas aulas irei abordar acerca das vitaminas. Acompanhe! Introdução O termo vitamina refere-se a um fator dietético essencial requerido por um organismo em
Reações orgânicas. Mestranda: Daniele Potulski Disciplina: Química da Madeira I
 Reações orgânicas Mestranda: Daniele Potulski Disciplina: Química da Madeira I Introdução Quase todos os compostos orgânicos tem moléculas apolares ou com baixa polaridade; Essa característica é um fator
Reações orgânicas Mestranda: Daniele Potulski Disciplina: Química da Madeira I Introdução Quase todos os compostos orgânicos tem moléculas apolares ou com baixa polaridade; Essa característica é um fator
UNIVERSIDADE FEDERAL DE ITAJUBÁ BIOLOGIA PROVA DE TRANSFERÊNCIA FACULTATIVA E PARA PORTADOR DE DIPLOMA DE CURSO SUPERIOR
 UNIVERSIDADE FEDERAL DE ITAJUBÁ BIOLOGIA PROVA DE TRANSFERÊNCIA FACULTATIVA E PARA PORTADOR DE DIPLOMA DE CURSO SUPERIOR 02/12/2012 Candidato: GABARITO Curso Pretendido: OBSERVAÇÕES: 01 Prova SEM consulta
UNIVERSIDADE FEDERAL DE ITAJUBÁ BIOLOGIA PROVA DE TRANSFERÊNCIA FACULTATIVA E PARA PORTADOR DE DIPLOMA DE CURSO SUPERIOR 02/12/2012 Candidato: GABARITO Curso Pretendido: OBSERVAÇÕES: 01 Prova SEM consulta
B) (até três pontos) Para os pares de espécies apresentados em i, ii e iii, tem-se, respectivamente, Al +, F - e Li.
 Química 1. O raio atômico (ou iônico) é uma propriedade periódica que exerce grande influência na reatividade dos átomos (ou dos íons). A) Explique, em termos de carga nuclear efetiva, a variação apresentada
Química 1. O raio atômico (ou iônico) é uma propriedade periódica que exerce grande influência na reatividade dos átomos (ou dos íons). A) Explique, em termos de carga nuclear efetiva, a variação apresentada
a) Qual a configuração eletrônica do cátion do alumínio isoeletrônico ao gás nobre neônio?
 Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
Questão 1: O Brasil é o campeão mundial da reciclagem de alumínio, colaborando com a preservação do meio ambiente. Por outro lado, a obtenção industrial do alumínio sempre foi um processo caro, consumindo
UFSC. Química (Amarela) 31) Resposta: 43. Comentário
 UFSC Química (Amarela) 1) Resposta: 4 01. Correta. Ao perder elétrons, o núcleo exerce maior atração sobre os elétrons restantes, diminuindo o raio. Li 1s2 2s 1 Li+ 1s 2 Raio atômico: átomo neutro > íon
UFSC Química (Amarela) 1) Resposta: 4 01. Correta. Ao perder elétrons, o núcleo exerce maior atração sobre os elétrons restantes, diminuindo o raio. Li 1s2 2s 1 Li+ 1s 2 Raio atômico: átomo neutro > íon
Escola Secundária Dr. Manuel Gomes de Almeida
 Escola Secundária Dr. Manuel Gomes de Almeida Ficha de trabalho de Biologia - 12º Ano Fermentação e actividade enzimática Nome: N º: Turma: Data: 1. A figura 1 representa um tipo de fermentação. Figura
Escola Secundária Dr. Manuel Gomes de Almeida Ficha de trabalho de Biologia - 12º Ano Fermentação e actividade enzimática Nome: N º: Turma: Data: 1. A figura 1 representa um tipo de fermentação. Figura
TRANSPORTE ATRAVÉS DA MEMBRANA. Luis Eduardo Maggi
 TRANSPORTE ATRAVÉS DA MEMBRANA Luis Eduardo Maggi Tipos de Transporte Passivo Difusão simples Difusão facilitada Osmose Ativo Impulsionado pelo gradiente iônico Bomba de Na/K Em Bloco Endocitose: (Fagocitose,
TRANSPORTE ATRAVÉS DA MEMBRANA Luis Eduardo Maggi Tipos de Transporte Passivo Difusão simples Difusão facilitada Osmose Ativo Impulsionado pelo gradiente iônico Bomba de Na/K Em Bloco Endocitose: (Fagocitose,
Propriedades Físicas de alguns compostos
 Propriedades Físicas de alguns compostos Tipo de ligação e temperatura de fusão COMPOSTO Tipo de ligação T fusão / o C NaCl iónica 801 Cu metálica 1083 Si covalente 1410 H 2 O intermolecular 0 C 6 H 6
Propriedades Físicas de alguns compostos Tipo de ligação e temperatura de fusão COMPOSTO Tipo de ligação T fusão / o C NaCl iónica 801 Cu metálica 1083 Si covalente 1410 H 2 O intermolecular 0 C 6 H 6
Forças intermoleculares, Disciplina de Química Geral Profa. Marcia Margarete Meier
 , líquidos e sólidos 1 Uma comparação entre líquidos e sólidos As propriedades físicas das substâncias entendidas em termos de teoria cinética molecular : Os gases são altamente compressíveis, assumem
, líquidos e sólidos 1 Uma comparação entre líquidos e sólidos As propriedades físicas das substâncias entendidas em termos de teoria cinética molecular : Os gases são altamente compressíveis, assumem
Separação e Cromatografia de Proteínas
 QBQ0316N: Bioquímica Experimental Farmácia São Paulo, 11 de setembro 2013 Separação e Cromatografia de Proteínas Universidade de São Paulo QBQ0316N: Bioquímica Experimental Farmácia São Paulo, 11 de setembro
QBQ0316N: Bioquímica Experimental Farmácia São Paulo, 11 de setembro 2013 Separação e Cromatografia de Proteínas Universidade de São Paulo QBQ0316N: Bioquímica Experimental Farmácia São Paulo, 11 de setembro
REVISÃO QUÍMICA. Profº JURANDIR QUÍMICA
 REVISÃO QUÍMICA Profº JURANDIR QUÍMICA DADOS 01. (ENEM 2004) Em setembro de 1998, cerca de 10.000 toneladas de ácido sulfúrico (H 2 SO 4 ) foram derramadas pelo navio Bahamas no litoral do Rio Grande
REVISÃO QUÍMICA Profº JURANDIR QUÍMICA DADOS 01. (ENEM 2004) Em setembro de 1998, cerca de 10.000 toneladas de ácido sulfúrico (H 2 SO 4 ) foram derramadas pelo navio Bahamas no litoral do Rio Grande
O fluxo da informação é unidirecional
 Curso - Psicologia Disciplina: Genética Humana e Evolução Resumo Aula 3- Transcrição e Tradução Dogma central TRANSCRIÇÃO DO DNA O fluxo da informação é unidirecional Processo pelo qual uma molécula de
Curso - Psicologia Disciplina: Genética Humana e Evolução Resumo Aula 3- Transcrição e Tradução Dogma central TRANSCRIÇÃO DO DNA O fluxo da informação é unidirecional Processo pelo qual uma molécula de
Núcleo Celular. Biomedicina primeiro semestre de 2012 Profa. Luciana Fontanari Krause
 Núcleo Celular Biomedicina primeiro semestre de 2012 Profa. Luciana Fontanari Krause Núcleo Celular Eucarioto: núcleo delimitado por membrana nuclear (carioteca) Portador dos fatores hereditários e controlador
Núcleo Celular Biomedicina primeiro semestre de 2012 Profa. Luciana Fontanari Krause Núcleo Celular Eucarioto: núcleo delimitado por membrana nuclear (carioteca) Portador dos fatores hereditários e controlador
Estrutura tridimensional de proteínas. Prof. Dr. Fernando Berton Zanchi
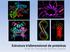 Estrutura tridimensional de proteínas Prof. Dr. Fernando Berton Zanchi Níveis de Estruturas Protéicas A conformação espacial das proteínas As proteínas não são traços rígidos porque suas ligações químicas
Estrutura tridimensional de proteínas Prof. Dr. Fernando Berton Zanchi Níveis de Estruturas Protéicas A conformação espacial das proteínas As proteínas não são traços rígidos porque suas ligações químicas
95% de água, 3% de substâncias orgânicas e 2% de sais minerais. uma secreção serosa outra secreção mucosa
 SISTEMA DIGESTÓRIO SALIVA A saliva é um líquido claro, viscoso, alcalino (ph entre 6 e 7), que contém em sua composição: 95% de água, 3% de substâncias orgânicas e 2% de sais minerais. Além disso, também
SISTEMA DIGESTÓRIO SALIVA A saliva é um líquido claro, viscoso, alcalino (ph entre 6 e 7), que contém em sua composição: 95% de água, 3% de substâncias orgânicas e 2% de sais minerais. Além disso, também
MEDICINA VETERINÁRIA. Disciplina: Genética Animal. Prof a.: Drd. Mariana de F. G. Diniz
 MEDICINA VETERINÁRIA Disciplina: Genética Animal Prof a.: Drd. Mariana de F. G. Diniz Gene, é a unidade fundamental da hereditariedade. Cada gene é formado por uma sequência específica de ácidos nucléicos
MEDICINA VETERINÁRIA Disciplina: Genética Animal Prof a.: Drd. Mariana de F. G. Diniz Gene, é a unidade fundamental da hereditariedade. Cada gene é formado por uma sequência específica de ácidos nucléicos
As forças atrativas entre duas moléculas são significativas até uma distância de separação d, que chamamos de alcance molecular.
 Tensão Superficial Nos líquidos, as forças intermoleculares atrativas são responsáveis pelos fenômenos de capilaridade. Por exemplo, a subida de água em tubos capilares e a completa umidificação de uma
Tensão Superficial Nos líquidos, as forças intermoleculares atrativas são responsáveis pelos fenômenos de capilaridade. Por exemplo, a subida de água em tubos capilares e a completa umidificação de uma
DIODOS. Professor João Luiz Cesarino Ferreira
 DIODOS A união de um cristal tipo p e um cristal tipo n, obtém-se uma junção pn, que é um dispositivo de estado sólido simples: o diodo semicondutor de junção. Figura 1 Devido a repulsão mútua os elétrons
DIODOS A união de um cristal tipo p e um cristal tipo n, obtém-se uma junção pn, que é um dispositivo de estado sólido simples: o diodo semicondutor de junção. Figura 1 Devido a repulsão mútua os elétrons
Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron:
 Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
Equação de Estado de Van der Waals Do ponto de vista da Termodinâmica, gás ideal é aquele para o qual vale, para quaisquer valores de P e T, a equação de estado de Clapeyron: P i V i = nrt em que colocamos
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo
 Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
Química Orgânica I Profª Dra. Alceni Augusta Werle Profª Dra.Tânia M. Sacramento Melo Ligação Química e Estudo do Átomo de Carbono Aula 1 1- INTRODUÇÃO Os átomos são formados por nêutrons, prótons e elétrons.
PROFESSOR LOURIVAL NETO
 QUÍMICA EM 1 DIA PROFESSOR LOURIVAL NETO UBERLÂNDIA LIGAÇÕES QUÍMICAS Iônica: Ocorre devido a transferência de elétrons! Ìons mantêmse em um cristal Retículo cristalino. A força eletrostática mantém os
QUÍMICA EM 1 DIA PROFESSOR LOURIVAL NETO UBERLÂNDIA LIGAÇÕES QUÍMICAS Iônica: Ocorre devido a transferência de elétrons! Ìons mantêmse em um cristal Retículo cristalino. A força eletrostática mantém os
-Estrutura, composição, características. -Aplicações e processamento. -Tecnologias associadas às aplicações industriais.
 Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Teófilo Otoni - MG Prof a. Dr a. Flaviana Tavares Vieira Tópicos : -Estrutura, composição, características.
Universidade Federal dos Vales do Jequitinhonha e Mucuri Bacharelado em Ciência e Tecnologia Teófilo Otoni - MG Prof a. Dr a. Flaviana Tavares Vieira Tópicos : -Estrutura, composição, características.
Dra. Kátia R. P. de Araújo Sgrillo. Sgrillo.ita@ftc.br
 Dra. Kátia R. P. de Araújo Sgrillo Sgrillo.ita@ftc.br E da onde vem esta energia?? E o que é Bioenergética? Para manterem-se vivos e desempenharem diversas funções biológicas os organismos necessitam continuamente
Dra. Kátia R. P. de Araújo Sgrillo Sgrillo.ita@ftc.br E da onde vem esta energia?? E o que é Bioenergética? Para manterem-se vivos e desempenharem diversas funções biológicas os organismos necessitam continuamente
TERMOQUÍMICA. Desta forma podemos dizer que qualquer mudança química geralmente envolve energia.
 TERMOQUÍMICA 1 Introdução A sociedade moderna depende das mais diversas formas de energia para sua existência. Quase toda a energia de que dependemos é obtida a partir de reações químicas, como a queima
TERMOQUÍMICA 1 Introdução A sociedade moderna depende das mais diversas formas de energia para sua existência. Quase toda a energia de que dependemos é obtida a partir de reações químicas, como a queima
Química Orgânica HIBRIDIZAÇÃO DO CARBONO
 Química Orgânica HIBRIDIZAÇÃO DO CARBONO amos Relembrar... Orbitais Atômicos casinha do elétrons Existem 4 orbitais atômicos s p d f Ligações sigma (σ) e ligações pi (π) Ligações do tipo sigma(σ) Ocorre
Química Orgânica HIBRIDIZAÇÃO DO CARBONO amos Relembrar... Orbitais Atômicos casinha do elétrons Existem 4 orbitais atômicos s p d f Ligações sigma (σ) e ligações pi (π) Ligações do tipo sigma(σ) Ocorre
- LIGAÇÕES IÔNICAS: Na (1s 2 2s 2 2p 6 3s 1 ) + Cl (1s 2 2s 2 2p 6 3s 2 3p 5 ) Na + (1s 2 2s 2 2p 6 ) + Cl - (1s 2 2s 2 2p 6 3s 2 3p 6 )
 - LIGAÇÕES IÔNICAS: A ligação iônica é a ligação química formada pela atração eletrostática entre íons positivos e íons negativos. A ligação se dá entre dois átomos quando um elétron, ou mais um, se transfere
- LIGAÇÕES IÔNICAS: A ligação iônica é a ligação química formada pela atração eletrostática entre íons positivos e íons negativos. A ligação se dá entre dois átomos quando um elétron, ou mais um, se transfere
Prova de Química e Biologia
 Provas Especialmente Adequadas Destinadas a Avaliar a Capacidade para a Frequência dos Cursos Superiores do IPVC dos Maiores de 23 Anos Prova de Química e Biologia Prova modelo Prova Específica de Química
Provas Especialmente Adequadas Destinadas a Avaliar a Capacidade para a Frequência dos Cursos Superiores do IPVC dos Maiores de 23 Anos Prova de Química e Biologia Prova modelo Prova Específica de Química
A descoberta da célula
 A descoberta da célula O que são células? As células são a unidade fundamental da vida CITOLOGIA A área da Biologia que estuda a célula, no que diz respeito à sua estrutura e funcionamento. Kytos (célula)
A descoberta da célula O que são células? As células são a unidade fundamental da vida CITOLOGIA A área da Biologia que estuda a célula, no que diz respeito à sua estrutura e funcionamento. Kytos (célula)
UNIDADE 3 - COORDENAÇÃO ATÔMICA
 A força de repulsão entre os elétrons de dois átomos, quando estão suficientemente próximos, é responsável, em conjunto com as forças de atração, pela posição de equilíbrio dos átomos na ligação química
A força de repulsão entre os elétrons de dois átomos, quando estão suficientemente próximos, é responsável, em conjunto com as forças de atração, pela posição de equilíbrio dos átomos na ligação química
95% de água, 3% de substâncias orgânicas e 2% de sais minerais. uma secreção serosa outra secreção mucosa
 SISTEMA DIGESTÓRIO SALIVA A saliva é um líquido claro, viscoso, alcalino (ph entre 6 e 7), que contém em sua composição: 95% de água, 3% de substâncias orgânicas e 2% de sais minerais. Além disso, também
SISTEMA DIGESTÓRIO SALIVA A saliva é um líquido claro, viscoso, alcalino (ph entre 6 e 7), que contém em sua composição: 95% de água, 3% de substâncias orgânicas e 2% de sais minerais. Além disso, também
Resumo Teórico. Fala Gás Nobre! Tudo bem?
 Resumo Teórico 2 Fala Gás Nobre! Tudo bem? Já assistimos todos os vídeos sobre a Poluição da Água. Estamos cada vez mais próximos do sucesso. Por isso quero te entregar esse material que contém o resumo
Resumo Teórico 2 Fala Gás Nobre! Tudo bem? Já assistimos todos os vídeos sobre a Poluição da Água. Estamos cada vez mais próximos do sucesso. Por isso quero te entregar esse material que contém o resumo
Química. Resolução das atividades complementares. Q50 Forças intermoleculares
 Resolução das atividades complementares 4 Química Q50 Forças intermoleculares p. 15 1 (Unifor-CE) Considerando a natureza das ligações químicas intermoleculares existentes nas substâncias: Etanol C 2 H
Resolução das atividades complementares 4 Química Q50 Forças intermoleculares p. 15 1 (Unifor-CE) Considerando a natureza das ligações químicas intermoleculares existentes nas substâncias: Etanol C 2 H
Replicação Quais as funções do DNA?
 Replicação Quais as funções do DNA? Aula nº 4 22/Set/08 Prof. Ana Reis Replicação O DNA é a molécula que contém a informação para todas as actividades da célula. Uma vez que as células se dividem, é necessário
Replicação Quais as funções do DNA? Aula nº 4 22/Set/08 Prof. Ana Reis Replicação O DNA é a molécula que contém a informação para todas as actividades da célula. Uma vez que as células se dividem, é necessário
Bioquímica: Componentes orgânicos e inorgânicos necessários à vida. Leandro Pereira Canuto
 Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
Bioquímica: orgânicos e inorgânicos necessários à vida Leandro Pereira Canuto Toda matéria viva: C H O N P S inorgânicos orgânicos Água Sais Minerais inorgânicos orgânicos Carboidratos Proteínas Lipídios
